| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава III. ДВОЙНЫЕ СИСТЕМЫ
III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
Двойная (бинарная) однофазная система имеет три степени свободы, ее состояние изображается точкой в трехмерном пространстве. В качестве параметров состояния обычно выбирают
температуру, давление и концентрацию (одного из компонентов, любого, поскольку 
Нас интересуют, в первую очередь, двухфазные системы жидкость — пар. Состояние двойной двухфазной системы определяется двумя независимыми переменными. В координатах  мы имеем две поверхности — жидкости и пара, на которых располагаются фигуративные точки, изображающие составы равновесных фаз. При этом, в силу условий равновесия, температуры и давления сосуществующих жидкости и пара одинаковы. Пространство между поверхностями жидкости и пара отвечает гетерогенной области, линии, соединяющие составы равновесных фаз, называют нодами (коннодами).
мы имеем две поверхности — жидкости и пара, на которых располагаются фигуративные точки, изображающие составы равновесных фаз. При этом, в силу условий равновесия, температуры и давления сосуществующих жидкости и пара одинаковы. Пространство между поверхностями жидкости и пара отвечает гетерогенной области, линии, соединяющие составы равновесных фаз, называют нодами (коннодами).
Равновесие между жидкостью и паром обычно изучают при постоянном давлении (изобарные данные) или постоянной температуре (изотермические данные). Соответственно, строят и диаграммы равновесия в  или
или  -плоскостях, эти диаграммы, хорошо известные, являются сечениями полной диаграммы состояния двойной двухфазной системы. В некоторых случаях при рассмотрении диаграмм равновесия в широком интервале условий, включающем область критических и закритических состояний, более удобными оказываются диаграммы в
-плоскостях, эти диаграммы, хорошо известные, являются сечениями полной диаграммы состояния двойной двухфазной системы. В некоторых случаях при рассмотрении диаграмм равновесия в широком интервале условий, включающем область критических и закритических состояний, более удобными оказываются диаграммы в  -координатах. Такие диаграммы, более
-координатах. Такие диаграммы, более

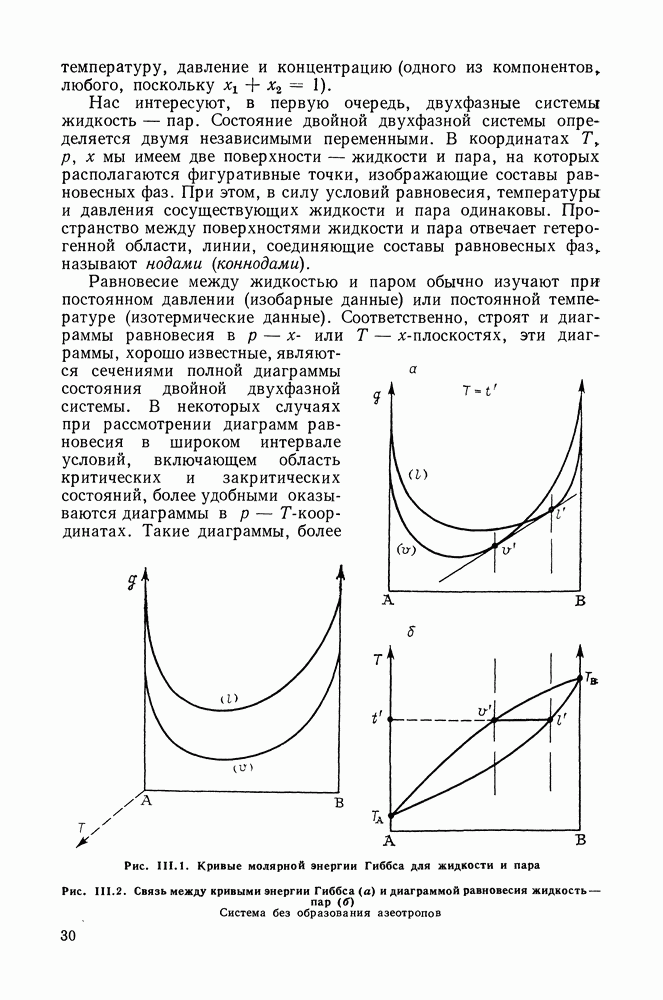
Рис. III. 1. Кривые молярной энергии Гиббса для жидкости и пара

Рис. II 1.2. Связь между кривыми энергии Гиббса (а) и диаграммой равновесия жидкость — пар (б) Система без образования азеотропов
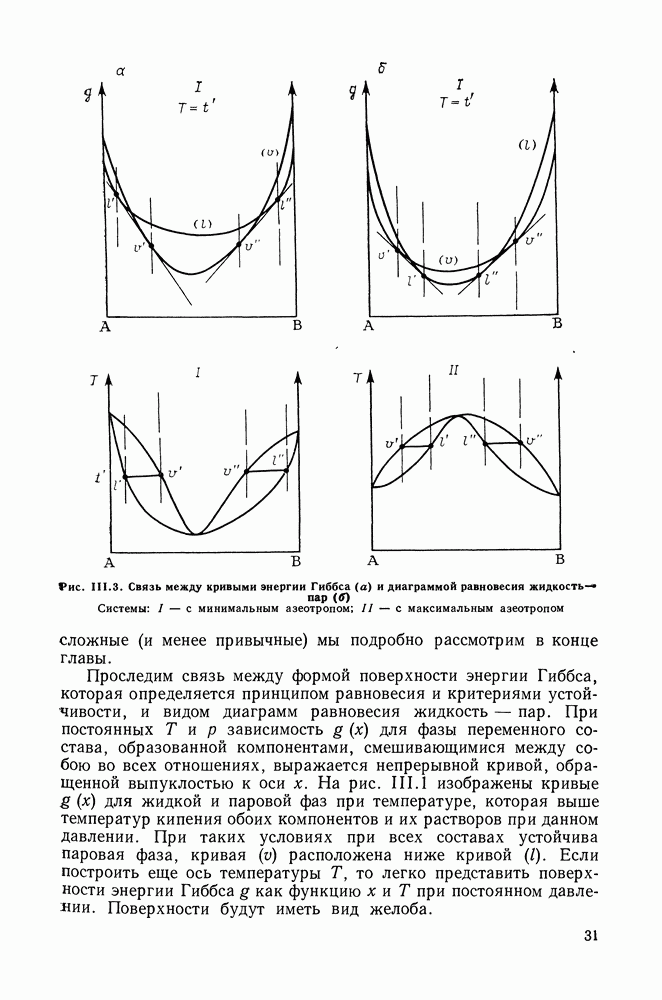
Рис. 111.3. (см. скан) Связь между кривыми энергии Гиббса (а) и диаграммой равновесия жидкость-пар (б) Системы: I — с минимальным азеотропом; II — с максимальным азеотропом
сложные (и менее привычные) мы подробно рассмотрим в конце главы.
Проследим связь между формой поверхности энергии Гиббса, которая определяется принципом равновесия и критериями устойчивости, и видом диаграмм равновесия жидкость — пар. При постоянных Тир зависимость  для фазы переменного состава, образованной компонентами, смешивающимися между собою во всех отношениях, выражается непрерывной кривой, обращенной выпуклостью к оси х. На рис. III. 1 изображены кривые
для фазы переменного состава, образованной компонентами, смешивающимися между собою во всех отношениях, выражается непрерывной кривой, обращенной выпуклостью к оси х. На рис. III. 1 изображены кривые  для жидкой и паровой фаз при температуре, которая выше температур кипения обоих компонентов и их растворов при данном давлении. При таких условиях при всех составах устойчива паровая фаза, кривая
для жидкой и паровой фаз при температуре, которая выше температур кипения обоих компонентов и их растворов при данном давлении. При таких условиях при всех составах устойчива паровая фаза, кривая  расположена ниже кривой
расположена ниже кривой  Если построить еще ось температуры
Если построить еще ось температуры  то легко представить поверхности энергии Гиббса
то легко представить поверхности энергии Гиббса  как функцию
как функцию  и
и  при постоянном давлении. Поверхности будут иметь вид желоба.
при постоянном давлении. Поверхности будут иметь вид желоба.
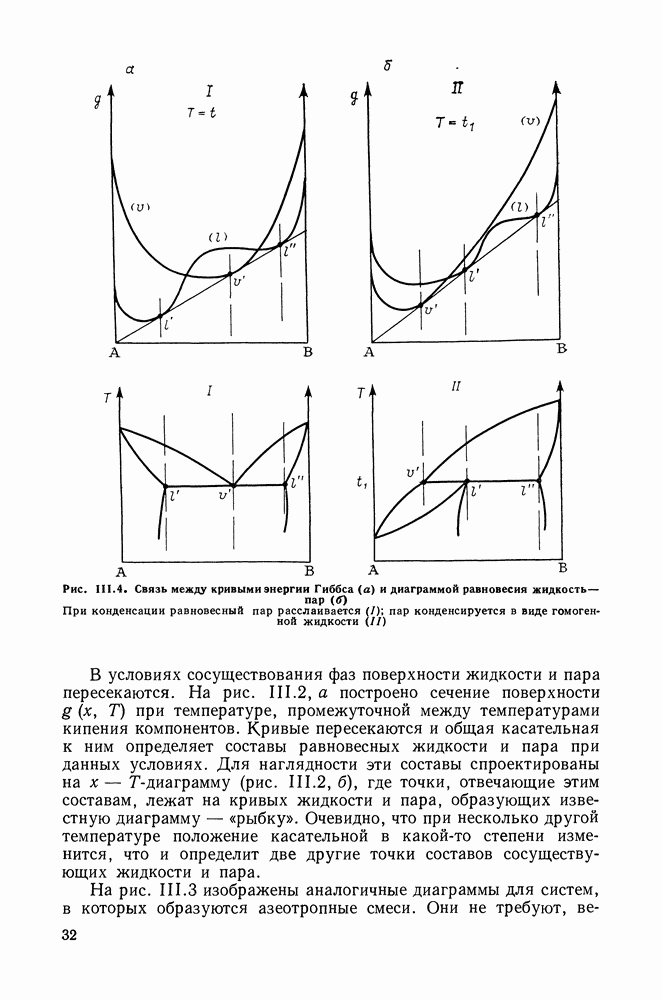
Рис. III.4. (см. скан) Связь между кривыми энергии Гиббса (а) и диаграммой равновесия жидкость—пар (б) При конденсации равновесный пар расслаивается (I); пар конденсируется в виде гомогенной жидкости (II)
В условиях сосуществования фаз поверхности жидкости и пара пересекаются. На рис. II 1.2, а построено сечение поверхности  при температуре, промежуточной между температурами кипения компонентов. Кривые пересекаются и общая касательная к ним определяет составы равновесных жидкости и пара при данных условиях. Для наглядности эти составы спроектированы на
при температуре, промежуточной между температурами кипения компонентов. Кривые пересекаются и общая касательная к ним определяет составы равновесных жидкости и пара при данных условиях. Для наглядности эти составы спроектированы на  -диаграмму (рис. III.2, б), где точки, отвечающие этим составам, лежат на кривых жидкости и пара, образующих известную диаграмму — «рыбку». Очевидно, что при несколько другой температуре положение касательной в какой-то степени изменится, что и определит две другие точки составов сосуществующих жидкости и пара.
-диаграмму (рис. III.2, б), где точки, отвечающие этим составам, лежат на кривых жидкости и пара, образующих известную диаграмму — «рыбку». Очевидно, что при несколько другой температуре положение касательной в какой-то степени изменится, что и определит две другие точки составов сосуществующих жидкости и пара.
На рис. II 1.3 изображены аналогичные диаграммы для систем, в которых образуются азеотропные смеси. Они не требуют,
вероятно, дополнительных пояснений. Отметим только, что через  обозначены равновесные фазы.
обозначены равновесные фазы.
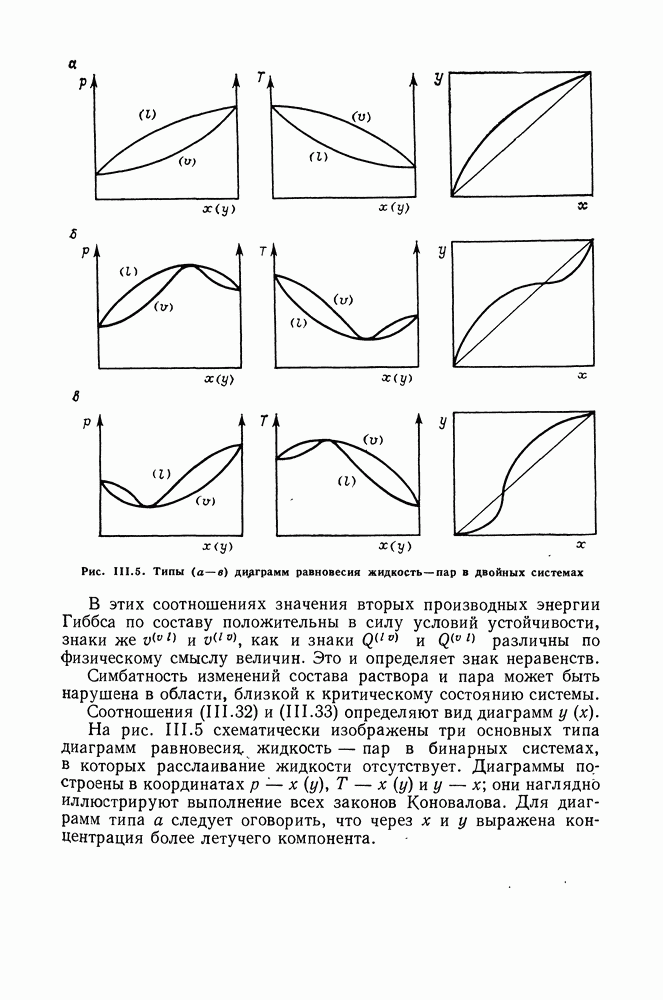
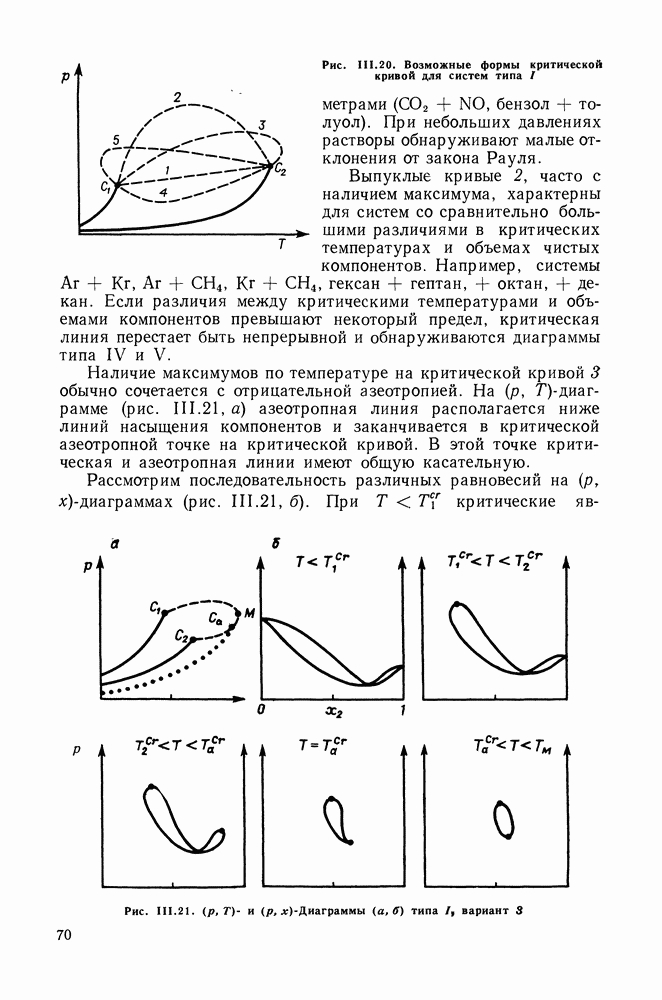
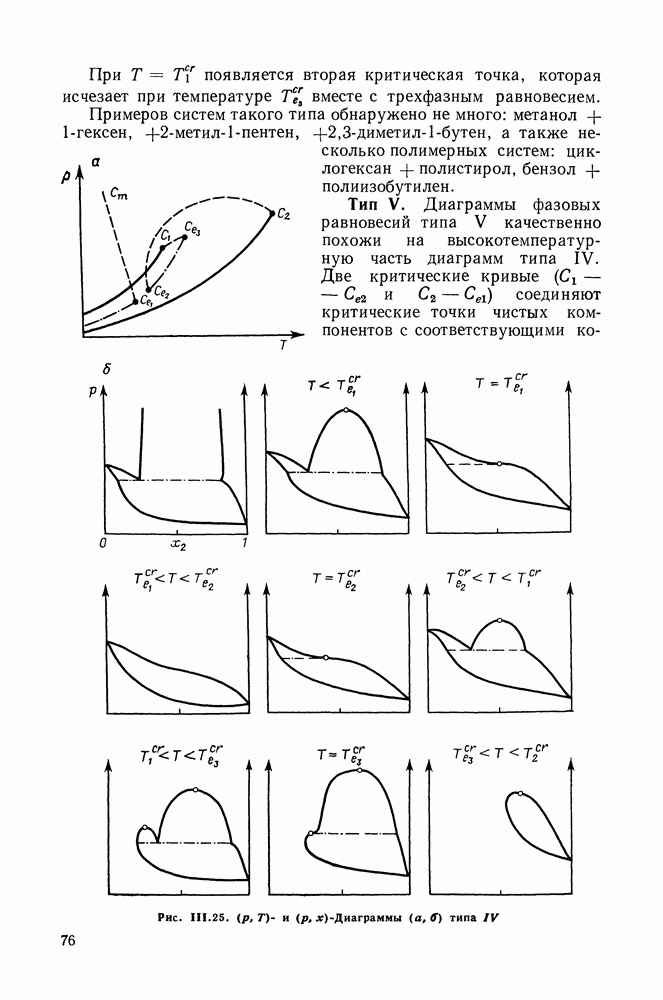
На рис. III.2 и III.3 представлены три типа диаграмм равновесия жидкость — пар в двойных системах: без образования азеотропной смеси и с минимальным и максимальным азеотропами. Диаграммы этих типов имеют иной вид в случаях, когда условия таковы, что температура и давление превышают критические значения для одного из компонентов или же для раствора какого-либо состава.
Несколько более сложны диаграммы для двойных систем, в которых образуются две жидкие фазы. В этом случае мы имеем равновесие трех фаз — двух жидких и пара — в двойной системе. Такая трехфазная система обладает только одной степенью свободы. Следовательно, задание одного из параметров — температуры, давления или состава одной из равновесных фаз однозначно определяет состояние системы. К диаграммам систем с расслаиванием мы еще возвратимся в разд. II 1.9, здесь же остановимся только на связи диаграмм с формой поверхности энергии Гиббса.
Напомним (см. разд. 1.4), что при расслаивании жидкости кривизна поверхности энергии Гиббса меняется. Поверхность же энергии Гиббса для пара имеет тот же вид, что и в системах с жидкой фазой без расслаивания. Но следует выделить два случая: в одном из них пар, равновесный с двумя жидкими слоями, при конденсации расслаивается на две фазы; в другом конденсат пара представляет собою гомогенный раствор. Диаграммы построены на рис. II 1.4. Очевидно, что в подобных системах должна быть общая касательная к линиям  для жидкой фазы и
для жидкой фазы и  для пара, причем на кривой
для пара, причем на кривой  имеются две точки касания, отвечающие составам равновесных жидких слоев.
имеются две точки касания, отвечающие составам равновесных жидких слоев.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
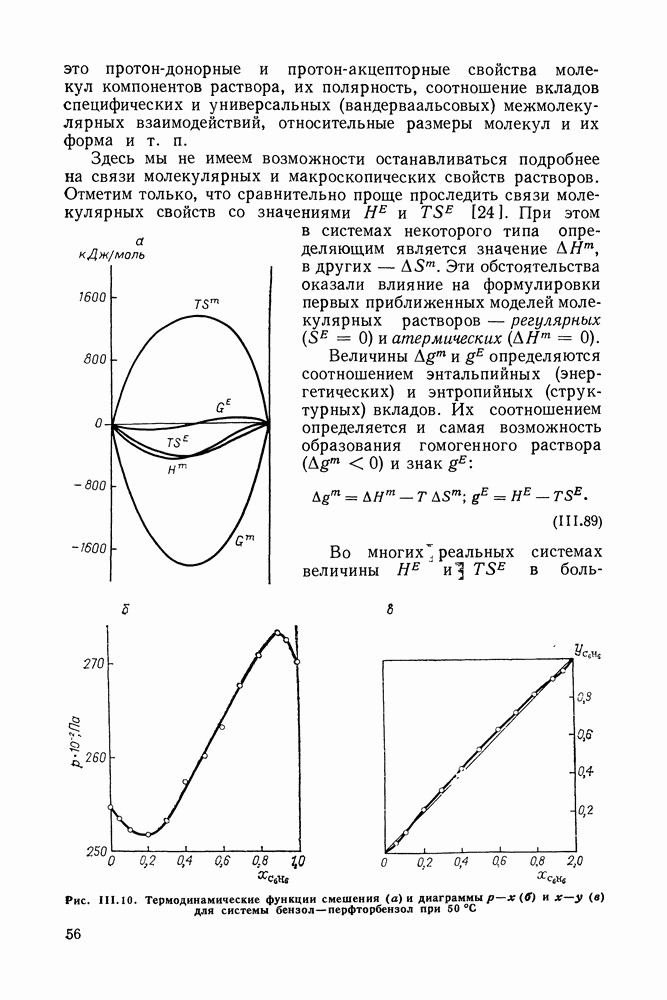
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
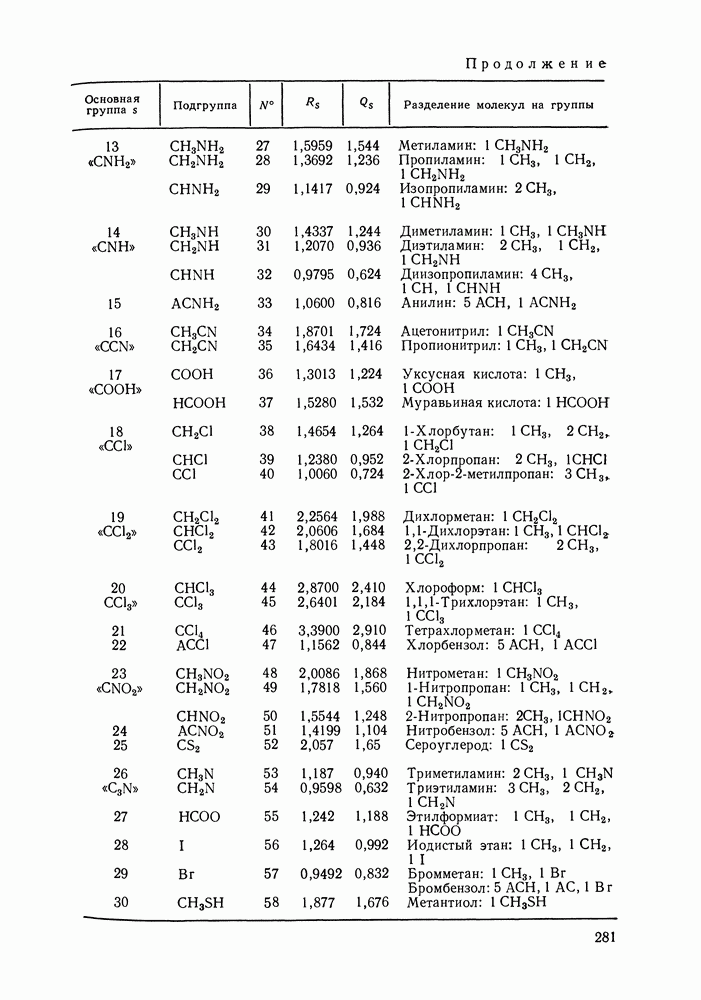
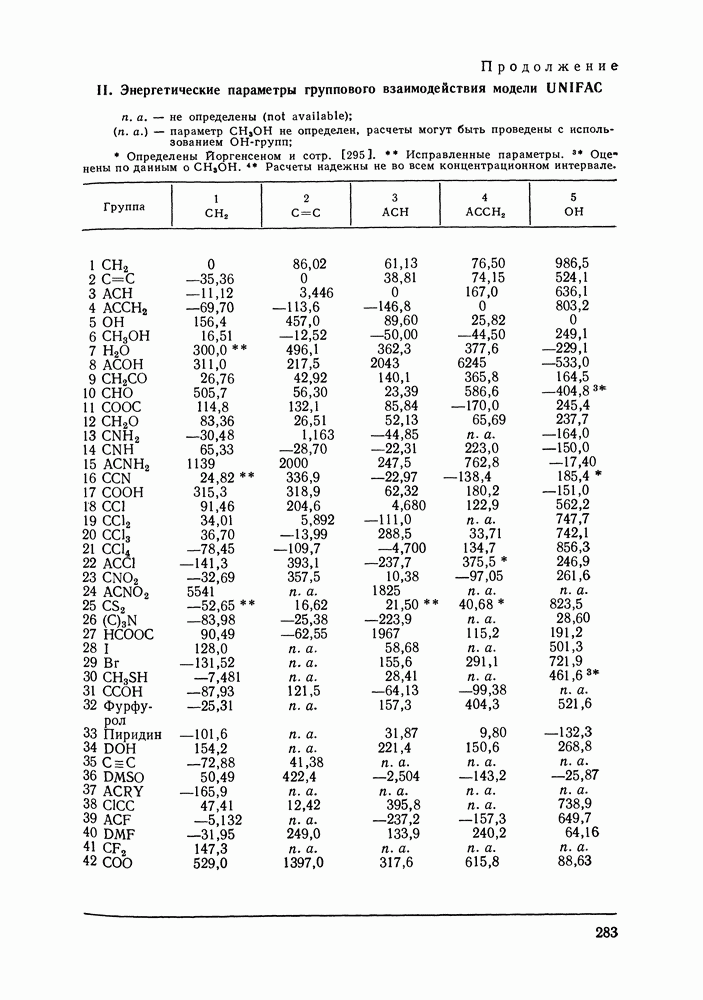
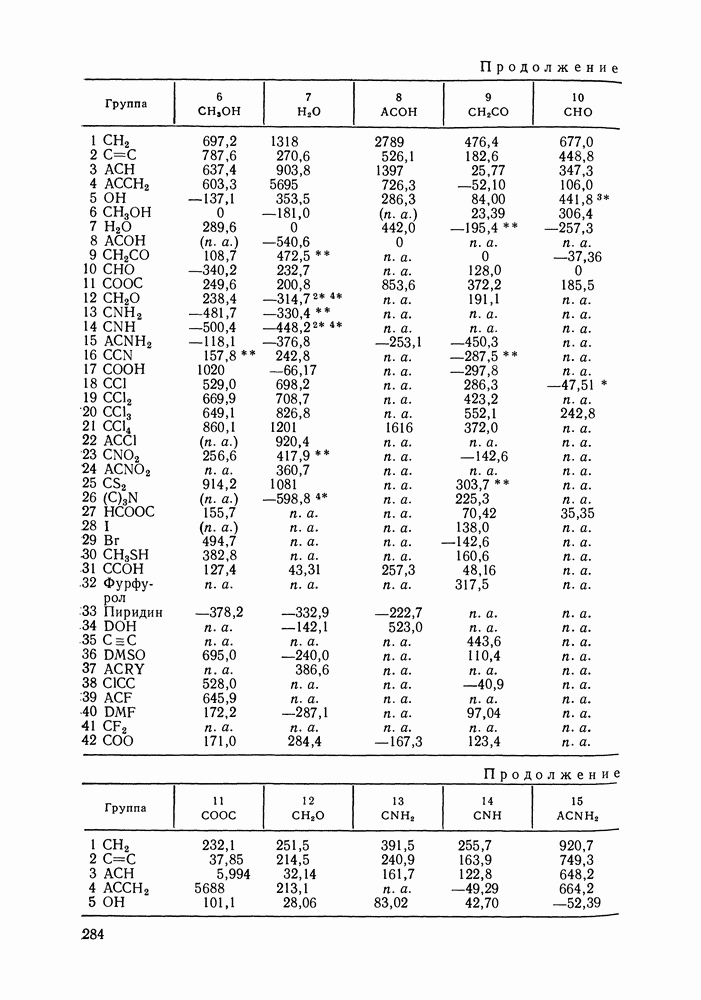
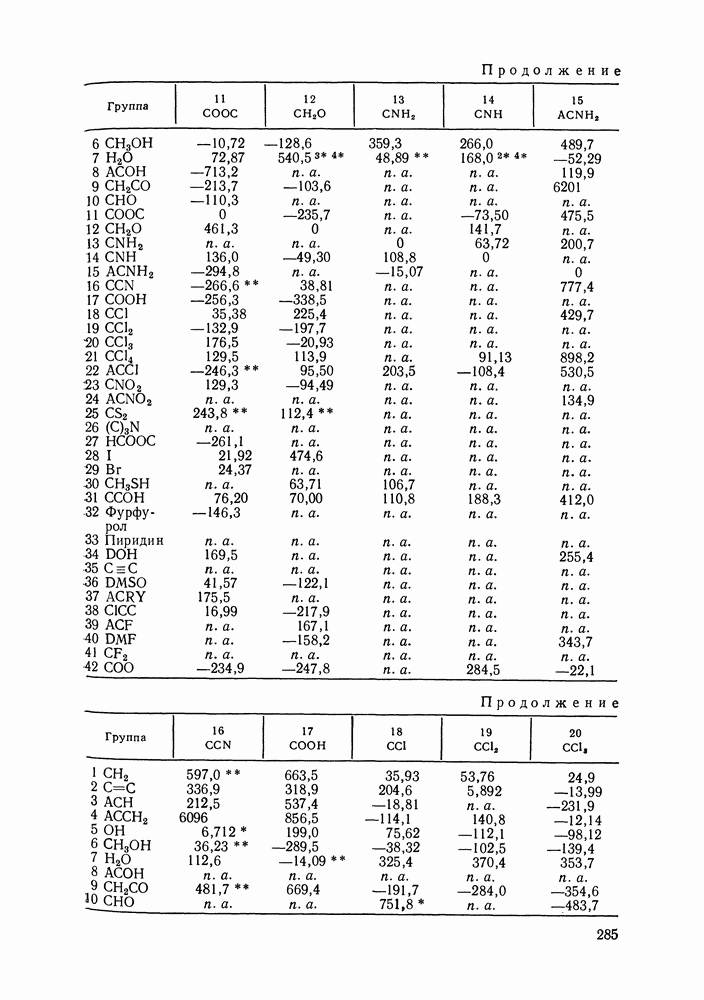
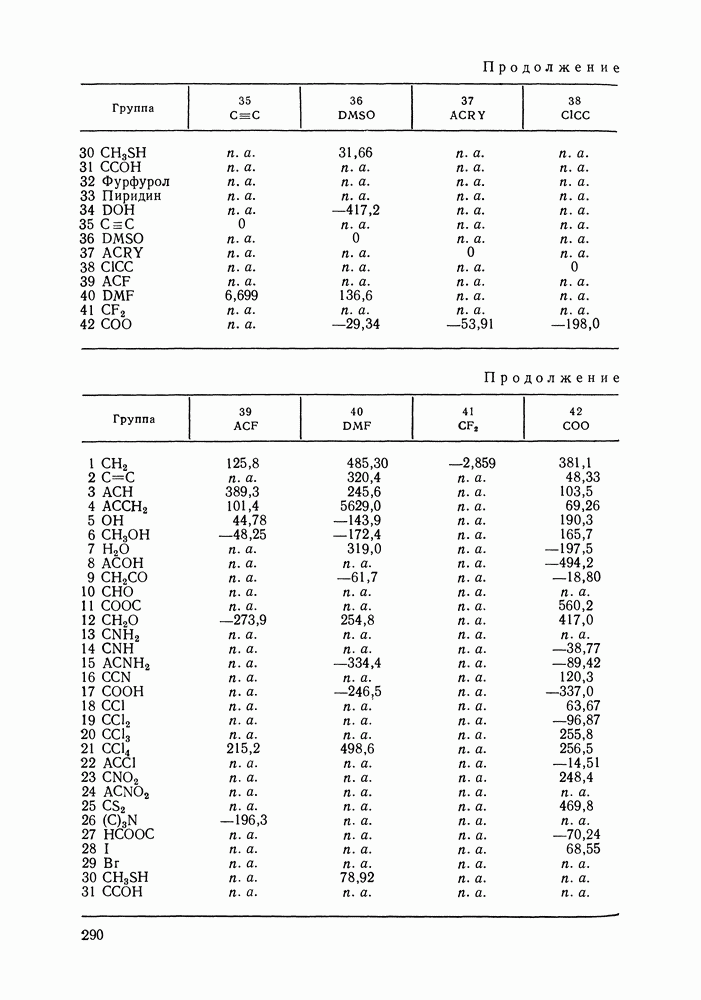
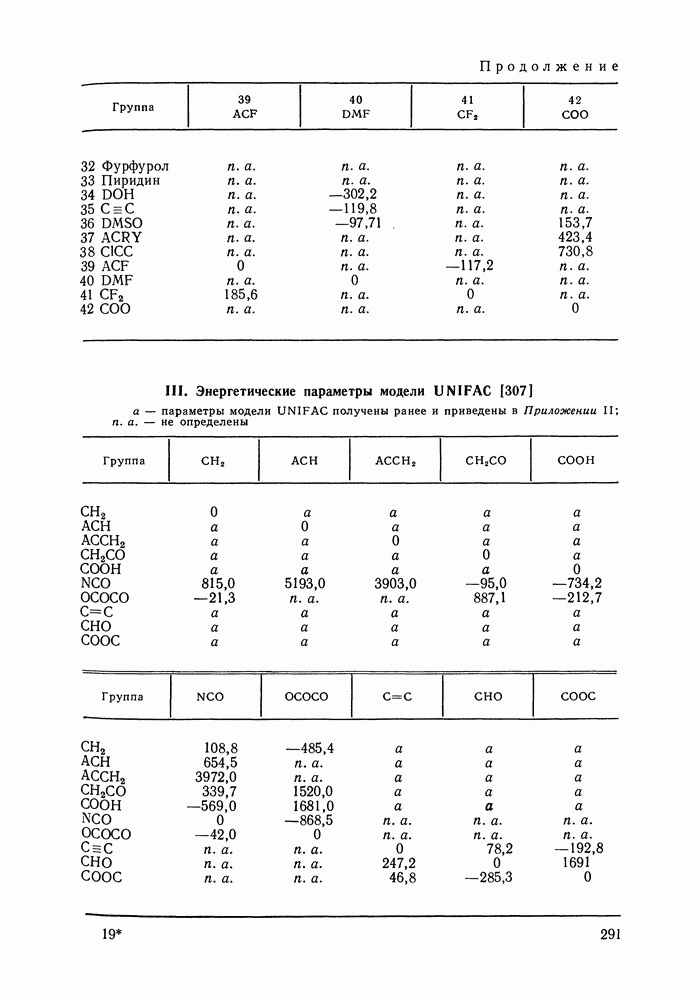
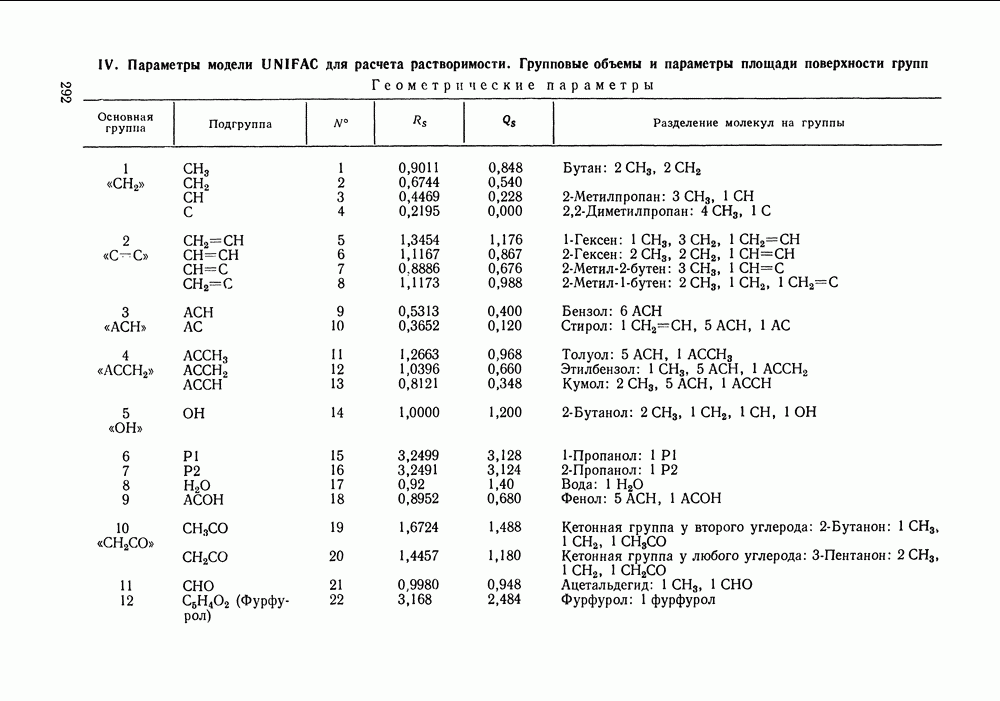
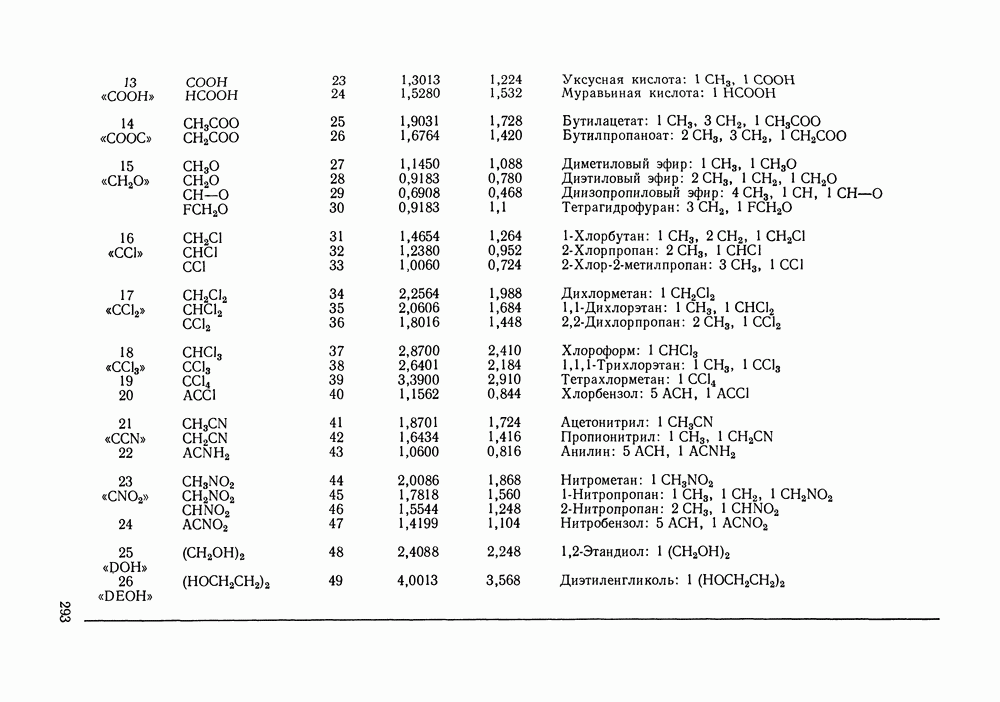
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
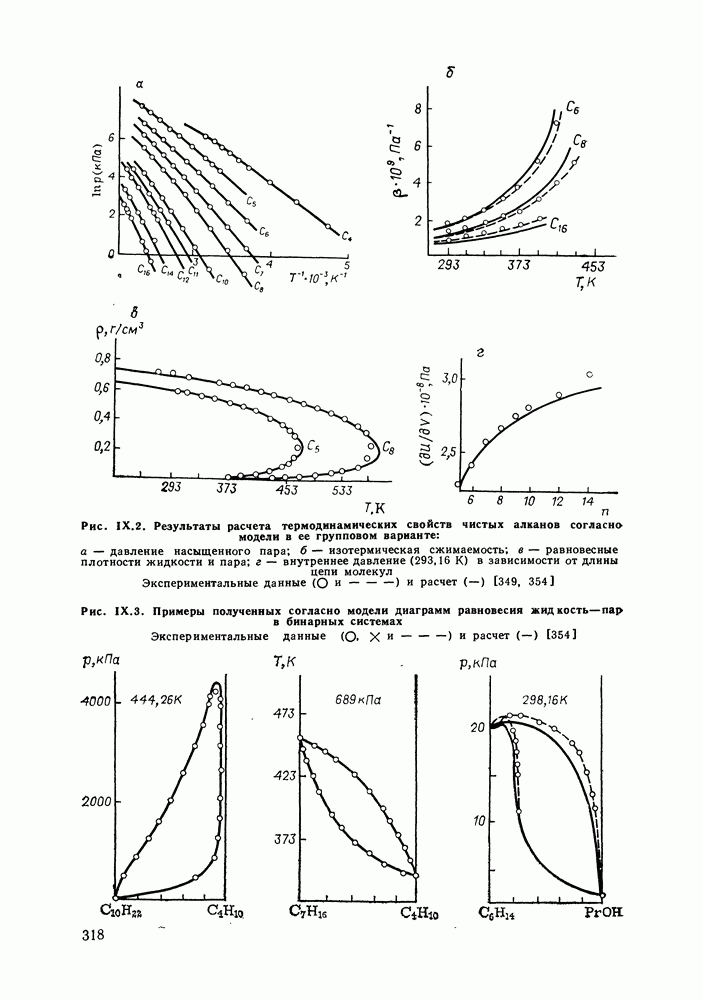
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА