| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
Методы расчета равновесий между жидкостью и паром прошли длительный путь развития от графических и формально-математических способов представления данных до аналитических методов, использующих результаты современных молекулярных теорий растворов [17, 63, 142—145]. В рассматриваемой области можно выделить ряд относительно самостоятельных задач.
Из них главная — это создание теоретически обоснованных моделей, способных с удовлетворительной точностью описывать свойства равновесных фаз, используя минимум экспериментальных данных. Ряд вопросов возникает при оценке эмпирических параметров моделей. Например, какие экспериментальные данные взять за основу и как сформулировать критерий оптимальности параметров, вопрос о температурной зависимости параметров, о выборе одного набора параметров из нескольких возможных и другие. Актуальна задача сопоставления моделей при описании фазовых равновесий определенного типа и при описании разнородных равновесных свойств, а также при описании систем различной химической природы. Наконец, существует потребность в совершенствовании расчетных алгоритмов и создании на их основе достаточно универсальных и быстродействующих программ для ЭВМ.
В последние годы большинство из перечисленных направлений претерпевает интенсивное развитие. Только в области моделирования фазовых равновесий при низких и средних давлениях опубликованы многие сотни работ, содержащих оригинальный вклад в решение проблемы или результаты массовых расчетов с целью сопоставления моделей и оценки их параметров [146].
Остановиться подробно на имеющихся в литературе сведениях в рамках настоящей главы не представляется возможным. Поэтому мы избегали изложения методов, преимущество которых перед уже получившими распространение проблематично или носит частный характер, а ограничились, в основном, описанием хорошо зарекомендовавших себя моделей фазового равновесия и вопросов, связанных с их практическим использованием. Представленный материал, тем не менее, достаточен для моделирования парожидкостного равновесия при низких и средних давлениях на современном уровне.
VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
Общие положения
Число переменных, однозначно задающих состояние гетерогенной системы, определяется правилом фаз (см. разд. 1.5). Так, в распространенном на практике случае  -компонентной двухфазной системы в соответствии с правилом фаз лишь
-компонентной двухфазной системы в соответствии с правилом фаз лишь  интенсивных параметров состояния независимы, могут быть заданы произвольно и полностью определяют состояние системы. Это означает, что существует возможность теоретического расчета всех интересующих нас интенсивных свойств равновесных фаз, если задано
интенсивных параметров состояния независимы, могут быть заданы произвольно и полностью определяют состояние системы. Это означает, что существует возможность теоретического расчета всех интересующих нас интенсивных свойств равновесных фаз, если задано  параметров.
параметров.
Выбор независимых переменных произволен и диктуется содержанием решаемой задачи. При моделировании процессов
дистилляции, например, типичны следующие сочетания независимых и зависимых переменных:

Заданные в (VII. 1)  переменных связаны с другими свойствами равновесной системы термодинамическими условиями фазового равновесия:
переменных связаны с другими свойствами равновесной системы термодинамическими условиями фазового равновесия:

где  фугитивности компонента
фугитивности компонента  в паровой и жидкой фазах;
в паровой и жидкой фазах; 
Решением системы  уравнений (VII.2) можно найти
уравнений (VII.2) можно найти  неизвестных, следовательно, можно найти все искомые термодинамические параметры в задаче (VII. 1). При необходимости список искомых переменных в правой части (VII. 1) можно дополнить другими интересующими нас неизвестными величинами. Для решения новой задачи придется и систему (VI 1.2) дополнить соответствующим числом уравнений, связывающих вновь введенные переменные с уже имеющимися (это могут быть термодинамические уравнения, уравнения материального баланса и другие).
неизвестных, следовательно, можно найти все искомые термодинамические параметры в задаче (VII. 1). При необходимости список искомых переменных в правой части (VII. 1) можно дополнить другими интересующими нас неизвестными величинами. Для решения новой задачи придется и систему (VI 1.2) дополнить соответствующим числом уравнений, связывающих вновь введенные переменные с уже имеющимися (это могут быть термодинамические уравнения, уравнения материального баланса и другие).
Два подхода к расчету парожидкостного равновесия
Для решения системы (VII.2) необходимо в явной форме раскрыть зависимость  от измеряемых параметров
от измеряемых параметров 
Классическая термодинамика, как известно, выражает эту зависимость в виде точных и общих дифференциальных соотношений, но для их интегрирования в каждом конкретном случае необходима информация, отражающая специфику рассматриваемой системы. Такая информация может быть получена в эксперименте или методами статистической физики. По способу ее преобразования в развернутую форму (VI 1.2) из существующих методов расчета фазовых равновесий можно выделить два основных.
I. Характерная особенность этого метода состоит в описании свойств и пара, и жидкости единым термическим уравнением состояния

где V — общий объем;  число молей компонента
число молей компонента 
Фугитивности компонентов выводят при этом из волюметрических свойств фазы с помощью строгих термодинамических соотношений. Например, для паровой фазы справедливо:

или

Здесь  коэффициент сжимаемости смеси;
коэффициент сжимаемости смеси;  ее молярный объем;
ее молярный объем;  парциальный молярный объем
парциальный молярный объем  компонента;
компонента;  молярный объем идеального газа при Тир смеси.
молярный объем идеального газа при Тир смеси.
Уравнения (VII.5) и (VII.6) равноценны, как равноценны и уравнения (VII.3) и (VII.4). При описании фазовых равновесий давление в качестве независимой переменной предпочтительнее объема, поэтому в дальнейшем используются уравнения (VI 1.4) и (VII.6).
Соотношения для фугитивностей компонентов жидкой фазы аналогичны приведенным и получаются из (VII.5), (VII.6) заменой  на
на  Заметим, что пределы интегрирования для
Заметим, что пределы интегрирования для  совпадают и, в соответствии с нормировкой фугитивности —
совпадают и, в соответствии с нормировкой фугитивности —

интегрирование для обеих фаз ведется от (или  состояния идеального разреженного газа.
состояния идеального разреженного газа.
Расчет парожидкостного равновесия состоит в нахождении таких двух наборов  которые в рамках физической модели, описываемой (VI 1.3) или (VI 1.4) при использовании соотношений (VI 1.5) или (VI 1.6), приводят к выполнению условий фазового равновесия (VI 1.2). Расчет равновесий по этому методу представляет собой математически довольно сложную задачу. Алгоритмы расчета можно найти, например, в [9, 1987; 147].
которые в рамках физической модели, описываемой (VI 1.3) или (VI 1.4) при использовании соотношений (VI 1.5) или (VI 1.6), приводят к выполнению условий фазового равновесия (VI 1.2). Расчет равновесий по этому методу представляет собой математически довольно сложную задачу. Алгоритмы расчета можно найти, например, в [9, 1987; 147].
Описанный метод расчета парожидкостного равновесия имеет ряд достоинств. Он строг, так как не содержит никаких упрощающих допущений. Точность его ограничена только точностью используемого уравнения состояния. Метод учитывает влияние давления на свойства обеих фаз, что делает его пригодным для описания равновесий при высоких давлениях и — при использовании специальных алгоритмов — для описания критических свойств смесей. Метод не требует определения отдельного стандартного состояния для компонентов жидкости, поэтому он одинаково
удобен для описания парожидкостного равновесия в системах, содержащих и не содержащих неконденсирующиеся при данных условиях компоненты (газы).
Успех метода, как уже отмечалось, определяется тем, насколько адекватно описываются свойства фаз уравнением состояния. В практике расчета равновесий широкую известность получили уравнения состояния Редлиха-Квонга, Соаве, Пенга-Робинсона, Бенедикта-Вебба-Рубина (подробней см. [9, 148]), позволяющие рассчитывать равновесие жидкость—пар в однокомпонентных, бинарных и многокомпонентных системах в весьма широком интервале внешних условий. Смеси неполярных веществ обычно с удовлетворительной точностью описывают только на основе данных о чистых компонентах. Параметры уравнений для смесей при этом находят с помощью определенных комбинационных правил на основе констант, характеризующих индивидуальные вещества. В более сложных случаях необходима оценка некоторых бинарных параметров по экспериментальным данным для смесей.
Недостатки метода на сегодняшний день связаны с трудностями выбора подходящего уравнения состояния, особенно для систем с полярными компонентами, большим числом эмпирически оцениваемых констант, сложностями вычислительного порядка. В инженерной практике метод используют, главным образом, для расчета равновесных свойств смесей углеводородов и некоторых других компонентов нефтей и природных газов.
Трудности метода, однако, постепенно преодолеваются. Он распространяется на системы сложной химической природы, включающие высокополярные, в том числе ассоциирующие вещества [149, 150]. Например, в одной из недавних работ [150] предложено уравнение состояния (вариант кубического уравнения «цепочки ротаторов»), с помощью которого авторы успешно описали равновесия жидкость—пар, жидкость—жидкость, критические и некоторые другие свойства смесей, состоящих из таких полярных веществ, как вода, уксусная кислота, простые и сложные эфиры, спирт, ацетон, ацетонитрил, хлористый водород и др. Для смесей разнообразной природы обнадеживающие результаты дает также уравнение состояния, основанное на дырочной модели (см. разд. IX.5). Учитывая постоянное совершенствование уравнений состояния, описанный выше метод расчета парожидкостного равновесия можно оценить как безусловно перспективный.
II. При описании фазовых равновесий в области низких и средних давлений наибольшее распространение получил другой термодинамический метод, в котором паровая и жидкая фазы представлены принципиально различными моделями. Такой подход оправдан, так как в области состояний, удаленной от критической, сами эти фазы по ряду свойств резко различны, и в описание каждой могут быть введены упрощения. Например, свойства пара при не слишком высоких давлениях обычно можно
аппроксимировать усеченным вириальным уравнением состояния со вторым вириальным коэффициентом, а при давлениях порядка атмосферного и ниже — уравнением состояния идеального газа. В последнем случае расчет свойств паровой фазы особенно упрощается.
В физической модели жидкой фазы из рассмотрения можно исключить параметр давления, влияние которого на свойства типичной жидкости невелико, сосредоточив основное внимание на важной для задачи фазового равновесия избыточной энергии Гиббса. Именно этот подход к расчету парожидкостного равновесия наиболее развит в настоящее время для смесей разнообразных по природе веществ. Его изложение составляет дальнейшее содержание настоящей главы и гл. VIII.
Связь фугитивностей компонентов с измеряемыми равновесными свойствами фаз в рамках данного метода формально выражают с помощью понятий коэффициента фугитивности компонента в паре  коэффициента активности компонента в жидкости
коэффициента активности компонента в жидкости  и стандартной фугитивности компонента жидкости
и стандартной фугитивности компонента жидкости 

где  активность компонента
активность компонента 
Коэффициенты фугитивности — это мера отклонения свойств паровой фазы от свойств идеальной газовой смеси, во всем интервале составов которой  [в реальном паре, как следует из (VI 1.7),
[в реальном паре, как следует из (VI 1.7),  при
при  Коэффициенты активности суммарно выражают отклонение свойств жидкой фазы от свойств идеального раствора, во всем интервале составов которого
Коэффициенты активности суммарно выражают отклонение свойств жидкой фазы от свойств идеального раствора, во всем интервале составов которого  Величины обеспечивают переход от активности к фугитивности.
Величины обеспечивают переход от активности к фугитивности.
Поскольку метод предполагает знание уравнения состояния паровой фазы, величины  связывают с
связывают с  через ее объемные свойства: из (VI 1.6) и (VI 1.8) следуют строгие соотношения для расчета:
через ее объемные свойства: из (VI 1.6) и (VI 1.8) следуют строгие соотношения для расчета:
коэффициентов фугитивности компонентов паровой смеси —

коэффициентов фугитивности чистых веществ —

где  определяемые с помощью уравнения состояния парциальный молярный и молярный объемы компонента в паре;
определяемые с помощью уравнения состояния парциальный молярный и молярный объемы компонента в паре;  давление насыщенного пара чистого компонента при температуре раствора.
давление насыщенного пара чистого компонента при температуре раствора.
Для жидкой фазы полное уравнение состояния в рамках данного подхода не рассматривается и нет средства прямо связать 
с  Взаимосвязь этих величин устанавливается более сложным путем с использованием некоторых минимальных экспериментальных данных о равновесии жидкость—пар в сочетании с условиями фазового равновесия и теми соотношениями для
Взаимосвязь этих величин устанавливается более сложным путем с использованием некоторых минимальных экспериментальных данных о равновесии жидкость—пар в сочетании с условиями фазового равновесия и теми соотношениями для  и которые дает термодинамика.
и которые дает термодинамика.
В соответствии с определениями фугитивности и активности

и уравнением (VI1.9)

где  стандартные значения химического потенциала.
стандартные значения химического потенциала.
Уравнение (VII. 12) выявляет смысл термина «стандартная фугитивность»: величина  в соотношении (VI 1.9) не связана с концентрацией раствора, а зависит только от выбора стандартных состояний компонентов жидкости. Выбор таких состояний одновременно задает численные значения
в соотношении (VI 1.9) не связана с концентрацией раствора, а зависит только от выбора стандартных состояний компонентов жидкости. Выбор таких состояний одновременно задает численные значения 
Симметричная и несимметричная нормировка коэффициентов активности
Если все компоненты при температурах системы могут быть сконденсированы, за стандартное состояние для каждого компонента жидкой фазы удобно принять его состояние в чистом жидком виде при температуре и давлении раствора, т. е. принять симметричную нормировку коэффициентов активности

и определить стандартную фугитивность как фугитивность чистой жидкости  при температуре и давлении раствора:
при температуре и давлении раствора:

При таком определении величина зависит только от свойств чистого компонента.
Способ нахождения указывают условия фазового равновесия — при равновесии  таким образом стандартную фугитивность жидкого компонента можно связать с параметрами его равновесного пара. Правда, найти непосредственно
таким образом стандартную фугитивность жидкого компонента можно связать с параметрами его равновесного пара. Правда, найти непосредственно  таким путем нельзя, так как при температуре
таким путем нельзя, так как при температуре  равновесное давление чистого компонента
равновесное давление чистого компонента  обычно не совпадает с давлением раствора. Для чистого вещества, находящегося в равновесии с собственным паром, справедливо:
обычно не совпадает с давлением раствора. Для чистого вещества, находящегося в равновесии с собственным паром, справедливо:

Пересчитав  с помощью (111.69) на давление раствора
с помощью (111.69) на давление раствора  и вспомнив (VII. 14), получим строгое соотношение для стандартной фугитивности
и вспомнив (VII. 14), получим строгое соотношение для стандартной фугитивности

где  молярный объем чистой жидкости
молярный объем чистой жидкости  при температуре раствора.
при температуре раствора.
Экспоненциальный член в (VII. 15), учитывающий влияние давления на фугитивность чистой жидкости, носит название поправки Пойнтинга [151].
Если рассматриваемый интервал давлений не слишком велик, то, ввиду малой сжимаемости жидкостей, можно пренебречь зависимостью  от
от  и проинтегрировать (VII. 15):
и проинтегрировать (VII. 15):

Соотношение  - основное рабочее соотношение для расчета стандартной фугитивности конденсирующегося компонента.
- основное рабочее соотношение для расчета стандартной фугитивности конденсирующегося компонента.
Данное выше определение стандартного состояния и стандартной фугитивности не подходит для компонентов, критическая температура которых ниже температуры раствора и которые, следовательно, при температуре раствора не могут существовать как чистая жидкость. Если критическая температура компонента лишь ненамного ниже температуры раствора, определения (VII. 13) и (VII.16), отвечающие симметричной нормировке  обычно все же сохраняют, экстраполируя
обычно все же сохраняют, экстраполируя  из докритической области (для жидкостей, подчиняющихся трехпараметрической теореме о соответственных состояниях [152], возможна также оценка
из докритической области (для жидкостей, подчиняющихся трехпараметрической теореме о соответственных состояниях [152], возможна также оценка  в околокритической области с помощью корреляции [153]).
в околокритической области с помощью корреляции [153]).
Далекая экстраполяция такого рода становится слишком неопределенной, и в общем случае в системе с неконденсирующимися компонентами приходится использовать так называемую несимметричную нормировку коэффициентов активности, которая состоит в следующем. Для каждого из конденсирующихся компонентов сохраняется определение стандартного состояния как состояния чистой жидкости, и остаются справедливыми соотношения  За стандартное состояние каждого неконденсирующегося компонента принимают гипотетическое состояние чистого компонента, совпадающее с его состоянием в бесконечно разбавленном растворе при давлении и температуре системы; коэффициент активности компонента в условиях предельного разбавления принимается за единицу:
За стандартное состояние каждого неконденсирующегося компонента принимают гипотетическое состояние чистого компонента, совпадающее с его состоянием в бесконечно разбавленном растворе при давлении и температуре системы; коэффициент активности компонента в условиях предельного разбавления принимается за единицу:

[здесь и далее  помечены величины, специфические для неконденсирующихся компонентов].
помечены величины, специфические для неконденсирующихся компонентов].
В бинарном растворе неконденсирующегося компонента  в жидком растворителе
в жидком растворителе  для стандартной фугитивности первого имеем [см. (VI 1.9) и (VI 1.17)]:
для стандартной фугитивности первого имеем [см. (VI 1.9) и (VI 1.17)]:

где  константа Генри, характеризующая разбавленный раствор
константа Генри, характеризующая разбавленный раствор 
Поскольку экспериментально константа Генри определяется в равновесных условиях — при давлении пара чистого растворителя, необходим пересчет экспериментальной  на давление раствора:
на давление раствора:

где  — парциальный молярный объем компонента
— парциальный молярный объем компонента  при бесконечном разбавлении в жидком растворителе
при бесконечном разбавлении в жидком растворителе 
При допущении  уравнение (VII.18) упрощается:
уравнение (VII.18) упрощается:

Величины  определяются природой не только растворенного вещества, но и растворителя, это характеристики раствора. Поэтому практически определить стандартную фугитивность неконденсирующегося компонента существенно сложнее, чем стандартную фугитивность конденсирующегося. Для определения констант Генри применяют специальные экспериментальные методы, сходные с методами измерения предельных коэффициентов активности [22], часто эти величины оценивают по данным о растворимости газов в жидкостях [154], для них предложены корреляционные соотношения [153, 155, 156], публикуются таблицы экспериментальных значений [143, 156—158].
определяются природой не только растворенного вещества, но и растворителя, это характеристики раствора. Поэтому практически определить стандартную фугитивность неконденсирующегося компонента существенно сложнее, чем стандартную фугитивность конденсирующегося. Для определения констант Генри применяют специальные экспериментальные методы, сходные с методами измерения предельных коэффициентов активности [22], часто эти величины оценивают по данным о растворимости газов в жидкостях [154], для них предложены корреляционные соотношения [153, 155, 156], публикуются таблицы экспериментальных значений [143, 156—158].
Константа Генри может быть найдена и непосредственно по обрабатываемым данным о равновесии жидкость—пар, если они охватывают область разбавленных растворов неконденсирующегося компонента. Наконец, при корреляции данных о равновесии в средней области концентраций с помощью уравнения для коэффициентов активности можно приближенно оценить  одновременно с параметрами уравнения — как дополнительный варьируемый параметр. Некоторые полуэмпирические соотношения предложены и для оценки величин
одновременно с параметрами уравнения — как дополнительный варьируемый параметр. Некоторые полуэмпирические соотношения предложены и для оценки величин  [153, 159].
[153, 159].
В многокомпонентной системе в общем случае может быть несколько неконденсирующихся и конденсирующихся компонентов. Нетрудно заметить, что в  при этом возникает неопределенность. К какому растворителю
при этом возникает неопределенность. К какому растворителю  отнести величины
отнести величины  Поступают по-разному: иногда в качестве компонента
Поступают по-разному: иногда в качестве компонента  выбирают любой из присутствующих
выбирают любой из присутствующих
в смеси конденсирующихся компонентов, в других случаях под компонентом  понимают смешанный растворитель с таким же соотношением концентраций конденсирующихся компонентов, что и в рассматриваемом растворе. Различные методики расчета парожидкостного равновесия с участием надкритических компонентов описаны в [143, 144, 157, 160].
понимают смешанный растворитель с таким же соотношением концентраций конденсирующихся компонентов, что и в рассматриваемом растворе. Различные методики расчета парожидкостного равновесия с участием надкритических компонентов описаны в [143, 144, 157, 160].
Следует отметить, что хотя описанный метод находит применение, он не пользуется большой популярностью [9]. Помимо трудностей, связанных с оценкой значений  и неопределенностей, возникающих в системах с несколькими растворителями, при моделировании равновесий с помощью уравнений для коэффициентов активности возникает еще одно неудобство. Классические формы этих уравнений выведены в предположении симметричной нормировки
и неопределенностей, возникающих в системах с несколькими растворителями, при моделировании равновесий с помощью уравнений для коэффициентов активности возникает еще одно неудобство. Классические формы этих уравнений выведены в предположении симметричной нормировки  и использование несимметричной требует соответствующей модификации модели жидкой фазы. Более перспективен для целей описания равновесий в системах с неконденсирующимися компонентами, вероятно, подход, основанный на едином уравнении состояния для пара и жидкости: перечисленные проблемы в нем попросту не возникают.
и использование несимметричной требует соответствующей модификации модели жидкой фазы. Более перспективен для целей описания равновесий в системах с неконденсирующимися компонентами, вероятно, подход, основанный на едином уравнении состояния для пара и жидкости: перечисленные проблемы в нем попросту не возникают.
Экспериментальные и рассчитанные по модели жидкой фазы коэффициенты активности
Для обоих способов нормировки коэффициентов активности условия парожидкостного равновесия (VI 1.2) с учетом (VI 1.8) и (VI 1.9) принимают вид:

Если имеются полные данные о равновесии жидкость—пар  , то уравнения (VII.20) в сочетании с условиями нормировки и соотношениями для
, то уравнения (VII.20) в сочетании с условиями нормировки и соотношениями для  позволяют определить экспериментальные значения коэффициентов активности
позволяют определить экспериментальные значения коэффициентов активности

которые относятся к давлению и температуре раствора и могут быть пересчитаны на другие  с помощью соотношений (III.79а) и (III.796).
с помощью соотношений (III.79а) и (III.796).
В случае симметричной нормировки коэффициентов активности — в дальнейшем будем использовать только ее — с учетом (VII. 16) и (VI 1.20) условия равновесия и соотношение для коэффициентов активности можно записать иначе:

где

Коэффициент  суммарно учитывает неидеальность паровой фазы и поправку Пойнтинга.
суммарно учитывает неидеальность паровой фазы и поправку Пойнтинга.
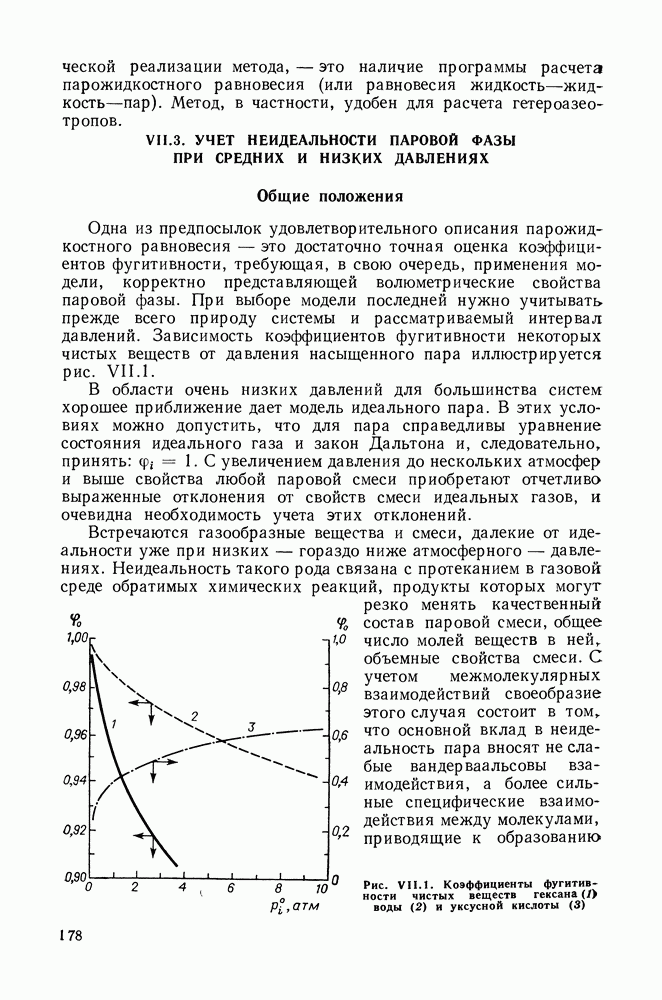
При давлениях порядка атмосферного и ниже в отсутствие сильно ассоциирующих в паре компонентов отклонение свойств паровой фазы от идеальности обычно невелико  Поправка Пойнтинга с неидеальностью пара не связана, однако в этих условиях она также близка к единице Поэтому при невысоких давлениях часто можно принять:
Поправка Пойнтинга с неидеальностью пара не связана, однако в этих условиях она также близка к единице Поэтому при невысоких давлениях часто можно принять:

При моделировании парожидкостного равновесия необходимо иметь способ расчета  по свойствам жидкой фазы, а не по данным о равновесии. Такой способ дают полуэмпирические уравнения, связывающие
по свойствам жидкой фазы, а не по данным о равновесии. Такой способ дают полуэмпирические уравнения, связывающие  с параметрами жидкости на основе ее физической модели. Математическая форма уравнений должна обеспечивать качественное соответствие экспериментальных и расчетных зависимостей для
с параметрами жидкости на основе ее физической модели. Математическая форма уравнений должна обеспечивать качественное соответствие экспериментальных и расчетных зависимостей для  Соответствие же значений экспериментальных и расчетных
Соответствие же значений экспериментальных и расчетных  устанавливается при оценке параметров модели по имеющимся экспериментальным данным о системе.
устанавливается при оценке параметров модели по имеющимся экспериментальным данным о системе.
Если модель дает аналитическое выражение, в явной форме связывающее избыточную энергию Гиббса  с параметрами
с параметрами  то соответствующее аналитическое выражение для
то соответствующее аналитическое выражение для  нетрудно получить, так как:
нетрудно получить, так как:

где  число молей компонента
число молей компонента 
Можно также воспользоваться эквивалентным соотношением, записанным через производные по составу:

Уравнения для  выведенные таким путем, независимо от математической формы и степени физической обоснованности, дают термодинамические согласованные (подчиняющиеся изотермо-изобар ному уравнению Гиббса-Дюгема) концентрационные зависимости расчетных коэффициентов активности.
выведенные таким путем, независимо от математической формы и степени физической обоснованности, дают термодинамические согласованные (подчиняющиеся изотермо-изобар ному уравнению Гиббса-Дюгема) концентрационные зависимости расчетных коэффициентов активности.
Модели раствора, предназначенные для описания фазовых равновесий при средних и низких давлениях, учитывают концентрационную, а часто и температурную зависимость  но не рассматривают влияние параметра давления на эти величины — на том основании, что в области состояний, удаленной от критической, давление мало влияет на свойства конденсированных фаз. Допущение
но не рассматривают влияние параметра давления на эти величины — на том основании, что в области состояний, удаленной от критической, давление мало влияет на свойства конденсированных фаз. Допущение  в данном случае приемлемо, так как вызванное им несоответствие между реальными свойствами системы и ее математическим описанием фактически перекрывается прочими
в данном случае приемлемо, так как вызванное им несоответствие между реальными свойствами системы и ее математическим описанием фактически перекрывается прочими
погрешностями моделей фаз и погрешностями экспериментальных данных, используемых для оценки параметров моделей. Таким образом, при средних и низких давлениях экспериментальные  и рассчитанные по модели
и рассчитанные по модели  считаются идентичными.
считаются идентичными.
Конкретные формы полуэмпирических уравнений, описывающих концентрационную и температурную зависимость коэффициентов активности, рассматриваются в разд. VII.4-VII.8 и гл. VIII. Методы оценки параметров этих уравнений по экспериментальным данным о фазовых равновесиях кратко излагаются в разд. VII.6.
Различные полуэмпирические соотношения используются также для расчета молярных и парциальных молярных объемов компонентов пара и коэффициентов фугитивности. Эти соотношения будут описаны в разд. VI 1.3.
Корреляционные соотношения для чистых веществ
Для описания температурной зависимости давлений насыщенных паров чистых веществ используют простые эмпирические уравнения, многие из которых являются частным случаем уравнения

где  константы, характерные для данного вещества.
константы, характерные для данного вещества.
Большое применение нашло уравнение Антуана:

константы  которого известны для многих веществ (см. разд. II.3).
которого известны для многих веществ (см. разд. II.3).
Температурная зависимость молярных объемов жидких веществ обычно с достаточной точностью описывается как квадратичная или линейная

Константы 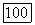 определяют по экспериментальным данным о молярных объемах веществ в интервале температур, в котором предполагается проводить расчет парожидкостного равновесия. Таких данных, особенно для повышенных температур, часто нет. Поэтому для расчета
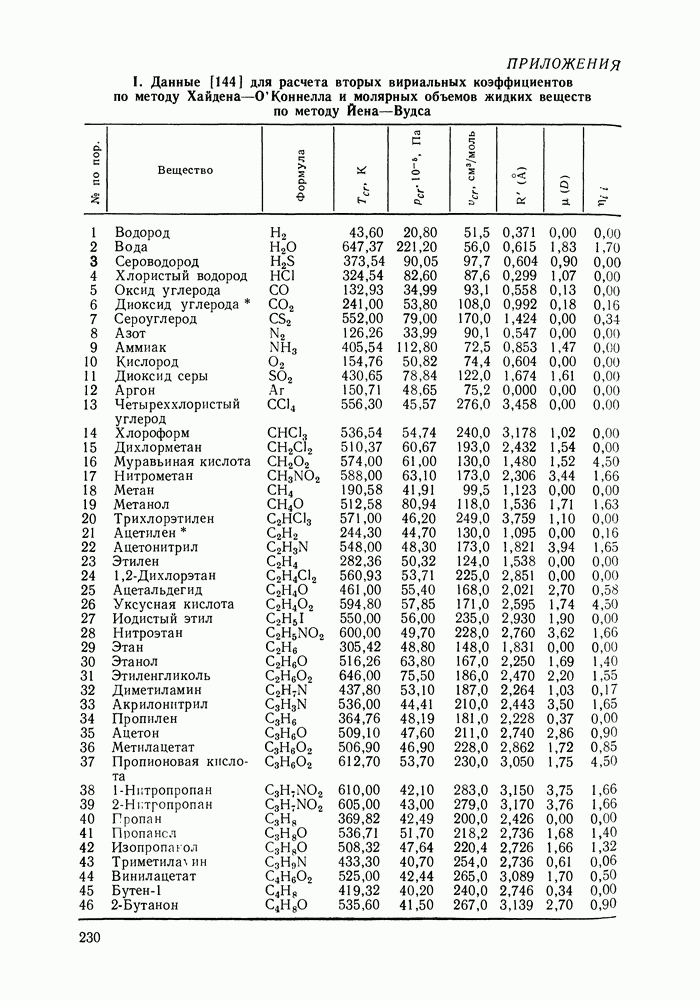
определяют по экспериментальным данным о молярных объемах веществ в интервале температур, в котором предполагается проводить расчет парожидкостного равновесия. Таких данных, особенно для повышенных температур, часто нет. Поэтому для расчета 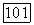 широко используют различные корреляции [9], в частности, Йена и Вудса [162], в которой жидкофазные молярные объемы веществ связаны с их критическими параметрами:
широко используют различные корреляции [9], в частности, Йена и Вудса [162], в которой жидкофазные молярные объемы веществ связаны с их критическими параметрами:

где

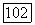 критический фактор сжимаемости;
критический фактор сжимаемости; 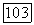 критические давление, объем и температура;
критические давление, объем и температура; 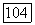 приведенная температура.
приведенная температура.
Молярные объемы жидких веществ, необходимые для расчета поправки Пойнтинга и входящие в некоторые уравнения для коэффициентов активности (например, в уравнение Вильсона), в отличие от 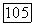 сравнительно слабо влияют на равновесные характеристики систем и нет нужды добиваться высокой точности их расчета. Погрешность в
сравнительно слабо влияют на равновесные характеристики систем и нет нужды добиваться высокой точности их расчета. Погрешность в 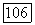 которую дает корреляция Йена и Вудса при средних и низких давлениях, вполне приемлема при расчете парожидкостного равновесия.
которую дает корреляция Йена и Вудса при средних и низких давлениях, вполне приемлема при расчете парожидкостного равновесия.
Общие термодинамические соотношения, приведенные ранее, вместе с соотношениями для расчета 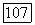 в конкретных системах, достаточны для решения задачи Барожидкостного равновесия. Однако решить ее в виде однократной последовательности математических действий возможно только в немногих простейших случаях. Как правило, приходится использовать метод последовательных приближений и проводить вычисления на ЭВМ. Объем вычислений и затраты машинного времени сильно зависят от применяемой математической методики, или алгоритма расчета равновесия. Некоторые из возможных методик описываются в разд. VI 1.2.
в конкретных системах, достаточны для решения задачи Барожидкостного равновесия. Однако решить ее в виде однократной последовательности математических действий возможно только в немногих простейших случаях. Как правило, приходится использовать метод последовательных приближений и проводить вычисления на ЭВМ. Объем вычислений и затраты машинного времени сильно зависят от применяемой математической методики, или алгоритма расчета равновесия. Некоторые из возможных методик описываются в разд. VI 1.2.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
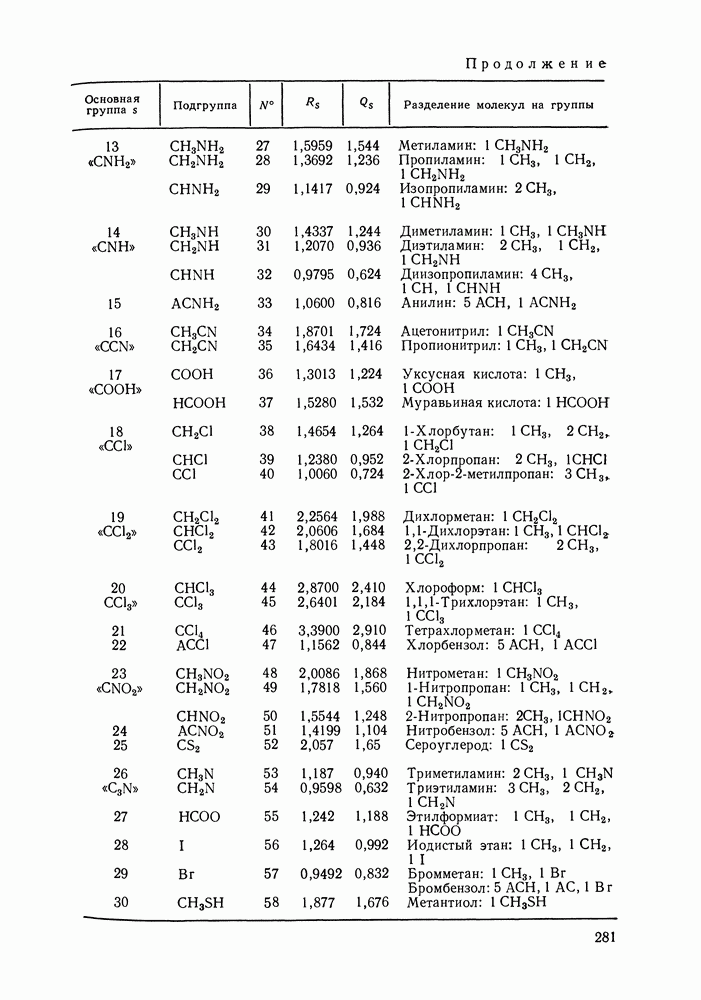
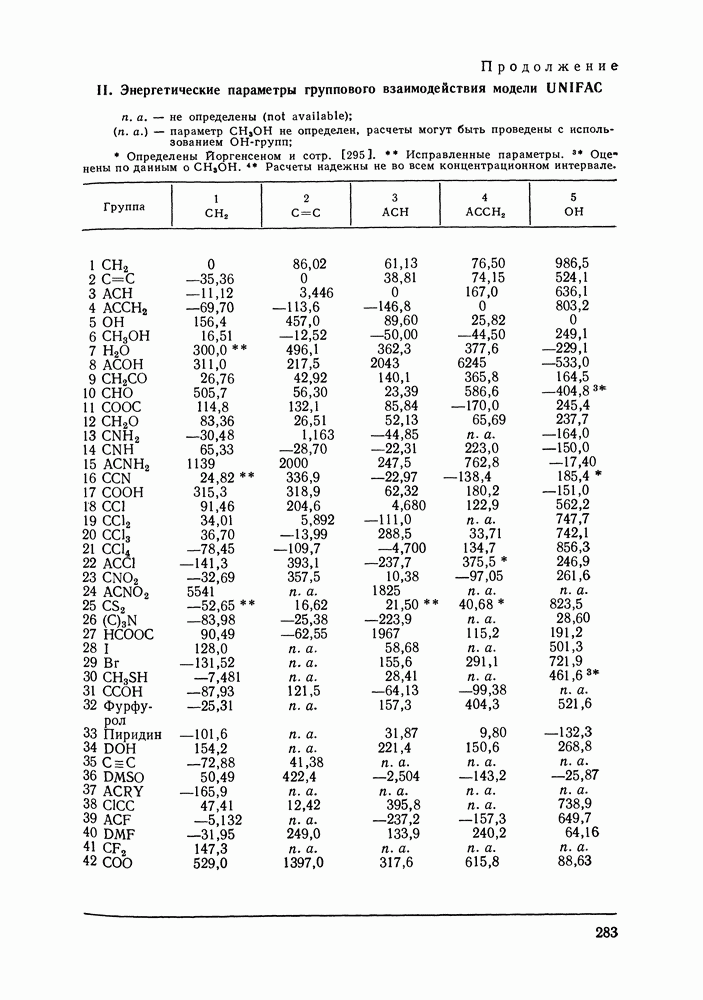
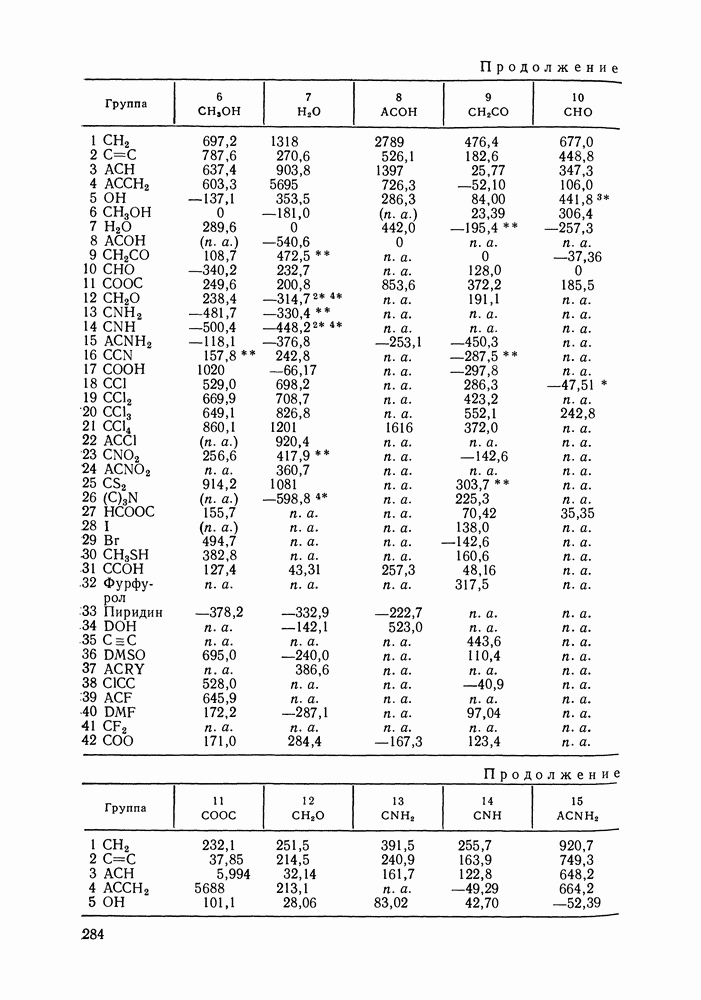
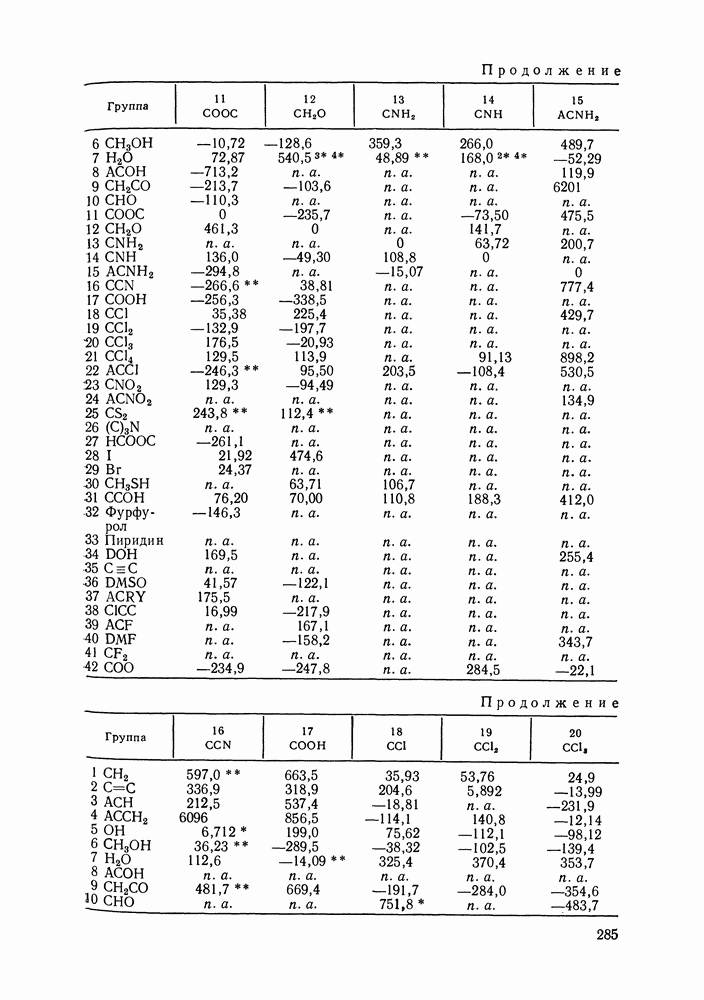
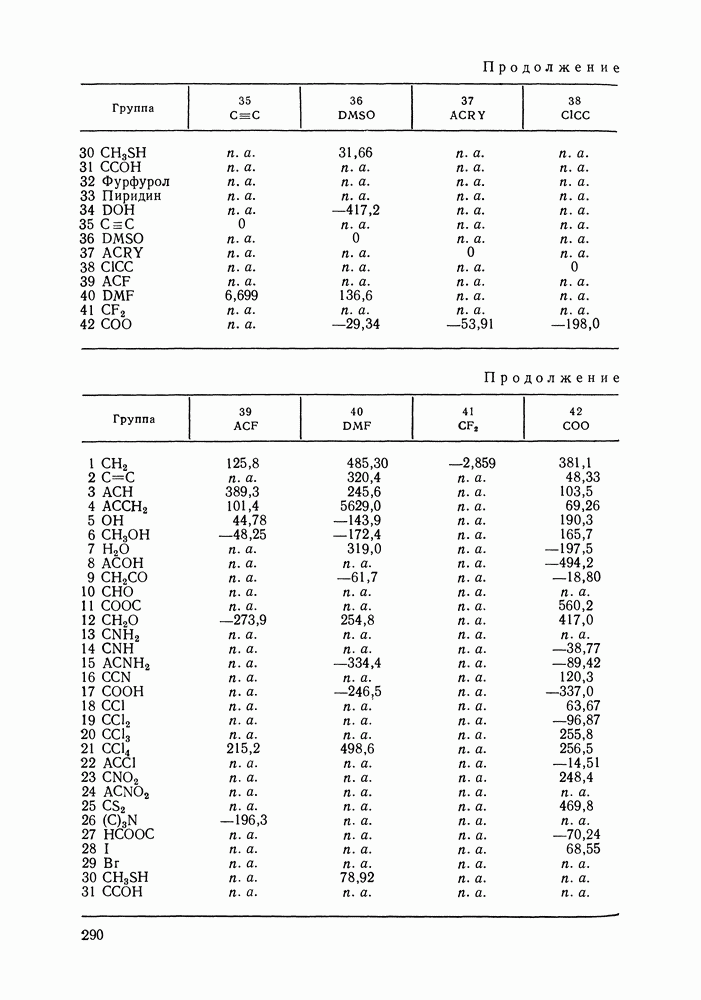
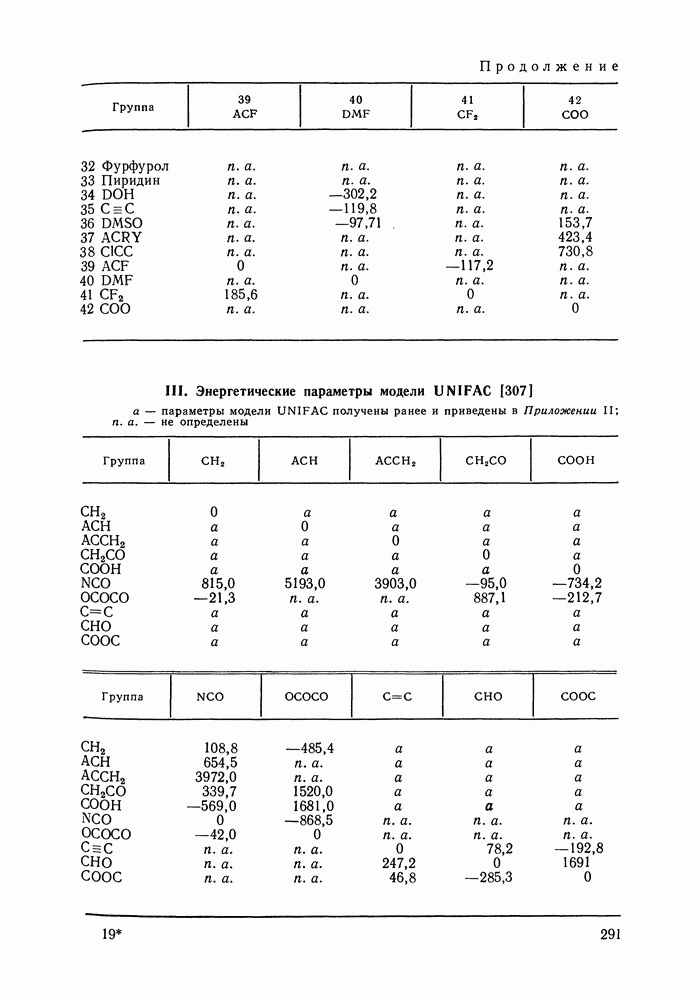
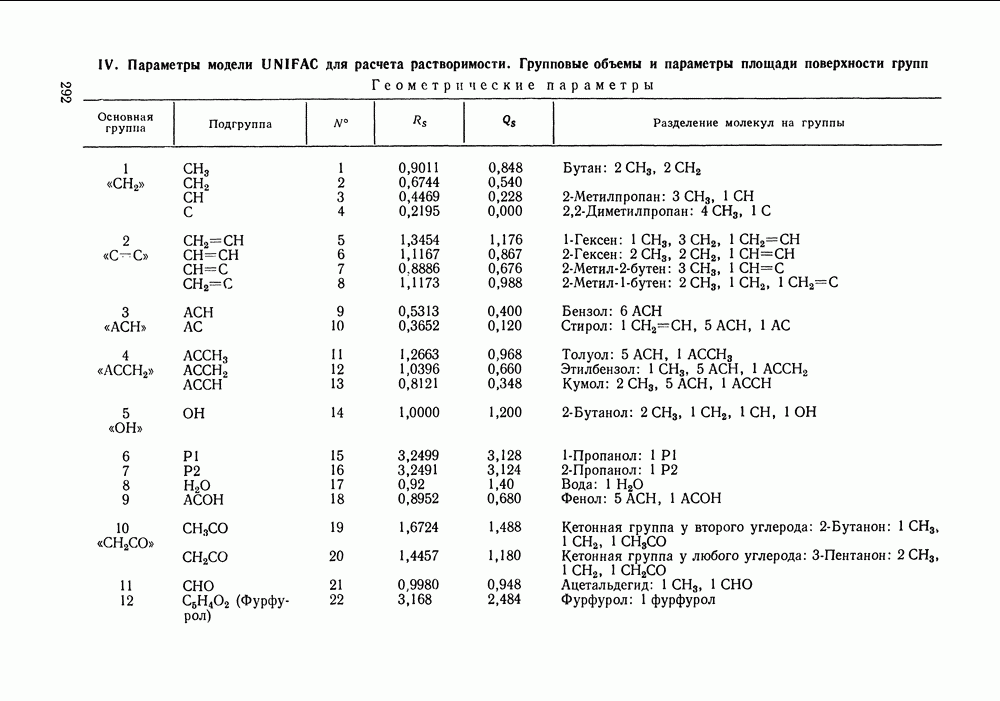
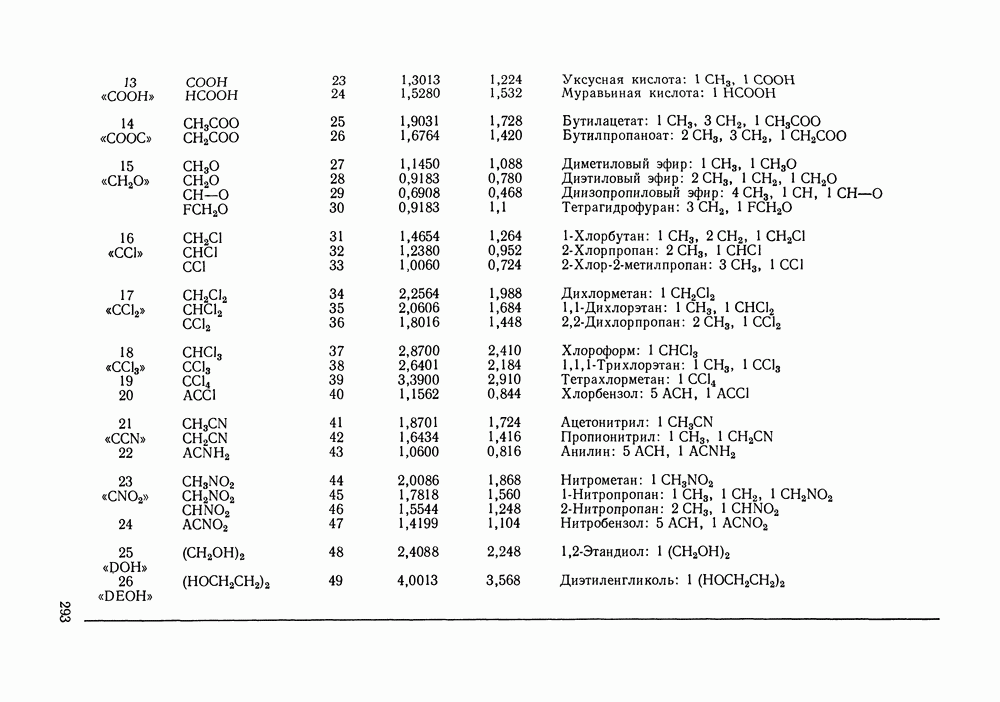
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА