| << Предыдущий параграф |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
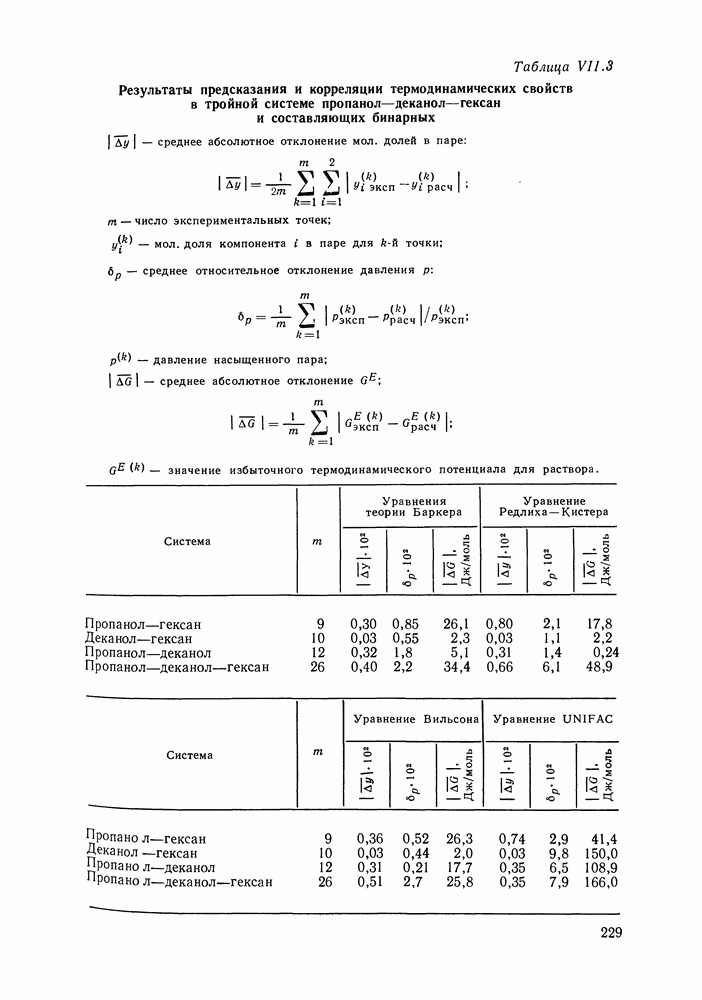
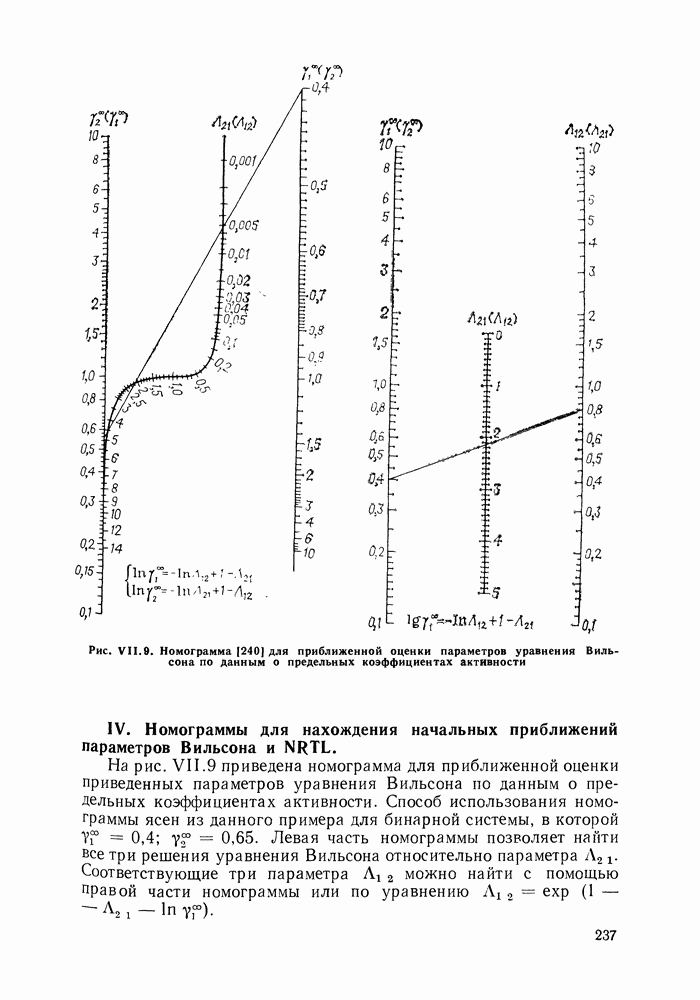
IX.6. ПРИМЕРЫ РАСЧЕТА
Рассмотрим более подробно процедуру оценки параметров и расчеты термодинамических свойств для чистого сероводорода и для смесей сероводород—алкан.
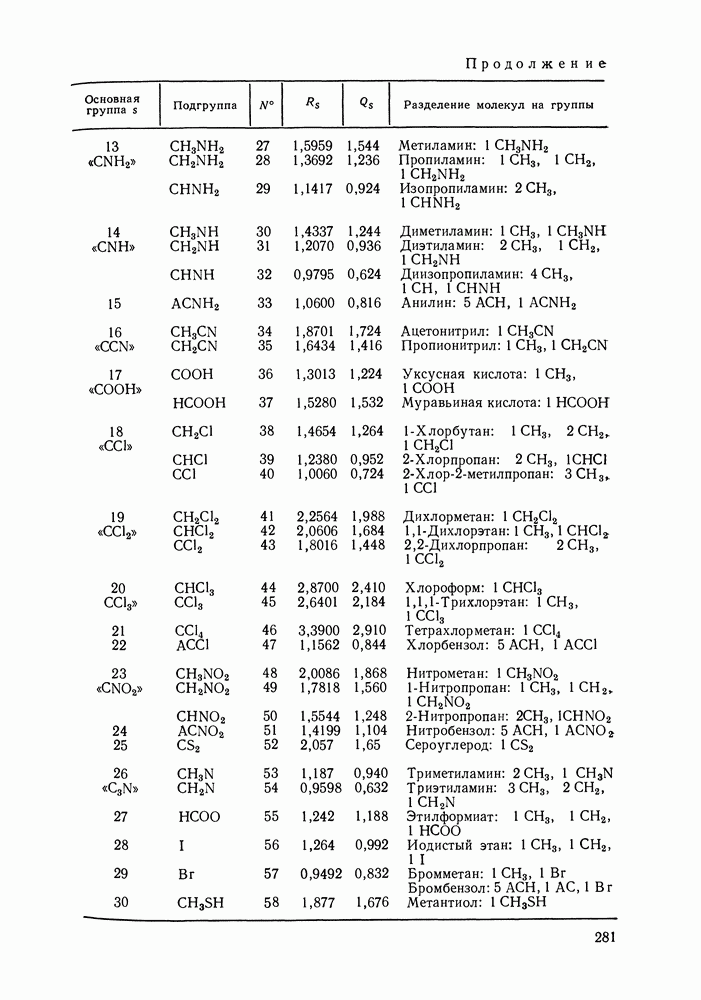
В молекулах сероводорода выделяем две  -группы, а также
-группы, а также  -группу. Полагаем, что суммарная площадь поверхности двух
-группу. Полагаем, что суммарная площадь поверхности двух  -групп
-групп  причем фактор объемности
причем фактор объемности  для молекулы в целом считаем равным нулю. Напомним, что в уравнение модели входят величины
для молекулы в целом считаем равным нулю. Напомним, что в уравнение модели входят величины  лишь для молекул, а не для образующих их групп.
лишь для молекул, а не для образующих их групп.
Если принять формально  то для выполнения условия
то для выполнения условия  следует положить
следует положить  Тогда из
Тогда из  вытекает
вытекает  что в сочетании с
что в сочетании с  и с требованием
и с требованием  позволяет рассчитывать площадь
позволяет рассчитывать площадь  -группы при известных
-группы при известных 
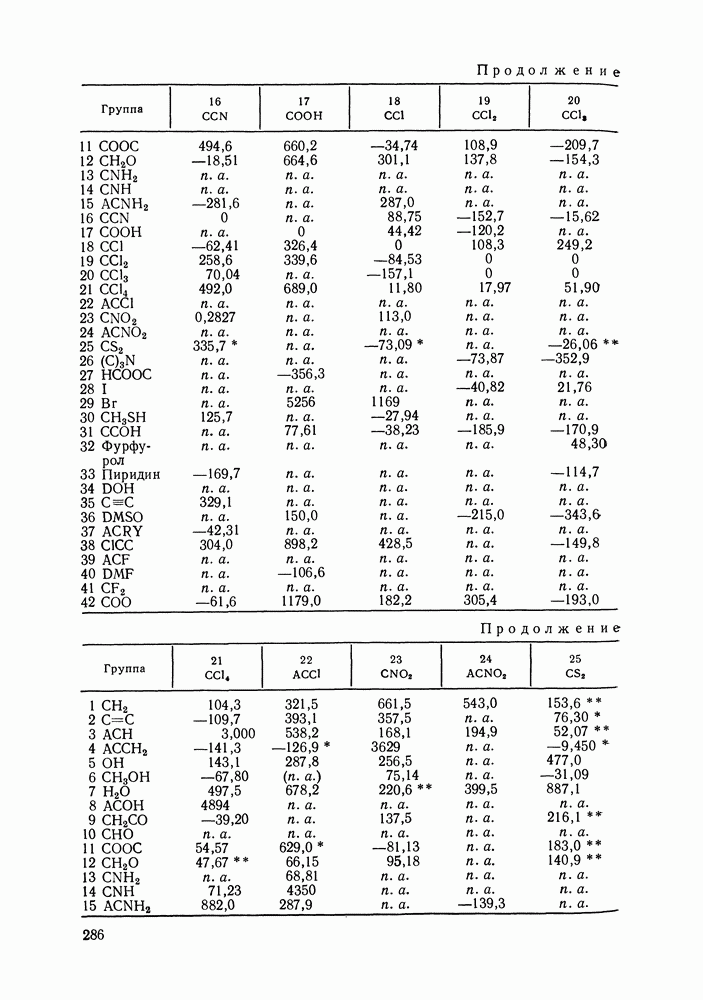
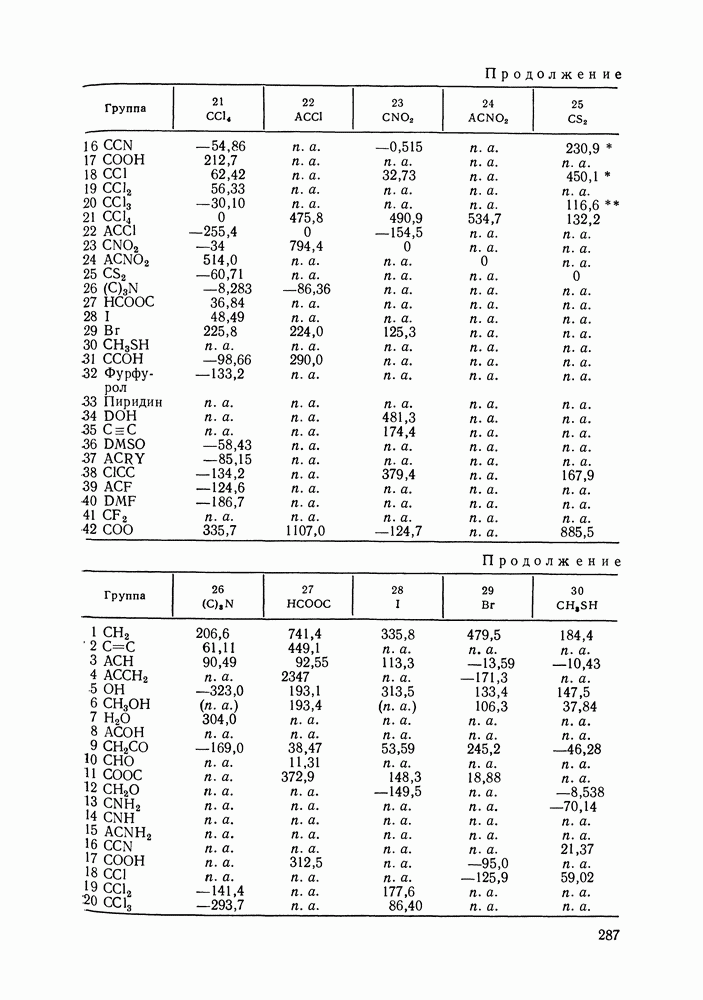
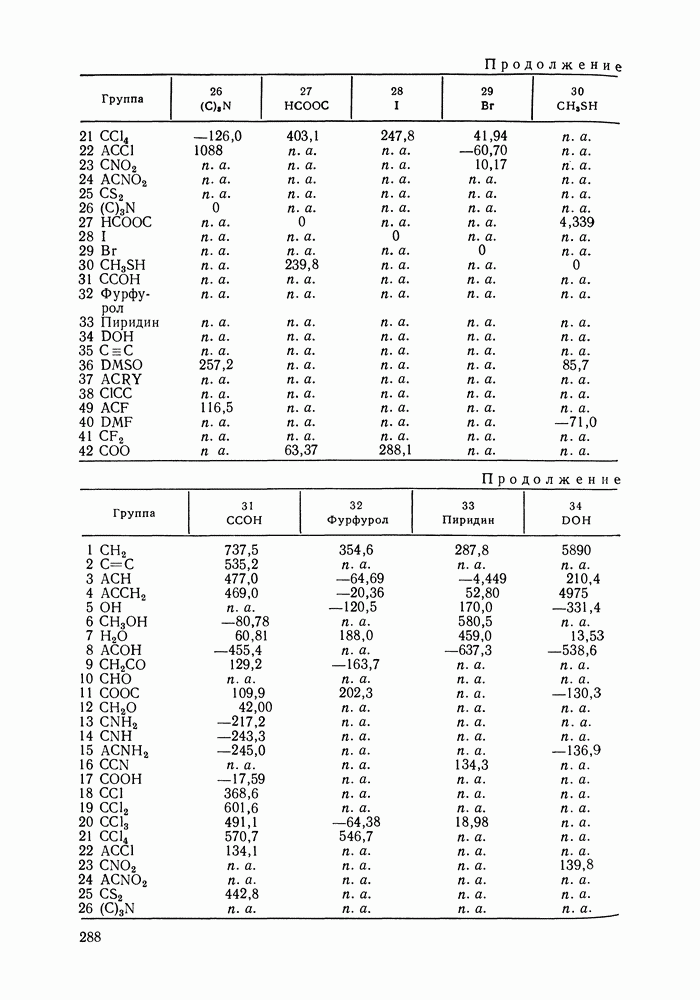
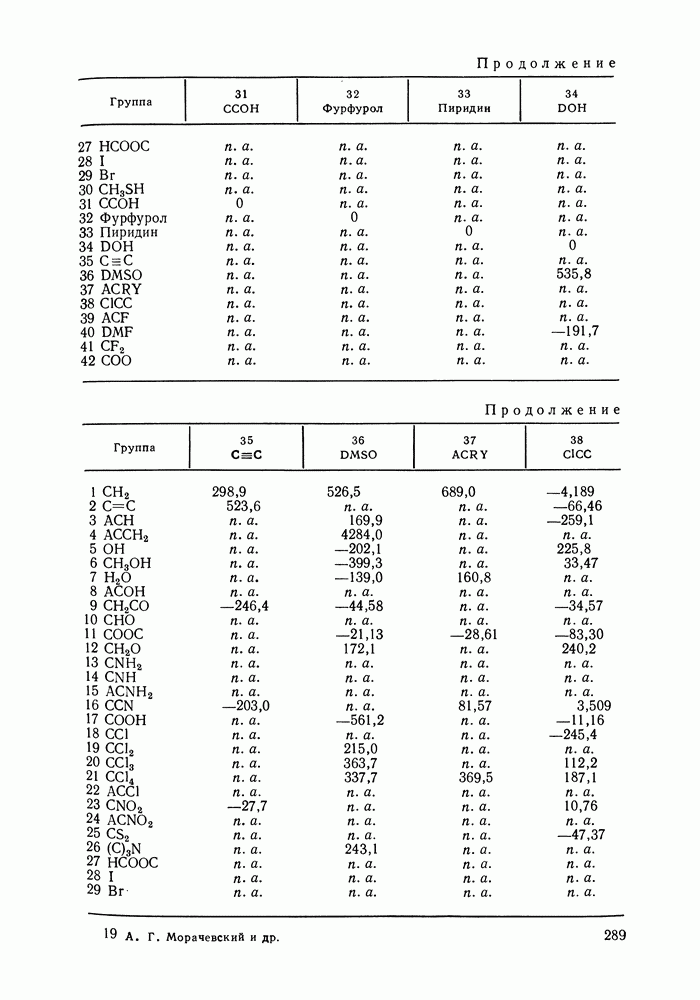
Различные способы контакта молекул считали энергетически эквивалентными, за исключением случаев образования  -контактов. Принимали:
-контактов. Принимали:
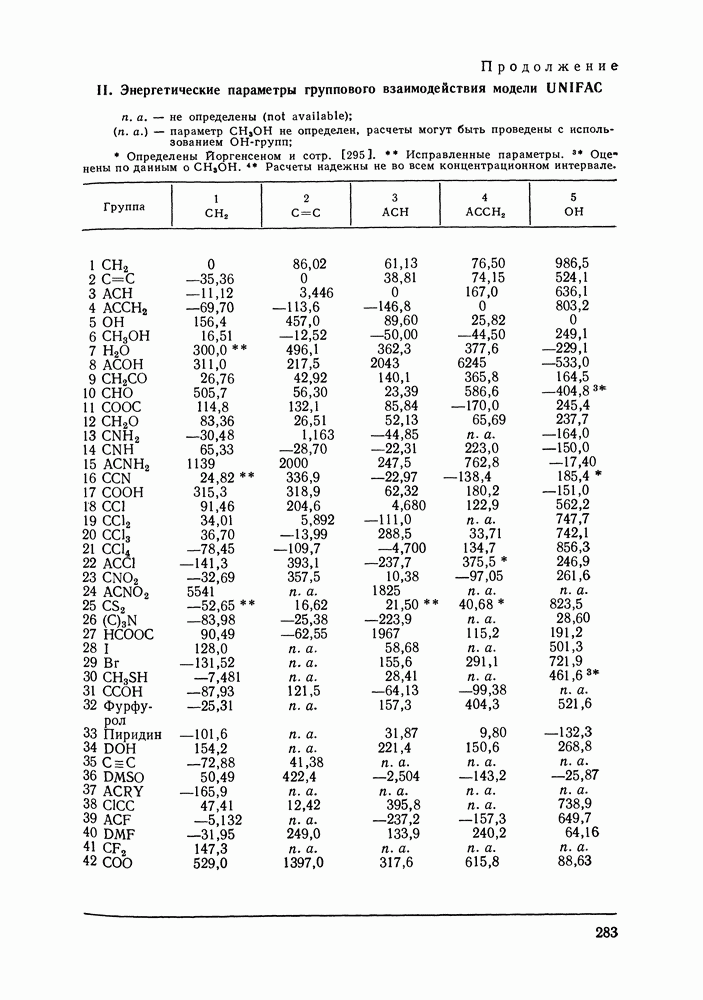
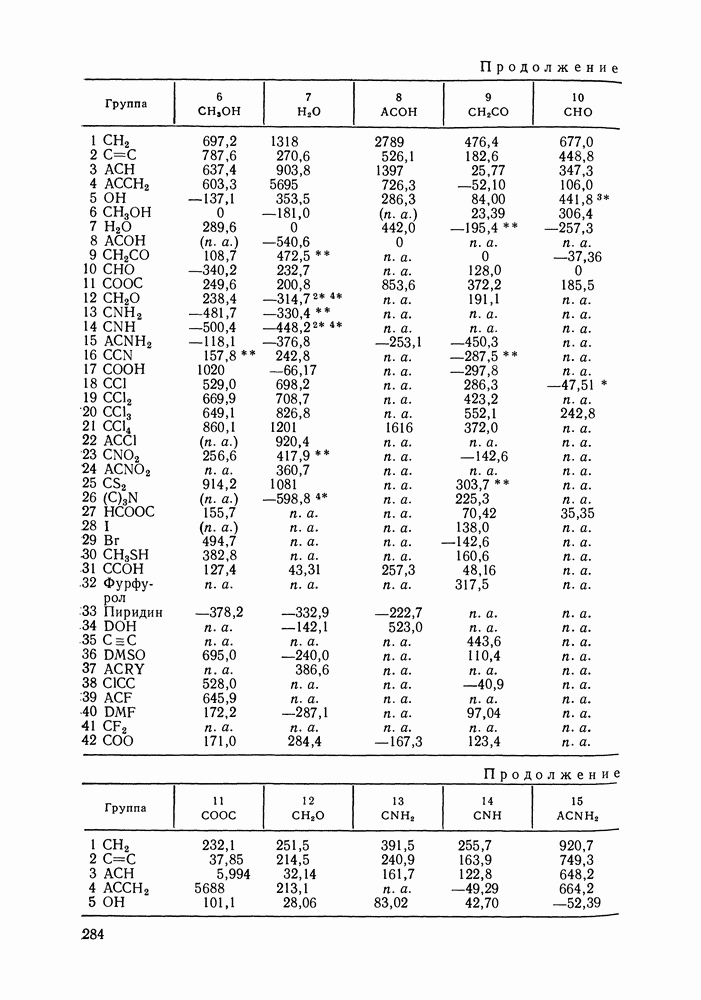
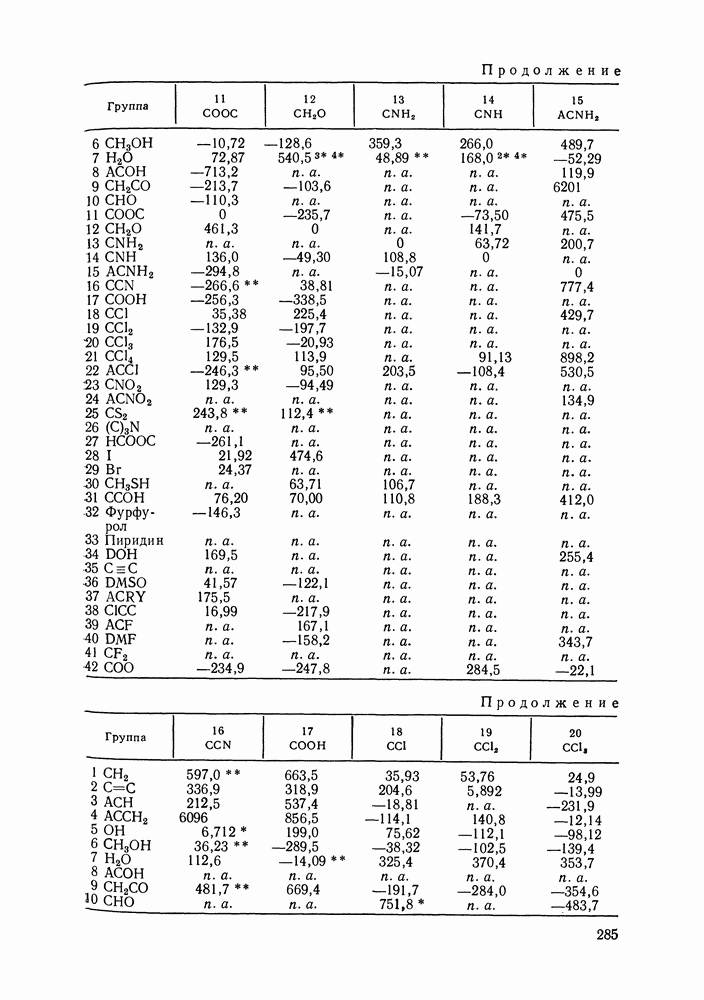
для энергий взаимодействия групп

для энергий взаимообмена

Аналогичные соотношения выполняются для энтальпий и теплоемкостей взаимообмена 
С учетом сказанного, для вычисления термодинамических функций сероводорода необходимо располагать следующими параметрами модели:  -дырка,
-дырка,  -дырка»
-дырка»  Их оценивали по экспериментальным данным о давлении насыщенного пара чистого сероводорода в интервале температур
Их оценивали по экспериментальным данным о давлении насыщенного пара чистого сероводорода в интервале температур  а также о плотностях жидкой и паровой фаз в интервале температур
а также о плотностях жидкой и паровой фаз в интервале температур  К [355]. При этом использовали следующую целевую функцию:
К [355]. При этом использовали следующую целевую функцию:

Здесь — плотность жидкости;  плотность пара;
плотность пара;  -давление насыщенного пара; все при
-давление насыщенного пара; все при  экспериментальной температуре;
экспериментальной температуре;  индексы расч. и эксп. обозначают рассчитанные по модели и экспериментальные величины; для весовых множителей
индексы расч. и эксп. обозначают рассчитанные по модели и экспериментальные величины; для весовых множителей  на основании опыта проведенных расчетов принято
на основании опыта проведенных расчетов принято  (такое значение весового множителя можно рекомендовать и для прочих индивидуальных веществ).
(такое значение весового множителя можно рекомендовать и для прочих индивидуальных веществ).
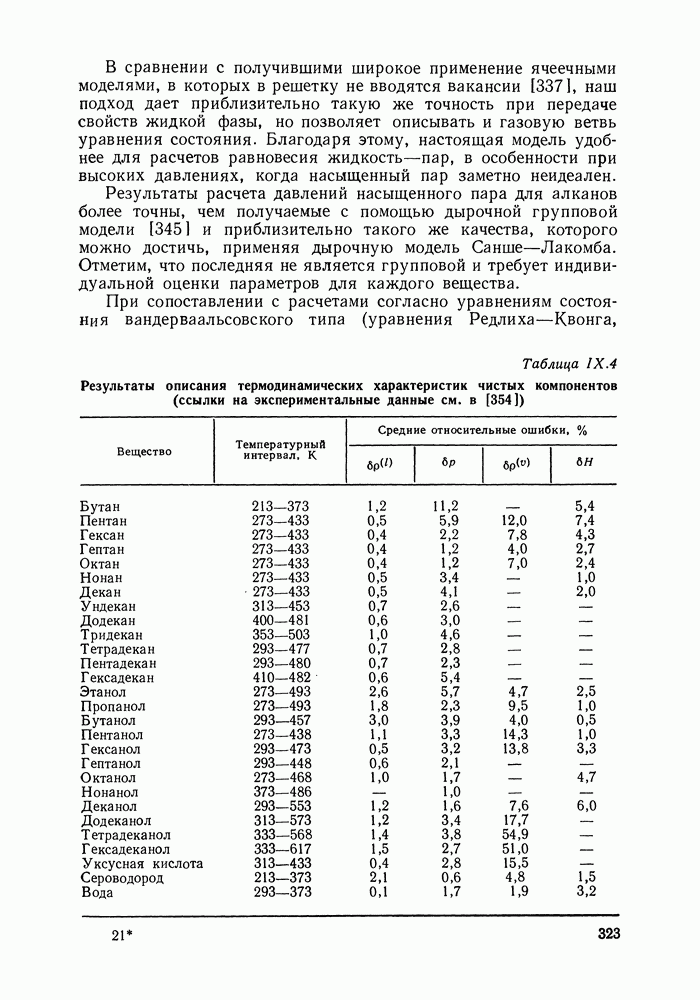
Результаты оценки параметров представлены в табл. IX.5.
При оценке параметров модели удобно использовать следующую стратегию поиска. Для температуры  рассчитанные по модели величины
рассчитанные по модели величины  (как и другие термодинамические свойства, не связанные с производными по температуре) не зависят от параметров
(как и другие термодинамические свойства, не связанные с производными по температуре) не зависят от параметров  а определяются значениями
а определяются значениями  и геометрическими параметрами модели. Согласно сформулированной модели, геометрические параметры не зависят от температуры. Параметры
и геометрическими параметрами модели. Согласно сформулированной модели, геометрические параметры не зависят от температуры. Параметры  также постоянны; значения их связаны лишь с выбором
также постоянны; значения их связаны лишь с выбором 
По экспериментальным данным для выбранной температуры  минимизацией
минимизацией  определяем
определяем  (см. табл. IX.5). Относительные ошибки описания плотностей
(см. табл. IX.5). Относительные ошибки описания плотностей
Таблица IX.5 (см. скан) Результаты оценки параметров для сероводорода  см.
см. 
жидкости, пара и давления пара составляют  Затем фиксируем
Затем фиксируем  и по данным для всего рассматриваемого интервала температур находим
и по данным для всего рассматриваемого интервала температур находим  табл. IX.5). В указанных выше температурных интервалах для средних отклонений рассчитанных величин от экспериментальных получим:
табл. IX.5). В указанных выше температурных интервалах для средних отклонений рассчитанных величин от экспериментальных получим:  Для пересчета параметров
Для пересчета параметров  с одной опорной температуры
с одной опорной температуры  на другую
на другую  воспользуемся следующими соотношениями:
воспользуемся следующими соотношениями:

где переменные со знаком  относятся к новой опорной температуре
относятся к новой опорной температуре 
Вычисленные по этим формулам параметры сероводорода приведены в табл. IX.2.
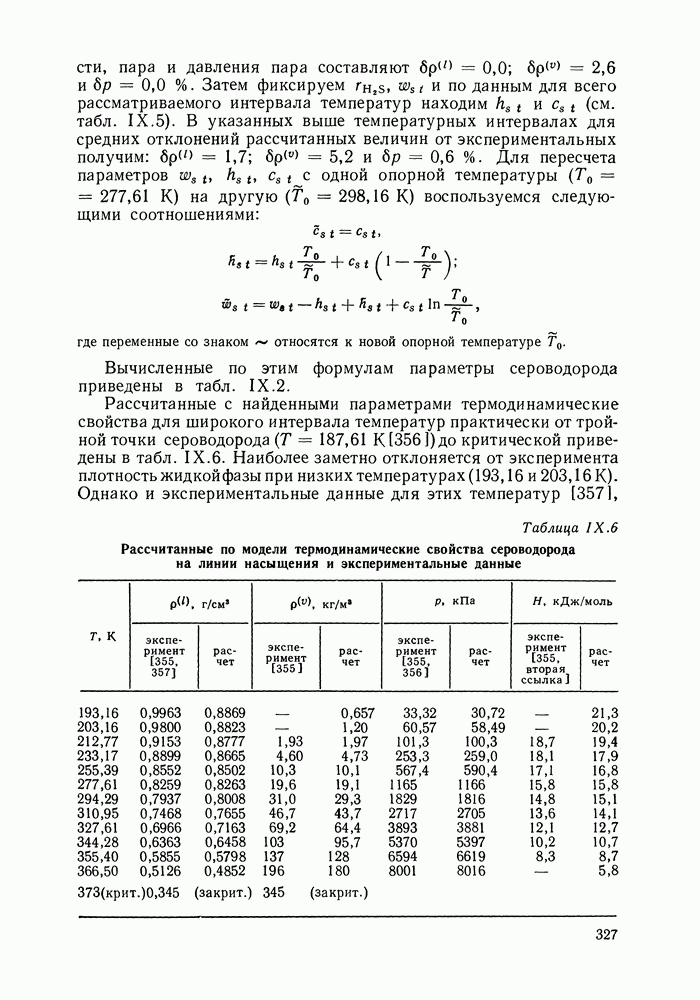
Рассчитанные с найденными параметрами термодинамические свойства для широкого интервала температур практически от тройной точки сероводорода (Т = 187,61 К [356]) до критической приведены в табл. IX.6. Наиболее заметно отклоняется от эксперимента плотность жидкой фазы при низких температурах (193,16 и 203,16 К). Однако и экспериментальные данные для этих температур [357],
Таблица IX.6 (см. скан) Рассчитанные по модели термодинамические свойства сероводорода на линии насыщения и экспериментальные данные
видимо, не слишком надежны; все же они приведены здесь для полноты.
При описании систем сероводород—алкан параметры  -групп для молекул алканов считались известными (см. табл. IX. 1, IX.2). Энергии взаимодействия сероводорода с
-групп для молекул алканов считались известными (см. табл. IX. 1, IX.2). Энергии взаимодействия сероводорода с  -группами не различали и характеризовали параметрами, усредненными по различным способам контактирования молекул:
-группами не различали и характеризовали параметрами, усредненными по различным способам контактирования молекул:

Температурную зависимость энергий взаимообмена учитывали приближенно с помощью параметра  (полагали
(полагали  Параметры
Параметры  искали по
искали по  данным для системы декан—сероводород при 277,61 и 310,95 К [355, первая ссылка]. Стратегия поиска параметров аналогична рассмотренной выше для индивидуального
данным для системы декан—сероводород при 277,61 и 310,95 К [355, первая ссылка]. Стратегия поиска параметров аналогична рассмотренной выше для индивидуального  При
При  по двум-трем точкам на фазовой диаграмме определяли
по двум-трем точкам на фазовой диаграмме определяли  минимизируя величину
минимизируя величину  где
где  давление насыщенного пара над бинарным раствором состава
давление насыщенного пара над бинарным раствором состава  номер экспериментальной точки. Затем при фиксированном
номер экспериментальной точки. Затем при фиксированном  нашли
нашли  по данным, относящимся к
по данным, относящимся к  Результаты оценки, пересчитанные на
Результаты оценки, пересчитанные на  содержатся в табл. IX.2.
содержатся в табл. IX.2.
Найденных параметров достаточно для вычисления термодинамических свойств бинарных и многокомпонентных смесей

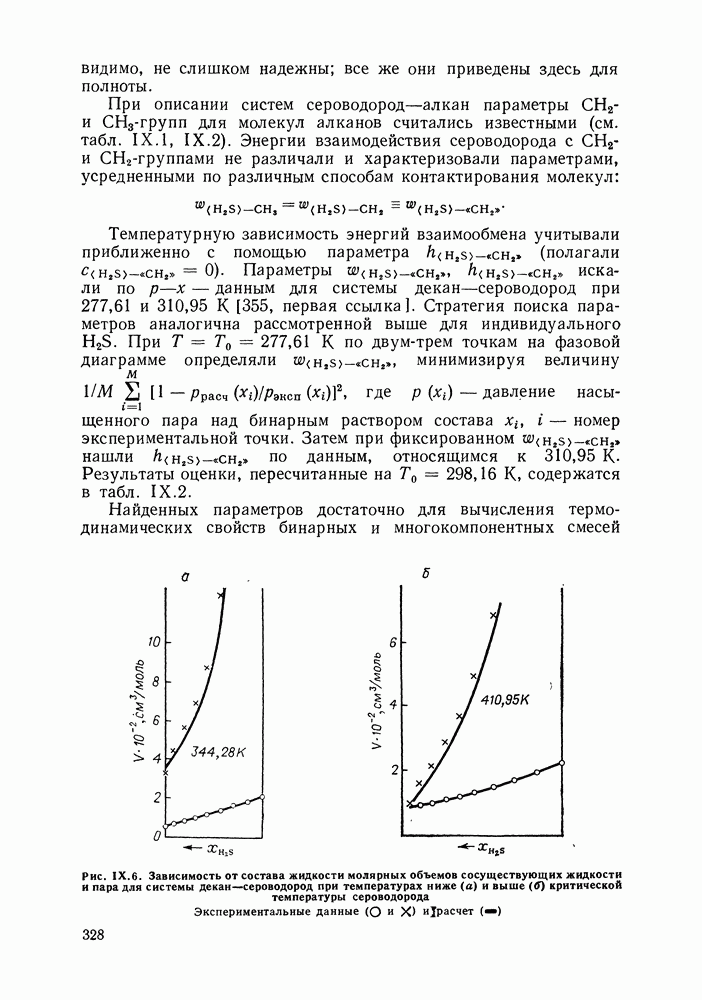
Рис. IX.6. Зависимость от состава жидкости молярных объемов сосуществующих жидкости и пара для системы декан—сероводород при температурах ниже (а) и выше (б) критической температуры сероводорода Экспериментальные данные 
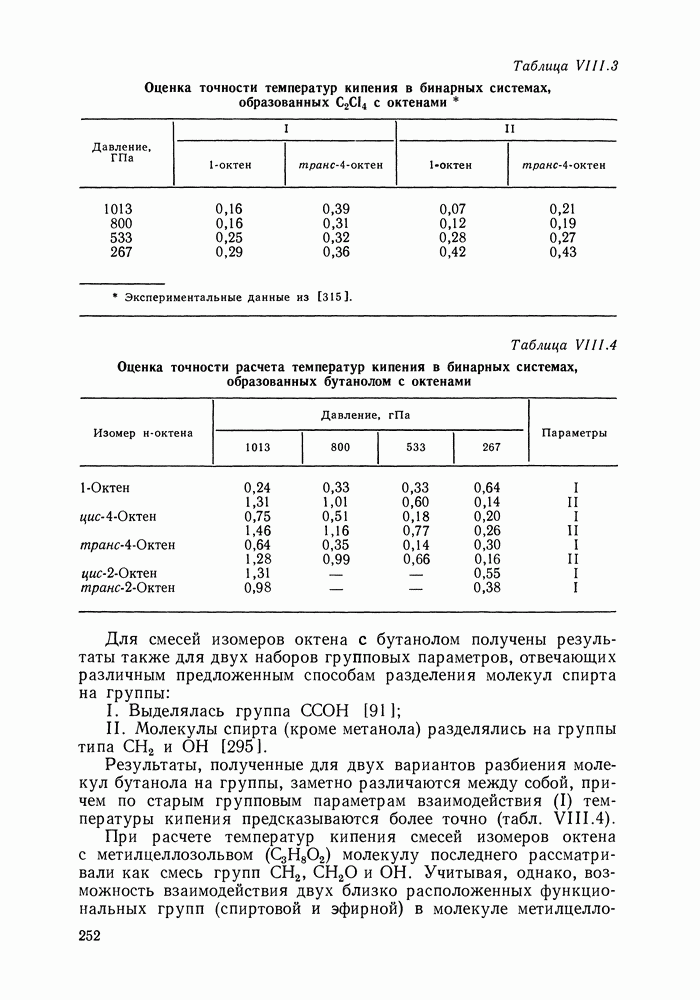
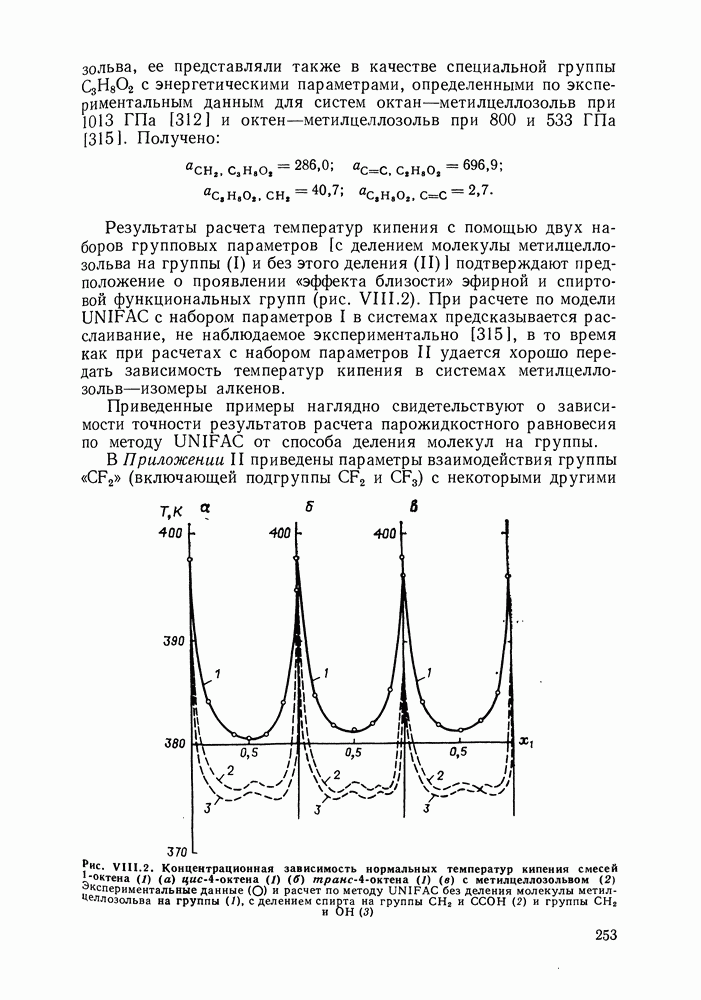
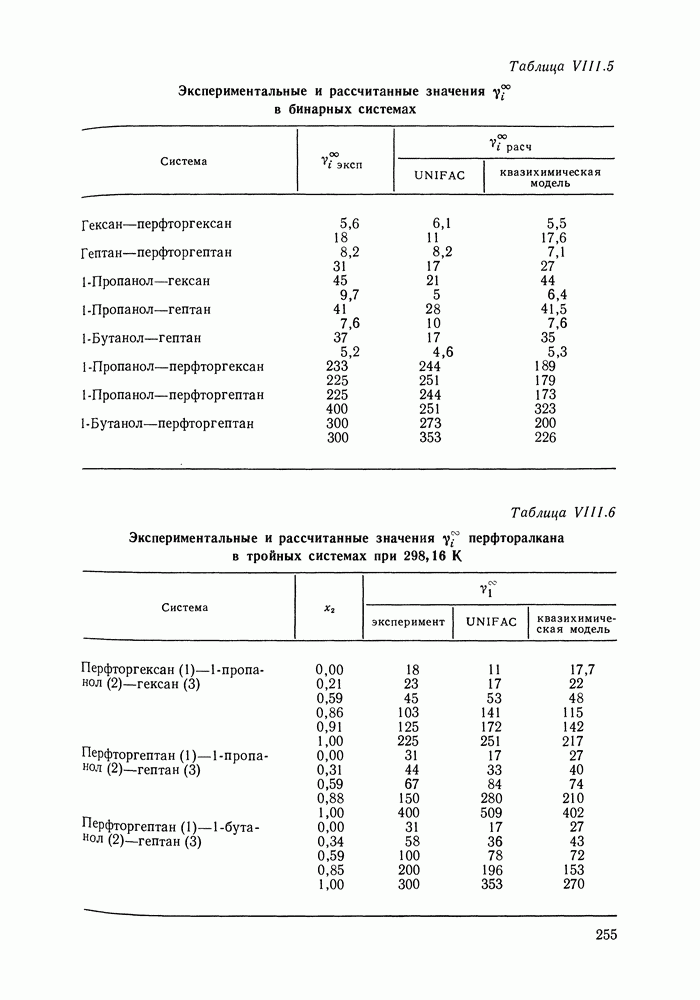
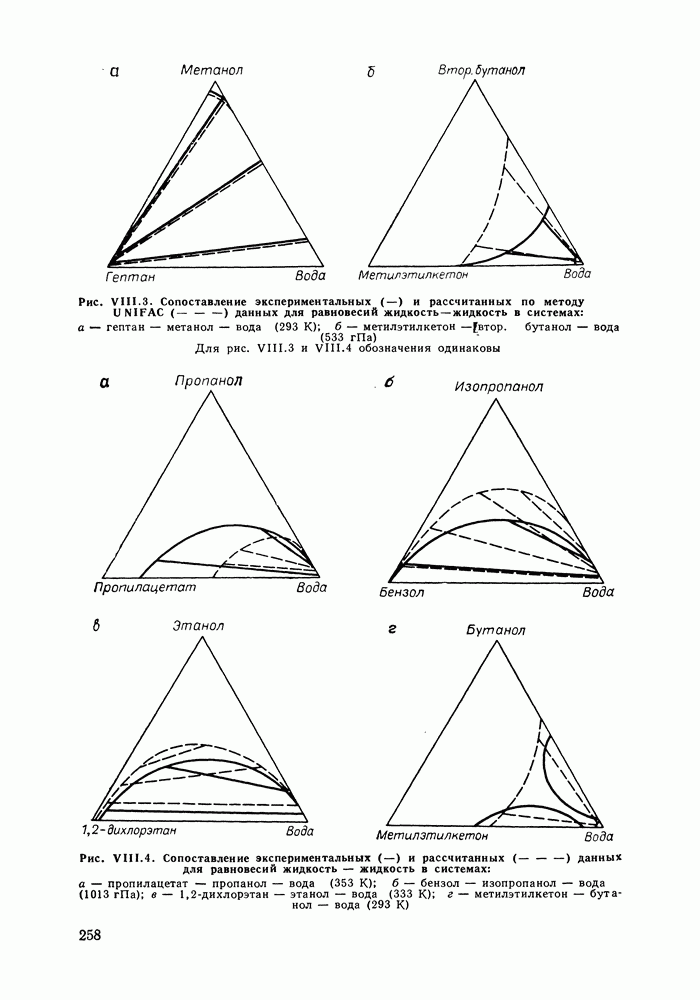
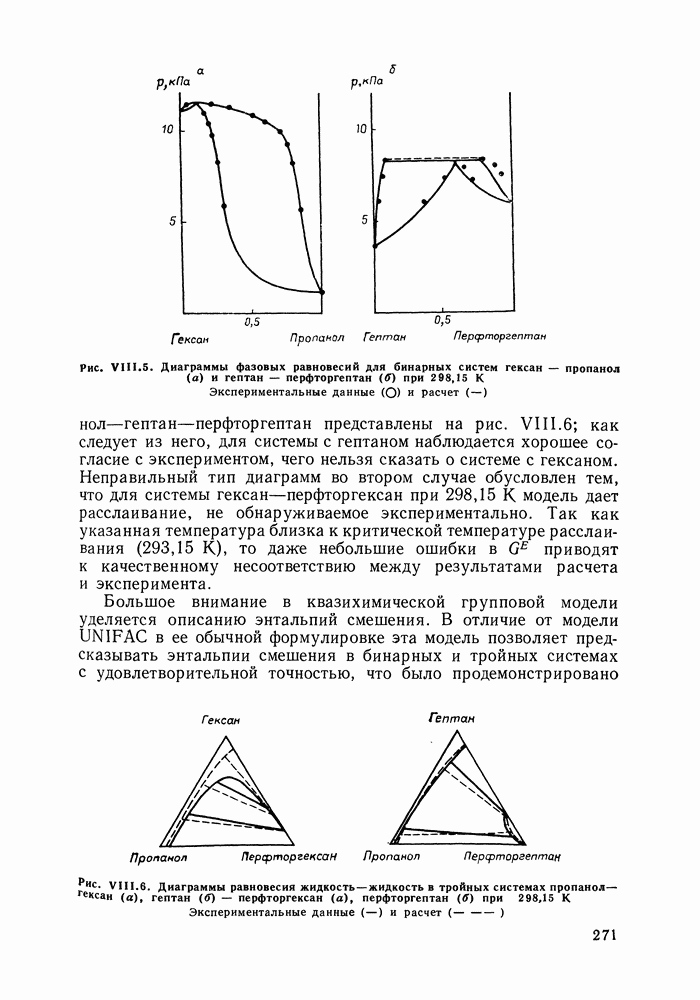
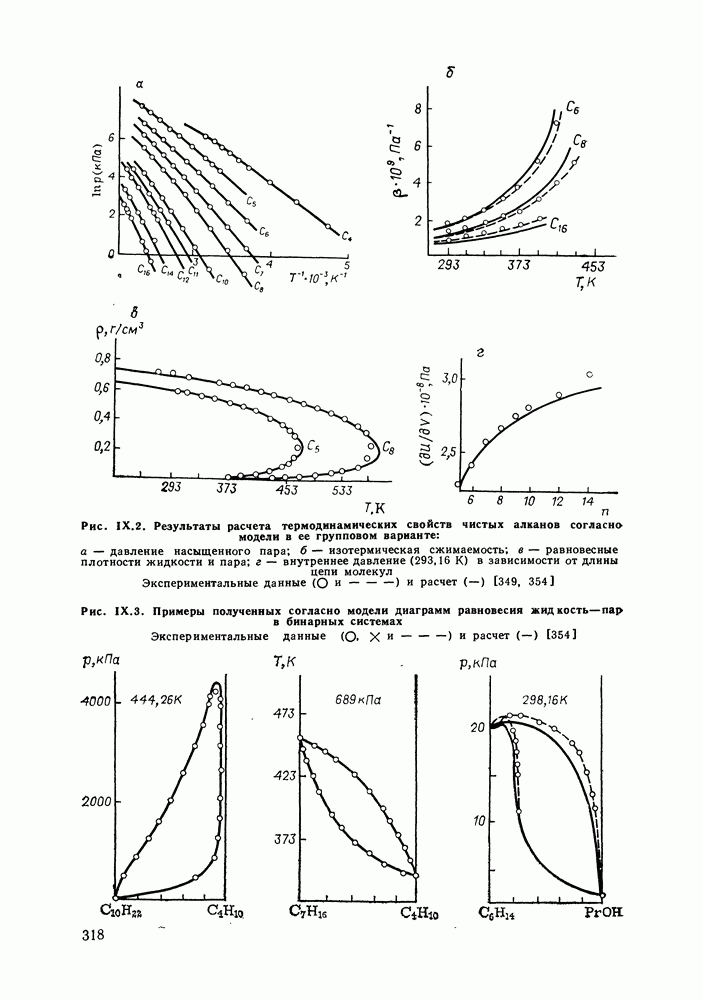
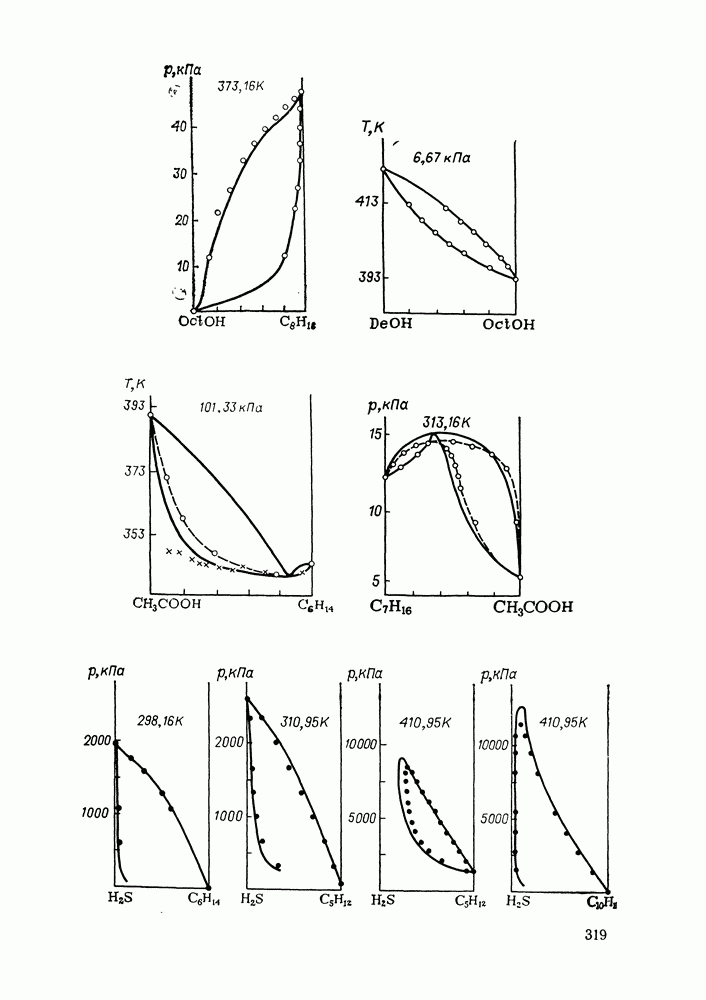
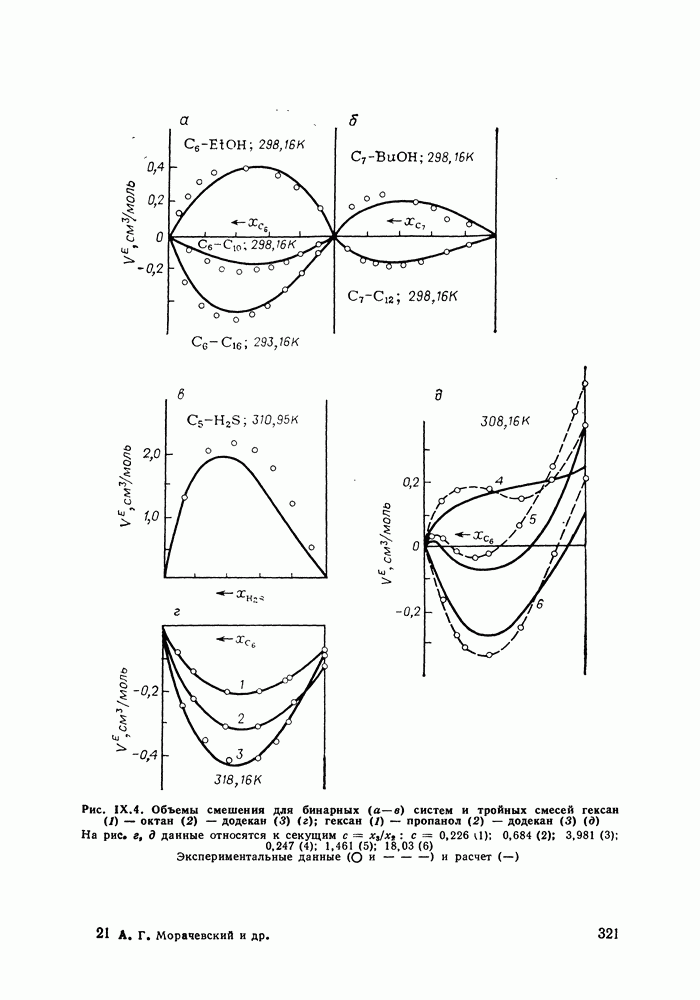
сероводорода с теми алканами, для которых приемлем групповой подход (согласно нашему опыту расчетов, это алканы не ниже бутана). Расчеты фазовых диаграмм, проведенные для бинарных смесей с  -алканами (те смеси, для которых имелись экспериментальные данные) дают удовлетворительные результаты (см. рис. IX.3) в рассматриваемом широком интервале температур и давлений. Верно предсказываются объемы смешения (см. рис. IX.4). Удается описать изменение знака Vе в системе сероводород—декан с ростом температуры, увеличение объемных эффектов при переходе от смесей с деканом к системам с пентаном.
-алканами (те смеси, для которых имелись экспериментальные данные) дают удовлетворительные результаты (см. рис. IX.3) в рассматриваемом широком интервале температур и давлений. Верно предсказываются объемы смешения (см. рис. IX.4). Удается описать изменение знака Vе в системе сероводород—декан с ростом температуры, увеличение объемных эффектов при переходе от смесей с деканом к системам с пентаном.
Непосредственное применение для смесей уравнения состояния, вытекающего из настоящей модели, проиллюстрировано на примере системы сероводород—декан (рис. IX.6). Изображены равновесные молярные объемы жидкой и паровой фаз в зависимости от состава жидкости. Расчеты выполнены для температур ниже и выше критической температуры сероводорода. Согласие с экспериментом хорошее.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
(см. скан)
(см. скан)
| << Предыдущий параграф |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
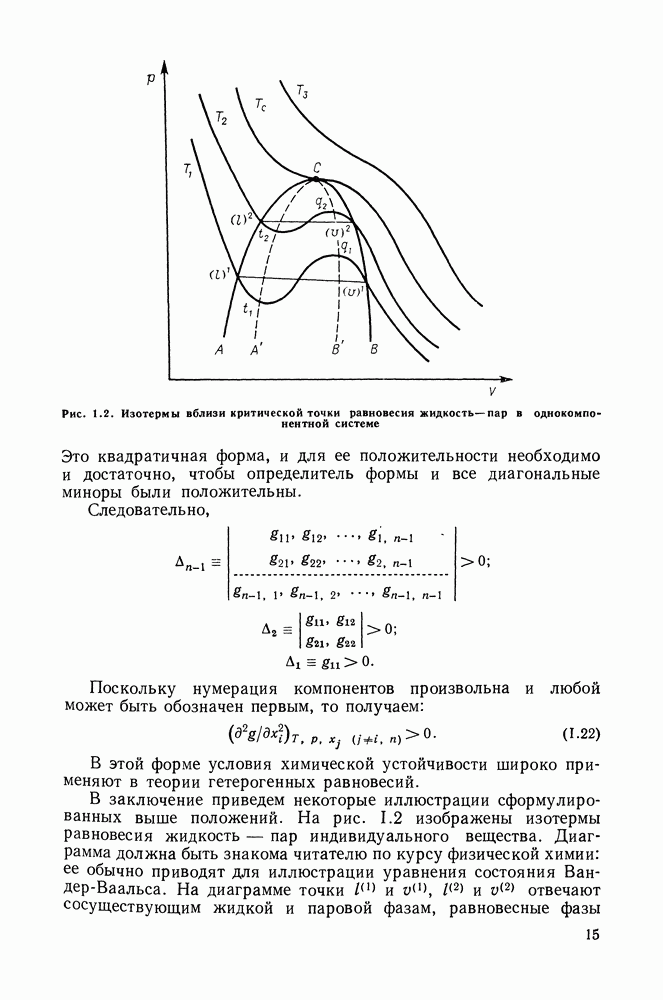
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
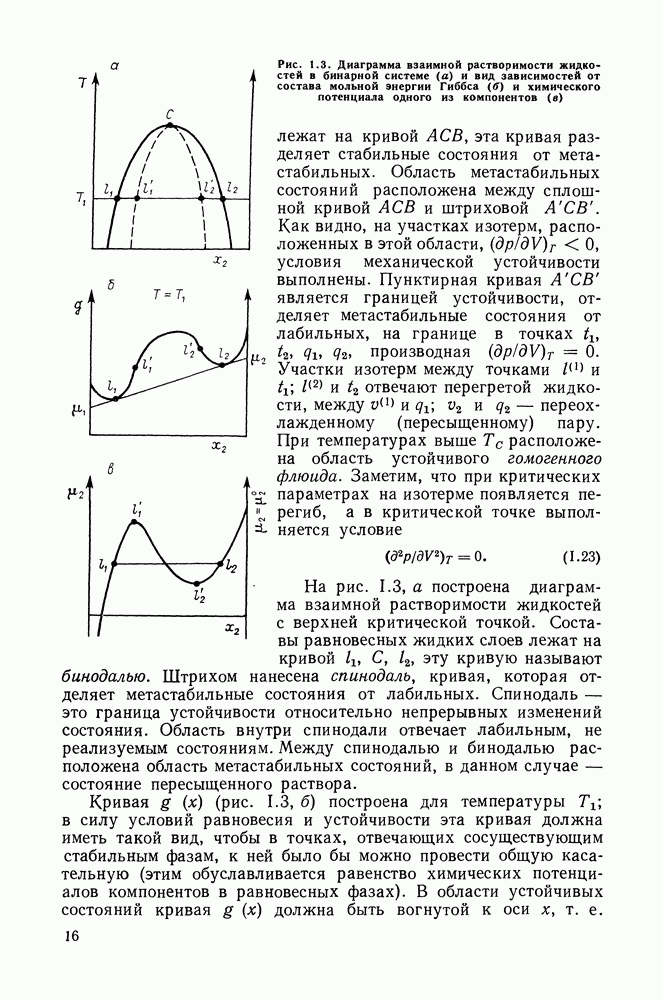
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
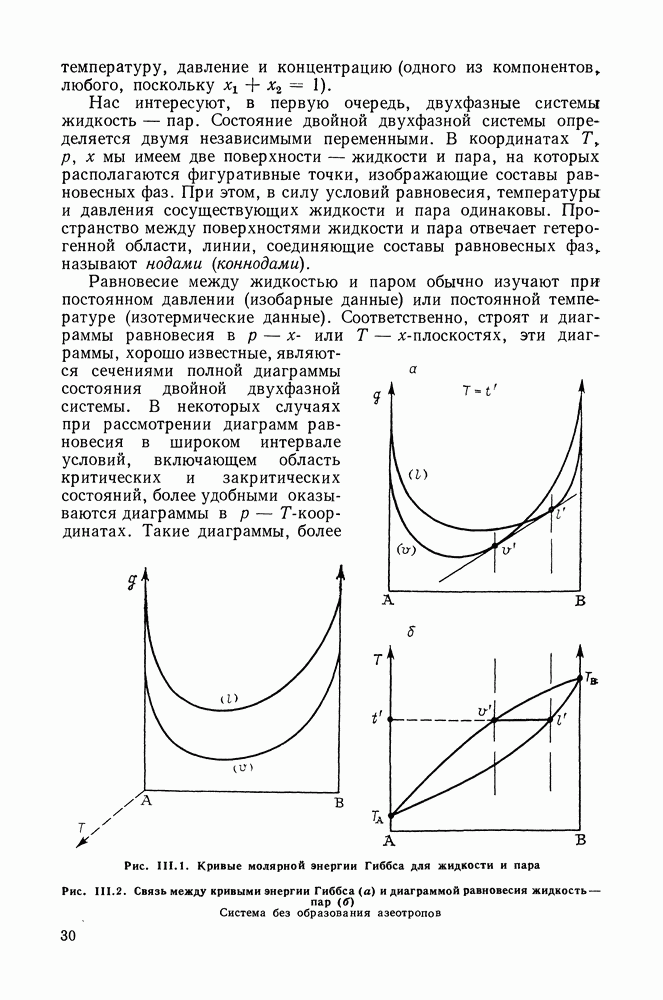
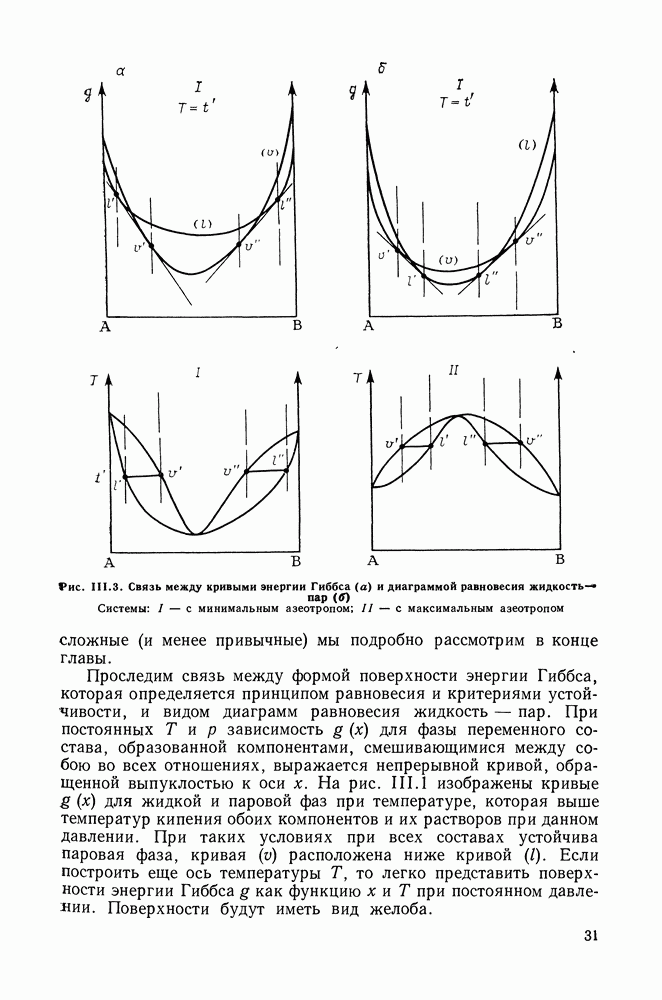
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
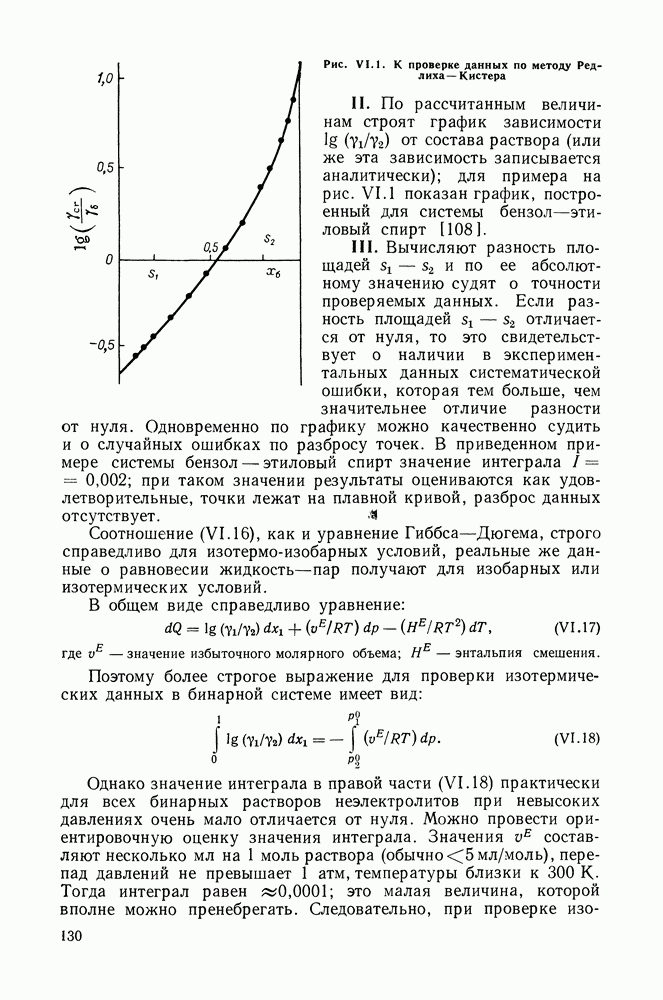
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
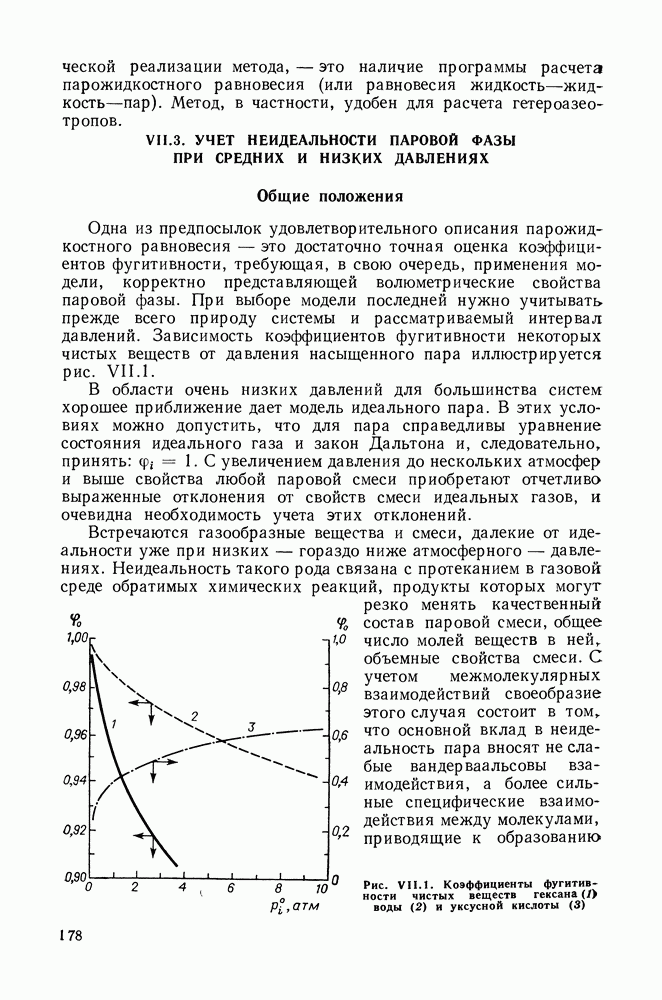
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
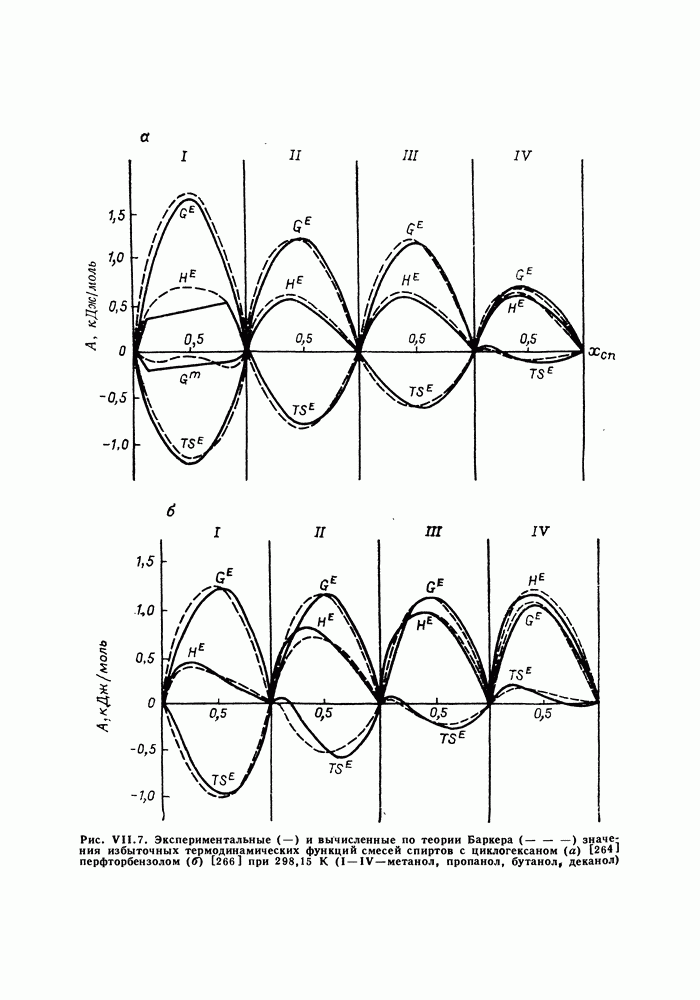
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА