| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
Методы расчета равновесного состава пара в бинарных системах при изотермических условиях по зависимости общего давления пара от состава раствора получили за последнее время широкое распространение, так как эти зависимости определяются экспериментально с большой степенью точности.
В связи с этим были предложены различные методы расчета, которые можно разделить на две группы. К первой относятся способы, заключающиеся в численном интегрировании одной из форм уравнения Гиббса-Дюгема, а ко второй — методы, основанные на использовании интерполяционных уравнений для описания зависимости коэффициентов активности, парциальных давлений компонентов или избыточного термодинамического потенциала  от состава раствора [17].
от состава раствора [17].
Строгий метод расчета состава пара в бинарной системе по зависимости  был предложен Кричевским и Казарновским [86]. Метод заключается в численном интегрировании одной из
был предложен Кричевским и Казарновским [86]. Метод заключается в численном интегрировании одной из
форм уравнения Дюгема-Маргулеса, записанного для идеального пара в виде:

Уравнение  интегрируют методом Рунге, при этом дифференциалы заменяют небольшими конечными приращениями:
интегрируют методом Рунге, при этом дифференциалы заменяют небольшими конечными приращениями:

Из этого уравнения находят изменение состава пара  исходя из определенного начального значения при изменении давления пара над раствором от
исходя из определенного начального значения при изменении давления пара над раствором от  до
до  Состав раствора, соответствующий выбранному значению
Состав раствора, соответствующий выбранному значению  находят графически по экспериментальным данным
находят графически по экспериментальным данным 
Особенность метода Рунге состоит в том, что ошибка при решении уравнения в два шага составляет «1/8 ошибки в решении, полученном с одним шагом, т. е., удваивая число шагов примерно на порядок, увеличивают точность расчета. Точность этого метода расчета лимитируется точностью экспериментального определения зависимости 
Некоторые затруднения возникают при выборе начальных условий, так как при  или
или  выражение
выражение  превращается в неопределенность типа
превращается в неопределенность типа  Начальные условия интегрирования находят, используя следующий прием: если
Начальные условия интегрирования находят, используя следующий прием: если  то в качестве первого приближения можно принять, что
то в качестве первого приближения можно принять, что  иными словами, выбирают точку близкую к чистому компоненту. Подставляя это значение в уравнение
иными словами, выбирают точку близкую к чистому компоненту. Подставляя это значение в уравнение  можно найти приближенное значение
можно найти приближенное значение  Затем значение
Затем значение  уточняют методом подбора до тех пор, пока новое значение
уточняют методом подбора до тех пор, пока новое значение  не станет близким к 1. Дальнейшие вычисления в сторону убывания
не станет близким к 1. Дальнейшие вычисления в сторону убывания  проводят методом Рунге.
проводят методом Рунге.
При численном интегрировании уравнения Дюгема-Маргулеса большое значение имеет направление интегрирования. Музил и Брайтенхубер [87] пришли к выводу, что интегрирование всегда лучше проводить в направлении увеличения давления. Более детально этот вопрос рассмотрен в работе [88].
Для неазеотропных систем интегрирование следует вести от  до
до  мол. доля летучего компонента в растворе), для систем с положительным бинарным азеотропом интегрирование ведут от точек
мол. доля летучего компонента в растворе), для систем с положительным бинарным азеотропом интегрирование ведут от точек  к азеотропу, а в случае отрицательного азеотропа интегрирование следует проводить от точки азеотропа к составам
к азеотропу, а в случае отрицательного азеотропа интегрирование следует проводить от точки азеотропа к составам 
При использовании мётода Баркера [89] расчета состава пара по зависимости  вводят поправку на неидеальность паровой фазы с помощью вторых вириальных коэффициентов.
вводят поправку на неидеальность паровой фазы с помощью вторых вириальных коэффициентов.
Коэффициенты активности и избыточные химические потенциалы компонентов связаны уравнениями:

где  — избыточный химический потенциал
— избыточный химический потенциал  компонента
компонента  — молярный объем жидкости;
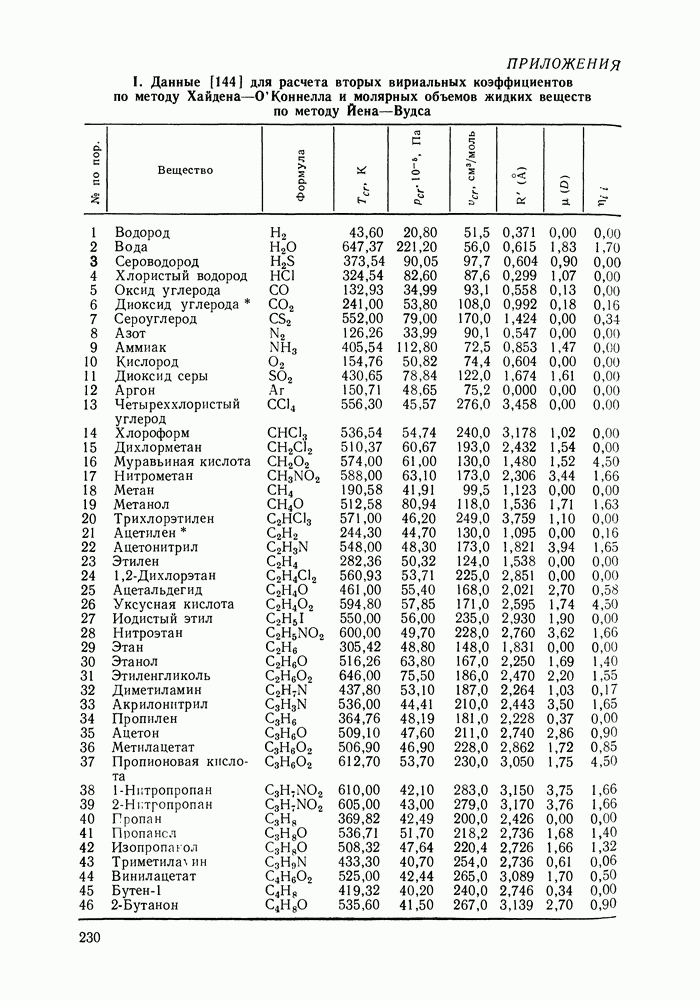
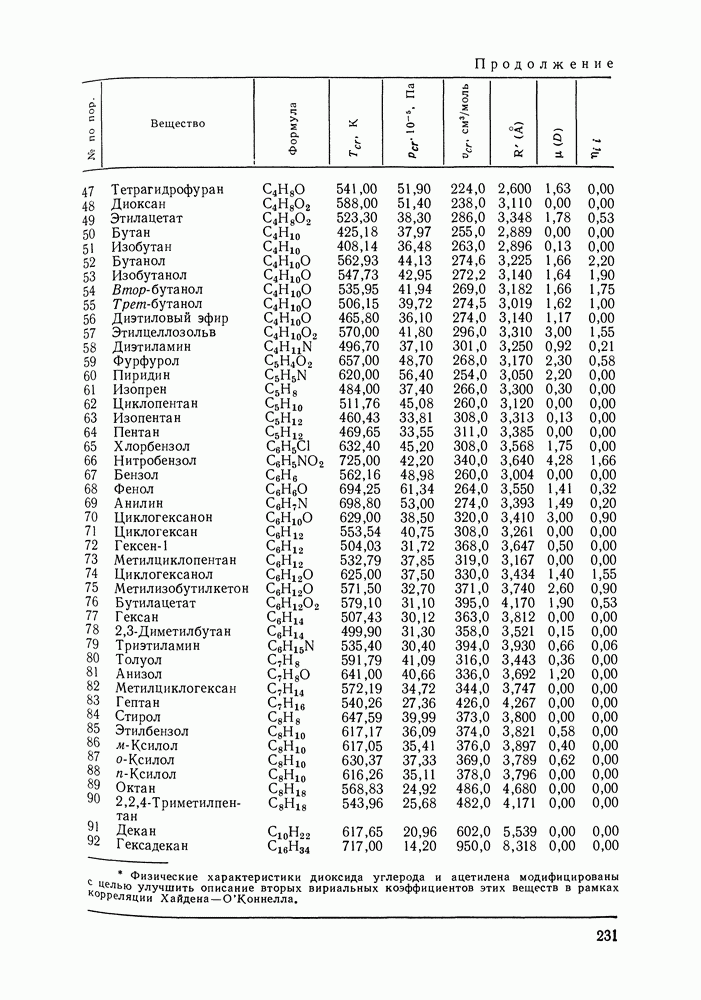
— молярный объем жидкости;  вторые вириальные коэффициенты;
вторые вириальные коэффициенты; 
Из уравнений  следует выражение для общего давления пара:
следует выражение для общего давления пара:

где

Зависимость коэффициентов активности от состава бинарного раствора представляется аналитически с помощью следующих соотношений

где 

Константы  находят методом последовательных приближений.
находят методом последовательных приближений.
В первом приближении полагают раствор регулярным  при этом константу А рассчитывают по формуле
при этом константу А рассчитывают по формуле

где  давление пара над эквимолярным раствором, определяемое из экспериментальной зависимости
давление пара над эквимолярным раствором, определяемое из экспериментальной зависимости 
Затем для всех экспериментальных составов раствора рассчитывают значения коэффициентов активности по уравнениям  далее с помощью уравнений
далее с помощью уравнений  в приближении идеального пара вычисляют равновесный состав пара, величины
в приближении идеального пара вычисляют равновесный состав пара, величины  по уравнениям
по уравнениям  и
и  общее давление пара по уравнению
общее давление пара по уравнению  разность между экспериментальными и расчетными давлениями
разность между экспериментальными и расчетными давлениями  и производные
и производные 
Приращения  для перехода к следующему приближению рассчитывают методом наименьших квадратов по уравнению
для перехода к следующему приближению рассчитывают методом наименьших квадратов по уравнению

где

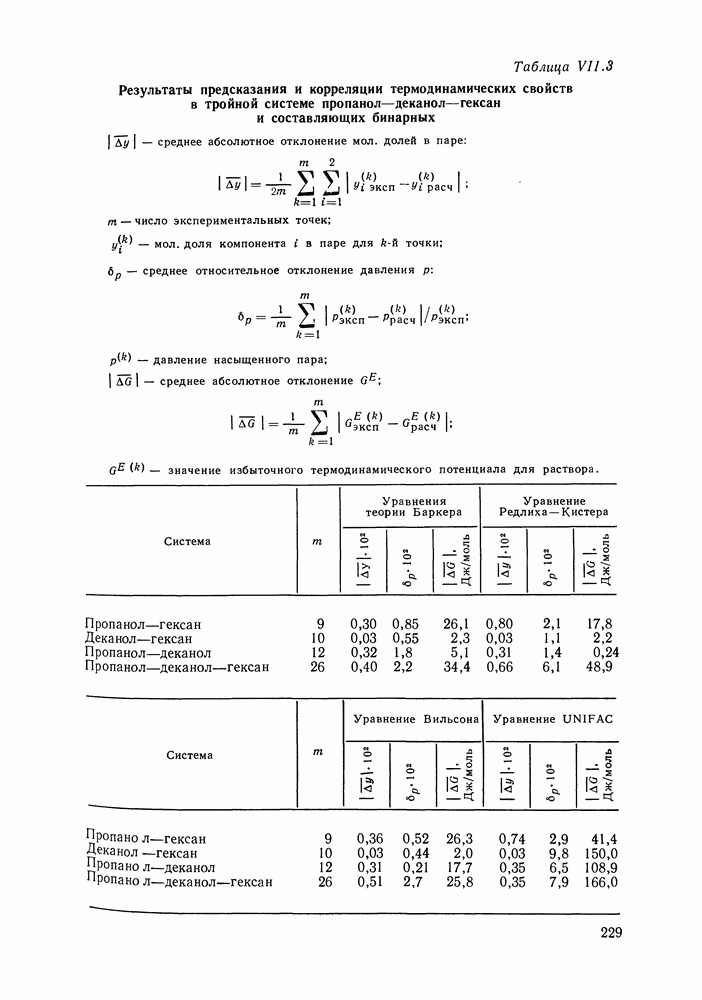
Расчет, выполненный для ряда систем, показал, что найденный указанным методом состав пара находится в хорошем согласии с результатами эксперимента.
Для вычисления состава пара и проверки экспериментальных данных о равновесии жидкость—пар на термодинамическую согласованность в настоящее время широко используют метод, предложенный Ван-Нессом с соавт. [90]. Для идеального пара:

Введя обозначения:  и используя уравнение Гиббса-Дюгема при
и используя уравнение Гиббса-Дюгема при  получим для бинарной системы
получим для бинарной системы

Подставим уравнения  в соотношение
в соотношение  получим следующее выражение для общего давления пара в бинарной системе:
получим следующее выражение для общего давления пара в бинарной системе:

Авторы работы [90] представляли  в виде уравнения с тремя константами:
в виде уравнения с тремя константами:

Однако более удобным в плане расчета является описание  с помощью ортогональных полиномов Лежандра
с помощью ортогональных полиномов Лежандра 

где  порядок полинома.
порядок полинома.

Коэффициенты разложения  находят методом наименьших квадратов, где минимизируется сумма квадратов отклонений между рэксп и давлением, рассчитанным по уравнению
находят методом наименьших квадратов, где минимизируется сумма квадратов отклонений между рэксп и давлением, рассчитанным по уравнению  как и в методе Баркера [89].
как и в методе Баркера [89].
Зная коэффициенты можно рассчитать коэффициенты активности, избыточный термодинамический потенциал, а также состав пара над раствором

Основная особенность этого метода состоит в том, что в виде полинома представляются не коэффициенты активности компонентов или давления пара, а функция  которая обычно имеет более простой вид. В работе [91] показано, что для описания зависимости
которая обычно имеет более простой вид. В работе [91] показано, что для описания зависимости  достаточно использовать полиномы третьей или четвертой степени. Привлечение полиномов более высоких степеней приводит к увеличению вычислительных погрешностей.
достаточно использовать полиномы третьей или четвертой степени. Привлечение полиномов более высоких степеней приводит к увеличению вычислительных погрешностей.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА