| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
МОЛЬНАЯ ИОННАЯ ЭЛЕКТРОПРОВОДНОСТЬ
Недавно принятые рекомендации, касающиеся единиц и символов, определяют подвижность иона и как его скорость в условиях единичного градиента потенциала. Однако в прошлом большинство авторов использовали этот термин как удобный синоним эквивалентной ионной электропроводности Л. Между ними существует соотношение  и его следует всегда помнить при чтении специальной литературы.
и его следует всегда помнить при чтении специальной литературы.
Выражение для ионной электропроводности получают комбинированием выражений для электропроводности и числа переноса (см.). Число переноса катиона электролита определяет долю тока, переносимого катионом; если мы умножим его на мольную электропроводность полностью диссоциированного бинарного электролита, то получим мольную электропроводность катиона  и аналогичным образом
и аналогичным образом  .
.
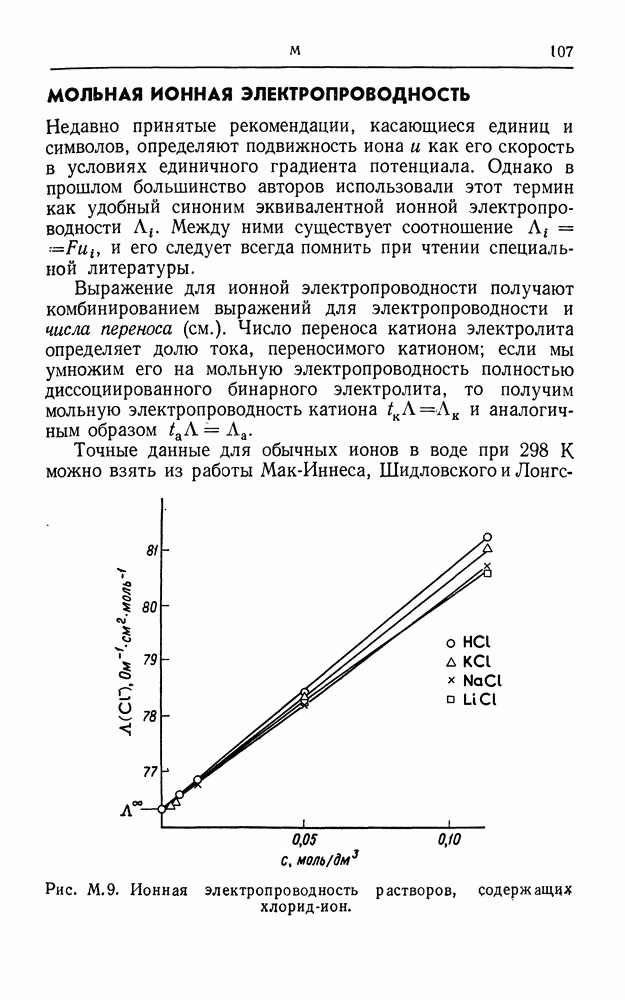
Точные данные для обычных ионов в воде при 298 К можно взять из работы Мак-Иннеса, Шидловского и Лонгсворта.

Рис. М. 9. Ионная электропроводность растворов, содержащие хлорид-ион.
ворта. Эти авторы определяли числа переноса и электропроводность  при различных концентрациях и затем вычисляли значения мольной электропроводности хлорид-иона в этих растворах. Полученные величины были экстраполированы в соответствии с уравнением Шидловского (см. электропроводность при бесконечном разбавлении) (рис. М. 9). Таким путем для хлорид-иона можно получить точную величину
при различных концентрациях и затем вычисляли значения мольной электропроводности хлорид-иона в этих растворах. Полученные величины были экстраполированы в соответствии с уравнением Шидловского (см. электропроводность при бесконечном разбавлении) (рис. М. 9). Таким путем для хлорид-иона можно получить точную величину  , а вычитанием ее из значений
, а вычитанием ее из значений  для четырех электролитов получаются величины
для четырех электролитов получаются величины  для четырех катионов. Числа переноса для других ионов теперь уже не нужны, так как мольную электропроводность катиона можно определить вычитанием мольной электропроводности хлорид-иона из
для четырех катионов. Числа переноса для других ионов теперь уже не нужны, так как мольную электропроводность катиона можно определить вычитанием мольной электропроводности хлорид-иона из  хлорида данного катиона, а мольную электропроводность аниона — вычитанием мольной электропроводности натрия или калия из
хлорида данного катиона, а мольную электропроводность аниона — вычитанием мольной электропроводности натрия или калия из  натриевой или калиевой соли. Для наиболее часто встречающихся ионов данные приведены в табл. М. 1.
натриевой или калиевой соли. Для наиболее часто встречающихся ионов данные приведены в табл. М. 1.
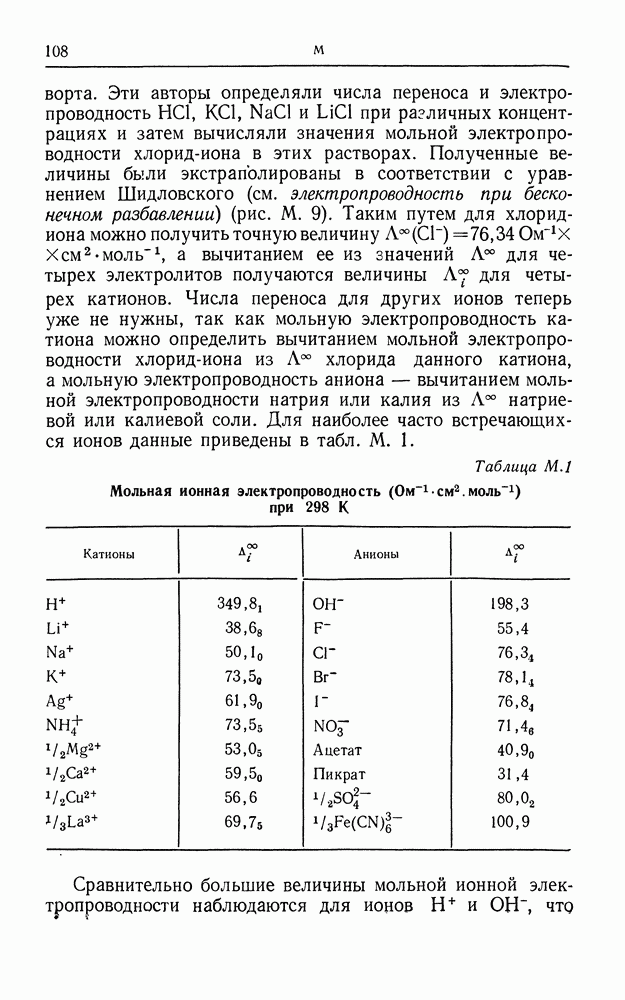
Таблица М. 1. Мольная ионная электропроводность  при 298 К (см. скан)
при 298 К (см. скан)
Сравнительно большие величины мольной ионной электропроводности наблюдаются для ионов 
связано со способностью молекул воды образовывать водородные связи. В результате протон приобретает способность двигаться под действием тока путем обмена между молекулами воды, и скорость такого передвижения оказывается более высокой, чем скорость передвижения протона путем обычного процесса миграции. Механизм «перескока» протона для воды выглядит следующим образом:

Аналогичный механизм имеет место и в случае иона  Значения мольной электропроводности для других ионов более близки между собой. Низкое значение мольной электропроводности для пикрат-иона является следствием его большого размера; такое же влияние размера прослеживается в гомологических рядах ионов органических кислот — с увеличением размера подвижность падает. Однако у щелочных металлов наблюдается противоположная зависимость величин мольной электропроводности от их радиуса. Это обусловлено эффектами гидратации; небольшой ион лития ориентирует и удерживает молекулы воды благодаря сильному ион-дипольному взаимодействию, тогда как более слабое притяжение молекул воды большими ионами приводит в итоге к эффекту разупорядочения структуры из-за того, что вблизи них наблюдается разрыв водородных связей между молекулами воды.
Значения мольной электропроводности для других ионов более близки между собой. Низкое значение мольной электропроводности для пикрат-иона является следствием его большого размера; такое же влияние размера прослеживается в гомологических рядах ионов органических кислот — с увеличением размера подвижность падает. Однако у щелочных металлов наблюдается противоположная зависимость величин мольной электропроводности от их радиуса. Это обусловлено эффектами гидратации; небольшой ион лития ориентирует и удерживает молекулы воды благодаря сильному ион-дипольному взаимодействию, тогда как более слабое притяжение молекул воды большими ионами приводит в итоге к эффекту разупорядочения структуры из-за того, что вблизи них наблюдается разрыв водородных связей между молекулами воды.
Роль заряда
Мольная электропроводность иона зависит от заряда, который он несет, и его подвижности при единичном градиенте потенциала. При сравнении мольных электропроводностей первый фактор обычно исключают; так, мольную электропроводность сульфат-иона при 298 К можно было бы представить как  но гораздо чаще задают величину
но гораздо чаще задают величину  Аналогичным образом
Аналогичным образом
получены данные и для других многозарядных ионов, представленных в табл. М. 1. Таким образом, принимают во внимание лишь второй фактор: сила, действующая на ион, движущийся в электрическом поле, пропорциональна его заряду, так что (при прочих равных условиях) можно ожидать пропорциональной зависимости между подвижностью и зарядом. Это практически и наблюдается в случае комплексных ионов — аммиакатов кобальта:

Однако у ионов меньших размеров положительное влияние увеличения заряда частично снижается из-за более сильного взаимодействия в системе ион—растворитель. Для двухосновных кислот, как правило, подвижность иона типа  примерно в 1,7 раза больше подвижности иона типа
примерно в 1,7 раза больше подвижности иона типа  эта тенденция к более медленному росту подвижности по сравнению с увеличением заряда наиболее отчетливо проявляется у простых элементарных ионов.
эта тенденция к более медленному росту подвижности по сравнению с увеличением заряда наиболее отчетливо проявляется у простых элементарных ионов.  имеют примерно одинаковый радиус в кристаллической решетке, а их подвижности при 298 К составляют соответственно 50,1, 59,5 и 69,7.
имеют примерно одинаковый радиус в кристаллической решетке, а их подвижности при 298 К составляют соответственно 50,1, 59,5 и 69,7.
Электропроводность и температура
Для величин ионной электропроводности характерны значительные температурные коэффициенты. Значения электропроводности
Таблица М.2. Зависимость мольной электропроводности хлорид-иона от температуры (см. скан)
в воде для ряда температур могут быть взяты из данных Гордона для хлорид-иона (табл. М. 2).
Из этих значений можно получить данные для других ионов. Сопоставление этих данных показывает, что на электропроводность основное влияние оказывает изменение вязкости растворителя. Если бы точно выполнялся закон Стокса, то произведение было бы постоянным. В грубом приближении это справедливо для больших ионов типа пикрата и  , а также для сильно «гидратированных» ионов, таких, как
, а также для сильно «гидратированных» ионов, таких, как  при условии что «эффективный радиус» этих ионов не изменяется с температурой. Для однозарядных ионов типа
при условии что «эффективный радиус» этих ионов не изменяется с температурой. Для однозарядных ионов типа  с большим ионным радиусом произведение уменьшается с увеличением температуры; при переходе от 237 к 373 К оно уменьшается примерно на
с большим ионным радиусом произведение уменьшается с увеличением температуры; при переходе от 237 к 373 К оно уменьшается примерно на  , что, по-видимому, является следствием ослабления «эффекта разупорядочения структуры» по мере уменьшения количества водородных связей в растворителе.
, что, по-видимому, является следствием ослабления «эффекта разупорядочения структуры» по мере уменьшения количества водородных связей в растворителе.
Ионные электропроводности в неводных растворителях
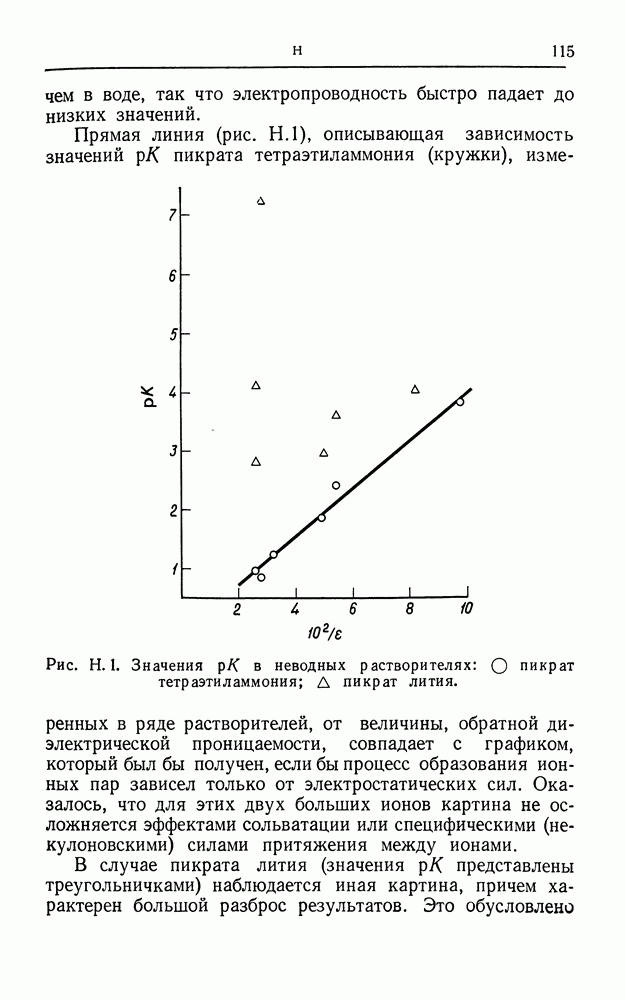
Данные по ионной электропроводности в неводных растворителях значительно более фрагментарны из-за небольшого количества проведенных измерений чисел переноса. Если таких данных нет, приближенные значения можно получить, используя правило Вальдена:  . Данные Вальдена подтвердили постоянство этого произведения, вытекающего из закона Стокса, для пикрата тетраэтиламмония в большом количестве растворителей; приближенные величины для других ионов можно получить, исходя из значения
. Данные Вальдена подтвердили постоянство этого произведения, вытекающего из закона Стокса, для пикрата тетраэтиламмония в большом количестве растворителей; приближенные величины для других ионов можно получить, исходя из значения  определенного для иона пикрата в воде.
определенного для иона пикрата в воде.
См. также [26].
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- О ПОЛЬЗОВАНИИ СЛОВАРЕМ
- СПИСОК ОСНОВНЫХ ОБОЗНАЧЕНИЙ
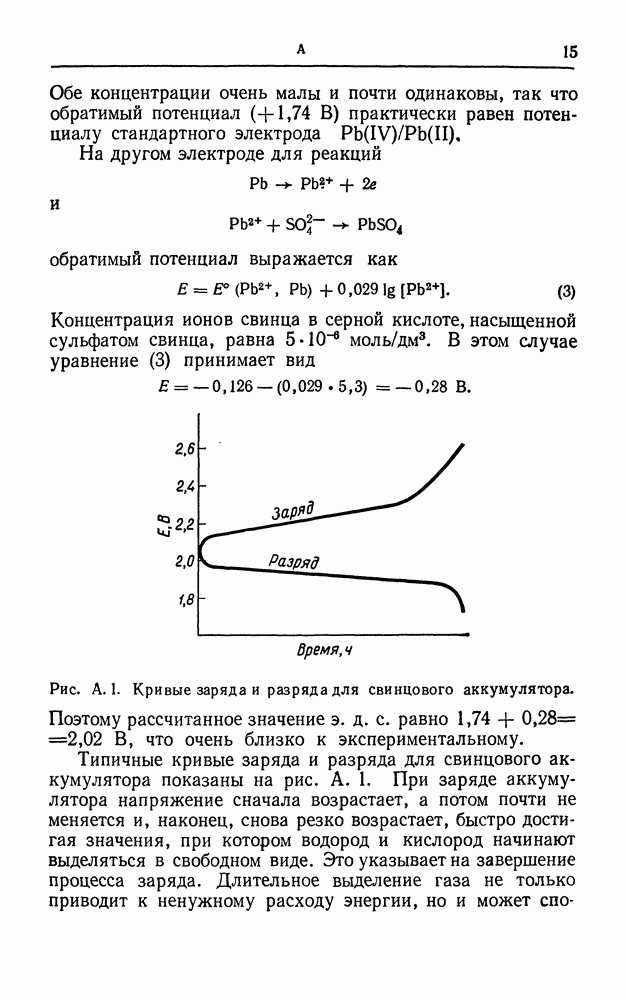
- АККУМУЛЯТОР
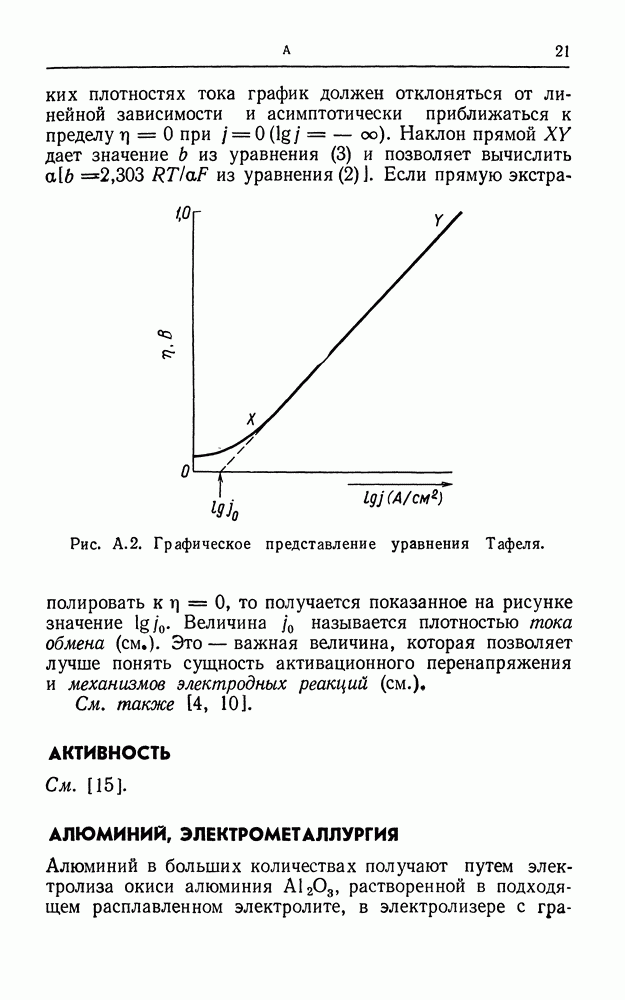
- АКТИВАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
- АКТИВНОСТЬ
- АЛЮМИНИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- АМАЛЬГАМНЫЙ ЭЛЕКТРОД
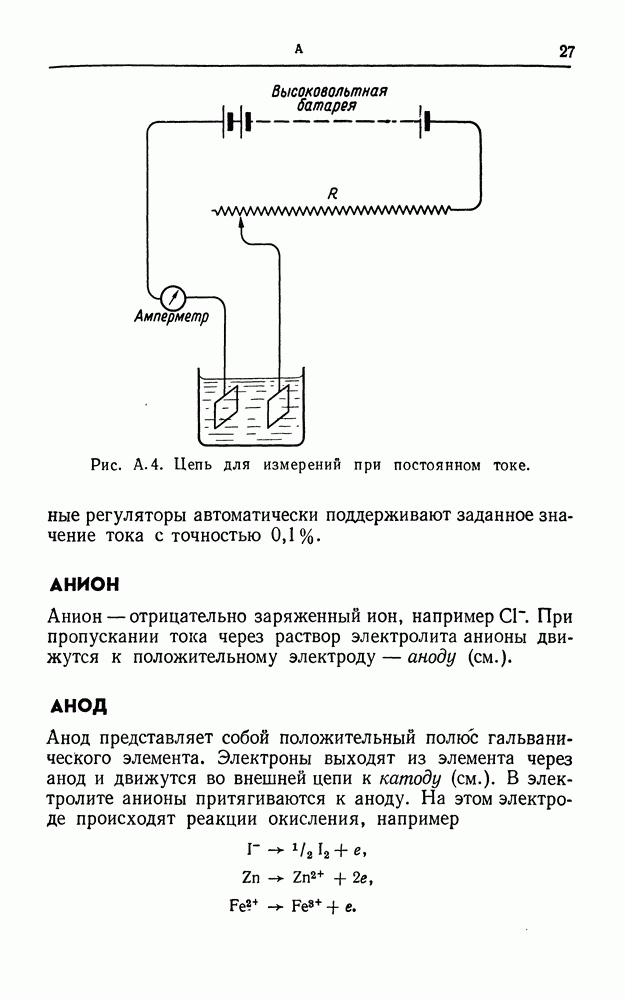
- АМПЕР
- АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- АМПЕРОСТАТ
- АНИОН
- АНОД
- АНОДИРОВАНИЕ
- БАТАРЕЯ
- БЕРИЛЛИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- БИПОЛЯРНЫЙ ЭЛЕКТРОД
- БЛЕСКООБРАЗОВАТЕЛИ
- БУФЕРНЫЙ РАСТВОР
- ВАГНЕРОВСКОЕ ЗАЗЕМЛЕНИЕ
- ВНУТРЕННИЙ ЭЛЕКТРОЛИЗ
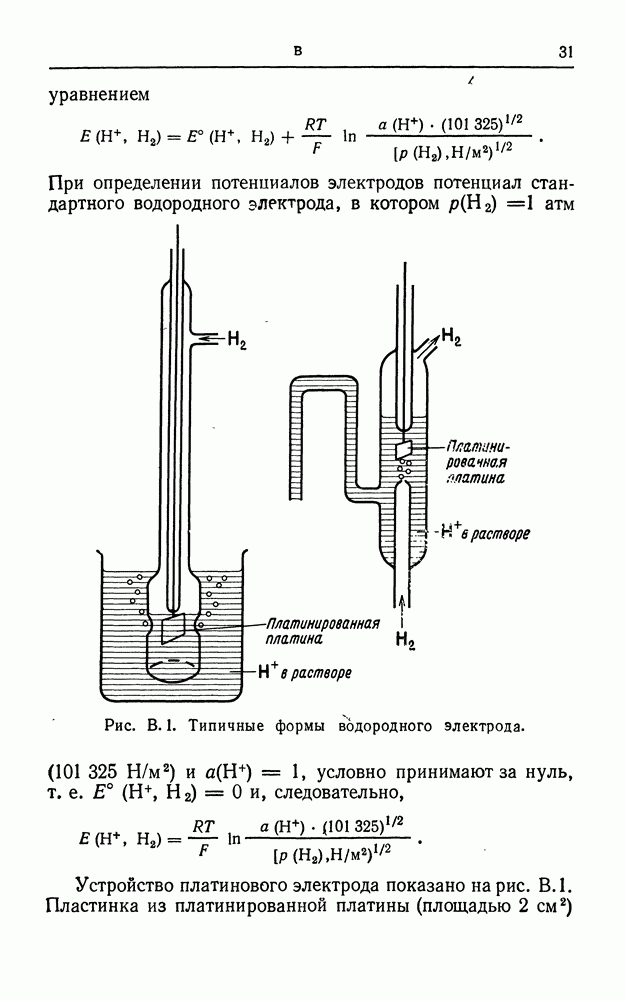
- ВОДОРОДНЫЙ ЭЛЕКТРОД
- ВОЛЬТ
- ВОЛЬФРАМОВЫЙ ЭЛЕКТРОД
- ВЫХОД ПО ТОКУ
- ГАЗОВЫЙ ЭЛЕКТРОД
- ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
- ГАЛЬВАНОПЛАСТИКА
- ГАЛЬВАНОСТАТ
- ГАЛЬВАНОСТЕГИЯ
- ГИДРАТАЦИЯ ИОНОВ
- ДАТЧИК АММИАКА
- ДАТЧИК СЕРНИСТОГО ГАЗА
- ДВОЙНОЙ СЛОЙ
- ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ
- ДЗЕТА-ПОТЕНЦИАЛ
- ДИФФУЗИОННЫЙ ПОТЕНЦИАЛ
- ДИФФУЗИЯ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- ДИЭЛЕКТРИЧЕСКАЯ ПОСТОЯННАЯ
- ДИЭЛЕКТРИЧЕСКАЯ ПРОНИЦАЕМОСТЬ
- ЗАКОН КОЛЬРАУША
- ЗАКОН РАЗВЕДЕНИЯ ОСТВАЛЬДА
- ЗАКОНЫ ФАРАДЕЯ
- ИНДИКАТОР
- ИНДИКАТОРНЫЙ ЭЛЕКТРОД
- ИНДИФФЕРЕНТНЫЙ (ФОНОВЫЙ) ЭЛЕКТРОЛИТ
- ИОДНЫЙ КУЛОНОМЕТР
- ИОННАЯ АТМОСФЕРА
- ИОННЫЕ ПАРЫ
- ИОННЫЕ РАСПЛАВЫ
- ИОНОСЕЛЕКТИВНЫЕ ЭЛЕКТРОДЫ
- КАДМИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- КАЛОМЕЛЬНЫЙ ЭЛЕКТРОД
- КАЛЬЦИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- КАПИЛЛЯР ЛУГГИНА
- КАТИОН
- КАТИОНОСЕЛЕКТИВНЫЙ ЭЛЕКТРОД
- КАТОД
- КАТОДНАЯ ЗАЩИТА
- КИСЛОРОДНОЕ ПЕРЕНАПРЯЖЕНИЕ
- КИСЛОРОДНЫЙ ЭЛЕКТРОД (КИСЛОРОДНЫЙ ЗОНД)
- КОМПЛЕКСНЫЕ ИОНЫ
- КОНВЕНЦИЯ О ЗНАКАХ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- КОНСТАНТА ДИССОЦИАЦИИ
- КОНТАКТНАЯ РАЗНОСТЬ ПОТЕНЦИАЛОВ
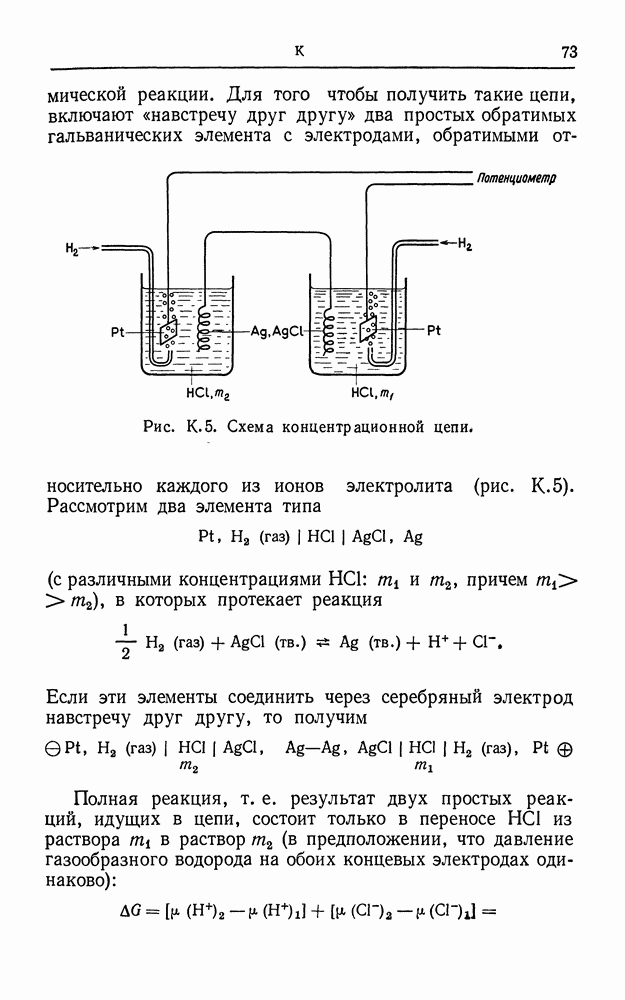
- КОНЦЕНТРАЦИОННАЯ ЦЕПЬ
- КОНЦЕНТРАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
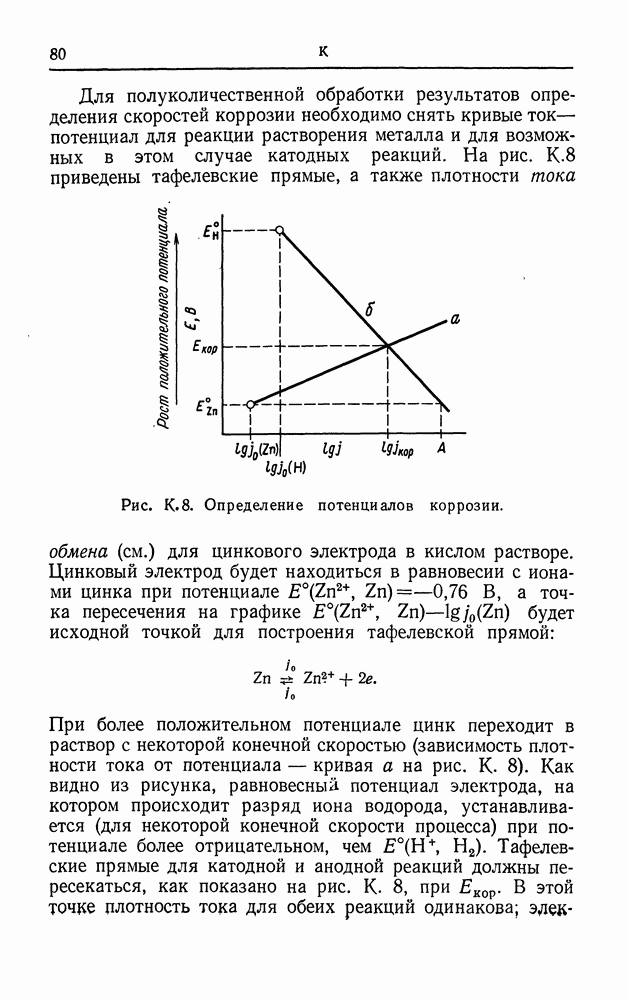
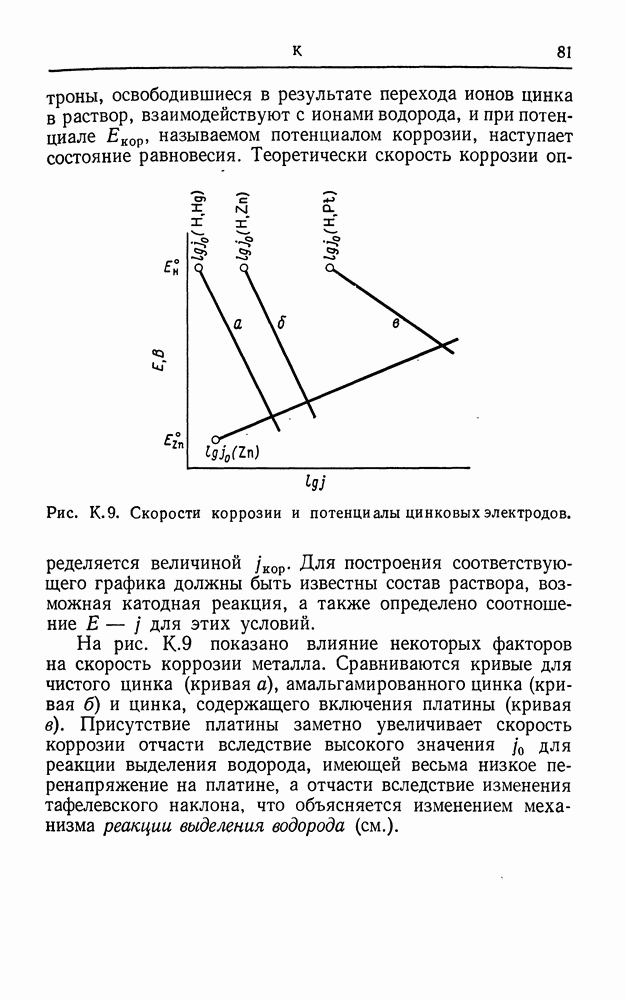
- КОРРОЗИЯ
- КОЭФФИЦИЕНТ АКТИВНОСТИ
- КУЛОН
- КУЛОНОМЕТР
- КУЛОНОМЕТРИЯ
- ЛИТИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- МАГНИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- МЕДНООКИСНЫЙ ЭЛЕМЕНТ
- МЕДНЫЙ КУЛОНОМЕТР
- МЕДЬ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- МЕМБРАННЫЙ ЭЛЕКТРОД
- МЕТАЛЛИЧЕСКИЙ ЭЛЕКТРОД
- МЕТАЛЛООКИСНЫЙ ЭЛЕКТРОД
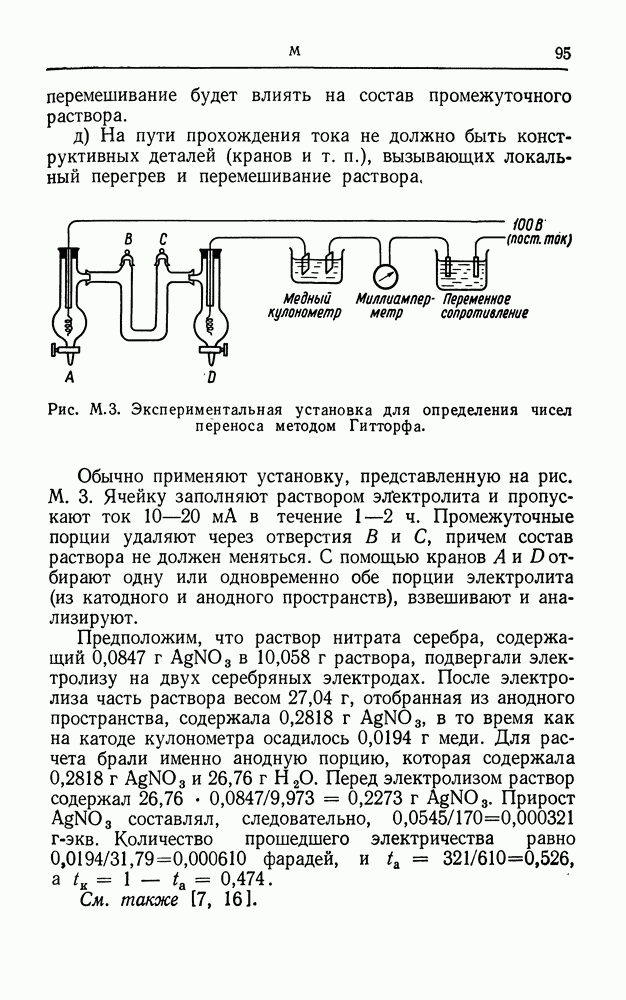
- МЕТОД ГИТТОРФА
- МЕТОД ДВИЖУЩЕЙСЯ ГРАНИЦЫ
- МЕХАНИЗМЫ ЭЛЕКТРОДНЫХ РЕАКЦИЙ
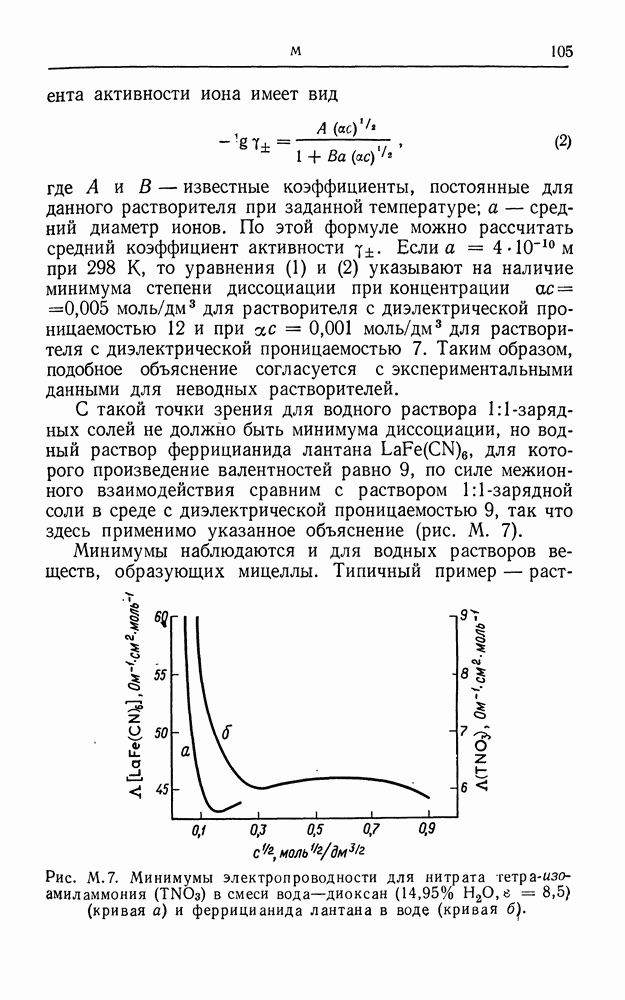
- МИНИМУМЫ ЭЛЕКТРОПРОВОДНОСТИ
- МОЛЬНАЯ ИОННАЯ ЭЛЕКТРОПРОВОДНОСТЬ
- МОСТ УИТСТОНА
- НАПРЯЖЕНИЕ РАЗЛОЖЕНИЯ
- НЕВОДНЫЕ РАСТВОРЫ
- НИКЕЛЬ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- ОБРАТИМЫЙ ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ (РЕДОКС) ЭЛЕКТРОДНАЯ СИСТЕМА
- ОМ
- ОПРЕСНЕНИЕ ВОДЫ
- ОСЦИЛЛОМЕТРИЯ
- ПАССИВНОСТЬ
- ПЕРВИЧНЫЙ ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
- ПЕРЕНАПРЯЖЕНИЕ
- ПЕРЕНАПРЯЖЕНИЕ ВОДОРОДА
- ПЕРЕХОДНОЕ ВРЕМЯ
- ПЕРСОЛИ
- ПЛАТИНОВЫЕ И ЗОЛОТЫЕ ЭЛЕКТРОДЫ
- рН-МЕТР
- ПОДВИЖНОСТЬ
- ПОДВИЖНОСТЬ ИОНОВ
- ПОЛУЭЛЕМЕНТ
- ПОЛЯРИЗАЦИОННЫЕ КРИВЫЕ
- ПОЛЯРИЗАЦИЯ
- ПОЛЯРИЗУЕМЫЕ ЭЛЕКТРОДЫ
- ПОЛЯРОГРАФИЯ
- ПОПРАВКА НА ЭЛЕКТРОПРОВОДНОСТЬ РАСТВОРИТЕЛЯ
- ПОСТОЯННАЯ ЯЧЕЙКИ
- ПОТЕНЦИАЛ, ОБРАТИМЫЕ ЭЛЕКТРОДЫ
- ПОТЕНЦИАЛ ПОЛУВОЛНЫ
- ПОТЕНЦИАЛ СЕДИМЕНТАЦИИ
- ПОТЕНЦИАЛ ТЕЧЕНИЯ
- ПОТЕНЦИОМЕТР
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ПОТЕНЦИОСТАТ
- ПРАВИЛО ВАЛЬДЕНА
- ПРЕДЕЛЬНЫЙ ТОК
- ПРОТЕКТОРНАЯ ЗАЩИТА
- РАСПЛАВЫ СОЛЕЙ
- РЕАКЦИЯ ВЫДЕЛЕНИЯ ВОДОРОДА
- РТУТНЫЙ ЭЛЕМЕНТ
- РЯД ПОТЕНЦИАЛОВ
- СВИНЦОВЫЙ АККУМУЛЯТОР
- СЕРЕБРЯНЫЙ КУЛОНОМЕТР
- СЕРЕБРЯНЫЙ ЭЛЕКТРОД
- СЛОЙ ГЕЛЬМГОЛЬЦА
- СЛОЙ ГУИ
- СОЛЕВОЙ МОСТИК
- СТАНДАРТНЫЕ РАСТВОРЫ ДЛЯ ЭЛЕКТРОПРОВОДНОСТИ
- СТАНДАРТНЫЙ ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
- СТАНДАРТНЫЙ ЭЛЕМЕНТ
- СТЕКЛЯННЫЙ ЭЛЕКТРОД
- СУРЬМЯНЫЙ ЭЛЕКТРОД
- СУХОЙ ЭЛЕМЕНТ
- ТЕОРИЯ ИОННОЙ АССОЦИАЦИИ БЬЕРРУМА
- ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ АРРЕНИУСА
- ТЕРМОДИНАМИКА ГАЛЬВАНИЧЕСКИХ ЭЛЕМЕНТОВ
- ТОК ОБМЕНА
- ТОПЛИВНЫЙ ЭЛЕМЕНТ
- УРАВНЕНИЕ БРЕНСТЕДА—БЬЕРРУМА
- УРАВНЕНИЕ ДЕБАЯ — ХЮККЕЛЯ
- УРАВНЕНИЕ ИЛЬКОВИЧА
- УРАВНЕНИЕ НЕРНСТА
- УРАВНЕНИЕ ОНЗАГЕРА
- УРАВНЕНИЕ ТАФЕЛЯ
- УРАВНЕНИЕ ЭЛЕКТРОПРОВОДНОСТИ ПИТТСА
- УРАВНЕНИЕ ЭЛЕКТРОПРОВОДНОСТИ ФУОССА
- УРАВНЕНИЯ ЭЛЕКТРОПРОВОДНОСТИ
- ХЕМОТРОНЫ
- ХИНГИДРОННЫЙ ЭЛЕКТРОД
- ХЛОРНЫЙ ЭЛЕКТРОД
- ХЛОРСЕРЕБРЯНЫЙ ЭЛЕКТРОД
- ХРОНОАМПЕРОМЕТРИЯ
- ХРОНОПОТЕНЦИОМЕТРИЯ
- ЦИНК-ВОЗДУШНЫЙ ЭЛЕМЕНТ
- ЦИНК-СЕРЕБРЯНЫЙ ЭЛЕМЕНТ
- ЦИНК, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- ЦИФРОВОЙ ВОЛЬТМЕТР
- ЧАСТОТНАЯ ЗАВИСИМОСТЬ ЭЛЕКТРОПРОВОДНОСТИ
- ЧИСЛА ПЕРЕНОСА
- ЧИСЛО ФАРАДЕЯ
- ЩЕЛОЧНЫЕ АККУМУЛЯТОРЫ
- ЭЛЕКТРИЧЕСКАЯ ЕМКОСТЬ
- ЭЛЕКТРИЧЕСКИЕ ЕДИНИЦЫ ИЗМЕРЕНИЯ
- ЭЛЕКТРОВЕСОВОЙ АНАЛИЗ
- ЭЛЕКТРОД
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА (Э.Д.С.)
- ЭЛЕКТРОДИАЛИЗ
- ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
- ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ
- ЭЛЕКТРОЛИЗ ВОДЫ
- ЭЛЕКТРОЛИЗЕР
- ЭЛЕКТРОЛИЗ РАСТВОРА ПОВАРЕННОЙ СОЛИ
- ЭЛЕКТРОЛИТИЧЕСКАЯ ОЧИСТКА (РАФИНИРОВАНИЕ)
- ЭЛЕКТРОЛИТИЧЕСКОЕ ВОССТАНОВЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ЭЛЕКТРОЛИТИЧЕСКОЕ ОКИСЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ЭЛЕКТРОЛИТИЧЕСКОЕ ПОЛИРОВАНИЕ
- ЭЛЕКТРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ЭЛЕКТРООСАЖДЕНИЕ МЕТАЛЛОВ
- ЭЛЕКТРООСАЖДЕНИЕ СПЛАВОВ
- ЭЛЕКТРООСМОС
- ЭЛЕКТРОПРОВОДНОСТЬ
- ЭЛЕКТРОПРОВОДНОСТЬ ВОДНЫХ РАСТВОРОВ
- ЭЛЕКТРОПРОВОДНОСТЬ НА ВЫСОКИХ ЧАСТОТАХ
- ЭЛЕКТРОПРОВОДНОСТЬ НЕВОДНЫХ РАСТВОРОВ
- ЭЛЕКТРОПРОВОДНОСТЬ ПРИ БЕСКОНЕЧНОМ РАЗБАВЛЕНИИ
- ЭЛЕКТРОПРОВОДНОСТЬ ПРИ ВЫСОКИХ НАПРЯЖЕННОСТЯХ ПОЛЯ
- ЭЛЕКТРОПРОВОДНОСТЬ РАСПЛАВОВ СОЛЕЙ
- ЭЛЕКТРОФОРЕЗ
- ЭЛЕКТРОХИМИЧЕСКАЯ РАЗМЕРНАЯ ОБРАБОТКА МЕТАЛЛОВ
- ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ ИНФОРМАЦИИ
- ЭЛЕКТРОХИМИЧЕСКИЙ ЭКВИВАЛЕНТ
- ЭЛЕМЕНТ ВЕСТОНА
- ЭЛЕМЕНТ ДАНИЭЛЯ
- ЭЛЕМЕНТ КЛАРКА
- ЭЛЕМЕНТЫ С МАГНИЕВЫМИ АНОДАМИ
- ЭФФЕКТ ВИНА
- ЭФФЕКТ ДОРНА
- ЭФФЕКТ ФАЛЬКЕНГАГЕНА
- СПИСОК ЛИТЕРАТУРЫ