| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
НЕВОДНЫЕ РАСТВОРЫ
С точки зрения электрохимии неводные растворители имеют то потенциальное преимущество, что они позволяют проводить процессы, которые не идут в воде. Однако широкое применение неводных растворителей сдерживается
ограниченной растворимостью в них большинства электролитов и необходимостью удаления следов воды (и кислорода) и проведения работ в отсутствие контакта с влагой воздуха. Так, раствор  в чистом апротонном растворителе является неэлектропроводным, но добавление всего лишь 0,018 г воды на
в чистом апротонном растворителе является неэлектропроводным, но добавление всего лишь 0,018 г воды на  превращает его в сильный электролит, содержащий ионы
превращает его в сильный электролит, содержащий ионы 
Электропроводность растворов солей
Растворитель влияет на электропроводность соли, изменяя следующие характеристики: а) вязкость, б) диэлектрическую проницаемость и в) силы взаимодействия с ионами (сольватация), которые зависят от структуры, размеров молекул растворителя, а также от расположения и ориентации диполей растворителя.
При бесконечном разбавлении мольная электропроводность определяется в первую очередь вязкостью; так, мольные электропроводности обычных ионов в ацетоне значительно выше, чем в воде. В тех случаях, когда данных не хватает, приближенные значения  можно вычислить из данных для другого растворителя, используя правило Вальдена
можно вычислить из данных для другого растворителя, используя правило Вальдена

Это правило не учитывает фактора «в», но довольно хорошо выполняется для больших ионов типа ионов тетраалкил-аммония и для большинства неполярных растворителей, для которых можно пренебречь сольватацией.
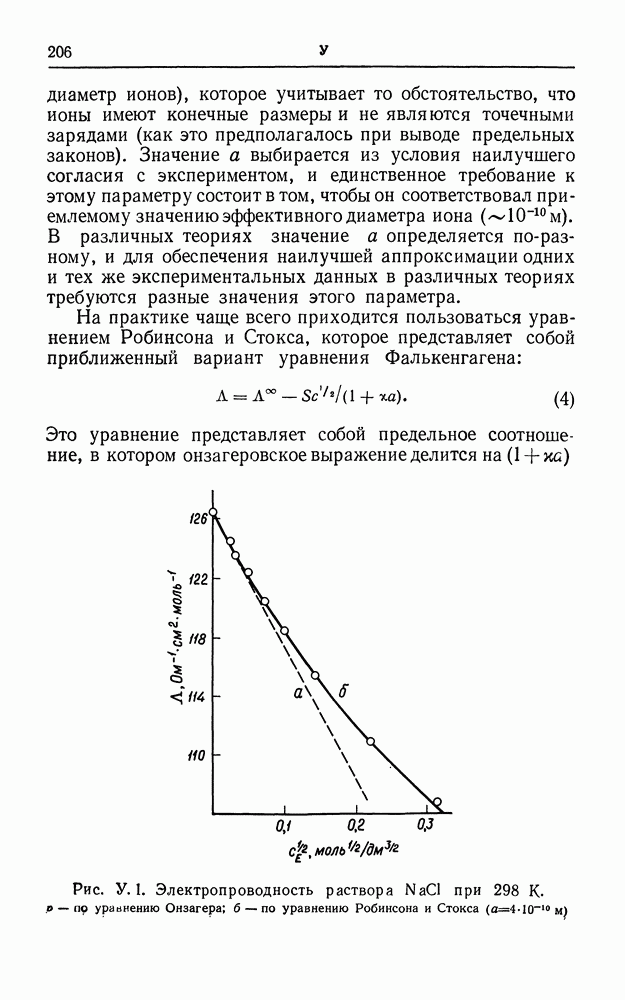
Измерения при очень низких концентрациях подтвердили применимость уравнения Онзагера (см.) для большого числа систем; можно предположить, что оно является достаточно общим. Однако при определенных концентрациях диэлектрическая проницаемость растворителя становится наиболее важным фактором. Величины диэлектрической проницаемости для некоторых употребительных растворителей (см. табл. II в конце книги) значительно ниже, чем для воды. В этих растворителях кулоновское притяжение значительно сильнее, наклоны графиков, построенных по уравнению Онзагера, существенно круче, образование ионных пар является более общим и глубоким процессом,
чем в воде, так что электропроводность быстро падает до низких значений.

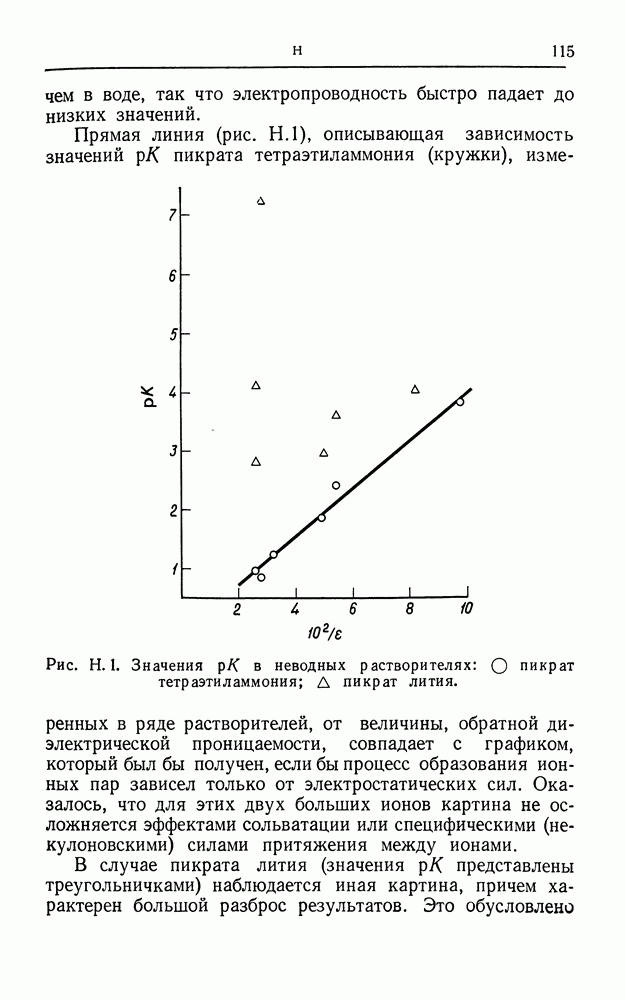
Рис. Н. 1. Значения  в неводных растворителях: О пикрат тетраэтиламмония;
в неводных растворителях: О пикрат тетраэтиламмония;  пикрат лития.
пикрат лития.
Прямая линия (рис. Н. 1), описывающая зависимость значений  пикрата тетраэтиламмония (кружки), измеренных в ряде растворителей, от величины, обратной диэлектрической проницаемости, совпадает с графиком, который был бы получен, если бы процесс образования ионных пар зависел только от электростатических сил. Оказалось, что для этих двух больших ионов картина не осложняется эффектами сольватации или специфическими (не-кулоновскими) силами притяжения между ионами.
пикрата тетраэтиламмония (кружки), измеренных в ряде растворителей, от величины, обратной диэлектрической проницаемости, совпадает с графиком, который был бы получен, если бы процесс образования ионных пар зависел только от электростатических сил. Оказалось, что для этих двух больших ионов картина не осложняется эффектами сольватации или специфическими (не-кулоновскими) силами притяжения между ионами.
В случае пикрата лития (значения  представлены треугольничками) наблюдается иная картина, причем характерен большой разброс результатов. Это обусловлено
представлены треугольничками) наблюдается иная картина, причем характерен большой разброс результатов. Это обусловлено
влиянием третьего из вышеупомянутых факторов — сольватации. В общем, четыре точки лежат примерно на прямой линии: вероятно, в четырех рассматриваемых растворителях — ацетонитриле, ацетоне, метилэтилкетоне и пиридине—катион малого размера сильно сольватирован, т. е. имеет оболочку из растворителя, которая с трудом замещается. Две другие точки соответствуют растворам в нитрометане и нитробензоле. Эти растворители обладают сравнительно высокой диэлектрической проницаемостью, а сольватация в них слишком слаба, чтобы предотвратить ассоциацию ионов; следовательно, небольшие ионы дают исключительно слабодиссоциирующие соли, причем их растворимости тоже являются низкими.
Проведение такого рода сравнений позволило классифицировать растворители на «выравнивающие» и «дифференцирующие». В выравнивающих растворителях, например в воде, гидроксилсодержащих растворителях и аминах, уравнение Онзагера соблюдается в широком интервале концентраций. При этом среди солей щелочных металлов соли  являются более сильными (меньше связываются в ионные пары), чем соли
являются более сильными (меньше связываются в ионные пары), чем соли  и К, а значения
и К, а значения  всех этих солей сравнимы со значениями
всех этих солей сравнимы со значениями  тетраалкиламмониевых солей. В дифференцирующих растворителях сольватацию можно обнаружить, но, как правило, она достаточно слабая и не обеспечивает выравнивания. В таких растворителях значения
тетраалкиламмониевых солей. В дифференцирующих растворителях сольватацию можно обнаружить, но, как правило, она достаточно слабая и не обеспечивает выравнивания. В таких растворителях значения  выше и варьируют больше, причем соли меньших ионов могут быть очень слабыми электролитами, тогда как для солей больших ионов различие между двумя классами несущественно.
выше и варьируют больше, причем соли меньших ионов могут быть очень слабыми электролитами, тогда как для солей больших ионов различие между двумя классами несущественно.
Сольватация может отчетливо проявляться в некоторых особых случаях. Например, известно, что ион серебра образует очень стабильные аммиакаты и в соответствии с этим серебряные соли растворимы и являются довольно сильными электролитами в азотсодержащих растворителях.
Кислоты и основания
Наличие у электролита кислотных свойств зависит от того, имеются ли в растворе молекулы основания, к которым могут присоединяться протоны. Хотя обсуждавшиеся выше
три фактора применимы также к кислотным и основным электролитам, решающее влияние на ионизацию и электропроводность кислоты оказывает сила растворителя как основания и наоборот. Поэтому вещества, которые в воде являются неэлектролитами, в уксусной или серной кислоте могут диссоциировать как основания. Аналогично измерениями электропроводности в аммиаке или другом основном растворителе можно обнаружить относительно сильные кислотные свойства у веществ, которые в водных растворах обладают слабыми кислотными свойствами. Точно так же кислоты, которые полностью диссоциируют в воде (например,  ), обнаруживают умеренную кислотность в менее основном по сравнению с водой растворителе, таком, как уксусная кислота или ацетонитрил.
), обнаруживают умеренную кислотность в менее основном по сравнению с водой растворителе, таком, как уксусная кислота или ацетонитрил.
Электрохимические процессы
Стандартный электродный потенциал (см.) в неводных растворителях часто мало отличается от такового в воде, хотя различия в степени сольватации ионов могут привести к некоторому его смещению. Для измерения электродных потенциалов в неводных растворителях обычно пригодны электроды сравнения, используемые для водных растворов. Однако при замене растворителя скорости электрохимических реакций могут радикально измениться, поскольку изменятся факторы, определяющие легкость перехода электронов на поверхности электрода. К таким факторам относятся сольватация электроактивных ионов, их способность к образованию ионных пар и комплексообразованию, адсорбируемость растворителя и активных частиц на поверхности электрода и ряд других, которые могут влиять на структуру двойного электрического слоя (см.).
Различные общеизвестные электроаналитические методы успешно использовались и в случае неводных растворителей. Другие представляют интерес с точки зрения применения к электроосаждению активных металлов,  и т. д., для чего обычно используют смеси расплавленных солей. Можно применять растворители типа формамида, ацетонитрила или этилендиамина, но их пригодность ограничена требованиями в отношении электропроводности
и т. д., для чего обычно используют смеси расплавленных солей. Можно применять растворители типа формамида, ацетонитрила или этилендиамина, но их пригодность ограничена требованиями в отношении электропроводности
растворов и другими практическими трудностями. Электролизом эфирных растворов получали бериллий, титан и цирконий. Чистые соли в эфире не проводят электрический ток, но смеси, например  и хлорида или бромида металла, обеспечивают нужную электропроводность и дают качественные осадки металлов.
и хлорида или бромида металла, обеспечивают нужную электропроводность и дают качественные осадки металлов.
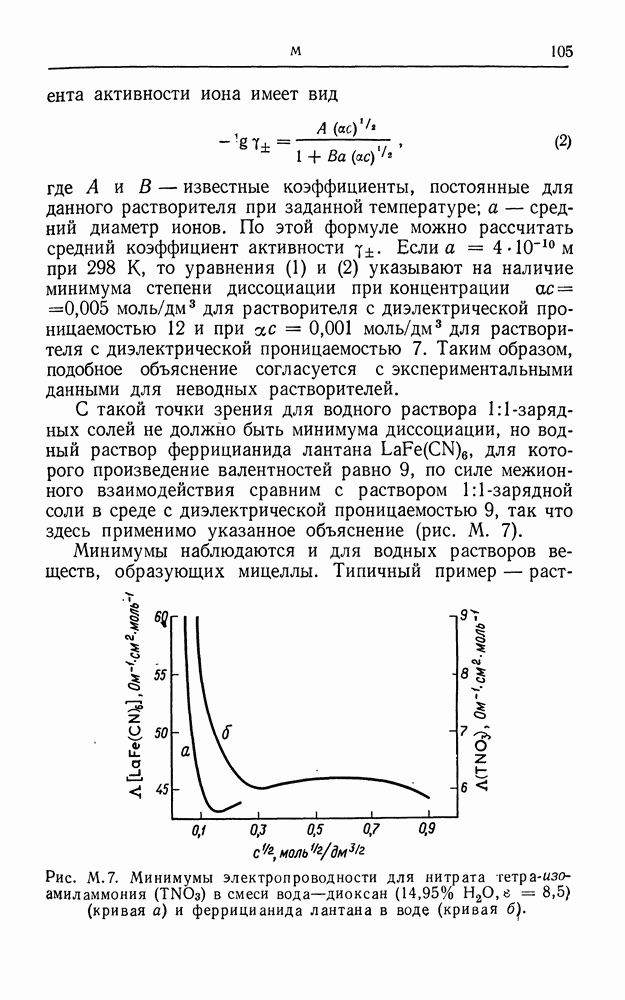
См. также Минимумы электропроводности; [6, 18].
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- О ПОЛЬЗОВАНИИ СЛОВАРЕМ
- СПИСОК ОСНОВНЫХ ОБОЗНАЧЕНИЙ
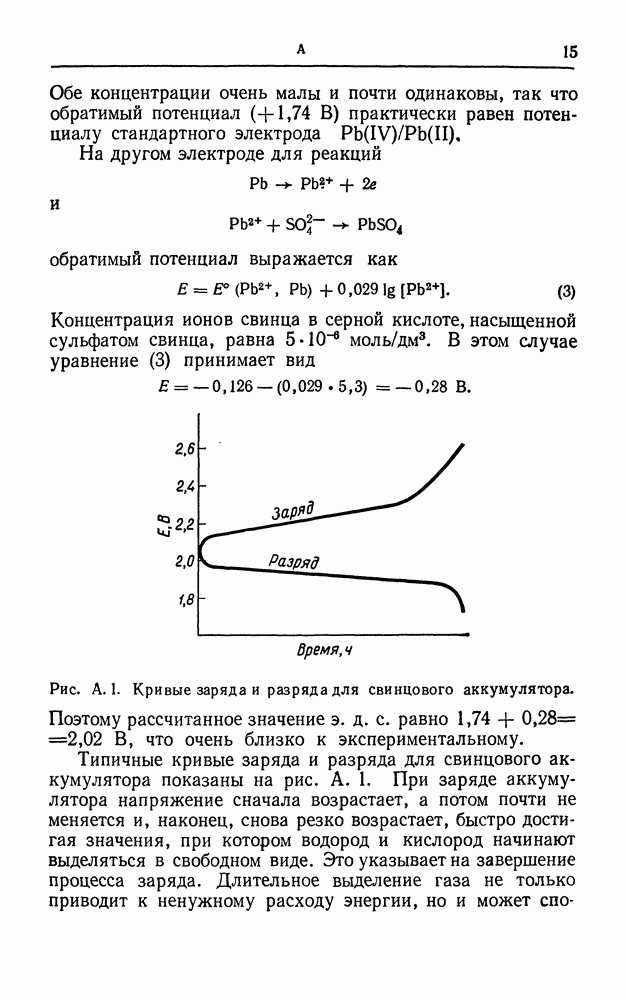
- АККУМУЛЯТОР
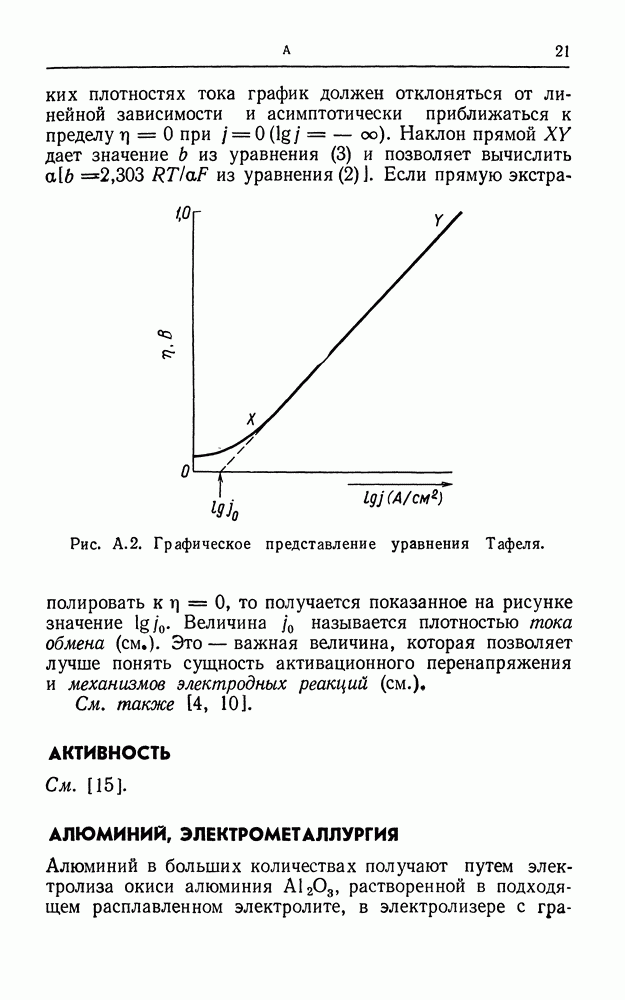
- АКТИВАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
- АКТИВНОСТЬ
- АЛЮМИНИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- АМАЛЬГАМНЫЙ ЭЛЕКТРОД
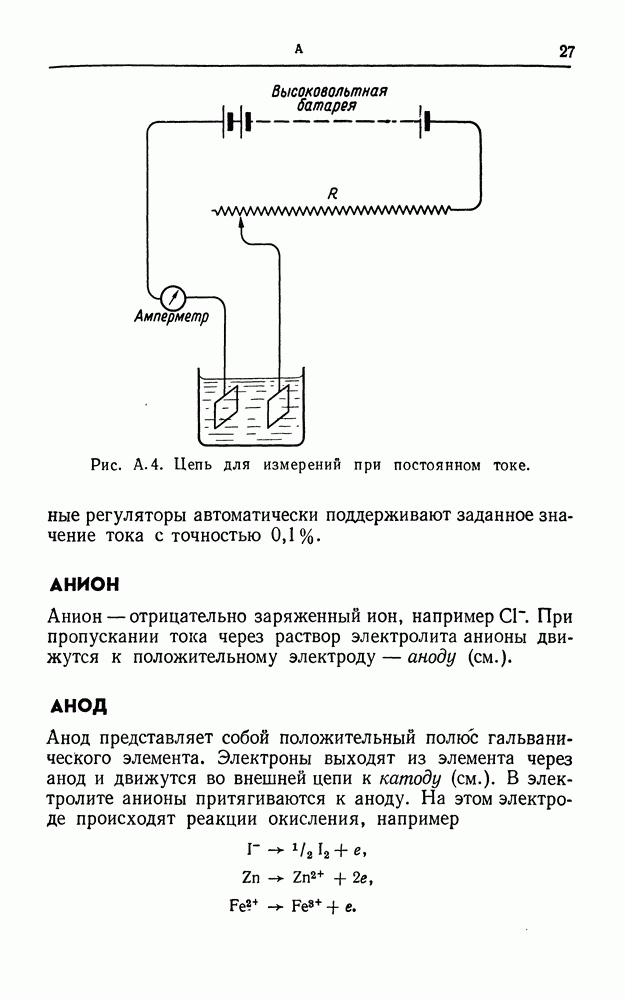
- АМПЕР
- АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- АМПЕРОСТАТ
- АНИОН
- АНОД
- АНОДИРОВАНИЕ
- БАТАРЕЯ
- БЕРИЛЛИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- БИПОЛЯРНЫЙ ЭЛЕКТРОД
- БЛЕСКООБРАЗОВАТЕЛИ
- БУФЕРНЫЙ РАСТВОР
- ВАГНЕРОВСКОЕ ЗАЗЕМЛЕНИЕ
- ВНУТРЕННИЙ ЭЛЕКТРОЛИЗ
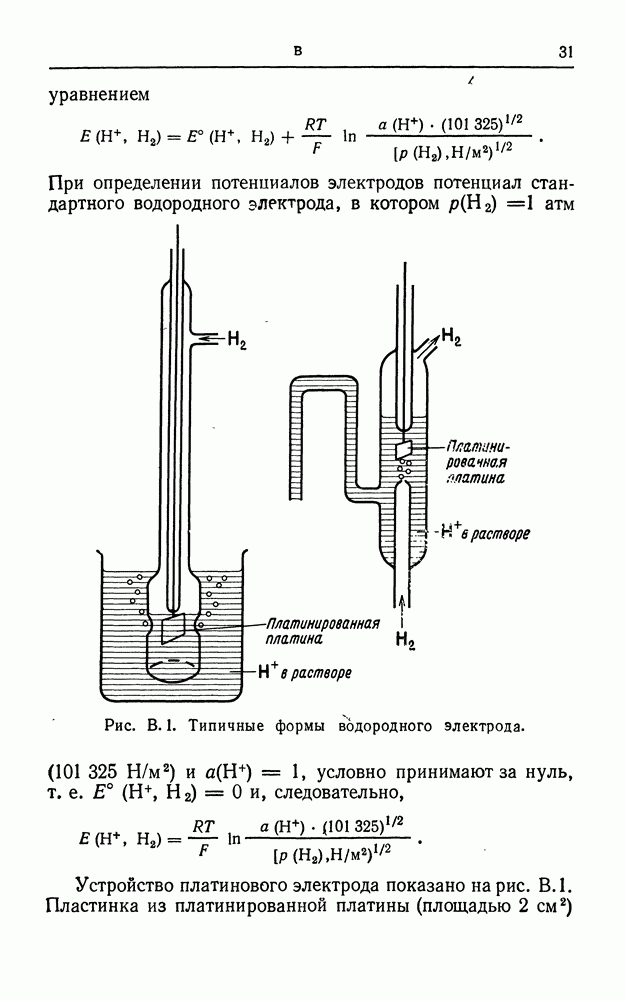
- ВОДОРОДНЫЙ ЭЛЕКТРОД
- ВОЛЬТ
- ВОЛЬФРАМОВЫЙ ЭЛЕКТРОД
- ВЫХОД ПО ТОКУ
- ГАЗОВЫЙ ЭЛЕКТРОД
- ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
- ГАЛЬВАНОПЛАСТИКА
- ГАЛЬВАНОСТАТ
- ГАЛЬВАНОСТЕГИЯ
- ГИДРАТАЦИЯ ИОНОВ
- ДАТЧИК АММИАКА
- ДАТЧИК СЕРНИСТОГО ГАЗА
- ДВОЙНОЙ СЛОЙ
- ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ
- ДЗЕТА-ПОТЕНЦИАЛ
- ДИФФУЗИОННЫЙ ПОТЕНЦИАЛ
- ДИФФУЗИЯ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- ДИЭЛЕКТРИЧЕСКАЯ ПОСТОЯННАЯ
- ДИЭЛЕКТРИЧЕСКАЯ ПРОНИЦАЕМОСТЬ
- ЗАКОН КОЛЬРАУША
- ЗАКОН РАЗВЕДЕНИЯ ОСТВАЛЬДА
- ЗАКОНЫ ФАРАДЕЯ
- ИНДИКАТОР
- ИНДИКАТОРНЫЙ ЭЛЕКТРОД
- ИНДИФФЕРЕНТНЫЙ (ФОНОВЫЙ) ЭЛЕКТРОЛИТ
- ИОДНЫЙ КУЛОНОМЕТР
- ИОННАЯ АТМОСФЕРА
- ИОННЫЕ ПАРЫ
- ИОННЫЕ РАСПЛАВЫ
- ИОНОСЕЛЕКТИВНЫЕ ЭЛЕКТРОДЫ
- КАДМИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- КАЛОМЕЛЬНЫЙ ЭЛЕКТРОД
- КАЛЬЦИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- КАПИЛЛЯР ЛУГГИНА
- КАТИОН
- КАТИОНОСЕЛЕКТИВНЫЙ ЭЛЕКТРОД
- КАТОД
- КАТОДНАЯ ЗАЩИТА
- КИСЛОРОДНОЕ ПЕРЕНАПРЯЖЕНИЕ
- КИСЛОРОДНЫЙ ЭЛЕКТРОД (КИСЛОРОДНЫЙ ЗОНД)
- КОМПЛЕКСНЫЕ ИОНЫ
- КОНВЕНЦИЯ О ЗНАКАХ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- КОНСТАНТА ДИССОЦИАЦИИ
- КОНТАКТНАЯ РАЗНОСТЬ ПОТЕНЦИАЛОВ
- КОНЦЕНТРАЦИОННАЯ ЦЕПЬ
- КОНЦЕНТРАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
- КОРРОЗИЯ
- КОЭФФИЦИЕНТ АКТИВНОСТИ
- КУЛОН
- КУЛОНОМЕТР
- КУЛОНОМЕТРИЯ
- ЛИТИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- МАГНИЙ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- МЕДНООКИСНЫЙ ЭЛЕМЕНТ
- МЕДНЫЙ КУЛОНОМЕТР
- МЕДЬ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- МЕМБРАННЫЙ ЭЛЕКТРОД
- МЕТАЛЛИЧЕСКИЙ ЭЛЕКТРОД
- МЕТАЛЛООКИСНЫЙ ЭЛЕКТРОД
- МЕТОД ГИТТОРФА
- МЕТОД ДВИЖУЩЕЙСЯ ГРАНИЦЫ
- МЕХАНИЗМЫ ЭЛЕКТРОДНЫХ РЕАКЦИЙ
- МИНИМУМЫ ЭЛЕКТРОПРОВОДНОСТИ
- МОЛЬНАЯ ИОННАЯ ЭЛЕКТРОПРОВОДНОСТЬ
- МОСТ УИТСТОНА
- НАПРЯЖЕНИЕ РАЗЛОЖЕНИЯ
- НЕВОДНЫЕ РАСТВОРЫ
- НИКЕЛЬ, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- ОБРАТИМЫЙ ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ (РЕДОКС) ЭЛЕКТРОДНАЯ СИСТЕМА
- ОМ
- ОПРЕСНЕНИЕ ВОДЫ
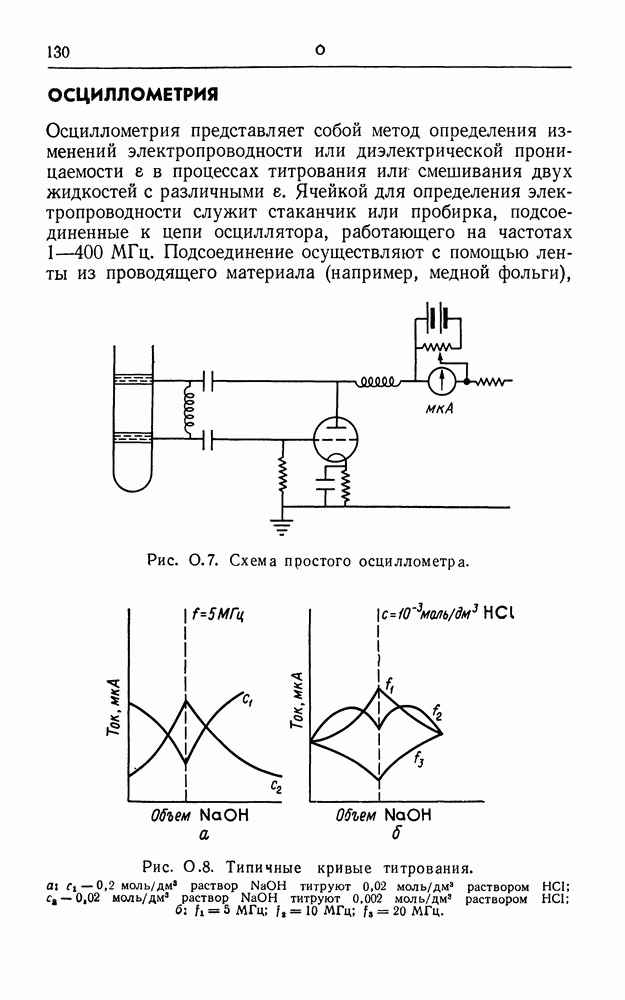
- ОСЦИЛЛОМЕТРИЯ
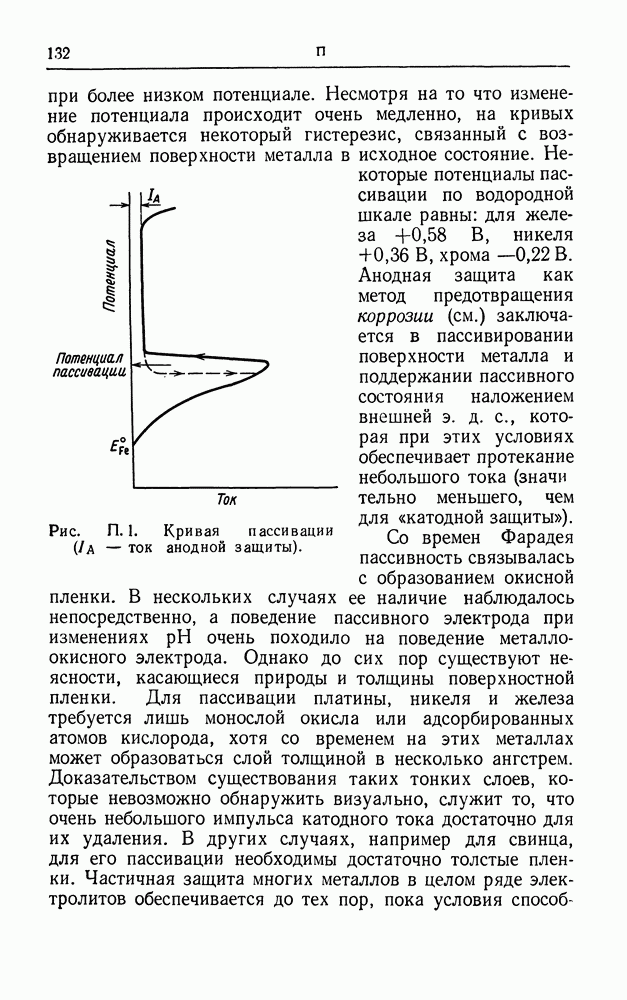
- ПАССИВНОСТЬ
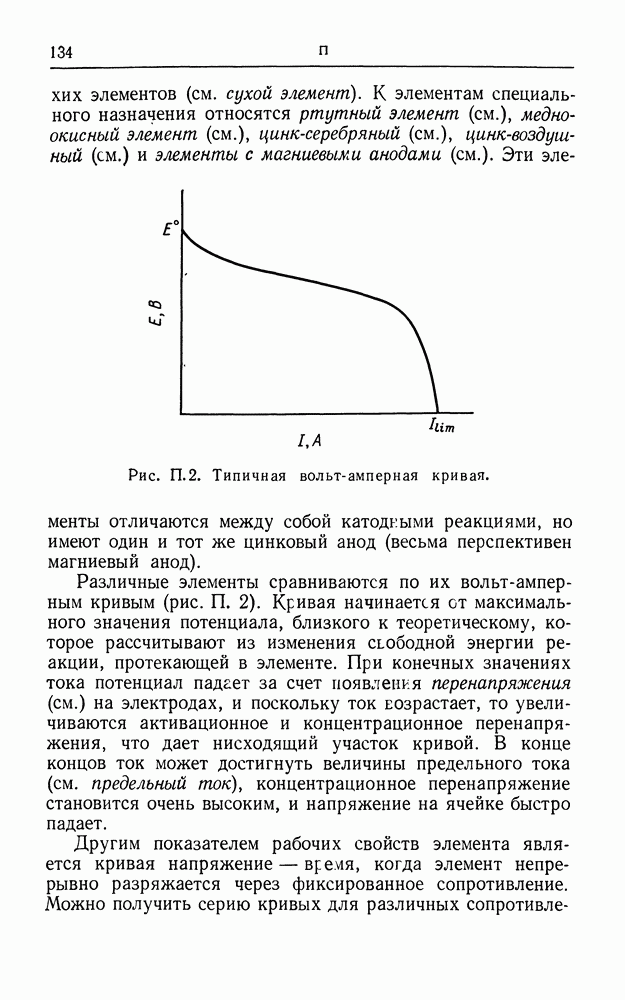
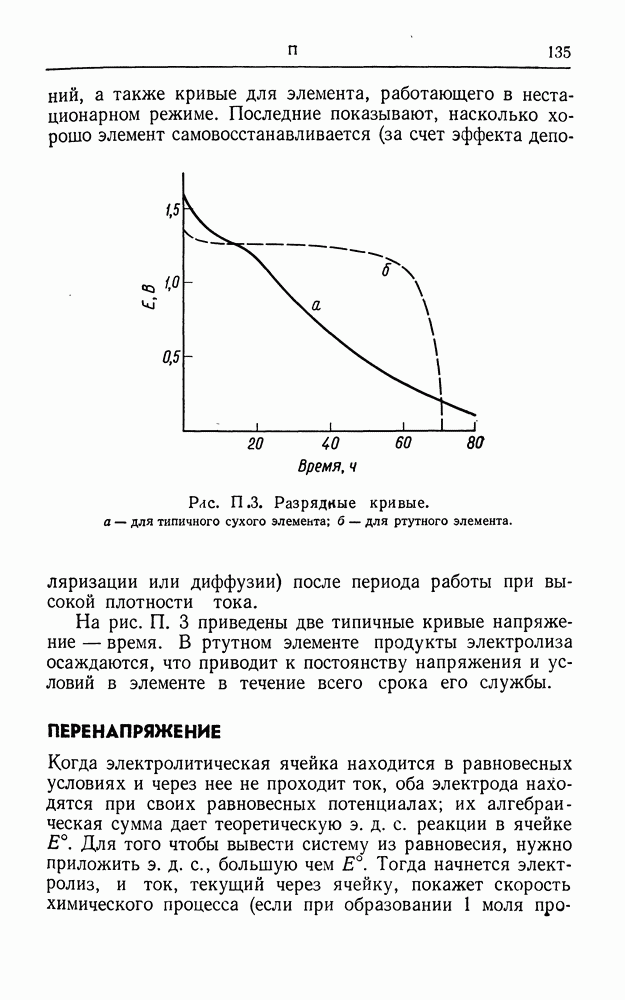
- ПЕРВИЧНЫЙ ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
- ПЕРЕНАПРЯЖЕНИЕ
- ПЕРЕНАПРЯЖЕНИЕ ВОДОРОДА
- ПЕРЕХОДНОЕ ВРЕМЯ
- ПЕРСОЛИ
- ПЛАТИНОВЫЕ И ЗОЛОТЫЕ ЭЛЕКТРОДЫ
- рН-МЕТР
- ПОДВИЖНОСТЬ
- ПОДВИЖНОСТЬ ИОНОВ
- ПОЛУЭЛЕМЕНТ
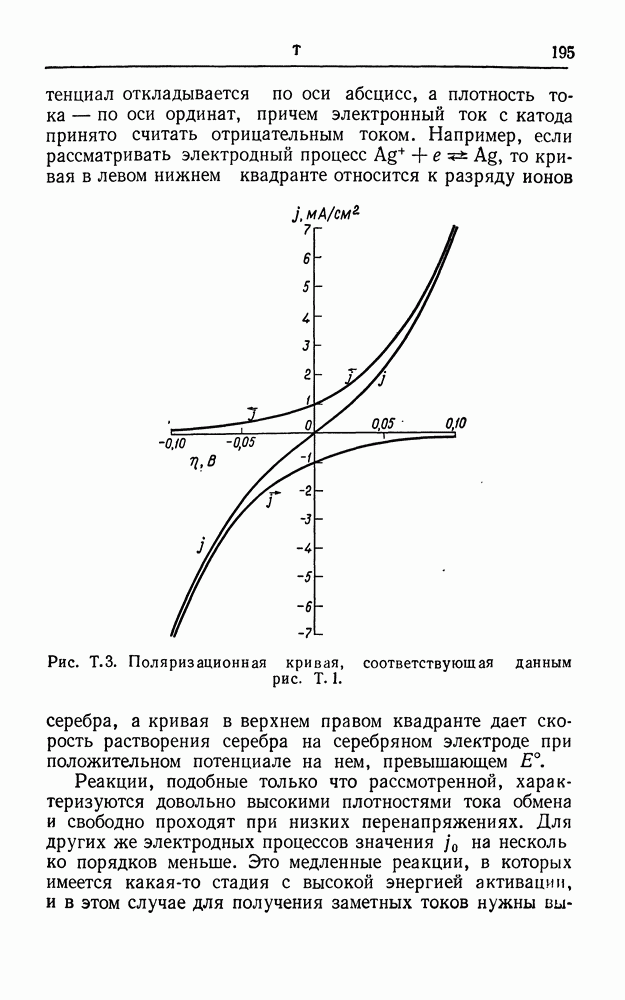
- ПОЛЯРИЗАЦИОННЫЕ КРИВЫЕ
- ПОЛЯРИЗАЦИЯ
- ПОЛЯРИЗУЕМЫЕ ЭЛЕКТРОДЫ
- ПОЛЯРОГРАФИЯ
- ПОПРАВКА НА ЭЛЕКТРОПРОВОДНОСТЬ РАСТВОРИТЕЛЯ
- ПОСТОЯННАЯ ЯЧЕЙКИ
- ПОТЕНЦИАЛ, ОБРАТИМЫЕ ЭЛЕКТРОДЫ
- ПОТЕНЦИАЛ ПОЛУВОЛНЫ
- ПОТЕНЦИАЛ СЕДИМЕНТАЦИИ
- ПОТЕНЦИАЛ ТЕЧЕНИЯ
- ПОТЕНЦИОМЕТР
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ПОТЕНЦИОСТАТ
- ПРАВИЛО ВАЛЬДЕНА
- ПРЕДЕЛЬНЫЙ ТОК
- ПРОТЕКТОРНАЯ ЗАЩИТА
- РАСПЛАВЫ СОЛЕЙ
- РЕАКЦИЯ ВЫДЕЛЕНИЯ ВОДОРОДА
- РТУТНЫЙ ЭЛЕМЕНТ
- РЯД ПОТЕНЦИАЛОВ
- СВИНЦОВЫЙ АККУМУЛЯТОР
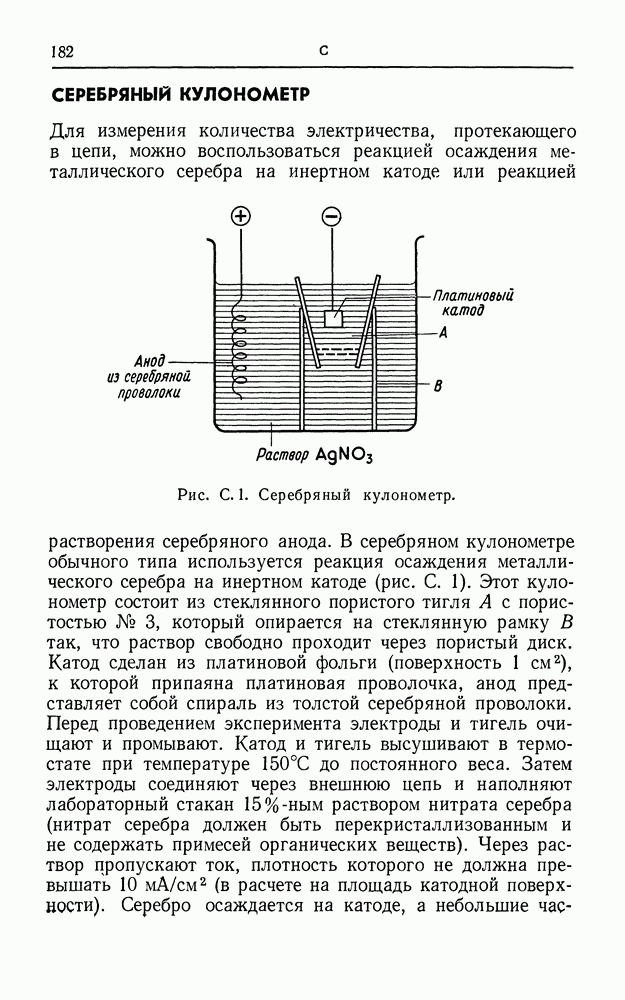
- СЕРЕБРЯНЫЙ КУЛОНОМЕТР
- СЕРЕБРЯНЫЙ ЭЛЕКТРОД
- СЛОЙ ГЕЛЬМГОЛЬЦА
- СЛОЙ ГУИ
- СОЛЕВОЙ МОСТИК
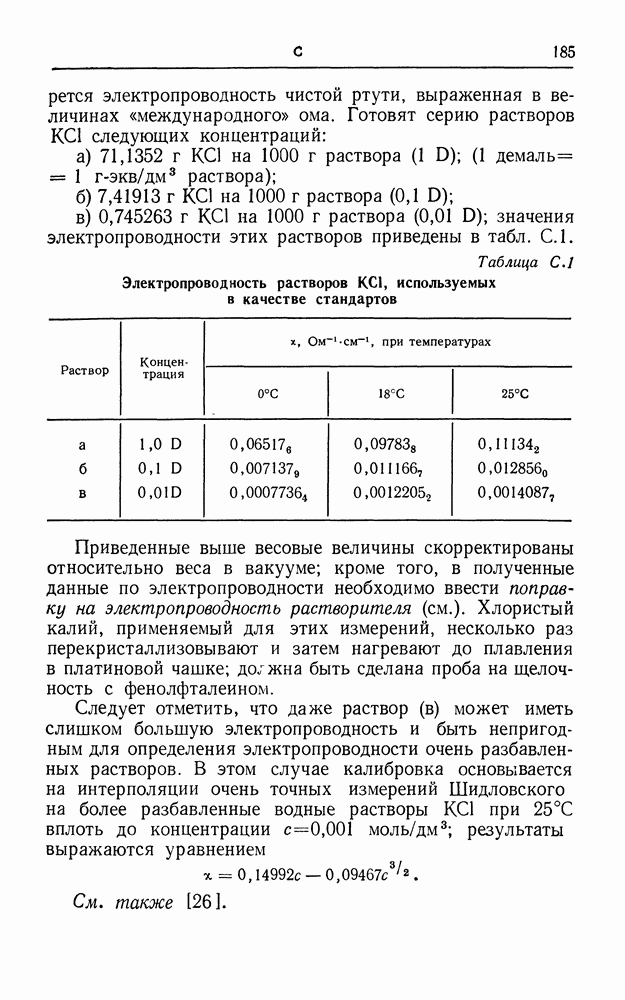
- СТАНДАРТНЫЕ РАСТВОРЫ ДЛЯ ЭЛЕКТРОПРОВОДНОСТИ
- СТАНДАРТНЫЙ ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
- СТАНДАРТНЫЙ ЭЛЕМЕНТ
- СТЕКЛЯННЫЙ ЭЛЕКТРОД
- СУРЬМЯНЫЙ ЭЛЕКТРОД
- СУХОЙ ЭЛЕМЕНТ
- ТЕОРИЯ ИОННОЙ АССОЦИАЦИИ БЬЕРРУМА
- ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ АРРЕНИУСА
- ТЕРМОДИНАМИКА ГАЛЬВАНИЧЕСКИХ ЭЛЕМЕНТОВ
- ТОК ОБМЕНА
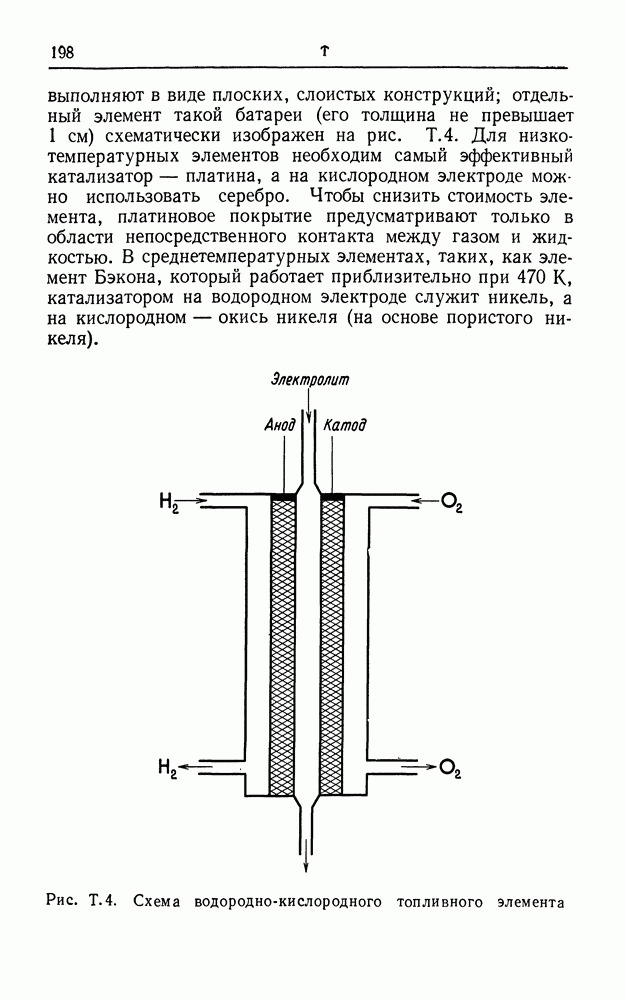
- ТОПЛИВНЫЙ ЭЛЕМЕНТ
- УРАВНЕНИЕ БРЕНСТЕДА—БЬЕРРУМА
- УРАВНЕНИЕ ДЕБАЯ — ХЮККЕЛЯ
- УРАВНЕНИЕ ИЛЬКОВИЧА
- УРАВНЕНИЕ НЕРНСТА
- УРАВНЕНИЕ ОНЗАГЕРА
- УРАВНЕНИЕ ТАФЕЛЯ
- УРАВНЕНИЕ ЭЛЕКТРОПРОВОДНОСТИ ПИТТСА
- УРАВНЕНИЕ ЭЛЕКТРОПРОВОДНОСТИ ФУОССА
- УРАВНЕНИЯ ЭЛЕКТРОПРОВОДНОСТИ
- ХЕМОТРОНЫ
- ХИНГИДРОННЫЙ ЭЛЕКТРОД
- ХЛОРНЫЙ ЭЛЕКТРОД
- ХЛОРСЕРЕБРЯНЫЙ ЭЛЕКТРОД
- ХРОНОАМПЕРОМЕТРИЯ
- ХРОНОПОТЕНЦИОМЕТРИЯ
- ЦИНК-ВОЗДУШНЫЙ ЭЛЕМЕНТ
- ЦИНК-СЕРЕБРЯНЫЙ ЭЛЕМЕНТ
- ЦИНК, ЭЛЕКТРОМЕТАЛЛУРГИЯ
- ЦИФРОВОЙ ВОЛЬТМЕТР
- ЧАСТОТНАЯ ЗАВИСИМОСТЬ ЭЛЕКТРОПРОВОДНОСТИ
- ЧИСЛА ПЕРЕНОСА
- ЧИСЛО ФАРАДЕЯ
- ЩЕЛОЧНЫЕ АККУМУЛЯТОРЫ
- ЭЛЕКТРИЧЕСКАЯ ЕМКОСТЬ
- ЭЛЕКТРИЧЕСКИЕ ЕДИНИЦЫ ИЗМЕРЕНИЯ
- ЭЛЕКТРОВЕСОВОЙ АНАЛИЗ
- ЭЛЕКТРОД
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА (Э.Д.С.)
- ЭЛЕКТРОДИАЛИЗ
- ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
- ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ
- ЭЛЕКТРОЛИЗ ВОДЫ
- ЭЛЕКТРОЛИЗЕР
- ЭЛЕКТРОЛИЗ РАСТВОРА ПОВАРЕННОЙ СОЛИ
- ЭЛЕКТРОЛИТИЧЕСКАЯ ОЧИСТКА (РАФИНИРОВАНИЕ)
- ЭЛЕКТРОЛИТИЧЕСКОЕ ВОССТАНОВЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ЭЛЕКТРОЛИТИЧЕСКОЕ ОКИСЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ЭЛЕКТРОЛИТИЧЕСКОЕ ПОЛИРОВАНИЕ
- ЭЛЕКТРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ЭЛЕКТРООСАЖДЕНИЕ МЕТАЛЛОВ
- ЭЛЕКТРООСАЖДЕНИЕ СПЛАВОВ
- ЭЛЕКТРООСМОС
- ЭЛЕКТРОПРОВОДНОСТЬ
- ЭЛЕКТРОПРОВОДНОСТЬ ВОДНЫХ РАСТВОРОВ
- ЭЛЕКТРОПРОВОДНОСТЬ НА ВЫСОКИХ ЧАСТОТАХ
- ЭЛЕКТРОПРОВОДНОСТЬ НЕВОДНЫХ РАСТВОРОВ
- ЭЛЕКТРОПРОВОДНОСТЬ ПРИ БЕСКОНЕЧНОМ РАЗБАВЛЕНИИ
- ЭЛЕКТРОПРОВОДНОСТЬ ПРИ ВЫСОКИХ НАПРЯЖЕННОСТЯХ ПОЛЯ
- ЭЛЕКТРОПРОВОДНОСТЬ РАСПЛАВОВ СОЛЕЙ
- ЭЛЕКТРОФОРЕЗ
- ЭЛЕКТРОХИМИЧЕСКАЯ РАЗМЕРНАЯ ОБРАБОТКА МЕТАЛЛОВ
- ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ ИНФОРМАЦИИ
- ЭЛЕКТРОХИМИЧЕСКИЙ ЭКВИВАЛЕНТ
- ЭЛЕМЕНТ ВЕСТОНА
- ЭЛЕМЕНТ ДАНИЭЛЯ
- ЭЛЕМЕНТ КЛАРКА
- ЭЛЕМЕНТЫ С МАГНИЕВЫМИ АНОДАМИ
- ЭФФЕКТ ВИНА
- ЭФФЕКТ ДОРНА
- ЭФФЕКТ ФАЛЬКЕНГАГЕНА
- СПИСОК ЛИТЕРАТУРЫ