| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
4.1. Предварительные эксперименты
Прежде чем начать кинетический анализ, следует четко определить реакцию, механизм которой хотят исследовать. Это означает, что обо всех реагентах и продуктах должна существовать качественная и количественная информация. Изучение материального баланса приводит к стехиометрическому уравнению и количество израсходованных веществ должно соответствовать количеству образовавшихся конечных продуктов. Как правило, знание стехиометрии более чем компенсирует время, затраченное на получение дополнительных экспериментальных данных, которые потребуются в отсутствие этих знаний. О необходимости точных сведений о рассматриваемой реакции свидетельствует, например, тот факт, что для большинства типов реакций расходование реагента соответствует одному и тому же закону скорости, например закону первого порядка. Поэтому знание лишь одного закона уменьшения концентрации исходного вещества далеко не достаточно для представления о механизме реакции.
Далее, нужно искать свойства реакционной смеси, которые меняются по мере того, как происходит реакция, и могут быть использованы как показатель хода реакции и ее глубины. Одно из требований состоит в том, чтобы выбранное свойство менялось при изменении концентрации каким-либо простым путем, желательнее всего линейно. Теоретически можно использовать любое свойство, степень изменения которого достаточна. Это означает, что такое свойство должно заметно различаться для реагентов и продуктов. Удобно выбрать свойство, изменение которого можно записывать автоматически и непрерывно. В противоположность этому для получения нужной кинетической кривой график экспериментальных данных должен строиться вручную. Обычно мы говорим «кривая  хотя, как правило, вместо абсолютных концентраций используются пропорциональные им физические величины. Среди свойств, которые можно непосредственно измерить, чаще всего используются кислотность (основность), окислительная (восстановительная) способность, агрегатное состояние (если
хотя, как правило, вместо абсолютных концентраций используются пропорциональные им физические величины. Среди свойств, которые можно непосредственно измерить, чаще всего используются кислотность (основность), окислительная (восстановительная) способность, агрегатное состояние (если
один из компонентов — газ), оптические и электрические свойства. Однако описание применяемых при этом методов выходит за рамки настоящей книги (читатель может обратиться, например, к работам [5, 46]). Частицы, ответственные за свойство, по которому следят за ходом превращения, мы будем называть кинетически измеряемыми частицами.
Другим необходимым условием успешного кинетического анализа является воспроизводимость экспериментальных результатов. Поэтому нужно быть уверенным в том, что растворы используемых веществ достаточно стабильны. В некоторых случаях бывает необходимо проверить, не зависят ли результаты эксперимента от той последовательности, в которой смешивают растворы реагентов. Для примера рассмотрим реакцию, включающую два реагента и катализатор. Было бы идеально объединить все эти три вещества одновременно при выбранной температуре. Но обычно это сделать невозможно. Тогда экспериментальные данные могут различаться в зависимости от того, какой из реагентов первым был смешан с катализатором.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
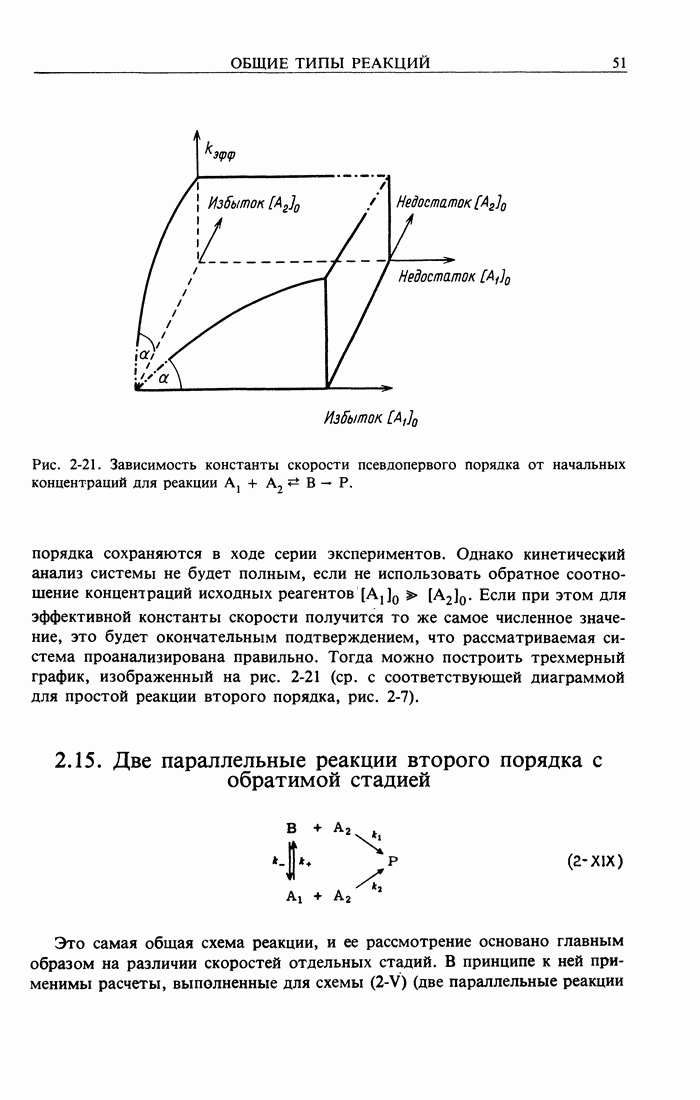
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
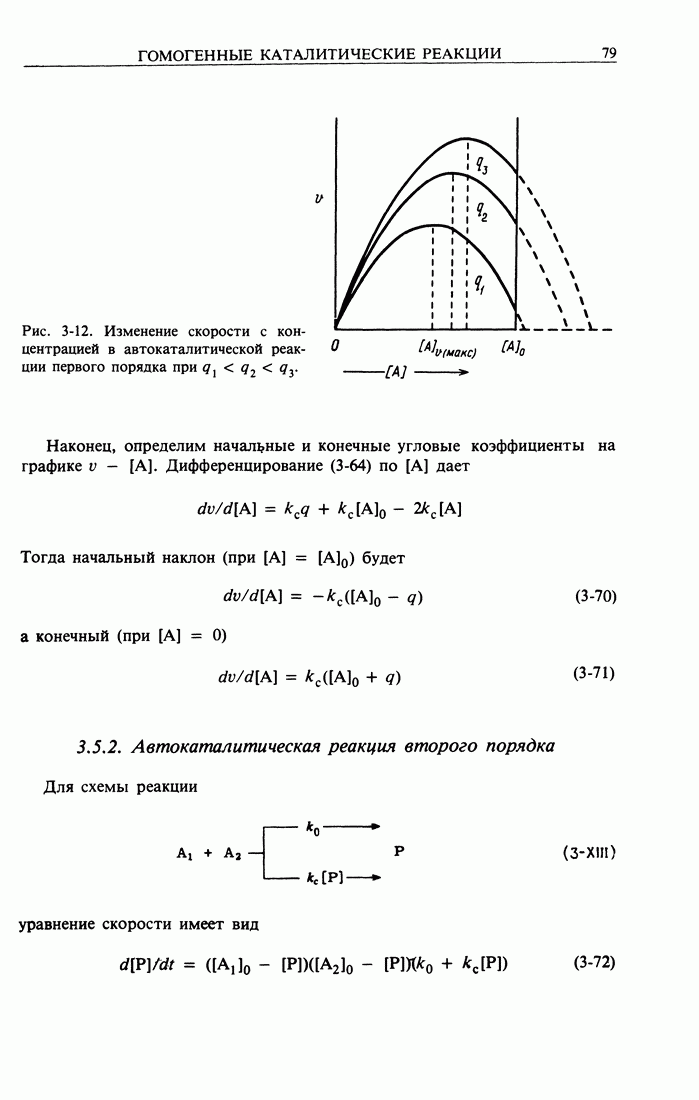
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
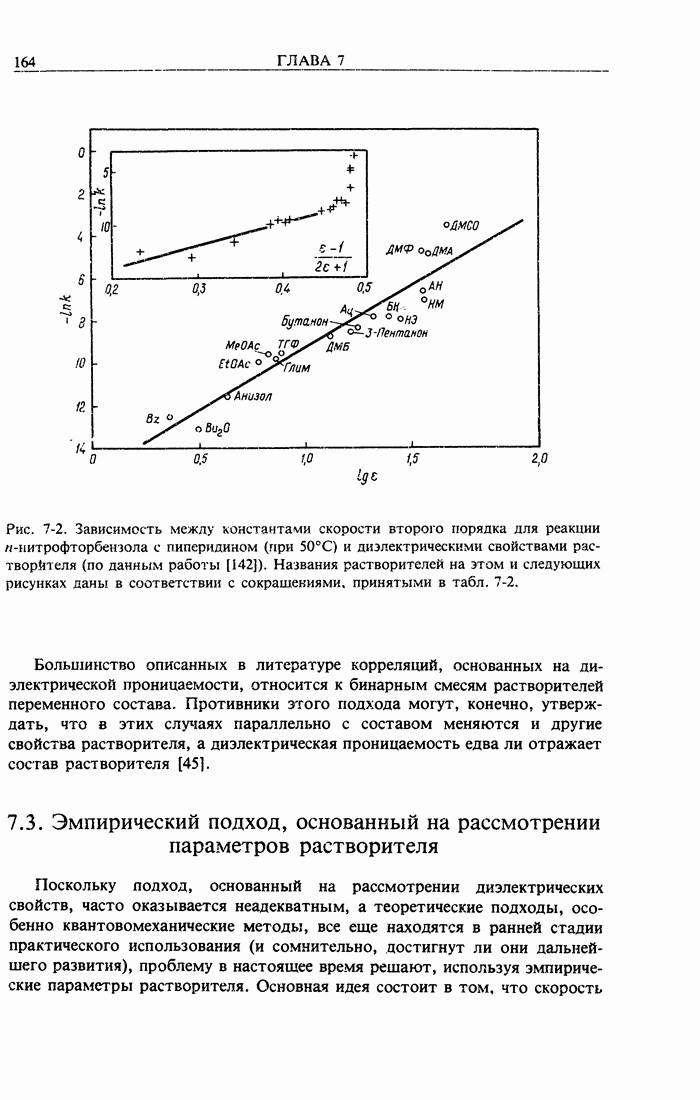
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
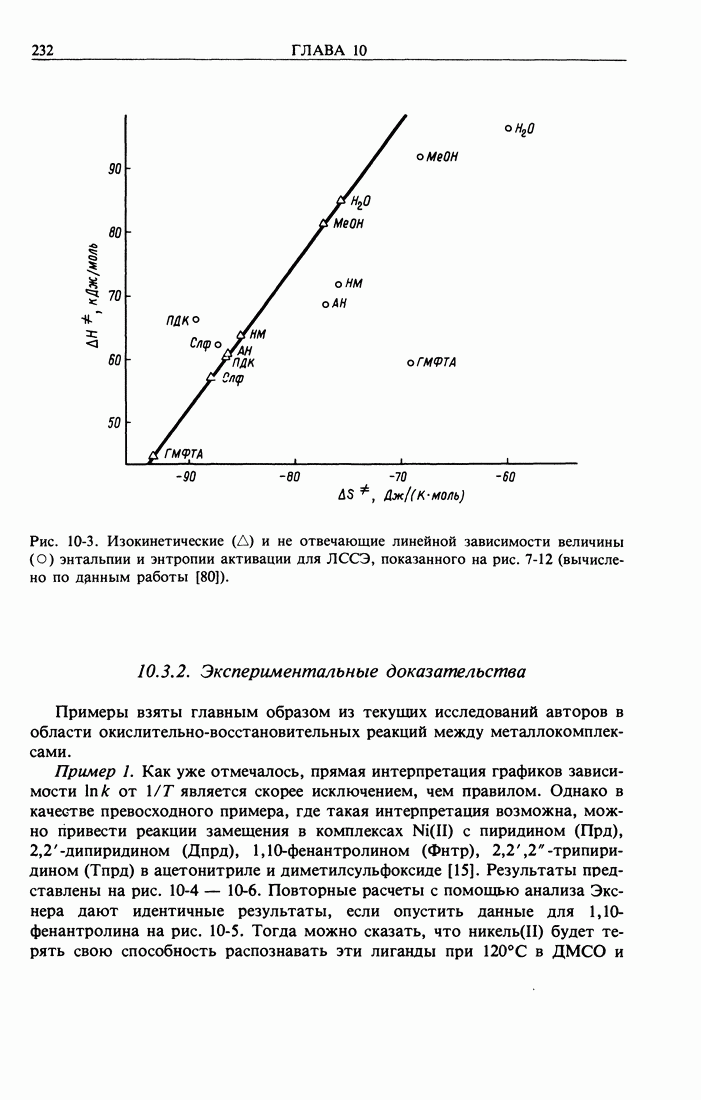
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений