| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
7.5. Современная ситуация
Как отмечалось, отклонения от корреляции для некоторых растворителей с низкой диэлектрической проницаемостью нельзя объяснить с точки зрения электростатической сольватации. Причина этих отклонений другая. Наиболее разумное объяснение состоит в том, что в растворителях с очень слабыми кислыми или основными свойствами эталонные соединения, используемые для построения шкалы, будут преимущественно подвергаться самоассоциации и тем самым имитировать сольватацию. Эти эффекты, по мнению авторов, обусловливают вторую концептуальную трудность в применении эмпирических параметров растворителя. Точно так же в растворителях с низкой координирующей способностью исходные соединения для реакции, кинетику которой изучают, могут оставаться ассоциированными, что приводит к усложнению механизма реакции. Необходимо еще раз подчеркнуть, что для получения физически осмысленных корреляционных диаграмм следует использовать константы скорости, относящиеся к определенной стадии реакции.
Имеется множество отклонений, причины которых неясны, что еще раз свидетельствует об очень сложной природе взаимодействий растворенных веществ с растворителем и о том, что в любой ситуации такое взаимодействие может оказаться особым случаем. Поэтому использование эмпирических параметров часто может оказаться напрасным трудом. Так что попытки найти общий подход к эффектам растворителя с помощью лишь двух параметров должны свидетельствовать о недопонимании проблемы. Как будет вкратце обсуждаться в следующей главе, влияние заместителей можно рассматривать как модель влияния растворителей. Среди эффектов заместителей также имеются особо сложные случаи, которые трудно поддаются исследованию. Прежде всего речь идет о сложностях, связанных с заместителями в орто-положении, так называемом орто-эффекте, включающем несколько различных эффектов (см. разд. 8.3). Однако это ничто по сравнению со сложностями, встречающимися при рассмотрении эффектов растворителя. Одним из важных факторов являются стерические явления; долгое время считалось, что они играют главную роль в особенностях влияния орто-заместителей. Точно так же существуют различные стерические требования и в отношении донорно-акцепторных взаимодействий, например, для больших молекул ГМФТА. Многие ионы металлов, такие, как  являющиеся, как известно, шестикоординационными в большинстве растворителей, образуют в ГМФТА четырехкоординационные сольваты [39]. Иногда более низкие координационные числа в ГМФТА считают причиной отклонения в направлении более высоких значений ДЧ на графиках зависимости
являющиеся, как известно, шестикоординационными в большинстве растворителей, образуют в ГМФТА четырехкоординационные сольваты [39]. Иногда более низкие координационные числа в ГМФТА считают причиной отклонения в направлении более высоких значений ДЧ на графиках зависимости  от ДЧ (рис. 7-4).
от ДЧ (рис. 7-4).
Линейные зависимости в шкале ДЧ и/или АЧ наблюдаются в тех случаях, когда нуклеофильная и/или электрофильная сольватация настолько
сильна (и, кроме того, не затруднена стерически), что становится преобладающим механизмом взаимодействия. В остальных случаях могут превалировать другие, более тонкие механизмы сольватации, которые в настоящее время не поддаются объяснению. Например, среди растворителей, влияющих чаще всего непредсказуемо, особенно зарекомендовал себя диоксан, так что Тафт и сотр. [146] в своем обширном исследовании зависимости эффектов заместителей от растворителя пришли к тому, что разделили все растворители на обычные, слабопротонные, диоксан и трифторуксусную кислоту (очень сильный акцептор). Цитируя работу Тафта, следует отметить, что зависимость эффектов заместителей от растворителя указывает на существование вторичных (т.е. неизвестных) механизмов сольватации. Этот вывод подтверждается и тем, что корреляции с величинами ДЧ и/или АЧ являются скорее исключениями, чем правилами (ср. с интерпретацией отклонений от линейных графиков Гаммета в разд. 8.4).
Таким образом, в настоящее время, пользуясь донорными и акцепторными числами (или эквивалентными им величинами) и иногда принимая во внимание диэлектрические проницаемости, можно часто получить довольно хорошее представление об изменении реакционной способности при переходе от одного растворителя к другому. С точки зрения механизма реакции изучение влияния растворителя на скорость означает, как правило, поиск ответа на вопрос, какие донорно-акцепторные взаимодействия происходят при образовании активированного комплекса или интермедйата. Зная это, можно судить о распределении заряда, а следовательно, и о его характере: повышение скорости с увеличением донорной (акцепторной) силы растворителя означает образование или локализацию положительного (отрицательного) заряда. И наоборот, уменьшение скорости с ростом донорной (акцепторной) силы растворителя означает, что положительный (отрицательный) заряд исчезает или дел окал изуется.
В следующем разделе будут приведены некоторые поучительные примеры, показывающие практическую пригодность шкалы ДЧ и АЧ. Но сначала довольно полная компиляция этих параметров представлена в табл. 7-2 для наиболее распространенных чистых растворителей. Чтобы расширить шкалу, мы дополнили таблицу данными  и АЧ. Первые основаны на уравнении
и АЧ. Первые основаны на уравнении

и получены с помощью анализа линейной регрессии для 13 растворителей, отмеченных темными кружками на рис. 7-3. Аналогичным образом величины  получены по данным для 21 растворителя (отмечены темными кружками на рис. 7-6), и соответствующее уравнение имеет вид
получены по данным для 21 растворителя (отмечены темными кружками на рис. 7-6), и соответствующее уравнение имеет вид

(см. скан)
(см. скан)
(см. скан)
Кроме возможности дополнительно включать другие растворители, практическую важность представляет отличие соответствующих шкал. Наиболее приемлемыми будут те значения, для которых наблюдается хорошее согласование величин АЧ (ДЧ) с величинами  Если же имеются большие расхождения в этих величинах, то предпочтительнее будет та шкала, которая дает лучшую корреляцию между реакционной способностью и характеристикой растворителя. В общем можно получить вполне удовлетворительную картину, поддающуюся интерпретации. Что касается шкалы акцепторных чисел растворителя, то, как уже упоминалось, корреляции с величинами
Если же имеются большие расхождения в этих величинах, то предпочтительнее будет та шкала, которая дает лучшую корреляцию между реакционной способностью и характеристикой растворителя. В общем можно получить вполне удовлетворительную картину, поддающуюся интерпретации. Что касается шкалы акцепторных чисел растворителя, то, как уже упоминалось, корреляции с величинами  часто дают лучшее согласование, чем с исходными величинами АЧ (ср., например,
часто дают лучшее согласование, чем с исходными величинами АЧ (ср., например,  -дихлорэтан и бензол на рис. 7-14).
-дихлорэтан и бензол на рис. 7-14).
Все приведенные выше рассуждения были ограничены случаями чистых растворителей. Остановимся кратко на смесях растворителей. По линейным функциям чистых растворителей невозможно предсказать значения ДЧ и АЧ в их смесях. По существу, взаимодействие растворитель — растворитель делает каждую смесь новым растворителем, имеющим свойства каждого из компонентов. Но, даже если удается найти донорные и акцепторные числа для смешанных растворителей [42, 88], применимость их довольно ограниченна. По-видимому, эффективные донорные и акцепторные числа смесей растворителей не являются постоянными, а представляют собой функции дополняющих друг друга свойств растворенного вещества благодаря явлению, называемому «предпочтительной» или «селективной» сольватацией (см. обзоры [41, 42, 129]).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
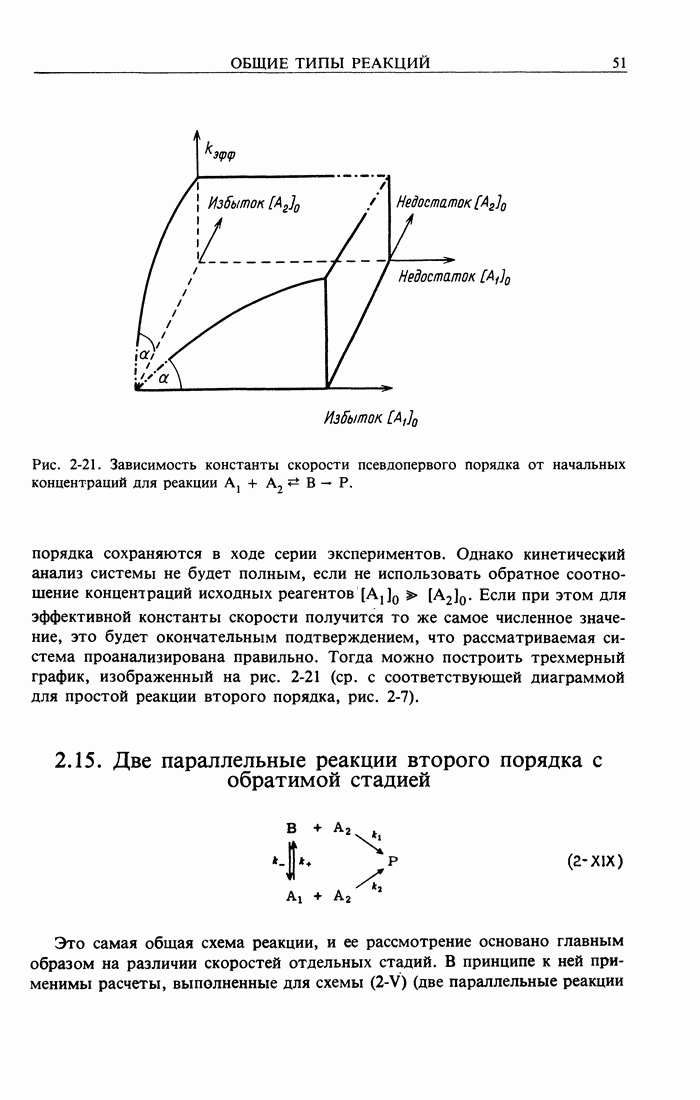
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
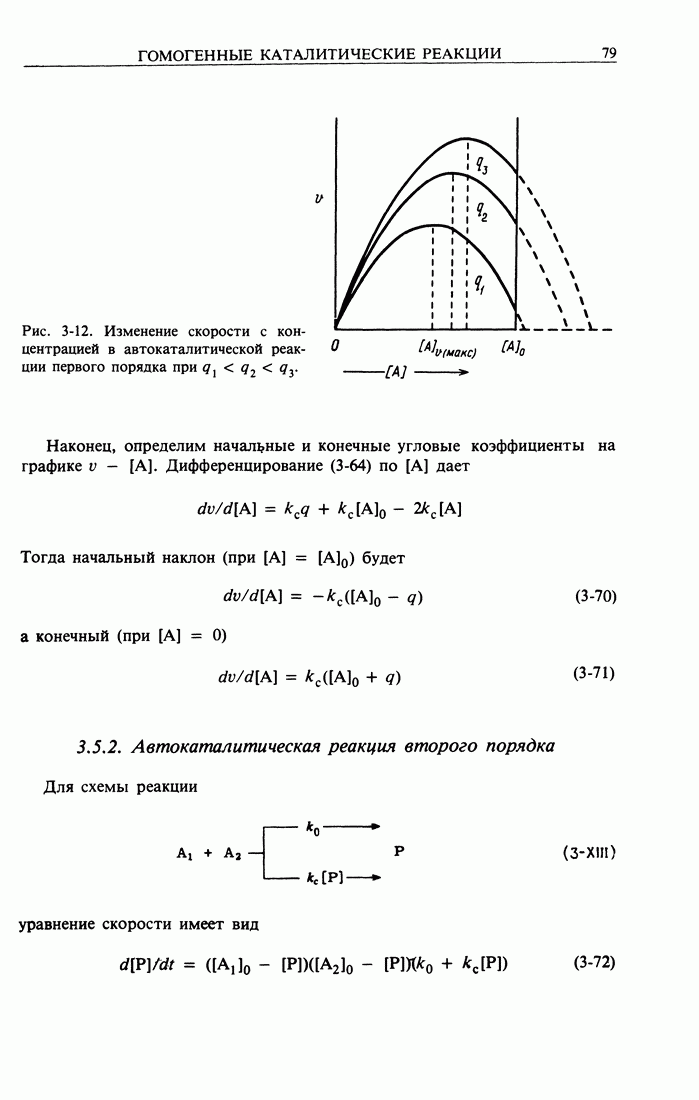
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
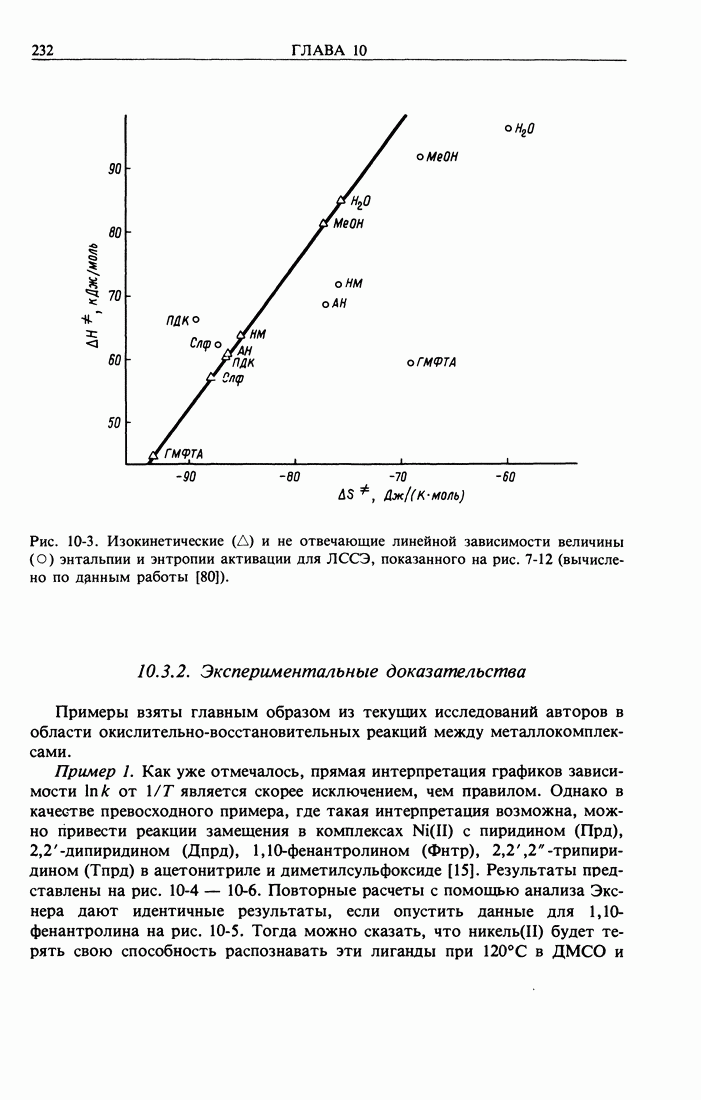
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений