| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
10.1. Основные положения
Любую эмпирическую корреляцию, учитывающую влияние заместителя, растворителя и т.п. на химическую реакцию, можно представить в таком виде, какой был показан в предыдущих разделах: левая часть уравнения содержит логарифм относительной константы скорости, т.е. отношения констант скоростей изучаемой и стандартной реакций. Известны также аналогичные корреляции, основанные на константах равновесия («корреляции по равновесию» в отличие от «корреляций по скорости»). Логарифм константы скорости пропорционален свободной энергии активации, а логарифм константы равновесия — свободной энергии реакции:

поэтому левые части обоих уравнений связаны со свободными энергиями. Правая часть эмпирических корреляционных уравнений содержит один член или алгебраическую сумму членов, каждый из которых в свою очередь является произведением эмпирического параметра, зависящего от заместителя или растворителя, и коэффициента чувствительности или константы реакции, зависящих от типа реакции и температуры.
Важной категорией эмпирических параметров являются величины свободной энергии, например константа Гаммета или свободная энергия переноса Паркера. Учитывая уравнение (10-1), корреляции реакционной способности с использованием этих параметров уместно определить как принцип линейности свободных энергий (принцип ЛСЭ). К другой категории параметров относятся величины, зависящие только от энтальпии, такие, как донорные числа. Корреляция реакционной способности с этими параметрами
возможна при условии, что энтропия остается постоянной в серии реакций или линейно связана с изменением энтальпии. Оба этих условия найдены экспериментально, хотя последнее встречается гораздо чаще. Более того, считается, что линейное соотношение между энтальпией и энтропией, которое называют также «изокинетическим соотношением» (ИКС), является необходимым условием справедливости простых линейных соотношений свободных энергий, т.е. условием выполнения принципа ЛСЭ [29, 127].
Все остальные используемые для корреляций параметры более или менее явно связаны либо со свободными энергиями, либо с энтальпиями. Поэтому вопрос можно поставить так: корреляция влияния растворителя и заместителя на скорость химической реакции с помощью эмпирических параметров невозможна без наличия двух физических фактов, выражаемых принципом ЛСЭ и ИКС. Прошло то время, когда линейные соотношения между энтальпией и энтропией считались математическим артефактом. По этому вопросу уже опубликованы обзоры, среди них особого внимания заслуживают работы Экснера [29, 30]. Возникает ощущение, что настает время, когда следует выяснить природу или физическое обоснование эмпирических корреляций, и понимание этих явлений уже не за горами. В следующих разделах рассматриваются по отдельности принцип ЛСЭ и ИКС.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
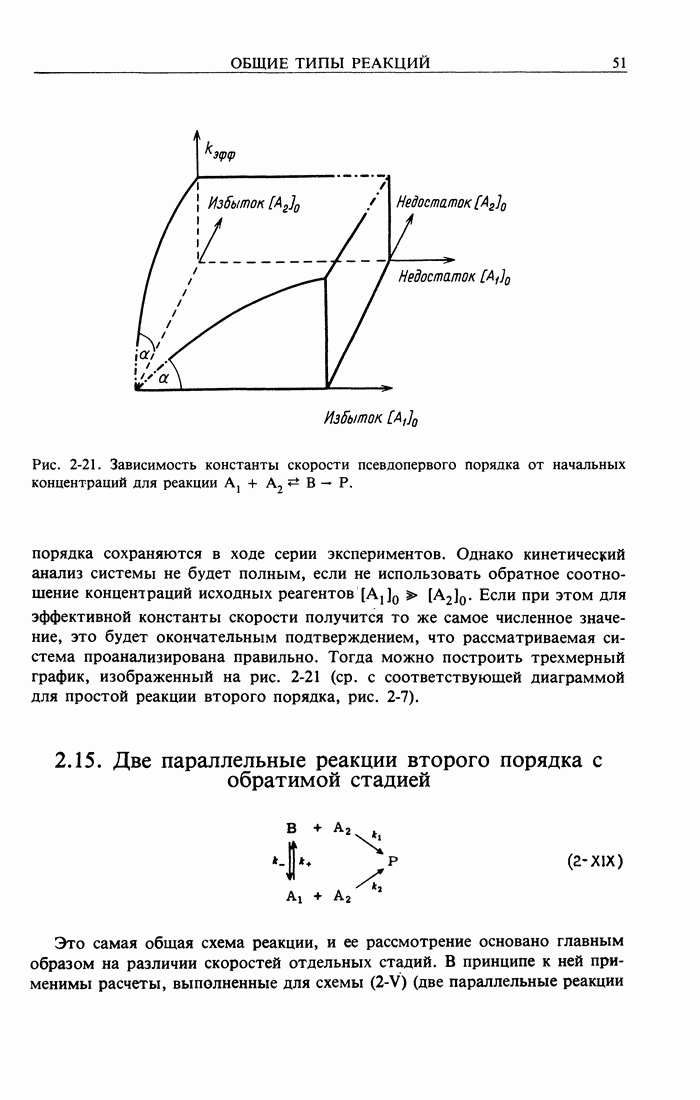
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
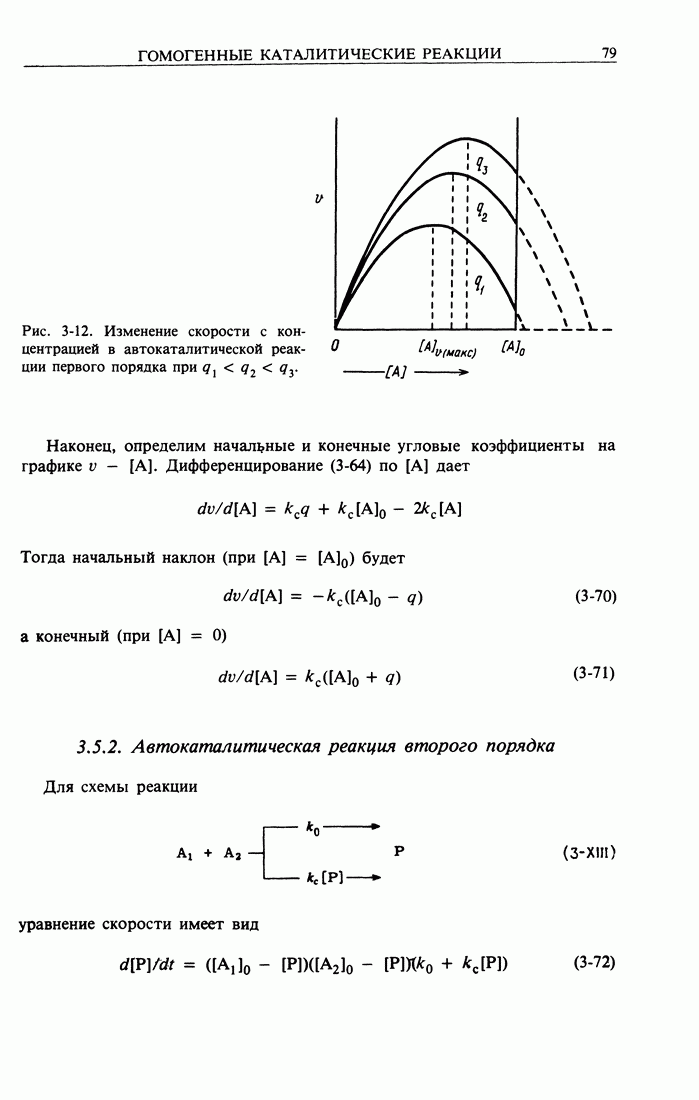
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
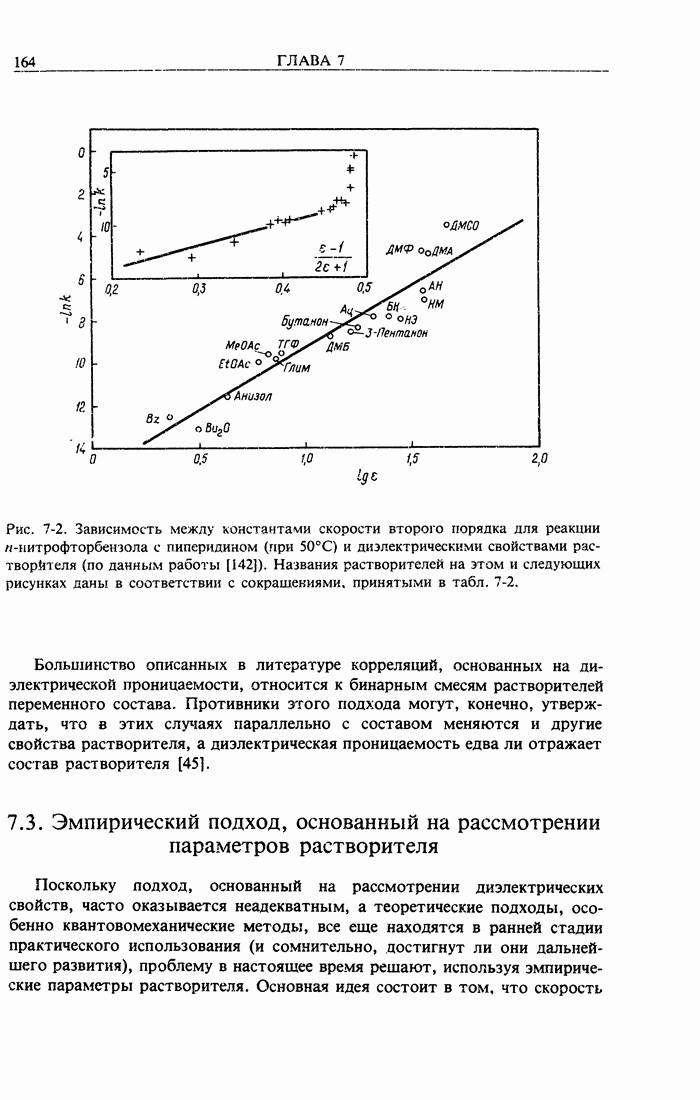
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
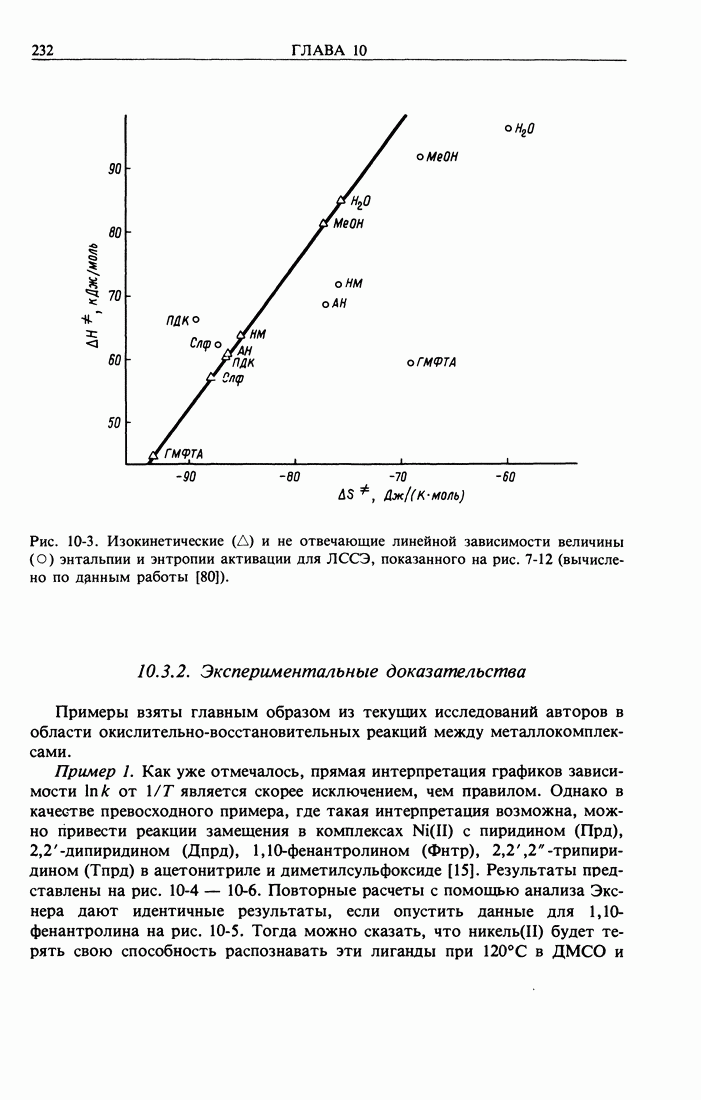
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений