| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
7.3.4. Выводы
Прежде всего наличие взаимных корреляций между эмпирическими шкалами растворителей, основанными на различных процессах, чувствительных к изменению растворителя, указывают на сходные механизмы сольватации. К таким процессам относятся образование водородных связей и кислотно-основных аддуктов, ион-дипольное взаимодействие, ковалентное связывание и т.д. Фактически донорно-акцепторная концепция сводит различавшиеся до сих пор понятия к общей формуле. Однако имеются и ощутимые отклонения от прямолинейных зависимостей, которые можно интерпретировать с точки зрения двух концептуальных трудностей, связанных, во-первых, с высокоструктурированными или ассоциированными растворителями и, во-вторых, с растворителями, имеющими низкую диэлектрическую проницаемость.
1. Высокоструктурированные растворитьли. Практически во всех приведенных выше корреляционных диаграммах точки, соответствующие
структурированным растворителям, таким, как вода, спирты, формамид и т.п., не укладываются в линейную зависимость, а смещены в направлении более высоких значений донорных и акцепторных чисел. Другими словами,  сильнее сольватируются в структурированных растворителях, чем все другие рассмотренные модельные субстраты. Это объясняется следующим образом.
сильнее сольватируются в структурированных растворителях, чем все другие рассмотренные модельные субстраты. Это объясняется следующим образом.
Высокоорганизованные структуры возникают в том случае, когда растворитель обладает выраженными донорными или акцепторными свойствами, т.е. молекулы растворителя вовлекаются в донорно-акцепторное взаимодействие друг с другом. Это особенно характерно для растворителей, молекулы которых содержат кислые атомы водорода. Такие растворители отличаются наличием водородных связей, их называют протонными в противоположность апротонным растворителям. Протонные растворители не могут действовать как доноры или акцепторы, если не разорваны связи между молекулами растворителя, а степень разрыва связей зависит в свою очередь от донорной или акцепторной силы растворенного вещества. Следовательно, химические координирующие свойства протонных растворителей не постоянны, а являются функцией комплементарных свойств растворенного вещества. Отмечая, что  более сильный акцептор, чем
более сильный акцептор, чем  или
или  точно так же, как
точно так же, как  более сильный донор, чем
более сильный донор, чем  и модельные субстраты для шкалы величин
и модельные субстраты для шкалы величин  и
и  можно сделать очевидный вывод, что донорные и акцепторные числа для структурированных растворителей должны быть выше, чем это можно предсказать по другим индексам: частицы с низкой полярностью очень слабо сольватируются в высокоструктурированных растворителях.
можно сделать очевидный вывод, что донорные и акцепторные числа для структурированных растворителей должны быть выше, чем это можно предсказать по другим индексам: частицы с низкой полярностью очень слабо сольватируются в высокоструктурированных растворителях.
В пользу такой интерпретации имеются экспериментальные доказательства. На рис. 7-8 показано соотношение между зависимой от растворителя скоростью сольволиза  -метоксинеофилтозилата, который был использован для определения индексов
-метоксинеофилтозилата, который был использован для определения индексов  [134], и химическим сдвигом сигналов
[134], и химическим сдвигом сигналов  в ЯМР-спектре
в ЯМР-спектре  -нитрозофторбензола [147] в тех же растворителях. Судя по акцепторным числам, на оба процесса преимущественное влияние оказывает акцепторная способность растворителя. Графическая зависимость
-нитрозофторбензола [147] в тех же растворителях. Судя по акцепторным числам, на оба процесса преимущественное влияние оказывает акцепторная способность растворителя. Графическая зависимость  к от АЧ показана позже на рис. 7-11. Найдено, что скорость сольволиза тозилата контролируется сольватацией образующегося тозилат-аниона. Обращает на себя внимание разница между графиками на рис. 7-8 и 7-11, состоящая в том, что отклонения от линейной зависимости для структурированных растворителей находятся по разные стороны от прямой. Можно с уверенностью предположить, что по относительной силе доноры располагаются в ряду
к от АЧ показана позже на рис. 7-11. Найдено, что скорость сольволиза тозилата контролируется сольватацией образующегося тозилат-аниона. Обращает на себя внимание разница между графиками на рис. 7-8 и 7-11, состоящая в том, что отклонения от линейной зависимости для структурированных растворителей находятся по разные стороны от прямой. Можно с уверенностью предположить, что по относительной силе доноры располагаются в ряду

Это объясняет, почему, с одной стороны, скорость сольволиза тозилата в структурированных растворителях больше, чем можно предсказать по

Рис. 7-8. Соотношение между зависимой от растворителя скоростью сольволиза  -метоксинеофилтозилата и химическим сдвигом
-метоксинеофилтозилата и химическим сдвигом  в ЯМР-спектре
в ЯМР-спектре  -нитрозофтор-бензола. Высокоструктурированные растворители отмечены значком
-нитрозофтор-бензола. Высокоструктурированные растворители отмечены значком 
химическому сдвигу  -нитрозофторбензола, но, с другой стороны, она меньше, чем можно предсказать по акцепторным числам. В конечном счете в особых случаях, когда рассматриваемый субстрат проявляет химические координирующие свойства, аналогичные модельному субстрату в используемой шкале растворителей, структурированные растворители могут и не выпадать из линейной зависимости. Например, корреляция между величинами
-нитрозофторбензола, но, с другой стороны, она меньше, чем можно предсказать по акцепторным числам. В конечном счете в особых случаях, когда рассматриваемый субстрат проявляет химические координирующие свойства, аналогичные модельному субстрату в используемой шкале растворителей, структурированные растворители могут и не выпадать из линейной зависимости. Например, корреляция между величинами  включает также и протонные растворители.
включает также и протонные растворители.
В заключение хотелось бы сделать несколько замечаний о термине «структурированный растворитель». Многие химики не хотят дискутировать о степени структурной организации различных жидкостей. Разумно описывать как структурированные не только протонные, но и другие растворители, такие, как ацетонитрил, нитрометан, диметилсульфоксид [103]. Об этом говорит, например, их относительно высокая по сравнению с молекулярной массой температура кипения. В практических целях, однако, можно с помощью акцепторных чисел отнести к высокоструктурированным те растворители, положение которых повторяется на диаграммах, показанных на рис. 7-6 и 7-7. Таким образом, можно считать, что любой
растворитель с АЧ выше, скажем, 25 принадлежит к классу высокоструктурированных растворителей. В то же время эти растворители не имеют характеристической области донорных чисел, хотя каждый такой растворитель должен, естественно, проявлять достаточную основность при образовании ассоциатов. Так, хлороформ и дихлорметан, например, обладают довольно кислыми атомами водорода. Несмотря на это, их нельзя считать высокоструктурированными растворителями из-за недостаточной донорной способности. Обычно значения ДЧ высокоструктурированных растворителей лежат где-то около 20 и таким образом попадают в среднюю область.
2. Растворители с низкой диэлектрической проницаемостью. Помимо сложностей, связанных с высокоструктурированными растворителями, есть и другая причина заметных отклонений от прямолинейной зависимости — низкая диэлектрическая проницаемость растворителей. Для таких растворителей диэлектрическая проницаемость не превышает 10. В последние годы начали дифференцировать электростатическую и координационно-химическую сольватацию. Свободную энергию сольватации рассматривают как сумму двух членов. Один из них соответствует донорно-акцепторным взаимодействиям между растворенным веществом и растворителем, находящимся в непосредственной близости от растворенного вещества («ближнее» взаимодействие или взаимодействие «по типу водородных связей», «специфическая» сольватация). Другой член не учитывает взаимодействия в этой сфере, а связан с диэлектрической поляризацией растворителя («дальнее» взаимодействие, «неспецифическая» сольватация или сольватация «типа Борна»). (См., например, [86].) Предложено также рассматривать пограничный тип сольватации, называемой «полуспецифической» [79] или сольватацией «во внешней сфере» [40, 45]; считают, что при такой сольватации заряды настолько размазаны, что выходят за пределы первой координационной сферы.
Изучая отклонения для растворителей с низкой диэлектрической проницаемостью, Паркер и сотр. [105] высказали мысль, что донорно-акцепторную концепцию нельзя распространять на этот тип растворителей. Эта мысль подтверждается исследованиями Фаулера и сотр. [34], которые сообщили, что можно значительно улучшить корреляцию эффектов растворителя, если величину  (которая, как считают, выражает специфическую сольватацию) скомбинировать с диэлектрической функцией (представляющей неспецифическую сольватацию). С другой стороны, в некоторых случаях наблюдается линейная корреляция между реакционной способностью и АЧ растворителей с низкой диэлектрической проницаемостью; поэтому Майер [86] предположил, что в акцепторные числа, возможно, вносят вклад и «дальние» взаимодействия. Это согласуется с представлениями Коппела и Пальма [69], которые пытались разделить эмпирические параметры растворителя на независимые вклады, связанные с двумя основными типами взаимодействия растворенное вещество — растворитель.
(которая, как считают, выражает специфическую сольватацию) скомбинировать с диэлектрической функцией (представляющей неспецифическую сольватацию). С другой стороны, в некоторых случаях наблюдается линейная корреляция между реакционной способностью и АЧ растворителей с низкой диэлектрической проницаемостью; поэтому Майер [86] предположил, что в акцепторные числа, возможно, вносят вклад и «дальние» взаимодействия. Это согласуется с представлениями Коппела и Пальма [69], которые пытались разделить эмпирические параметры растворителя на независимые вклады, связанные с двумя основными типами взаимодействия растворенное вещество — растворитель.
Важный вывод следует из соотношения между шкалой ДЧ и шкалой В (рис. 7-3), поскольку первую получают для разбавленных растворов дихлорэтана (т.е. при постоянном электростатическом вкладе), тогда как вторая основана на измерениях, выполненных в  растворах
растворах  в чистых растворителях. Для интерпретации этого наблюдения остаются две возможности: либо специфическое и неспецифическое взаимодействия меняются параллельно друг другу, либо традиционная электростатическая сольватация — как дополнение к специфической сольватации — не существует вообще или очень незначительна. В последующем обсуждении будет показано, что в действительности дифференциация между специфической и неспецифической сольватацией — явный артефакт, не имеющий физического смысла. Это следует из сопоставления диэлектрических проницаемостей с донорными и акцепторными числами растворителей, перечисленных в табл. 7-2. Чтобы включить в эту таблицу дополнительные растворители, мы составили также шкалы
в чистых растворителях. Для интерпретации этого наблюдения остаются две возможности: либо специфическое и неспецифическое взаимодействия меняются параллельно друг другу, либо традиционная электростатическая сольватация — как дополнение к специфической сольватации — не существует вообще или очень незначительна. В последующем обсуждении будет показано, что в действительности дифференциация между специфической и неспецифической сольватацией — явный артефакт, не имеющий физического смысла. Это следует из сопоставления диэлектрических проницаемостей с донорными и акцепторными числами растворителей, перечисленных в табл. 7-2. Чтобы включить в эту таблицу дополнительные растворители, мы составили также шкалы  и АЧ, вычисленные по линейным соотношениям между ДЧ и В и между АЧ и
и АЧ, вычисленные по линейным соотношениям между ДЧ и В и между АЧ и  соответственно (подробнее об этом см. в следующем разделе). Это сделано для того, чтобы убедиться в надежности отдельных значений.
соответственно (подробнее об этом см. в следующем разделе). Это сделано для того, чтобы убедиться в надежности отдельных значений.
Просматривая таблицу, можно заметить, что растворители с очень низкой диэлектрической проницаемостью делятся на три класса: а) растворители с незначительными по величине и донорными, и акцепторными числами (насыщенные углеводороды); б) растворители с низкими АЧ и высокими ДЧ (некоторые амины) или средними ДЧ (простые эфиры); в) растворители с низкими ДЧ и умеренными АЧ (хлорированные углеводороды, такие, как метиленхлорид и хлороформ).
Увеличение диэлектрической проницаемости должно привести нас к растворителям, обладающим одним из свойств в заметной степени. На другом конце шкалы мы находим  -метилформамид — растворитель, обладающий выраженными и донорными, и акцепторными свойствами. То же относится и к
-метилформамид — растворитель, обладающий выраженными и донорными, и акцепторными свойствами. То же относится и к  -метилацетамиду — растворителю с самой высокой из известных до сих пор диэлектрической проницаемостью. Общая тенденция в изменении донорно-акцепторных свойств вызывает впечатление, что диэлектрическая проницаемость является мерой амфотерного характера растворителя. Эта мысль имеет свои подтверждения.
-метилацетамиду — растворителю с самой высокой из известных до сих пор диэлектрической проницаемостью. Общая тенденция в изменении донорно-акцепторных свойств вызывает впечатление, что диэлектрическая проницаемость является мерой амфотерного характера растворителя. Эта мысль имеет свои подтверждения.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
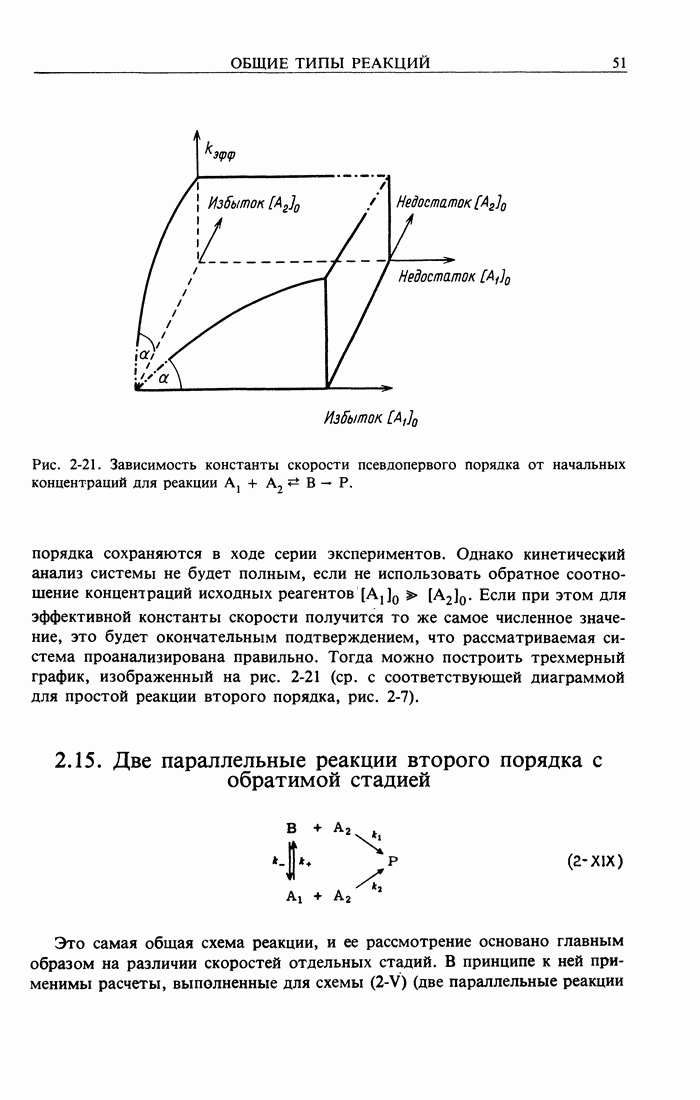
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
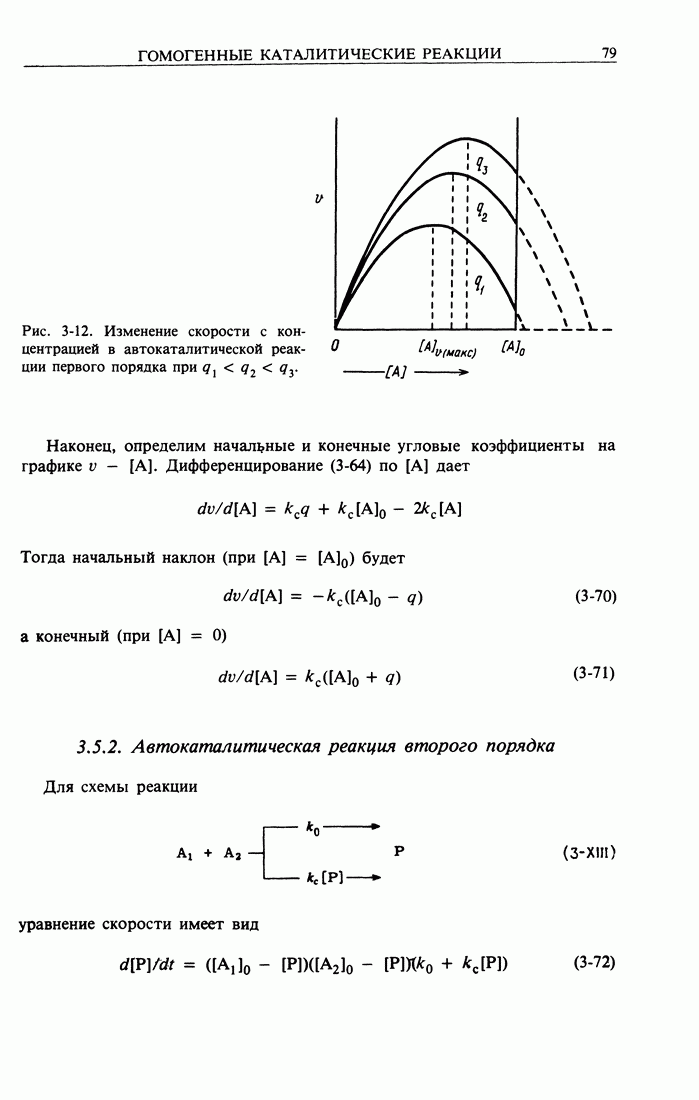
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений