| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
5.6. Физический смысл энергии активации
По сравнению с энтропией активации численное значение  не столь информативно, по крайней мере в настоящее время. Это объясняется тем, что по существу еще неизвестно, от чего в действительности зависит
не столь информативно, по крайней мере в настоящее время. Это объясняется тем, что по существу еще неизвестно, от чего в действительности зависит
энергия активации. Прежде всего предполагают ее корреляцию с данными об энергии связи: чем сильнее связь или связи, подлежащие разрыву, тем выше Ел. Такая зависимость действительно была найдена для некоторых экзотермических газофазных реакций и привела к правилам Хиршфельдера, сформулированным в 1941 г. [53] (см. также [36]). Например, величина Ел для простых реакций замещения второго порядка  составляет 5,5% энергии рвущейся связи. Для реакций другого типа
составляет 5,5% энергии рвущейся связи. Для реакций другого типа  энергия активации составляет около 28% суммарной энергии двух связей, которые должны разорваться в этой реакции. Были также получены некоторые эмпирические корреляции между
энергия активации составляет около 28% суммарной энергии двух связей, которые должны разорваться в этой реакции. Были также получены некоторые эмпирические корреляции между  и энтальпией реакции для экзотермических реакций в гомологических рядах:
и энтальпией реакции для экзотермических реакций в гомологических рядах:

где а и с — эмпирические константы (Семенов, 1958 г. [131], см. также [36, 92]). Это уравнение может быть справедливо для реакций, экзотермичность которых линейно связана с энергией рвущихся связей. Это означает, что образующиеся связи лишь незначительно различаются по энергии. Остается еще очевидный вопрос о физическом смысле величины а в уравнении (5-29), или, иначе говоря, почему именно тот или иной процент энергии рвущихся связей необходим для активации.
Исходя из правила Вант-Гоффа, согласно которому скорость реакции удваивается или утраивается при повышении температуры на 10° С, можно утверждать, что для энергий активации типичны величины от 50 до  Однако это правило слишком эмпирическое и потому имеет большие ограничения; действительно, названный интервал энергий активации типичен для реакций с периодом полупревращения от нескольких минут до нескольких часов при комнатной температуре. Только такие реакции и могли быть исследованы во времена Вант-Гоффа. Реакции же, которые завершаются за несколько секунд или даже за меньшее время, характеризуются энергиями активации в пределах
Однако это правило слишком эмпирическое и потому имеет большие ограничения; действительно, названный интервал энергий активации типичен для реакций с периодом полупревращения от нескольких минут до нескольких часов при комнатной температуре. Только такие реакции и могли быть исследованы во времена Вант-Гоффа. Реакции же, которые завершаются за несколько секунд или даже за меньшее время, характеризуются энергиями активации в пределах  при этом скорость не успевает даже удвоиться за
при этом скорость не успевает даже удвоиться за  -ный скачок температуры
-ный скачок температуры 
Необходимо также учитывать, что в тех случаях, когда реакция включает быстрое экзотермическое предравновесие, энергия активации может быть очень низкой или даже отрицательной величиной. Тогда измеряемая величина  представляет собой разность
представляет собой разность  (см. ниже). Процессы,
(см. ниже). Процессы,
контролируемые диффузией, также характеризуются низкой энергией активации. В отличие от этого очень высокие значения должны появляться в тех случаях, когда в лимитирующей стадии реакции образуются высокореакционноспособные интермедиаты, такие, как радикалы.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
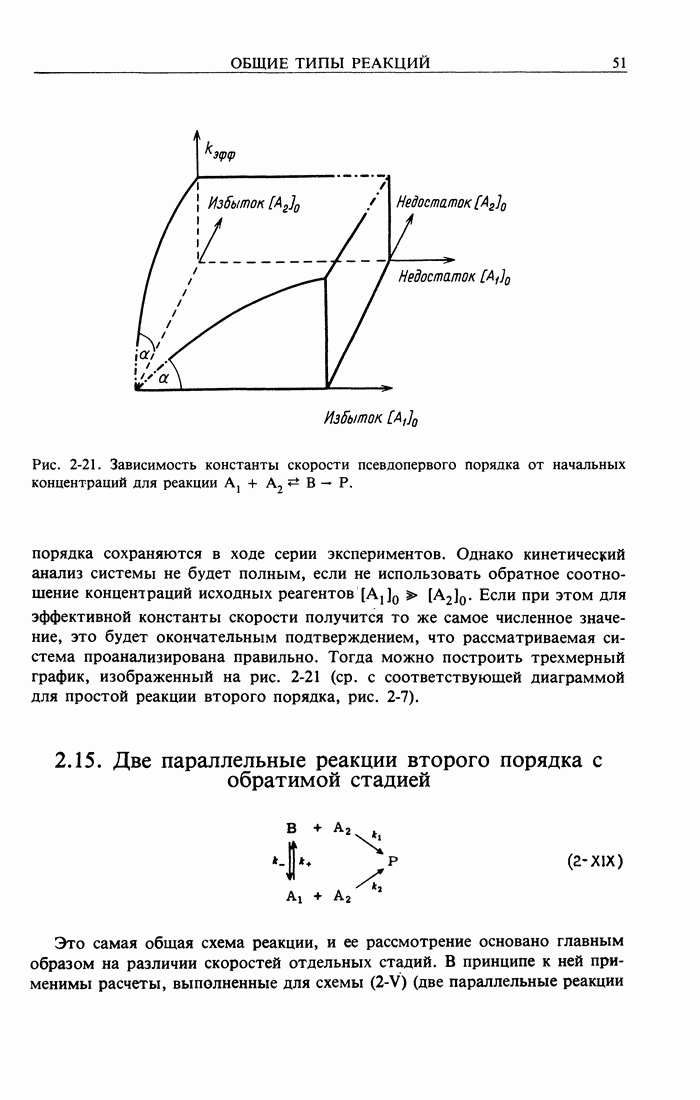
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
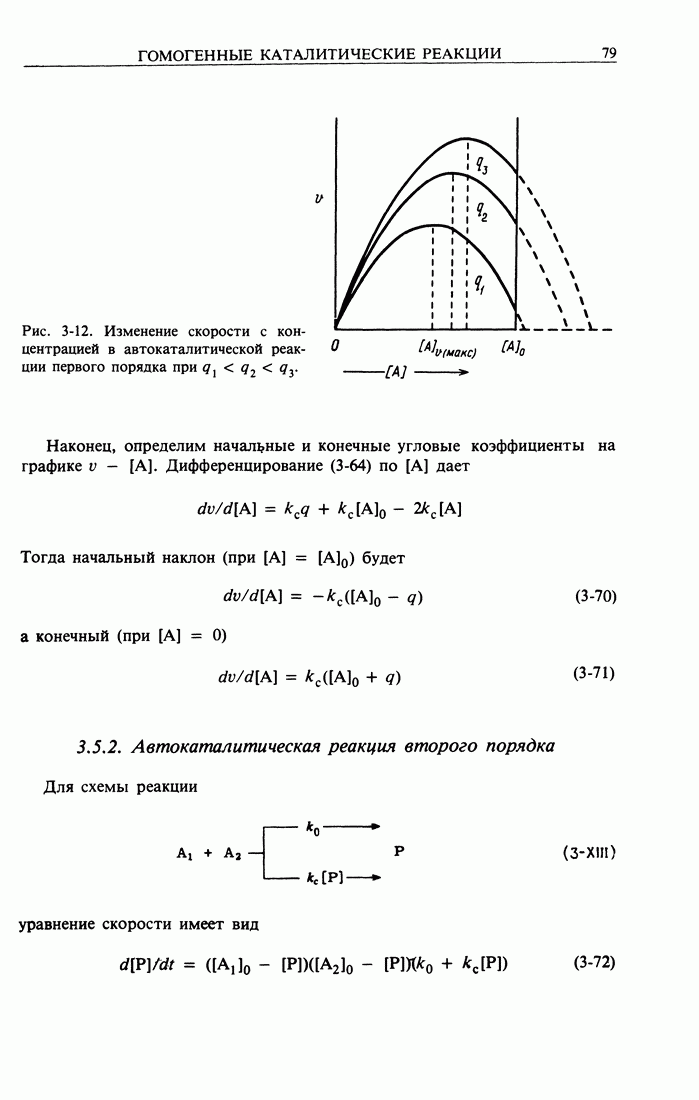
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
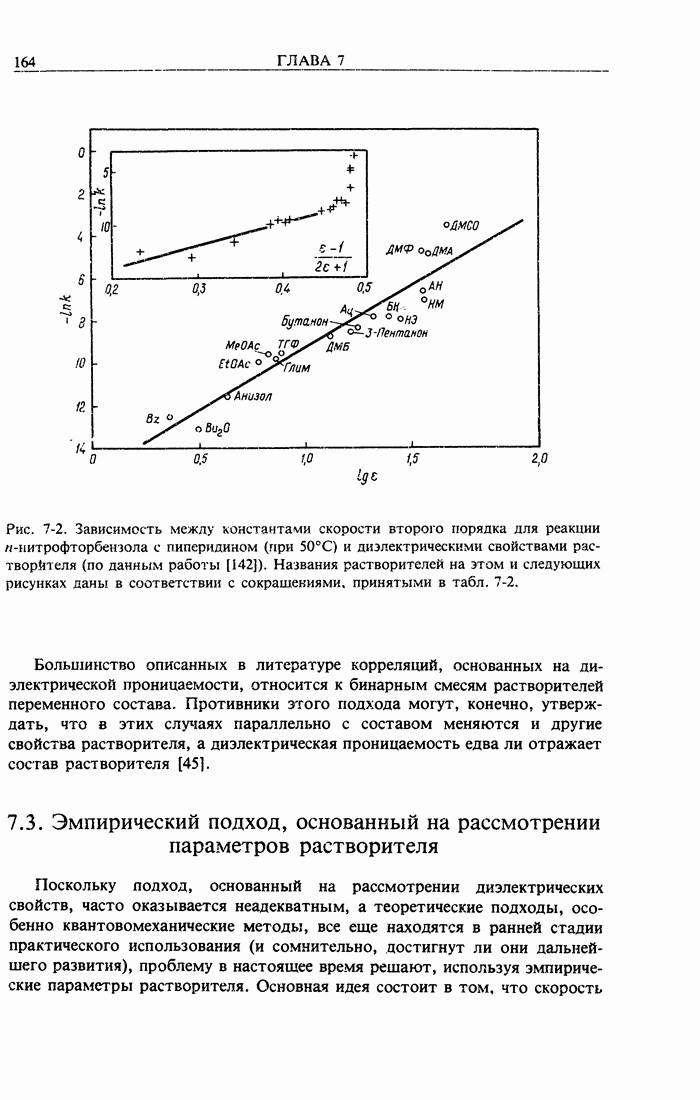
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
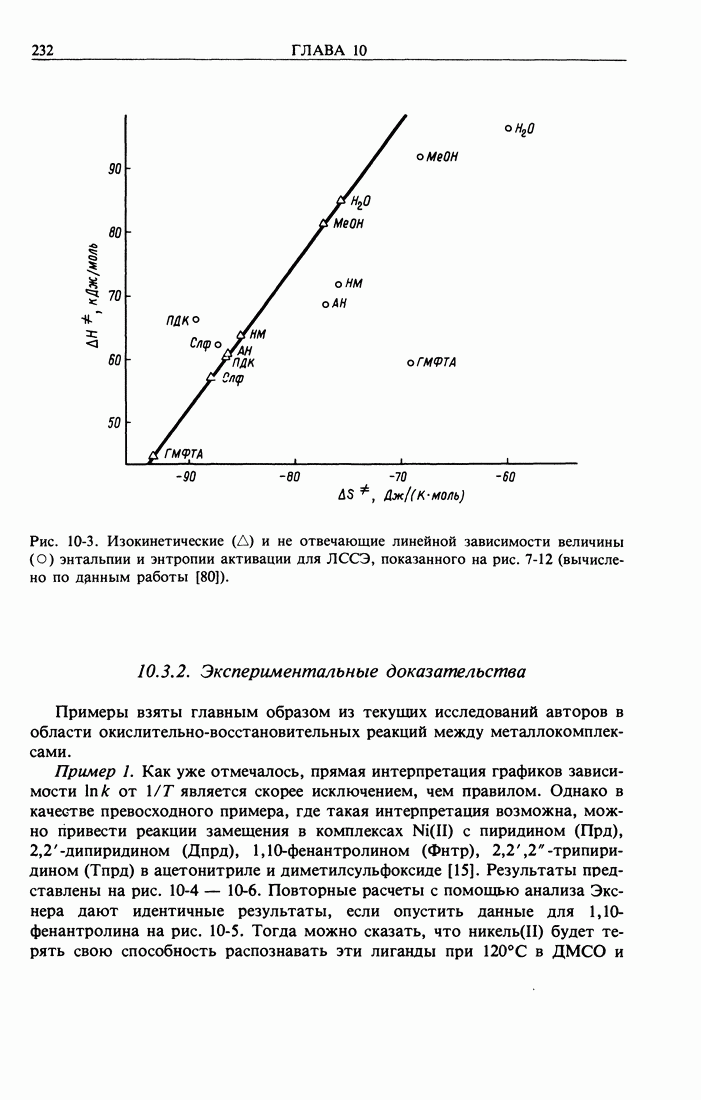
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений