| << Предыдущий параграф |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
10.3.3. Практические следствия из изокинетических соотношений
Наиболее интересное следствие из соотношения между энтальпией и энтропией — обращение последовательности реакционной способности в серии реакций при прохождении температуры через  На первый взгляд трудно поверить, что эффекты заместителя или растворителя могут менять знак просто при изменении температуры. Это хотя и кажется странным, но является логическим следствием того, что свободные энергии — величины аддитивные, состоящие из энтальпии и энтропии, на которые изменение параметров влияет в одном направлении. Другими словами, в природе конкурируют тенденции к минимальной энергии и минимальному стерическому напряжению молекулы. Чем сильнее взаимодействия в активированном комплексе, тем значительнее будет уменьшение
На первый взгляд трудно поверить, что эффекты заместителя или растворителя могут менять знак просто при изменении температуры. Это хотя и кажется странным, но является логическим следствием того, что свободные энергии — величины аддитивные, состоящие из энтальпии и энтропии, на которые изменение параметров влияет в одном направлении. Другими словами, в природе конкурируют тенденции к минимальной энергии и минимальному стерическому напряжению молекулы. Чем сильнее взаимодействия в активированном комплексе, тем значительнее будет уменьшение  но одновременно тем меньше будет степеней свободы внутреннего движения, а следовательно, тем больше уменьшение
но одновременно тем меньше будет степеней свободы внутреннего движения, а следовательно, тем больше уменьшение  Это означает, например, что эффект растворителя, «помогающий» энтальпии реакции благодаря сольватации (энтальпия сольватации), будет делать это за счет энтропийного члена, так как в сольватной оболочке плотность выше. Поэтому изменения
Это означает, например, что эффект растворителя, «помогающий» энтальпии реакции благодаря сольватации (энтальпия сольватации), будет делать это за счет энтропийного члена, так как в сольватной оболочке плотность выше. Поэтому изменения
параметров оказывают меньшее влияние на  т.е. на скорость, чем можно было бы предсказать по изменениям в энтальпии активации (это, как уже говорилось, эффект компенсации). Относительные вклады членов, соответствующих энтальпии и энтропии, зависят от температуры. Повышение температуры от значений ниже Гизо свидетельствует о том, что скорости отдельных реакций данной серии приближаются друг к другу, т.е. наклон ЛССЭ уменьшается. Иными словами, селективность реагента становится меньше. При изокинетической температуре вклады энтальпии и энтропии взаимно уравновешиваются, так что разницы в реакционной способности совсем не наблюдается. При температуре выше Гизо изменение
т.е. на скорость, чем можно было бы предсказать по изменениям в энтальпии активации (это, как уже говорилось, эффект компенсации). Относительные вклады членов, соответствующих энтальпии и энтропии, зависят от температуры. Повышение температуры от значений ниже Гизо свидетельствует о том, что скорости отдельных реакций данной серии приближаются друг к другу, т.е. наклон ЛССЭ уменьшается. Иными словами, селективность реагента становится меньше. При изокинетической температуре вклады энтальпии и энтропии взаимно уравновешиваются, так что разницы в реакционной способности совсем не наблюдается. При температуре выше Гизо изменение  более чем возмещается еще большим изменением
более чем возмещается еще большим изменением  так что меняется знак изменения
так что меняется знак изменения  Поэтому принято считать, что ЛССЭ контролируется энтальпией при температурах ниже Гизо и энтропией при температурах выше Гизо. Очевидно, интерпретация разницы реакционной способности должна быть различной при температурах выше и ниже Гизо. Этот вопрос побуждает сделать комментарий относительно реакции, представленной на рис. 10-9. Однако на этот раз интересующая нас стадия реакции остается неясной, так как не имеется подробных сведений о составе кинетически наблюдаемого интермедиата и, кроме того, нельзя отличить разложение предшественника, сопровождаемое переносом электрона, от разложения последующего продукта.
Поэтому принято считать, что ЛССЭ контролируется энтальпией при температурах ниже Гизо и энтропией при температурах выше Гизо. Очевидно, интерпретация разницы реакционной способности должна быть различной при температурах выше и ниже Гизо. Этот вопрос побуждает сделать комментарий относительно реакции, представленной на рис. 10-9. Однако на этот раз интересующая нас стадия реакции остается неясной, так как не имеется подробных сведений о составе кинетически наблюдаемого интермедиата и, кроме того, нельзя отличить разложение предшественника, сопровождаемое переносом электрона, от разложения последующего продукта.
Недостаточность доказательств обращения реакционной способности с изменением температуры (см. [93] или рис. 10-11) может быть связана с тем, что экспериментально доступен лишь довольно узкий интервал температур; тогда не должно оставаться сомнений в том, что и знак, и численное значение констант реакции зависят от отношения температуры эксперимента к изокинетической температуре. Поэтому нужно с осторожностью подходить к интерпретации констант реакции как критериев механизма, если они получены при одной температуре. Необходимо, однако, допустить, что в большинстве случаев изокинетическая температура может лежать много выше температурного интервала опыта. Иначе не должно было бы возникнуть представления или даже правила, что увеличение энергии активации вызывает торможение реакции. Следовательно, мы можем вернуться к интерпретациям эффектов растворителя или заместителя, данным в гл. 7 и 8, хотя, строго говоря, эти интерпретации справедливы только при температурах ниже Гизо. Правда, следовало бы ввести в практику исследование любых эффектов как минимум при двух температурах. Тогда можно было бы провести грань между сериями реакций, в которых селективность уменьшается или увеличивается при повышении температуры, а также узнать, Гизо выше или ниже, чем температурный интервал опыта (при соблюдении ИКС). Для начала этого может оказаться достаточно, чтобы правильно интерпретировать ЛССЭ. Полный температурный анализ ЛССЭ дает дополнительную и исключительно ценную информацию,
позволяющую ответить на вопросы, выполняется ли ИКС, однородны ли данные по всей серии реакций или их надо разделить на подгруппы, или исключить некоторые реакции из серии; поэтому всегда рекомендуется провести такой анализ. Кроме того, весьма желательно знать численные значения  для разных серий реакций, так как изокинетическая температура может оказаться характеристической величиной, на основании которой можно создать правильную классификацию серий реакций [8]. К сожалению, большинство имеющихся в литературе значений Гизо ненадежно или даже ошибочно из-за неправильной оценки корреляций. Поэтому описанные случаи следует тщательно пересмотреть со статистической точки зрения.
для разных серий реакций, так как изокинетическая температура может оказаться характеристической величиной, на основании которой можно создать правильную классификацию серий реакций [8]. К сожалению, большинство имеющихся в литературе значений Гизо ненадежно или даже ошибочно из-за неправильной оценки корреляций. Поэтому описанные случаи следует тщательно пересмотреть со статистической точки зрения.
Таким образом, остается вопрос, касающийся не самого по себе физического смысла изокинетической температуры, а ее численного значения. Иными словами, ясно, что при  вклад энтропии компенсирует вклад энтальпии, но почему это происходит только при той или иной температуре. Так, возвращаясь к примеру 1, естественно спросить, почему
вклад энтропии компенсирует вклад энтальпии, но почему это происходит только при той или иной температуре. Так, возвращаясь к примеру 1, естественно спросить, почему  теряет способность различать некоторые лиганды при 120°С в ДМСО, но при 65°С в ацетонитриле. Ответ на подобные вопросы все еще остается задачей будущих теорий. В самом общем виде можно утверждать, что чем выше Гизо, тем в большей степени природа наблюдаемого эффекта связана с электронными явлениями, а чем ниже Гизо, тем больше роль стерических факторов. Недавно было показано [72], что чем выше изокинетическая температура, тем больше средняя высота потенциального барьера реакций данной серии и тем меньше число участвующих в процессе степеней свободы, Это должно означать, что Гизо является мерой средней энергии, сохраняемой каждой степенью свободы при распределении по степеням свободы в активированном состоянии.
теряет способность различать некоторые лиганды при 120°С в ДМСО, но при 65°С в ацетонитриле. Ответ на подобные вопросы все еще остается задачей будущих теорий. В самом общем виде можно утверждать, что чем выше Гизо, тем в большей степени природа наблюдаемого эффекта связана с электронными явлениями, а чем ниже Гизо, тем больше роль стерических факторов. Недавно было показано [72], что чем выше изокинетическая температура, тем больше средняя высота потенциального барьера реакций данной серии и тем меньше число участвующих в процессе степеней свободы, Это должно означать, что Гизо является мерой средней энергии, сохраняемой каждой степенью свободы при распределении по степеням свободы в активированном состоянии.
Прежде чем закончить настоящий раздел, хотелось бы упомянуть особый случай линейного соотношения между энтальпией и энтропией, при котором общая точка пересечения на графике Аррениуса лежит в области отрицательных температур. Это указывает на то, что энтальпия и энтропия изменяются в противоположных направлениях, т.е. имеет место так называемая антикомпенсация в отличие от известного эффекта компенсации. В таком случае должен получиться изокинетический график с отрицательным наклоном. До настоящего времени эффект антикомпенсации оставался мало понятным и неприемлемым с теоретической точки зрения [76]. Действительно, он несовместим с конкурентной природой минимальной энергии и минимального стерического напряжения молекулы. Встречавшиеся иногда случаи отрицательной изокинетической температуры только поддерживали ту точку зрения, что изокинетическая температура сама по себе не имеет достаточного физического смысла.
Недавно появлению антикомпенсации было дано простое объяснение: она может иметь место, если рассматриваемые константы скорости (или равновесия) являются составными и относятся по крайней мере к двум
стадням реакции, на которые изменение параметров влияет в противоположном направлении, и если при этом одна стадия сильно воздействует на общую энергию, а другая — на общую энтропию [122]. Таким образом, можно утверждать, что антикомпенсация не может проявляться в элементарной стадии.
Примером такого способа понимания антикомпенсации должны служить представленные здесь результаты по восстановлению комплексов замещенного железо(III)фенантролина железом(И) [см. схему (8-11)]. График Аррениуса, построенный по методу Экснера, для констант скорости второго порядка этого процесса показан на рис. 10-15 (из него следует, что Гизо  Очевидно, что измеренная константа скорости связана с величиной
Очевидно, что измеренная константа скорости связана с величиной  произведением константы равновесия ковалентной гидратации
произведением константы равновесия ковалентной гидратации  и константы скорости последующего образования мостика, приводящего к комплексу
и константы скорости последующего образования мостика, приводящего к комплексу  Отсюда
Отсюда

Что касается членов, включающих энергию, то, как было показано, в  большой вклад вносит
большой вклад вносит  В отличие от этого для энтропийных членов разумно предположить, что состоит главным образом из
В отличие от этого для энтропийных членов разумно предположить, что состоит главным образом из  что обусловлено захватом больших ионов
что обусловлено захватом больших ионов  приводящим к
приводящим к

Рис. 10-15. Аррениусовский график, показывающий влияние заместителя на константу скорости второго порядка в реакции восстановления  пятизамещенных комплексов
пятизамещенных комплексов  в воде [122].
в воде [122].
значительной потере энтропии. Поэтому, например, при переходе от незамещенных к  -замещенным комплексам
-замещенным комплексам  уменьшается благодаря нуклеофильной атаке молекулой воды, которой способствует энтальпийный член,
уменьшается благодаря нуклеофильной атаке молекулой воды, которой способствует энтальпийный член,  становится менее отрицательной благодаря меньшему стерическому напряжению в предшественнике, так как кислород, поставляемый группой
становится менее отрицательной благодаря меньшему стерическому напряжению в предшественнике, так как кислород, поставляемый группой  менее основный. Это экспериментальная модель фактов, наблюдаемых для параметров активации.
менее основный. Это экспериментальная модель фактов, наблюдаемых для параметров активации.
При обобщении этих особенностей утверждалось, что все отрицательные изокинетические температуры связаны с эффективными константами, подобными рассмотренным выше. Такая точка зрения подтверждается, если принять во внимание, что все известные из литературы примеры антикомпенсации укладываются в эту схему. Например, антикомпенсация, обусловленная влияниемл заместителя на термодинамические функции ионизации .медш-замещецных фенолов [9], легко объясняется, если принять, что энергия реакции главным образом относится к ионизации самой молекулы, тогда как энтропия реакции контролируется сольватацией фенолят-аниона. Известно; что в случае реакций в растворах с участием заряженных частиц эффекты сольватации часто оказывают доминирующее влияние как на энтропию реакции, так и на энтропию активации. Поэтому можно предсказать, что оттягивание электронов от реакционного центра должно приводить к уменьшению  и к менее отрицательной
и к менее отрицательной  Именно это и найдено экспериментально.
Именно это и найдено экспериментально.
Замечание о том, что наличие антикомпенсации может указывать на составной характер рассматриваемой константы скорости, возвращает нас к основной цели кинетического анализа — разделению химической реакции на элементарные стадии. Из материала гл. 5—10 очевидно, что изучение изменения параметров может пролить свет на отдельные стадии реакции, которые не удается определить на основании данных о зависимости концентрации от времени. Чтобы проиллюстрировать эту точку зрения, вернемся к наиболее распространенному типу сложных реакций, неоднократно упоминавшемуся в настоящей книге, а именно к процессу, в котором простой реакции с константой к предшествует равновесие с константой К (ср. с разд. 4.7):

При систематическом анализе такого случая предравновесие остается скрытым, если во всем интервале концентраций произведение  много меньше единицы. Тогда анализ дает простую константу скорости второго порядка, которая на самом деле является произведением
много меньше единицы. Тогда анализ дает простую константу скорости второго порядка, которая на самом деле является произведением  Изменение других, отличных от концентрации параметров должно, по существу, означать изменение численного значения К. При этом может оказаться, что
Изменение других, отличных от концентрации параметров должно, по существу, означать изменение численного значения К. При этом может оказаться, что
член  станет более значительным, что приведет к нелинейному графику, например, в аррениусовских или гамметовских координатах. В таком случае очень желательно повторить кинетический анализ с подходящей корректировкой параметров так, чтобы прийти к полному уравнению скорости (т.е. в рассматриваемом случае наблюдать насыщение
станет более значительным, что приведет к нелинейному графику, например, в аррениусовских или гамметовских координатах. В таком случае очень желательно повторить кинетический анализ с подходящей корректировкой параметров так, чтобы прийти к полному уравнению скорости (т.е. в рассматриваемом случае наблюдать насыщение  при больших значениях
при больших значениях  Однако изменение параметров может оказаться недостаточным, если величина произведения
Однако изменение параметров может оказаться недостаточным, если величина произведения  продолжает оставаться незначительной. Даже тогда для серии реакций может выполняться изокине-тическое соотношение, и предравновесие будет скрытым, если на него не укажет наличие антикомпенсации.
продолжает оставаться незначительной. Даже тогда для серии реакций может выполняться изокине-тическое соотношение, и предравновесие будет скрытым, если на него не укажет наличие антикомпенсации.
Следовательно, варьирование параметров, отличных от концентрации, может помочь выяснению более общих схем реакций.
ЛИТЕРАТУРА
(см. скан)
(см. скан)
| << Предыдущий параграф |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
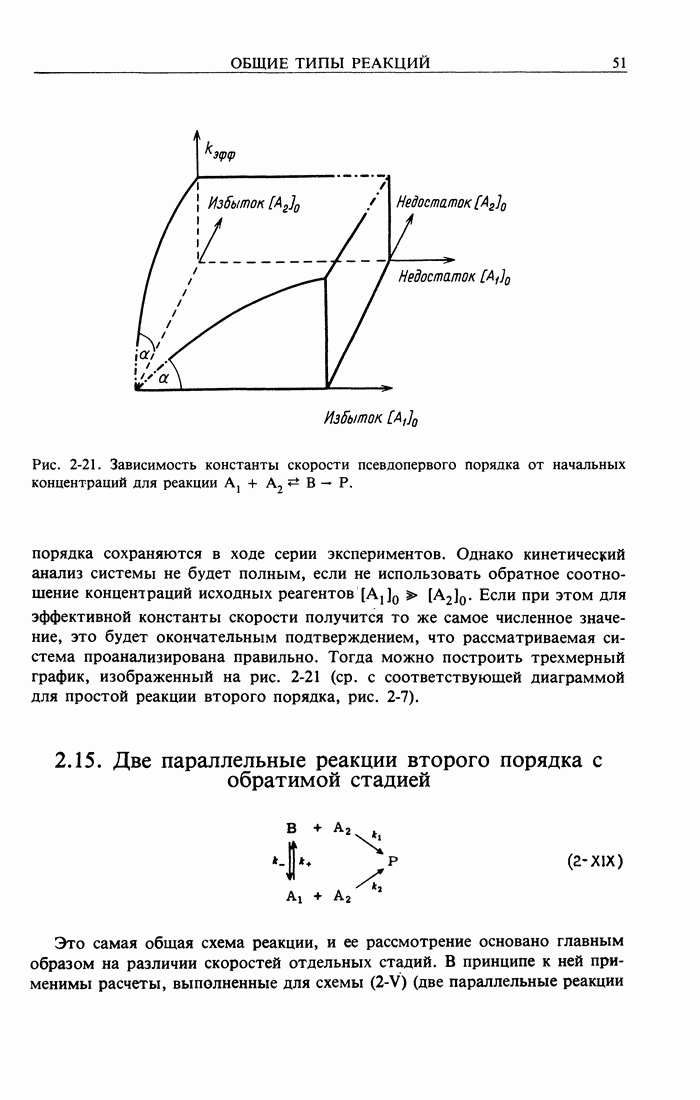
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
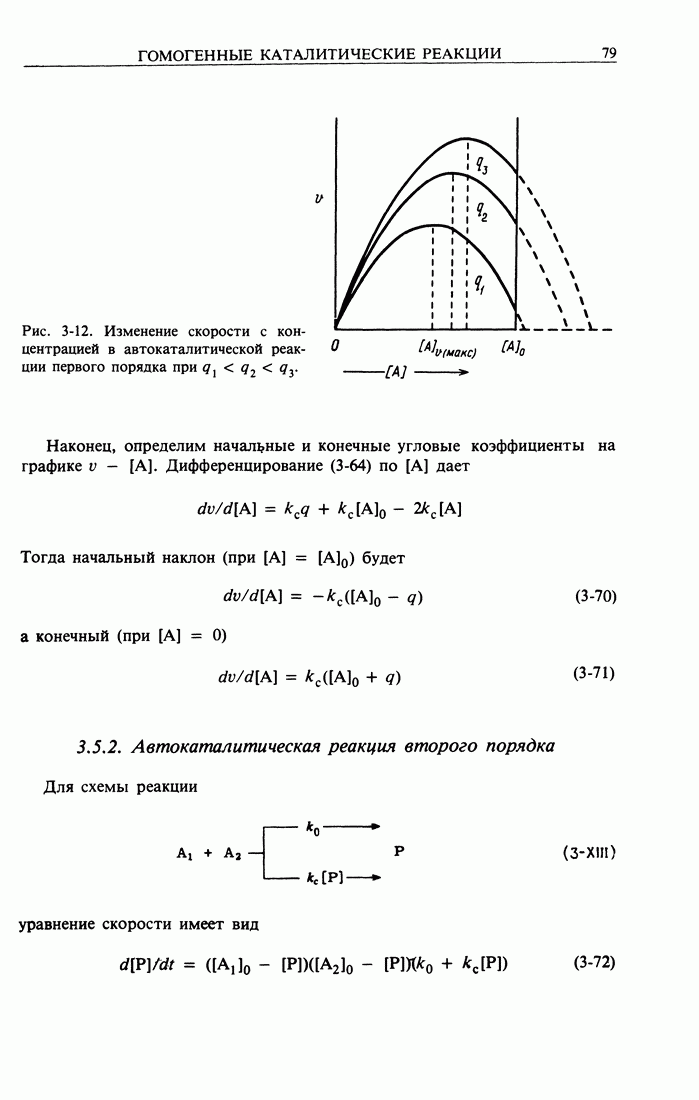
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
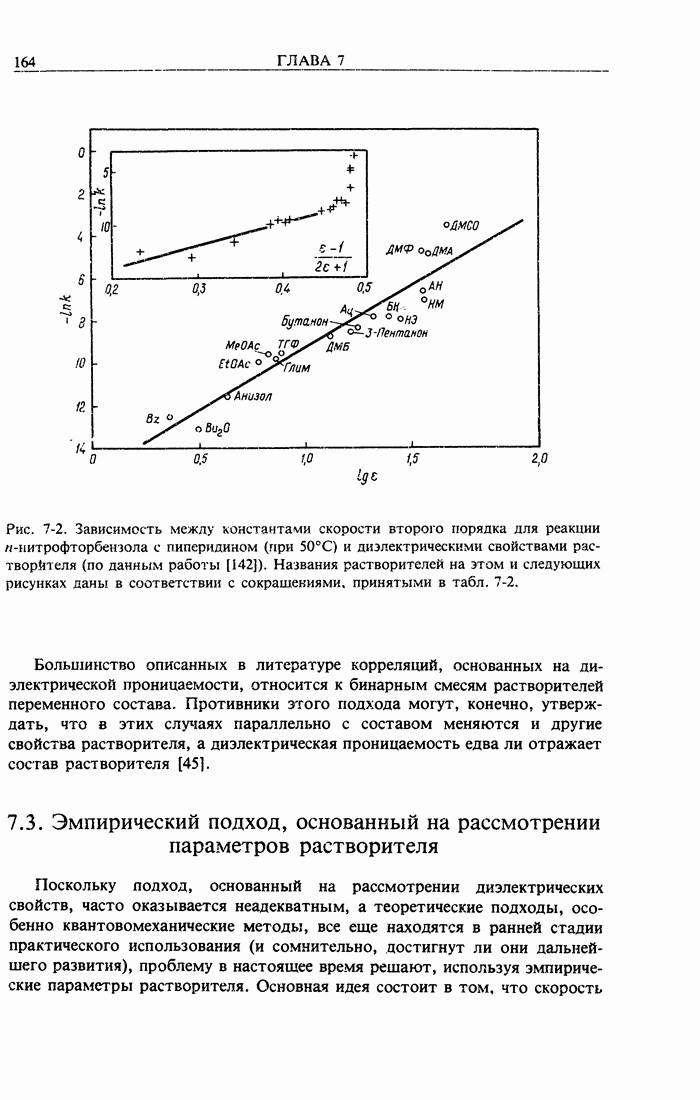
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
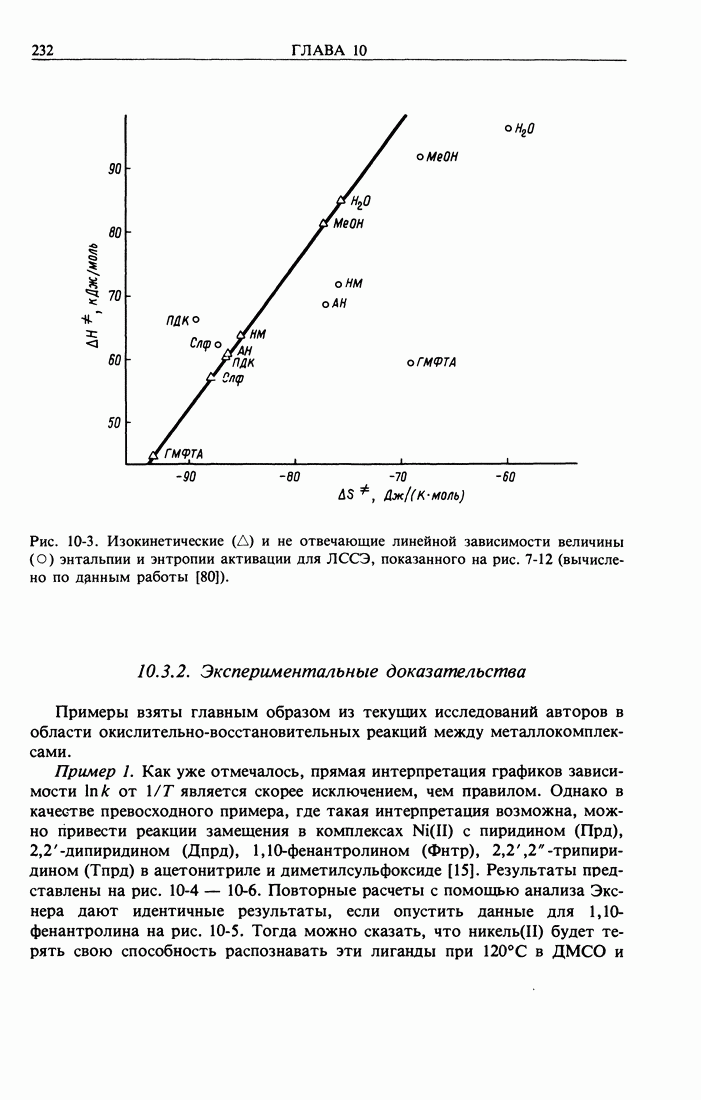
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений