| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
Рассмотрим показанное на рис. 10-1 линейное соотношение свободных энергий (ЛССЭ) между двумя реакциями (А) и (В), в реагентах которых варьируют заместители х, у и z. Представленный здесь график описывается уравнением

Для того чтобы выполнялась эта зависимость, необходимы два допущения.
Первое допущение. Свободные энергии реакций данной серии состоят из двух членов, и только один из них зависит от заместителя. Если изменение свободной энергии реакции (А) х-замещенного реагента принять за стандартное:


Рис. 10-1. Модельное ЛССЭ для двух реакций, в которых варьируют х, у и z.
то для реакции у-замещенного реагента

а для  -замещенного реагента
-замещенного реагента

или в общем виде для заместителя 

Аналогично для реакции 

Второе допущение. Вклады членов, зависимых от заместителя,  меняются линейно:
меняются линейно:

Подстановка (10-9) в (10-7) дает

Заменив второй член правой части на (10-8):

получаем уравнение, аналогичное (10-3):

где член в скобках идентичен  из уравнения (10-3).
из уравнения (10-3).
Теперь рассмотрим разность свободных энергий  для реакций (А) и
для реакций (А) и  и
и  -замещенными реагентами. Вычитание двух уравнений (10-12), где
-замещенными реагентами. Вычитание двух уравнений (10-12), где  является
является  соответственно, дает
соответственно, дает

С помощью (10-1) или (10-2) соотношение констант скорости или констант равновесия можно выразить как

где  константа скорости или равновесия реакции (А) для
константа скорости или равновесия реакции (А) для  -замещенного реагента и т.д. Или в другом виде
-замещенного реагента и т.д. Или в другом виде

Из последних двух уравнений можно вывести любое линейное соотношение свободных энергий. Например, уравнение Бренстеда для катализируемых кислотой реакций следует из уравнения (10-15), если  константа скорости катализируемой кислотой реакции
константа скорости катализируемой кислотой реакции  константа ионизации кислоты
константа ионизации кислоты 

Уравнение Гаммета  следует из уравнения (10-14), если реакция
следует из уравнения (10-14), если реакция  является ионизацией замещенных бензойных кислот и выбрана в качестве стандартной.
является ионизацией замещенных бензойных кислот и выбрана в качестве стандартной.
Уравнение Бренстеда можно интерпретировать в терминах корреляции между двумя реакциями с переносом протона от кислоты  к субстрату
к субстрату  (эффект по
(эффект по  и к воде (эффект по
и к воде (эффект по 

Это означает, что так называемый коэффициент Бренстеда а связан с разницей свободных энергий сольватации катионов  Поскольку свободная энергия гидратации
Поскольку свободная энергия гидратации  достаточно велика, коэффициент а должен быть меньше единицы; экспериментально найдено, что его значение находится в интервале от 0,3 до 0,9.
достаточно велика, коэффициент а должен быть меньше единицы; экспериментально найдено, что его значение находится в интервале от 0,3 до 0,9.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
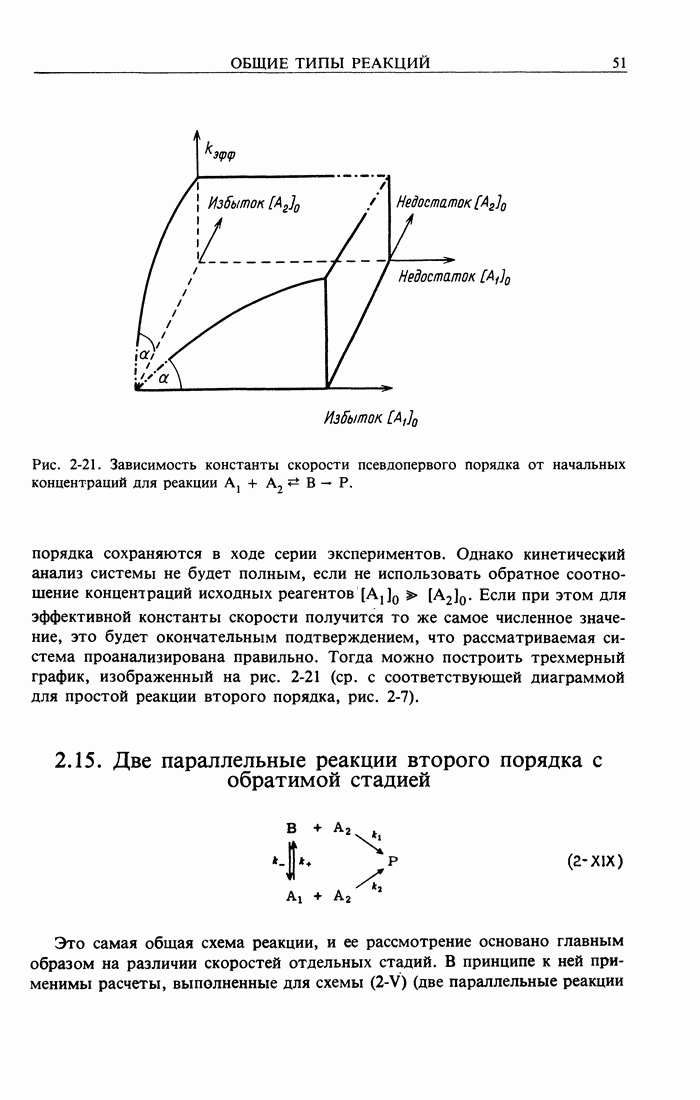
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
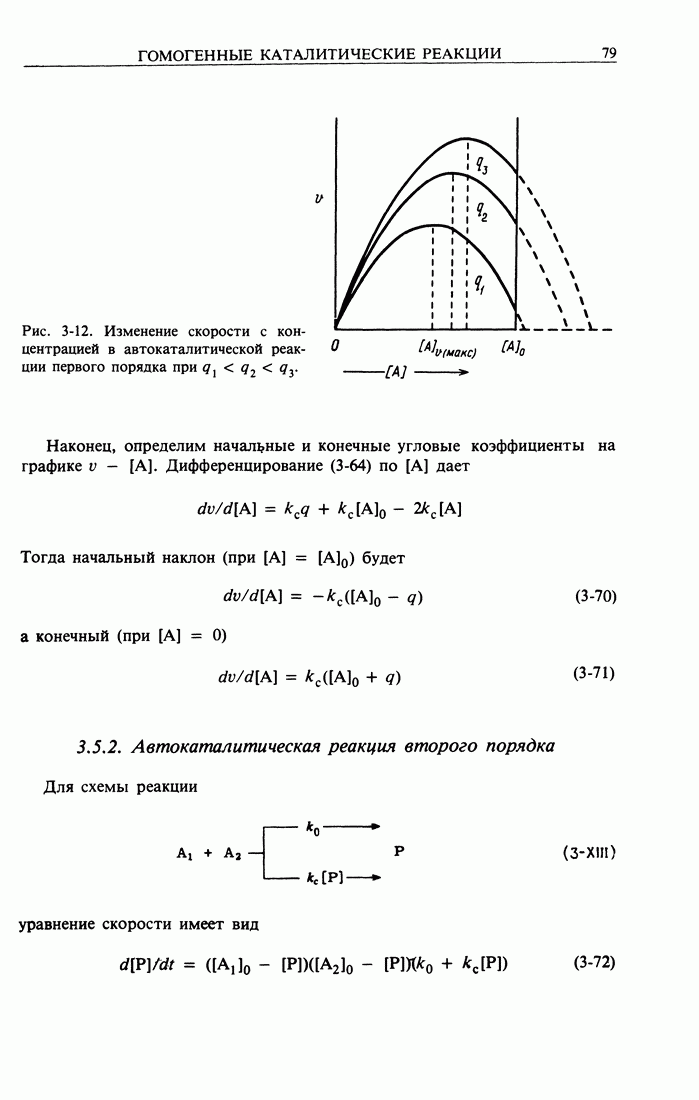
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
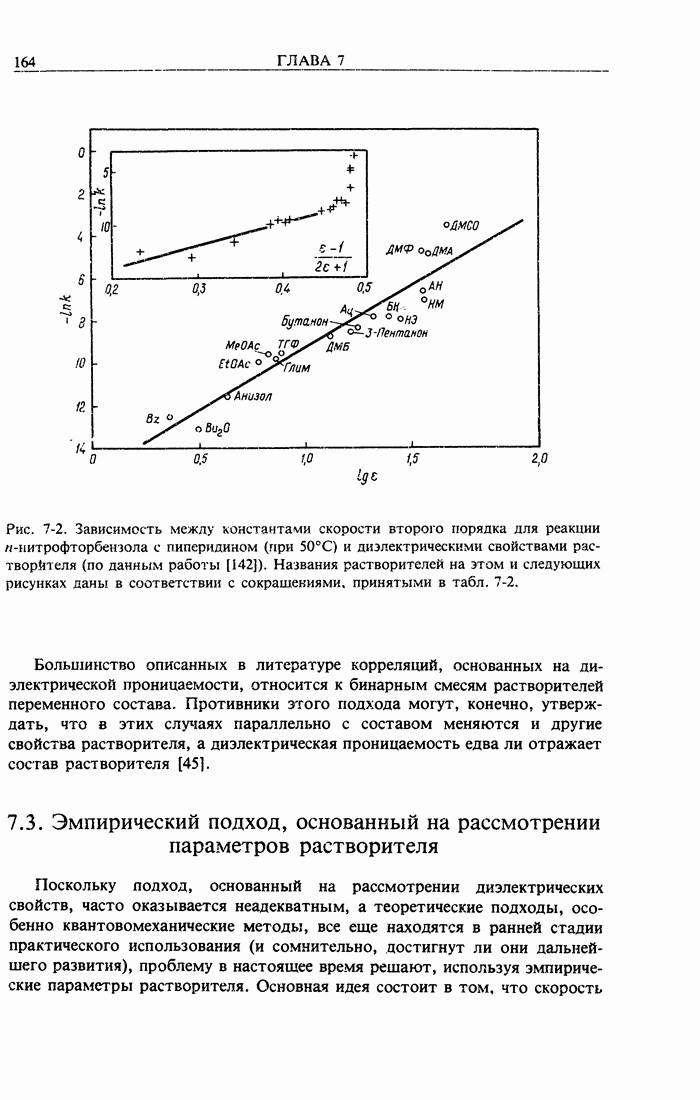
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
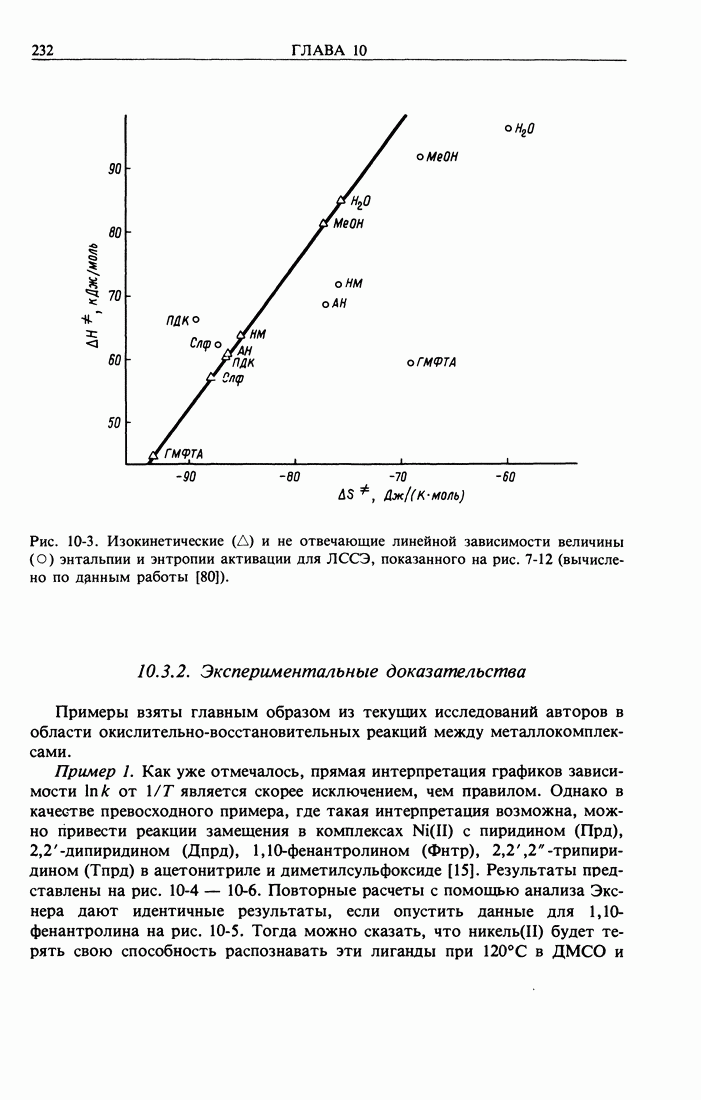
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений