| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
10.3. Изокинетическое соотношение (ИКС)
С целью анализа данных по энтальпии и энтропии рассмотрим температурную зависимость линейного соотношения свободных энергий (ЛССЭ) на основании уравнения Гаммета, принятого за модельное. Запишем уравнение  в новом виде, подставляя (10-1) и выражая свободные энергии
в новом виде, подставляя (10-1) и выражая свободные энергии 
тивации через энтропию и энтальпию активации. Тогда для реакции с незамещенными реагентами ( вместо
вместо  получим
получим

где все обозначения соответствуют уравнениям (10-4) — (10-7), т.е. 6 означает изменения  и
и  при варьировании параметра. В левой части уравнения (10-17) переменной является только температура, а в правой части — только коэффициент чувствительности
при варьировании параметра. В левой части уравнения (10-17) переменной является только температура, а в правой части — только коэффициент чувствительности  т.е. наклон прямой, соответствующей ЛССЭ. Температурной зависимостью эмпирических параметров, в данном случае параметра
т.е. наклон прямой, соответствующей ЛССЭ. Температурной зависимостью эмпирических параметров, в данном случае параметра  можно пренебречь точно так же, как и температурной зависимостью членов
можно пренебречь точно так же, как и температурной зависимостью членов  и
и  (ср. с разд. 5.7), при условии, что каждую реакцию данной серии проводят в одном и том же интервале температур. Эмпирические параметры, хотя и определенные при одной температуре, можно использовать для корреляции реакционной способности при других температурах и при этом получить соотношения свободной энергии, которые сохраняют линейную форму.
(ср. с разд. 5.7), при условии, что каждую реакцию данной серии проводят в одном и том же интервале температур. Эмпирические параметры, хотя и определенные при одной температуре, можно использовать для корреляции реакционной способности при других температурах и при этом получить соотношения свободной энергии, которые сохраняют линейную форму.
При некоторой температуре Гизо, обозначаемой  в литературе:
в литературе:

коэффициент  становится равным нулю, так как вклады
становится равным нулю, так как вклады  и
и  взаимно уравновешивают друг друга. Тогда в уравнениях (10-5) — (10-7) член
взаимно уравновешивают друг друга. Тогда в уравнениях (10-5) — (10-7) член  исчезает. Следовательно,
исчезает. Следовательно,  а значит, и константы скорости остаются постоянными в данной серии реакций. При разделении свободных энергий в уравнениях (10-5) —
а значит, и константы скорости остаются постоянными в данной серии реакций. При разделении свободных энергий в уравнениях (10-5) —  на две части, энтальпийную и энтропийную, становится очевидным, что
на две части, энтальпийную и энтропийную, становится очевидным, что  и
и  линейно меняются с изменением
линейно меняются с изменением  и
и  соответственно. Таким образом, так называемый изокинетический график зависимости
соответственно. Таким образом, так называемый изокинетический график зависимости  от
от  будет линейным с положительным наклоном, равным Гизо. То же самое можно вывести и для аррениусовского графика, поскольку реакции одной серии дают набор прямых, пересекающихся в одной точке с абсциссой, равной 7. Совпадение численных значений Гизо, полученных по двум графикам, убедительно доказывает наличие эффекта, который называют изокинетическим соотношением (ИКС) или эффектом компенсации. Величину
будет линейным с положительным наклоном, равным Гизо. То же самое можно вывести и для аррениусовского графика, поскольку реакции одной серии дают набор прямых, пересекающихся в одной точке с абсциссой, равной 7. Совпадение численных значений Гизо, полученных по двум графикам, убедительно доказывает наличие эффекта, который называют изокинетическим соотношением (ИКС) или эффектом компенсации. Величину  называют изокинетической температурой (в кинетических терминах) или температурой компенсации (в терминах энергии). (Аналогичное соотношение между
называют изокинетической температурой (в кинетических терминах) или температурой компенсации (в терминах энергии). (Аналогичное соотношение между  называют изоравновесным или изотермодинамическим соотношением. Подобным аррениусовскому является график Вант-Гоффа для зависимости логарифма константы равновесия от
называют изоравновесным или изотермодинамическим соотношением. Подобным аррениусовскому является график Вант-Гоффа для зависимости логарифма константы равновесия от  Последние примеры см. в работе [1].)
Последние примеры см. в работе [1].)
Картина, подобная представлению ИКС на аррениусовском графике, появляется на графике Гаммета и в других линейных соотношениях свободных энергий, когда исследование проводят при различных температурах. Прямые здесь также пересекаются в одной точке, соответствующей значению параметра для изокинетического заместителя или растворителя

Рис. 10-2. Температурная зависимость правильного ЛССЭ.
В левой части — график Аррениуса: введение изокинетического заместителя  должно сделать удельную скорость нечувствительной к температуре (верхняя пунктирная линия). В правой части — график Гаммета: при изокинетической температуре
должно сделать удельную скорость нечувствительной к температуре (верхняя пунктирная линия). В правой части — график Гаммета: при изокинетической температуре  удельная скорость нечувствительна к замене заместителя.
удельная скорость нечувствительна к замене заместителя.
 введение которого делает скорость реакции нечувствительной к температуре. Соотношение между графиками Аррениуса и Гаммета, которые можно рассматривать как точно соответствующие друг другу, показано на рис. 10-2. Рассмотрим удельную скорость как функцию двух параметров — температуры и константы Гаммета:
введение которого делает скорость реакции нечувствительной к температуре. Соотношение между графиками Аррениуса и Гаммета, которые можно рассматривать как точно соответствующие друг другу, показано на рис. 10-2. Рассмотрим удельную скорость как функцию двух параметров — температуры и константы Гаммета:

Эту функцию можно представить графически с помощью температурной зависимости наклона «гамметовской линии» или с помошью зависимости наклона «аррениусовской линии» от заместителя. Нулевой наклон обеих линий имеет место в частном случае, как можно видеть из уравнения (10-17), которое равно  Разность скоростей становится равной нулю, если члены, соответствующие энтальпии и энтропии, сокрашаются,
Разность скоростей становится равной нулю, если члены, соответствующие энтальпии и энтропии, сокрашаются,
а это достигается одним из двух указанных ниже способов при допущении, что выполняется ИКС.
а) Меняют температуру при постоянных параметрах активации (заместитель остается неизменным). При изокинетической температуре

б) Меняют параметры активации (равномерно, чтобы не нарушалось ИКС), а температуру поддерживают постоянной. Тогда вклады энтальпии и энтропии взаимно уравновешиваются при введении изокинетического заместителя, для которого

Уравнение (10-17) подразумевает, что величина  является линейной функцией обратной температуры (ср. с
является линейной функцией обратной температуры (ср. с 

где  произвольно выбранные константы. Тогда (10-17) можно переписать в виде
произвольно выбранные константы. Тогда (10-17) можно переписать в виде

Из этого уравнения легко вывести условия для получения общей точки пересечения на любом графике. Так, для графика Аррениуса эта точка задается выражением

Таким образом, температура, при которой можно найти общую точку пересечения, т.е. изокинетическая температура, выражается как

Это согласуется с данными Экснера [29], который отмечал, что уравнение (10-19) может быть справедливым при любой произвольно выбранной температуре только в том случае, если в левой части уравнения первый и второй члены равны соответственно  Это еще раз указывает, что ИКС оказывается необходимым условием для существования простых ЛССЭ.
Это еще раз указывает, что ИКС оказывается необходимым условием для существования простых ЛССЭ.
Общая точка пересечения на графике Гаммета задается как

Тогда из уравнения (10-19) получаем

Это означает, что либо  либо Тазо
либо Тазо  Нулевое значение А должно указывать на изоэнтальпийную серию реакций, а это исключено, если на графике Аррениуса нет общей точки пересечения. Следовательно, общая точка пересечения на графике Гаммета может появляться при бесконечно малой или бесконечно большой Гизо [127]. В любом случае серия реакций, для которой существует общая точка пересечения на графике Гаммета, должна иметь такую же точку и на графике Аррениуса. В том, что при этом
Нулевое значение А должно указывать на изоэнтальпийную серию реакций, а это исключено, если на графике Аррениуса нет общей точки пересечения. Следовательно, общая точка пересечения на графике Гаммета может появляться при бесконечно малой или бесконечно большой Гизо [127]. В любом случае серия реакций, для которой существует общая точка пересечения на графике Гаммета, должна иметь такую же точку и на графике Аррениуса. В том, что при этом  нетрудно убедиться, так как удельная скорость при изокинетическрй температуре
нетрудно убедиться, так как удельная скорость при изокинетическрй температуре  нечувствительна к изменению заместителя и поэтому включает также изокинетический заместитель и наоборот. Кроме того, как видно из рис. 10-2, общие точки пересечения на обоих графиках соответствуют одной и той же удельной скорости.
нечувствительна к изменению заместителя и поэтому включает также изокинетический заместитель и наоборот. Кроме того, как видно из рис. 10-2, общие точки пересечения на обоих графиках соответствуют одной и той же удельной скорости.
Если рассмотреть ЛССЭ со многими параметрами точно так же, как простое уравнение Гаммета, то ИКС определить не удается, поскольку нельзя предположить, чтобы различные коэффициенты чувствительности имели бы одинаковую температурную зависимость. Поэтому считается, что разница в реакционной способности в серии реакций, для которой выполняется ИКС, относится к единственному или преобладающему механизму взаимодействия (этот механизм следует отличать от механизма реакции в целом, хотя наличие определенного механизма реакции, является необходимым, но не достаточным условием для выполнения ИКС). Другими словами, разница в реакционной способности контролируется тем, что мы произвольно называем единственным, специфическим эффектом, связанным с изменением специфического параметра. Это означает, что ИКС необязательно выполняется для ЛССЭ по одному параметру, поскольку используемый параметр может быть составным, как, например, константы  Они включают не только электронный эффект, но и стабилизацию электронообогащенного или электронодефицитного переходного состояния. Было показано, что в действительности для линейных соотношений
Они включают не только электронный эффект, но и стабилизацию электронообогащенного или электронодефицитного переходного состояния. Было показано, что в действительности для линейных соотношений  изокинетическое соотношение не выполняется [76, 321]. Возвращаясь к эффектам растворителя, можно утверждать, что в отличие от эффектов заместителя изокинетическое поведение первых является скорее исключением, чем правилом, так как эффекты растворителя редко можно связать с одним параметром. ИКС должно выполняться в предельных случаях, когда доминирующим является одно из свойств растворителя. Это будет показано на примере реакции, ЛССЭ для которой представлено на рис. 7-12.
изокинетическое соотношение не выполняется [76, 321]. Возвращаясь к эффектам растворителя, можно утверждать, что в отличие от эффектов заместителя изокинетическое поведение первых является скорее исключением, чем правилом, так как эффекты растворителя редко можно связать с одним параметром. ИКС должно выполняться в предельных случаях, когда доминирующим является одно из свойств растворителя. Это будет показано на примере реакции, ЛССЭ для которой представлено на рис. 7-12.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
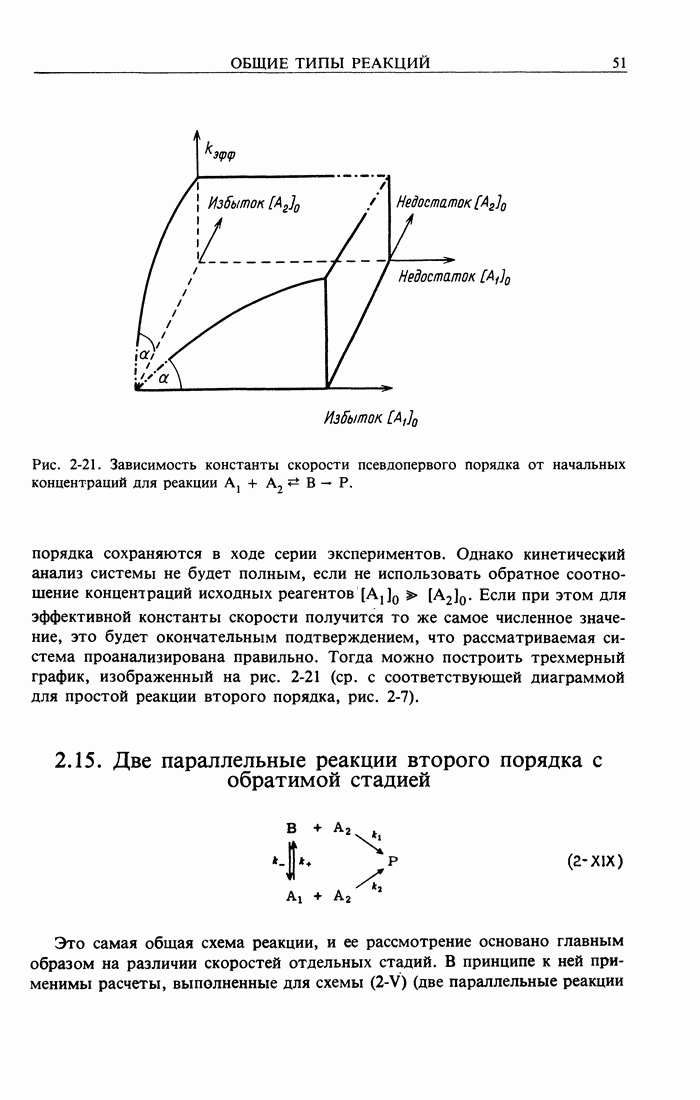
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
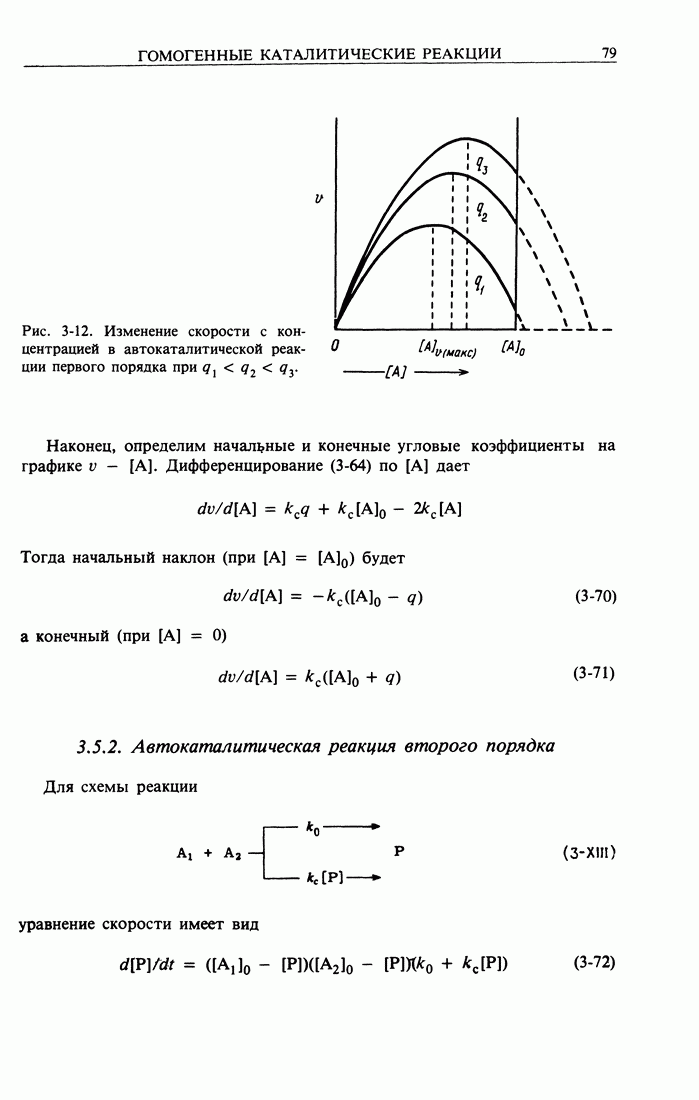
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
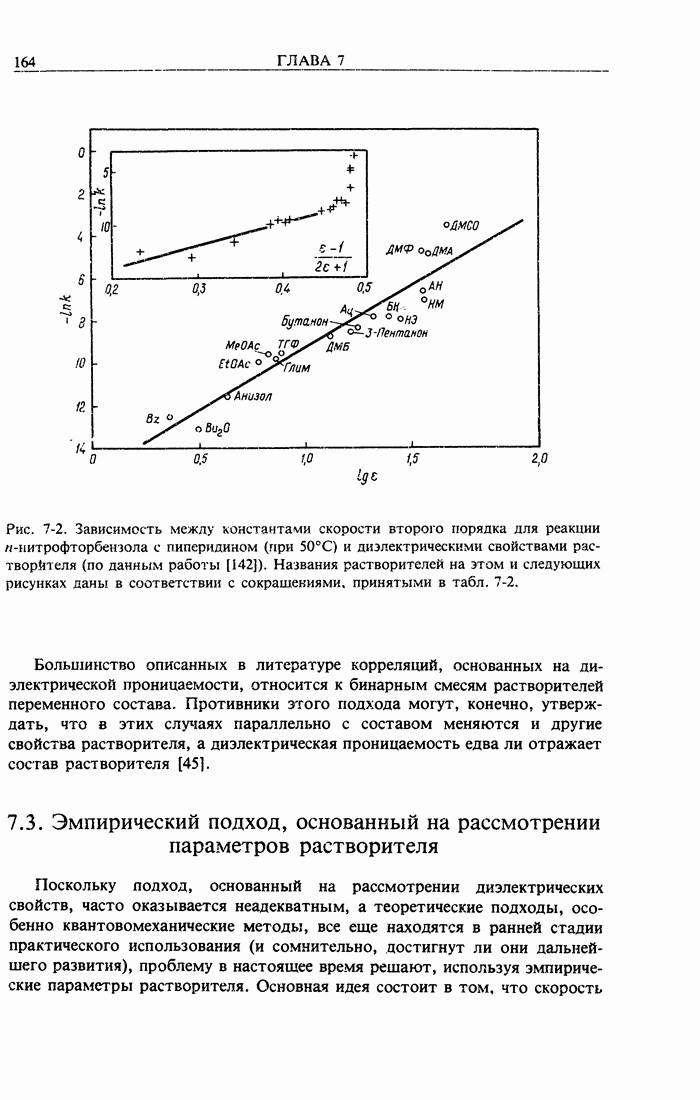
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
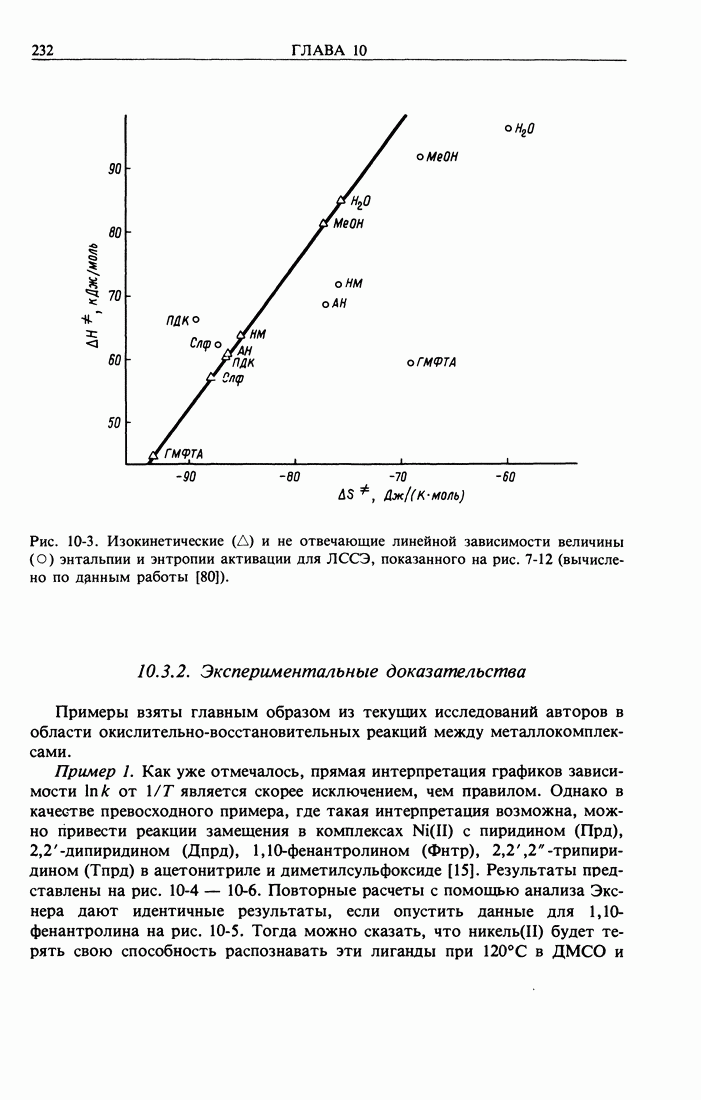
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений