| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
5.5. Физический смысл энтропии активации
Из уравнения (5-21) видно, что энтропия активации связана со стерическим фактором. Это следует также из закона Больцмана  (ср. с [78]). Если записать его для перехода начального состояния
(ср. с [78]). Если записать его для перехода начального состояния  в активированное состояние
в активированное состояние  то получим
то получим

где  термодинамические вероятности активированного и начального состояний. Преобразуя последнее уравнение, приходим к величине Р:
термодинамические вероятности активированного и начального состояний. Преобразуя последнее уравнение, приходим к величине Р:

выражающей вероятность того, что при столкновении частицы имеют стерическую ориентацию, необходимую для протекания реакции. Согласно уравнению (5-27), стерический фактор, равный единице, должен соответствовать нулевой энтропии активации. Это наблюдается в случае элементарной реакции первого порядка, где молекулярная ориентация не имеет значения. Чем больше молекул, участвующих в образовании активированного комплекса, тем большую роль должна играть их ориентация. Таким образом, мы получаем  и отрицательную энтропию активации. Положительные величины
и отрицательную энтропию активации. Положительные величины  найденные экспериментально, нельзя объяснить с точки зоения стерического фактора, поскольку последний, естественно, не может быть больше единицы. Поэтому понятие энтропии активации, которая может быть положительной величиной, имеет определенные преимущества перед менее точным понятием фактора вероятности
найденные экспериментально, нельзя объяснить с точки зоения стерического фактора, поскольку последний, естественно, не может быть больше единицы. Поэтому понятие энтропии активации, которая может быть положительной величиной, имеет определенные преимущества перед менее точным понятием фактора вероятности  Главное преимущество связано с тем, что теория активированного комплекса допускает внутреннее движение молекулярных частиц. Поскольку величина
Главное преимущество связано с тем, что теория активированного комплекса допускает внутреннее движение молекулярных частиц. Поскольку величина  является разностью функций распределения активированного комплекса и реагирующих частиц, она представляет собой меру изменения степеней свободы внутреннего движения при переходе от начального состояния к активированному комплексу. Приобретение и потеря степеней свободы отражаются соответственно в положительной и отрицательной величинах
является разностью функций распределения активированного комплекса и реагирующих частиц, она представляет собой меру изменения степеней свободы внутреннего движения при переходе от начального состояния к активированному комплексу. Приобретение и потеря степеней свободы отражаются соответственно в положительной и отрицательной величинах  Так, для элементарной реакции первого порядка
Так, для элементарной реакции первого порядка  должна быть положительной или небольшой отрицательной величиной, если система приходит к конечному состоянию через циклический активированный комплекс (экспериментальные примеры можно найти в работе [130]). Чем сложнее конфигурация активированного комплекса, тем более отрицательной становится величина
должна быть положительной или небольшой отрицательной величиной, если система приходит к конечному состоянию через циклический активированный комплекс (экспериментальные примеры можно найти в работе [130]). Чем сложнее конфигурация активированного комплекса, тем более отрицательной становится величина  Однако в растворе может быть настолько сложная ситуация, что этот прогноз окажется несостоятельным. Это связано с тем, что в растворе и реагенты, и активированные комплексы нельзя рассматривать как изолированные частицы, так как и те и другие в той или иной степени сольватированы; подробнее этот вопрос будет рассмотрен в гл. 7. Здесь же отметим только главное: на общей величине
Однако в растворе может быть настолько сложная ситуация, что этот прогноз окажется несостоятельным. Это связано с тем, что в растворе и реагенты, и активированные комплексы нельзя рассматривать как изолированные частицы, так как и те и другие в той или иной степени сольватированы; подробнее этот вопрос будет рассмотрен в гл. 7. Здесь же отметим только главное: на общей величине  сказывается различие в степени сольватации, т.е. в степени взаимодействия с растворителем, при переходе от начального состояния к активированному комплексу, поэтому величину
сказывается различие в степени сольватации, т.е. в степени взаимодействия с растворителем, при переходе от начального состояния к активированному комплексу, поэтому величину  можно рассматривать как сумму внешнего (за счет сольватации) и внутреннего (за счет истинной реакции) вкладов [50, 51, 74]:
можно рассматривать как сумму внешнего (за счет сольватации) и внутреннего (за счет истинной реакции) вкладов [50, 51, 74]:

Чем сильнее связаны молекулы растворителя, тем больше они ориентированы и тем больше ограничена их свобода. Естественно, что потеря поступательных и вращательных степеней свободы в связанных молекулах растворителя должна приводить к понижению энтропии. Такая интерпретация подтверждается изменением парциальной молярной энтропии, наблюдаемым при обратимом переносе электрона в растворе и полученным экспериментально путем измерения потенциала ячейки как функции температуры. Найдено, что изменение энтропии электродной реакции между двумя положительно заряженными частицами положительное, например

тогда как в случае переноса электрона между отрицательно заряженными частицами изменение энтропии отрицательное, например

Оба измерения проведены в воде. Можно считать, что эти данные отражают увеличение упорядоченности растворителя вокруг частиц с меньшим зарядом [71].
Таким образом, присутствие активированного комплекса, более сильно сольватированного по сравнению с исходными веществами, будет сдвигать  в сторону более отрицательных значений и наоборот. Поэтому изменение энтропии за счет различия в степени сольватации может более чем компенсировать энтропию активации самой реакции. Например, стадия диссоциации, включающай высокополярный и потому хорошо сольватированный активированный комплекс, может показать отрицательную
в сторону более отрицательных значений и наоборот. Поэтому изменение энтропии за счет различия в степени сольватации может более чем компенсировать энтропию активации самой реакции. Например, стадия диссоциации, включающай высокополярный и потому хорошо сольватированный активированный комплекс, может показать отрицательную  С другой стороны, бимолекулярная реакция иона с высоким зарядом и большой нейтральной молекулы может показать даже положительную
С другой стороны, бимолекулярная реакция иона с высоким зарядом и большой нейтральной молекулы может показать даже положительную  Это можно объяснить рассредоточением заряда, вследствие чего активированный комплекс оказывается намного менее сольватированным, чем исходный ион [4, 127].
Это можно объяснить рассредоточением заряда, вследствие чего активированный комплекс оказывается намного менее сольватированным, чем исходный ион [4, 127].
Очевидно, что экспериментальные значения  не позволяют сделать определенных выводов о молекулярности измеряемой стадии реакции. Однако вместе с другими данными значение
не позволяют сделать определенных выводов о молекулярности измеряемой стадии реакции. Однако вместе с другими данными значение  дает исключительно полезные сведения о природе активированного комплекса.
дает исключительно полезные сведения о природе активированного комплекса.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
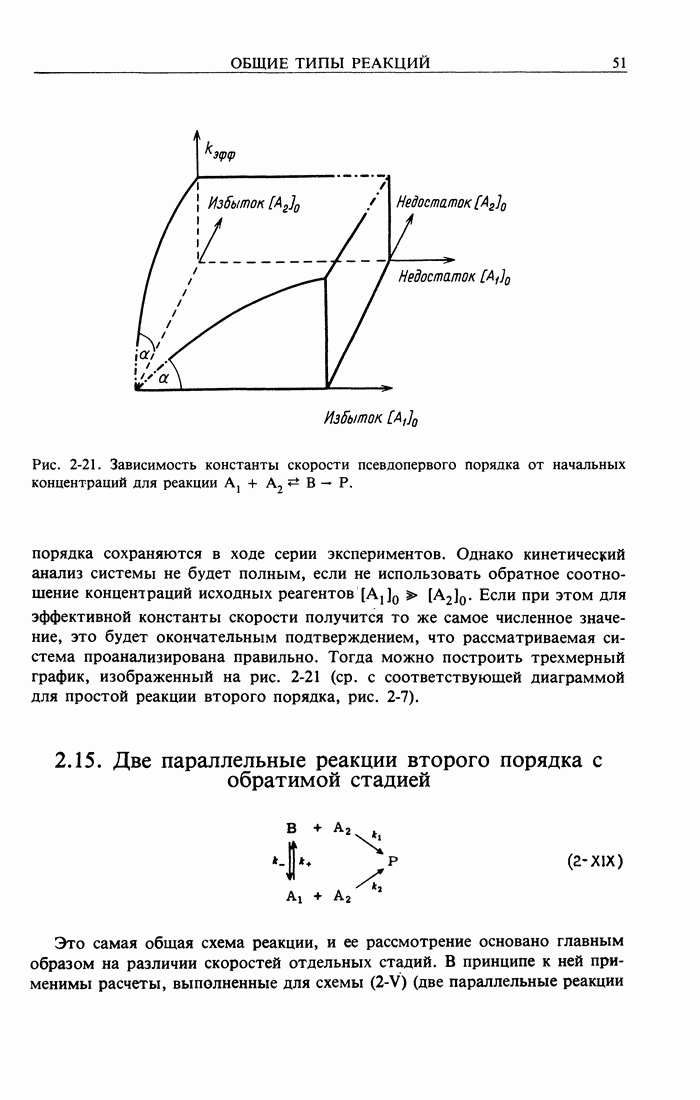
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
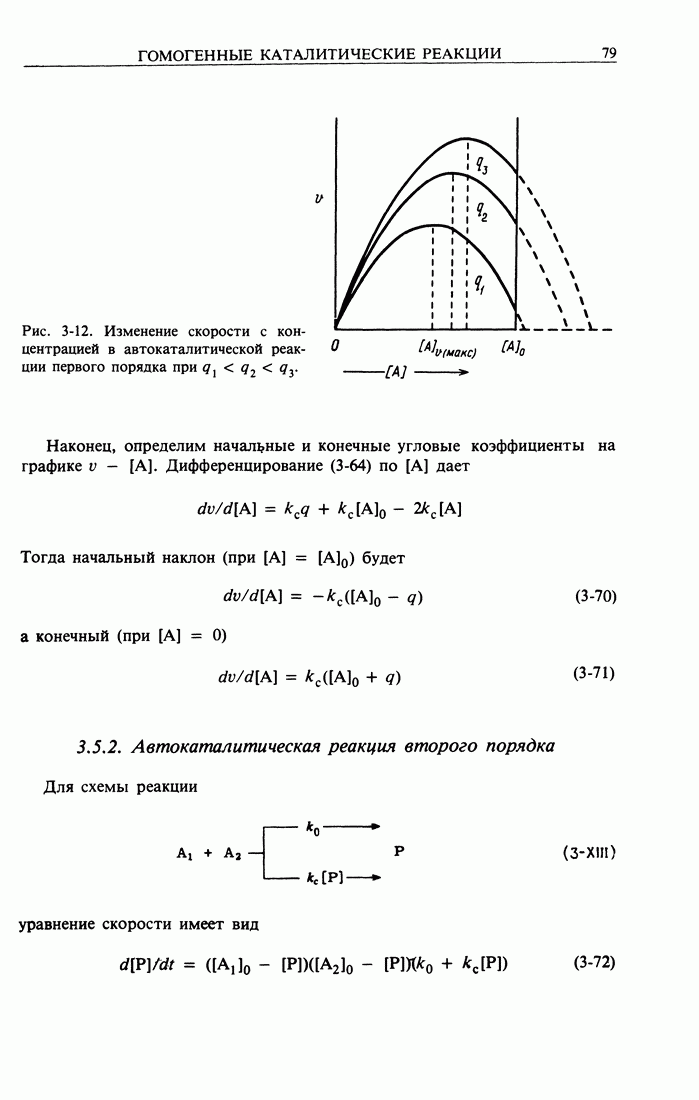
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
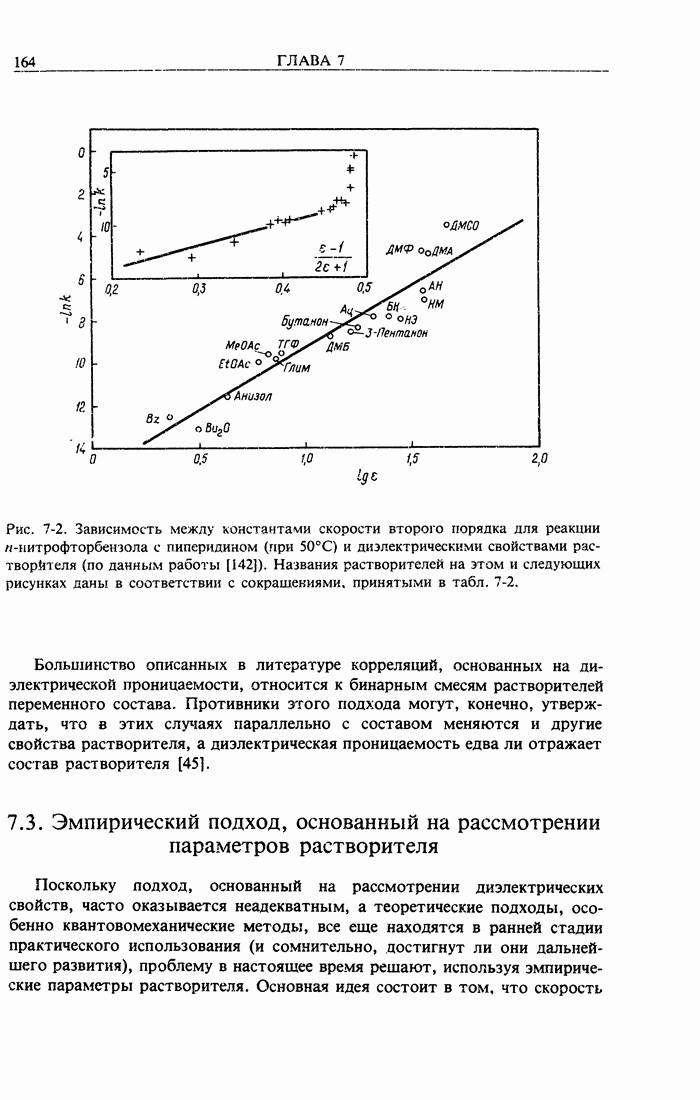
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
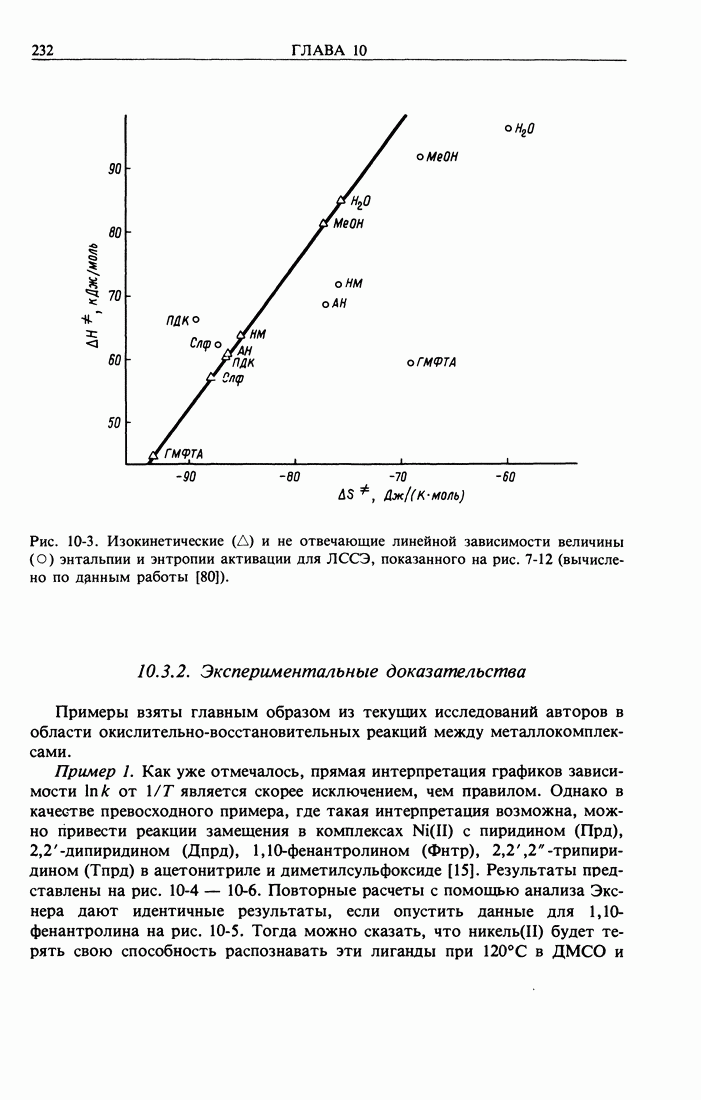
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений