| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
Поскольку подход, основанный на рассмотрении диэлектрических свойств, часто оказывается неадекватным, а теоретические подходы, особенно квантовомеханические методы, все еще находятся в ранней стадии практического использования (и сомнительно, достигнут ли они дальнейшего развития), проблему в настоящее время решают, используя эмпирические параметры растворителя. Основная идея состоит в том, что скорость
определенной реакции, равновесие или спектральный эффект могут быть пригодны для того, чтобы служить моделью для других реакций. Одно из первых наблюдений в этом направлении принадлежит Грюнвальду и Уинстейну 138], которые нашли, что величины  для сольволиза некоторых соединений во многих растворителях меняются линейно с величинами
для сольволиза некоторых соединений во многих растворителях меняются линейно с величинами  для сольволиза трет-бутилхлорида в тех же растворителях. Они предложили последнюю величину считать количественной мерой «ионизирующей способности» раствори гелей. Поскольку использование этого параметра оказалось очень ограниченным, были приняты и другие индексы, и в настоящее время имеется целый ряд таких параметров. Особенно много параметров, основанных на влиянии растворителя на
для сольволиза трет-бутилхлорида в тех же растворителях. Они предложили последнюю величину считать количественной мерой «ионизирующей способности» раствори гелей. Поскольку использование этого параметра оказалось очень ограниченным, были приняты и другие индексы, и в настоящее время имеется целый ряд таких параметров. Особенно много параметров, основанных на влиянии растворителя на  видимые,
видимые,  и ЯМР-спектры некоторых соединений, выбранных в качестве эталонов. Сравнительные обзоры по эмпирическим параметрам растворителей опубликованы Даком [18] и Рейхардтом [113]. Мы не хотим пытаться дублировать их работы, просто настало время пересмотреть эти параметры и упорядочить их по величине. Это делается путем изучения различных параметров в отношении друг к цругу. Кроме того, применение параметров к данным о реакционной способности неводных растворителей обнаруживает массу интересных особенностей, касающихся влияния растворителя на химические реакции, и позволяет перевести эти корреляции в физические модели взаимодействия растворенное вещество — растворитель. В последующем обсуждении будут отмечены главные моменты такого анализа.
и ЯМР-спектры некоторых соединений, выбранных в качестве эталонов. Сравнительные обзоры по эмпирическим параметрам растворителей опубликованы Даком [18] и Рейхардтом [113]. Мы не хотим пытаться дублировать их работы, просто настало время пересмотреть эти параметры и упорядочить их по величине. Это делается путем изучения различных параметров в отношении друг к цругу. Кроме того, применение параметров к данным о реакционной способности неводных растворителей обнаруживает массу интересных особенностей, касающихся влияния растворителя на химические реакции, и позволяет перевести эти корреляции в физические модели взаимодействия растворенное вещество — растворитель. В последующем обсуждении будут отмечены главные моменты такого анализа.
Нет такого единственного параметра, который можно было бы эффективно применять ко всем типам явлений, меняющихся с растворителем. Это связано с тем, что процесс сольватации может одновремекно включать несколько механизмов взаимодействия. Двумя важнейшими свойствами растворителя являются донорная (нуклеофильная, основная, катион-сольватирующая) способность и акцепторная (электрофияьиая, кислотная, анион-сольватирующая) способность, с точки зрения которых взаимодействия растворенное вещество — растворитель можно рассматривать как кислотно-основные реакции в самом широком смысле этого слова. Большинство используемых растворителей практически амфотерно, что не позволяет найти корреляцию между их донорной и акцепторной силой.
7.3.1. Донорное число и акцепторное число
Нашей целью теперь является описание влияния растворителя на скорость реакции с помощью линейной функции двух независимых, но дополняющих друг друга параметров, каждый из которых соответствует одному из двух свойств. Чтобы получить более широко применимую зависимость, важно выбрать параметры, которые позволяют разделить характеристики двух свойств, т.е. параметры, основанные на модельных субстратах, влияние растворителя на которые преимущественно определяется
одним из свойств. Такая задача требует как химического понимания, так и интуиции. Мы остановимся на донорном числе  и акцепторном числе
и акцепторном числе  предложенным школой Гутмана при разработке донорно-акцепторного подхода [41]. Одним из достоинств этого подхода является простота структуры эталонных соединений (пентахлорида сурьмы и триэтилфосфиноксида) и известный для каждого соединения механизм взаимодействия с растворителями:
предложенным школой Гутмана при разработке донорно-акцепторного подхода [41]. Одним из достоинств этого подхода является простота структуры эталонных соединений (пентахлорида сурьмы и триэтилфосфиноксида) и известный для каждого соединения механизм взаимодействия с растворителями:

Эти числа определяются следующим образом.
Донорное число  измеряет способность растворителя поделить свою электронную пару с подходящим акцептором («отдать» электроны); оно определяется как отрицательная величина, равная энтальпии образования аддукта между эталонной кислотой
измеряет способность растворителя поделить свою электронную пару с подходящим акцептором («отдать» электроны); оно определяется как отрицательная величина, равная энтальпии образования аддукта между эталонной кислотой  и молекулой растворителя в сильноразбавленном растворе
и молекулой растворителя в сильноразбавленном растворе  -дихлорэтана. Растворители, характеризующиеся наличием донорного числа, называют донорными растворителями.
-дихлорэтана. Растворители, характеризующиеся наличием донорного числа, называют донорными растворителями.
Акцепторное число  измеряет способность растворителя поделить электронную пару, принадлежащую подходящему донору («принять» электроны). Это число выводится из химических сдвигов фосфора в спектрах ЯМР, регистрируемых для
измеряет способность растворителя поделить электронную пару, принадлежащую подходящему донору («принять» электроны). Это число выводится из химических сдвигов фосфора в спектрах ЯМР, регистрируемых для  в различных растворителях. В произвольно выбранной шкале АЧ за нулевое значение принят химический сдвиг в гексане, цена деления соответствует 1/100 сдвига аддукта
в различных растворителях. В произвольно выбранной шкале АЧ за нулевое значение принят химический сдвиг в гексане, цена деления соответствует 1/100 сдвига аддукта  в
в  -дихлорэтане. Растворители, характеризующиеся наличием акцепторного числа, называют акцепторными растворителями.
-дихлорэтане. Растворители, характеризующиеся наличием акцепторного числа, называют акцепторными растворителями.
Пользуясь этими числами, зависимость скорости реакции от растворителя можно представить уравнением

где  константа скорости в эталонном растворителе,
константа скорости в эталонном растворителе,  и
и  коэффициенты чувствительности скорости рассматриваемой реакции к акцепторным и донорным свойствам растворителя. Уравнение
коэффициенты чувствительности скорости рассматриваемой реакции к акцепторным и донорным свойствам растворителя. Уравнение  можно записать и в другом, на наш взгляд, более удобном виде
можно записать и в другом, на наш взгляд, более удобном виде

где  логарифм константы скорости реакции в некоординирующем растворителе. Положительные коэффициенты чувствительности указывают на то, что реакция ускоряется при увеличении ДЧ и АЧ и наоборот. Корреляции по двум параметрам типа
логарифм константы скорости реакции в некоординирующем растворителе. Положительные коэффициенты чувствительности указывают на то, что реакция ускоряется при увеличении ДЧ и АЧ и наоборот. Корреляции по двум параметрам типа  и
и  установлены с помощью
установлены с помощью
анализа линейной регрессии методом наименьших квадратов. Однако по причинам, которые станут ясны далее, в таком анализе нельзя смешивать протонные и апротонные растворители. Обычно это должно означать, что протонные растворители следует исключить; см., например,  на рис. 7-10,б. В предельных случаях, которые еще нередко встречаются в практике, приведенные выше уравнения сводят к приближениям по одному параметру. Тогда если катионы или катионные центры либо не участвуют во взаимодействии, либо экранированы, т.е. ни реагенты, ни активированный комплекс не являются акцепторными, то член
на рис. 7-10,б. В предельных случаях, которые еще нередко встречаются в практике, приведенные выше уравнения сводят к приближениям по одному параметру. Тогда если катионы или катионные центры либо не участвуют во взаимодействии, либо экранированы, т.е. ни реагенты, ни активированный комплекс не являются акцепторными, то член  будет пренебрежимо мал по сравнению с членом
будет пренебрежимо мал по сравнению с членом  Противоположный предельный случай возникает, когда ни анион, ни анионные центры не участвуют во взаимодействии. Примеры приведены в разд. 7.6.
Противоположный предельный случай возникает, когда ни анион, ни анионные центры не участвуют во взаимодействии. Примеры приведены в разд. 7.6.
Предложены также аналогичные уравнения с другими параметрами [23, 32, 83, 105]. Они применимы, когда имеется взаимная корреляция между шкалой ДЧ и АЧ и некоторыми другими эмпирическими шкалами (см. ниже).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ОБЩИЕ ТИПЫ РЕАКЦИЙ
- 2.1. Простая реакция первого порядка
- 2.2. Простая реакция второго порядка
- 2.3. Две параллельные реакции первого порядка
- 2.4. Две параллельные реакции первого порядка с общим продуктом
- 2.5. Последовательность двух реакций первого порядка
- 2.6. Последовательность трех реакций первого порядка
- 2.7. Последовательность реакций смешанного (второго и первого) порядка
- 2.8. Обратимая реакция первого порядка
- 2.9. Обратимая реакция второго порядка
- 2.10. Обратимая реакция смешанного (первого и второго) порядка
- 2.11. Последовательность двух реакций первого порядка с обратимой первой стадией
- 2.12. Последовательность двух обратимых реакций первого порядка
- 2.13. Две параллельные обратимые реакции первого порядка с общим продуктом
- 2.14. Последовательность двух реакций второго и первого порядков с обратимой первой стадией
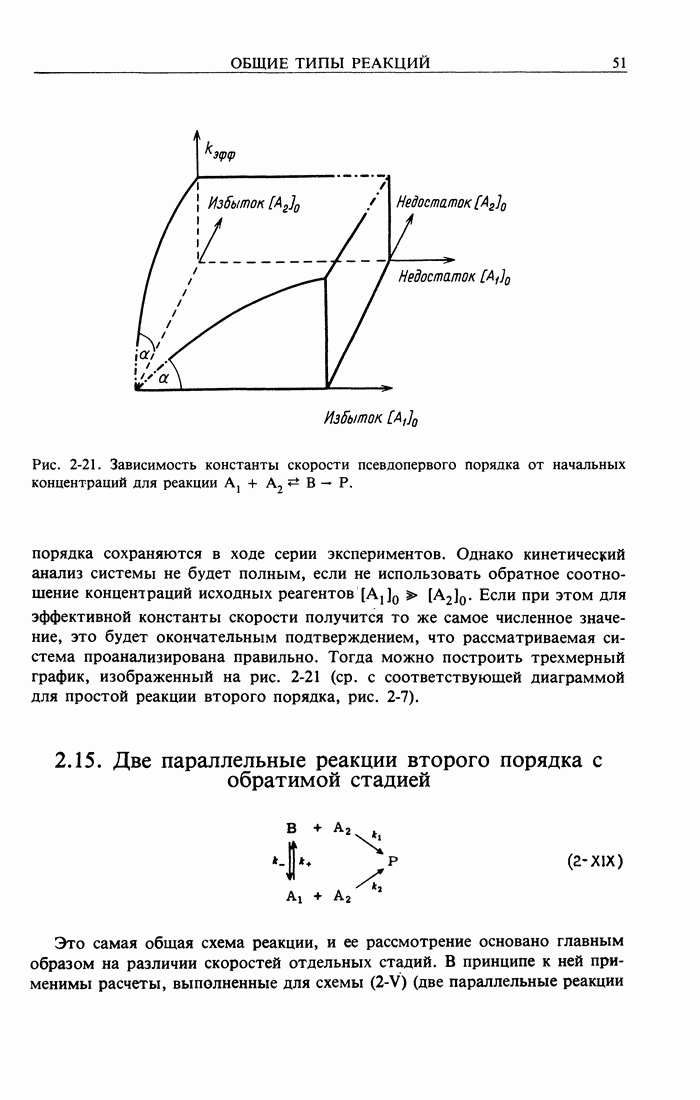
- 2.15. Две параллельные реакции второго порядка с обратимой стадией
- 3. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ РЕАКЦИИ
- 3.2. Каталитическая реакция первого порядка
- 3.3. Реакция нулевого порядка
- 3.4. Ингибирование катализатора
- 3.4.1. Обратимое ингибирование
- 3.4.2. Необратимое ингибирование
- 3.5. Автокаталитические реакции
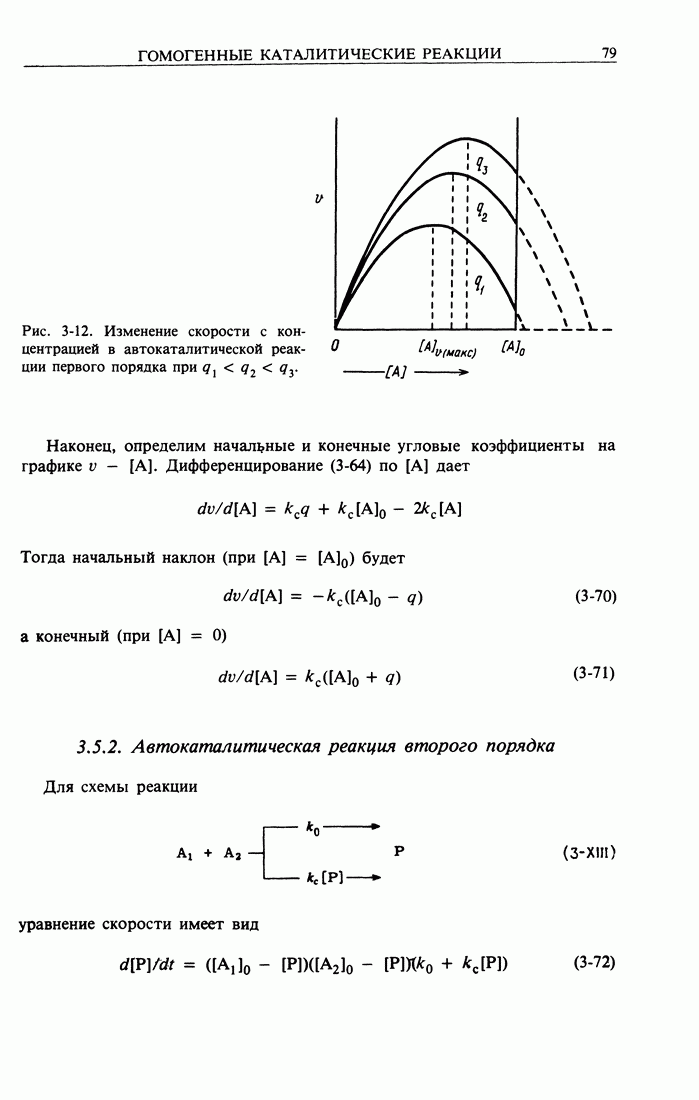
- 3.5.2. Автокаталитическая реакция второго порядка
- 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ: СИСТЕМАТИЧЕСКИЙ КИНЕТИЧЕСКИЙ АНАЛИЗ
- 4.2. Выбор условий эксперимента
- 4.3. Методы анализа кривых зависимости концентрации от времени
- 4.4. Порядок реакции и его значение
- 4.5. Математическая модель реакции
- 4.5.2. Из второй серии опытов
- 4.5.3. Из последующих серий опытов
- 4.6. Физическая модель реакции
- 4.7. Выводы
- 4.8. Схема и механизм реакции
- 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 5.1. Уравнение Аррениуса
- 5.2. Теория активированного комплекса
- 5.3. Теория столкновений
- 5.4. Сравнение выведенных уравнений
- 5.5. Физический смысл энтропии активации
- 5.6. Физический смысл энергии активации
- 5.7. Формы аррениусовских графиков
- 6. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ РАСТВОРИТЕЛЯ
- 7.2. Подход, основанный на рассмотрении диэлектрической проницаемости
- 7.3. Эмпирический подход, основанный на рассмотрении параметров растворителя
- 7.5.2. Корреляции между донорными числами и другими шкалами
- 7.3.3. Корреляции между акцепторными числами и другими шкалами
- 7.3.4. Выводы
- 7.4. Согласование двух подходов
- 7.5. Современная ситуация
- 7.6. Экспериментальные доказательства
- 7.7. Влияние ионной силы растворителя
- 7.8. Сравнительная шкала донорной и акцепторной способности
- 8. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- 8.2. Электронные эффекты
- 8.3. Стерические эффекты
- 8.4. Сведения о механизмах реакций
- 9. ПРИЛОЖЕНИЕ К ГЛАВАМ 7 И 8
- 10. ФИЗИЧЕСКОЕ ОБОСНОВАНИЕ ЭМПИРИЧЕСКИХ КОРРЕЛЯЦИЙ
- 10.2. Принцип линейности свободных энергий (принцип ЛСЭ)
- 10.3. Изокинетическое соотношение (ИКС)
- 10.3.1. Метод Экснера для установления ИКС
- 10.3.2. Экспериментальные доказательства
- 10.3.3. Практические следствия из изокинетических соотношений