| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
Краткое содержание главы
Длинноцепочечные насыщенные жирные кислоты синтезируются из ацетил-СоА цитоплазматическим комплексом ферментов, к числу которых относится и ацилпереносящий белок (АПБ), содержащий в качестве простетической группы фосфопантетеин. В молекуле 3-кетоацил-АПБ—синтазы имеются две существенные для ее каталитической активности SH-группы, одна из которых принадлежит фосфопантетеину  а другая - остатку цистеина (Cys). АПБ функционирует как переносчик промежуточных продуктов синтеза жирных кислот. Образующийся из ацетил-СоА ацетил-S-Cys-AnE реагирует с малонил-S-АПБ, образовавшимся из малонил-СоА, в результате чего получается ацетоацетил-S-AnE и выделяется
а другая - остатку цистеина (Cys). АПБ функционирует как переносчик промежуточных продуктов синтеза жирных кислот. Образующийся из ацетил-СоА ацетил-S-Cys-AnE реагирует с малонил-S-АПБ, образовавшимся из малонил-СоА, в результате чего получается ацетоацетил-S-AnE и выделяется  . Вслед за этим происходит восстановление ацетоацетил-Б-АПБ в D-3-гидроксипроизвод-ное, которое затем гидратируется до транс-
. Вслед за этим происходит восстановление ацетоацетил-Б-АПБ в D-3-гидроксипроизвод-ное, которое затем гидратируется до транс- -бутеноил-8-АПБ; двойная связь в ацильной группе этого соединения восстанавливается и насыщается за счет NADPH с образованием бутирил-S-АПБ. Далее к карбоксильному концу растущей цепи жирной кислоты последовательно присоединяются еще шесть молекул малонил-S-АПБ и в результате получается пальмитоил-S—Cys-АПБ — конечный продукт реакций, катализируемых синтазным комплексом для образования жирных кислот. Затем происходит гидролитическое отщепление свободной пальмитиновой кислоты. При удлинении пальмитиновой кислоты возникает 18-углеродная стеариновая кислота. Под действием оксигеназ со смешанной функцией в молекулах пальмитиновой и стеариновой кислот возникают двойные связи, что приводит к образованию соответственно пальмитолеиновой и олеиновой кислот.
-бутеноил-8-АПБ; двойная связь в ацильной группе этого соединения восстанавливается и насыщается за счет NADPH с образованием бутирил-S-АПБ. Далее к карбоксильному концу растущей цепи жирной кислоты последовательно присоединяются еще шесть молекул малонил-S-АПБ и в результате получается пальмитоил-S—Cys-АПБ — конечный продукт реакций, катализируемых синтазным комплексом для образования жирных кислот. Затем происходит гидролитическое отщепление свободной пальмитиновой кислоты. При удлинении пальмитиновой кислоты возникает 18-углеродная стеариновая кислота. Под действием оксигеназ со смешанной функцией в молекулах пальмитиновой и стеариновой кислот возникают двойные связи, что приводит к образованию соответственно пальмитолеиновой и олеиновой кислот.
Млекопитающие не способны синтезировать линолевую кислоту и должны получать ее с пищей растительного происхождения; экзогенную линолевую кислоту они могут превращать в арахидоновую кислоту, которая служит предшественником простагландинов.
Триацилглицеролы синтезируются путем взаимодействия двух молекул СоА - производных жирных кислот с глицерол-3-фосфатом; при этом образуется фосфатидная кислота, которая затем дефосфорилируется до диацилглицерола. Последний ацилируется третьей молекулой СоА-производного жирной кислоты с образованием триацилглицерола. Диацилглицеролы являются также главными предшественниками фосфоглицеролов. Голова молекулы фосфатидилэтаноламина сначала формируется в виде цитидиндифосфатэтаноламина путем взаимодействия цитидинтрифосфата (СТР) с фосфоэтаноламином. Далее фосфоэтаноламинная группа переносится на диацилглицерол, что приводит к образованию фосфатидилэтаноламина. Фосфатидилхолин образуется путем метилирования фосфатидилэтаноламина или при взаимодействии диацилглицерола с цитидиндифосфатхолином. Холестерол также синтезируется из ацетил-СоА в результате очень сложной последовательности реакций, в которых образуются важные промежуточные соединения - гидроксиметилглутарил-СоА, мевалонат и линейный углеводород сквален. Последний циклизуется с образованием циклической стероидной системы конденсированных колец с боковой цепью. Биосинтез холестерола ингибируется поступающим с пищей холестеролом.
ЛИТЕРАТУРА
Биосинтез жирных кислот Cunningham Е.В. Biochemistry: Mechanisms of Metabolism, McGraw-Hill, New York, 1978. В гл. 12 приведено много дополнительных сведений, касающихся энзимологии и механизма синтеза жирных кислот.
Jeffcoat R. The Biosynthesis of Unsaturated Fatty Acids and Its Control in Mammalian Liver, Essays Biochem., 15, 1-36 (1979).
Биосинтез липидов
Snyder F. (ed.). Lipid Metabolism in Mammals, vols. 1 and 2, Plenum, New York, 1977.
Обмен холестерола
Bloch К. S. The Biological Synthesis of Cholesterol, Science, 150, 19-28 (1965).
Brown M. S., Goldstein J. L. Receptor-Mediated Control of Cholesterol Metabolism, Science, 191, 150-154 (1976).
Общие вопросы
Clarke M. R. The Head of the Sperm Whale, Sci. Am., 240, 128-141, January 1979. Более подробные сведения о биологической функции спермацета у кашалотов.
Nelson R. A. Protein and Fat Metabolism in Hibernating Bears, Fed. Proc., 39, 2955-2958 (1980).
Генетические нарушения липидного обмена
Allison А. С. Lysosomes. In: J. J. Head (ed.). Carlina Biology Readers, Carolina Biological Supply Company, Burlington, N. C., 1977.
Brown M. S., Goldstein J. L. Familial Hypercholesterolemia: Defective Binding of Lipoproteins to Cultured Fibroblasts Associated with Impaired Regulation of 3-Hydroxy-3-methylglutaryl Coenzyme
A Reductase Activity, Proc. Natl. Acad. Sci. USA, 71, 788-792 (1974).
Dietschy J. M, Gotto A. M, Jr., Ontko J. A. (eds.). Disturbances in Lipid and Lipoprotein Metabolism, American Physiological Society, 1978.
Stanbury J. B., Wyngaarden J. B., Fredrickson D. S. (eds.). The Metabolic Besis of Inherited Disease, 4th ed, McGraw-Hill, New York, 1978.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
- ГЛАВА 13. МЕТАБОЛИЗМ. ОБЩИЙ ОБЗОР
- 13.1. Живые организмы принимают участие в круговороте углерода и кислорода
- 13.2. В биосфере существует круговорот азота
- 13.3. Метаболические пути представляют собой последовательности реакций, катализируемых мультиферментными системами
- 13.4. Метаболизм включает катаболические и анаболические пути (процессы распада и процессы синтеза)
- 13.5. Катаболические пути сходятся — образуется лишь небольшое число конечных продуктов
- 13.6. Биосинтетические (анаболические) пути расходятся — образуется много разных продуктов
- 13.7. Соответствующие катаболические и анаболические пути различаются, и эти различия имеют важное значение.
- 13.8. Энергия перелается от катаболических реакций к анаболическим при помощи АТР
- 13.9. NADPH переносит энергию в форме восстановительной способности
- 13.10. Клеточный метаболизм — это экономичный, строго регулируемый лроцесс
- 13.11. Регуляция метаболических путей осуществляется на трех уровнях
- 13.12. Вторичный метаболизм
- 13.13. Метаболические пути могут быть идентифицированы в прямых опытах
- 13.14. Промежуточные стадии метаболизма можно выявлять с помощью мутантных организмов
- 13.15. Включение изотопной метки — весьма эффективный метод изучения метаболизма
- 13.16. Различные метаболические пути могут быть локализованы в разных участках клетки
- ЛИТЕРАТУРА
- ГЛАВА 14. ATP — ЦИКЛ И БИОЭНЕРГЕТИКА КЛЕТКИ
- 14.1. Первый и второй законы термодинамики
- 14.2. Клеткам необходима свободная энергия
- 14.3. Изменение стандартной свободной энергии химической реакции можно вычислить
- 14.4. Химические реакции характеризуются определенной величиной
- 14.5. Величины различаются, и это различие имеет важное значение
- 14.6. Изменения стандартной свободной энергии химических реакций аддитивны
- 14.8. Химические свойства АТР хорошо известны
- 14.9. Характерное значение, стандартной свободной энергии АТР
- 14.10. Почему стандартная свободная энергия гидролиза АТР относительно велика?
- 14.11. АТР служит общим промежуточным продуктом в реакциях переноса фосфатных групп
- 14.12. При расщеплении глюкозы до лактата образуются два сверхвысокоэнергетических фосфорилированных соединения
- 14.13. В результате переноса фосфатной группы от АТР на какую-нибудь акцепторную молекулу этой молекуле сообщается энергия
- 14.14. АТР используется для обеспечения энергией мышечного сокращения
- 14.15. Креатинфосфат в мышцах выполняет роль резервуара высокоэнергетических фосфатных групп
- 14.17. АТР может расщепляться также до АМР и пирофосфата
- 14.18. Помимо АТР есть и другие высокоэнергетические нуклеотид-5-трифосфаты
- 14.19. Система АТР функционирует в стационарно-динамическом режиме
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 15. ГЛИКОЛИЗ-ЦЕНТРАЛЬНЫЙ ПУТЬ КАТАБОЛИЗМА ГЛЮКОЗЫ
- 15.1. Гликолиз является одним из центральных метаболических путей у большинства организмов
- 15.2. С гликолизом сопряжен синтез АТР
- 15.3. В продуктах гликолиза сохраняется еще много свободной энергии
- 15.4. Гликолиз включает две стадии
- 15.5. В ходе гликолиза образуются фосфорилированные промежуточные продукты
- 15.6. Первая сталия гликолиза завершается расщеплением углеродного скелета глюкозы
- 15.7. На второй стадии гликолиза запасается энергия
- 15.8. Пути, ведущие от гликогена и других углеводов, к центральному гликолитическому пути
- 15.9. В гликолиз могут вовлекаться и другие простые сахара
- 15.10. Дисахариды должны предварительно подвергнуться гидролизу то моносахаридов
- 15.11. Вовлечение остатков глюкозы в процесс гликолиза регулируется
- 15.12. Взаимопревращения фосфорилазы а и фосфорилазы b регулируются в конечном счете гормонами
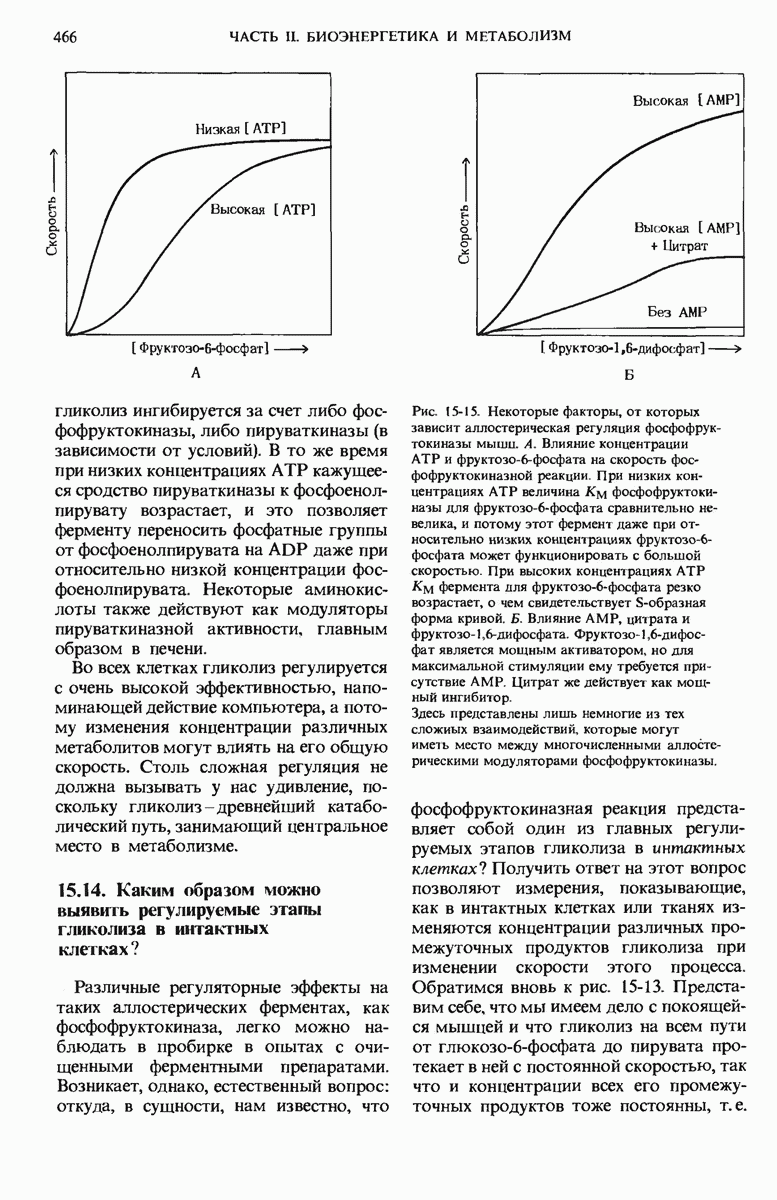
- 15.13. Сама последовательность гликолитических реакций регулируется на двух главных этапах
- 15.14. Каким образом можно выявить регулируемые этапы гликолиза в интактных клетках?
- 15.15. Спиртовое брожение отличается от гликолиза только на последних этапах
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 16. ЦИКЛ ЛИМОННОЙ КИСЛОТЫ
- 16.1. При окислении глюкозы до СО2 и Н2О высвобождается значительно больше энергии, чем при гликолизе
- 16.2. Пируват должен сначала окислиться до ацетил-СоА и СО2
- 16.3. Цикл лимонной кислоты — это не линейный, а замкнутый путь
- 16.4. Как родилась сама мысль о существовании цикла лимонной кислоты?
- 16.5. Цикл лимонной кислоты включает восемь стадий
- 16.6. Общая характеристика цикла
- 16.7. В чем смысл цикла лимонной кислоты?
- 16.8. Применение изотопных методов в изучении цикла лимонной кислоты
- 16.9. Превращение пирувата в ацетил-СоА регулируется
- 16.10. Цикл лимонной кислоты регулируется
- 16.11. Промежуточные продукты цикла лимонной кислоты используются также и в других метаболических реакциях, а убыль их постоянно восполняется
- 16.12. Глиоксилатный цикл — одна из модификаций цикла лимонной кислоты
- 16.13. Вторичные пути катаболизма глюкозы: пентозофосфатный путь
- 16.14. Вторичный путь, по которому происходит превращение глюкозы в глюкуроновую и аскорбиновую кислоты
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 17. ПЕРЕНОС ЭЛЕКТРОНОВ, ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И РЕГУЛЯЦИЯ СИНТЕЗА АТР
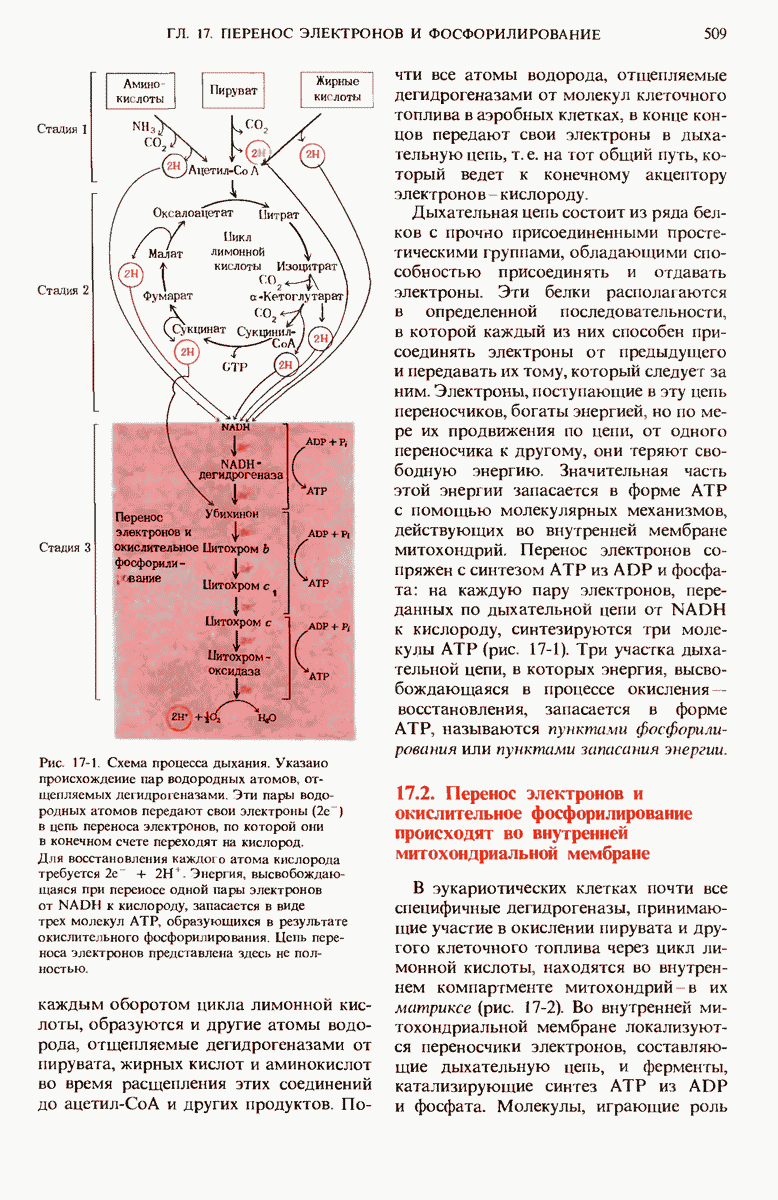
- 17.1. Перенос электронов от субстратов на кислород служит источником энергии АТР
- 17.2. Перенос электронов и окислительное фосфорилирование происходят во внутренней митохондриальной мембране
- 17.3. Реакции переноса электронов — это окислительновосстановительные реакции
- 17.4. Каждая сопряженная окислительно-восстановительная пара характеризуется определенным стандартным потенциалом
- 17.5. Перенос электронов сопровождается изменениями свободной энергии
- 17.6. Цепь переноса электронов включает большое число переносчиков
- 17.7. Пиридиновые нуклеотиды выполняют коллекторную функцию
- 17.8. NАDH-дегидpoгеназа принимает электроны от NADH
- 17.9. Убихинон представляет собой жирорастворимый хинон
- 17.10. Цитохромы — это гемопротеины, осуществляющие перенос электронов
- 17.11. Неполное восстановление кислорода ведет к повреждению клеток
- 17.12. Переносчики электронов действуют всегда в определенной последовательности
- 17.13. Энергия, выделяемая при переносе электронов, запасается в результате окислительного фосфорилирования
- 17.14. Фермент, катализирующий синтез АТР, был выделен и реконструирован
- 17.15. Каким образом окислительно-восстановительная энергия переноса электронов передается АТР-синтетазе?
- 17.16. Согласно хемиосмотической гипотезе энергия переноса электронов передается на синтез АТР через протонный градиент
- 17.17. Энергия переноса электронов используется и для других целей
- 17.18. В бактериальных клетках и в хлоропластах также имеются цепи переноса электронов, транспортирующие ионы
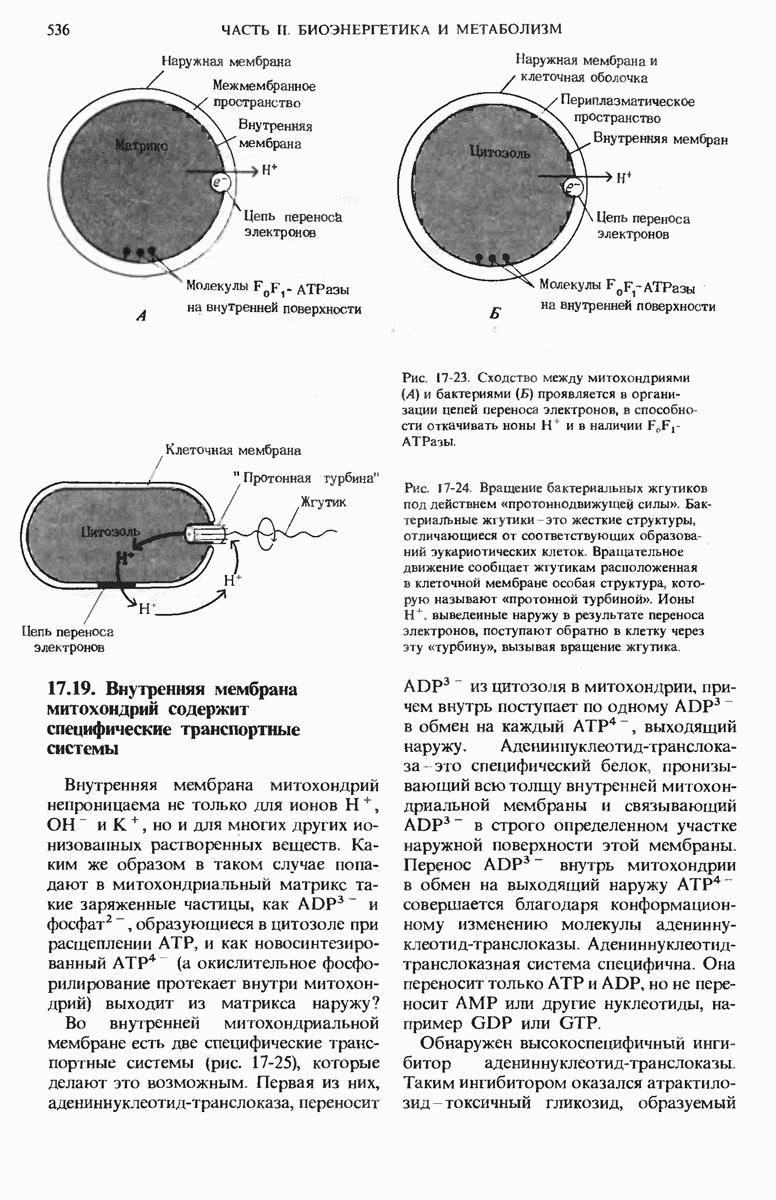
- 17.19. Внутренняя мембрана митохондрий содержит специфические транспортные системы
- 17.20. В окислении внемитохондриального NADH участвуют челночные системы
- 17.21. При полном окислении молекулы глюкозы образуется 38 молекул АТР
- 17.22. Образование АТР путем окислительного фосфорилирования регулируется в соответствии с энергетическими нуждами клетки
- 17.23. Энергетический заряд служит еще одним показателем энергетического состояния клеток
- 17.24. Регуляторные механизмы гликолиза, цикла лимонной кислоты и окислительного фосфорилирования взаимосвязаны
- 17.25. В клетках имеются и другие ферменты, использующие в качестве акцептора электронов кислород
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 18. ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ В ТКАНЯХ ЖИВОТНЫХ
- 18.1. Жирные кислоты активируются и окисляются в митохондриях
- 18.2. Процесс поступления жирных кислот в митохондрии состоит из трех этапов
- 18.3. Окисление жирных кислот включает две сталии
- 18.4. Первая стадия окисления насыщенных жирных кислот состоит из четырех этапов
- 18.5. На первой стадии окисления жирных кислот образуются ацетил-СоА и АТР
- 18.7. Окисление ненасыщенных жирных кислот требует двух дополнительных ферментативных этапов
- 18.8. Окисление жирных кислот с нечетным числом атомов углерода
- 18.9. Гипоглицин (токсичное вещество, вырабатываемое некоторыми растениями) подавляет окисление жирных кислот
- 18.10. Образование кетоновых тел в печени и их окисление в других органах
- 18.11. Регуляция окисления жирных кислот и образования кетоновых тел
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 19. ОКИСЛИТЕЛЬНОЕ РАСЩЕПЛЕНИЕ АМИНОКИСЛОТ. ЦИКЛ МОЧЕВИНЫ
- 19.1. Перенос а-аминогрупп катализируется трансаминазами
- 19.2. Аммиак образуется из глутамата
- 19.3. Существует 20 различных путей для расщепления углеродных скелетов аминокислот
- 19.4. Десять аминокислот превращаются в результате расщепления в ацетил-СоА
- 19.5. Наследственные нарушения катаболизма фенилаланина
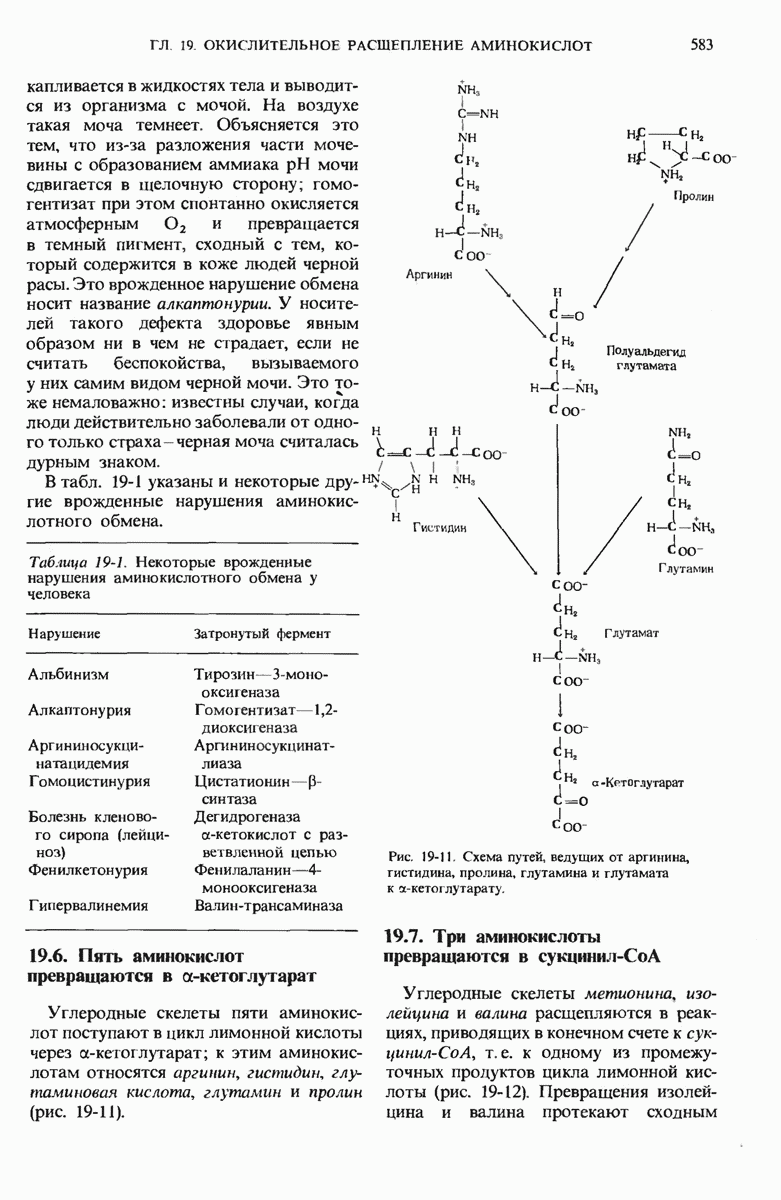
- 19.6. Пять аминокислот превращаются в а-кетоглутарат
- 19.7. Три аминокислоты превращаются в сукцинил-СоА
- 19.8. Из фенилаланина и тирозина образуется фумарат
- 19.9. Оксалоацетатный путь
- 19.10. Некоторые аминокислоты могут превращаться в глюкозу, а другие — в кетоновые тела
- 19.11. Аммиак для животных токсичен
- 19.12. Аммиак переносится в печень из многих периферических тканей в виде глутамина
- 19.13. Аммиак переносится из мышц в печень в виде аланина
- 19.14. Выведение аминиого азота из организма составляет еще одну сложную биохимическую проблему
- 19.15. В выделении аммиака участвует глутаминаза
- 19.16. Мочевина образуется в цикле мочевины
- 19.17. Цикл мочевины включает ряд сложных стадий
- 19.18. Энергетическая цена синтеза мочевины
- 19.19. Генетические дефекты, затрагивающие цикл мочевины, вызывают накопление аммиака в крови
- 19.20. У птиц, змей и ящериц из организма выводится мочевая кислота
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 20. БИОСИНТЕЗ УГЛЕВОДОВ В ЖИВОТНЫХ ТКАНЯХ
- 20.1. Путь глюконеогенеза включает семь этапов, общих с процессом гликолиза
- 20.2. Обходный путь требуется для превращения пирувата в фосфоенолпируват
- 20.3. Второй обходный путь в глюконеогенезе — это превращение фруктозо-1,6-дифосфата во фруктозо-6-фосфат
- 20.4. Третий обходный путь — это путь, ведущий от глюкозо-6-фосфата к свободной глюкозе
- 20.5. Глюконеогенез требует значительных затрат энергии
- 20.6. Реципрокная регуляция глюконеогенеза и гликолиза
- 20.7. Промежуточные продукты цикла лимонной кислоты являются также предшественниками глюкозы
- 20.8. Большинство аминокислот относится к глюкогенным
- 20.9. Глюконеогенез происходит в период восстановления после мышечной работы
- 20.10. Особенно активный глюконеогенез свойствен жвачным животным
- 20.11. Алкоголь тормозит глюконеогенез
- 20.12. «Холостые» циклы в углеводном обмене
- 20.13. Путь биосинтеза гликогена отличается от пути его расщепления
- 20.14. Гликоген-синтаза и гликоген-фосфорилаза регулируются реципрокно
- 20.15. Существуют генетические болезни, при которых обмен гликогена нарушен
- 20.16. Синтез лактозы регулируется особым образом
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 21. БИОСИНТЕЗ ЛИПИДОВ
- 21.1. Путь биосинтеза жирных кислот отличается от пути их окисления
- 21.2. Малонил-СоА образуется из ацетил-СоА
- 21.3. Синтазная система, катализирующая образование жирных кислот, имеет семь активных центров
- 21.4. Сульфгидрильные группы синтазы жирных кислот вначале взаимодействуют с ацильными группами
- 21.5. Присоединение каждого двухуглеродного фрагмента происходит в четыре этапа
- 21.6. Пальмитиновая кислота служит предшественником других длннноцепочечных жирных кислот
- 21.7. Регуляция биосинтеза жирных кислот
- 21.8. Биосинтез триацилглицеролов и глицеролфосфатидов начинается с общих предшественников
- 21.9. Биосинтез триацилглицеролов регулируется гормонами
- 21.10. Триацилглицеролы — источник энергии для некоторых впадающих в спячку животных
- 21.11. Для биосинтеза фосфоглицеролов нужны группы, образующие головы молекул
- 21.12. Фосфатидилхолин образуется двумя разными путями
- 21.13. Полярные липиды встраиваются в клеточные мембраны
- 21.14. Генетические дефекты липидного обмена
- 21.15. Существуют многочисленные лизосомные болезни
- 21.16. Холестерол и другие стероиды также синтезируются из двухуглеродных предшественников
- 21.17. И зопентенилпирофосфат служит предшественником многих жирорастворимых биомолекул
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 22. БИОСИНТЕЗ АМИНОКИСЛОТ И НУКЛЕОТИДОВ
- 22.1. Некоторые аминокислоты должны поступать в организм с пищей
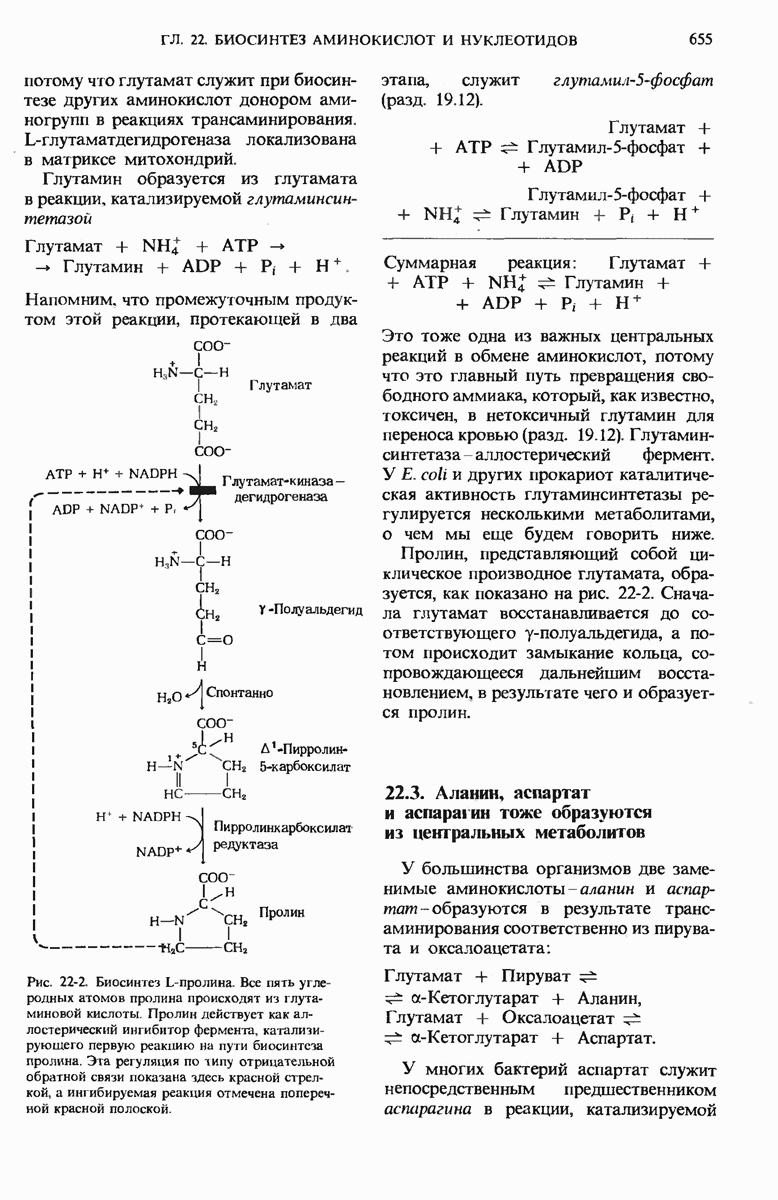
- 22.2. К глутамату, глутамину и пролину ведет общий биосинтетический путь
- 22.3. Аланин, аспартат и аспарагин тоже образуются из центральных метаболитов
- 22.4. Тирозин образуется из незаменимой аминокислоты фенилаланина
- 22.5. Цистеин образуется из двух других аминокислот — метионина и серина
- 22.6. Серии служиг предшественником глицина
- 22.7. Биосинтез незаменимых аминокислот
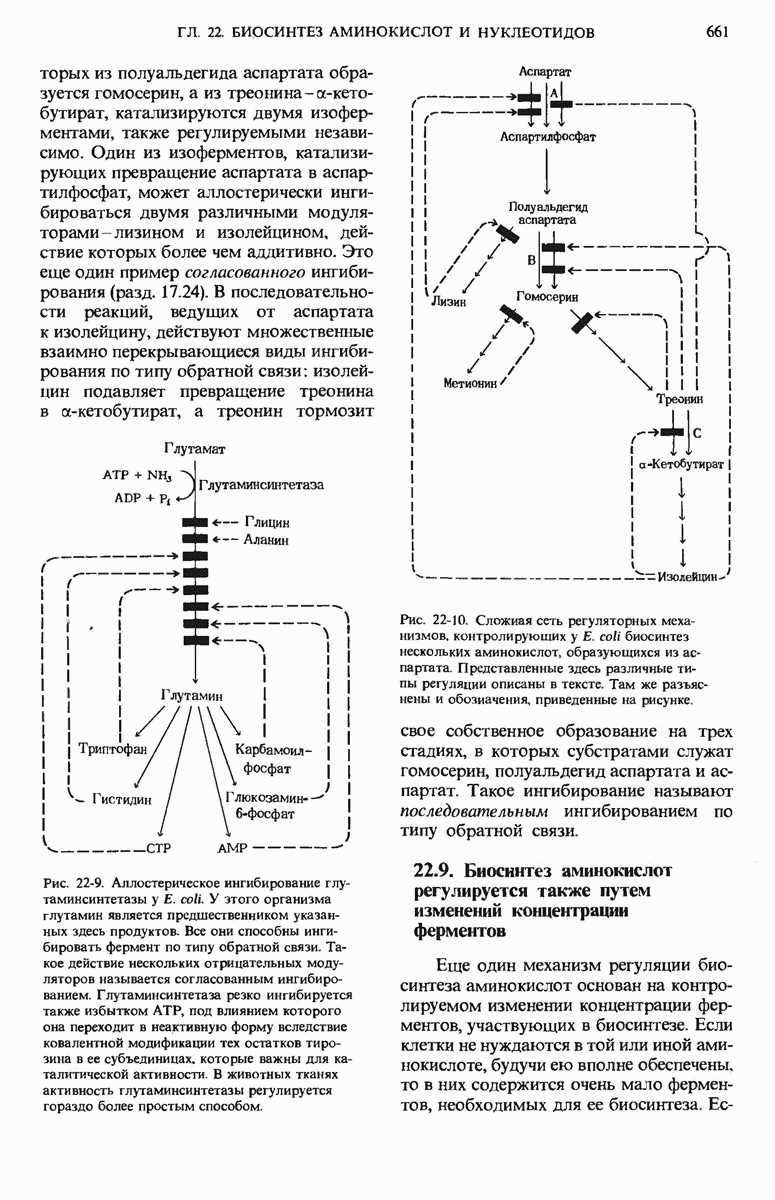
- 22.8. Биосинтез аминокислот регулируется аллостерическими механизмами
- 22.9. Биосинтез аминокислот регулируется также путем изменений концентрации ферментов
- 22.10. Глицин является предшественником порфиринов
- 22.11. При некоторых генетических заболеваниях накапливаются производные порфиринов
- 22.12. В результате распада гемогрупп образуются желчные пигменты
- 22.13. Пуриновые нуклеотиды синтезируются сложным путем
- 22.14. Биосинтез пуриновых нуклеотидов регулируется по типу обратной связи
- 22.15. Пиримидиновые нуклеотиды синтезируются из аспартата и рибозофосфата
- 22.16. Регуляция биосинтеза пиримидиновых нуклеотидов
- 22.17. Рибонуклеотиды служат предшественниками дезоксирибонуклеотидов
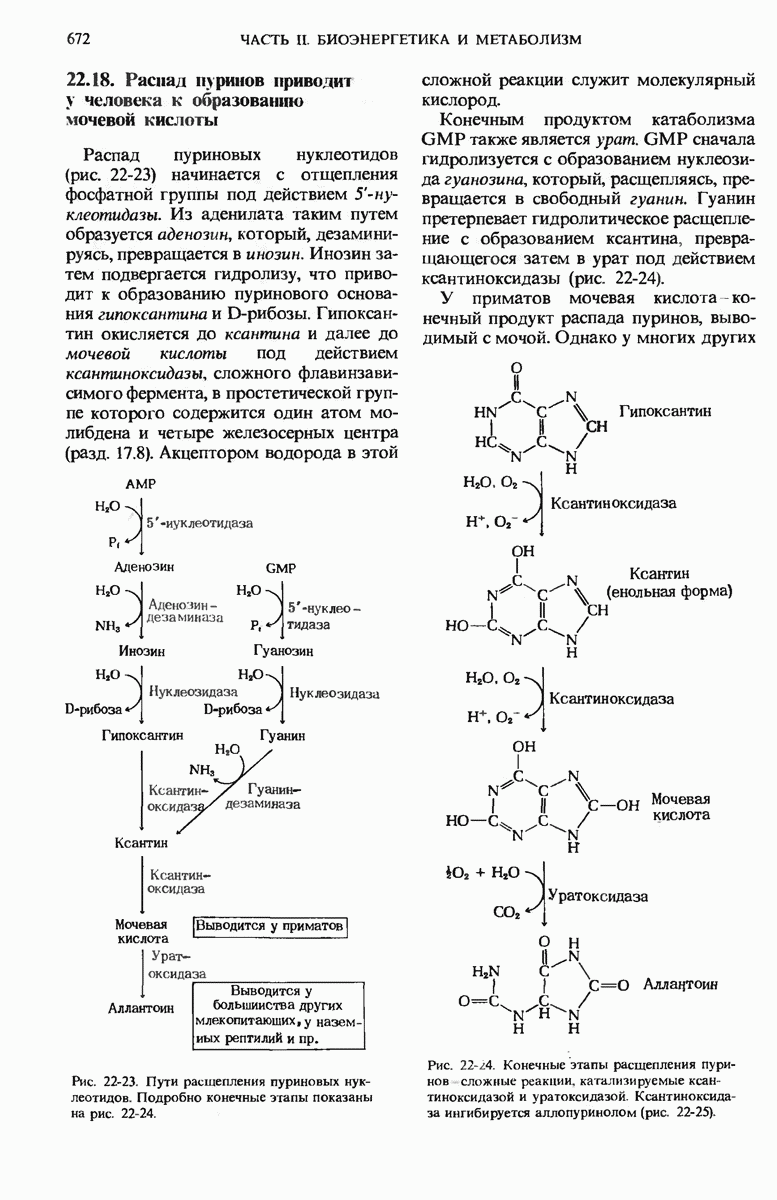
- 22.18. Распад пуринов приводит у человека к образованию мочевой кислоты
- 22.19. Реутилизация пуриновых оснований
- 22.20. Избыточное образование мочевой кислоты вызывает подагру
- 22.21. Круговорот азота
- 22.22. Способность фиксировать атмосферный азот присуща немногим организмам
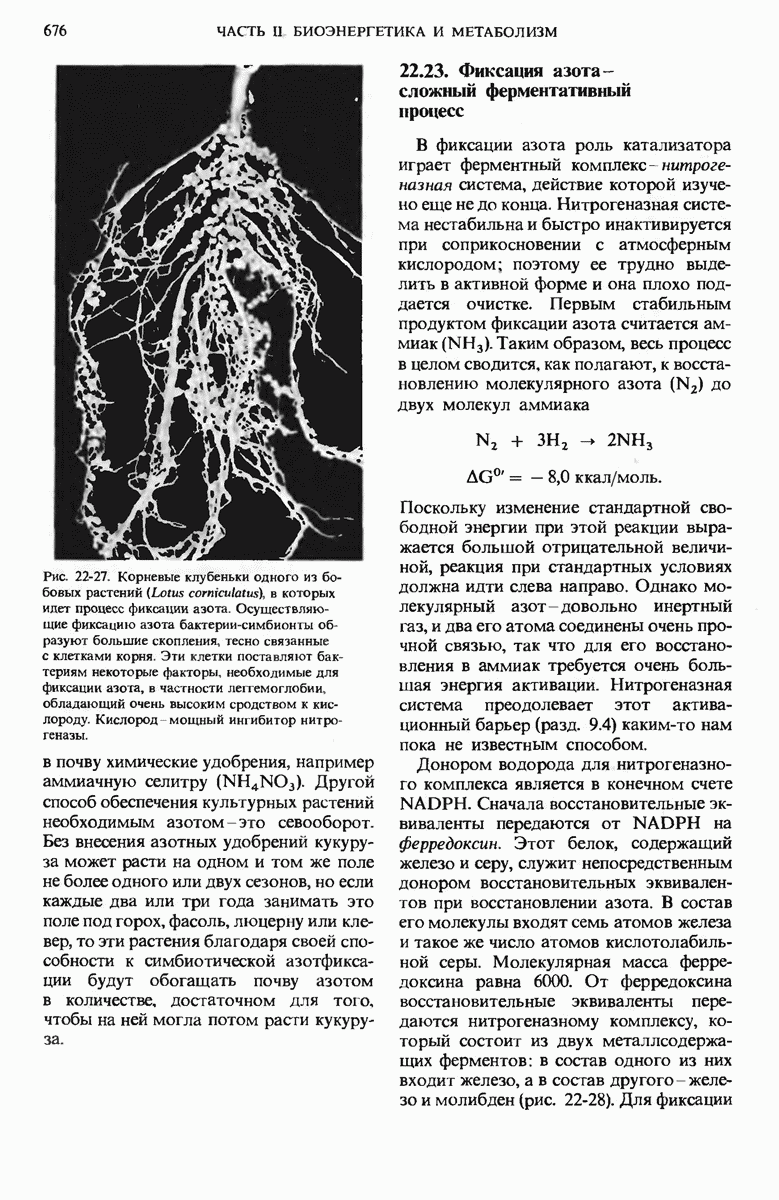
- 22.23. Фиксация азота — сложный ферментативный процесс
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 23. ФОТОСИНТЕЗ
- 23.1. О том, как было выведено уравнение фотосинтеза
- 23.2. Фотосинтезирующие организмы чрезвычайно разнообразны
- 23.3. Доноры водорода у разных фотосинтезирующих организмов различны
- 23.4. Процесс фотосинтеза состоит из двух фаз — световой и темновой
- 23.5. Фотосинтез растений протекает в хлоропластах
- 23.6. Поглощение света переводит молекулы в возбужденное состояние
- 23.7. Хлорофиллы — это главные светопоглощающие пигменты
- 23.8. В тилакоидах содержатся также вспомогательные пигменты
- 23.9. В мембранах тилакоидов содержатся два типа фотохимических реакционных систем
- 23.10. Свет индуцирует в хлоропластах поток электронов
- 23.11. Улавливаемам световая энергия создает поток электронов, направленный «вверх»
- 23.12. Перенос электронов от H2O к NADP+ происходит в результате взаимодействия фотосистем I и II
- 23.13. Z-схема представляет фотосинтетический перенос электронов в виде энергетической диаграммы
- 23.14. В фотосинтетическом переносе электронов принимает участие ряд переносчиков
- 23.15. Фосфорилирование ADP сопряжено с фотосинтетическим переносом электронов
- 23.16. В хлоропластах возможен также циклический поток электронов и циклическое фотофосфорилирование
- 23.17. Фотосинтетическое фосфорилирование сходно с окислительным фосфорилированием
- 23.18. Общее уравнение фотосинтеза растений
- 23.19. Фотосинтетическое образование гексоз связано с реальным восстановлением двуокиси углерода
- 23.20. Двуокись углерода фиксируется в форме фосфоглицерата
- 23.21. Глюкоза образуется из СО2 в цикле Кальвина
- 23.22. Глюкоза служит предшественником типичных растительных углеводов — сахарозы, крахмала и целлюлозы
- 23.23. Регуляция темновых реакций
- 23.24. В тропических растениях используется С4-путь, или путь Хэтча-Слэка
- 23.25. С4-путь обеспечивает необходимую концентрацию СО2
- 23.26. Фотодыхание ограничивает продуктивность С3-растений
- 23.27. Фотодыхание серьезная проблема для земледелия умеренной зоны
- 23.28. Галофильные бактерии используют световую энергию для синтеза АТР
- 23.29. Фотосинтезирующие организмы служат моделями для конструирования солнечных батарей
- Краткое содержание главы
- Вопросы и задачи
- Приложение. Ответы