| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
17.7. Пиридиновые нуклеотиды выполняют коллекторную функцию
Большинство электронных пар поступает в дыхательную цепь благодаря действию дегидрогеназ, использующих в качестве акцепторов электронов коферменты  или
или  (рис. 17-6). Всю эту группу в целом называют
(рис. 17-6). Всю эту группу в целом называют  ависимыми дегидрогеназами.
ависимыми дегидрогеназами.

Рис. 17-5. Полный набор переносчиков электронов, входящих в состав дыхательной цепи.
На участке 1 имеется не менее пяти различных железо-серных центров. Участок 2 включает две разные формы цитохрома b (с разными максимумами поглощения) и один железо-серный центр, отличный от тех, какие имеются на участке 1. Участок 3 содержит в дополнение к цитохромам  еще и два иона меди. Ни точной последовательности, ни функции всех этих окислительно-восстановительных центров мы пока еще не знаем.
еще и два иона меди. Ни точной последовательности, ни функции всех этих окислительно-восстановительных центров мы пока еще не знаем.
Мы уже встречались с отдельными ее представителями, когда рассматривали процесс гликолиза и цикл лимонной кислоты. Существует, однако, еще и много других. Некоторые биологически важные реакции, катализируемые такими дегидрогеназами, приведены в табл. 17-2.
Дегидрогеназы катализируют обратимые реакции, которые в общем виде могут быть записаны следующим образом:

Подавляющее большинство таких дегидрогеназ содержит NAD+ (табл. 17-2). У некоторых, как, например, у глюкозо-6-фосфатдегидрогеназы (разд. 16.13), акцептором электронов служит NADP+ . И лишь совсем немногие такие, как глутаматдегидрогеназа, способны взаимодействовать как с NAD+ , так и с NADP (табл. 17-2). Часть пиридинзависимых дегидрогеназ локализована в цитозоле, часть в митохондриях, а некоторые присутствуют и здесь, и там. Дегидрогеназы цитозоля способны взаимодействовать только с теми пиридиновыми нуклеотидами, которые находятся в цитозоле; сходным образом обстоит дело и с митохондриальными дегидрогеназами - обычно они взаимодействуют только с пиридиновыми нуклеотидами матрикса митохондрий.


Рис. 17-6. Никотинамидадениндинуклеотид (NAD) и ннкотинамидадениндинуклеотидфосфат (NADP). А. Окисленные формы (NAD+ и NADP). Никотинамид (на красном фоне) представляет собой один из витаминов группы В (разд. 10.6); это та часть молекулы NAD, которая принимает участие в переносе электронов. Б Восстановление никотинамидного кольца NAD+ субстратом. Два восстановительных эквивалента переносятся от субстрата (обозначенного здесь  ) на NAD+ в форме гидрид-иона
) на NAD+ в форме гидрид-иона  . Второй водородный атом, отщепляемый от субстрата, превращается в ион
. Второй водородный атом, отщепляемый от субстрата, превращается в ион  .
.
Цитозольный и митохондриальный пулы NAD и NADP отделены друг от друга митохондриальной мембраной, которая для этих коферментов непроницаема. Мы еще вернемся к этому вопросу.
Среди NAD-зависимых дегидрогеназ, участвующих в углеводном обмене, главную роль играют глицералъдегидфосфатдегидрогеназа и лактатдегидрогеназа гликолитической системы, локализующиеся в цитозоле, а также пируватдегидрогеназа, находящаяся в митохондриях (табл. 17-2). Три NAD-зависимые дегидрогеназы участвуют в митохондриях в цикле лимонной кислоты: изоцитрат-дегидрогепаза,  -кетоглутаратдегидроге-наза и малатдегидрогеназа.
-кетоглутаратдегидроге-наза и малатдегидрогеназа.
Таблица 17-2. Некоторые важные реакции, катализируемые NAD(P)-зависимыми дегидрогеназами

К числу других важных митохондриальных дегидрогеназ относятся: 3-гидроксиацил-СоА-дегидрогенаэа, участвующая в цикле окисления жирных кислот,  -гидроксибути-ратдегидрогеназа (гл. 18) и глутаматдегидрогепаза, функция которой связана с катаболизмом аминокислот (гл. 19).
-гидроксибути-ратдегидрогеназа (гл. 18) и глутаматдегидрогепаза, функция которой связана с катаболизмом аминокислот (гл. 19).
Пиридинзависимые дегидрогеназы отщепляют от своих субстратов по два водородных атома. Один из них в виде гидрид-иона  переносится на NAD + или NADP+ , а второй в виде иона
переносится на NAD + или NADP+ , а второй в виде иона  переходит в среду. Каждый гидрид-ион несет два восстановительных эквивалента; один из них в форме водородного атома присоединяется к четвертому углеродному атому никотинамидного кольца, а второй в виде элек грона передается азоту этого кольца (рис. 17-6).
переходит в среду. Каждый гидрид-ион несет два восстановительных эквивалента; один из них в форме водородного атома присоединяется к четвертому углеродному атому никотинамидного кольца, а второй в виде элек грона передается азоту этого кольца (рис. 17-6).
Поскольку большая часть клеточных дегидрогеназ переносит водородные атомы от субстратов на NAD+, можно сказать, что эгот кофермент выполняет коллекторную функцию - собирает пары восстановительных эквивалентов, поступающие от разных субстратов, в одной молекулярной форме, в форме NADH (рис. 17-7). В конечном счете NAD может собирать в этой форме также и восстановительные эквиваленты от субстратов, на которые действуют NADP-зависимые дегидрогеназы. Это оказывается возможным благодаря действию пиридининуклеотид-тринсгидрогеназы - сложного фермента, катализирующего реакцию

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
- ГЛАВА 13. МЕТАБОЛИЗМ. ОБЩИЙ ОБЗОР
- 13.1. Живые организмы принимают участие в круговороте углерода и кислорода
- 13.2. В биосфере существует круговорот азота
- 13.3. Метаболические пути представляют собой последовательности реакций, катализируемых мультиферментными системами
- 13.4. Метаболизм включает катаболические и анаболические пути (процессы распада и процессы синтеза)
- 13.5. Катаболические пути сходятся — образуется лишь небольшое число конечных продуктов
- 13.6. Биосинтетические (анаболические) пути расходятся — образуется много разных продуктов
- 13.7. Соответствующие катаболические и анаболические пути различаются, и эти различия имеют важное значение.
- 13.8. Энергия перелается от катаболических реакций к анаболическим при помощи АТР
- 13.9. NADPH переносит энергию в форме восстановительной способности
- 13.10. Клеточный метаболизм — это экономичный, строго регулируемый лроцесс
- 13.11. Регуляция метаболических путей осуществляется на трех уровнях
- 13.12. Вторичный метаболизм
- 13.13. Метаболические пути могут быть идентифицированы в прямых опытах
- 13.14. Промежуточные стадии метаболизма можно выявлять с помощью мутантных организмов
- 13.15. Включение изотопной метки — весьма эффективный метод изучения метаболизма
- 13.16. Различные метаболические пути могут быть локализованы в разных участках клетки
- ЛИТЕРАТУРА
- ГЛАВА 14. ATP — ЦИКЛ И БИОЭНЕРГЕТИКА КЛЕТКИ
- 14.1. Первый и второй законы термодинамики
- 14.2. Клеткам необходима свободная энергия
- 14.3. Изменение стандартной свободной энергии химической реакции можно вычислить
- 14.4. Химические реакции характеризуются определенной величиной
- 14.5. Величины различаются, и это различие имеет важное значение
- 14.6. Изменения стандартной свободной энергии химических реакций аддитивны
- 14.8. Химические свойства АТР хорошо известны
- 14.9. Характерное значение, стандартной свободной энергии АТР
- 14.10. Почему стандартная свободная энергия гидролиза АТР относительно велика?
- 14.11. АТР служит общим промежуточным продуктом в реакциях переноса фосфатных групп
- 14.12. При расщеплении глюкозы до лактата образуются два сверхвысокоэнергетических фосфорилированных соединения
- 14.13. В результате переноса фосфатной группы от АТР на какую-нибудь акцепторную молекулу этой молекуле сообщается энергия
- 14.14. АТР используется для обеспечения энергией мышечного сокращения
- 14.15. Креатинфосфат в мышцах выполняет роль резервуара высокоэнергетических фосфатных групп
- 14.17. АТР может расщепляться также до АМР и пирофосфата
- 14.18. Помимо АТР есть и другие высокоэнергетические нуклеотид-5-трифосфаты
- 14.19. Система АТР функционирует в стационарно-динамическом режиме
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 15. ГЛИКОЛИЗ-ЦЕНТРАЛЬНЫЙ ПУТЬ КАТАБОЛИЗМА ГЛЮКОЗЫ
- 15.1. Гликолиз является одним из центральных метаболических путей у большинства организмов
- 15.2. С гликолизом сопряжен синтез АТР
- 15.3. В продуктах гликолиза сохраняется еще много свободной энергии
- 15.4. Гликолиз включает две стадии
- 15.5. В ходе гликолиза образуются фосфорилированные промежуточные продукты
- 15.6. Первая сталия гликолиза завершается расщеплением углеродного скелета глюкозы
- 15.7. На второй стадии гликолиза запасается энергия
- 15.8. Пути, ведущие от гликогена и других углеводов, к центральному гликолитическому пути
- 15.9. В гликолиз могут вовлекаться и другие простые сахара
- 15.10. Дисахариды должны предварительно подвергнуться гидролизу то моносахаридов
- 15.11. Вовлечение остатков глюкозы в процесс гликолиза регулируется
- 15.12. Взаимопревращения фосфорилазы а и фосфорилазы b регулируются в конечном счете гормонами
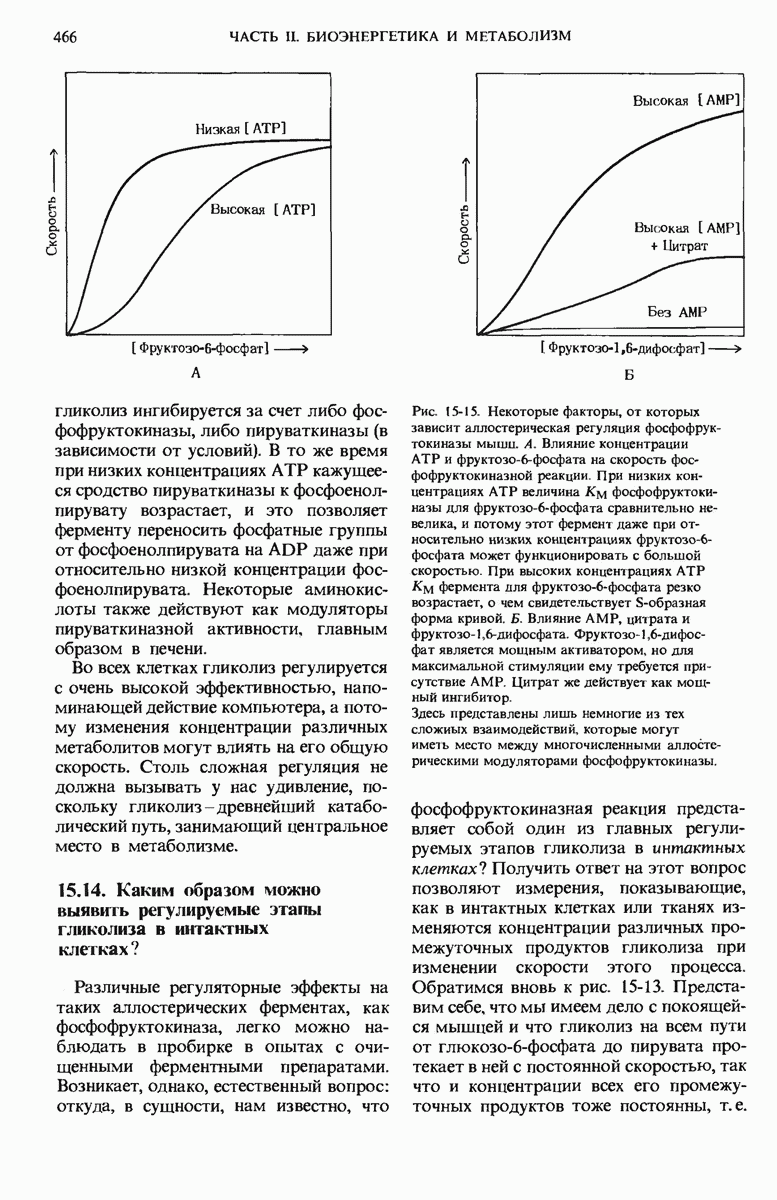
- 15.13. Сама последовательность гликолитических реакций регулируется на двух главных этапах
- 15.14. Каким образом можно выявить регулируемые этапы гликолиза в интактных клетках?
- 15.15. Спиртовое брожение отличается от гликолиза только на последних этапах
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 16. ЦИКЛ ЛИМОННОЙ КИСЛОТЫ
- 16.1. При окислении глюкозы до СО2 и Н2О высвобождается значительно больше энергии, чем при гликолизе
- 16.2. Пируват должен сначала окислиться до ацетил-СоА и СО2
- 16.3. Цикл лимонной кислоты — это не линейный, а замкнутый путь
- 16.4. Как родилась сама мысль о существовании цикла лимонной кислоты?
- 16.5. Цикл лимонной кислоты включает восемь стадий
- 16.6. Общая характеристика цикла
- 16.7. В чем смысл цикла лимонной кислоты?
- 16.8. Применение изотопных методов в изучении цикла лимонной кислоты
- 16.9. Превращение пирувата в ацетил-СоА регулируется
- 16.10. Цикл лимонной кислоты регулируется
- 16.11. Промежуточные продукты цикла лимонной кислоты используются также и в других метаболических реакциях, а убыль их постоянно восполняется
- 16.12. Глиоксилатный цикл — одна из модификаций цикла лимонной кислоты
- 16.13. Вторичные пути катаболизма глюкозы: пентозофосфатный путь
- 16.14. Вторичный путь, по которому происходит превращение глюкозы в глюкуроновую и аскорбиновую кислоты
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 17. ПЕРЕНОС ЭЛЕКТРОНОВ, ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И РЕГУЛЯЦИЯ СИНТЕЗА АТР
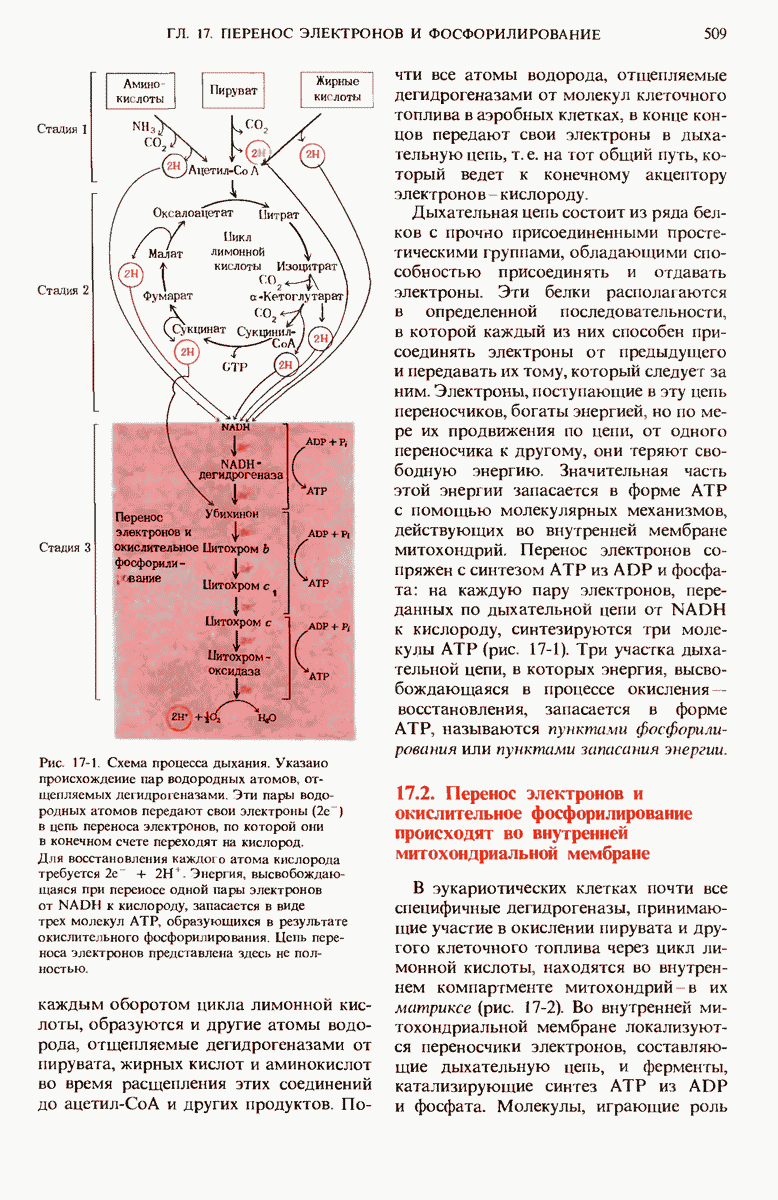
- 17.1. Перенос электронов от субстратов на кислород служит источником энергии АТР
- 17.2. Перенос электронов и окислительное фосфорилирование происходят во внутренней митохондриальной мембране
- 17.3. Реакции переноса электронов — это окислительновосстановительные реакции
- 17.4. Каждая сопряженная окислительно-восстановительная пара характеризуется определенным стандартным потенциалом
- 17.5. Перенос электронов сопровождается изменениями свободной энергии
- 17.6. Цепь переноса электронов включает большое число переносчиков
- 17.7. Пиридиновые нуклеотиды выполняют коллекторную функцию
- 17.8. NАDH-дегидpoгеназа принимает электроны от NADH
- 17.9. Убихинон представляет собой жирорастворимый хинон
- 17.10. Цитохромы — это гемопротеины, осуществляющие перенос электронов
- 17.11. Неполное восстановление кислорода ведет к повреждению клеток
- 17.12. Переносчики электронов действуют всегда в определенной последовательности
- 17.13. Энергия, выделяемая при переносе электронов, запасается в результате окислительного фосфорилирования
- 17.14. Фермент, катализирующий синтез АТР, был выделен и реконструирован
- 17.15. Каким образом окислительно-восстановительная энергия переноса электронов передается АТР-синтетазе?
- 17.16. Согласно хемиосмотической гипотезе энергия переноса электронов передается на синтез АТР через протонный градиент
- 17.17. Энергия переноса электронов используется и для других целей
- 17.18. В бактериальных клетках и в хлоропластах также имеются цепи переноса электронов, транспортирующие ионы
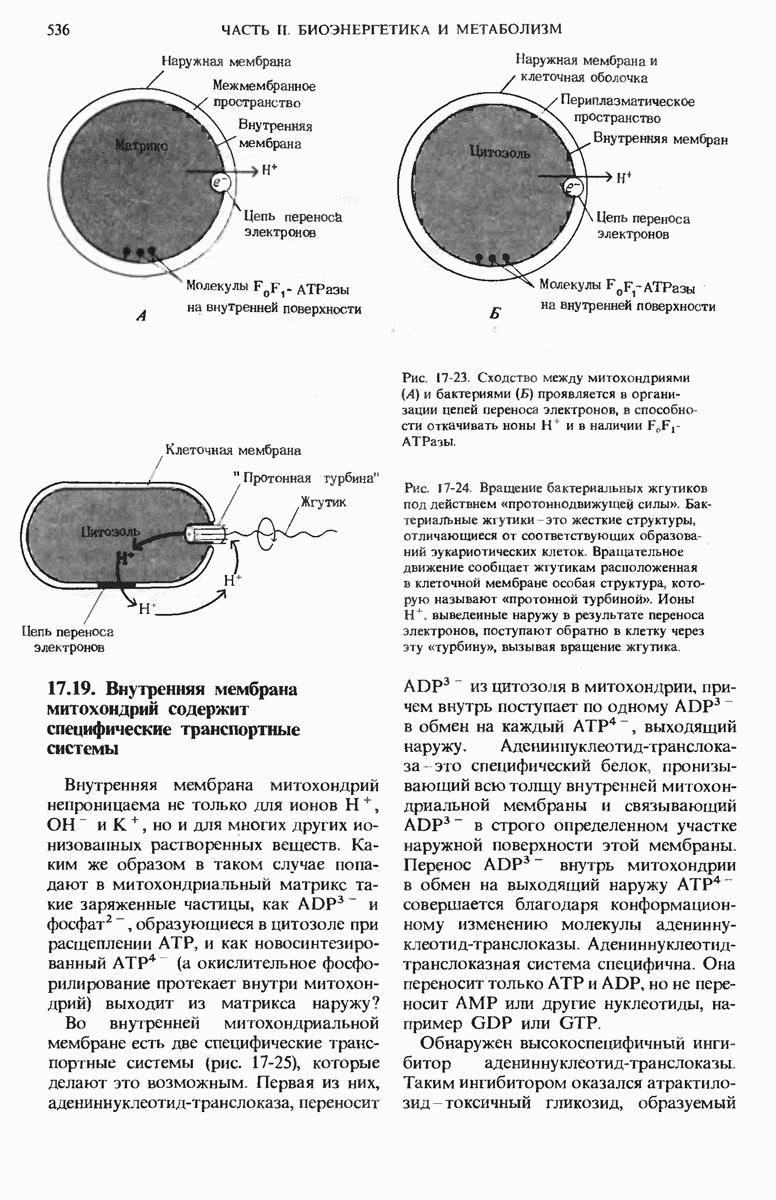
- 17.19. Внутренняя мембрана митохондрий содержит специфические транспортные системы
- 17.20. В окислении внемитохондриального NADH участвуют челночные системы
- 17.21. При полном окислении молекулы глюкозы образуется 38 молекул АТР
- 17.22. Образование АТР путем окислительного фосфорилирования регулируется в соответствии с энергетическими нуждами клетки
- 17.23. Энергетический заряд служит еще одним показателем энергетического состояния клеток
- 17.24. Регуляторные механизмы гликолиза, цикла лимонной кислоты и окислительного фосфорилирования взаимосвязаны
- 17.25. В клетках имеются и другие ферменты, использующие в качестве акцептора электронов кислород
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 18. ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ В ТКАНЯХ ЖИВОТНЫХ
- 18.1. Жирные кислоты активируются и окисляются в митохондриях
- 18.2. Процесс поступления жирных кислот в митохондрии состоит из трех этапов
- 18.3. Окисление жирных кислот включает две сталии
- 18.4. Первая стадия окисления насыщенных жирных кислот состоит из четырех этапов
- 18.5. На первой стадии окисления жирных кислот образуются ацетил-СоА и АТР
- 18.7. Окисление ненасыщенных жирных кислот требует двух дополнительных ферментативных этапов
- 18.8. Окисление жирных кислот с нечетным числом атомов углерода
- 18.9. Гипоглицин (токсичное вещество, вырабатываемое некоторыми растениями) подавляет окисление жирных кислот
- 18.10. Образование кетоновых тел в печени и их окисление в других органах
- 18.11. Регуляция окисления жирных кислот и образования кетоновых тел
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 19. ОКИСЛИТЕЛЬНОЕ РАСЩЕПЛЕНИЕ АМИНОКИСЛОТ. ЦИКЛ МОЧЕВИНЫ
- 19.1. Перенос а-аминогрупп катализируется трансаминазами
- 19.2. Аммиак образуется из глутамата
- 19.3. Существует 20 различных путей для расщепления углеродных скелетов аминокислот
- 19.4. Десять аминокислот превращаются в результате расщепления в ацетил-СоА
- 19.5. Наследственные нарушения катаболизма фенилаланина
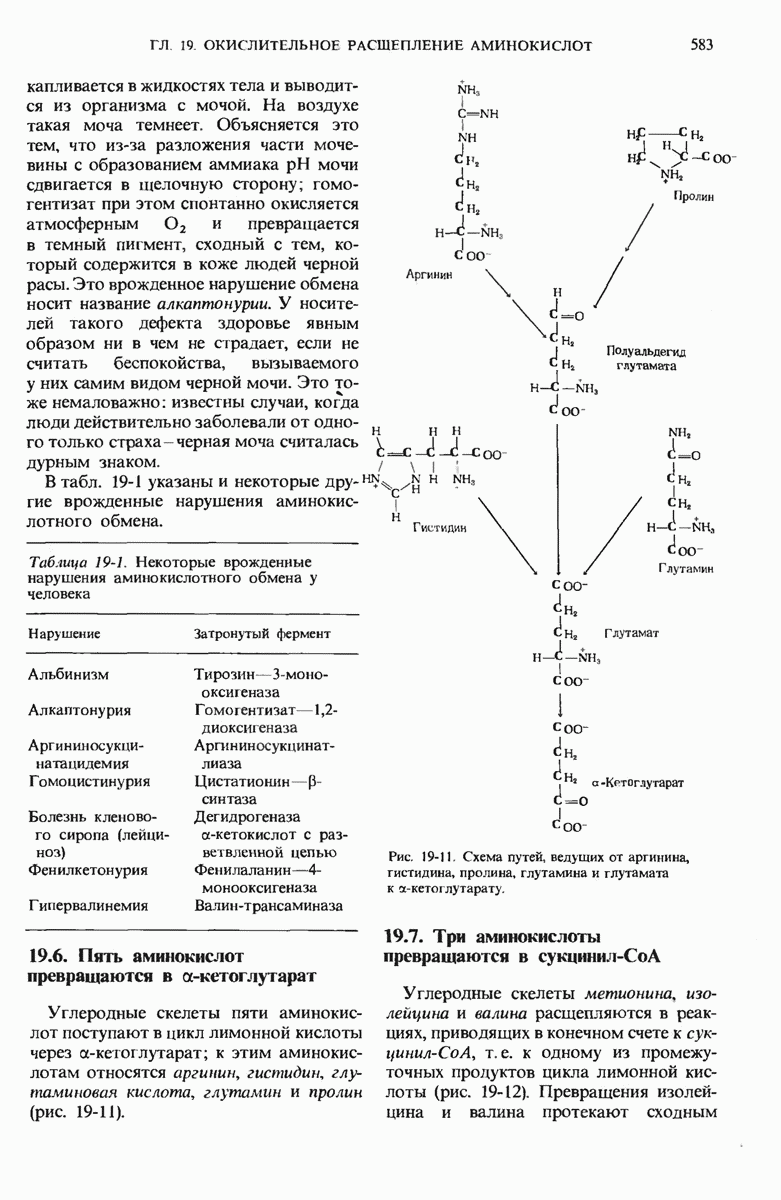
- 19.6. Пять аминокислот превращаются в а-кетоглутарат
- 19.7. Три аминокислоты превращаются в сукцинил-СоА
- 19.8. Из фенилаланина и тирозина образуется фумарат
- 19.9. Оксалоацетатный путь
- 19.10. Некоторые аминокислоты могут превращаться в глюкозу, а другие — в кетоновые тела
- 19.11. Аммиак для животных токсичен
- 19.12. Аммиак переносится в печень из многих периферических тканей в виде глутамина
- 19.13. Аммиак переносится из мышц в печень в виде аланина
- 19.14. Выведение аминиого азота из организма составляет еще одну сложную биохимическую проблему
- 19.15. В выделении аммиака участвует глутаминаза
- 19.16. Мочевина образуется в цикле мочевины
- 19.17. Цикл мочевины включает ряд сложных стадий
- 19.18. Энергетическая цена синтеза мочевины
- 19.19. Генетические дефекты, затрагивающие цикл мочевины, вызывают накопление аммиака в крови
- 19.20. У птиц, змей и ящериц из организма выводится мочевая кислота
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 20. БИОСИНТЕЗ УГЛЕВОДОВ В ЖИВОТНЫХ ТКАНЯХ
- 20.1. Путь глюконеогенеза включает семь этапов, общих с процессом гликолиза
- 20.2. Обходный путь требуется для превращения пирувата в фосфоенолпируват
- 20.3. Второй обходный путь в глюконеогенезе — это превращение фруктозо-1,6-дифосфата во фруктозо-6-фосфат
- 20.4. Третий обходный путь — это путь, ведущий от глюкозо-6-фосфата к свободной глюкозе
- 20.5. Глюконеогенез требует значительных затрат энергии
- 20.6. Реципрокная регуляция глюконеогенеза и гликолиза
- 20.7. Промежуточные продукты цикла лимонной кислоты являются также предшественниками глюкозы
- 20.8. Большинство аминокислот относится к глюкогенным
- 20.9. Глюконеогенез происходит в период восстановления после мышечной работы
- 20.10. Особенно активный глюконеогенез свойствен жвачным животным
- 20.11. Алкоголь тормозит глюконеогенез
- 20.12. «Холостые» циклы в углеводном обмене
- 20.13. Путь биосинтеза гликогена отличается от пути его расщепления
- 20.14. Гликоген-синтаза и гликоген-фосфорилаза регулируются реципрокно
- 20.15. Существуют генетические болезни, при которых обмен гликогена нарушен
- 20.16. Синтез лактозы регулируется особым образом
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 21. БИОСИНТЕЗ ЛИПИДОВ
- 21.1. Путь биосинтеза жирных кислот отличается от пути их окисления
- 21.2. Малонил-СоА образуется из ацетил-СоА
- 21.3. Синтазная система, катализирующая образование жирных кислот, имеет семь активных центров
- 21.4. Сульфгидрильные группы синтазы жирных кислот вначале взаимодействуют с ацильными группами
- 21.5. Присоединение каждого двухуглеродного фрагмента происходит в четыре этапа
- 21.6. Пальмитиновая кислота служит предшественником других длннноцепочечных жирных кислот
- 21.7. Регуляция биосинтеза жирных кислот
- 21.8. Биосинтез триацилглицеролов и глицеролфосфатидов начинается с общих предшественников
- 21.9. Биосинтез триацилглицеролов регулируется гормонами
- 21.10. Триацилглицеролы — источник энергии для некоторых впадающих в спячку животных
- 21.11. Для биосинтеза фосфоглицеролов нужны группы, образующие головы молекул
- 21.12. Фосфатидилхолин образуется двумя разными путями
- 21.13. Полярные липиды встраиваются в клеточные мембраны
- 21.14. Генетические дефекты липидного обмена
- 21.15. Существуют многочисленные лизосомные болезни
- 21.16. Холестерол и другие стероиды также синтезируются из двухуглеродных предшественников
- 21.17. И зопентенилпирофосфат служит предшественником многих жирорастворимых биомолекул
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 22. БИОСИНТЕЗ АМИНОКИСЛОТ И НУКЛЕОТИДОВ
- 22.1. Некоторые аминокислоты должны поступать в организм с пищей
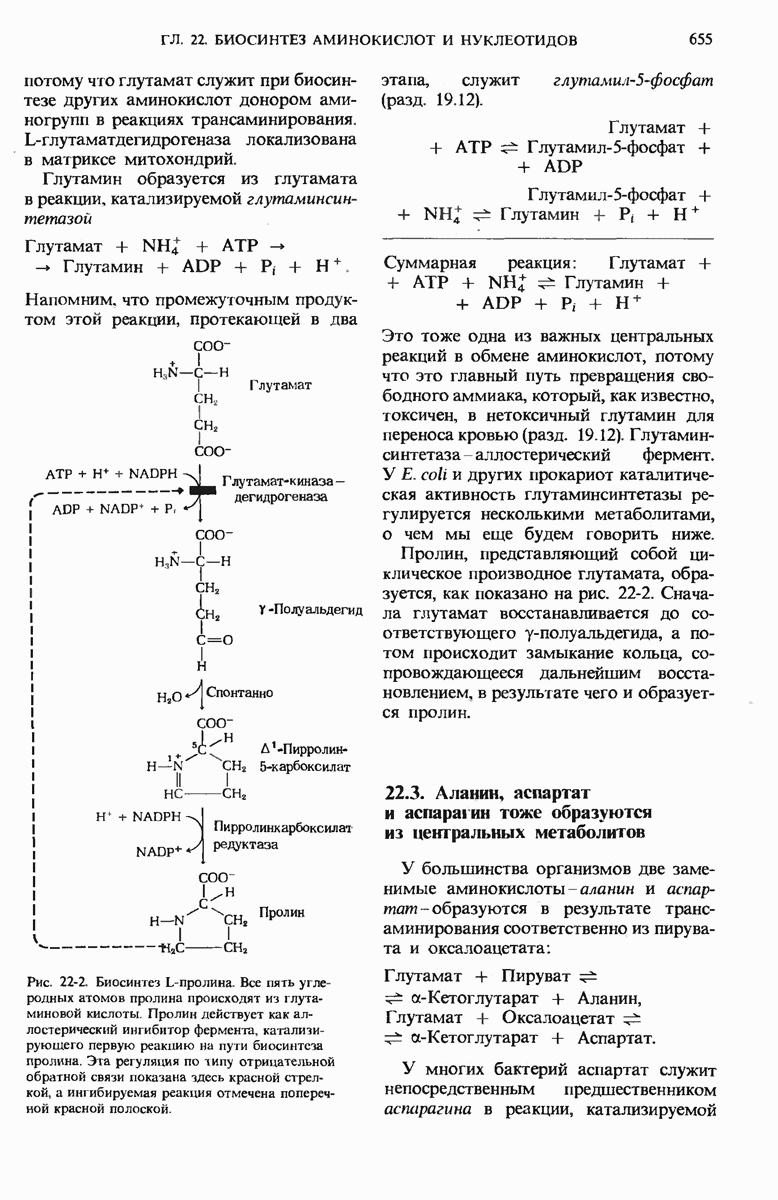
- 22.2. К глутамату, глутамину и пролину ведет общий биосинтетический путь
- 22.3. Аланин, аспартат и аспарагин тоже образуются из центральных метаболитов
- 22.4. Тирозин образуется из незаменимой аминокислоты фенилаланина
- 22.5. Цистеин образуется из двух других аминокислот — метионина и серина
- 22.6. Серии служиг предшественником глицина
- 22.7. Биосинтез незаменимых аминокислот
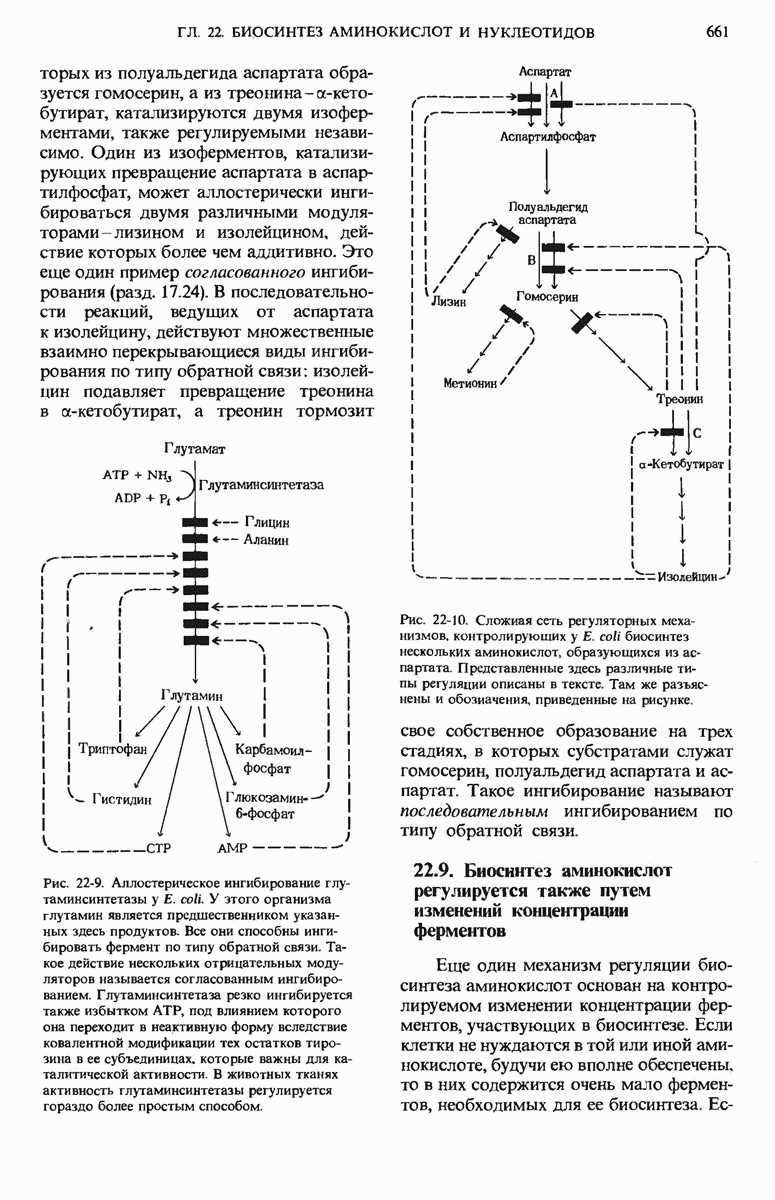
- 22.8. Биосинтез аминокислот регулируется аллостерическими механизмами
- 22.9. Биосинтез аминокислот регулируется также путем изменений концентрации ферментов
- 22.10. Глицин является предшественником порфиринов
- 22.11. При некоторых генетических заболеваниях накапливаются производные порфиринов
- 22.12. В результате распада гемогрупп образуются желчные пигменты
- 22.13. Пуриновые нуклеотиды синтезируются сложным путем
- 22.14. Биосинтез пуриновых нуклеотидов регулируется по типу обратной связи
- 22.15. Пиримидиновые нуклеотиды синтезируются из аспартата и рибозофосфата
- 22.16. Регуляция биосинтеза пиримидиновых нуклеотидов
- 22.17. Рибонуклеотиды служат предшественниками дезоксирибонуклеотидов
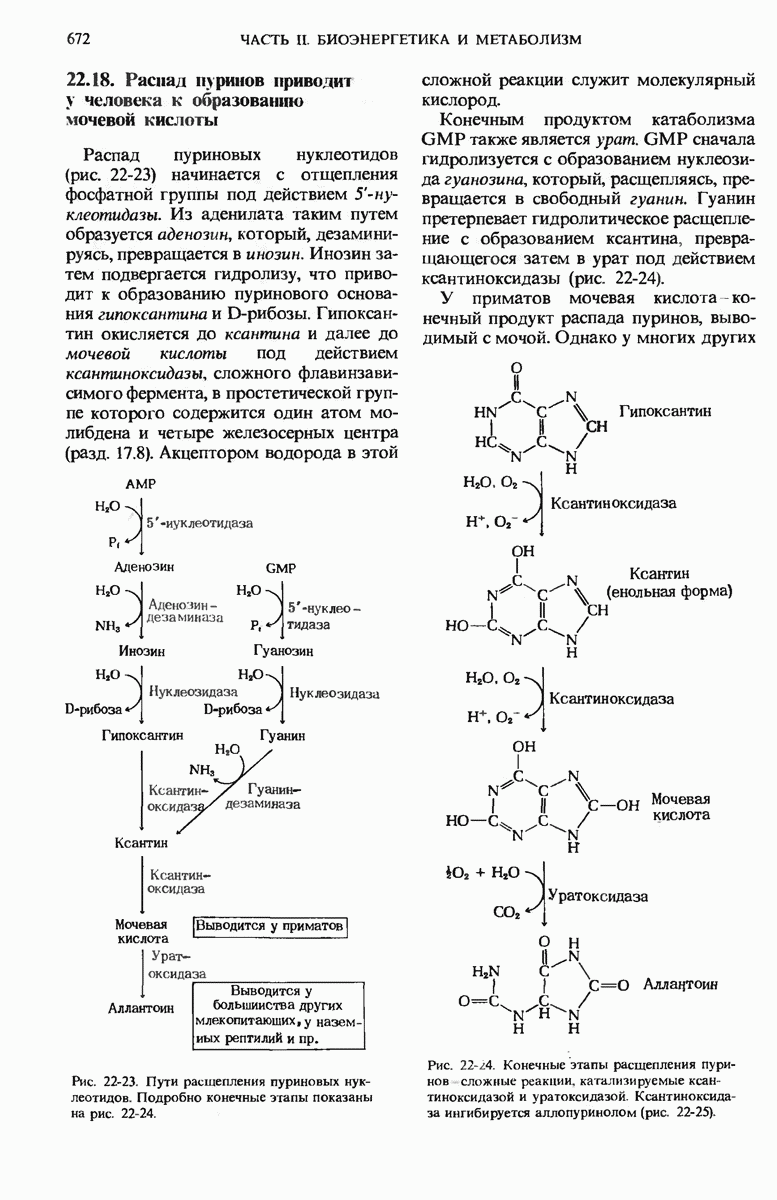
- 22.18. Распад пуринов приводит у человека к образованию мочевой кислоты
- 22.19. Реутилизация пуриновых оснований
- 22.20. Избыточное образование мочевой кислоты вызывает подагру
- 22.21. Круговорот азота
- 22.22. Способность фиксировать атмосферный азот присуща немногим организмам
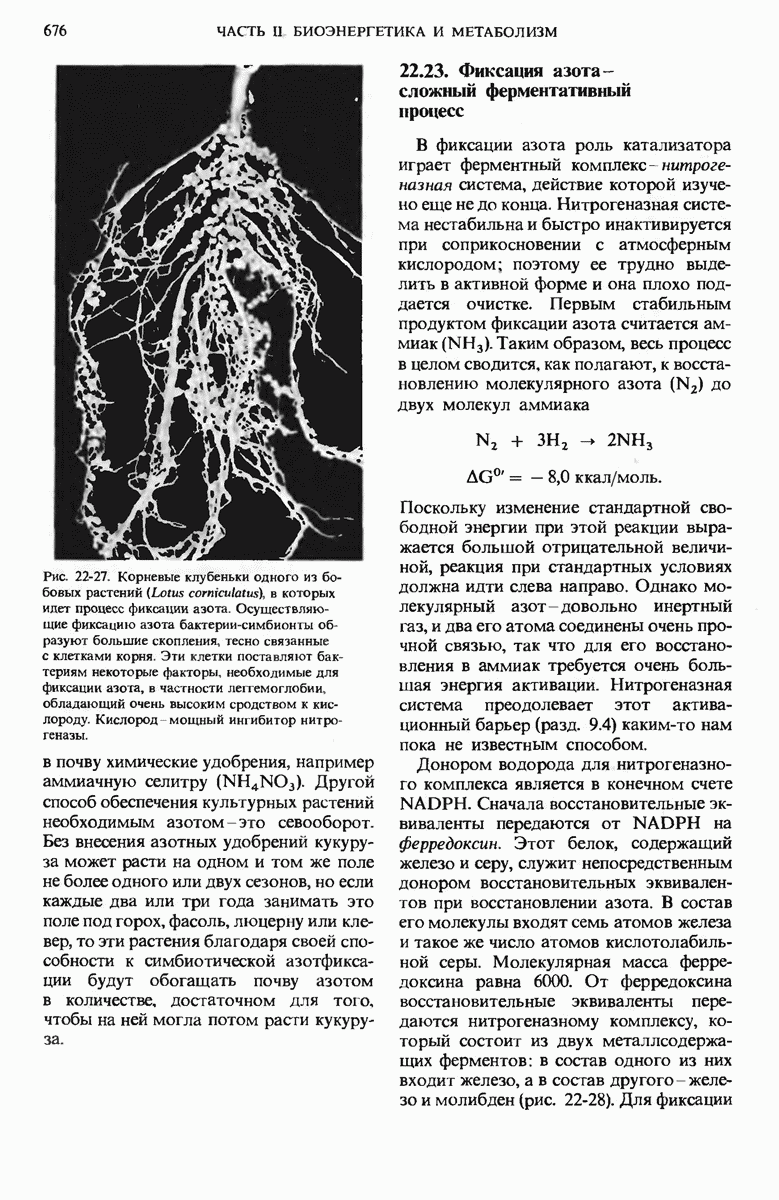
- 22.23. Фиксация азота — сложный ферментативный процесс
- Краткое содержание главы
- Вопросы и задачи
- ГЛАВА 23. ФОТОСИНТЕЗ
- 23.1. О том, как было выведено уравнение фотосинтеза
- 23.2. Фотосинтезирующие организмы чрезвычайно разнообразны
- 23.3. Доноры водорода у разных фотосинтезирующих организмов различны
- 23.4. Процесс фотосинтеза состоит из двух фаз — световой и темновой
- 23.5. Фотосинтез растений протекает в хлоропластах
- 23.6. Поглощение света переводит молекулы в возбужденное состояние
- 23.7. Хлорофиллы — это главные светопоглощающие пигменты
- 23.8. В тилакоидах содержатся также вспомогательные пигменты
- 23.9. В мембранах тилакоидов содержатся два типа фотохимических реакционных систем
- 23.10. Свет индуцирует в хлоропластах поток электронов
- 23.11. Улавливаемам световая энергия создает поток электронов, направленный «вверх»
- 23.12. Перенос электронов от H2O к NADP+ происходит в результате взаимодействия фотосистем I и II
- 23.13. Z-схема представляет фотосинтетический перенос электронов в виде энергетической диаграммы
- 23.14. В фотосинтетическом переносе электронов принимает участие ряд переносчиков
- 23.15. Фосфорилирование ADP сопряжено с фотосинтетическим переносом электронов
- 23.16. В хлоропластах возможен также циклический поток электронов и циклическое фотофосфорилирование
- 23.17. Фотосинтетическое фосфорилирование сходно с окислительным фосфорилированием
- 23.18. Общее уравнение фотосинтеза растений
- 23.19. Фотосинтетическое образование гексоз связано с реальным восстановлением двуокиси углерода
- 23.20. Двуокись углерода фиксируется в форме фосфоглицерата
- 23.21. Глюкоза образуется из СО2 в цикле Кальвина
- 23.22. Глюкоза служит предшественником типичных растительных углеводов — сахарозы, крахмала и целлюлозы
- 23.23. Регуляция темновых реакций
- 23.24. В тропических растениях используется С4-путь, или путь Хэтча-Слэка
- 23.25. С4-путь обеспечивает необходимую концентрацию СО2
- 23.26. Фотодыхание ограничивает продуктивность С3-растений
- 23.27. Фотодыхание серьезная проблема для земледелия умеренной зоны
- 23.28. Галофильные бактерии используют световую энергию для синтеза АТР
- 23.29. Фотосинтезирующие организмы служат моделями для конструирования солнечных батарей
- Краткое содержание главы
- Вопросы и задачи
- Приложение. Ответы