| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
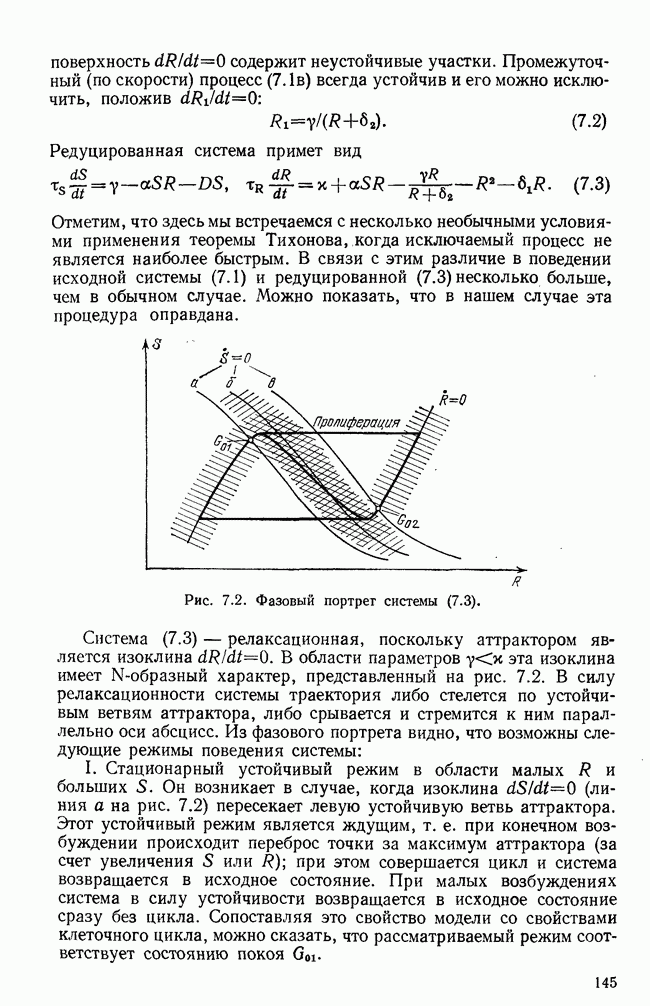
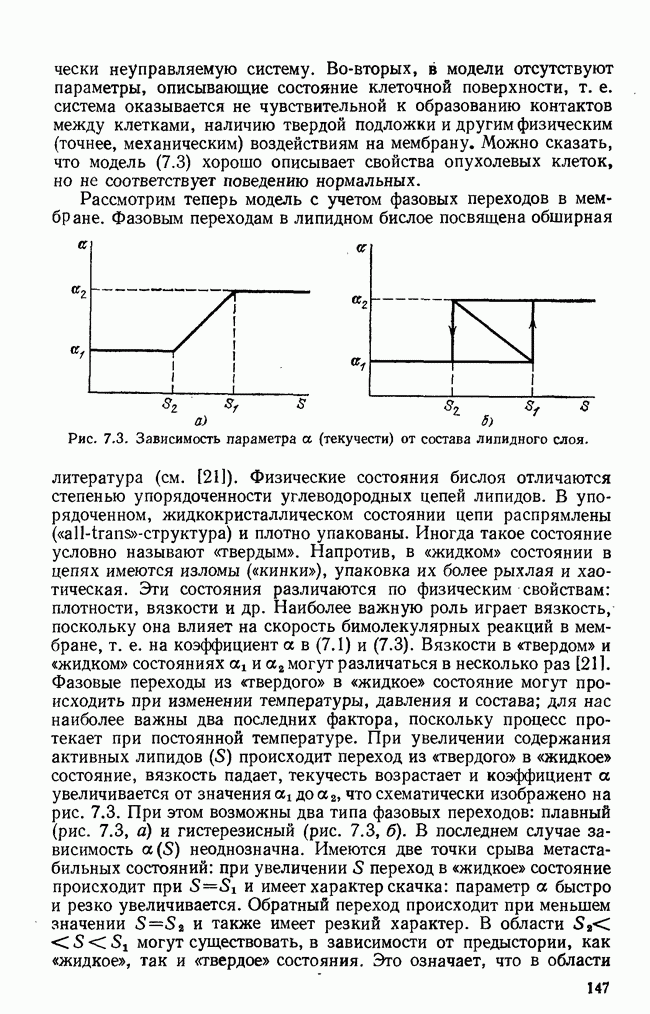
§ 3. Системное действие опухоли на организм
В этом параграфе мы изложим результаты моделирования одного из важнейших аспектов системного действия опухоли на организм, а именно действия опухоли как «ловушки глюкозы» [20, 21]. В модели учтено четыре фактора взаимодействия опухоли и иммунной системы. Три из них уже были рассмотрены в предыдущем параграфе. Это: 1) активация иммунных сил опухолевым антигеном,
2) иммунологический паралич при значительных опухолях, например за счет действия специфических лимфоцитов-супрессоров;
3) уничтожение клеток опухоли лимфоцитами-киллерами. Четвертый фактор, характерный именно для этой задачи, — инактивация
лимфоцитов гормонами-глюкокортикоидами. Выработка этих гормонов в организме опухоленосителя в условиях глюкозного голодания возрастает; с другой стороны, доказано их угнетающее действие на лимфоидную систему.
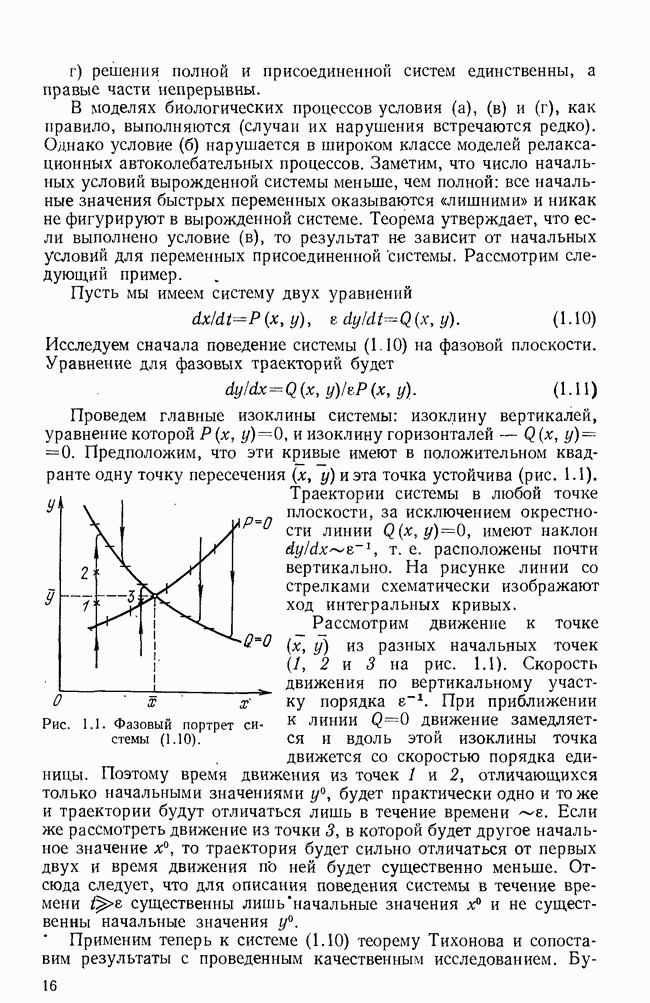
Запишем сначала динамику клеток опухоли х и лимфоцитов у:

Эта система отличается от модели (6.7) наличием члена — описывающего гибель лимфоцитов при взаимодействии с глюкокортикоидами, концентрация - которых обозначена через  Кроме того, в модели (6.8) предполагается зависимость удельных скоростей размножения клеток от концентрации глюкозы как лимитирующего субстрата. При этом
Кроме того, в модели (6.8) предполагается зависимость удельных скоростей размножения клеток от концентрации глюкозы как лимитирующего субстрата. При этом  зависит от концентрации глюкозы в крови
зависит от концентрации глюкозы в крови 
 — от локальной концентрации вблизи опухоли
— от локальной концентрации вблизи опухоли  Как отмечалось в § 1, локальная концентрация может быть значительно ниже
Как отмечалось в § 1, локальная концентрация может быть значительно ниже  однако она должна быть пропорциональна ей:
однако она должна быть пропорциональна ей:
Естественно предположить, что зависимость скорости репродукции от концентрации субстрата выражается законом Моно:

Отметим попутно, что константа Михаэлиса для опухолевых клеток  по крайней мере, на порядок меньше, чем для нормальных клеток организма. Для особо злокачественных, бурно растущих клеток асцитной карциномы Эрлиха это различие достигает даже трех порядков:
по крайней мере, на порядок меньше, чем для нормальных клеток организма. Для особо злокачественных, бурно растущих клеток асцитной карциномы Эрлиха это различие достигает даже трех порядков:  против
против  для клеток печени (см. [6]).
для клеток печени (см. [6]).
Чтобы замкнуть модель, запишем уравнение глюкозного баланса в организме:

Здесь первые два члена описывают потребление глюкозы опухолью и лимфоцитами, пропорциональное скорости прироста их биомассы  удельное потребление). Следующий член в (6.10) — потребление глюкозы остальными клетками организма
удельное потребление). Следующий член в (6.10) — потребление глюкозы остальными клетками организма  это масса организма, отнесенная к объему крови). Удельное потребление
это масса организма, отнесенная к объему крови). Удельное потребление  можно считать пропорциональным концентрации глюкозы, так как насыщение глюкозой происходит при концентрациях, превышающих норму, по крайней мере, в два раза. Таким образом, имеем
можно считать пропорциональным концентрации глюкозы, так как насыщение глюкозой происходит при концентрациях, превышающих норму, по крайней мере, в два раза. Таким образом, имеем

Приток глюкозы извне (с пищей)  можно для удобства разбить на два члена: основной
можно для удобства разбить на два члена: основной  определяемый потребностями организма в норме, и малый добавок (отклонение от нормы в ту или иную
определяемый потребностями организма в норме, и малый добавок (отклонение от нормы в ту или иную
сторону):

Далее, член  представляет синтез глюкозы (глюконеогенез), пропорциональный концентрации глюкокортикоидов
представляет синтез глюкозы (глюконеогенез), пропорциональный концентрации глюкокортикоидов  Наконец, функция
Наконец, функция  описывает запасание гликогена
описывает запасание гликогена  при избытке глюкозы в крови и обратный процесс — расщепление гликогена с образованием глюкозы при ее недостатке. Представим эту функцию в виде
при избытке глюкозы в крови и обратный процесс — расщепление гликогена с образованием глюкозы при ее недостатке. Представим эту функцию в виде

Форма записи (6.13) позволяет объяснить работу гликогенного депо, поддерживающего концентрацию глюкозы 5 вблизи нормы при значительных изменениях запаса гликогена  -константа скорости накопления гликогена).
-константа скорости накопления гликогена).
Динамику гликогена выразим уравнением

где член —  характеризует паразитный отток гликогена; мы будем считать его малым (он может играть заметную роль лишь при очень высоких значениях
характеризует паразитный отток гликогена; мы будем считать его малым (он может играть заметную роль лишь при очень высоких значениях 
Обсудим сразу же количественный аспект глюкозного баланса. Отметим, прежде всего, одно важное обстоятельство. На первый взгляд кажется, что количественные оценки можно делать, имея в виду только какой-то определенный вид животных. Однако, поскольку мы используем относительные единицы измерения переменных, некоторые условные «концентрации» (а именно массу клеток, отнесенную к общему объему крови), то значения параметров уравнений оказываются очень близкими даже для столь различных млекопитающих, как человек и мышь. Действительно, и в том, и в другом случае кровь составляет примерно 7% массы тела, так что  . С другой стороны, концентрации глюкозы в крови у всех млекопитающих поразительно близки и составляют в норме
. С другой стороны, концентрации глюкозы в крови у всех млекопитающих поразительно близки и составляют в норме  Поэтому мы будем использовать разные оценки [6, 22], не оговаривая специально, к какому организму они относятся.
Поэтому мы будем использовать разные оценки [6, 22], не оговаривая специально, к какому организму они относятся.
Оценим прежде всего потребности в глюкозе всего организма и раковых клеток. Первые составляют (в норме)  на
на  массы, или в наших обозначениях
массы, или в наших обозначениях  Общее потребление всего организма массой
Общее потребление всего организма массой  тогда будет
тогда будет  -сутки). Сравним с этими цифрами скорости потребления глюкозы раковыми клетками карциномы Эрлиха в благоприятных условиях (при
-сутки). Сравним с этими цифрами скорости потребления глюкозы раковыми клетками карциномы Эрлиха в благоприятных условиях (при  и в реальных условиях
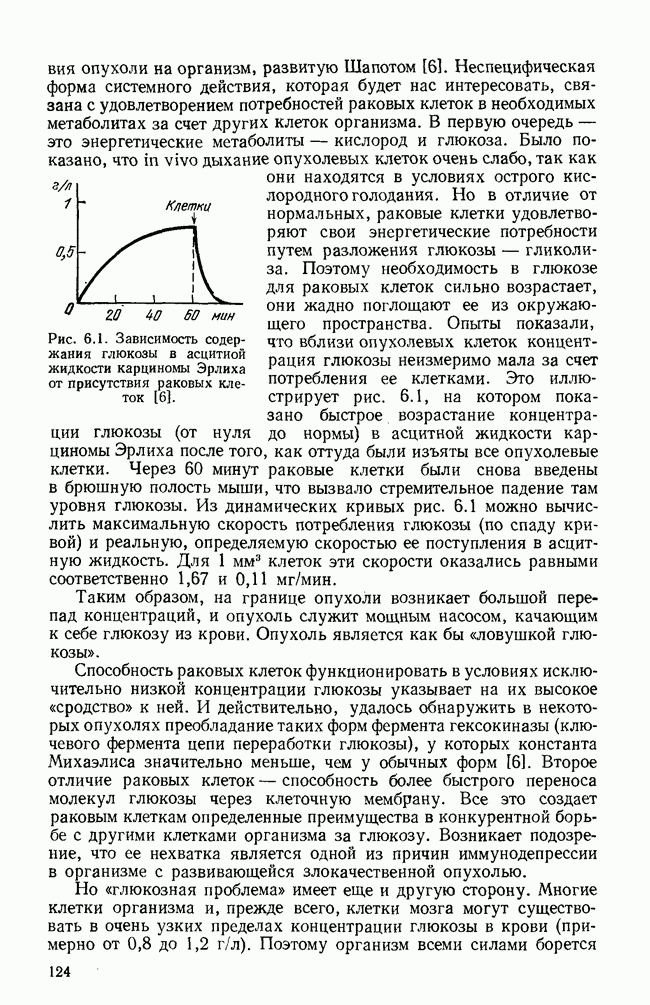
и в реальных условиях  (см. рис. 6.1). Имеем соответственно
(см. рис. 6.1). Имеем соответственно  Мы видим, что даже реальные скорости, лимитированные низким содержанием глюкозы в асцитной жидкости, почти в 30 раз превышают удельную скорость потребления нормальной ткани. Однако общее потребление опухолью будет мало, так как масса ее составляет ничтожную долю от массы организма:
Мы видим, что даже реальные скорости, лимитированные низким содержанием глюкозы в асцитной жидкости, почти в 30 раз превышают удельную скорость потребления нормальной ткани. Однако общее потребление опухолью будет мало, так как масса ее составляет ничтожную долю от массы организма:  Еще в большей мере это
Еще в большей мере это
относится к потреблению глюкозы лимфоцитами, масса которых сравнима с массой опухоли, а скорость потребления — та же, что и у любой другой нормальной ткани. Поэтому в (6.10) членом  мы в дальнейшем пренебрегаем.
мы в дальнейшем пренебрегаем.
Из сделанных оценок становится ясно, что рост опухоли в реальных пределах не может существенно повлиять на концентрацию глюкозы в крови. Вместе с тем, потребление глюкозы растет, что вызывает, в первую очередь, уменьшение запасов гликогена, а затем активизацию глюконеогенеза. При этом регулирующим фактором процесса образования эндогенной глюкозы не может служить практически неизменная концентрация глюкозы в крови. Таким регулирующим фактором может быть, согласно гипотезе Шапота, уменьшение запасов гликогена (см. также [23]).
Здесь мы снова сталкиваемся с распространенным в биологии законом: первопричиной процессов, ведущих к существенным последствиям, является изменение потребления субстрата (в нашем случае глюкозы). Однако ввиду важной роли и универсальности субстрата концентрация его в организме стабилизирована. Поэтому регуляторные функции возлагаются на другие вещества, содержание которых сильно изменяется при изменении потребления субстрата.
В нашей модели будем предполагать,  уменьшение запасов гликогена
уменьшение запасов гликогена  вызывает увеличение скорости синтеза гормонов — глюкокортикоидов
вызывает увеличение скорости синтеза гормонов — глюкокортикоидов  которые, в свою очередь, активизируют процесс глюконеогенеза. Динамику концентрации гормонов запишем тогда в следующем виде:
которые, в свою очередь, активизируют процесс глюконеогенеза. Динамику концентрации гормонов запишем тогда в следующем виде:

где константа  определяет скорость инактивации гормона в организме,
определяет скорость инактивации гормона в организме,  параметры процесса активации.
параметры процесса активации.
Процессы, описываемые уравнениями (6.10), (6.14), (6.15), т. е. изменение концентраций глюкозы, гликогена и гормонов, протекают быстро (за минуты и часы) по сравнению с развитием опухоли. Поэтому величины  всегда успевают достичь своих стационарных значений, которые мы и будем исследовать. Прежде всего перейдем к безразмерным переменным
всегда успевают достичь своих стационарных значений, которые мы и будем исследовать. Прежде всего перейдем к безразмерным переменным

Тогда для стационарных значений имеем

Параметр  характеризует отношение паразитного оттока гликогена к поступлению его из крови. Считая
характеризует отношение паразитного оттока гликогена к поступлению его из крови. Считая  мы можем приближенно выразить
мы можем приближенно выразить  (вдали от точки
(вдали от точки 

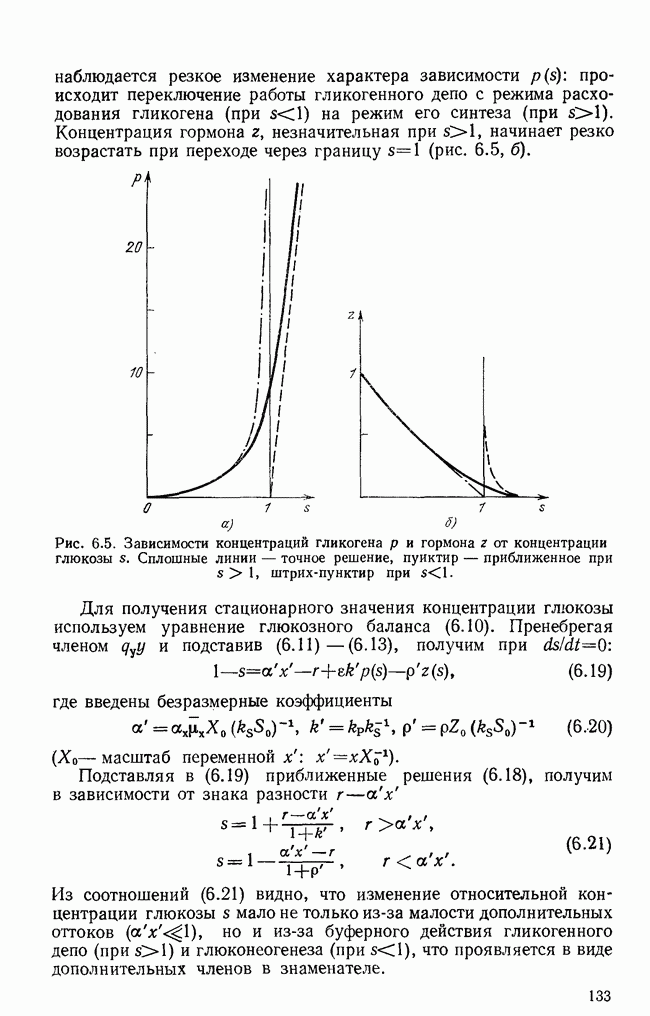
На рис. 6.5 приведены точные решения (6.17) и приближенные (6.18) при  Из рис. 6.5, а видно, что вблизи значения
Из рис. 6.5, а видно, что вблизи значения 
наблюдается резкое изменение характера зависимости  происходит переключение работы гликогенного депо с режима расходования гликогена
происходит переключение работы гликогенного депо с режима расходования гликогена  на режим его синтеза
на режим его синтеза  Концентрация гормона
Концентрация гормона  незначительная при
незначительная при  начинает резко возрастать при переходе через границу
начинает резко возрастать при переходе через границу 

Рис. 6.5. Зависимости концентраций гликогена  и гормона
и гормона  от концентрации глюкозы
от концентрации глюкозы  Сплошные линии — точное решение, пуиктир — приближенное при
Сплошные линии — точное решение, пуиктир — приближенное при  штрих-пунктир при
штрих-пунктир при 
Для получения стационарного значения концентрации глюкозы используем уравнение глюкозного баланса (6.10). Пренебрегая членом  и подставив
и подставив  получим при
получим при 

где введены безразмерные коэффициенты

(Хо—масштаб переменной 
Подставляя в (6.19) приближенные решения (6.18), получим в зависимости от знака разности 

Из соотношений (6.21) видно, что изменение относительной концентрации глюкозы  мало не только из-за малости дополнительных оттоков
мало не только из-за малости дополнительных оттоков  но и из-за буферного действия гликогенного депо (при
но и из-за буферного действия гликогенного депо (при  и глюконеогенеза (при
и глюконеогенеза (при  что проявляется в виде дополнительных членов в знаменателе.
что проявляется в виде дополнительных членов в знаменателе.
Вернемся теперь к системе (6.8), описывающей динамику клеток опухоли и лимфоцитов, и рассмотрим ее в условиях, когда поглощение глюкозы опухолью мало, но все же превышает дополнительный приток 
Прежде всего заметим, что коэффициенты репродукции ,их  можно с большой степенью точности принять постоянными, поскольку мы показали, что концентрация глюкозы
можно с большой степенью точности принять постоянными, поскольку мы показали, что концентрация глюкозы  в широких пределах изменения х остается практически постоянной
в широких пределах изменения х остается практически постоянной  (константа
(константа  входит в выражение для а в (6.20)).
входит в выражение для а в (6.20)).
Таким образом, системное действие опухоли как «ловушки» глюкозы сводится в модели к изменению концентрации глюкокортикоидов  угнетающих лимфоидную систему. Подставив для случая
угнетающих лимфоидную систему. Подставив для случая  в (6.15), имеем при
в (6.15), имеем при 

т. е. концентрация глюкокортикоидов растет линейно с увеличением х. Приведем систему (6.8) к безразмерному виду, введя переменные и коэффициенты по формулам

Окончательно имеем

Как мы видим, параметры системы (6.24) являются комбинацией многих «внутренних» параметров модели, т. е. мы здесь снова имеем пример «свертки информации». Глюкозное голодание сложным образом влияет, во-первых, на коэффициент подавления лимфоцитов опухолью  а во-вторых, на коэффициент «естественной гибели» лимфоцитов х. В последнем случае эффект зависит от знака дополнительного притока глюкозы
а во-вторых, на коэффициент «естественной гибели» лимфоцитов х. В последнем случае эффект зависит от знака дополнительного притока глюкозы  Если приток положителен, коэффициент убыли лимфоцитов уменьшается и это благотворно действует на иммунную систему. Если же внешний приток глюкозы будет меньше, чем в норме
Если приток положителен, коэффициент убыли лимфоцитов уменьшается и это благотворно действует на иммунную систему. Если же внешний приток глюкозы будет меньше, чем в норме  то это приведет к дополнительной гибели лимфоцитов, т. е. к ослаблению иммунитета.
то это приведет к дополнительной гибели лимфоцитов, т. е. к ослаблению иммунитета.
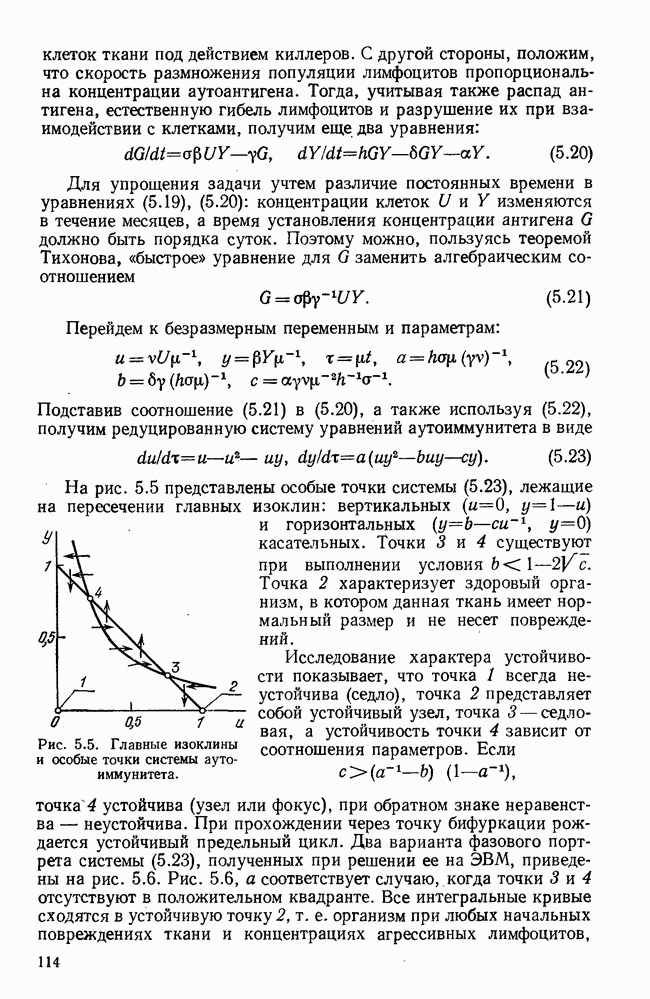
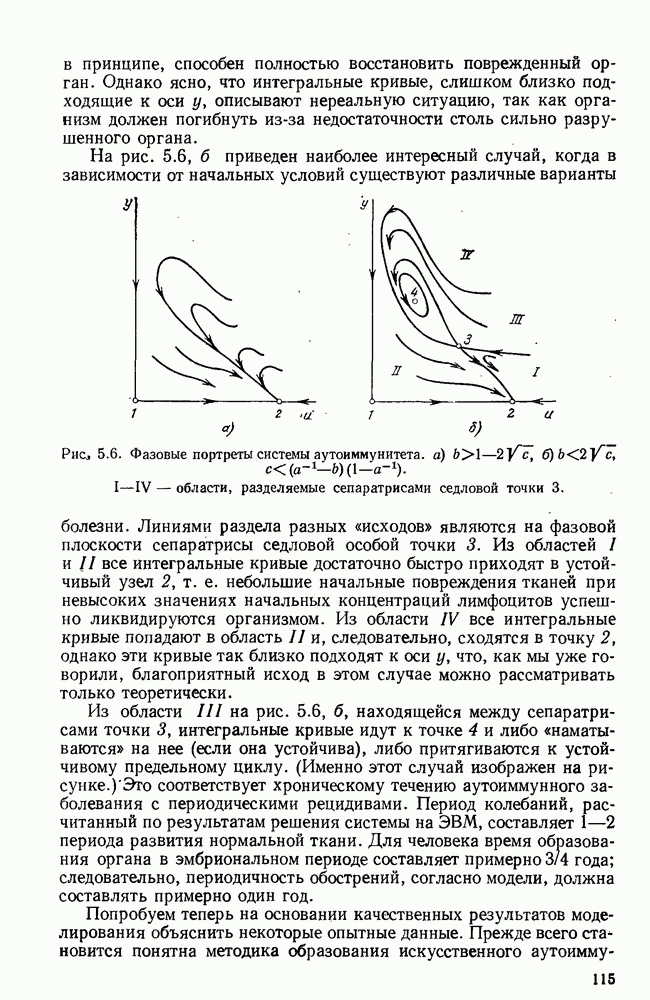
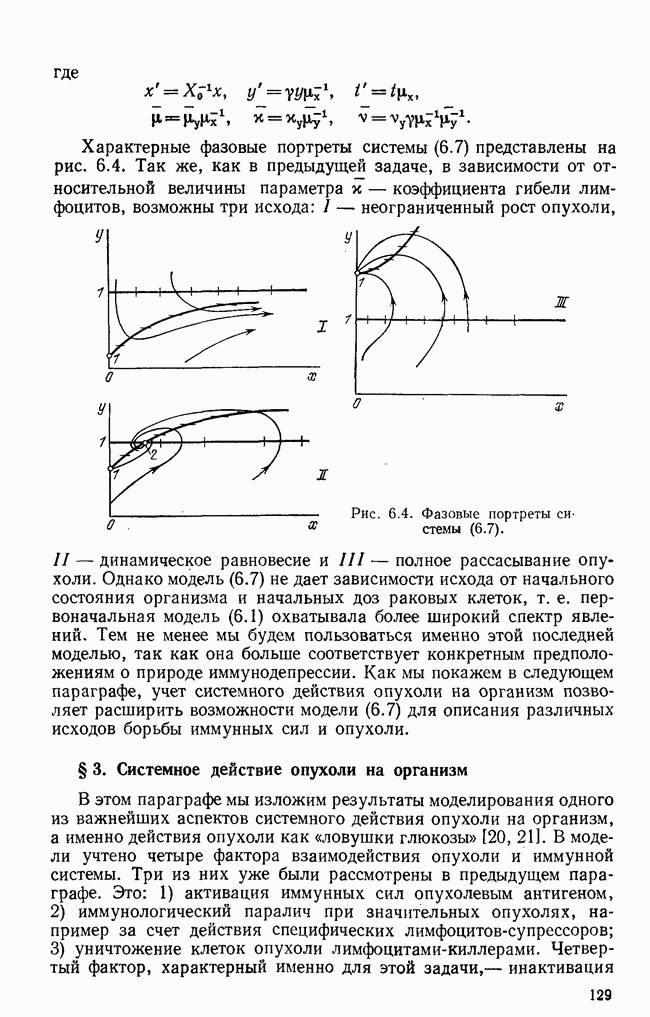
Обратимся теперь к исследованию модели (6.24). Качественно поведение этой системы полностью аналогично модели (6.1), описанной в § 2. А именно, может быть три случая. I) В положительном квадранте существует одна неустойчивая особая точка 1 (рис. 6.3, I), и все интегральные кривые уходят в бесконечность. II) Существуют три особых точки, когда поведение системы зависит от начальных условий: либо мы попадаем на траекторию, уходящую в
бесконечность и соответствующую гибели организма, либо на траекторию, навивающуюся на устойчивое состояние равновесия  . В положительном квадранте — две особые точки; точка 1 устойчива, т. е. возможно полное рассасывание опухоли, однако из других начальных условий траектории снова попадают в зону притяжения бесконечно удаленной точки
. В положительном квадранте — две особые точки; точка 1 устойчива, т. е. возможно полное рассасывание опухоли, однако из других начальных условий траектории снова попадают в зону притяжения бесконечно удаленной точки  (рис. 6.3, III).
(рис. 6.3, III).

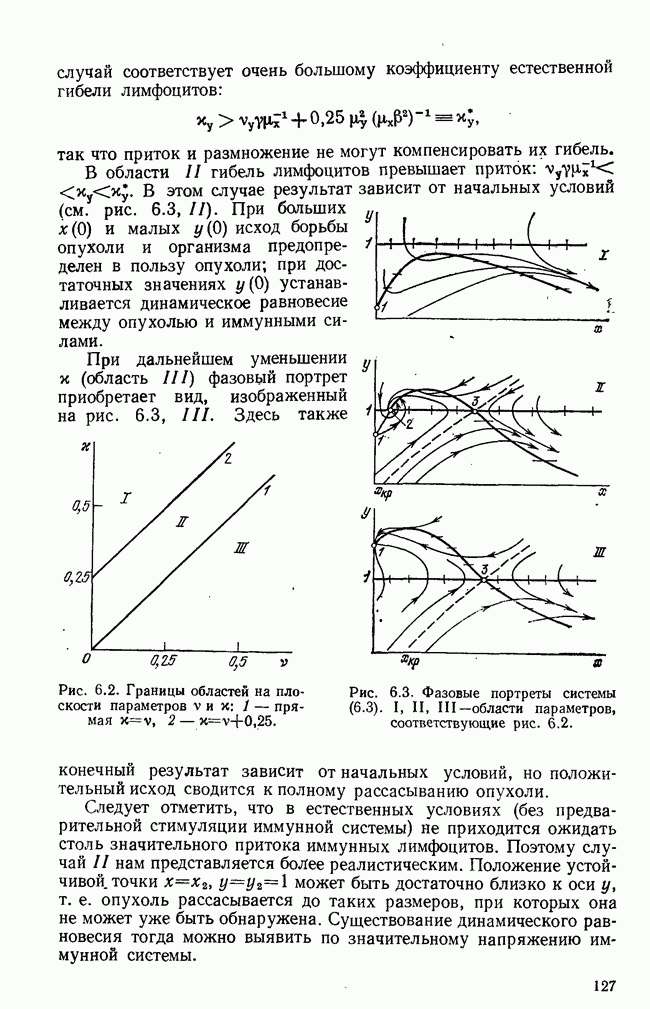
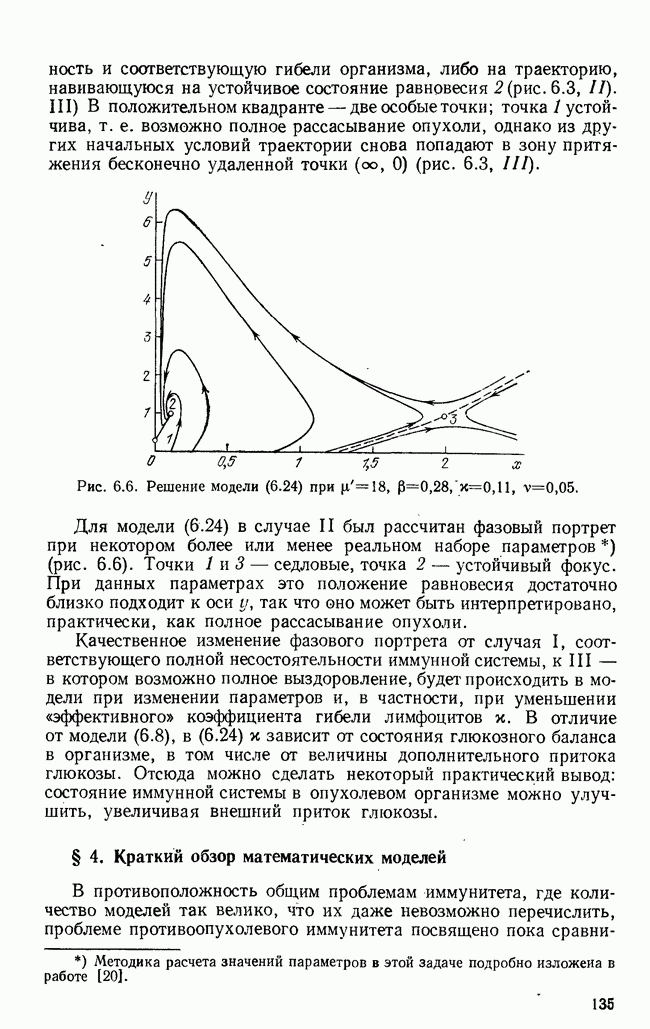
Рис. 6.6. Решение модели (6.24) при 
Для модели (6.24) в случае II был рассчитан фазовый портрет при некотором более или менее реальном наборе параметров (рис. 6.6). Точки 1 и 3 — седловые, точка 2 — устойчивый фокус. При данных параметрах это положение равновесия достаточно близко подходит к оси у, так что оно может быть интерпретировано, практически, как полное рассасывание опухоли.
Качественное изменение фазового портрета от случая I, соответствующего полной несостоятельности иммунной системы, к III — в котором возможно полное выздоровление, будет происходить в модели при изменении параметров и, в частности, при уменьшении «эффективного» коэффициента гибели лимфоцитов х. В отличие от модели (6.8), в (6.24) и зависит от состояния глюкозного баланса в организме, в том числе от величины дополнительного притока глюкозы. Отсюда можно сделать некоторый практический вывод: состояние иммунной системы в опухолевом организме можно улучшить, увеличивая внешний приток глюкозы.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ЧАСТЬ I. МАТЕМАТИЧЕСКИЕ МОДЕЛИ БИОФИЗИЧЕСКОЙ КИНЕТИКИ
- § 1. Особенности биологической кинетики
- § 2. Элементы качественной теории динамических систем второго порядка
- § 3. Методы упрощения систем кинетических уравнений
- § 4. Редукция систем и теория катастроф
- ГЛАВА 2. МАТЕМАТИЧЕСКИЕ МОДЕЛИ ЭВОЛЮЦИИ И РАЗВИТИЯ
- § 1. Первичный гиперцикл
- § 2. Проблема выбора единого кода
- § 3. Дивергентная эволюция
- § 4. Модели развития организма
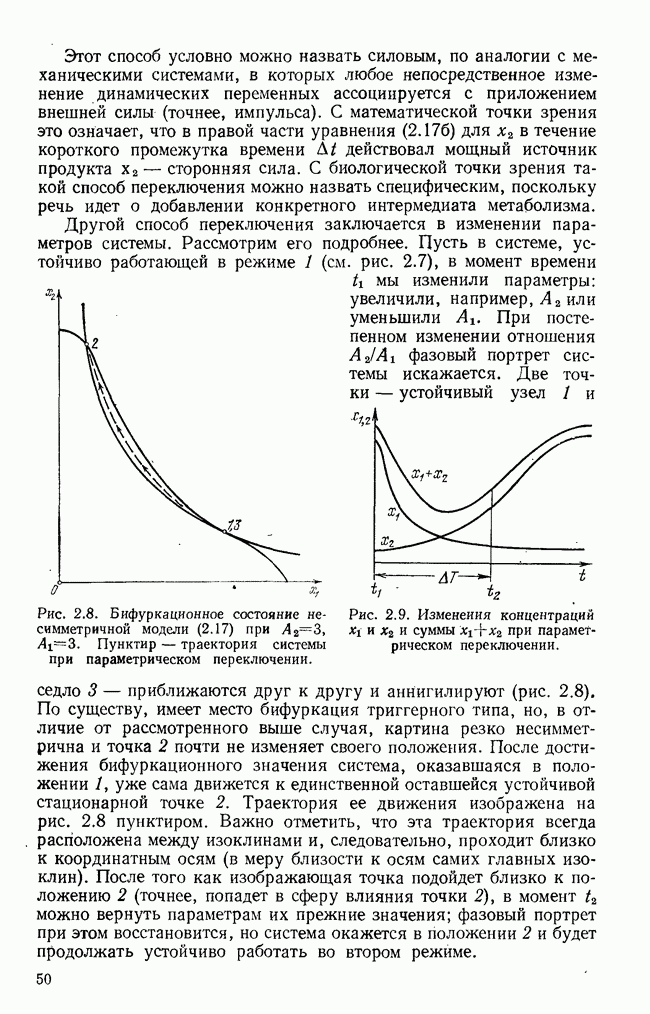
- § 5. Силовое и параметрическое переключение
- ГЛАВА 3. ДИНАМИЧЕСКИЕ МОДЕЛИ КЛЕТОЧНЫХ ПОПУЛЯЦИЙ
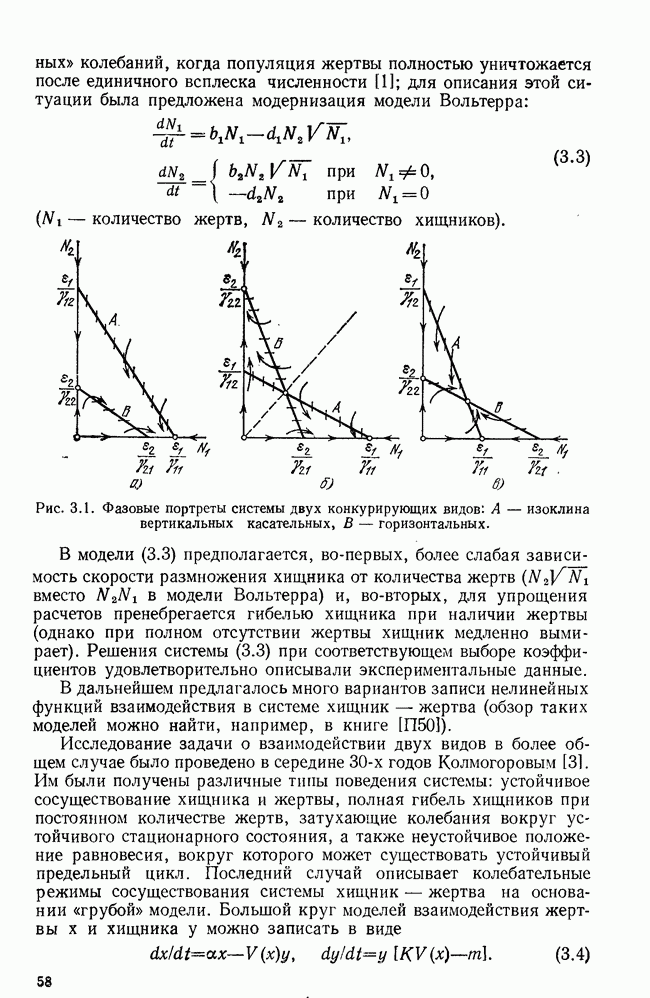
- § 1. Простейшие популяционные модели
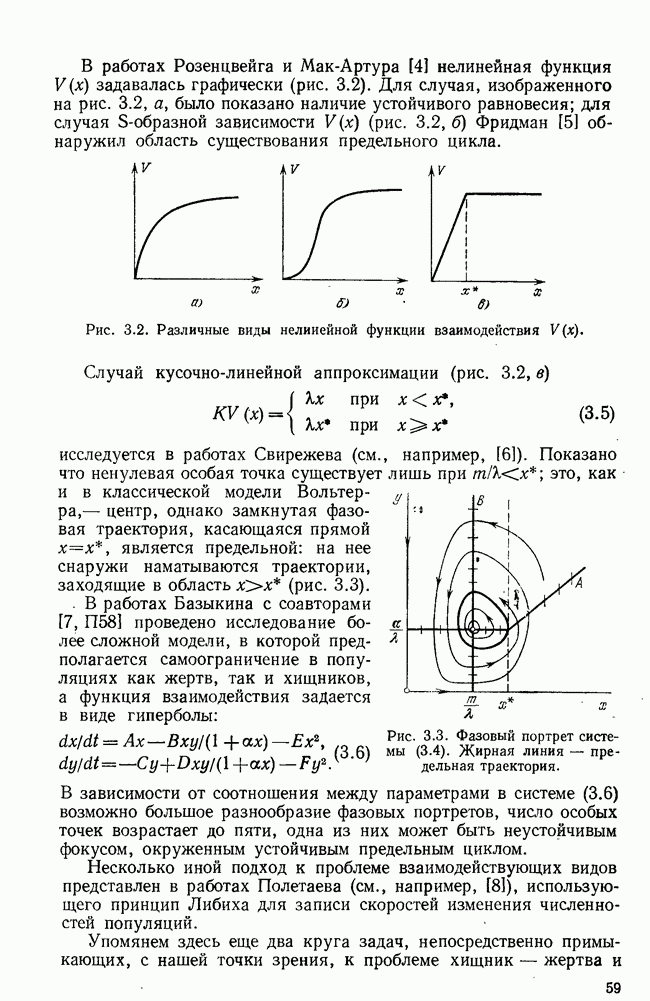
- § 2. Влияние среды на рост популяций
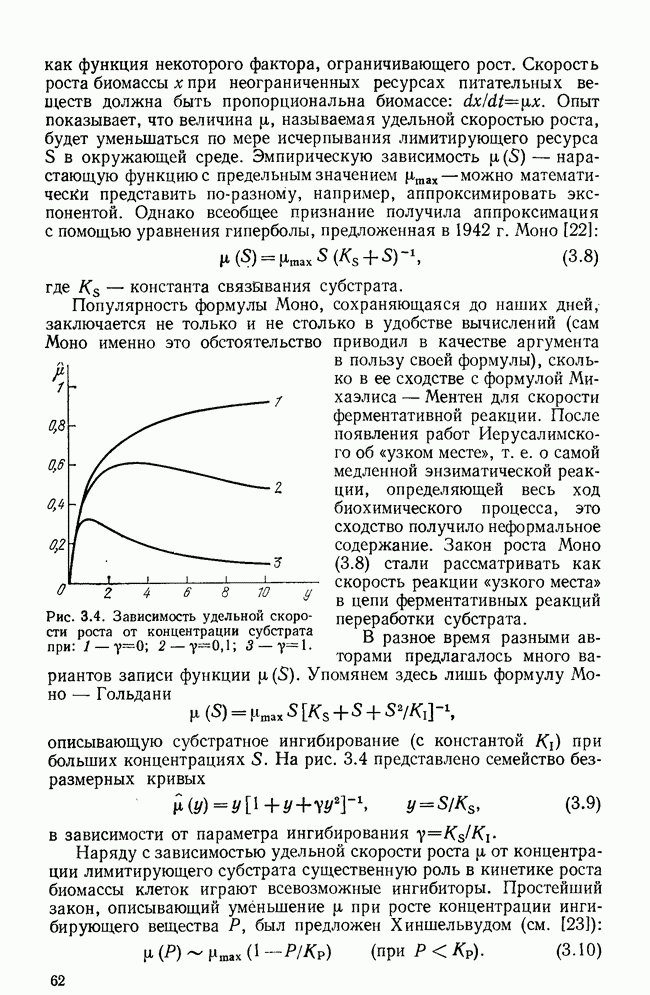
- § 3. Математические модели в микробиологии
- § 4. Проблема биологической инерционности
- ГЛАВА 4. РАСПРЕДЕЛЕНИЕ КЛЕТОК ПО ВОЗРАСТАМ
- § 1. Двухвозрастная модель клеточной популяции
- § 2. Непрерывные возрастные модели
- § 3. Функции распределения клеток по размерам
- ГЛАВА 5. ДИНАМИКА ИММУННОЙ РЕАКЦИИ
- § 1. Популяции иммунных клеток в организме
- § 2. Математическая модель иммунного ответа
- § 3. Кооперативное взаимодействие лимфоцитов
- § 4. Инфекционные болезни
- § 5. Проблема аутоиммунитета
- § 6. Краткий обзор математических моделей иммунитета
- ГЛАВА 6. СПЕЦИФИЧЕСКИЙ ИММУНИТЕТ И РАК
- § 2. Модели взаимодействия опухоли и организма
- § 3. Системное действие опухоли на организм
- § 4. Краткий обзор математических моделей
- ГЛАВА 7. МОДЕЛИ РЕГУЛЯЦИИ КЛЕТОЧНОГО ЦИКЛА
- § 2. Тип модели и основные гипотезы
- § 3. Модель регуляции клеточного цикла
- § 4. Биологические следствия
- ЧАСТЬ II. РАСПРЕДЕЛЕННЫЕ КИНЕТИЧЕСКИЕ СИСТЕМЫ И БИОЛОГИЧЕСКАЯ СИНЕРГЕТИКА
- ГЛАВА 8. МАТЕМАТИЧЕСКИЕ МОДЕЛИ АВТОВОЛНОВЫХ ПРОЦЕССОВ
- § 1. Математическая модель распределенной системы
- § 2. Стационарные однородные решения и их устойчивость
- § 3. Автоколебания и диссипативные структуры в почти гармонических системах
- § 4. Классификация автоволновых процессов и основные экспериментальные данные
- ГЛАВА 9. РАСПРОСТРАНЕНИЕ ВОЗМУЩЕНИЙ В ВОЗБУДИМЫХ СРЕДАХ
- § 1. Распространение фронта возмущения
- § 2. Базовая модель релаксационных возбудимых сред
- § 3. Стационарные бегущие импульсы
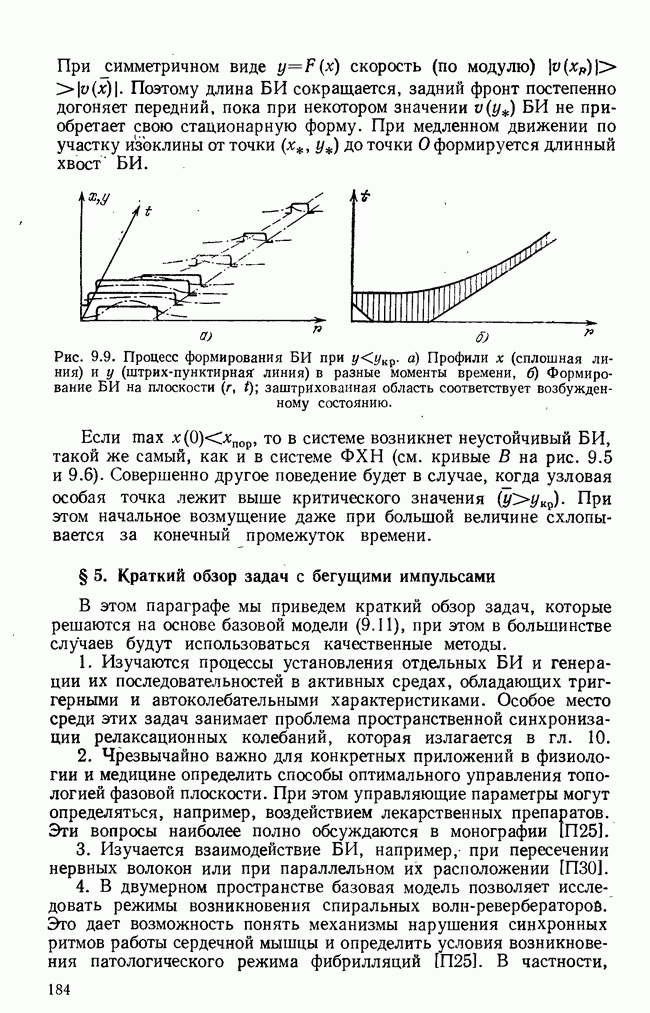
- § 4. Процесс установления бегущего импульса
- § 5. Краткий обзор задач с бегущими импульсами
- § 6. Автономные источники волн в гомогенной активной среде
- ГЛАВА 10. СИНХРОНИЗАЦИЯ АВТОКОЛЕБАНИЙ В НЕОДНОРОДНОМ ПРОСТРАНСТВЕ
- § 1. Базовая модель неоднородной распределенной системы
- § 2. Синхронизация в квазигармонической системе
- § 3. Случай релаксационной системы
- § 4. Приложения в химии и биологии
- § 5. Процессы установления синхронного режима
- § 6. Шумы и синхронизация
- § 7. Автоколебательные системы, связанные через общую среду
- ГЛАВА 11. ДИССИПАТИВНЫЕ СТРУКТУРЫ И ПРОБЛЕМЫ САМООРГАНИЗАЦИИ
- § 2. Контрастные диссипативные структуры; базовые модели
- § 3. Стационарные контрастные ДС типа складки
- § 4. Стационарные ДС типа сборки
- § 5. Устойчивость диссипативных структур
- § 6. Конкретные модели диссипативных структур
- § 7. Кинетика образования ДС
- § 8. Некоторые выводы
- ГЛАВА 12. ТЕРМОДИНАМИКА, ИНФОРМАЦИЯ, БИОЛОГИЯ
- § 1. Механика и статистика
- § 2. Информация и энтропия
- § 3. Ценность информации
- § 4. Биологическая информация
- § 5. Эффективность биологической информации
- ЗАКЛЮЧЕНИЕ