| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 2. Тип модели и основные гипотезы
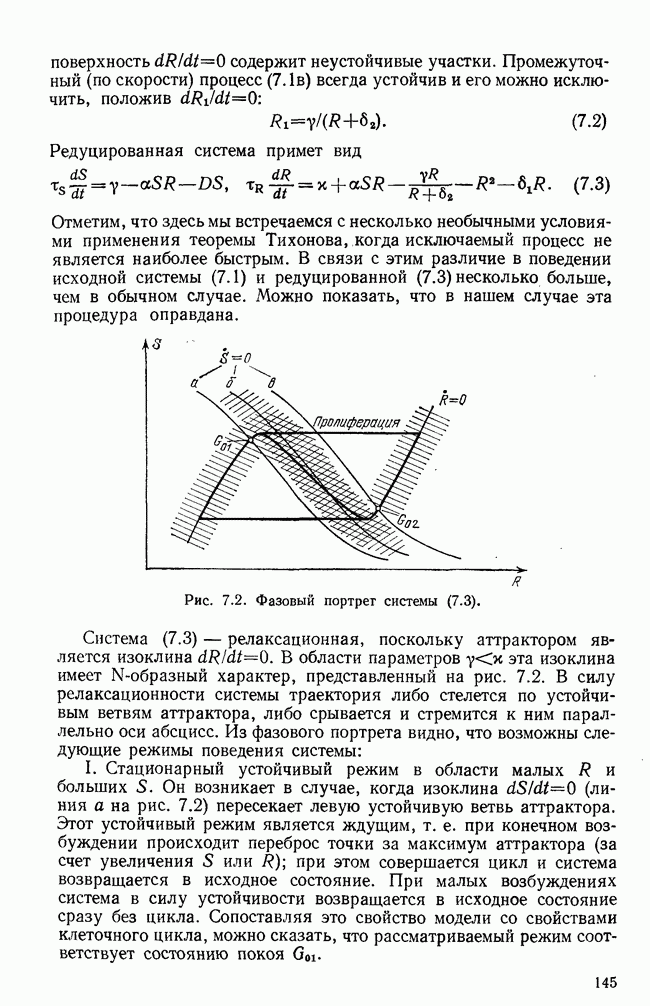
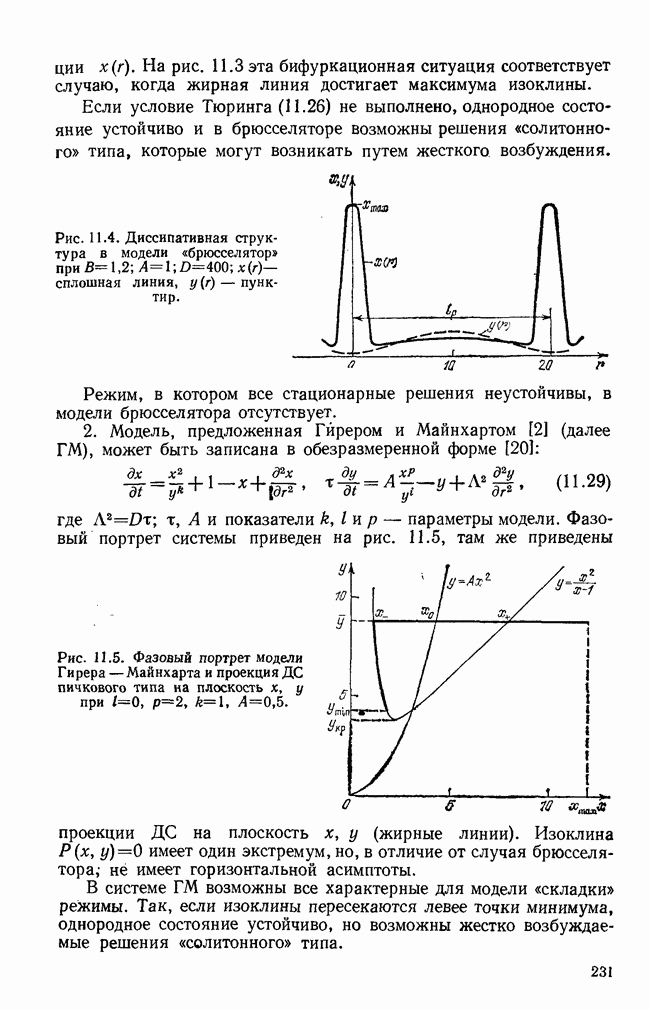
Упомянутые свойства процесса позволяют выбрать класс моделей, описывающих особенности клеточного цикла нормальных и опухолевых клеток. Существование циклического режима (пролиферации) и наряду с ним режимов покоя означает, что минимальная динамическая модель должна иметь  -образную изоклину, характерную для катастрофы типа складки, и при этом быть достаточно релаксационной. (Напомним, что именно в «складке» возможны периодический и стационарные ждущие режимы (см. гл. 1).) Стохастичность клеточного цикла означает, что модель должна быть не очень грубой, т. е. «рабочая» область параметров модели должна быть близка к бифуркации типа складки и включать ее.
-образную изоклину, характерную для катастрофы типа складки, и при этом быть достаточно релаксационной. (Напомним, что именно в «складке» возможны периодический и стационарные ждущие режимы (см. гл. 1).) Стохастичность клеточного цикла означает, что модель должна быть не очень грубой, т. е. «рабочая» область параметров модели должна быть близка к бифуркации типа складки и включать ее.
Отметим, что для описания клеточного цикла широко используются вероятностные модели (см., например, [7]), в которых как раз главным свойством цикла считается его стохастичность. В них переменными являются вероятности застать клетку в той или иной фазе, а коэффициенты перехода являются параметрами. Эти модели удобны для феноменологического описания поведения популяции клеток и широко используются при обработке экспериментальных данных с целью извлечения информации о длительностях фаз и дисперсиях. Однако вероятностные модели трудно связать с механизмом продвижения клетки по циклу; как правило, такая задача в них и не ставится. Ниже мы рассмотрим динамические модели клеточного цикла и специально обсудим вопрос об их стохастизации (что может служить связующим звеном с вероятностным подходом).
Обсудим теперь гипотезы, лежащие в основе динамических моделей, и историю их возникновения. Первые попытки построить модель клеточного цикла относятся к началу нашего века (см.[П71]). Они основывались на предположении об определяющей роли осмотических процессов. Клетка рассматривалась как набухающий сосуд с эластичными стенками. Акт деления приурочивался к моменту, когда оболочка разрывается. Эта модель была популярна и оценки приводили к правдоподобным результатам. Однако по накоплению экспериментальных данных модель была оставлена.
Следующий шаг был связан с проникновением в биохимию идей об автоколебаниях. Тогда же началось интенсивное изучение периодических процессов в клетке и циркадных ритмов. Это направление известно под названием «биологические часы».
Высказывались предположения о том, что ритмический процесс, ответственный за ход «часов», управляет одновременно и клеточным делением. Сейчас можно считать установленным, что «часы» в клетке действительно есть [8], их период сохраняется постоянным с завидной точностью и мало чувствителен к температуре. Это значит, что механизм часов защищен от внешних влияний, в том числе на клеточную мембрану. В работах Селькова (см. [П25]) показано, что роль часового механизма могут играть автоколебания в энергетическом метаболизме. Таким образом, требования, предъявляемые к механизму часов и регуляции клеточного цикла, существенно различны и один какой-либо процесс не может выполнить обе функции.
Сформулируем теперь важную для моделирования гипотезу: регуляторные аппараты дтоль сложного процесса, как клеточная деятельность, должны быть достаточно просты, автономны и обособлены от регулируемого процесса. Эта гипотеза равно относится к клеточным часам, к регуляции деления и вообще к управлению поведением сложной системы. Гипотеза не тривиальна, поскольку можно сформулировать альтернативу: автономного регулятора нет и в управлении циклом равно участвуют все клеточные процессы (а их порядка нескольких тысяч!). Гипотеза важна для нас, поскольку только она позволяет построить модель регуляции.
Следующий этап относится к определению места, в котором локализован аппарат, управляющий клеточным циклом. По этому поводу были высказаны три возможные гипотезы: регуляторный аппарат сосредоточен в клеточном ядре [П52], в цитоплазме [9] и в клеточной мембране [10—16]; соответственно были предложены различные модели. Затем, однако, выяснилось, что модели автоколебательных процессов в цитоплазме более соответствуют клеточными часам, о чем уже упоминалось.
Модель, основанная на процессах в генетическом аппарате, была построена Цаневым и Сендовым [П52] и привела к ряду интересных результатов, в частности к описанию эффекта блокировки (см. гл. 2). Однако применение ее к описанию регуляции клеточного цикла оказалось затруднительным.
Гипотеза о том, что регулятор цикла находится в клеточной мембране, высказывалась сравнительно давно и в разных работах [10, 11]. Наиболее веские соображения в ее пользу состоят в следующем. Регулятор должен вырабатывать сигналы к синтезу ДНК (или к делению) на основании информации о ситуации во внешней по отношению к клетке среде. Такая информация поступает прежде всего на клеточную мембрану, поэтому и сам регулятор естественно поместить там же. Помещение регулятора цикла в клеточное ядро было бы неразумно. Одна из главных функций ядра — сохранение генетической информации, для чего нужно по возможности защитить ядро от внешних влияний; ясно, что эту задачу трудно совместить с задачей сбора информации извне.
Ниже мы обсудим модель, основанную на мембранном механизме регуляции, следуя работам [16-18, ПЗ]. Задача заключается в построении модели возникновения в клеточной мембране
сигналов к переходу из покоя в пролиферацию и (или) перехода из одной фазы цикла в другую. Вопрос о том, как эти сигналы преобразуются в цитоплазме и клеточном ядре, может рассматриваться отдельно и независимо от первой задачи. Мы этого вопроса касаться не будем.
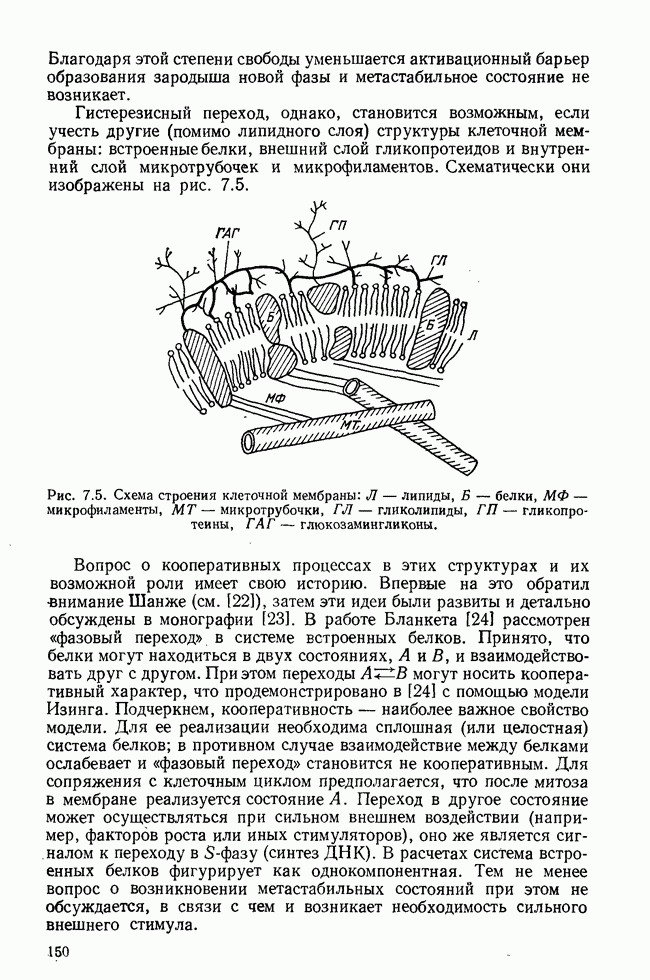
В клеточной мембране можно выделить два типа процессов: химические и физические. К первым относятся изменение липидного состава, окисление липидов и их удаление; на их возможную роль в регуляции цикла впервые было обращено внимание в работах Бурлаковой [10, 19]. К физическим процессам относится изменение фазового состояния липидного бислоя, его текучести, упругости и т. д. Помимо этого в мембране протекает множество ферментативных процессов; деятельность ферментов зависит как от липидного состава, так и от фазового состояния клеточной мембраны. Эти белки-энзимы могут играть роль первичных акцепторов сигналов, генерируемых в мембране.
Мы последовательно рассмотрим оба типа процессов.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ЧАСТЬ I. МАТЕМАТИЧЕСКИЕ МОДЕЛИ БИОФИЗИЧЕСКОЙ КИНЕТИКИ
- § 1. Особенности биологической кинетики
- § 2. Элементы качественной теории динамических систем второго порядка
- § 3. Методы упрощения систем кинетических уравнений
- § 4. Редукция систем и теория катастроф
- ГЛАВА 2. МАТЕМАТИЧЕСКИЕ МОДЕЛИ ЭВОЛЮЦИИ И РАЗВИТИЯ
- § 1. Первичный гиперцикл
- § 2. Проблема выбора единого кода
- § 3. Дивергентная эволюция
- § 4. Модели развития организма
- § 5. Силовое и параметрическое переключение
- ГЛАВА 3. ДИНАМИЧЕСКИЕ МОДЕЛИ КЛЕТОЧНЫХ ПОПУЛЯЦИЙ
- § 1. Простейшие популяционные модели
- § 2. Влияние среды на рост популяций
- § 3. Математические модели в микробиологии
- § 4. Проблема биологической инерционности
- ГЛАВА 4. РАСПРЕДЕЛЕНИЕ КЛЕТОК ПО ВОЗРАСТАМ
- § 1. Двухвозрастная модель клеточной популяции
- § 2. Непрерывные возрастные модели
- § 3. Функции распределения клеток по размерам
- ГЛАВА 5. ДИНАМИКА ИММУННОЙ РЕАКЦИИ
- § 1. Популяции иммунных клеток в организме
- § 2. Математическая модель иммунного ответа
- § 3. Кооперативное взаимодействие лимфоцитов
- § 4. Инфекционные болезни
- § 5. Проблема аутоиммунитета
- § 6. Краткий обзор математических моделей иммунитета
- ГЛАВА 6. СПЕЦИФИЧЕСКИЙ ИММУНИТЕТ И РАК
- § 2. Модели взаимодействия опухоли и организма
- § 3. Системное действие опухоли на организм
- § 4. Краткий обзор математических моделей
- ГЛАВА 7. МОДЕЛИ РЕГУЛЯЦИИ КЛЕТОЧНОГО ЦИКЛА
- § 2. Тип модели и основные гипотезы
- § 3. Модель регуляции клеточного цикла
- § 4. Биологические следствия
- ЧАСТЬ II. РАСПРЕДЕЛЕННЫЕ КИНЕТИЧЕСКИЕ СИСТЕМЫ И БИОЛОГИЧЕСКАЯ СИНЕРГЕТИКА
- ГЛАВА 8. МАТЕМАТИЧЕСКИЕ МОДЕЛИ АВТОВОЛНОВЫХ ПРОЦЕССОВ
- § 1. Математическая модель распределенной системы
- § 2. Стационарные однородные решения и их устойчивость
- § 3. Автоколебания и диссипативные структуры в почти гармонических системах
- § 4. Классификация автоволновых процессов и основные экспериментальные данные
- ГЛАВА 9. РАСПРОСТРАНЕНИЕ ВОЗМУЩЕНИЙ В ВОЗБУДИМЫХ СРЕДАХ
- § 1. Распространение фронта возмущения
- § 2. Базовая модель релаксационных возбудимых сред
- § 3. Стационарные бегущие импульсы
- § 4. Процесс установления бегущего импульса
- § 5. Краткий обзор задач с бегущими импульсами
- § 6. Автономные источники волн в гомогенной активной среде
- ГЛАВА 10. СИНХРОНИЗАЦИЯ АВТОКОЛЕБАНИЙ В НЕОДНОРОДНОМ ПРОСТРАНСТВЕ
- § 1. Базовая модель неоднородной распределенной системы
- § 2. Синхронизация в квазигармонической системе
- § 3. Случай релаксационной системы
- § 4. Приложения в химии и биологии
- § 5. Процессы установления синхронного режима
- § 6. Шумы и синхронизация
- § 7. Автоколебательные системы, связанные через общую среду
- ГЛАВА 11. ДИССИПАТИВНЫЕ СТРУКТУРЫ И ПРОБЛЕМЫ САМООРГАНИЗАЦИИ
- § 2. Контрастные диссипативные структуры; базовые модели
- § 3. Стационарные контрастные ДС типа складки
- § 4. Стационарные ДС типа сборки
- § 5. Устойчивость диссипативных структур
- § 6. Конкретные модели диссипативных структур
- § 7. Кинетика образования ДС
- § 8. Некоторые выводы
- ГЛАВА 12. ТЕРМОДИНАМИКА, ИНФОРМАЦИЯ, БИОЛОГИЯ
- § 1. Механика и статистика
- § 2. Информация и энтропия
- § 3. Ценность информации
- § 4. Биологическая информация
- § 5. Эффективность биологической информации
- ЗАКЛЮЧЕНИЕ