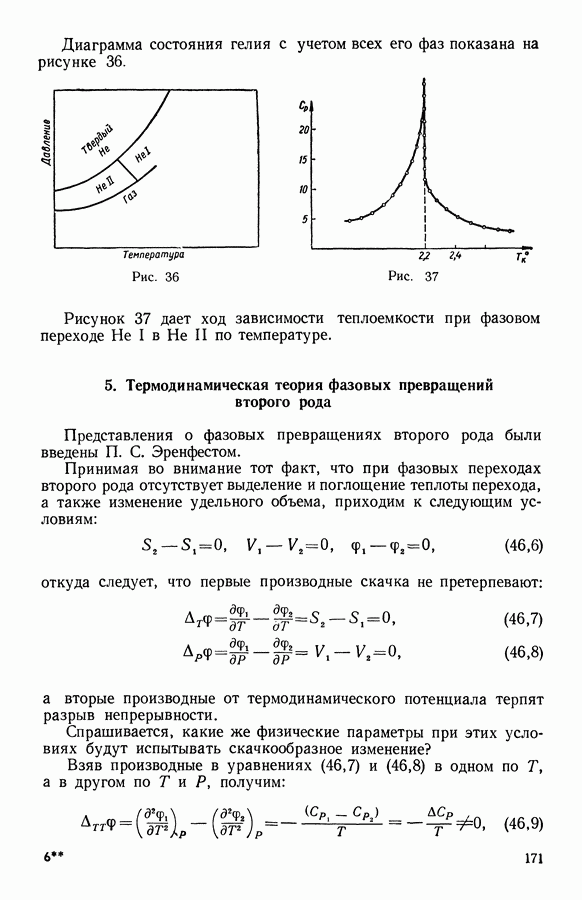
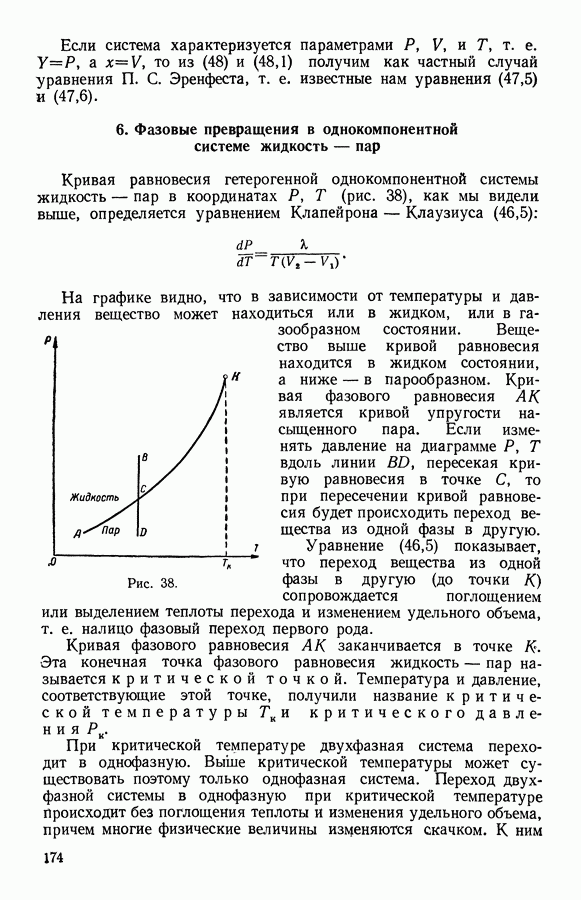
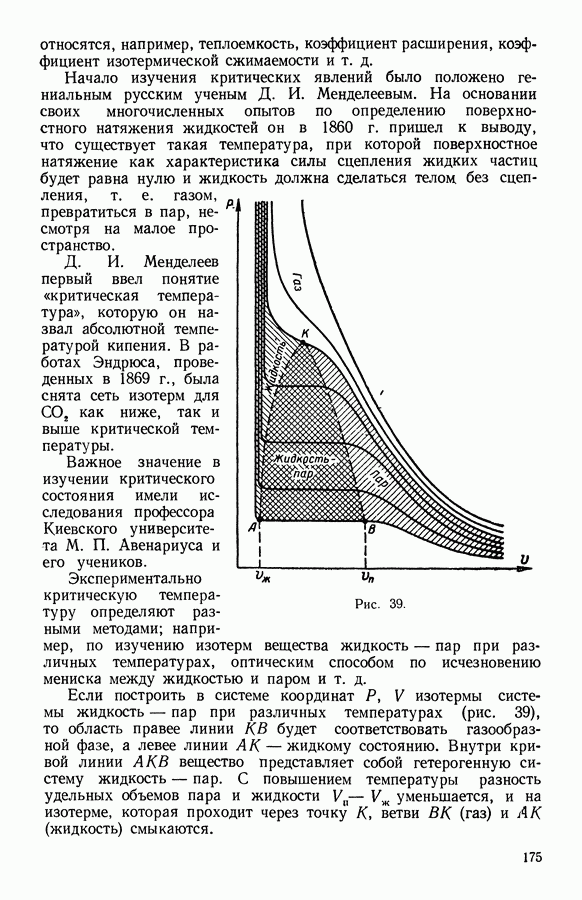
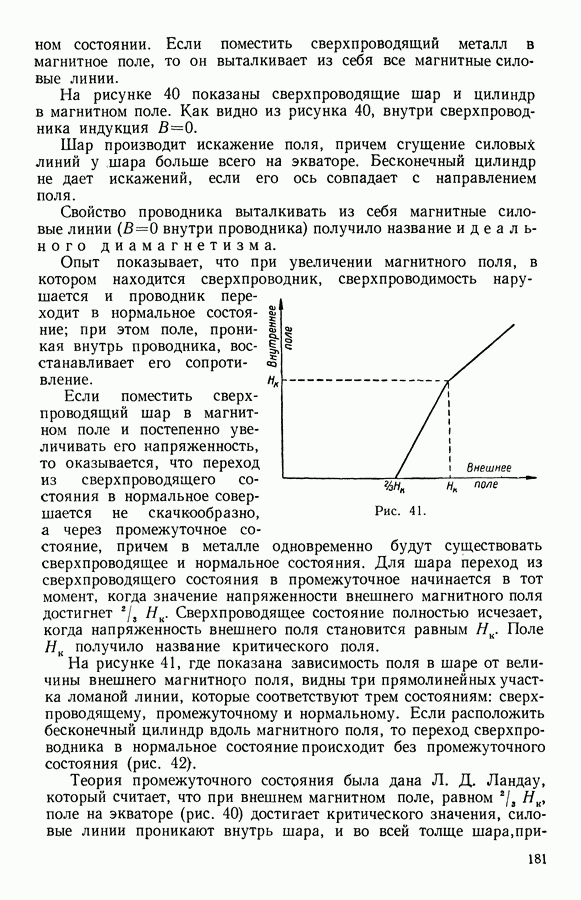
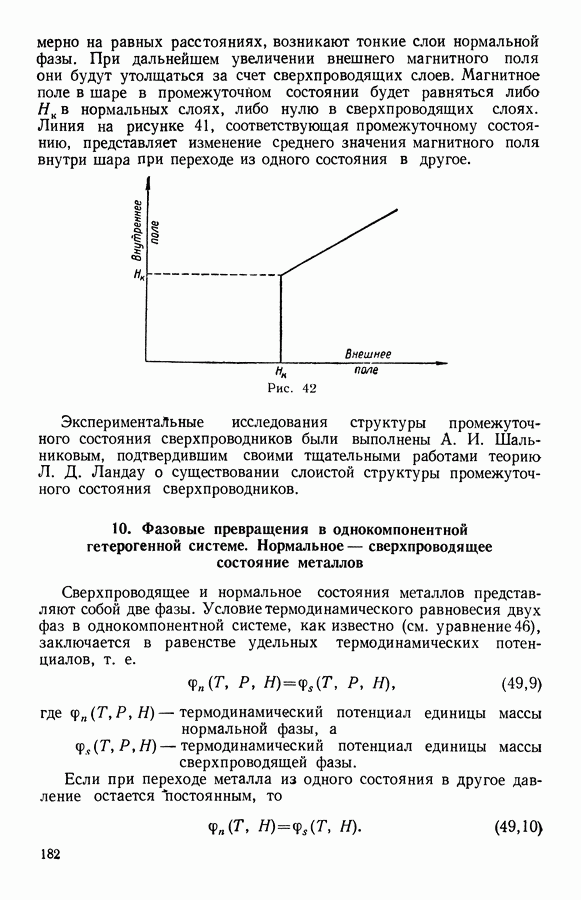
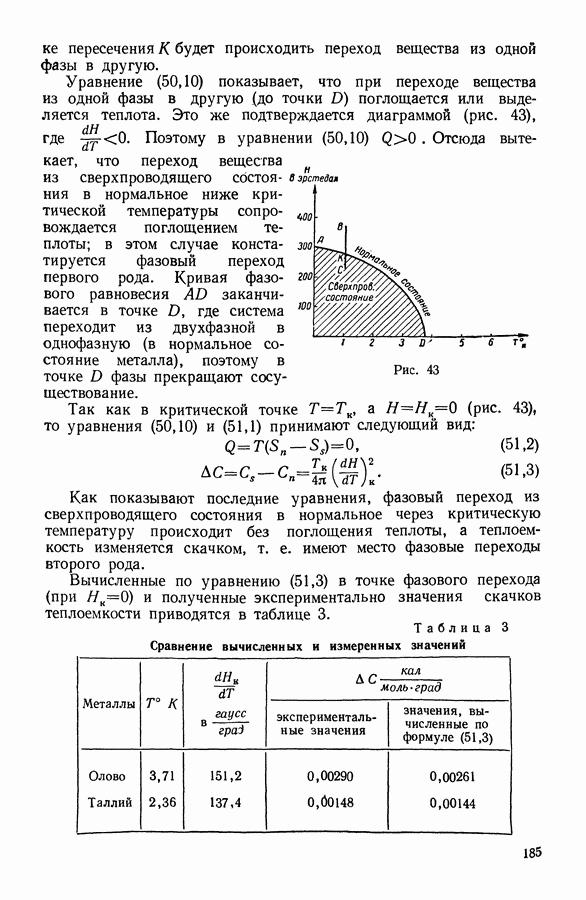
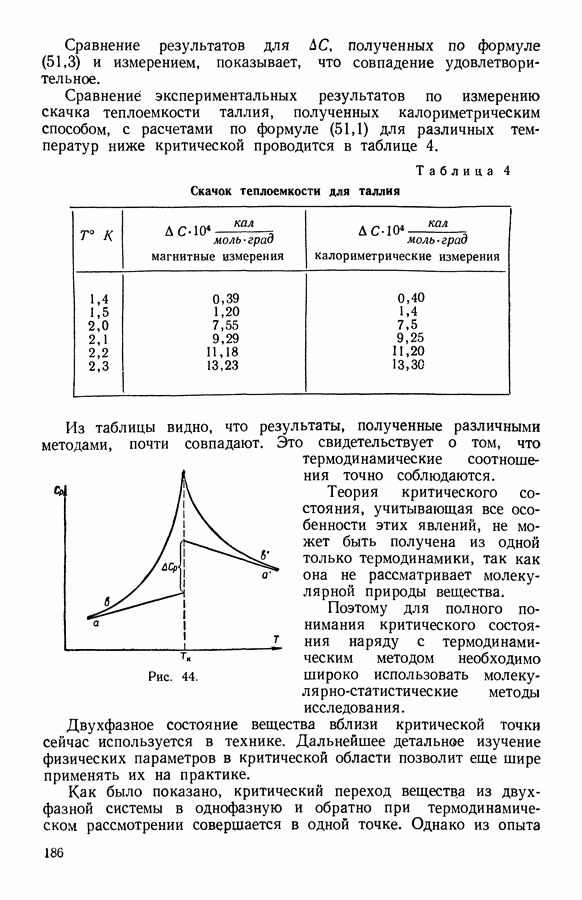
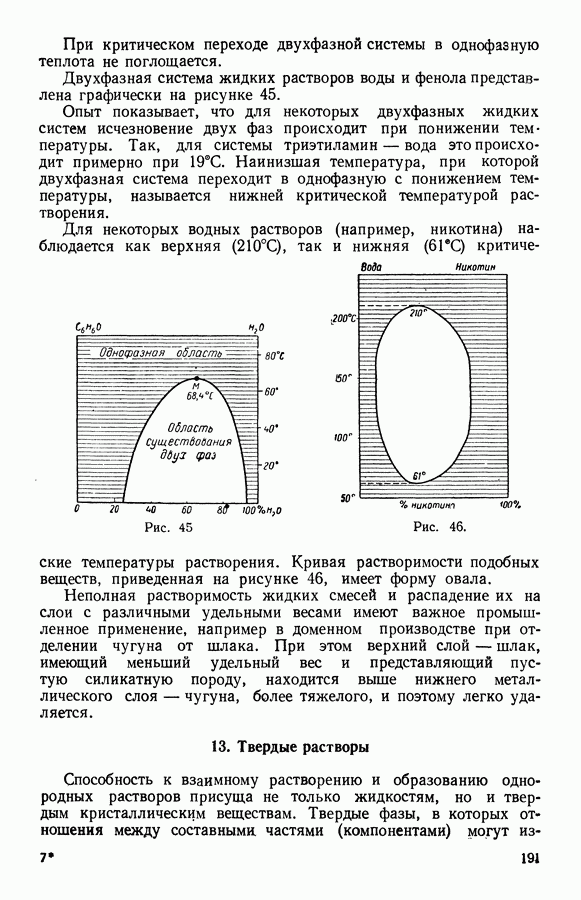
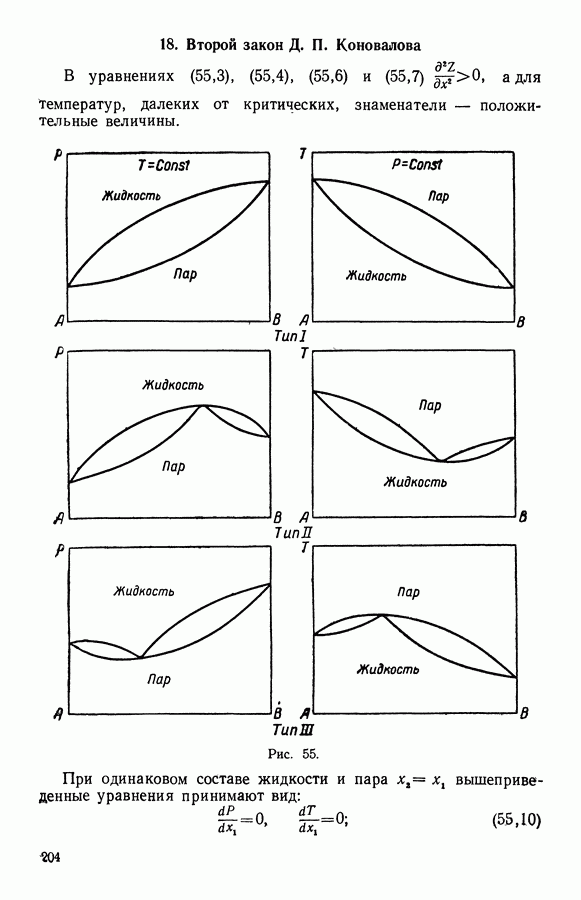
| Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
ВВЕДЕНИЕ
Предмет и метод термодинамики
Термодинамика представляет собой раздел теоретической физики и занимается изучением общих свойств физических и химических систем при равновесии. Кроме того, она рассматривает также общие закономерности, которые имеют место при установлении равновесия в системах.
Термодинамика исторически возникла как раздел физического учения о превращении теплоты в механическую работу. В настоящее время термодинамический метод исследования имеет широкое применение в различных разделах физики и физической химии. В зависимости от задач исследования термодинамику делят на физическую, химическую и техническую.
Физическая термодинамика изучает общие теоретические основы термодинамики, ее аксиоматику, а также устанавливает методы термодинамического исследования различных свойств изучаемых тел (систем).
Химическая термодинамика использует теоретические основы термодинамики и ее метод при исследовании химического и фазового равновесий, а также применяется при расчетах тепловых эффектов химических реакций.
Техническая термодинамика использует основные законы термодинамики при изучении взаимного превращения теплоты и работы. Основная цель ее — разработка теории тепловых двигателей.
В термодинамике применяются два метода исследования: метод круговых процессов и метод термодинамических функций и геометрических построений. Последний метод был разработан в классических работах Гиббса и получил за последнее время наибольшее распространение, так как он дает большие по сравнению с первым методом результаты.
Метод круговых процессов (принадлежащий Карно и Клаузиусу) позволил обосновать второй закон термодинамики, который приводит к определению абсолютной температуры и энтропии сначала для идеальных газов, а затем для любого вещества. Кроме того, метод круговых процессов позволяет доказать недостижимость абсолютного нуля температуры.
В работах Гельмгольца, Шиллера, а позднее Каратеодори и Афанасьевой-Эренфест аналитически было показано, что для определения абсолютной температуры и энтропии при равновесных процессах не требуется ни рассмотрения круговых процессов, ни допущения существования идеальных газов. Доказательство Шиллера — Каратеодори о существовании энтропии и абсолютной температуры основано на голономности дифференциального уравнения для количества теплоты.
Хотя в настоящей книге используются оба метода, однако предпочтение отдается методу термодинамических функций.
Термодинамика, в отличие от статистической физики, не базируется на определенной модели строения вещества, а исходит из небольшого числа весьма общих законов, полученных экспериментально. Оба метода исследования не исключают друг друга, а, наоборот, дополняют.
Основой термодинамического метода являются следующие общие законы:
1. Закон сохранения и превращения энергии.
2. Второй закон термодинамики, который утверждает, что теплота самопроизвольно не может переходить от тел менее нагретых к телам более нагретым. Этот закон определяет направление, по которому протекают процессы в природе; второй закон термодинамики имеет более ограниченную сферу применения, чем закон сохранения и превращения энергии.
3. Третий закон термодинамики, постулирующий, что абсолютный нуль температуры недостижим. Закон этот имеет еще более ограниченное значение, чем второй и особенно первый законы термодинамики.
Основное содержание и ценность термодинамического метода исследования состоит в том, что он, используя основные начала (законы) термодинамики, позволяет установить теоретическим путем ряд закономерностей изменения различных свойств тел.
Кроме указанных выше законов термодинамики, необходимо знать также уравнение состояния, которое может быть получено либо из молекулярно-кинетической теории, либо опытным путем.
| Следующий параграф >> |
Оглавление
- ВВЕДЕНИЕ
- ГЛАВА ПЕРВАЯ. ОСНОВНЫЕ ПОНЯТИЯ
- 1. Макроскопическая система
- 2. Состояние макроскопической система
- 3. Термодинамический процесс
- 4. Равновесное состояние
- 5. Функция состояния
- 6. Закон сохранения и превращения энергии
- 7. Внутренняя энергия системы
- 8. Количество теплоты
- 9. Температура
- 10. Работа
- 11. Условие полного дифференциала
- ГЛАВА ВТОРАЯ. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 1. Внутренняя энергия как функция состояния системы
- 2. Аддитивность внутренней энергии
- 3. Количественная формулировка первого закона для различных термодинамических систем
- 4. Определение теплоемкости
- 5. Применение первого закона термодинамики к некоторым простейшим процессам
- 6. Идеальный газ
- 7. Уравнение Майера для идеального газа
- 8. Адиабатный процесс
- 9. Уравнение адиабаты для идеального газа
- 10. Политропические процессы
- 11. Уравнение адиабаты для общего случая
- 12. Связь между модулями упругости и отношением теплоемкостей …
- 13. Связь отношения теплоемкостей со скоростью звука
- 14. Теплота процесса
- 15. Закон Гесса
- 16. Уравнение Кирхгофа
- ГЛАВА ТРЕТЬЯ. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
- 1. Необратимые процессы
- 2. Равновесные (обратимые) процессы
- 3. Значение равновесных (обратимых) процессов
- 4. Формулировка Клаузиуса
- 5. Формулировка Томсона
- 6. Циклы
- 7. Обратимый цикл Карно
- 8. Обратимый цикл Карно с идеальным газом
- 9. Эквивалентность формулировок Клаузиуса и Томсона
- 10. Теорема Карно
- 11. Количественная формулировка второго закона
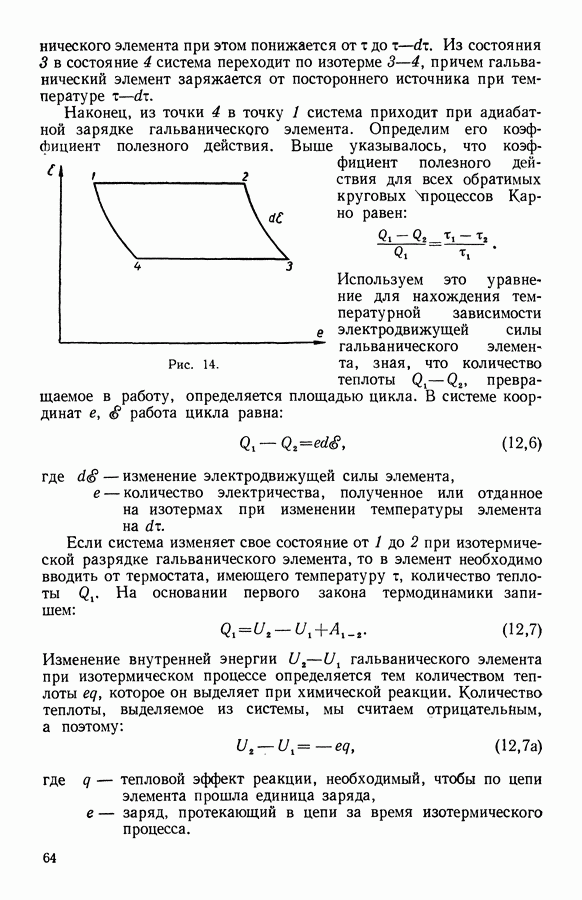
- 12. Зависимость электродвижущей силы гальванического элемента от температуры
- 13. Температурная шкала
- 14. Разнообразие шкал
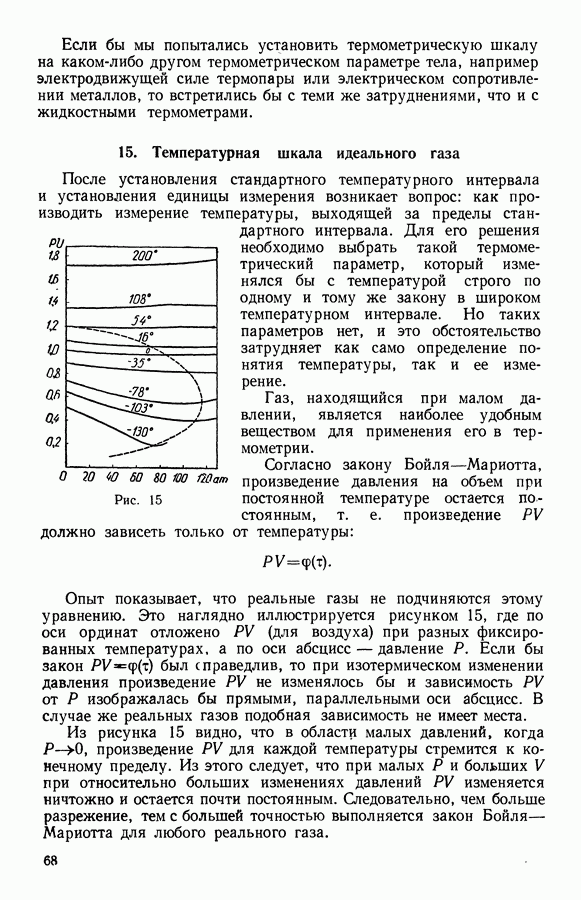
- 15. Температурная шкала идеального газа
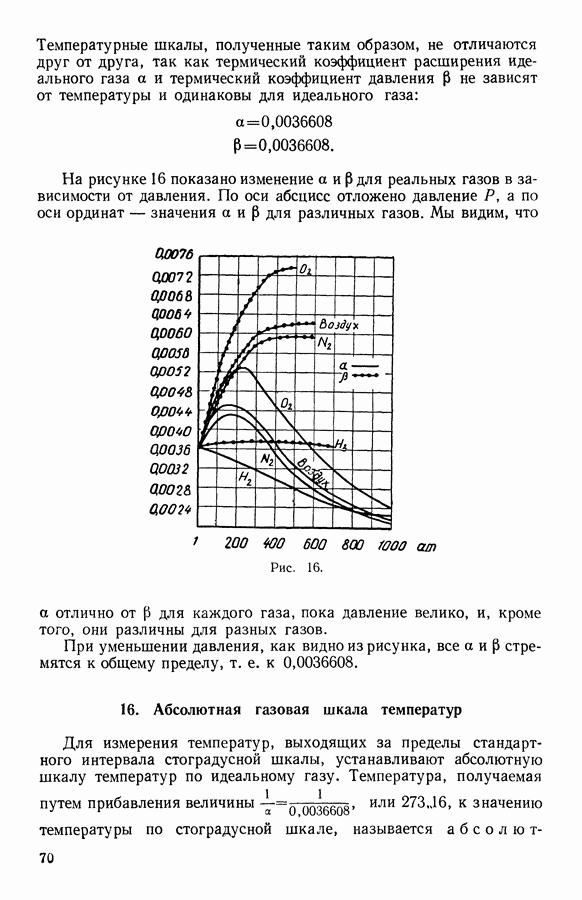
- 16. Абсолютная газовая шкала температур
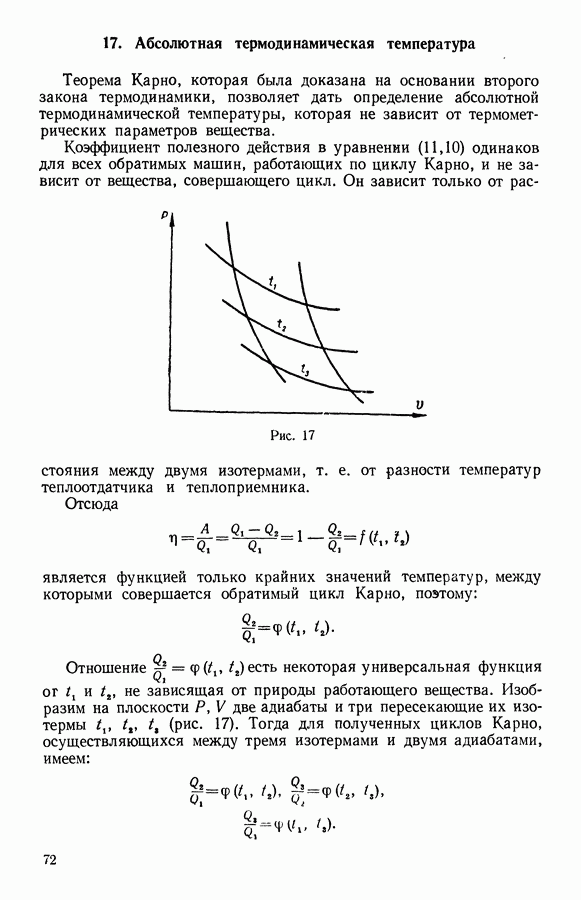
- 17. Абсолютная термодинамическая температура
- 18. Тождество шкалы идеального газа и газа, подчиняющегося уравнению Ван-дер-Ваальса, с термодинамической шкалой
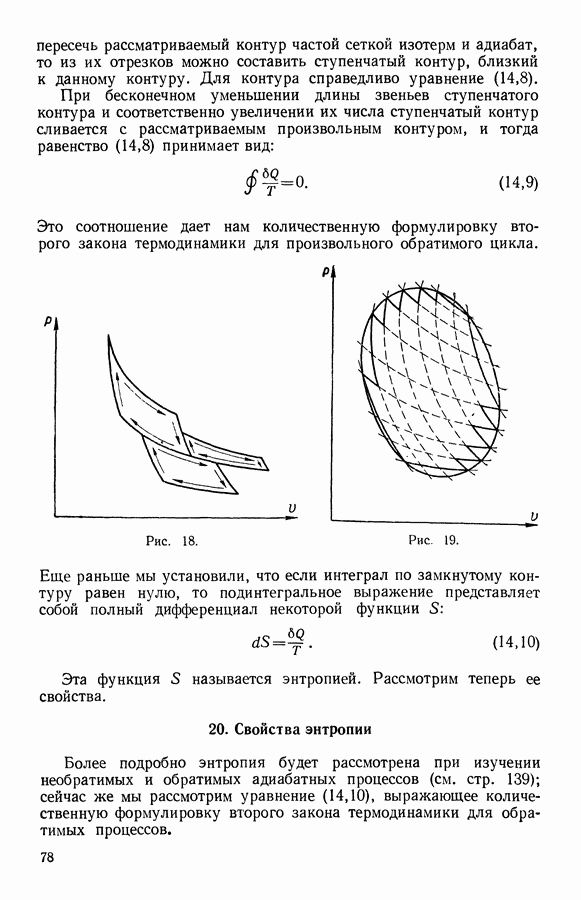
- 19. Обобщение количественной формулировки второго закона термодинамики
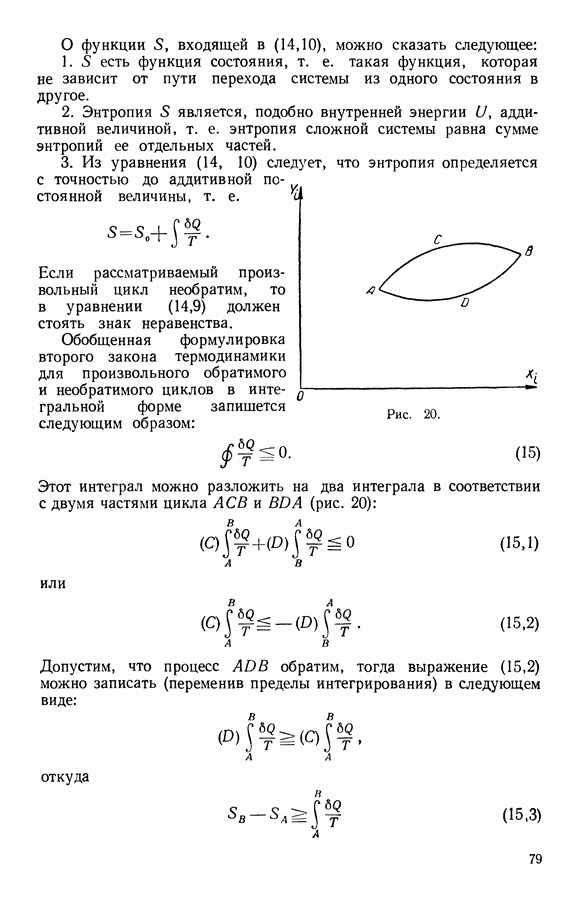
- 20. Свойства энтропии
- 21. Аксиоматика второго закона термодинамики для равновесных (обратимых) процессов
- 22. Статистический характер второго закона термодинамики
- ГЛАВА ЧЕТВЕРТАЯ. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ
- 2. Внутренняя энергия
- 3. Энтальпия
- 4. Свободная энергия
- 5. Термодинамический потенциал
- ГЛАВА ПЯТАЯ. РЕШЕНИЕ КОНКРЕТНЫХ ЗАДАЧ С ПОМОЩЬЮ ТЕРМОДИНАМИЧЕСКИХ ФУНКЦИЙ
- 1. Вычисление энтропии при изменении агрегатного состояния при изотермическом процессе
- 2. Уравнение Клапейрона — Клаузиуса
- 3. Зависимость поверхностного натяжения от температуры
- 4. Энтропия как функция Т и x
- 5. Энтропия как функция T и Y
- 6. Энтропия как функция x и Y
- 7. Вычисление Cy-Cx
- 8. Связь теплоемкостей со скоростью звука
- 9. Зависимость Cv от объема
- 10. Зависимость Ср от давления
- 11. Изменение температуры в адиабатных системах
- 12. Уравнение адиабаты для газа, подчиняющегося уравнению Ван-дер-Ваальса
- 13. Уравнение Гиббса — Гельмгольца
- 14. Уравнение максимальной работы
- 15. Поверхностная энергия чистой жидкости
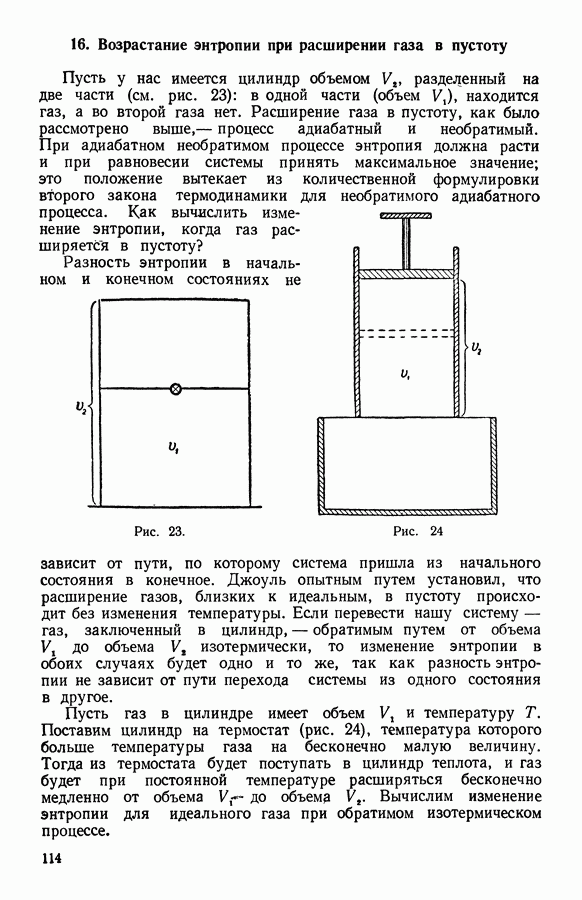
- 16. Возрастание энтропии при расширении газа в пустоту
- 17. Явление Джоуля — Томсона (дроссельный эффект)
- 18. Изотермическое дросселирование
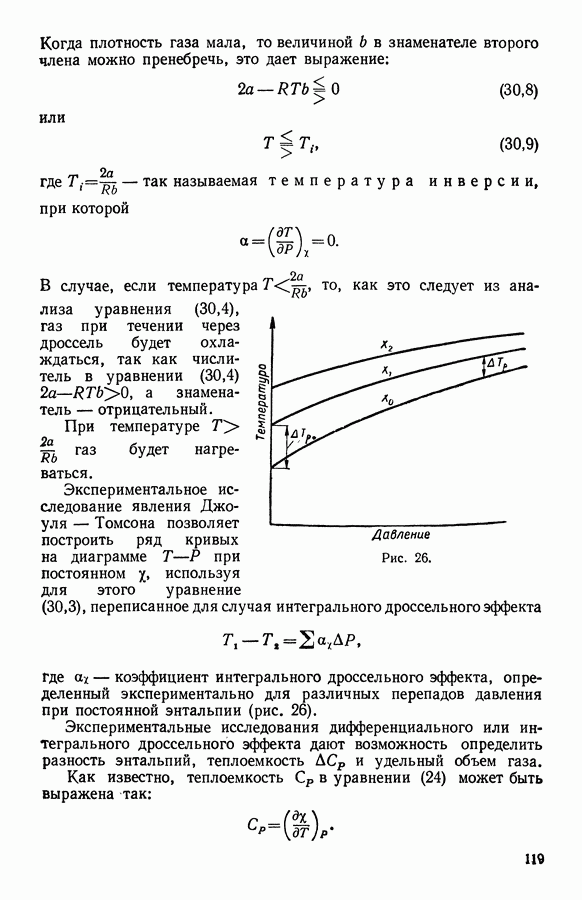
- 19. Методы определения дифференциального и интегрального адиабатного дроссельного эффекта
- 20. Задачи
- ГЛАВА ШЕСТАЯ. ТЕРМОДИНАМИКА ИЗЛУЧЕНИЯ
- 1. Тепловое излучение
- 2. Закон Кирхгофа
- 3. Световое давление
- 4. Закон Стефана — Больцмана
- 5. Формула и закон смещения Вина
- ГЛАВА СЕДЬМАЯ. ТЕРМОДИНАМИЧЕСКОЕ УЧЕНИЕ О РАВНОВЕСИИ
- 2. Гетерогенная и гомогенная системы
- 3. Компоненты
- 4. Необратимые процессы и общие условия равновесия
- 5. Химический потенциал
- 6. Идеальные газовые смеси
- 7. Свободная энергия системы идеальных газов до смешения
- 8. Свободная энергия идеальных газов после смешения
- 9. Химический потенциал компонента идеального газа
- 10. Термодинамический вывод закона действующих масс
- 11. Термодинамический вывод уравнения работы химической реакции
- 12. Зависимость константы равновесия от температуры
- 13. Зависимость константы равновесия Ky от давления
- 14. Условие равновесия в гетерогенной системе
- 14. Правило фаз
- ГЛАВА ВОСЬМАЯ. ФАЗОВЫЕ ПРЕВРАЩЕНИЯ
- 1. Фазовые превращения в однокомпонентных системах
- 2. Фазовые превращения первого рода
- 3. Общее уравнение равновесия двух фаз однокомпонентной системы
- 4. Фазовые превращения второго рода
- 5. Термодинамическая теория фазовых превращений второго рода
- 6. Фазовые превращения в однокомпонентной системе жидкость — пар
- 7. Термодинамическое условие равновесия системы жидкость — пар в критическом состоянии
- 8. Определение … из уравнения Ван-дер-Ваальса
- 9. Сверхпроводящее состояние металлов
- 10. Фазовые превращения в однокомпонентной гетерогенной системе. Нормальное — сверхпроводящее состояние металлов
- 11. Бинарные системы
- 12. О взаимной растворимости жидкостей
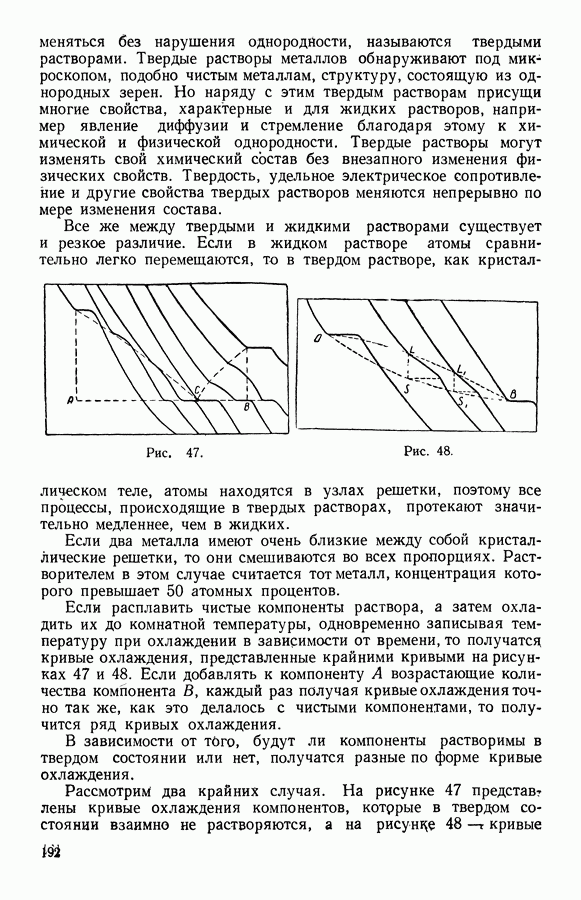
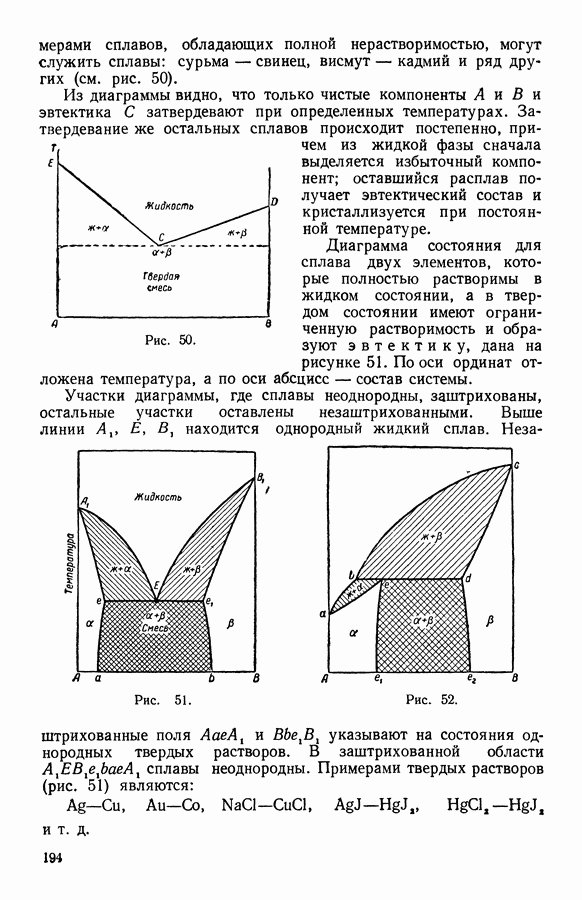
- 13. Твердые растворы
- 14. Уравнение Ван-дер-Ваальса для бинарных смесей
- 15. Разбавленные растворы
- 16. Растворимость газа в жидкости
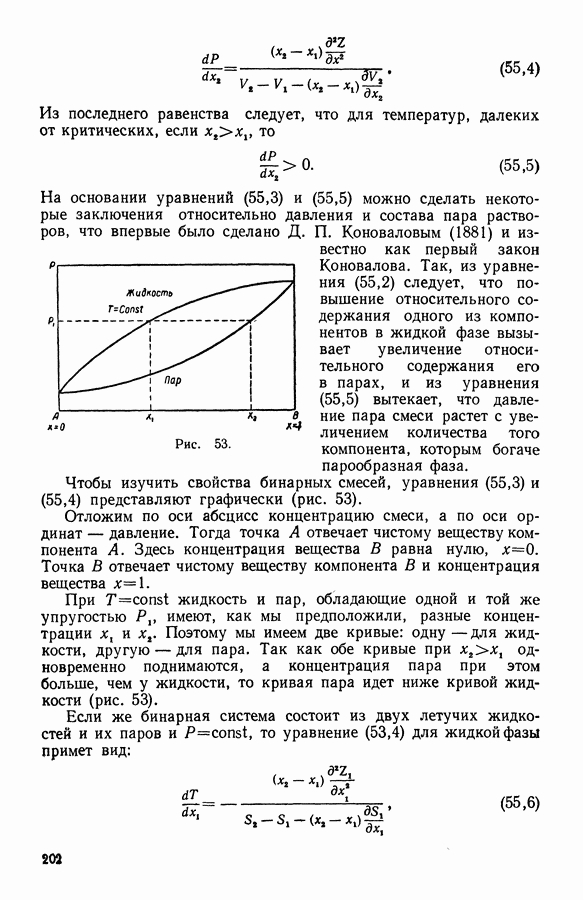
- 17. Первый закон Д. П. Коновалова
- 18. Второй закон Д. П. Коновалова
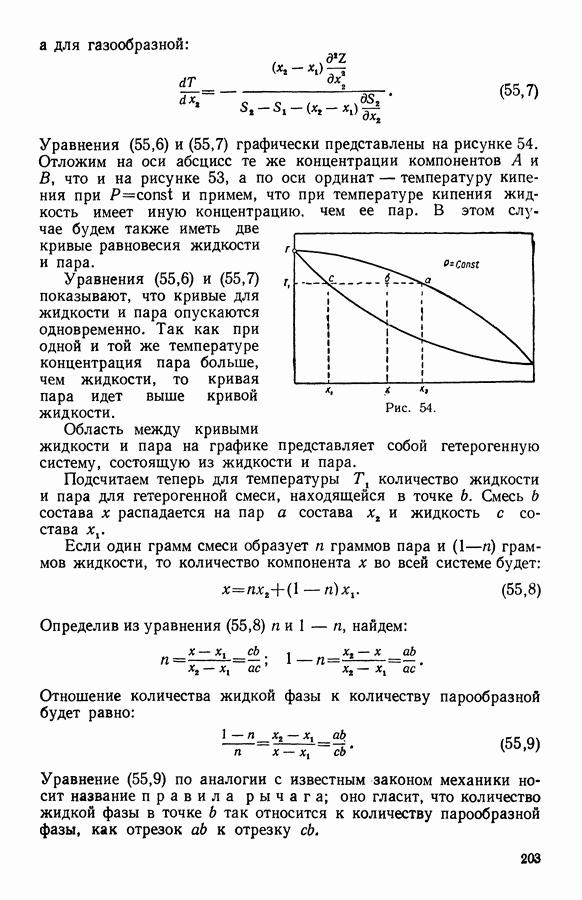
- 19. Температура кипения раствора и дистилляция двойных смесей
- ГЛАВА ДЕВЯТАЯ. НИЗКИЕ ТЕМПЕРАТУРЫ
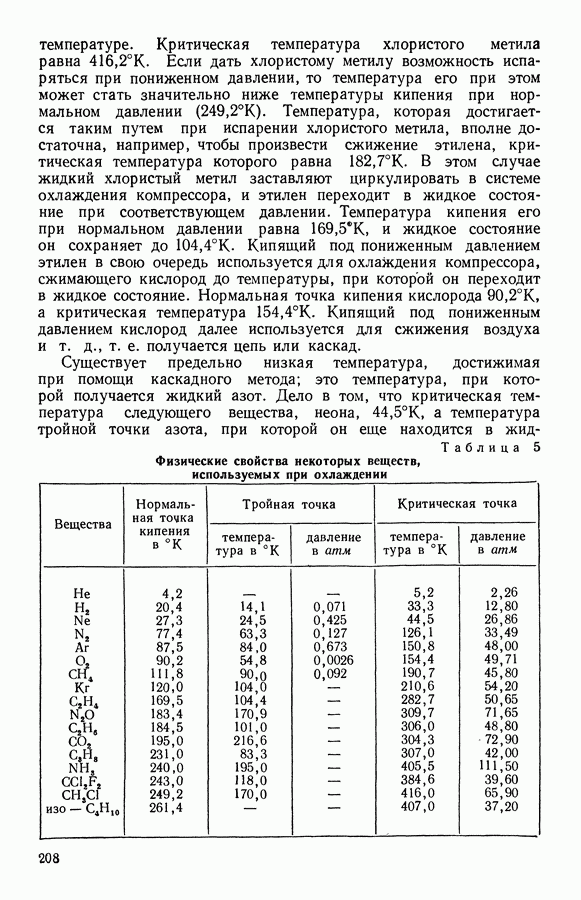
- 1. Получение низких температур, их значение для техники и научных исследований
- 2. Каскадный метод
- 3. Метод дросселирования
- 4. Получение низких температур при расширении сжатого газа с отдачей внешней работы
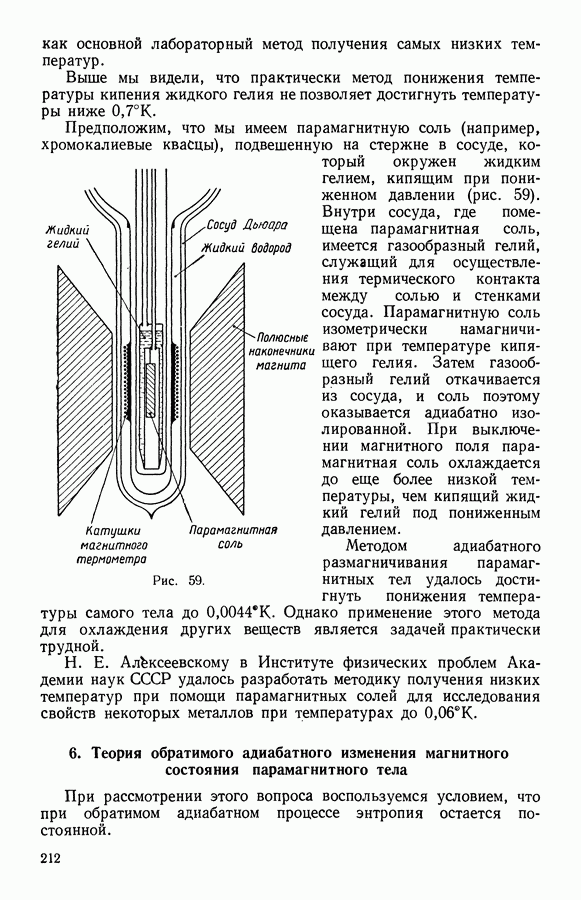
- 5. Охлаждение методом адиабатного размагничивания
- 6. Теория обратимого адиабатного изменения магнитного состояния парамагнитного тела
- 7. Тепловая теорема Нернста
- 8. О третьем законе термодинамики
- 9. Свойства вещества вблизи абсолютного нуля
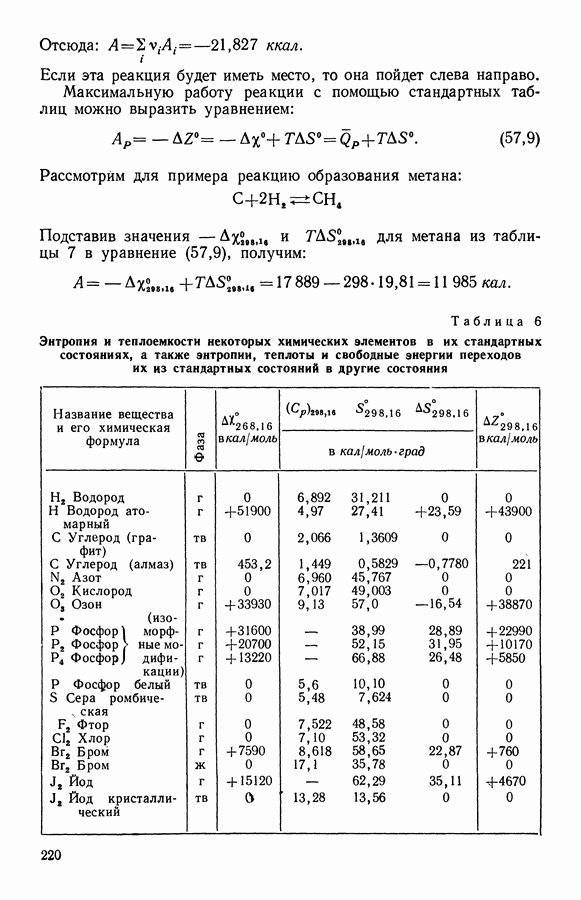
- 10. Стандартные таблицы термодинамических функций
- 11. Вычисление стандартных величин при изменении температуры
- 12. Вычисление стандартных величин при изменении давления
- 13. Применение стандартных таблиц
- 14. Вычисление стандартных величин
- 15. Задачи для всех разделов курса