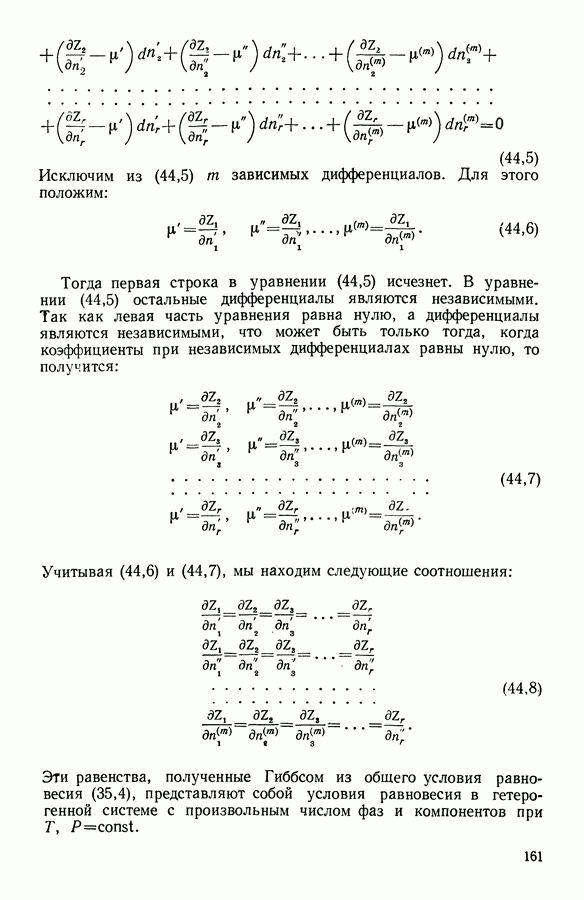
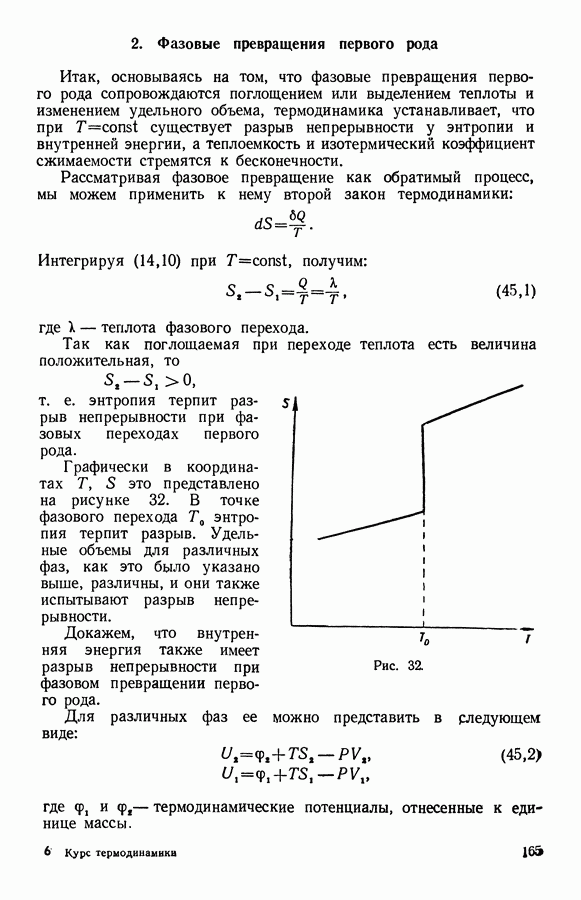
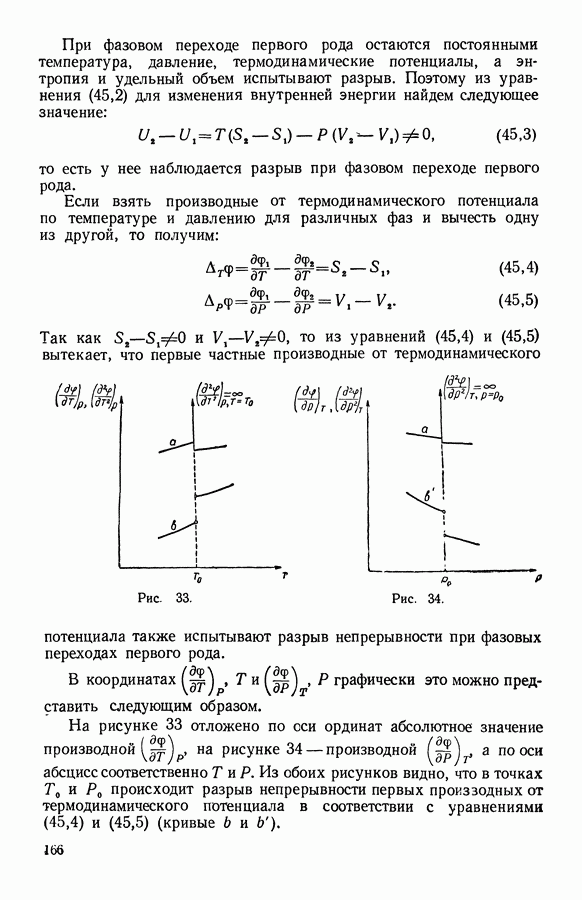
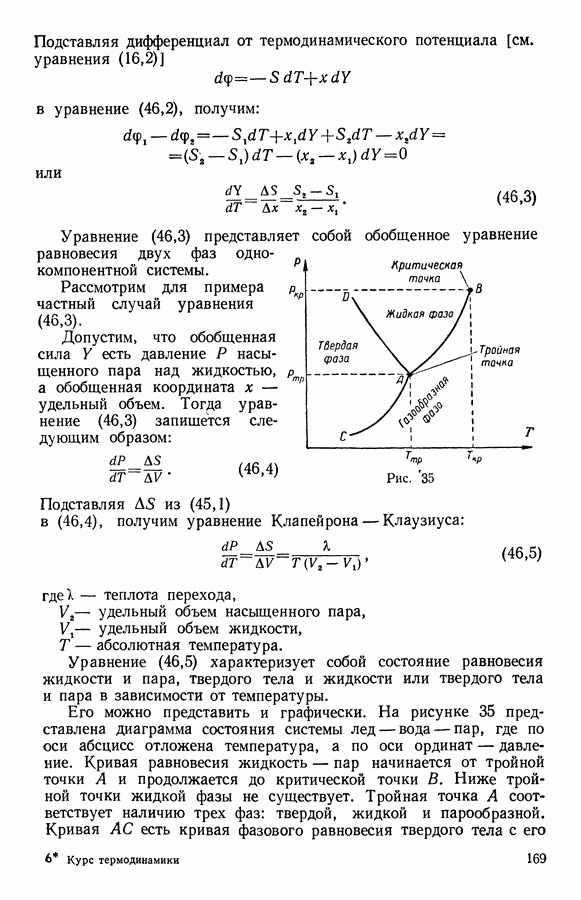
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
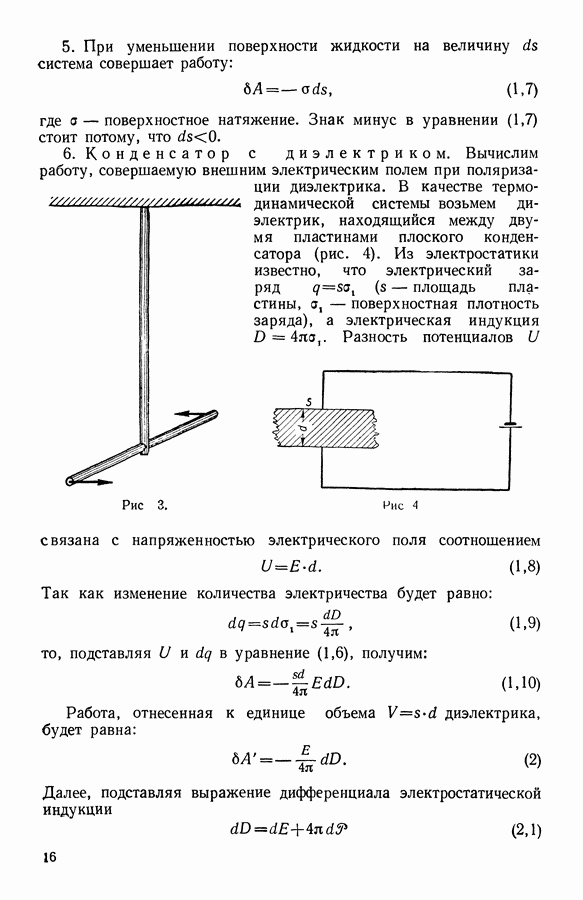
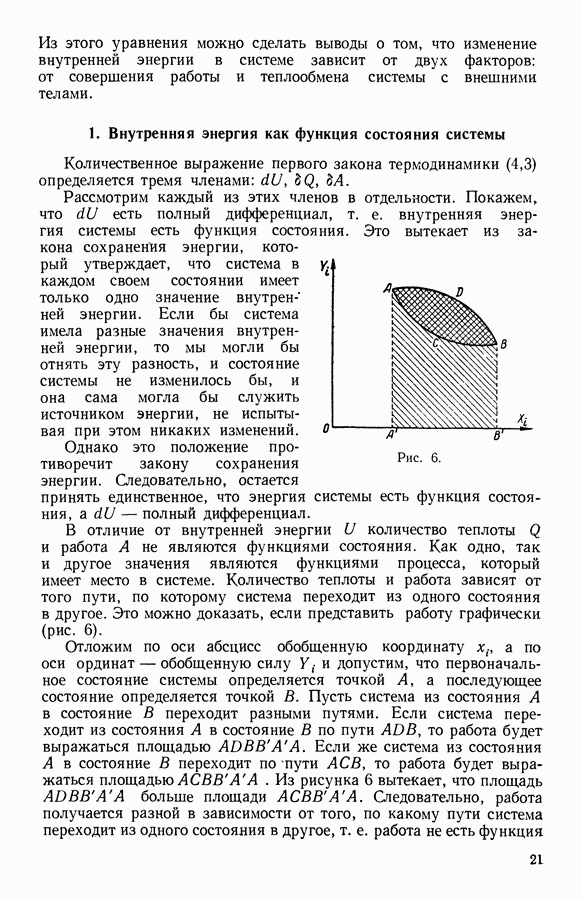
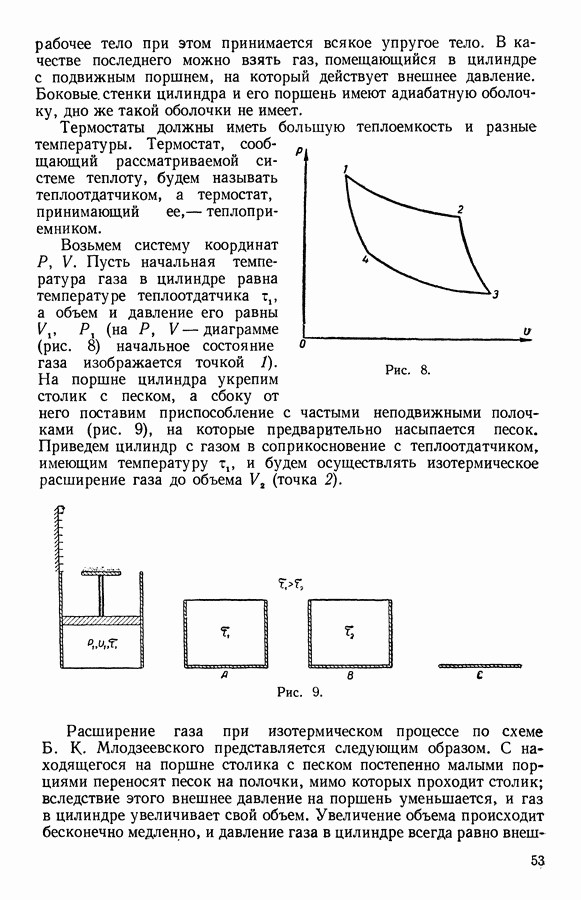
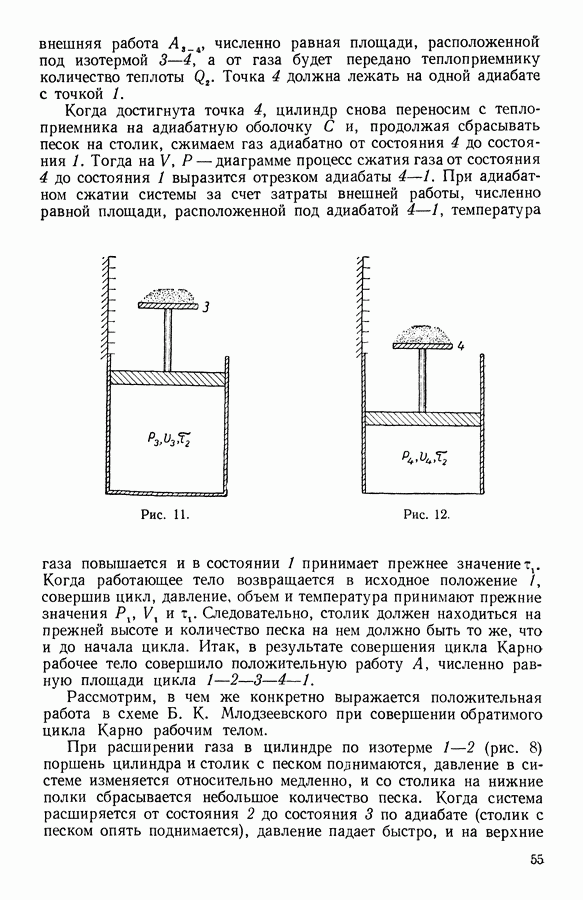
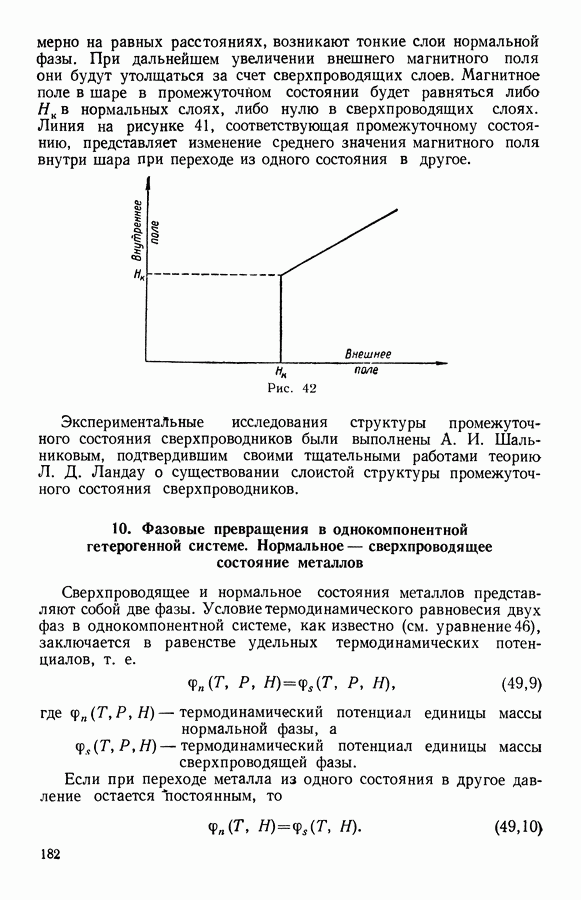
12. Зависимость электродвижущей силы гальванического элемента от температуры
Электродвижущая сила гальванического элемента зависит от химического состава электролита и электродов, а также от температуры элемента и давления в нем. Применим второй закон термодинамики к обратимому гальваническому элементу.
Обратимыми гальваническими элементами называются такие элементы, в которых при пропускании тока в противоположном направлении происходят обратные химические реакции. Если сила тока мала и джоулевым теплом можно пренебречь, то прохождение тока через такой элемент можно рассматривать как обратимый процесс.
Возьмем систему координат  Отложим по оси абсцисс заряд
Отложим по оси абсцисс заряд  проходящий по гальванической цепи, а по оси ординат
проходящий по гальванической цепи, а по оси ординат  гальванического элемента
гальванического элемента 
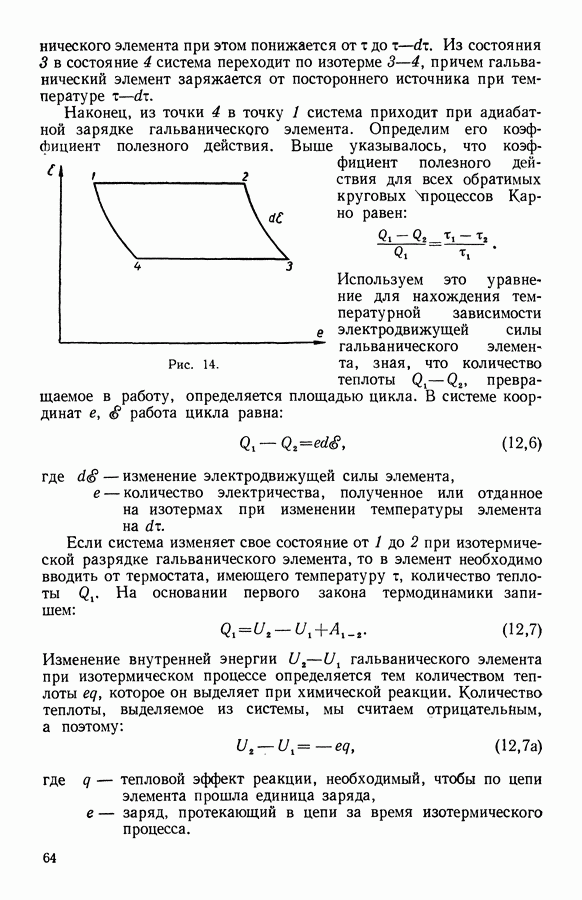
Начальное состояние системы на диаграмме  изображается точкой 1 (рис. 14).
изображается точкой 1 (рис. 14).
При изотермическом процессе разрядки гальванического элемента его электродвижущая сила остается постоянной и изотерма 1—2 в цикле Карно представится прямой, параллельной оси абсцисс. При переводе системы из состояния 2 в состояние 3 разрядка гальванического элемента ведется адиабатически и температура
гальванического элемента при этом понижается от  до
до  Из состояния 3 в состояние 4 система переходит по изотерме 3—4, причем гальванический элемент заряжается от постороннего источника при температуре
Из состояния 3 в состояние 4 система переходит по изотерме 3—4, причем гальванический элемент заряжается от постороннего источника при температуре 

Рис. 14.
Наконец, из точки 4 в точку 1 система приходит при адиабатной зарядке гальванического элемента. Определим его коэффициент полезного действия. Выше указывалось, что коэффициент полезного действия для всех обратимых круговых Процессов Карно равен:

Используем это уравнение для нахождения температурной зависимости электродвижущей силы гальванического элемента, зная, что количество теплоты  превращаемое в работу, определяется площадью цикла. В системе координат
превращаемое в работу, определяется площадью цикла. В системе координат  работа цикла равна:
работа цикла равна:

где  изменение электродвижущей силы элемента,
изменение электродвижущей силы элемента,  количество электричества, полученное или отданное на изотермах при изменении температуры элемента на
количество электричества, полученное или отданное на изотермах при изменении температуры элемента на 
Если система изменяет свое состояние от 1 до 2 при изотермической разрядке гальванического элемента, то в элемент необходимо вводить от термостата, имеющего температуру  количество теплоты
количество теплоты  На основании первого закона термодинамики запишем:
На основании первого закона термодинамики запишем:

Изменение внутренней энергии  гальванического элемента при изотермическом процессе определяется тем количеством теплоты
гальванического элемента при изотермическом процессе определяется тем количеством теплоты  которое он выделяет при химической реакции. Количество теплоты, выделяемое из системы, мы считаем отрицательным, а поэтому:
которое он выделяет при химической реакции. Количество теплоты, выделяемое из системы, мы считаем отрицательным, а поэтому:

где  тепловой эффект реакции, необходимый, чтобы по цепи элемента прошла единица заряда,
тепловой эффект реакции, необходимый, чтобы по цепи элемента прошла единица заряда,  заряд, протекающий в цепи за время изотермического процесса.
заряд, протекающий в цепи за время изотермического процесса.
Подставляя это значение в выражение первого закона, получим:

Уравнение (12,8) показывает, что при изотермической разрядке гальванического элемента работа на изотерме 1—2 производится за счет теплоты, притекающей из термостата  и теплоты реакции
и теплоты реакции 
Работа на изотерме 1—2 по формуле (1,6) равна:

Подставив и  в уравнение (12,8), получим:
в уравнение (12,8), получим:

Заменяя во втором законе термодинамики  их значениями из уравнений (12,6) и (12,9), находим:
их значениями из уравнений (12,6) и (12,9), находим:

или

Полученное уравнение устанавливает зависимость электродвижущей силы гальванического элемента от температуры. Это уравнение называется уравнением Гельмгольца. Электродвижущая сила гальванического элемента может быть больше или меньше теплового эффекта реакции в зависимости от знака перед  Если электродвижущая сила мало зависит от температуры, т. е. если величиной
Если электродвижущая сила мало зависит от температуры, т. е. если величиной  можно пренебречь, то электродвижущая сила гальванического элемента определяется из теплоты реакции в нем при прохождении по цепи заряда в один кулон.
можно пренебречь, то электродвижущая сила гальванического элемента определяется из теплоты реакции в нем при прохождении по цепи заряда в один кулон.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ВВЕДЕНИЕ
- ГЛАВА ПЕРВАЯ. ОСНОВНЫЕ ПОНЯТИЯ
- 1. Макроскопическая система
- 2. Состояние макроскопической система
- 3. Термодинамический процесс
- 4. Равновесное состояние
- 5. Функция состояния
- 6. Закон сохранения и превращения энергии
- 7. Внутренняя энергия системы
- 8. Количество теплоты
- 9. Температура
- 10. Работа
- 11. Условие полного дифференциала
- ГЛАВА ВТОРАЯ. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 1. Внутренняя энергия как функция состояния системы
- 2. Аддитивность внутренней энергии
- 3. Количественная формулировка первого закона для различных термодинамических систем
- 4. Определение теплоемкости
- 5. Применение первого закона термодинамики к некоторым простейшим процессам
- 6. Идеальный газ
- 7. Уравнение Майера для идеального газа
- 8. Адиабатный процесс
- 9. Уравнение адиабаты для идеального газа
- 10. Политропические процессы
- 11. Уравнение адиабаты для общего случая
- 12. Связь между модулями упругости и отношением теплоемкостей …
- 13. Связь отношения теплоемкостей со скоростью звука
- 14. Теплота процесса
- 15. Закон Гесса
- 16. Уравнение Кирхгофа
- ГЛАВА ТРЕТЬЯ. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
- 1. Необратимые процессы
- 2. Равновесные (обратимые) процессы
- 3. Значение равновесных (обратимых) процессов
- 4. Формулировка Клаузиуса
- 5. Формулировка Томсона
- 6. Циклы
- 7. Обратимый цикл Карно
- 8. Обратимый цикл Карно с идеальным газом
- 9. Эквивалентность формулировок Клаузиуса и Томсона
- 10. Теорема Карно
- 11. Количественная формулировка второго закона
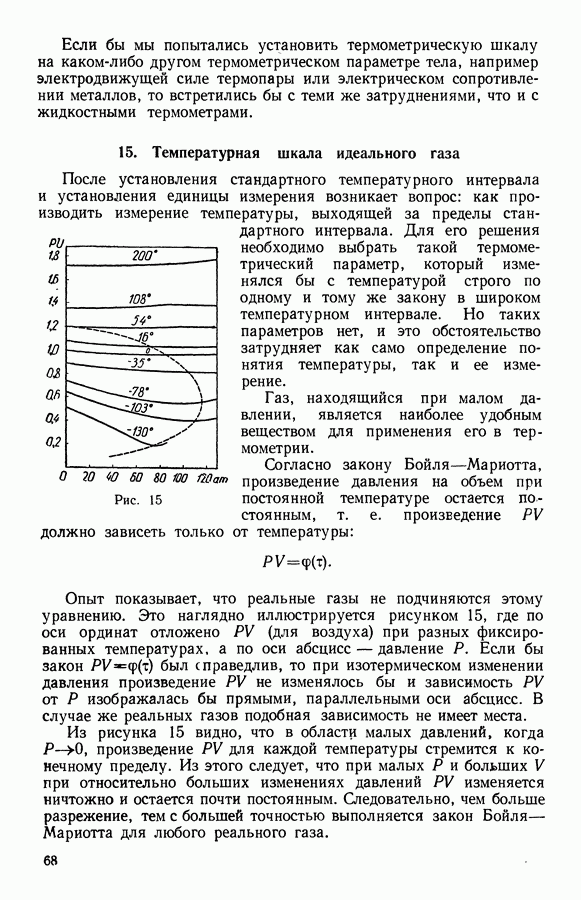
- 12. Зависимость электродвижущей силы гальванического элемента от температуры
- 13. Температурная шкала
- 14. Разнообразие шкал
- 15. Температурная шкала идеального газа
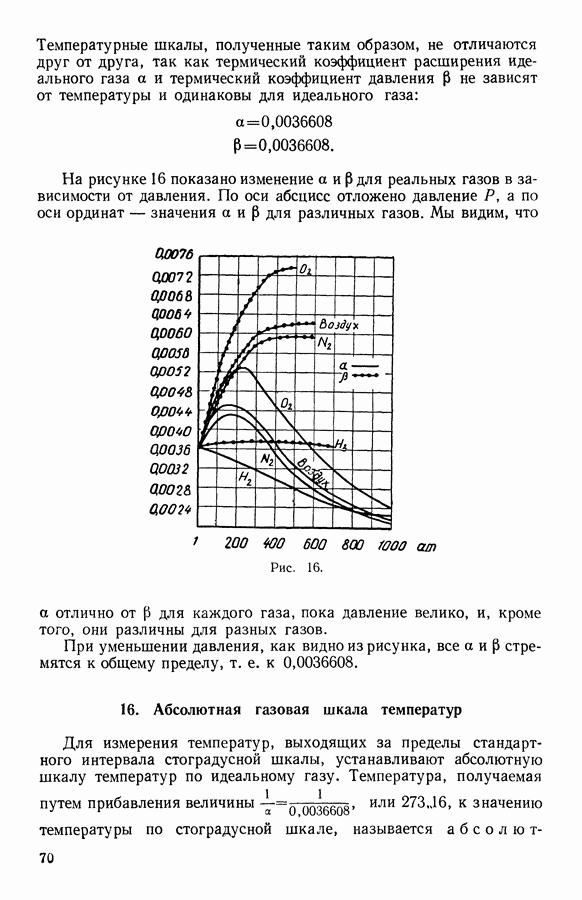
- 16. Абсолютная газовая шкала температур
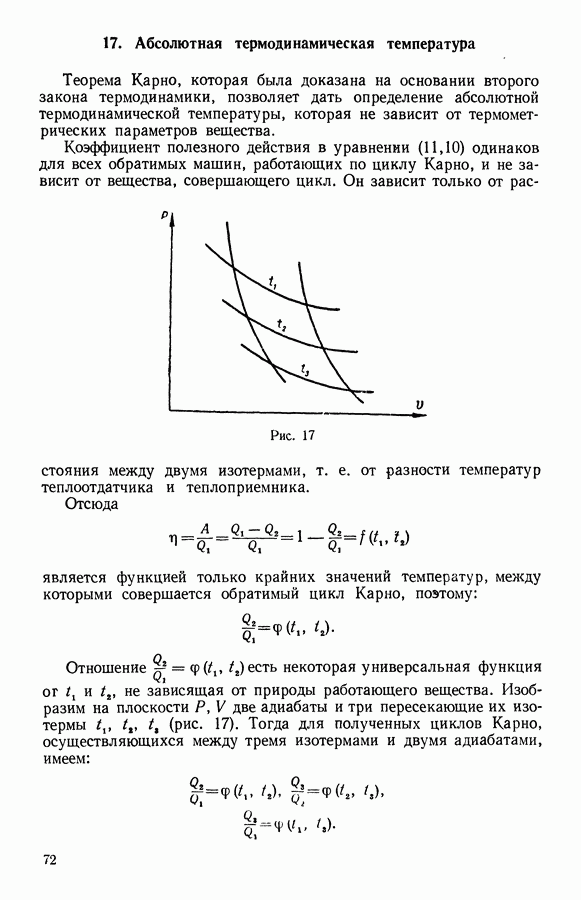
- 17. Абсолютная термодинамическая температура
- 18. Тождество шкалы идеального газа и газа, подчиняющегося уравнению Ван-дер-Ваальса, с термодинамической шкалой
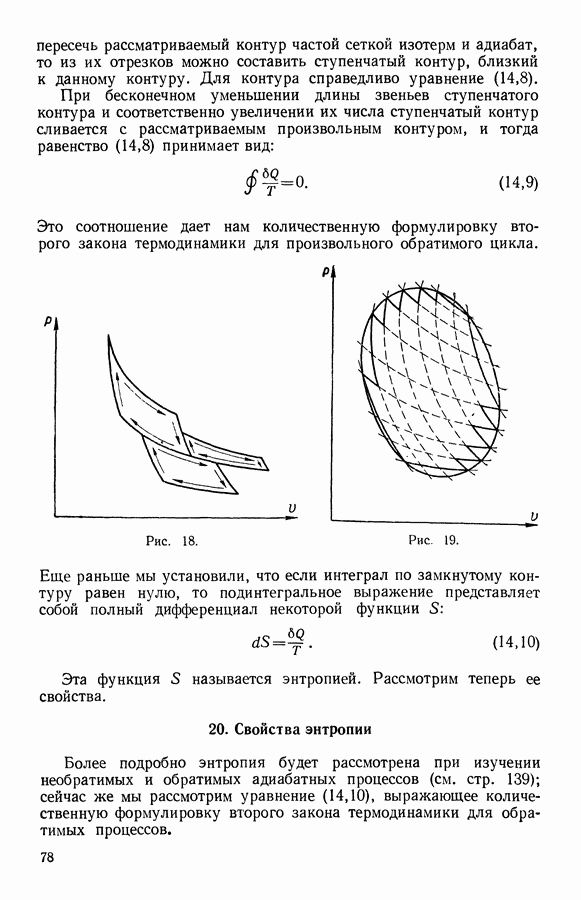
- 19. Обобщение количественной формулировки второго закона термодинамики
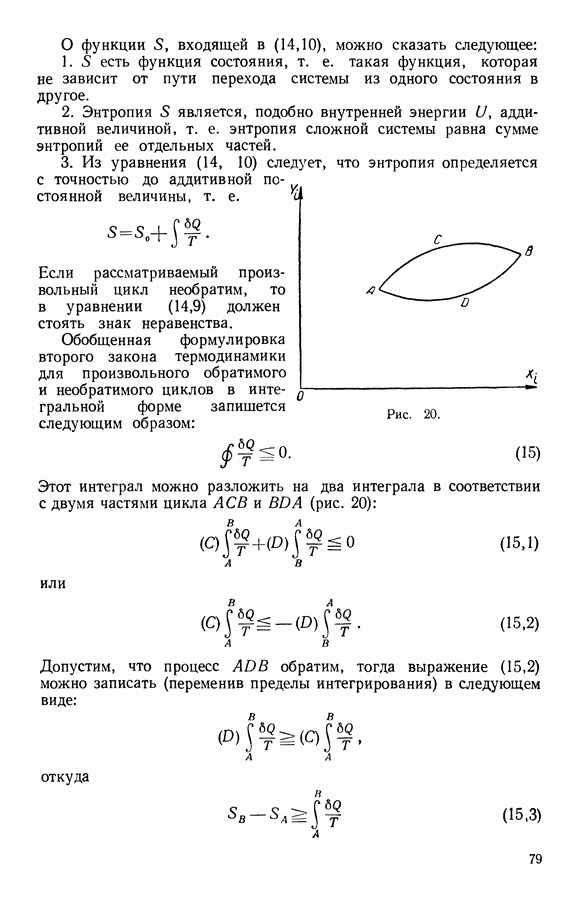
- 20. Свойства энтропии
- 21. Аксиоматика второго закона термодинамики для равновесных (обратимых) процессов
- 22. Статистический характер второго закона термодинамики
- ГЛАВА ЧЕТВЕРТАЯ. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ
- 2. Внутренняя энергия
- 3. Энтальпия
- 4. Свободная энергия
- 5. Термодинамический потенциал
- ГЛАВА ПЯТАЯ. РЕШЕНИЕ КОНКРЕТНЫХ ЗАДАЧ С ПОМОЩЬЮ ТЕРМОДИНАМИЧЕСКИХ ФУНКЦИЙ
- 1. Вычисление энтропии при изменении агрегатного состояния при изотермическом процессе
- 2. Уравнение Клапейрона — Клаузиуса
- 3. Зависимость поверхностного натяжения от температуры
- 4. Энтропия как функция Т и x
- 5. Энтропия как функция T и Y
- 6. Энтропия как функция x и Y
- 7. Вычисление Cy-Cx
- 8. Связь теплоемкостей со скоростью звука
- 9. Зависимость Cv от объема
- 10. Зависимость Ср от давления
- 11. Изменение температуры в адиабатных системах
- 12. Уравнение адиабаты для газа, подчиняющегося уравнению Ван-дер-Ваальса
- 13. Уравнение Гиббса — Гельмгольца
- 14. Уравнение максимальной работы
- 15. Поверхностная энергия чистой жидкости
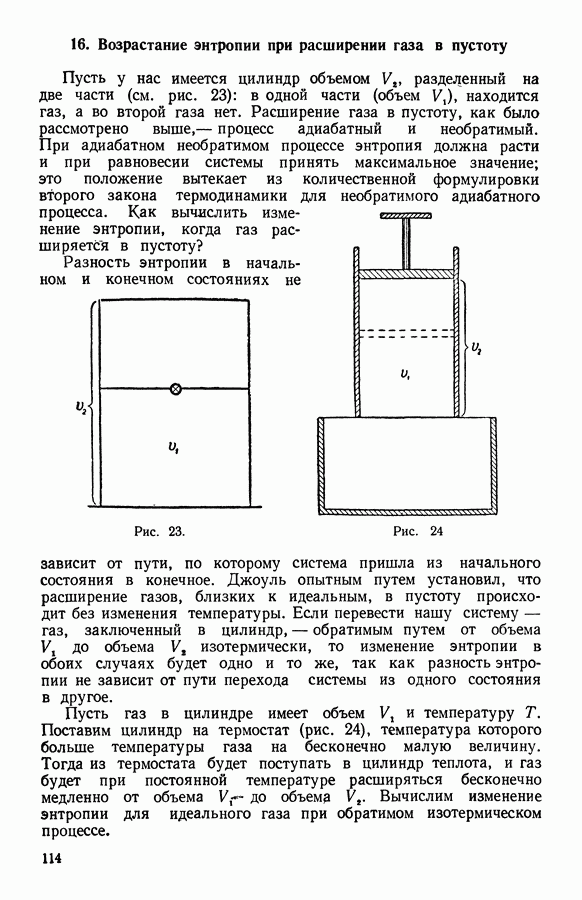
- 16. Возрастание энтропии при расширении газа в пустоту
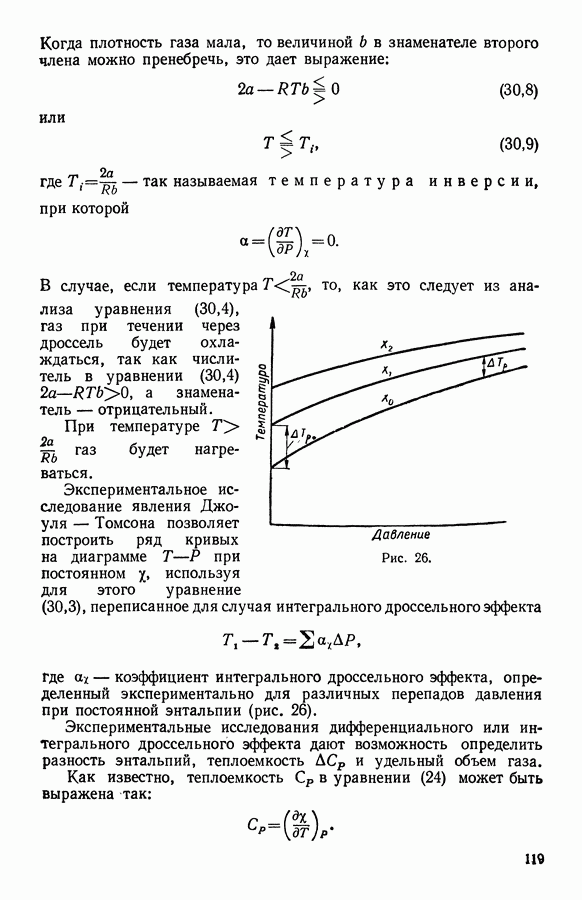
- 17. Явление Джоуля — Томсона (дроссельный эффект)
- 18. Изотермическое дросселирование
- 19. Методы определения дифференциального и интегрального адиабатного дроссельного эффекта
- 20. Задачи
- ГЛАВА ШЕСТАЯ. ТЕРМОДИНАМИКА ИЗЛУЧЕНИЯ
- 1. Тепловое излучение
- 2. Закон Кирхгофа
- 3. Световое давление
- 4. Закон Стефана — Больцмана
- 5. Формула и закон смещения Вина
- ГЛАВА СЕДЬМАЯ. ТЕРМОДИНАМИЧЕСКОЕ УЧЕНИЕ О РАВНОВЕСИИ
- 2. Гетерогенная и гомогенная системы
- 3. Компоненты
- 4. Необратимые процессы и общие условия равновесия
- 5. Химический потенциал
- 6. Идеальные газовые смеси
- 7. Свободная энергия системы идеальных газов до смешения
- 8. Свободная энергия идеальных газов после смешения
- 9. Химический потенциал компонента идеального газа
- 10. Термодинамический вывод закона действующих масс
- 11. Термодинамический вывод уравнения работы химической реакции
- 12. Зависимость константы равновесия от температуры
- 13. Зависимость константы равновесия Ky от давления
- 14. Условие равновесия в гетерогенной системе
- 14. Правило фаз
- ГЛАВА ВОСЬМАЯ. ФАЗОВЫЕ ПРЕВРАЩЕНИЯ
- 1. Фазовые превращения в однокомпонентных системах
- 2. Фазовые превращения первого рода
- 3. Общее уравнение равновесия двух фаз однокомпонентной системы
- 4. Фазовые превращения второго рода
- 5. Термодинамическая теория фазовых превращений второго рода
- 6. Фазовые превращения в однокомпонентной системе жидкость — пар
- 7. Термодинамическое условие равновесия системы жидкость — пар в критическом состоянии
- 8. Определение … из уравнения Ван-дер-Ваальса
- 9. Сверхпроводящее состояние металлов
- 10. Фазовые превращения в однокомпонентной гетерогенной системе. Нормальное — сверхпроводящее состояние металлов
- 11. Бинарные системы
- 12. О взаимной растворимости жидкостей
- 13. Твердые растворы
- 14. Уравнение Ван-дер-Ваальса для бинарных смесей
- 15. Разбавленные растворы
- 16. Растворимость газа в жидкости
- 17. Первый закон Д. П. Коновалова
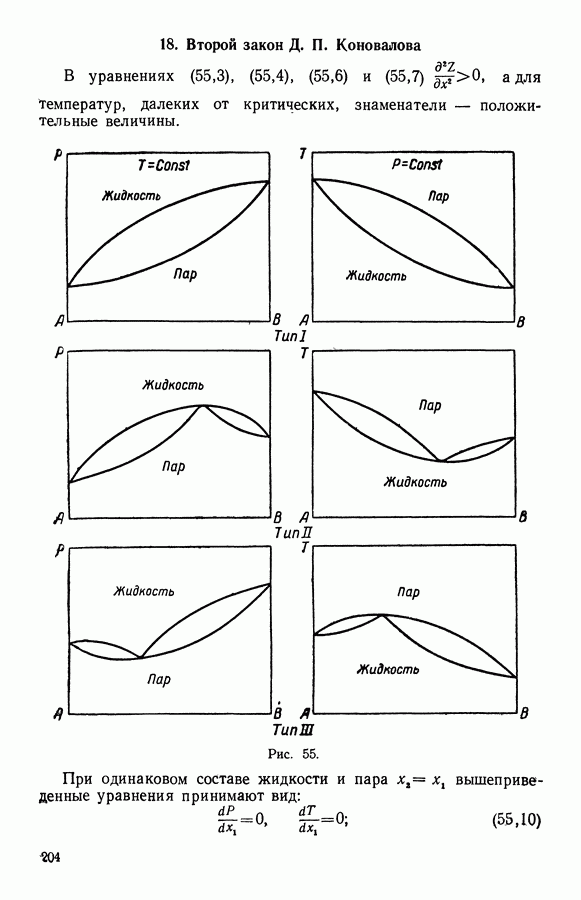
- 18. Второй закон Д. П. Коновалова
- 19. Температура кипения раствора и дистилляция двойных смесей
- ГЛАВА ДЕВЯТАЯ. НИЗКИЕ ТЕМПЕРАТУРЫ
- 1. Получение низких температур, их значение для техники и научных исследований
- 2. Каскадный метод
- 3. Метод дросселирования
- 4. Получение низких температур при расширении сжатого газа с отдачей внешней работы
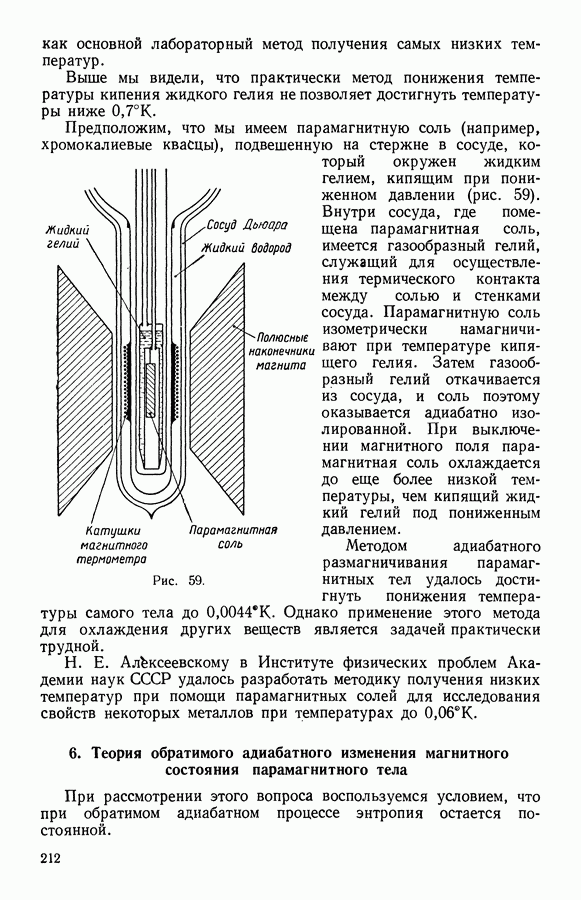
- 5. Охлаждение методом адиабатного размагничивания
- 6. Теория обратимого адиабатного изменения магнитного состояния парамагнитного тела
- 7. Тепловая теорема Нернста
- 8. О третьем законе термодинамики
- 9. Свойства вещества вблизи абсолютного нуля
- 10. Стандартные таблицы термодинамических функций
- 11. Вычисление стандартных величин при изменении температуры
- 12. Вычисление стандартных величин при изменении давления
- 13. Применение стандартных таблиц
- 14. Вычисление стандартных величин
- 15. Задачи для всех разделов курса