| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
5.3 Энергия и структура
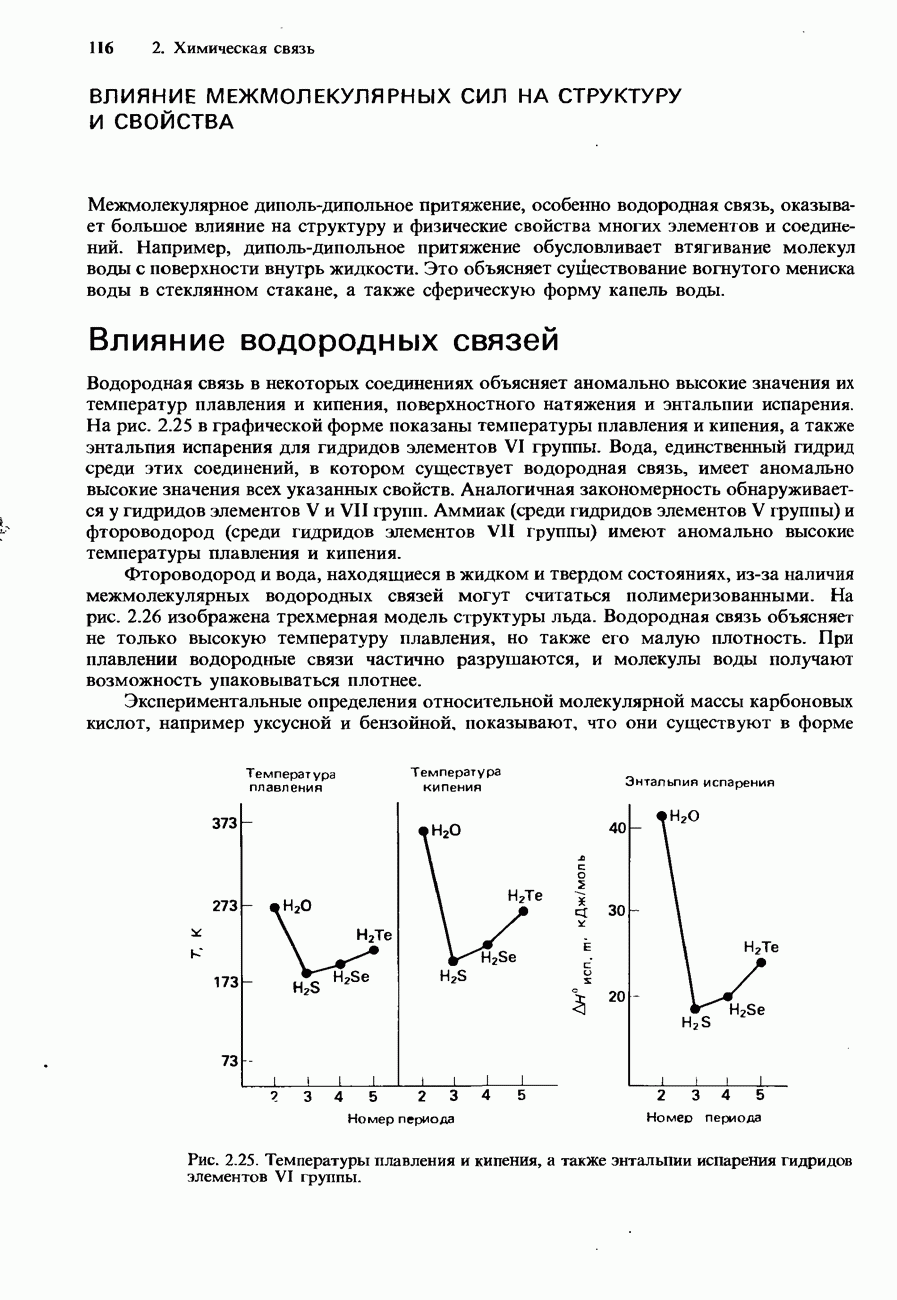
ЭНТАЛЬПИИ ХИМИЧЕСКИХ СВЯЗЕЙ
Стандартной энтальпией диссоциации связи называется изменение энтальпии, которым сопровождается разрыв одного моля связей при условии, что исходные молекулы и результирующие фрагменты находятся в своих стандартных состояниях при температуре 298 К и давлении 1 атм.
Энтальпия диссоциации связи характеризует определенную связь в молекуле. Ее численная величина зависит от того конкретного химического окружения, в котором находится рассматриваемая связь. Например, в молекуле метана имеются четыре связи  и, следовательно, для метана можно определить четыре энтальпии диссоциации связи. Они называются соответственно первой, второй, третьей и четвертой энтальпией диссоциации связи и характеризуются соответствующими реакциями и численными значениями:
и, следовательно, для метана можно определить четыре энтальпии диссоциации связи. Они называются соответственно первой, второй, третьей и четвертой энтальпией диссоциации связи и характеризуются соответствующими реакциями и численными значениями:

Аналогично для воды можно определить две энтальпии диссоциации связи 

Обратим внимание на то обстоятельство, что энтальпии диссоциации связей имеют положительные значения, т. е. соответствуют эндотермическим процессам. Это и естественно: ведь для разрыва химической связи необходимо затратить энергию.
Таблица 5.6. Средние энтальпии связей

Если усреднить значения четырех стандартных энтальпий диссоциации связей для молекулы метана, получится значение  . Среднее значение стандартной энтальпии диссоциации связи
. Среднее значение стандартной энтальпии диссоциации связи  для молекул любых типов, включая молекулу метана, равно
для молекул любых типов, включая молекулу метана, равно  . Оно называется средней энтальпией диссоциации связи, средней энтальпией связи или просто энергией связи. В табл. 5.6 приведены значения средних энтальпий диссоциации для некоторых наиболее распространенных связей.
. Оно называется средней энтальпией диссоциации связи, средней энтальпией связи или просто энергией связи. В табл. 5.6 приведены значения средних энтальпий диссоциации для некоторых наиболее распространенных связей.
Средняя энтальпия связи для простых веществ (свободных элементов) или соединений, существующих в форме двухатомных молекул, представляет собой просто энтальпию диссоциации связи. Для таких простых веществ (элементов) и соединений энтальпия диссоциации связи равна удвоенному значению энтальпии атомизации (см. ниже).
Стандартной энтальпией атомизации свободного элемента называется изменение энтальпии, которым сопровождается образование одного моля изолированных газообразных атомов из рассматриваемого свободного элемента, находящегося в своем стандартном состоянии при температуре 298 К и давлении 1 атм. Например, стандартная энтальпия атомизации водорода характеризуется следующей реакцией и численным значением:

а стандартная энтальпия диссоциации связи водорода характеризуется следующим образом:

Для твердых элементов (находящихся при стандартных условиях в твердом состоянии) энтальпия атомизации равна энтальпии сублимации. Сублимацией называется превращение твердого вещества в газ при нагревании, если оно осуществляется, минуя жидкое состояние; обратное превращение газа в твердое вещество, минуя жидкое состояние, называется осаждением из паровой фазы.
Определение энтальпий связей
Для определения энтальпий связей используются спектроскопические методы (см. разд. 17.1), методы электронного удара (см. разд. 1.2) либо термохимические методы. Термохимические методы включают калориметрическое определение энтальпий сгорания, образования и других процессов. Данные, полученныеэтими способами, используются затем для вычисления энтальпий связей. Энтальпии связей не поддаются определению прямыми термохимическими измерениями.
Экспериментальным подтверждением согласованности и приблизительного постоянства энтальпий связей в широком ряду соединений могут служить стандартные молярные энтальпии сгорания в гомологическом ряду алканов (см. разд. 17.1). Если

Рис. 5.12. Стандартные молярные энтальпии сгорания для шести первых членов гомологического ряда алка-нов,  энтальпия сгорания.)
энтальпия сгорания.)
Таблица 5.7. Стандартные молярные энтальпии сгорания алканов

построить график зависимости энтальпий сгорания алканои от числа атомов углерода, входящих в состав каждого из них, получится прямая линия (рис. 5.12). Разность между стандартными молярными энтальпиями сгорания каждых двух последовательных членов ряда алканов составляет приблизительно  . По своему строению каждый следующий член ряда алканов отличается от предыдущего члена дополнительной группой
. По своему строению каждый следующий член ряда алканов отличается от предыдущего члена дополнительной группой  . Следовательно, величина 660 кДж/моль соответствует диссоциации и образованию связей при сгорании одного моля групп
. Следовательно, величина 660 кДж/моль соответствует диссоциации и образованию связей при сгорании одного моля групп  Сгорание каждой группы -
Сгорание каждой группы -  включает: 1) диссоциацию двух связей
включает: 1) диссоциацию двух связей  диссоциацию одной связи
диссоциацию одной связи  образование двух двойных связей
образование двух двойных связей  при образовании молекулы
при образовании молекулы  образование двух связей
образование двух связей  при образовании молекулы
при образовании молекулы 
Приблизительное постоянство величины 660 кДж/моль в ряду алканов указывает на то, что энтальпии связей  в этом ряду хорошо согласуются между собой.
в этом ряду хорошо согласуются между собой.
Определение средней энтальпии связи С-Н
Для того чтобы определить среднюю энтальпию связи  из экспериментальных данных, можно воспользоваться стандартной энтальпией атомизации метана
из экспериментальных данных, можно воспользоваться стандартной энтальпией атомизации метана

Эта стандартная энтальпия атомизации в четыре раза больше средней энтальпии связи 

Стандартную энтальпию атомизации метана можно вычислить с помощью закона Гесса, если известны экспериментальные значения стандартных энтальпий следующих
процессов:
1. Стандартная энтальпия атомизации графита

Эта энтальпия установлена путем измерения температурной зависимости давления паров графита.
2. Стандартная энтальпия атомизации водорода

Эту энтальпию можно определить спектроскопическими методами.
3. Стандартная энтальпия образования метана

Эту величину можно вычислить из стандартной энтальпии сгорания метана и стандартных энтальпий образования диоксида углерода и воды. Все эти три энтальпии можно определить экспериментально калориметрическими методами.
Применим теперь закон Гесса в форме, описываемой уравнением (12), к процессу атомизации метана:

Теперь воспользуемся уравнением (13) и получим

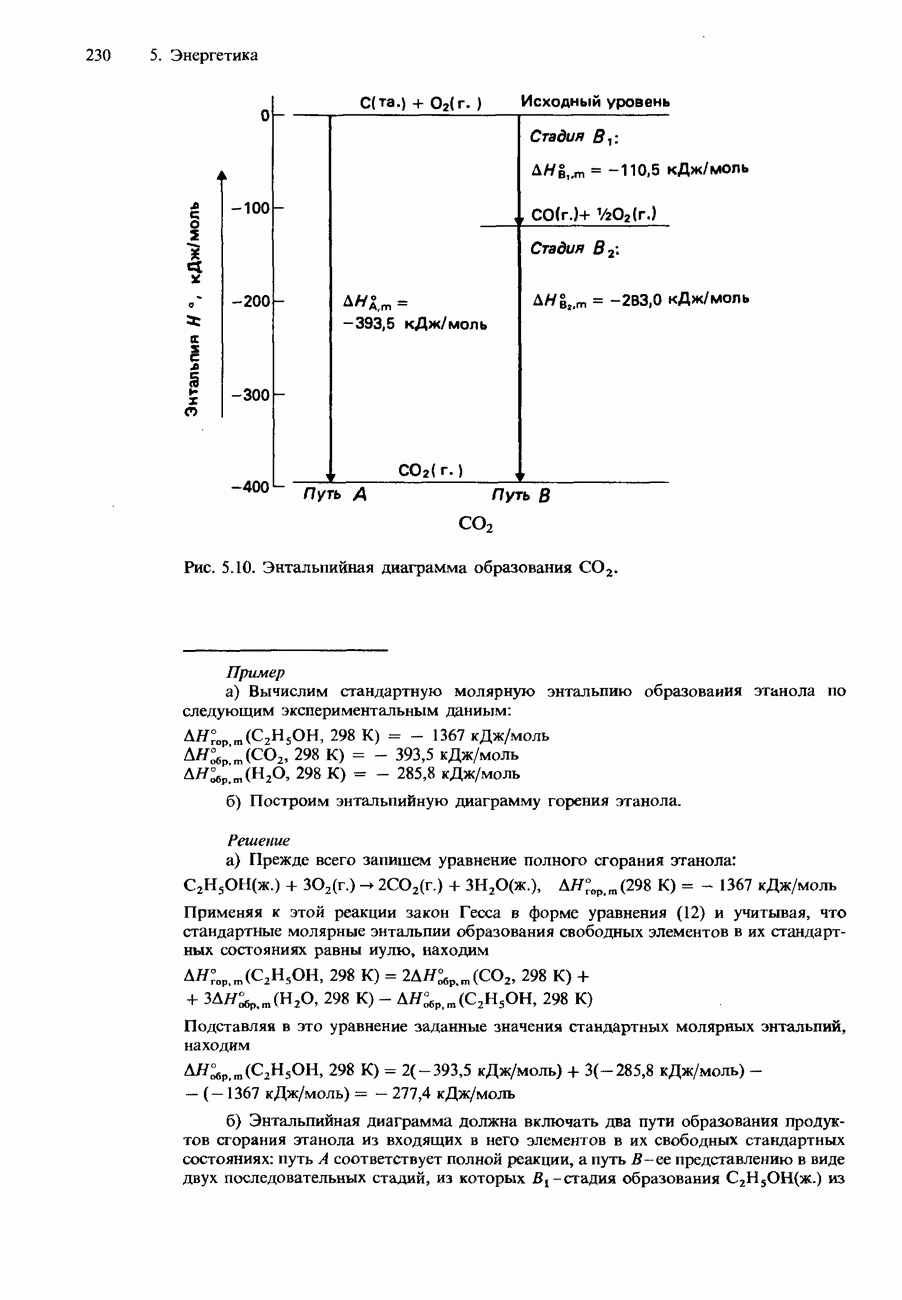
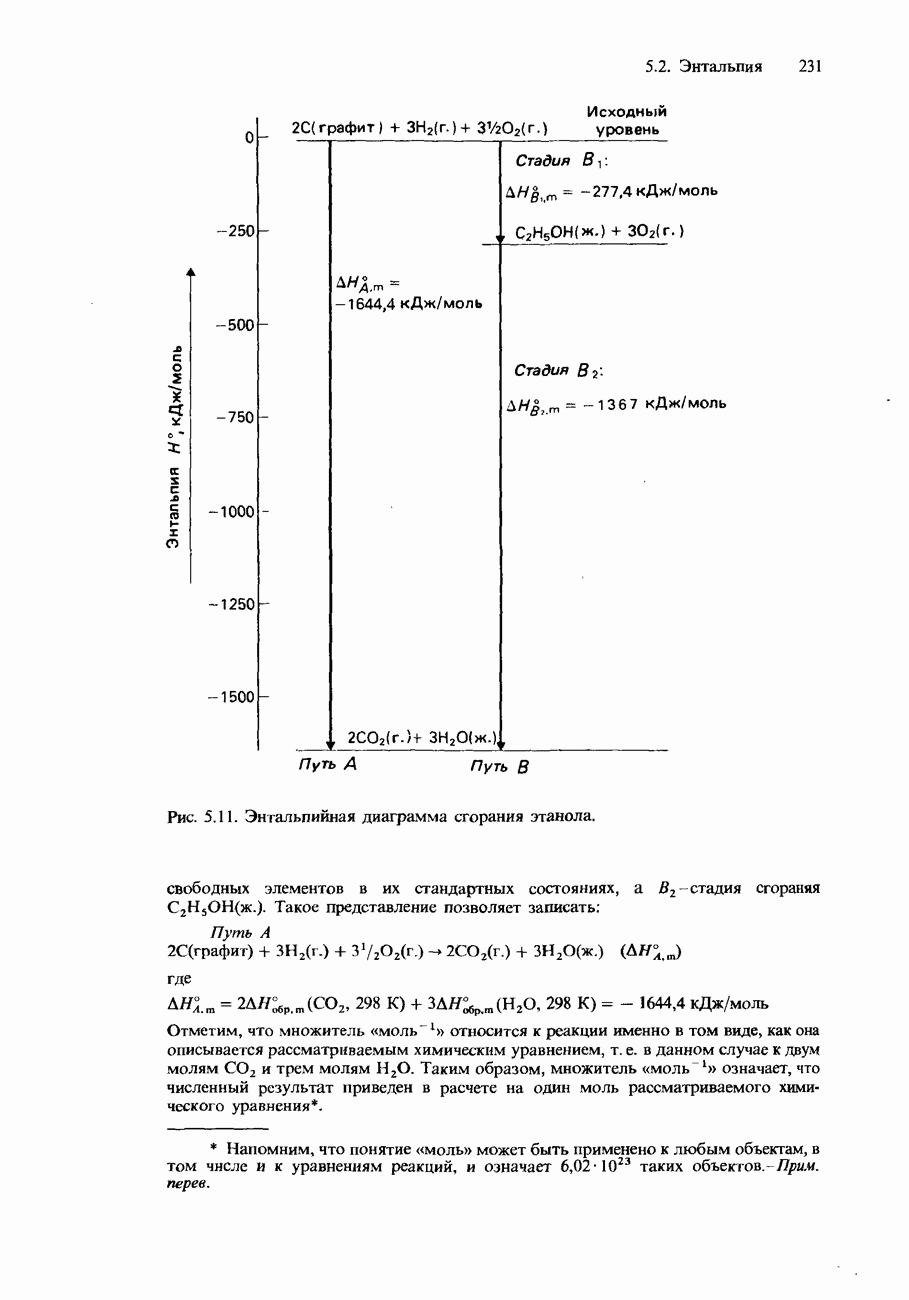
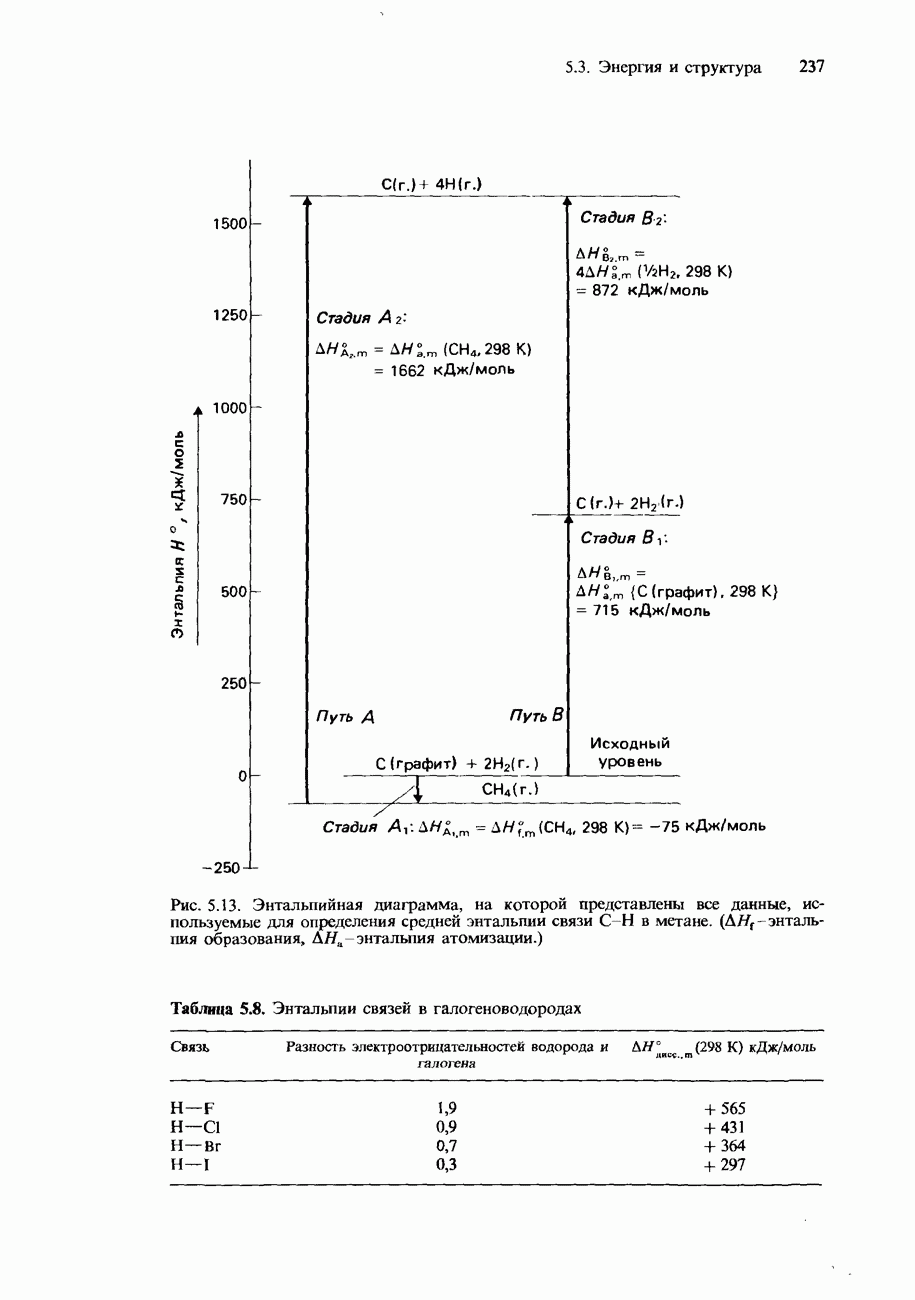
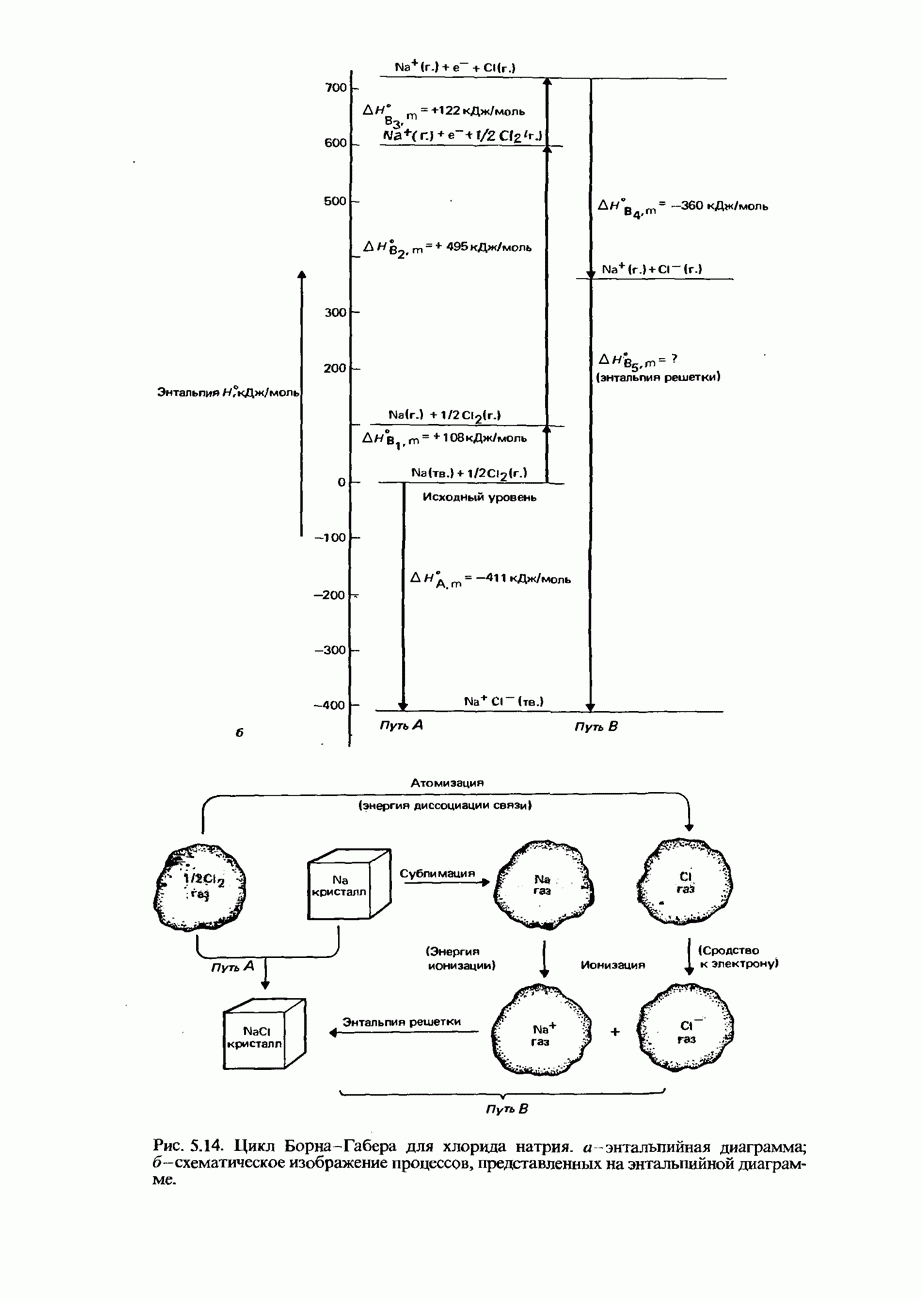
Сведения, которыми необходимо располагать для вычисления средней энтальпии связи С-Н, можно представить в графической форме с помощью энтальпийной диаграммы (рис. 5.13).
Интерпретация и практическое использование энтальпий связей
Знание энтальпий связей позволяет понять структуру ковалентных соединений, а также механизмы (см. гл. 9) их химических реакций.
В разд. 2.1 мы указывали, что шкала Полинга электроотрицательности элементов основывается на учете энтальпий связей. Как правило, с уменьшением разности электроотрицательностей двух элементов, образующих связь, происходит и уменьшение энтальпии этой связи. Эту закономерность можно проиллюстрировать путем сопоставления разностей электроотрицательности между водородом и галогенами с энтальпиями связи в ряду галогеноводородов (табл. 5.8).
Приведенные в табл. 5.9 данные показывают, что энтальпии связей увеличиваются с возрастанием числа связей между двумя атомами (т.е. с возрастанием кратности связи). Дело в том, что прочность всякой связи зависит от числа связывающих электронов. При увеличении числа связывающих электронов длина связи уменьшается, а прочность связи возрастает.
(см. скан)
Рис. 5.13. Энтальпийная диаграмма, на которой представлены все данные, используемые для определения средней энтальпии связи  в метане. (
в метане. ( — энтальпия образования,
— энтальпия образования,  — энтальпия атомизации.)
— энтальпия атомизации.)
Таблица 5.8. Энтальпии связей в галогеноводородах

Таблица 5.9. Уменьшение энтальпии связи при увеличении длины связи

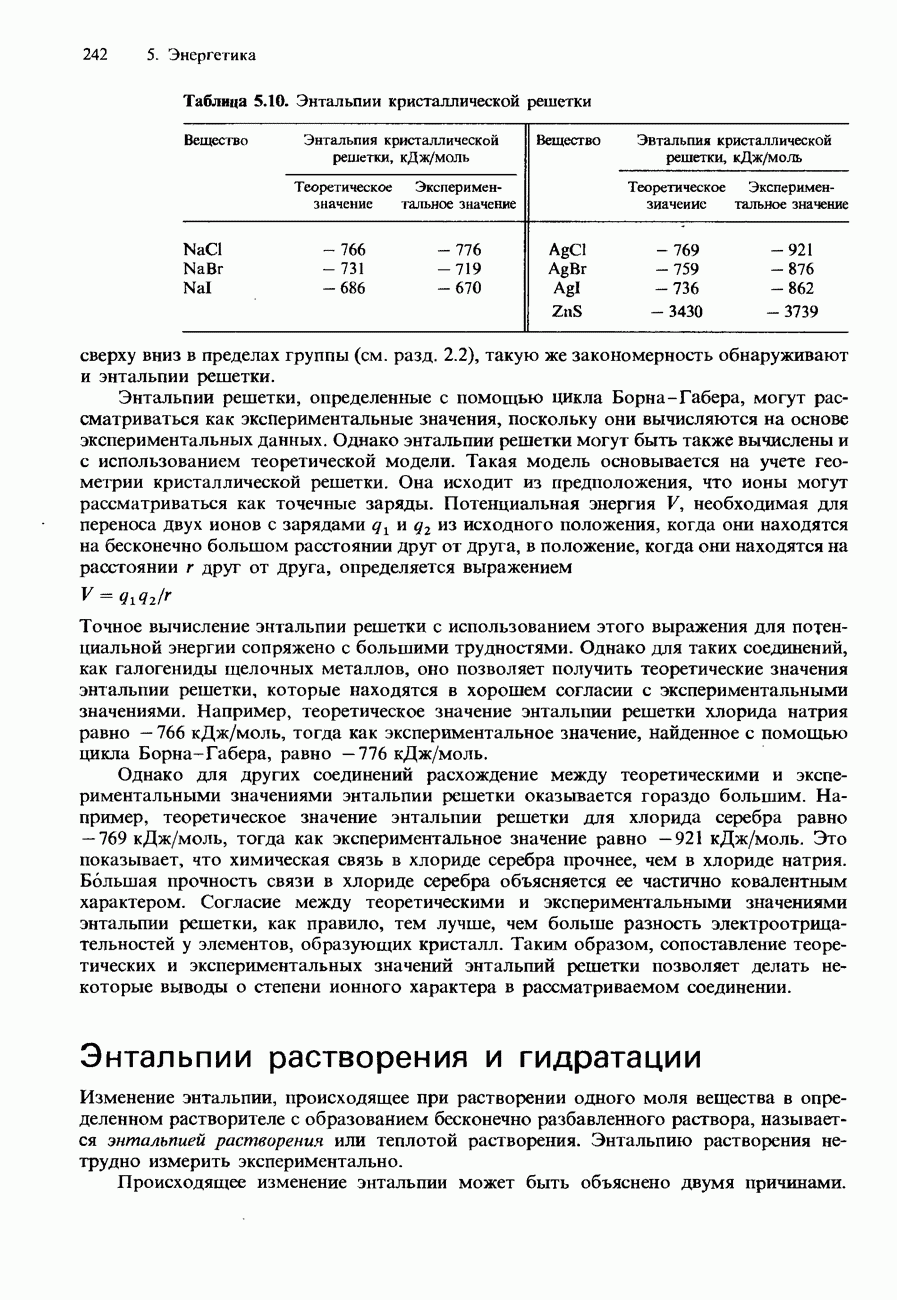
Размер атомов тоже влияет на энтальпию связи и длину связи. В табл. 5.9 сопоставляются эти характеристики двухатомных молекул в группе галогенов. При перемещении сверху вниз в этой группе атомы становятся все больше, а в результате длина связи увеличивается из-за возрастающего отталкивания между атомами. Поэтому уменьшается прочность связи, и энтальпии связи становятся все меньше.
Значение энтальпий связи позволяет вычислить энтальпии реакций, в которых участвуют ковалентные молекулы. С этой целью используется уравнение

Пример
Вычислим стандартную молярную энтальпию реакции гидрирования этилена при помощи данных, приведенных в табл. 5.6 и 5.9.

Решение
Разорванные связи 
Образовавшиеся связи: 
При помощи уравнения (14) находим

Подставив сюда необходимые данные из табл. 5.6 и 5.9, получим

Устойчивость бензола
Экспериментальное значение стандартной молярной энтальпии гидрирования этилена равно -137 кДж/моль. Это несколько больше, чем вычисленное в приведенном выше примере значение -119 кДж/моль. Однако в случае гидрирования бензола расхождение между экспериментальным значением и значением, вычисленным с помощью энтальпий связей, оказывается намного большим.
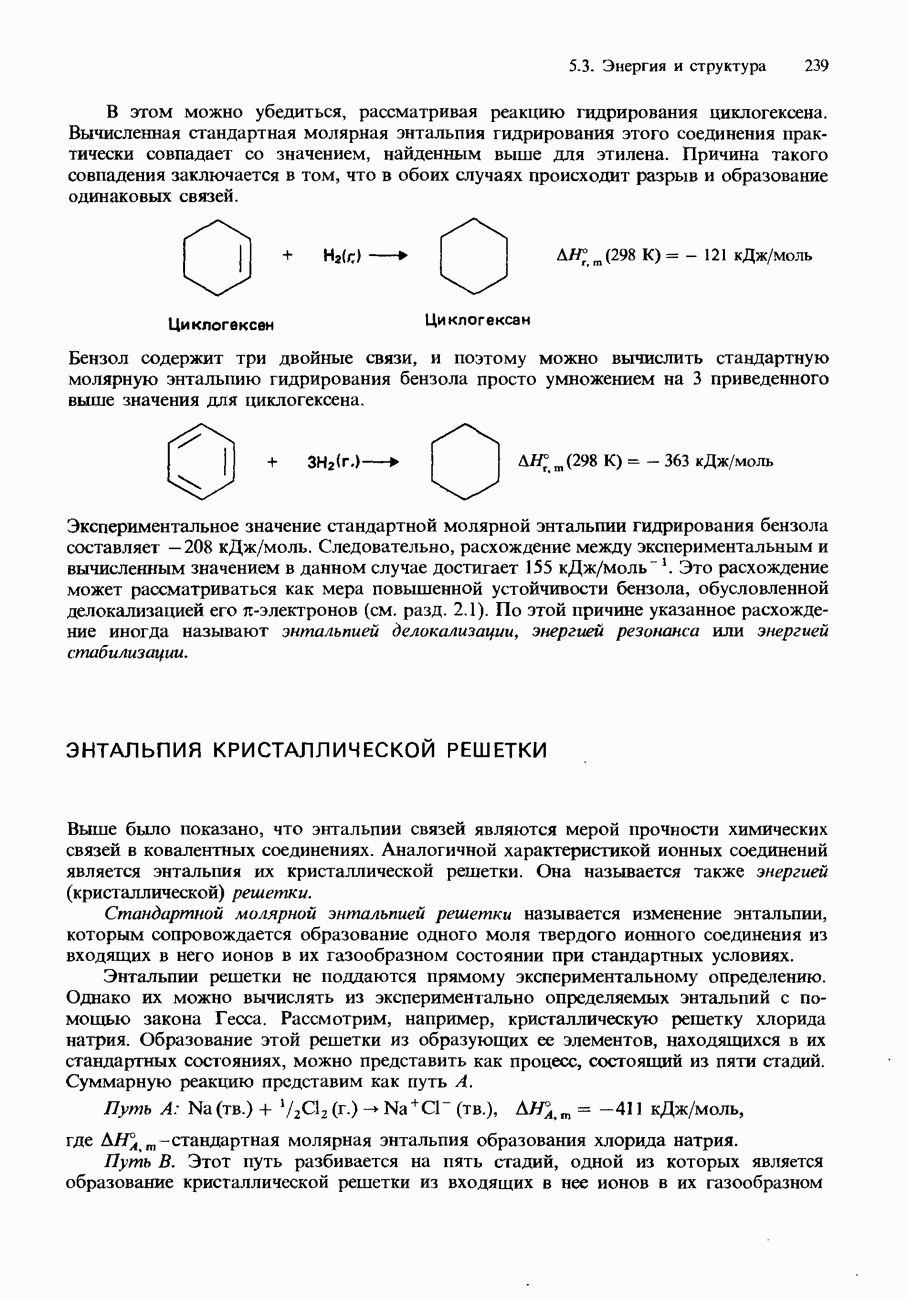
В этом можно убедиться, рассматривая реакцию гидрирования циклогексена. Вычисленная стандартная молярная энтальпия гидрирования этого соединения практически совпадает со значением, найденным выше для этилена. Причина такого совпадения заключается в том, что в обоих случаях происходит разрыв и образование одинаковых связей.

Бензол содержит три двойные связи, и поэтому можно вычислить стандартную молярную энтальпию гидрирования бензола просто умножением на 3 приведенного выше значения для циклогексена.

Экспериментальное значение стандартной молярной энтальпии гидрирования бензола составляет -208 кДж/моль. Следовательно, расхождение между экспериментальным и вычисленным значением в данном случае достигает 155 кДж/моль. Это расхождение может рассматриваться как мера повышенной устойчивости бензола, обусловленной делокализацией его  -электронов (см. разд. 2.1). По этой причине указанное расхождение иногда называют энтальпией делокализации, энергией резонанса или энергией стабилизации.
-электронов (см. разд. 2.1). По этой причине указанное расхождение иногда называют энтальпией делокализации, энергией резонанса или энергией стабилизации.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
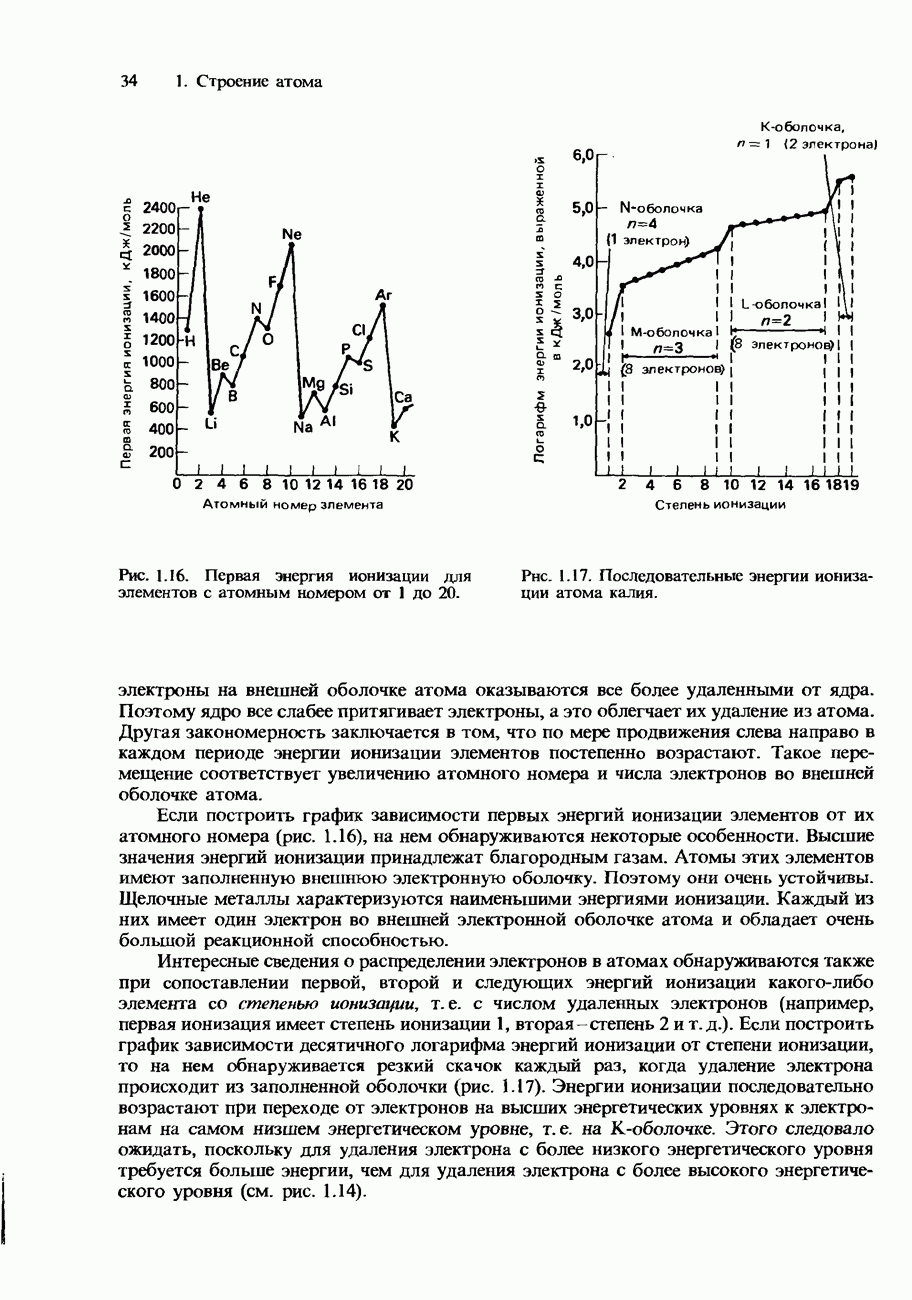
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
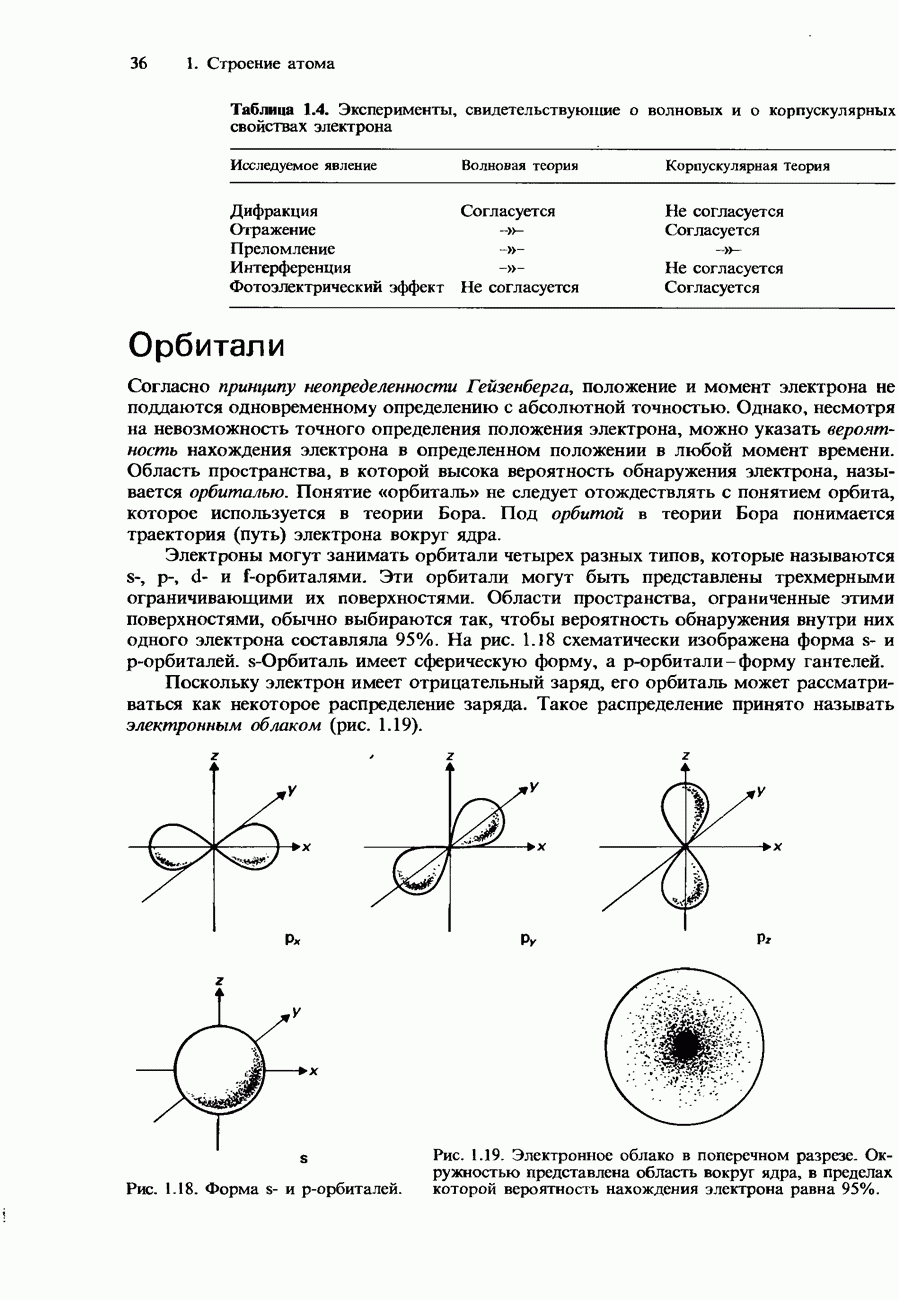
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
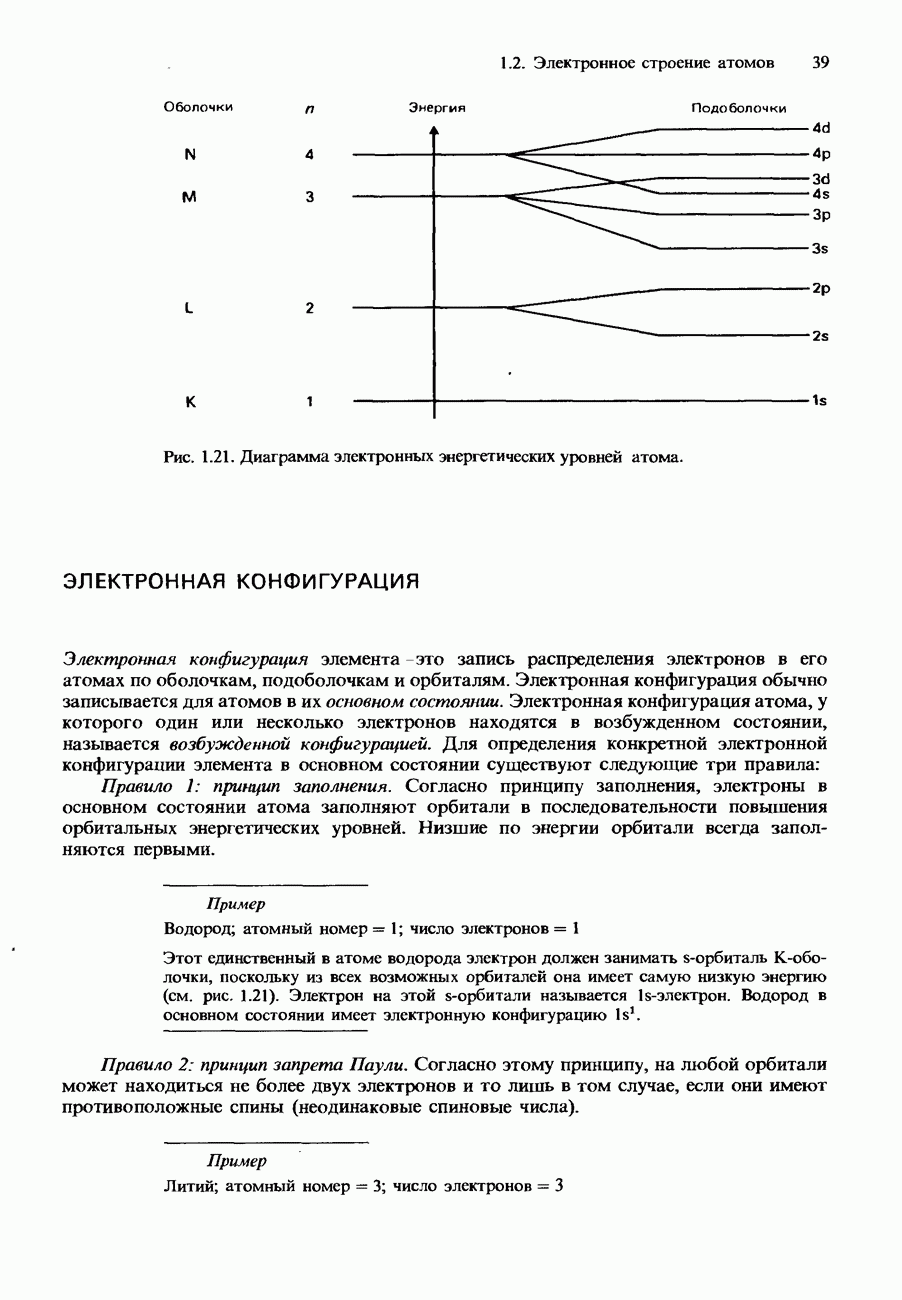
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
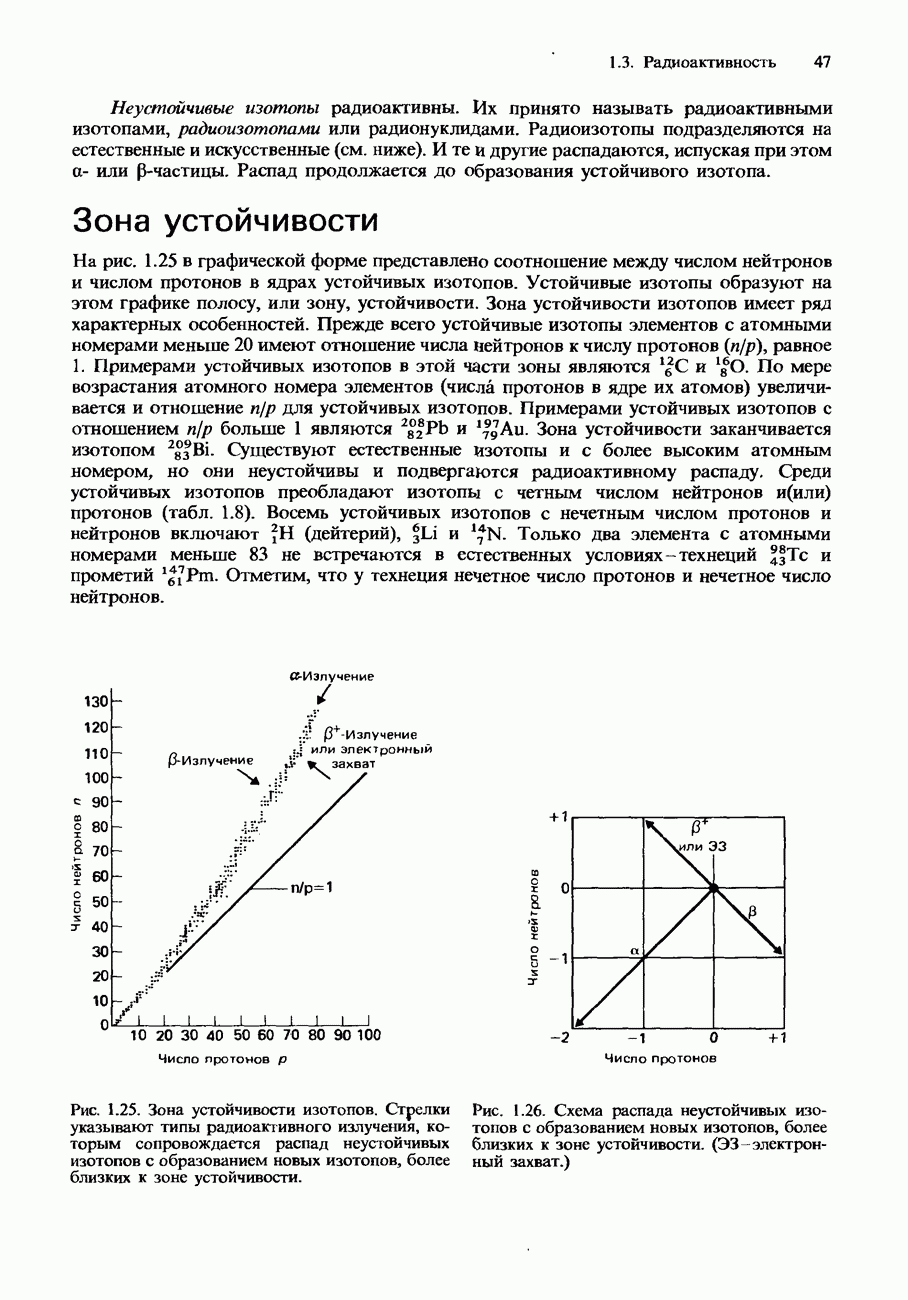
- Зона устойчивости
- Период полураспада
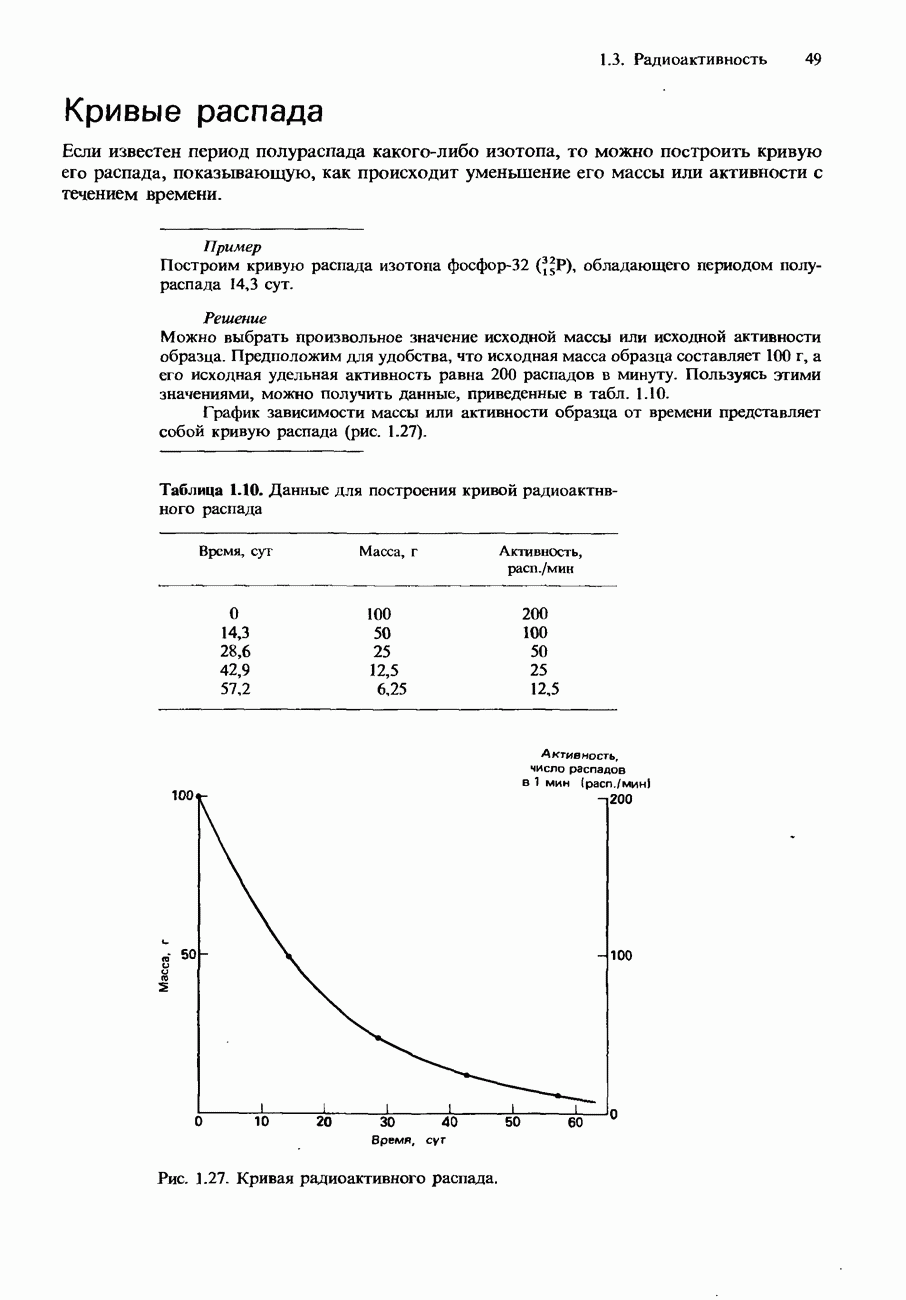
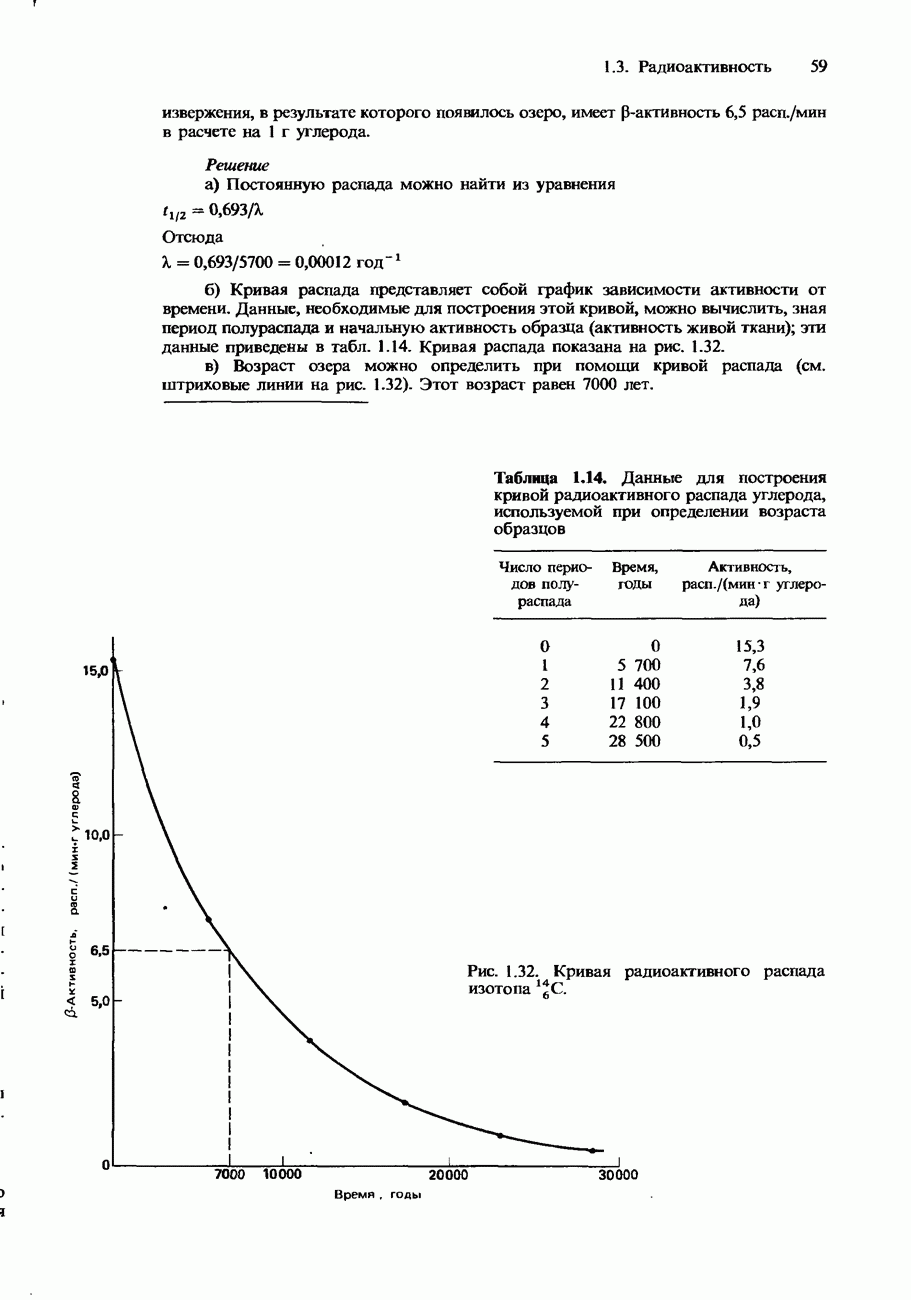
- Кривые распада
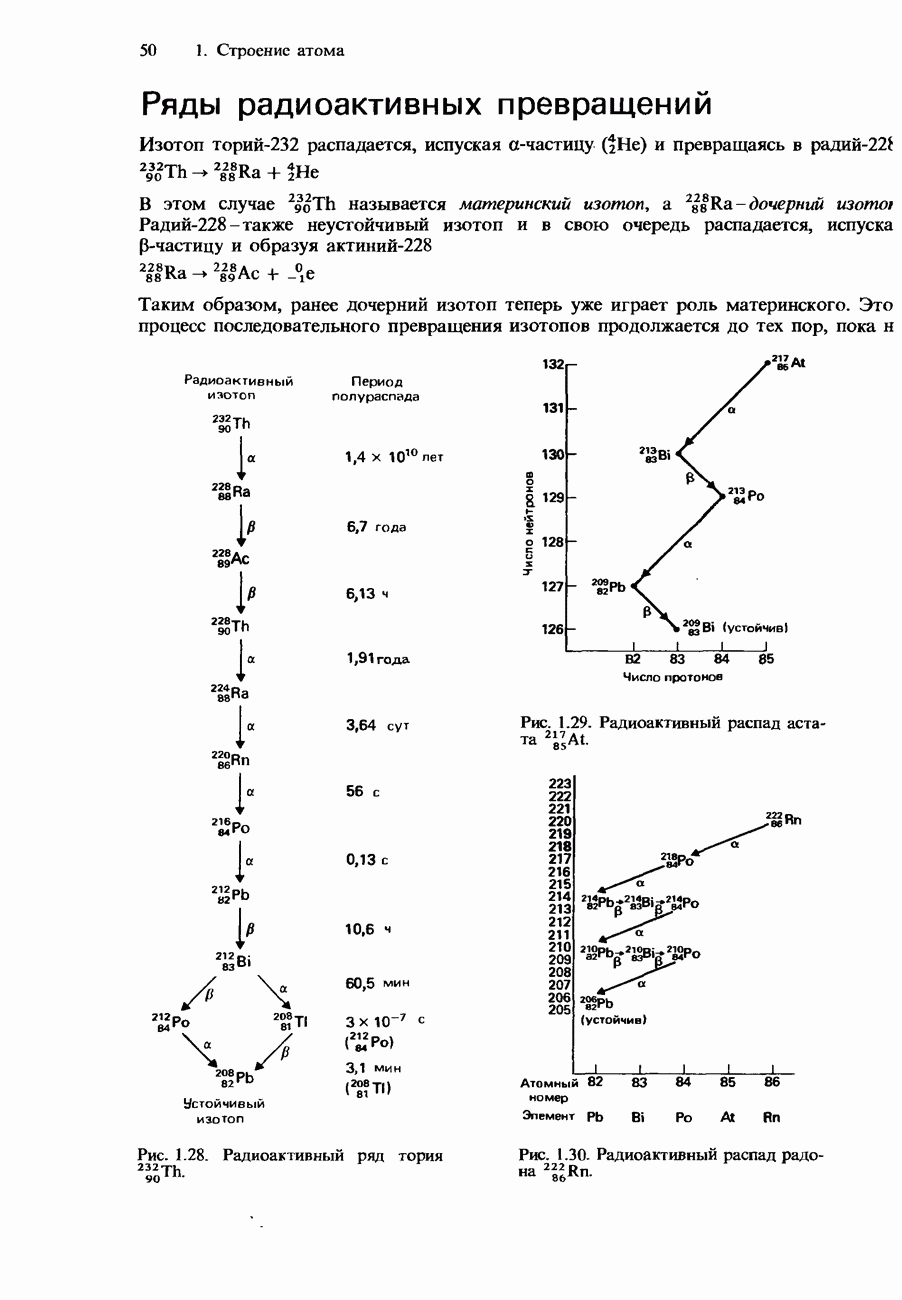
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
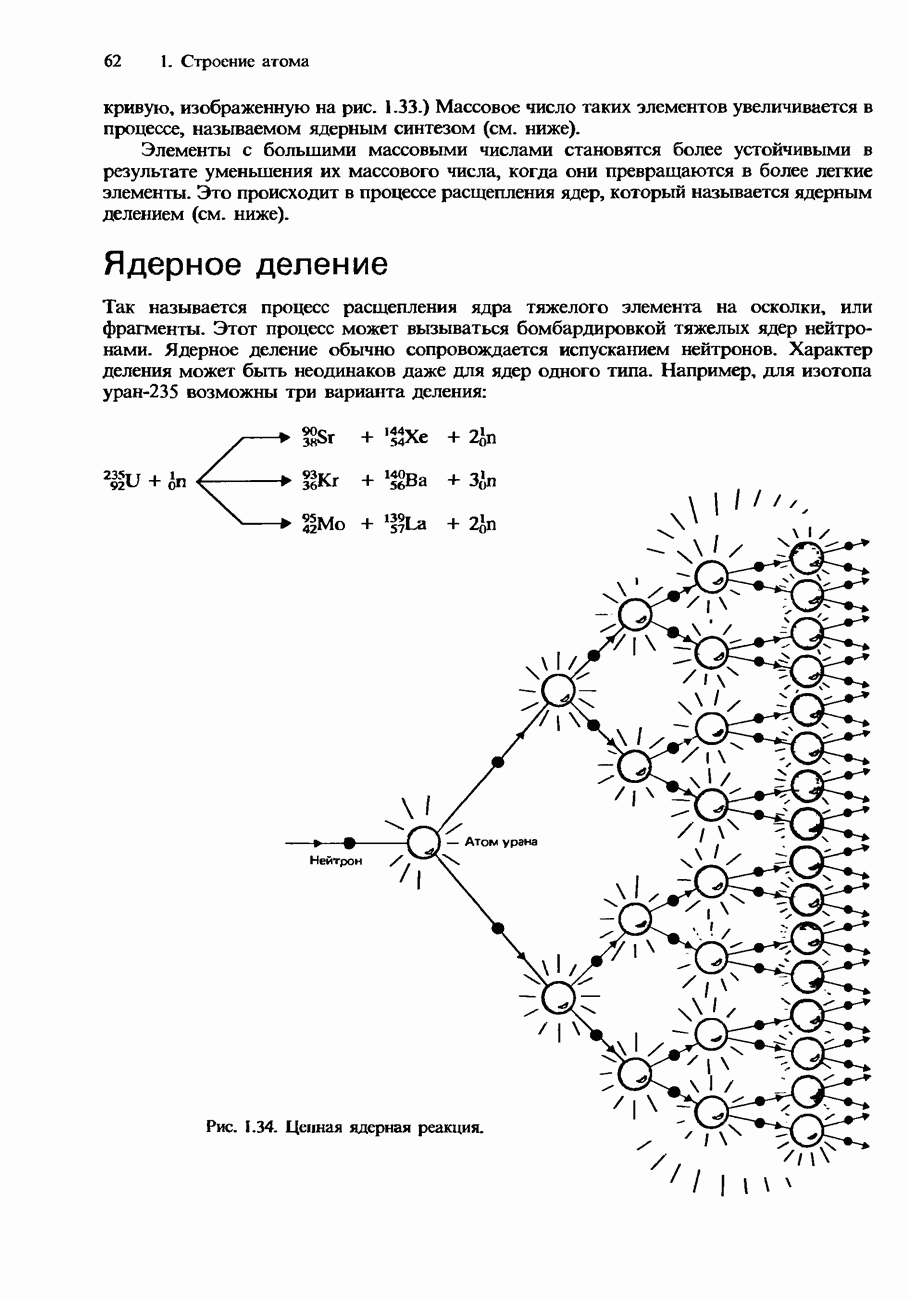
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
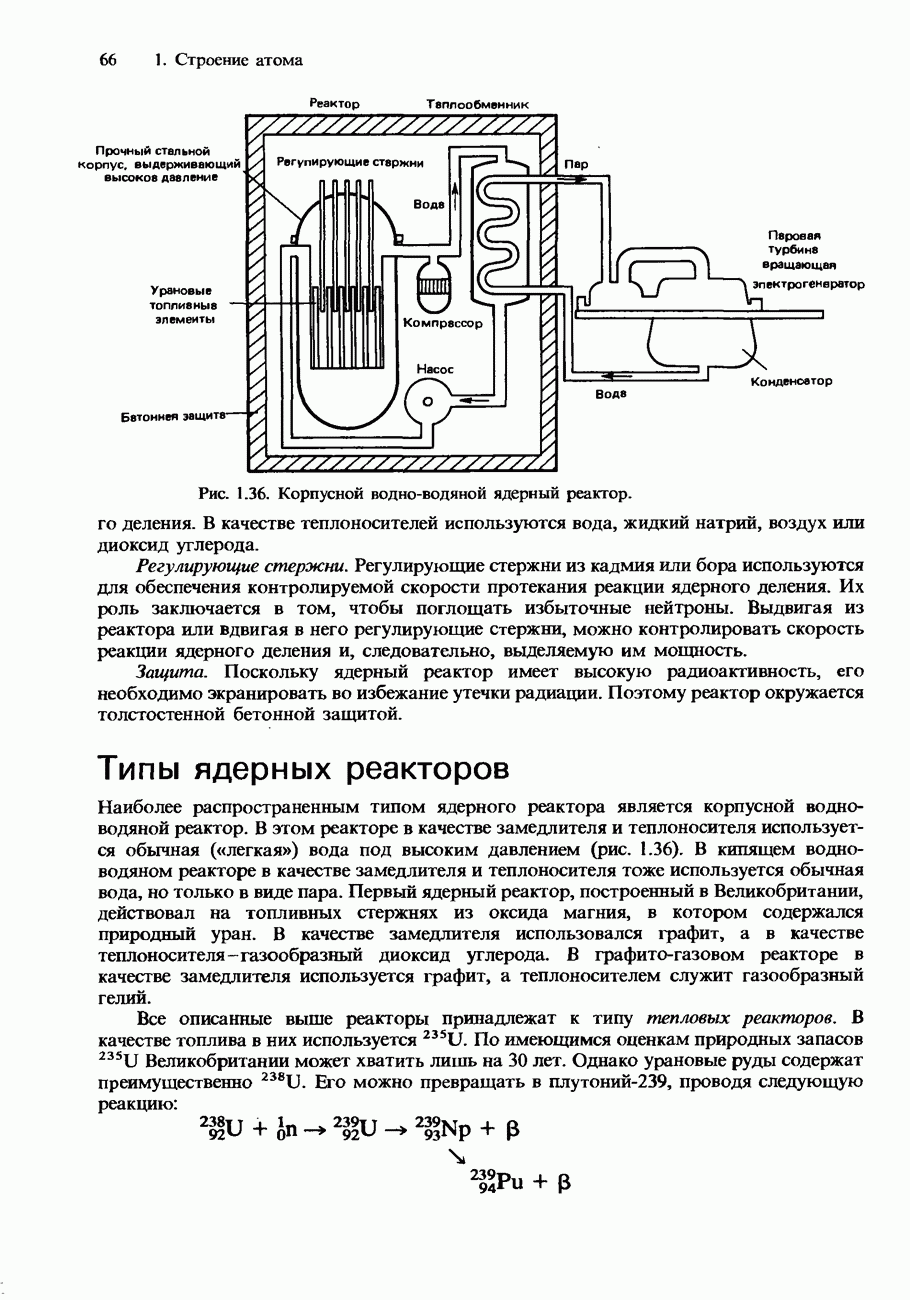
- Типы ядерных реакторов
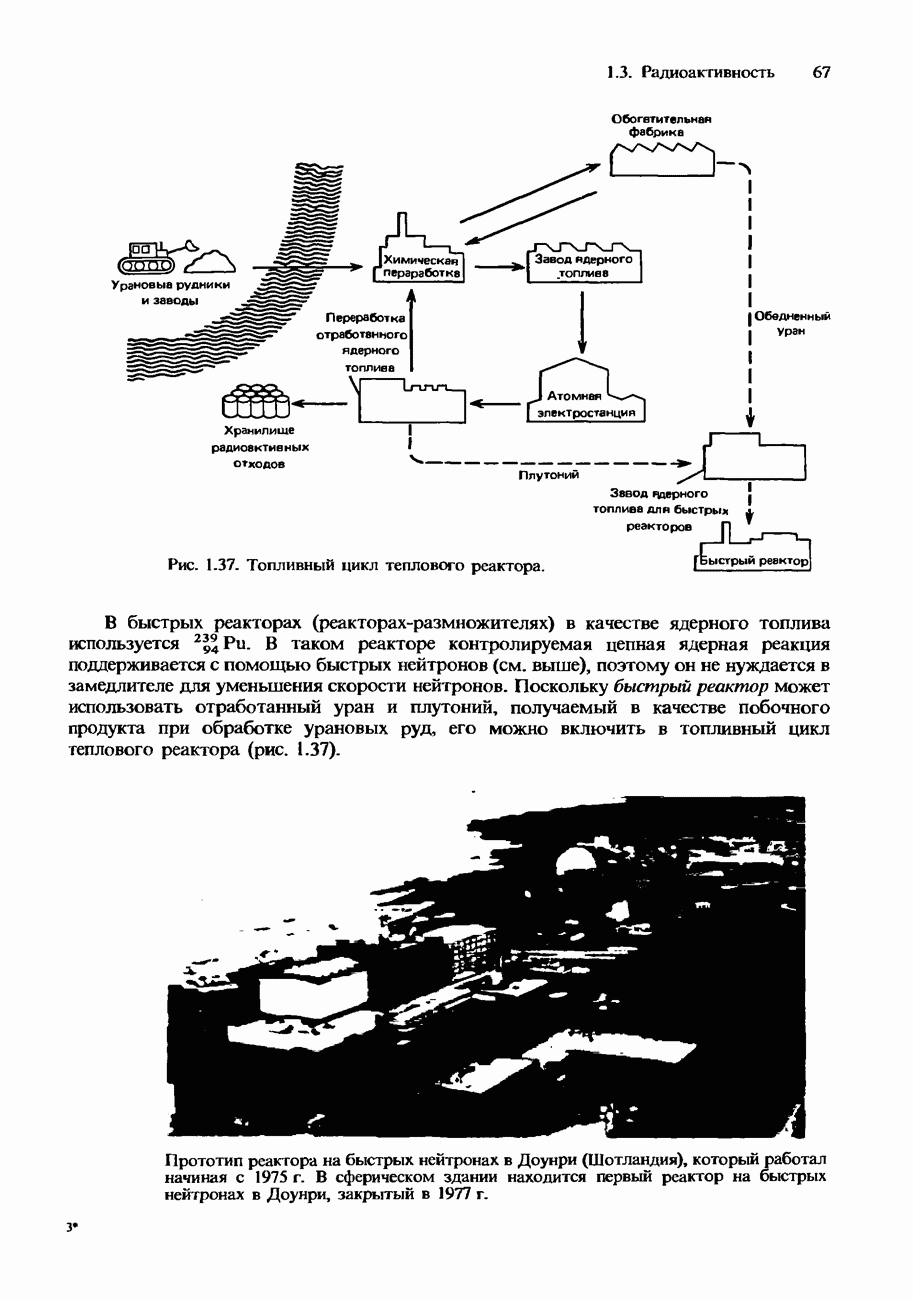
- Радиоактивные ядерные отходы и их переработка
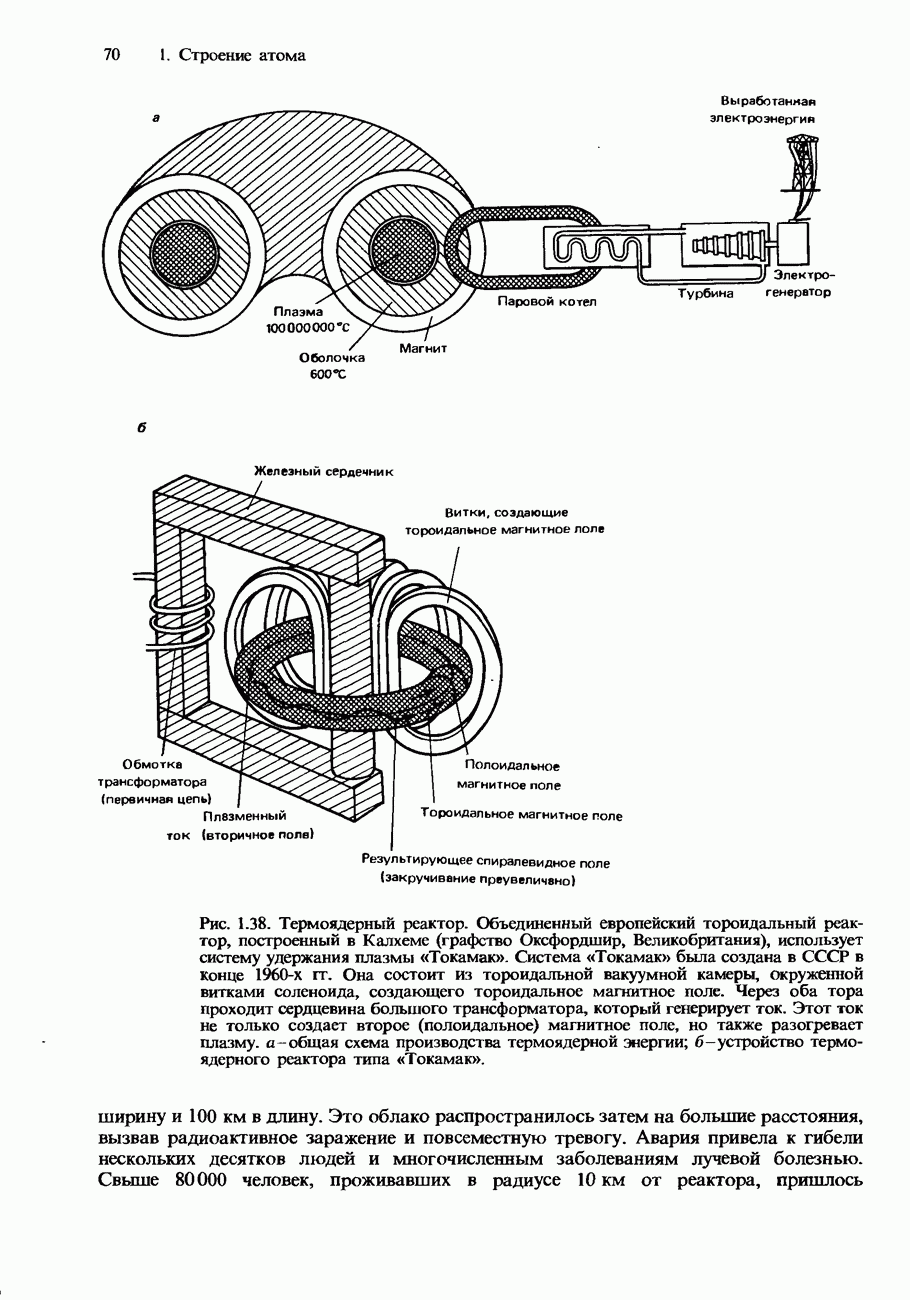
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
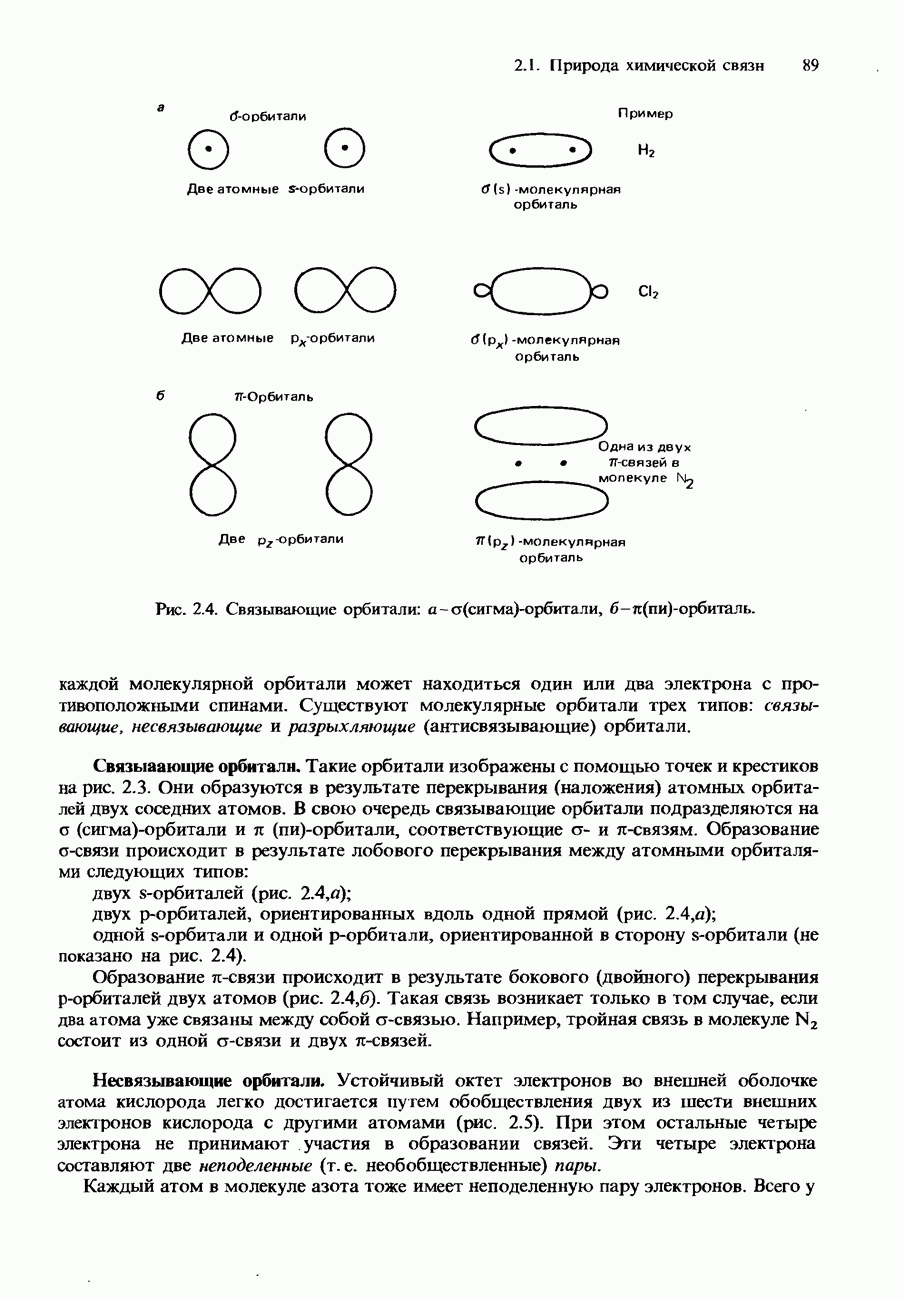
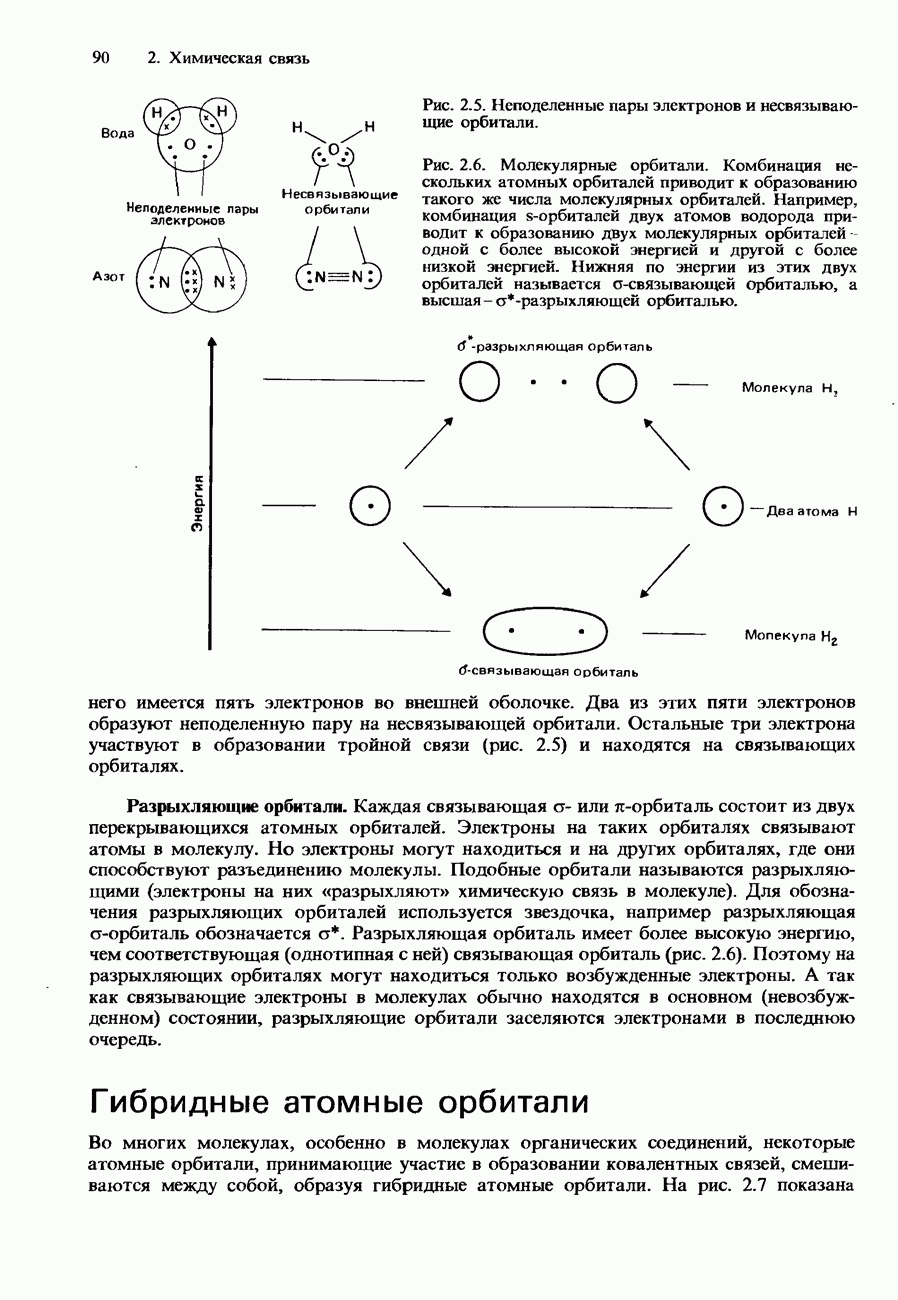
- Молекулярные орбитали
- Гибридные атомные орбитали
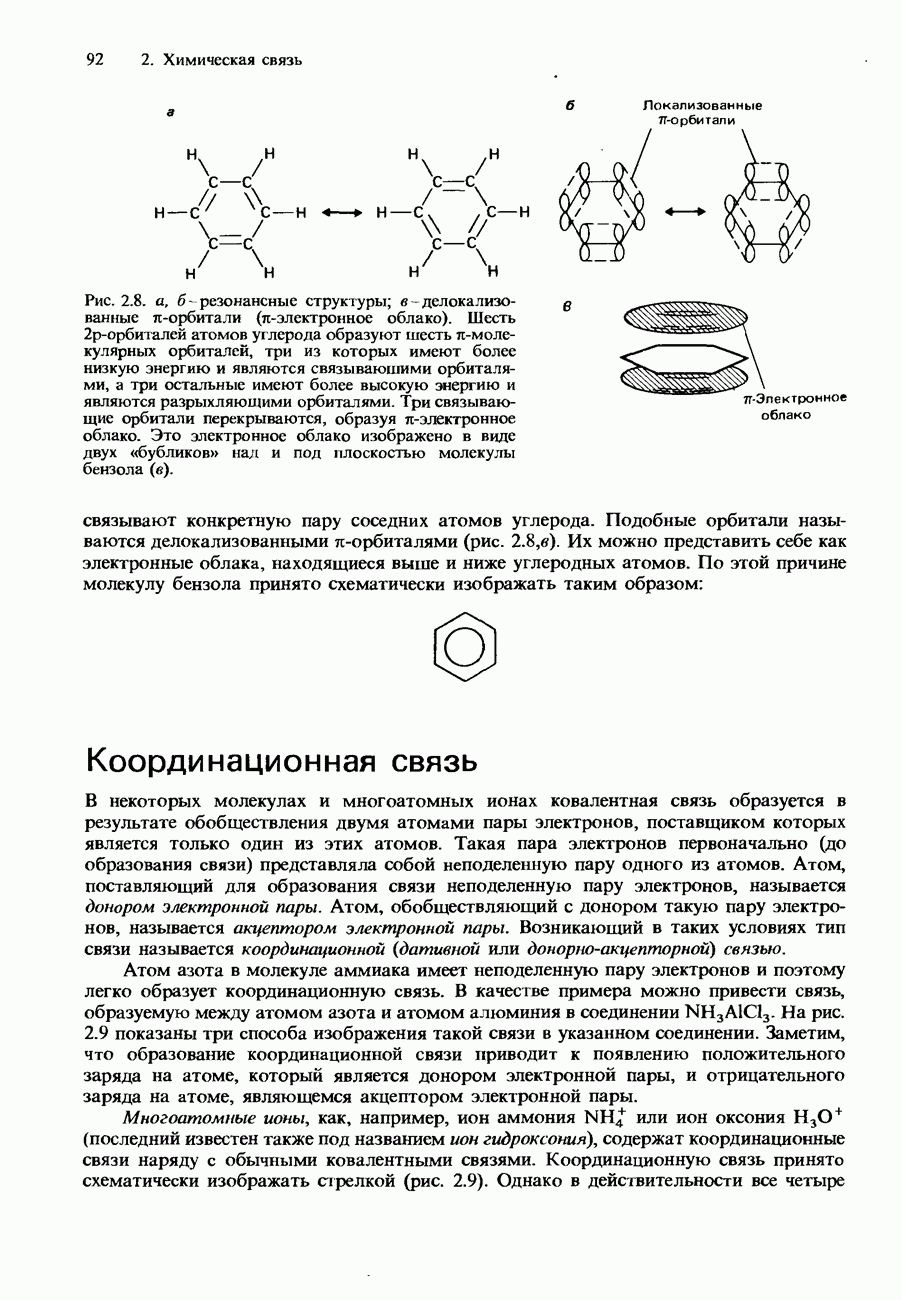
- Делокализованные орбитали
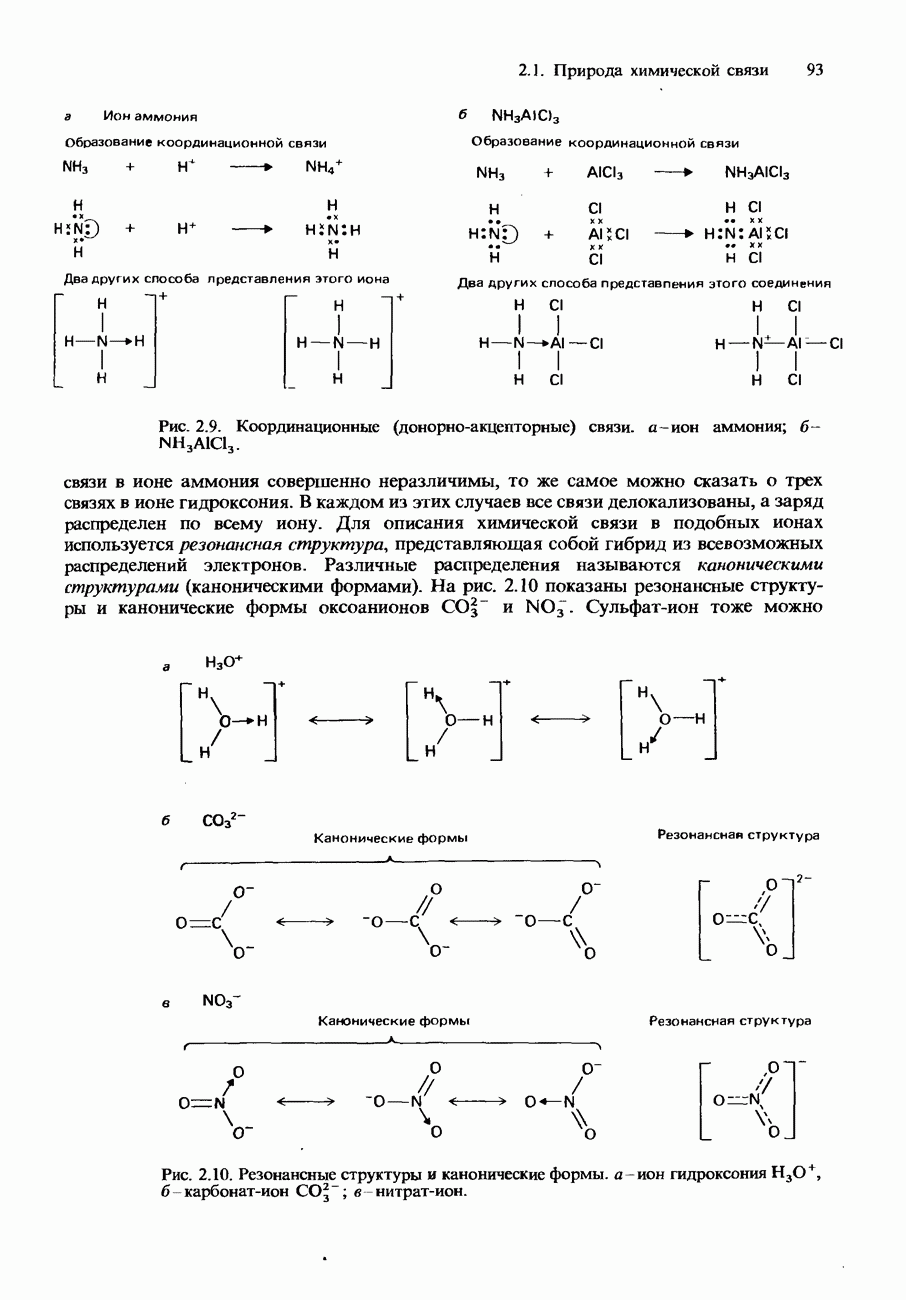
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
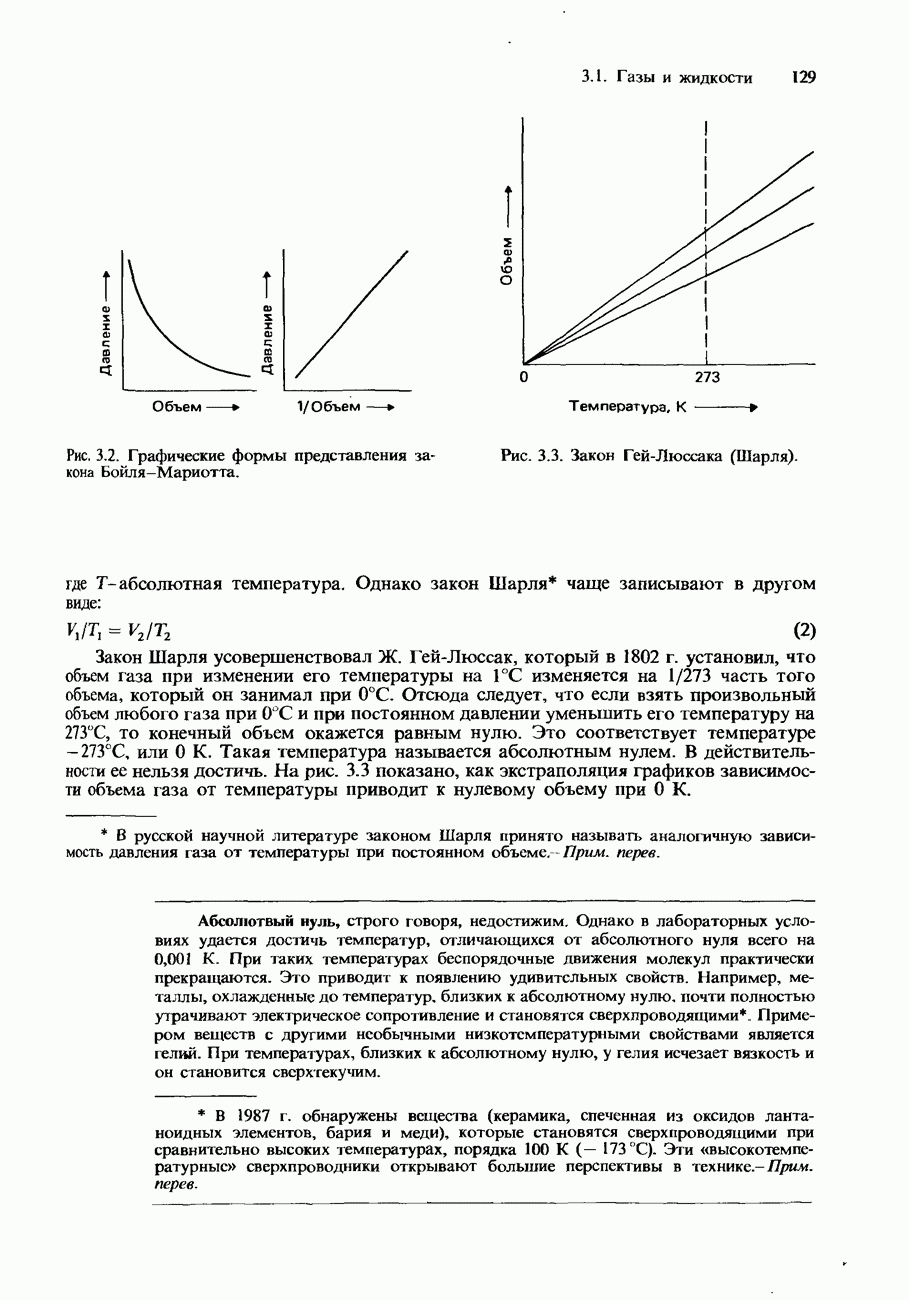
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
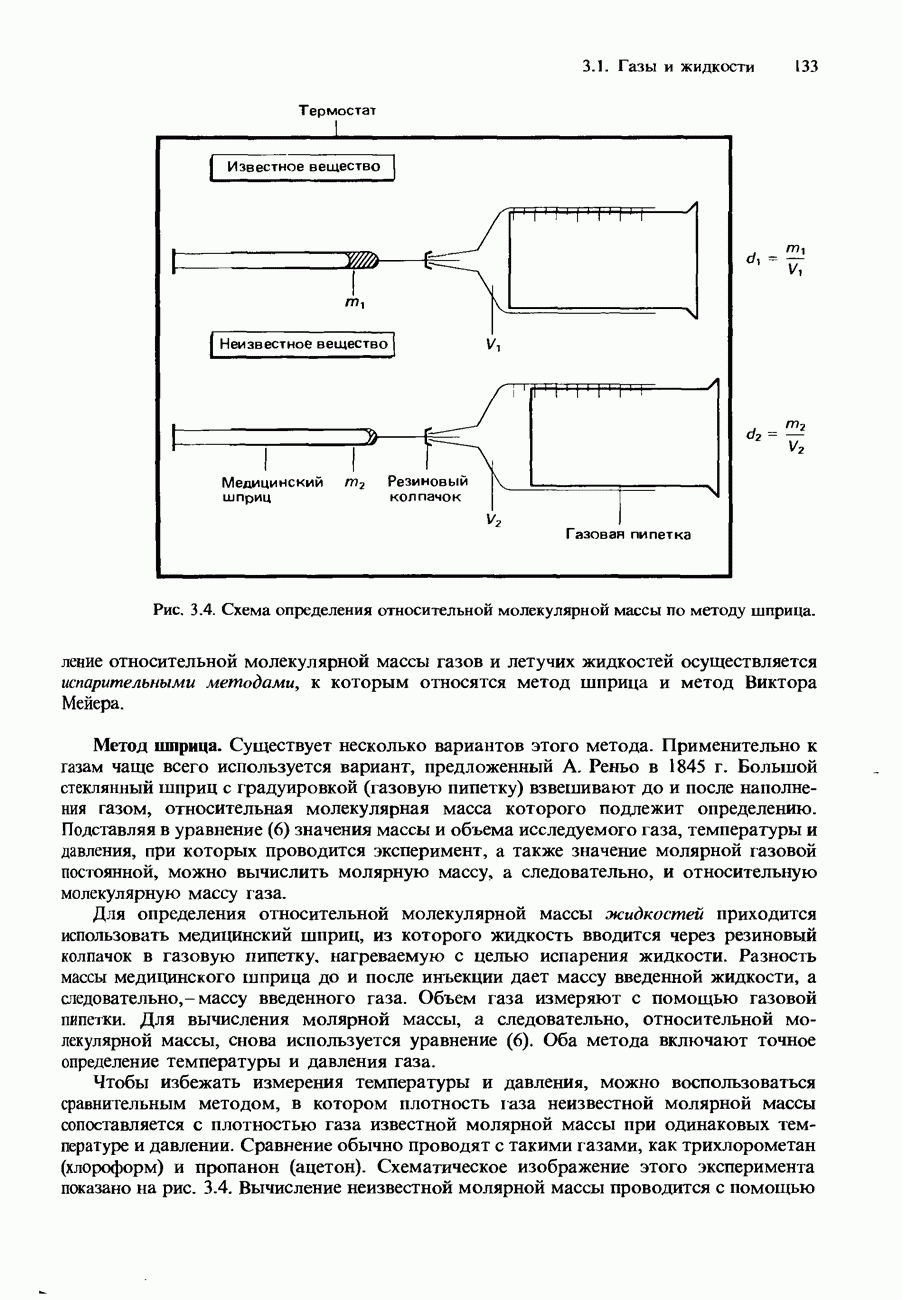
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
- Сжижение газов
- ЖИДКОСТИ
- Свойства жидкостей
- 3.2. Твердые вещества
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
- Ионные кристаллы
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
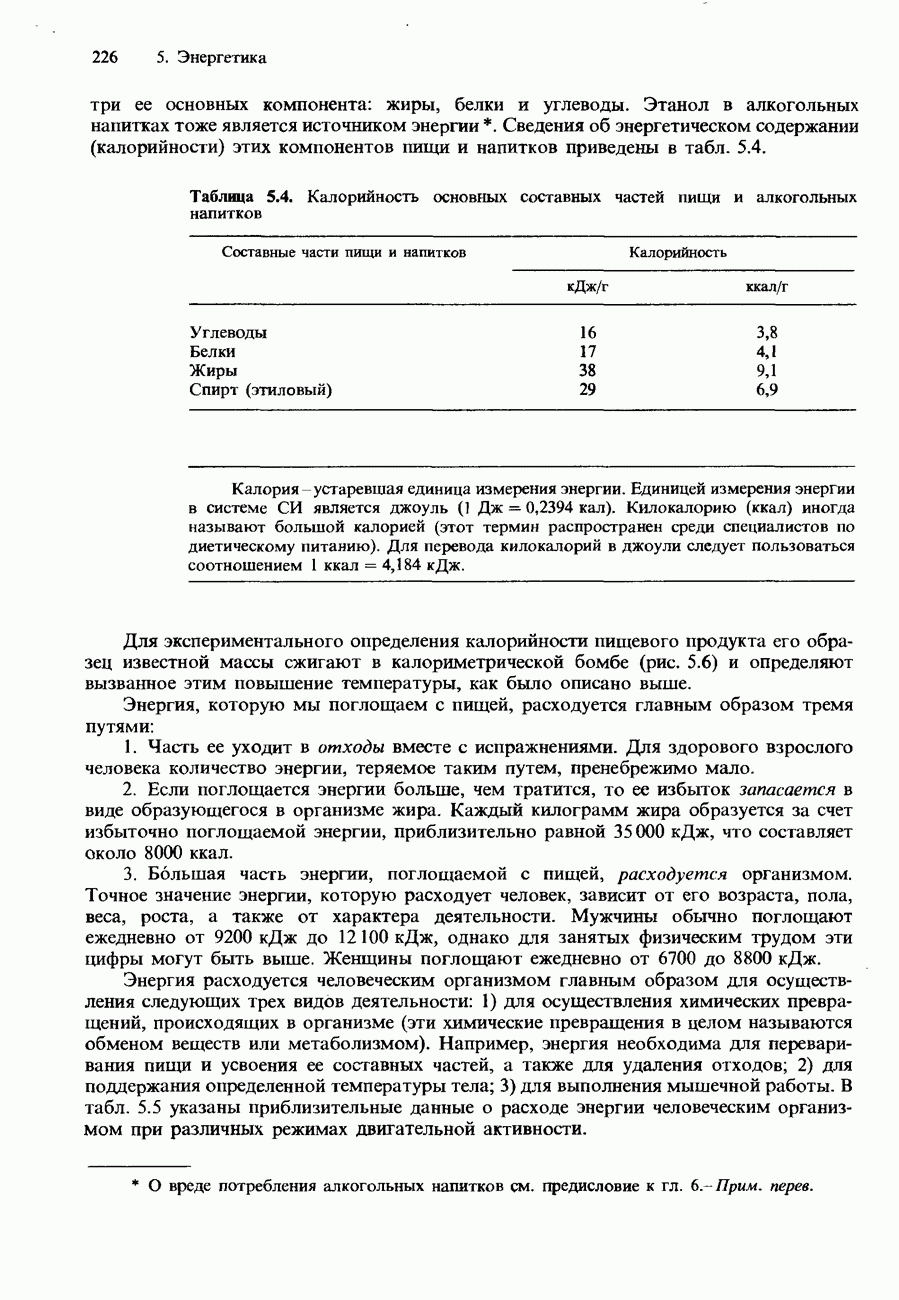
- КАЛОРИЙНОСТЬ ПИЩИ
- ЗАКОН ГЕССА
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
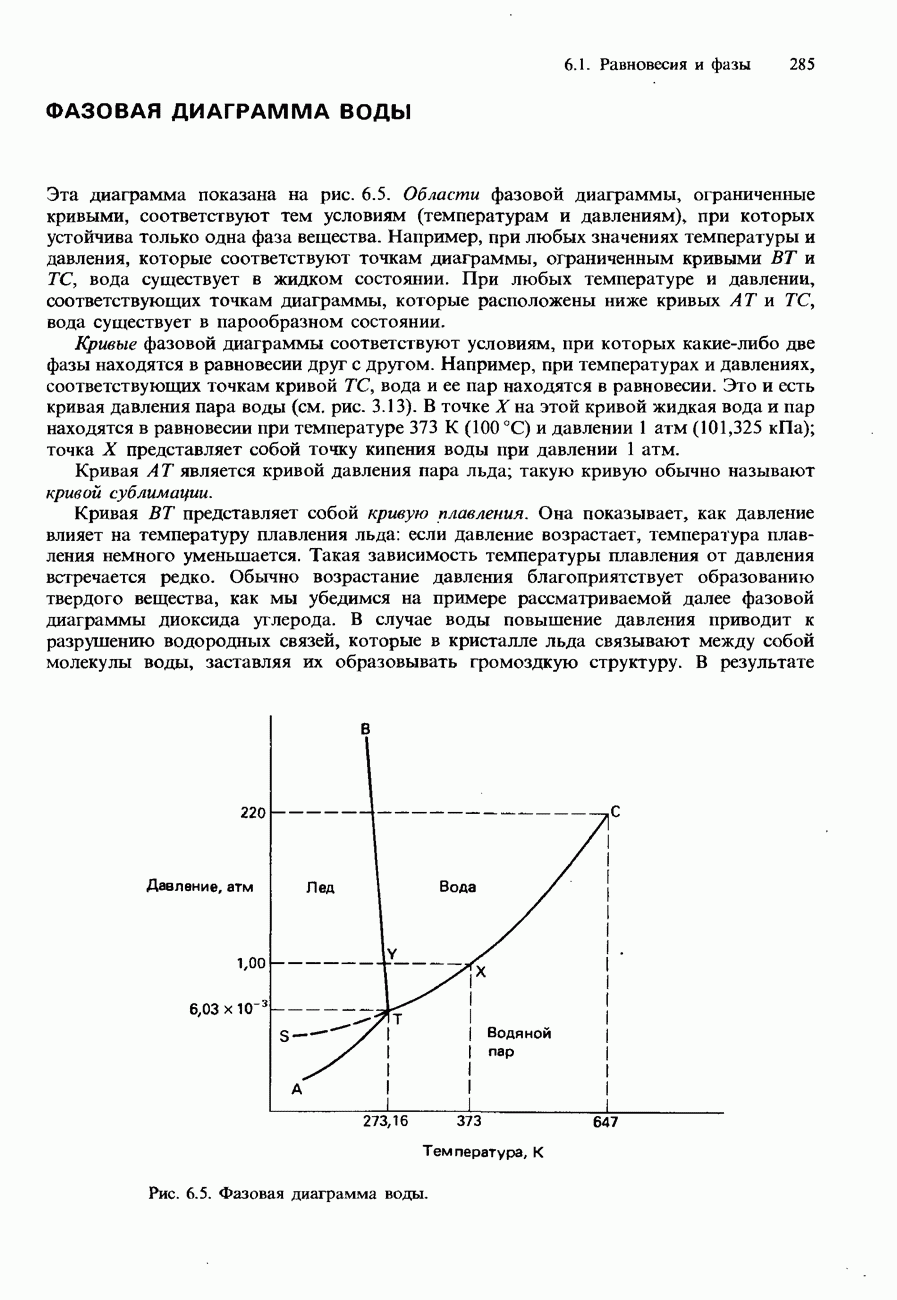
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
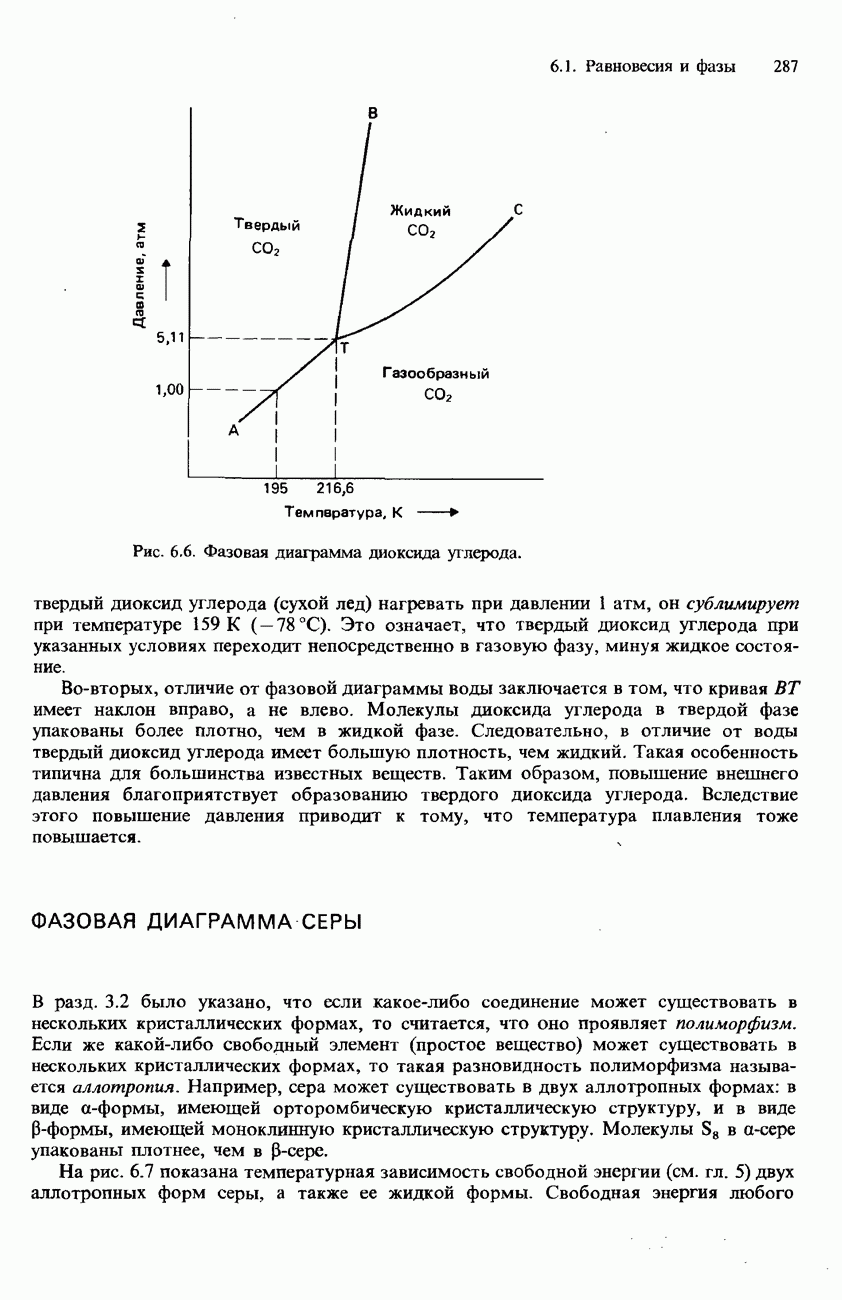
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
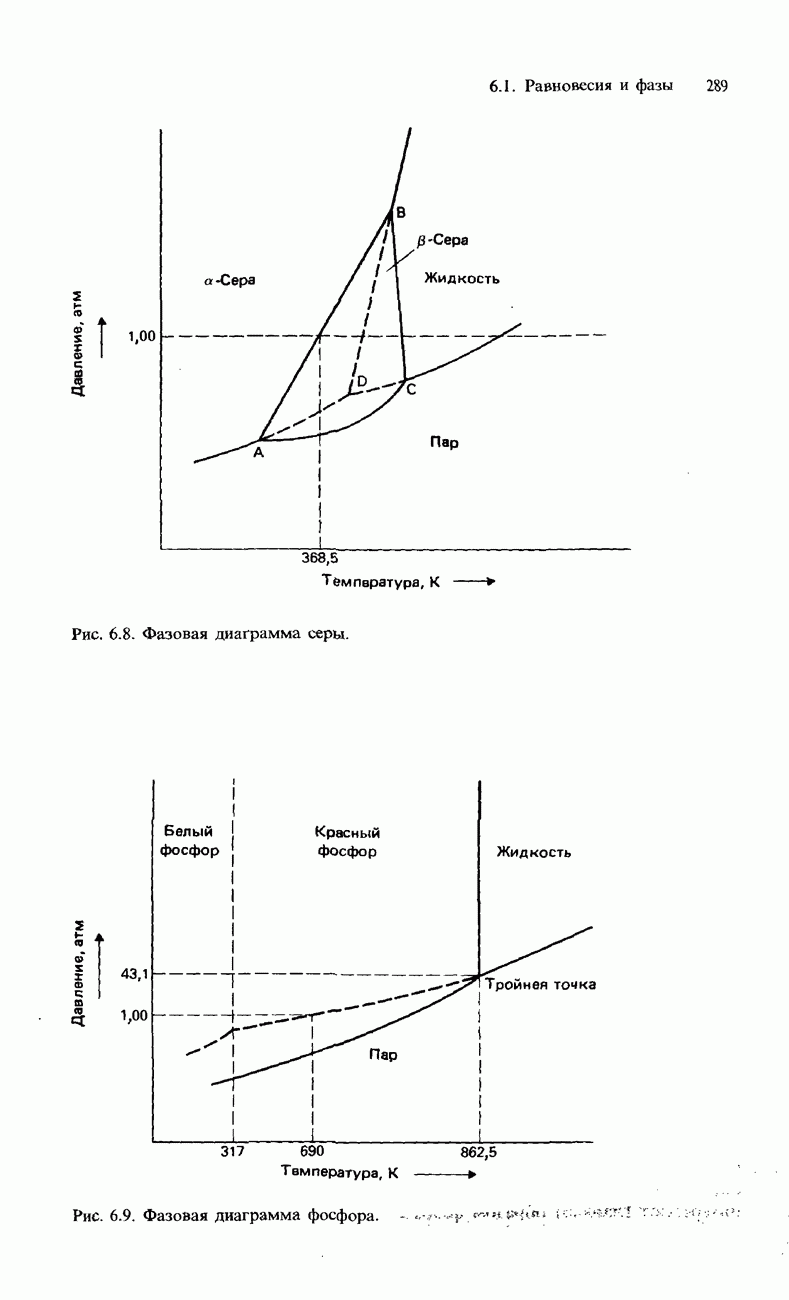
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
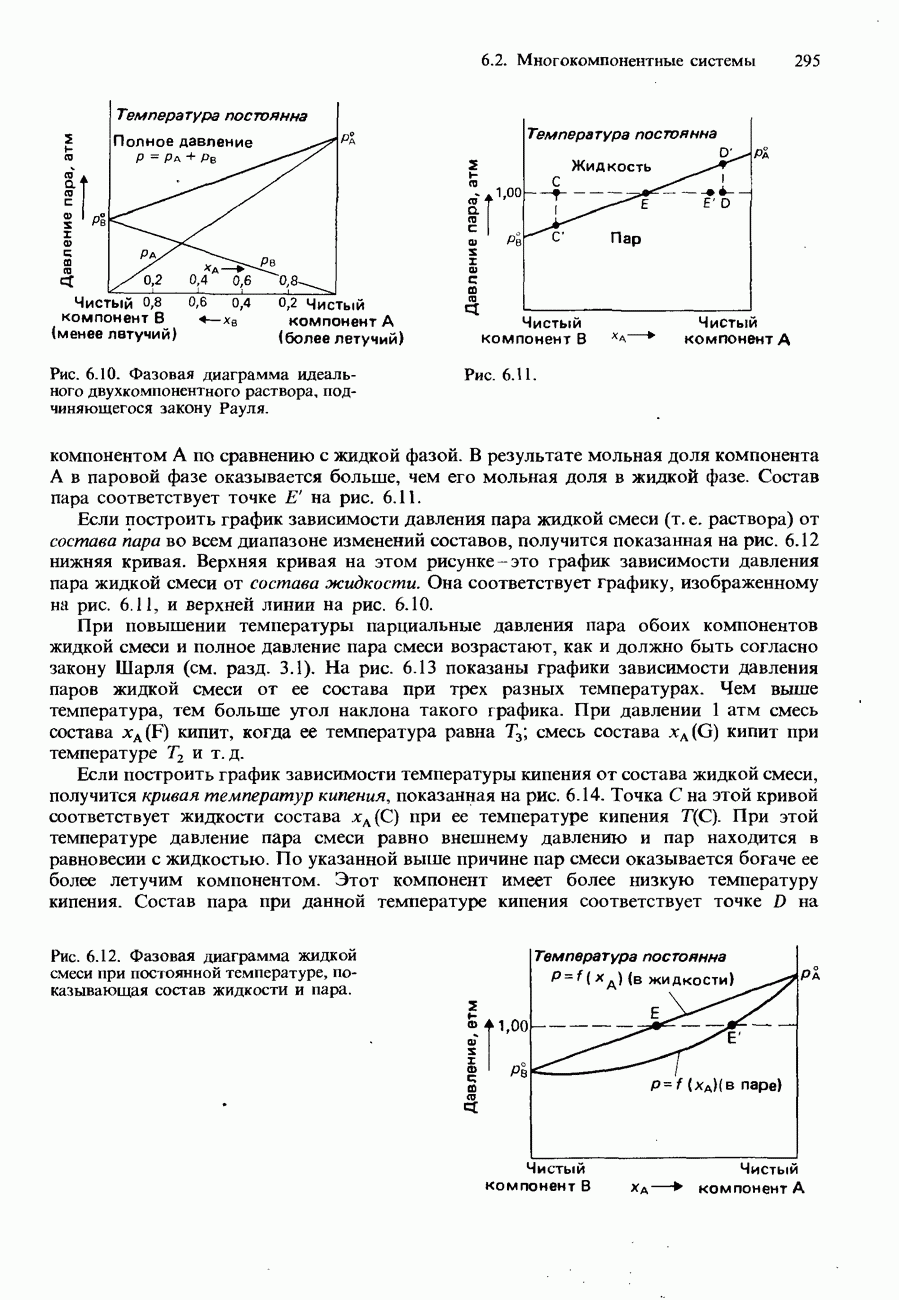
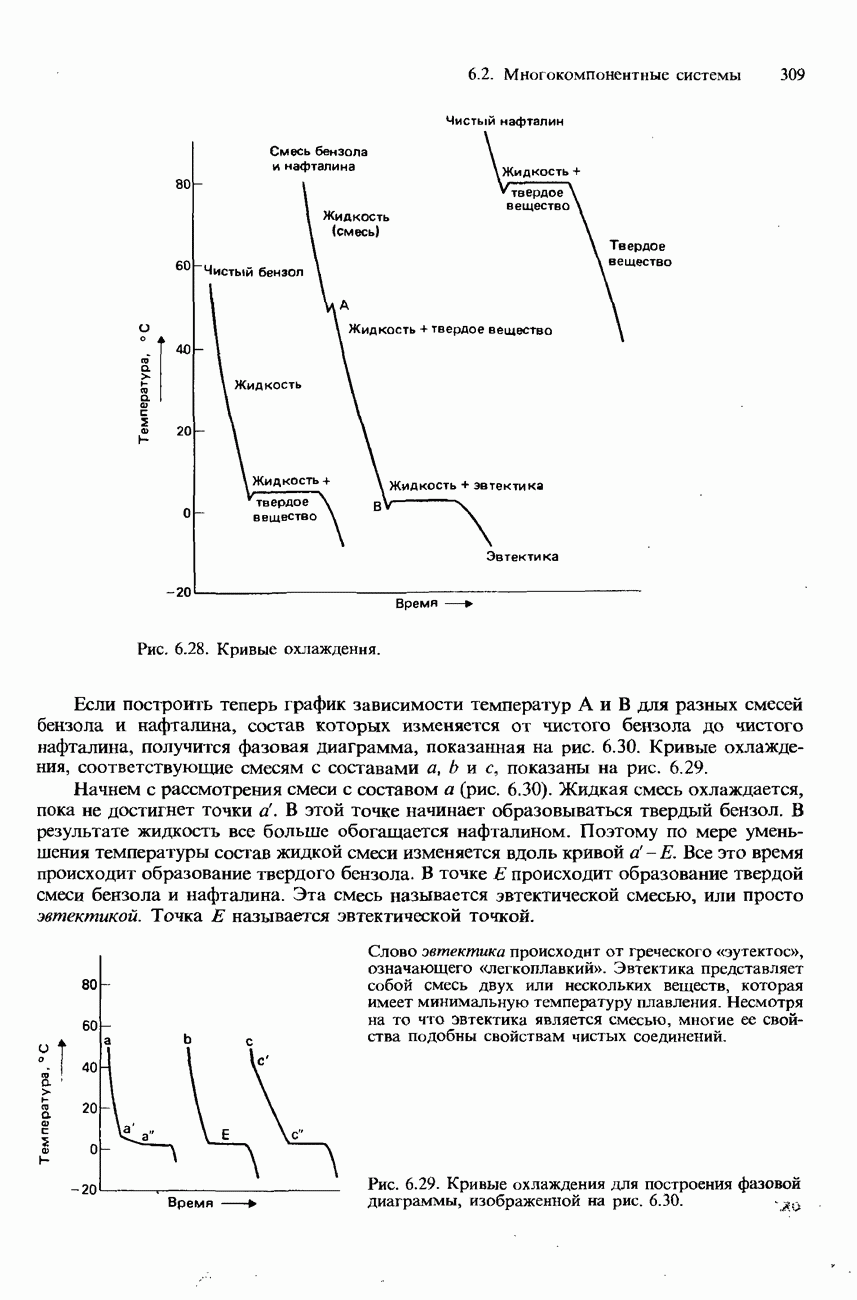
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- Фазовые диаграммы полностью смешивающихся жидкостей
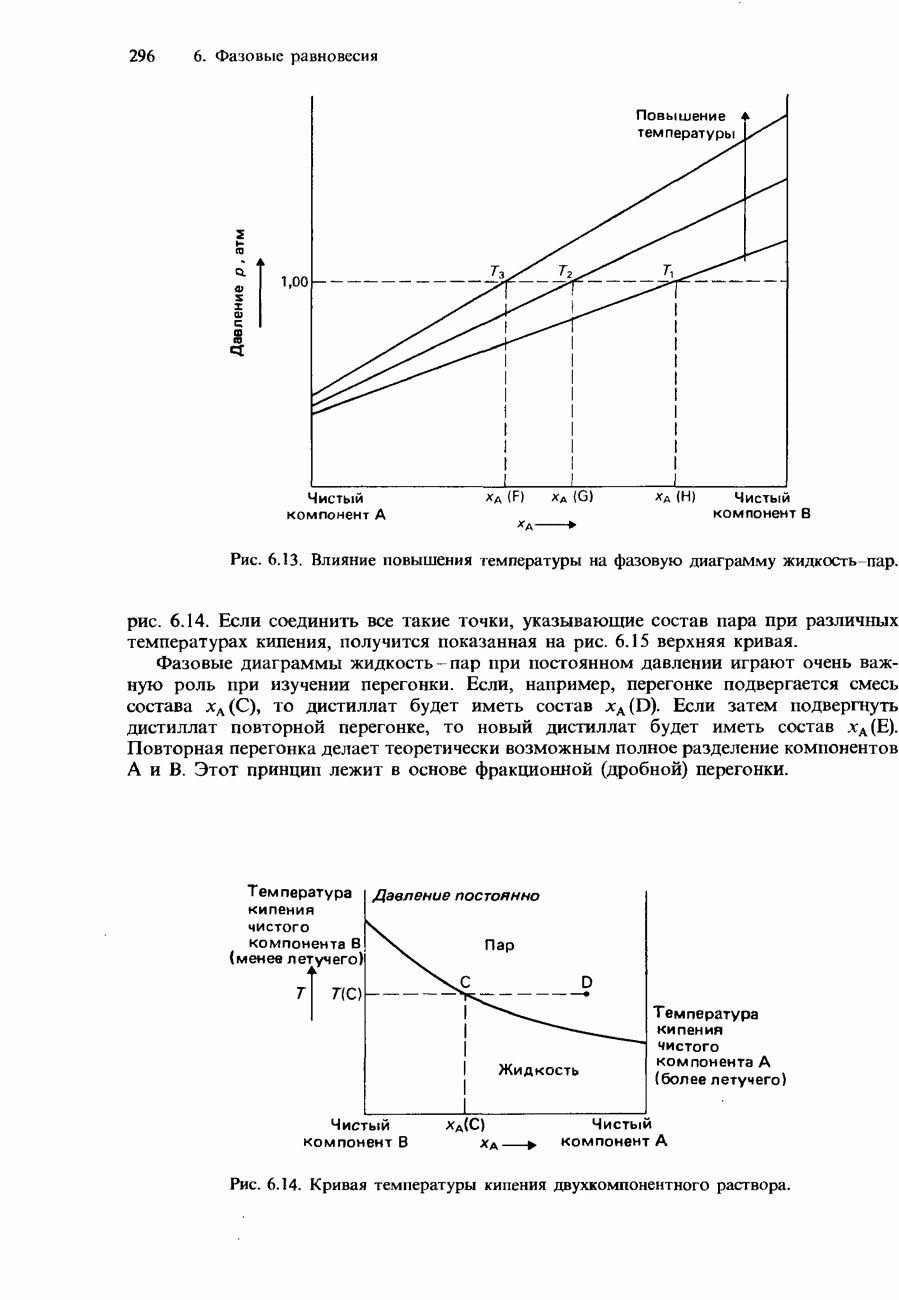
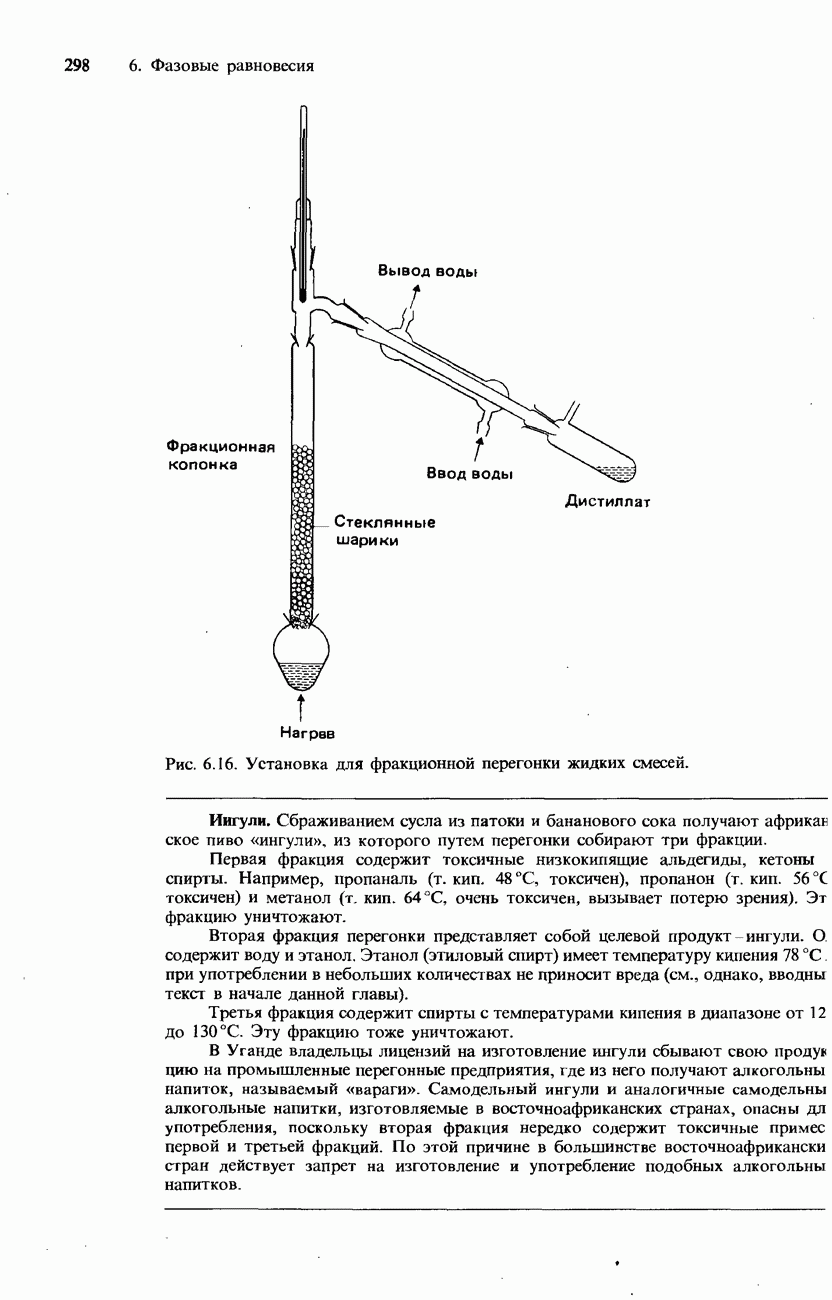
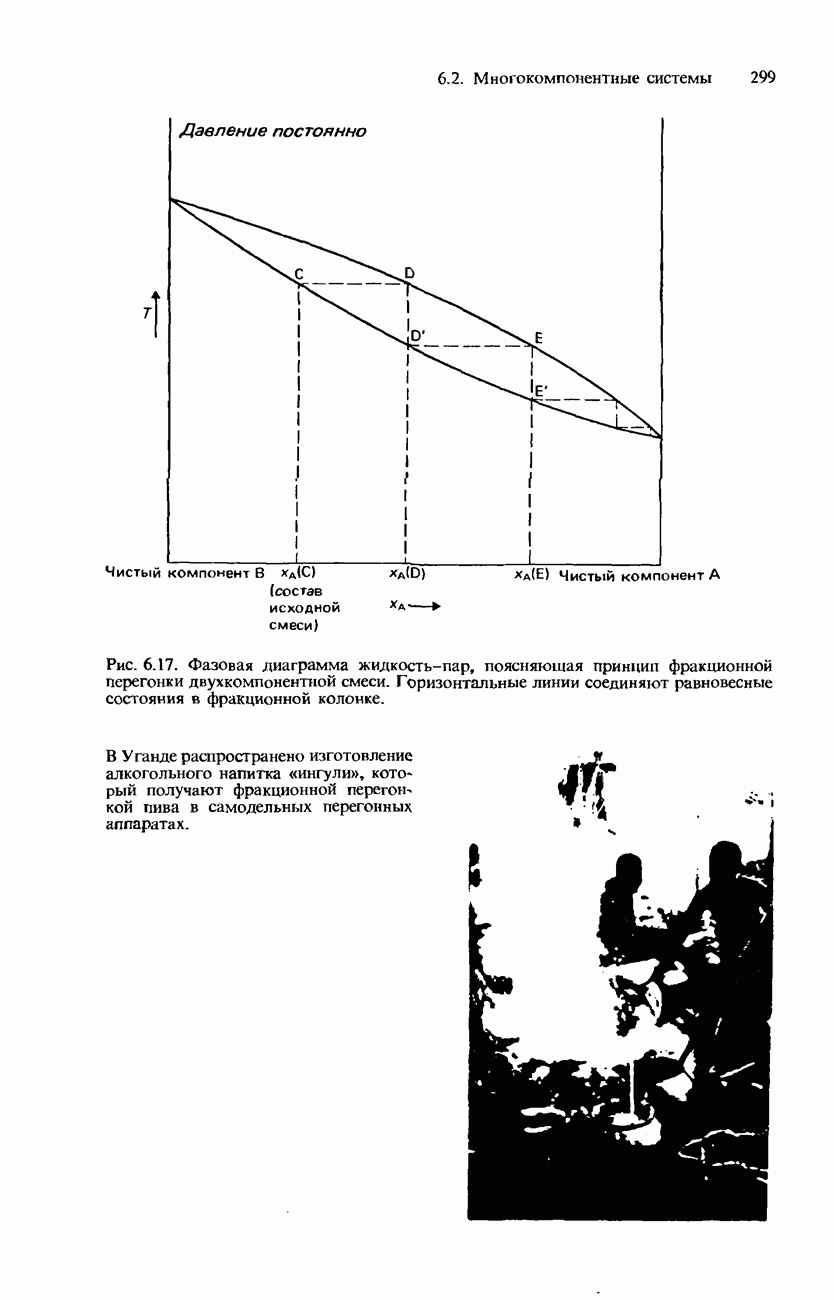
- Фракционная перегонка
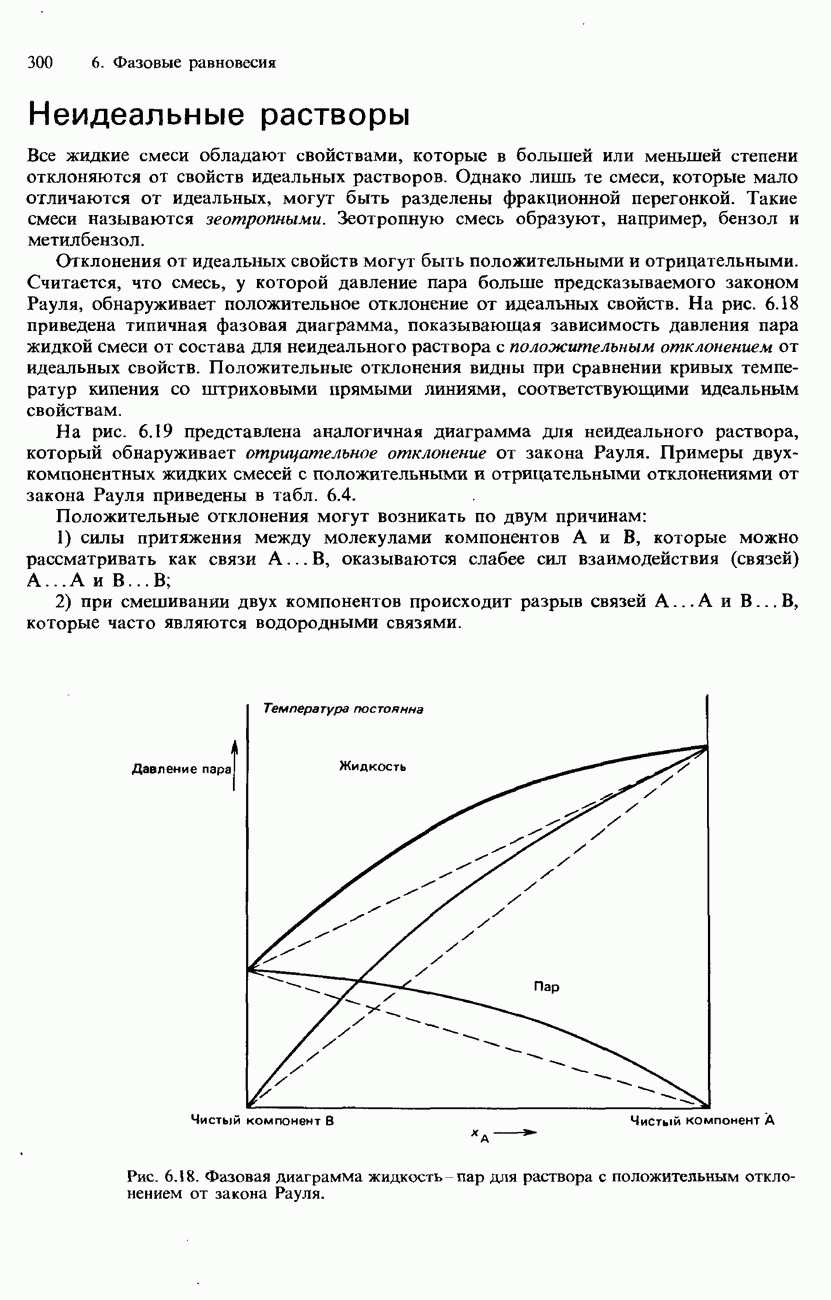
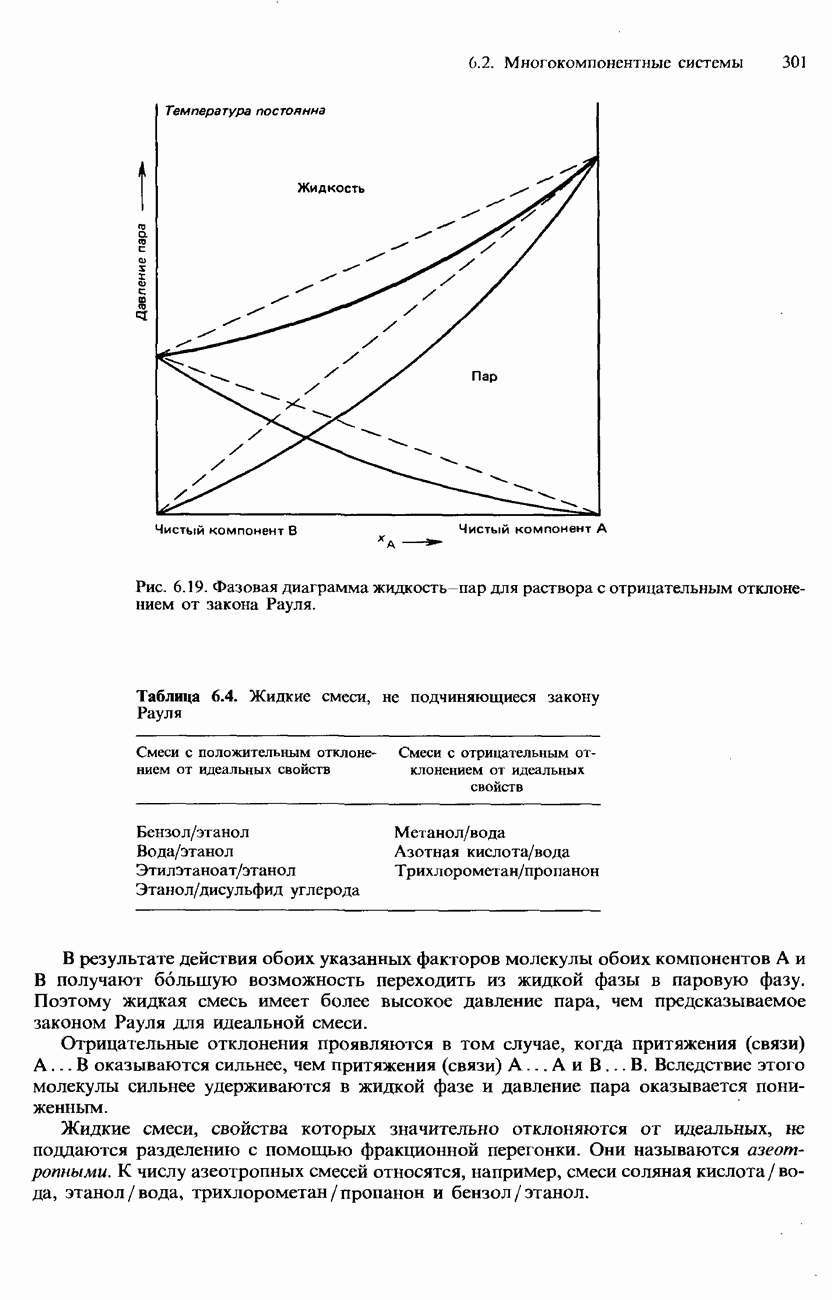
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
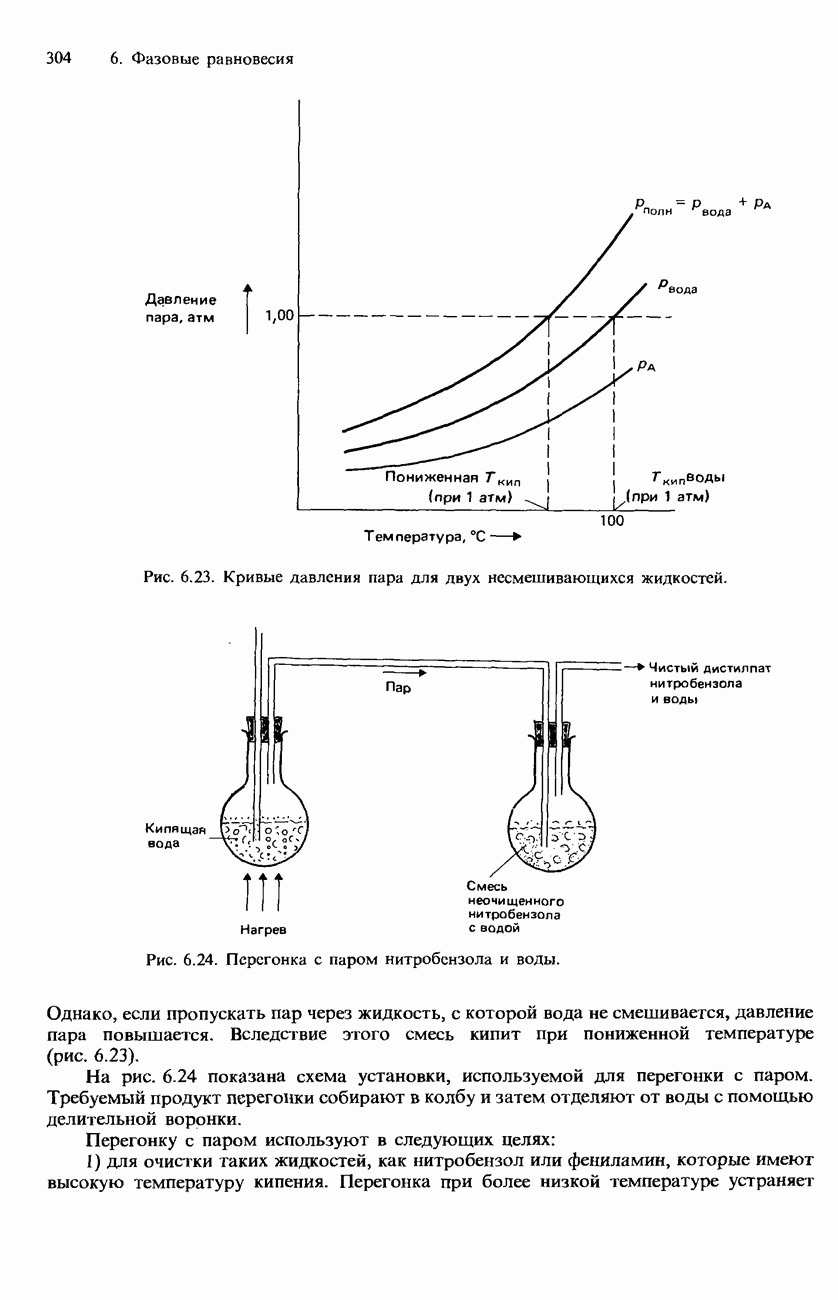
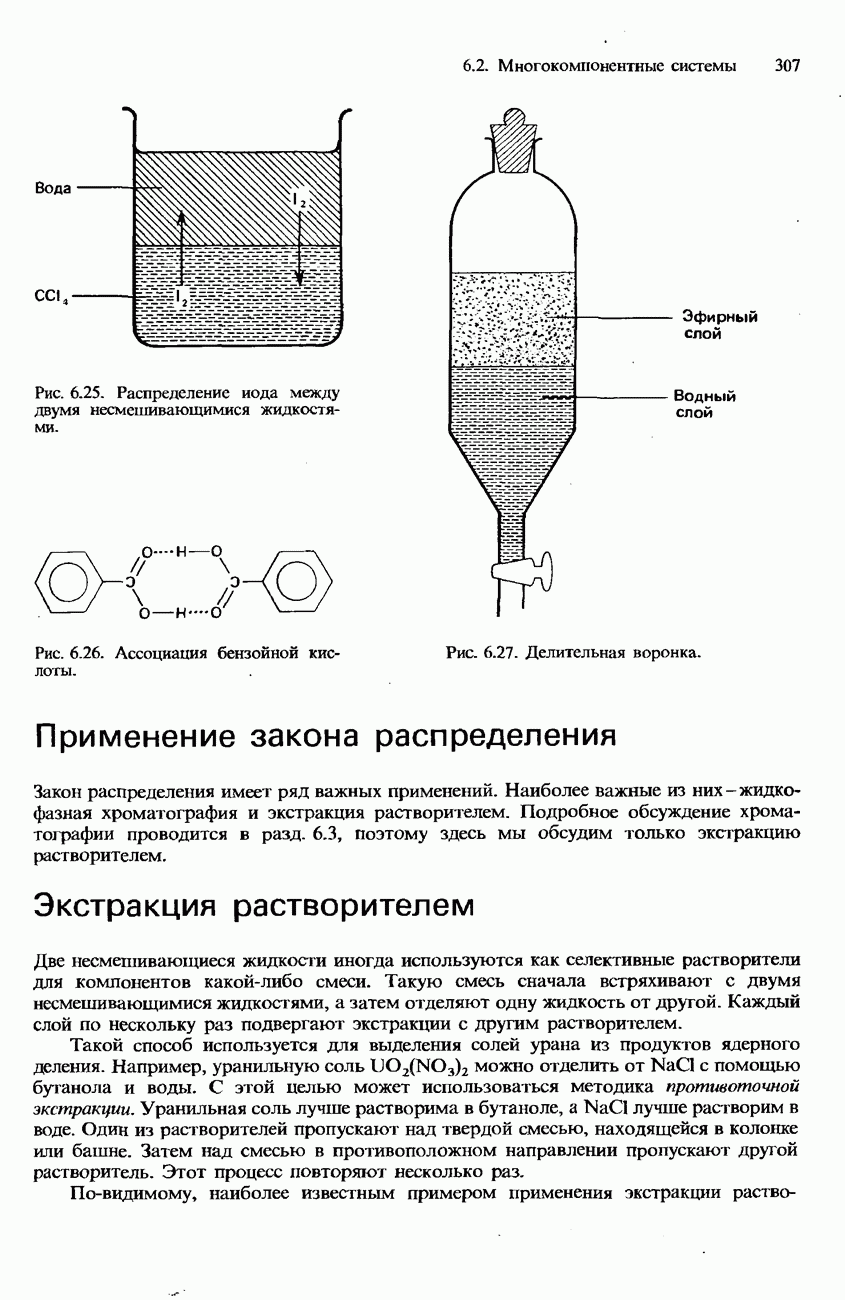
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
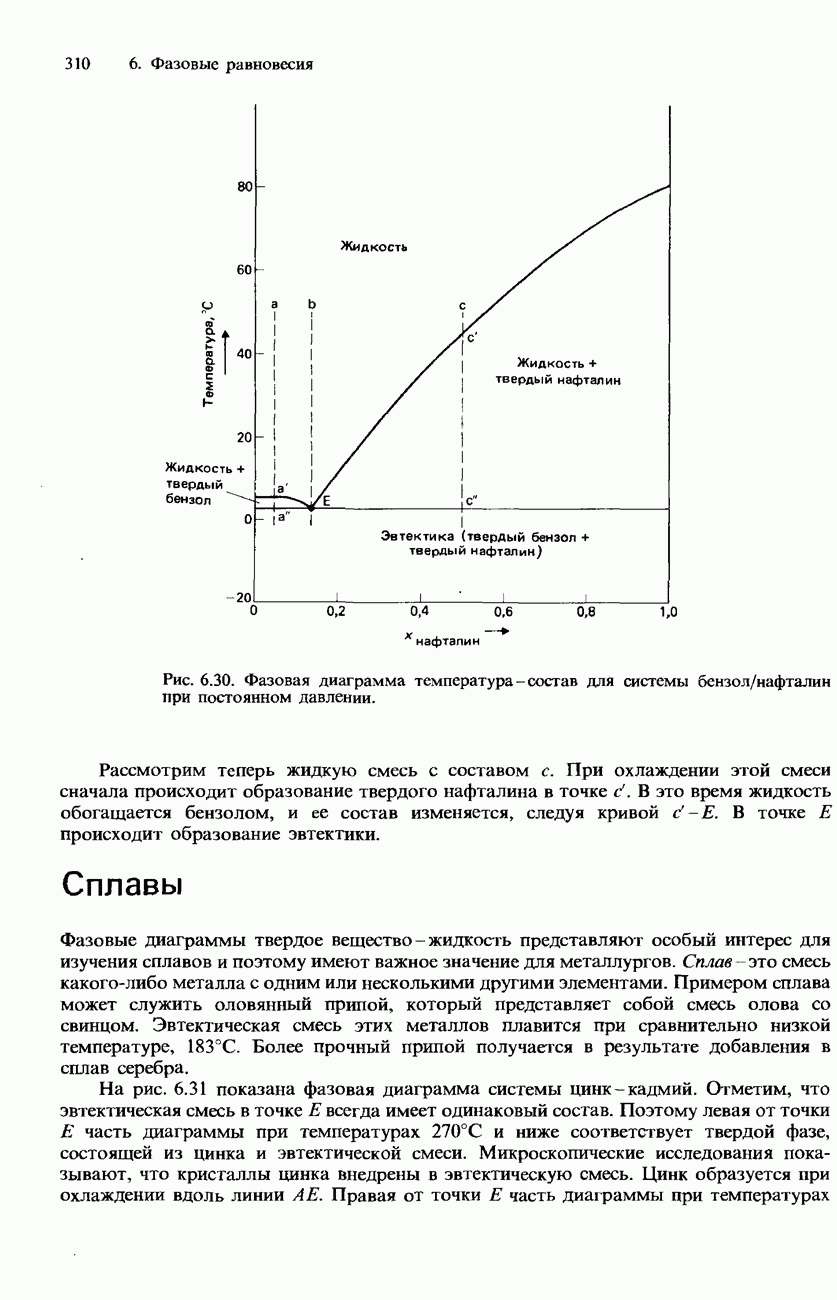
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
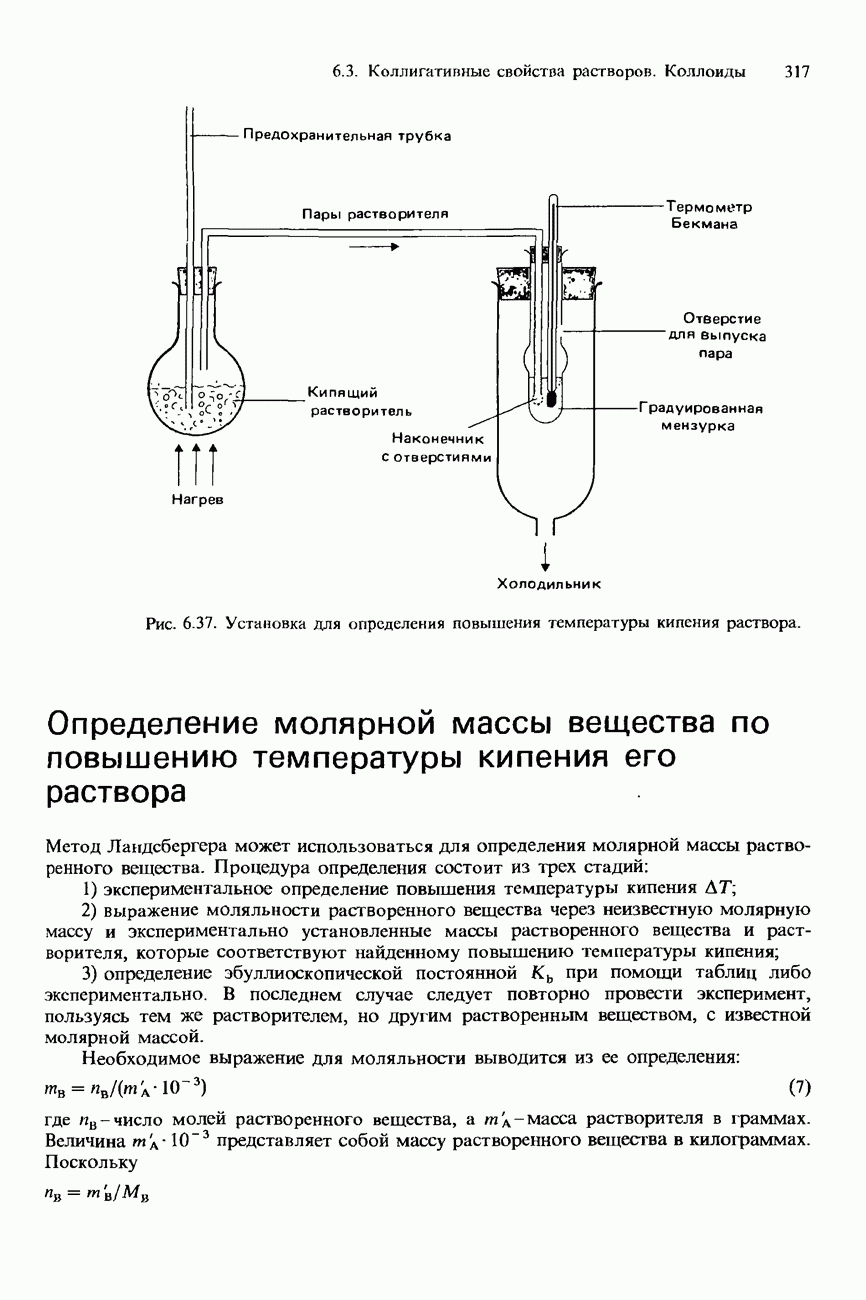
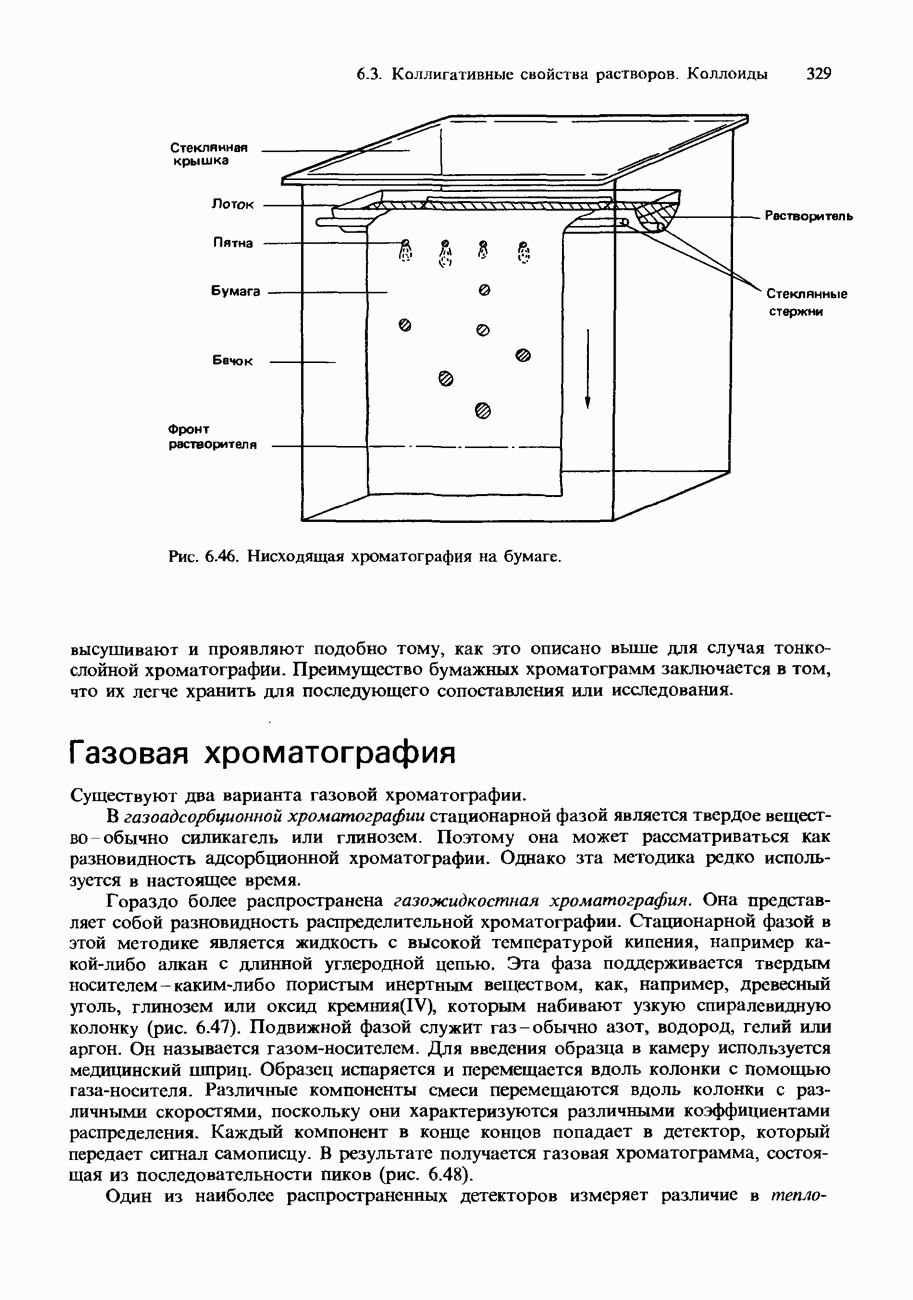
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
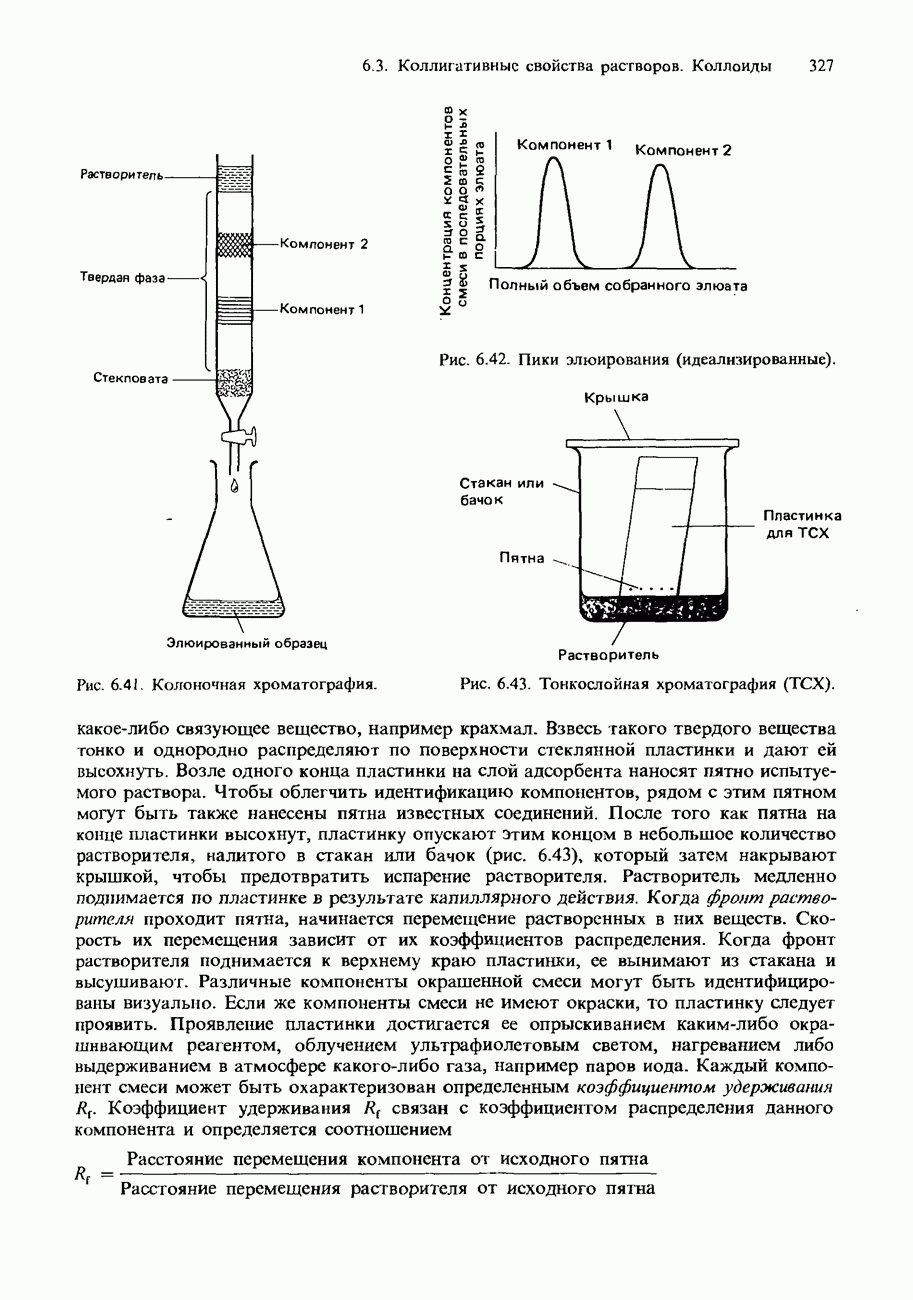
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
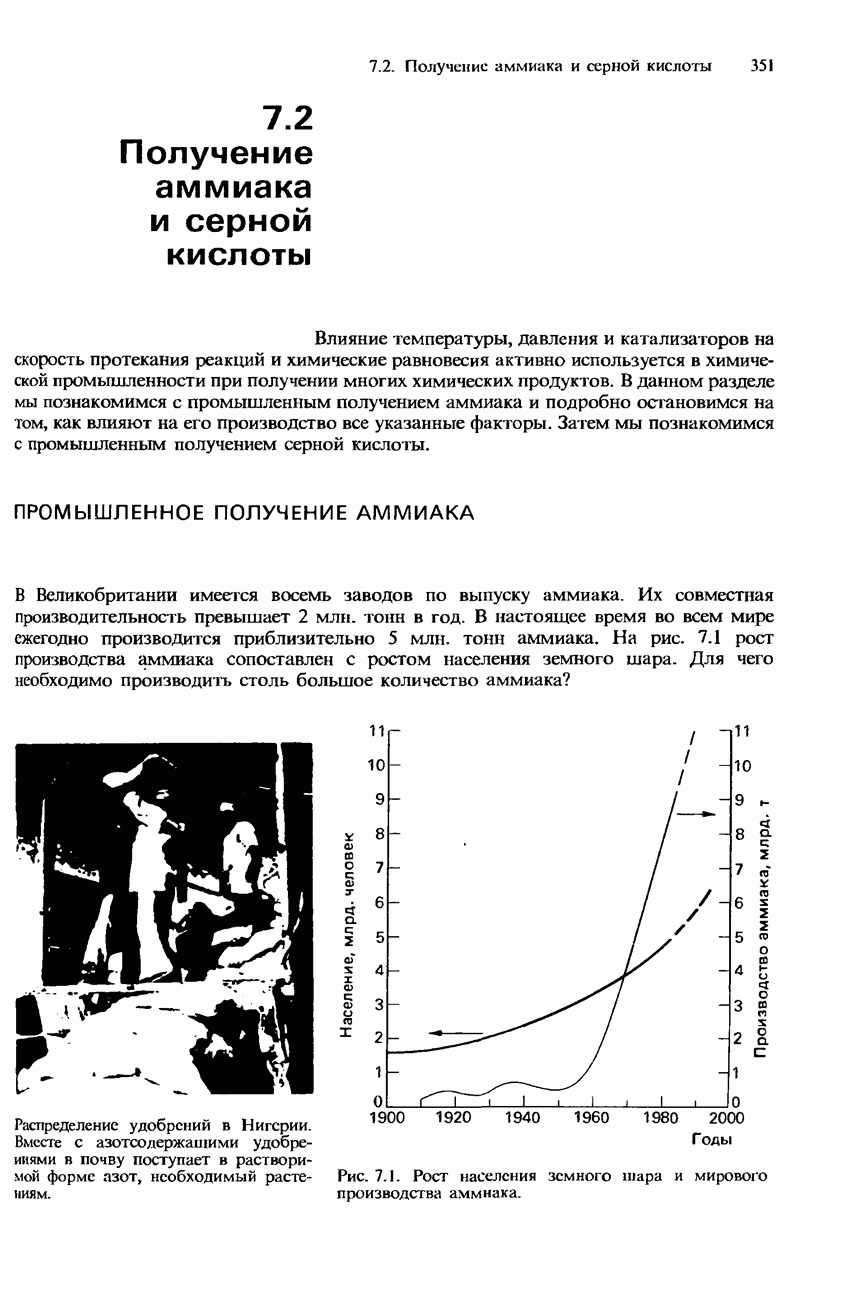
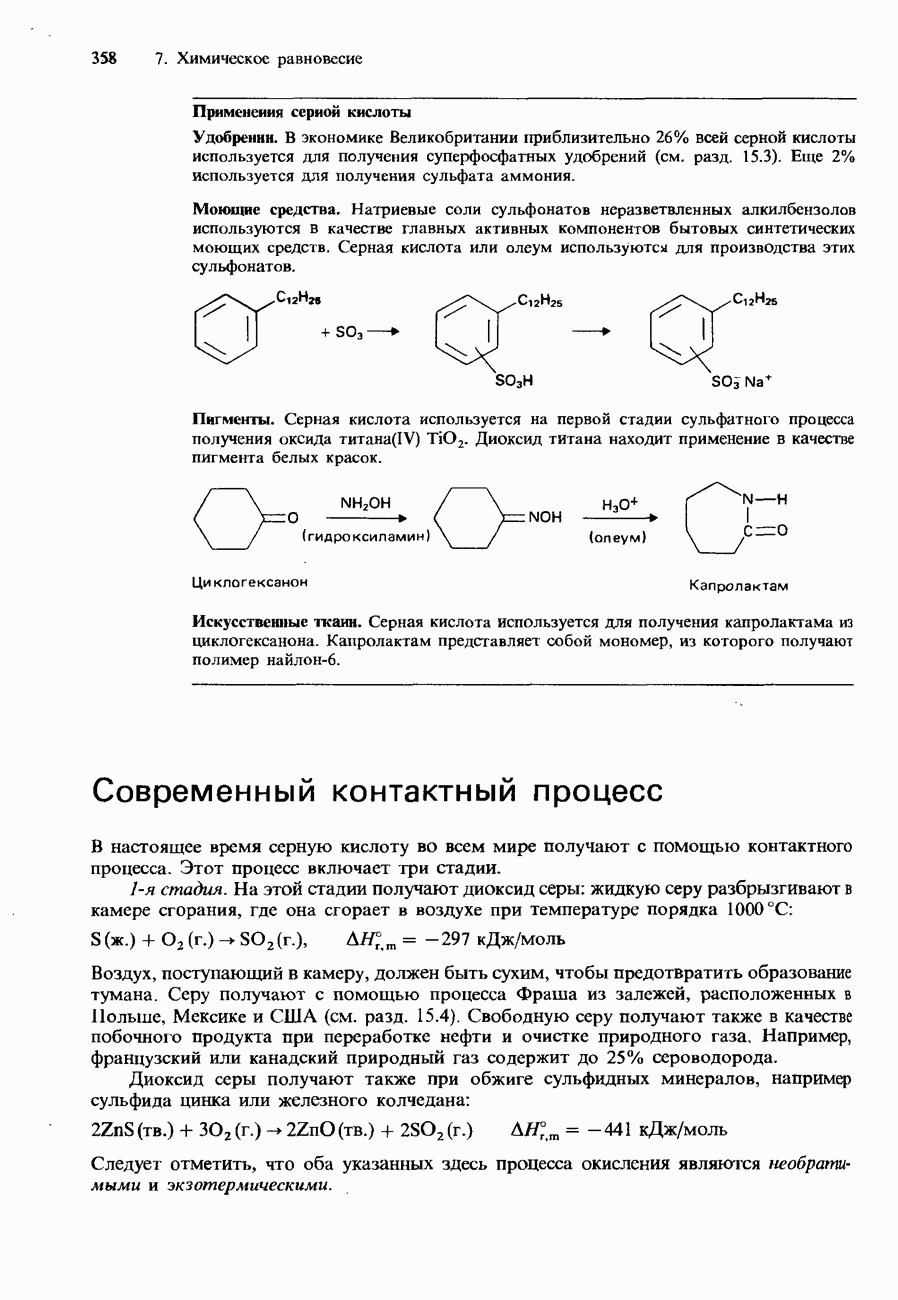
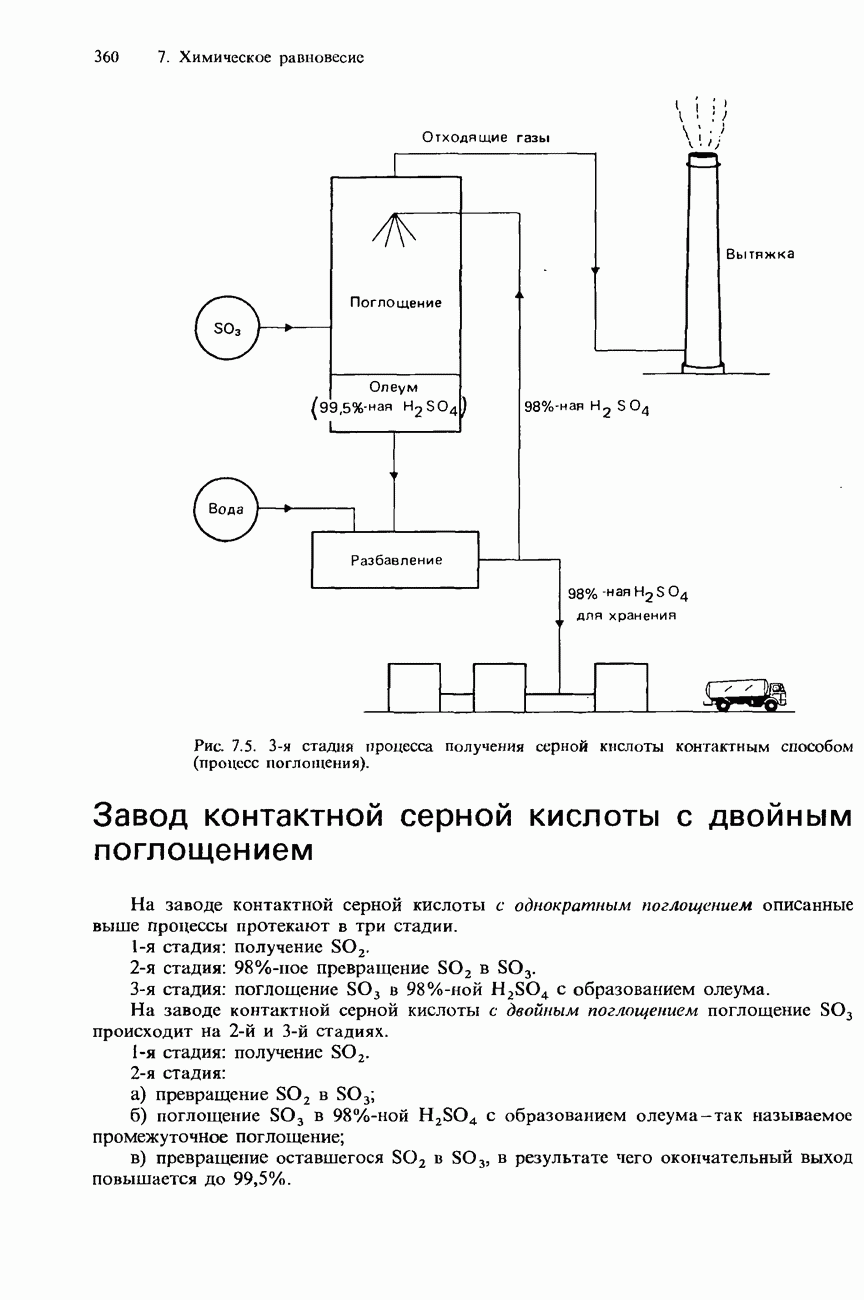
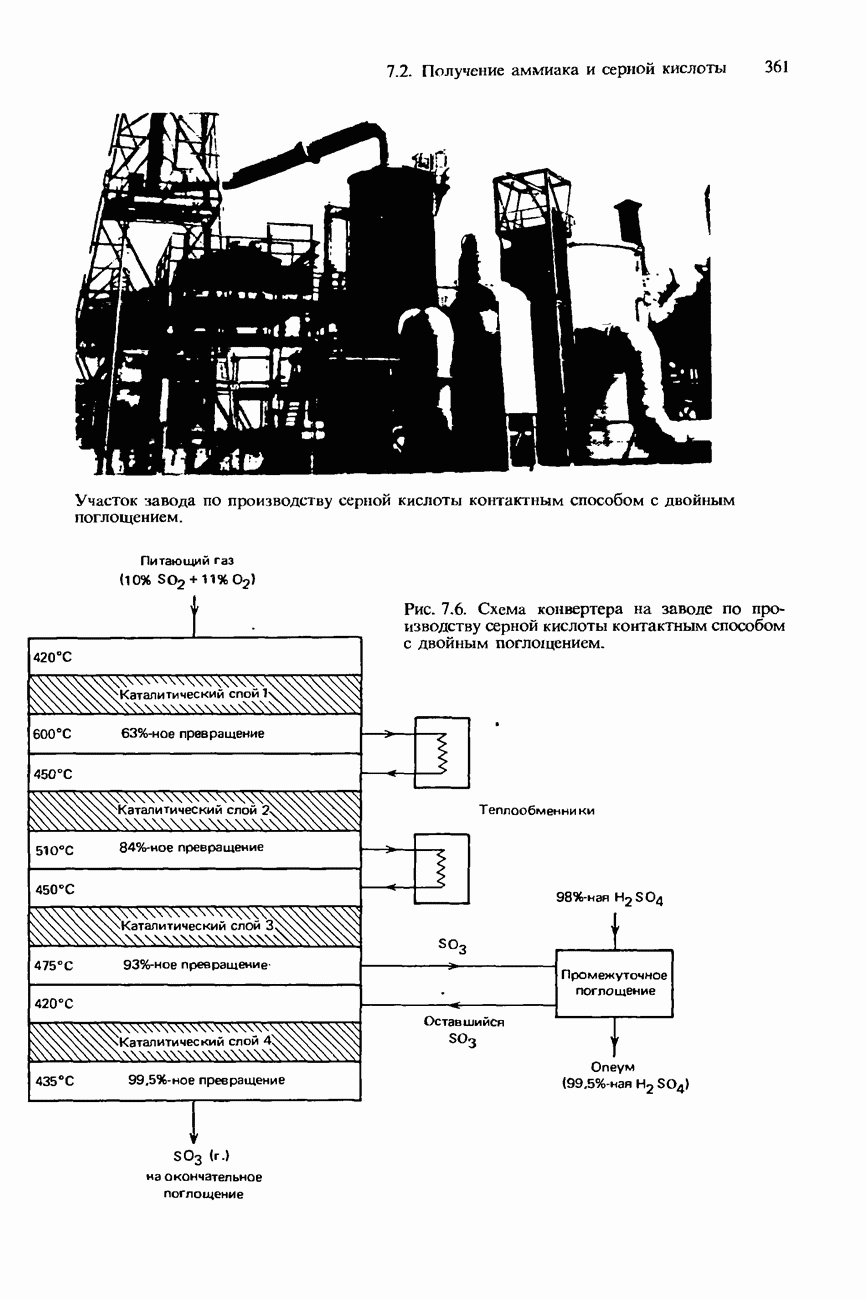
- 7.2. Получение аммиака и серной кислоты
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
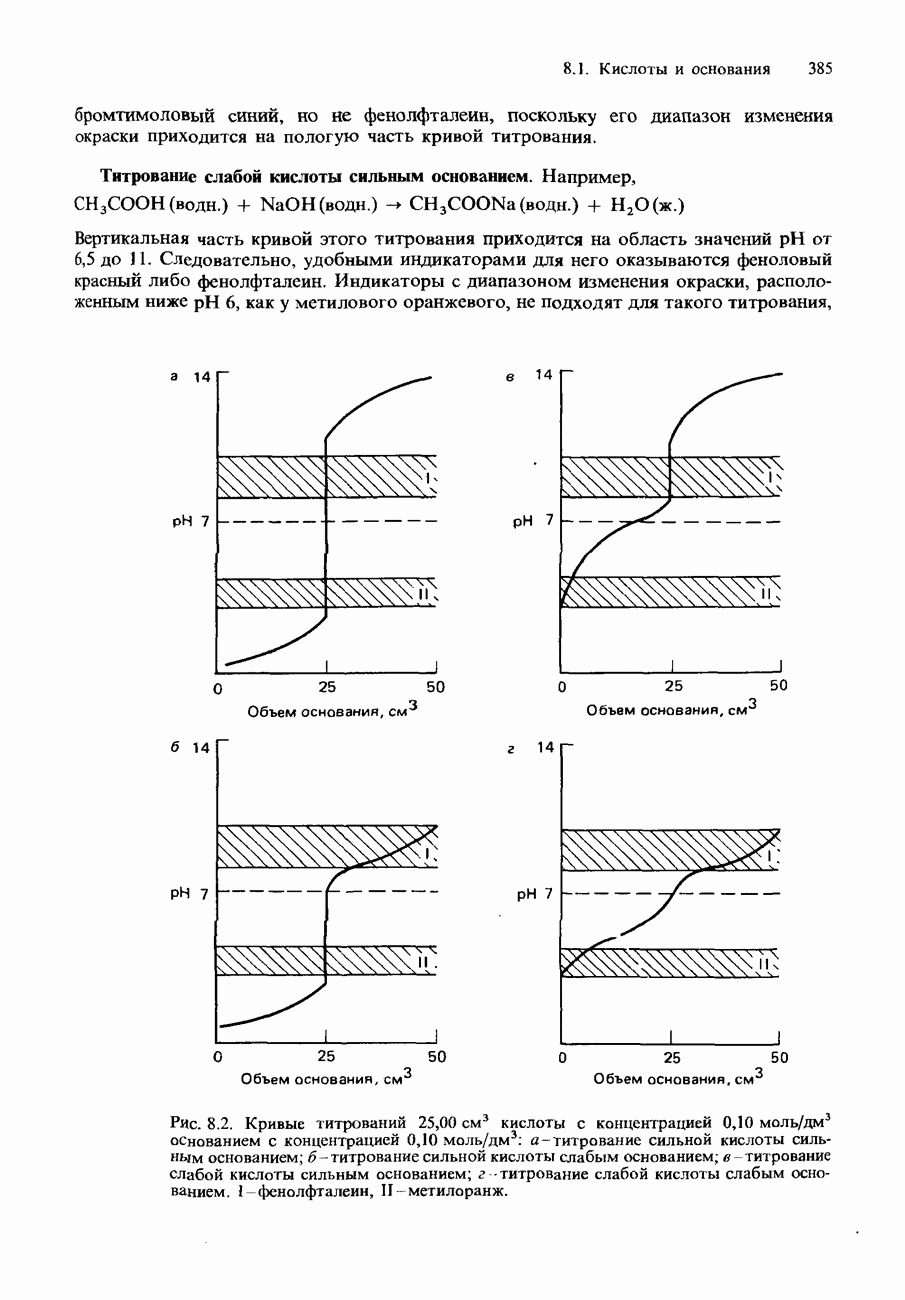
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
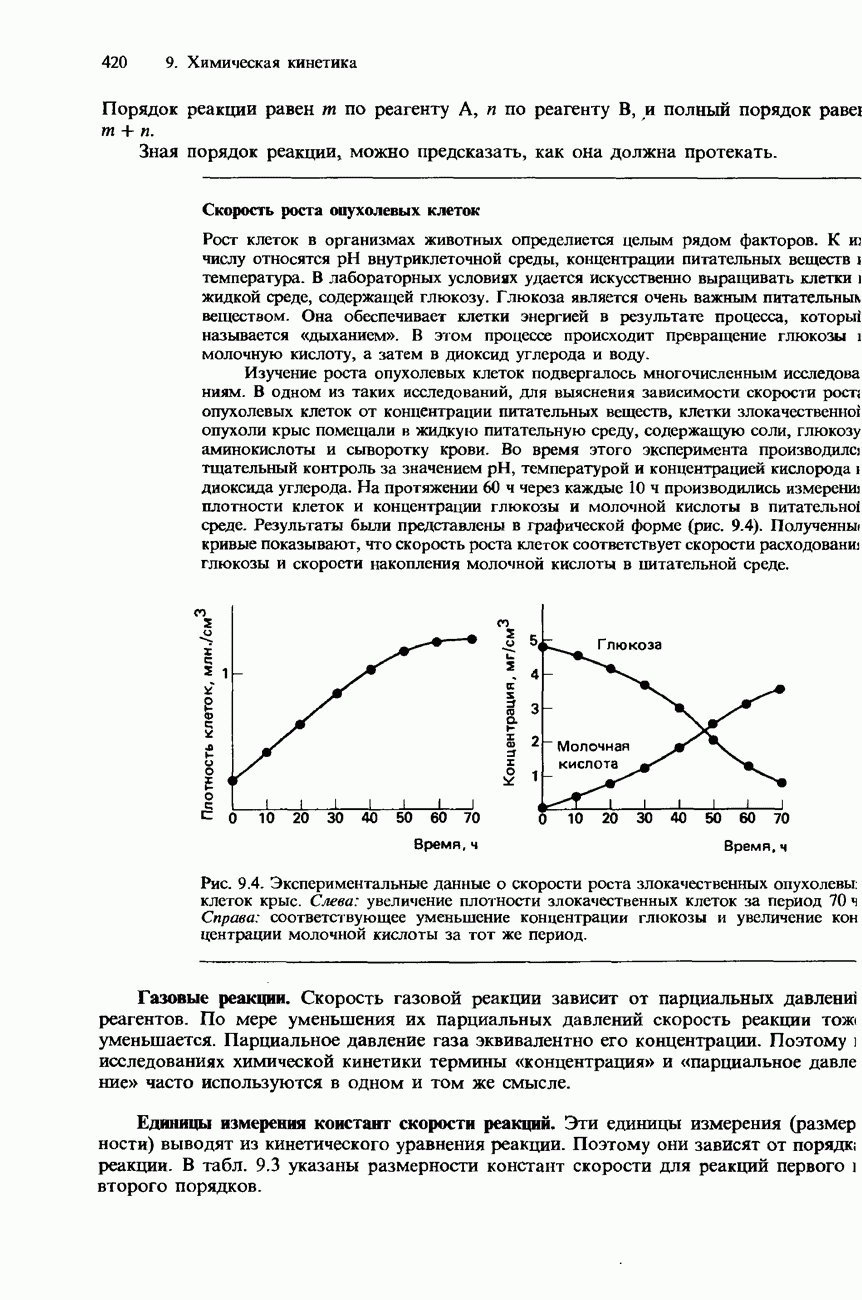
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
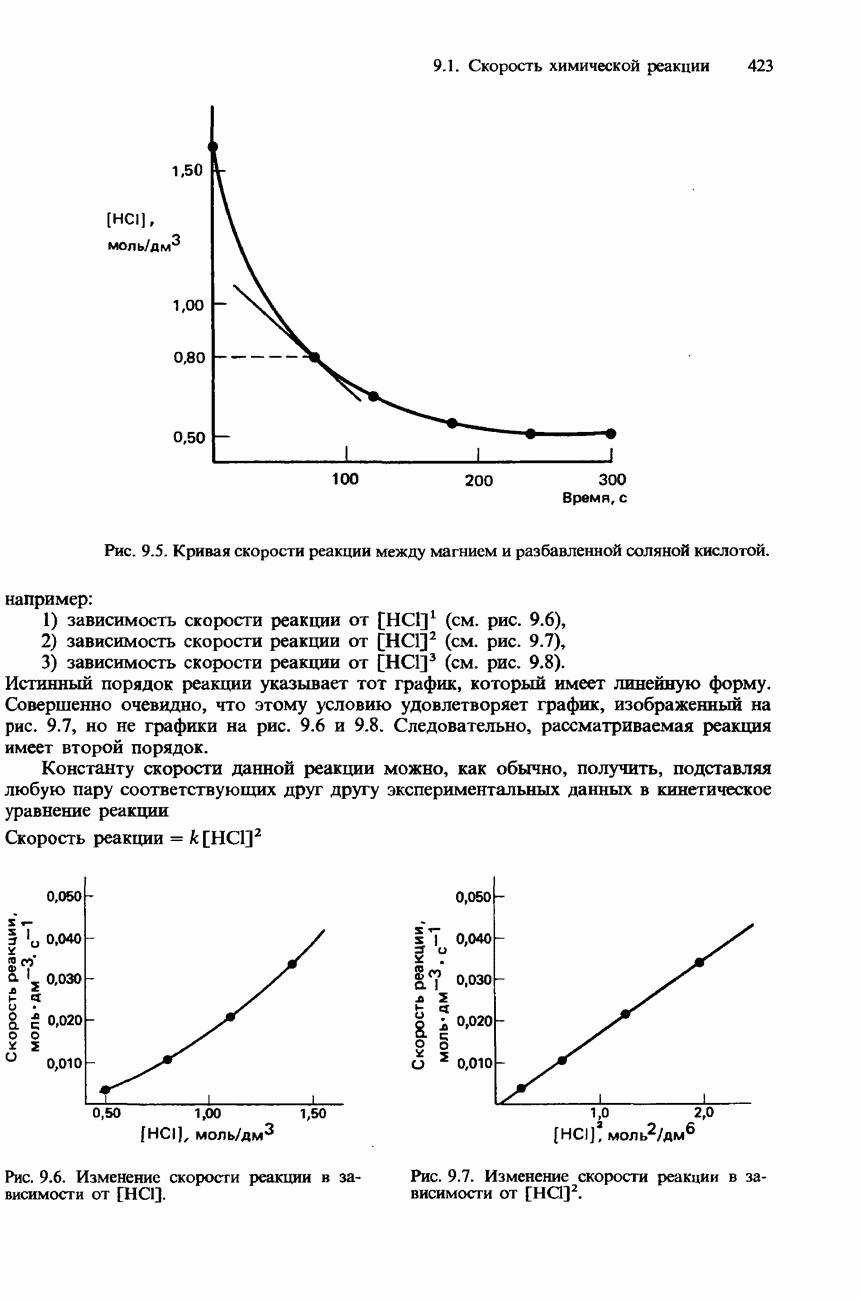
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
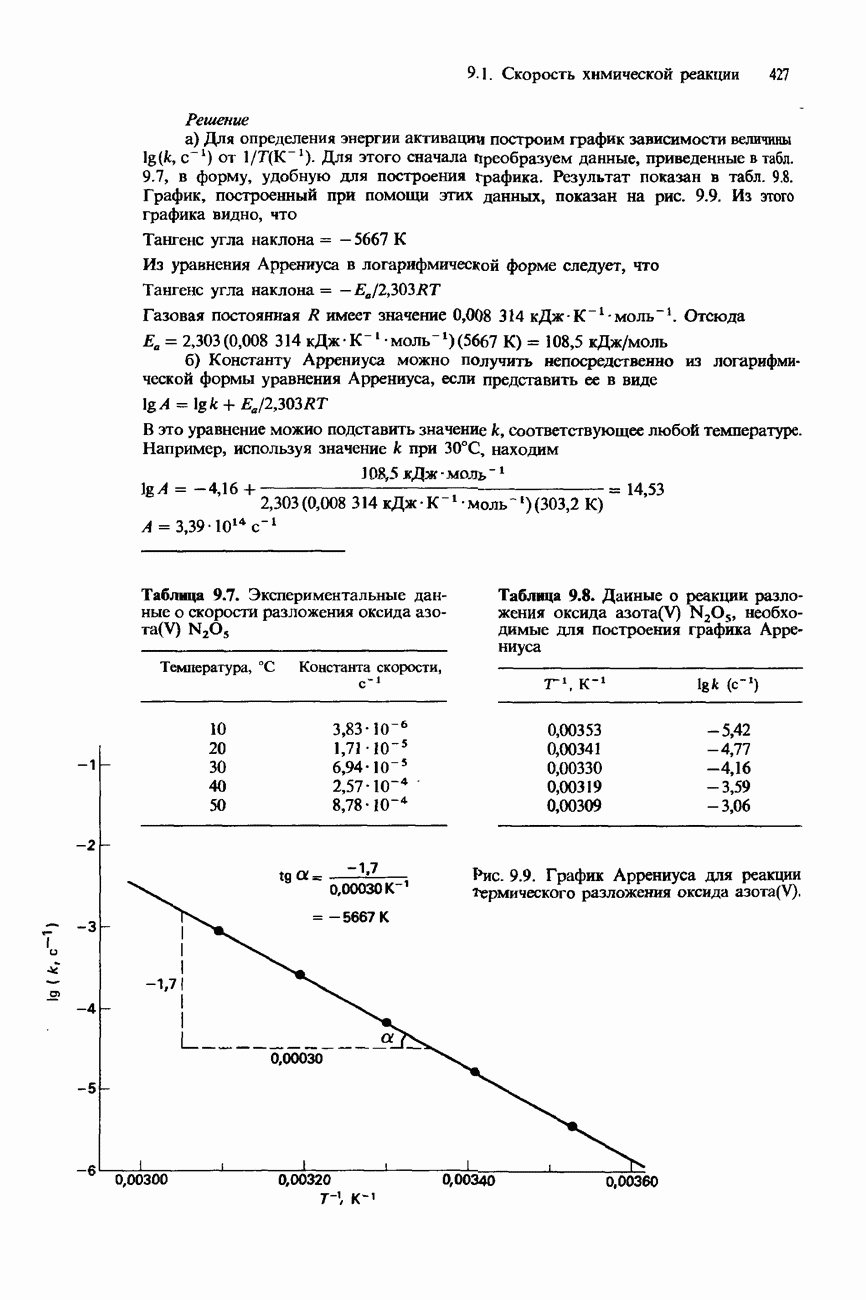
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
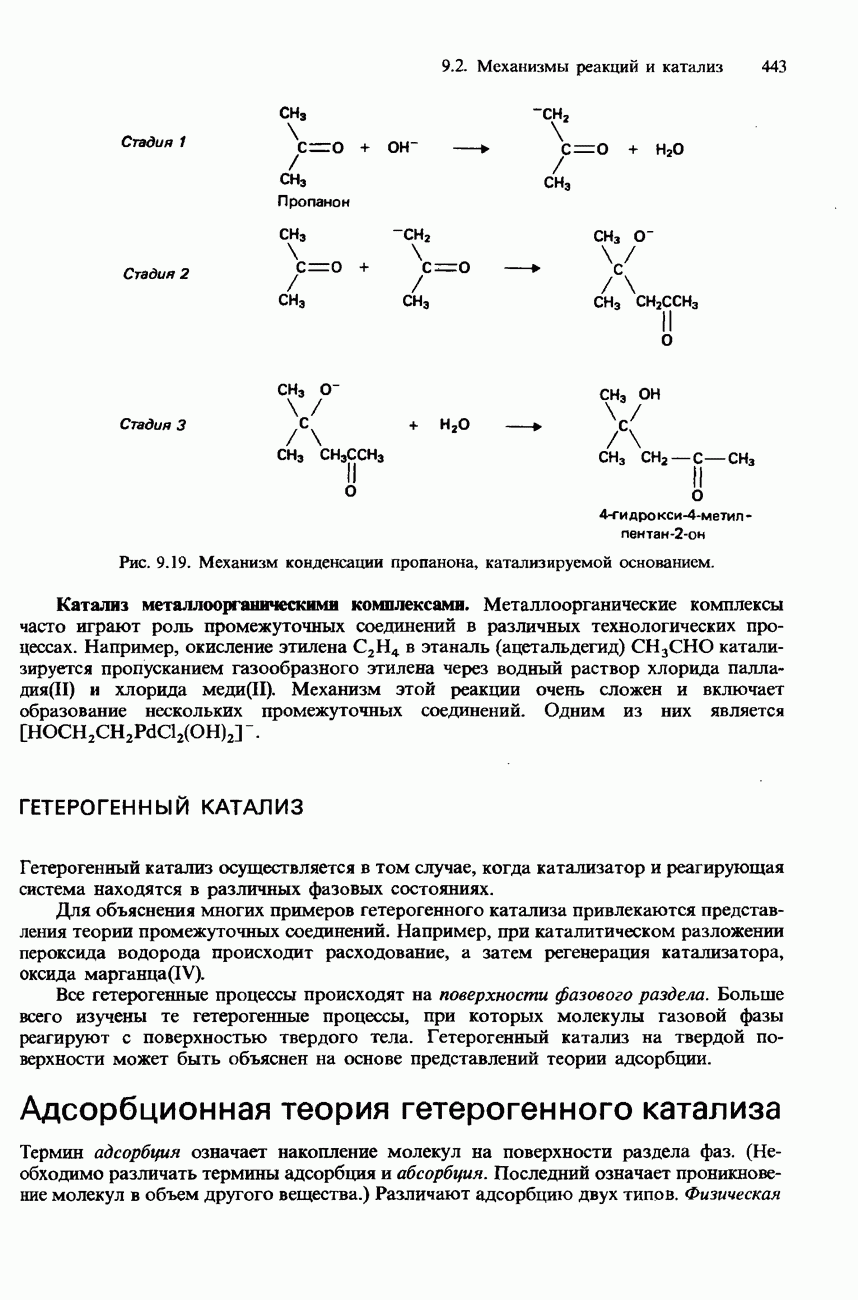
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
- 10.4. Химические источники тока
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
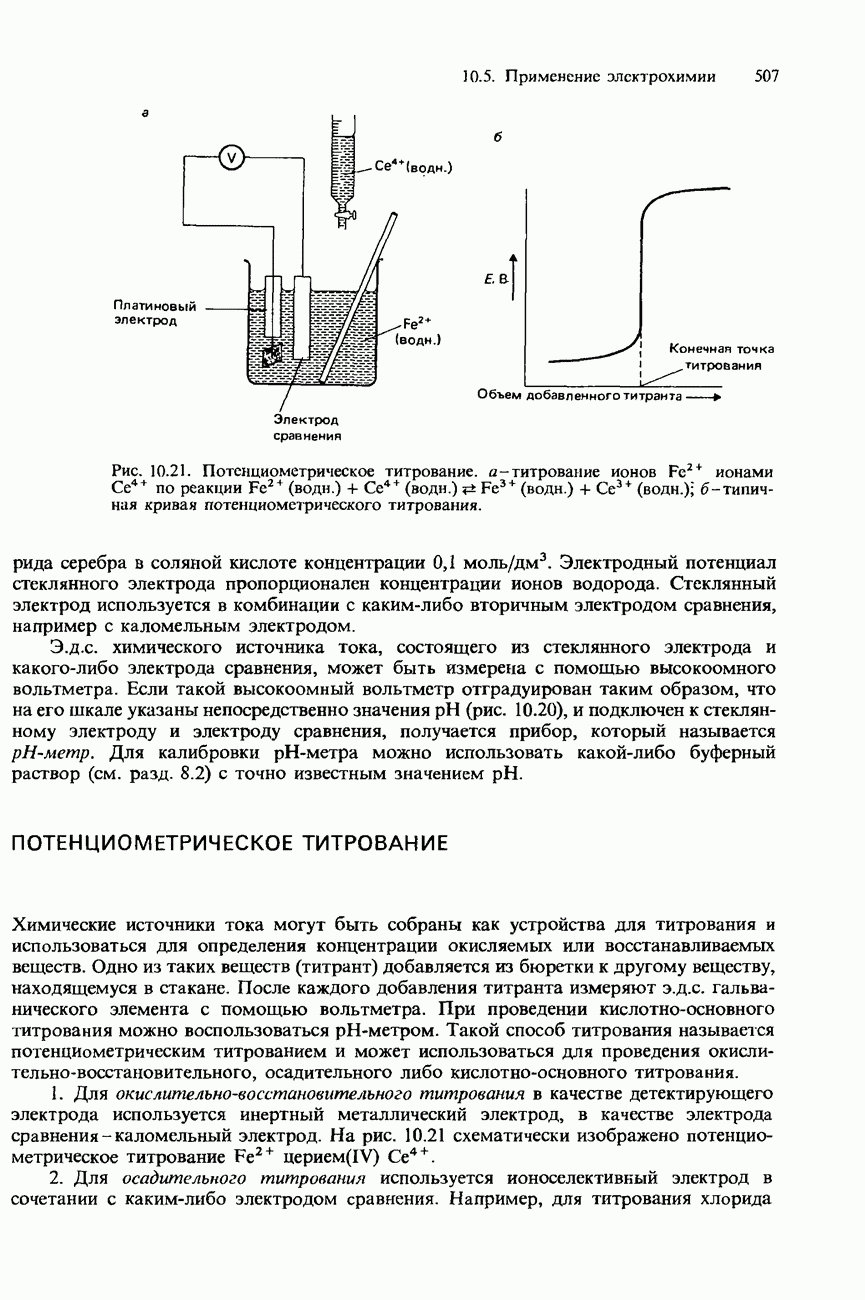
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
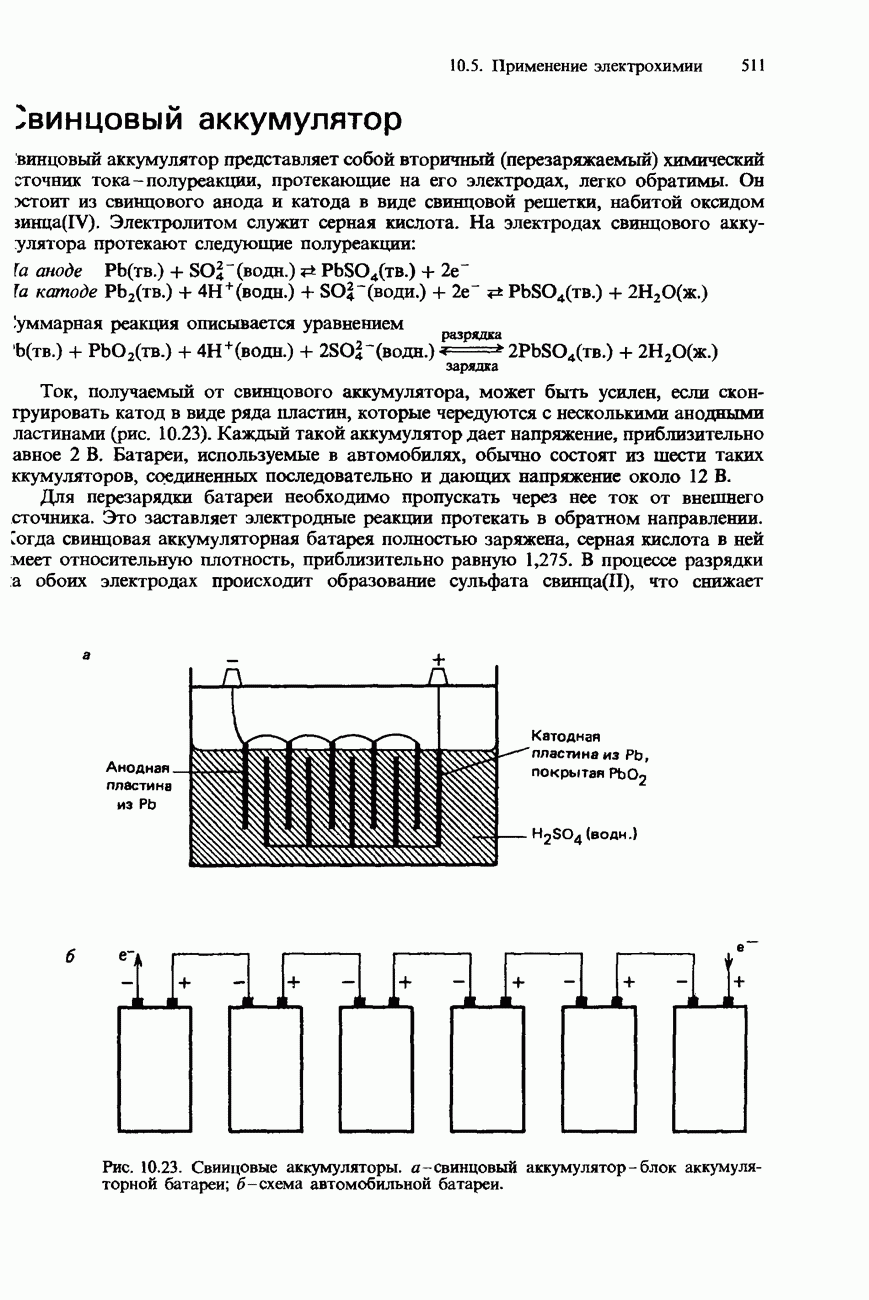
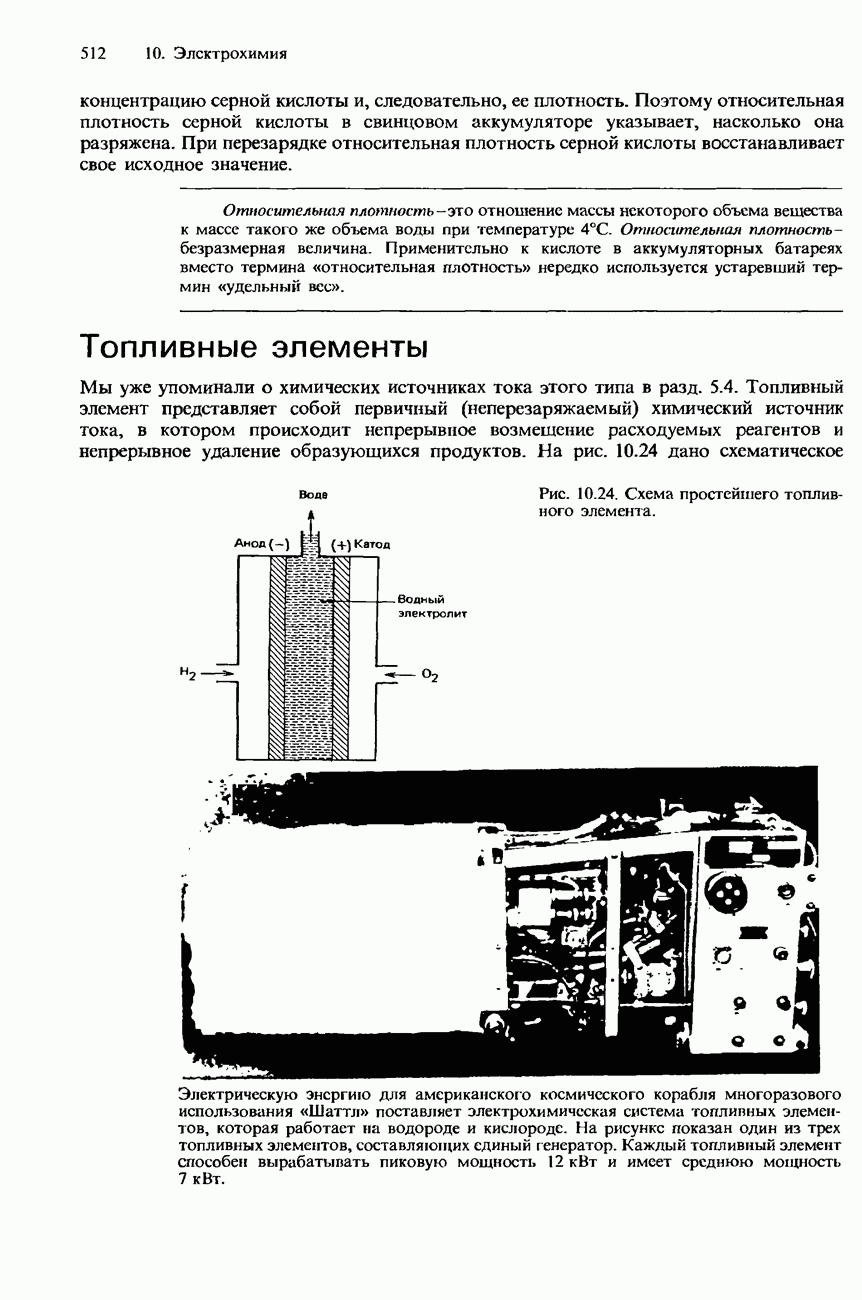
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
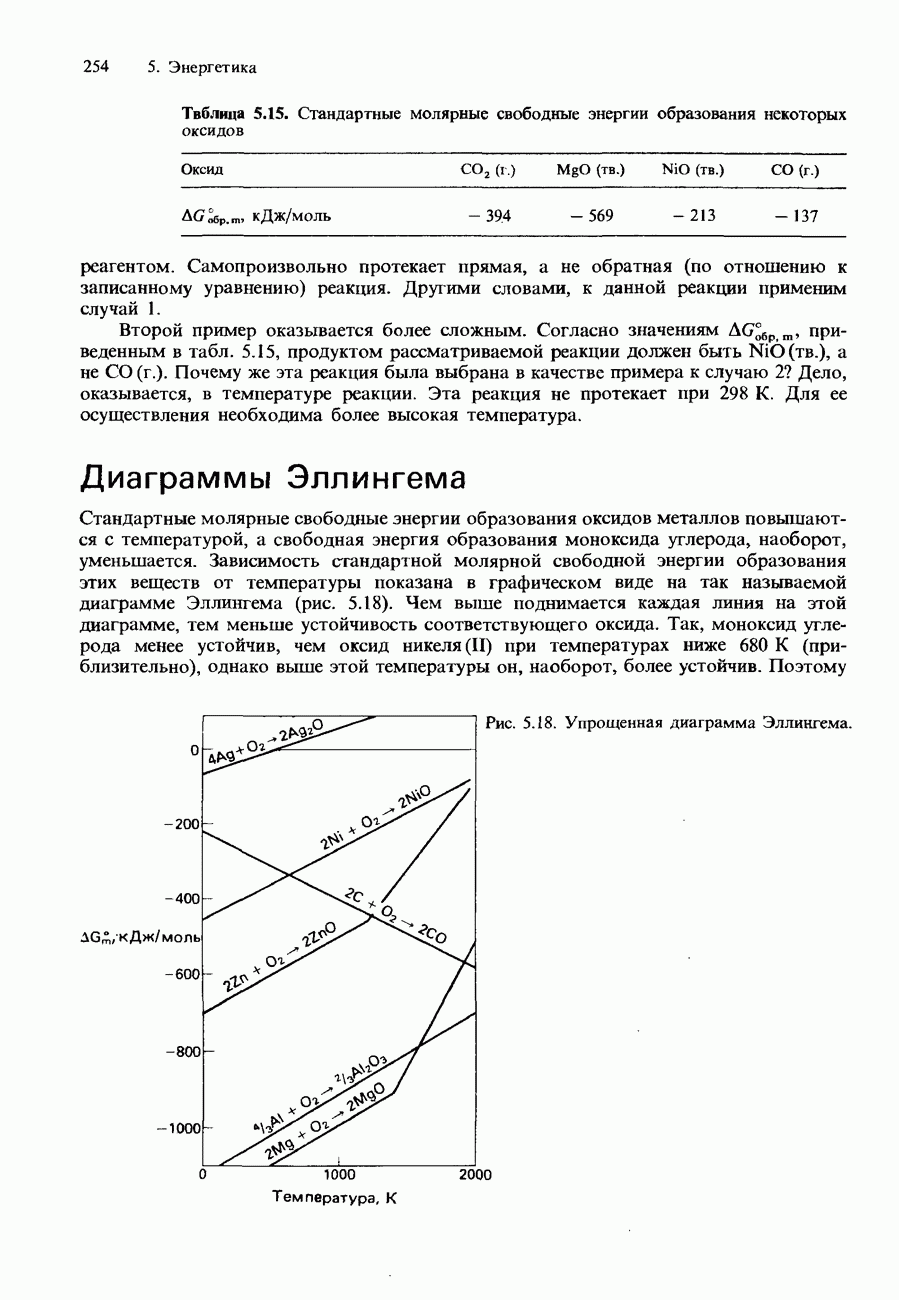
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ