| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
10. ЭЛЕКТРОХИМИЯ
Электрохимия со времен Древней Месопотамии и до наших дней
В 1800 г. Алессандро Вольта, итальянский ученый, создал первый современный химический источник постоянного тока - электричеекую батарею. Спустя несколько месяцев двое англичан, Никольсон и Карлайл, сумели разложить вещество на составные части, пропуская через него электрический ток. В этом эксперименте электрический ток пропускали через воду, которая разлагалась на водород и кислород.
Несколькими годами позже английский ученый Г. Дэви предложил военно-морскому флоту прикреплять небольшой железный лист к медной обшивке деревянных кораблей с целью ее предохранения от коррозии. Этот способ получил название катодной защиты и в настоящее время широко используется во всем мире для защиты от коррозии трубопроводов. Однако проблема коррозии металлов остается по-прежнему актуальной. В 1975 г. коррозия обошлась Соединенным Штатам приблизительно в 75 млрд. долларов, что составило четверть валового национального продукта этой страны за указанный год.
Современные применения электрохимии чрезвычайно разнообразны - от миниатюрных батареек, регулирующих сердцебиение людей, страдающих сердечными заболеваниями, до водородных топливных элементов, обеспечивающих электроэнергией космические корабли; от изготовления микроэлектронных схем с помощью электролитического осаждения и травления до электрохимического фрезерования металлов. Электрохимия может найти применение для получения горючих топливных веществ, например водорода, под действием солнечного света с помощью «фотоэлектрохимической» системы, а также для очистки воды аналогичными методами; для анализа загрязняющих микронримссей, содержащихся в воздухе и воде, и контроля окружающей среды; для регулирования содержания в мозговых тканях веществ, которые ответственны за возникновение таких заболеваний, как, например, болезнь Паркинсона.
Батареи сухих элементов, изобретенные Лекланше, и перезаряжаемые свинцовые аккумуляторы, разработанные Планте, были единственными источниками электрического тока, доступными в первой половине XIX века. Без создания в свое
время таких источников электричества сегодня были бы невозможны портативные радиоприемники, электроавтомобили, электрические шагомеры для страдающих сердечными заболеваниями, электрические фонари, электронные наручные часы и электрические уличные часы, портативные магнитофоны. Даже некоторые виды современного оружия приводятся в действие от сигнала электрических батареек.
Электрохимия позволила также открыть новое важное направление в проведении промышленных процессов. Оно называется «электрофоретическое осаждение» и обеспечивает повышенное качество сцепления красок и пластмассовых покрытий, а также имеет другие технологические преимущества над классическими процессами распыления.
Создание еще одной новой технологии - электрохимической обработки металлов, или электрохимического фрезерования, - сделало возможными операции, которые недостижимы обычными методами механической обработки. Матрица, форму которой должно принять изделие, выполняет при этом роль катода и внедряется в обрабатываемый материал, который играет роль анода. Между катодом и анодом пропускается быстрый поток электролита; при прохождении через него электрического тока происходит обработка материала в результате растворения анода. Электролит служит не только для пропускания тока, но также уносит с собой растворяемые продукты и охлаждает систему, отводя тепло.
Электрохимические процессы особенно удобны для количественного анализа химических веществ, поскольку получаемые при этом сигналы легко вводятся в электронные приборы и поддаются обработке с помощью ЭВМ. За разработку такого метода чехословацкий ученый Я. Гейровски в 1959 г. получил Нобелевскую премию. Усовершенствование этого «метода полярографии» позволяет обнаруживать даже сотую часть одного слоя атомов какого-либо металла на поверхности другого металла и, кроме того, прослеживать механизм реакции этих металлов между собой.
Такая чувствительность не была достижима ни одним из известных до сих пор методов аналитической химии. Легкость автоматизации, избирательность и чувствительность электрохимических систем привели к широкому использованию электрохимических датчиков для обнаружения большинства загрязняющих примесей в воздухе и в природных водах, а также в других средах, оказывающих влияние на жизиь человека и его окружение.
При раскопках парфянского поселения, существовавшего в Месопотамии 2200 лет назад, была обнаружена древняя «батарея». С технической точки зрения она представляет собой электрохимический источник тока типа гальванического элемента одноразового действия и состоит из железного стержня и медного листа, свернутого в цилиндр вокруг этого стержня; оба они помещены в керамический горшок из-под виноградного сока. По-видимому, это устройство выполняло роль таинственного источника энергии в процессе нанесения гальванических покрытий из золота или серебра на поверхность металлических предметов.
Д-р Р. М. Уайтмен с химического факультета Университета штата Индиана в США использовал электрохимические электроды для измерения содержания различных химических веществ в мозге крыс. На основании данных, полученных в этих экспериментах, электрофизиологи изучают, каким образом химические вещества, содержащиеся в мозге, осуществляют свое действие. Эти сведения могут в конце концов привести к новым методам контроля или предотвращения некоторых заболеваний, связанных с деятельностью мозга.
Например, болезнь Паркинсона, проявляющаяся в заметном непроизвольном дрожании конечностей и головы, обусловлена недостаточным содержанием до-памина в мозге больных. Допамин относится к числу так называемых нейротрансмиттеров химических веществ, выделяемых нервными клетками мозга; с помощью этих веществ осуществляется передача сигналов мозга. Д-р Уайтмен в ходе многолетних экспериментов обнаружил, что содержание нейротрансмиттеров поддается прямым измерениям с помощью электрохимических методов. Это может привести к успешному лечению болезни Паркинсона путем возмещения недостаточного содержания допамина.
Дэвид Спурджеон
После изучения главы 10 вы сможете:
1) описать, как измеряется электролитическая проводимость раствора;
2) указать характер зависимости молярной проводимости от концентрации раствора;
3) вычислить ионную подвижность электролита, используя закон Кольрауша об аддитивности ионных подвижностей
4) провести сопоставление кондуктометрического титрования сильной кислоты и сильного, основания с аналогичным процессом для слабой кислоты и сильного основания;
5) определить стехиометрические коэффициенты в уравнениях окислительно-восстановительных реакций;
6) объяснить смысл терминов а) степень (состояние) окисления, б) диспропорционирование
7) привести примеры окислителей и восстановителей;
8) изложить важнейшие положения ионной теории электролиза;
9) сформулировать и применять законы электролиза Фарадея;
10) привести примеры технических и других применений электролиза;
11) дать определения терминам окисление и восстановление и привести примеры реакций каждого из этих типов;
12) выполнить схематические изображения простейших электрохимических источников тока (гальванических элементов);
13) объяснить и интерпретировать стандартные окислительно-восстановительные потенциалы,
14) вычислить электродвижущую силу (э.д.с.) гальванического элемента;
15) описать, как осуществляется измерение э.д.с. гальванического элемента и электродных потенциалов;
16) описать важнейшие особенности электрохимического ряда (ряда напряжений) и объяснить, для чего он используется;
17) вычислить константы равновесий с помощью уравнения Иернста;
18) объяснить, как осуществляется измерение pH с помощью стеклянного электрода;
19) описать характерные черты потенциометрического титрования;
20) определить осуществимость окислительно-восстановительной реакции на основании рассмотрения электродных потенциалов полуреакций;
21) объяснить принцип действия типичных электрохимических батарей и промышленных электролизеров;
22) кратко описать применение электрохимии в металлургии;
23) изложить основные положения электрохимической теории коррозии и описать способы защиты от коррозии.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
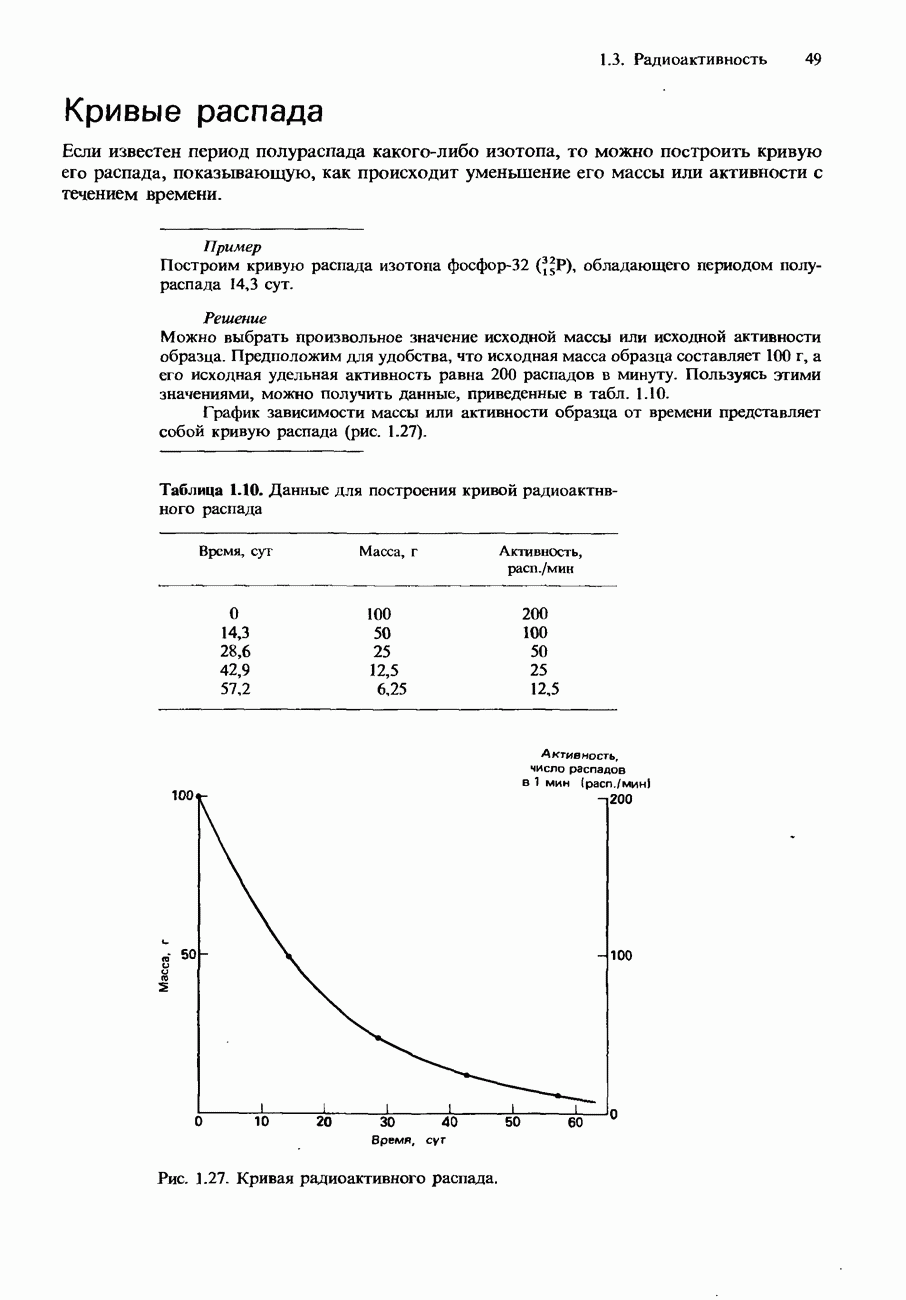
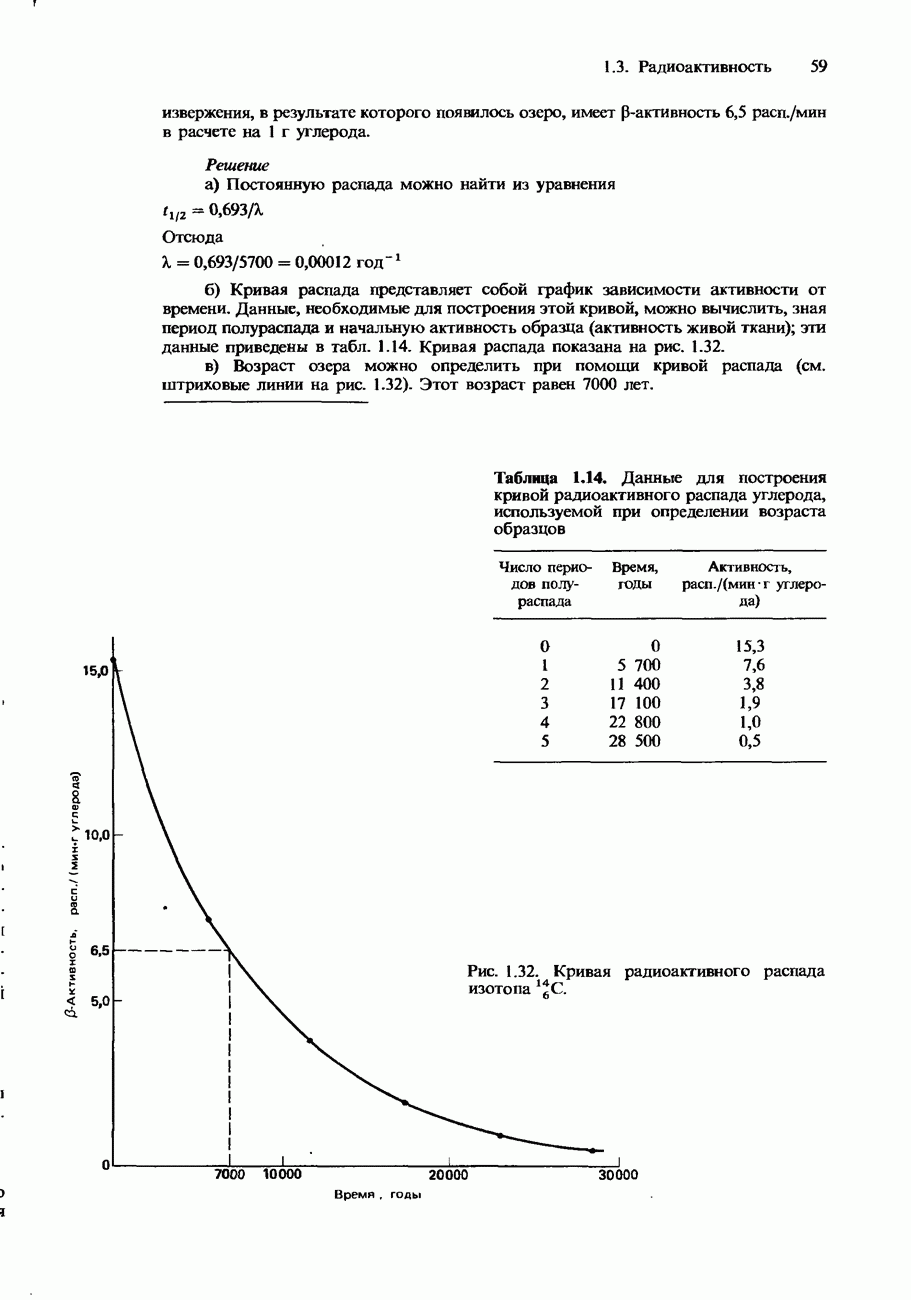
- Кривые распада
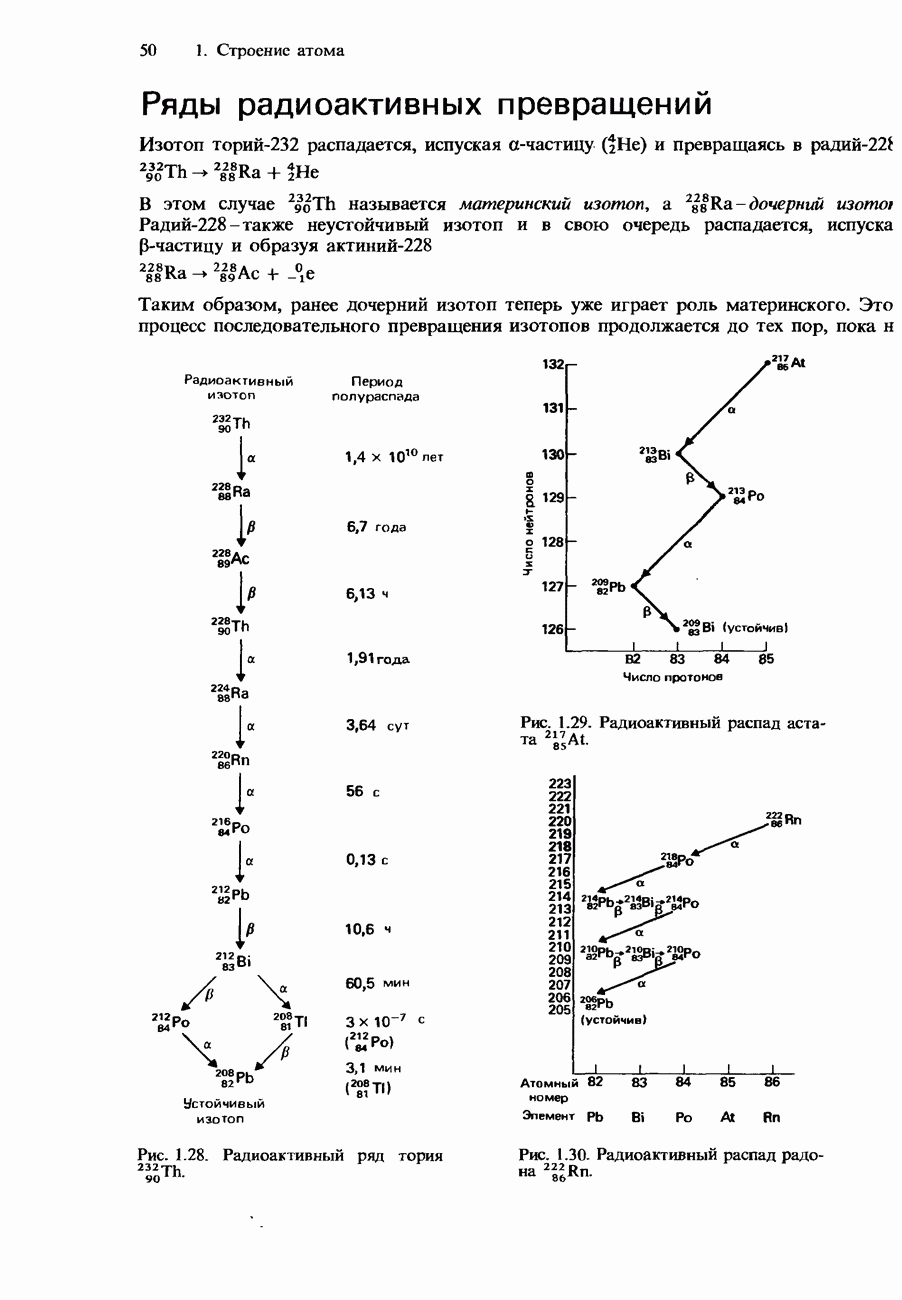
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
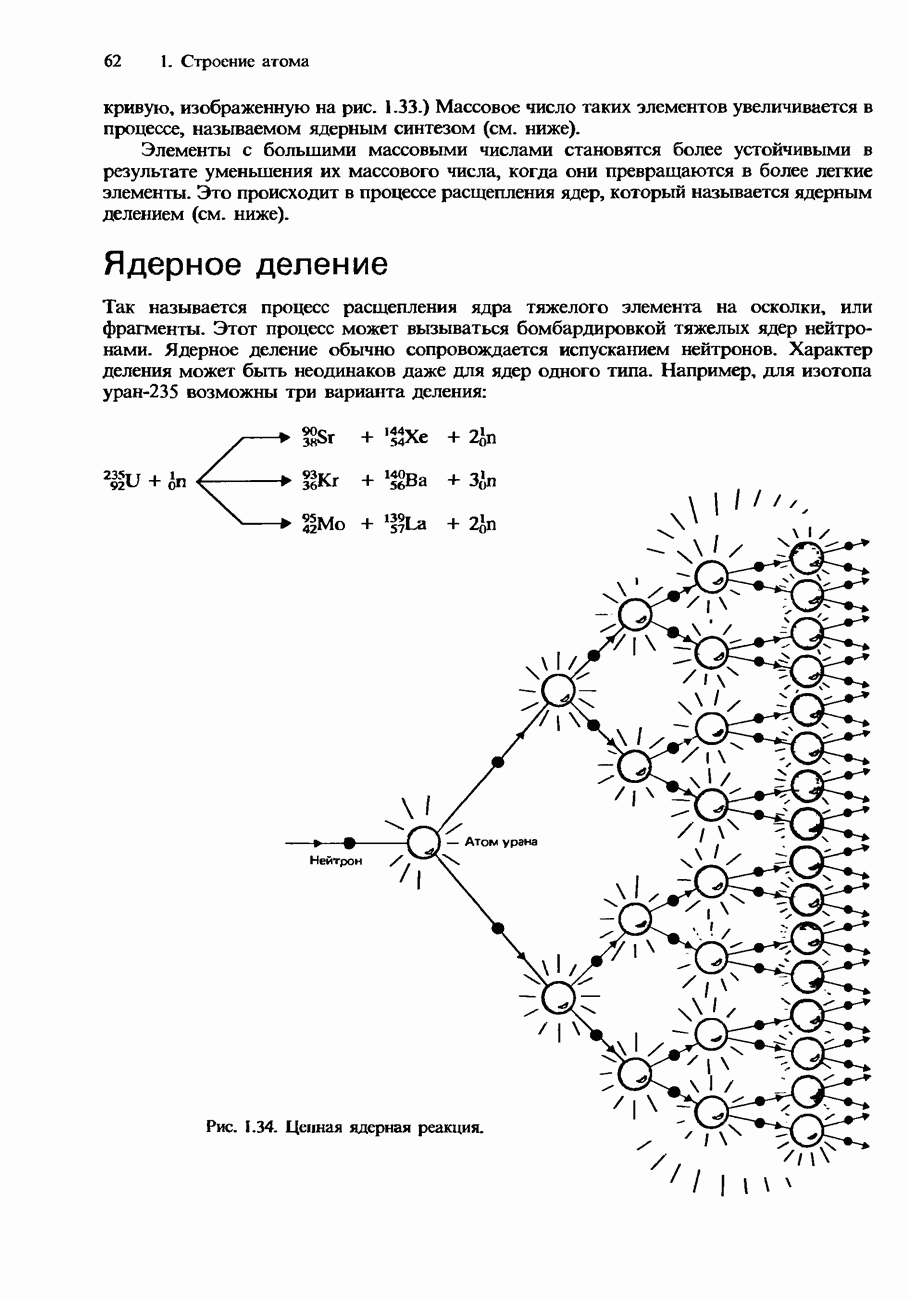
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
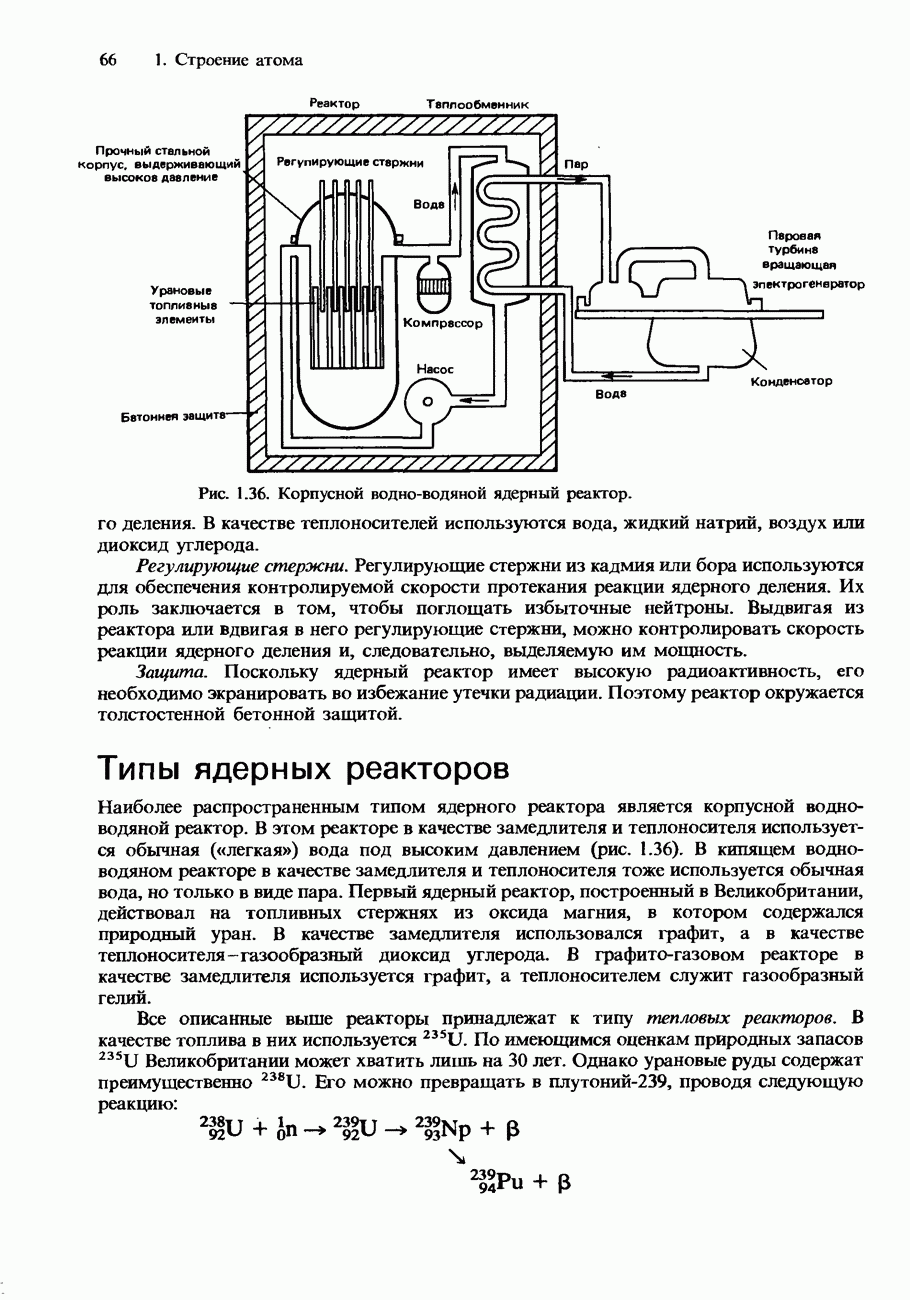
- Типы ядерных реакторов
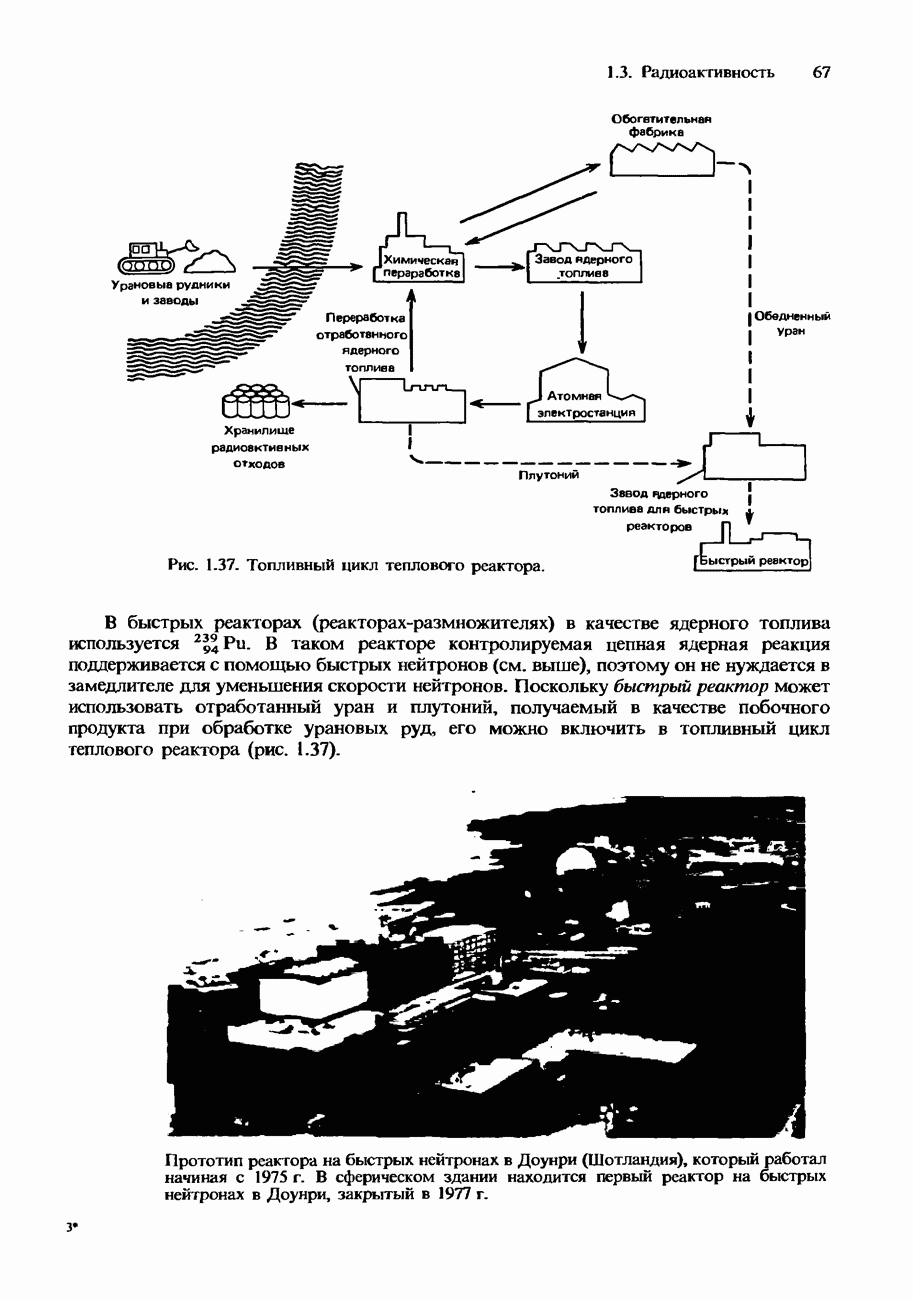
- Радиоактивные ядерные отходы и их переработка
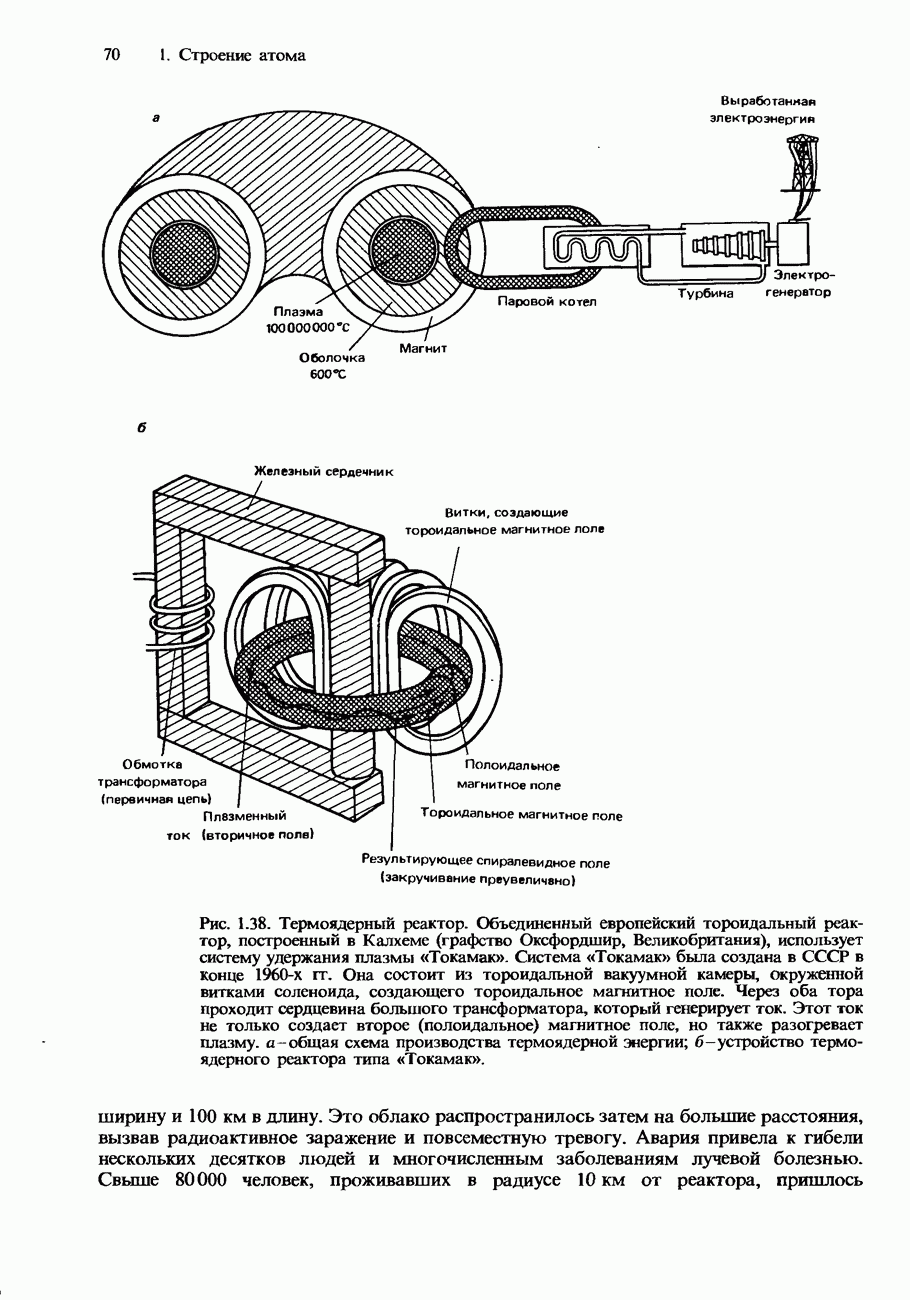
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
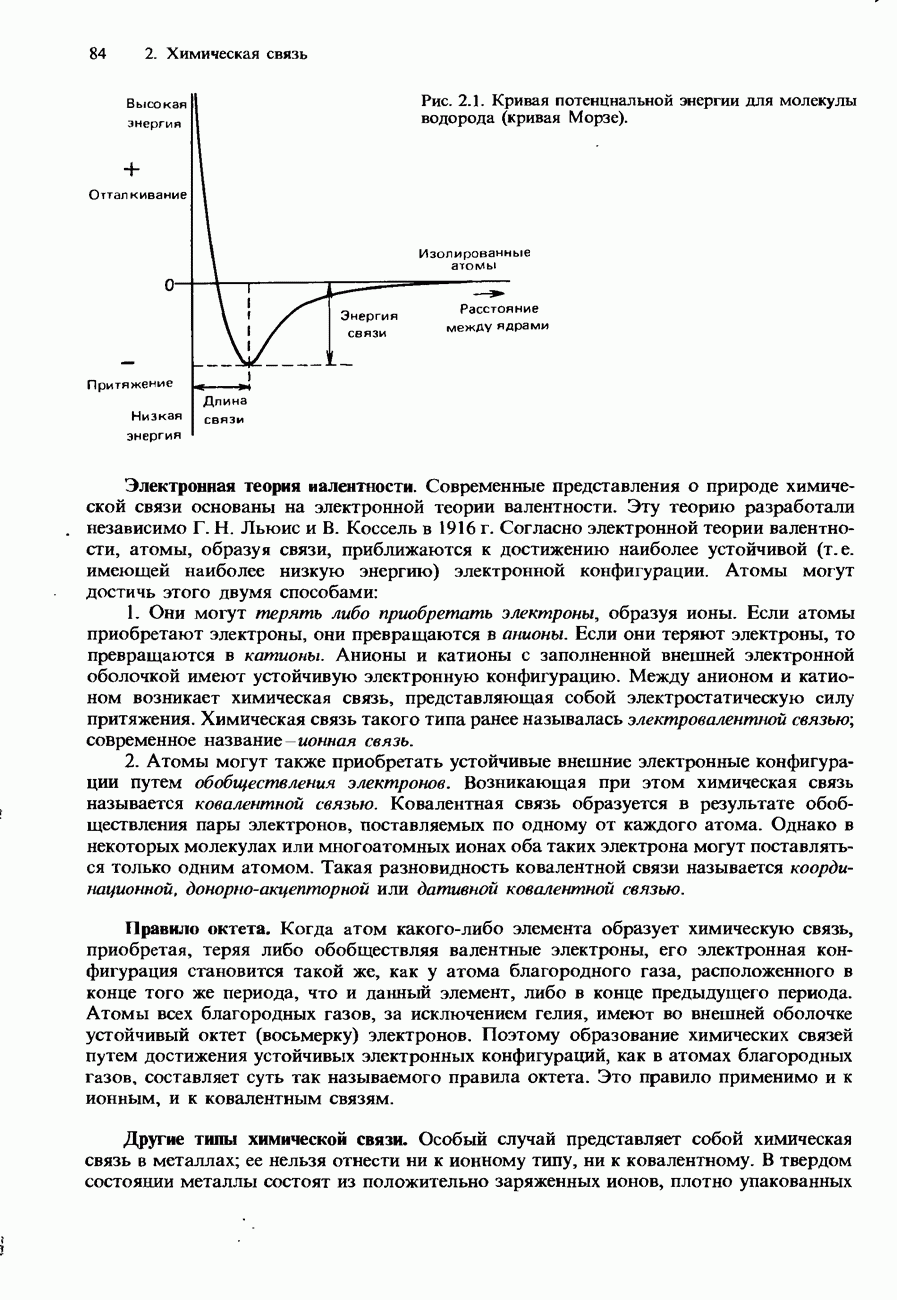
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
- Молекулярные орбитали
- Гибридные атомные орбитали
- Делокализованные орбитали
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
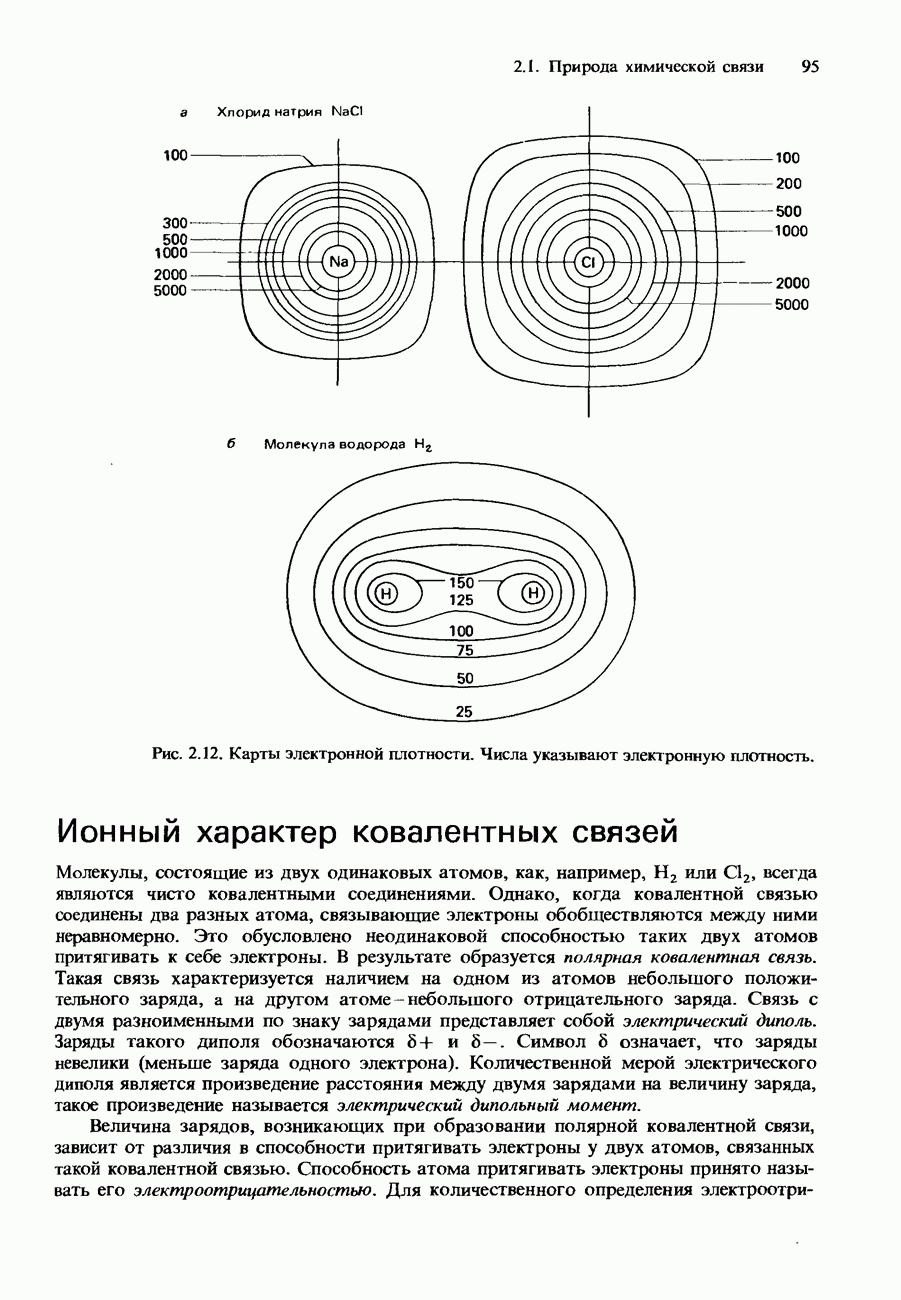
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
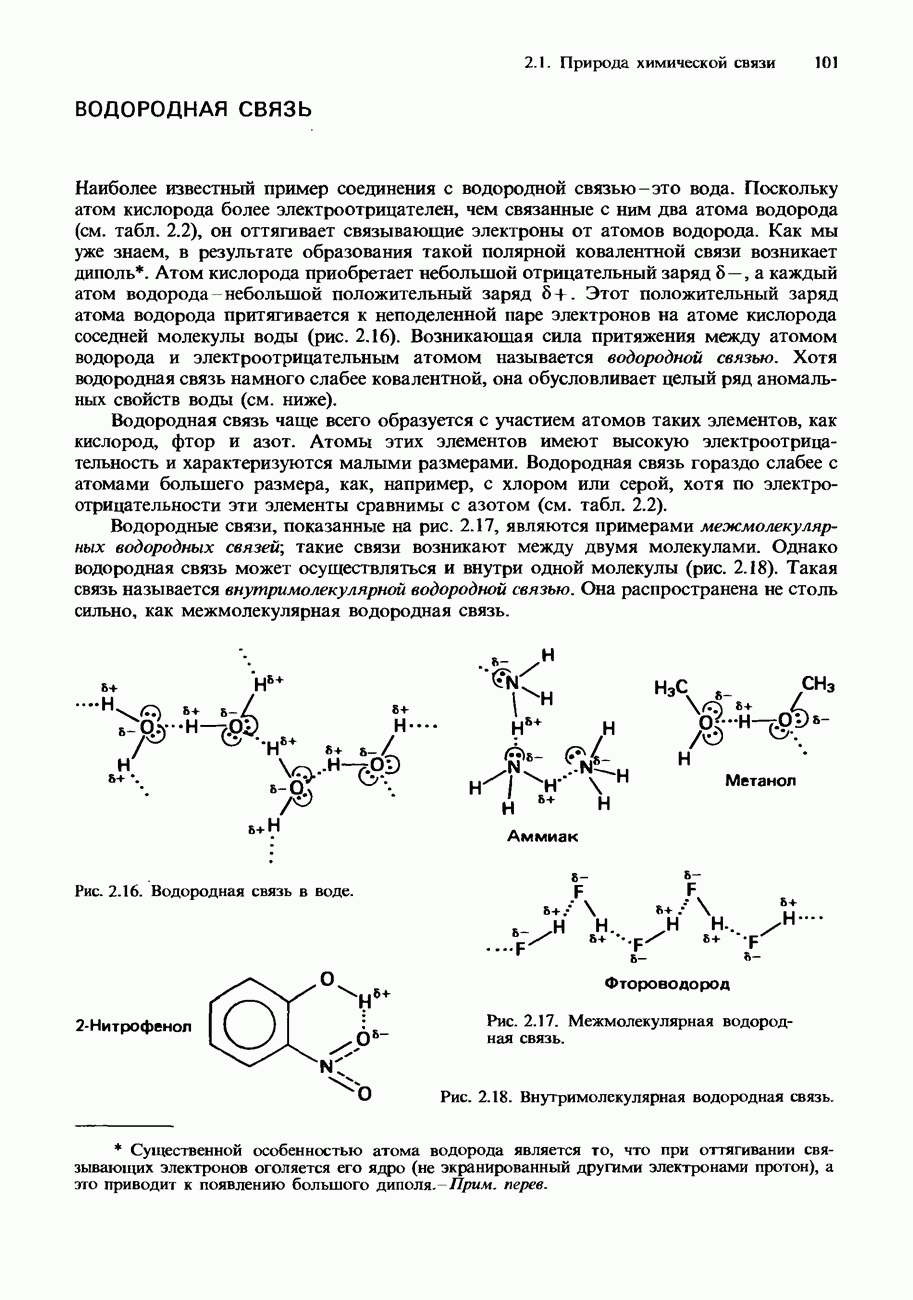
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
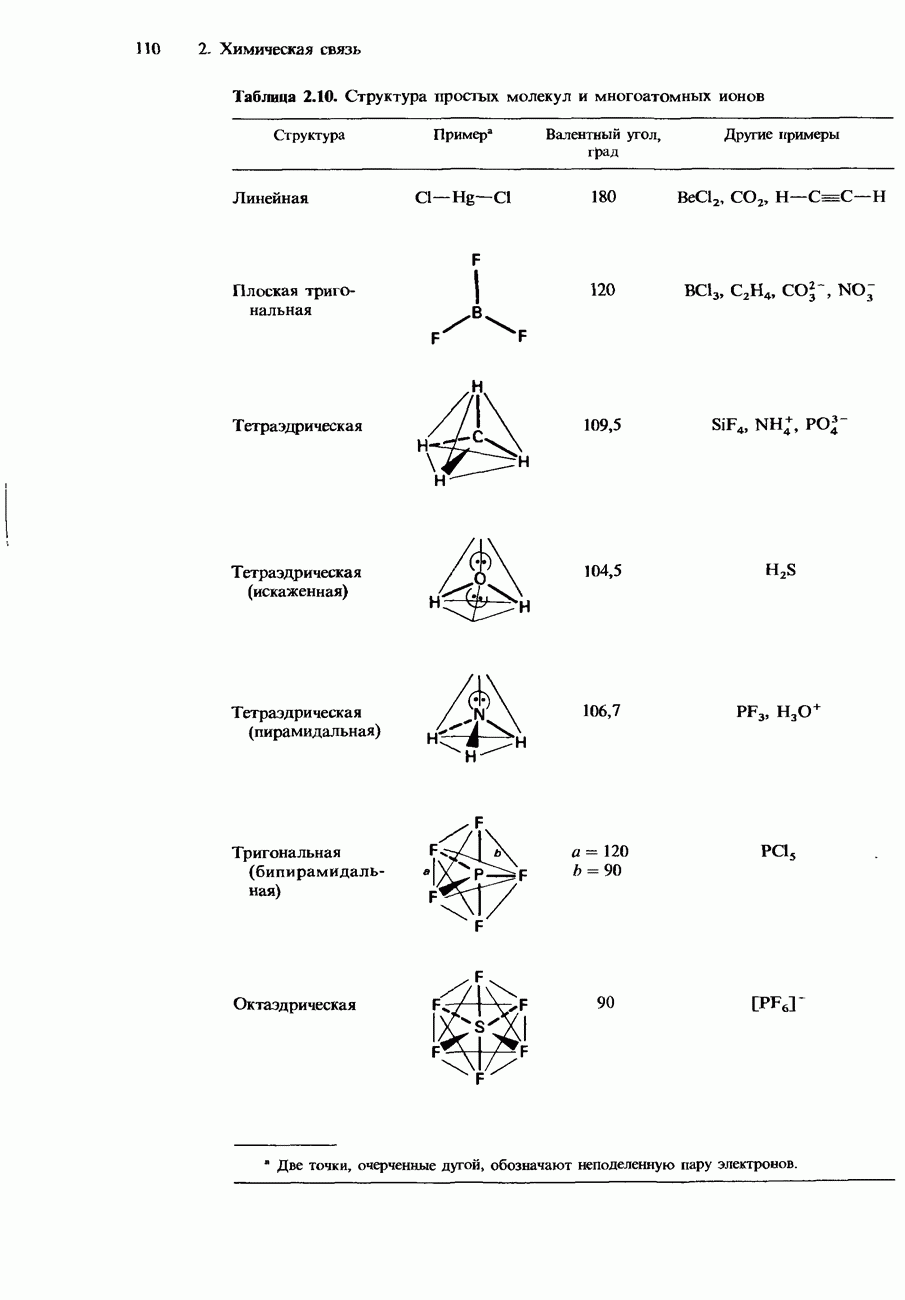
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
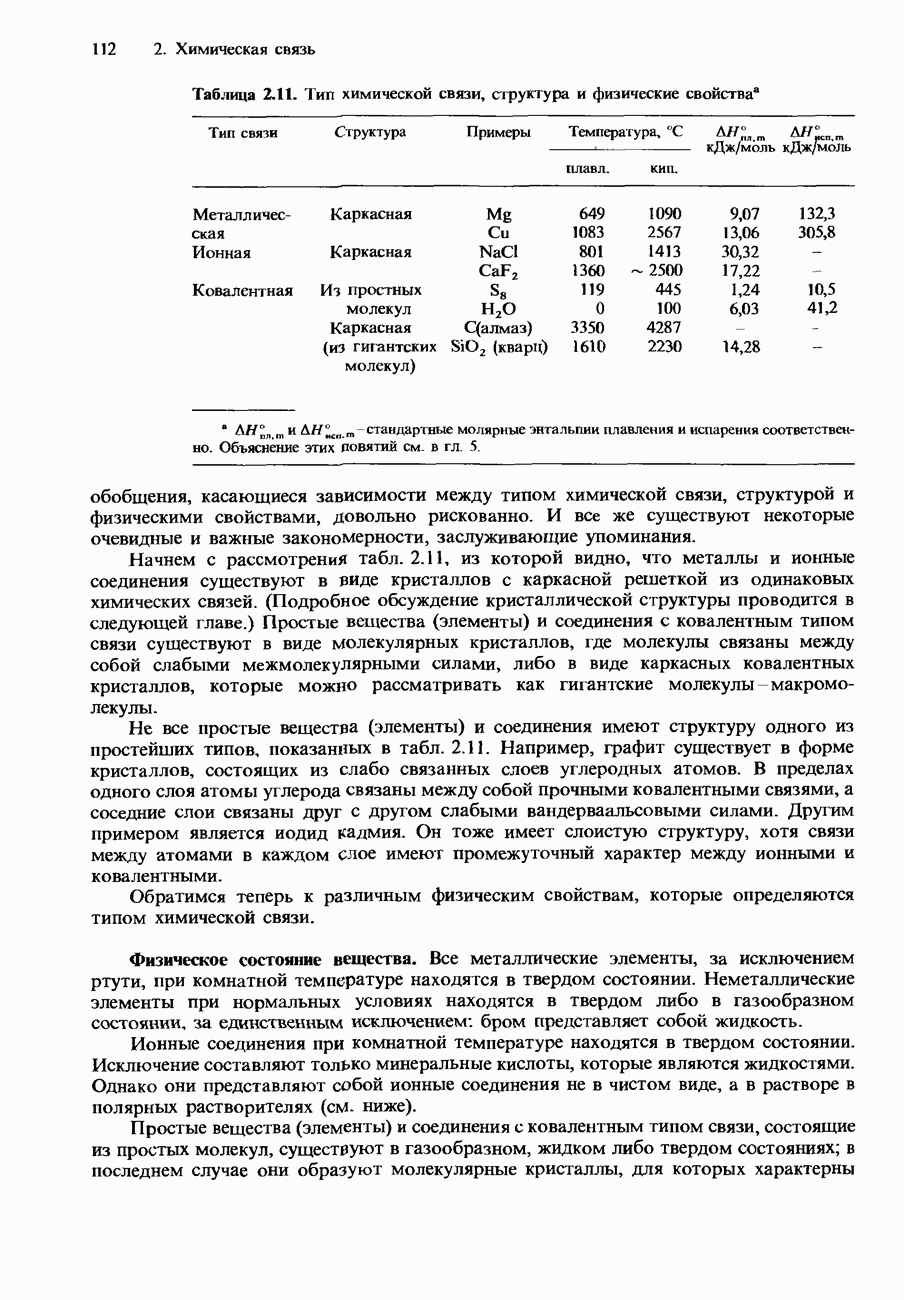
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
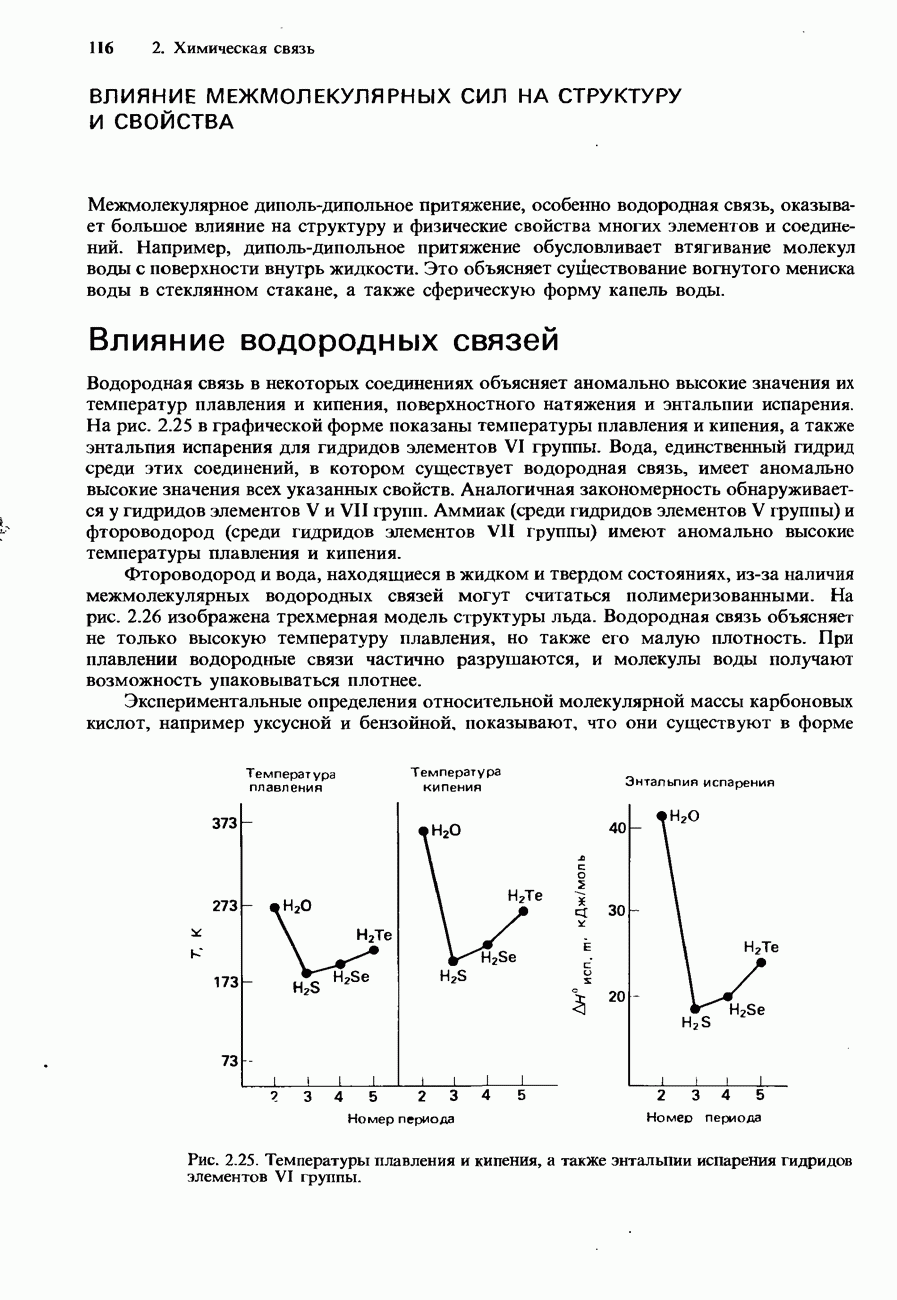
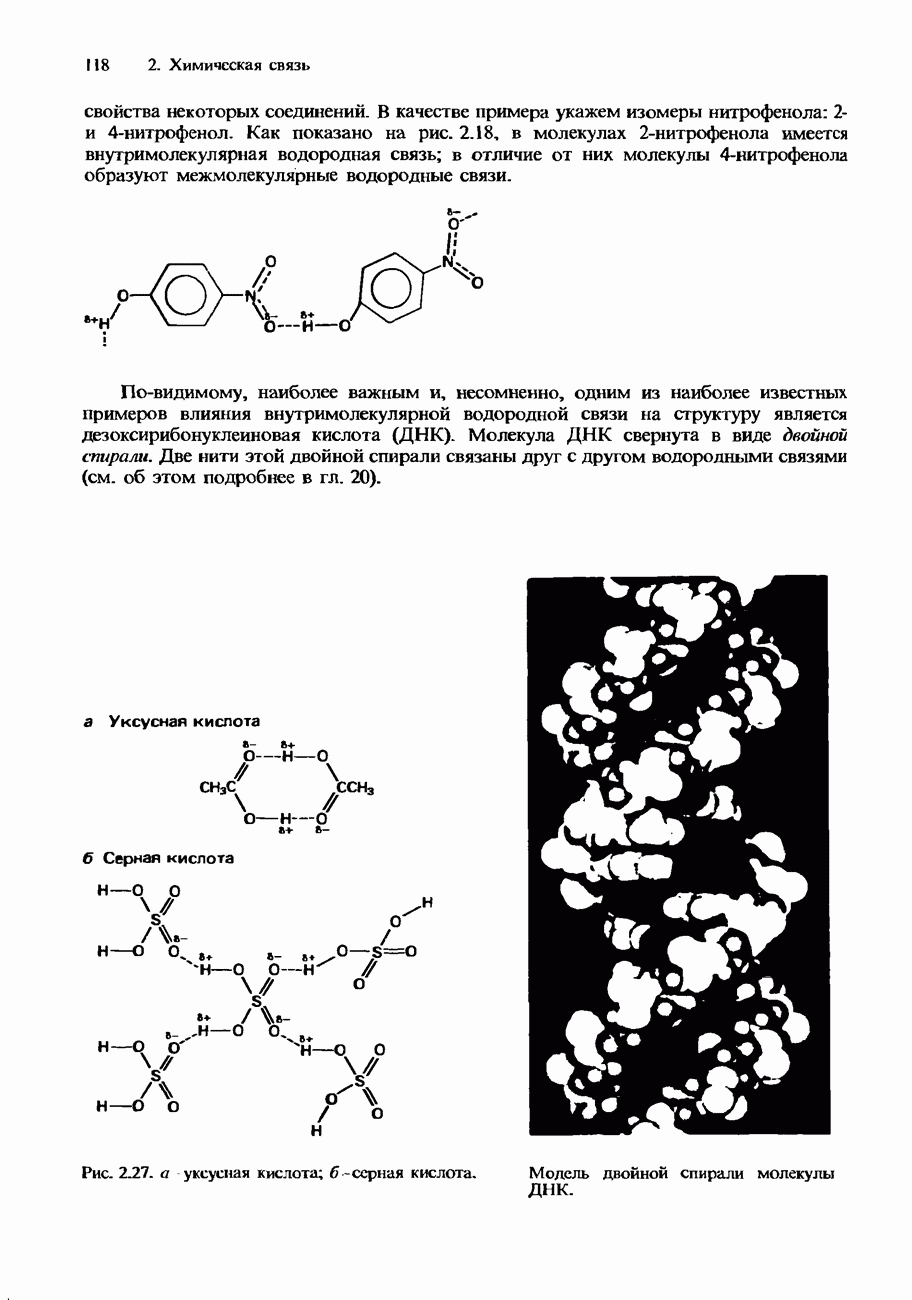
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
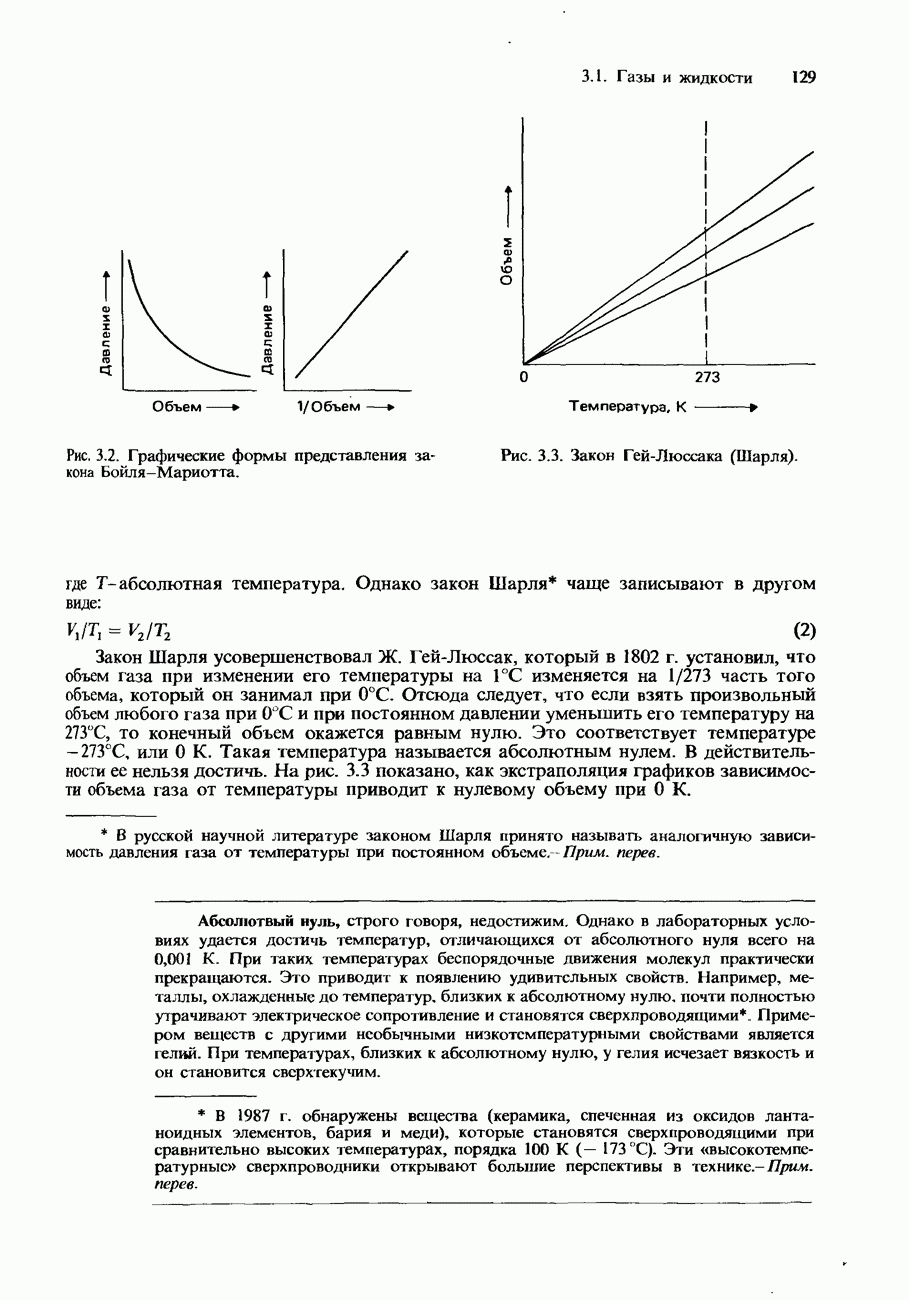
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
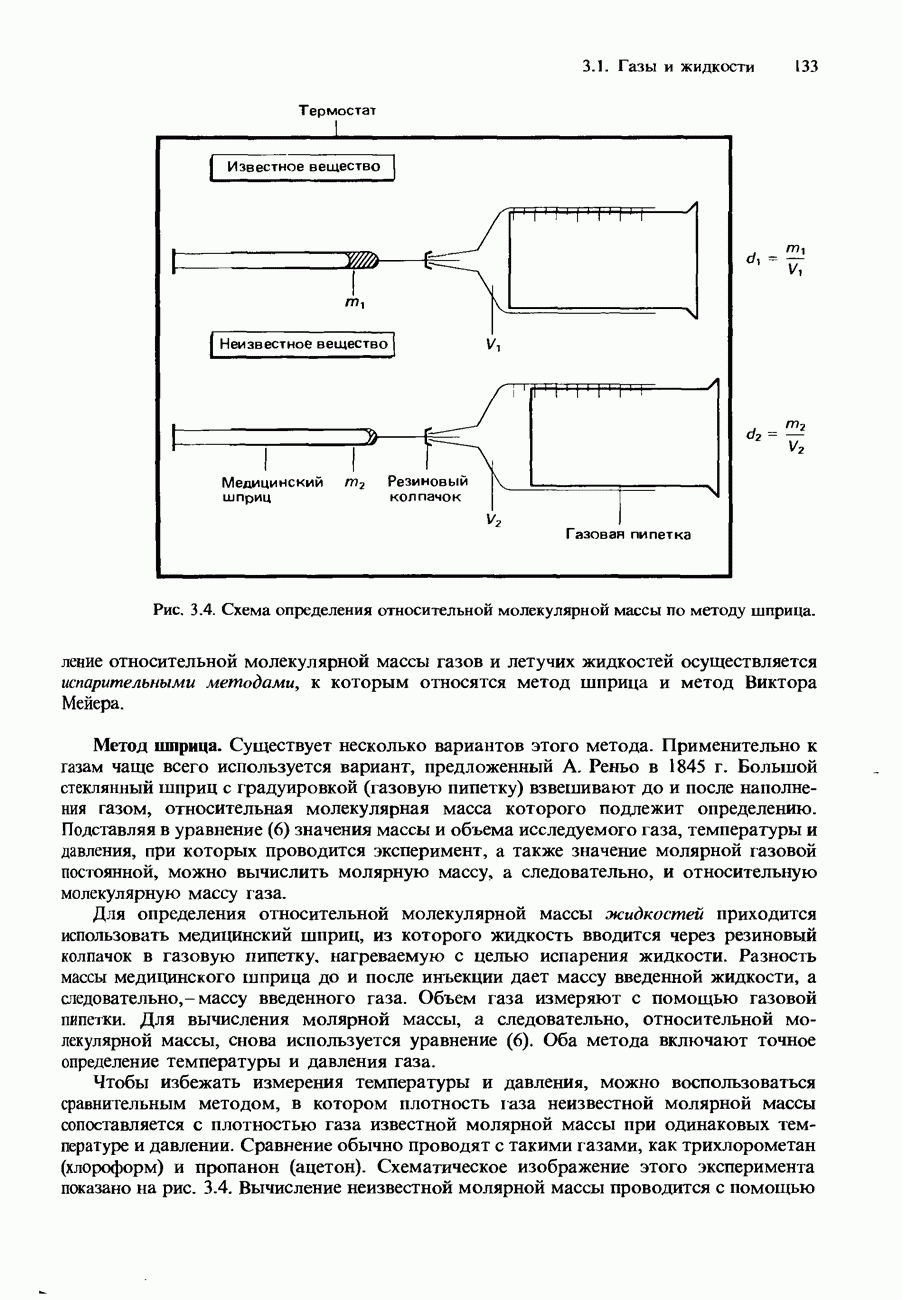
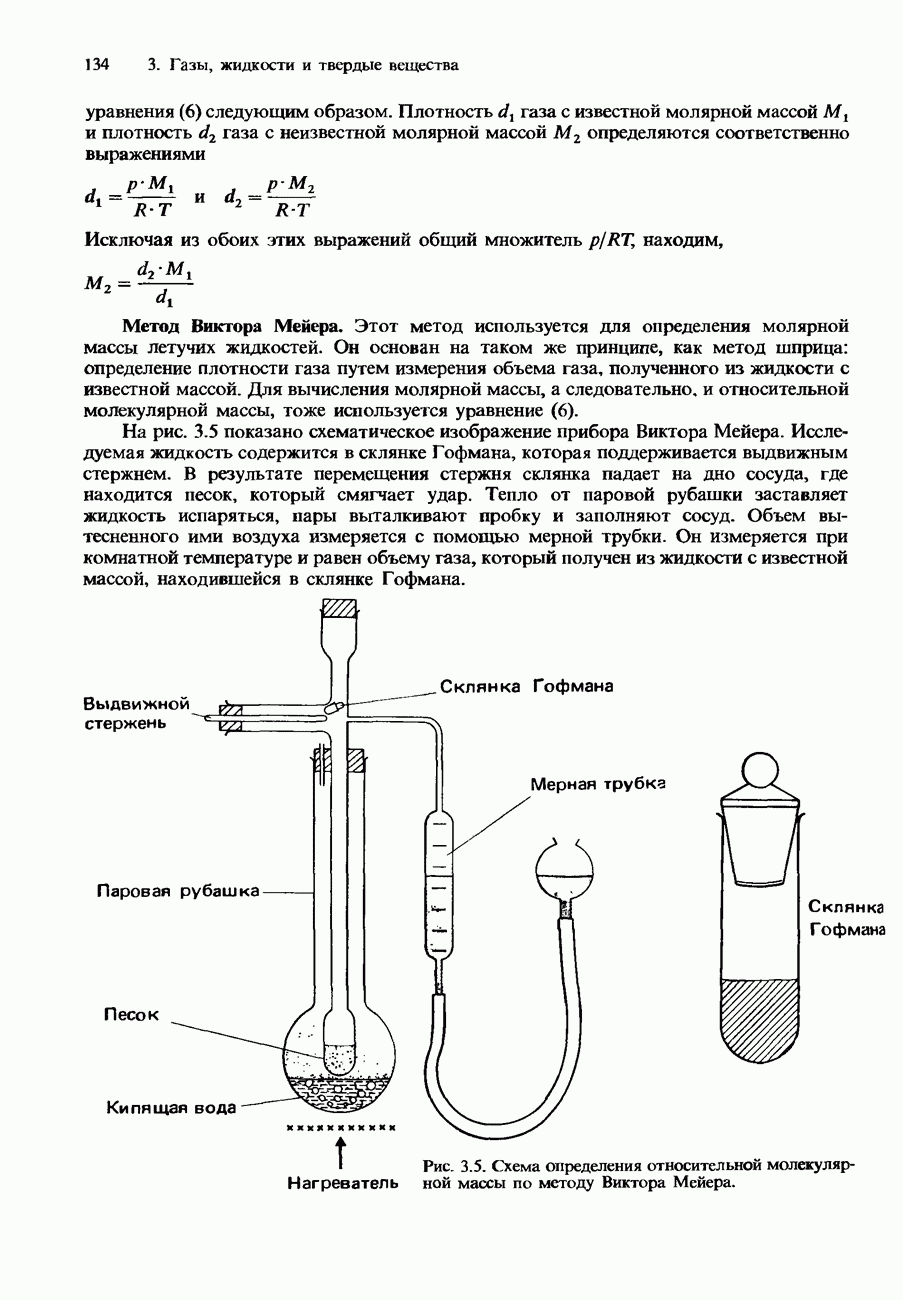
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- Скорости молекул
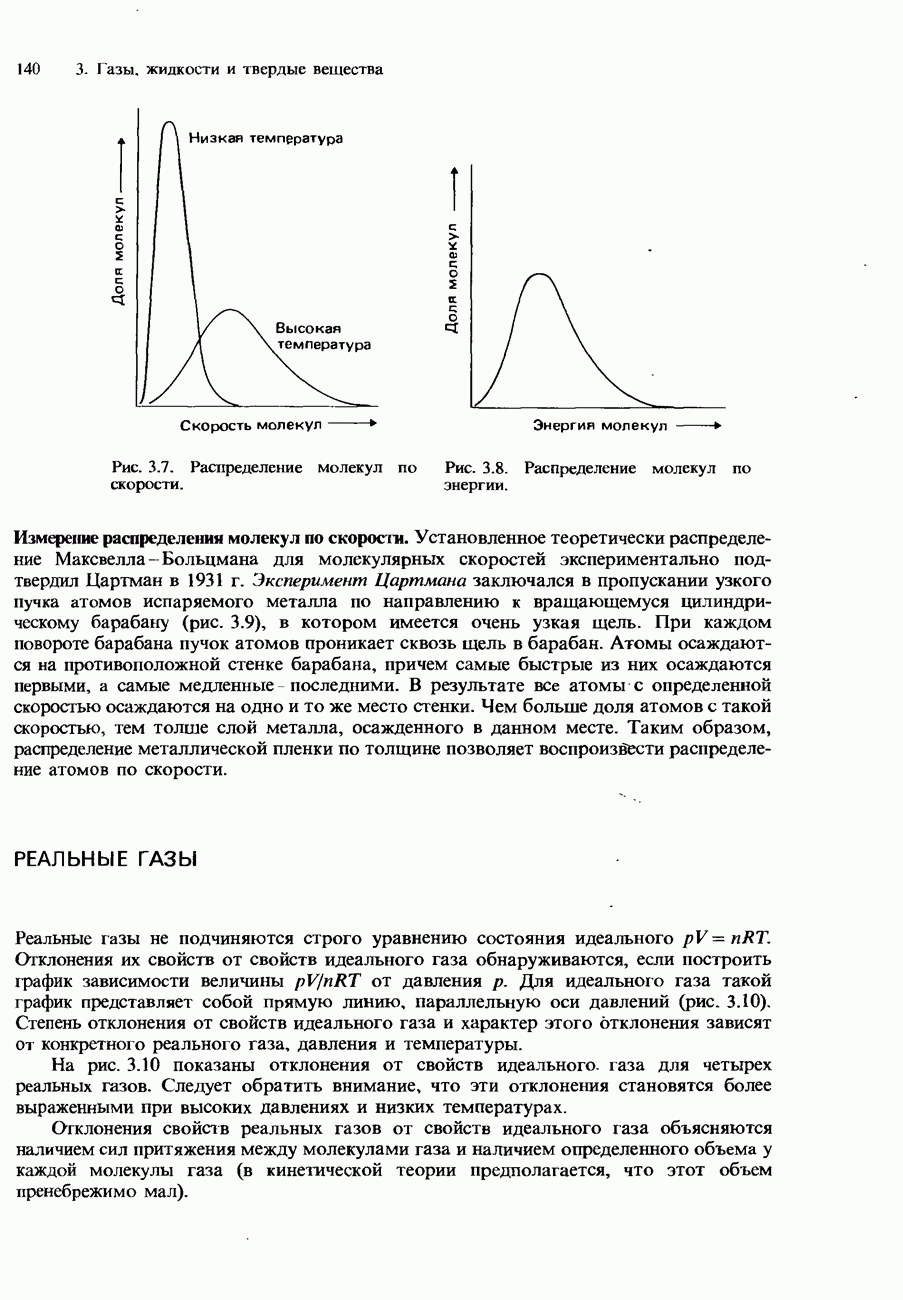
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
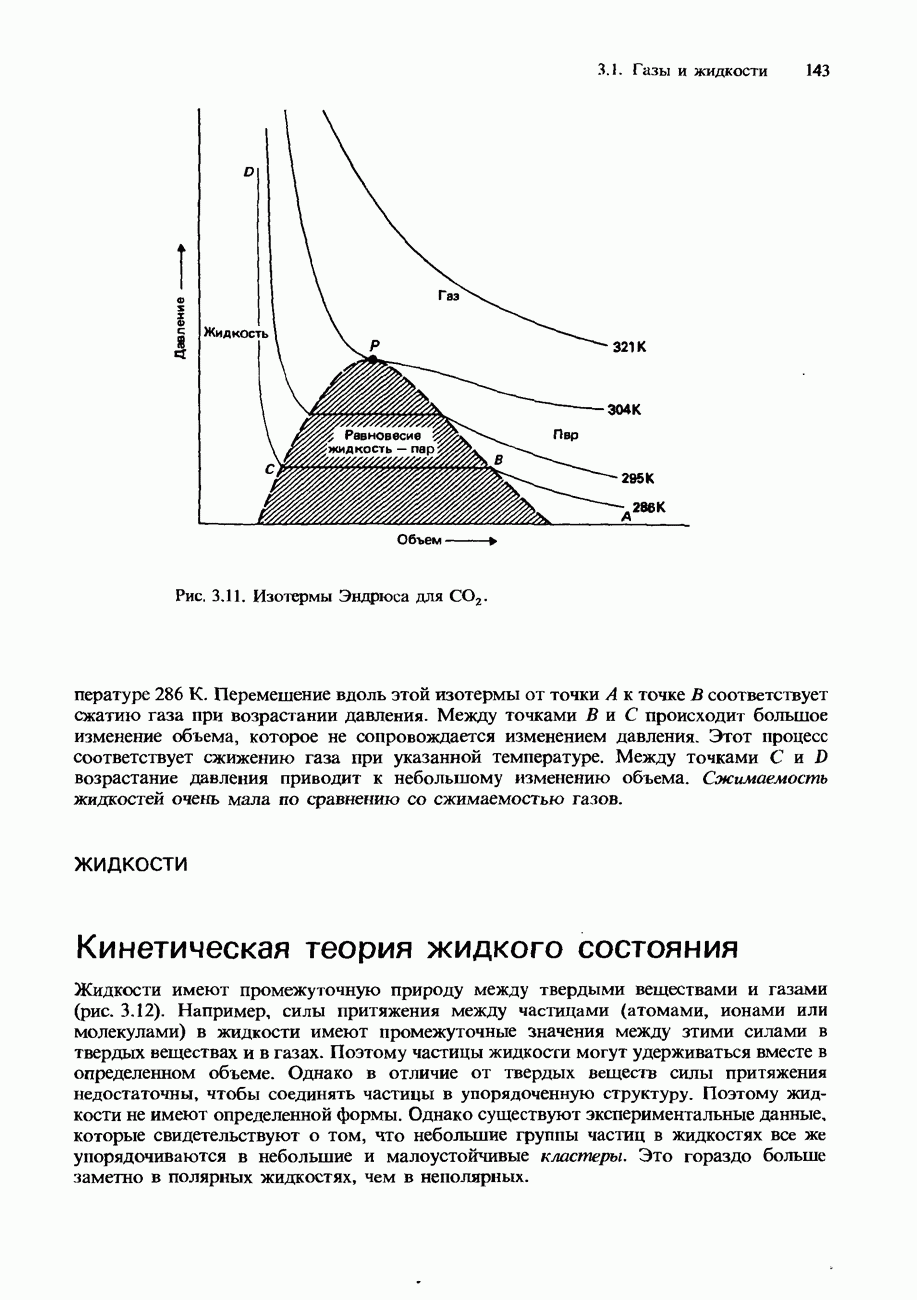
- Сжижение газов
- ЖИДКОСТИ
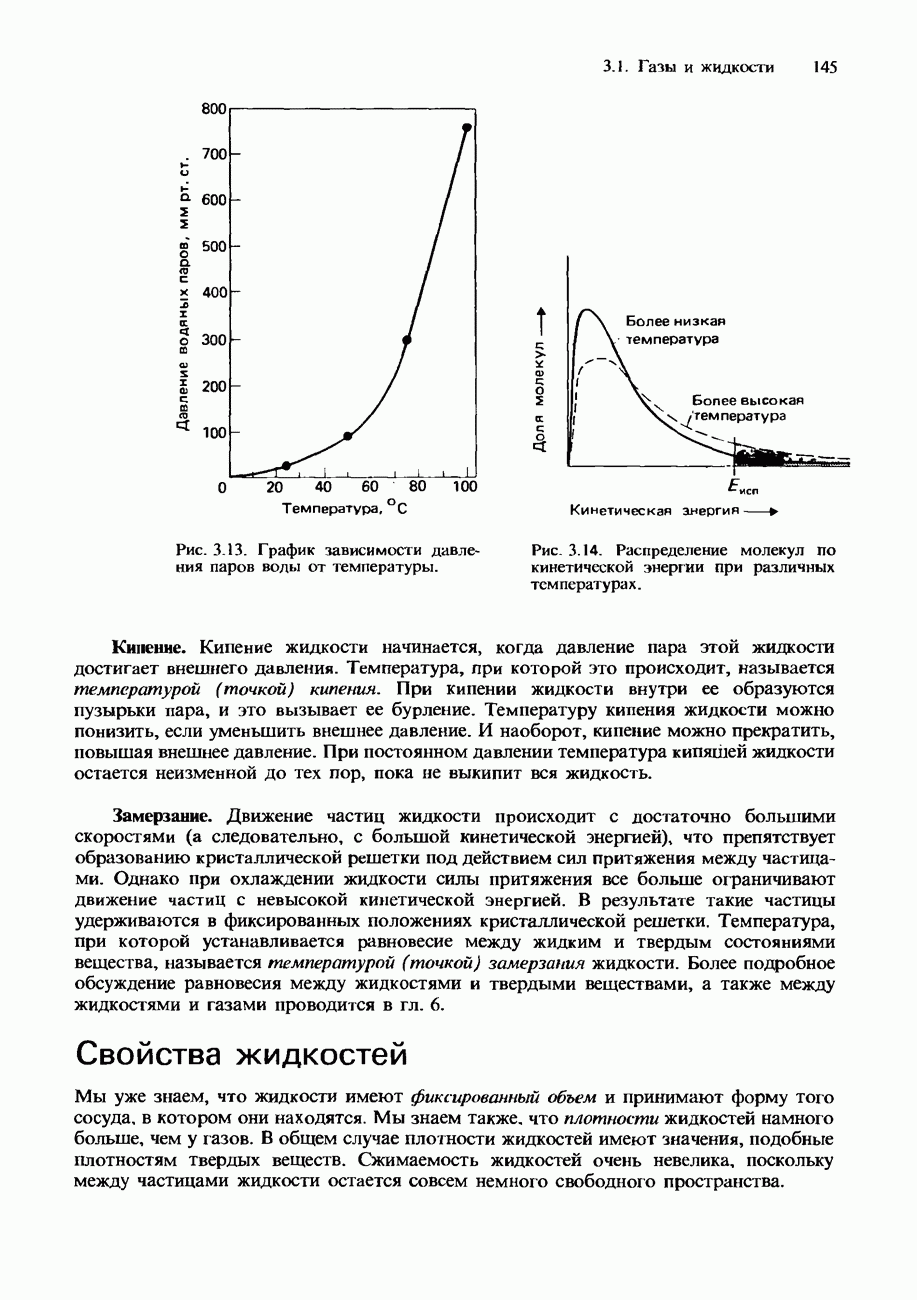
- Свойства жидкостей
- 3.2. Твердые вещества
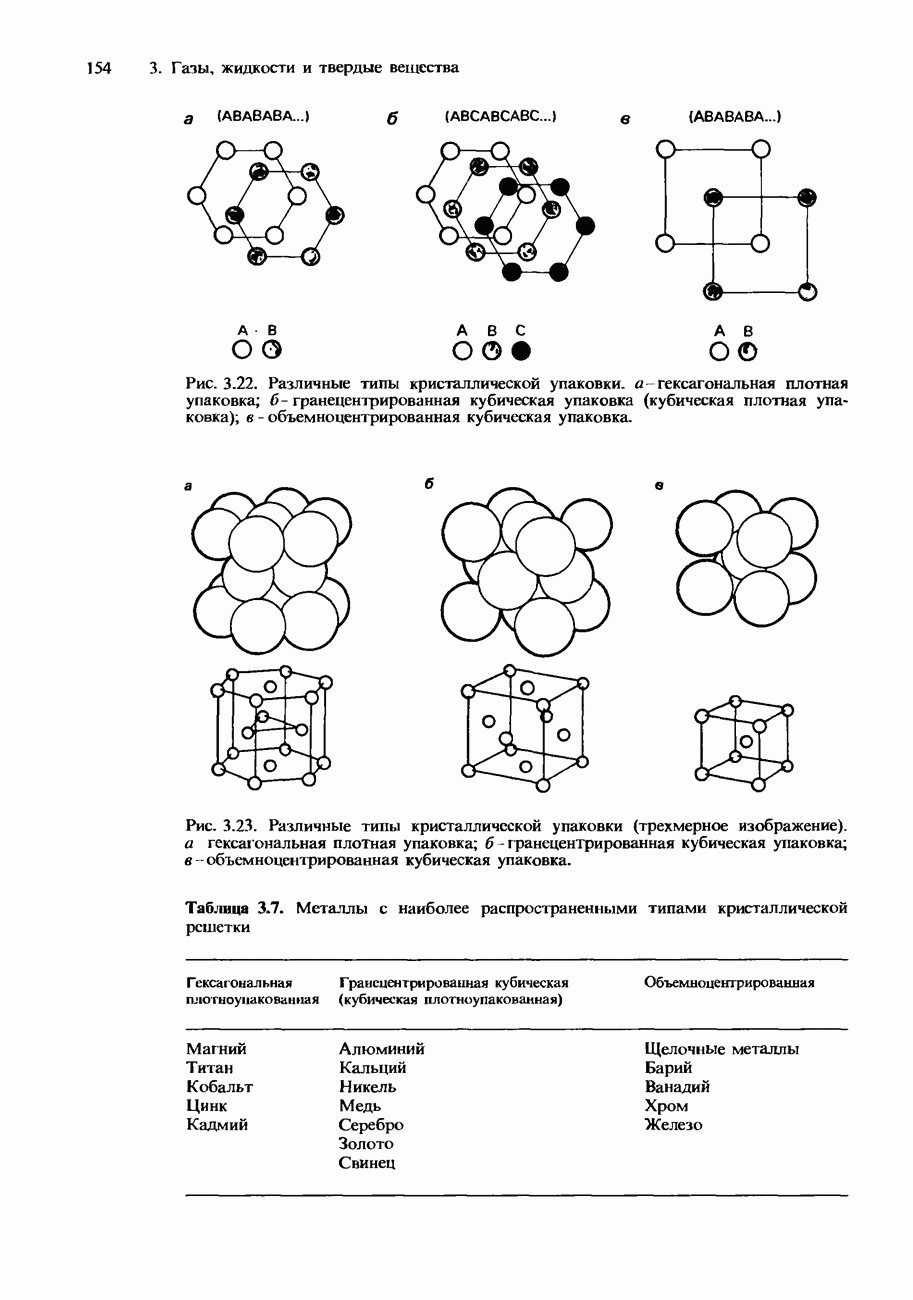
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
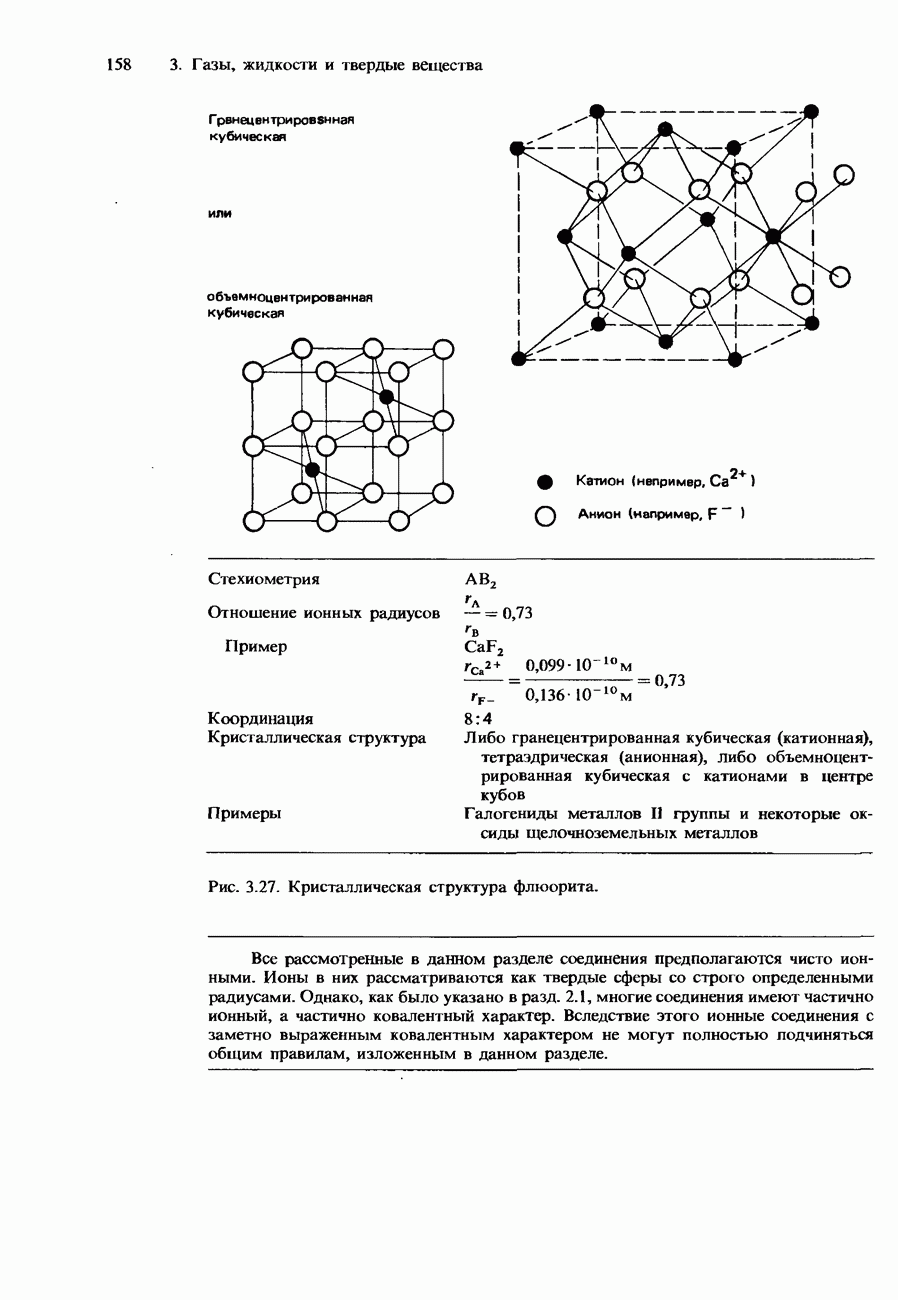
- Ионные кристаллы
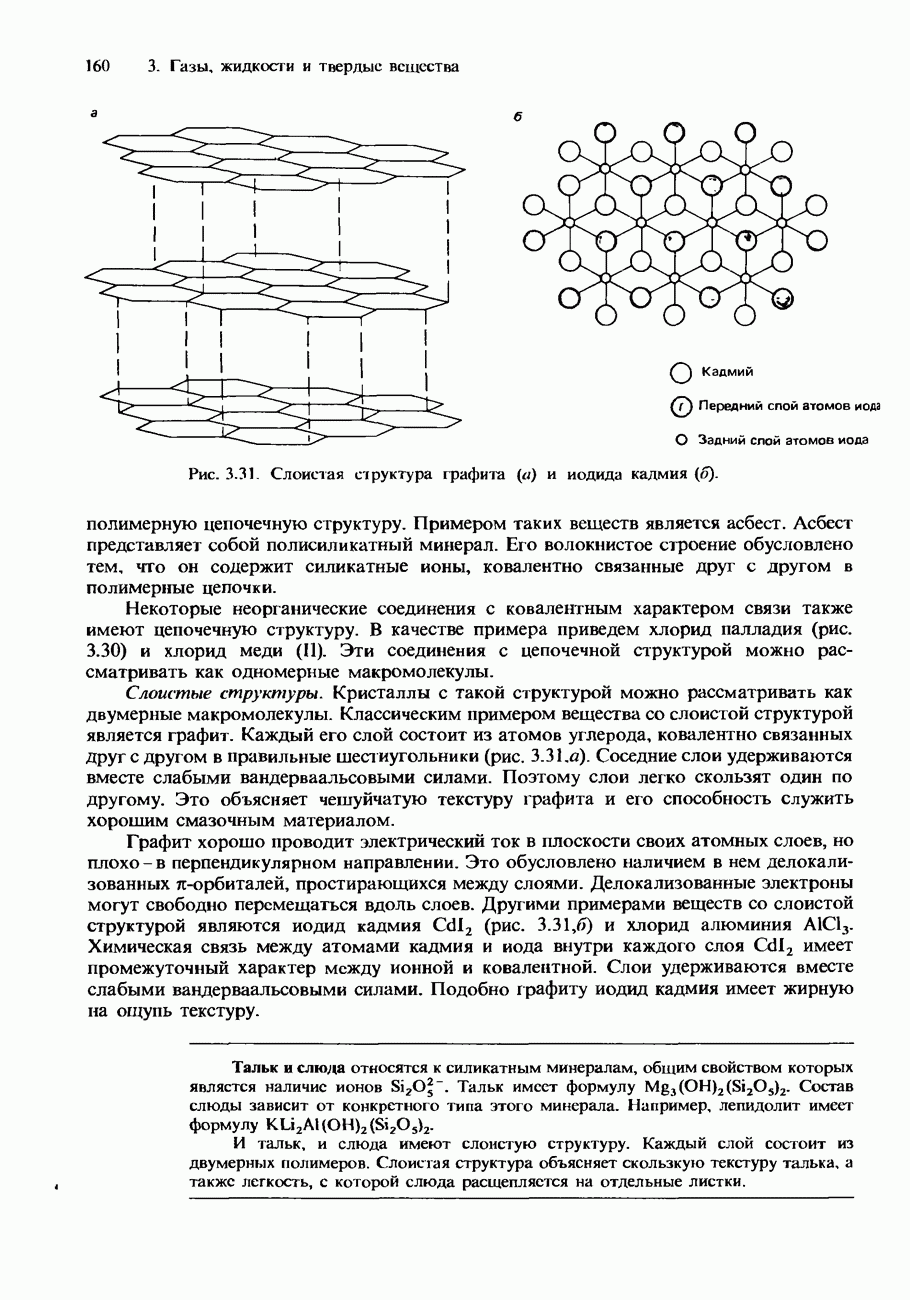
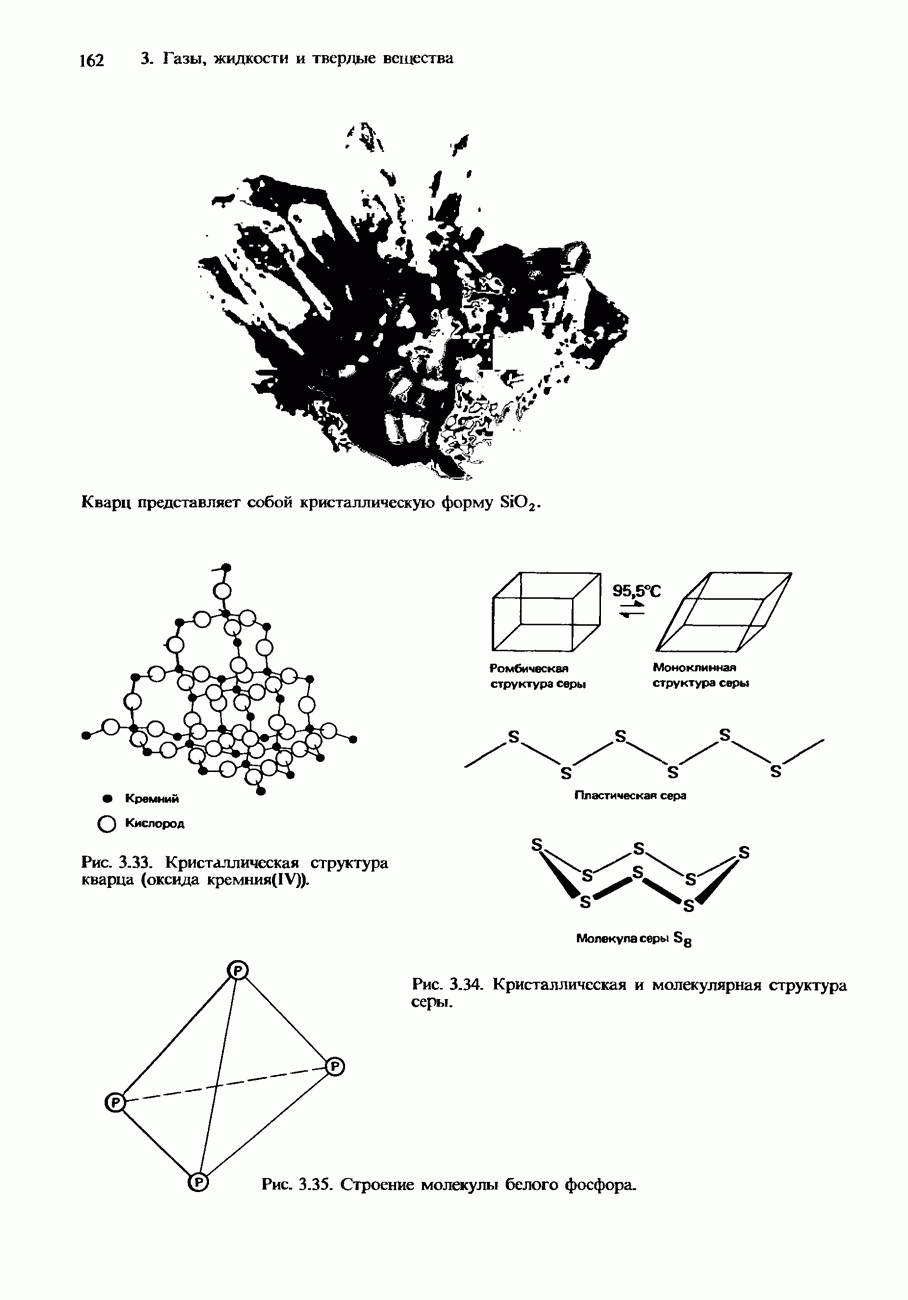
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
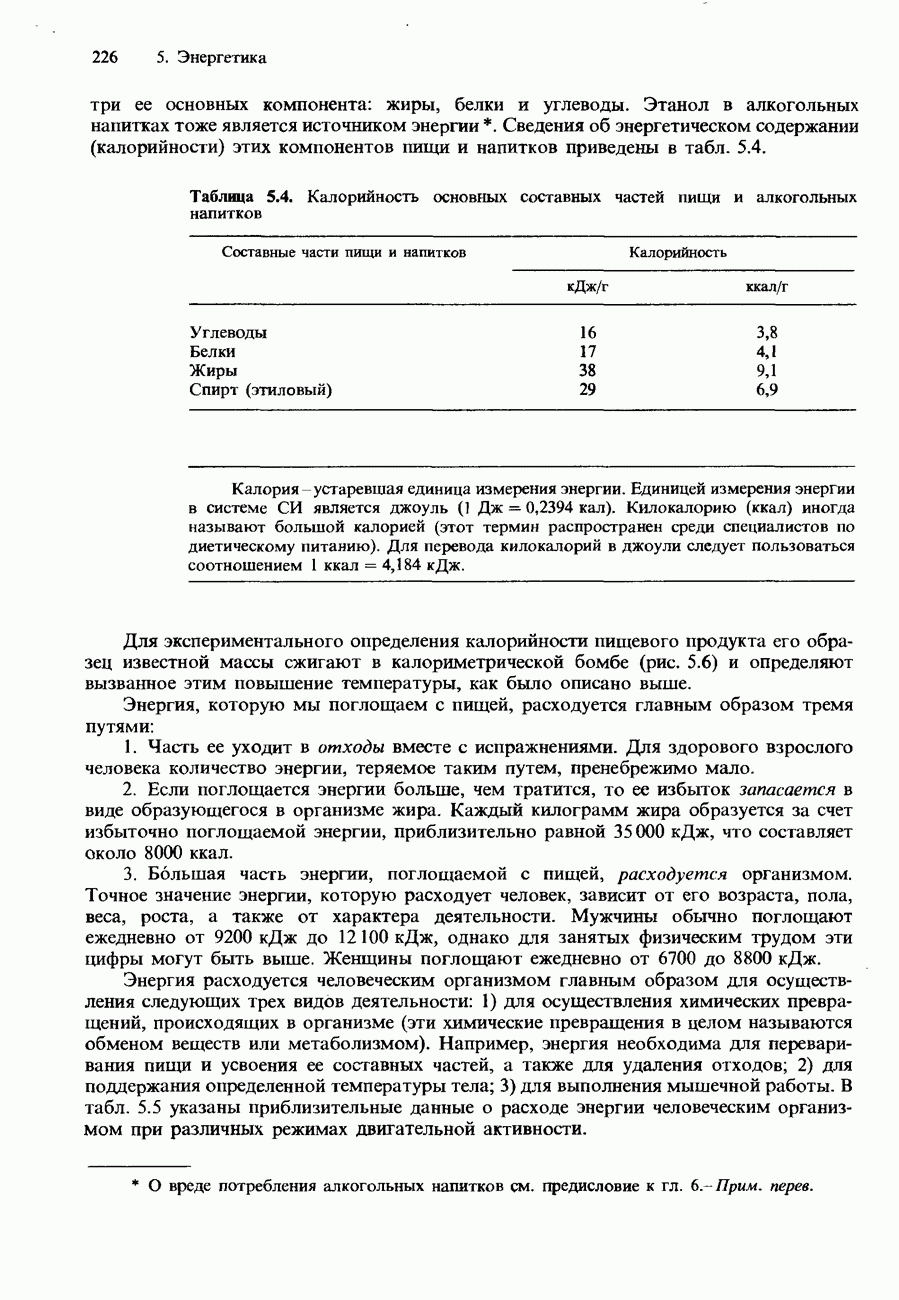
- КАЛОРИЙНОСТЬ ПИЩИ
- ЗАКОН ГЕССА
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
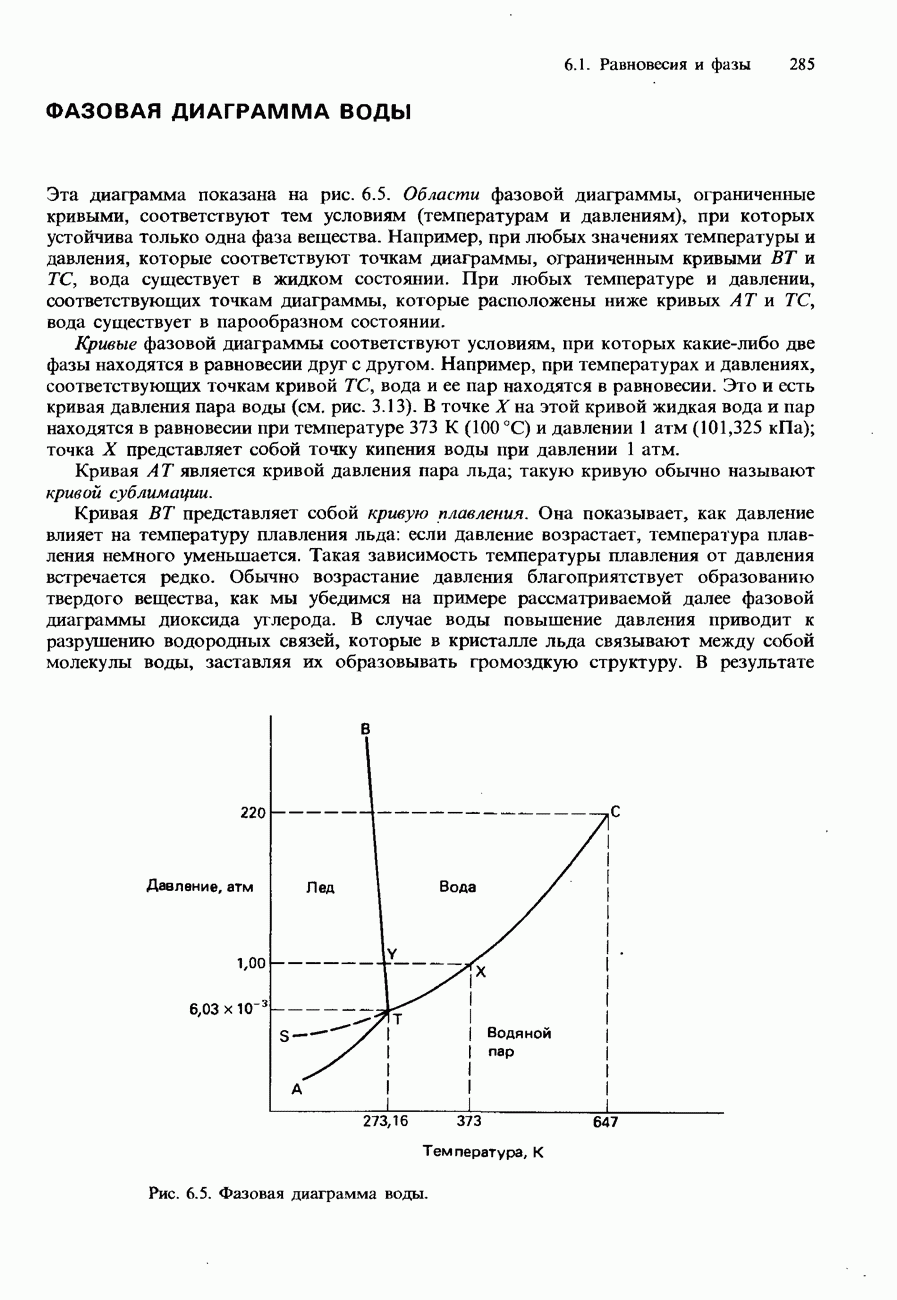
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
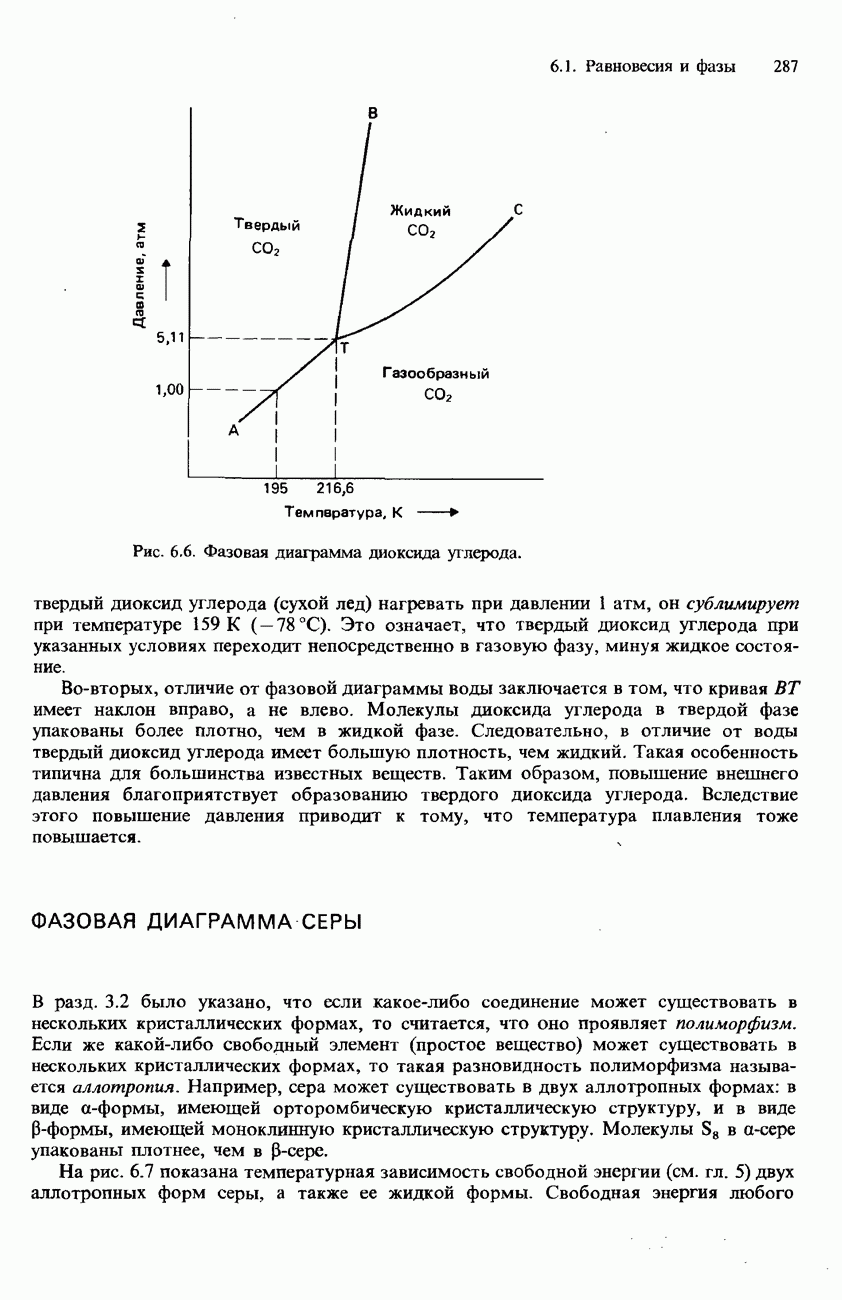
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
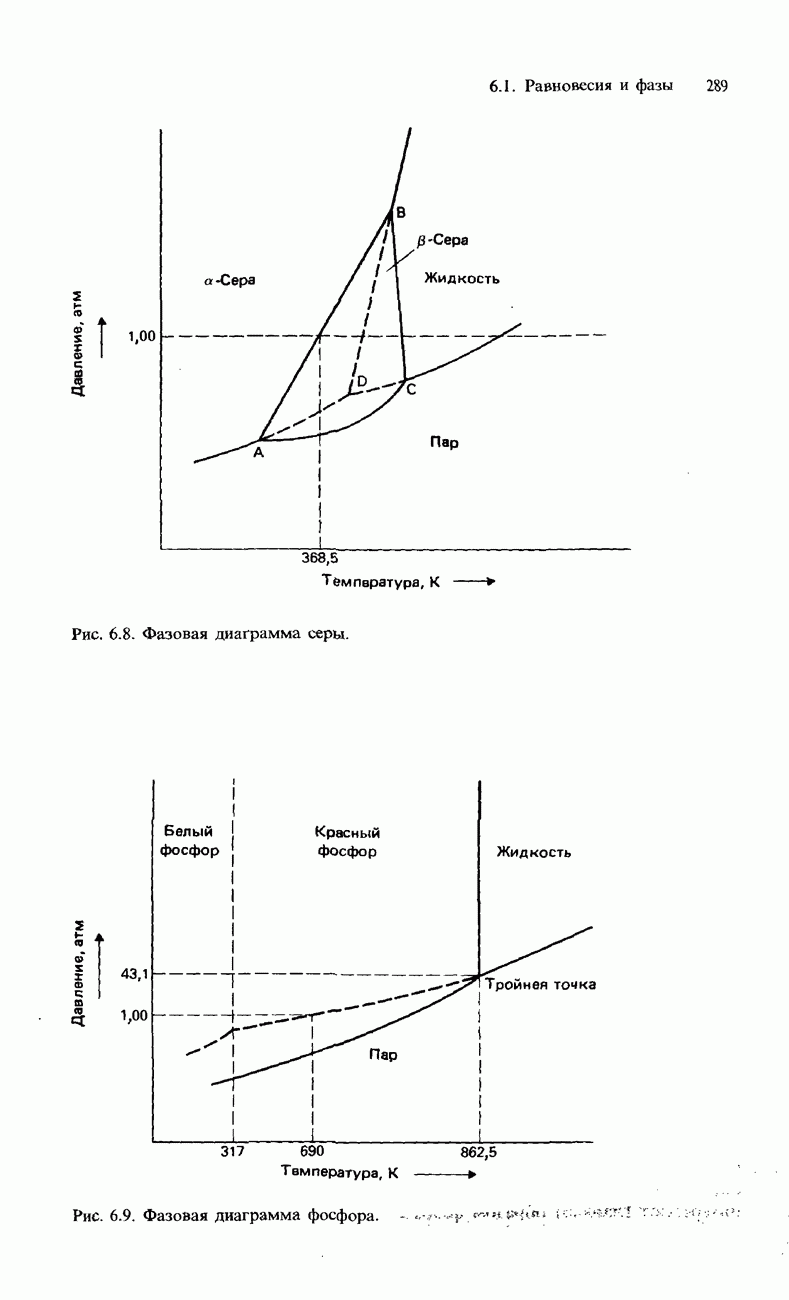
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
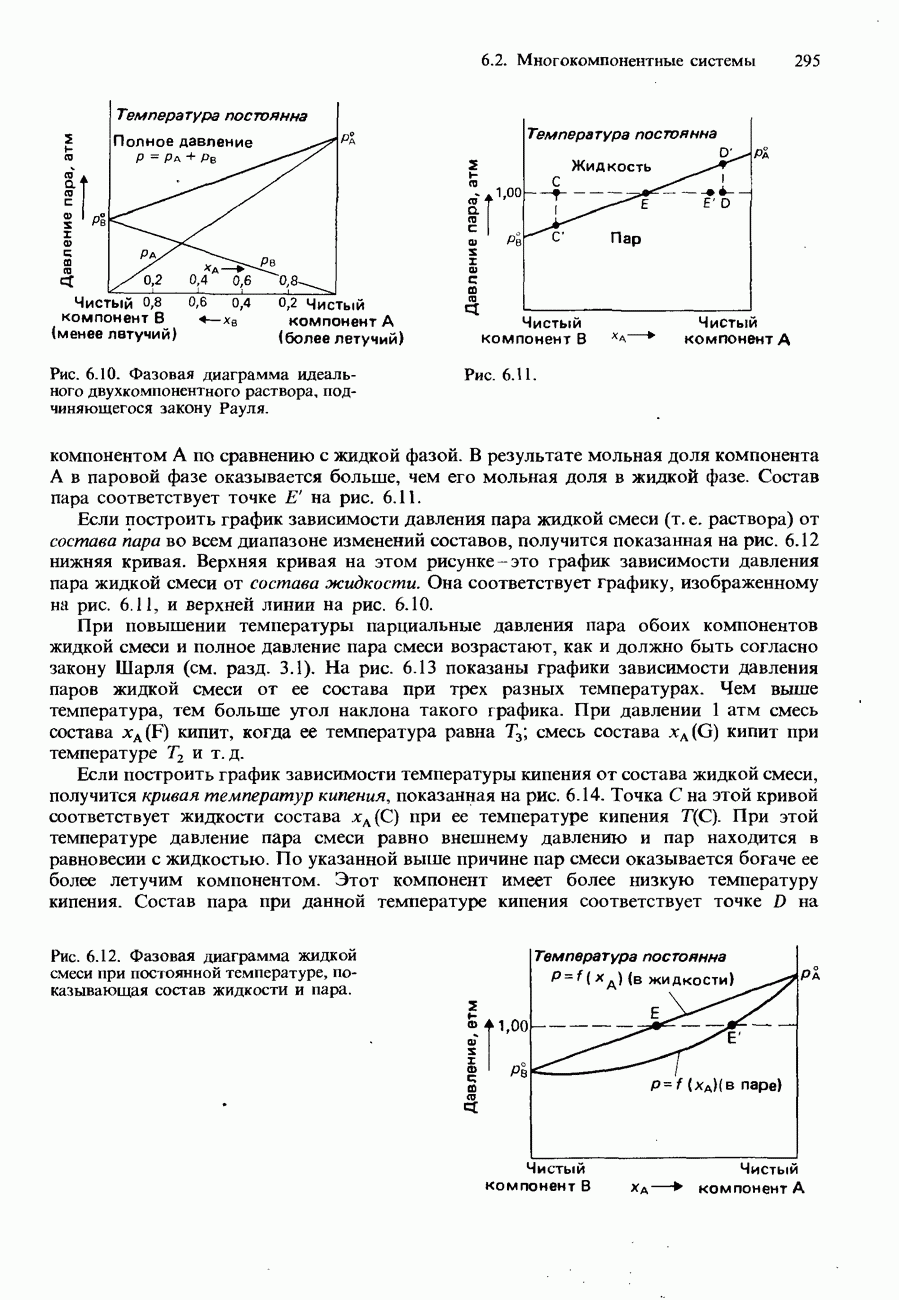
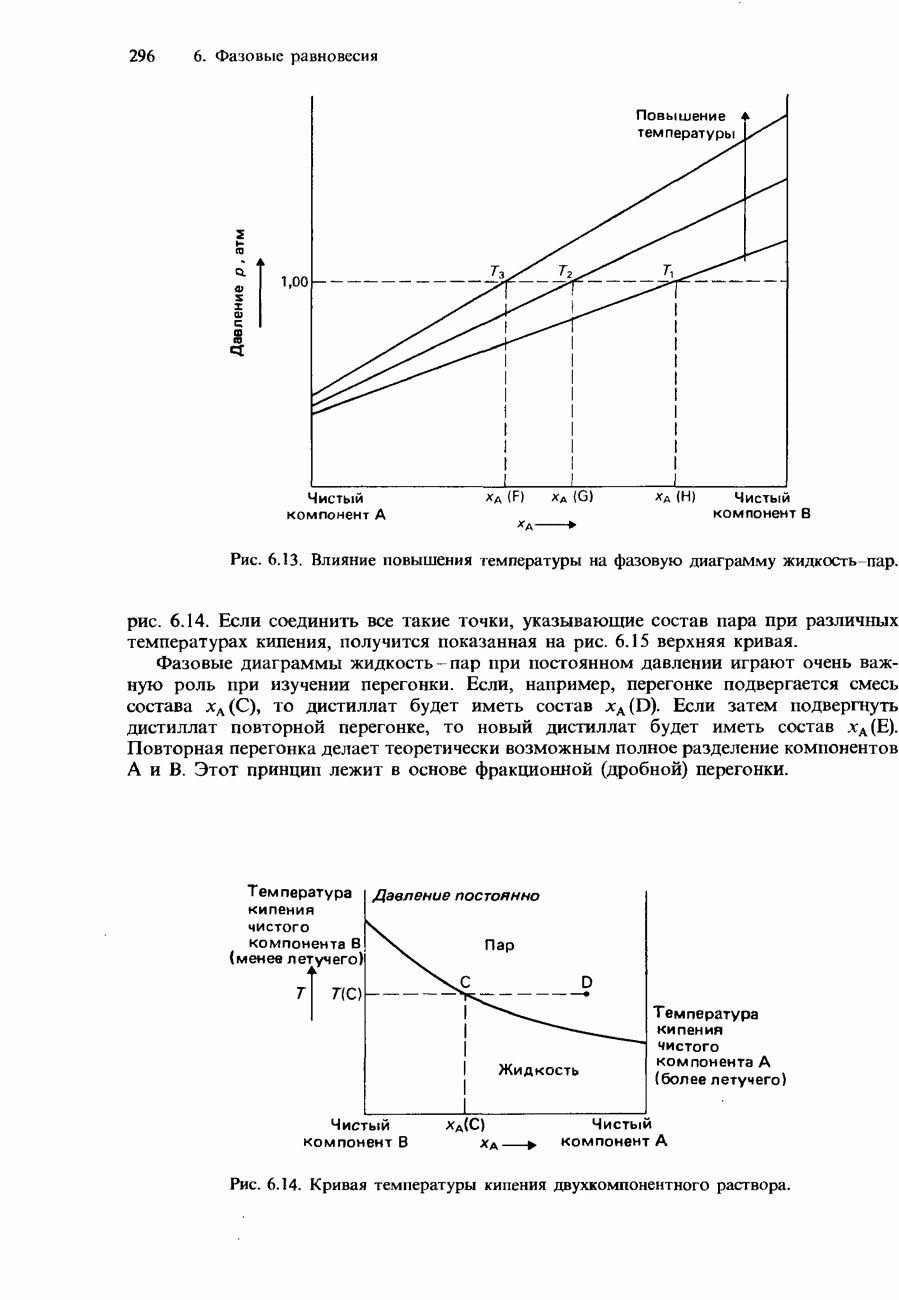
- Фазовые диаграммы полностью смешивающихся жидкостей
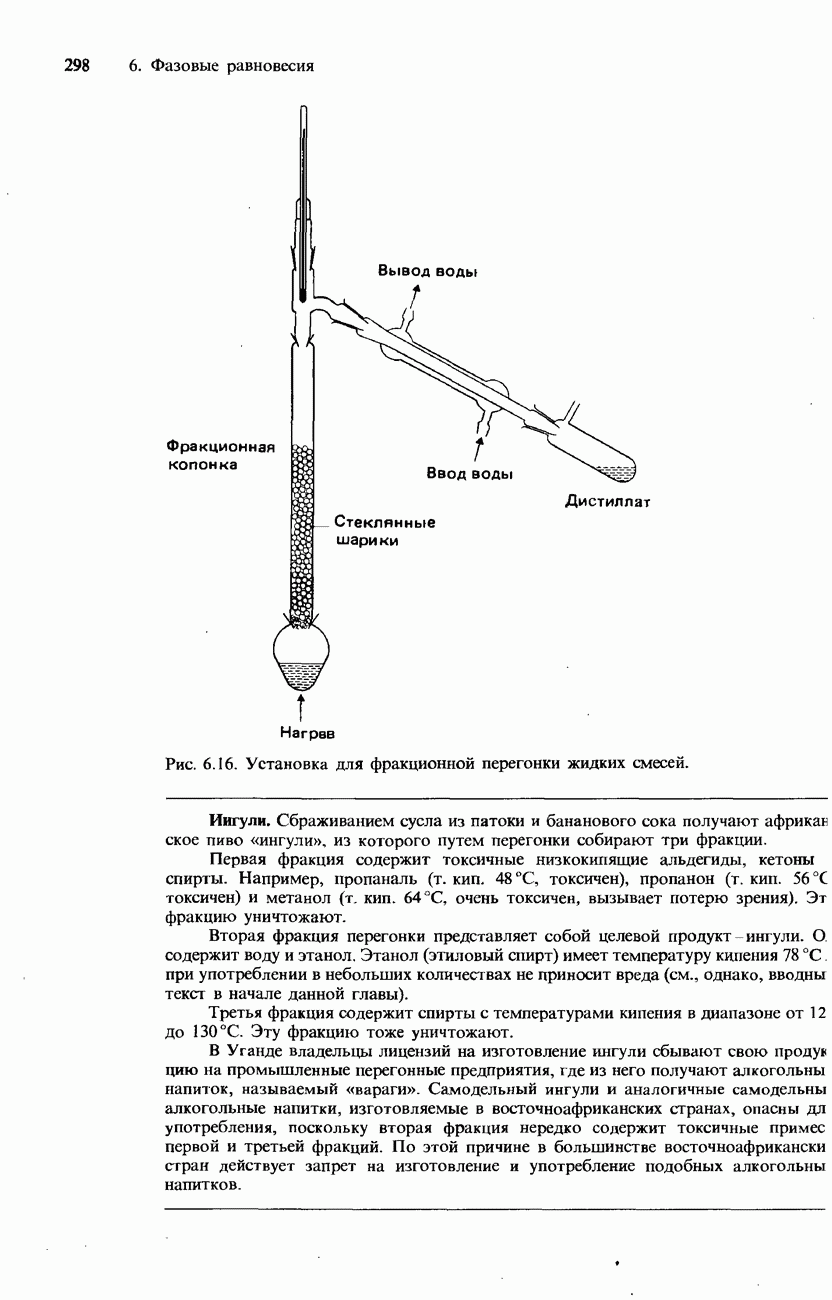
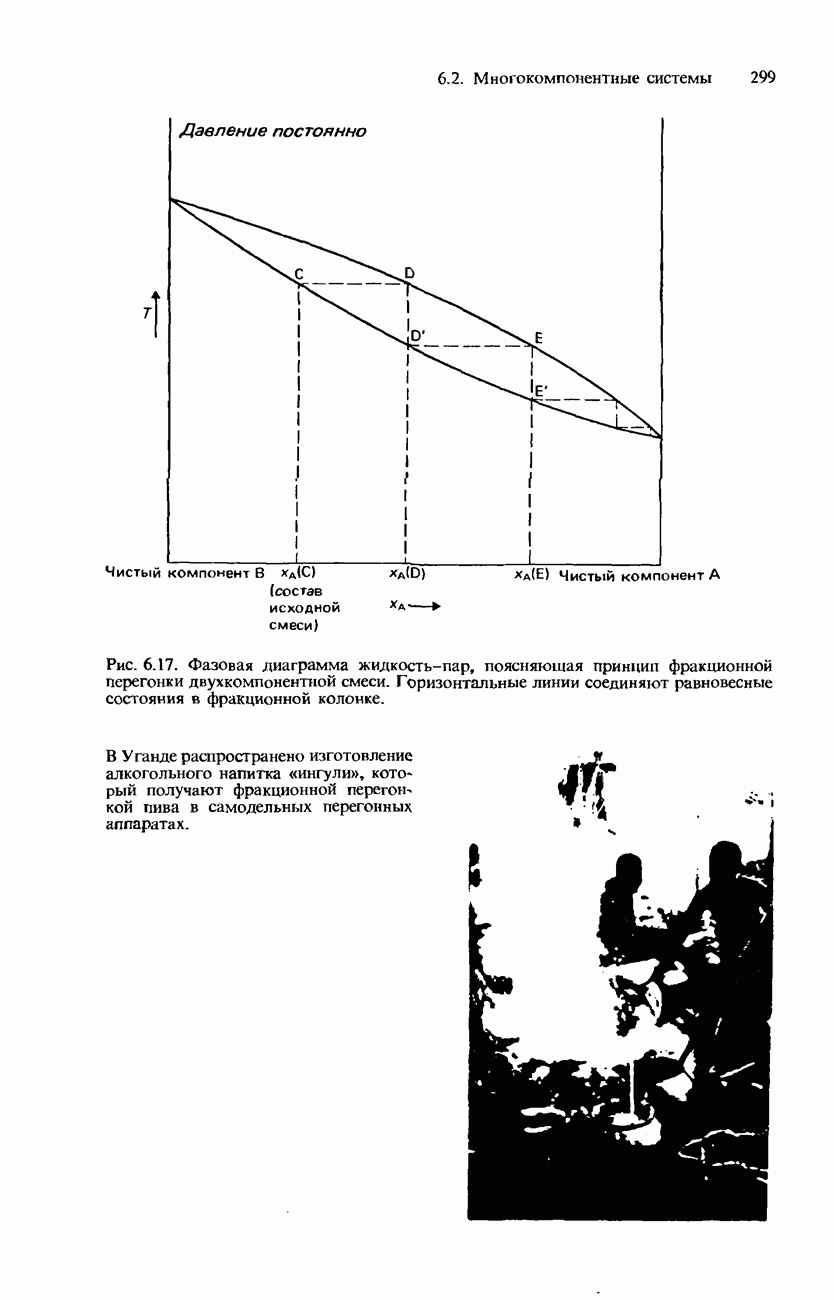
- Фракционная перегонка
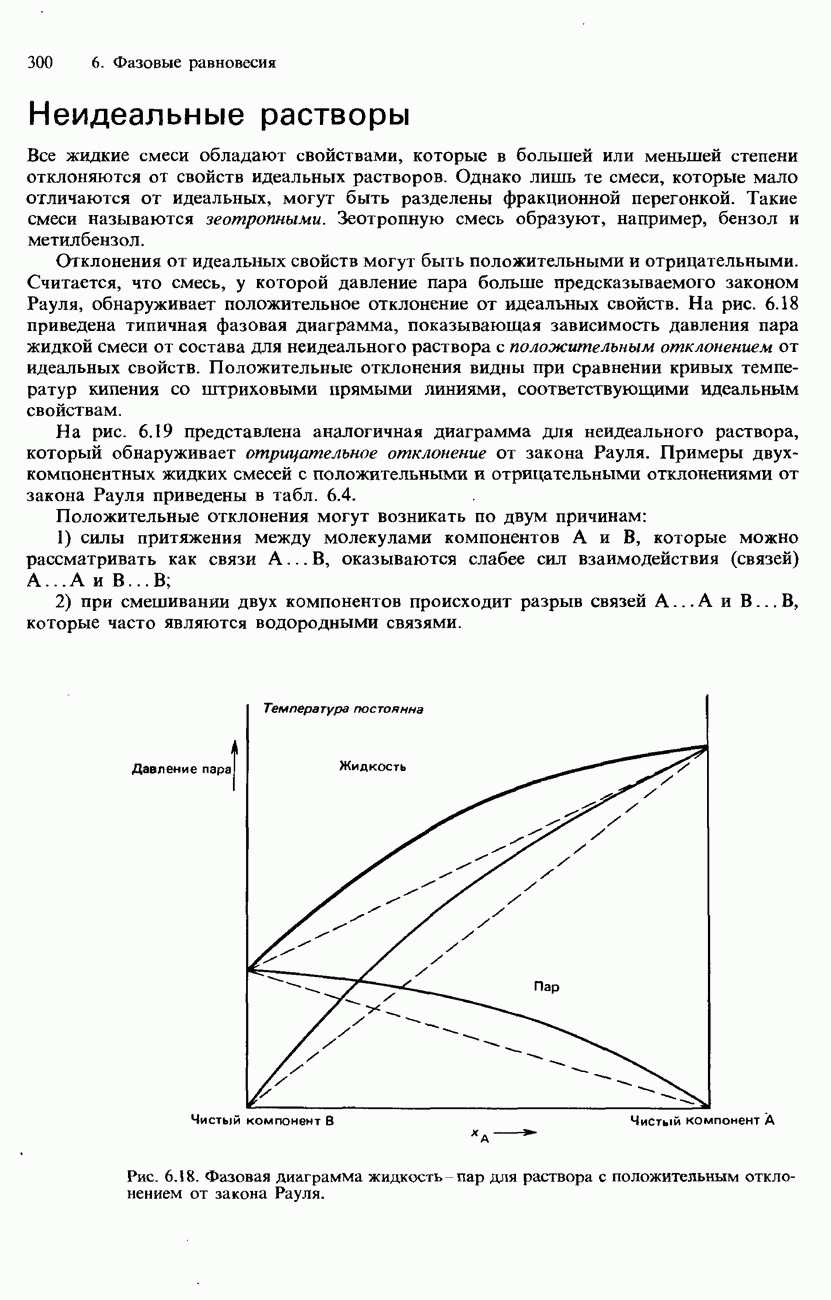
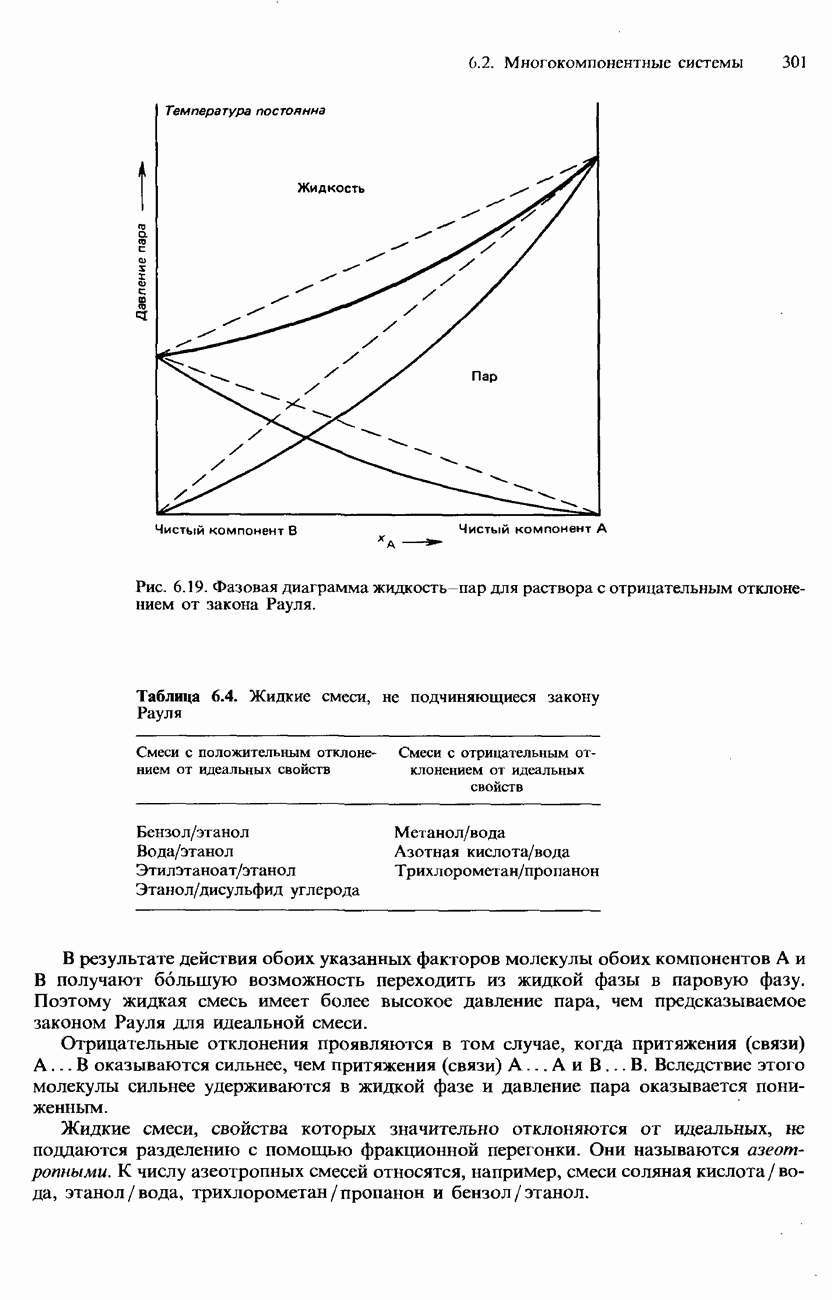
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
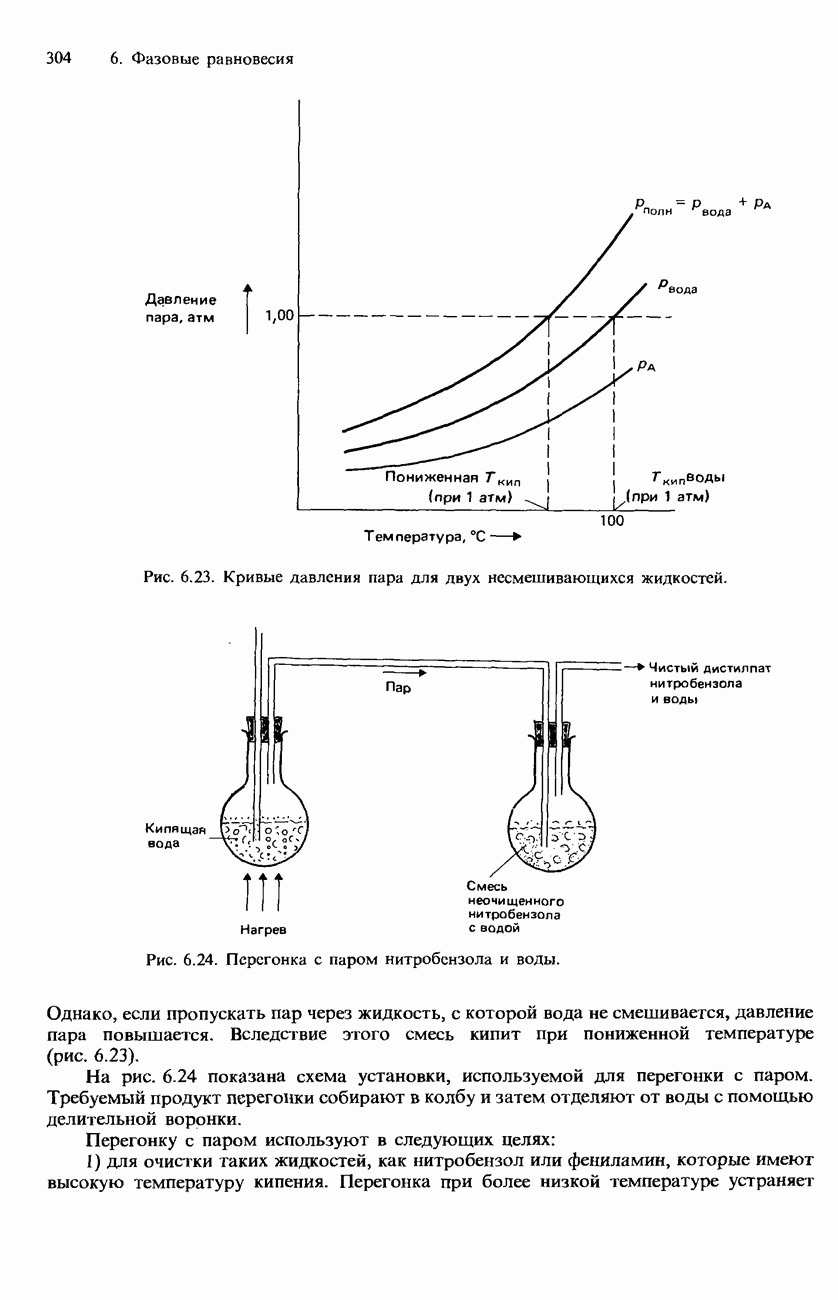
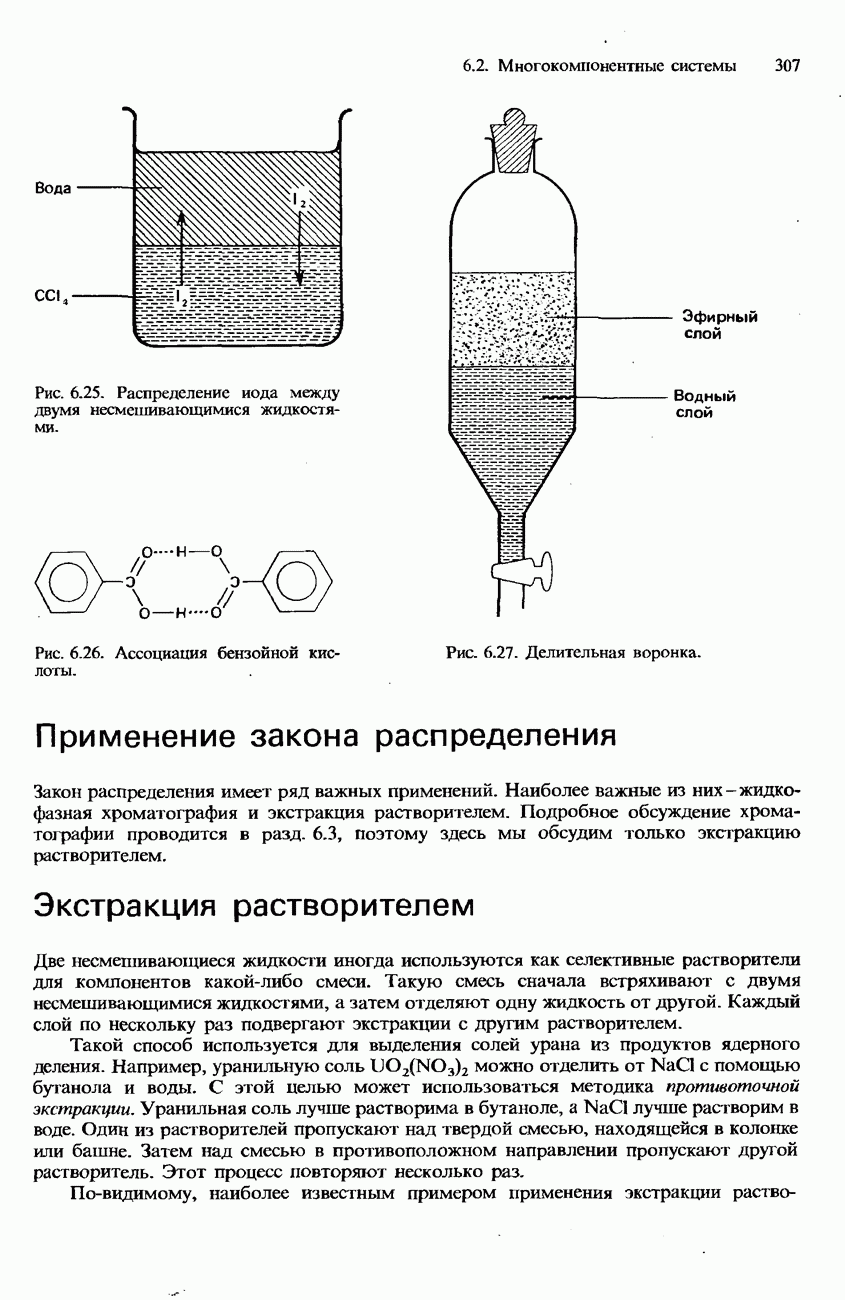
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
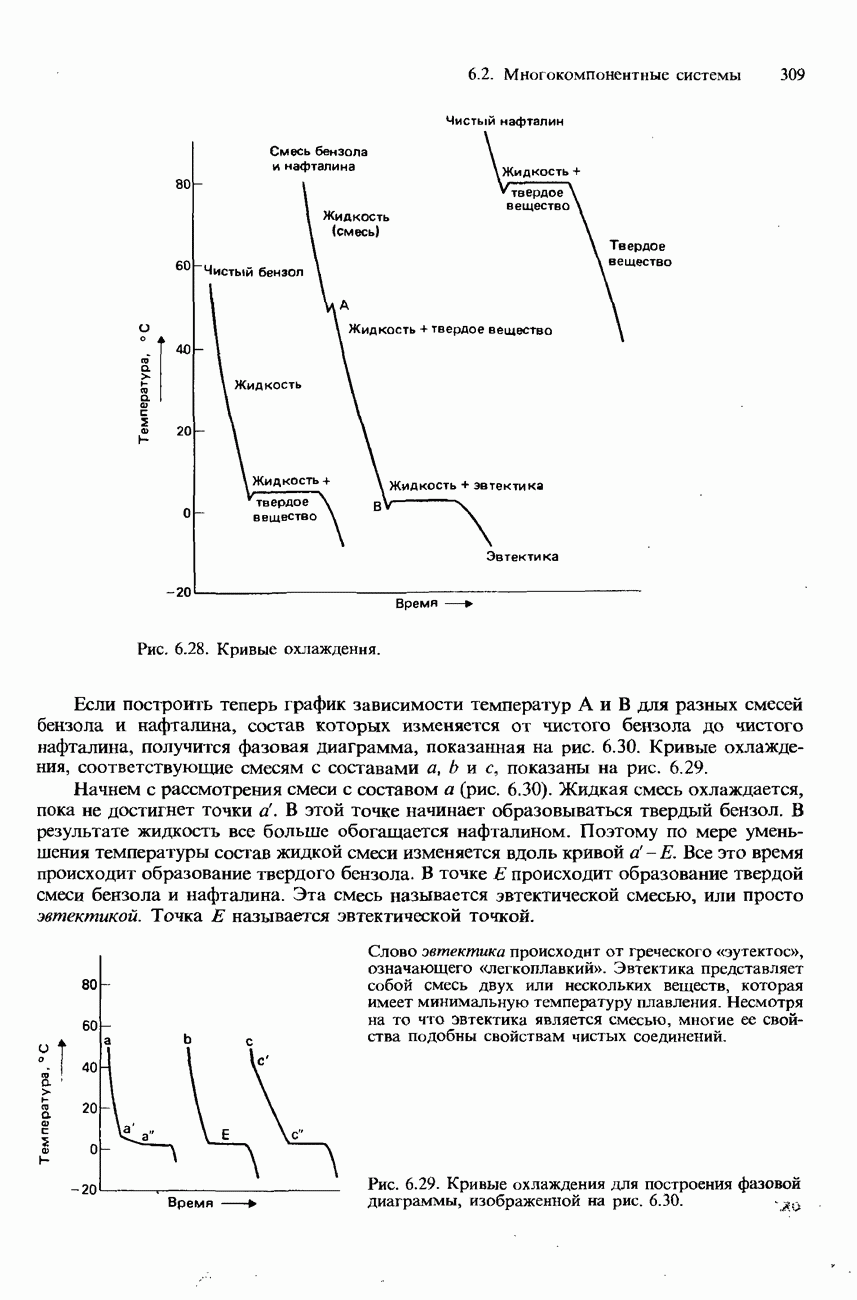
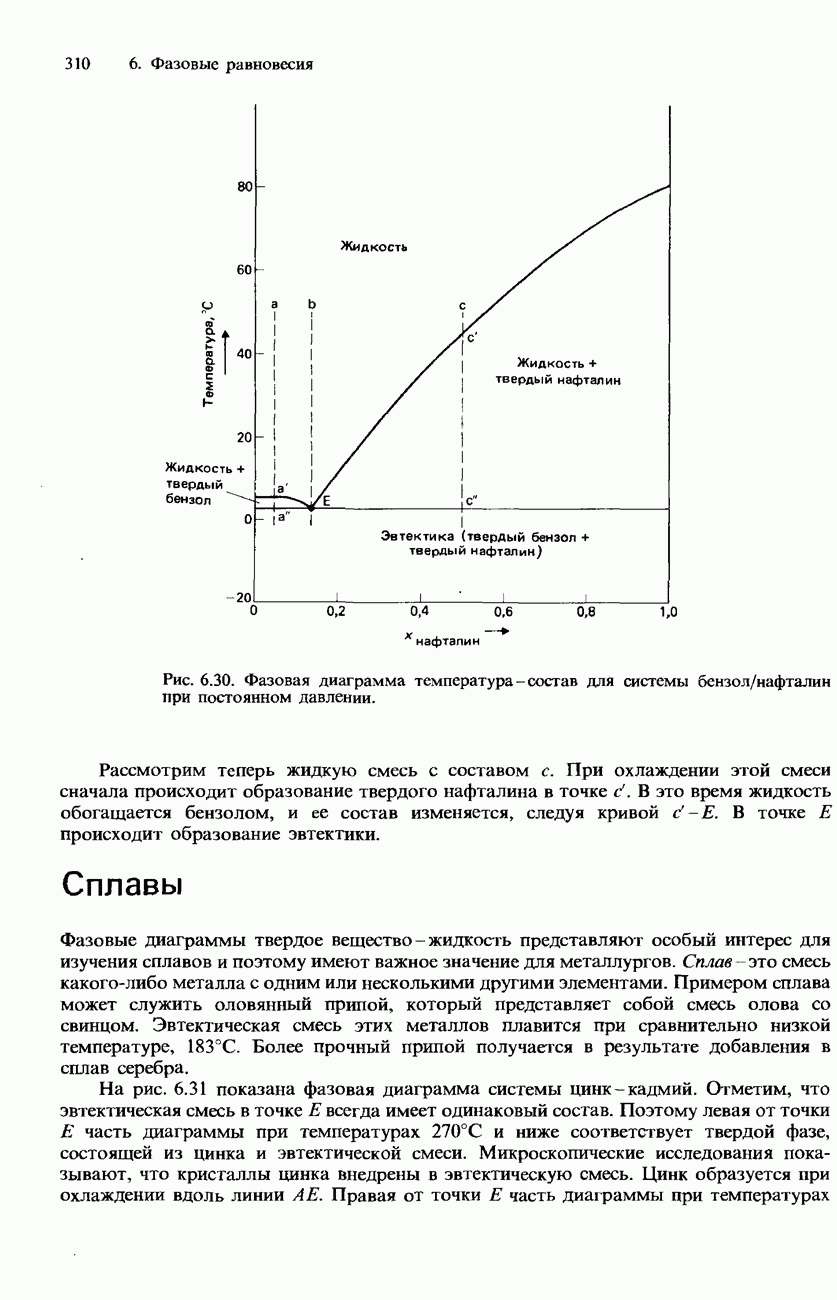
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
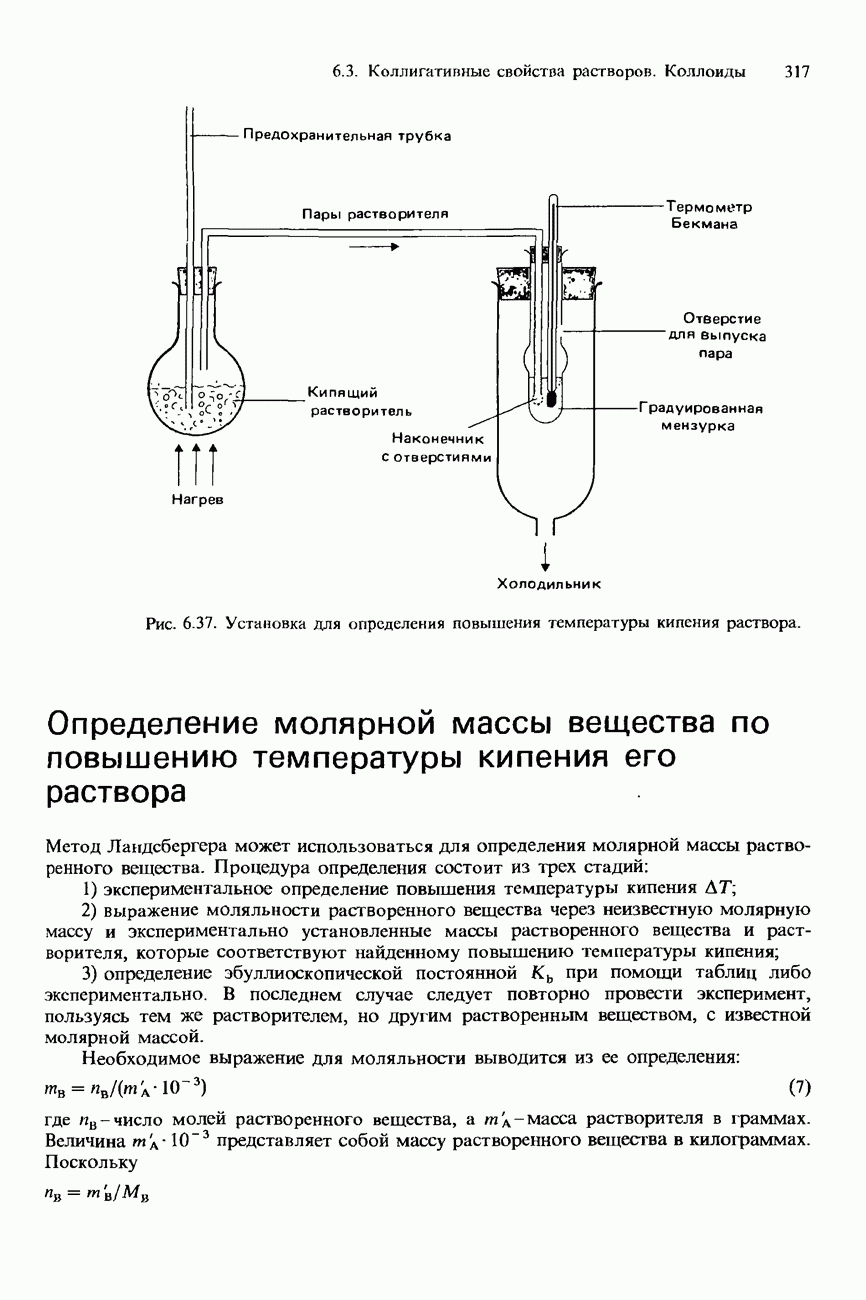
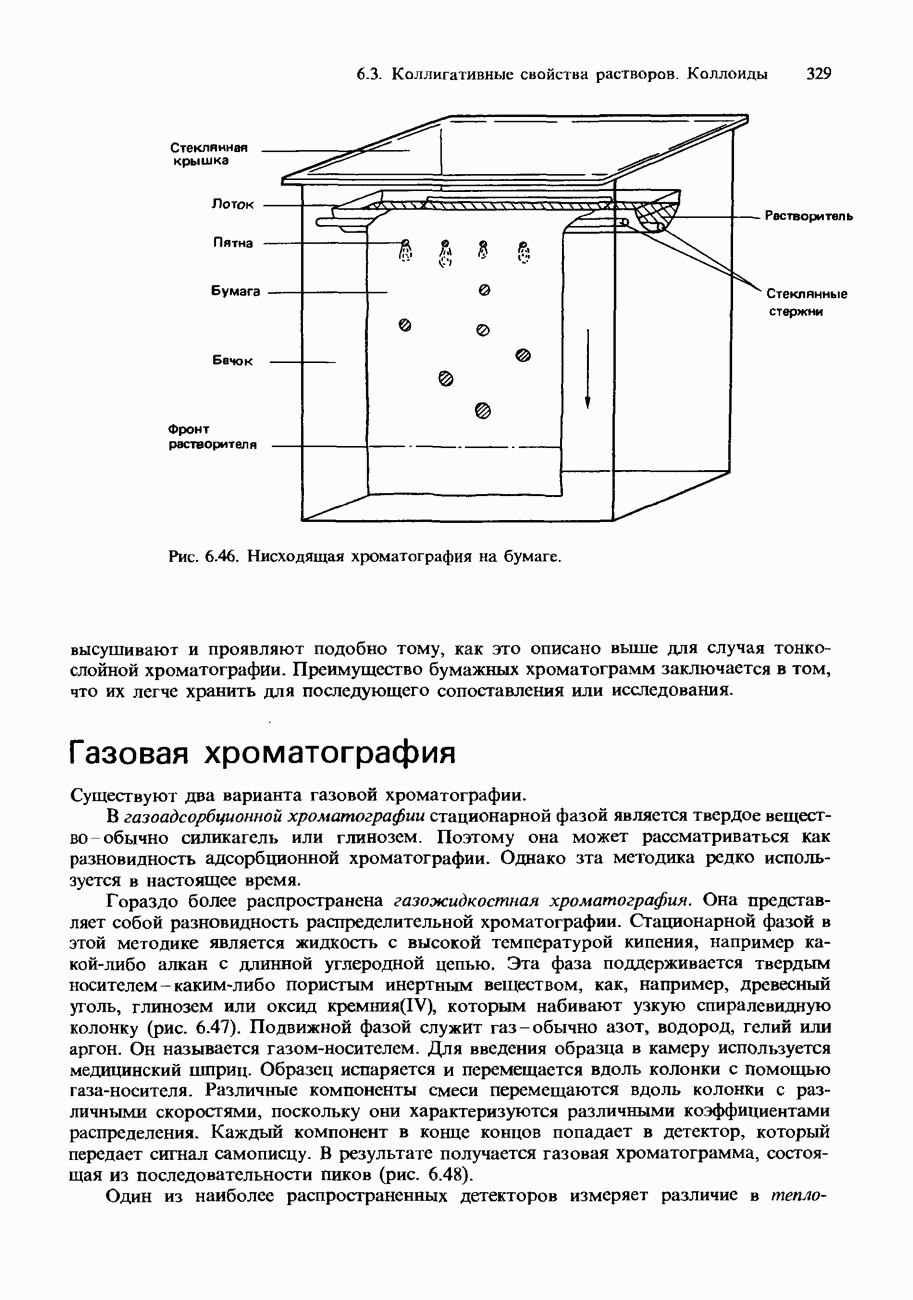
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
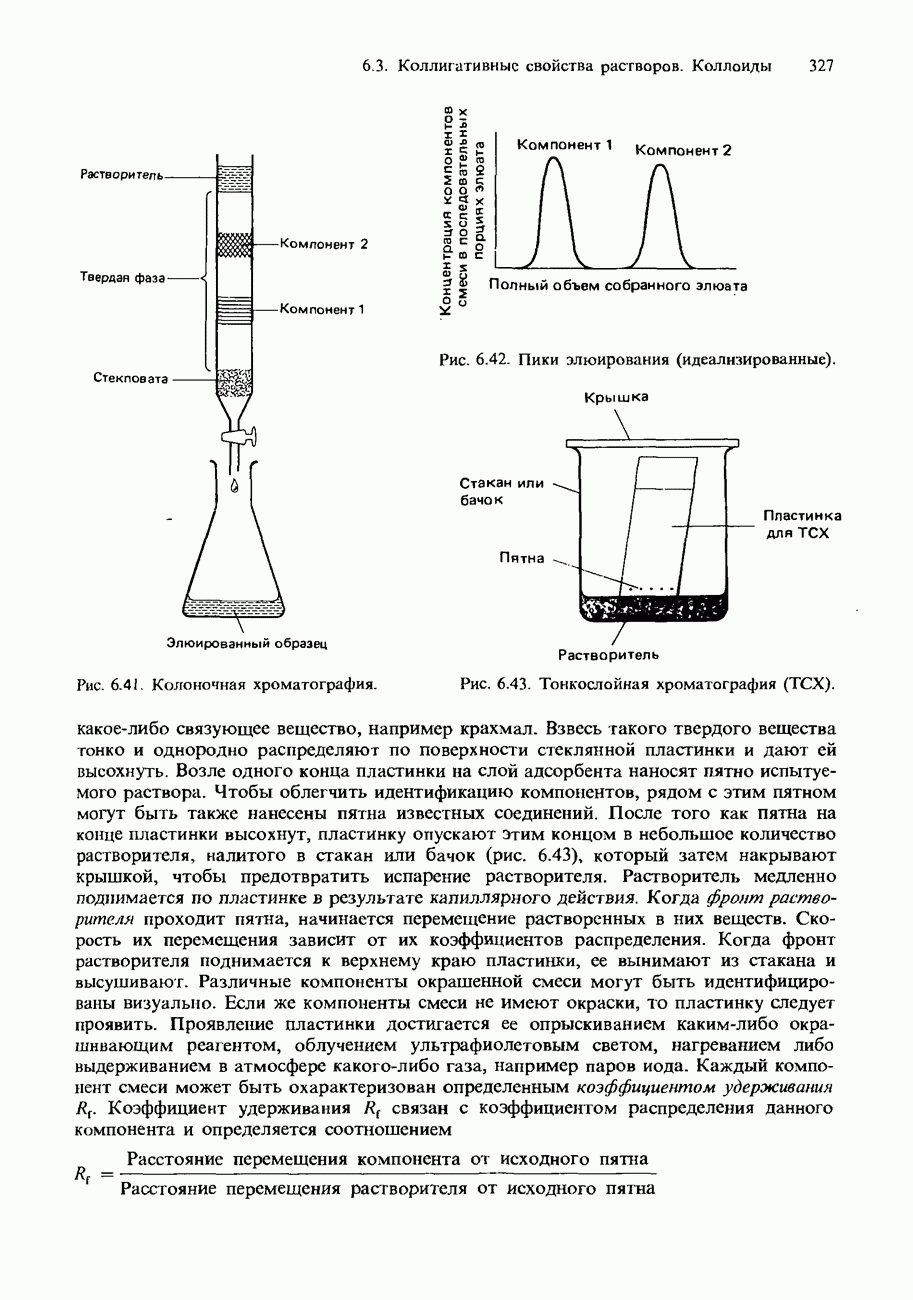
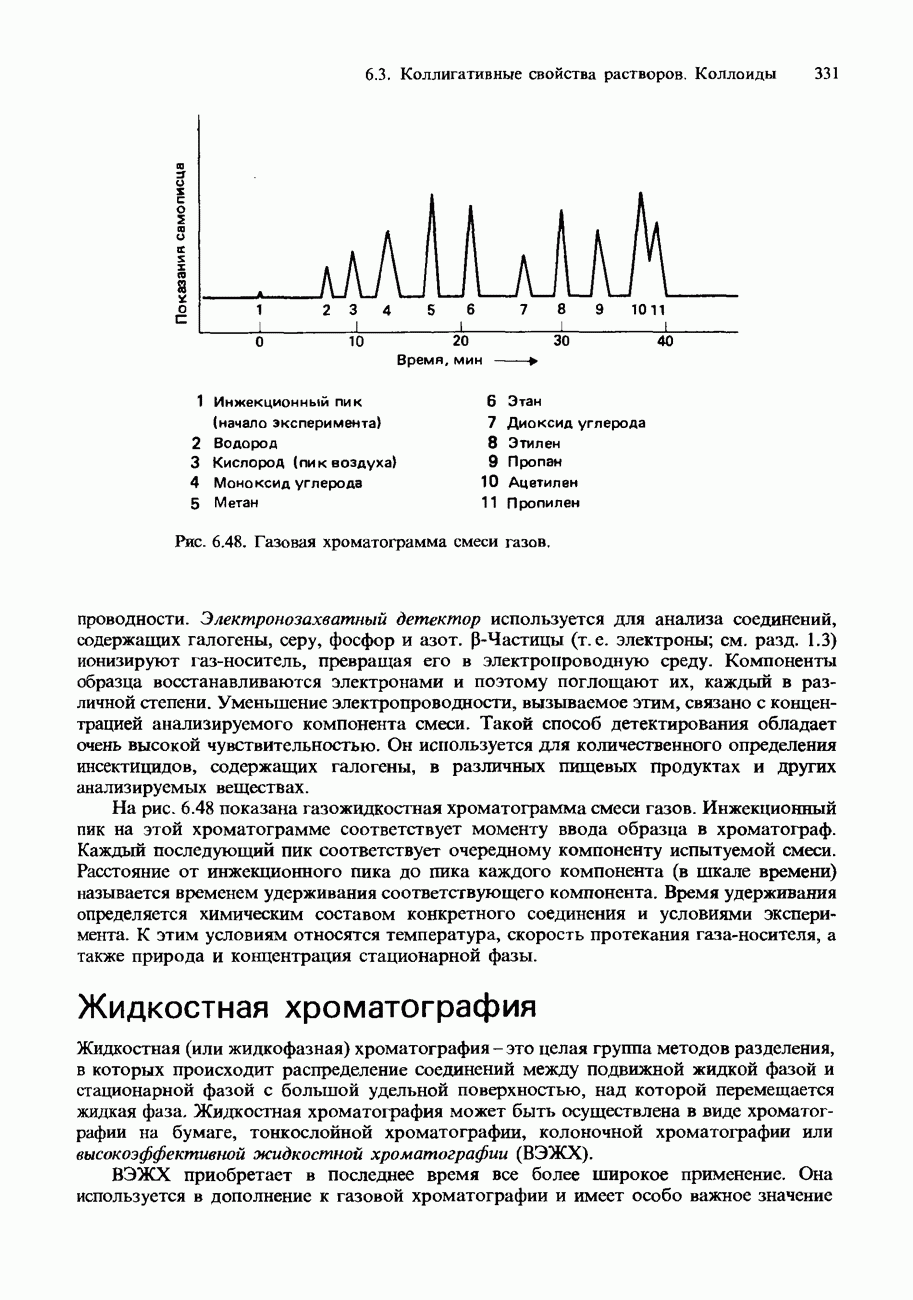
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
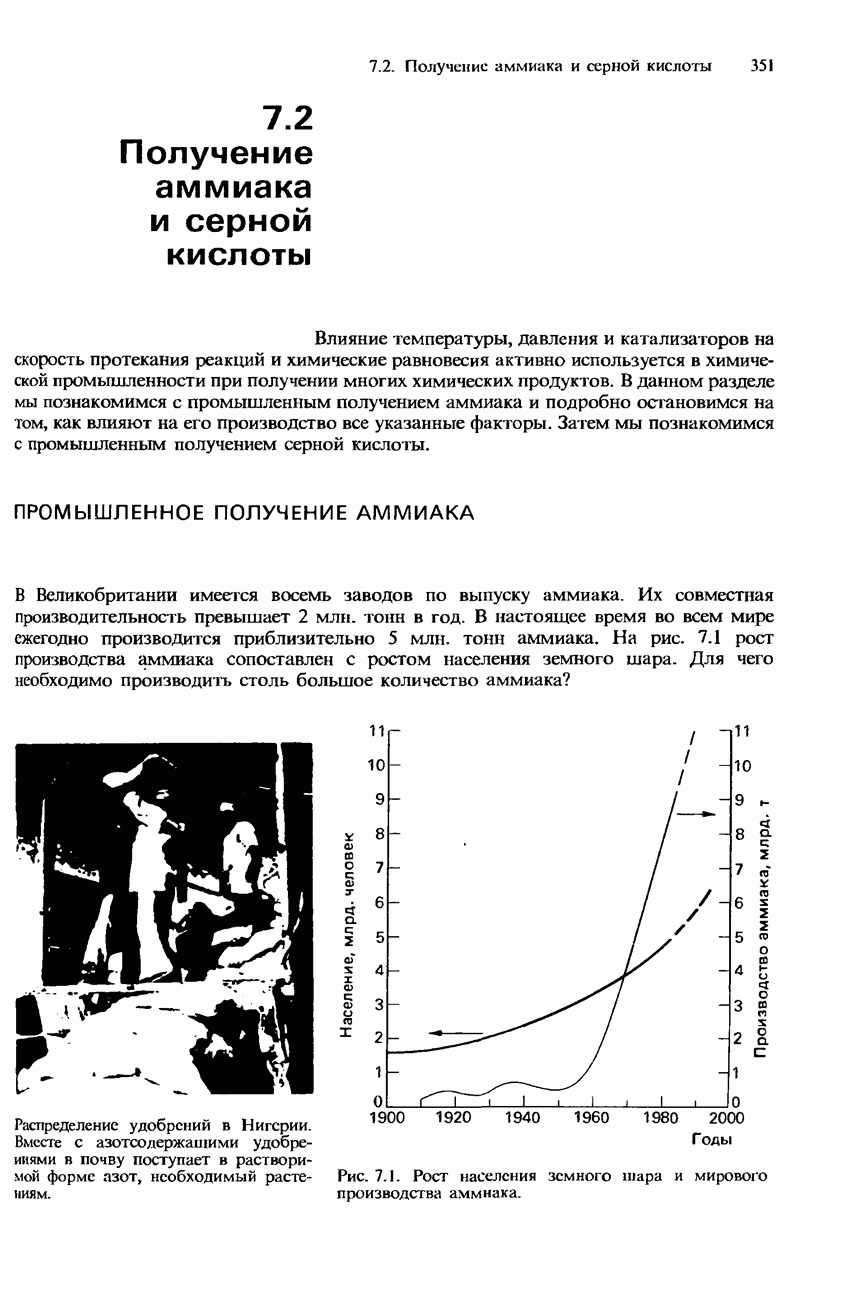
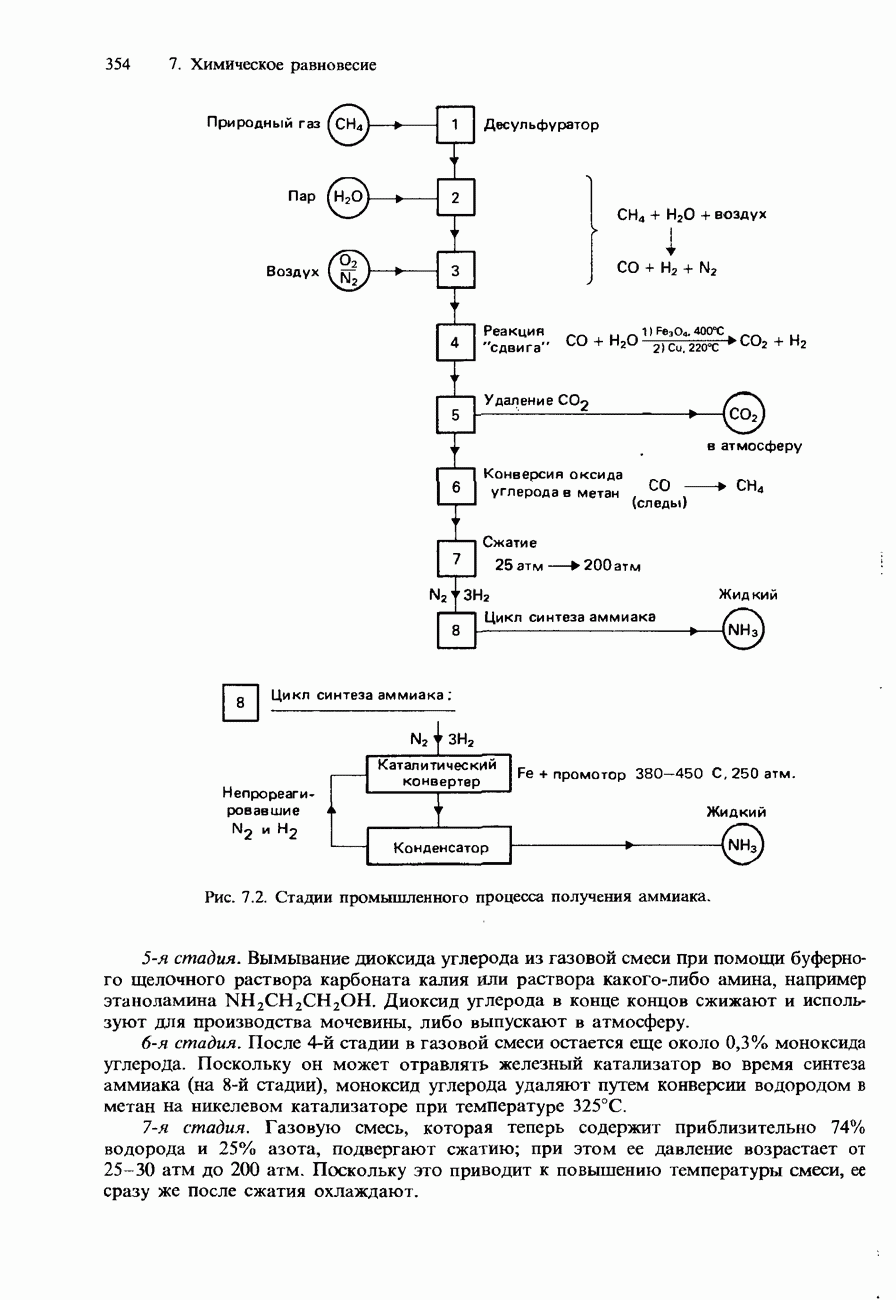
- 7.2. Получение аммиака и серной кислоты
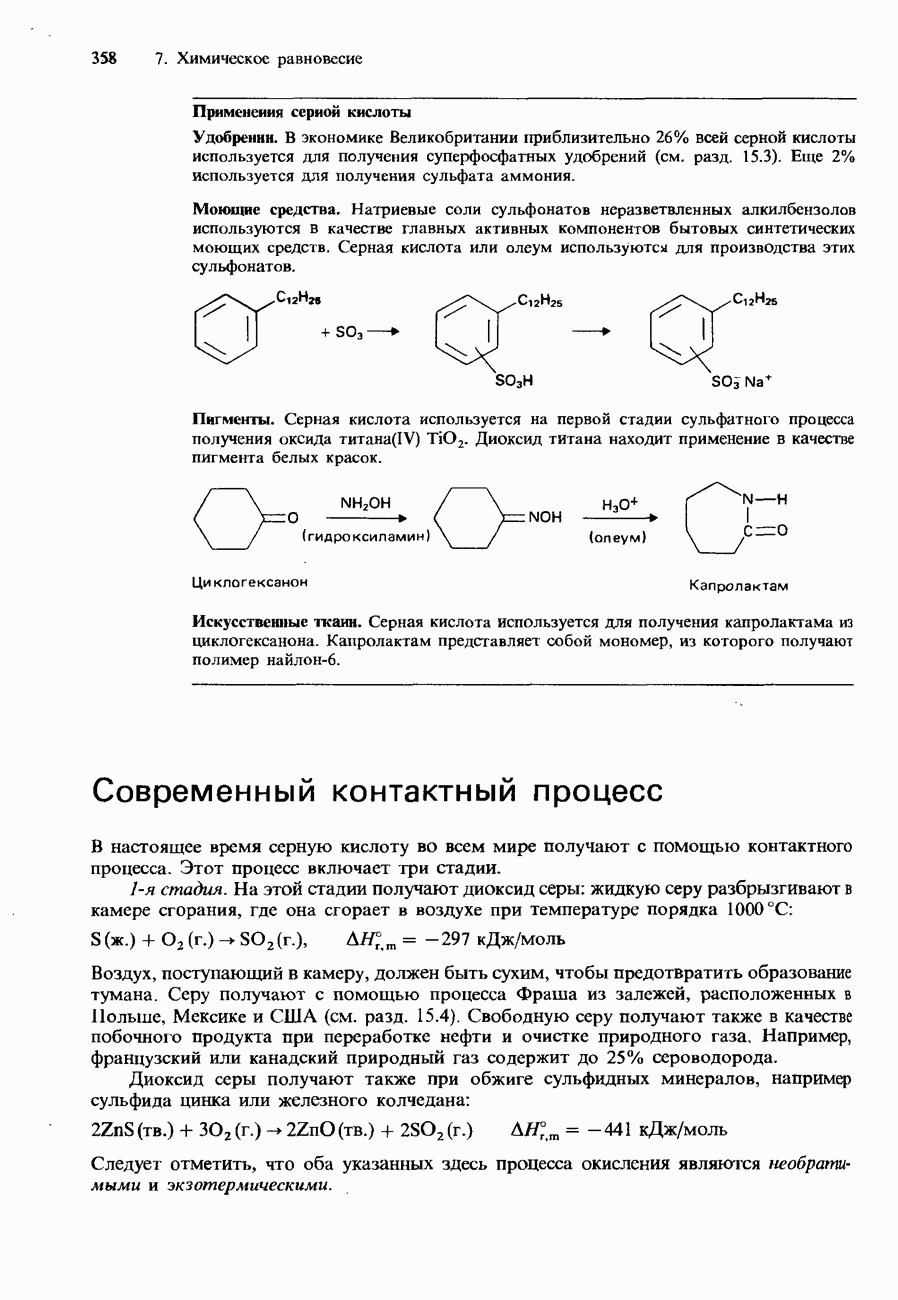
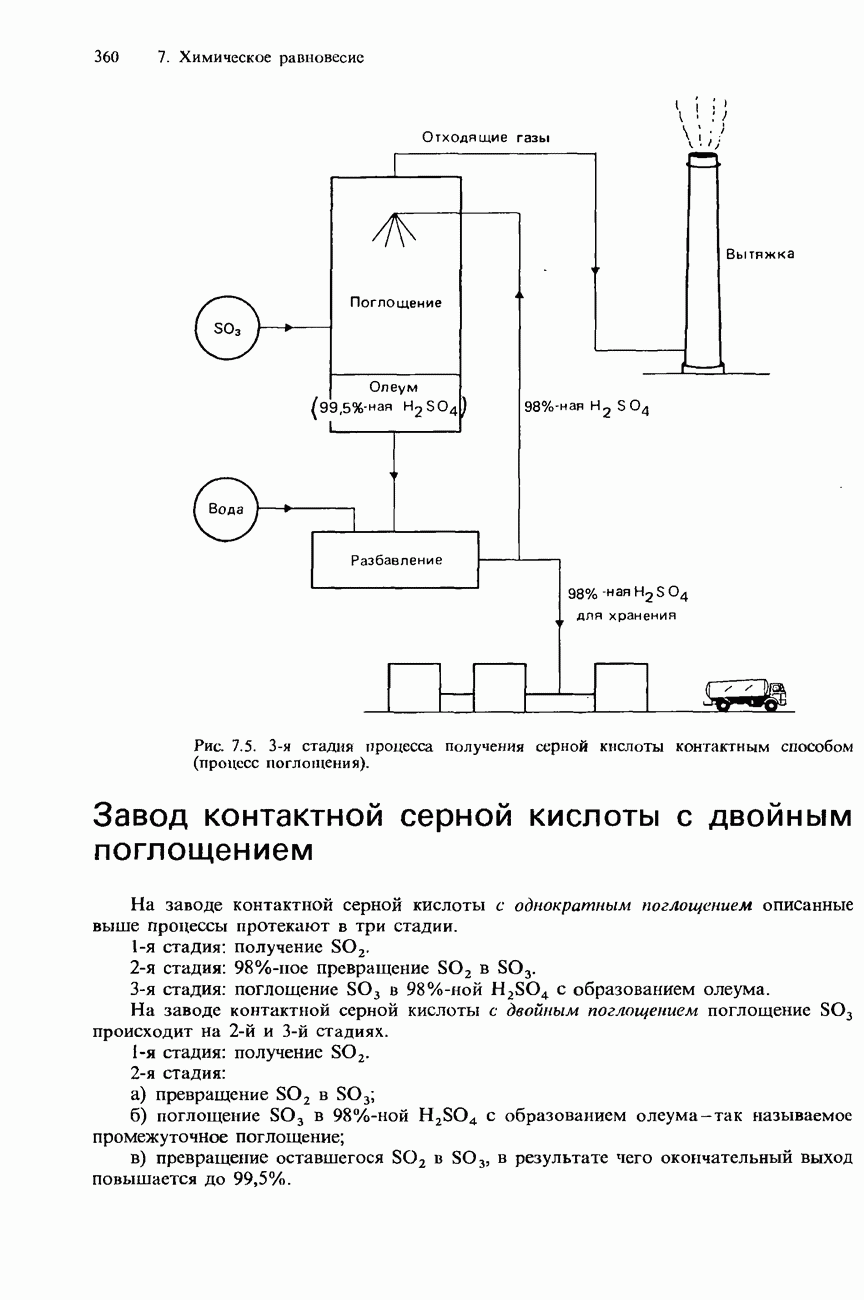
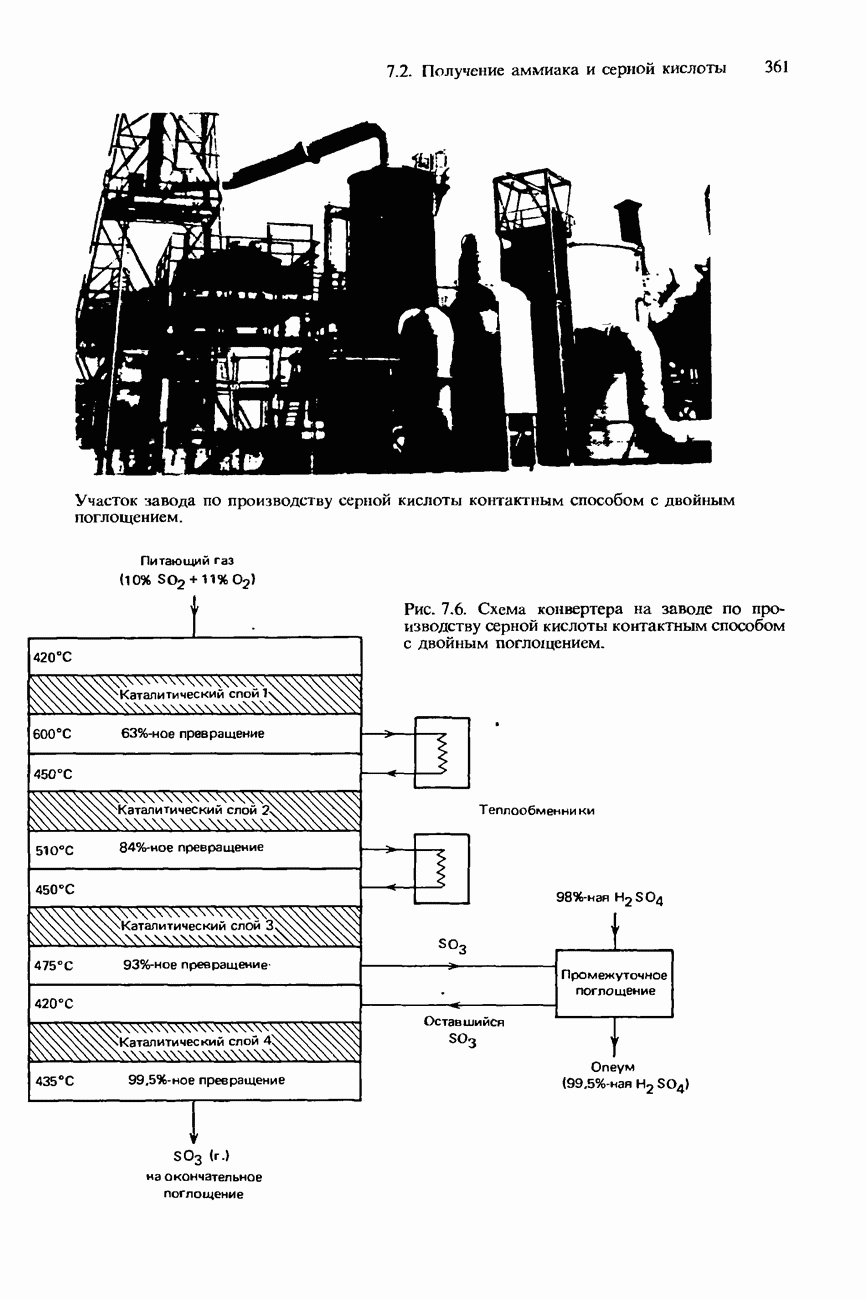
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
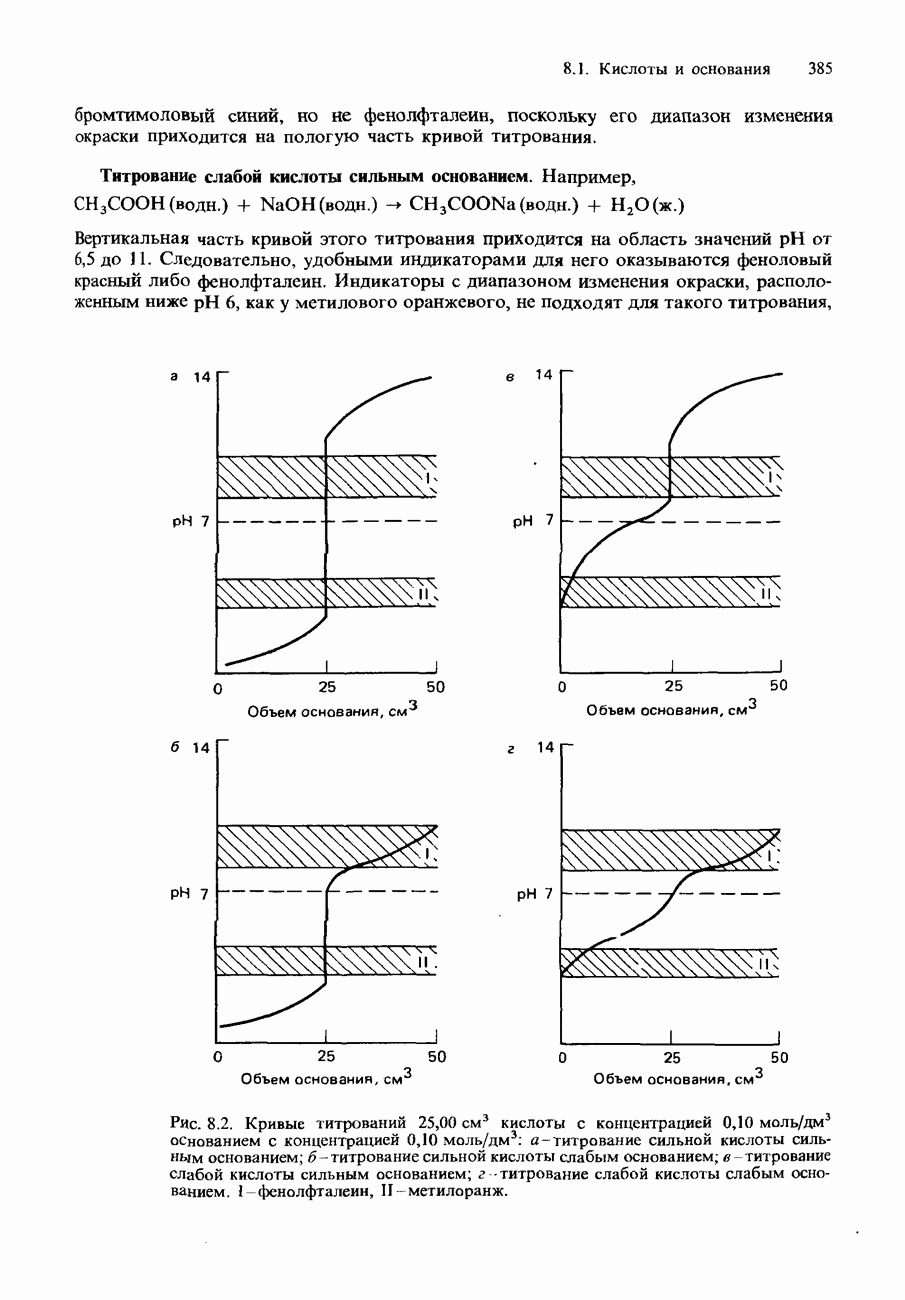
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
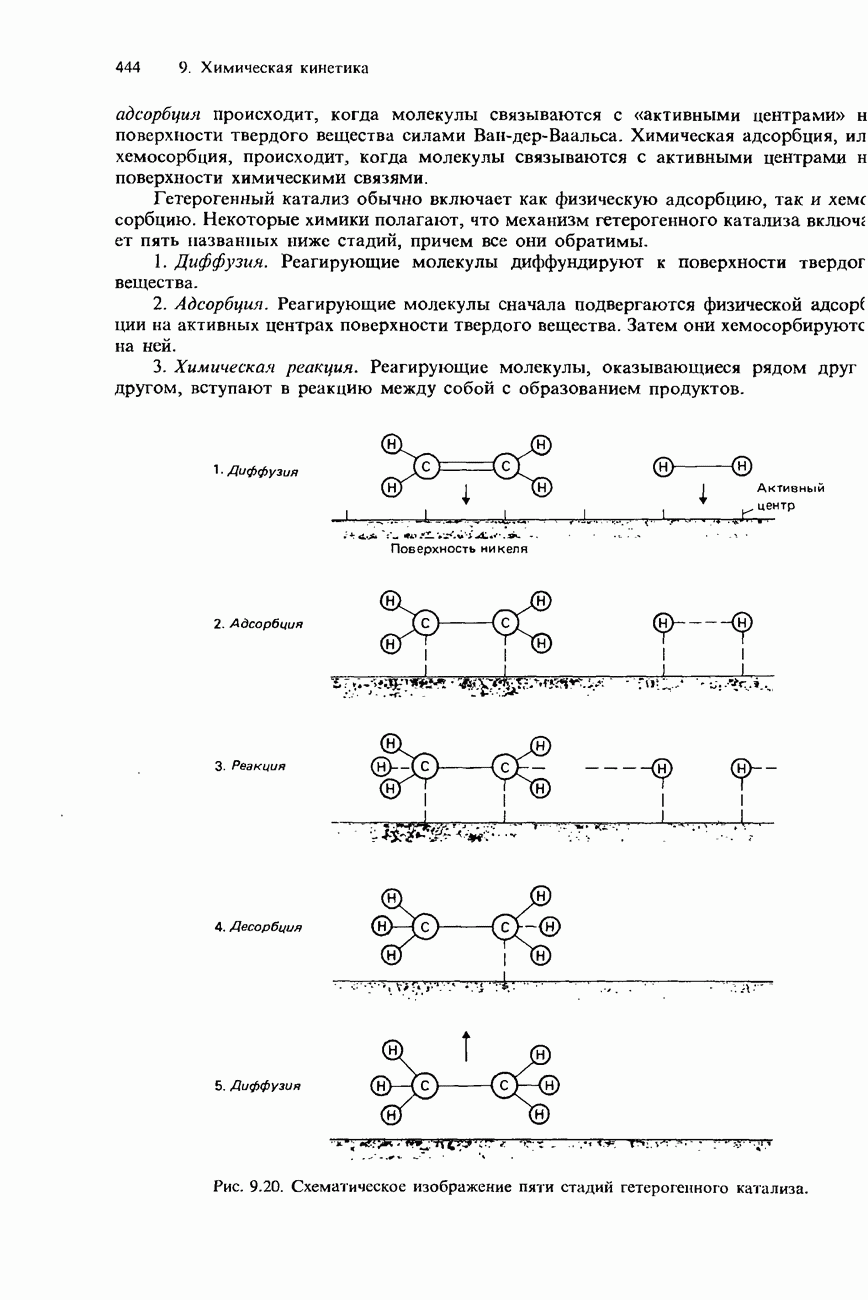
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
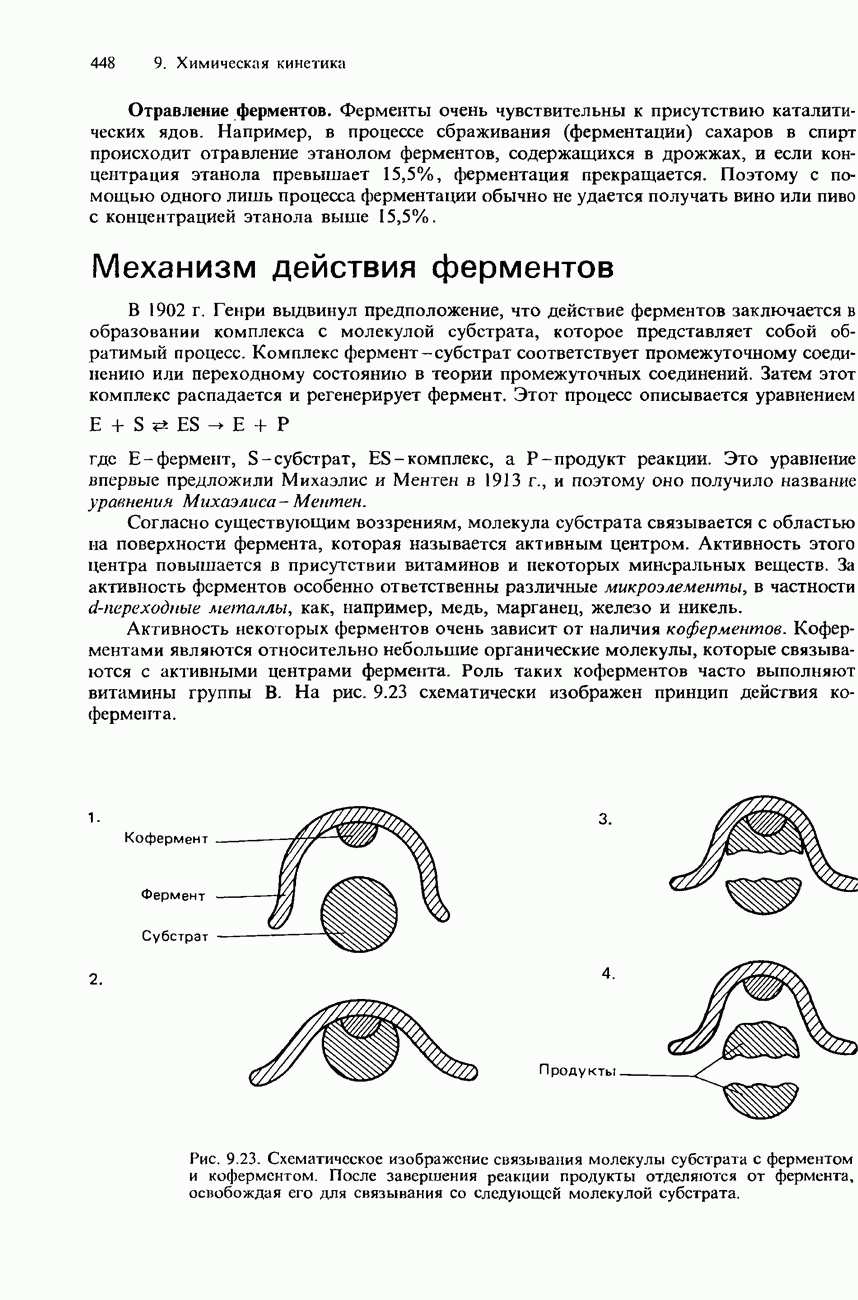
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
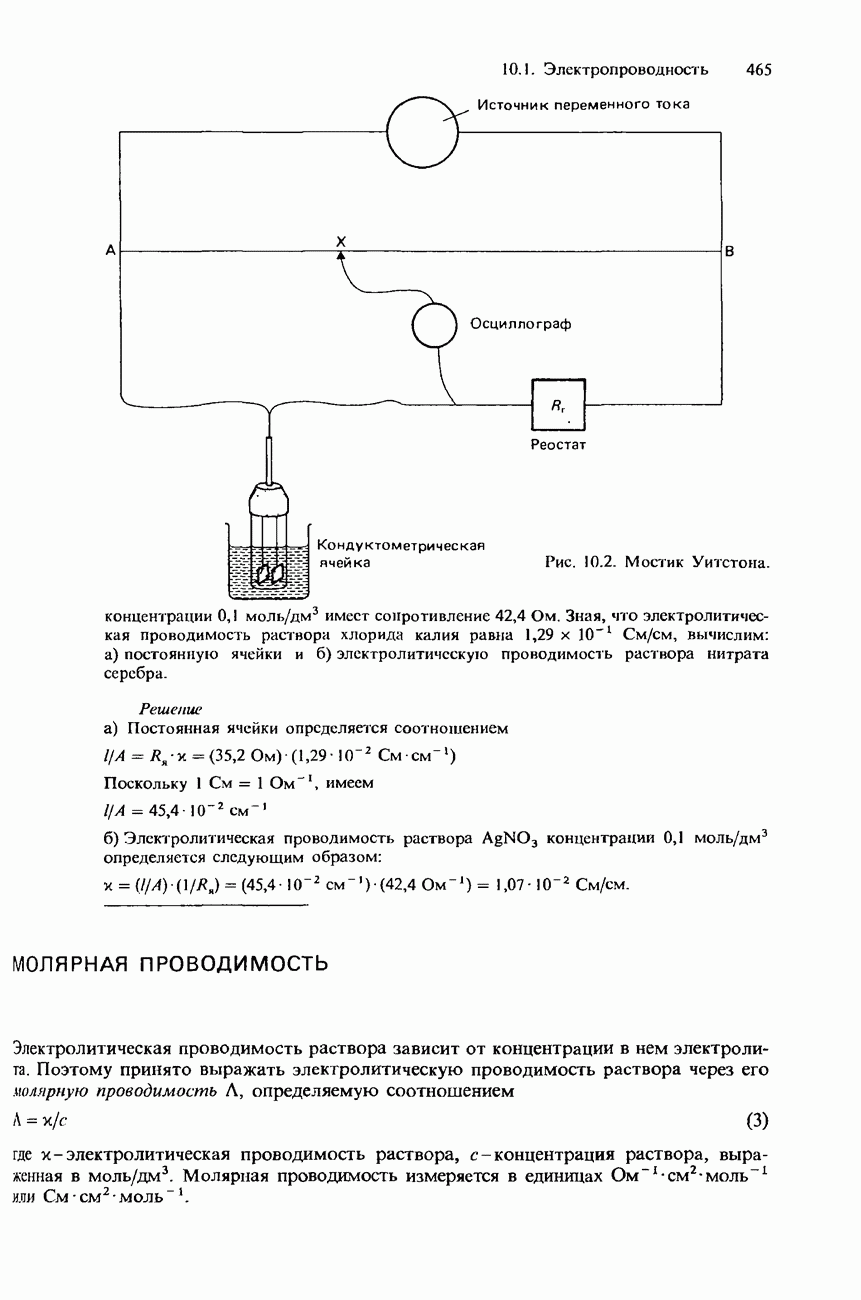
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
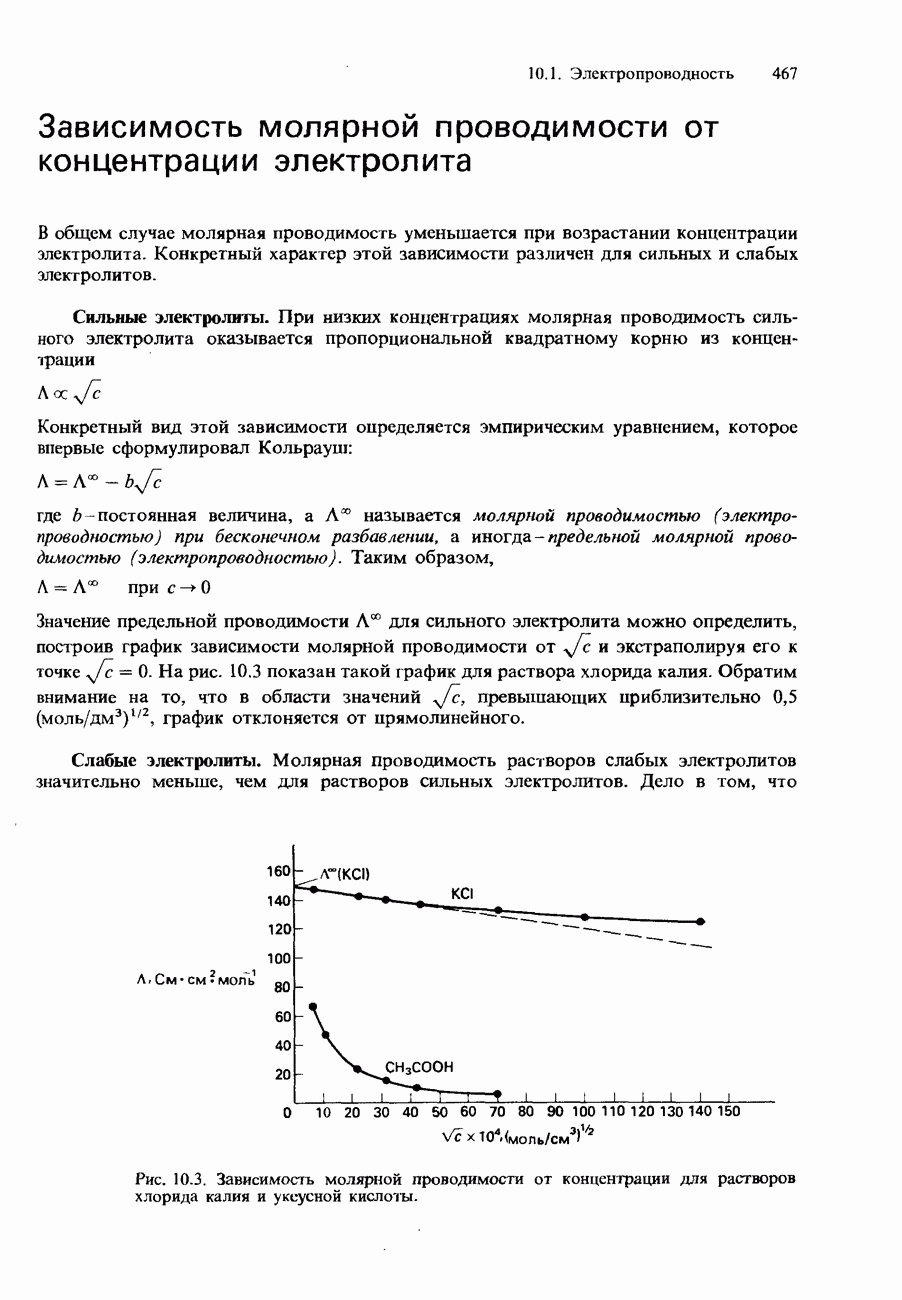
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
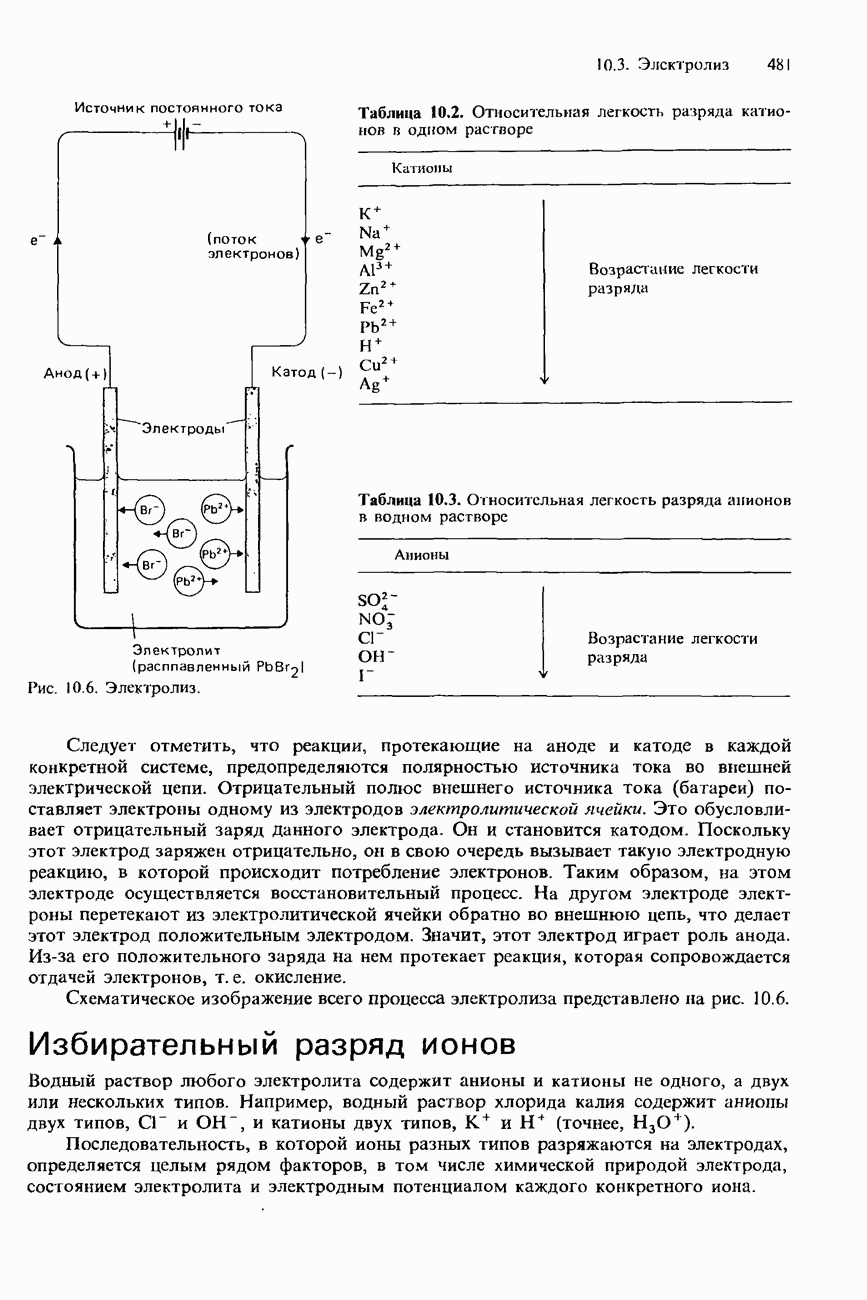
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
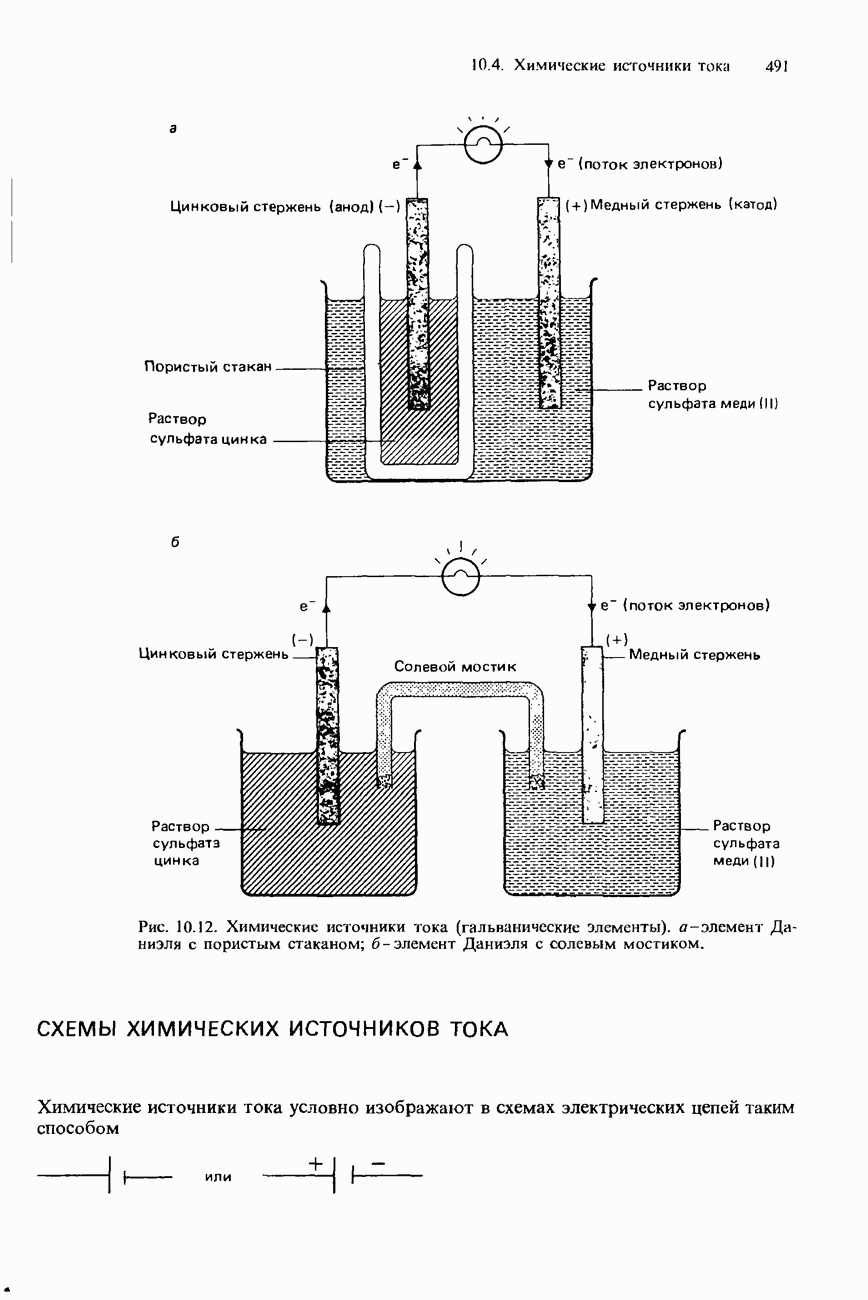
- 10.4. Химические источники тока
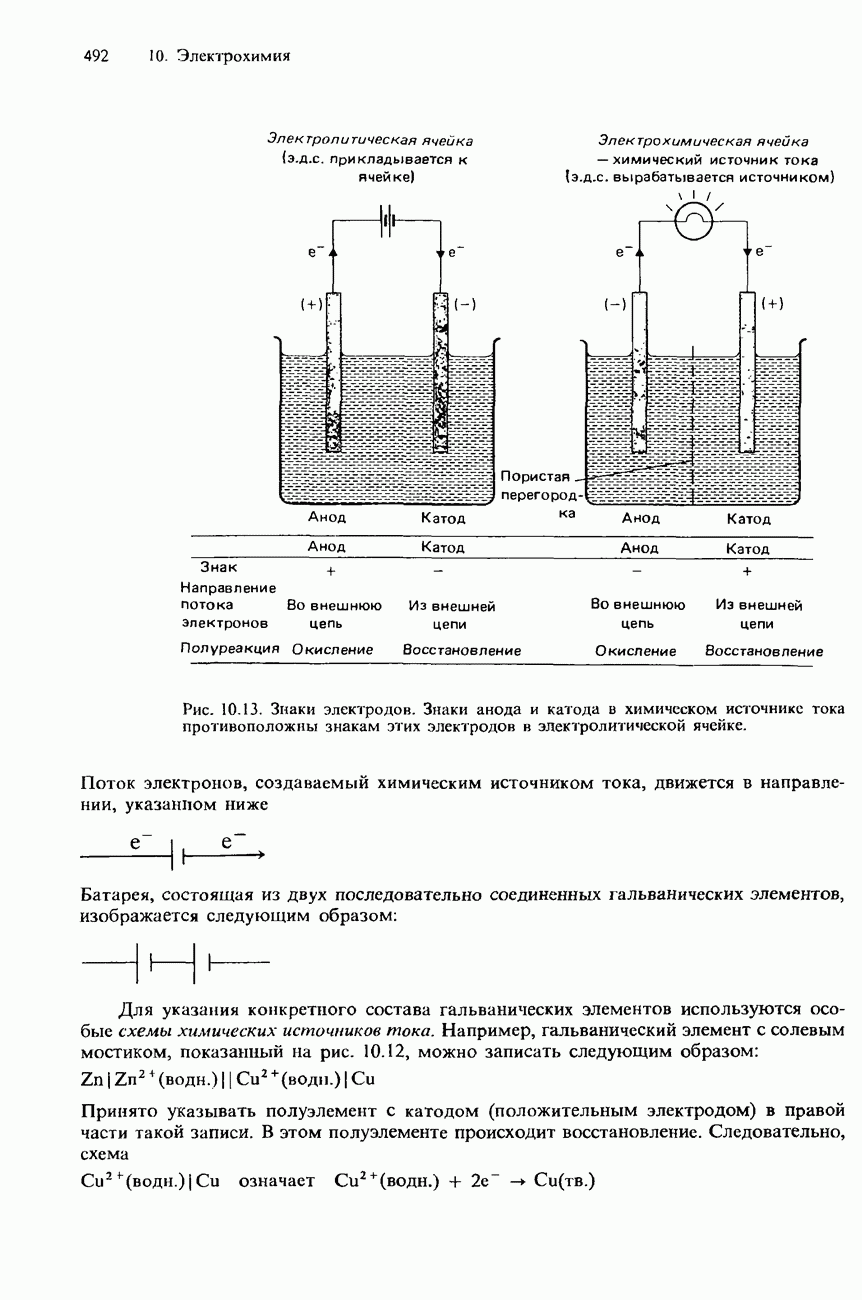
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
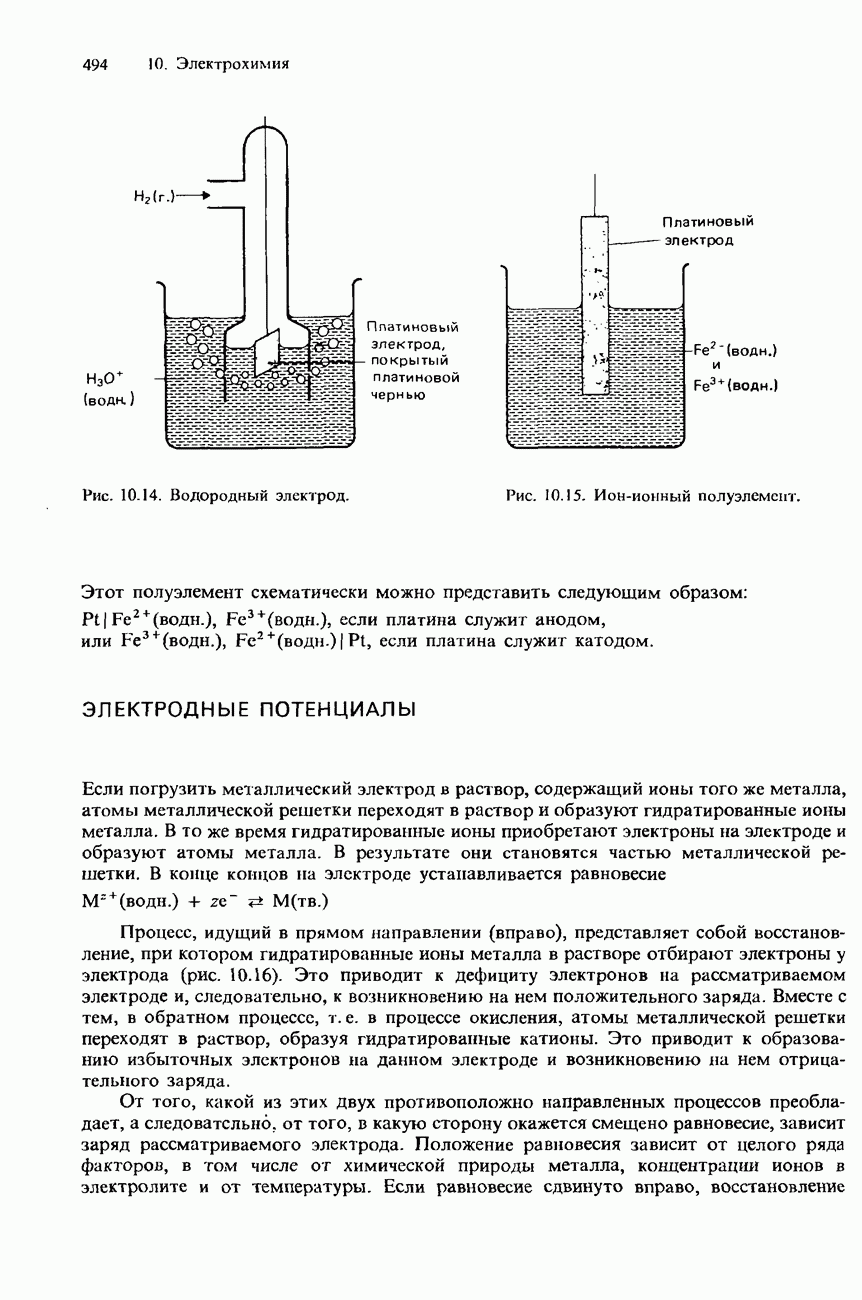
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
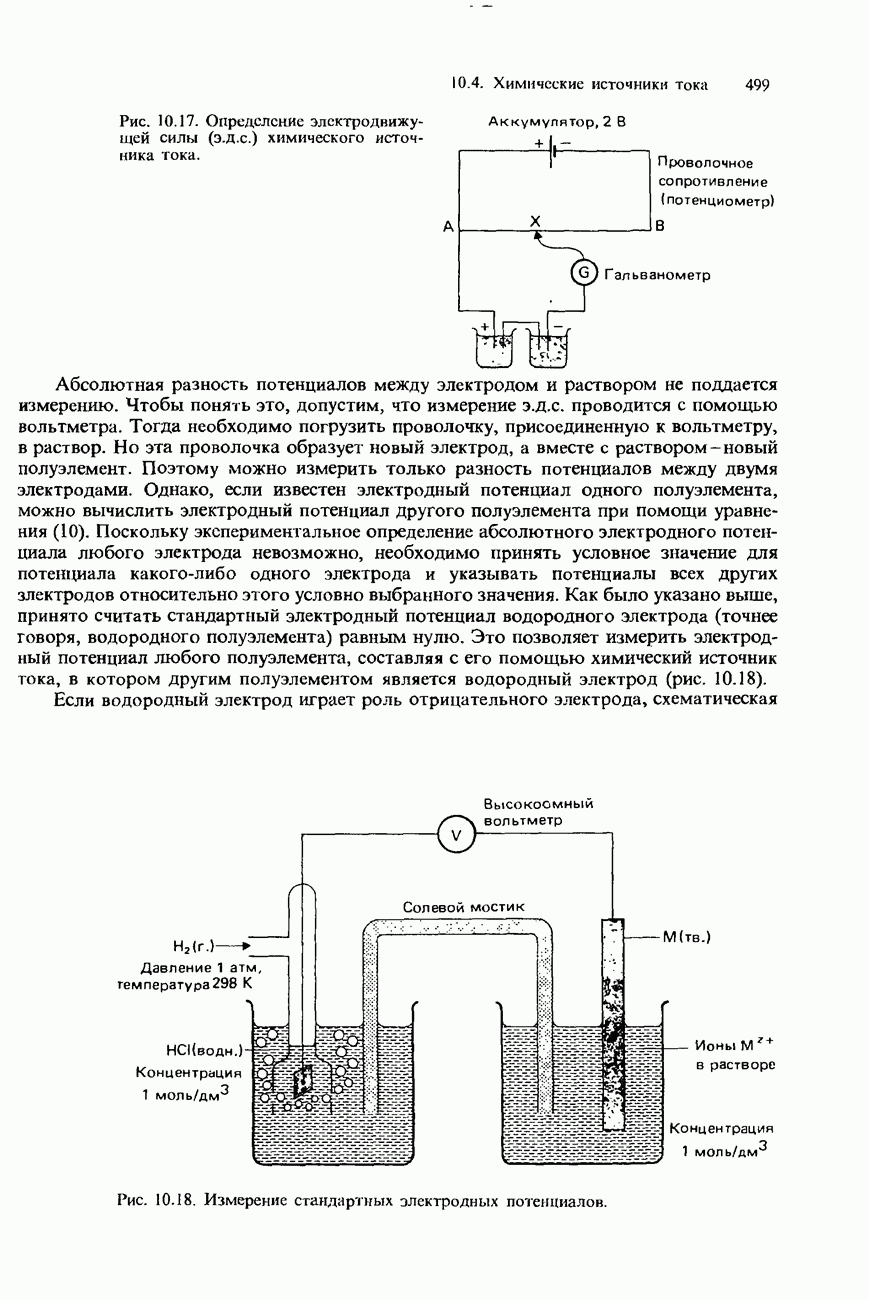
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
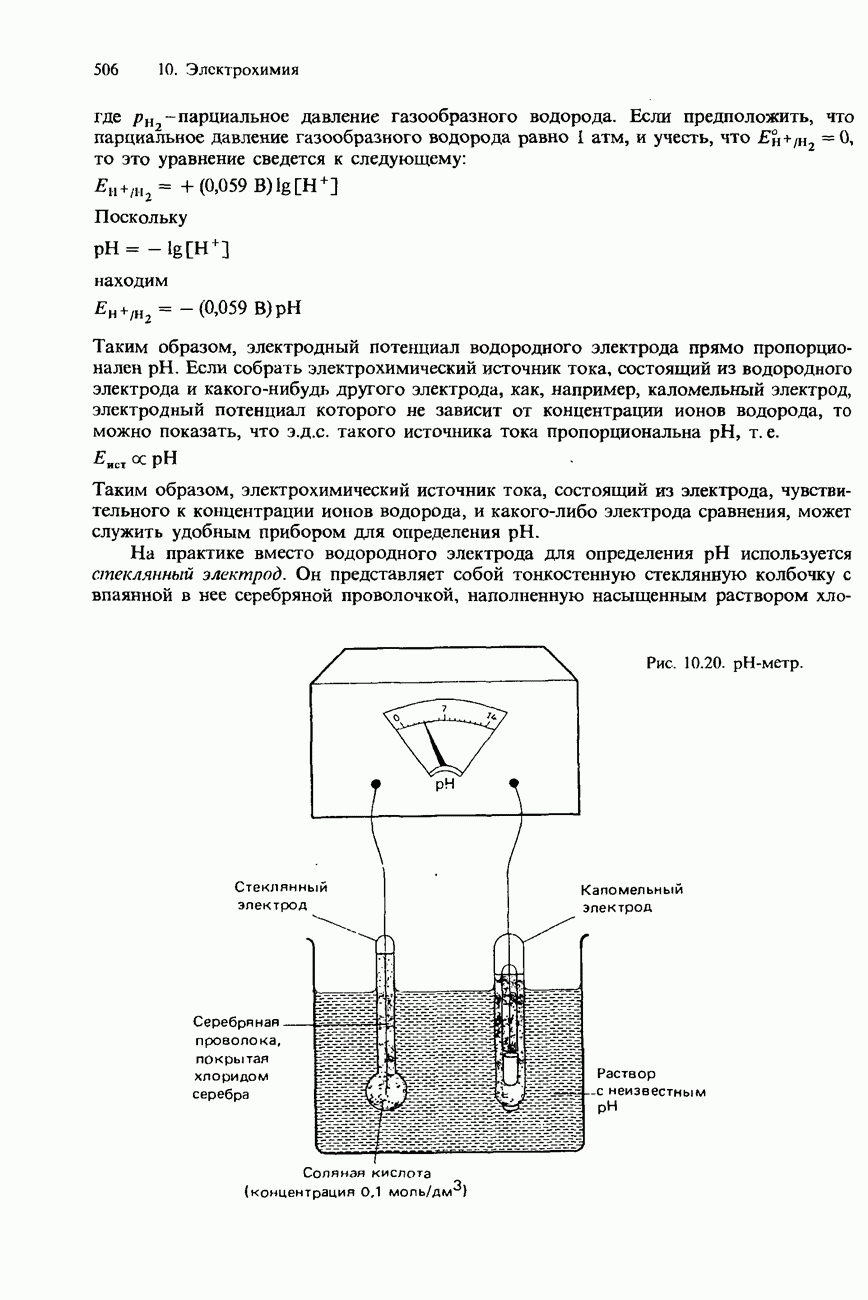
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
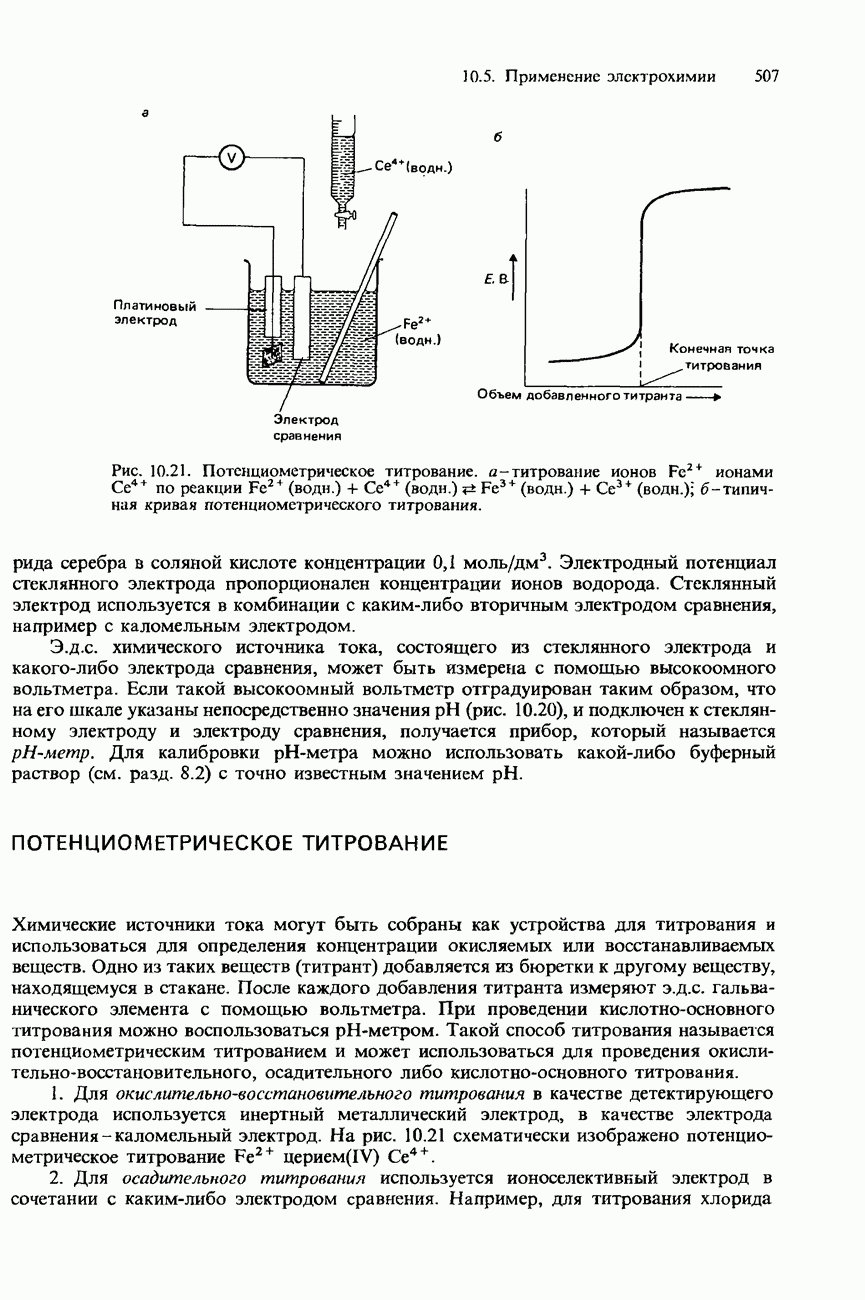
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
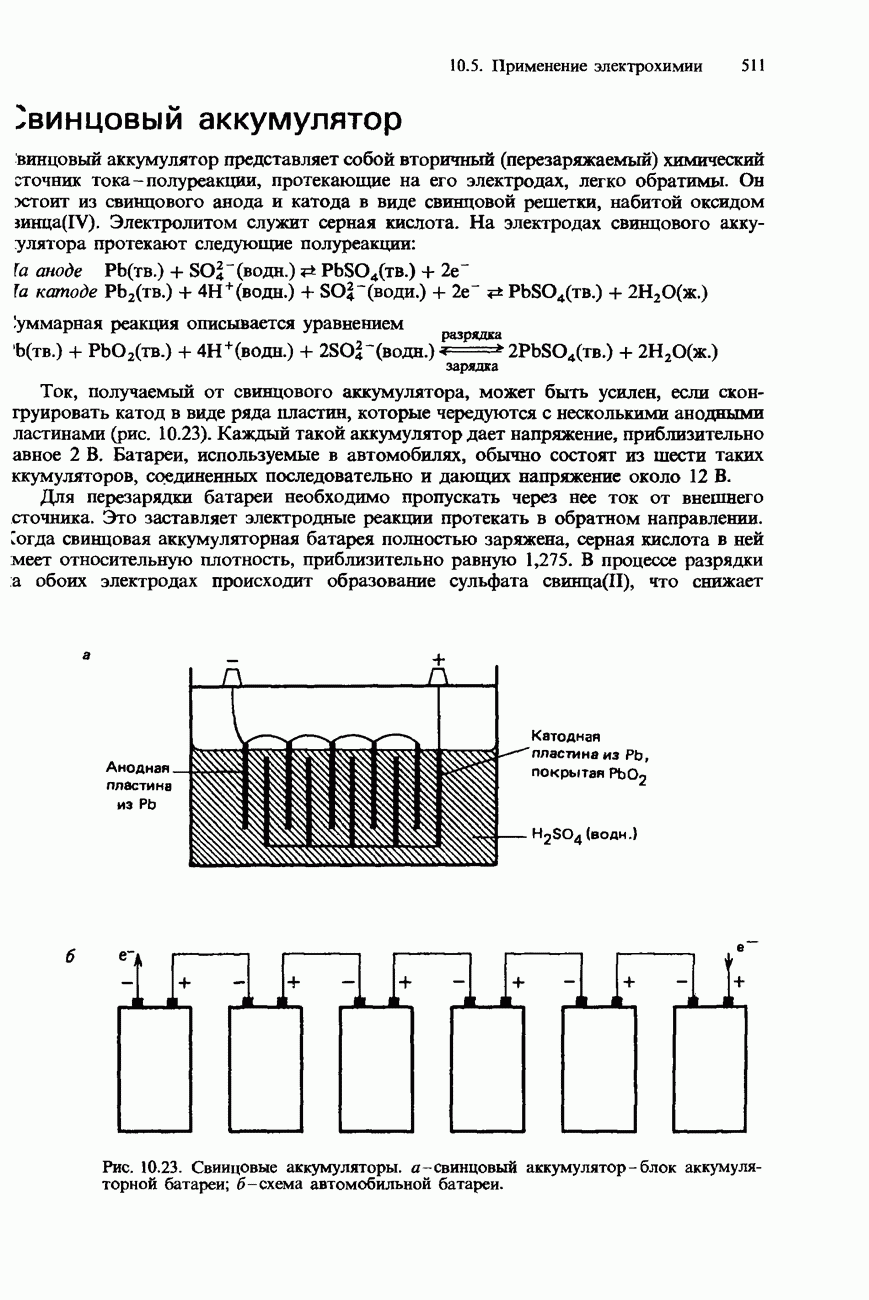
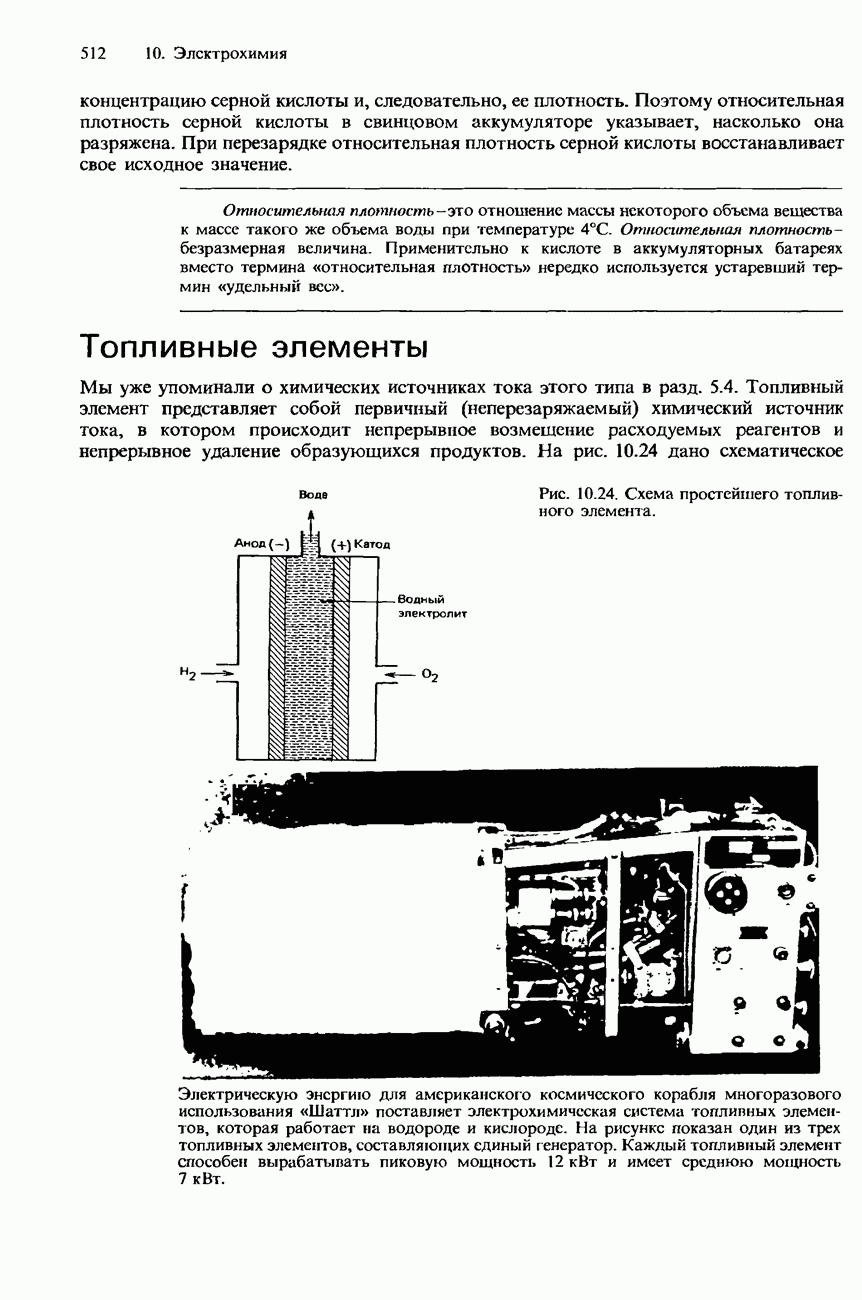
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ