| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОПРОСЫ ДЛЯ ПРОВЕРКИ
1. а) Кратко опишите экспериментальные факты, которые привели к открытию нейтрона.
б) Укажите одно экспериментальное подтверждение волновой природы электрона.
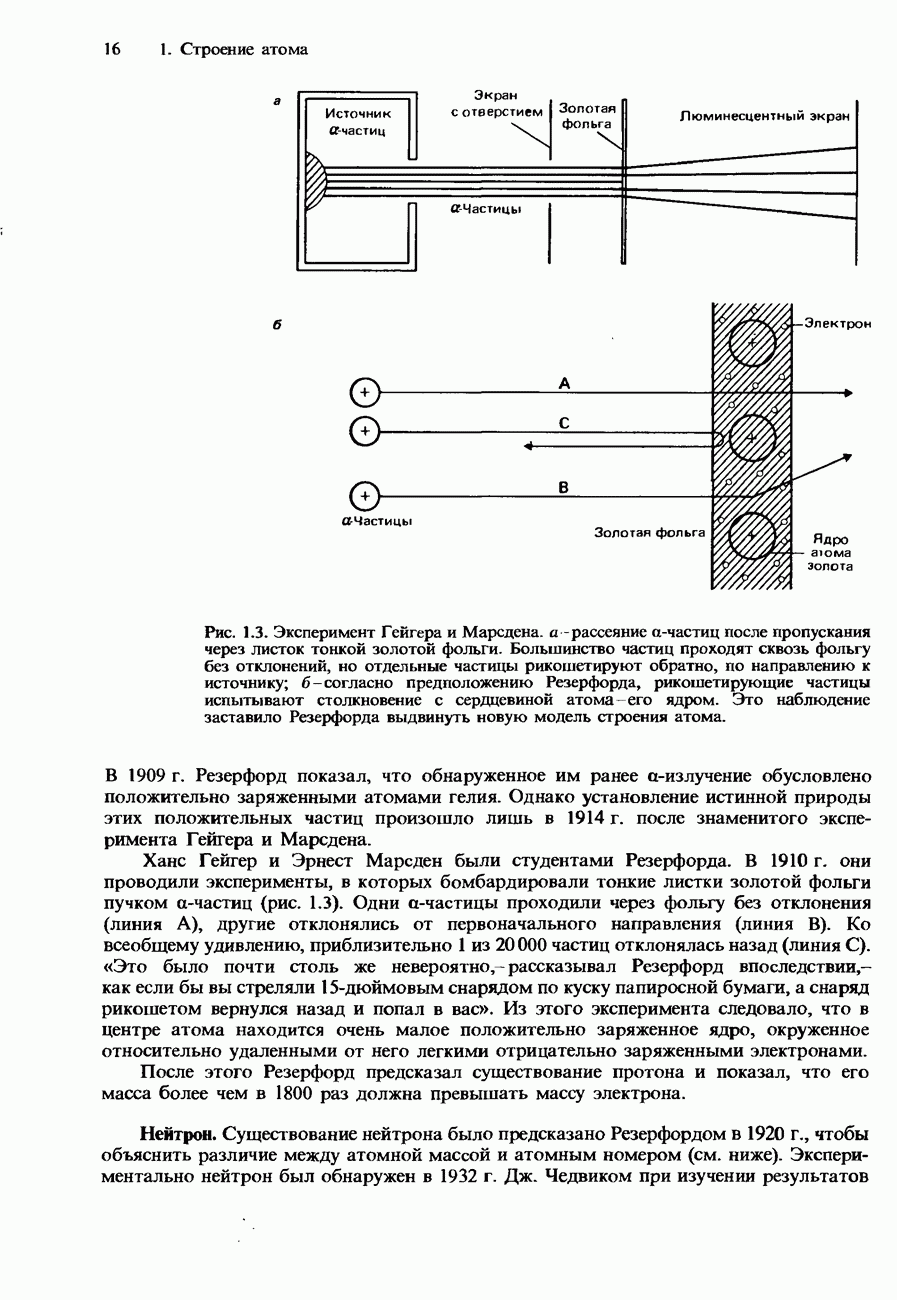
2. В 1909 г. Гейгер и Марсден сообщили о результатах экспериментов, в ходе которых пучок а-частиц направлялся на очень тонкую металлическую фольгу.
Большая часть а-частиц проходила сквозь фольгу без отклонения, но некоторые из них отклонялись от прямолинейной траектории, а очень малая часть отклонялась или рассеивалась назад.
а) Что представляет собой а-частица? Укажите ее массовое число и заряд.
б) Почему большая часть а-частиц не отклонялась от прямолинейной траектории?
в) Почему некоторые а-частицы отклонялись от прямолинейной траектории или даже рассеивались назад?
г) Какие сведения дают эти эксперименты о строении атомов металла?
д) Укажите еще один метод отклонения а-частиц.
е) Радиоактивный распад  происходит с испусканием а-частицы. Запишите уравнение происходящей при этом ядерной реакции.
происходит с испусканием а-частицы. Запишите уравнение происходящей при этом ядерной реакции.
3. Что понимается под следующими терминами: а) относительная атомная масса, б) изотоп?
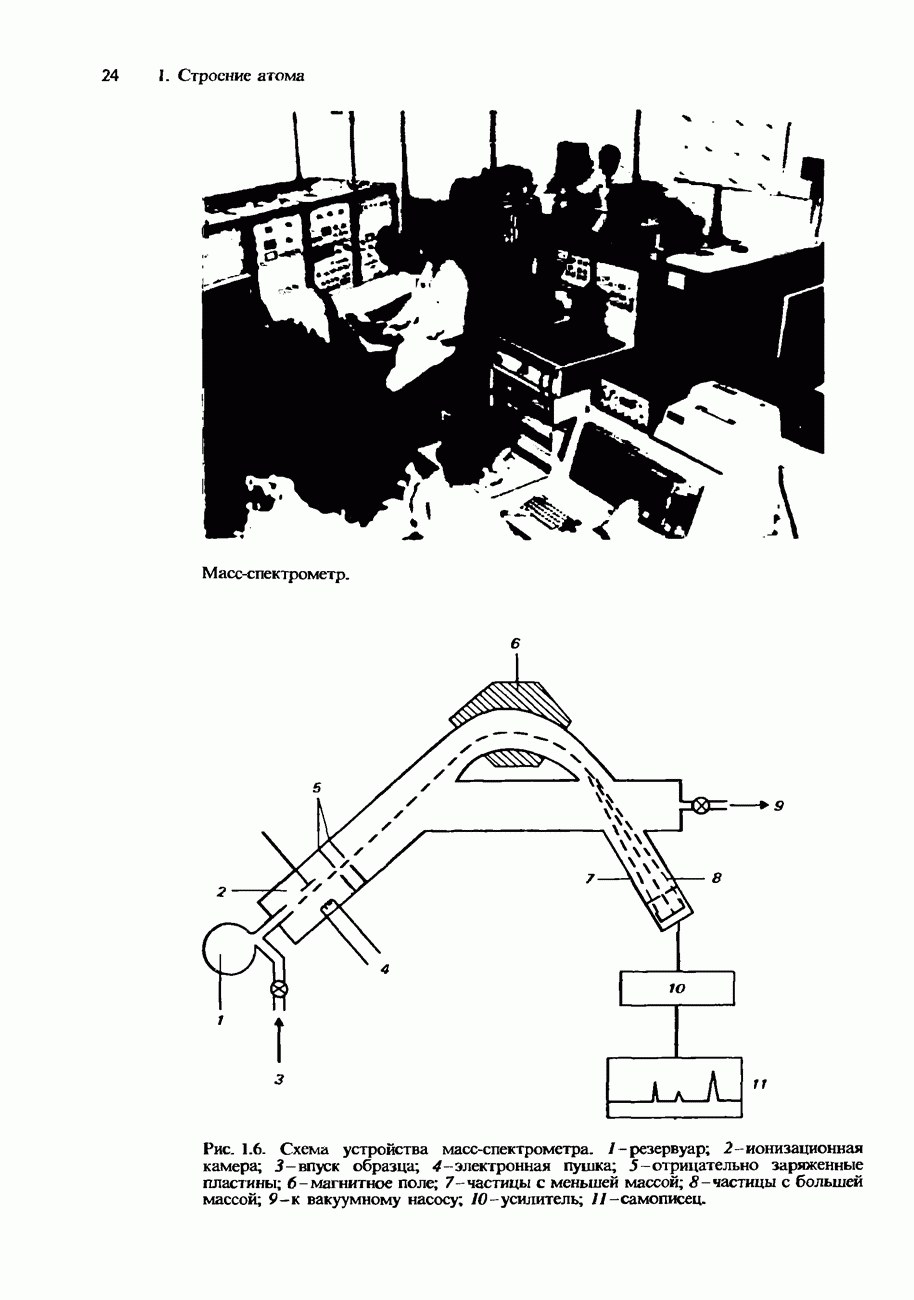
Воспользуйтесь схематическим изображением масс-спектрометра, на котором указаны его важнейшие составные части, и опишите, как используется этот прибор для определении относительных атомных масс.
Масс-спектр этанола содержит пики, соответствующие значениям  равным 15, 28, 31, 45 и 46. Постарайтесь как можно более полно объяснить появление этих пиков.
равным 15, 28, 31, 45 и 46. Постарайтесь как можно более полно объяснить появление этих пиков.
4. а) Нарисуйте схематическое изображение масс-спектрометра с подробным указанием его важнейших составных частей и опишите принцип его действия, б) Высокотоксичный загрязнитель окружающей среды гетрахлородибензодиок-син (TCDD,  ) обнаруживается в образцах почвы даже при столь малой концентрации, как
) обнаруживается в образцах почвы даже при столь малой концентрации, как  млн. д. с помощью масс-спектрометрии, по наличию в масс-спектре молекулярного иона
млн. д. с помощью масс-спектрометрии, по наличию в масс-спектре молекулярного иона  имеющего массовое число 322.
имеющего массовое число 322.

Остаток пестицида (средства для борьбы с сельскохозяйственными вредителями)  который загрязняет образцы почвы, тоже дает в масс-спектре молекулярный ион
который загрязняет образцы почвы, тоже дает в масс-спектре молекулярный ион  с массовым числом 322.
с массовым числом 322.
1) Исходя из предположения, что С, Н и О - практически чистые по изотопному составу элементы, вычислите массовые числа всех молекулярных ионов 
2) Кратко объясните, почему следующие точные значения изотопных масс  не во всех случаях являются целыми числами
не во всех случаях являются целыми числами
3) Какую минимальную разность масс должен различать масс-спектрометр (иными словами, каким должно быть его разрешение), чтобы с его помощью можно было отличить TCDD от DDE по пикам молекулярных ионов с массовыми числами, приблизительно равными 322?
5. а) Поясните смысл следующих терминов: атомный номер; массовое число; изотопы.
б) Относительную атомную массу элемента можно определить как средневзвешенное значение масс всех атомов в образце данного элемента с нормальным изотопным содержанием, выраженных в шкале, по которой масса одного атома изотопа углерода-12 имеет точное значение 12,0000.
Элемент медь имеет относительную атомную массу 63,55 и содержит атомы с массовыми числами 63 и 65.
Вычислите по этим данным процентный состав образца меди с нормальным изотопным содержанием.
в) Хлор содержит изотопы  в отношении
в отношении  а бром содержит изотопы
а бром содержит изотопы  в отношении
в отношении  Исходя из предположения, что углерод содержит только атомы с массовым числом 12, а водород только атомы с массовым числом 1, вычислите возможные значения массы для пиков молекулярных ионов в масс-спектре соединения с формулой
Исходя из предположения, что углерод содержит только атомы с массовым числом 12, а водород только атомы с массовым числом 1, вычислите возможные значения массы для пиков молекулярных ионов в масс-спектре соединения с формулой  и относительные интенсивности этих пиков.
и относительные интенсивности этих пиков.
г) Объясните значение термина дефект массы применительно к атомному ядру.
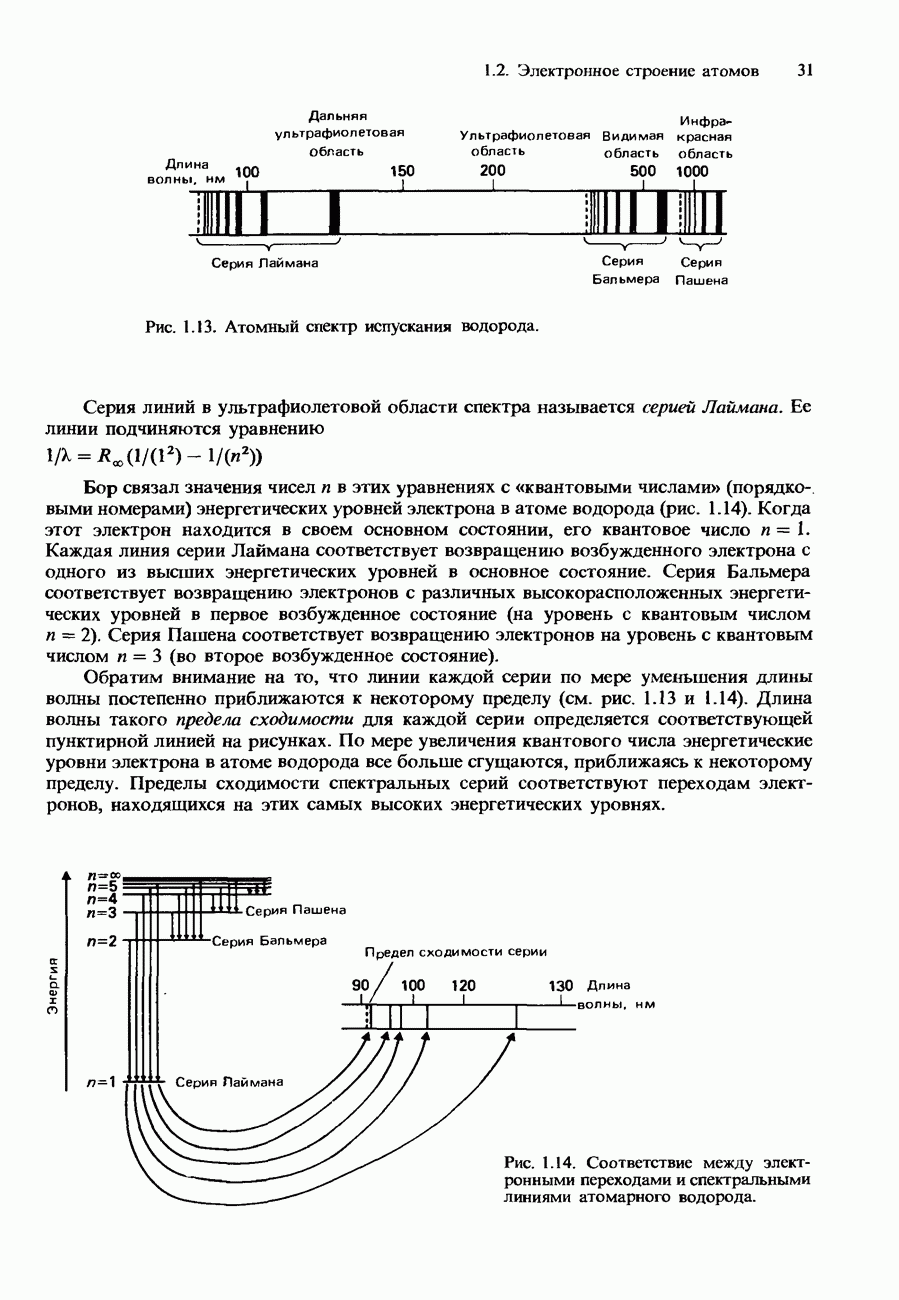
6. а) Оптический спектр атомарного водорода содержит серию линий в ультрафиолетовой области. Расстояние между этими линиями последовательно уменьшается по мере возрастания частоты (т. е. уменьшения длины волны), и в конце концов линии сливаются. Аналогичная серия линий начинается в видимой области спектра. Объясните эти факты.
б) Приведите один пример применения изотопов, который иллюстрирует установление механизма какой-либо органической реакции либо решение какой-либо проблемы, имеющей промышленное или технологическое значение.
в) Элемент бор имеет два изотопа с относительными атомными массами 10,01 и 11,01. Относительные атомные массы природных образцов бора несколько различаются в зависимости от их происхождения. Относительная атомная масса бора, полученного из калифорнийского минерала, имеет значение (найденное химическим способом) 10,84, а бора, полученного из итальянского минерала, - значение 10,82. Вычислите процентное содержание более легкого изотопа в двух указанных образцах бора. Укажите (без подробного объяснения), какой эксперимент следовало бы выполнить, чтобы решить, насколько реально это различие в относительной атомной массе бора из двух образцов.
7. а) Опишите, как выглядит спектр атомарного водорода, и укажите, как можно с его помощью определить энергию ионизации водорода.
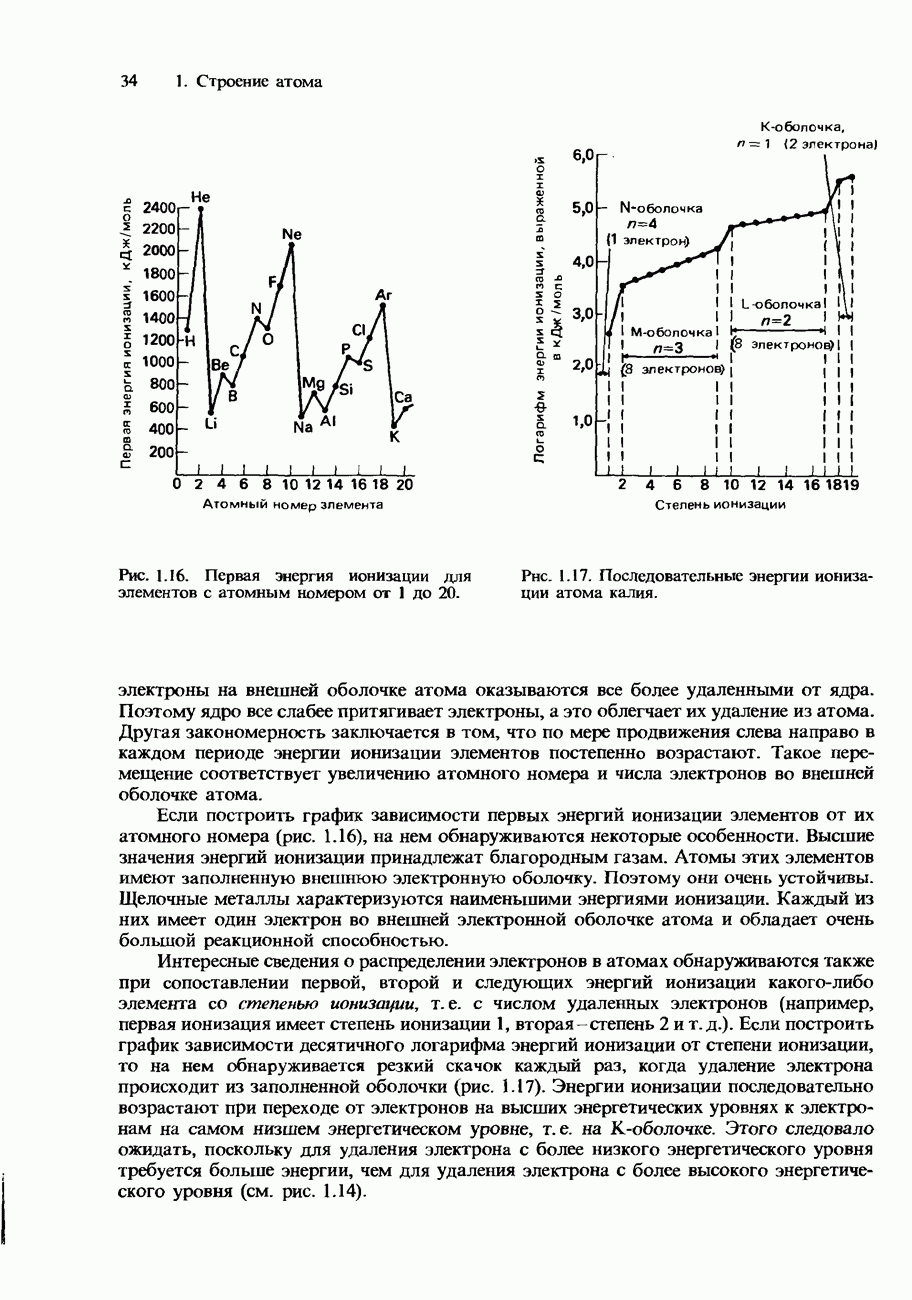
б) Постройте график, показывающий, как изменяются энергии последовательной ионизации углерода в зависимости от числа удаляемых при этом электронов, и объясните форму этого графика.
в) Объясните, как изменения первой энергии ионизации у элементов  периода (при перемещении от
периода (при перемещении от  до
до  ) свидетельствуют о существовании электронных подоболочек.
) свидетельствуют о существовании электронных подоболочек.
г) Укажите, какие изменения первой энергии ионизации происходят у элементов I группы периодической таблицы при перемещении сверху вниз вдоль группы, и объясните причину этих изменений.
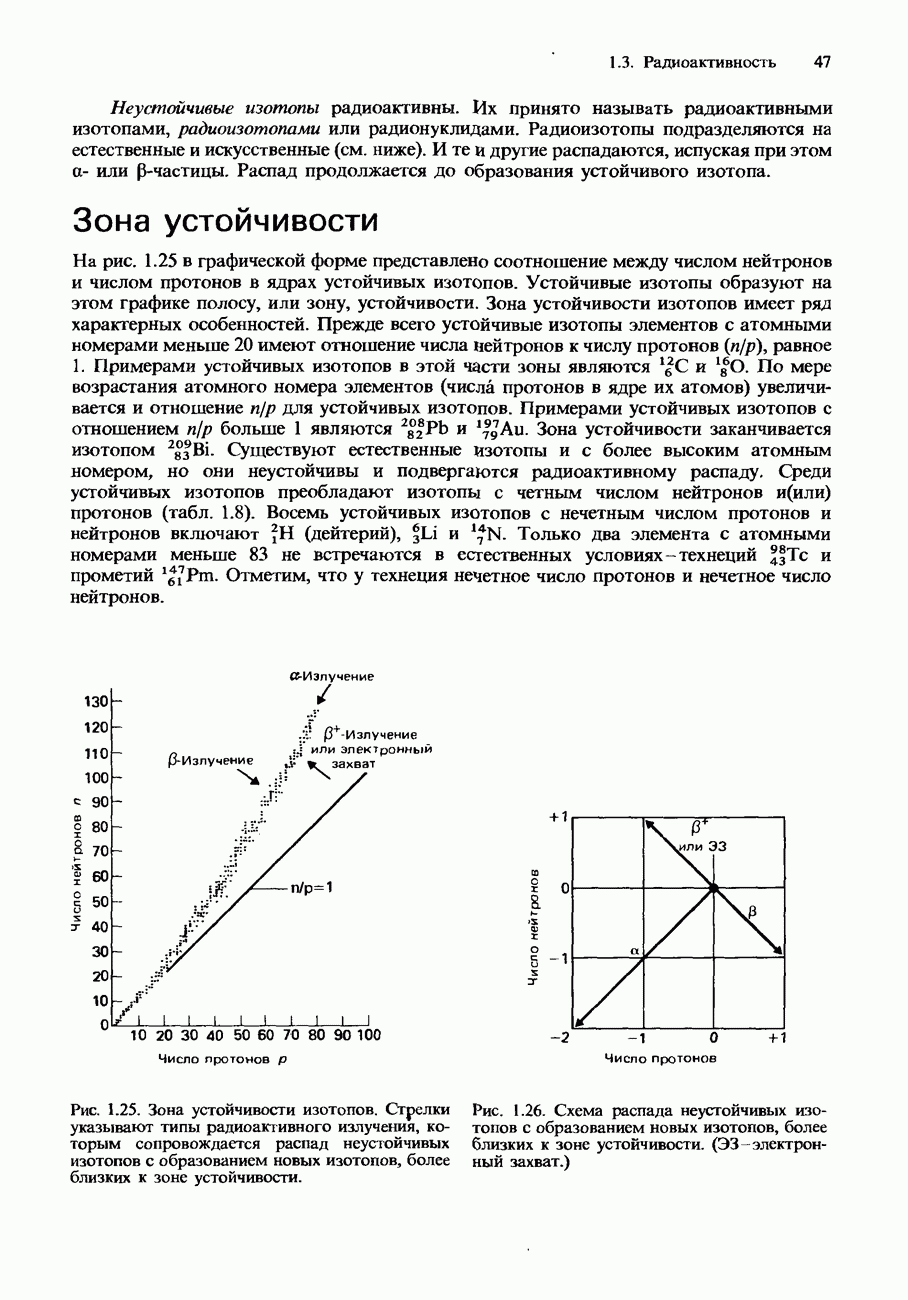
8. а) Опишите явление радиоактивного распада, указав причину и природу радиоактивного излучения, а также используя понятия об изотопах, нейтронно-протонном соотношении и о периоде полураспада.
6) Опишите два способа применения радиоизотопов.
9. а) Укажите три основных типа радиоактивного излучения и опишите их важнейшие свойства.
б) Укажите два примера использования радиоактивности  радиоактивных изотопов и объясните, на каком принципе они основаны.
радиоактивных изотопов и объясните, на каком принципе они основаны.
в) В ряду радиоактивного превращения урана имеются следующие стадии:

1) Какие частицы испускаются на первых двух стадиях?
2) Укажите, какой изотоп X образуется на третьей стадии, если она сопровождается испусканием  -частицы.
-частицы.
3) Какой период полураспада имеет  если его активность по истечении 48 дней уменьшается на
если его активность по истечении 48 дней уменьшается на 
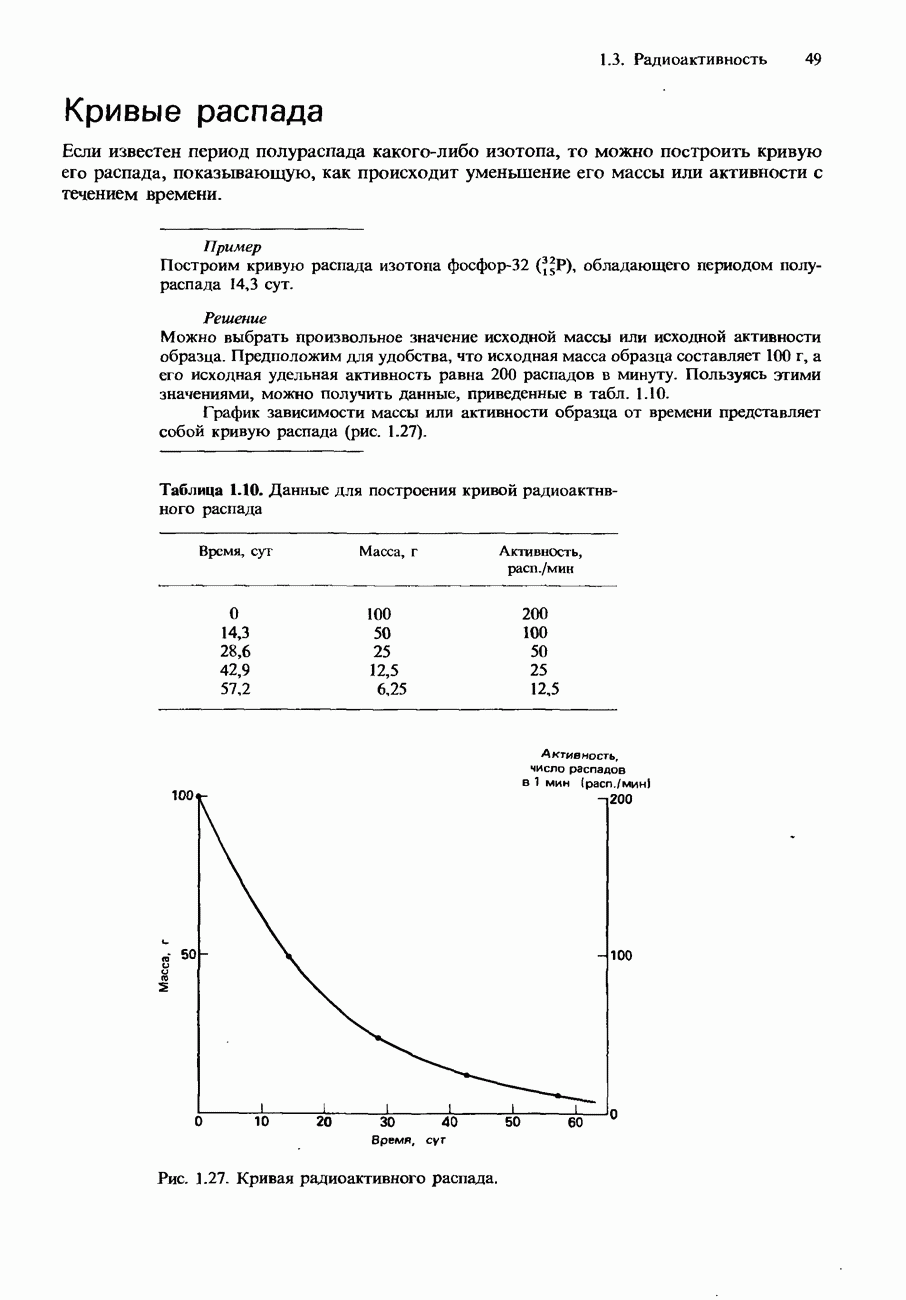
Постройте график распада  пользуясь миллиметровой бумагой и выбрав удобный масштаб; период полураспада
пользуясь миллиметровой бумагой и выбрав удобный масштаб; период полураспада  составляет 1 мин.
составляет 1 мин.
10. а) Укажите, на каких принципах основано определение атомной массы изотопов с помощью масс-спектрометра, б) В несколько сокращенном виде ряд радиоактивного превращения U можно представить следующим образом:

1) Укажите массовое число и атомный номер изотопа X и определите, какому элементу он принадлежит.
2) Укажите, какие частицы и в каком количестве испускаются на стадиях Р и 
3) Вычислите процентный состав (по массе) смеси двух изотопов свинца,  , имеющий среднюю атомную массу 209,32.
, имеющий среднюю атомную массу 209,32.
в) Что представляют собой  -излучение и как ведет себя каждое из них при пропускании:
-излучение и как ведет себя каждое из них при пропускании:
1) через магнитное поле; 2) через бумагу; 3) через газ?
г) Определите, к какому типу относится излучение, обозначенное символами J, К и L, в следующих ядерных превращениях:

В каком из этих превращений испускаемое излучение представляет собой частицы, а в каком - нет?
д) В некотором образце воды отношение числа атомов трития  к числу атомов водорода
к числу атомов водорода  составляло
составляло  Исходя из того что период полураспада трития равен 12,25 лет, вычислите, какое число атомов трития останется в 10 г этой воды по истечении 49 лет.
Исходя из того что период полураспада трития равен 12,25 лет, вычислите, какое число атомов трития останется в 10 г этой воды по истечении 49 лет.
11. а) Допустим, что Р представляет собой радиоизотоп, который подвергается следующим превращениям:

Если атомный номер изотопа Р равен 88, а его массовое число равно 228, то каковы атомный номер и массовое число изотопа S? б) Укажите, одинаков ли период полураспада у двух образцов каждой указанной ниже пары:

12. а) Что следует вписать вместо  и z в уравнениях следующих ядерных реакций?
и z в уравнениях следующих ядерных реакций?

б) Период полураспада изотопа свинца с массовым числом 210 равен 21 году. Спустя какое время после получения образца этого изотопа в нем останется лишь восьмая часть его исходной массы?
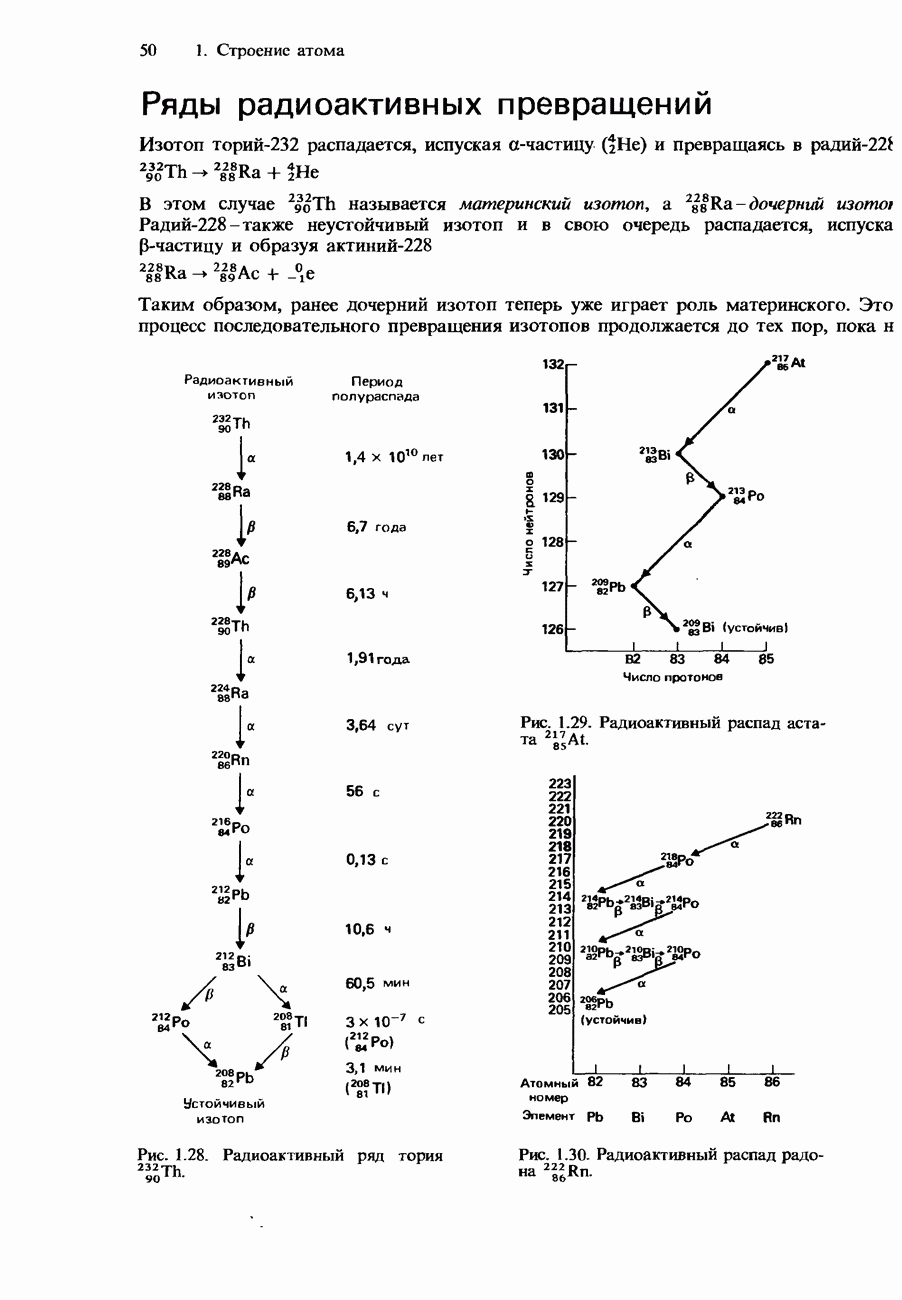
в) Радиоактивный изотоп элемента тория с массовым числом 232 и атомным номером 90 распадается, испуская а-излучение и превращаясь в элемент X, который затем испускает р-частицу и превращается в элемент Y; последний в свою очередь также теряет р-частицу и образует элемент Z. Каковы массовое число и атомный номер элемента 
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
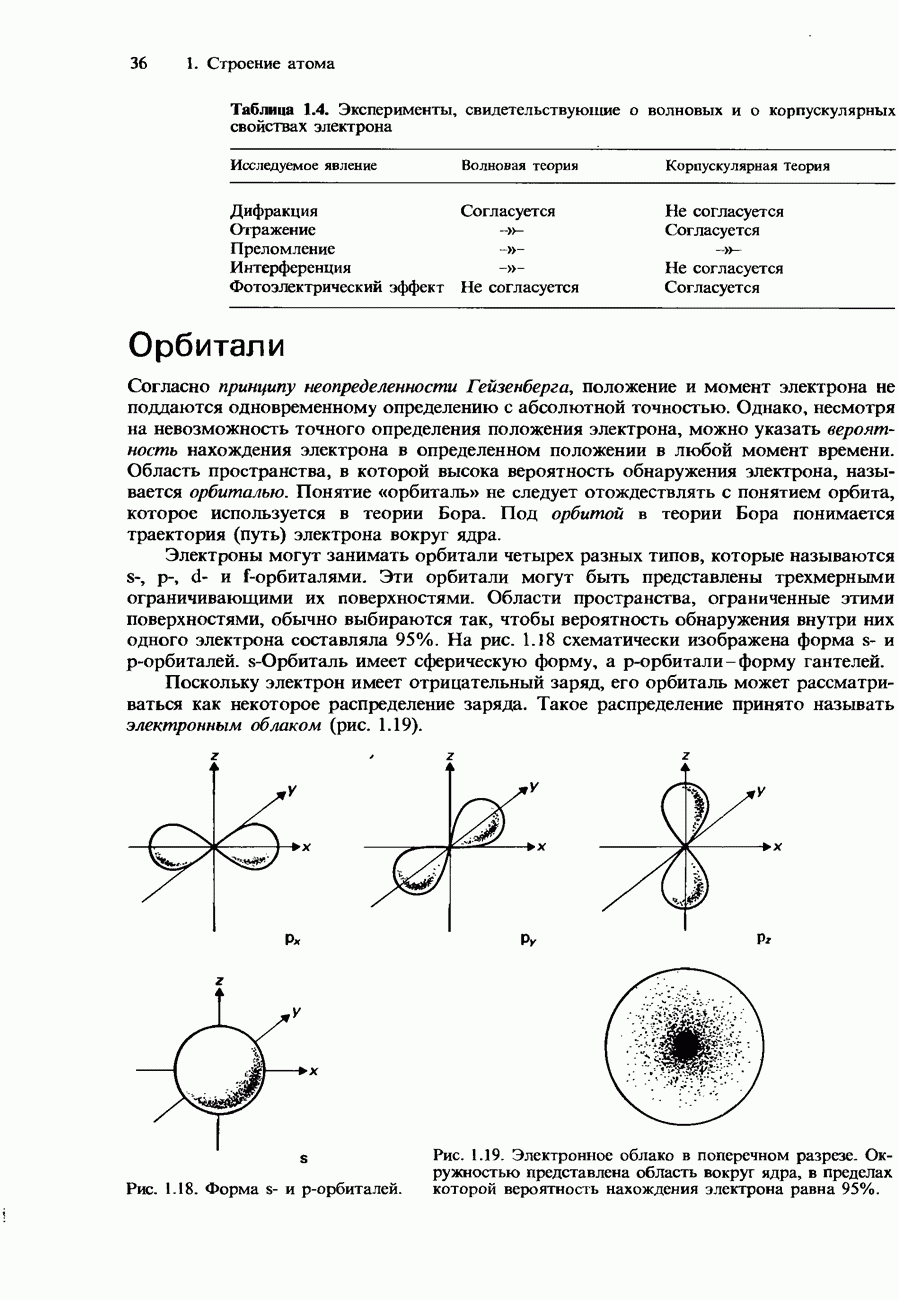
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
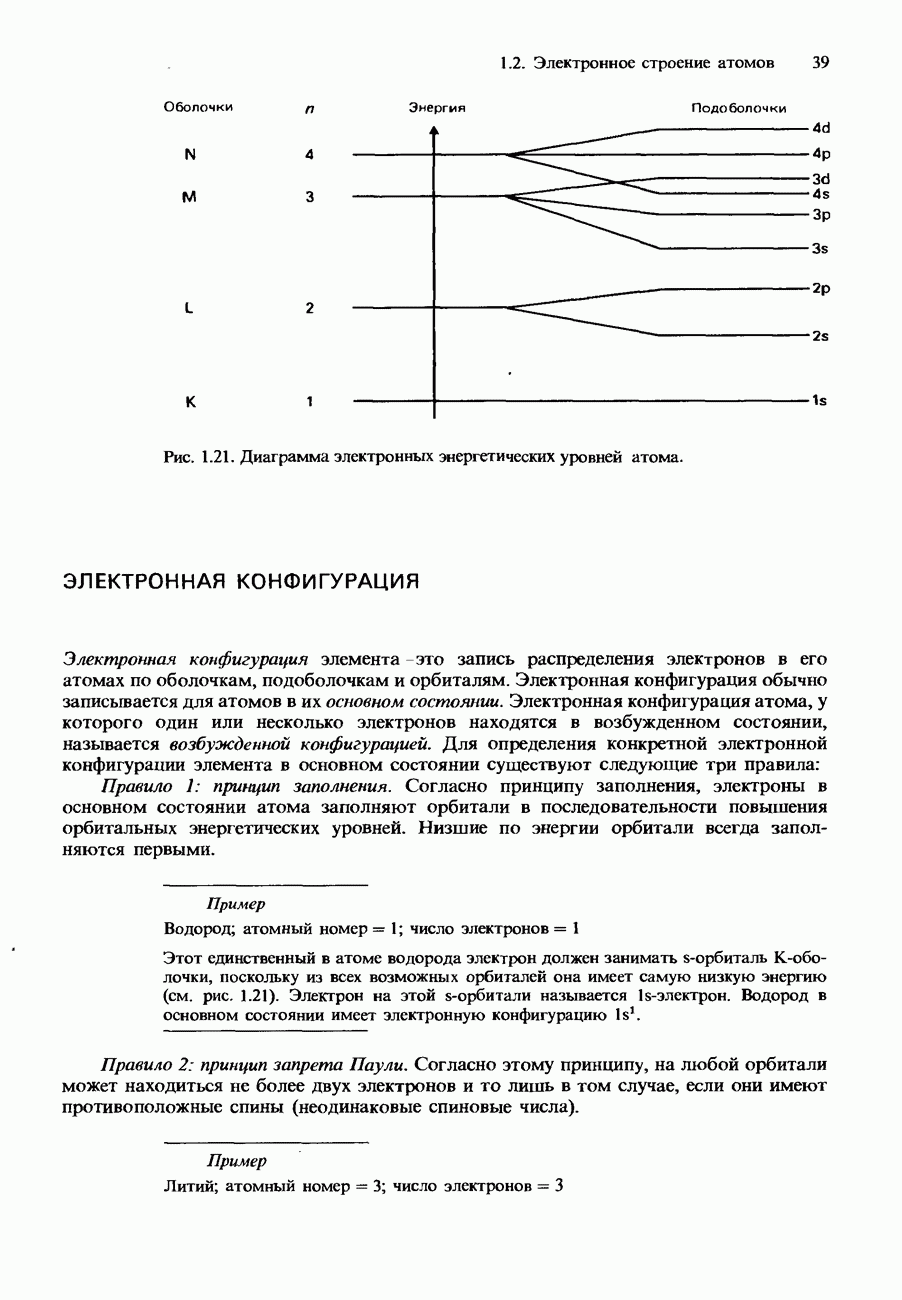
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
- Кривые распада
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
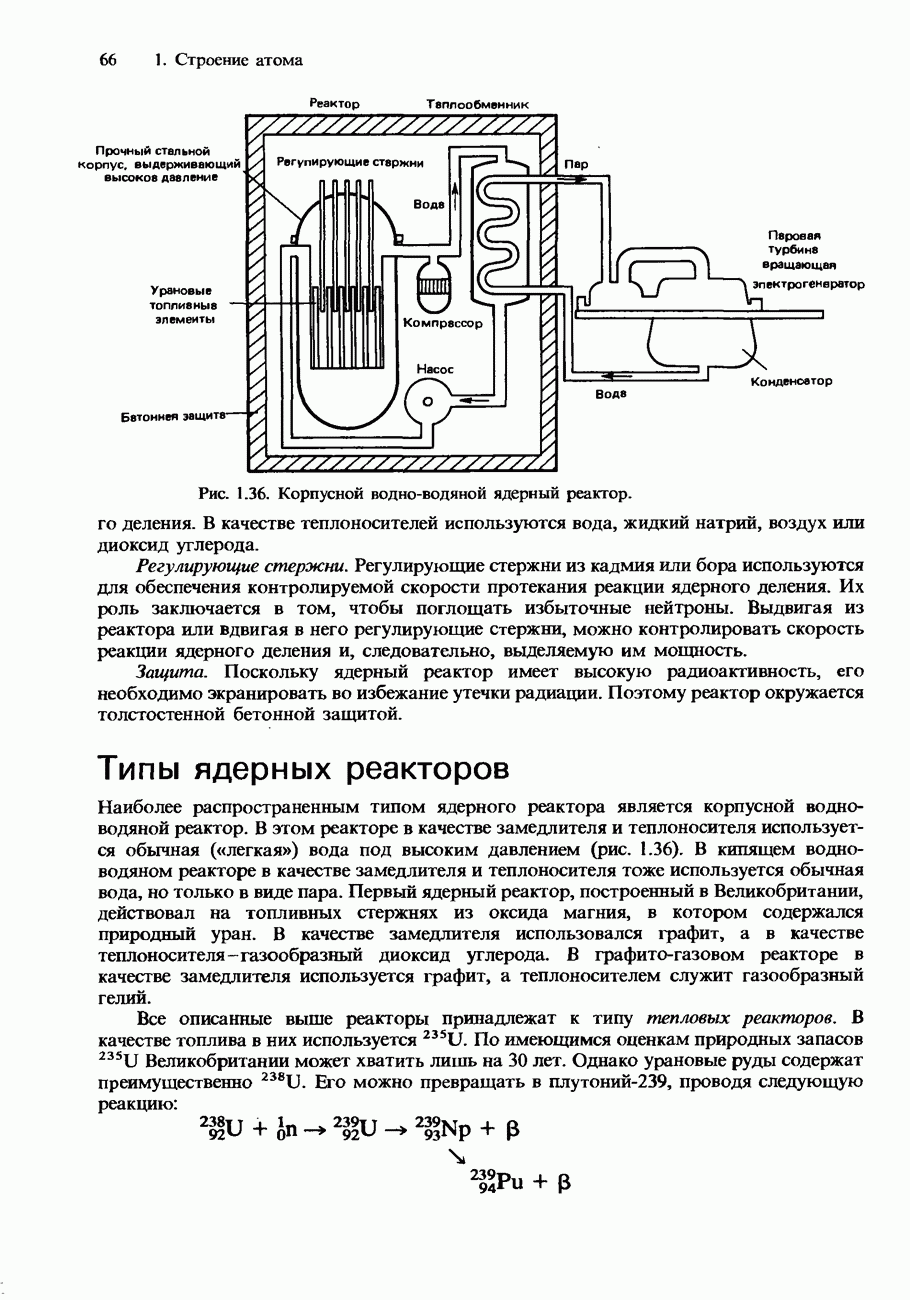
- Типы ядерных реакторов
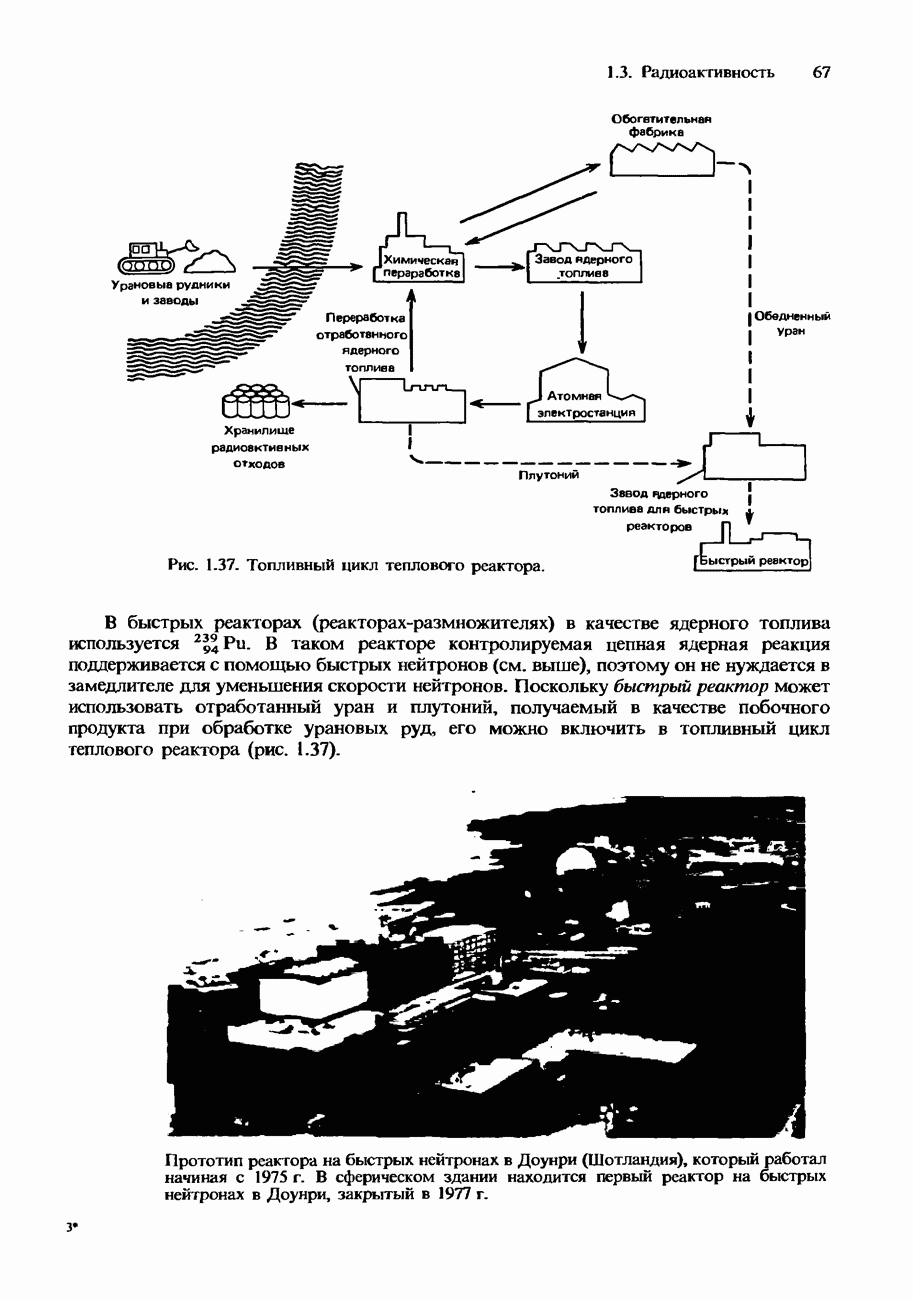
- Радиоактивные ядерные отходы и их переработка
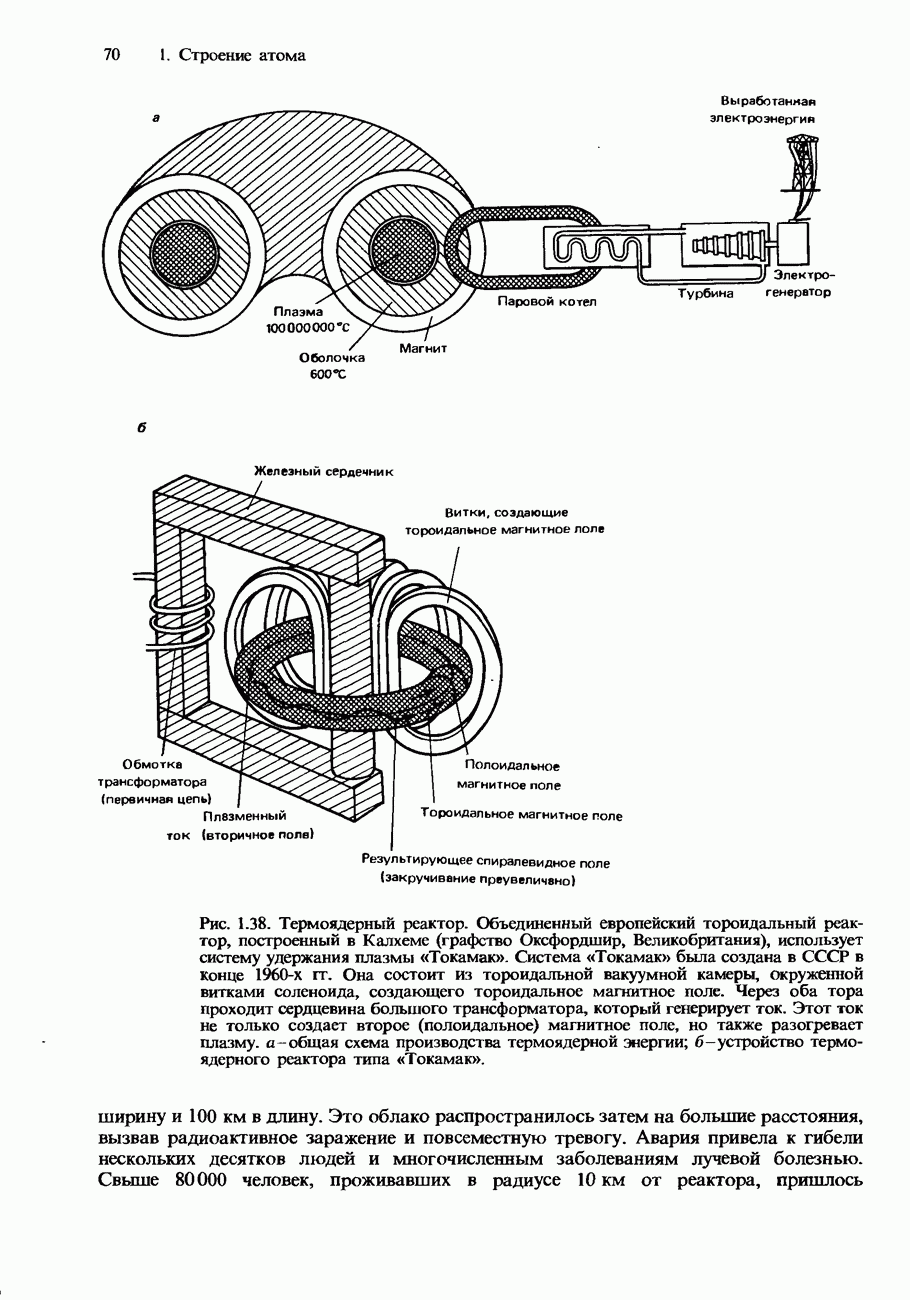
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
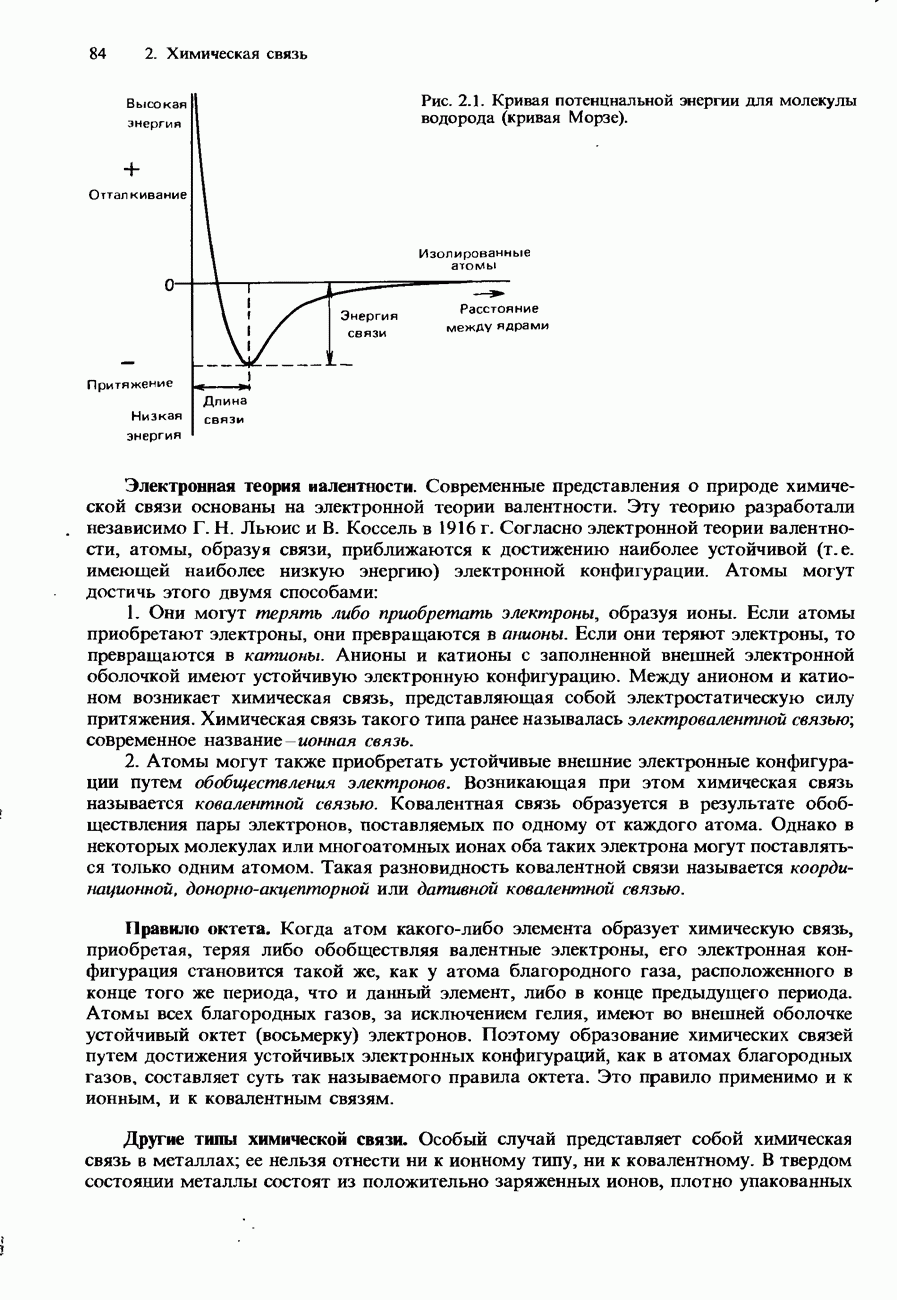
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
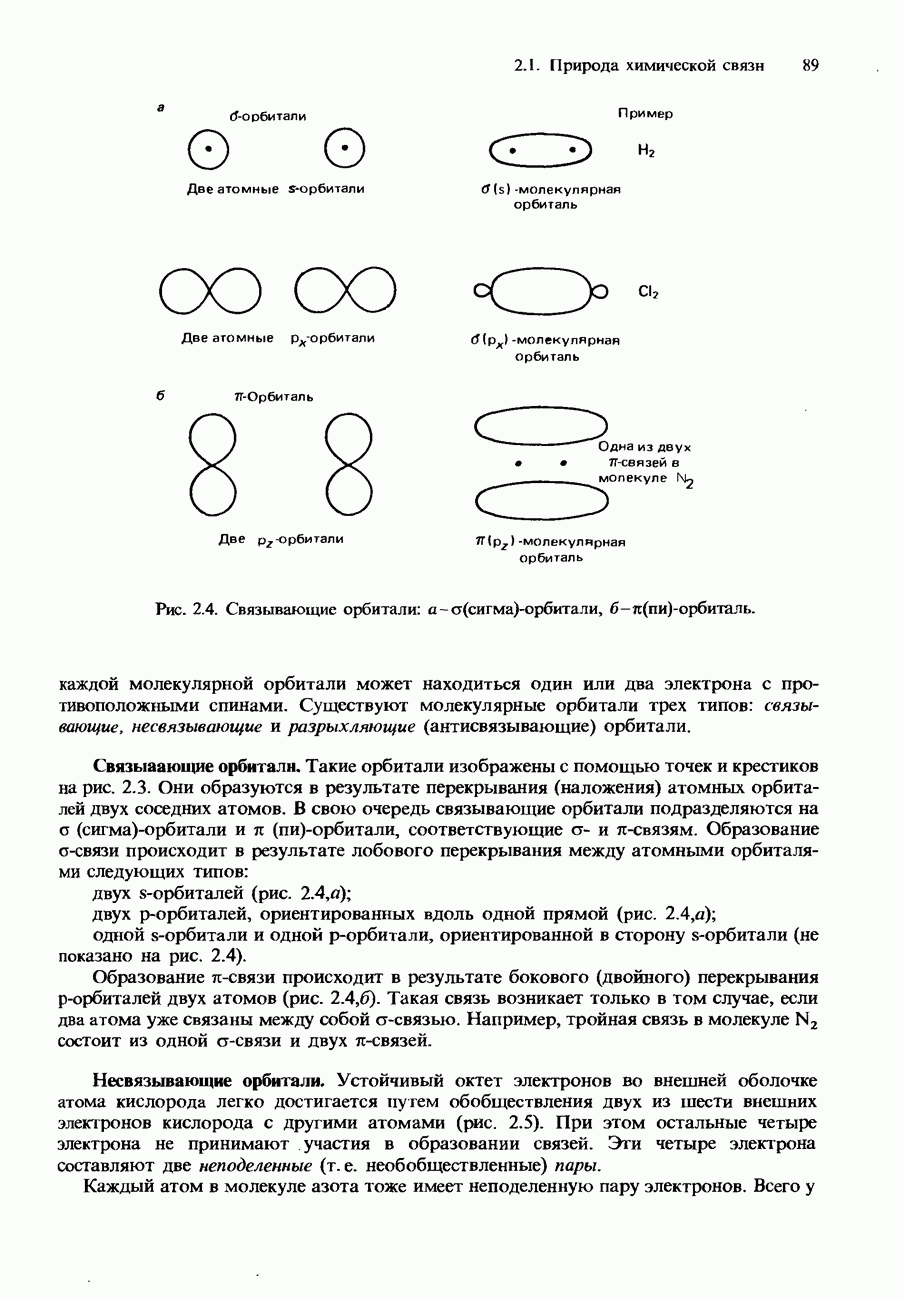
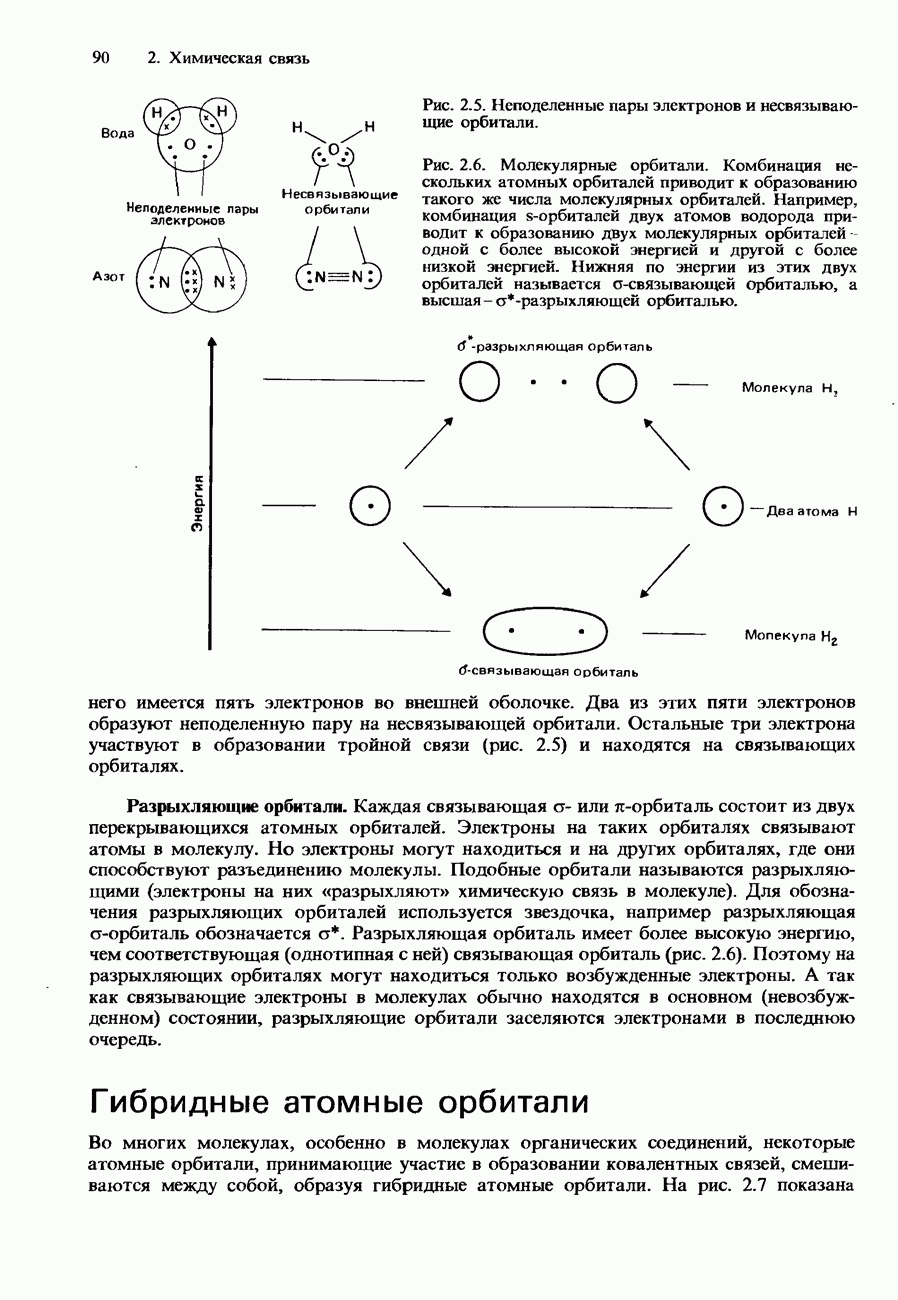
- Молекулярные орбитали
- Гибридные атомные орбитали
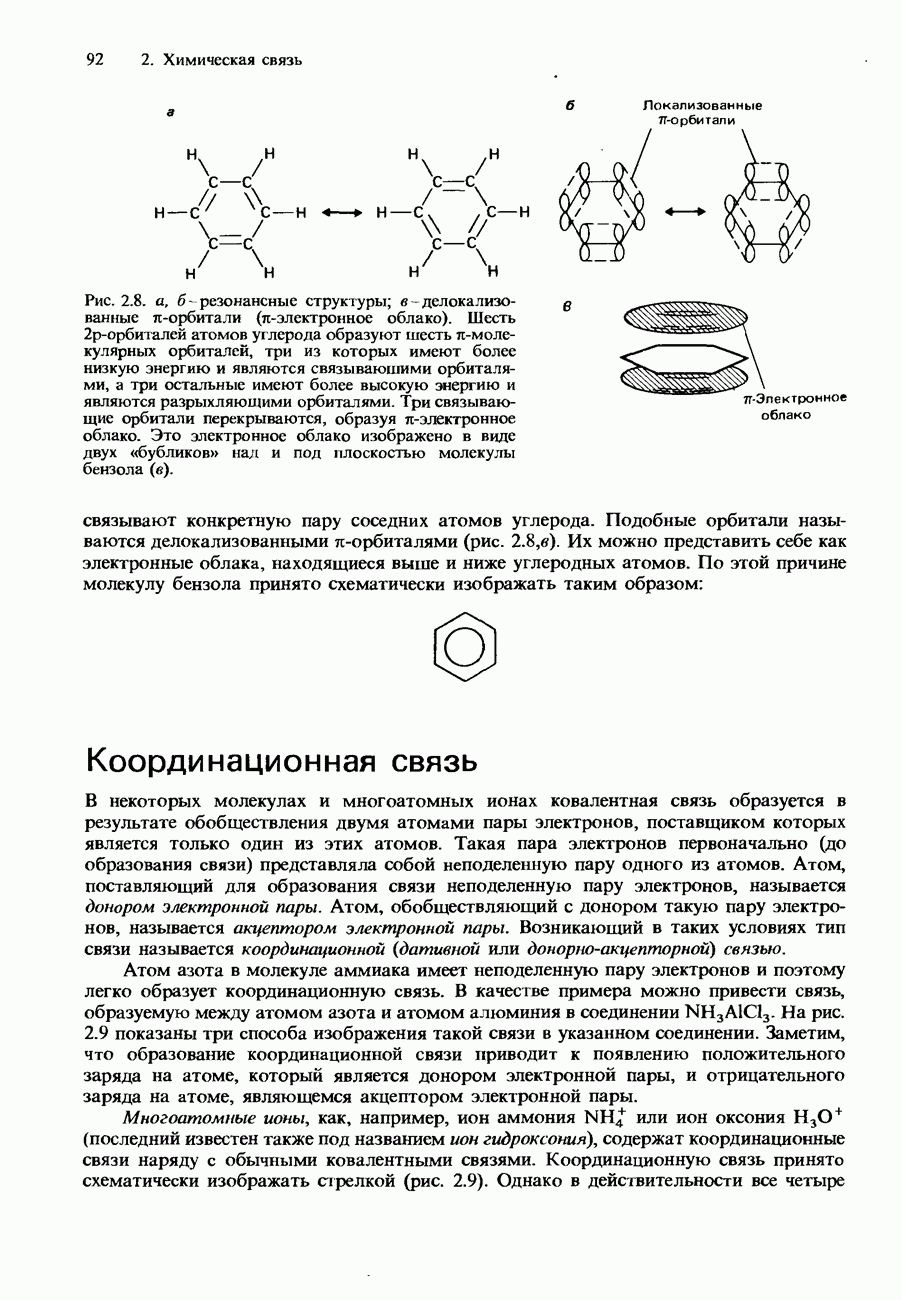
- Делокализованные орбитали
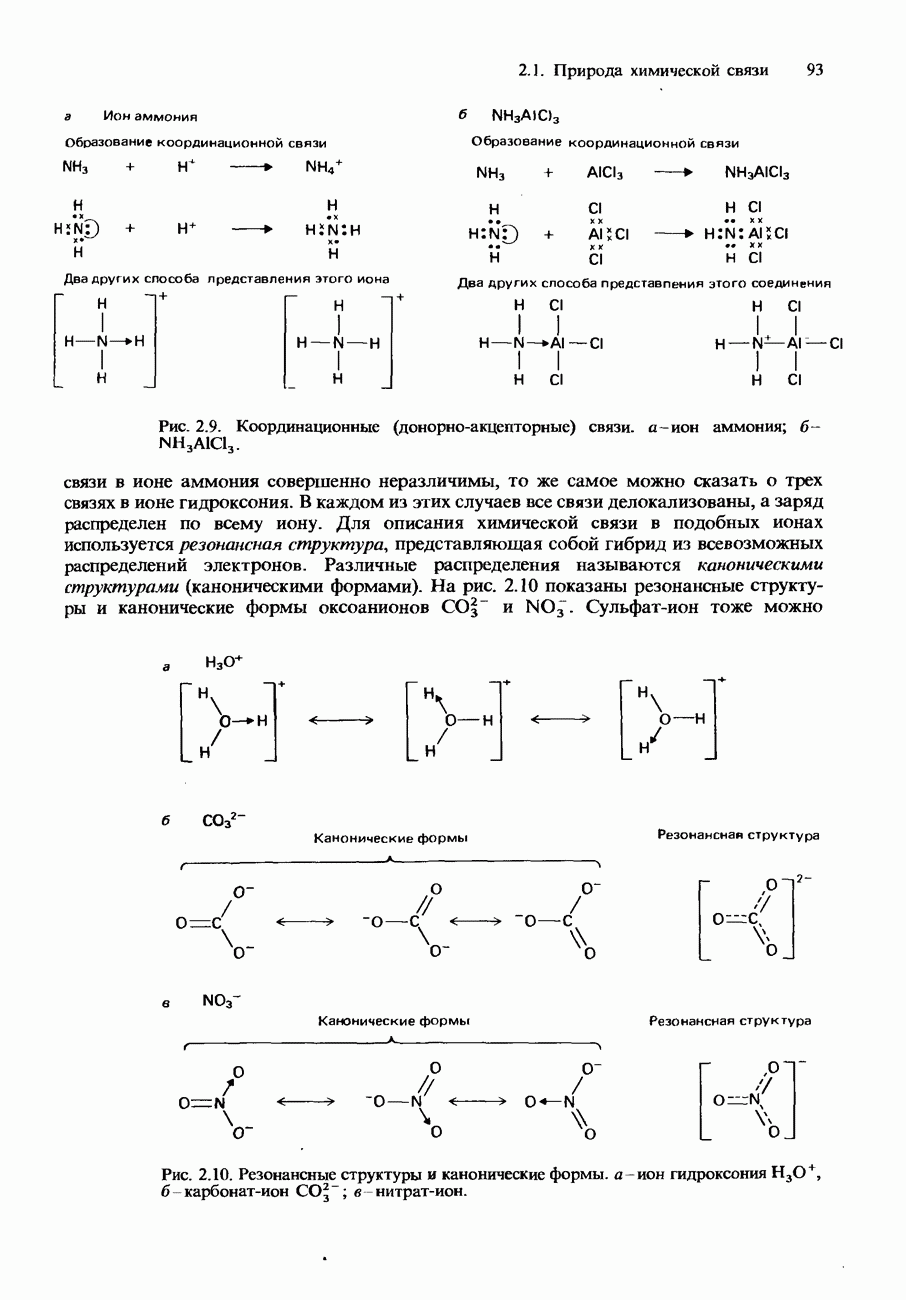
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
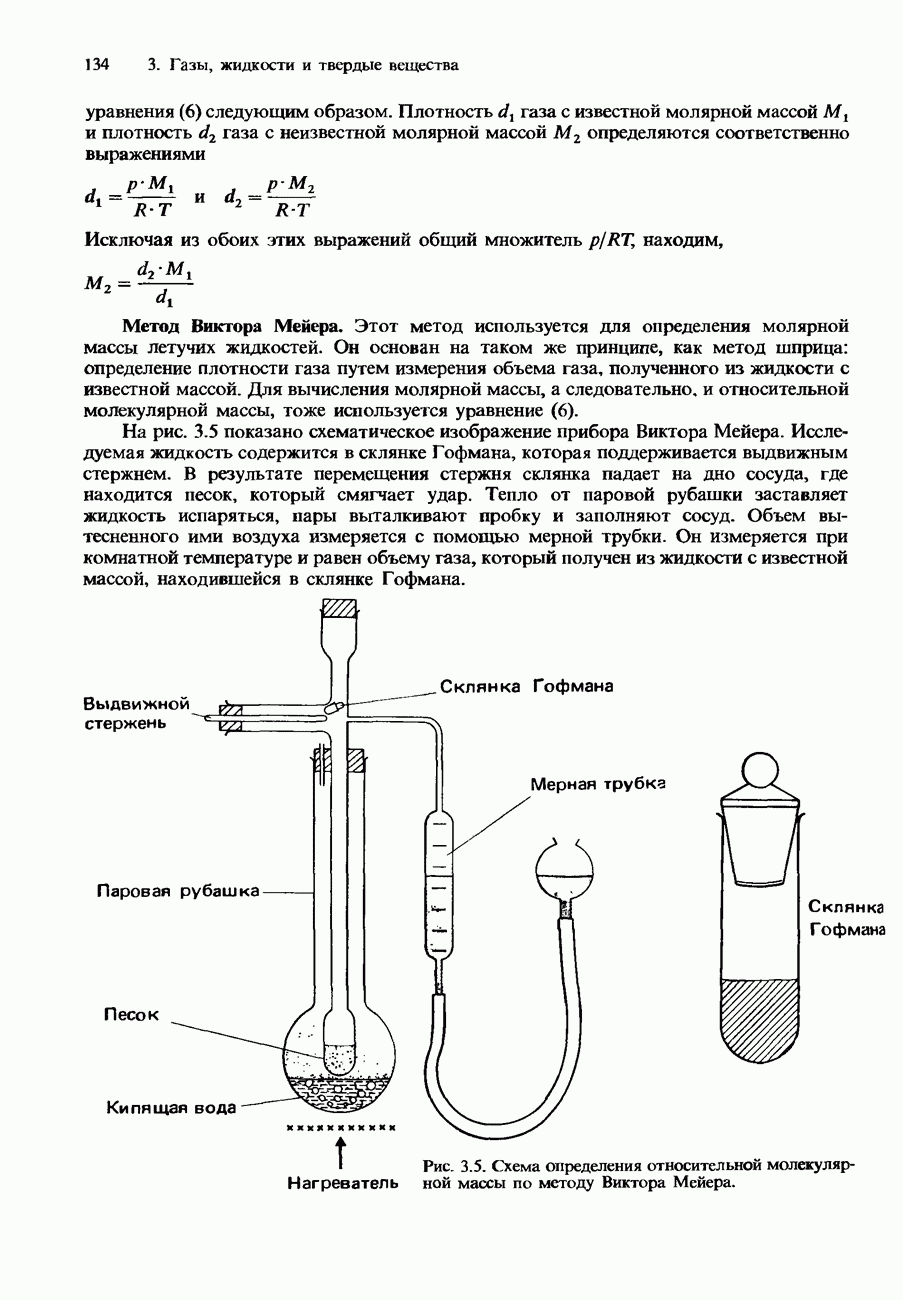
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
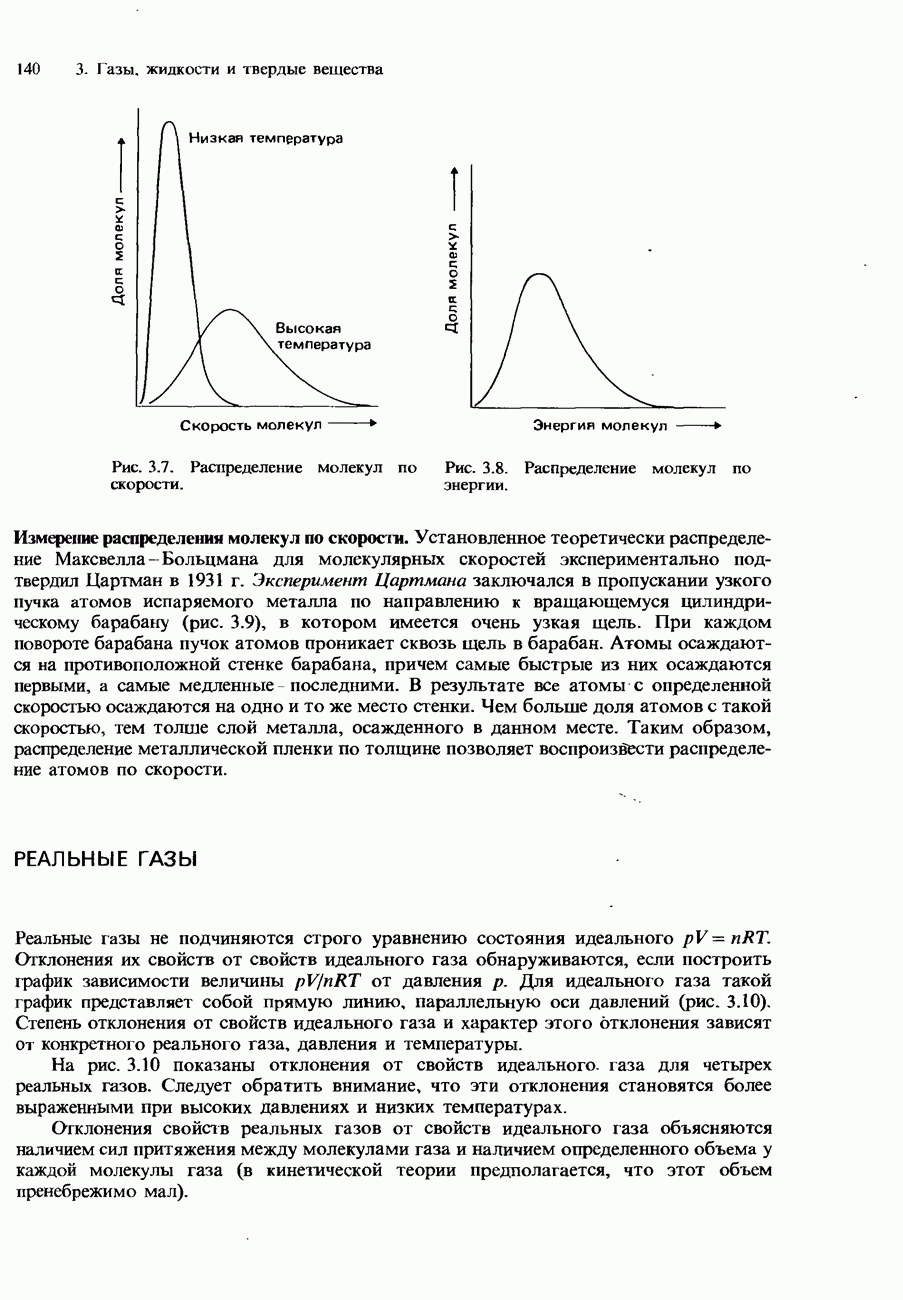
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
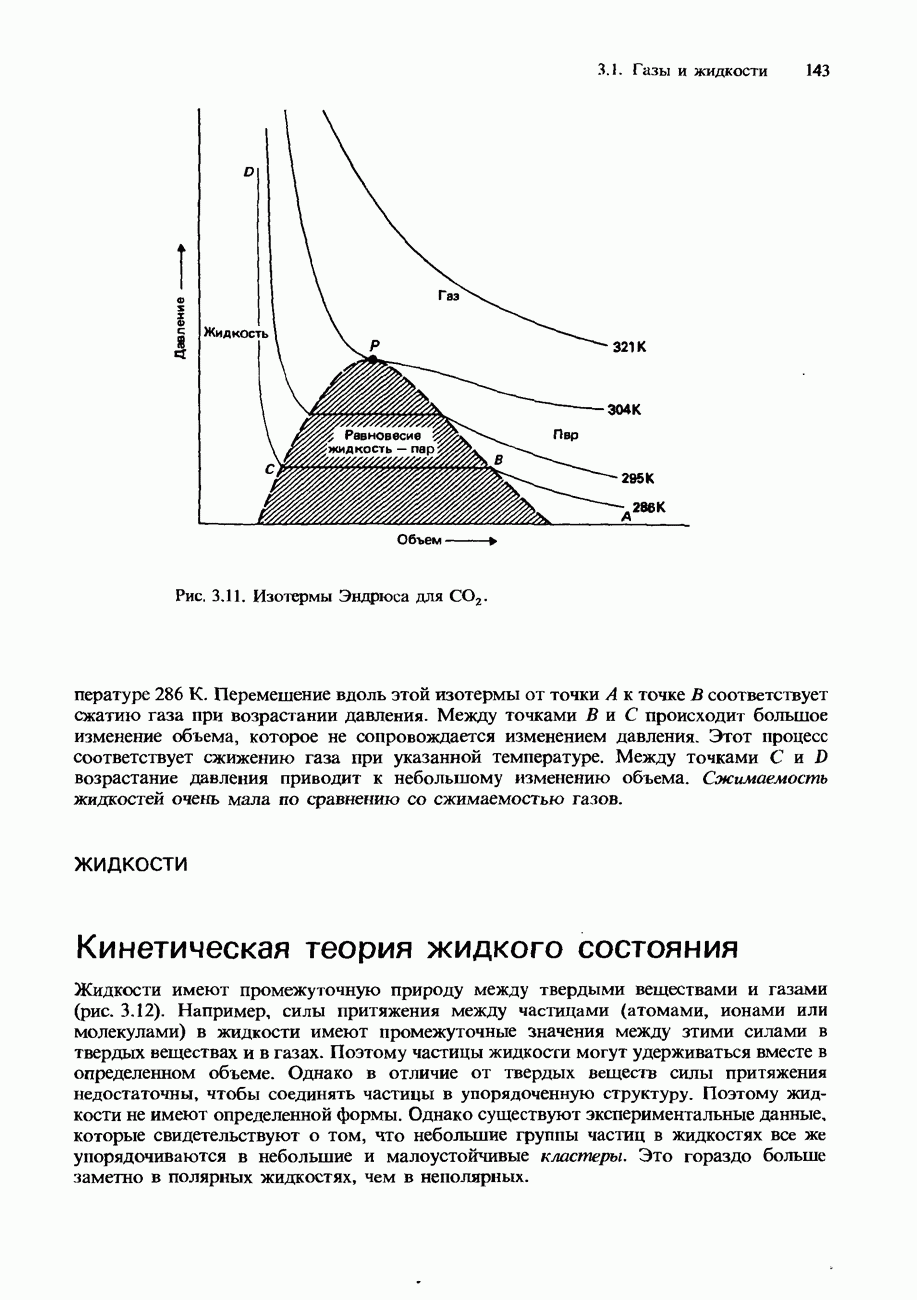
- Сжижение газов
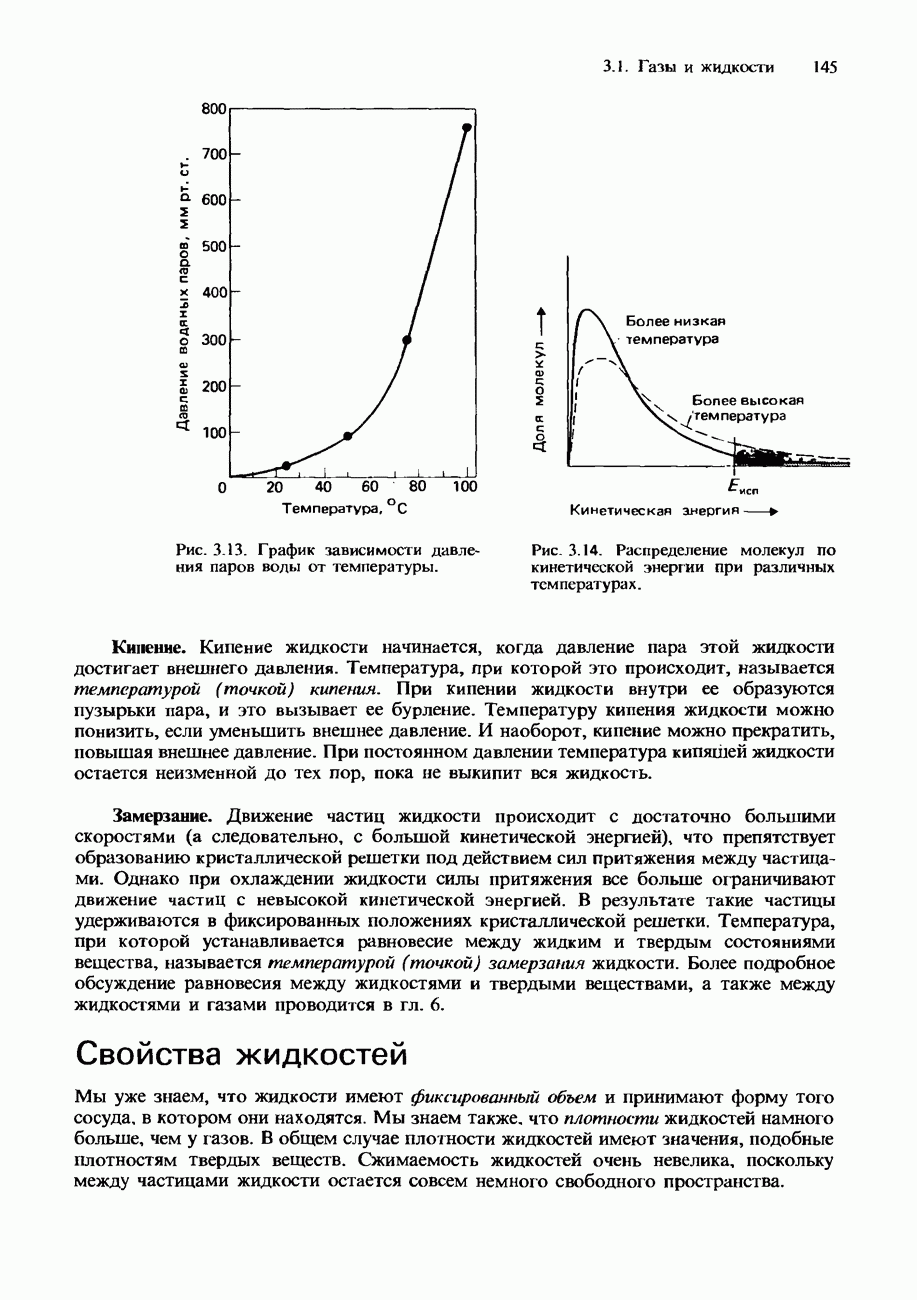
- ЖИДКОСТИ
- Свойства жидкостей
- 3.2. Твердые вещества
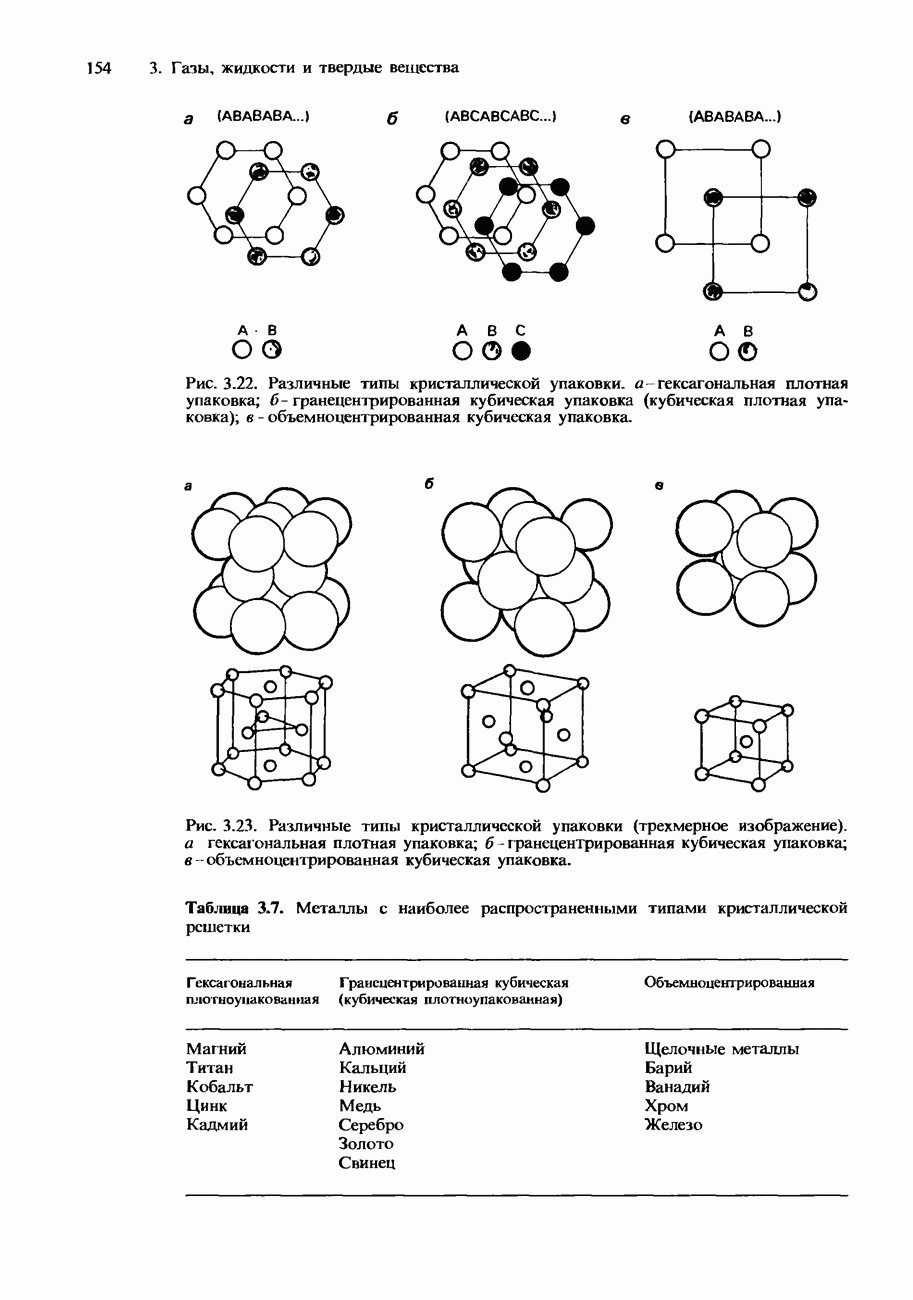
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
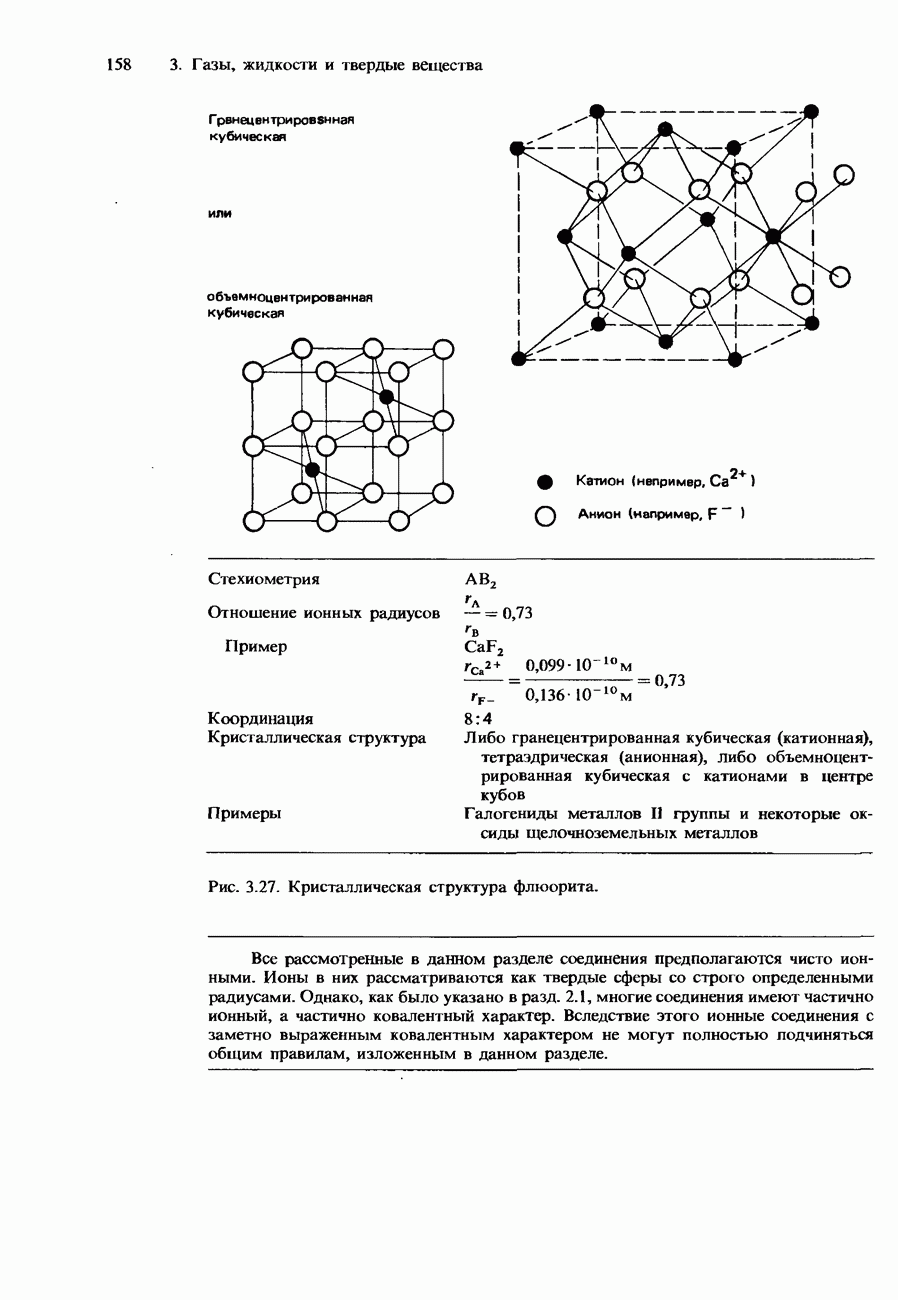
- Ионные кристаллы
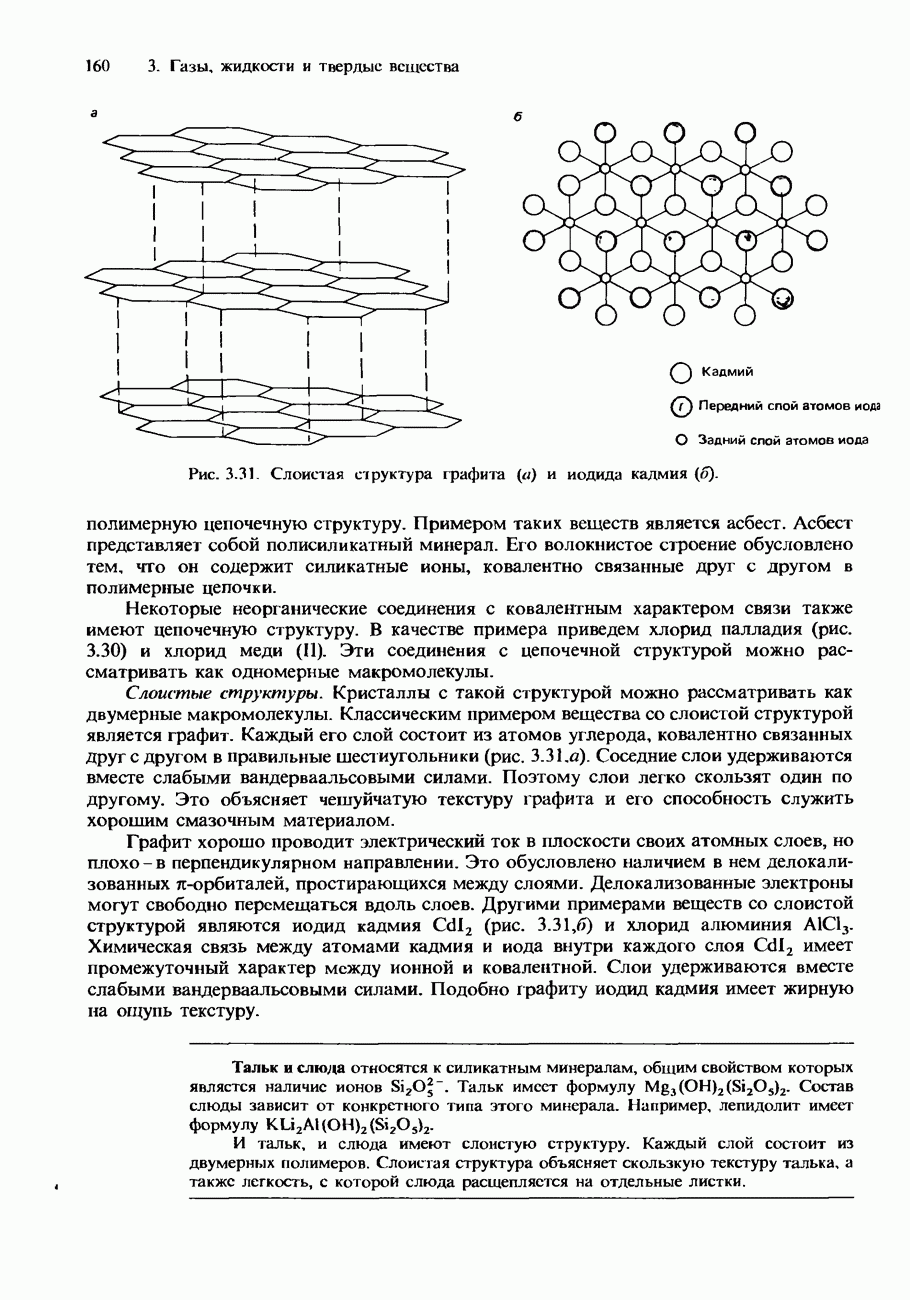
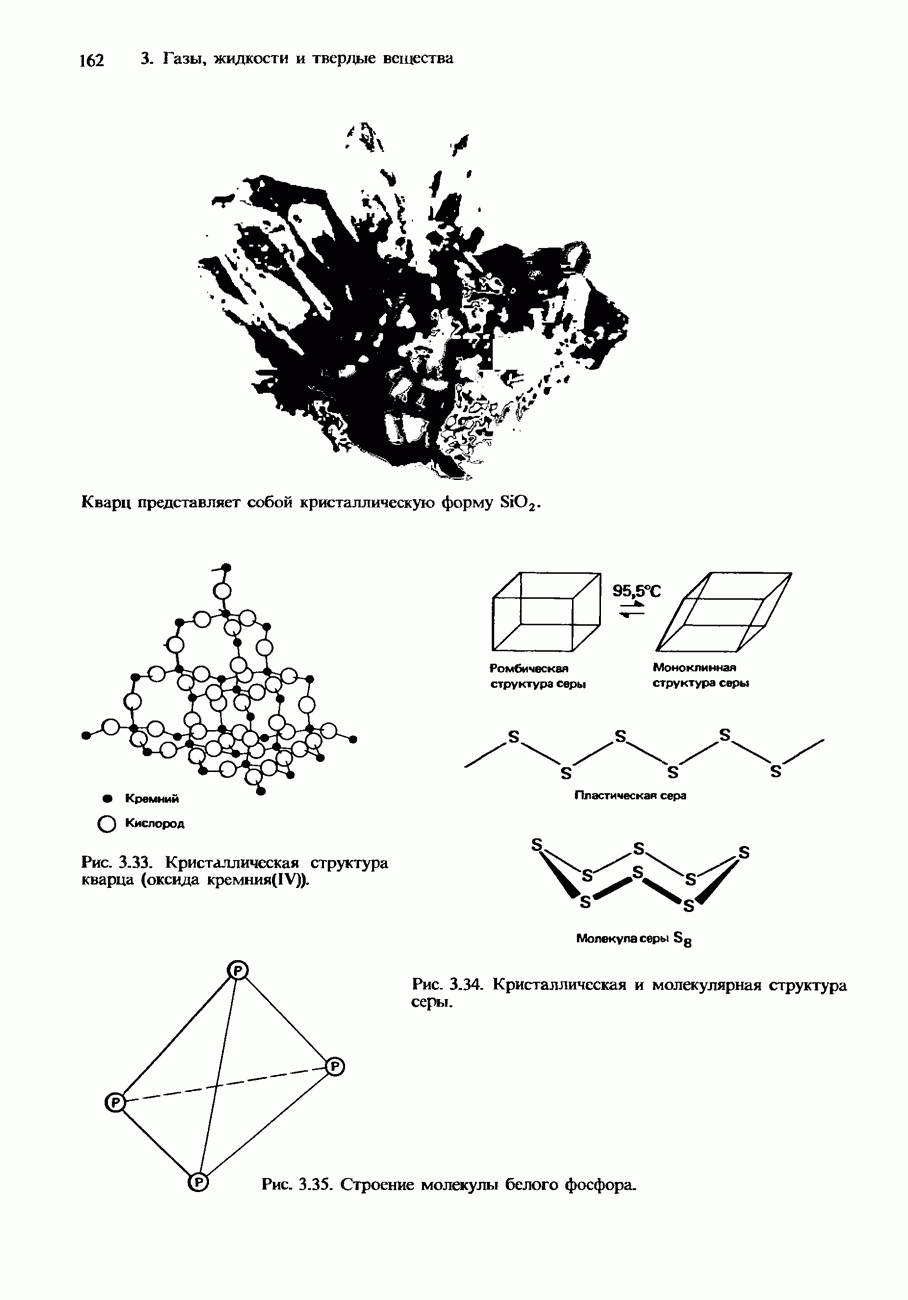
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
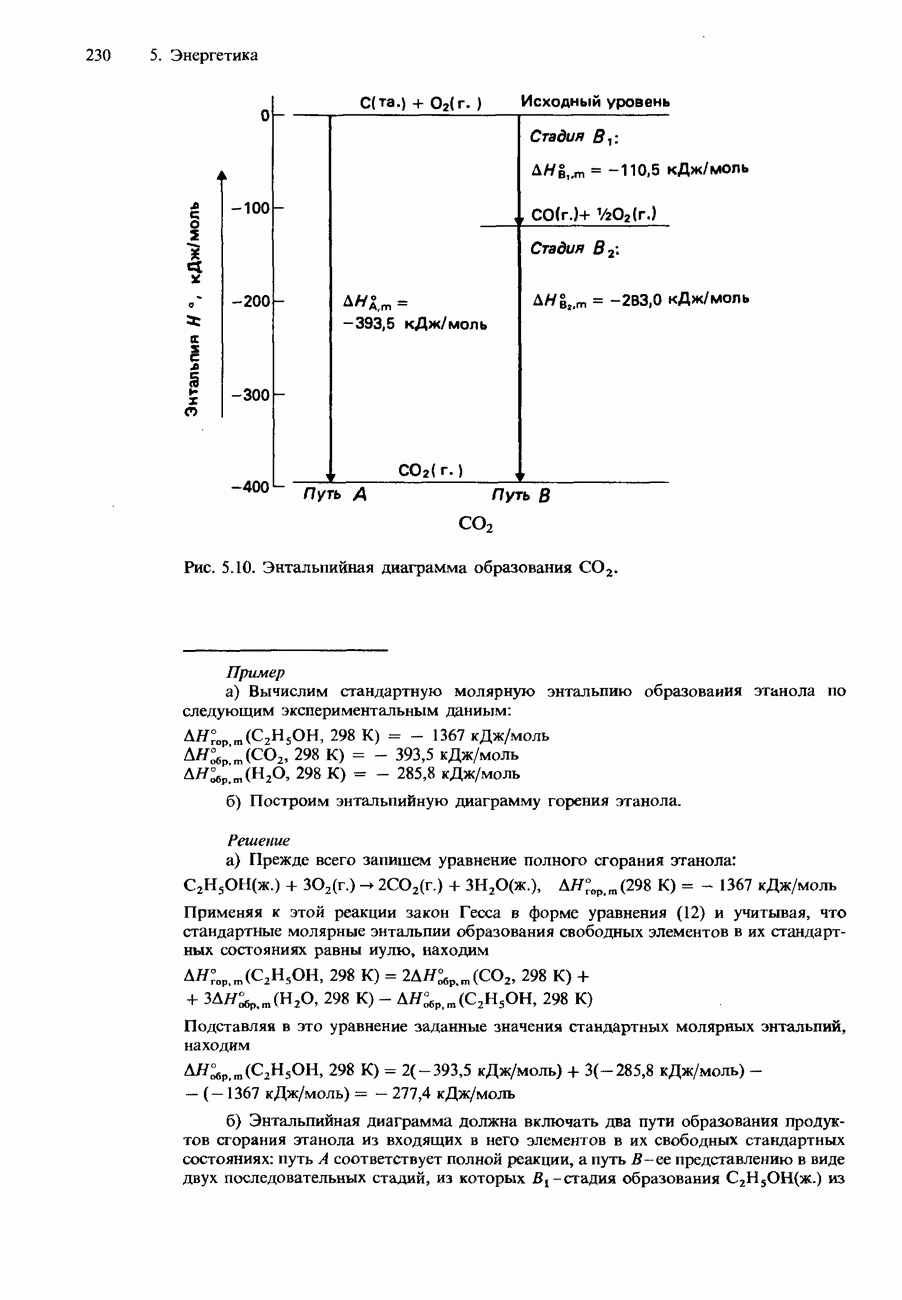
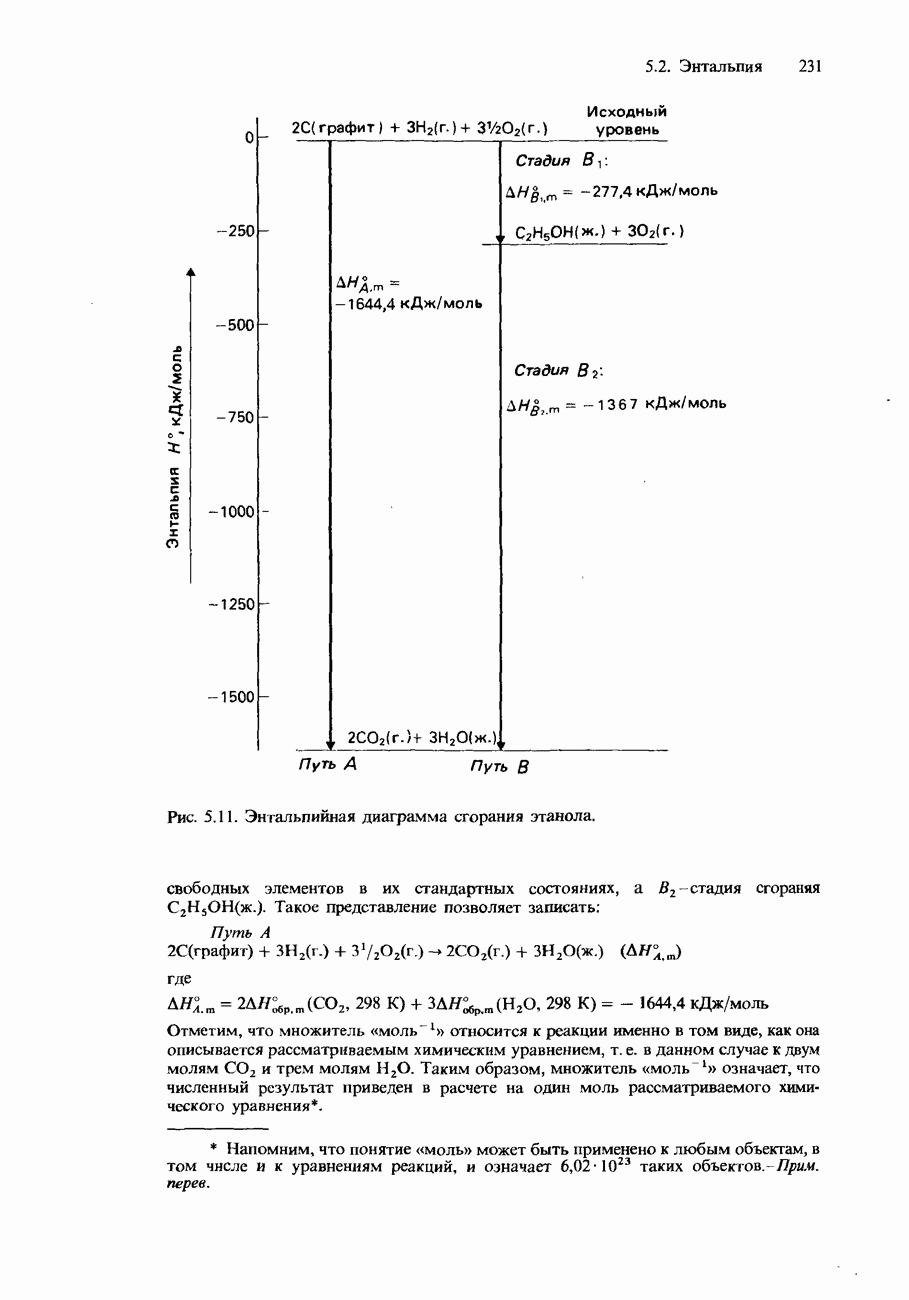
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
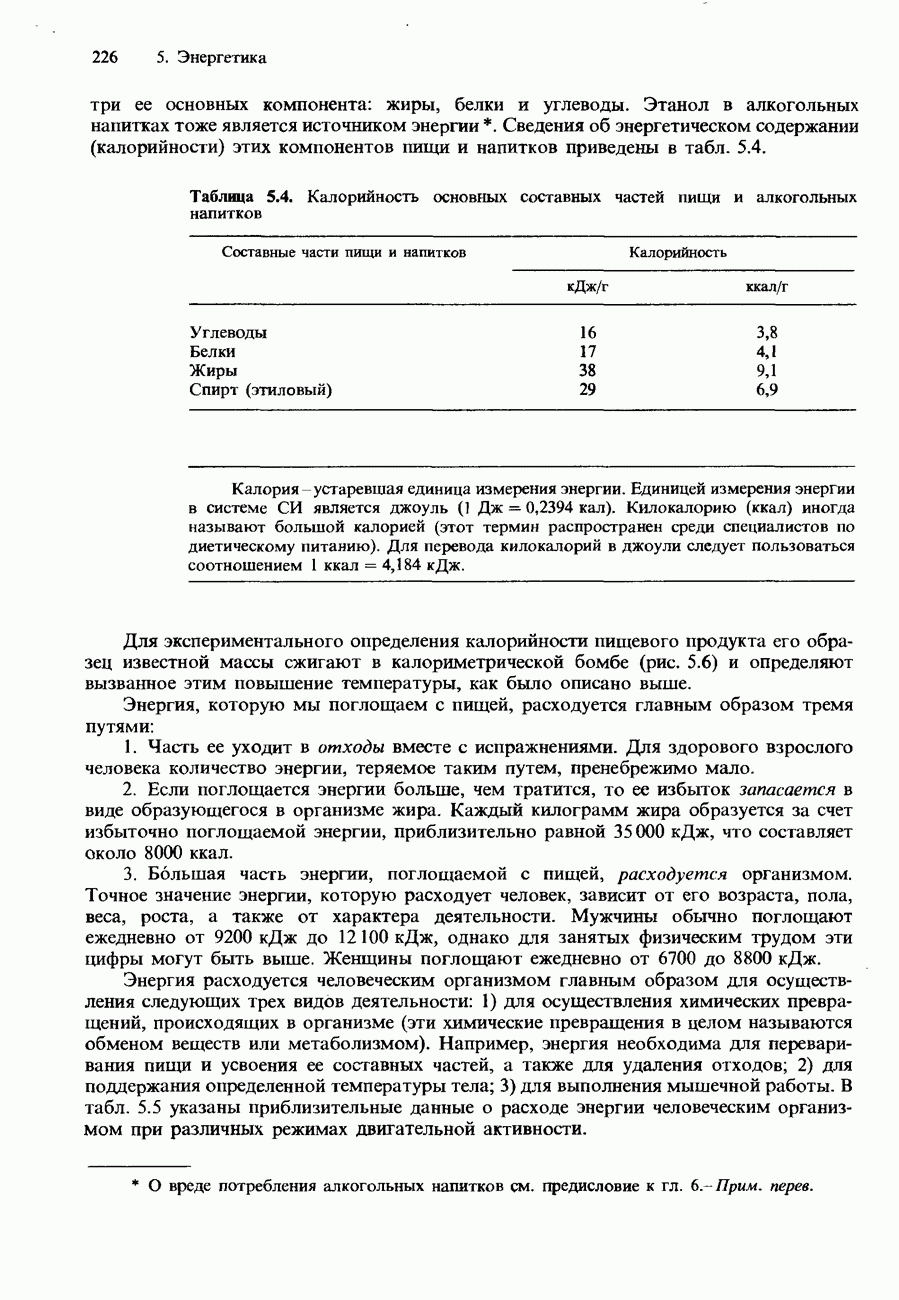
- КАЛОРИЙНОСТЬ ПИЩИ
- ЗАКОН ГЕССА
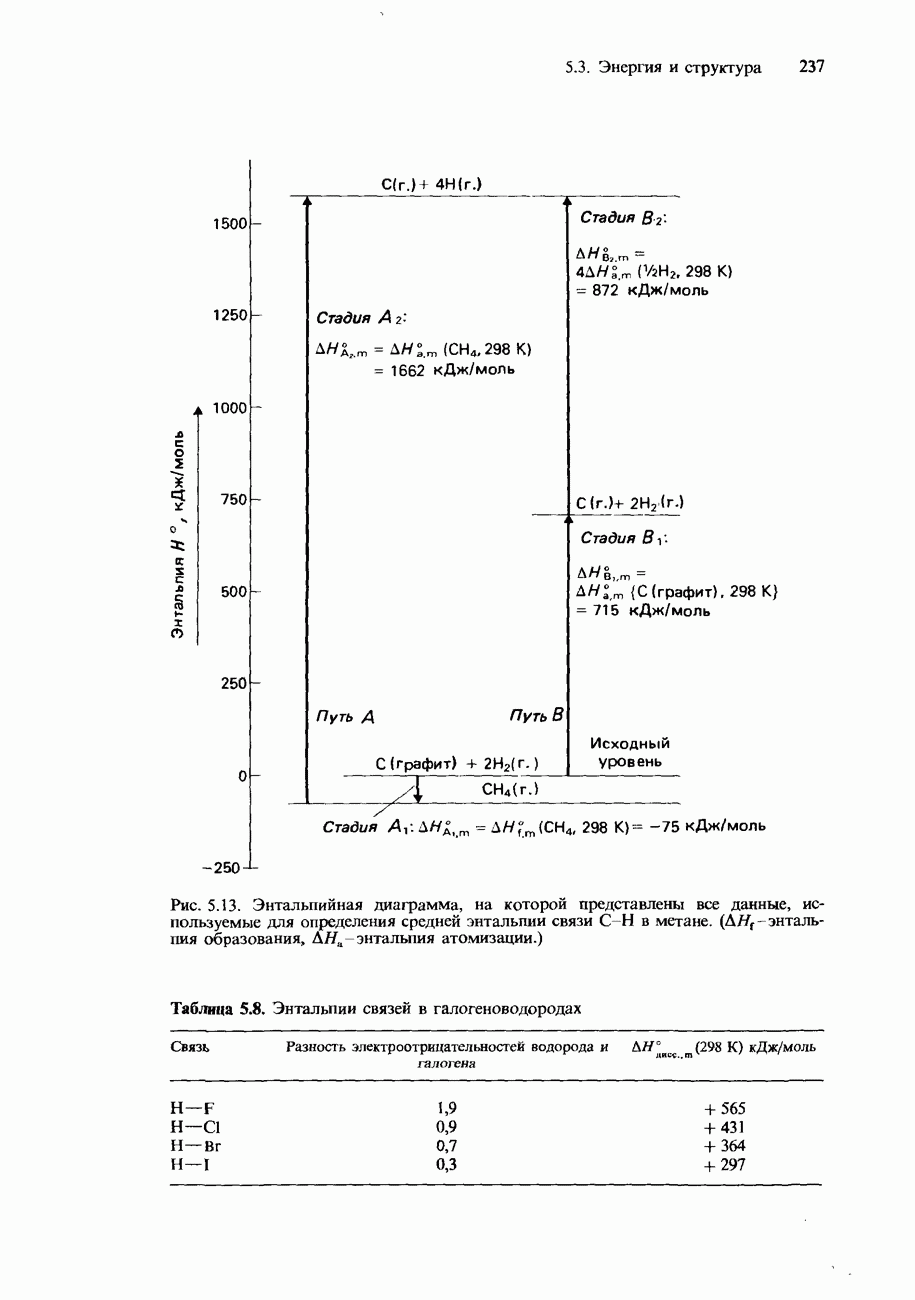
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
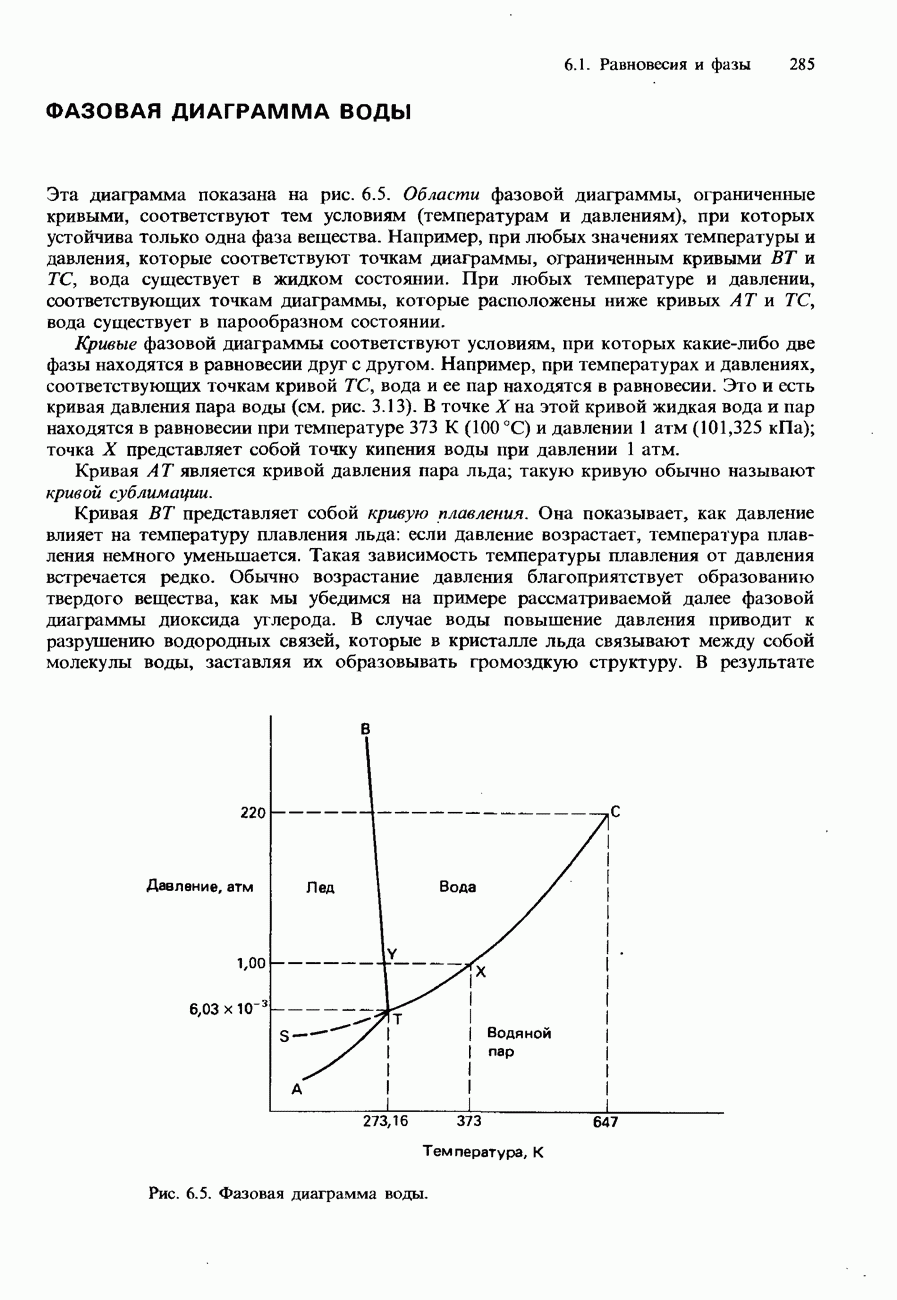
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
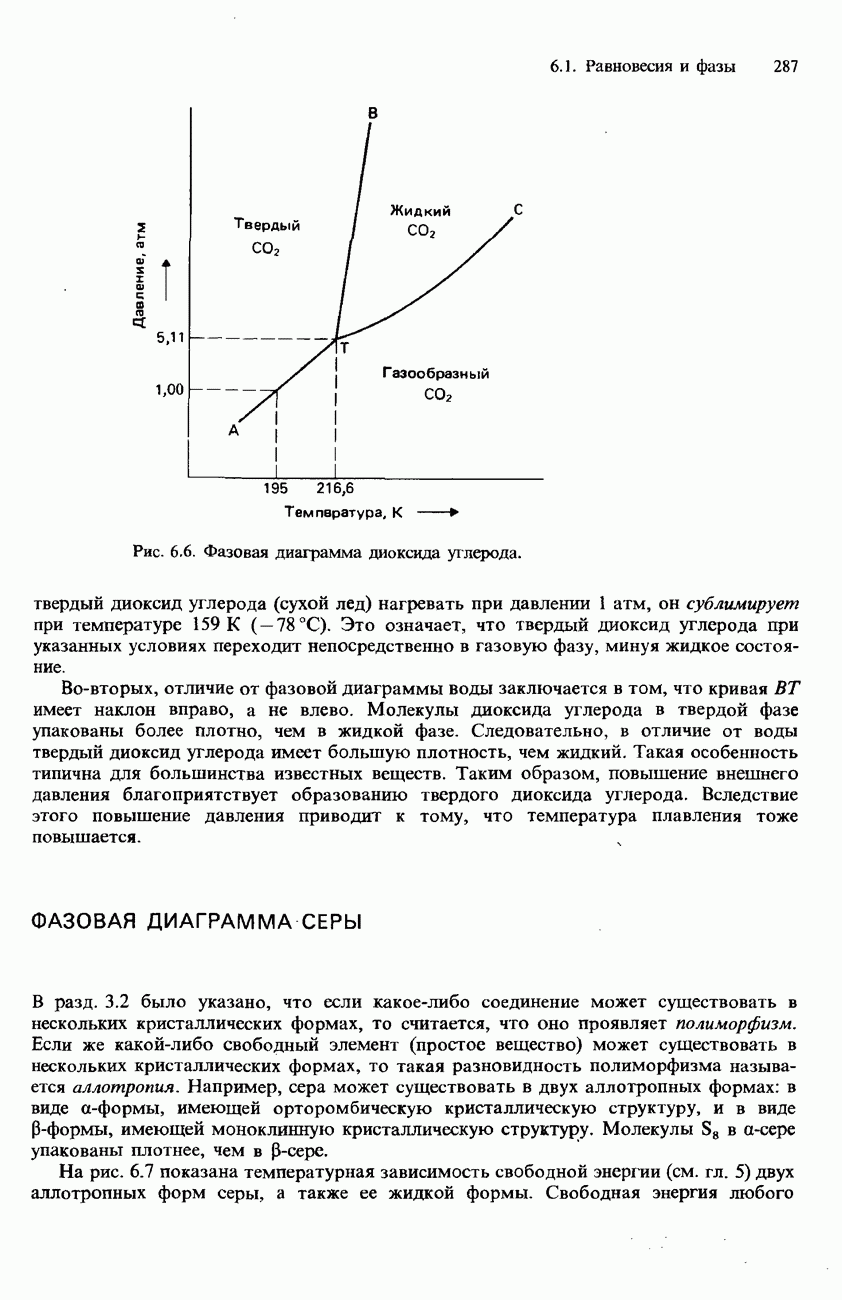
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
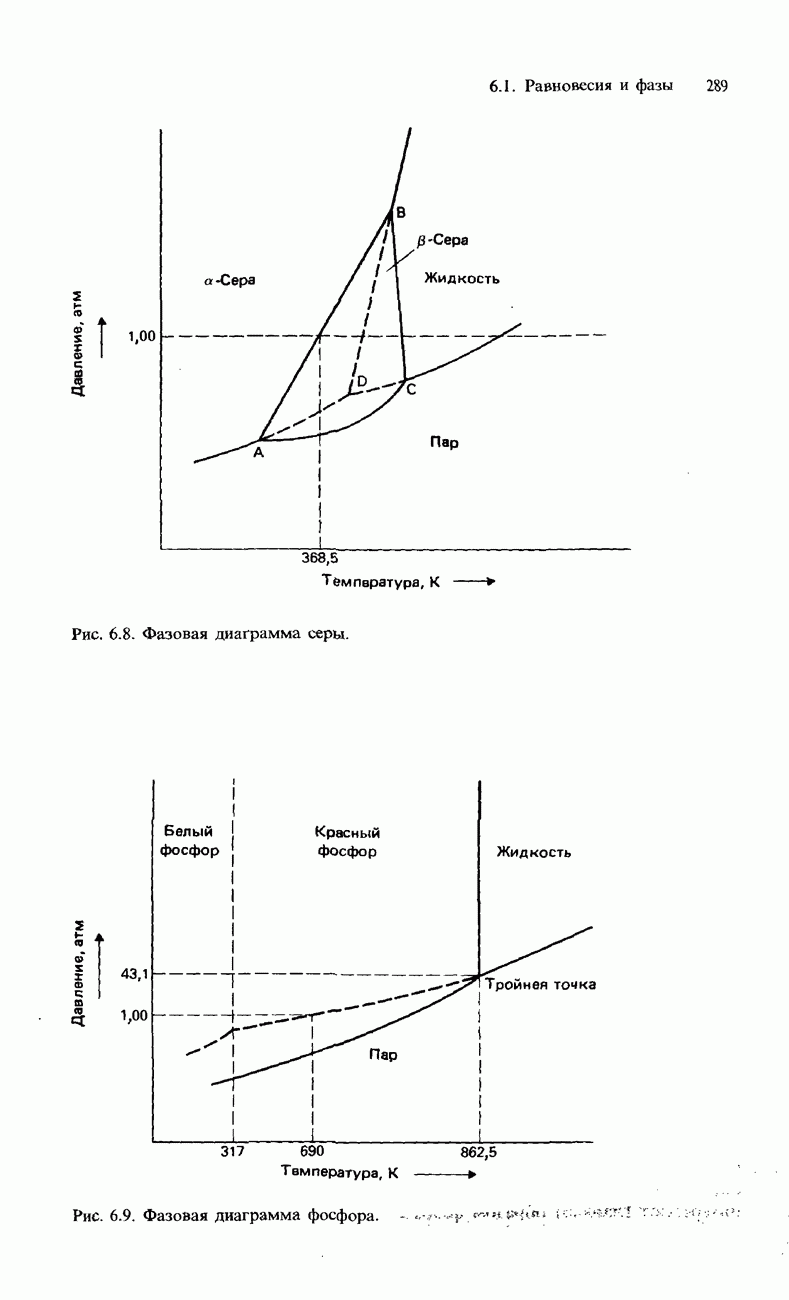
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
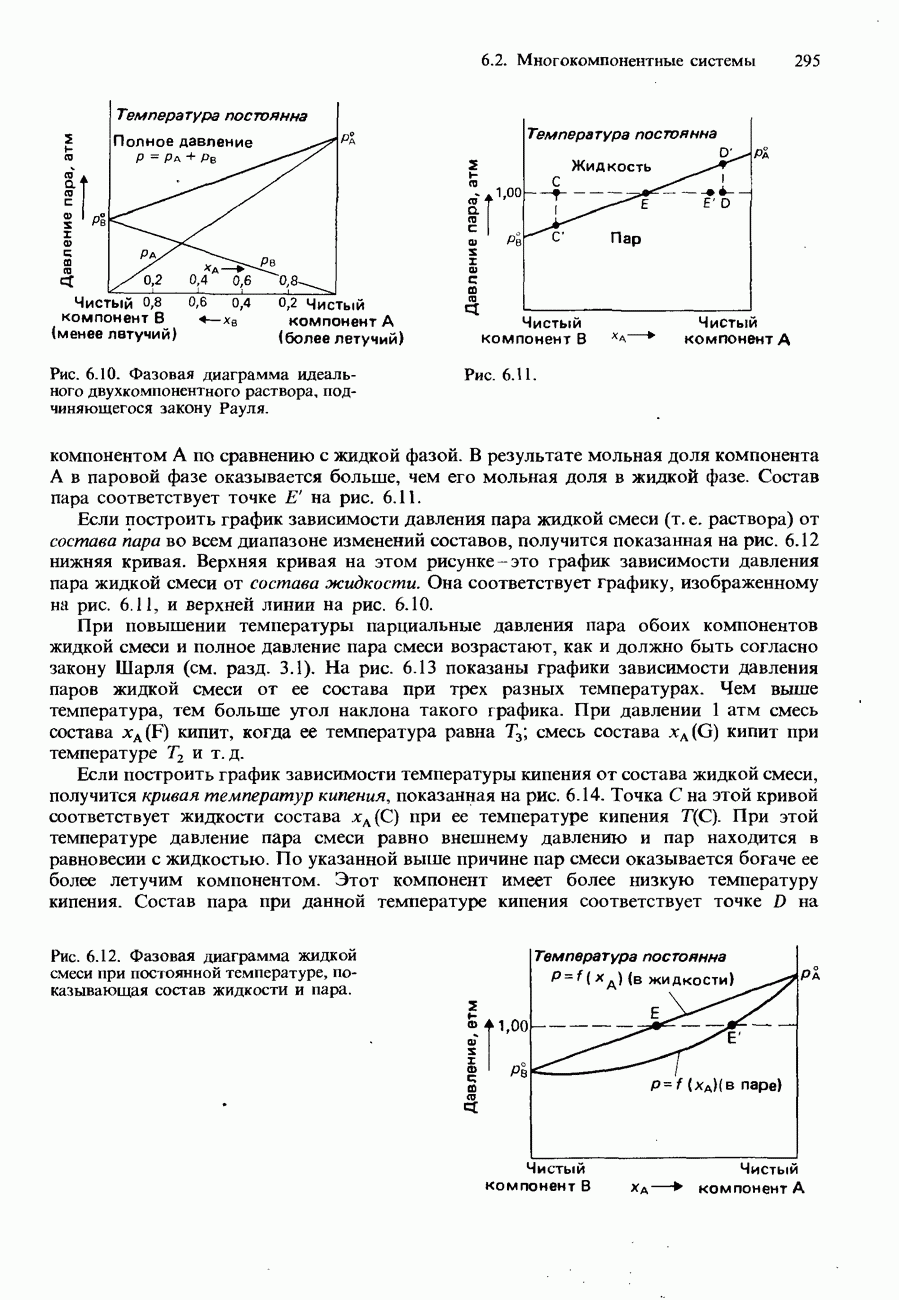
- Фазовые диаграммы полностью смешивающихся жидкостей
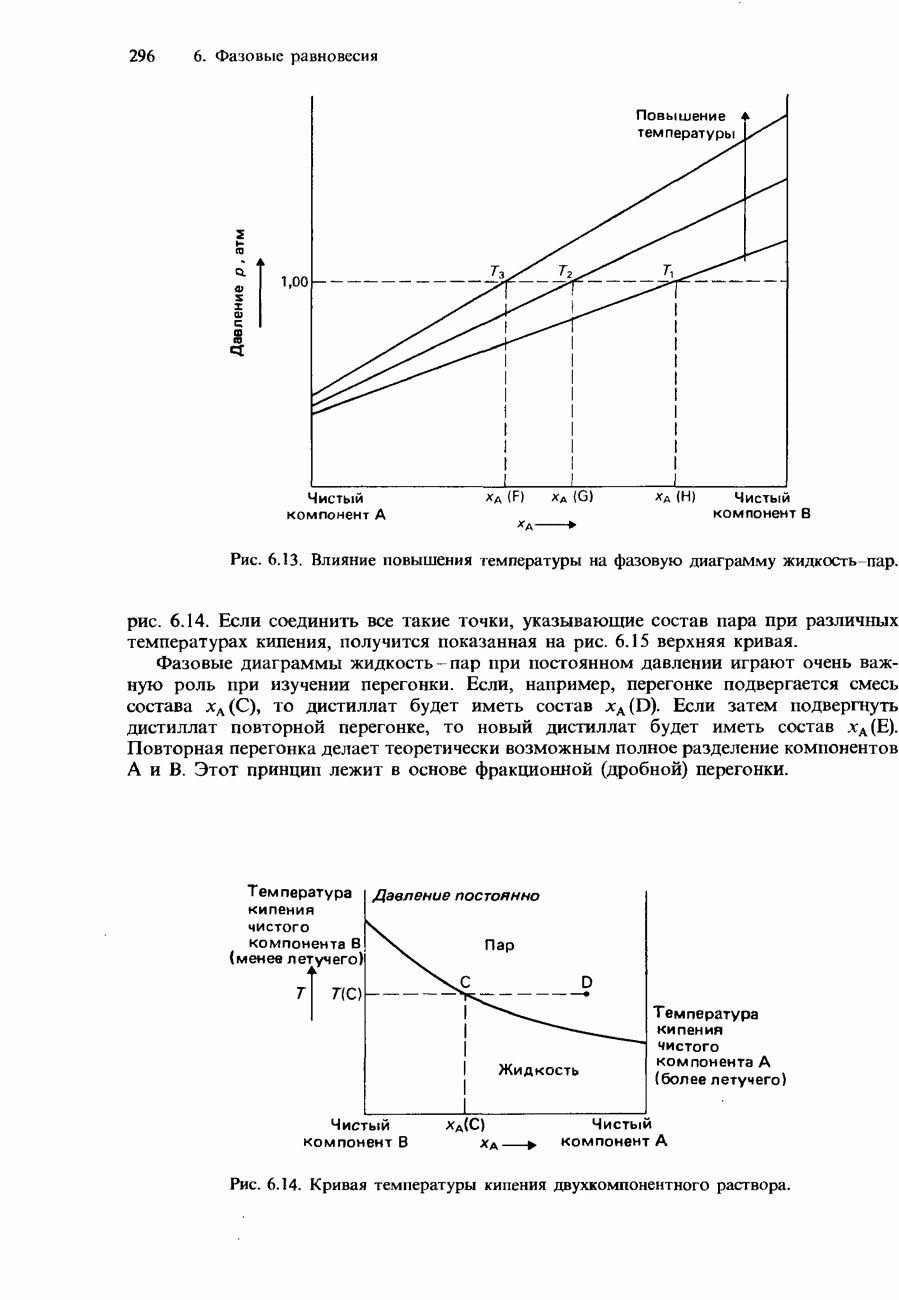
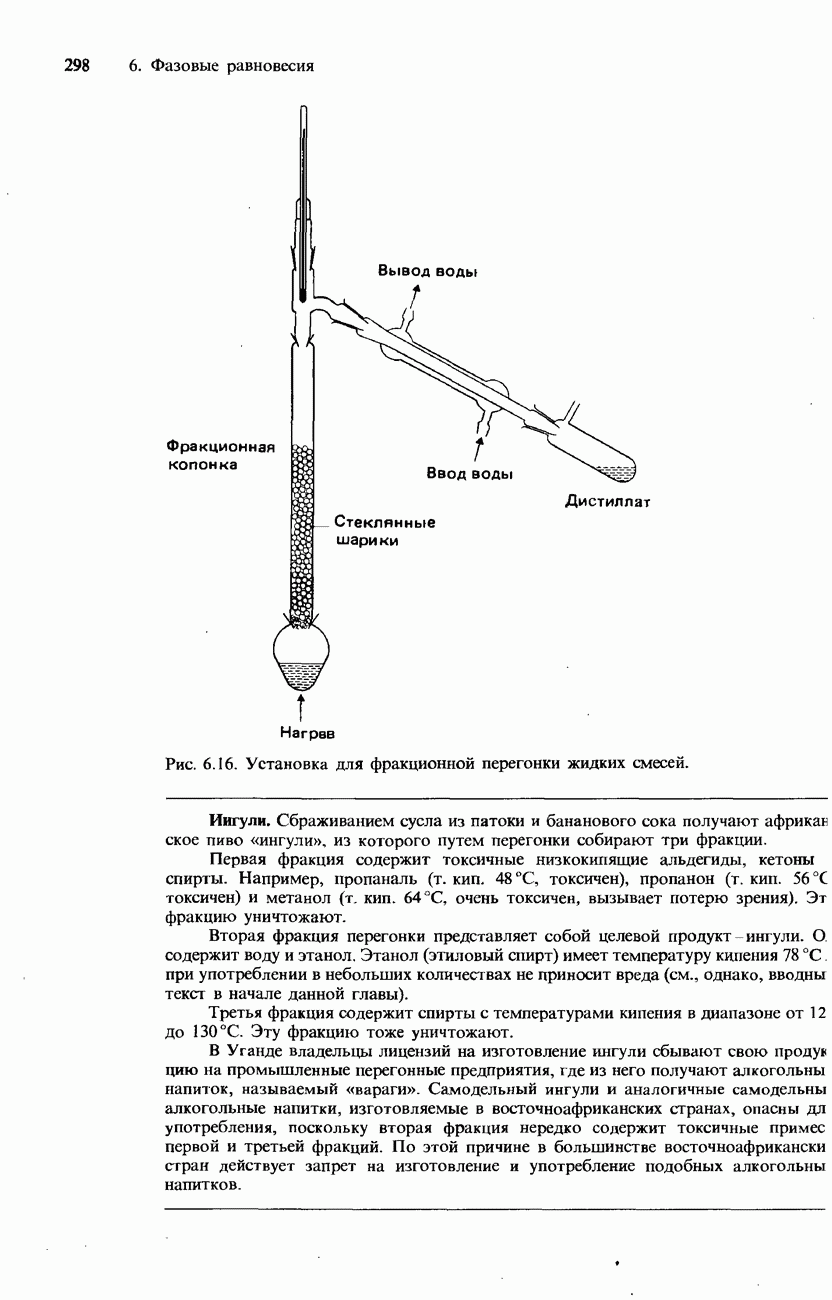
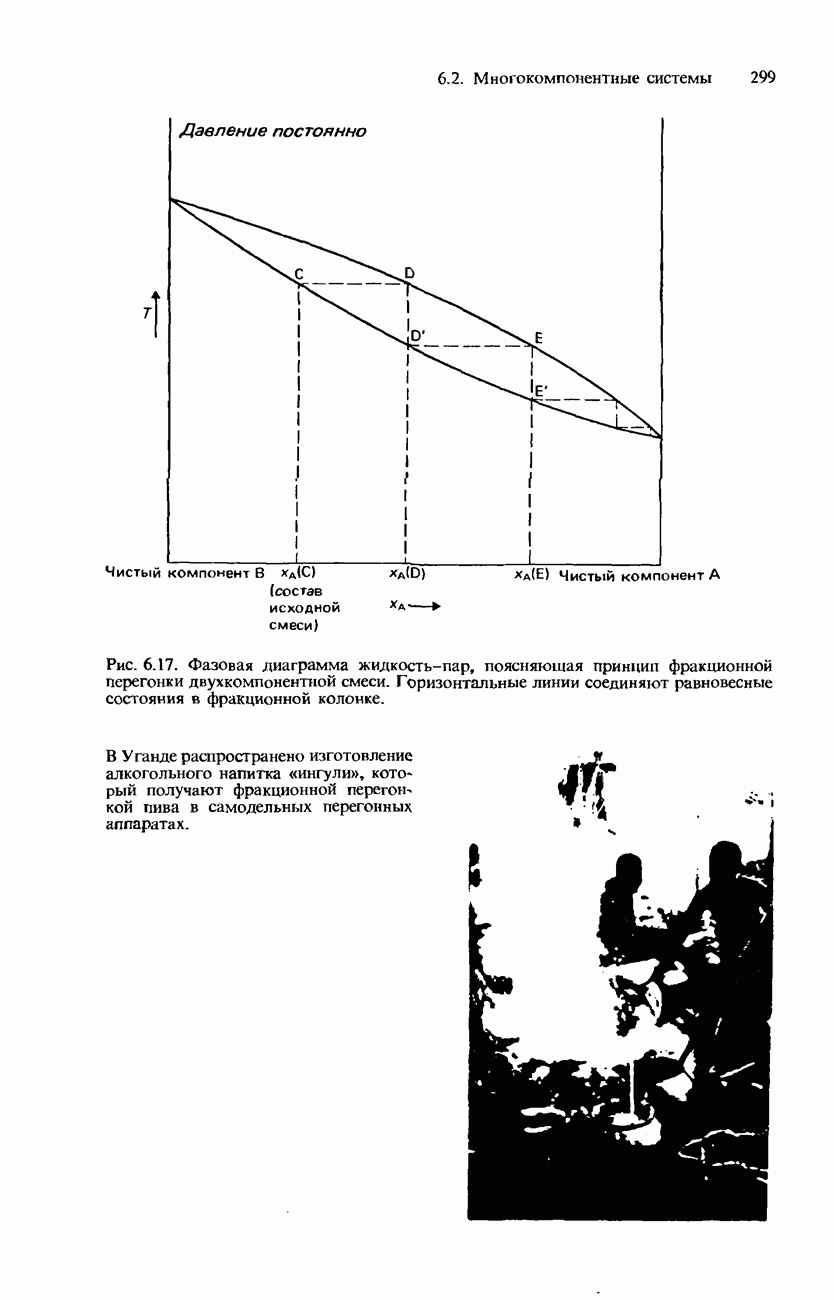
- Фракционная перегонка
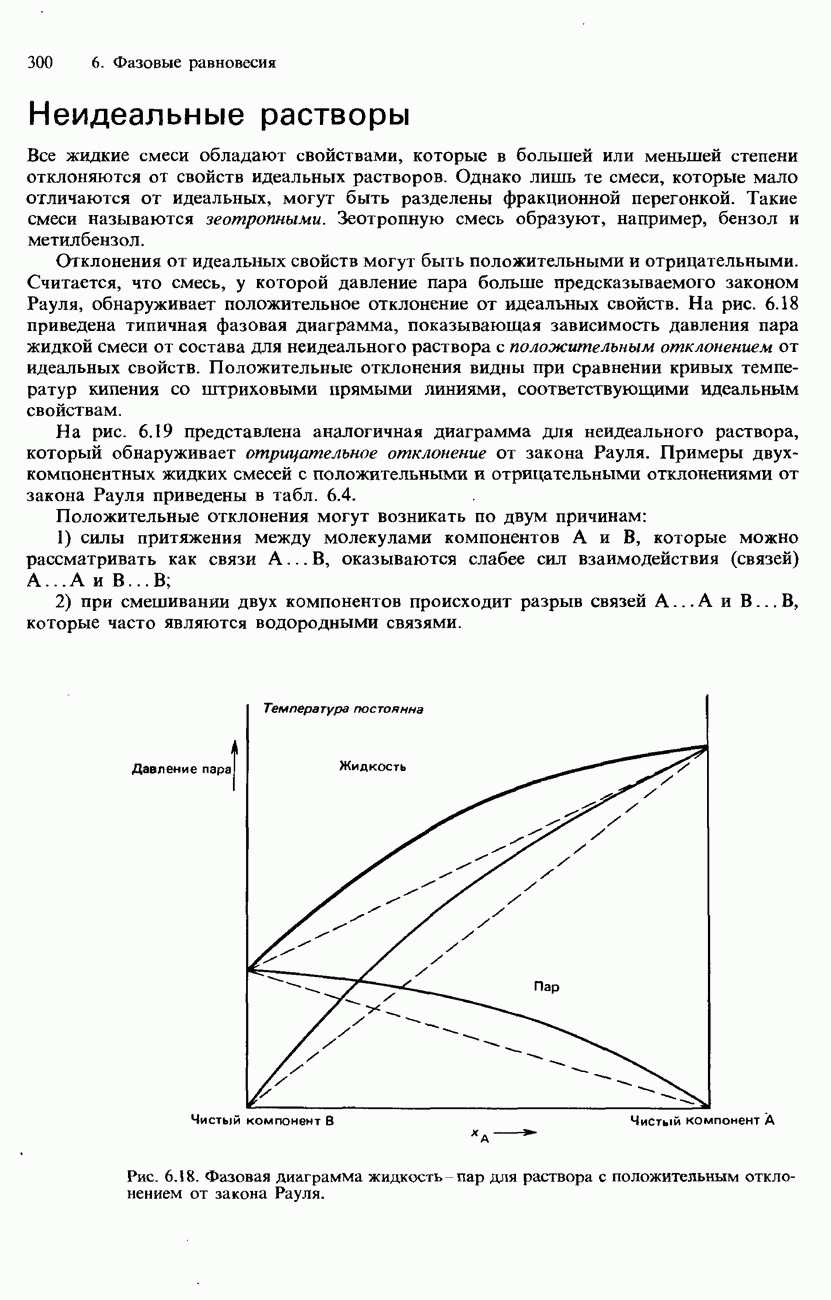
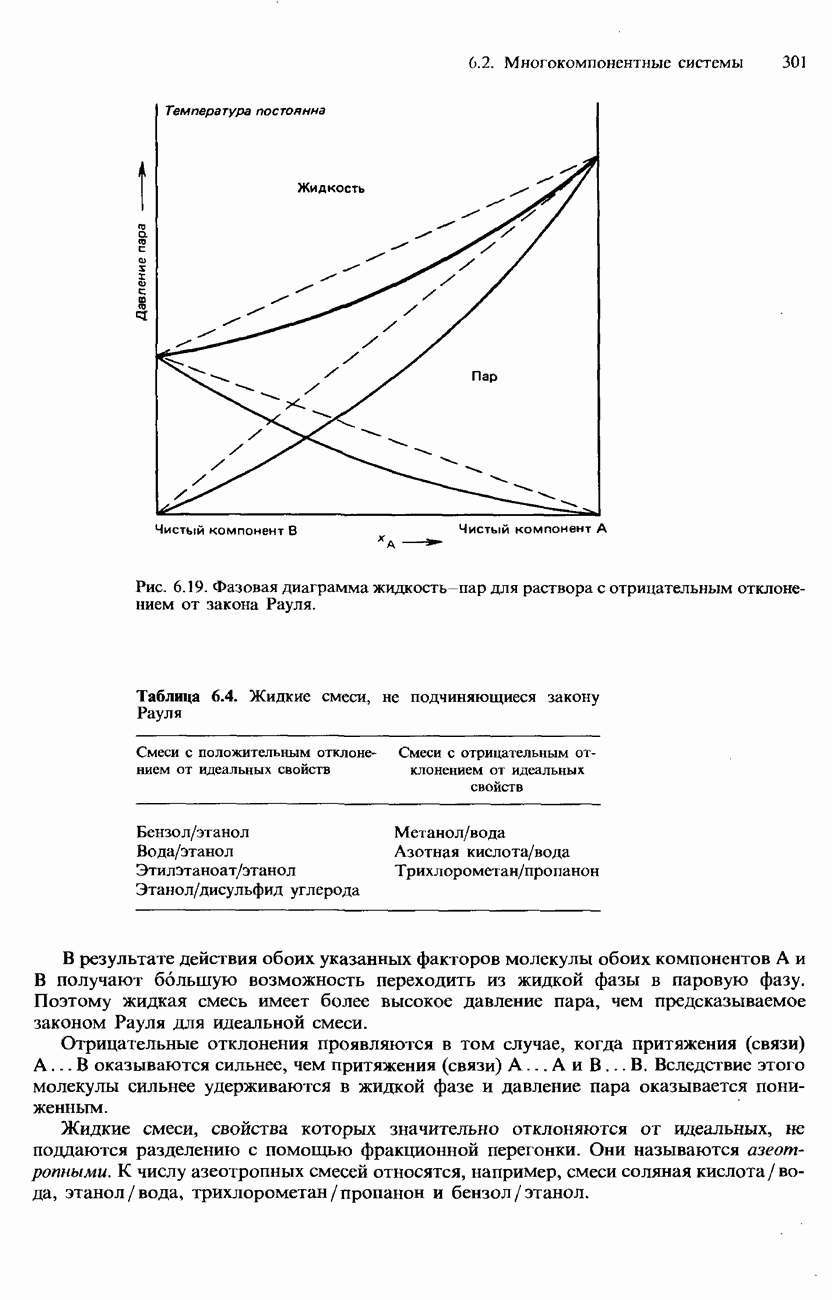
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
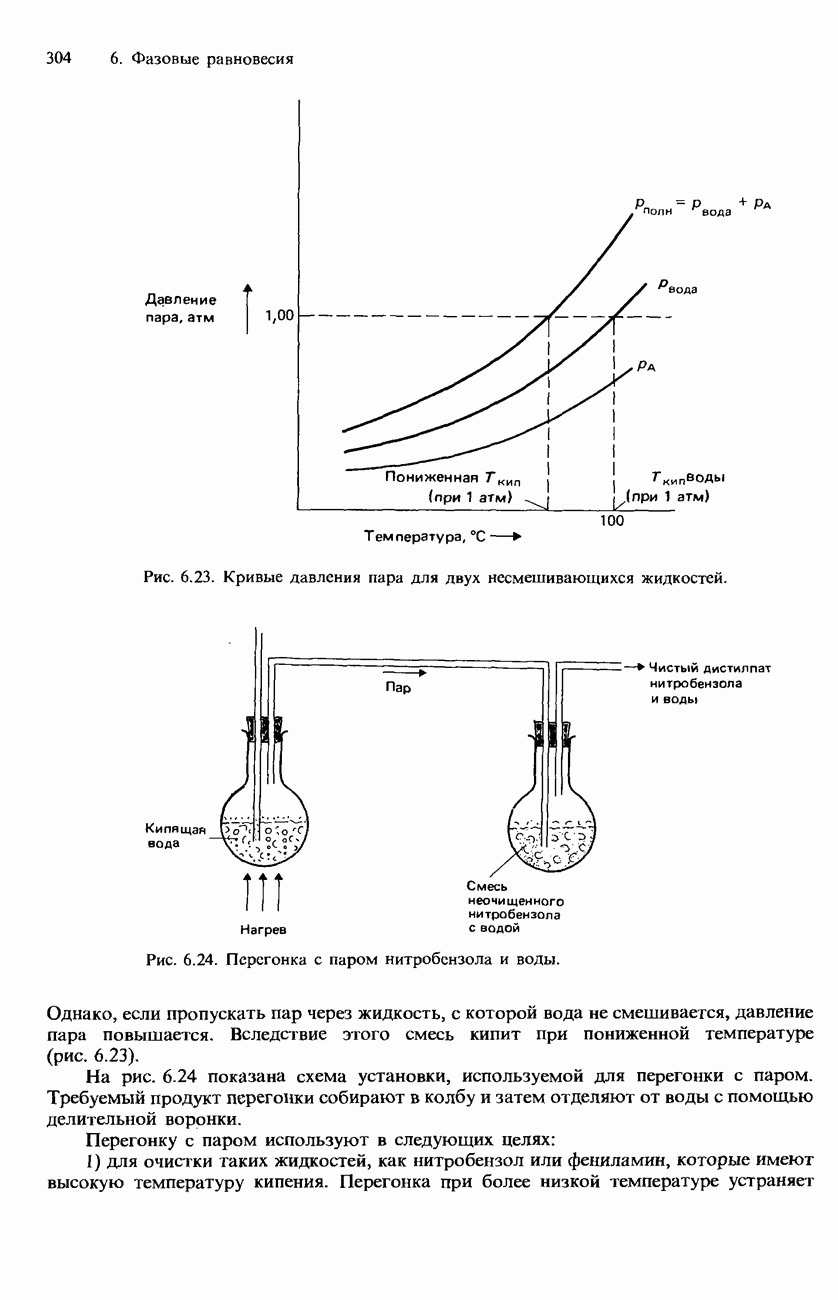
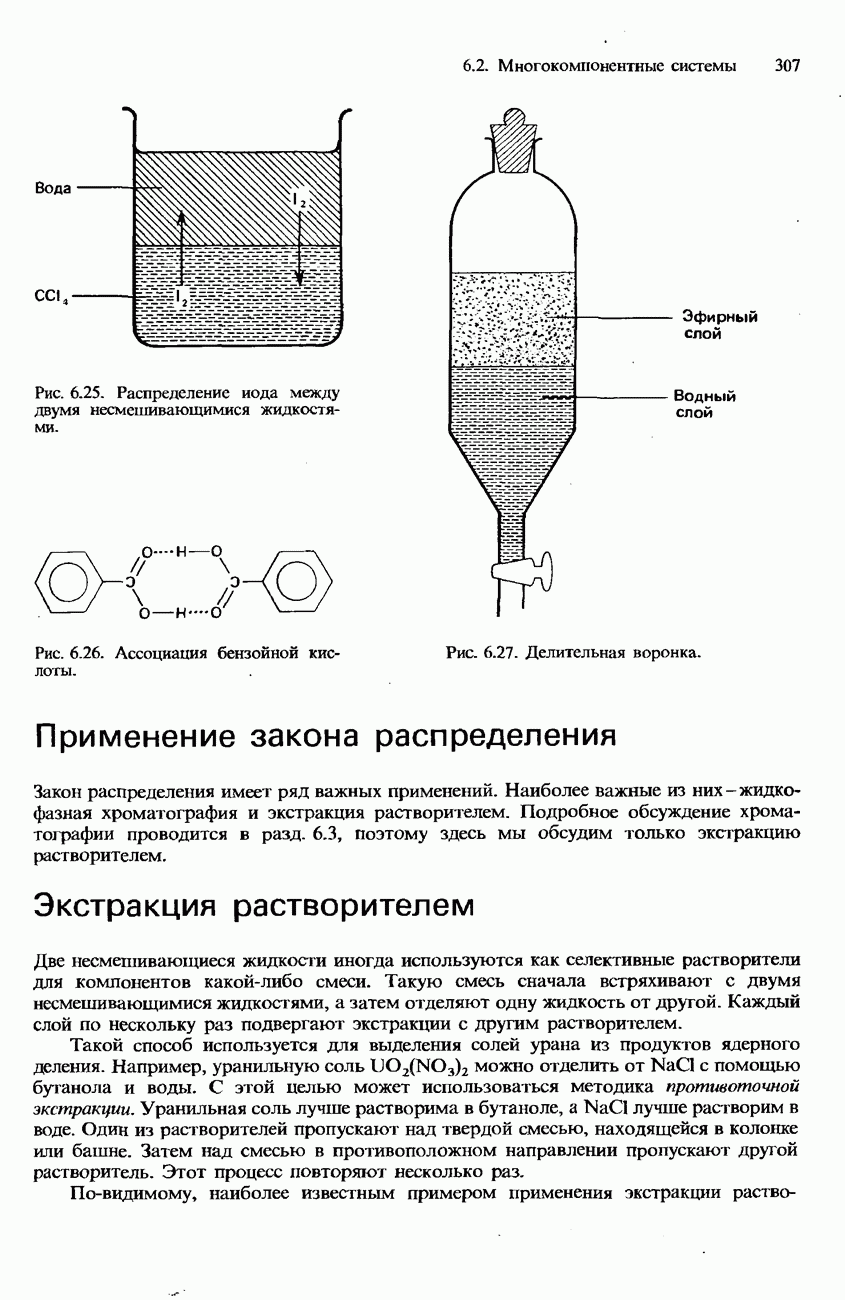
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
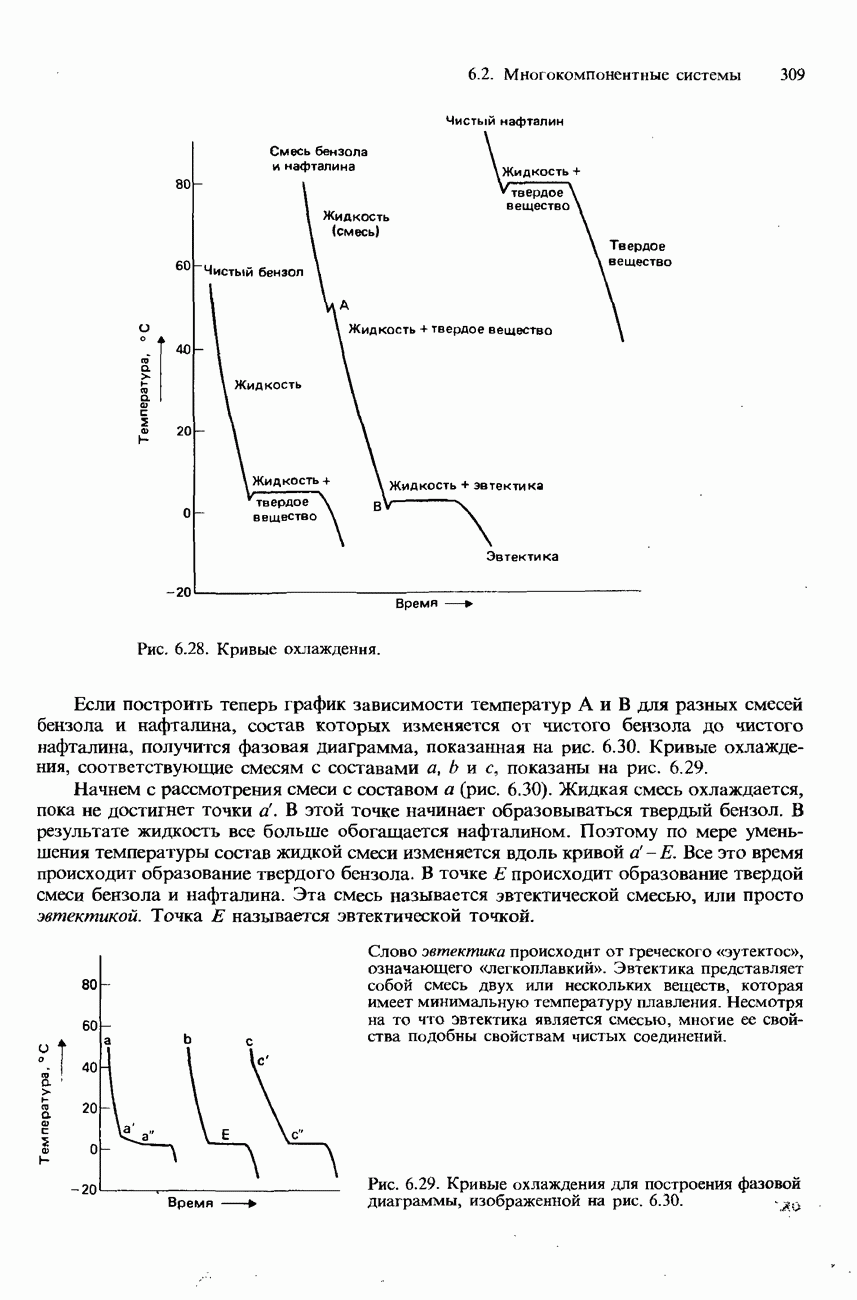
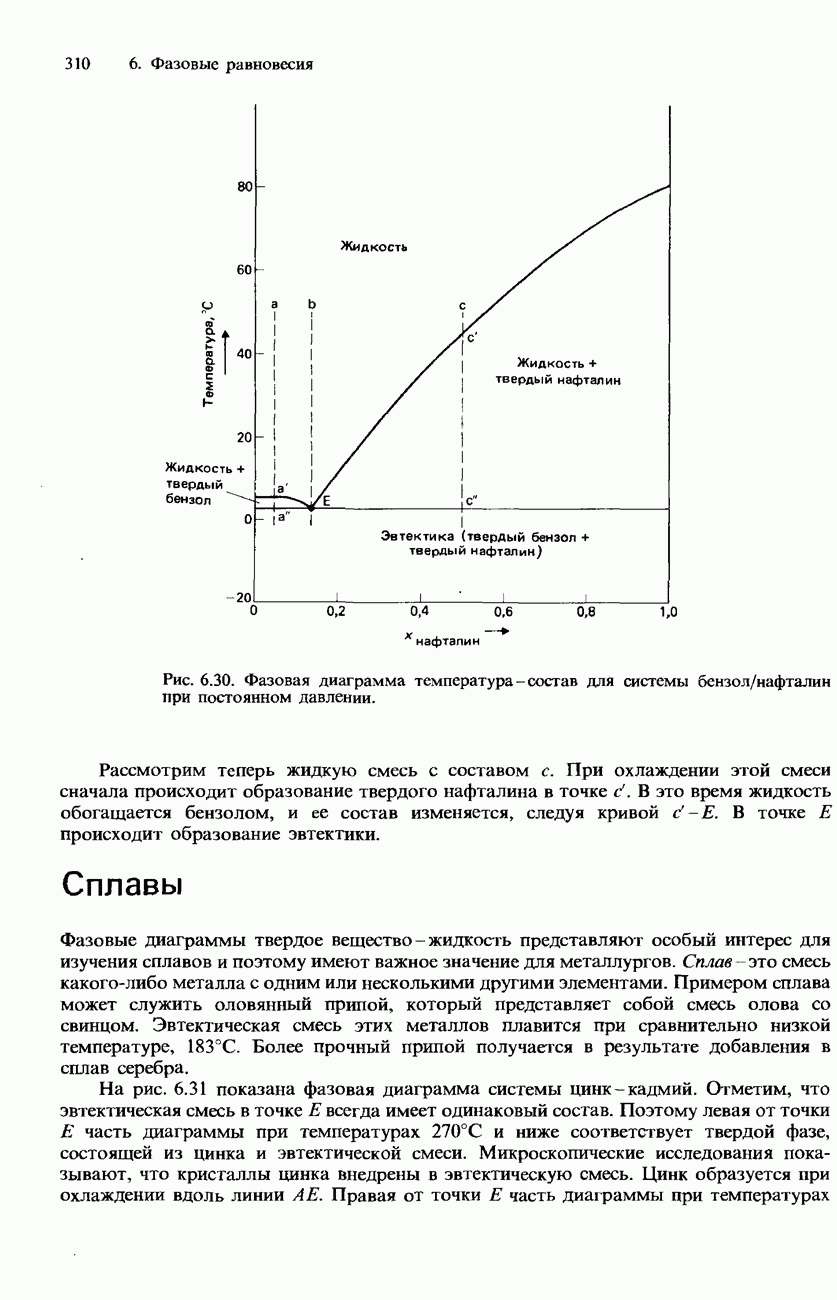
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
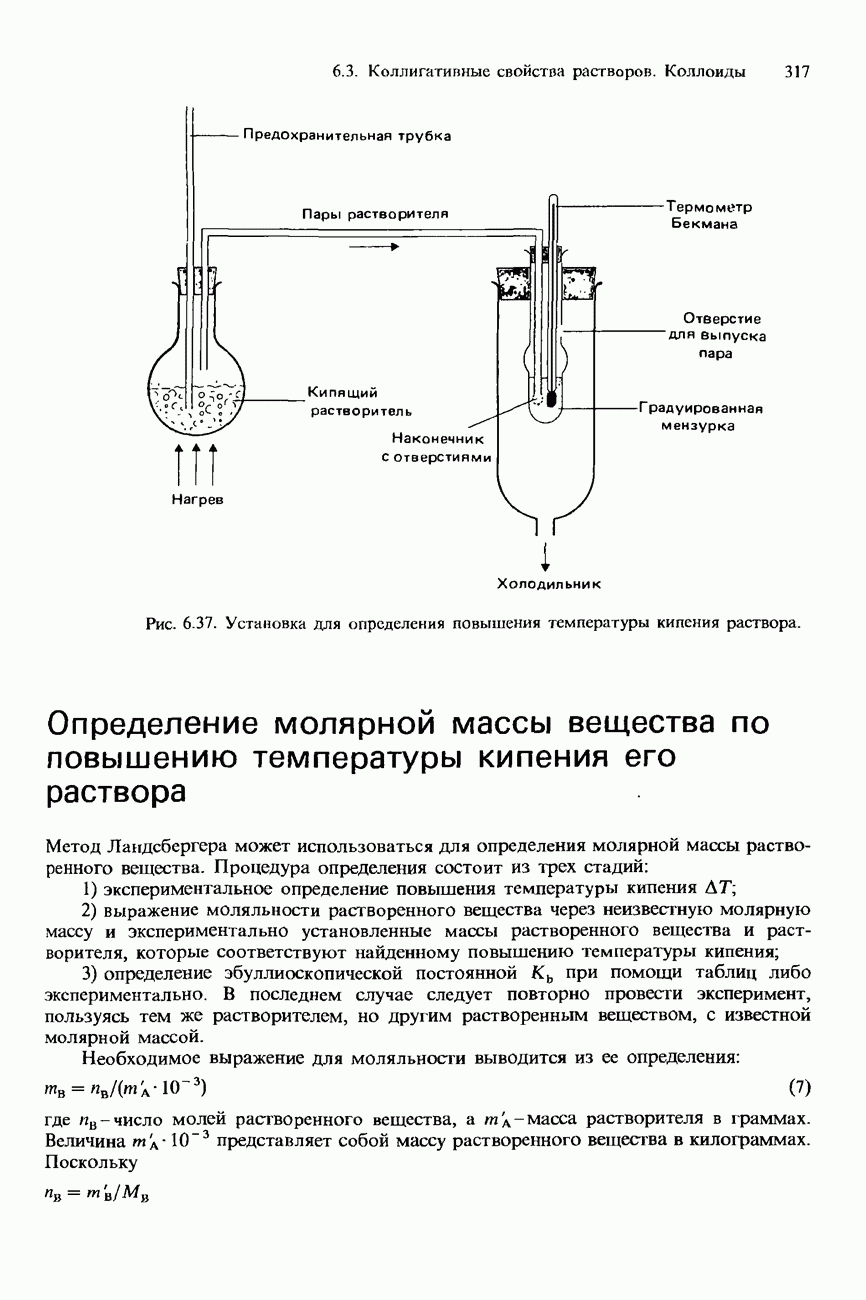
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
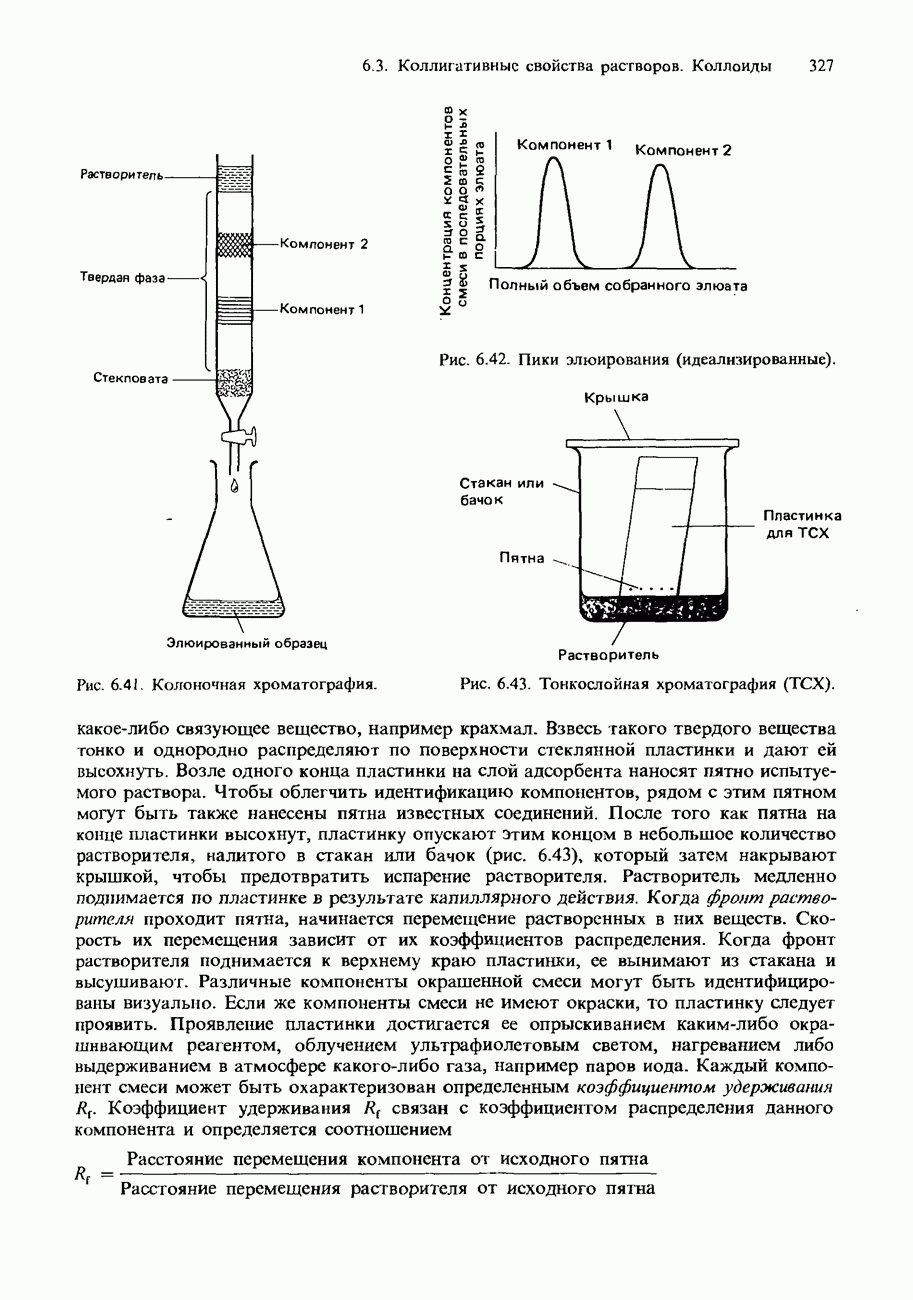
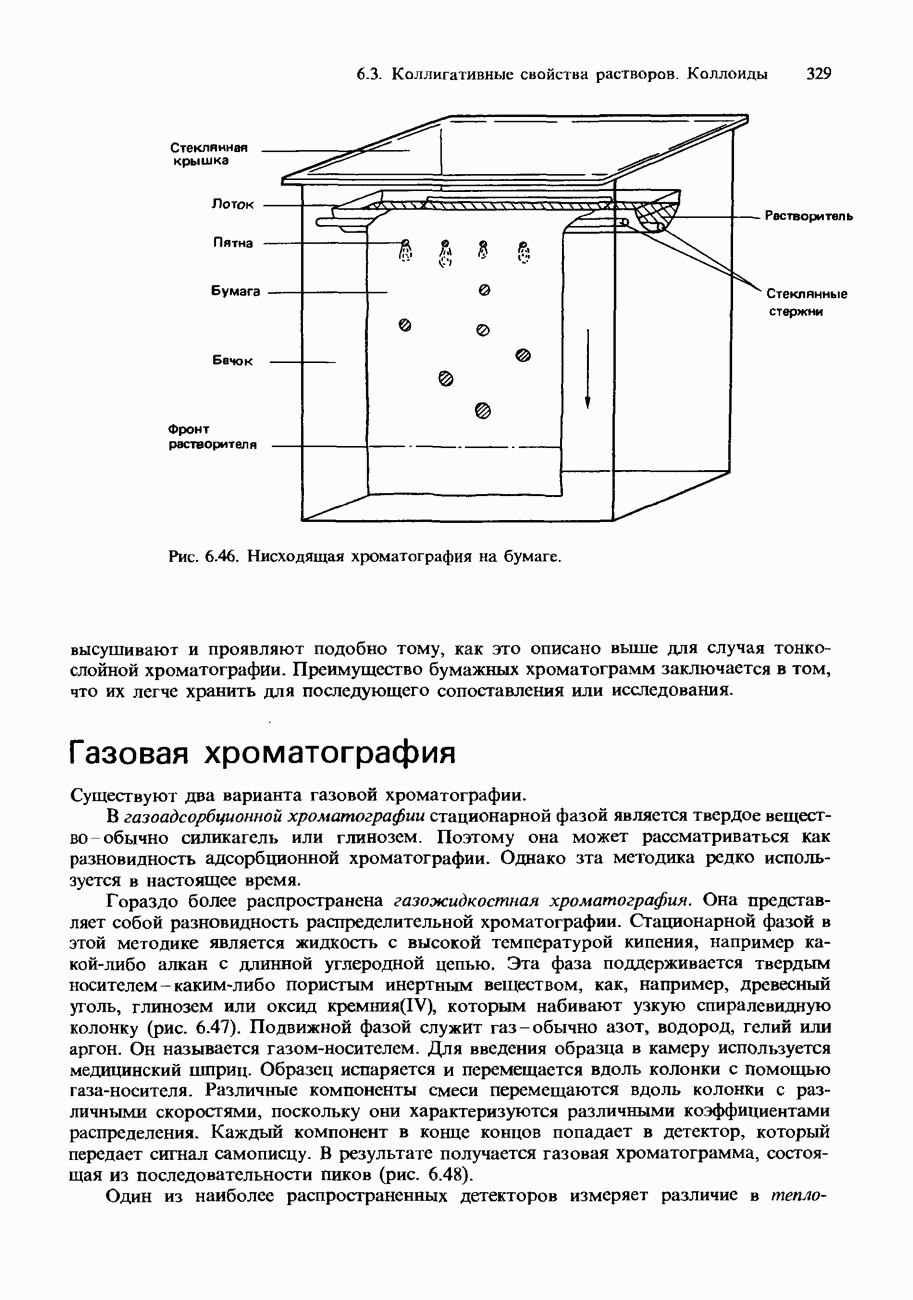
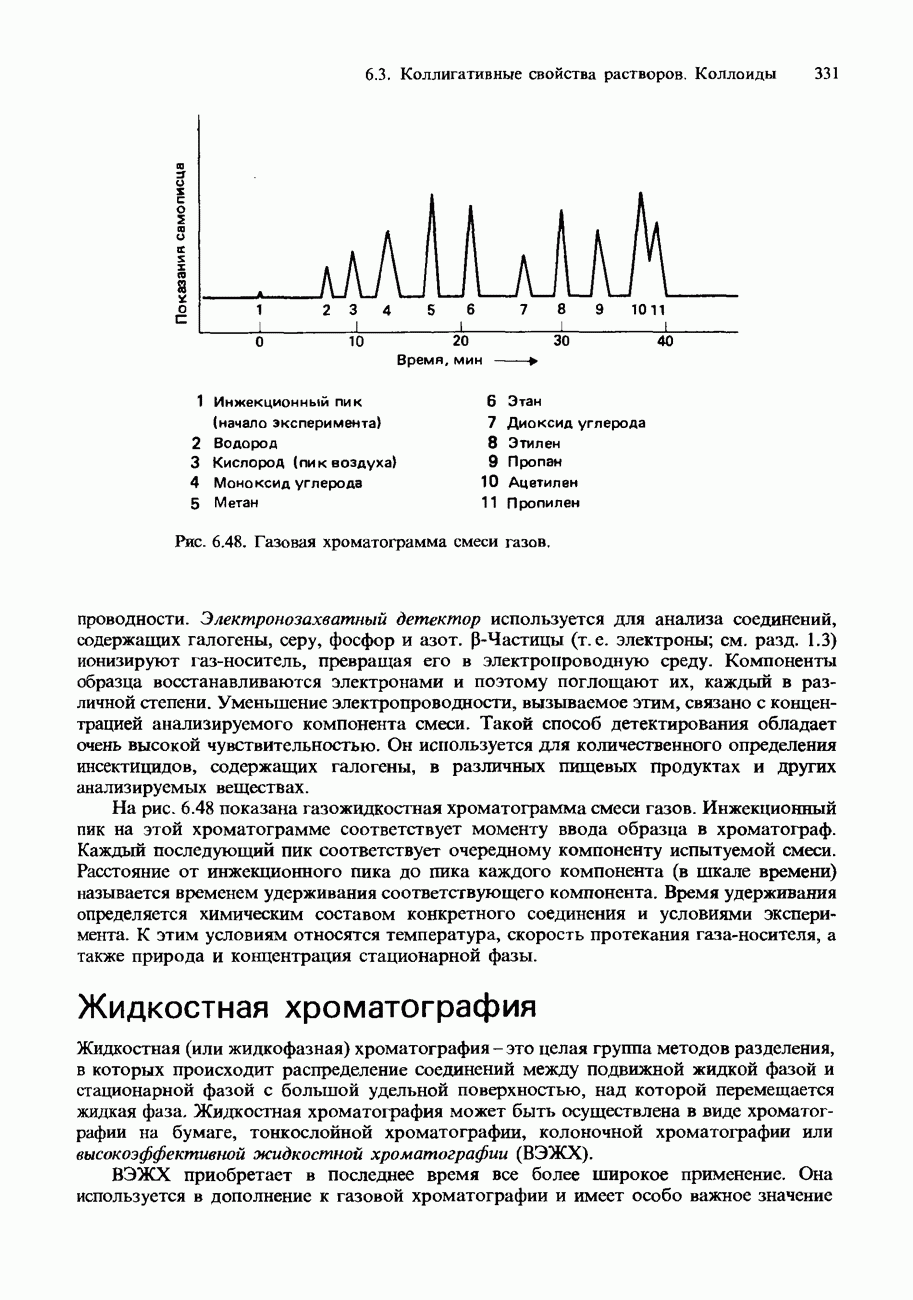
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
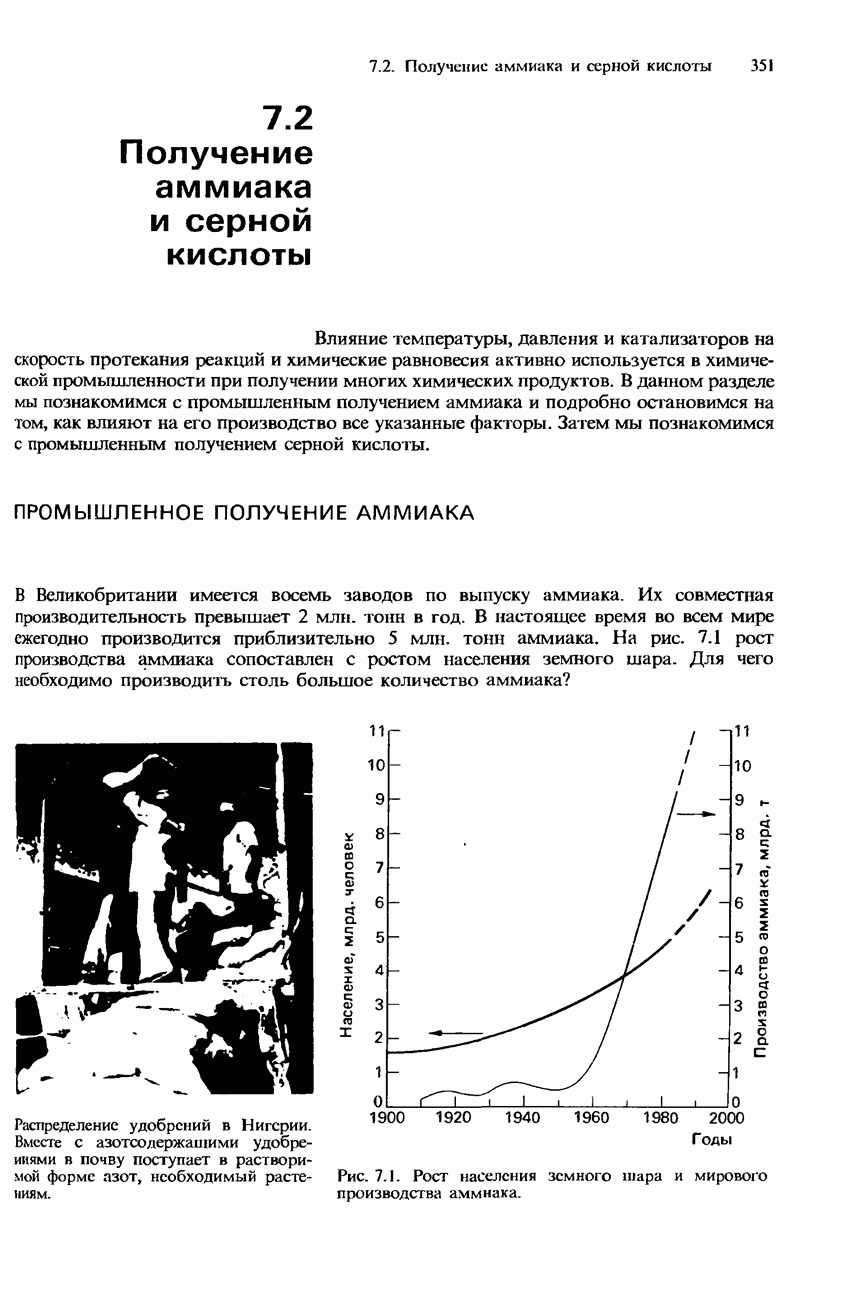
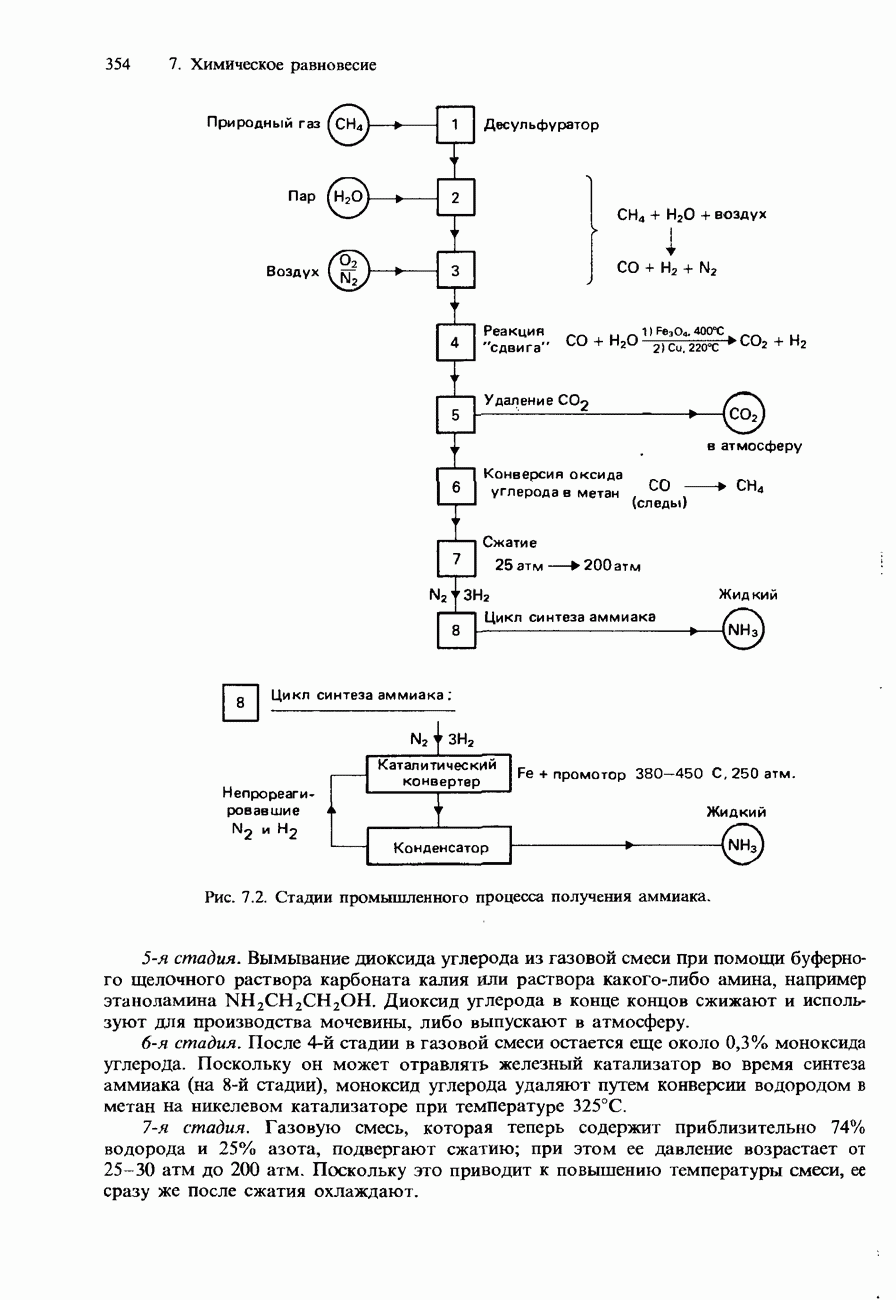
- 7.2. Получение аммиака и серной кислоты
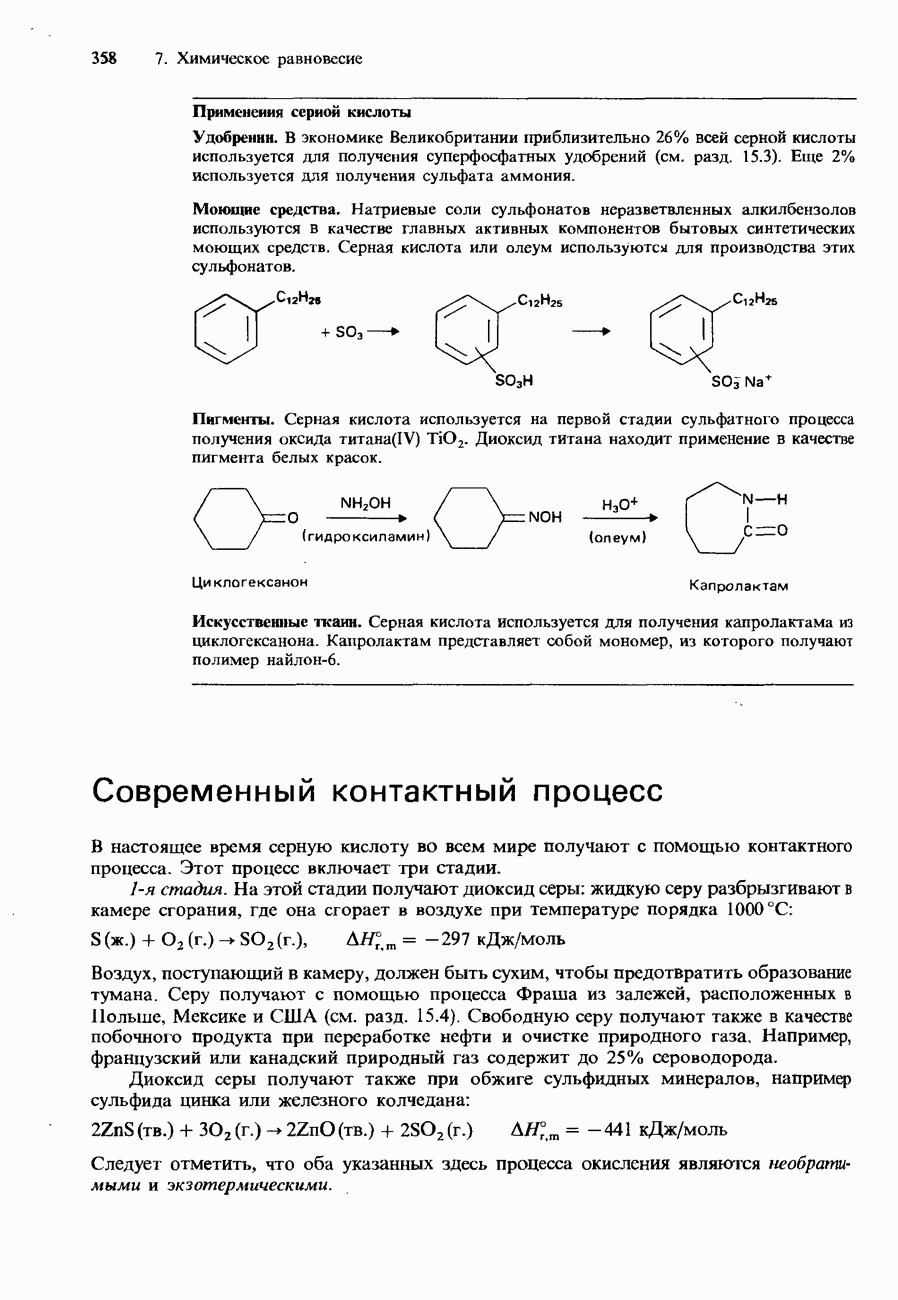
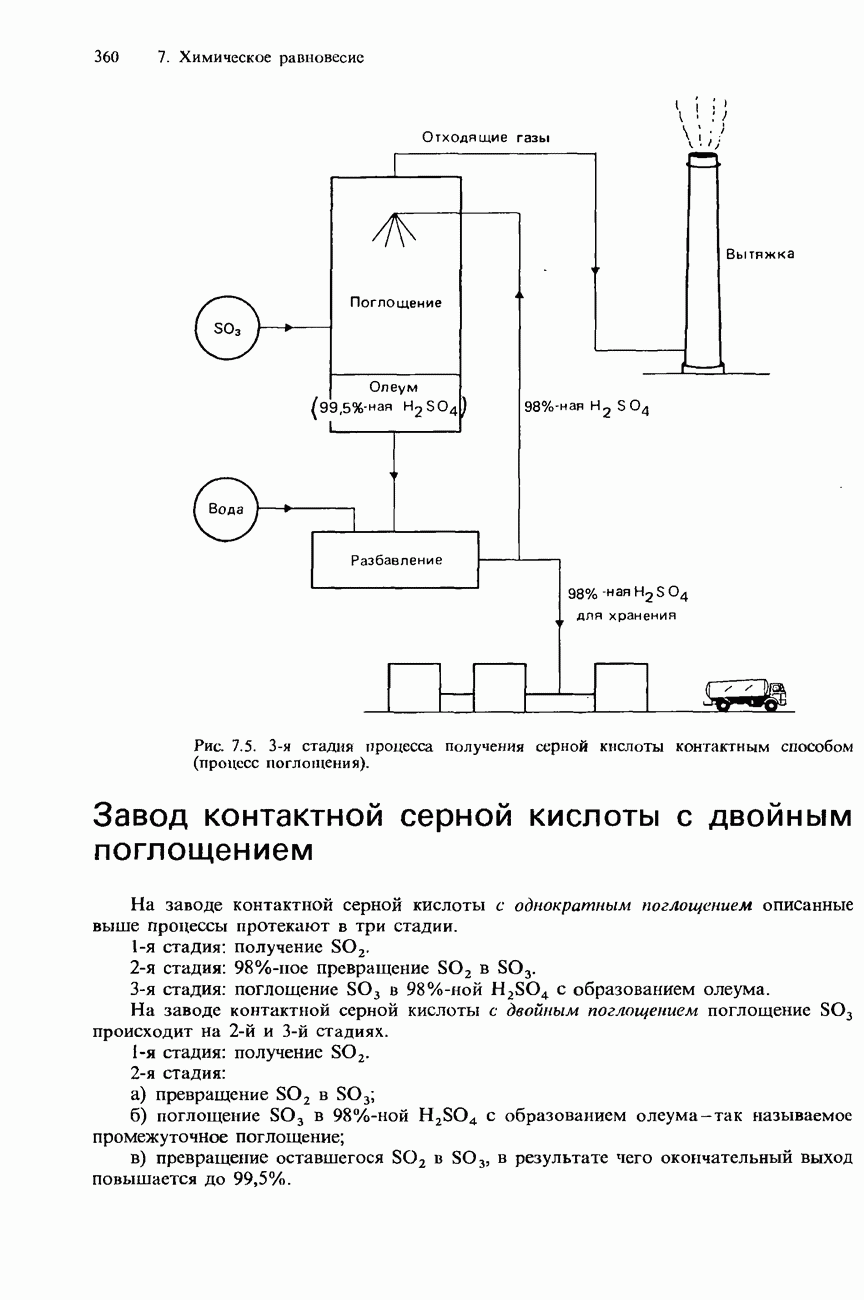
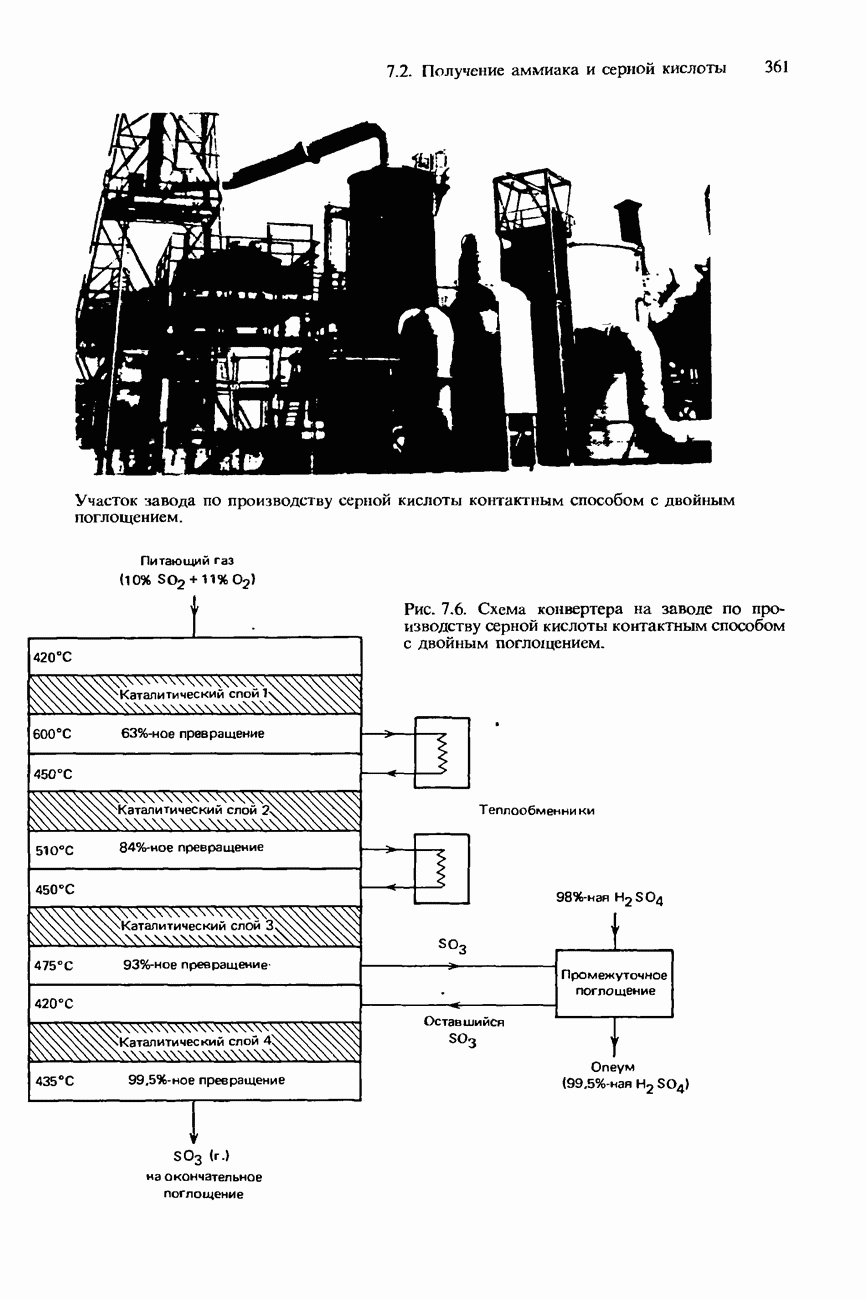
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
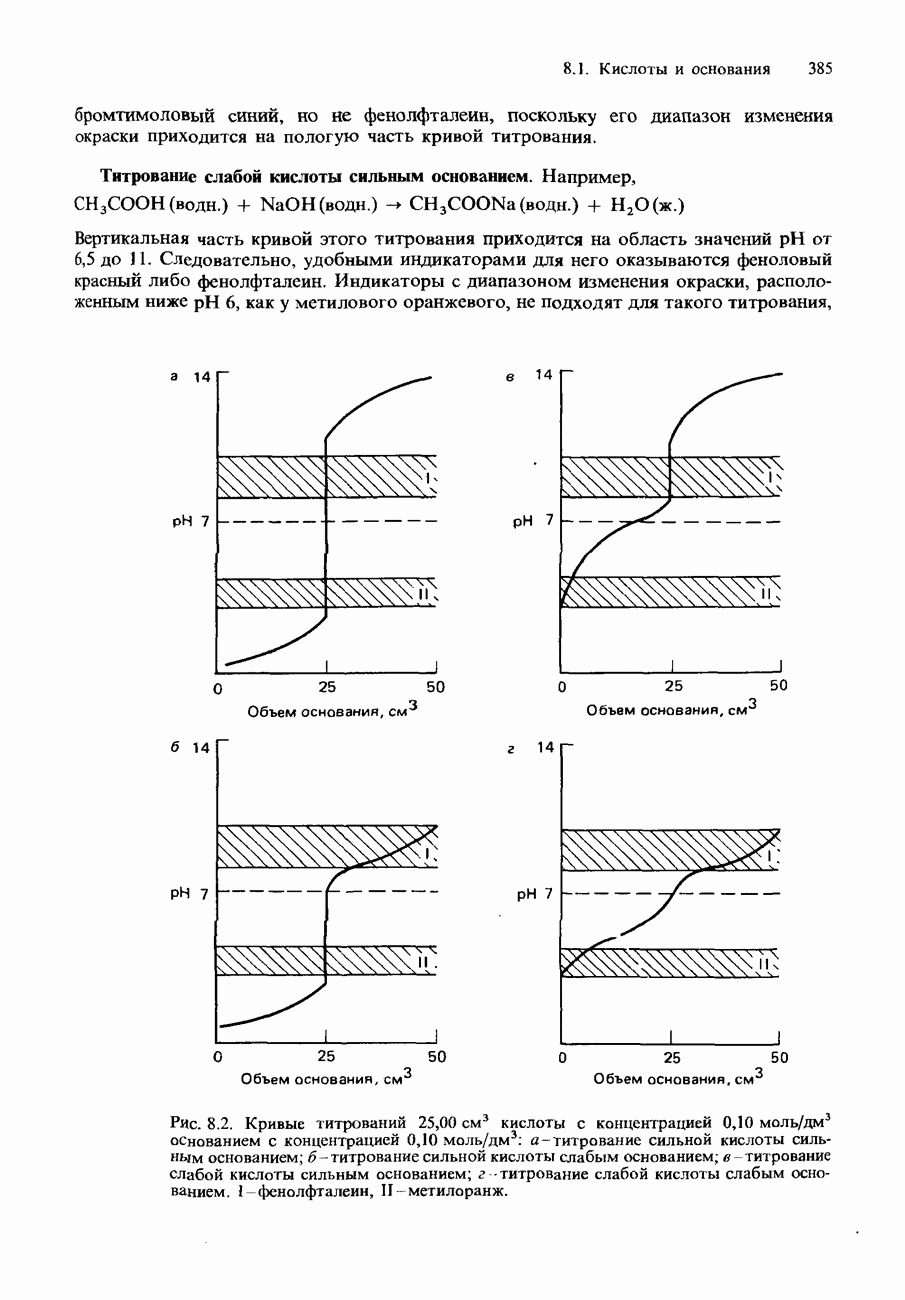
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
- 10.4. Химические источники тока
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
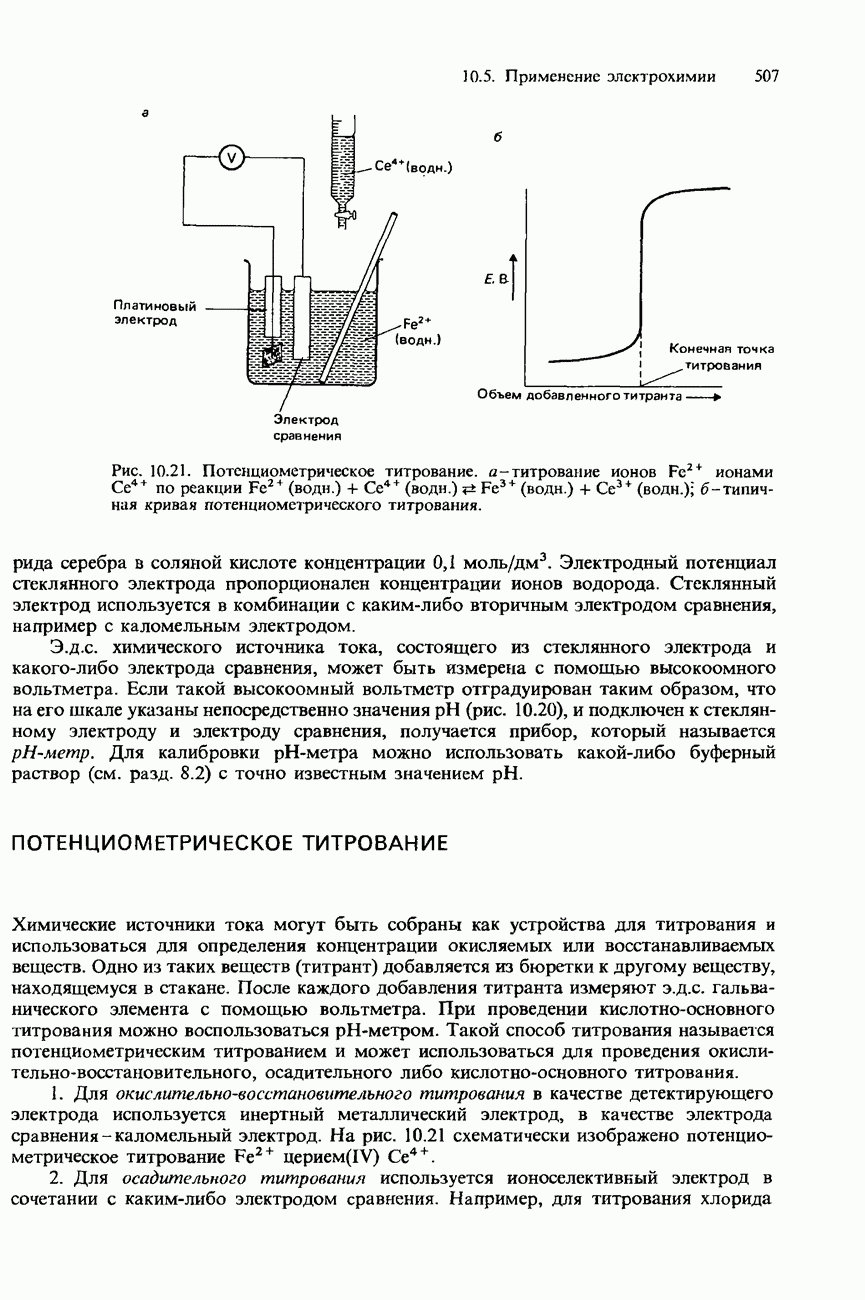
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
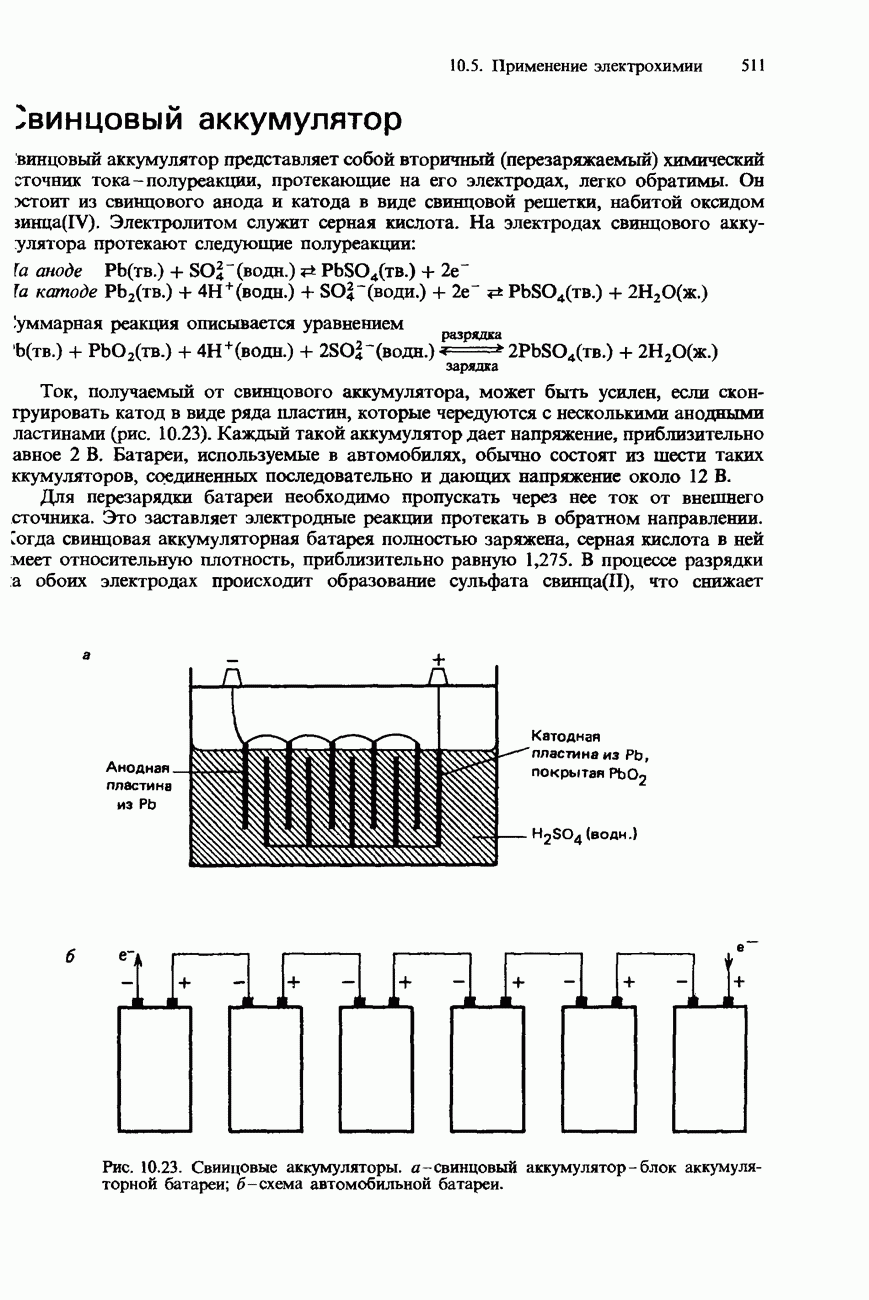
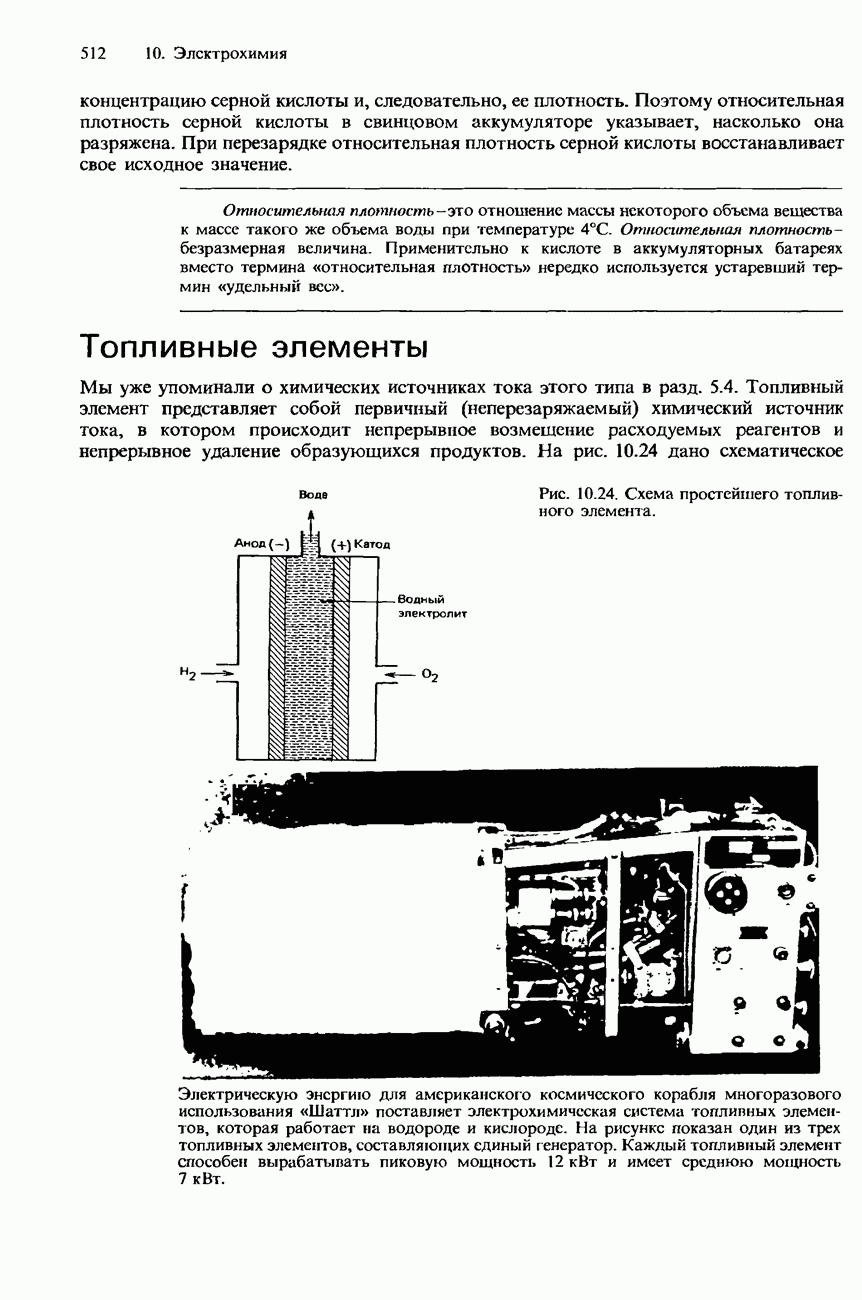
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ