| << Предыдущий параграф |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОПРОСЫ ДЛЯ ПРОВЕРКИ
1. а) Объясните смысл терминов электропроводность (проводимость) и молярная электропроводность (молярная проводимость), а также покажите с помощью соответствующих графиков, как по изменению молярной проводимости в зависимости от концентрации раствора можно получить сведения об относительной степени ионизации слабых и сильных электролитов.
б) 1) Кратко опишите, приведя соответствующий график, как осуществить кондуктометрическое титрование какого-либо окрашенного раствора раствором гидроксида натрия, если невозможно использовать кислотно-основные индикаторы.
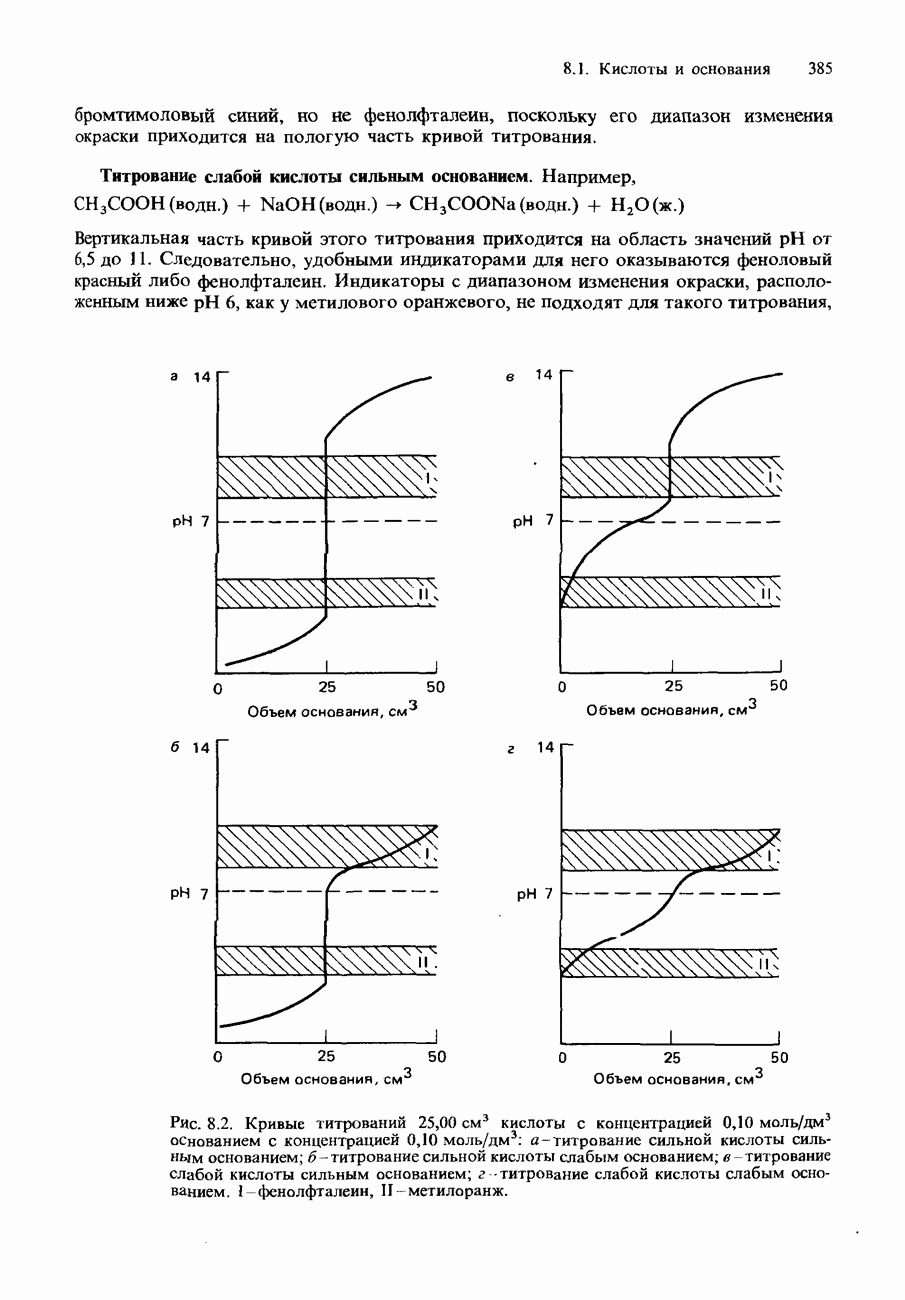
2) Кратко обсудите форму кривой потенциометрического титрования (графика зависимости проводимости от объема добавляемого основания) для случая титрования уксусной кислоты раствором гидроксида натрия. Постройте эту кривую для децимолярных растворов.
в) Исходя из того, что константа кислотности уксусной кислоты при  равна
равна  вычислите
вычислите  раствора до и после добавления 1,00 г ацетата натрия к
раствора до и после добавления 1,00 г ацетата натрия к  раствора уксусной кислоты.
раствора уксусной кислоты. 
г) Выведите закон разбавления Оствальда и покажите, каким образом он согласуется с ионной теорией электролитической диссоциации Аррениуса.
2. а) Объясните смысл следующих терминов: электролитическая проводимость (удельная проводимость); постоянная ячейки; молярная проводимость.
б) 1) В конкретной кондуктометрической ячейке водный раствор  концентрации
концентрации  имеет сопротивление 74,58 Ом. Исходя из того, что молярная проводимость этого раствора
имеет сопротивление 74,58 Ом. Исходя из того, что молярная проводимость этого раствора  равна
равна  определите постоянную ячейки.
определите постоянную ячейки.
2) При исследовании зависимости молярной проводимости А от концентрации с для водного раствора  были получены следующие данные:
были получены следующие данные:

Покажите, что эти данные соответствуют соотношению

где  - молярная проводимость раствора при бесконечном разбавлении, а - постоянная. Пользуясь приведенными данными, определите А" для
- молярная проводимость раствора при бесконечном разбавлении, а - постоянная. Пользуясь приведенными данными, определите А" для 
Для раствора ацетата калия  для раствора соляной кислоты
для раствора соляной кислоты  и для раствора хлорида калия
и для раствора хлорида калия  Ом
Ом  моль 1. Вычислите
моль 1. Вычислите  для уксусной кислоты и объясните, на чем основывался ваш расчет.
для уксусной кислоты и объясните, на чем основывался ваш расчет.
3. а) Объясните, что означает термин окисление, пользуясь представлением о переносе электронов.
Укажите степень (состояние) окисления хлора 1) в хлорид-ионе,
2) в хло-рат-ионе CIOJ.
б) Запишите полные ионные уравнения для следующих реакций:
1) газообразный хлор вытесняет иод из водного раствора, содержащего иодид-ионы;
2) твердый иод вытесняет газообразный хлор из водного раствора, содержащего хлорат-ионы  в то время как иод превращается в ионы
в то время как иод превращается в ионы 
в) При продувании газообразного хлора через горячий водный раствор гидроксида натрия образуется смесь хлорид-ионов и хлорат-ионов CIOJ. Составьте стехиометрическое ионное уравнение этой реакции со стехиометри-ческими коэффициентами.
Пользуясь представлениями об окислении и восстановлении, объясните, какую роль играет хлор в этой реакции, г) Ионы  содержащиеся в
содержащиеся в  водного раствора концентрации
водного раствора концентрации  были восстановлены химическим способом. Затем полученные частицы, содержащие вольфрам, были вновь превращены в их исходную форму на электроде электролитической ячейки в результате пропускания постоянного тока силой 0,100 А в течение
были восстановлены химическим способом. Затем полученные частицы, содержащие вольфрам, были вновь превращены в их исходную форму на электроде электролитической ячейки в результате пропускания постоянного тока силой 0,100 А в течение  мин.
мин.
1) На каком электроде происходило повторное окисление - положительном или отрицательном?
2) Сколько молей вольфрама находится в  водного раствора WOJ концентрации
водного раствора WOJ концентрации 
3) Сколько молей электронов приняло участие в процессе повторного окисления? (Постоянная Фарадея 
4) Сравнивая свои ответы на вопросы 2 и 3, определите степень окисления вольфрама в восстановленной форме. (Можно принять предположение, что степень окисления кислорода в этом процессе остается неизменной.)
5) Запишите ионное уравнение со стехиометрическими коэффициентами для одной из двух реакций окисления или восстановления.
4. а) Обсудите, основываясь на конкретных примерах, какой смысл имеют термины окисление и восстановление, при помощи представлений о переносе электронов.
Как вы понимаете термин окислительно-восстановительная реакция?
б) Что означает термин диспропорционирование?
Приведите пример такой реакции.
в) Обсудите, в каких пределах возможно использование таблицы стандартных электродных потенциалов для предсказания направления химического превращения.
г) Водный раствор ванадата аммония восстанавливают кипячением с цинковым порошком. Полученный раствор можно подвергнуть повторному окислению с образованием ванадат-ионов, обрабатывая его раствором манганата  калия. Опишите эксперименты, которые необходимо провести для этого, и последующее использование экспериментальных данных для того, чтобы определить изменение степени окисления ванадия.
калия. Опишите эксперименты, которые необходимо провести для этого, и последующее использование экспериментальных данных для того, чтобы определить изменение степени окисления ванадия.
5. а) При растворении нитрата калия в чистой серной кислоте образуется раствор, имеющий высокую электропроводность, и физические измерения показывают, что из каждого моля нитрата калия образуется шесть молей частиц растворенного вещества.
1) Как можно объяснить эти экспериментальные данные?
2) Какой физический метод мог быть использован для определения числа частиц, образующихся при растворении нитрата калия?
3) Как можно использовать указанный раствор в органической химии?
б) После разбавления водой раствора, который указан в части (а), его помещения в катодное отделение электролитической ячейки и пропускания в течение некоторого времени электрического тока происходит восстановление азотсодержащих частиц, и из восстановленного электролита можно выделить соль 
После обработки одного моля этой соли двумя молями гидроксида натрия можно выделить соединение, содержащее только N, Н и О; его относительная молекулярная масса равна 33, и оно содержит 
Какую химическую формулу имеет  Какова структура
Какова структура 
в) При титровании 5 ммолей указанной соли раствором  калия в разбавленной серной кислоте для окисления соли требуется 6 ммолей
калия в разбавленной серной кислоте для окисления соли требуется 6 ммолей  и в качестве конечного продукта восстановления
и в качестве конечного продукта восстановления  образуется
образуется  ммоль
ммоль  моля.)
моля.)
Какова степень окисления азота в продукте реакции с 
6. а) Определите стехиометрические коэффициенты в уравнениях указанных ниже окислительно-восстановительных реакций, учитывая либо перенос электронов,
либо изменение степени окисления:

б) Кратко обсудите электролиз каждого из следующих растворов:

в) 1) Через расплавленный оксид алюминия пропускали ток силой 3,21 А в течение 10 мин. Объем газообразного кислорода, собранного на аноде, составил  при нормальных условиях. Вычислите массу алюминия, выделившегося на катоде, а также заряд 1 моля электронов (постоянную Фарадея).
при нормальных условиях. Вычислите массу алюминия, выделившегося на катоде, а также заряд 1 моля электронов (постоянную Фарадея).

При пропускание такого же количества электричества через расплавленный хлорид некоторого металла М (относительная атомная масса 137,3) масса полученного металла М составила 1,373 г. Вычислите заряд катиона 
Заряд электрона равен  Кл. Вычислите значение постоянной Авогадро
Кл. Вычислите значение постоянной Авогадро 
Стандартные электродные потенциалы трех металлов X, Y не равны  В соответственно. Укажите, какой из металлов, X или Y, должен служить более эффективной защитой железа от коррозии, и объясните ответ.
В соответственно. Укажите, какой из металлов, X или Y, должен служить более эффективной защитой железа от коррозии, и объясните ответ.
7. Промышленное получение кальция основано на электролизе расплава хлорида кальция.
а) Запишите ионное уравнение реакции получения кальция.
б) Какая масса кальция получится при пропускании тока силой 20 А в течение 32 мин 10 с?
8. а) Для получения частиц золя могут использоваться процессы диспергирования или конденсации. Какая разница между этими двумя процессами? Опишите, как осуществляется получение золя гидроксида  либо сульфида мышьяка с помощью одного из этих процессов.
либо сульфида мышьяка с помощью одного из этих процессов.
б) Указанные золи следует освободить от наличия в них каких-либо электролитов, образовавшихся в процессе их получения, с помощью процесса, который называется диализ.
1) Объясните, для чего необходимо удаление электролита, и опишите этот процесс.
2) Какими двумя правилами характеризуется коагуляция коллоидов (эти правила иногда называют правилами Гарди-Шульца).
в) Для коллоидов типичны электрофорез и эффект Тиндаля. Опишите и объясните эти явления, используя в качестве примера золь, получение которого было описано вами при ответе на вопрос (а).
9. а) Кратко объясните, как представление об окислении и восстановлении было развито в представление о них как о реакциях электронного переноса, б) Объясните, какой смысл имеет следующая схематическая запись химического источника тока:

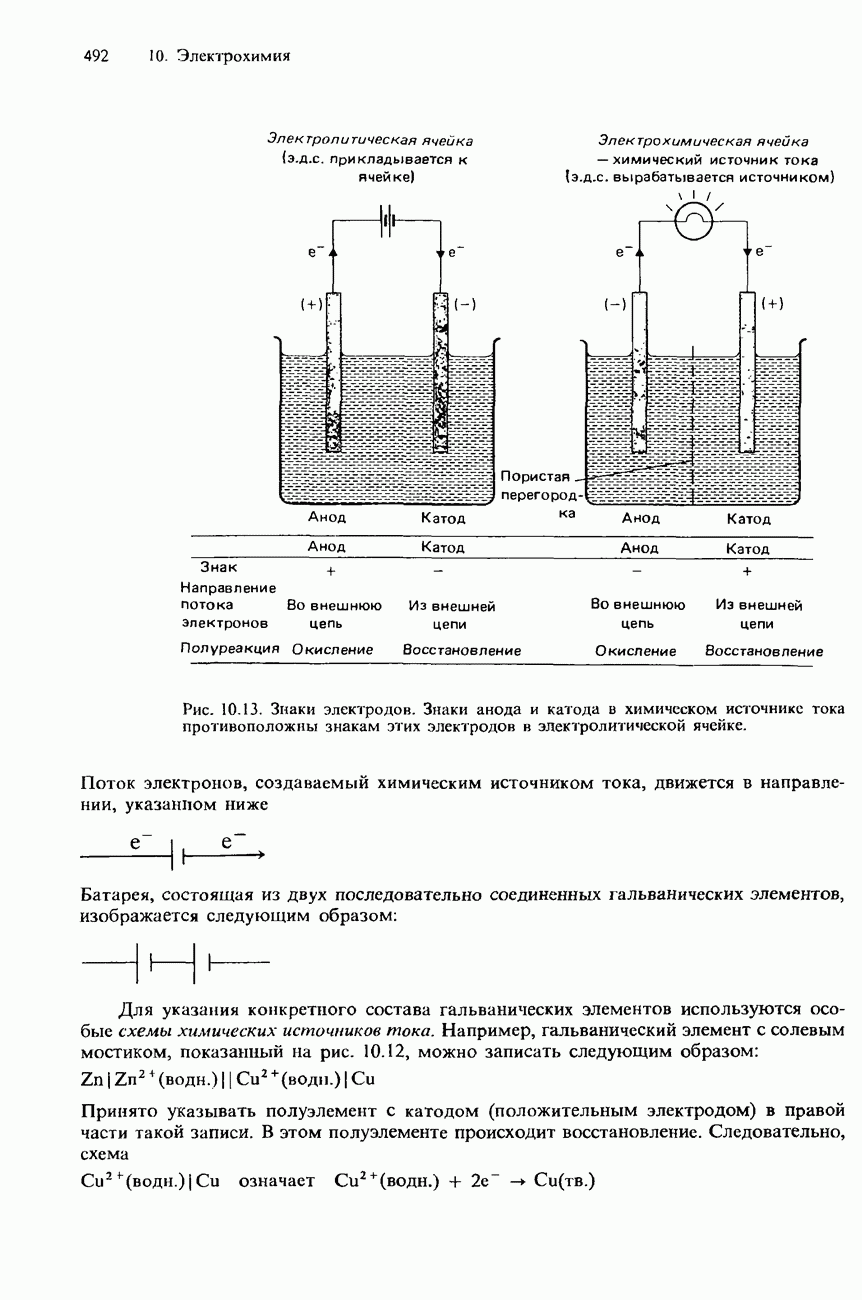
Приведите схему этого источника тока и укажите соответствующими надписями его важнейшие части.
Объясните смысл терминов анод и катод и укажите на вашем рисунке направление потока электронов во внешней цепи, а также анод и катод.
Покажите, как следует вычислить электродвижущую силу обсуждаемого источника тока, используя указанные значения относительных стандартных электродных потенциалов при 298 К:

Какие еще сведения требуются обычно для такого расчета?
в) Что должно произойти при введении ионов  виде солей) в раствор, который содержит, кроме того, избыток разбавленной серной кислоты. Воспользуйтесь для этого следующими значениями стандартных окислительно-восстановительных потенциалов, относящимися к 298 К:
виде солей) в раствор, который содержит, кроме того, избыток разбавленной серной кислоты. Воспользуйтесь для этого следующими значениями стандартных окислительно-восстановительных потенциалов, относящимися к 298 К:

Запишите порознь иониые уравнения реакций для каждого из реагентов и используйте их для получения окончательного уравнения реакции.
г) 2,8 г чистой железной проволоки растворили в отсутствие воздуха в избытке разбавленной серной кислоты, к которой было добавлено 2,00 г  калия (перманганат калия). Какой из твердых реагентов оказался в избытке и в каком количестве?
калия (перманганат калия). Какой из твердых реагентов оказался в избытке и в каком количестве? 
Опишите, указывая только важнейшие практические подробности, как используется раствор  калия в титриметрическом (волюметрическом) анализе, и укажите какое-либо важное ограничение для его использования с этой целью.
калия в титриметрическом (волюметрическом) анализе, и укажите какое-либо важное ограничение для его использования с этой целью.
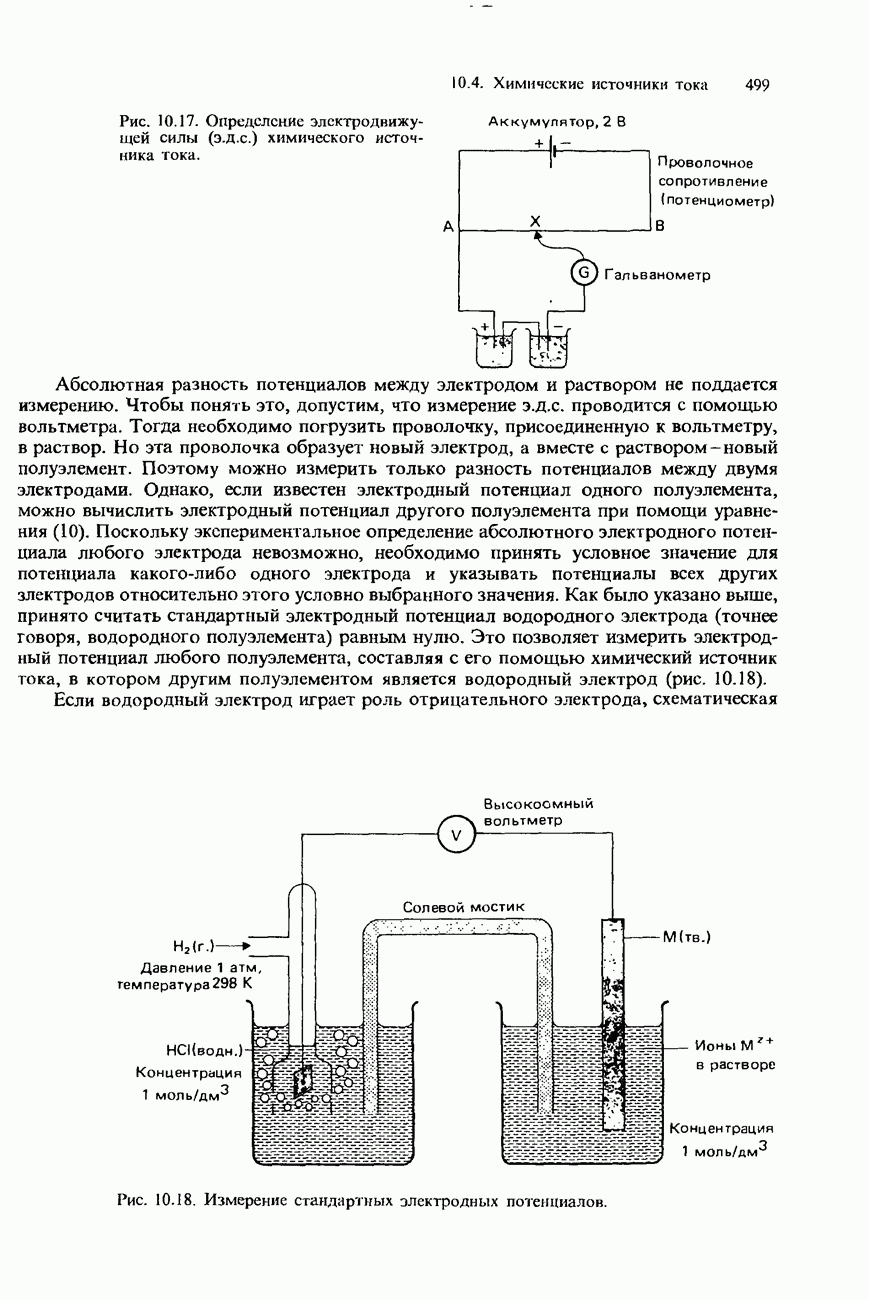
10. Стандартный электродный потенциал для электрода  измеряют непосредственно соединением двух полуэлементов с помощью солевого мостика.
измеряют непосредственно соединением двух полуэлементов с помощью солевого мостика.
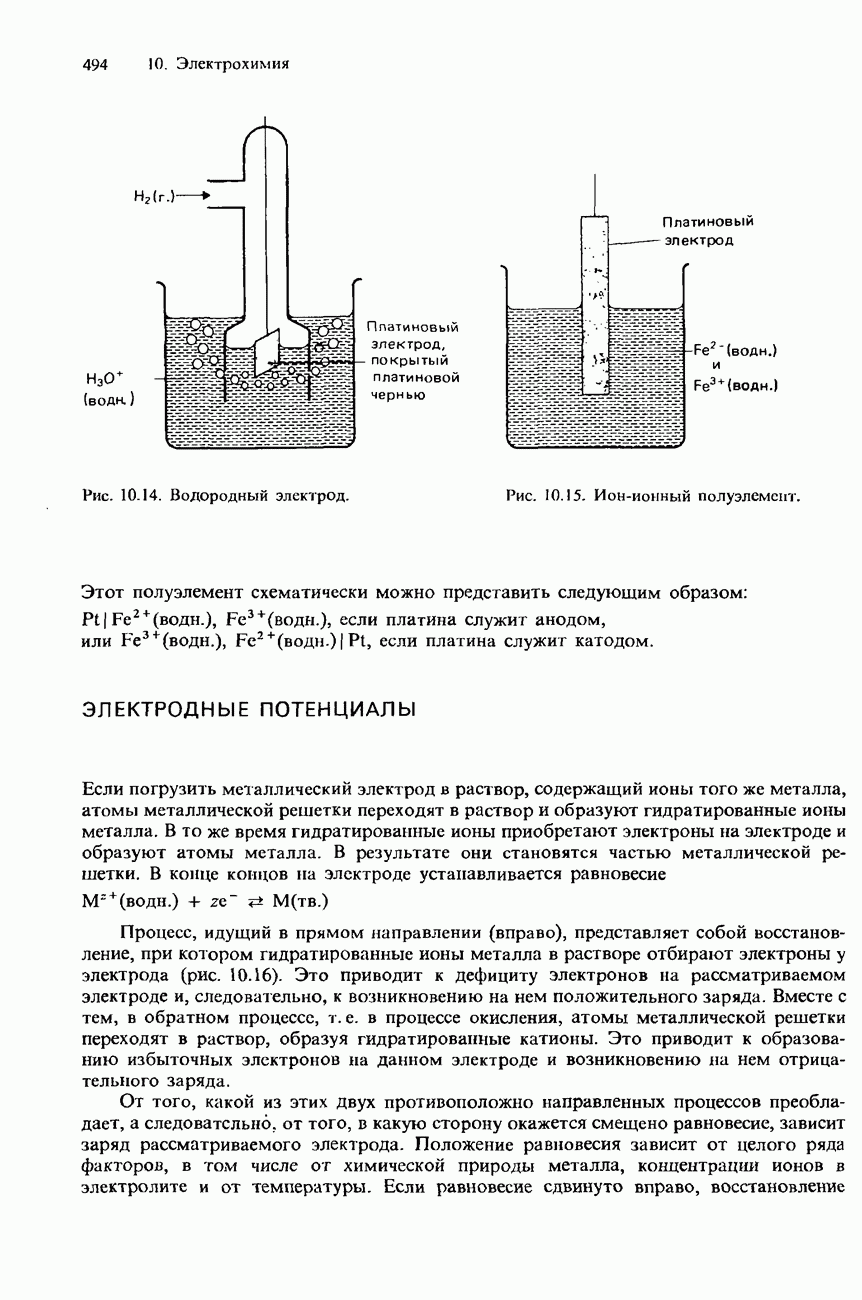
а) Какие химические вещества могут быть использованы в полуэлементе  и какие условия необходимы для этого?
и какие условия необходимы для этого?
б) Какие химические вещества могут быть использованы в другом полуэлементе и какие условия необходимы для этого?
в) Каково назначение солевого мостика и чем он может быть наполнен?
г) Каково, по определению, значение электродного потенциала для стандартного полуэлемента, указанного вами в ответе на вопрос 
д) Запишите уравнения реакций, протекающих в каждом из двух полуэлементов, указывая в них состояния окисления либо ионные заряды.
11. а) Дайте определение термина стандартный электродный потенциал и объясните причину возникновения разности потенциалов между каким-либо металлом и раствором одной из его солей, б) В химическом источнике тока

протекает реакция

Какое влияние (увеличение, уменьшение либо отсутствие эффекта) должны оказать на напряжение источника тока следующие изменения (приведите обоснование своих ответов):
1) увеличение концентрации 
2) одновременное увеличение концентрации  в одинаковое число раз;
в одинаковое число раз;
3) добавление твердого серебра;
4) добавление некоторого количества хлорида натрия в раствор, содержащий ионы 
5) добавление избытка цианида калия в раствор, содержащий ионы 
Опишите, какие методы, прямые и косвенные, могут использоваться для определения констант равновесия.
Для реакции

а) Приведите схематическую запись источника тока, в котором протекает указанная реакция, и на основании ее определите стандартный электродный потенциал такого источника.
б) Вычислите изменение свободной энергии, которым сопровождается указанная реакция, при стандартных условиях.
в) Вычислите  для указанной реакции.
для указанной реакции.
13. а) Опишите, какие методы используются для извлечения следующих металлов:
1) натрия из хлорида натрия, 2) цинка из сульфида  ртути из сульфида
ртути из сульфида  описание промышленной установки приводить не требуется.)
описание промышленной установки приводить не требуется.)
б) Объясните, с учетом легкости восстановления, почему для извлечения указанных в пункте (а) металлов используются неодинаковые методы.
в) Объясните, почему для извлечения магния из хлорида магния не удалось бы вытеснять этот металл натрием.
г) Постройте диаграмму, позволяющую объяснить важнейшие особенности металлической связи. Выбрав два характерных физических свойства металлов, объясните их на основе представлений о металлической связи.
д) Объясните, почему нанесение цинкового покрытия на поверхность железа лучше предохраняет его от коррозии, чем нанесение оловянного покрытия.
14. а) Укажите один из механизмов ржавления железа и объясните, на чем основан какой-либо из методов защиты железа от коррозии.
б) Обсудите протекание реакций между железом и 1) газообразным хлором,
2) водным раствором соляной кислоты.
в) Железо реагирует с расплавленным гидроксидом калия в присутствии воздуха, образуя соединение Z, которое растворяется в воде; при этом получается раствор пурпурной окраски.
1) Образец водного раствора, содержащего 19,8 г Z и приблизительно 200 г серной кислоты в  восстанавливали избыточным количеством цинка. Образец восстановленного раствора объемом
восстанавливали избыточным количеством цинка. Образец восстановленного раствора объемом  обесцвечивает
обесцвечивает  раствора
раствора  калия, имеющего концентрацию
калия, имеющего концентрацию  Запишите уравнение реакции окисления
Запишите уравнение реакции окисления  в кислом растворе и вычислите число молей железа в
в кислом растворе и вычислите число молей железа в  исходного раствора вещества
исходного раствора вещества 
Образец исходного раствора Z объемом  был обесцвечен
был обесцвечен  раствора сульфата
раствора сульфата  имеющего концентрацию
имеющего концентрацию  Полученный в результате смешивания раствор имел желтую окраску, и при добавлении в него водного раствора аммиака в нем образовывался красновато-коричневый осадок.
Полученный в результате смешивания раствор имел желтую окраску, и при добавлении в него водного раствора аммиака в нем образовывался красновато-коричневый осадок.
Какова степень окисления железа в соединении 
Предположите, какую формулу имеет соединение Z, если известно, что оно содержит приблизительно 39% калня по массе.
| << Предыдущий параграф |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
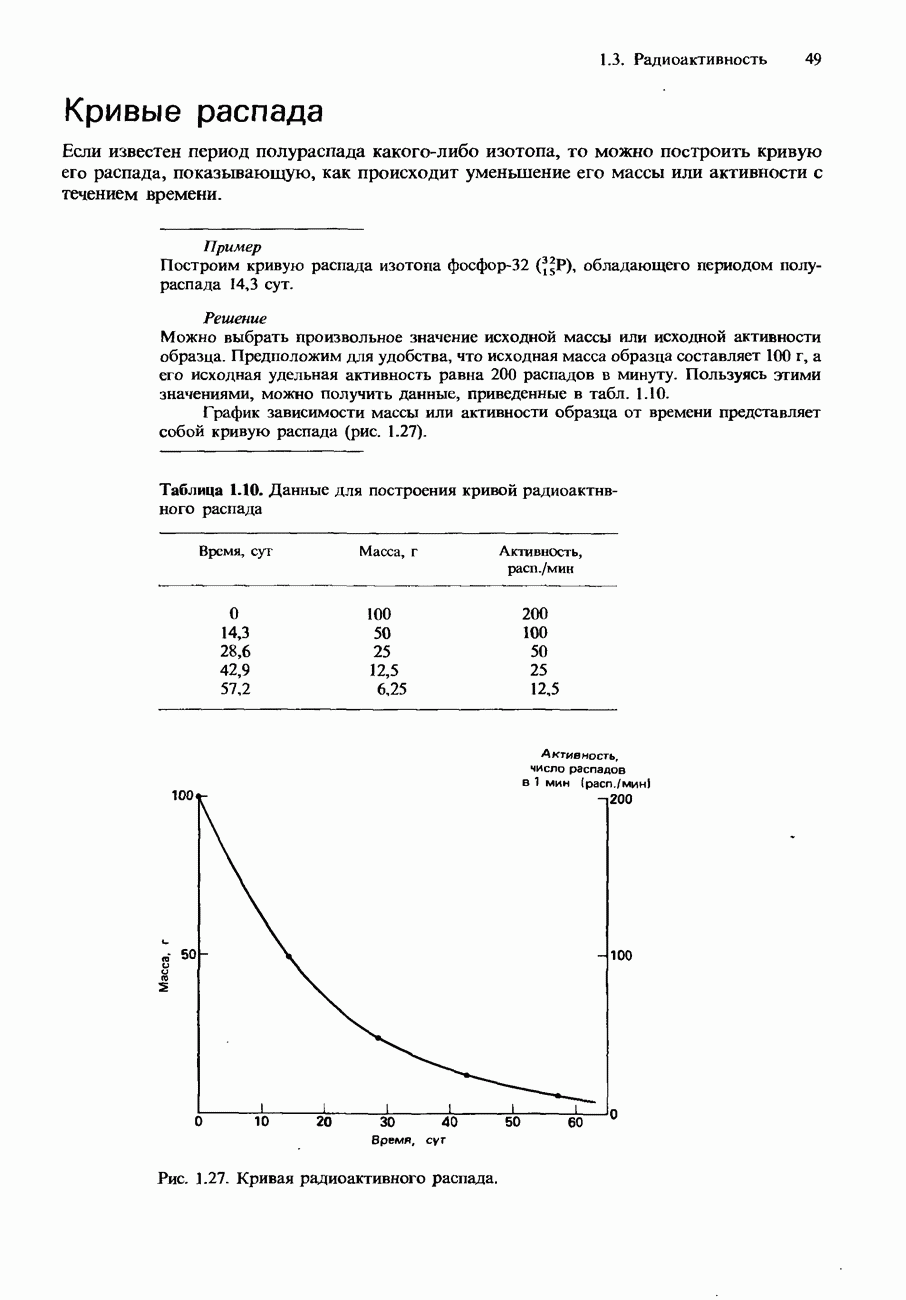
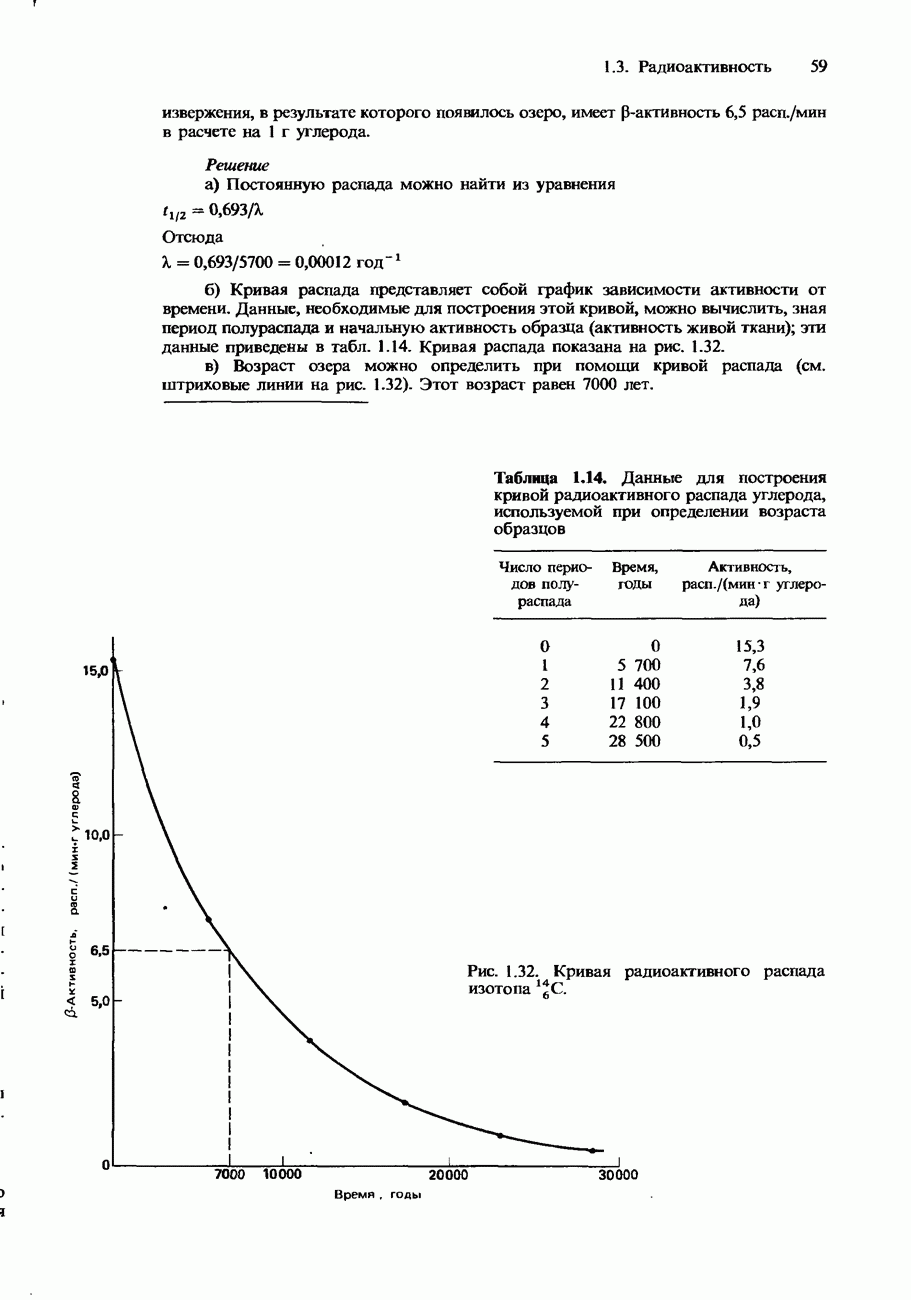
- Кривые распада
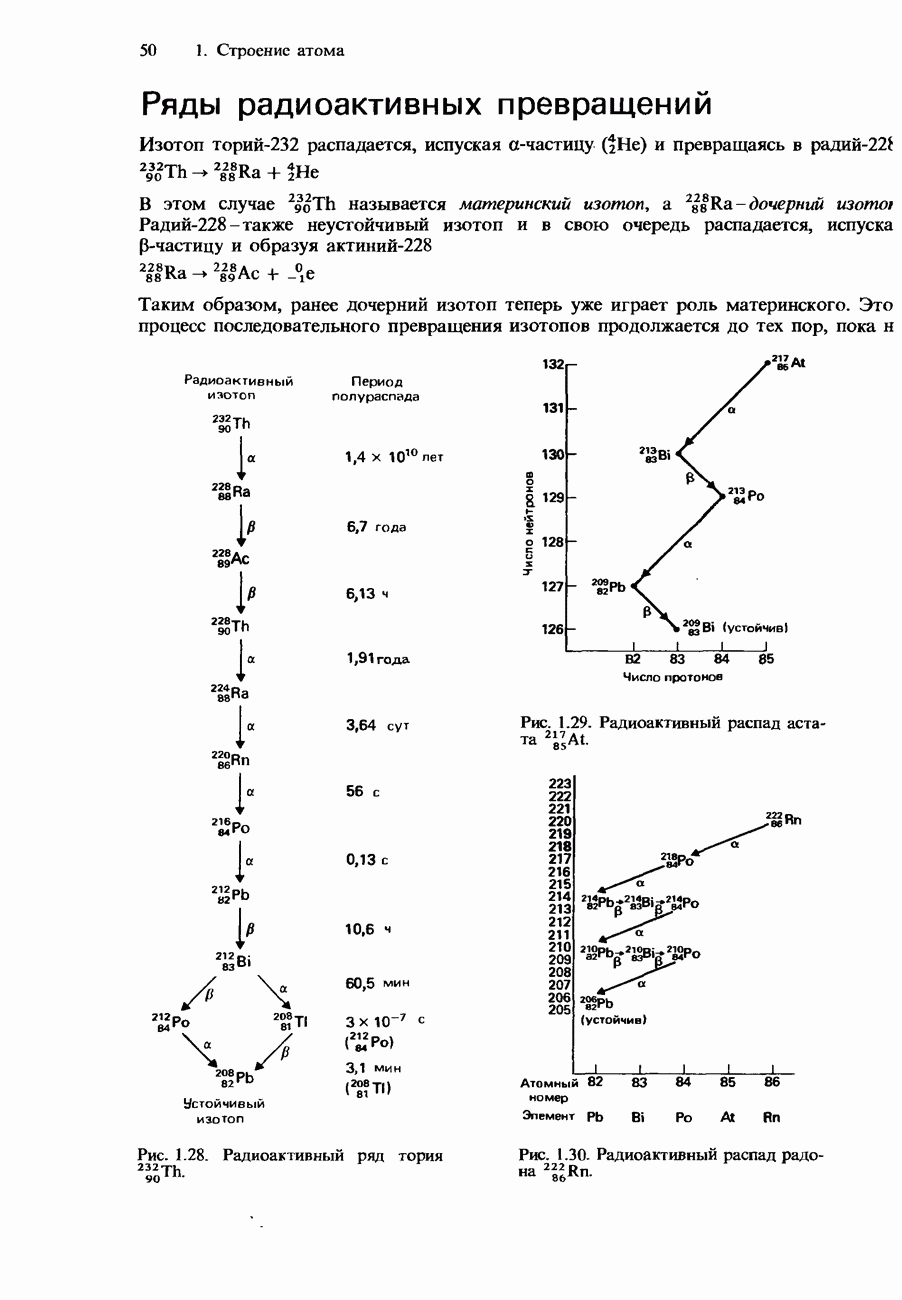
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
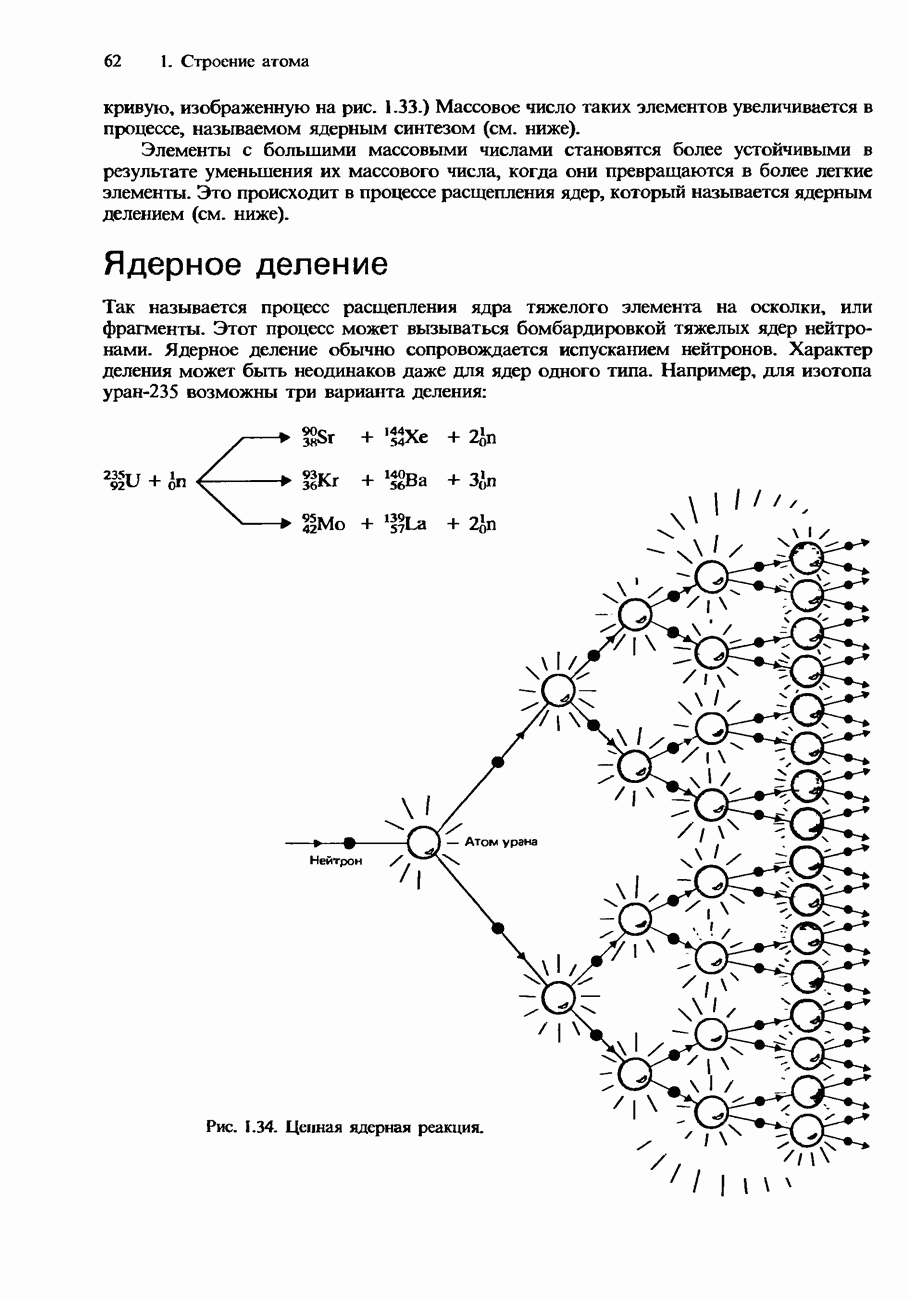
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
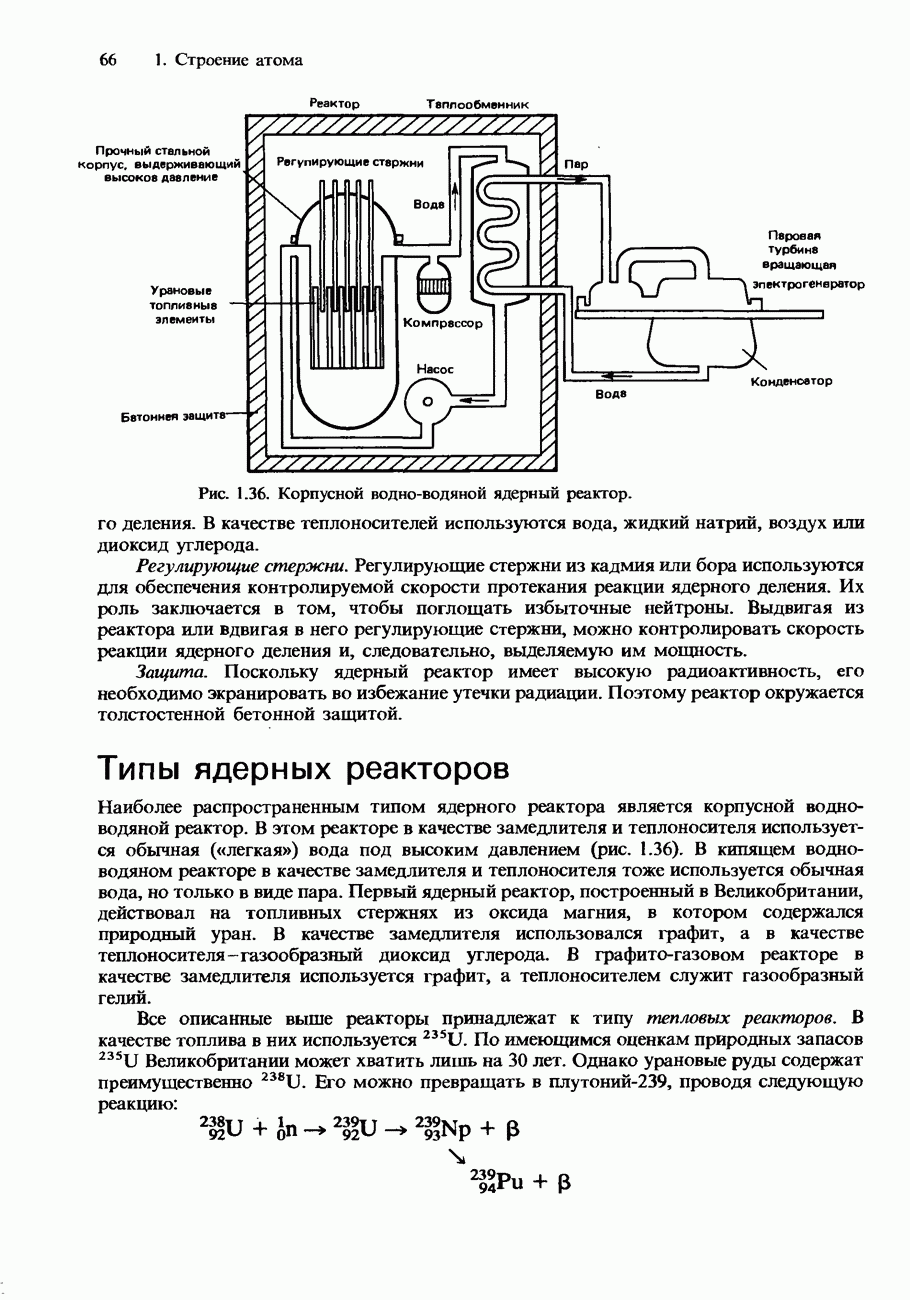
- Типы ядерных реакторов
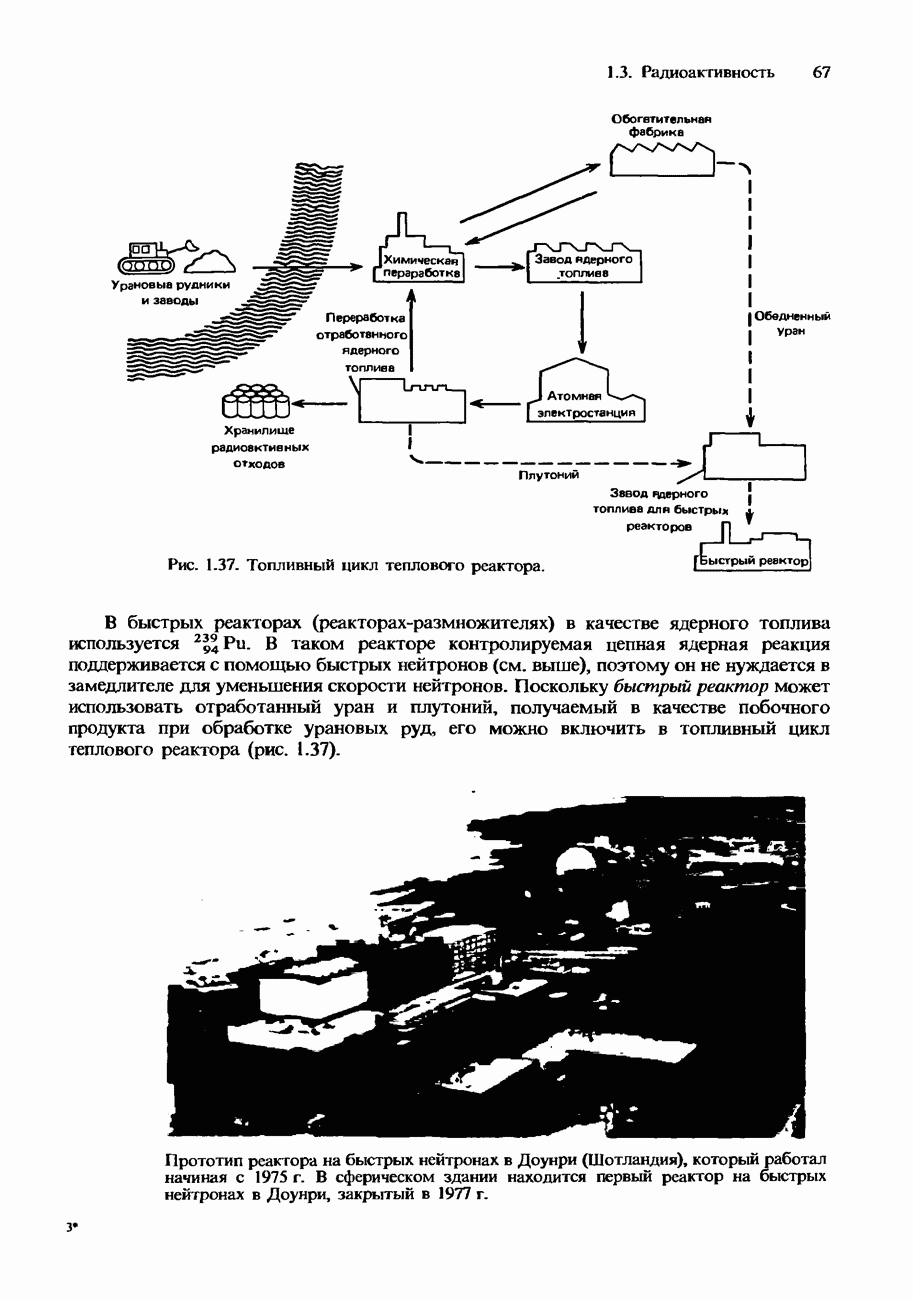
- Радиоактивные ядерные отходы и их переработка
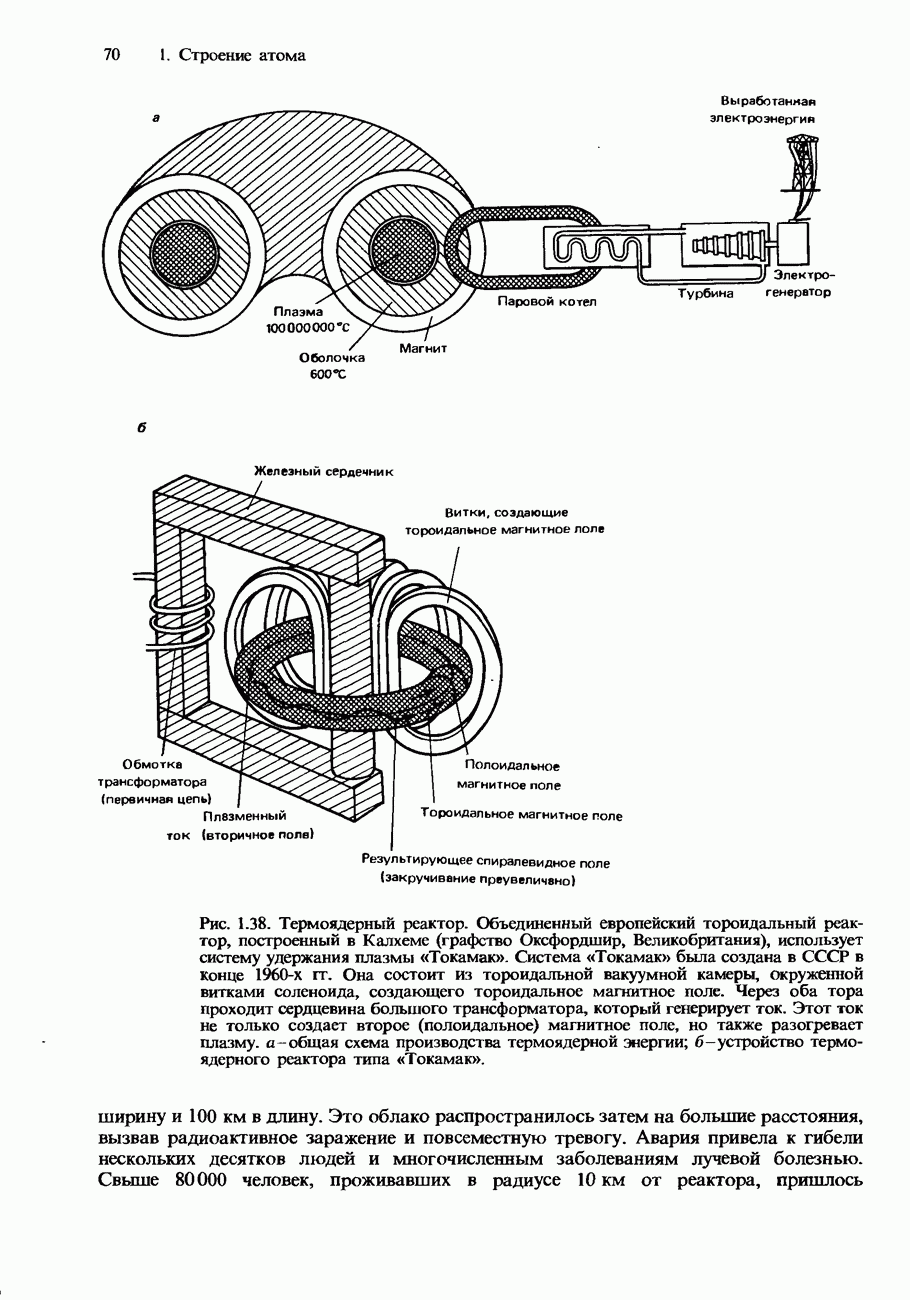
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
- Молекулярные орбитали
- Гибридные атомные орбитали
- Делокализованные орбитали
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
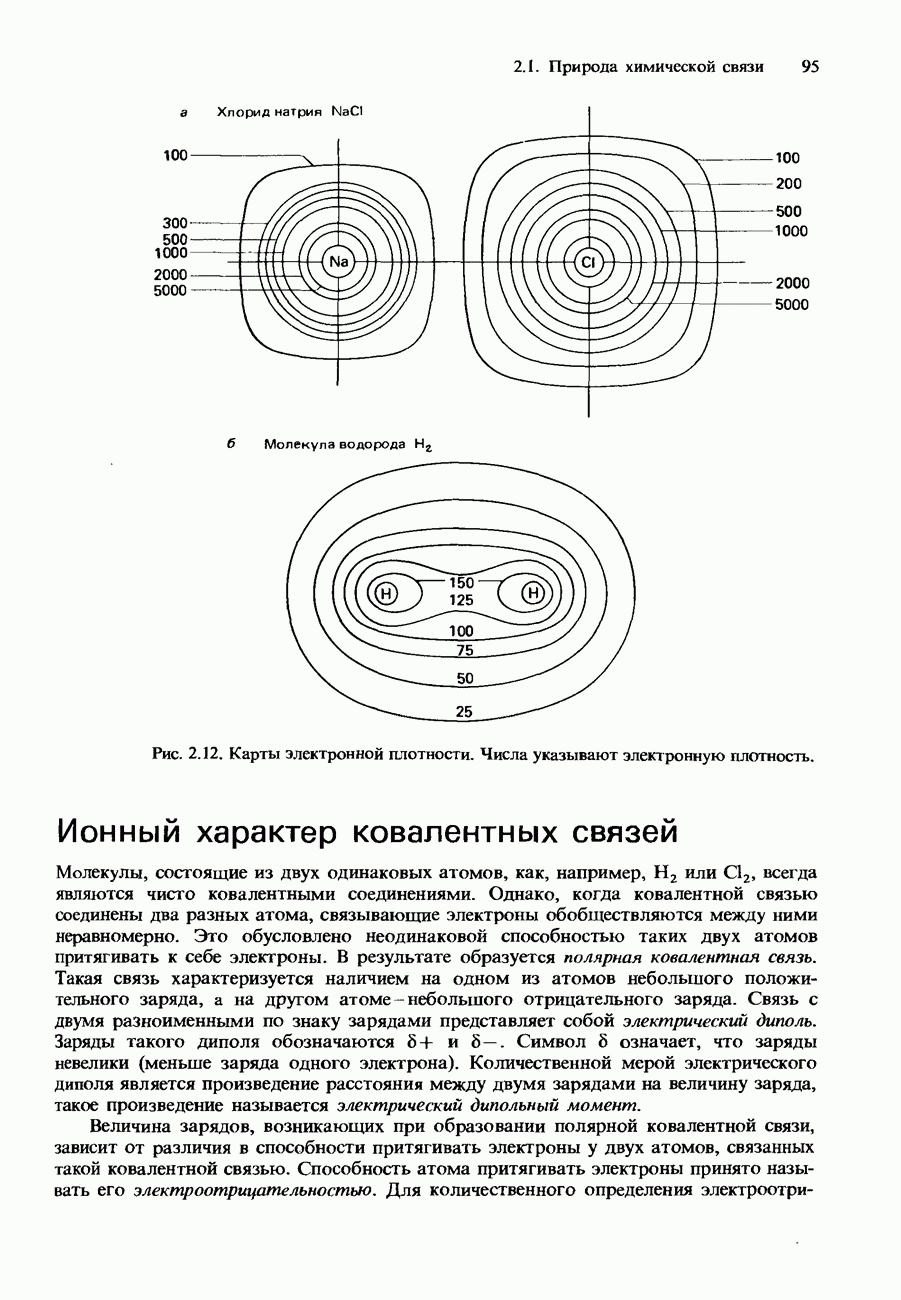
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
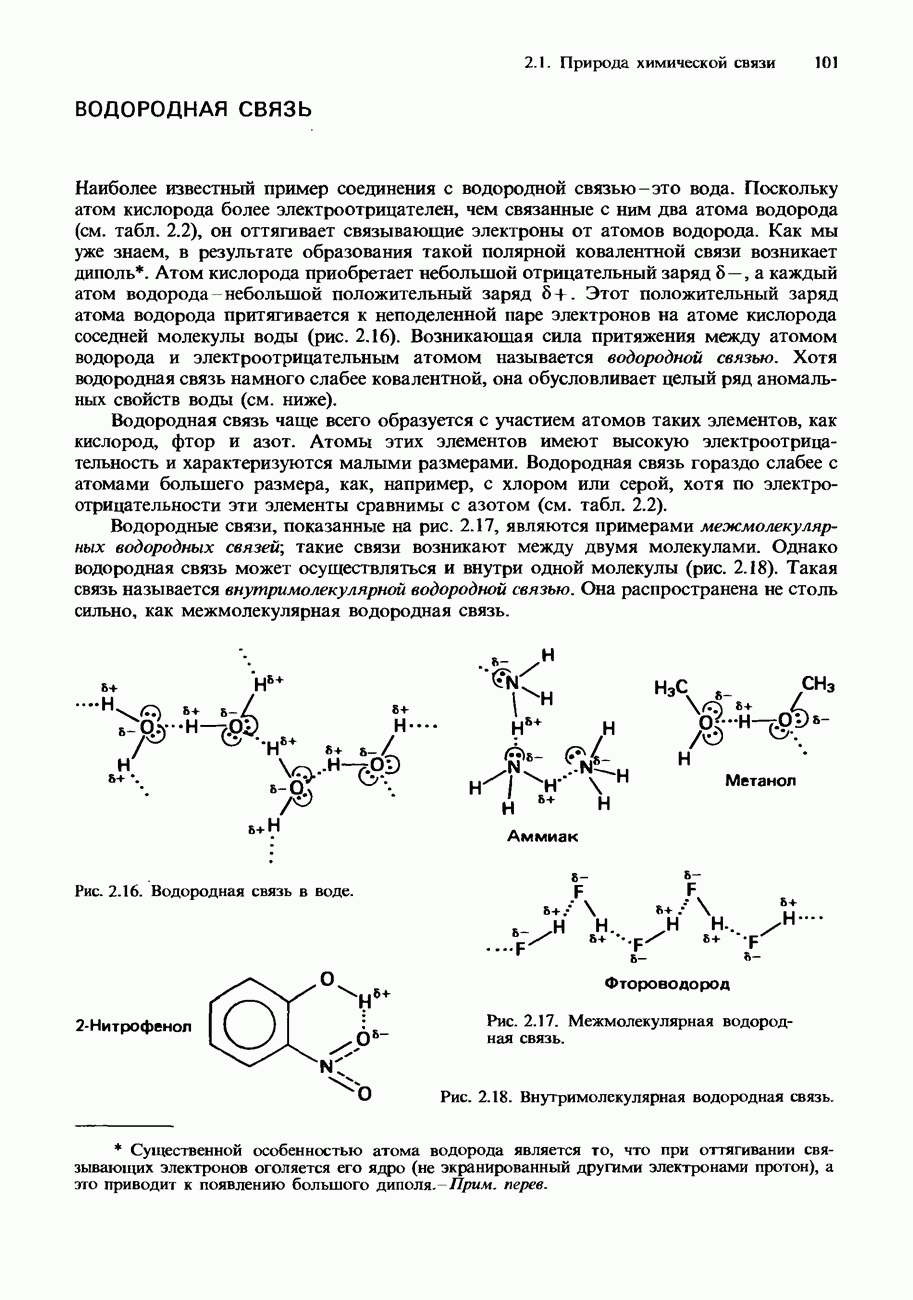
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
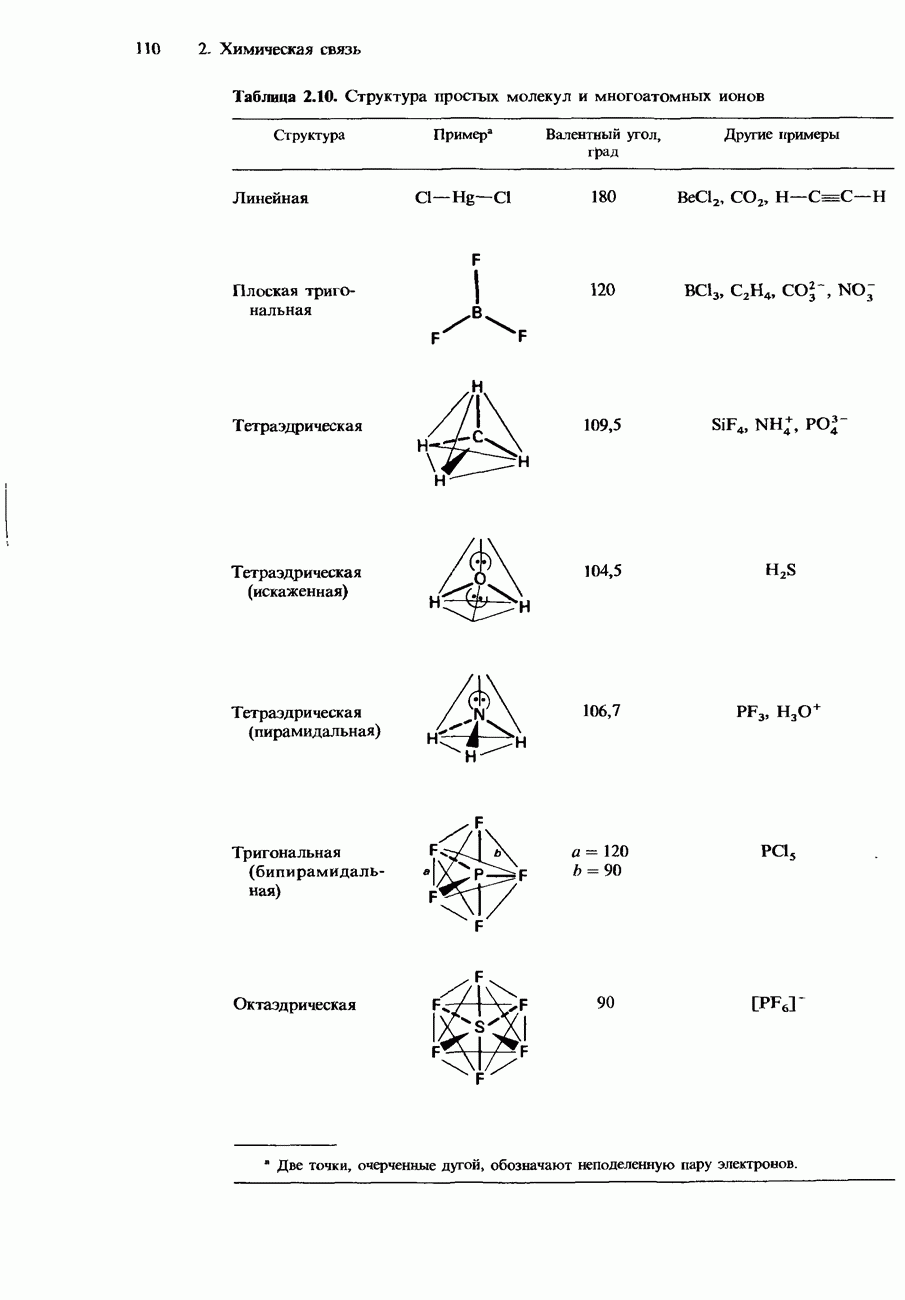
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
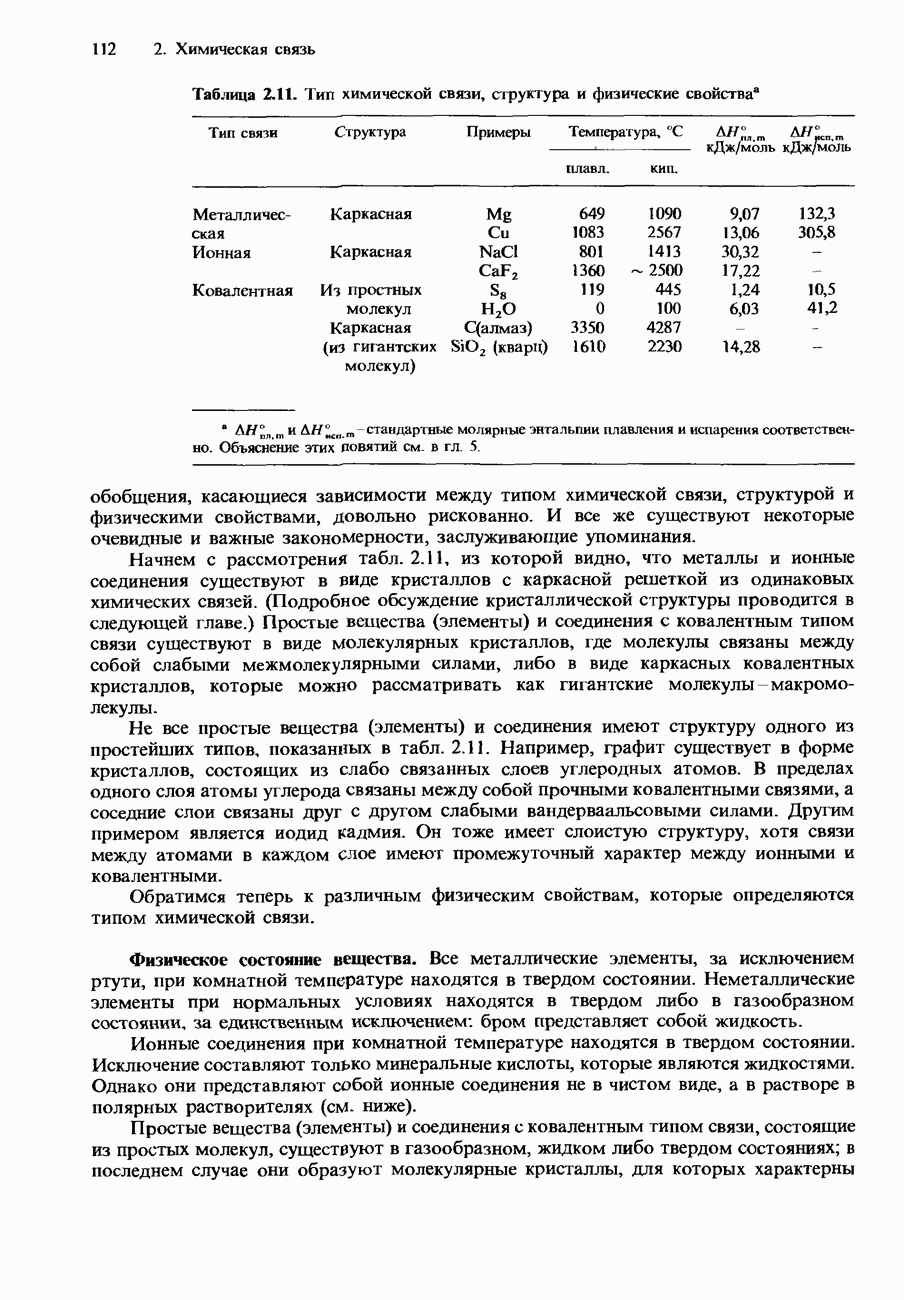
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
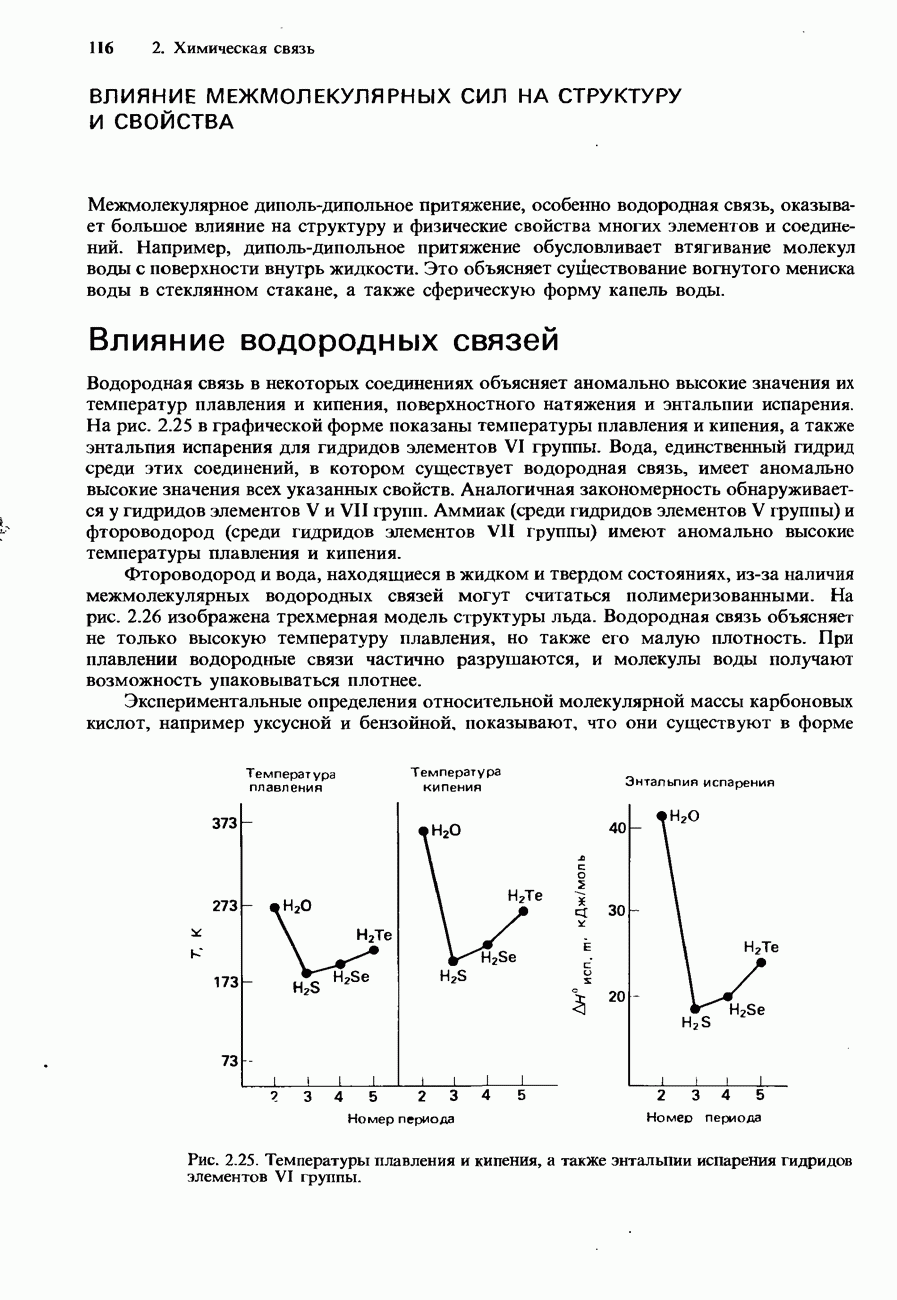
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
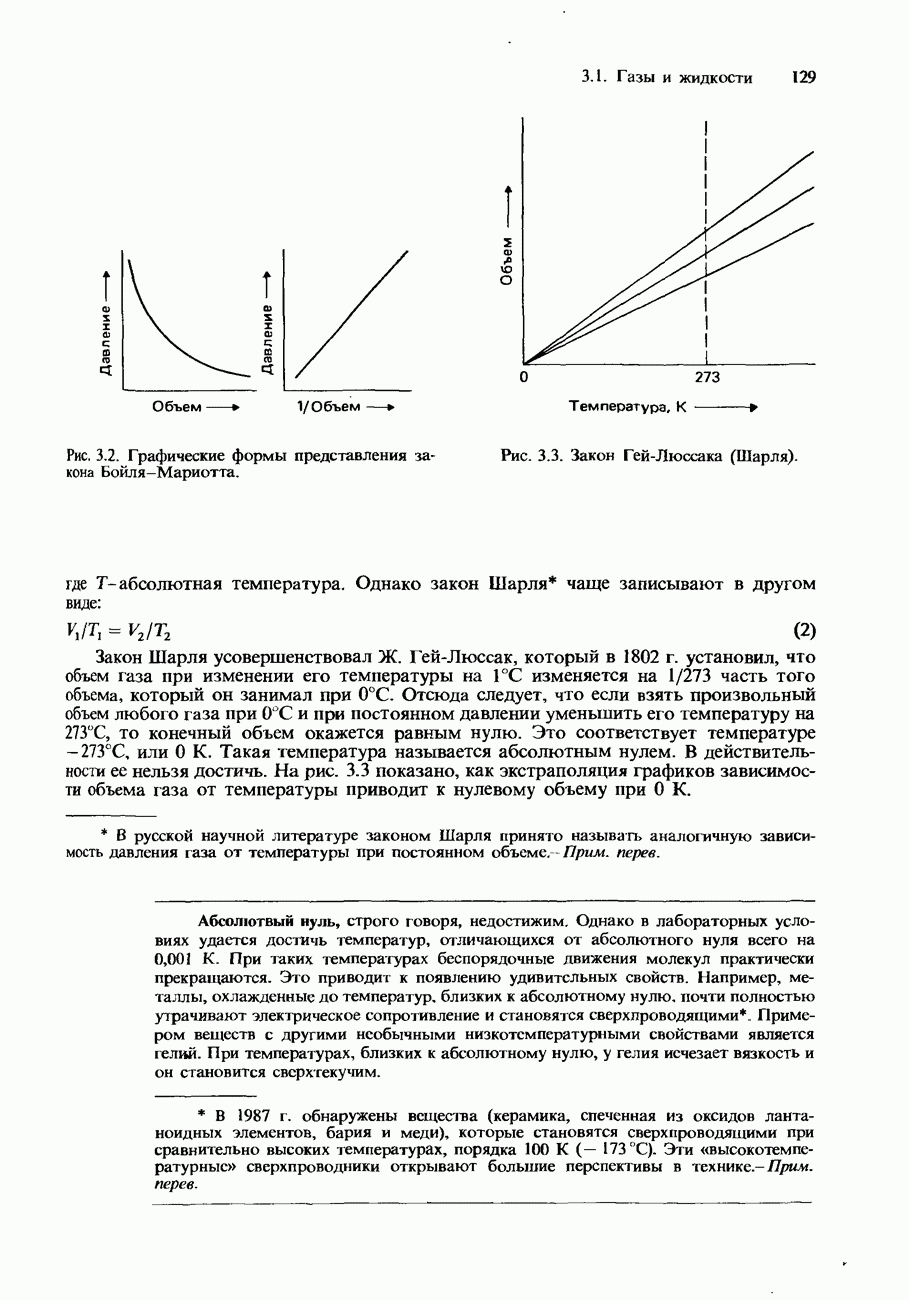
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
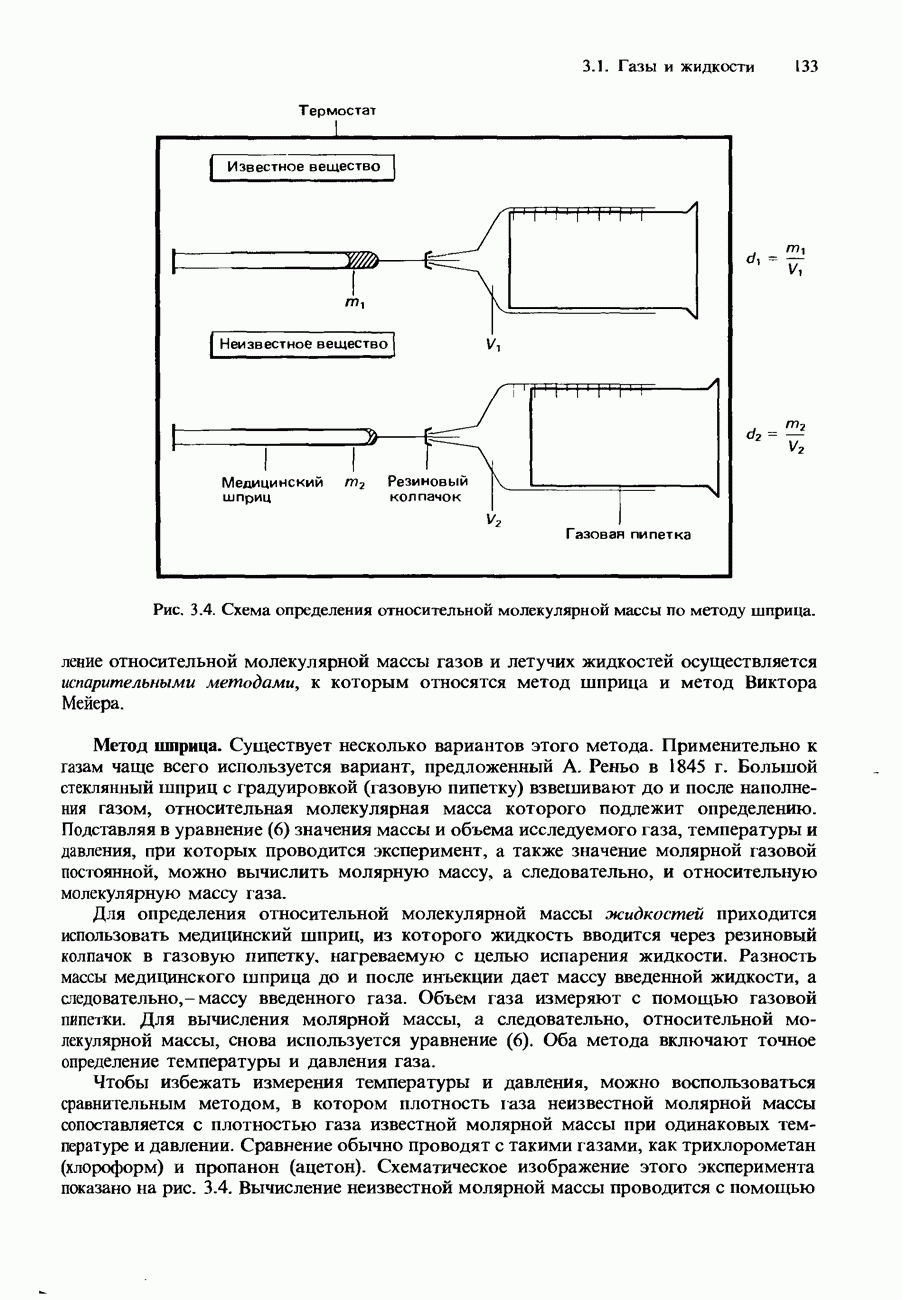
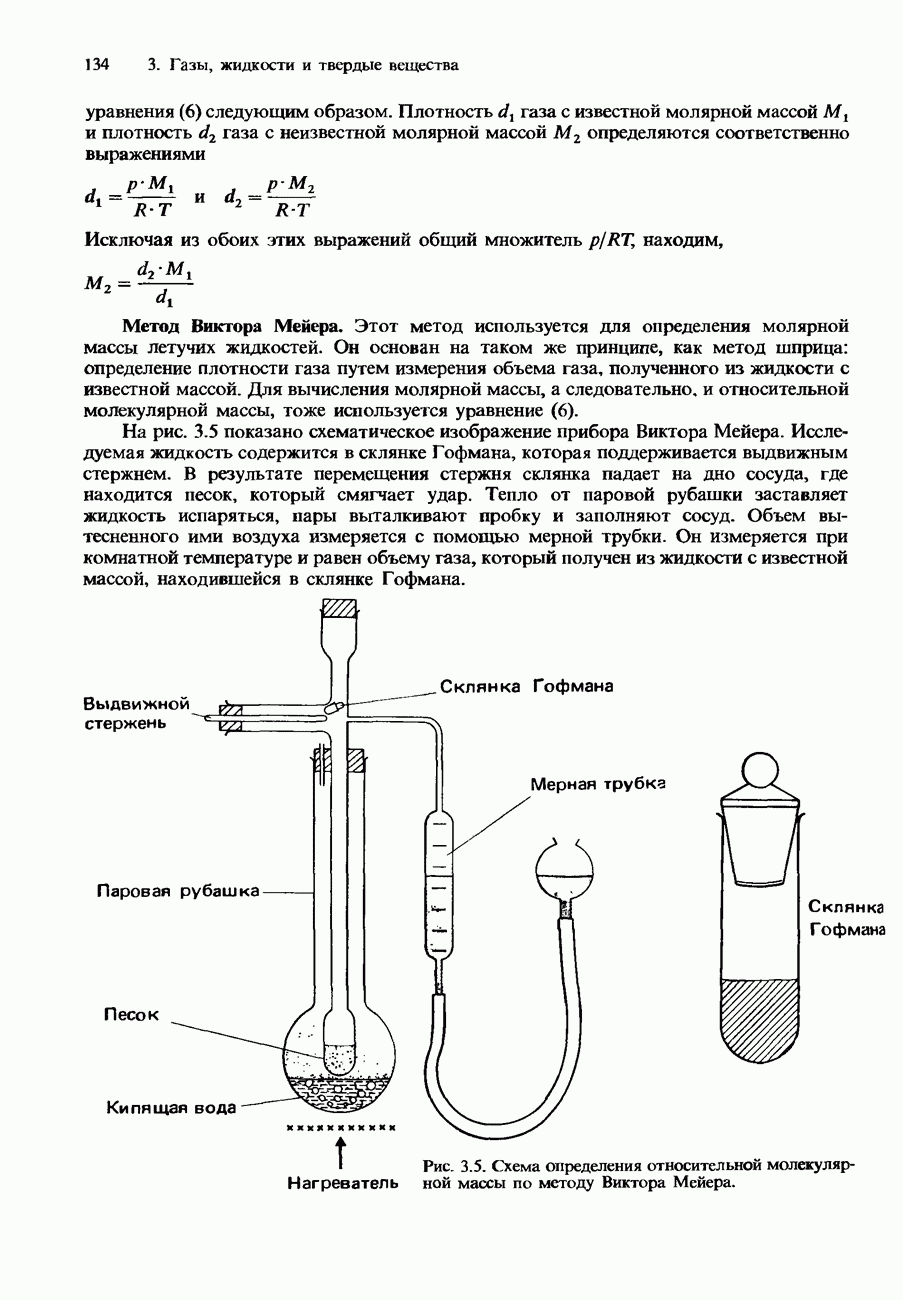
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- Скорости молекул
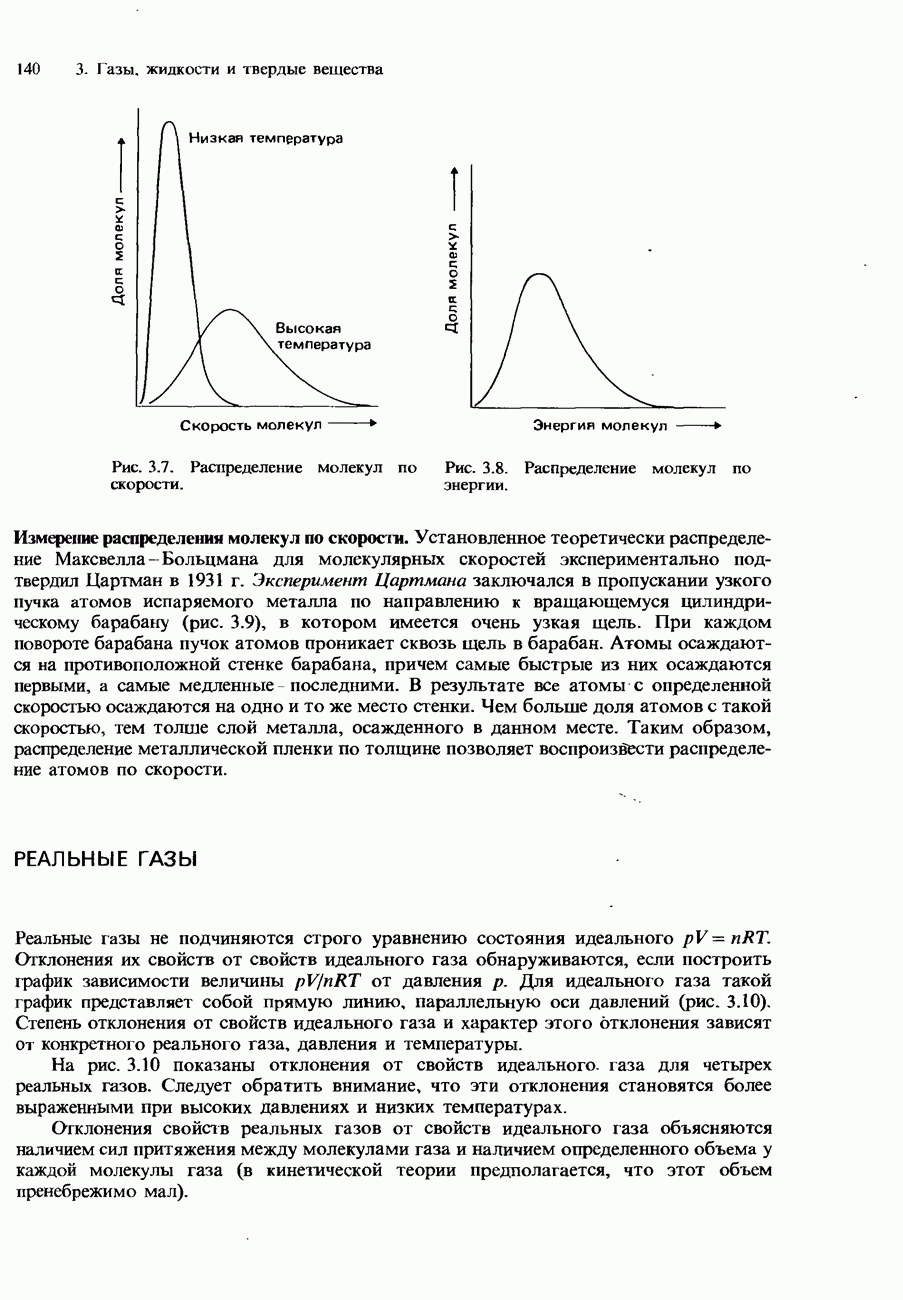
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
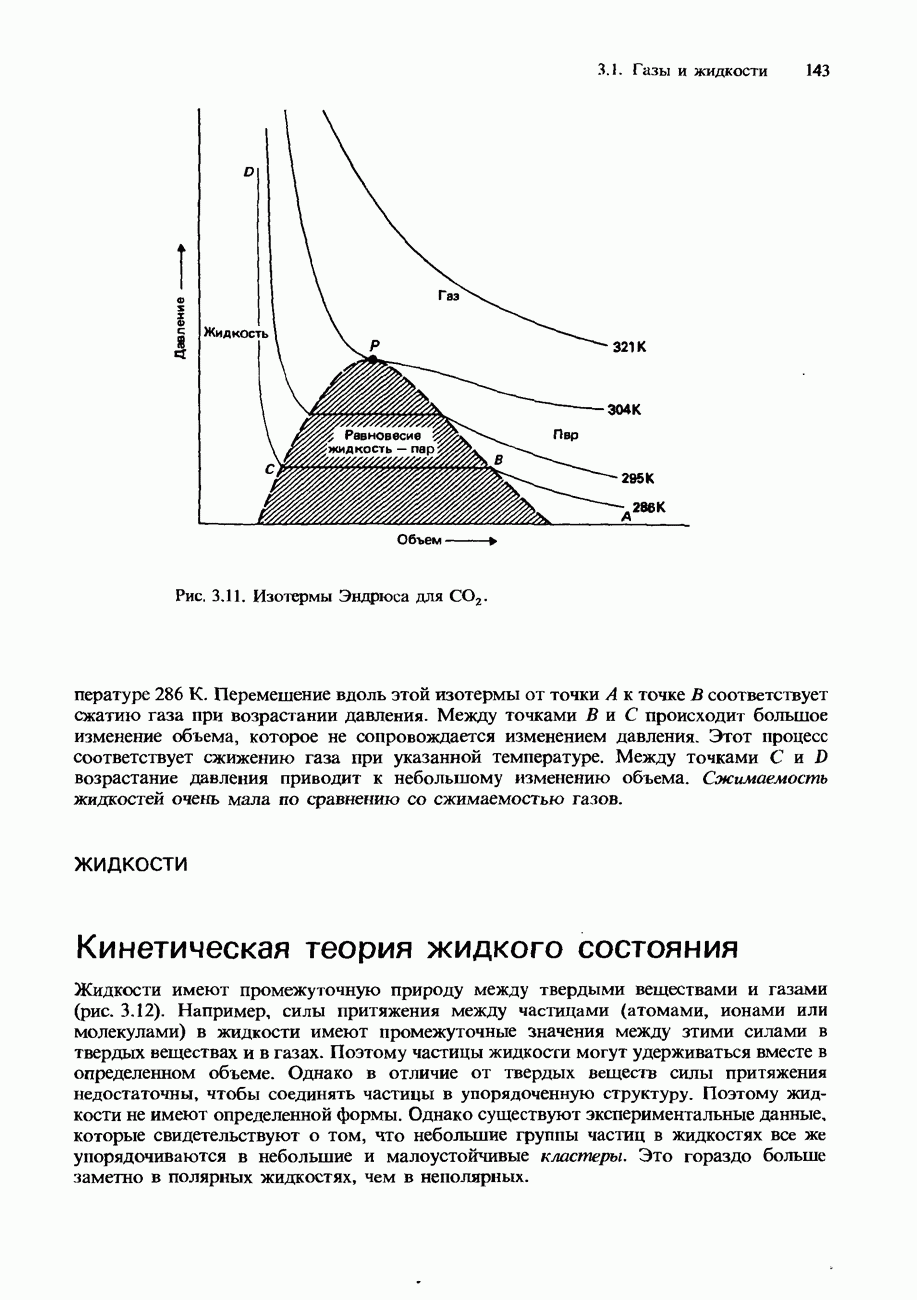
- Сжижение газов
- ЖИДКОСТИ
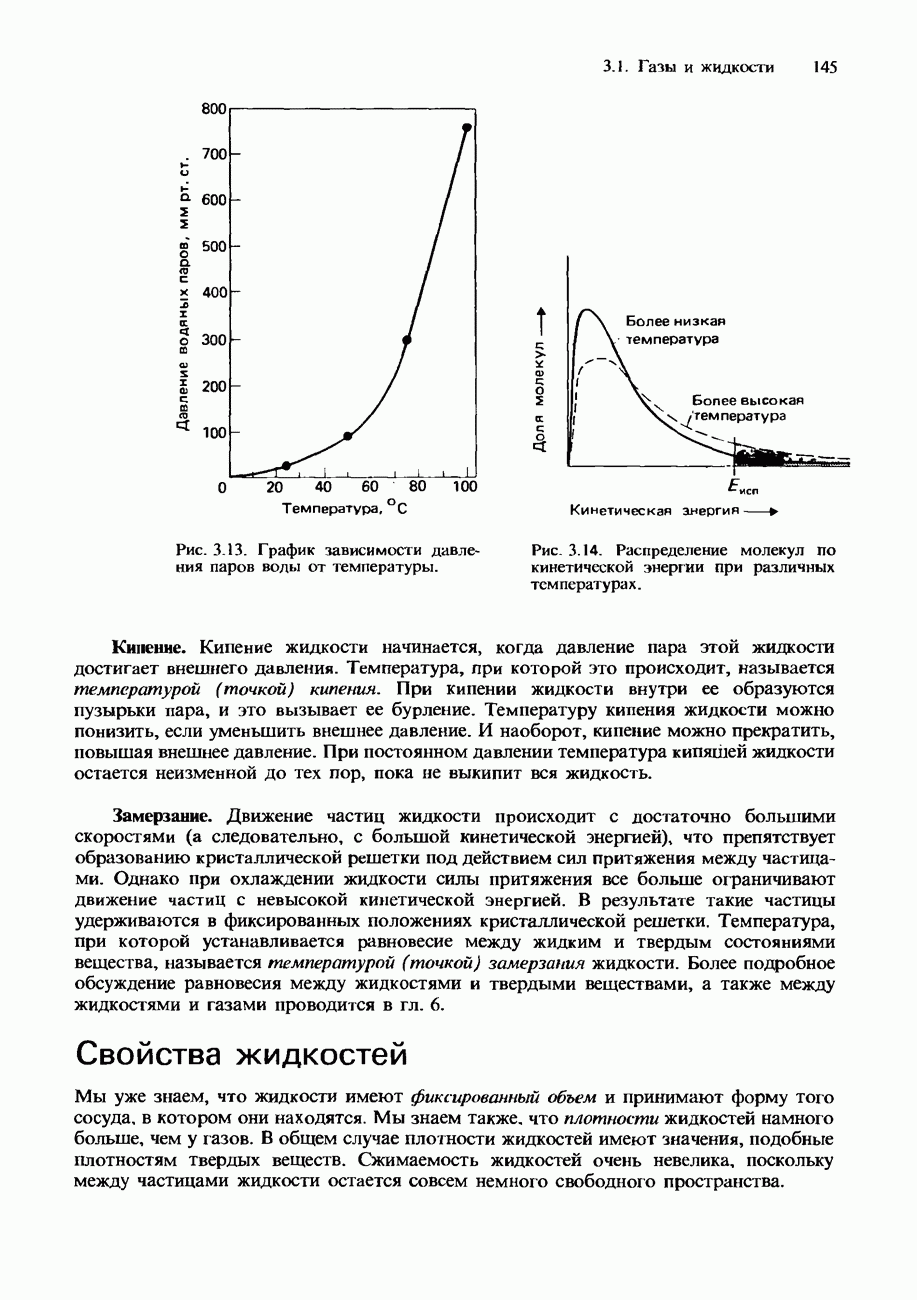
- Свойства жидкостей
- 3.2. Твердые вещества
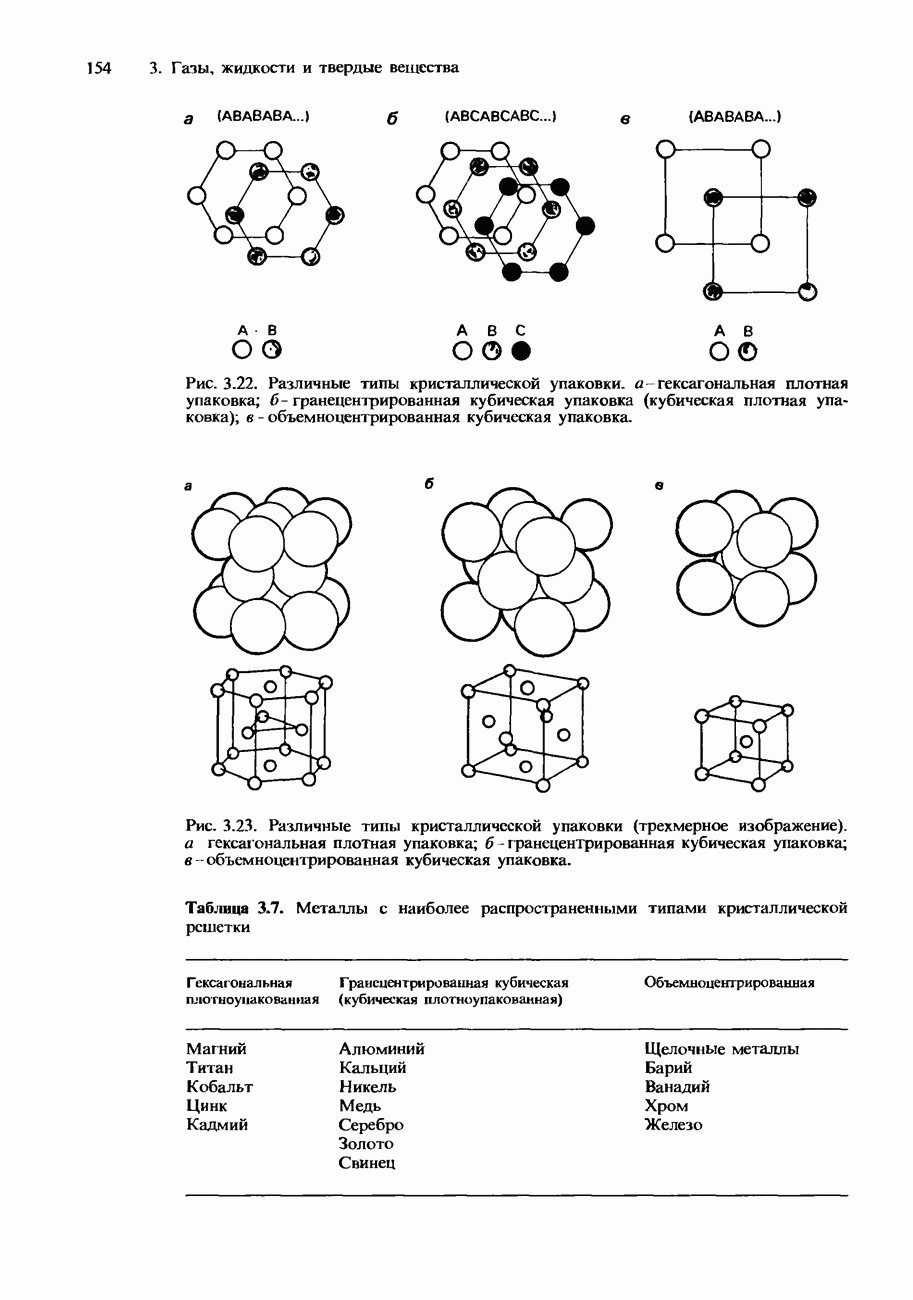
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
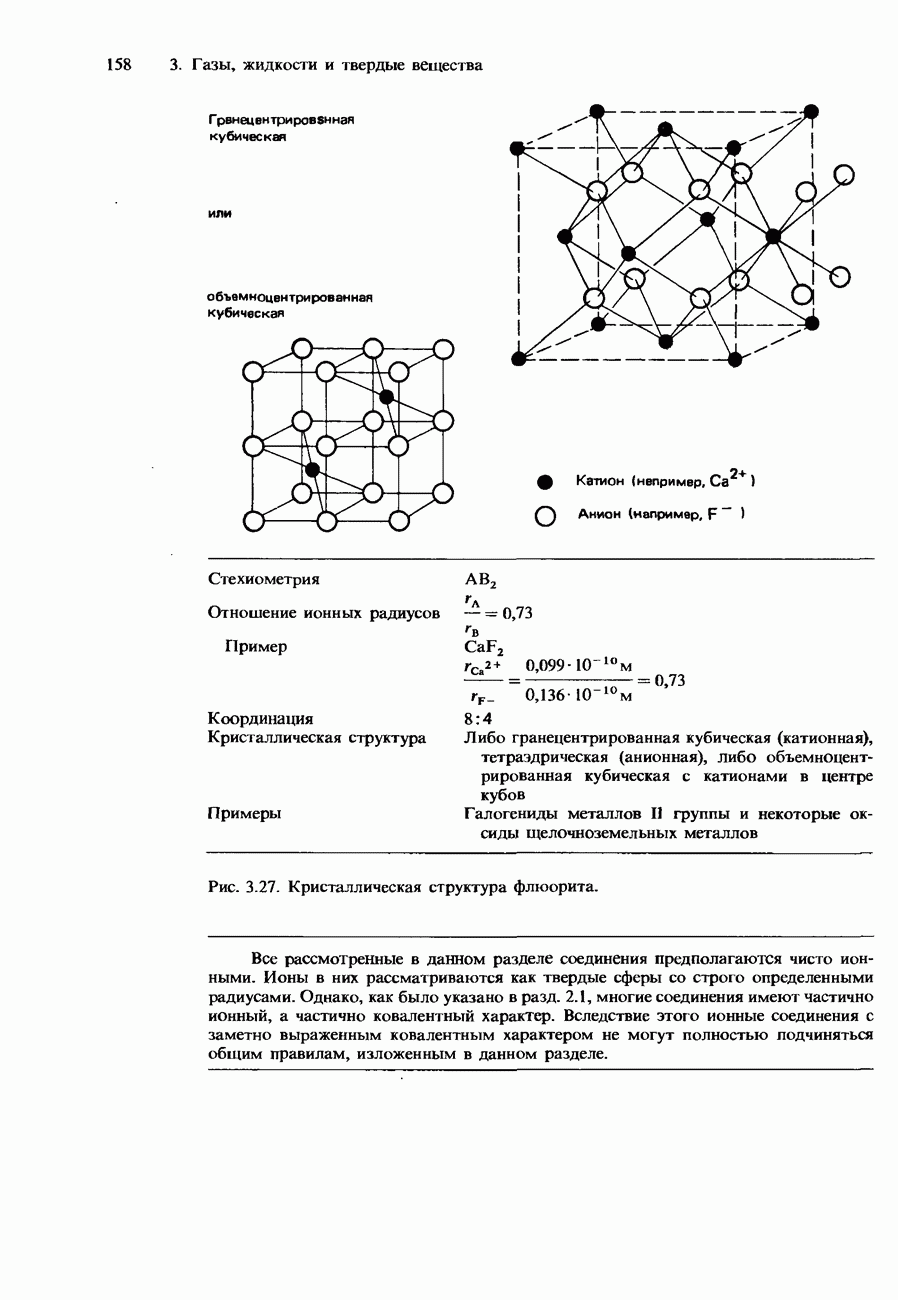
- Ионные кристаллы
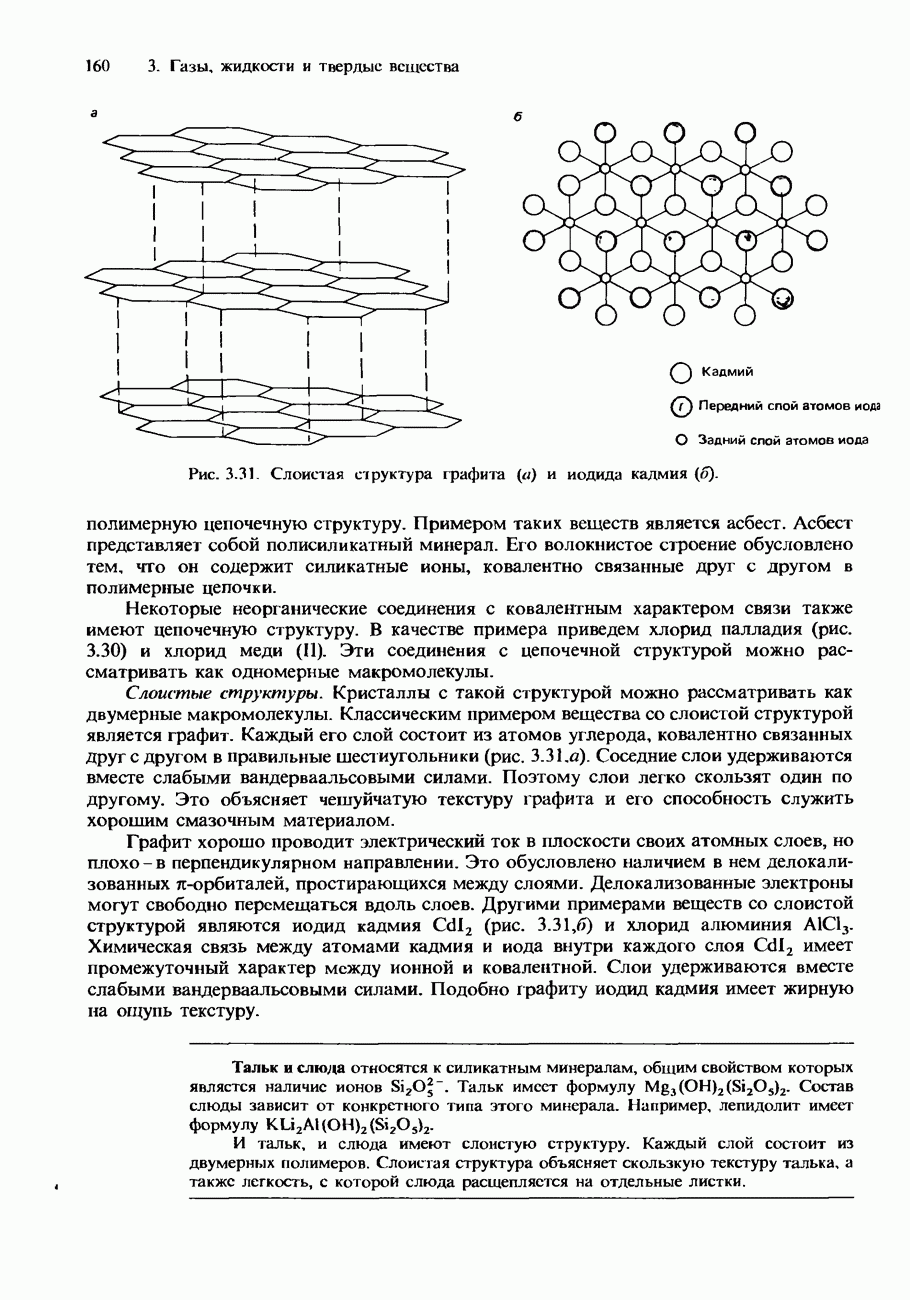
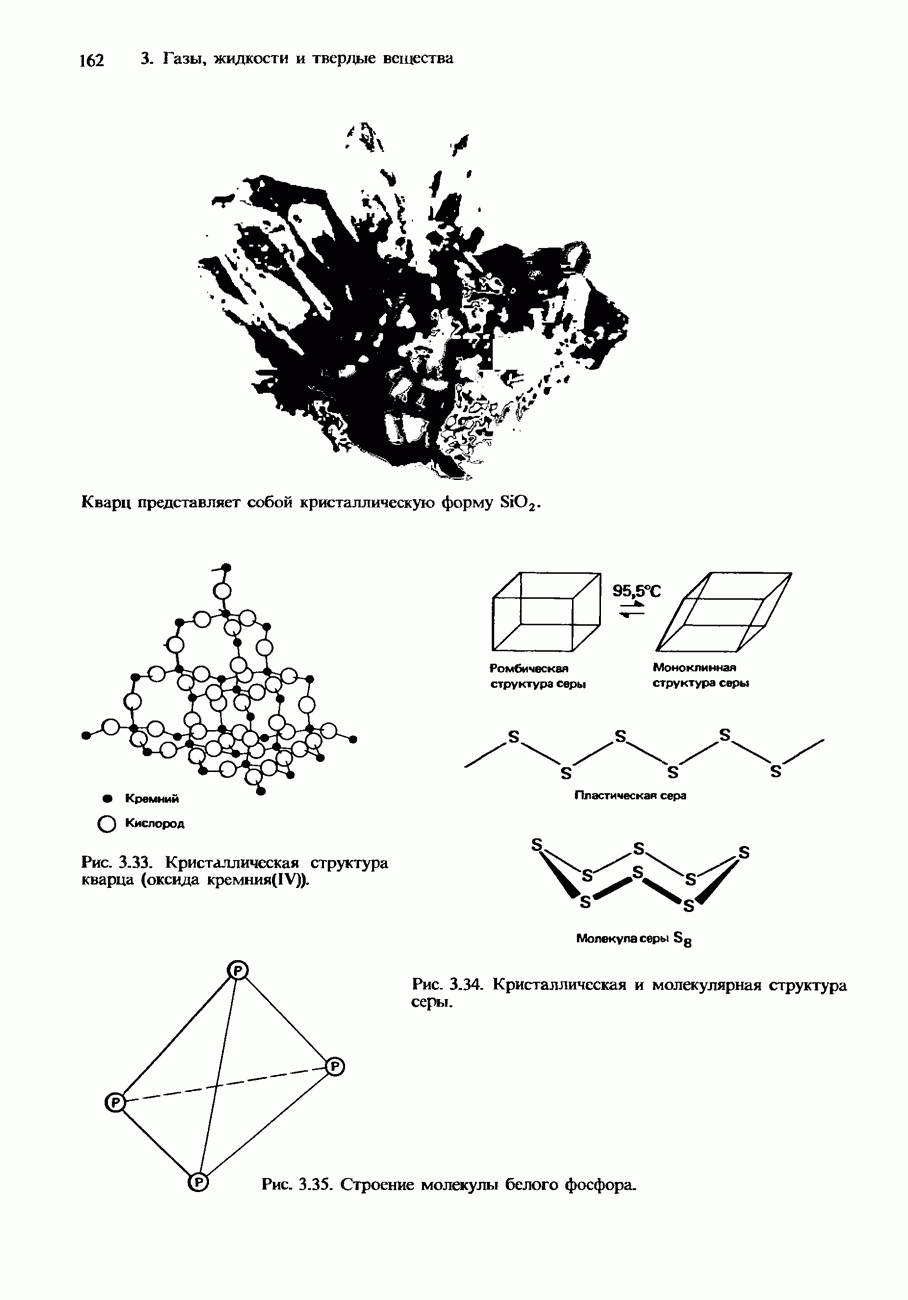
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
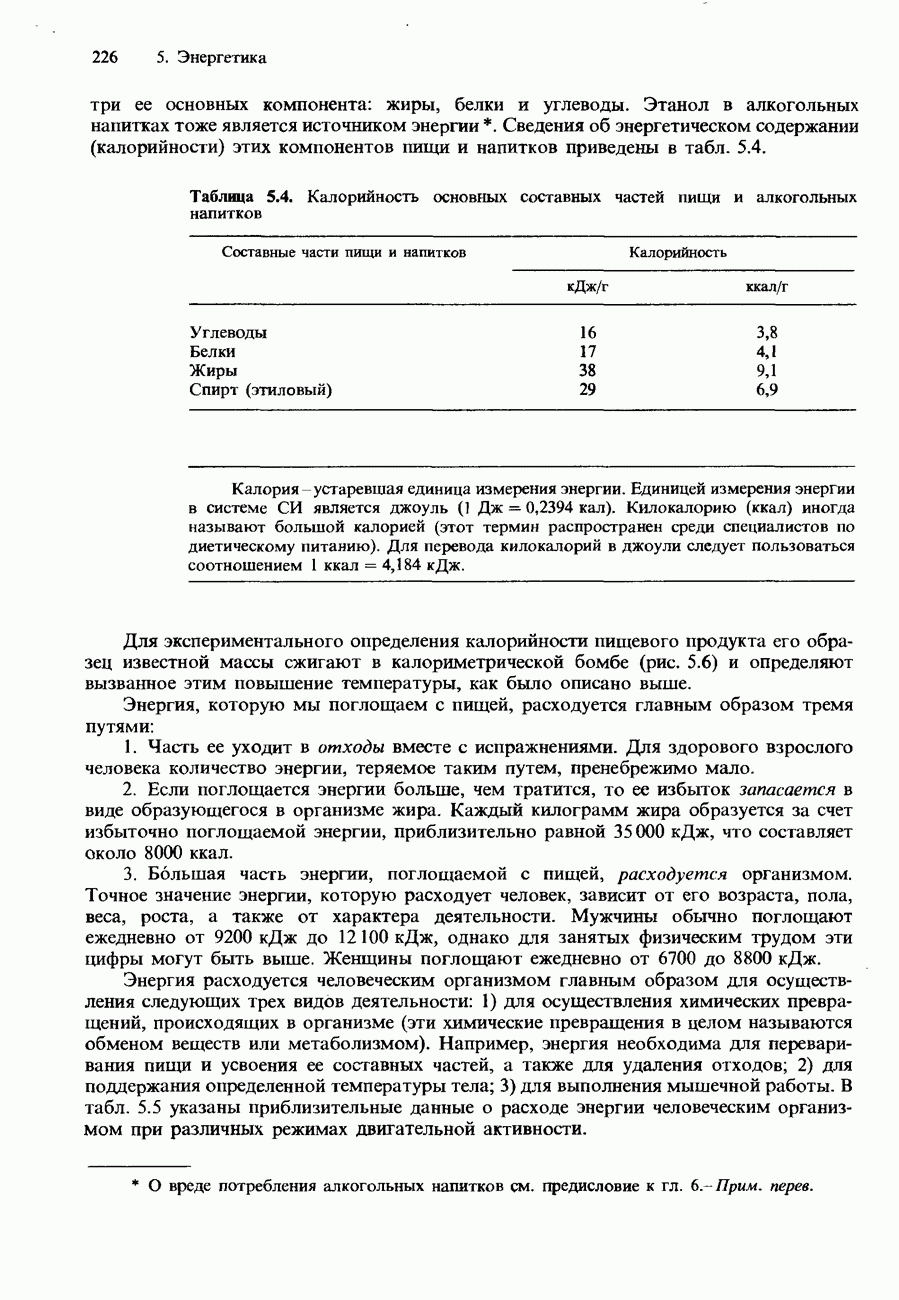
- КАЛОРИЙНОСТЬ ПИЩИ
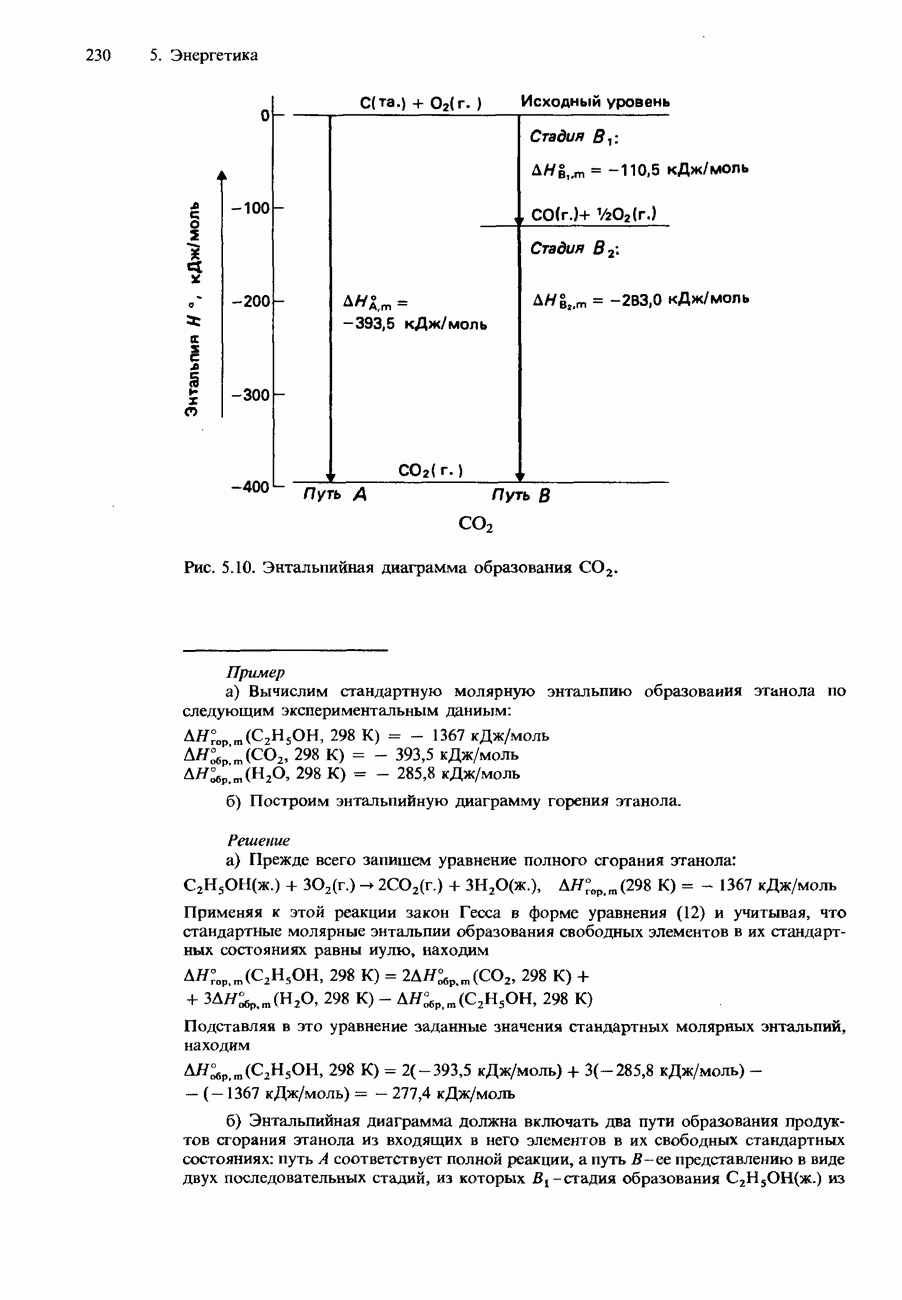
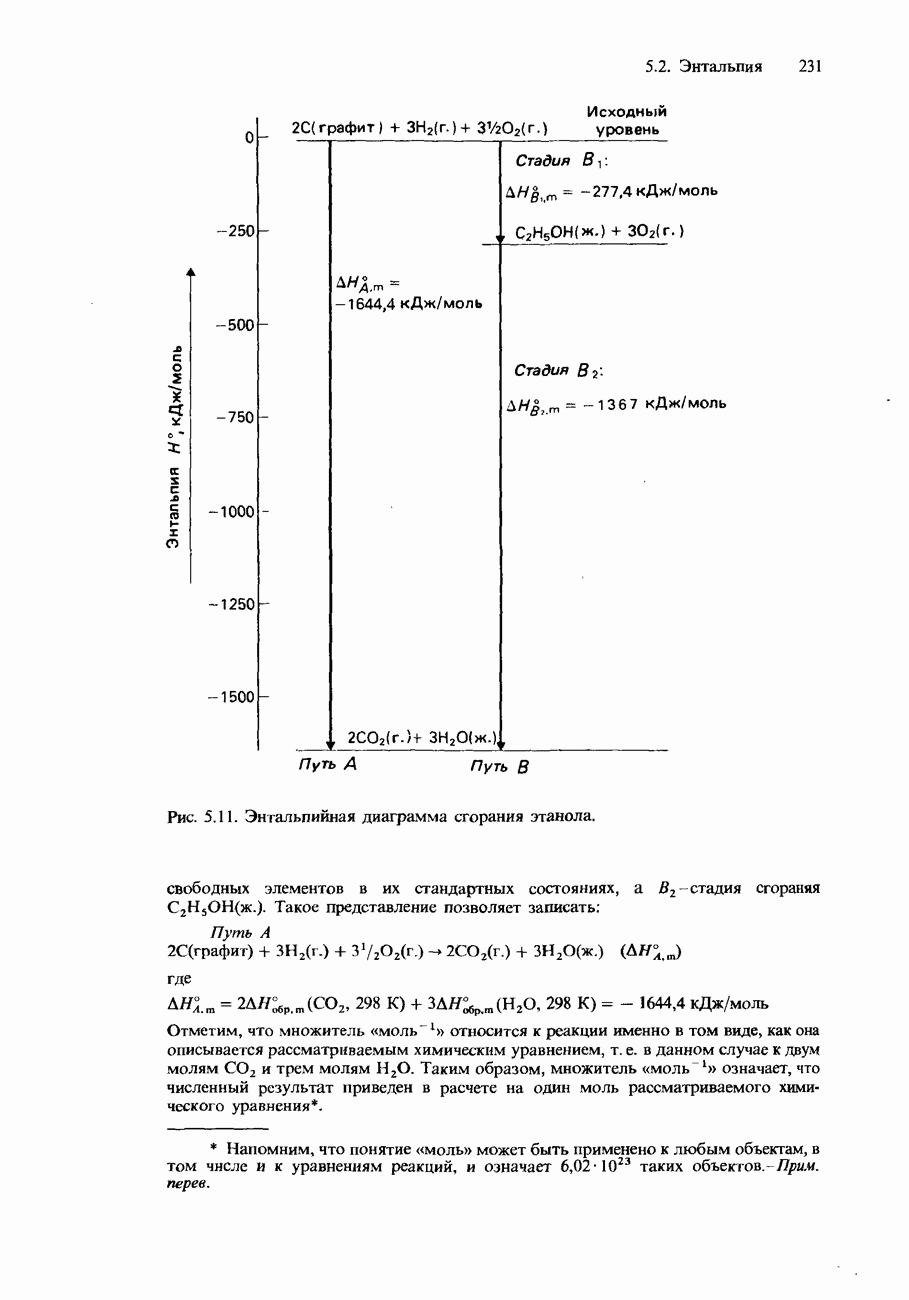
- ЗАКОН ГЕССА
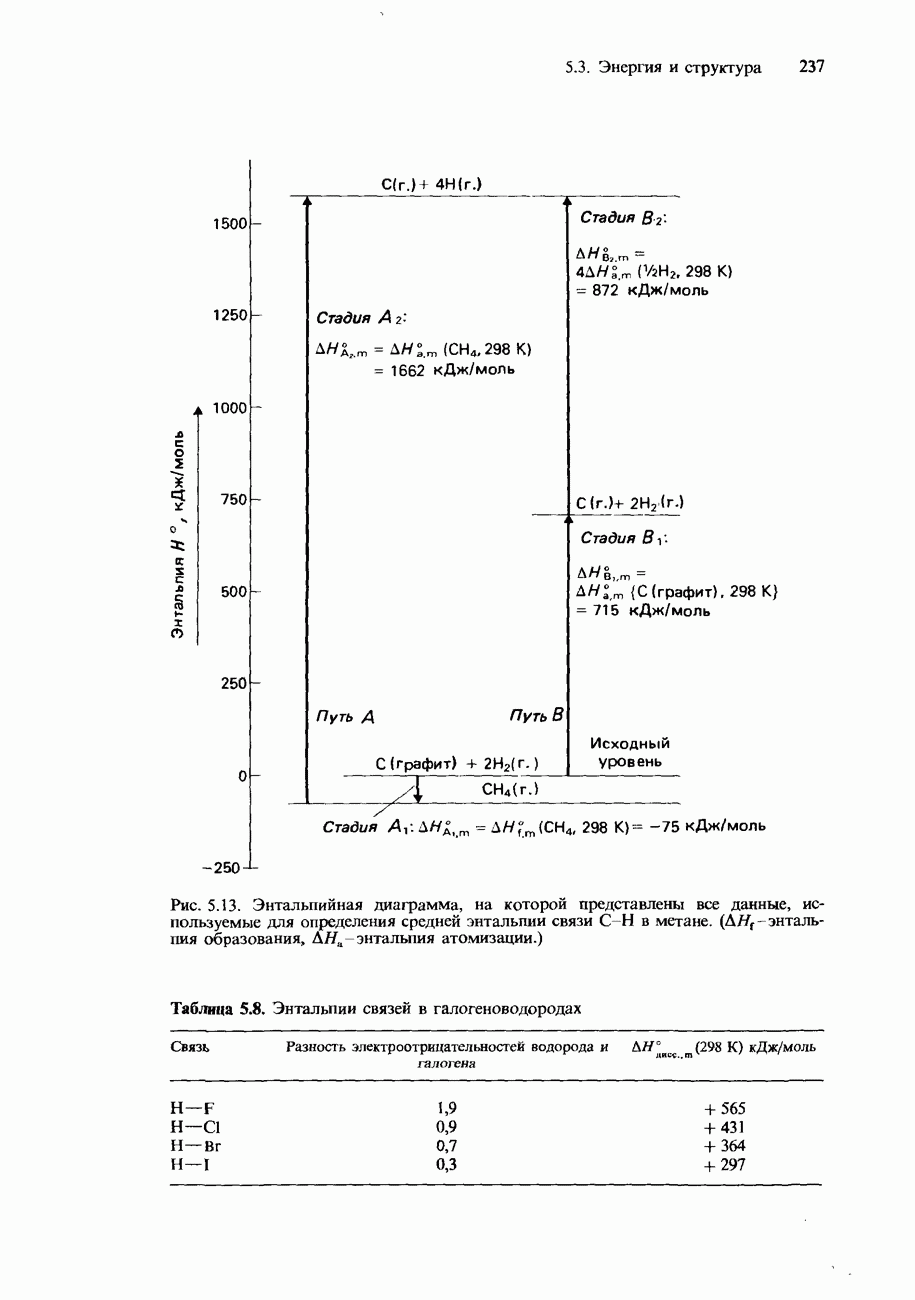
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
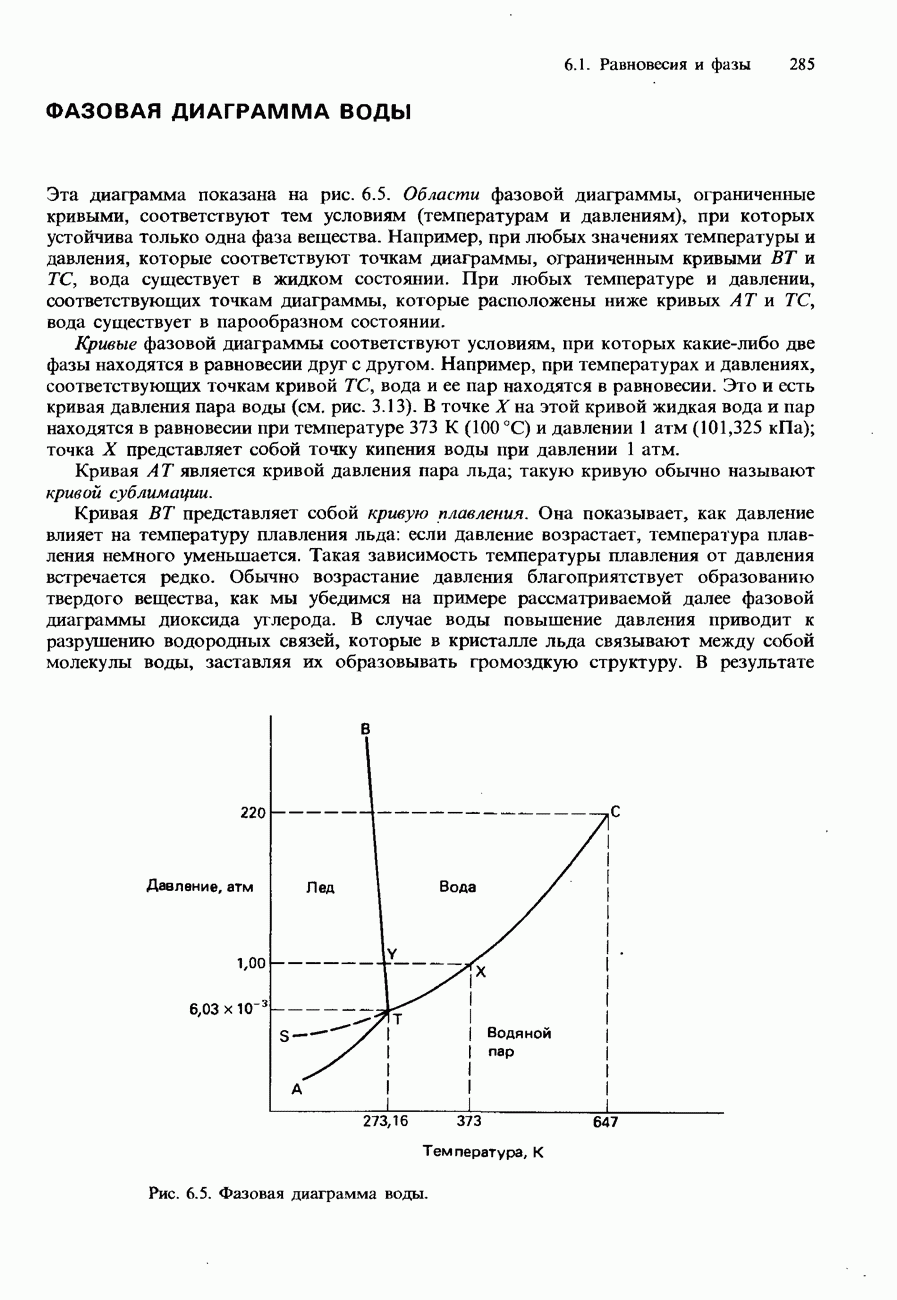
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
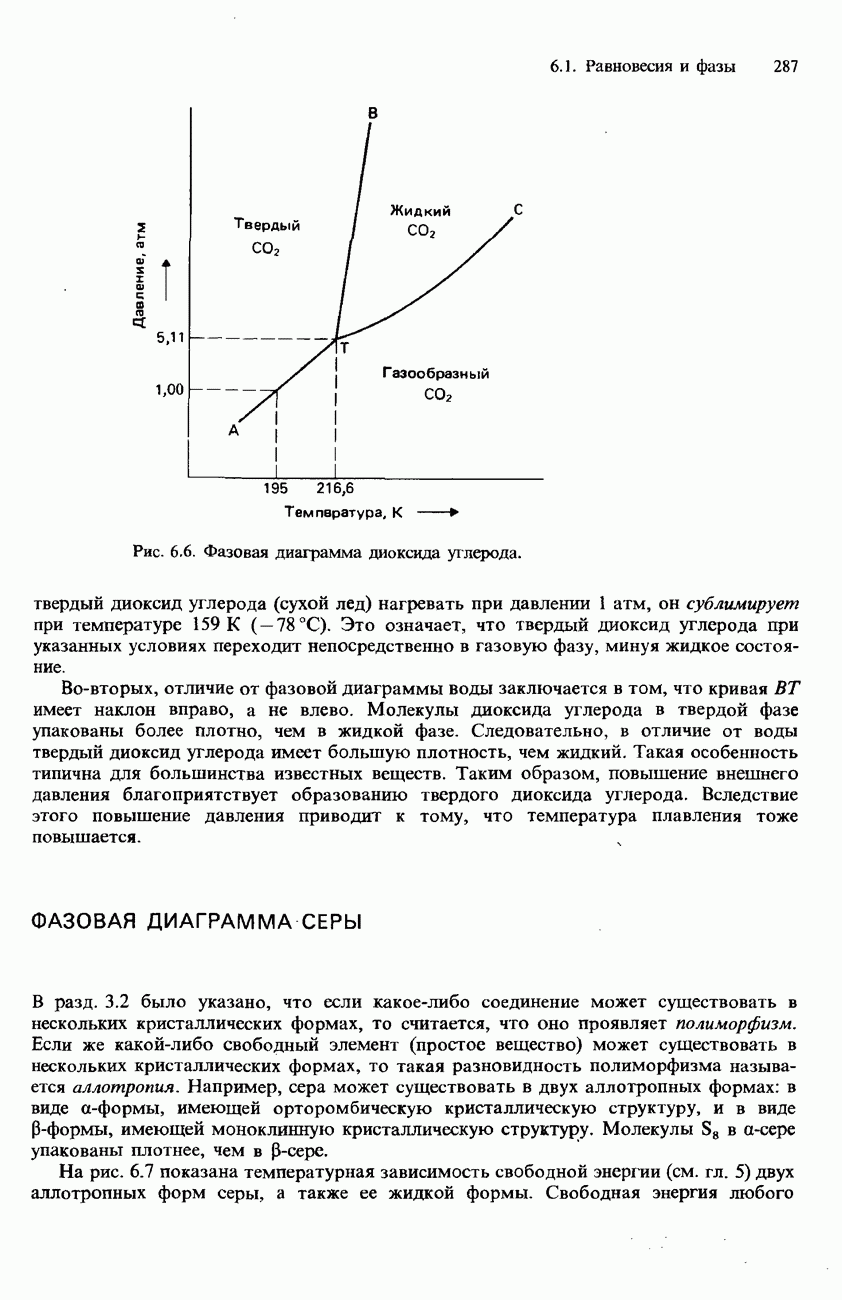
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
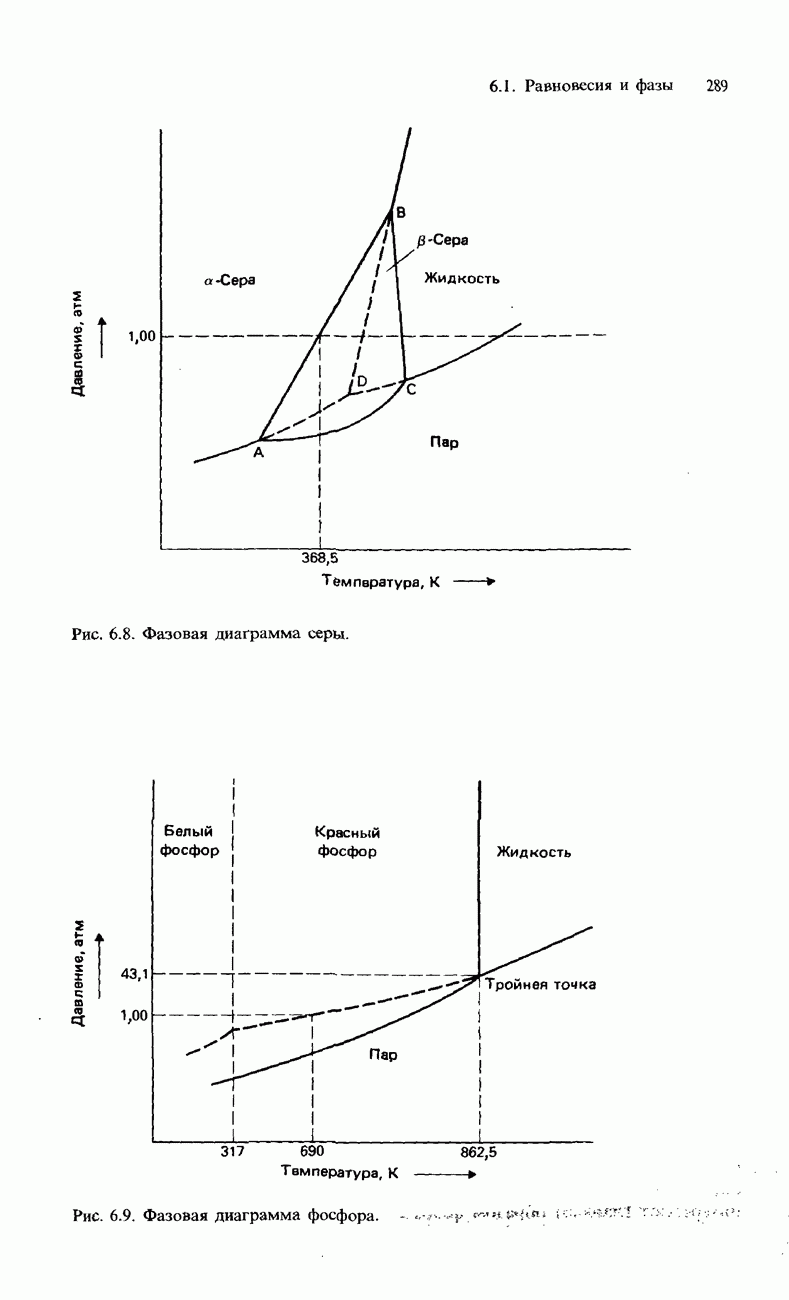
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- Фазовые диаграммы полностью смешивающихся жидкостей
- Фракционная перегонка
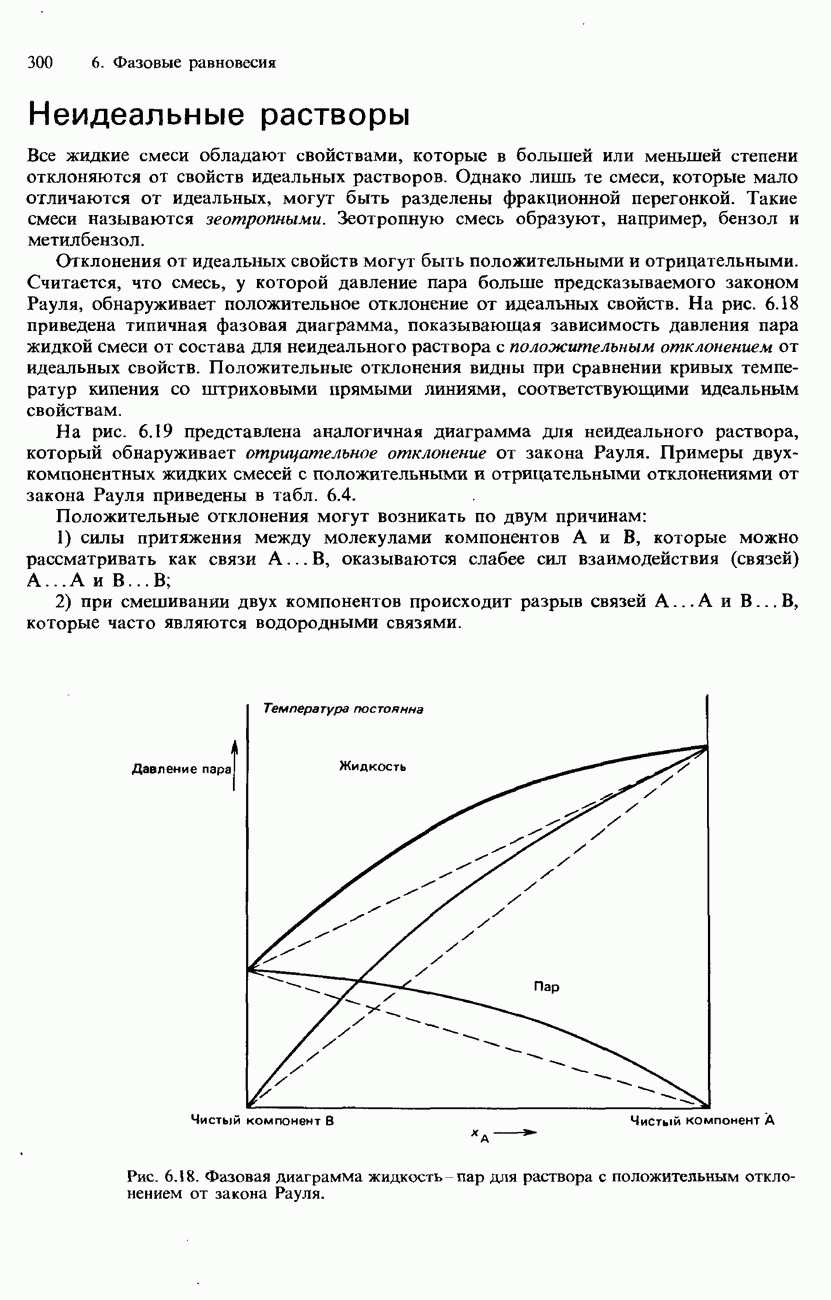
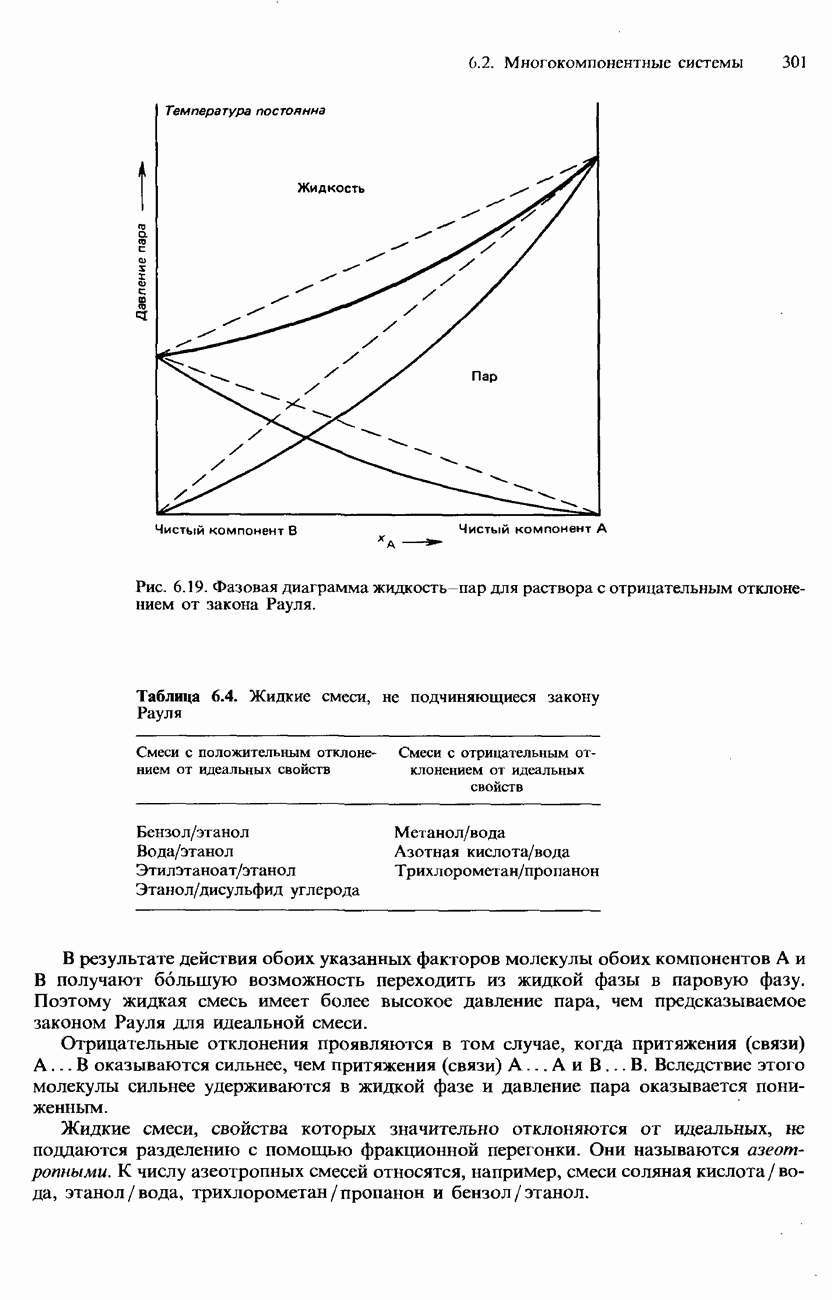
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
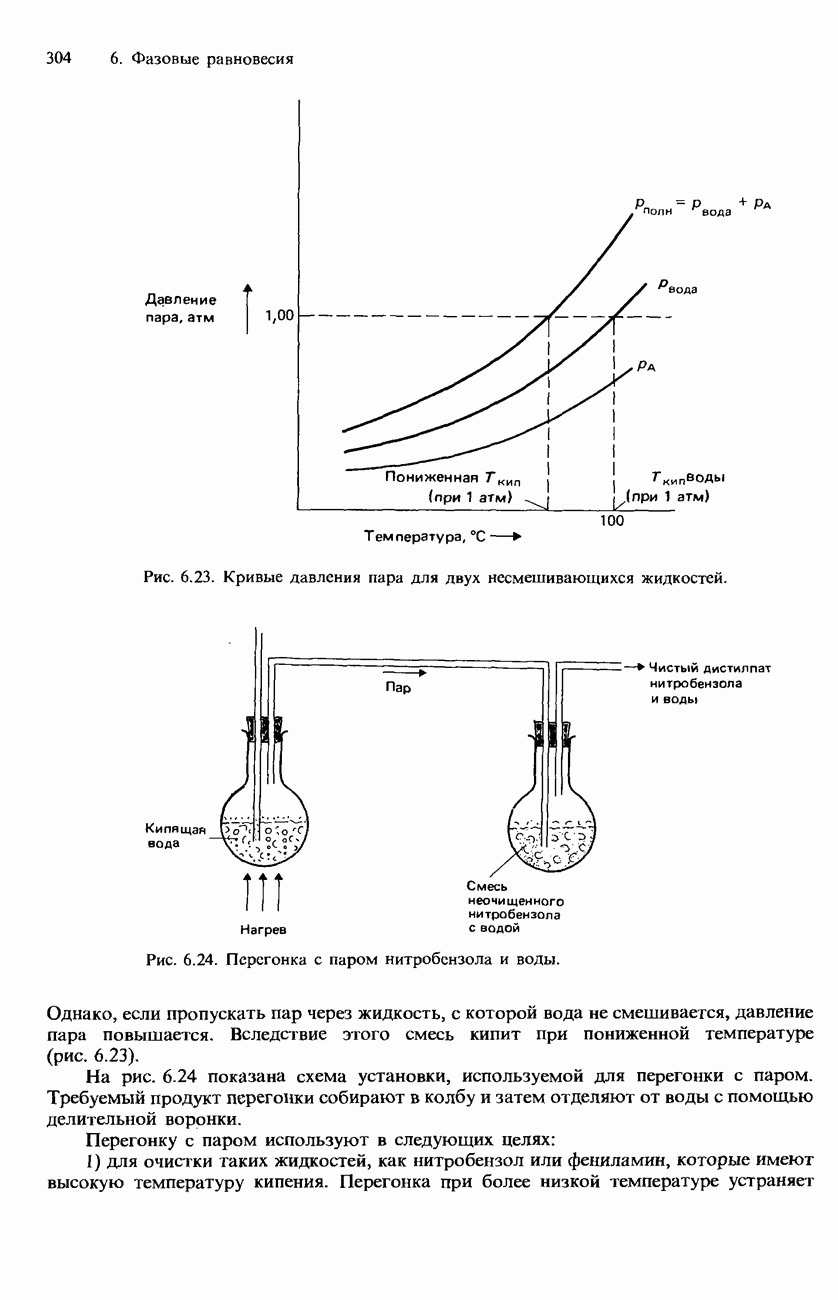
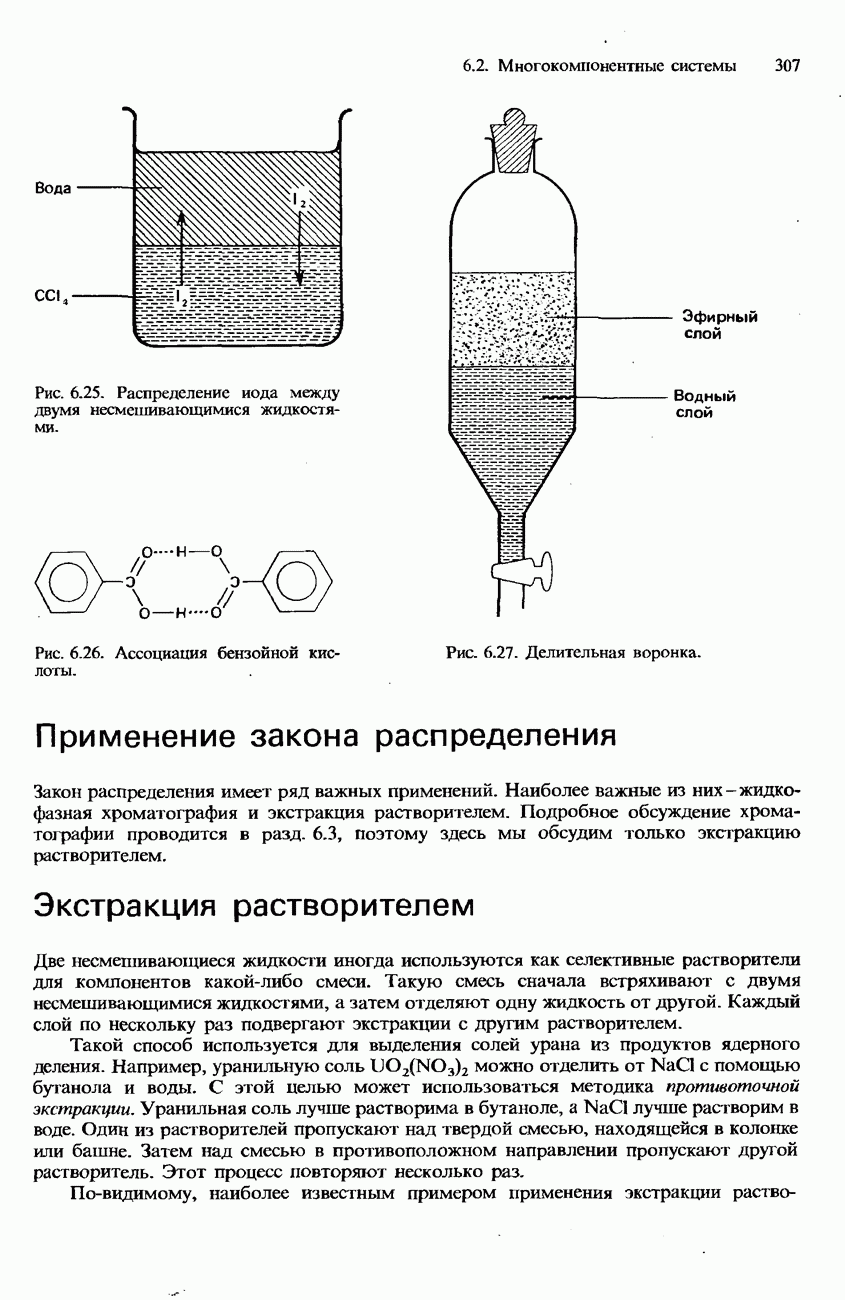
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
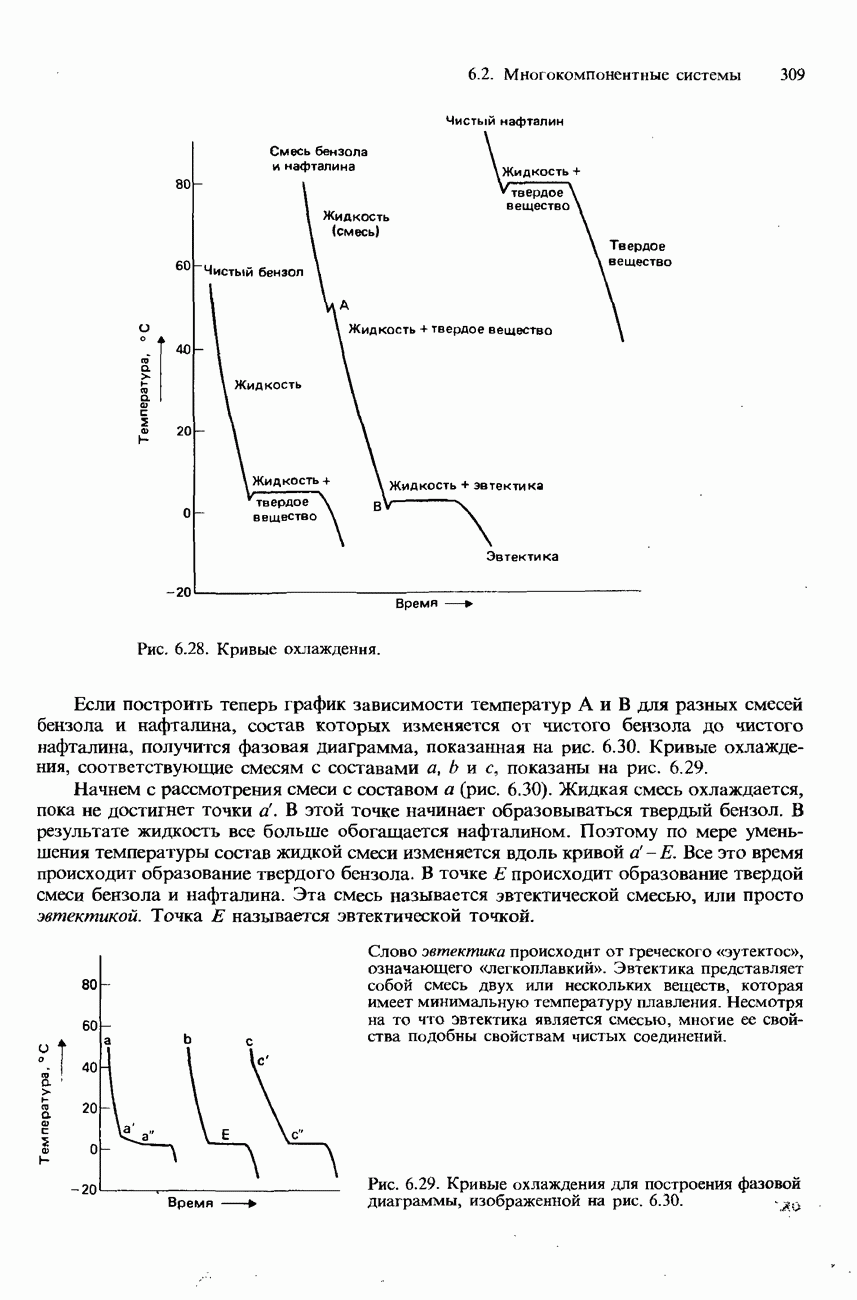
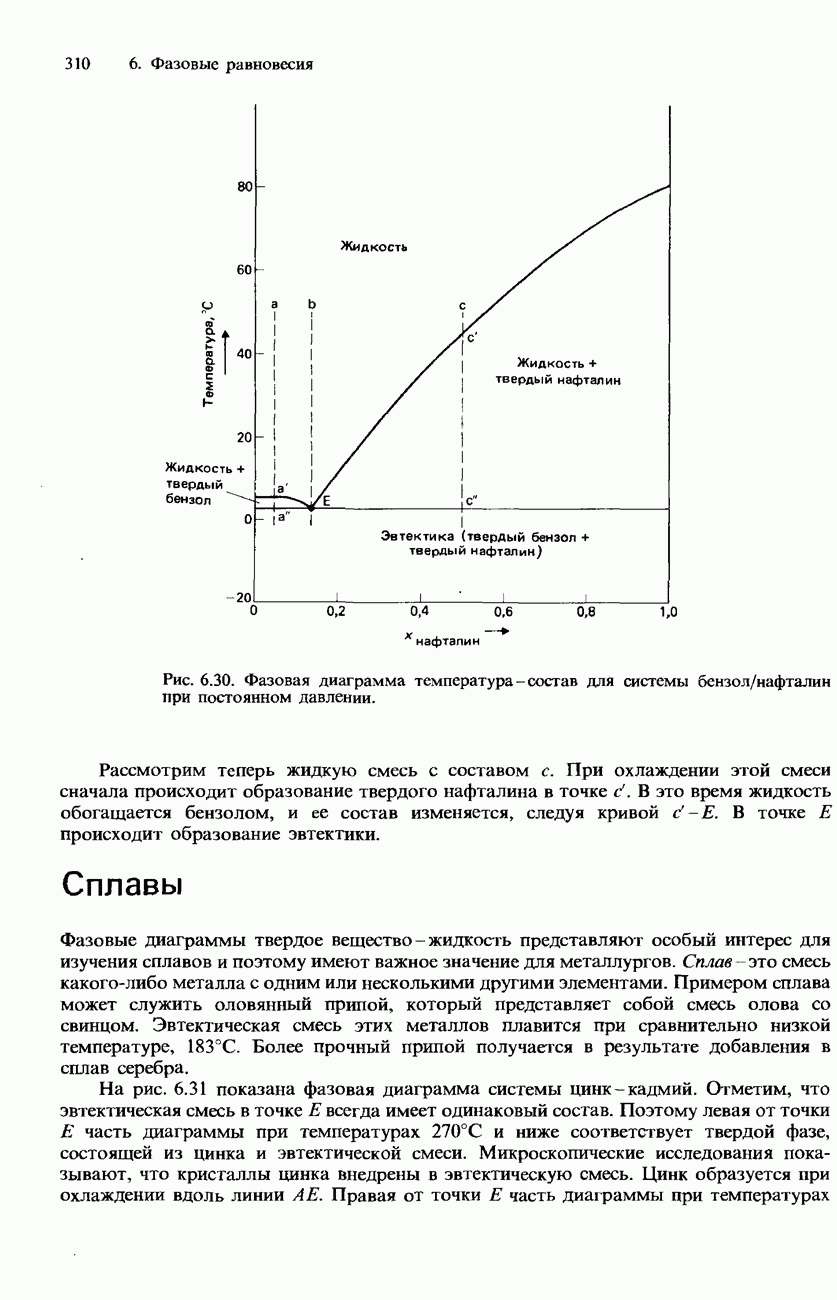
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
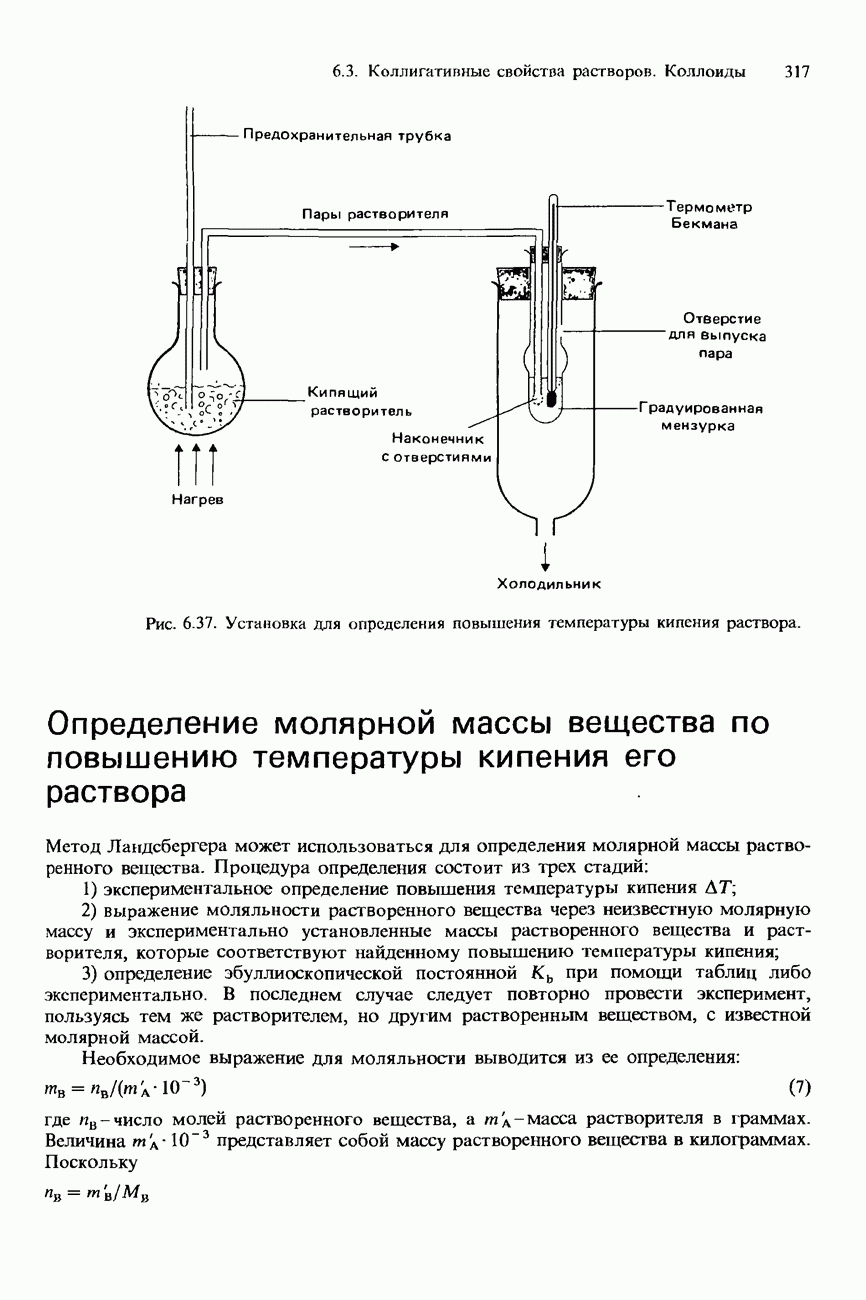
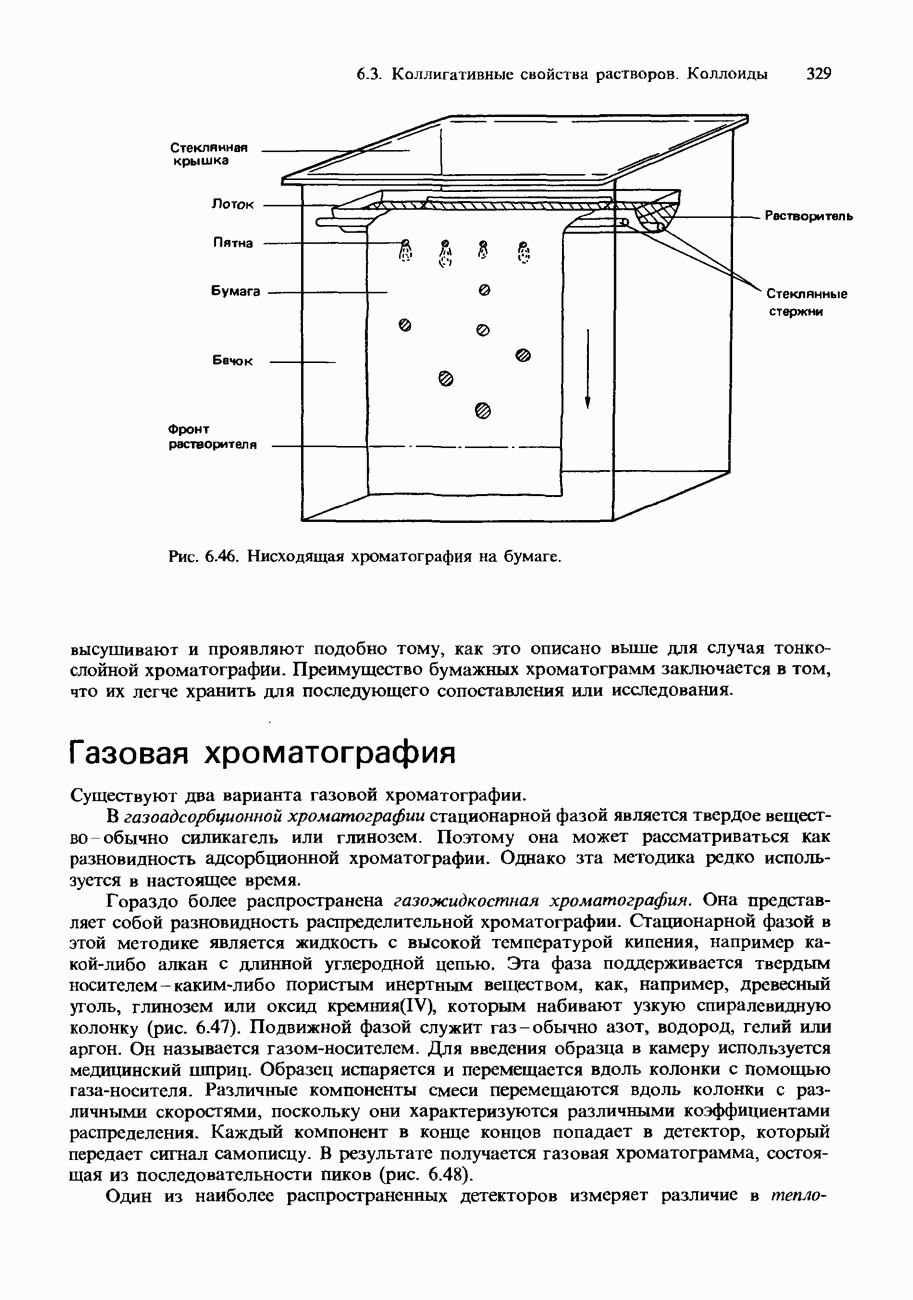
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
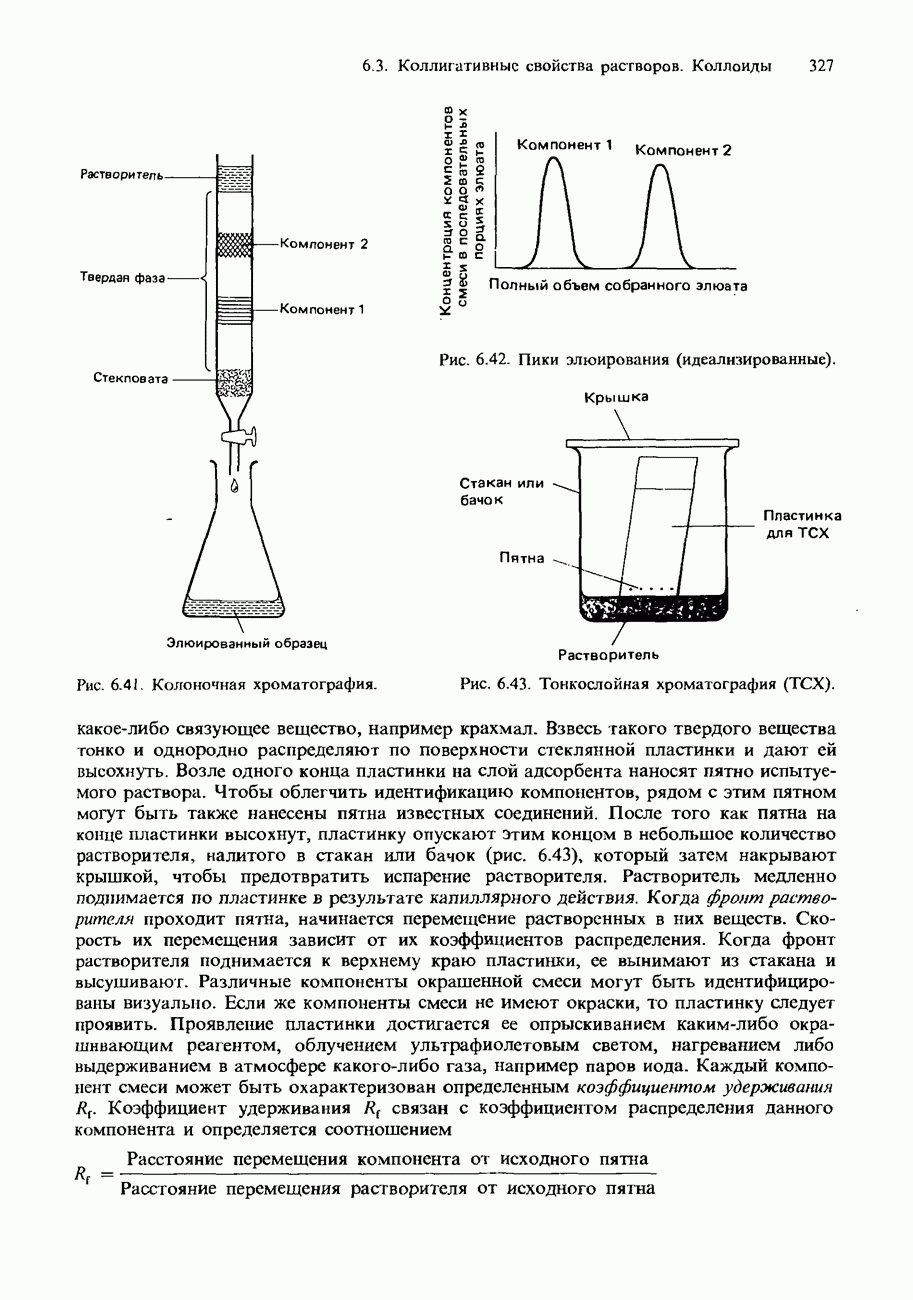
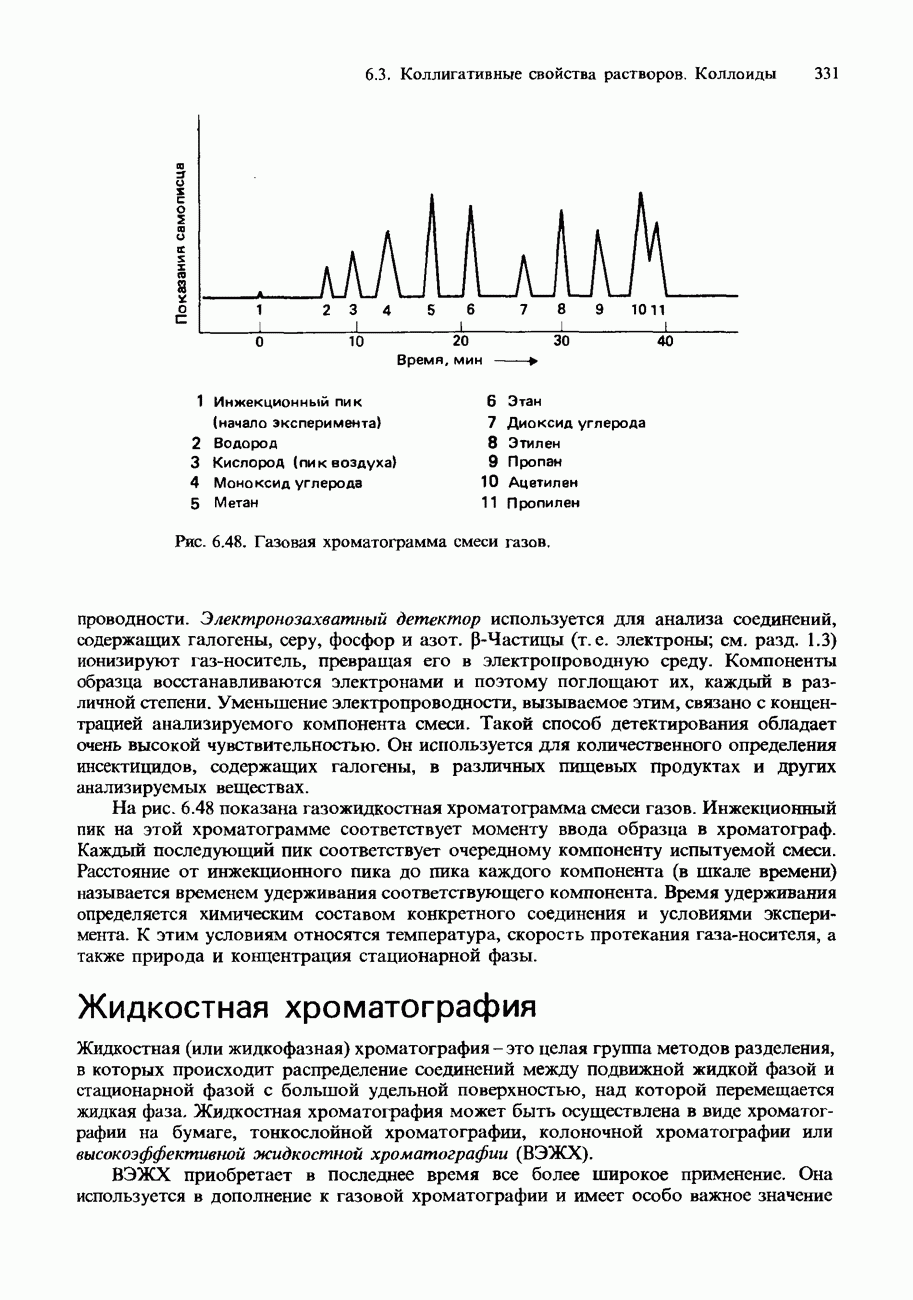
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
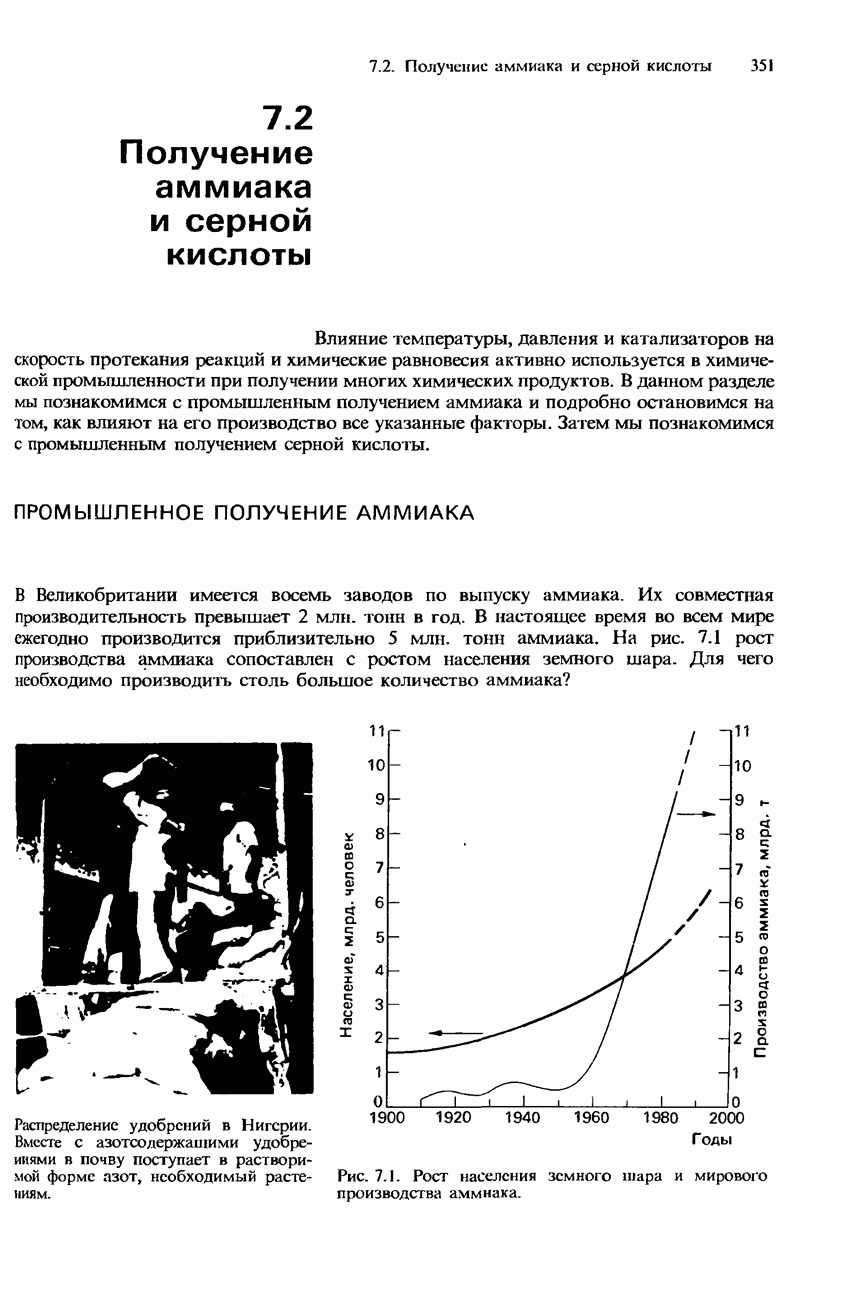
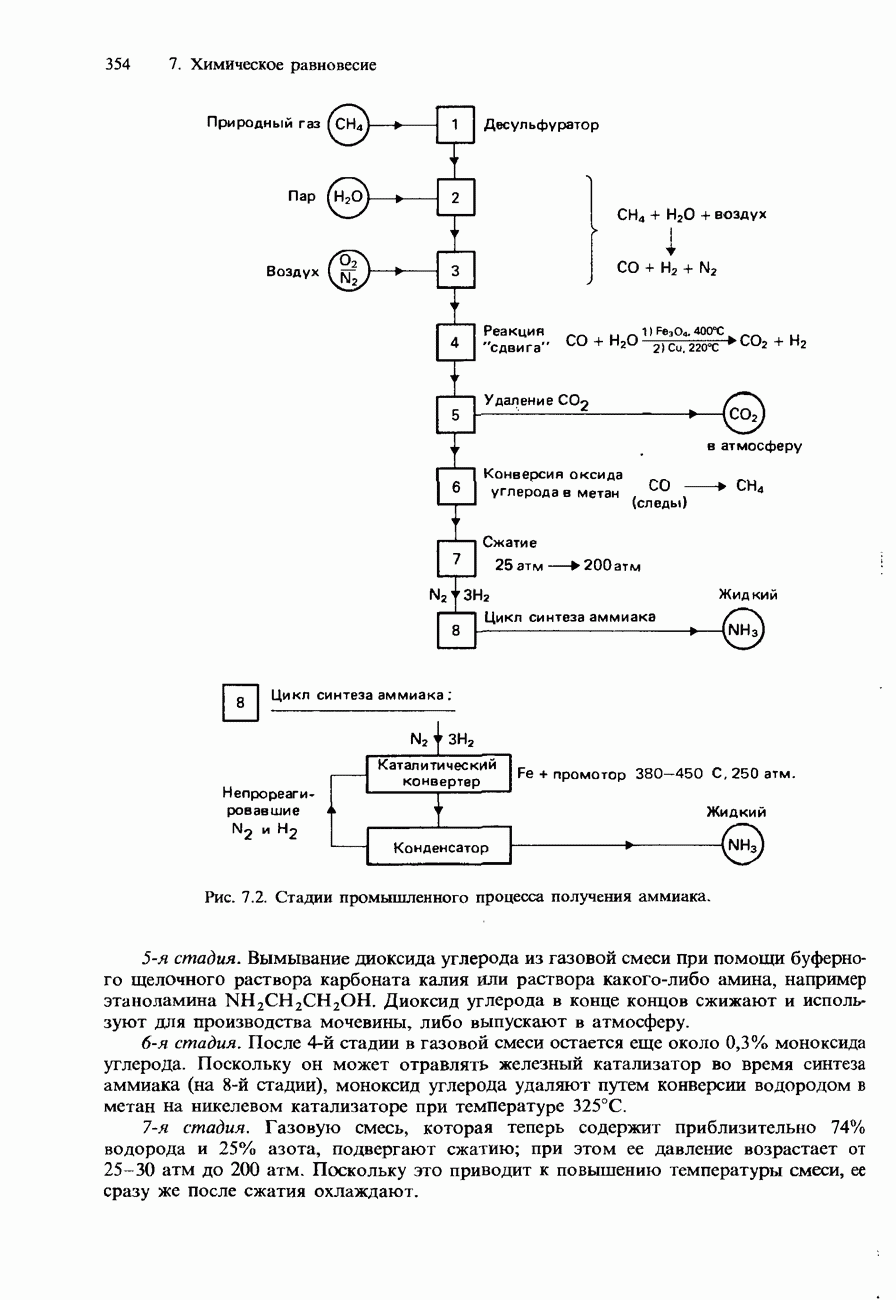
- 7.2. Получение аммиака и серной кислоты
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
- 10.4. Химические источники тока
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
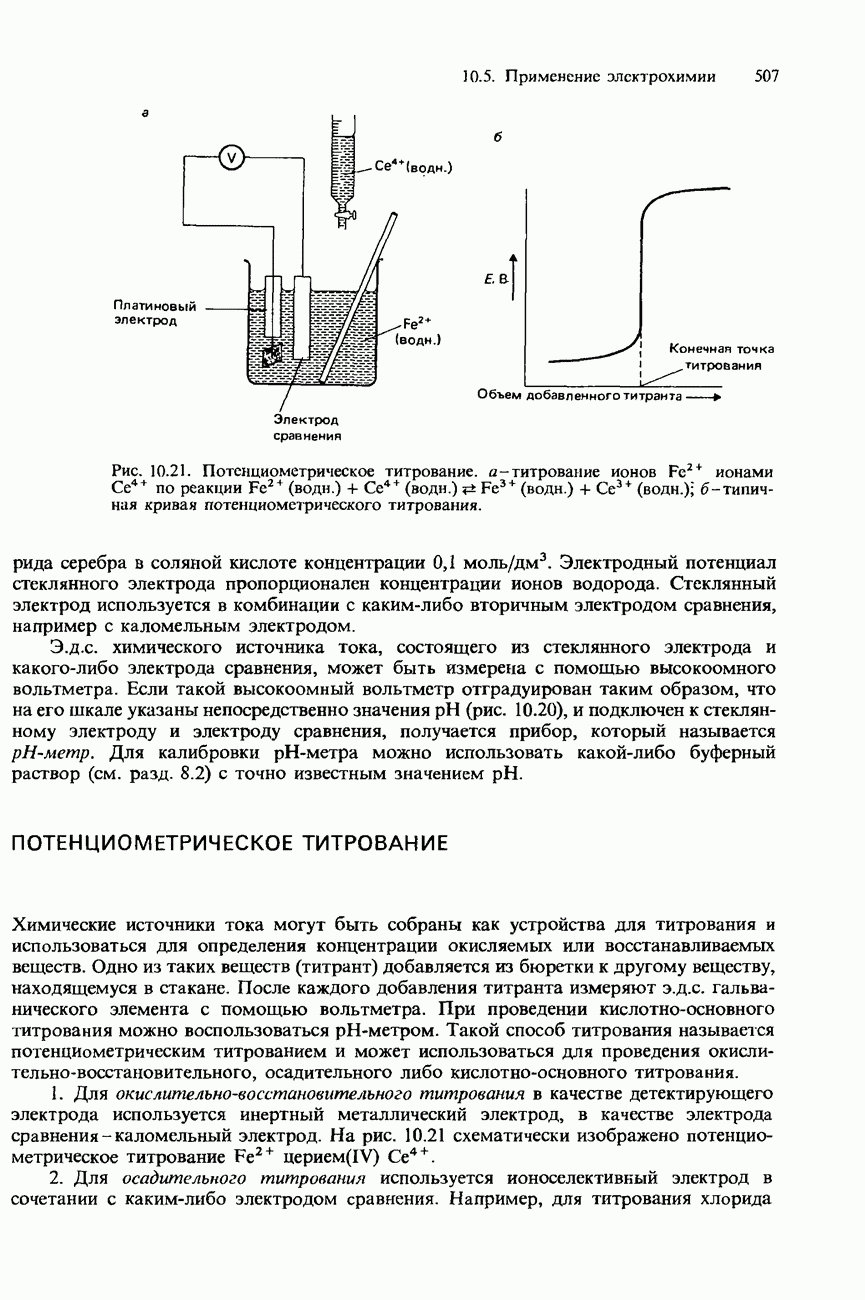
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
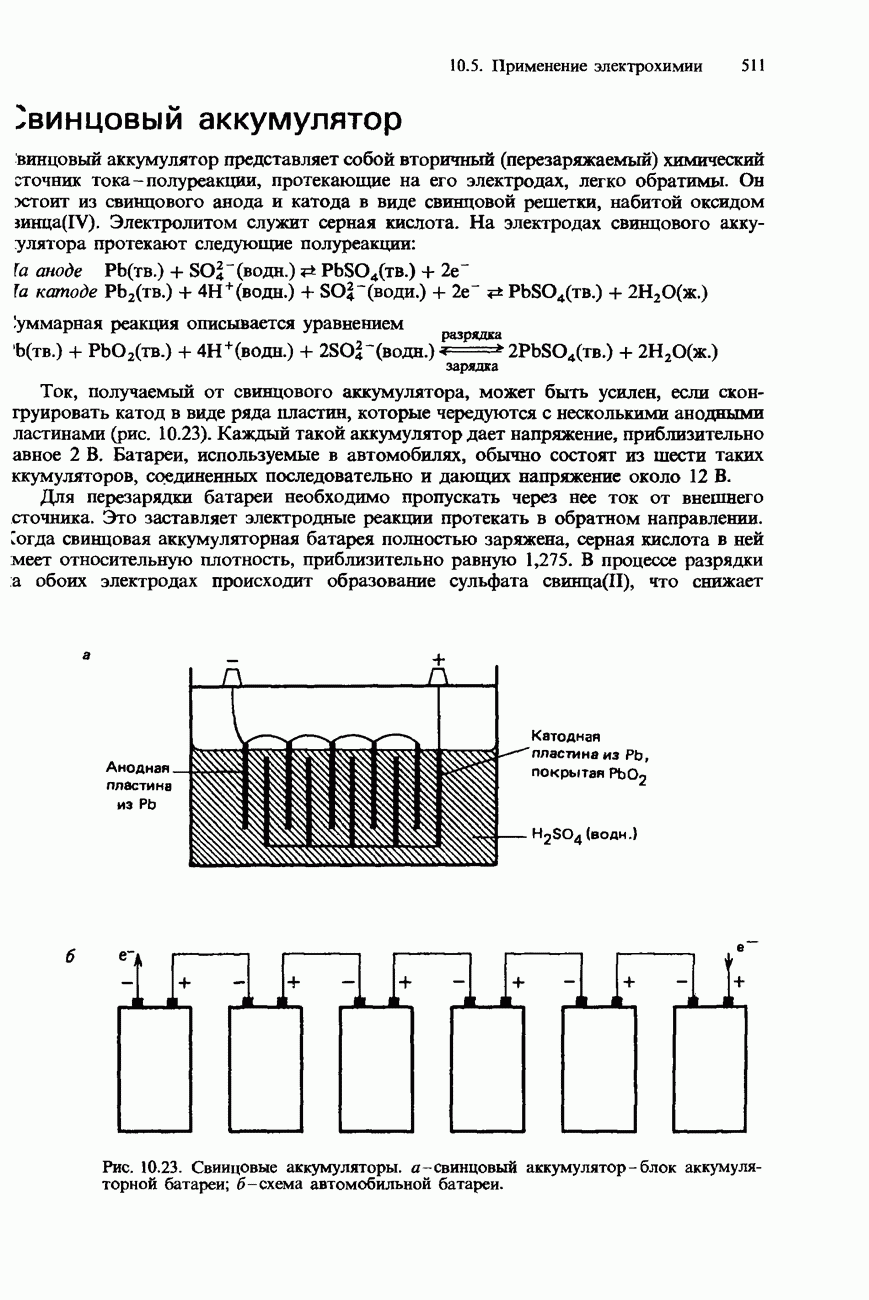
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ