| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
Мы уже указывали, что свободная энергия Гиббса позволяет получать информацию двоякого рода. Во-первых, свободная энергия образования химического соединения является мерой устойчивости этого соединения. Во-вторых, изменение свободной энергии в химической реакции является мерой самопроизвольной осуществимости этой реакции. Самопроизвольное протекание возможно только для таких реакций, которые характеризуются отрицательными значениями  . Однако свободная энергия Гиббса позволяет получать не только такие сведения.
. Однако свободная энергия Гиббса позволяет получать не только такие сведения.
Равновесие
Если система находится в состоянии динамического равновесия, то

Если реакция характеризуется большим по абсолютной величине и отрицательным по знаку значением  , то можно заключить, что равновесие в данной реакции сильно сдвинуто вправо (если судить по уравнению реакции), т.е. в сторону образования продуктов. Если же свободная энергия реакции имеет большое положительное значение, то равновесие сдвинуто влево - в сторону образования реагентов.
, то можно заключить, что равновесие в данной реакции сильно сдвинуто вправо (если судить по уравнению реакции), т.е. в сторону образования продуктов. Если же свободная энергия реакции имеет большое положительное значение, то равновесие сдвинуто влево - в сторону образования реагентов.
Полезная работа
Мы уже знаем, что если в системе происходит превращение при постоянном давлении, то энергия, передаваемая в форме теплоты между системой и ее окружением, называется изменением энтальпии  . Если представить это изменение энтальпии с помощью уравнения (24), то видно, что оно выражается в виде суммы двух частей
. Если представить это изменение энтальпии с помощью уравнения (24), то видно, что оно выражается в виде суммы двух частей 

 представляет собой часть изменения энтальпии, которая может использоваться для выполнения полезной работы (рис. 5.17). Остальная часть изменения энтальпии не может использоваться для выполнения работы. Она соответствует энтропийному члену
представляет собой часть изменения энтальпии, которая может использоваться для выполнения полезной работы (рис. 5.17). Остальная часть изменения энтальпии не может использоваться для выполнения работы. Она соответствует энтропийному члену 

Рис. 5.17. Две составляющие, в виде суммы которых можно представить изменение энтальпии:  полное изменение энергии при постоянной температуре;
полное изменение энергии при постоянной температуре;  - свободная энергия (доступная для выполнения полезной работы);
- свободная энергия (доступная для выполнения полезной работы);  - несвободная энергия (недоступная для выполнения полезной работы).
- несвободная энергия (недоступная для выполнения полезной работы).
Оценка возможности получения металлов из их оксидов по величине
Металлы можно получать, восстанавливая их оксиды (см. разд. 10.5). Для этой цели используются такие восстановители, как углерод и другие металлы. Но как можно определить, будет ли углерод или другой металл самопроизвольно восстанавливать оксид конкретного металла? Чтобы ответить на этот вопрос, рассмотрим два следующих случая.
Случай 1

Например,

В этом случае металл играет роль восстановителя. Он восстанавливает углерод из диоксида углерода.
Случай 2

Например,

В этом случае роль восстановителя играет углерод. Он восстанавливает металл из его оксида.
Нетрудно видеть, что случай 2 является обратным по отношению к случаю 1. К некоторым металлам применим случай 1, а к другим металлам-случай 2. Каким же образом можно заранее предсказать, какой случай применим к какому-либо конкретно рассматриваемому металлу? Другими словами, как предсказать-какая реакция окажется самопроизвольной: соответствующая случаю 1 или случаю 2?
Ответ заключается в сопоставлении устойчивости оксидов. Выше было указано, что мерой устойчивости соединения является свободная энергия его образования. Мы видели также, что для самопроизвольного протекания реакции изменение свободной энергии  , которым она сопровождается, должно быть отрицательным, т. е.
, которым она сопровождается, должно быть отрицательным, т. е.  Если применить это условие к изменению свободной энергии, выраженному с помощью уравнения (25), то получится следующее условие самопроизвольного протекания реакции:
Если применить это условие к изменению свободной энергии, выраженному с помощью уравнения (25), то получится следующее условие самопроизвольного протекания реакции:

В каждом из двух рассмотренных выше случаев один из продуктов и один из реагентов являются свободными элементами. Поскольку стандартные молярные свободные энергии образования свободных элементов равны нулю, условие самопроизвольного протекания рассмотренных реакций приобретает следующий вид:

Следовательно, в обоих случаях более устойчивый оксид, т. е. оксид с более отрицательным значением свободной энергии образования  должен быть продуктом, а не реагентом. Стандартные молярные свободные энергии образования оксидов, рассмотренных в примерах, приведены в табл. 5.15. Эти значения показывают, что в первом из рассмотренных выше примеров оксид магния обладает большей устойчивостью, чем диоксид углерода. Поэтому оксид магния оказывается продуктом, а не
должен быть продуктом, а не реагентом. Стандартные молярные свободные энергии образования оксидов, рассмотренных в примерах, приведены в табл. 5.15. Эти значения показывают, что в первом из рассмотренных выше примеров оксид магния обладает большей устойчивостью, чем диоксид углерода. Поэтому оксид магния оказывается продуктом, а не
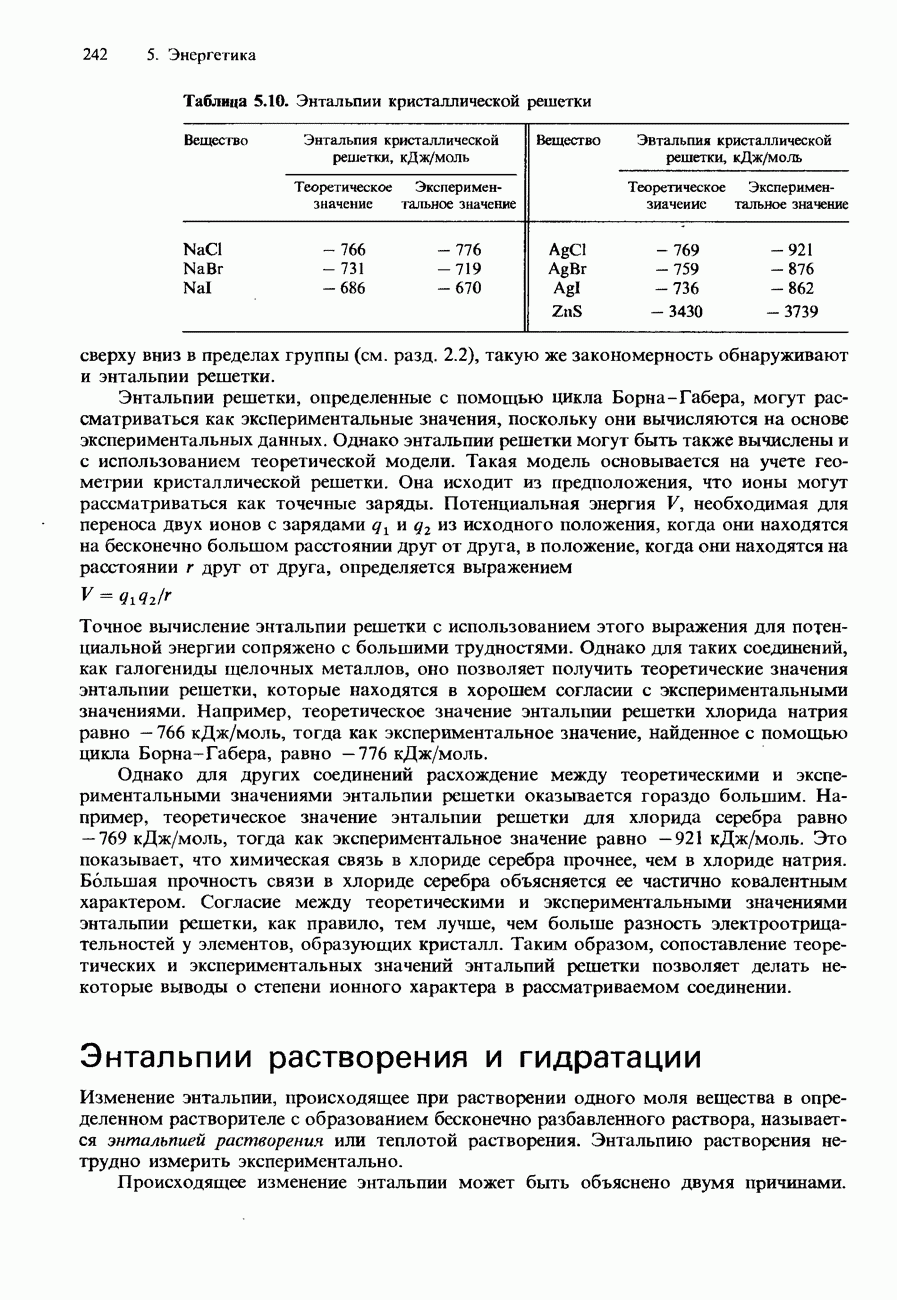
Твблица 5.15. Стандартные молярные свободные энергии образования некоторых оксидов

реагентом. Самопроизвольно протекает прямая, а не обратная (по отношению к записанному уравнению) реакция. Другими словами, к данной реакции применим случай 1.
Второй пример оказывается более сложным. Согласно значениям  приведенным в табл. 5.15, продуктом рассматриваемой реакции должен быть
приведенным в табл. 5.15, продуктом рассматриваемой реакции должен быть  а не
а не  Почему же эта реакция была выбрана в качестве примера к случаю 2? Дело, оказывается, в температуре реакции. Эта реакция не протекает при 298 К. Для ее осуществления необходима более высокая температура.
Почему же эта реакция была выбрана в качестве примера к случаю 2? Дело, оказывается, в температуре реакции. Эта реакция не протекает при 298 К. Для ее осуществления необходима более высокая температура.
Диаграммы Эллингема
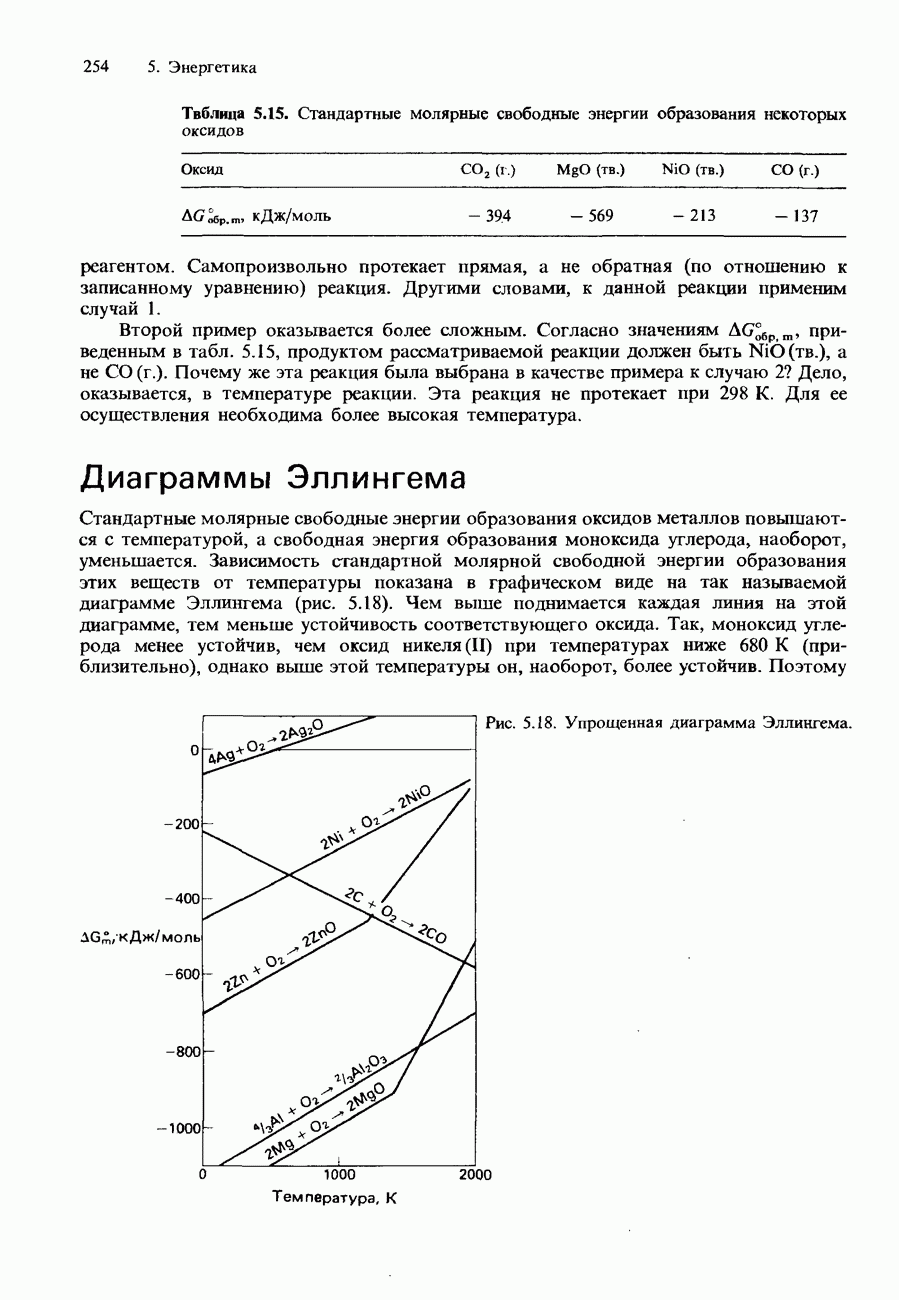
Стандартные молярные свободные энергии образования оксидов металлов повышаются с температурой, а свободная энергия образования моноксида углерода, наоборот, уменьшается. Зависимость стандартной молярной свободной энергии образования этих веществ от температуры показана в графическом виде на так называемой диаграмме Эллингема (рис. 5.18). Чем выше поднимается каждая линия на этой диаграмме, тем меньше устойчивость соответствующего оксида. Так, моноксид углерода менее устойчив, чем оксид никеля (II) при температурах ниже 680 К (приблизительно), однако выше этой температуры он, наоборот, более устойчив. Поэтому

Рис. 5.18. Упрощенная диаграмма Эллингема.
реакцию восстановления оксида никеля углеродом обычно проводят при температурах выше 680 К.
Диаграммы Эллингема позволяют наглядно определять, какой оксид будет восстанавливаться в каждой конкретной реакции. При заданной температуре восстанавливаться должен тот оксид, линия которого расположена выше. Так, при 1000 К магний должен восстанавливать оксид алюминия, однако при 2000 К алюминий будет восстанавливать оксид магния. Вместе с тем, как показывает диаграмма, магний должен восстанавливать оксид цинка при любой температуре ниже 2000 К. Изломы линий на диаграмме Эллингема указывают фазовые превращения (плавление или кипение) металлов. При этих фазовых превращениях происходит резкое возрастание энтропии и соответственное изменение  . Отметим также, что свободная энергия образования оксида серебра отрицательна при низких температурах, но становится положительной при повышении температуры. Изменение знака свободной энергии (т. е. достижение точки, в которой
. Отметим также, что свободная энергия образования оксида серебра отрицательна при низких температурах, но становится положительной при повышении температуры. Изменение знака свободной энергии (т. е. достижение точки, в которой  происходит при температуре 440 К.
происходит при температуре 440 К.
Итак, повторим еще раз!
1. Стандартная энтальпия диссоциации связи - это изменение энтальпии, которым сопровождается разрыв одного моля связей при условии, что исходные молекулы и их фрагменты находятся в своих стандартных состояниях при температуре 298 К и давлении 1 атм.
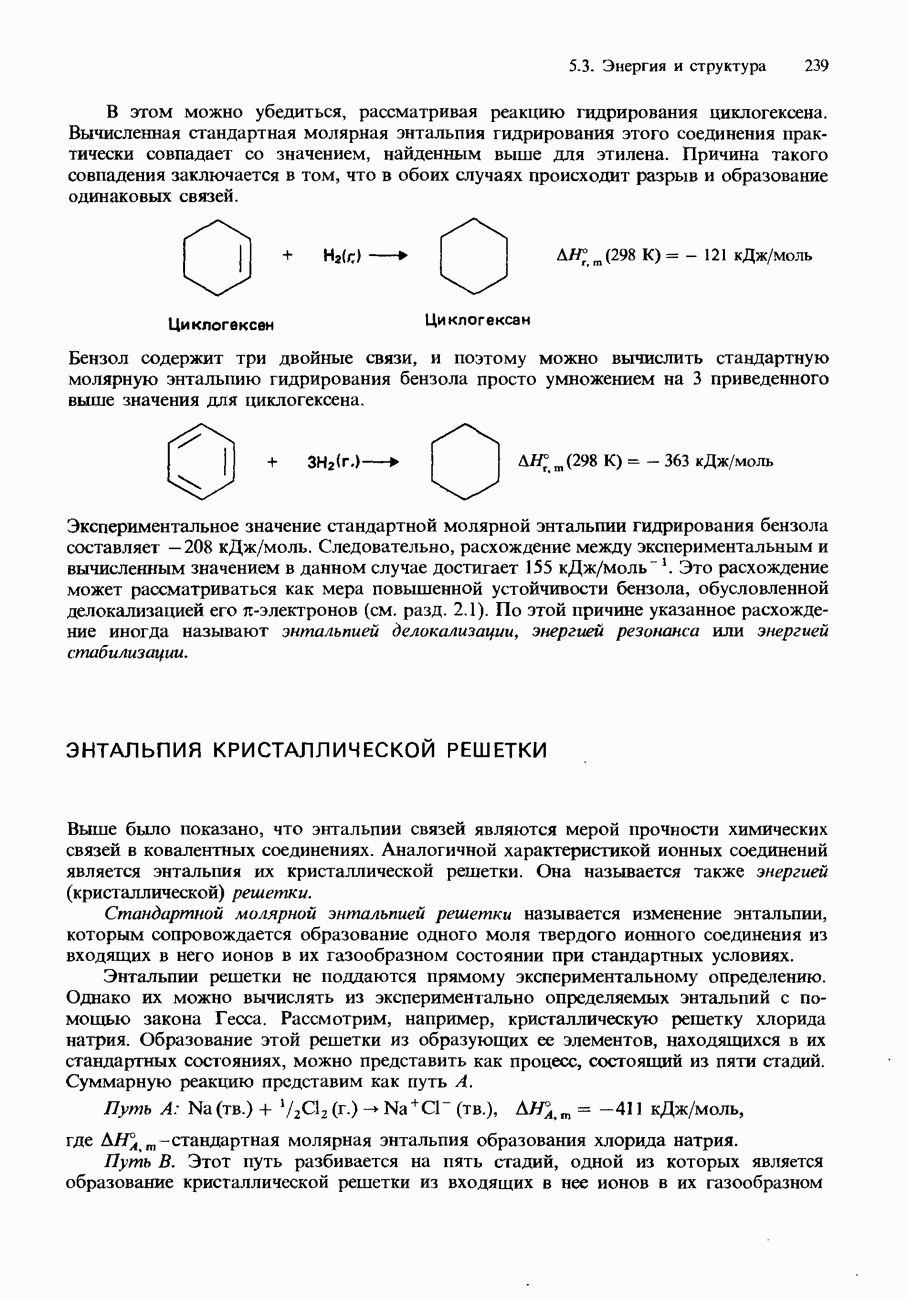
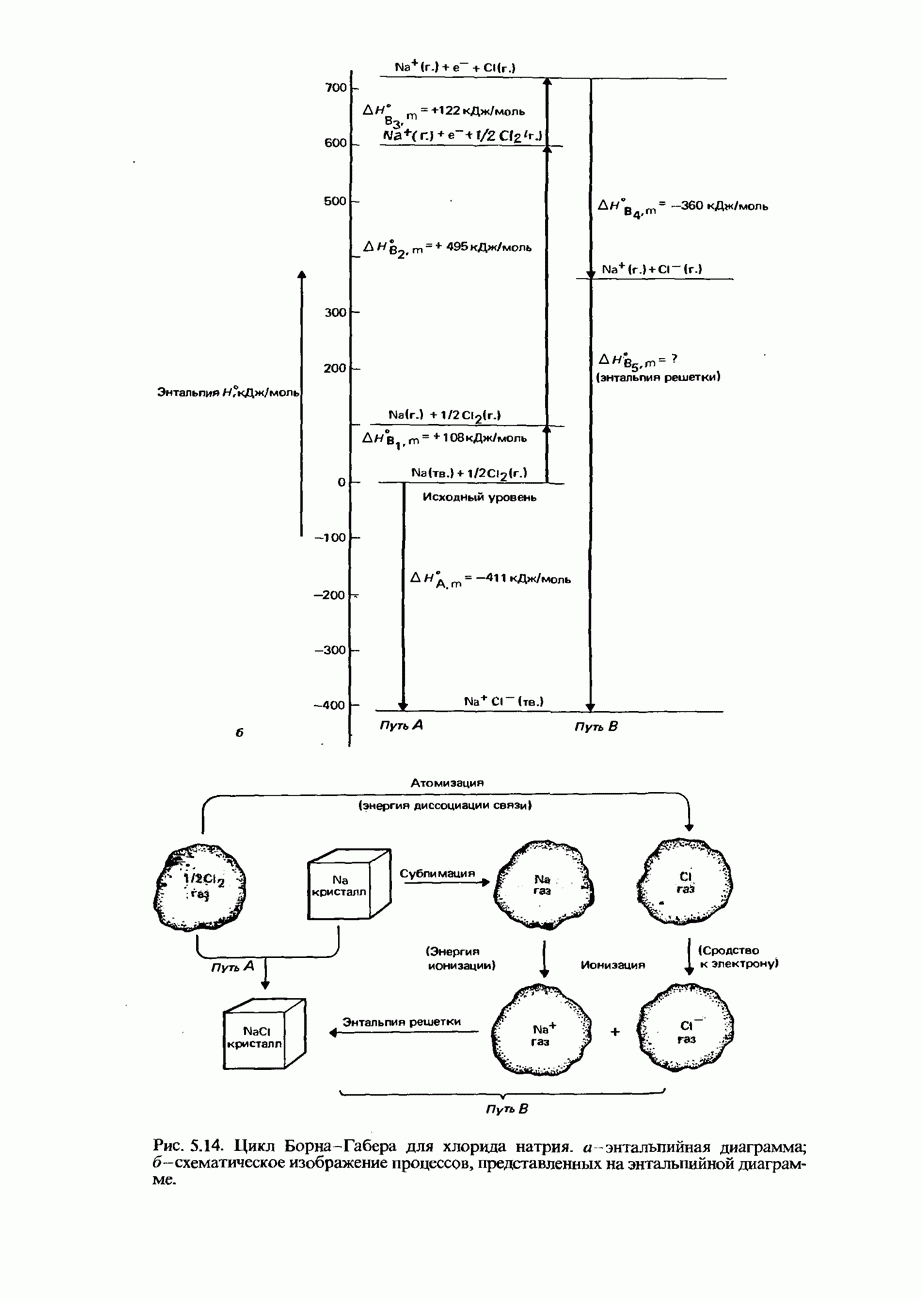
2. Стандартная молярная энтальпия решетки - это изменение энтальпии, которым сопровождается образование одного моля кристаллического ионного соединения из входящих в него газообразных ионов в их стандартных состояниях.
3. Цикл Борна Габера - это энтальпийная диаграмма, по которой можно определить энтальпию ионной решетки соли.
4. Стандартная молярная энтальпия растворения определяется соотношением

5. Второй закон термодинамики утверждает, что полная энтропия системы и ее окружения при любых самопроизвольных процессах возрастает.
6. Для любых самопроизвольных процессов полное изменение энтропии в системе и ее окружении должно быть положительным

где  .
.
7. Стандартное молярное изменение энтропии в химической реакции определяется выражением

8. Изменение свободной энергии Гиббса связано с суммарным изменением энтропии в системе и ее окружении соотношением

9. Изменение свободной энергии Гиббса в химической реакции является мерой самопроизвольной осуществимости этой реакции.
10. Для реакционной системы

11. Реакция может протекать самопроизвольно только при условии

12. Стандартное молярное изменение свободной энергии в химической реакции определяется выражением

13. Для системы, находящейся в состоянии динамического равновесия,

14. Изменение свободной энергии  представляет собой ту часть изменения энтальпии, которая доступна для выполнения полезной работы.
представляет собой ту часть изменения энтальпии, которая доступна для выполнения полезной работы.
15. Диаграммы Эллингема показывают зависимость стандартной молярной свободной энергии образования соединений от температуры.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
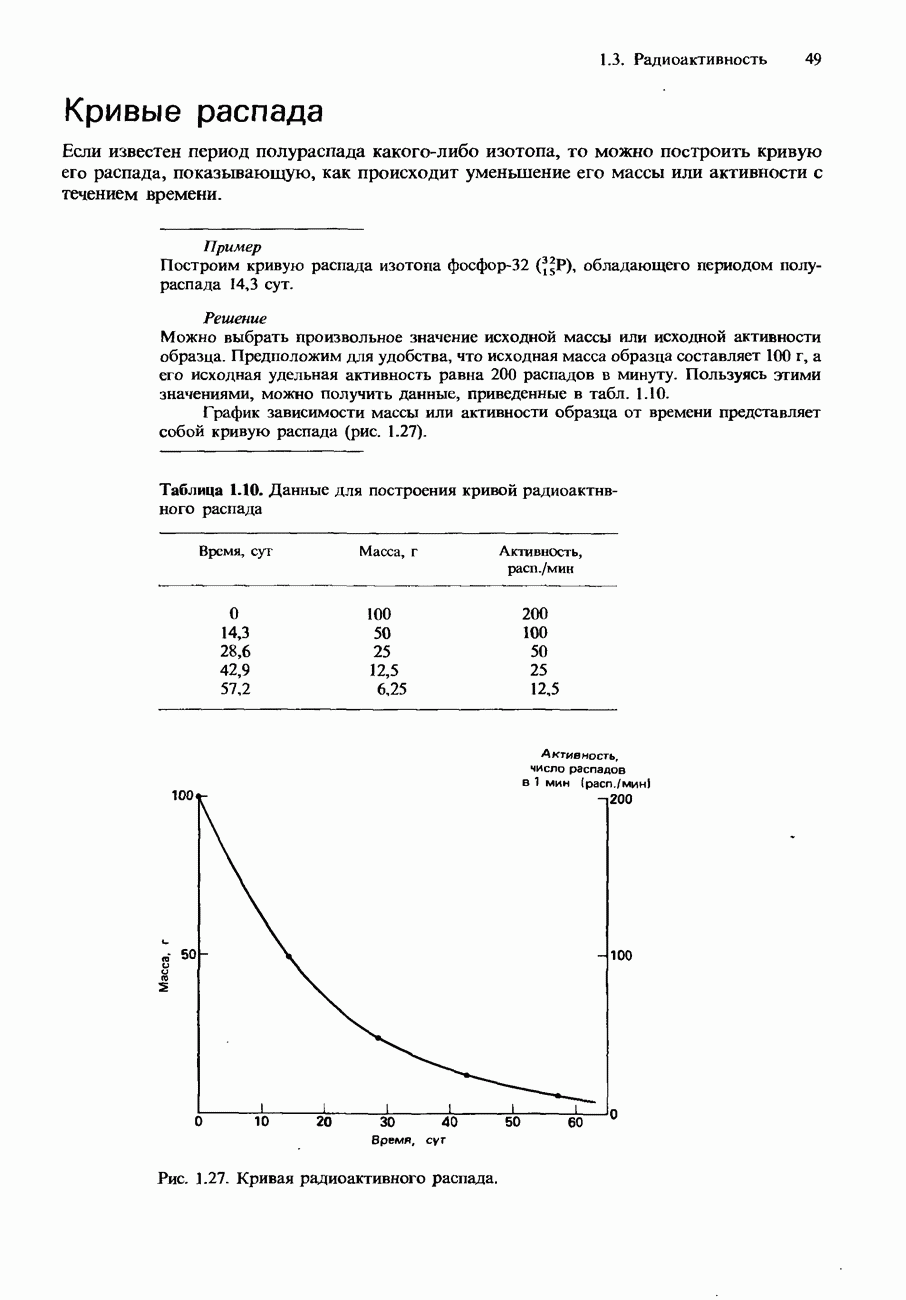
- Кривые распада
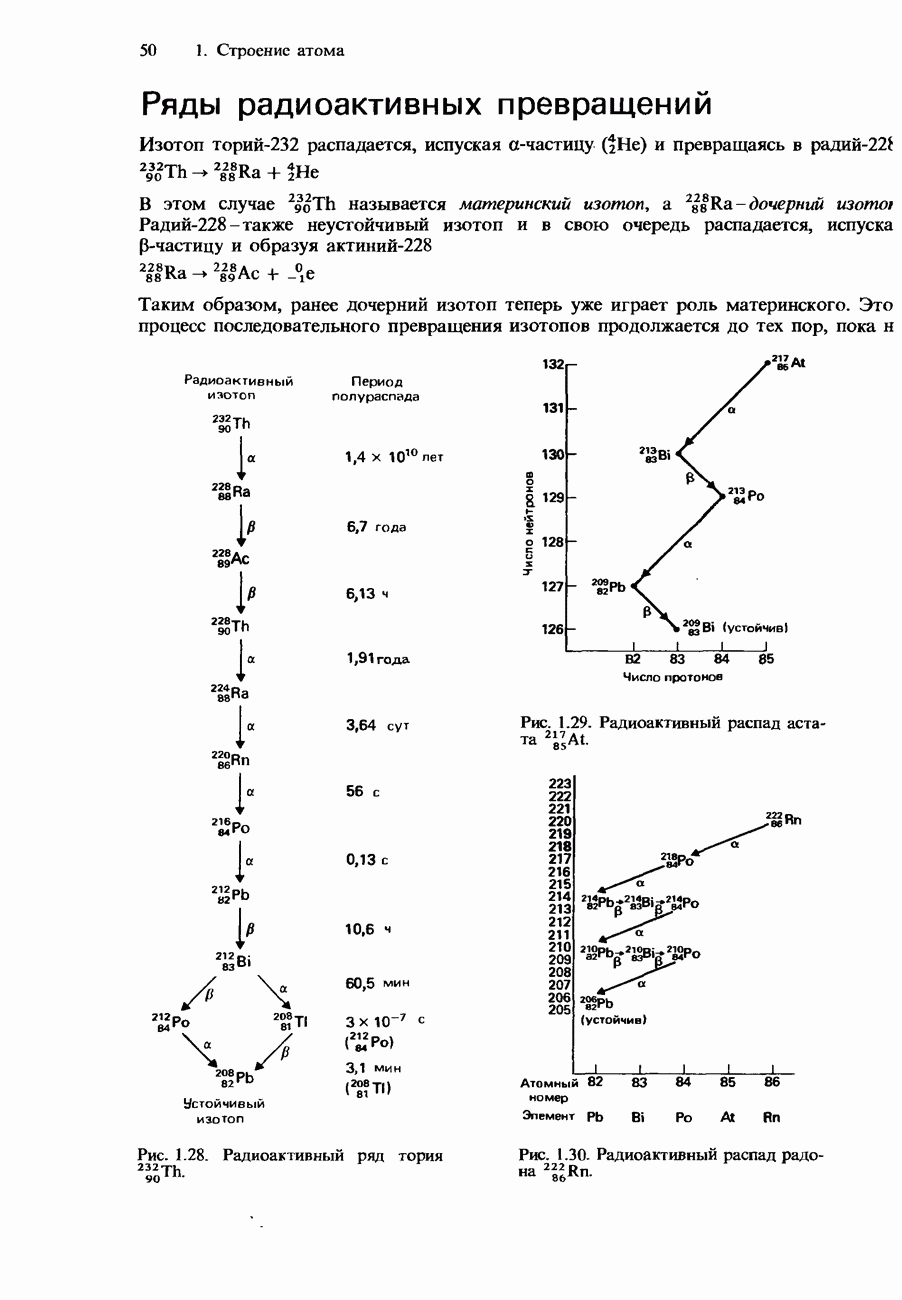
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
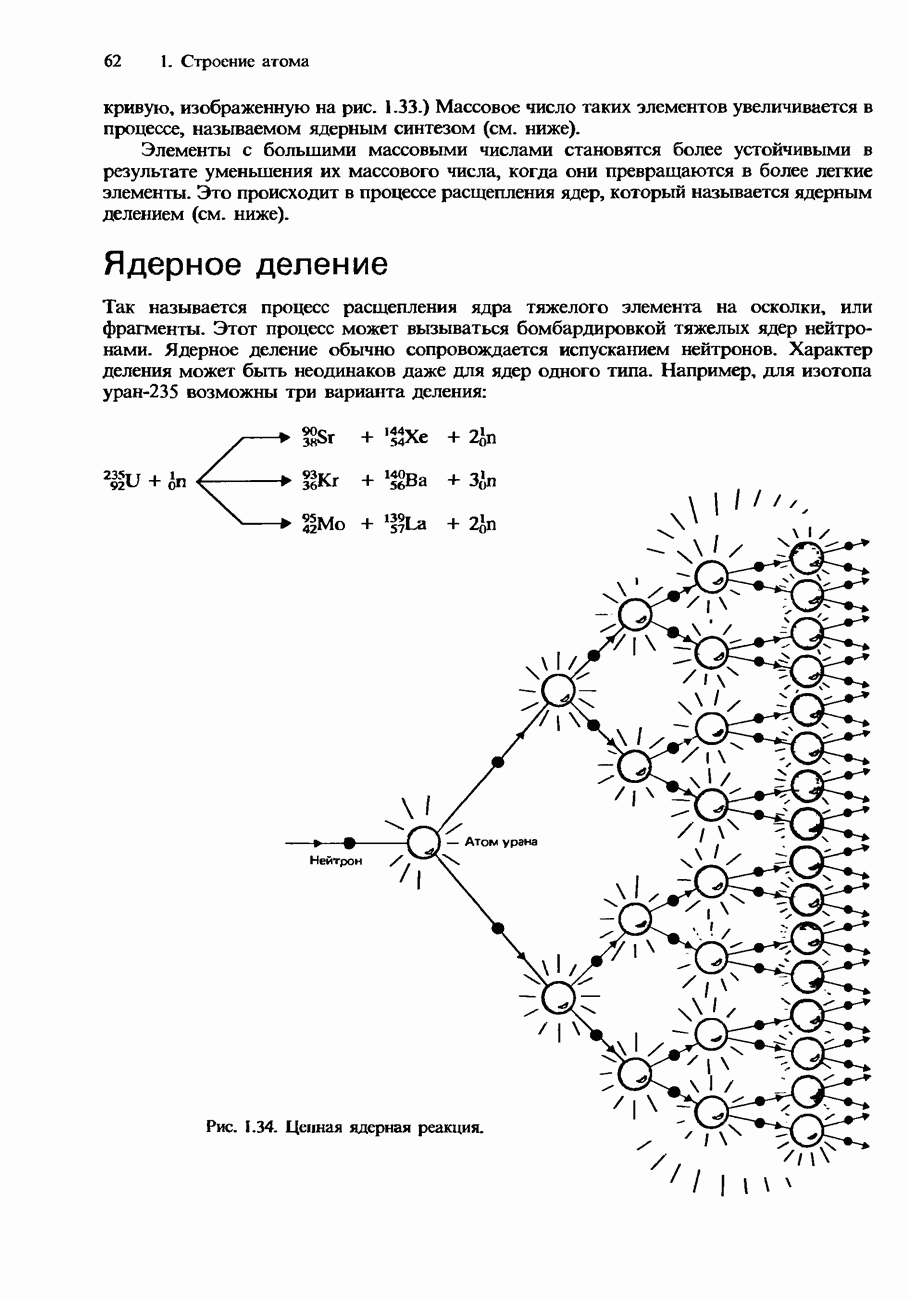
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
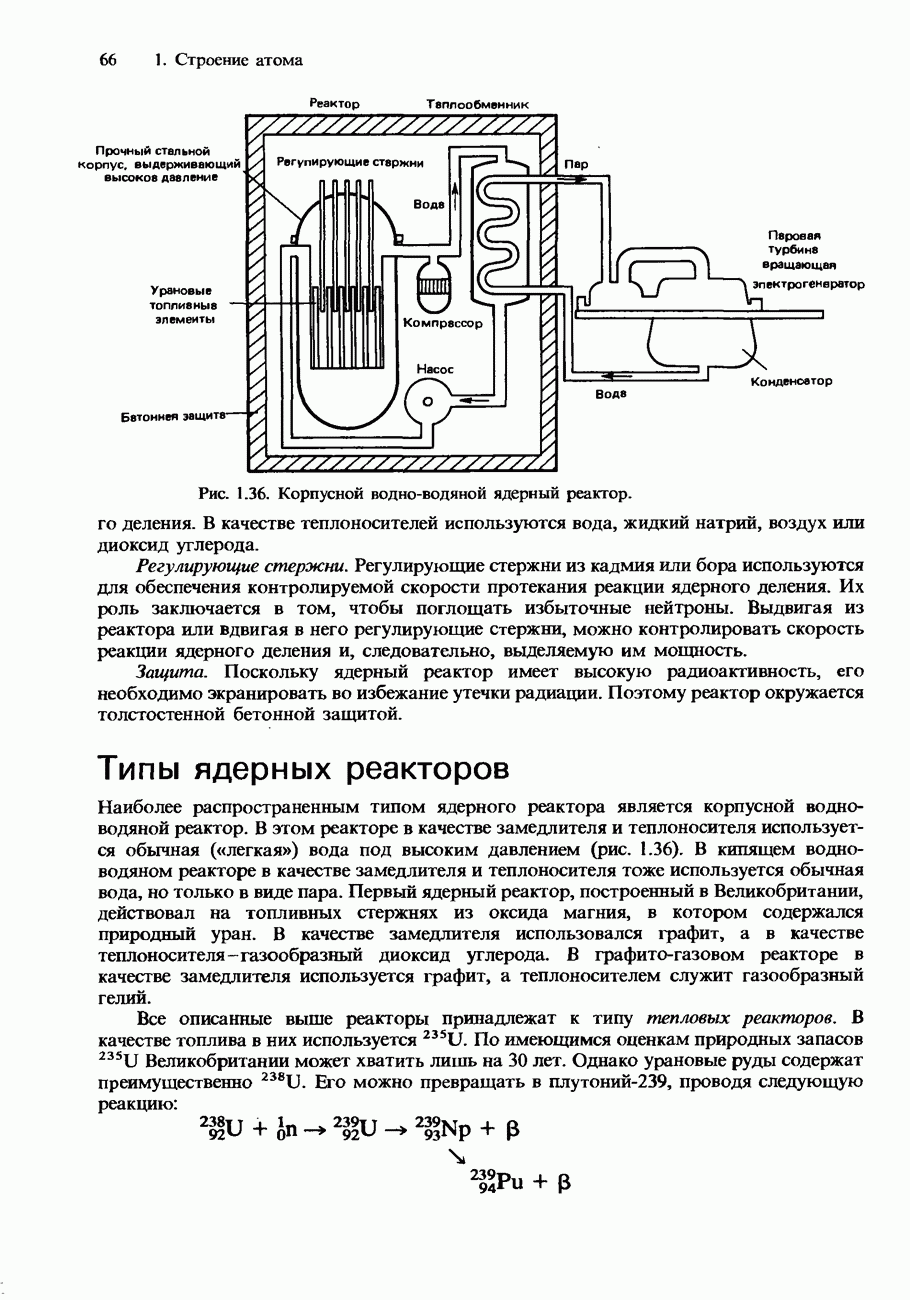
- Типы ядерных реакторов
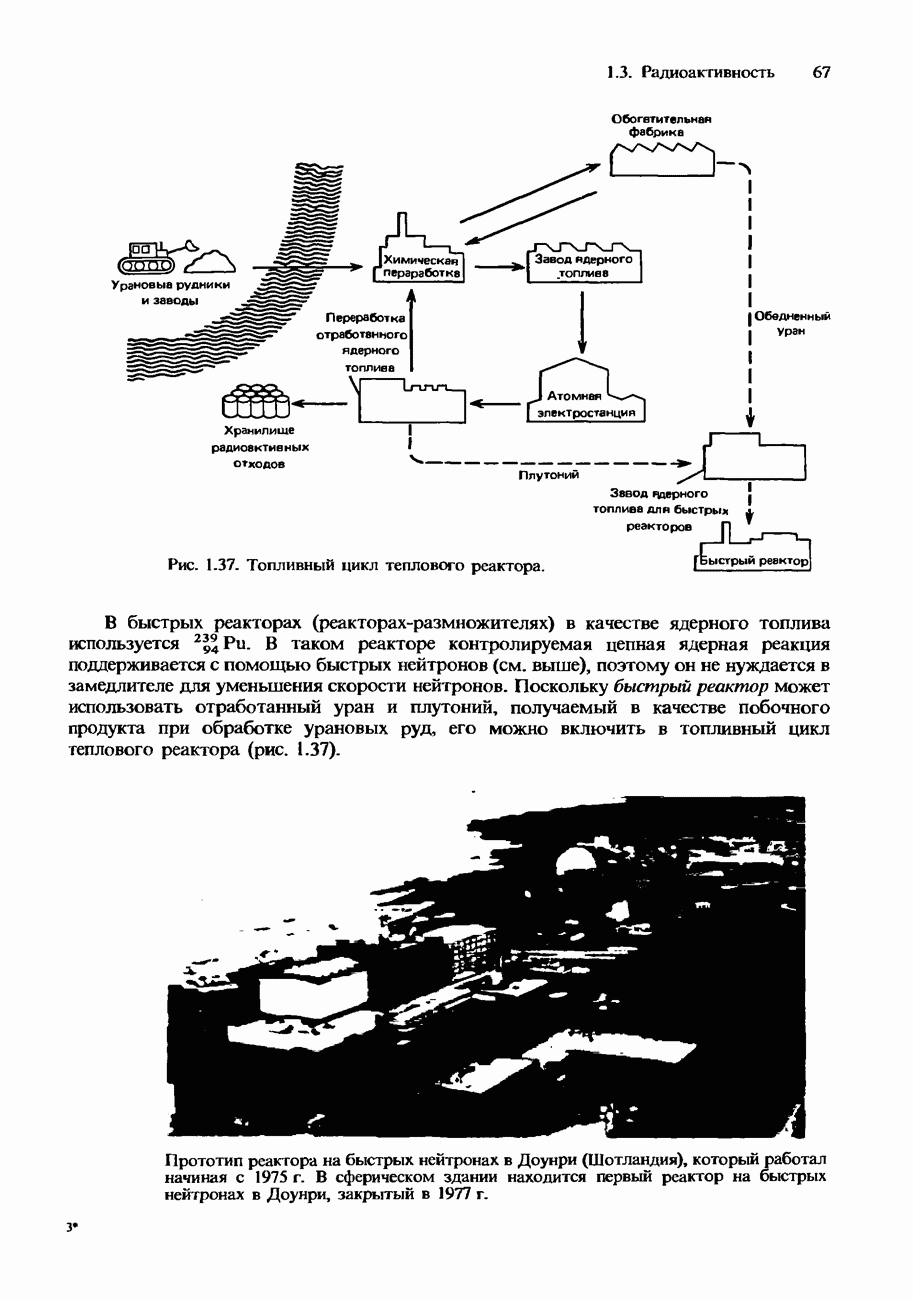
- Радиоактивные ядерные отходы и их переработка
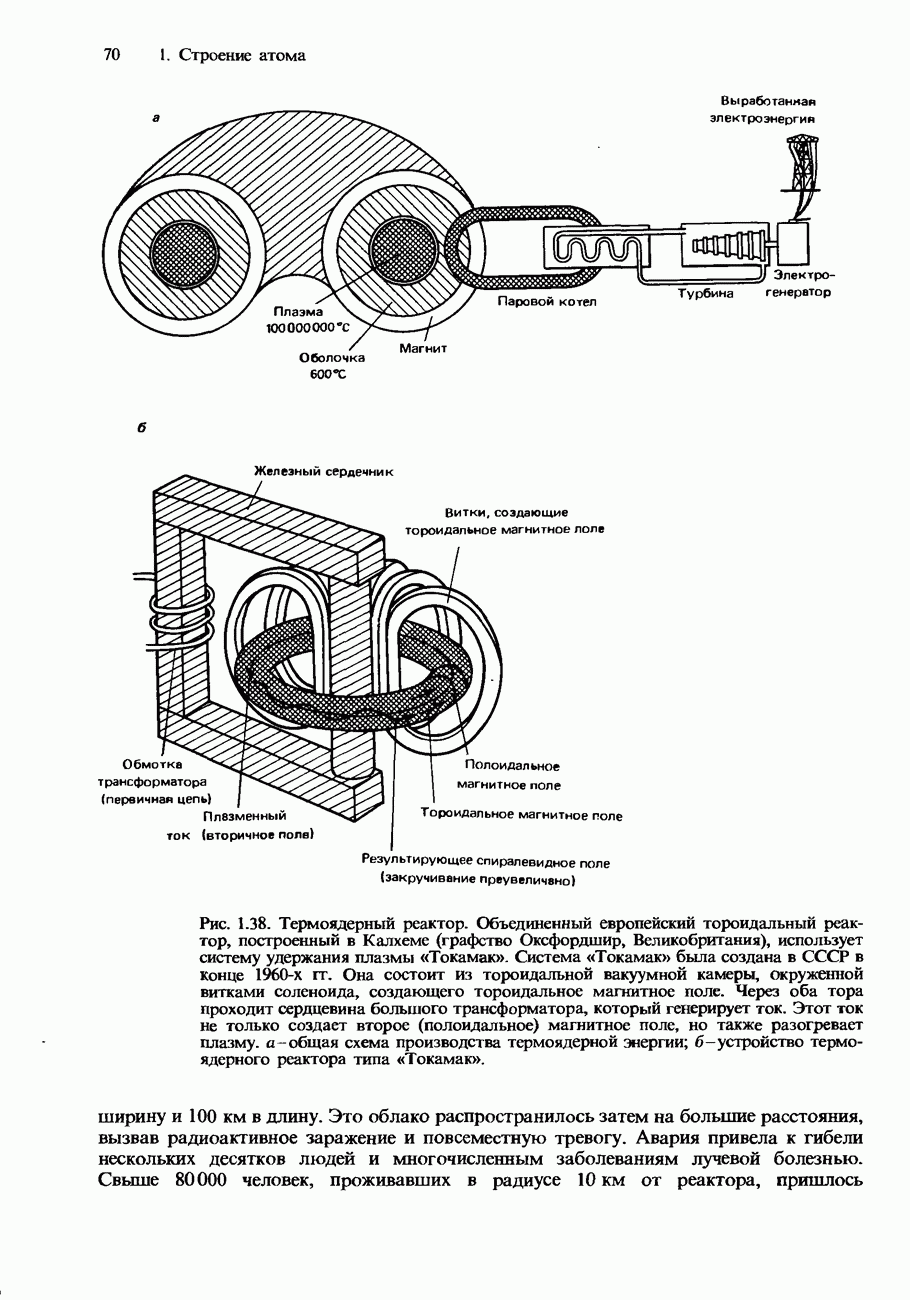
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
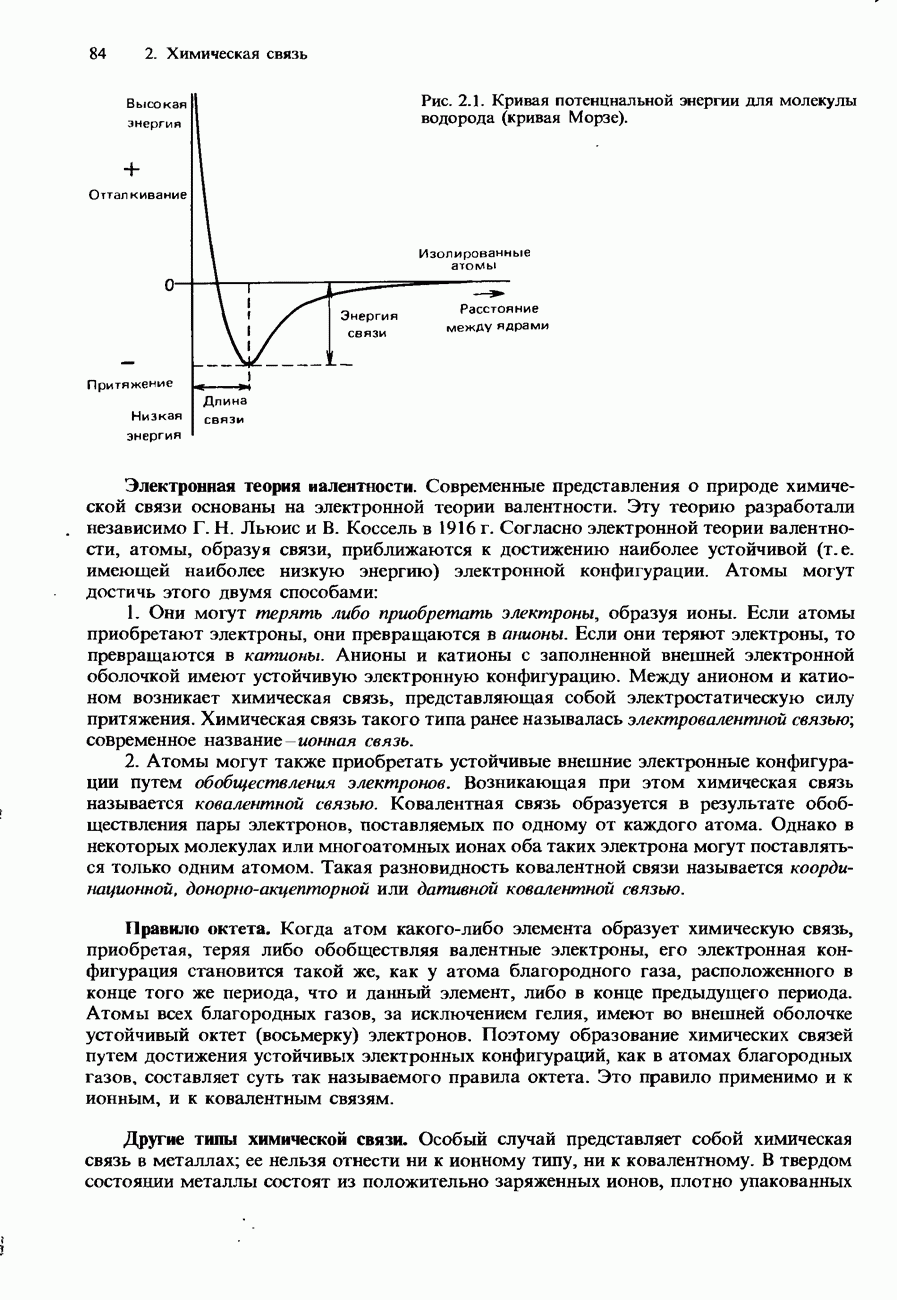
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
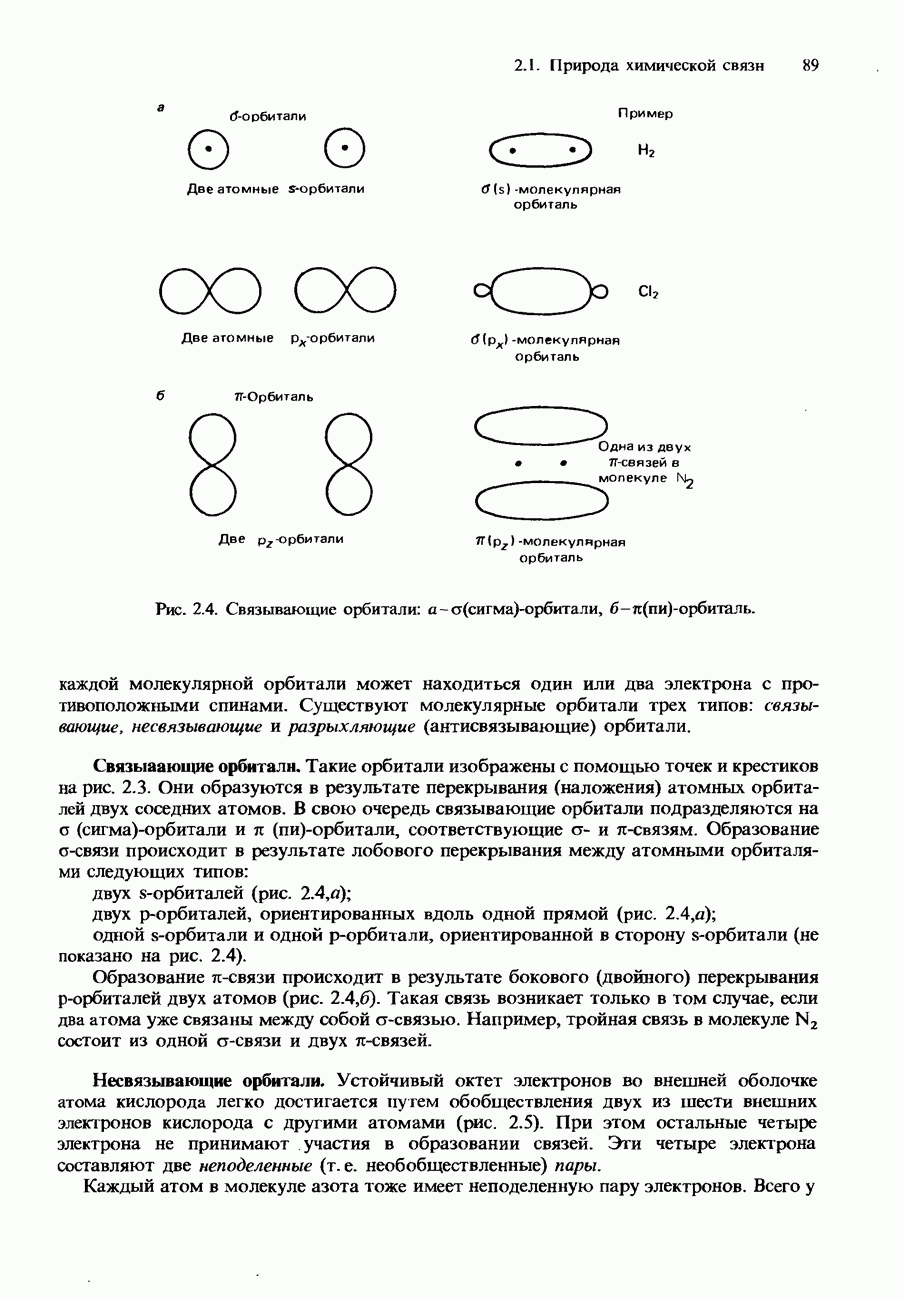
- КОВАЛЕНТНАЯ СВЯЗЬ
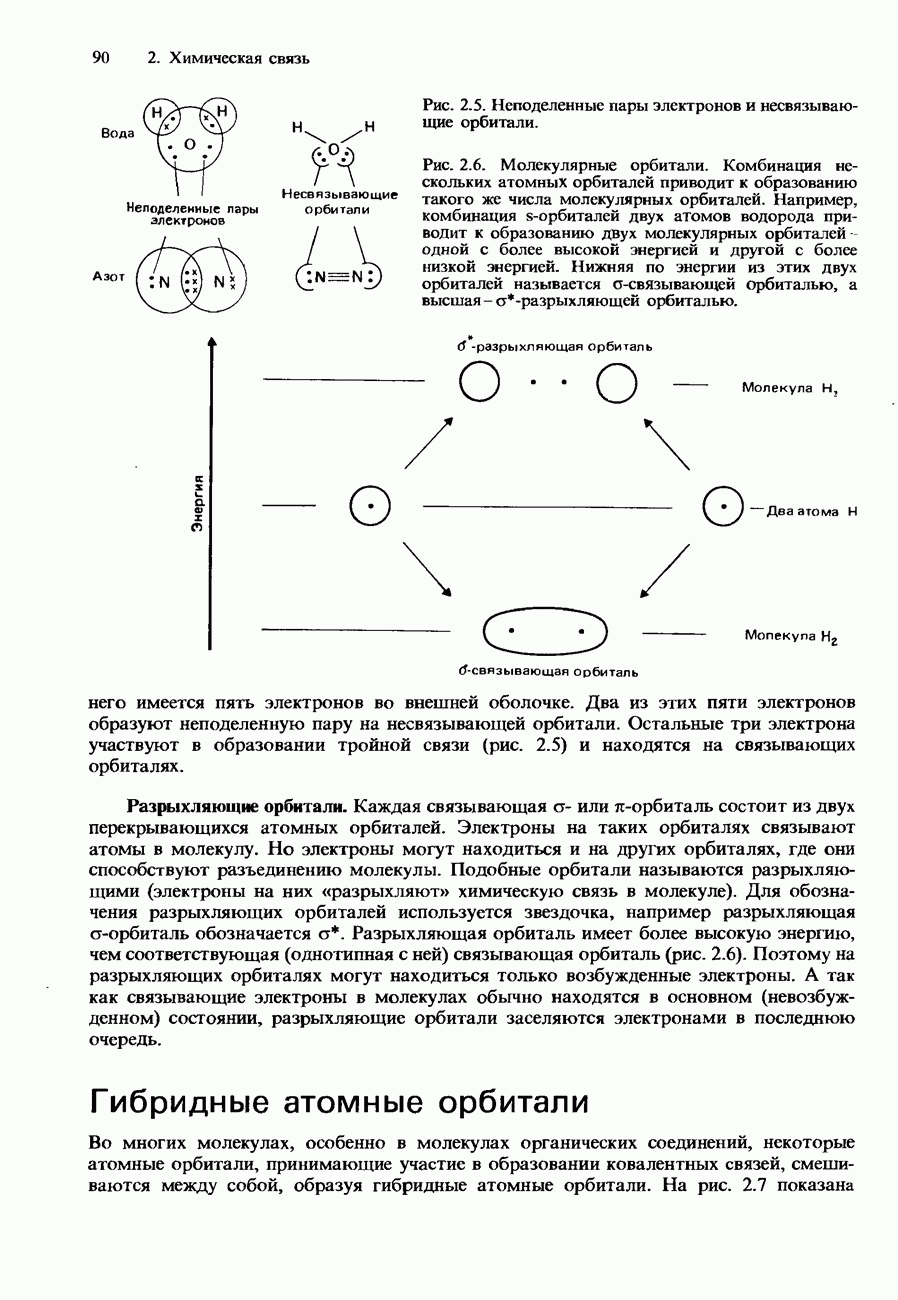
- Молекулярные орбитали
- Гибридные атомные орбитали
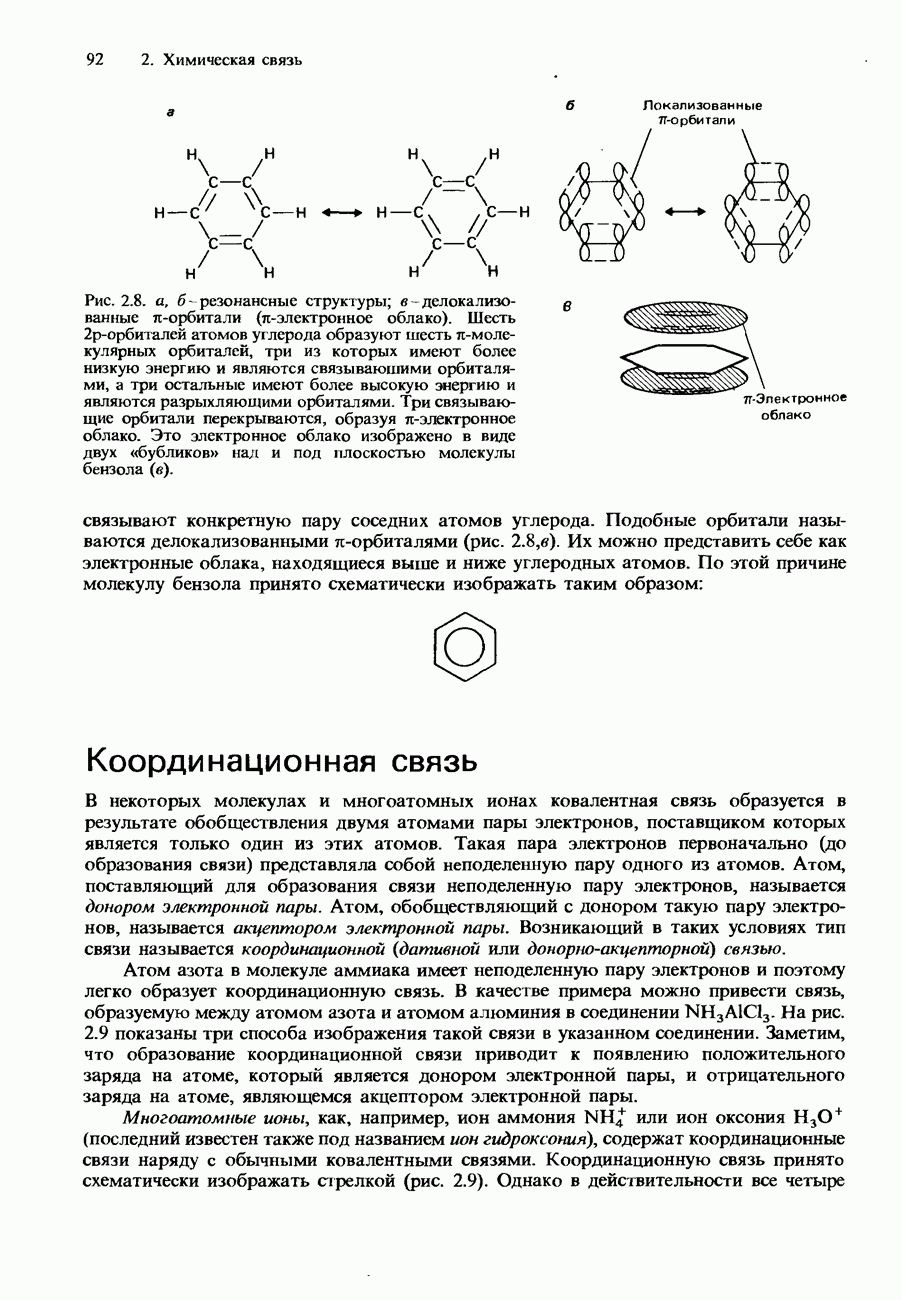
- Делокализованные орбитали
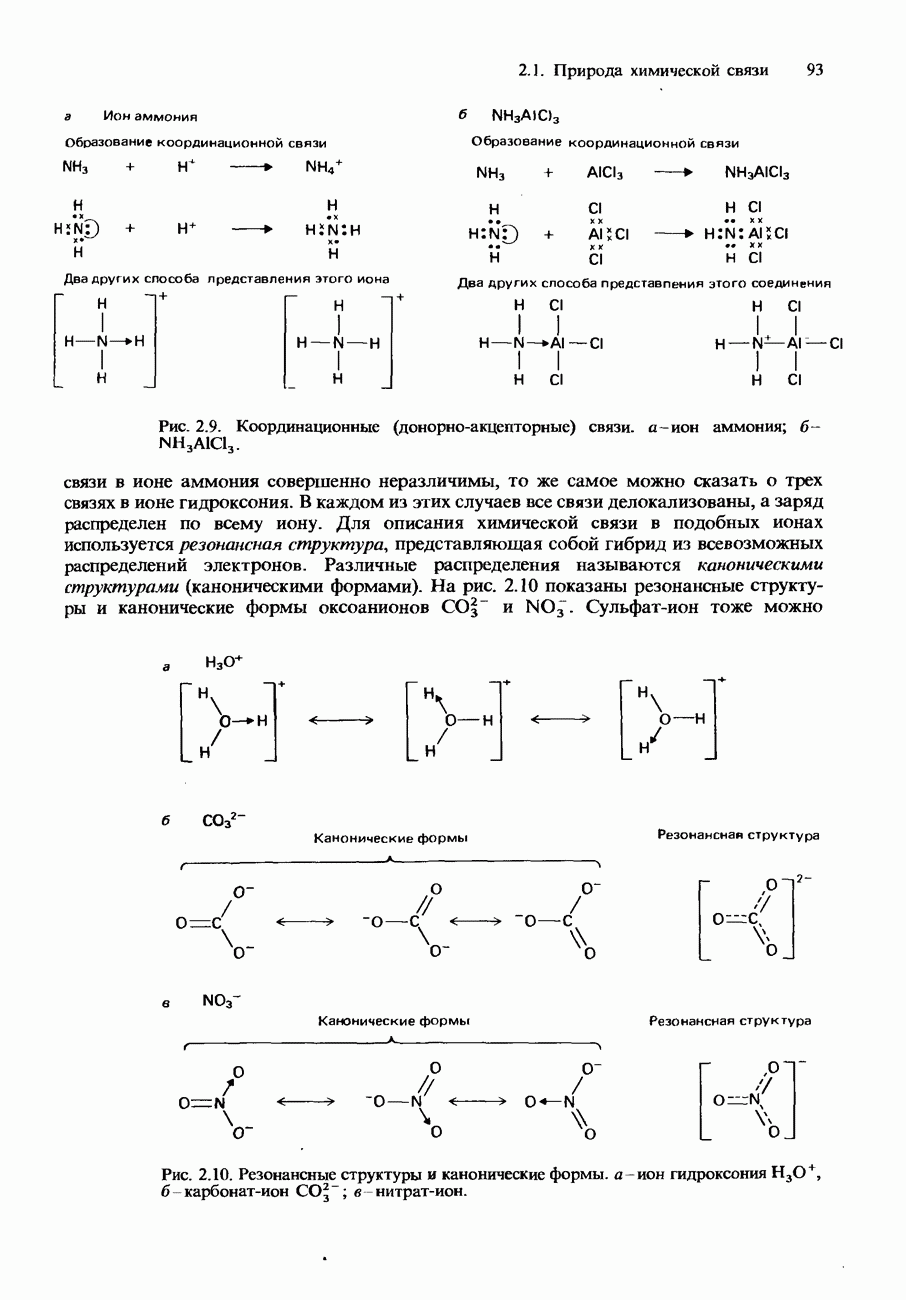
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
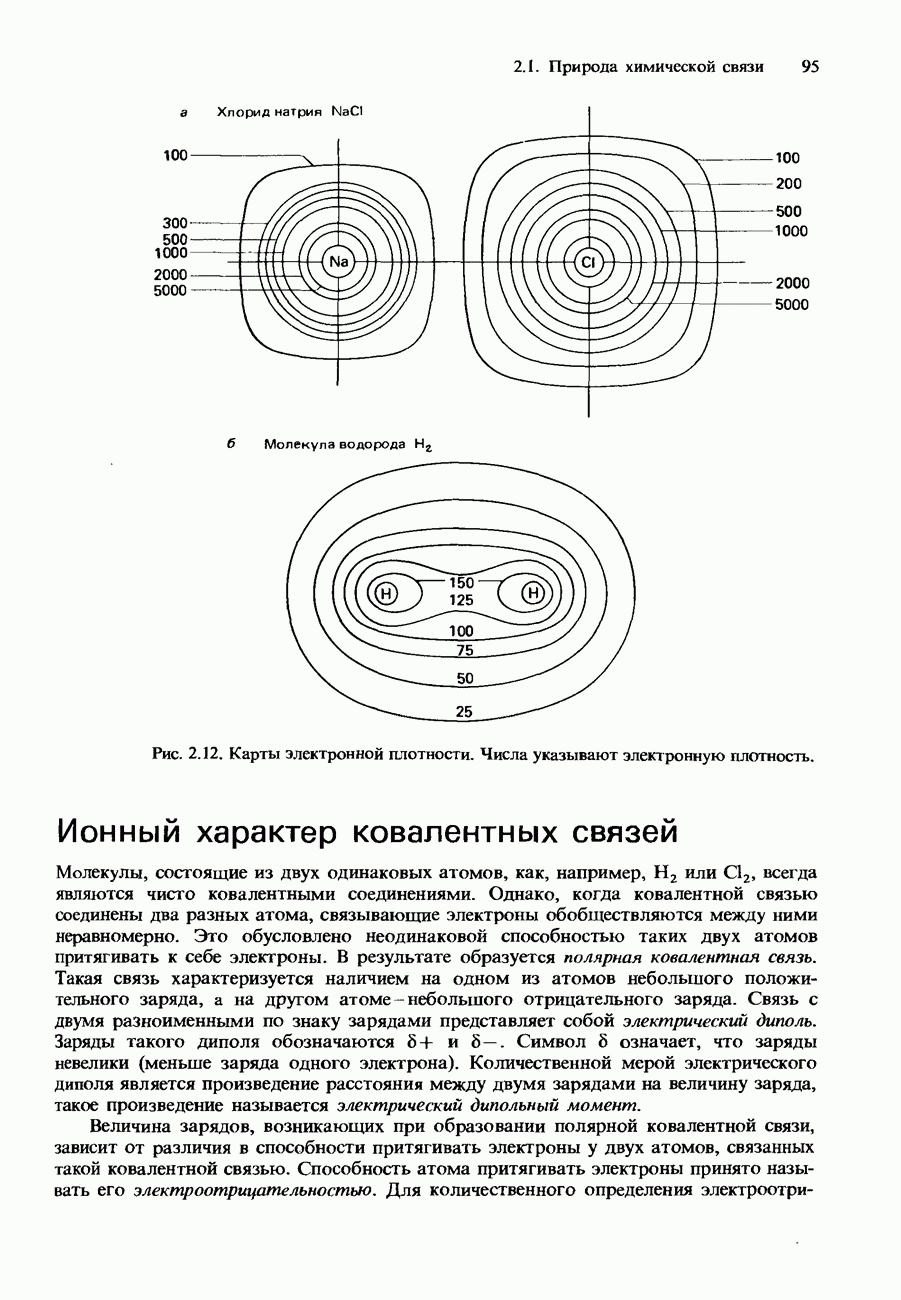
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
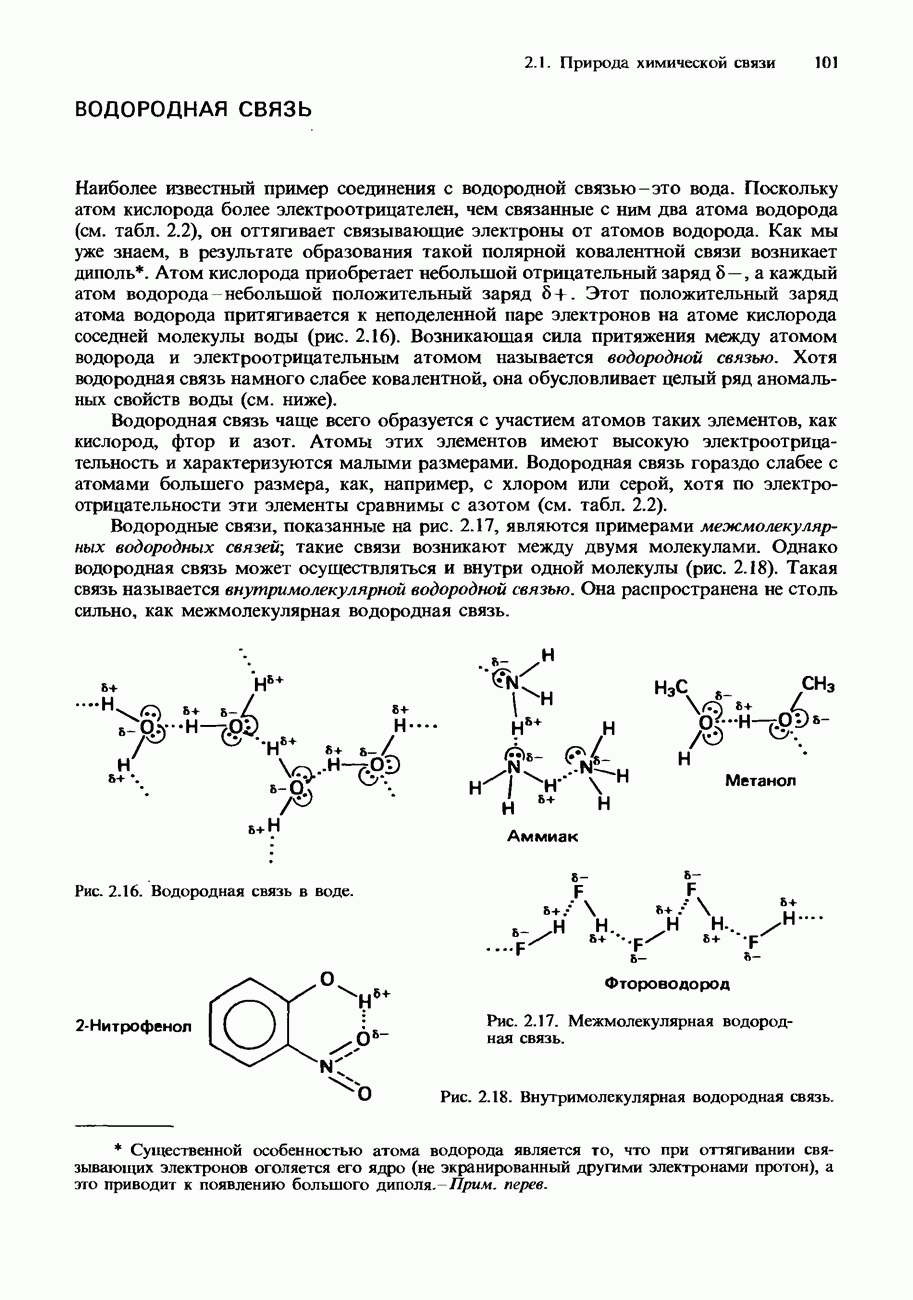
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
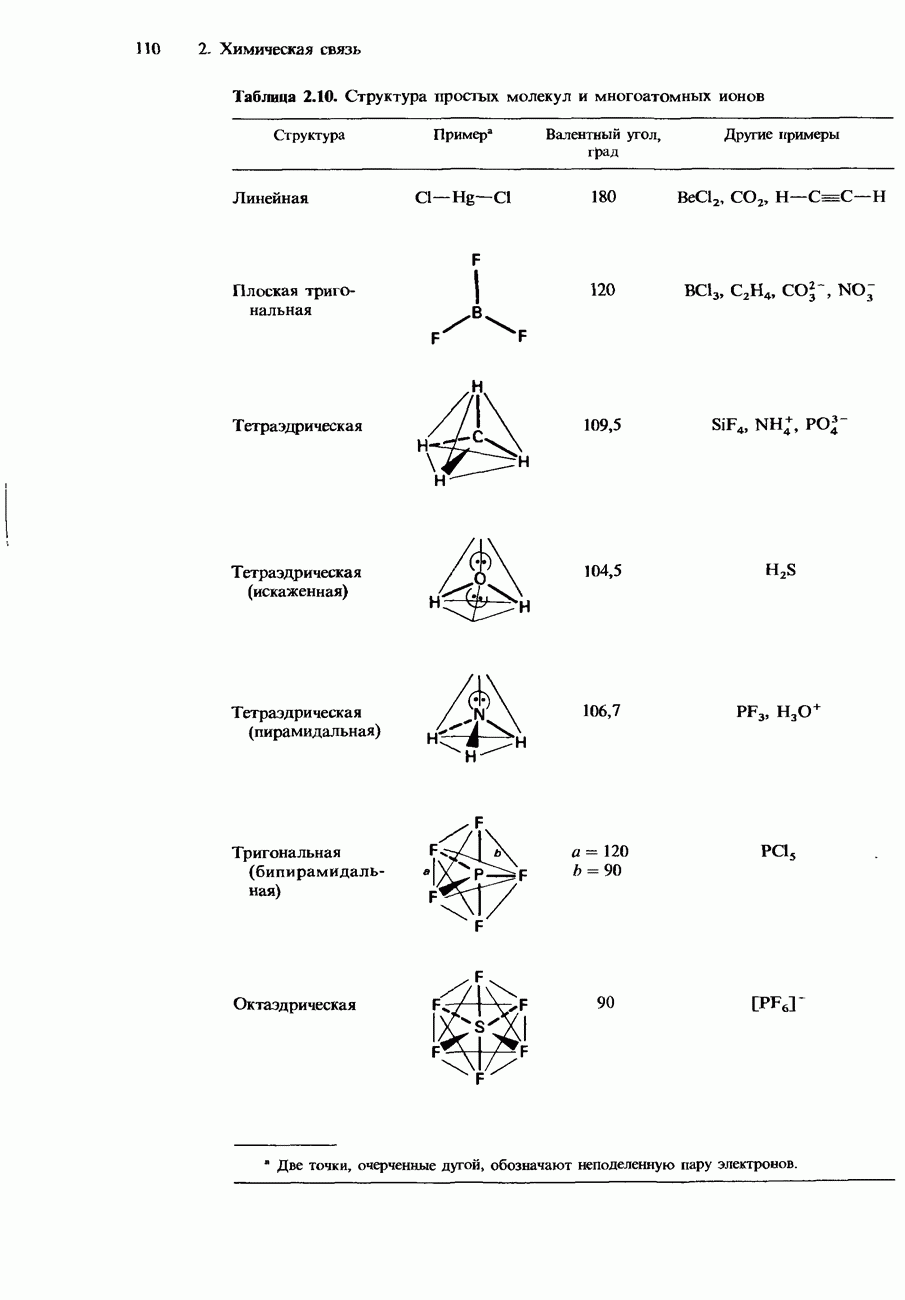
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
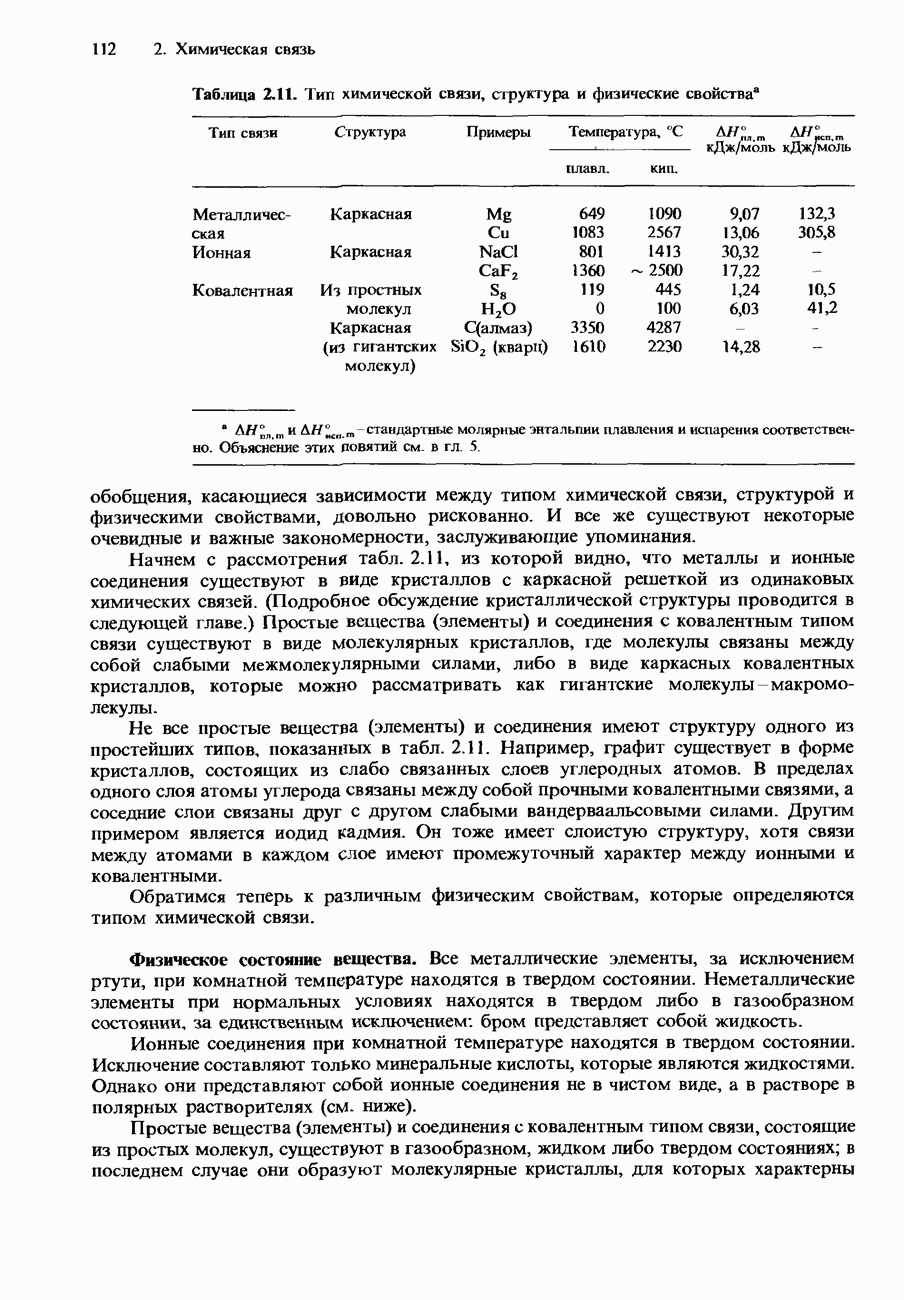
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
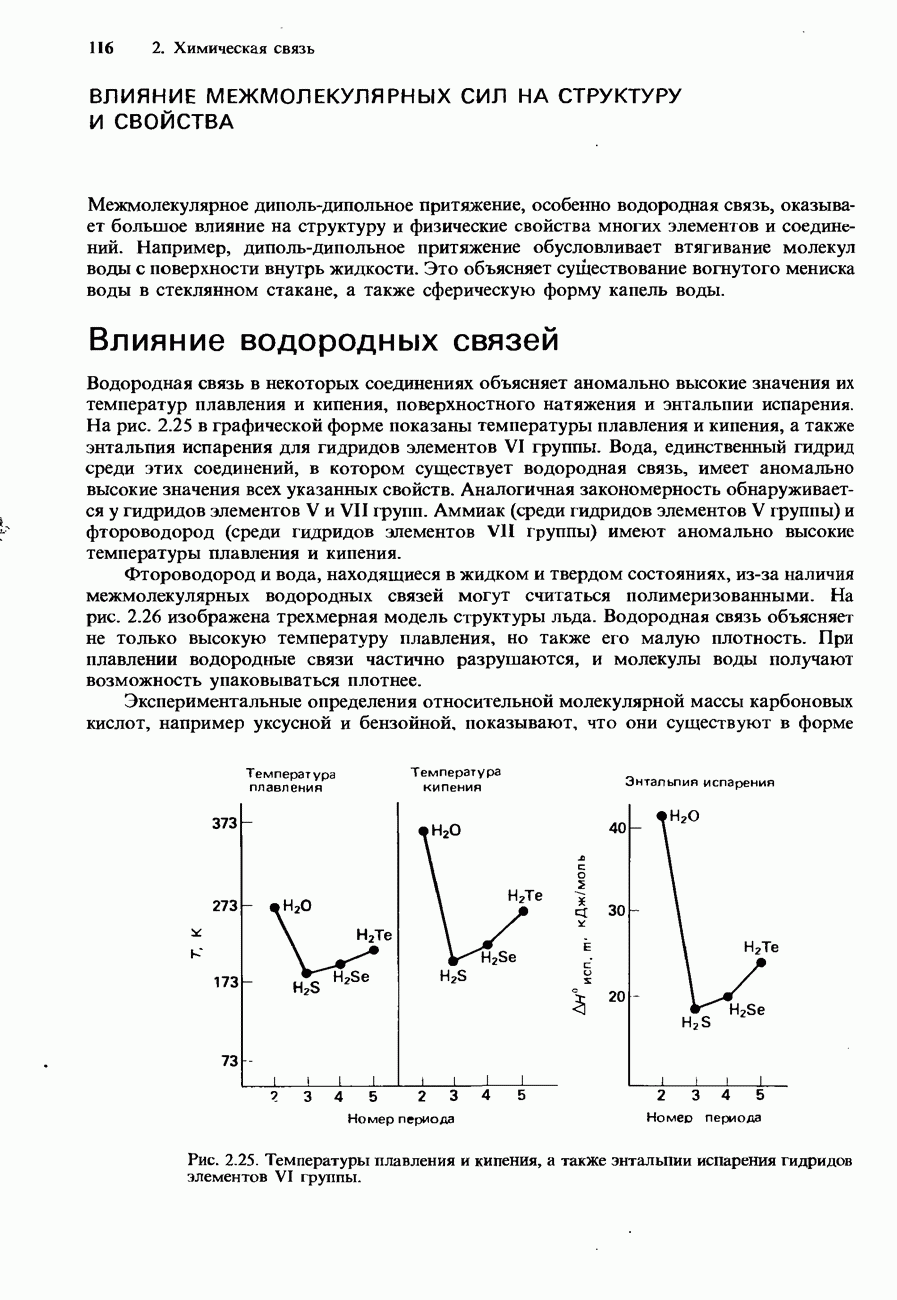
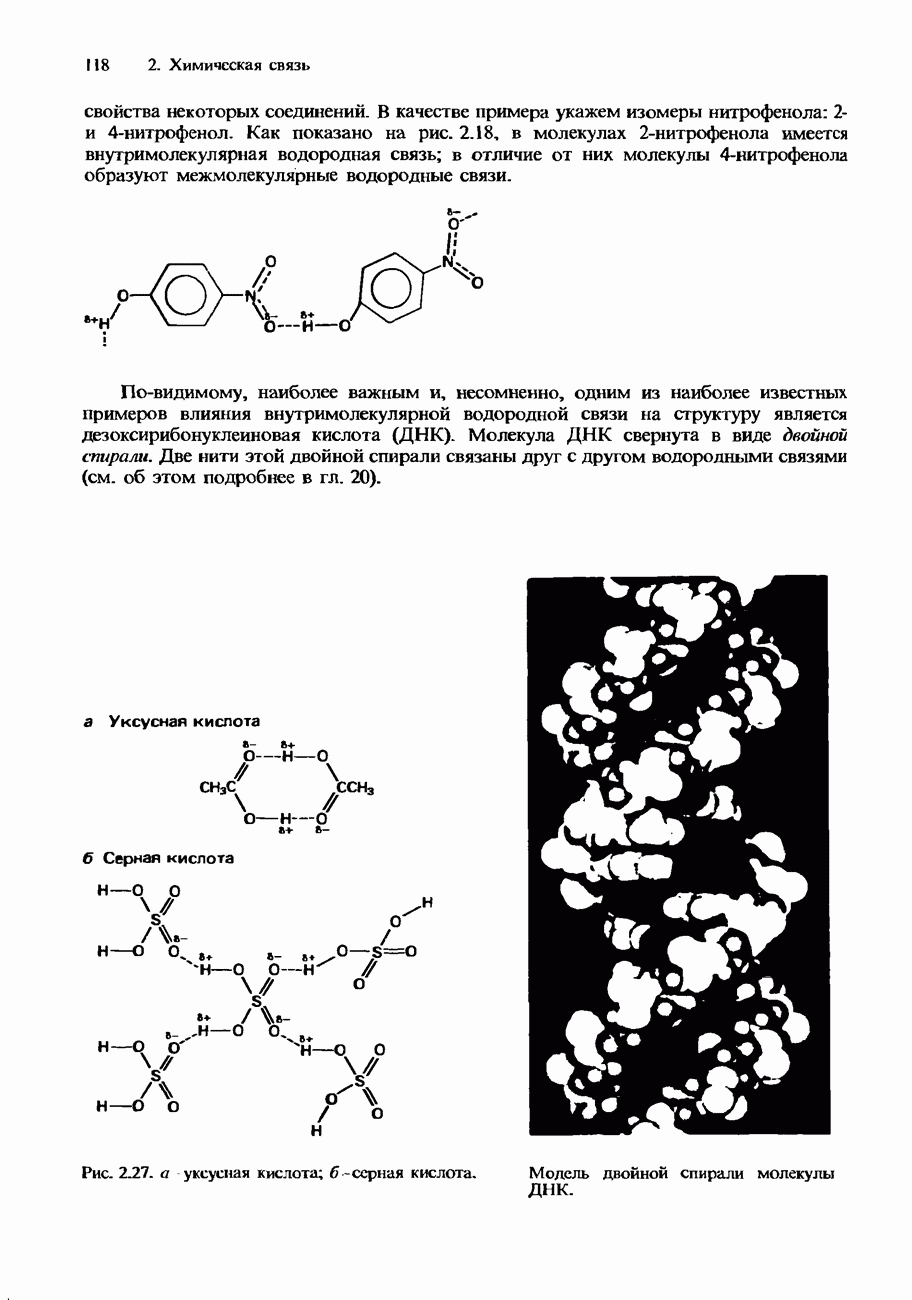
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
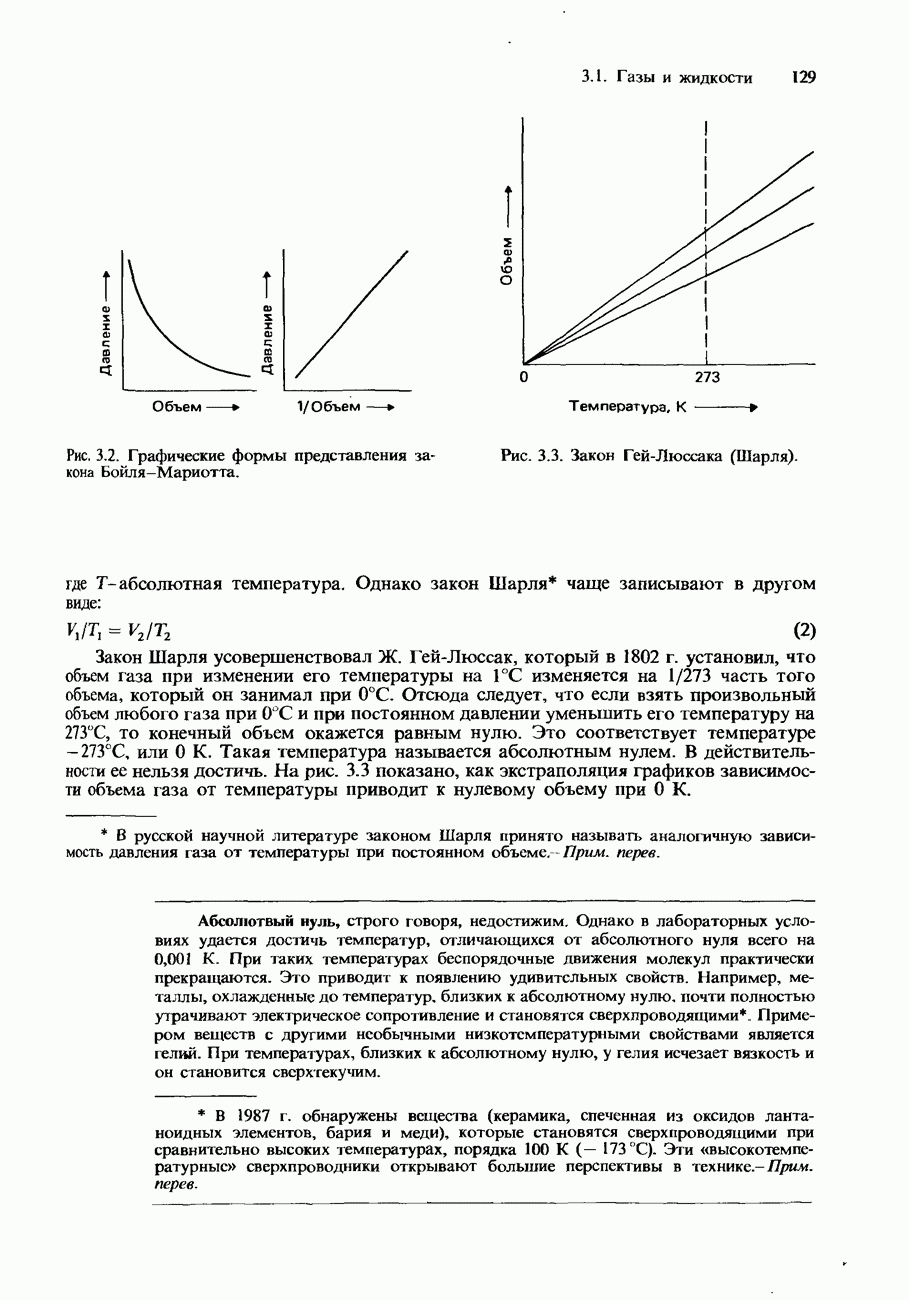
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
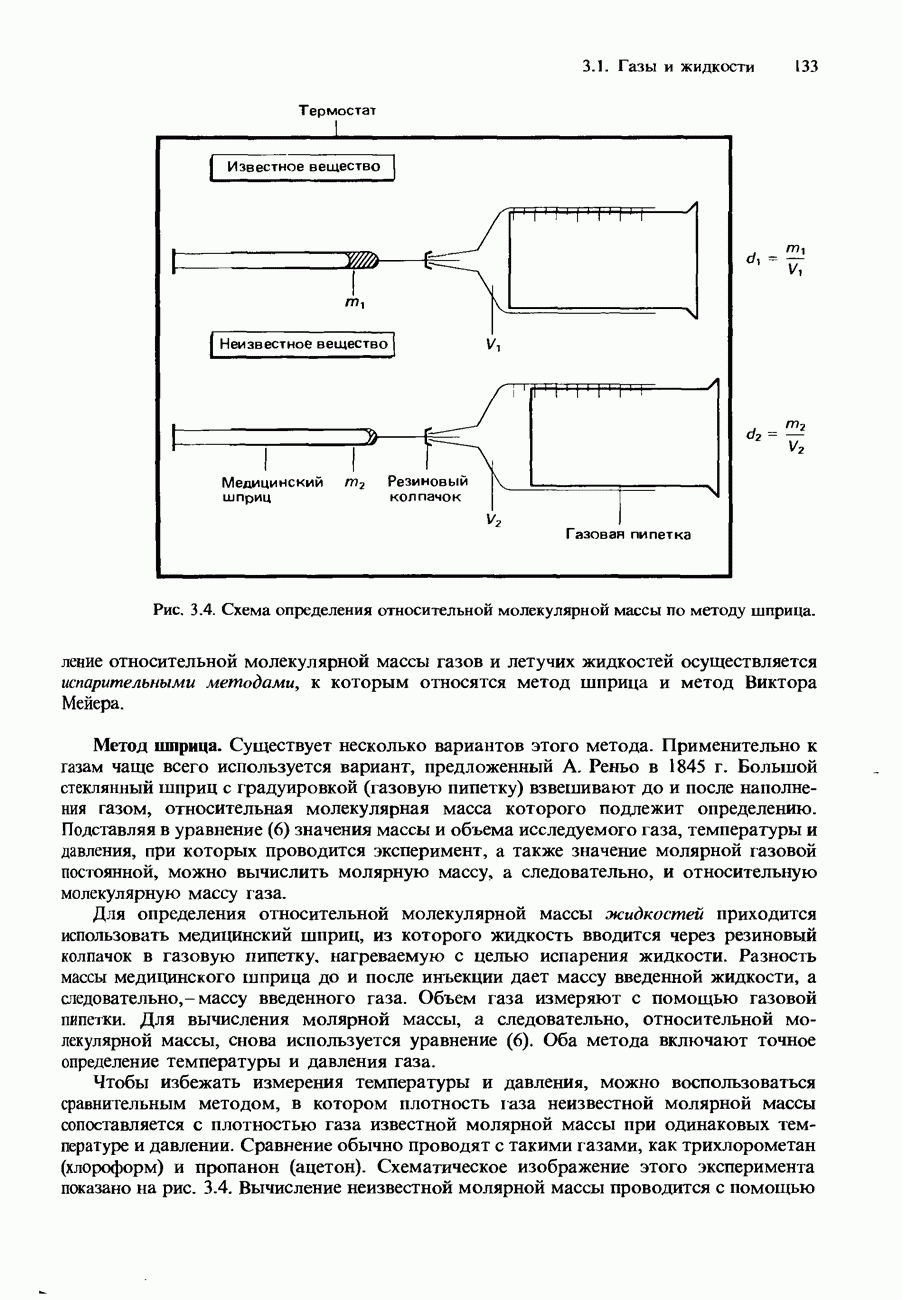
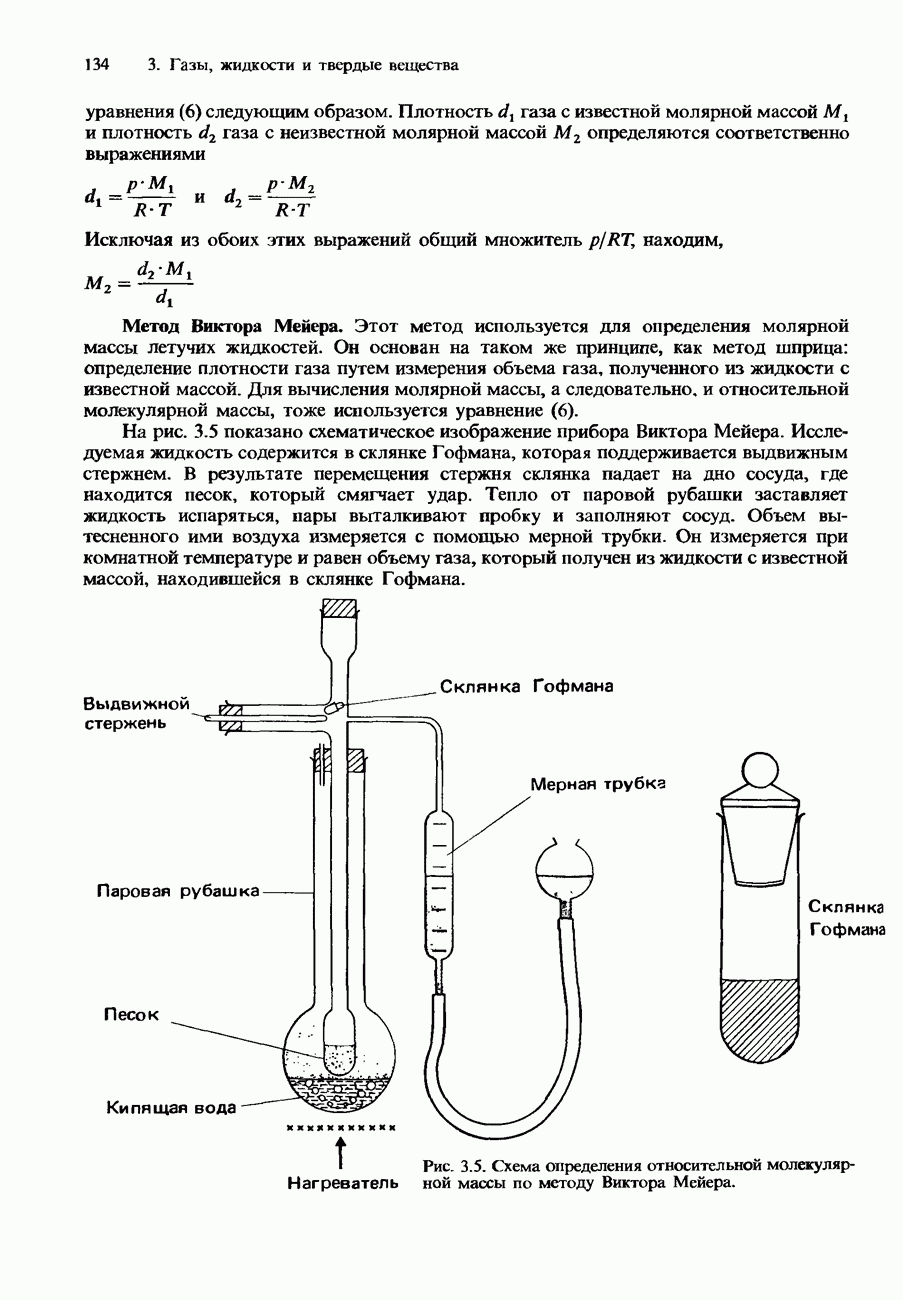
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
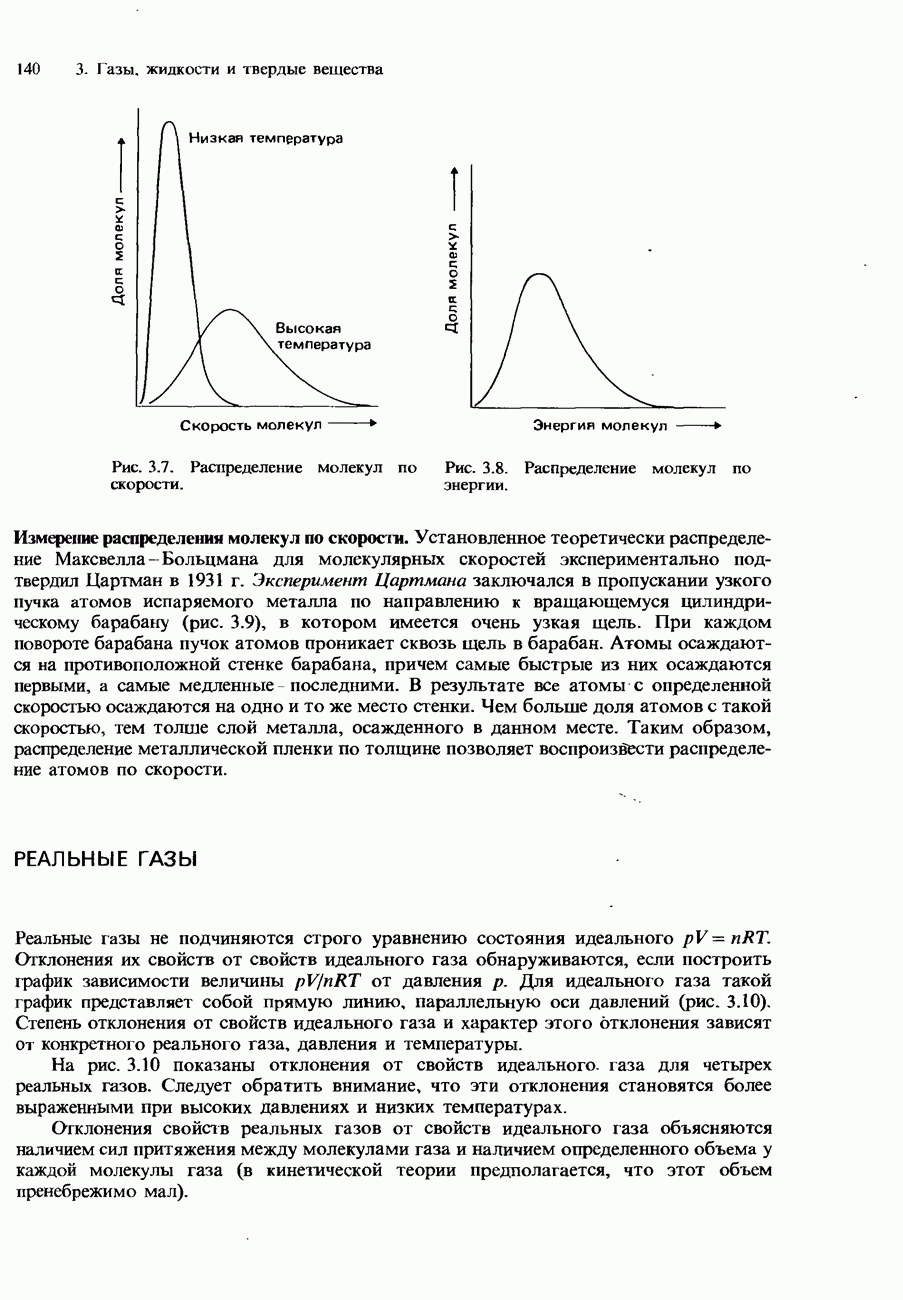
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
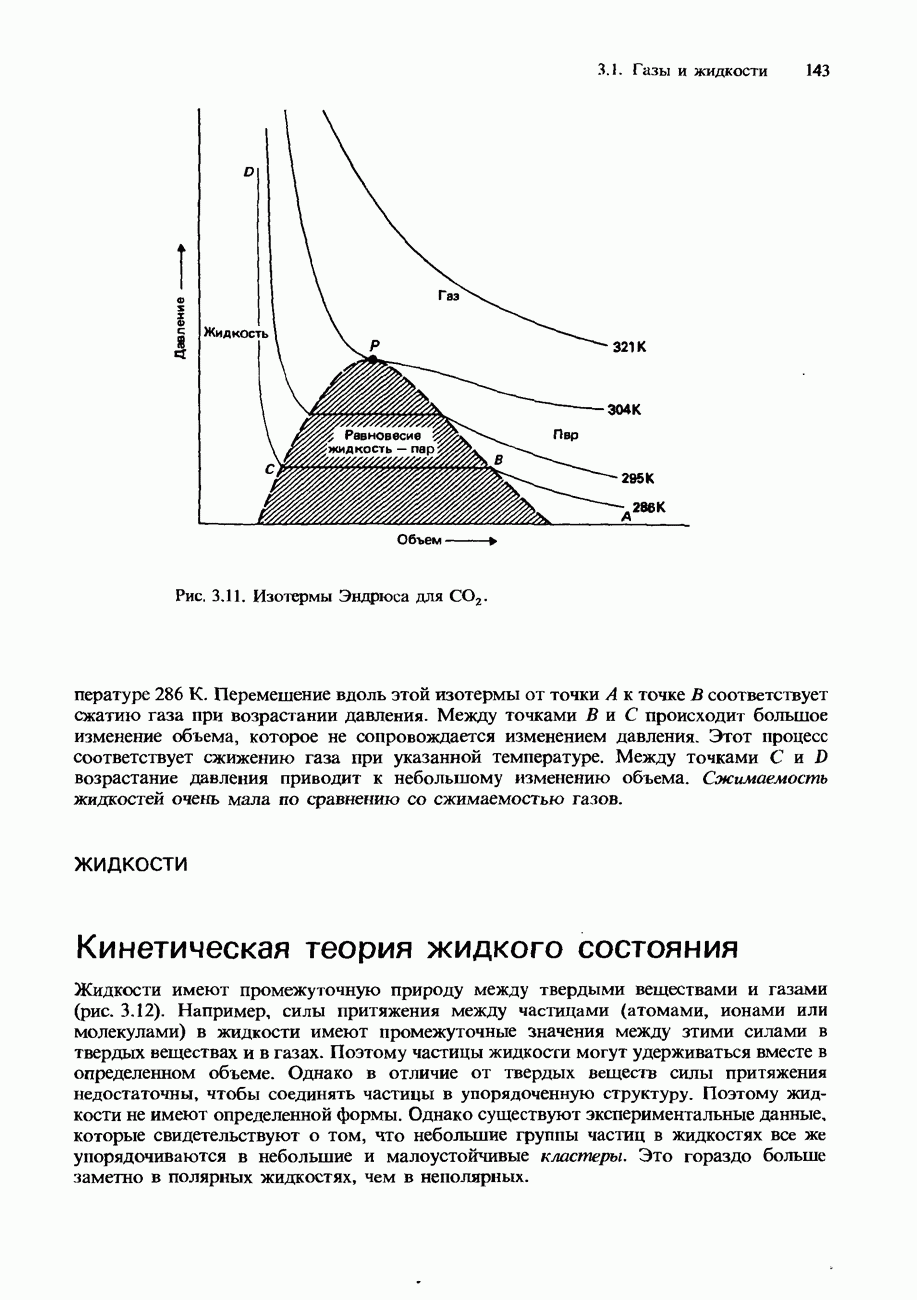
- Сжижение газов
- ЖИДКОСТИ
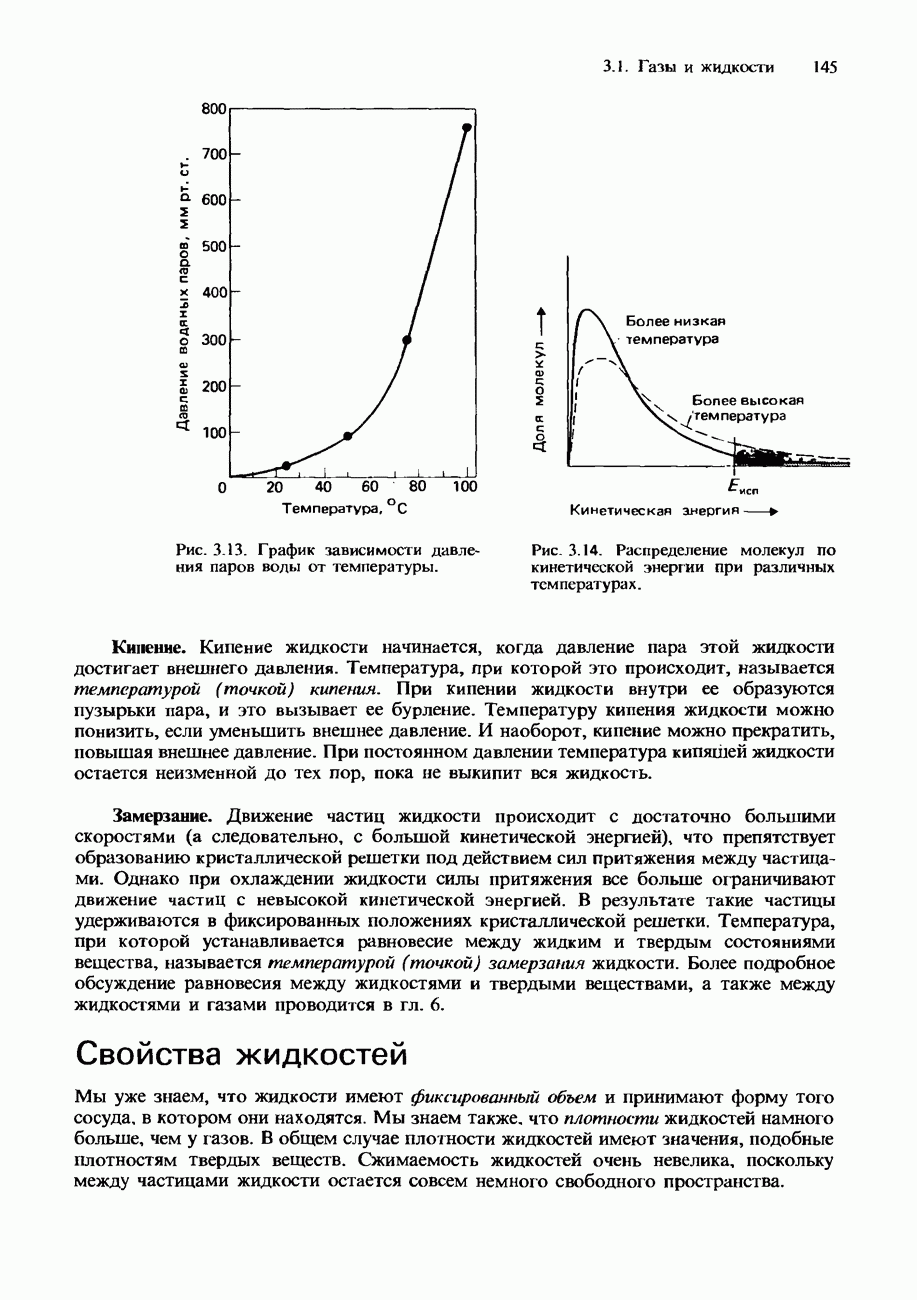
- Свойства жидкостей
- 3.2. Твердые вещества
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
- Ионные кристаллы
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
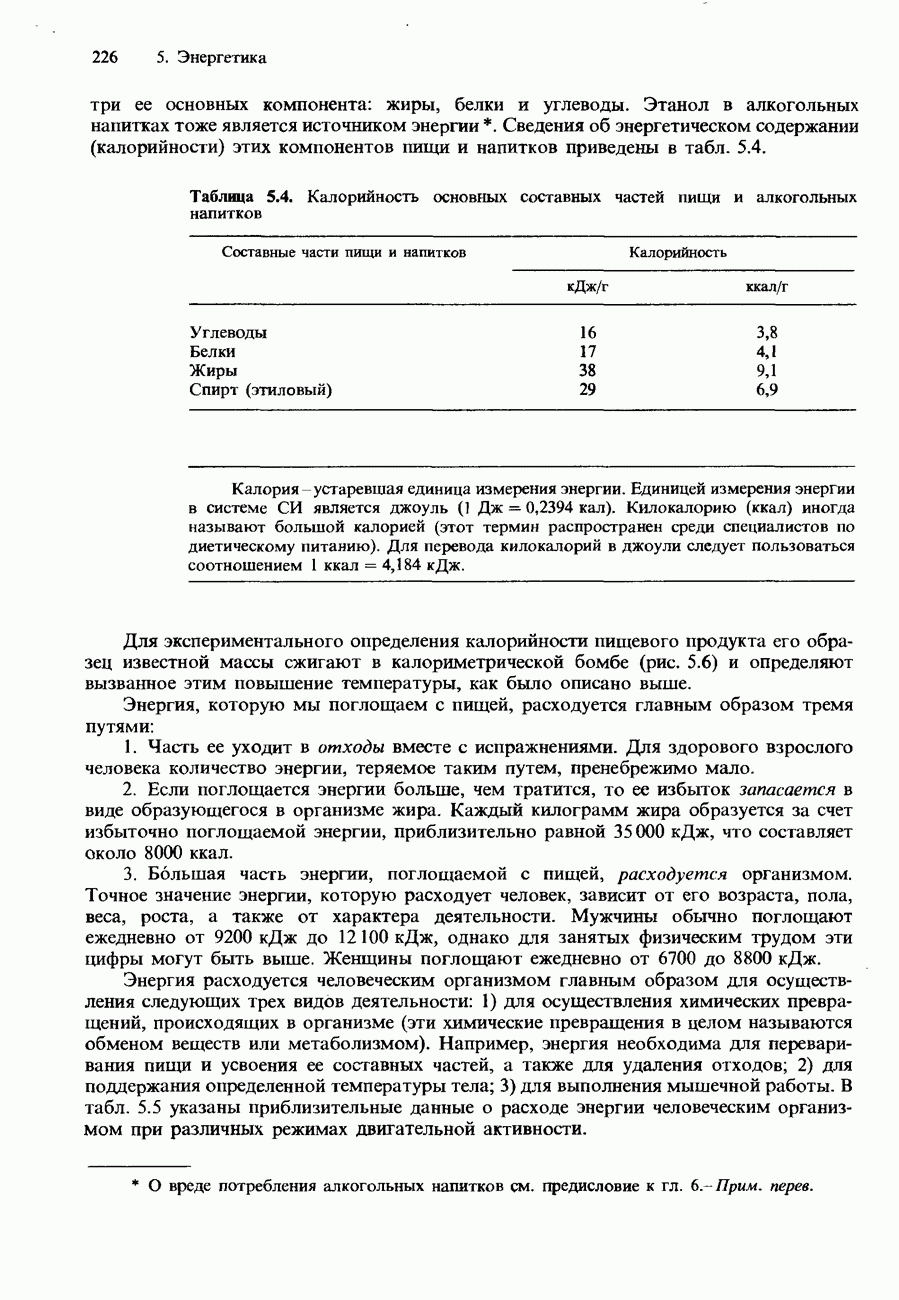
- КАЛОРИЙНОСТЬ ПИЩИ
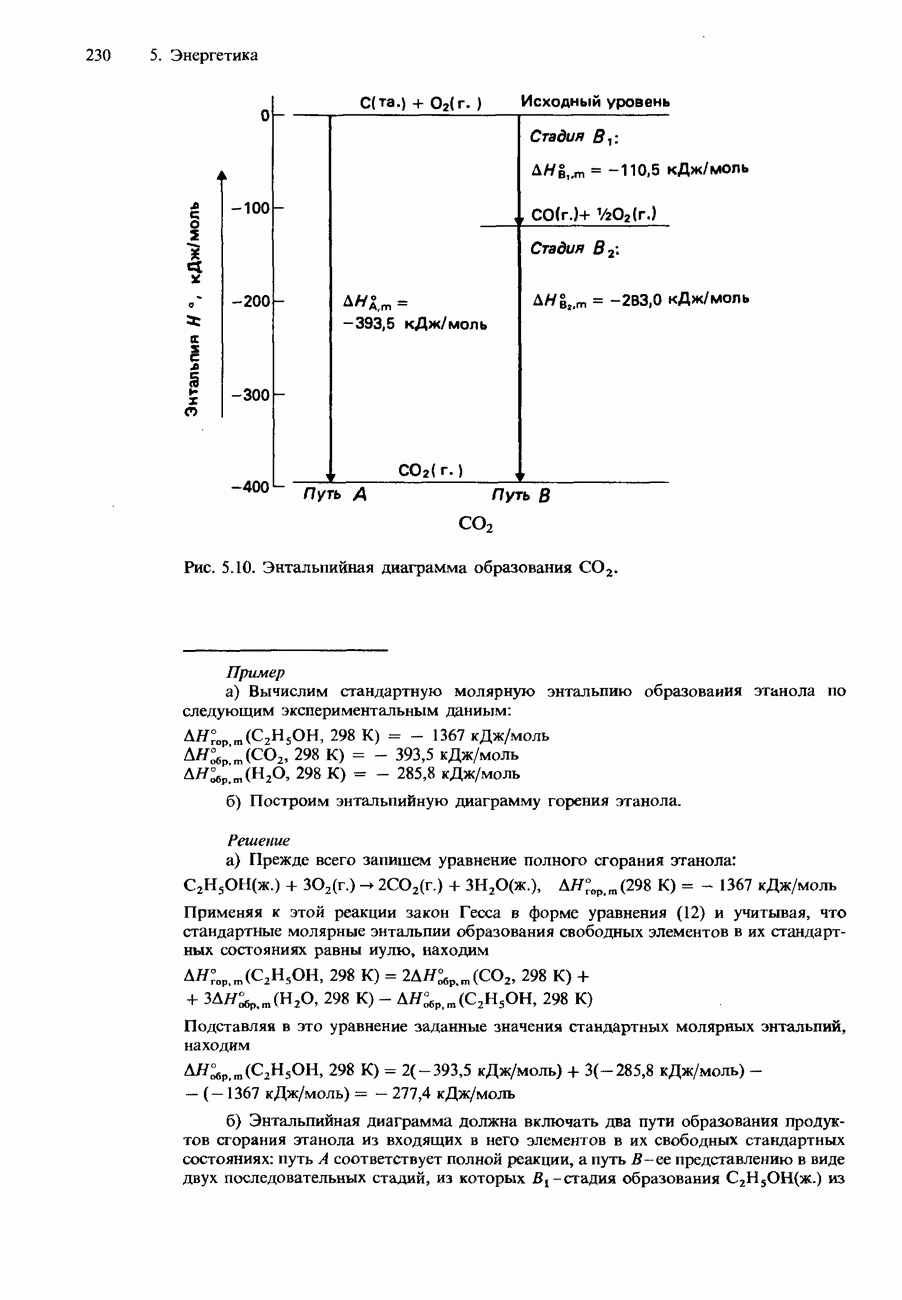
- ЗАКОН ГЕССА
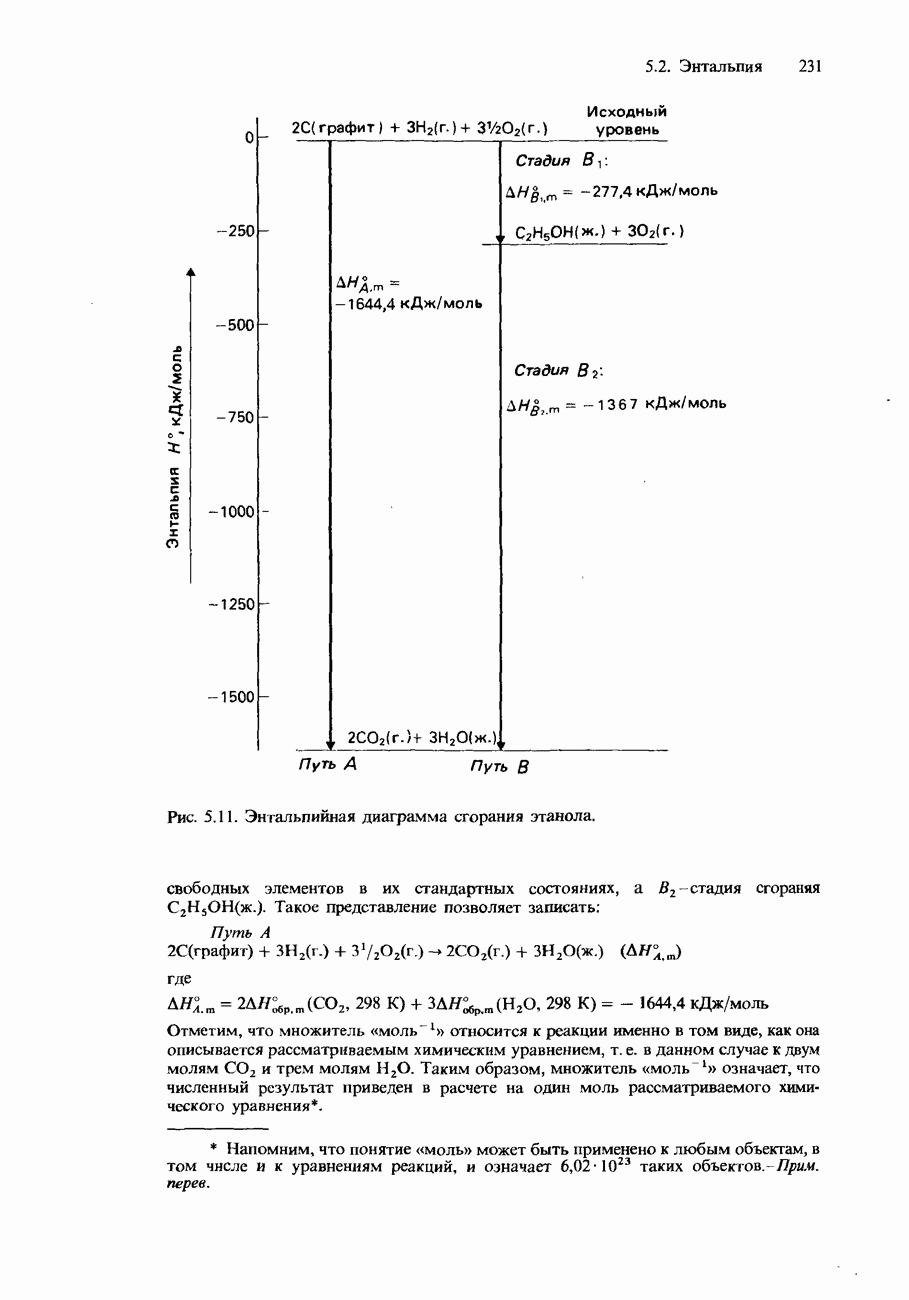
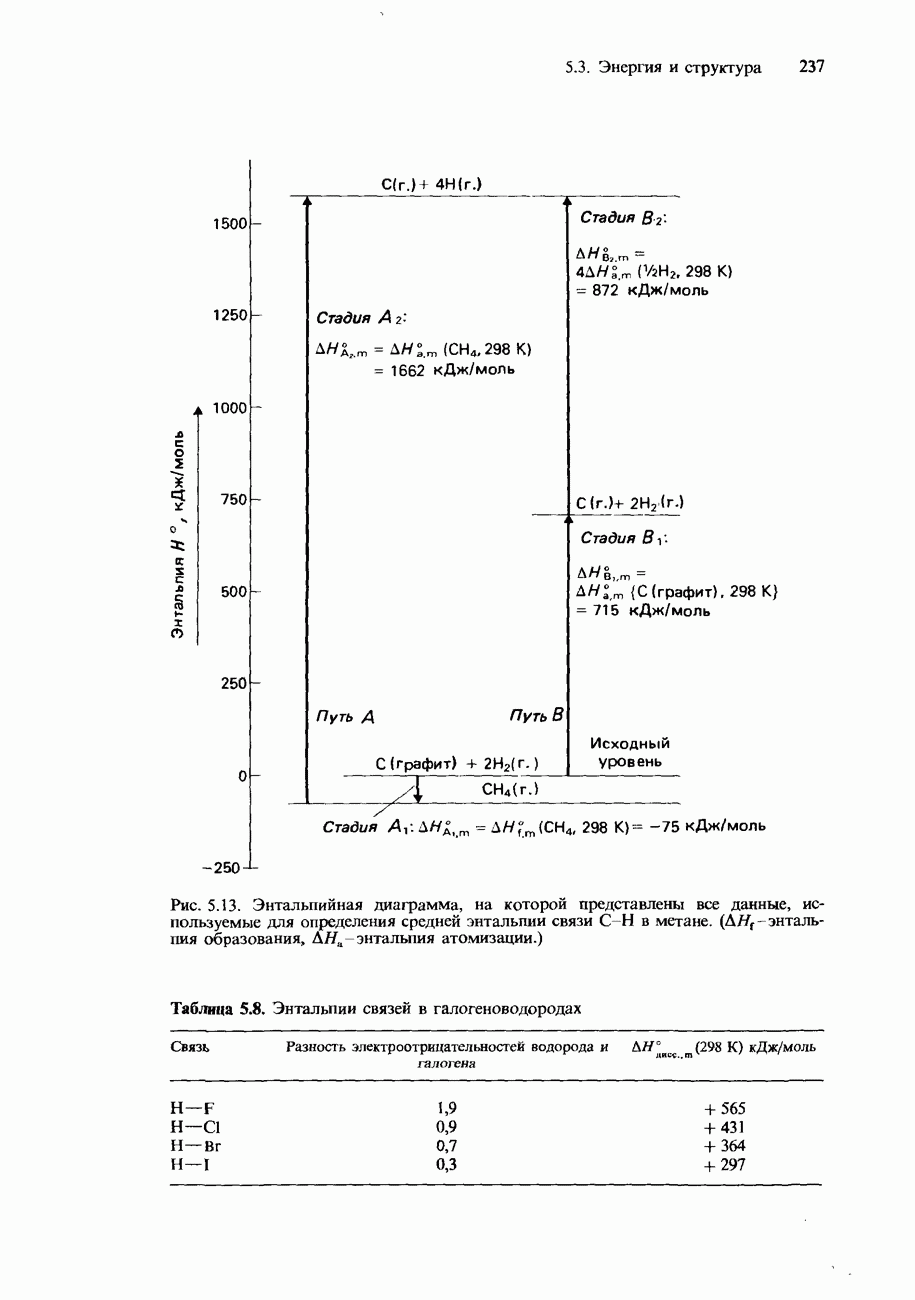
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
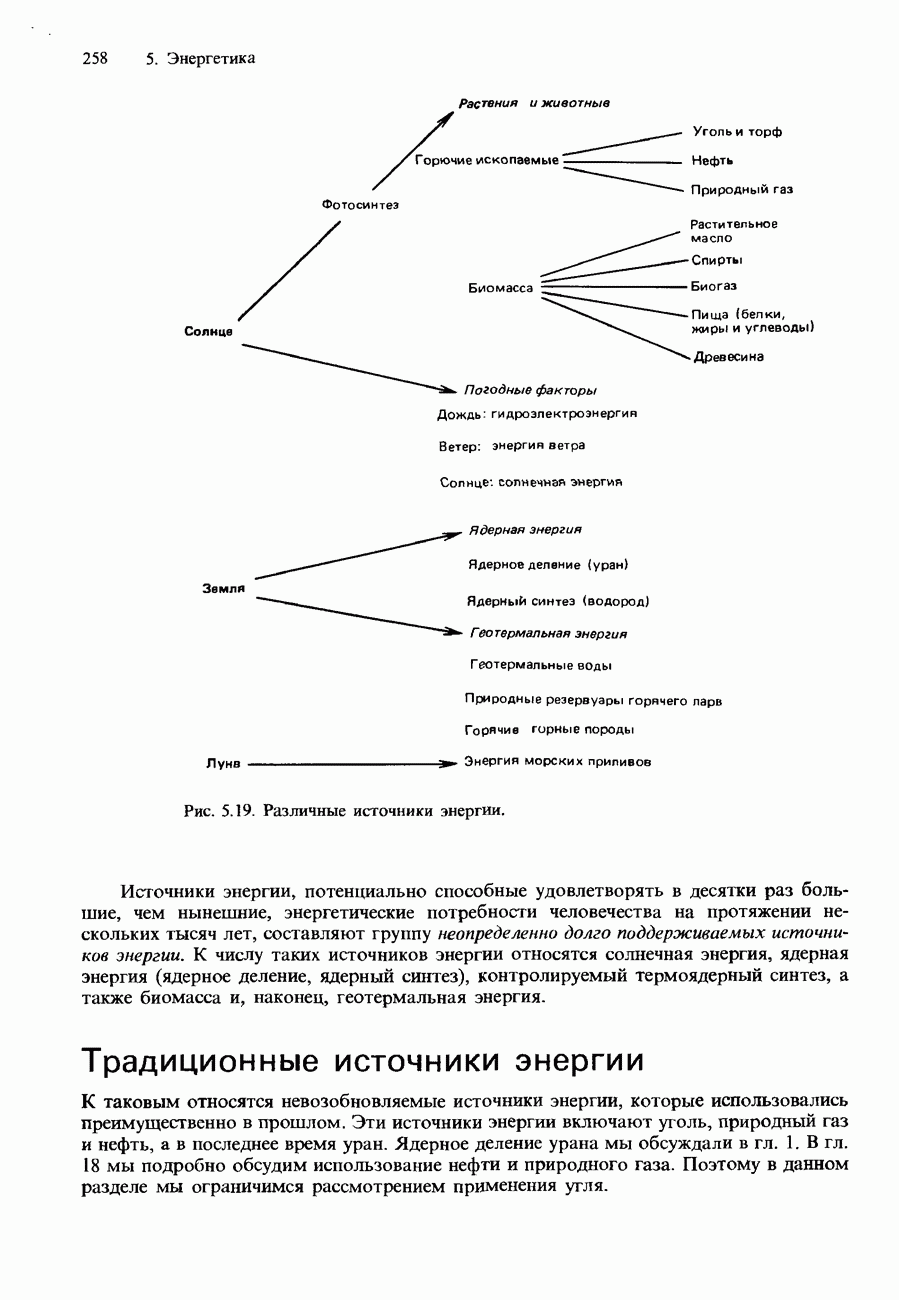
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
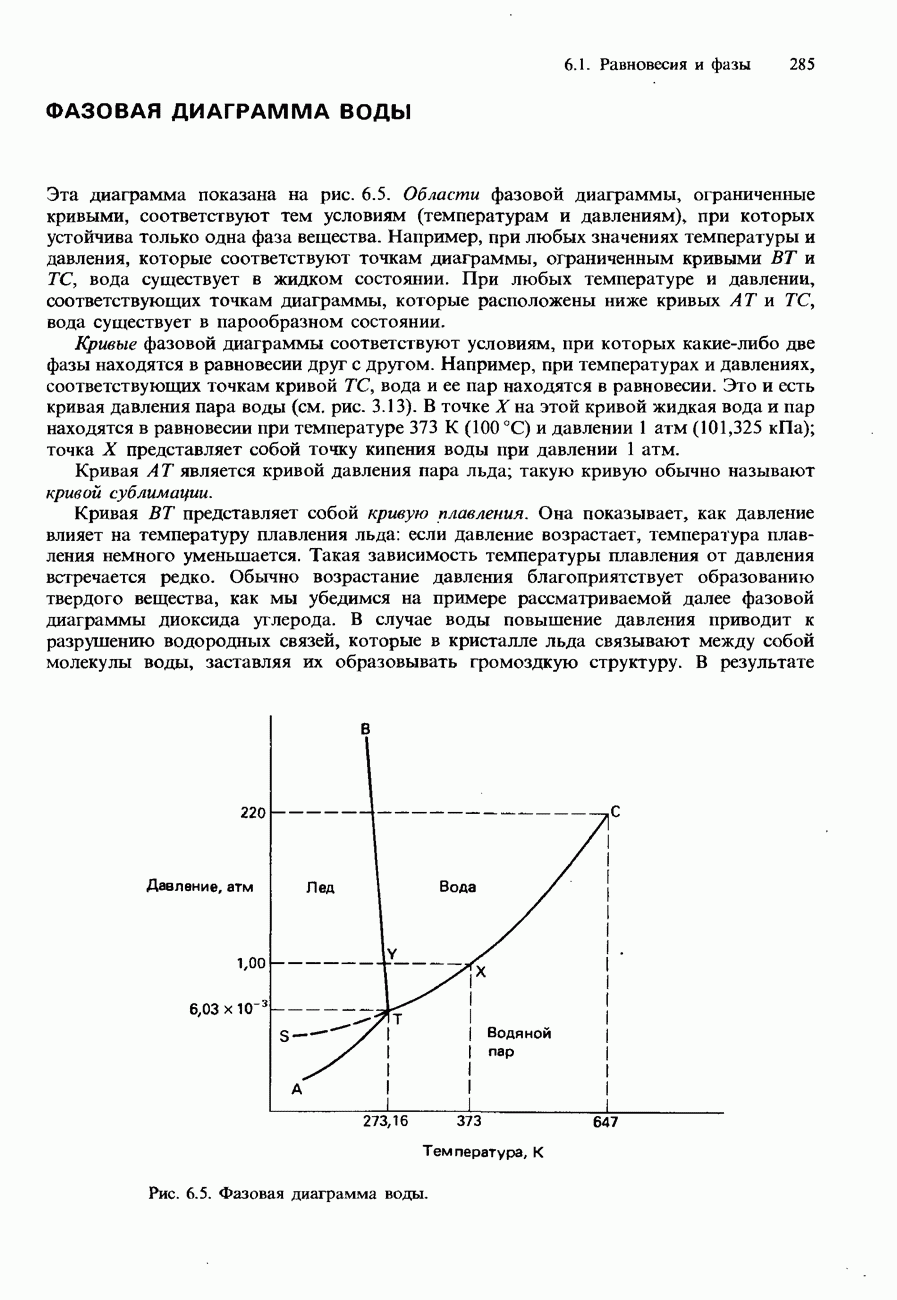
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
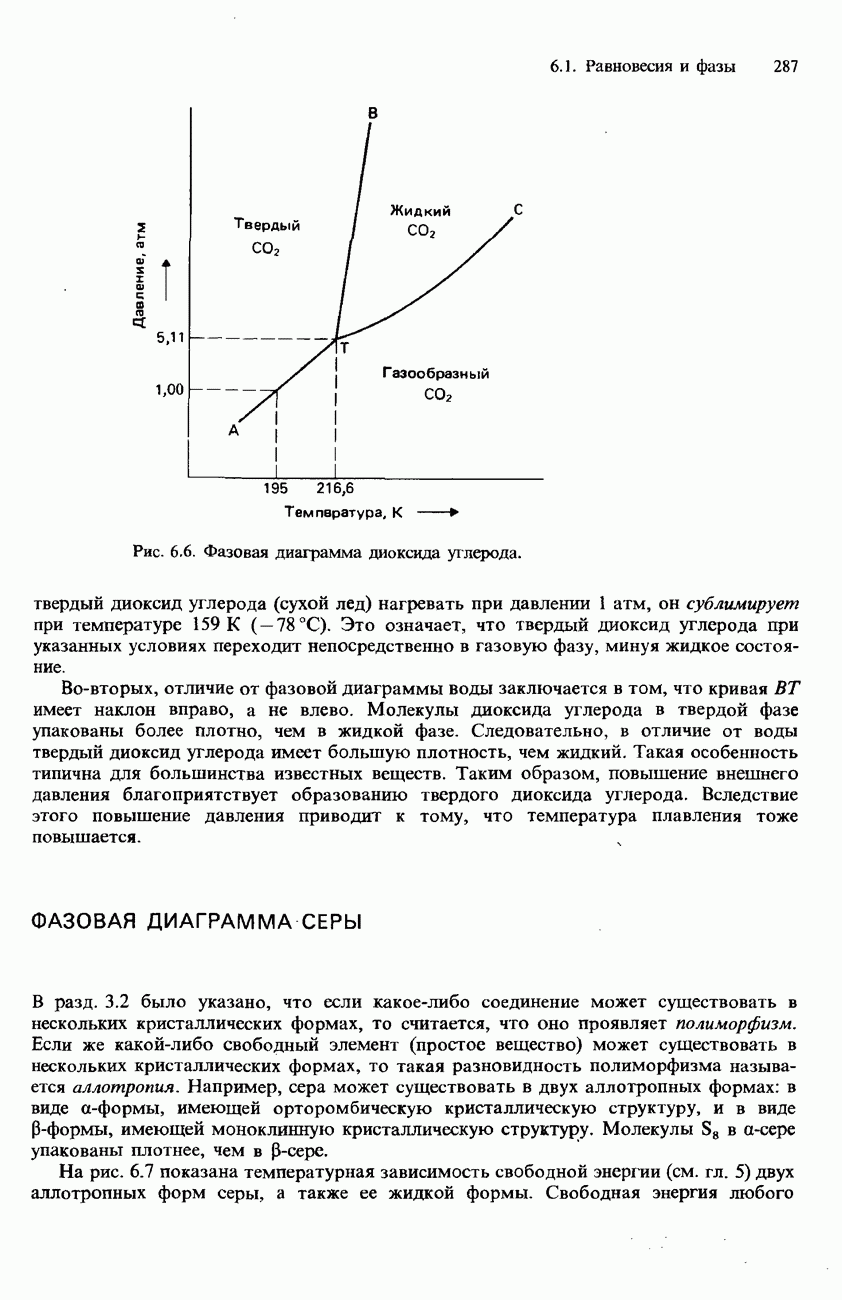
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
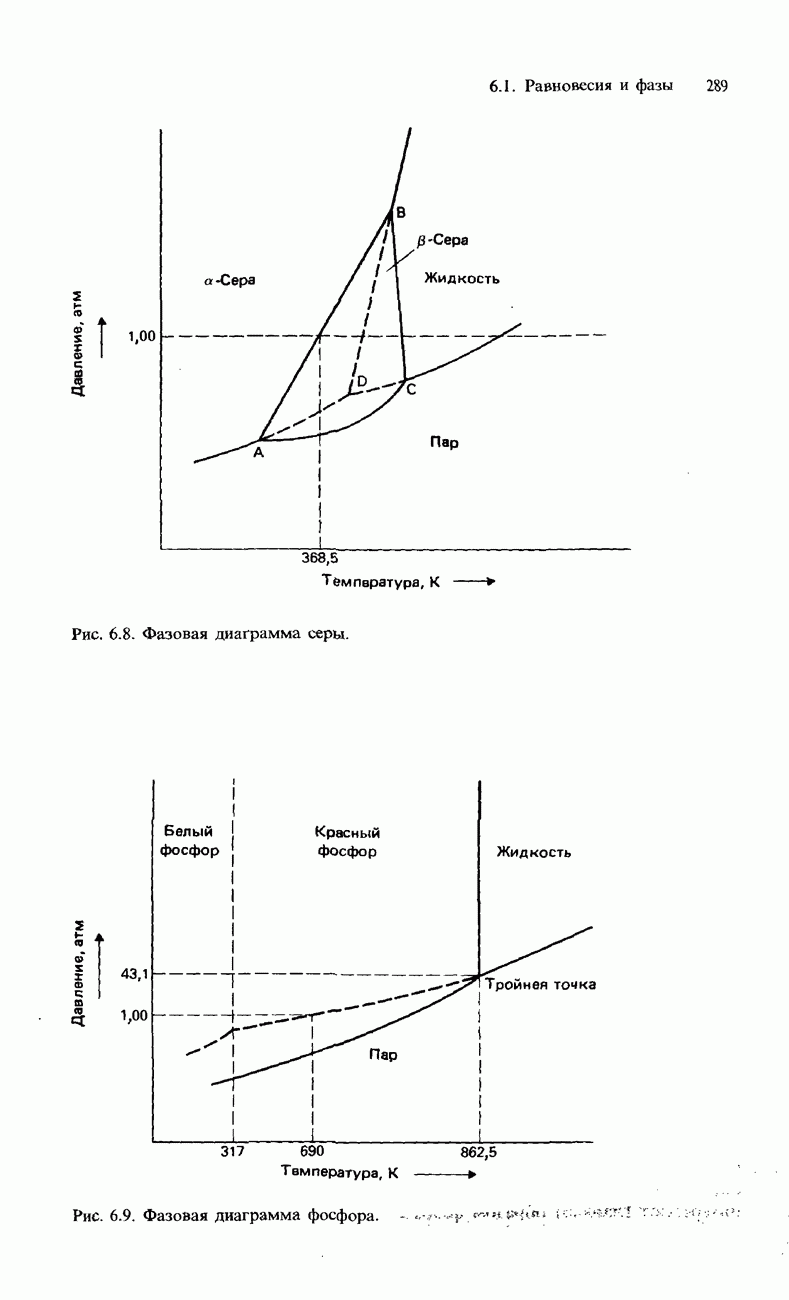
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
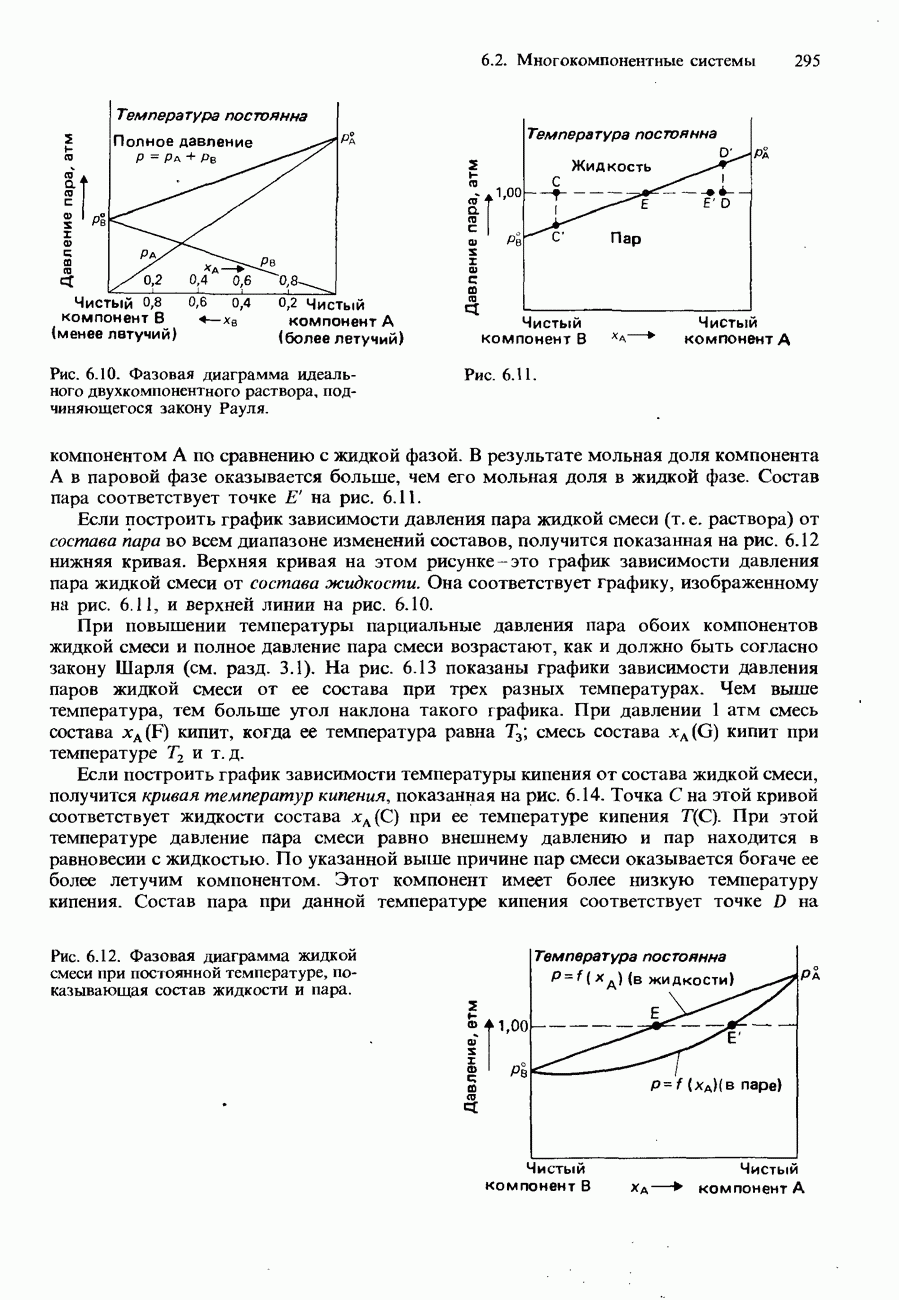
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- Фазовые диаграммы полностью смешивающихся жидкостей
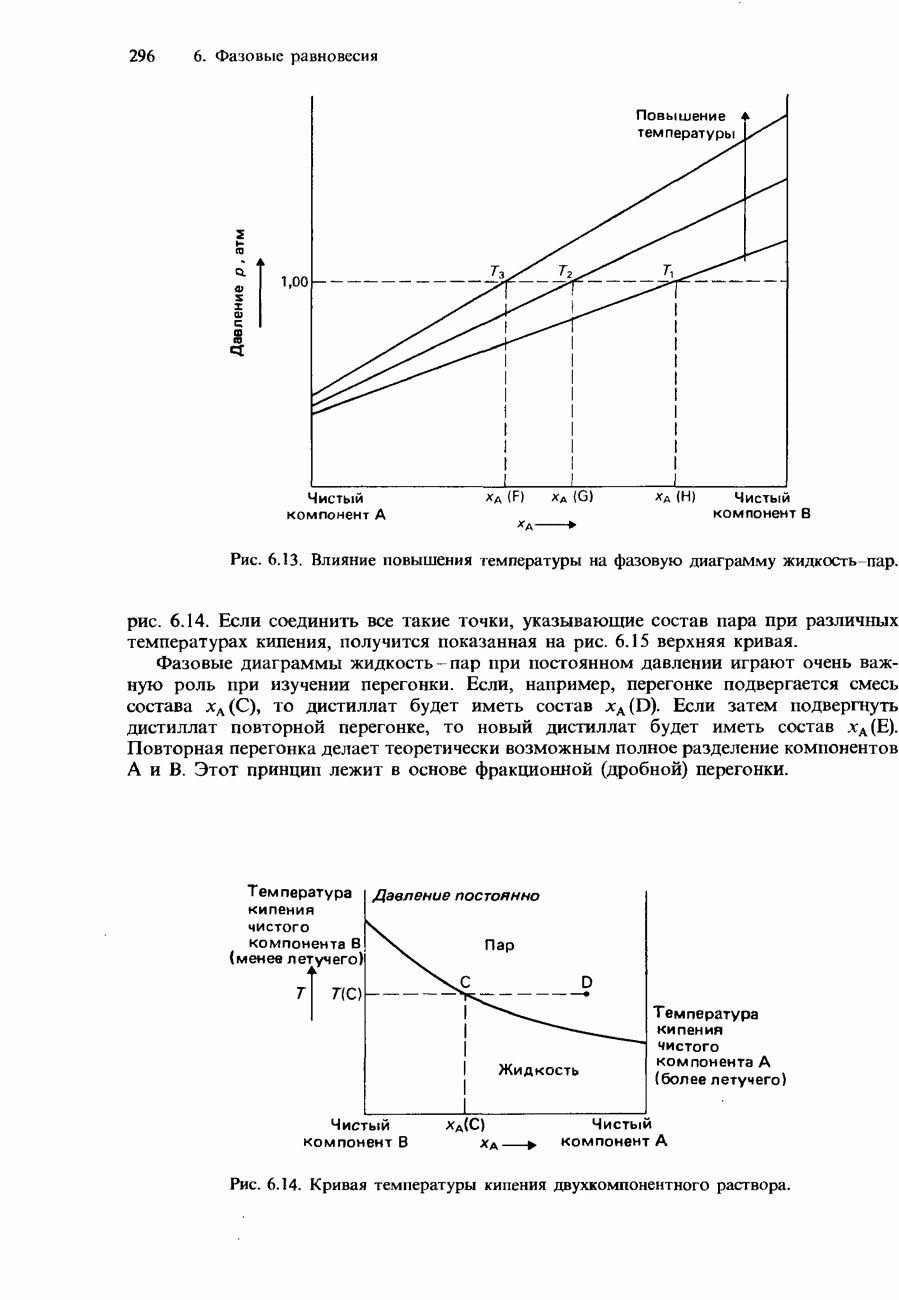
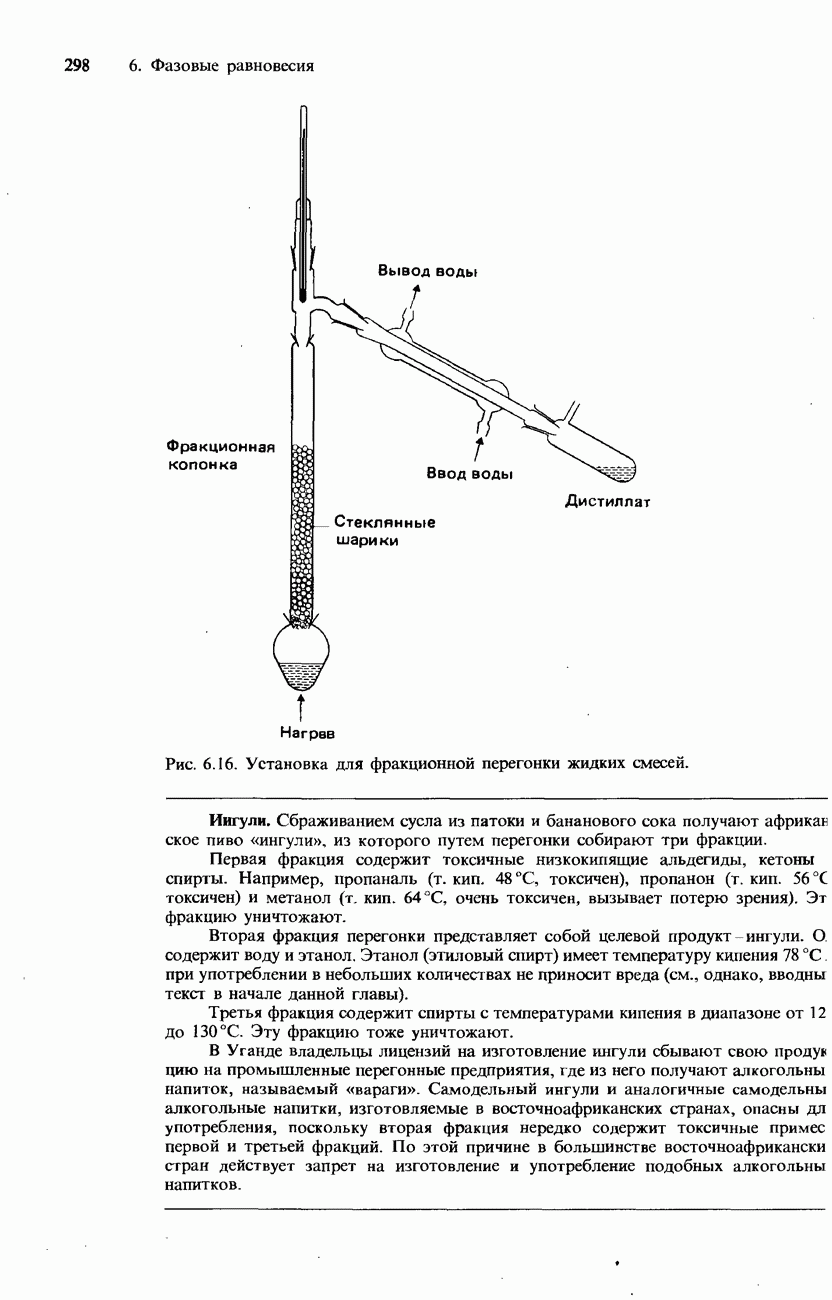
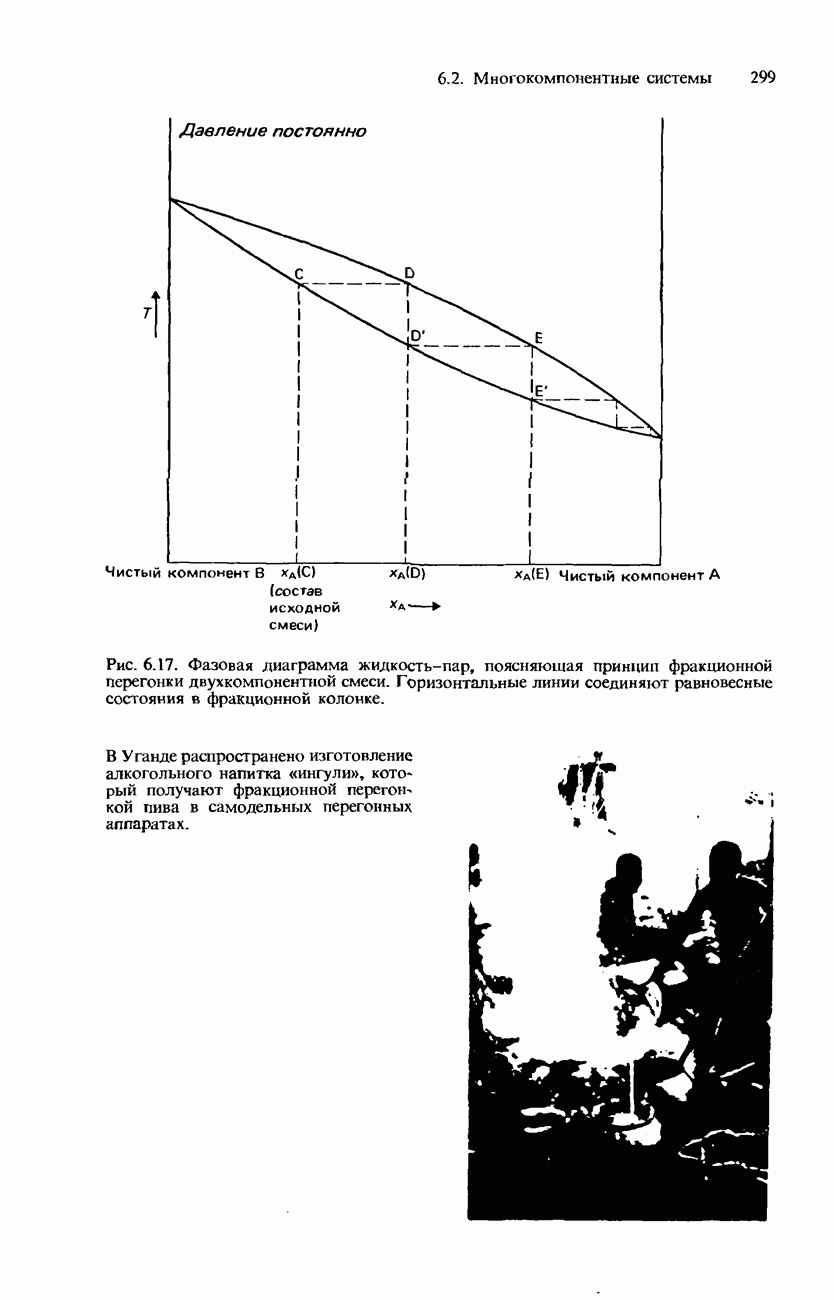
- Фракционная перегонка
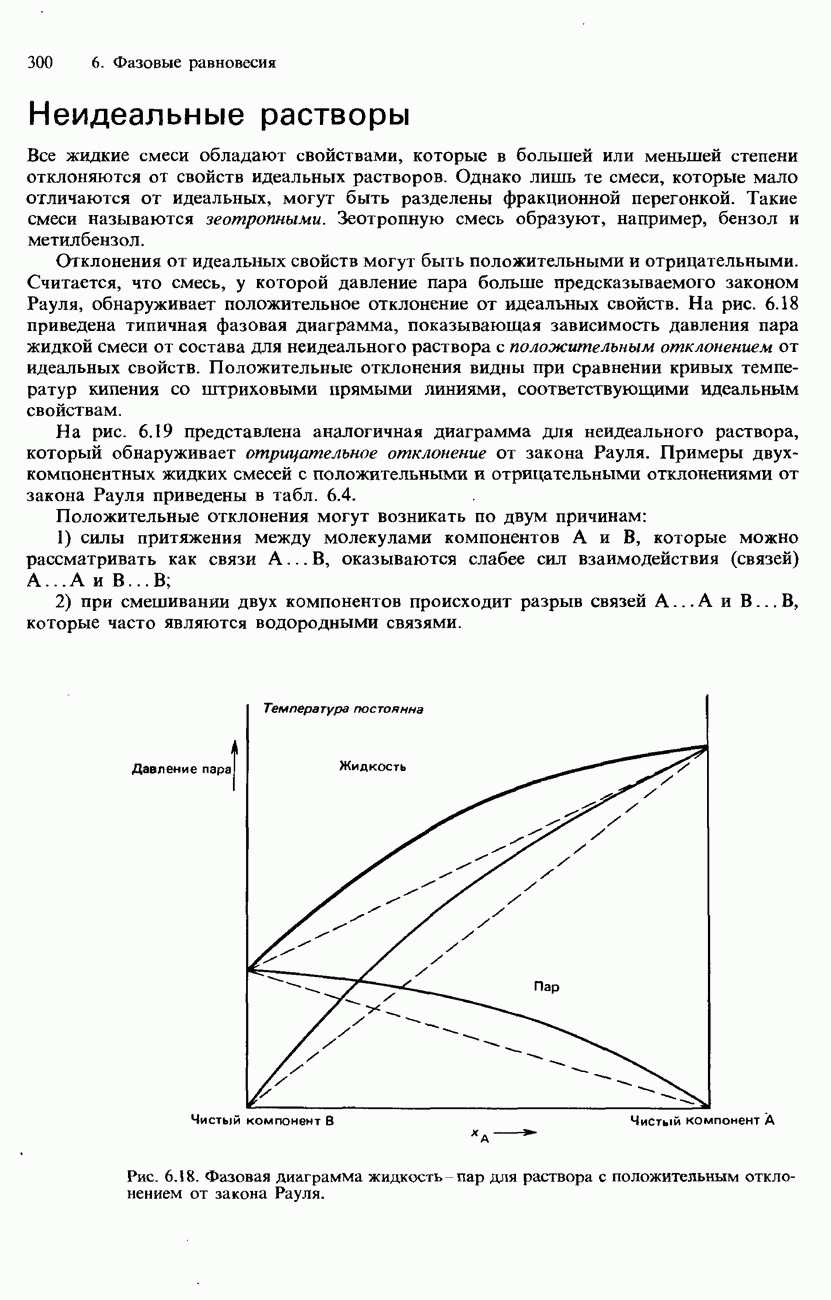
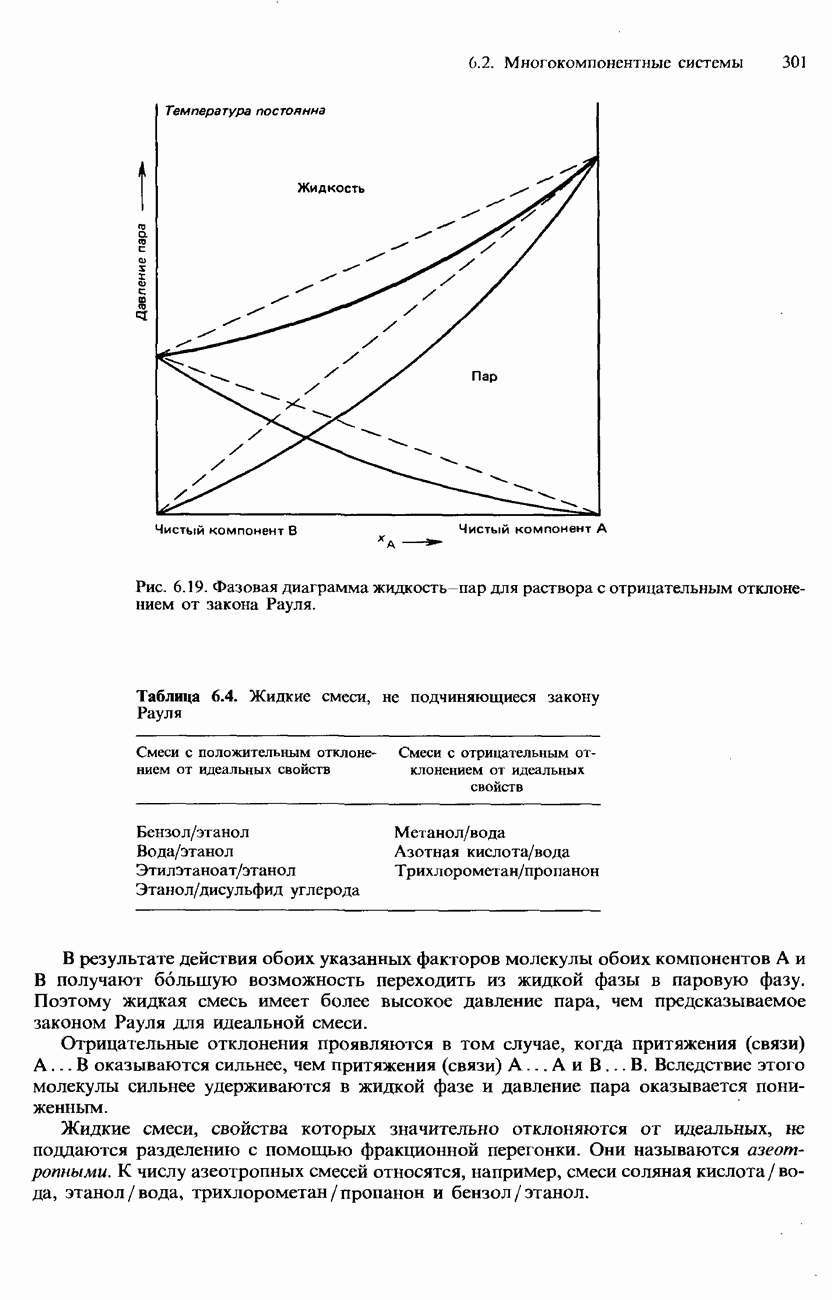
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
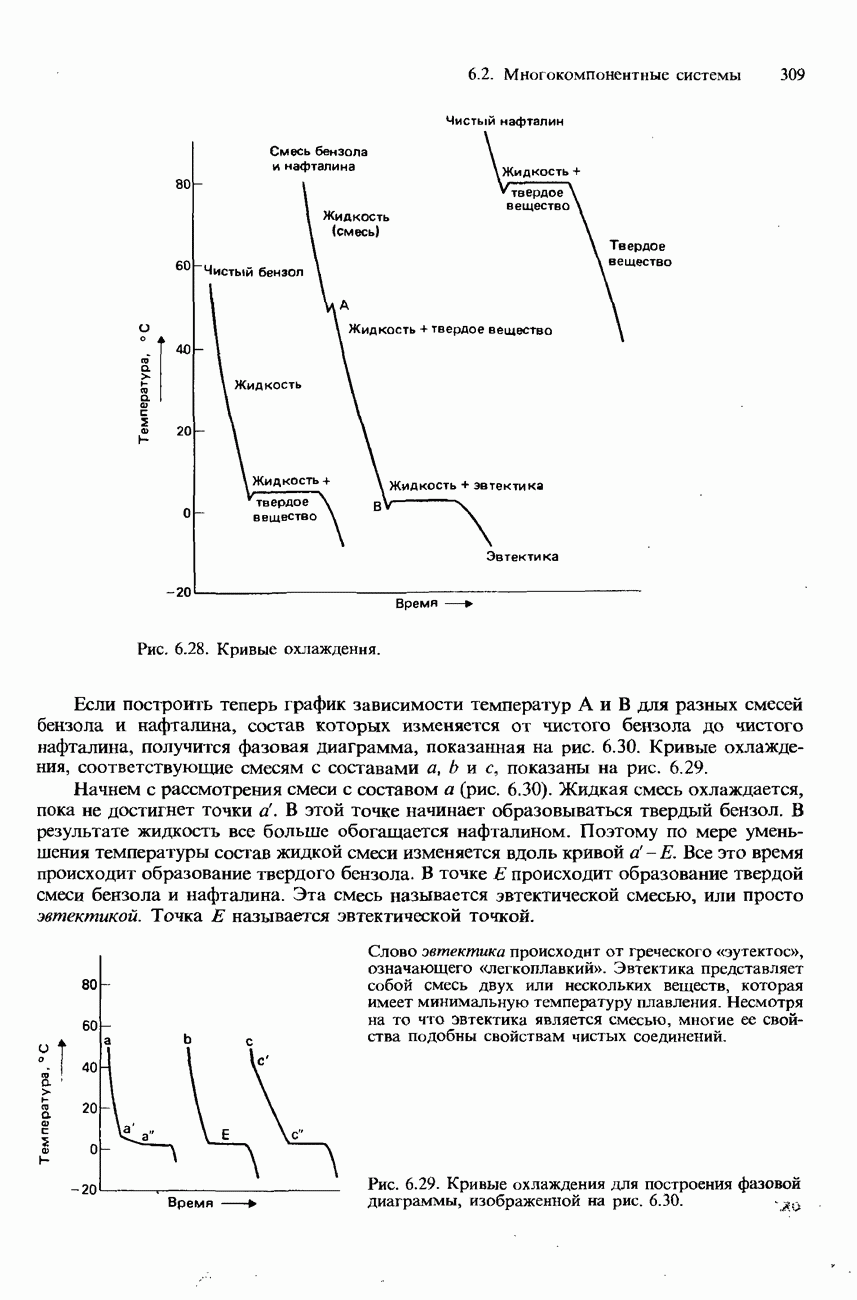
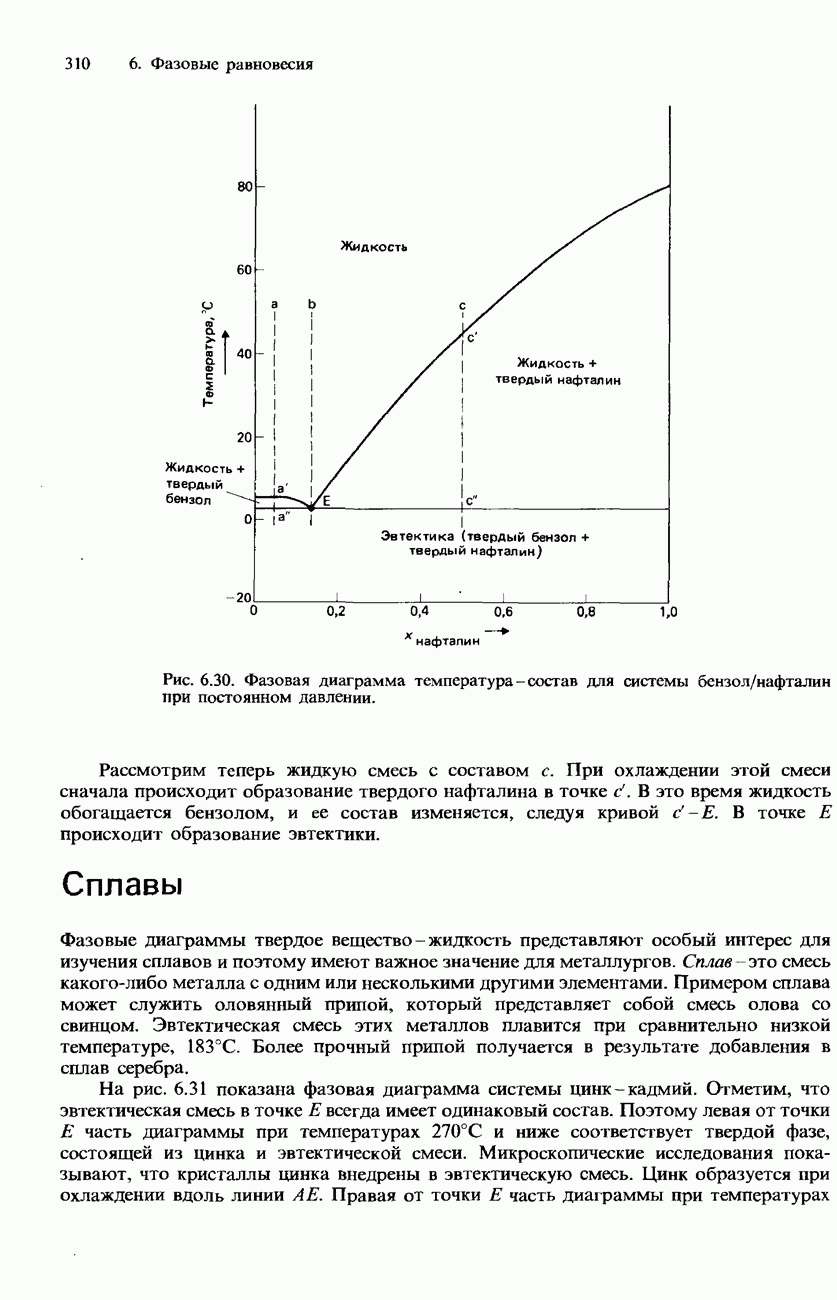
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
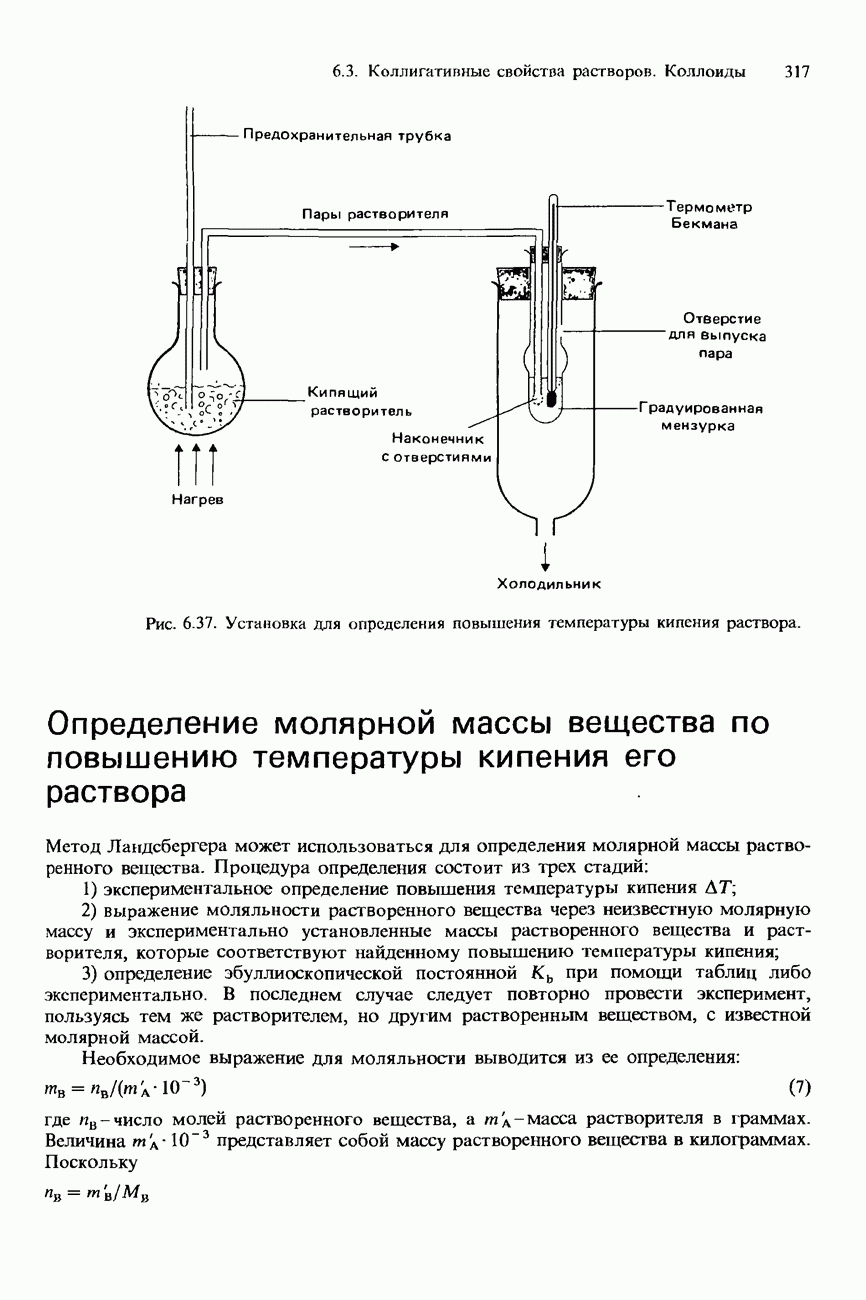
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
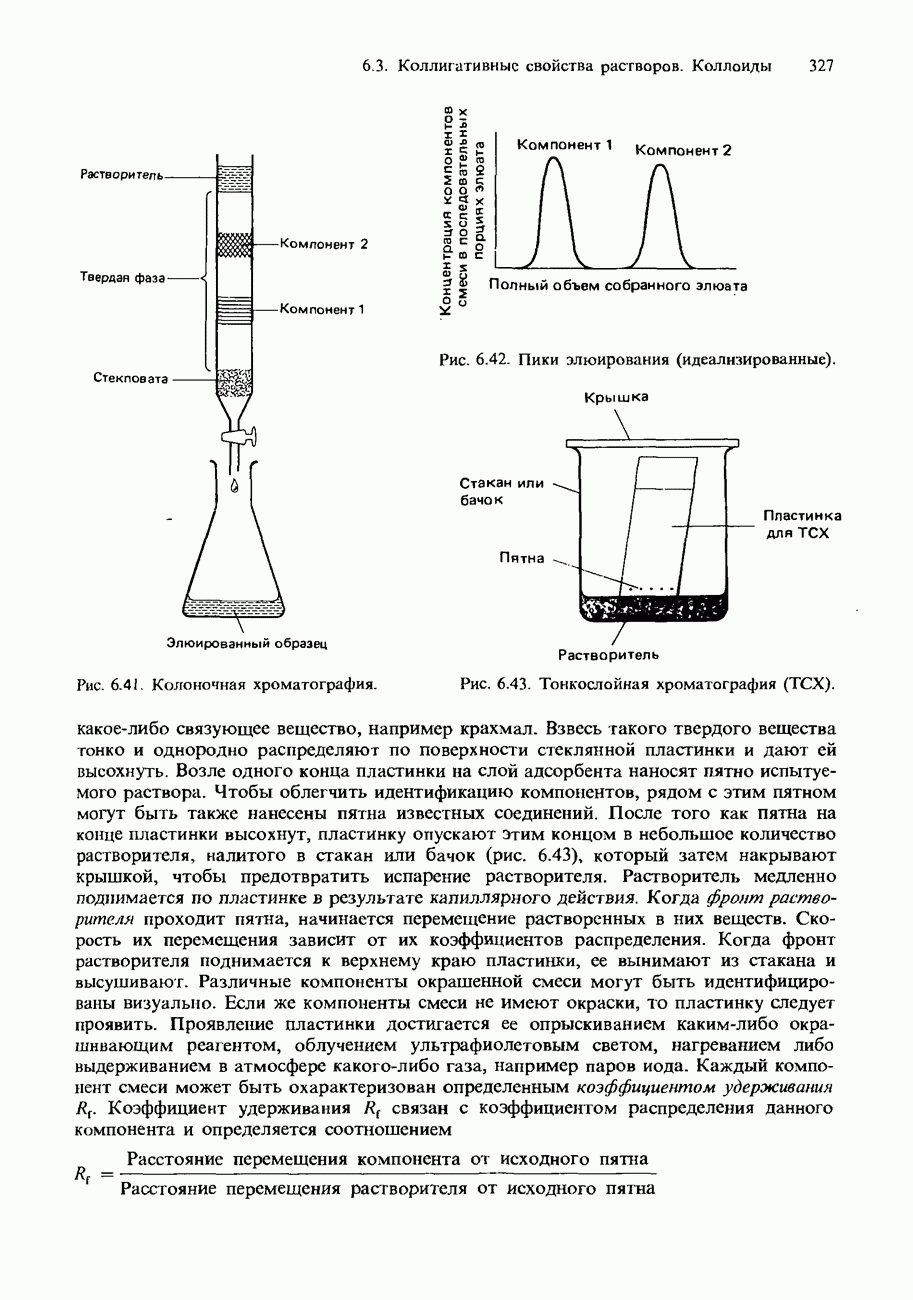
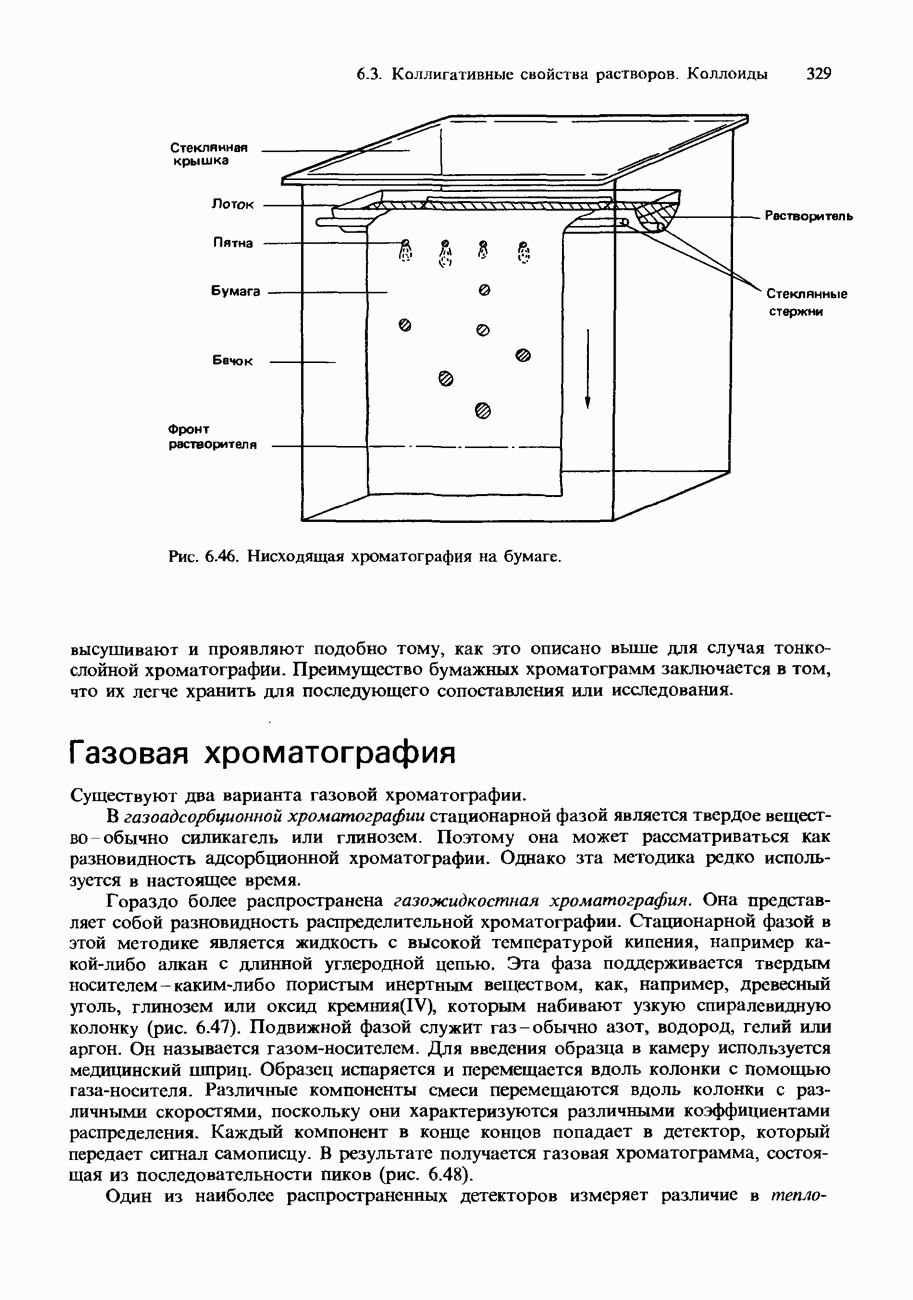
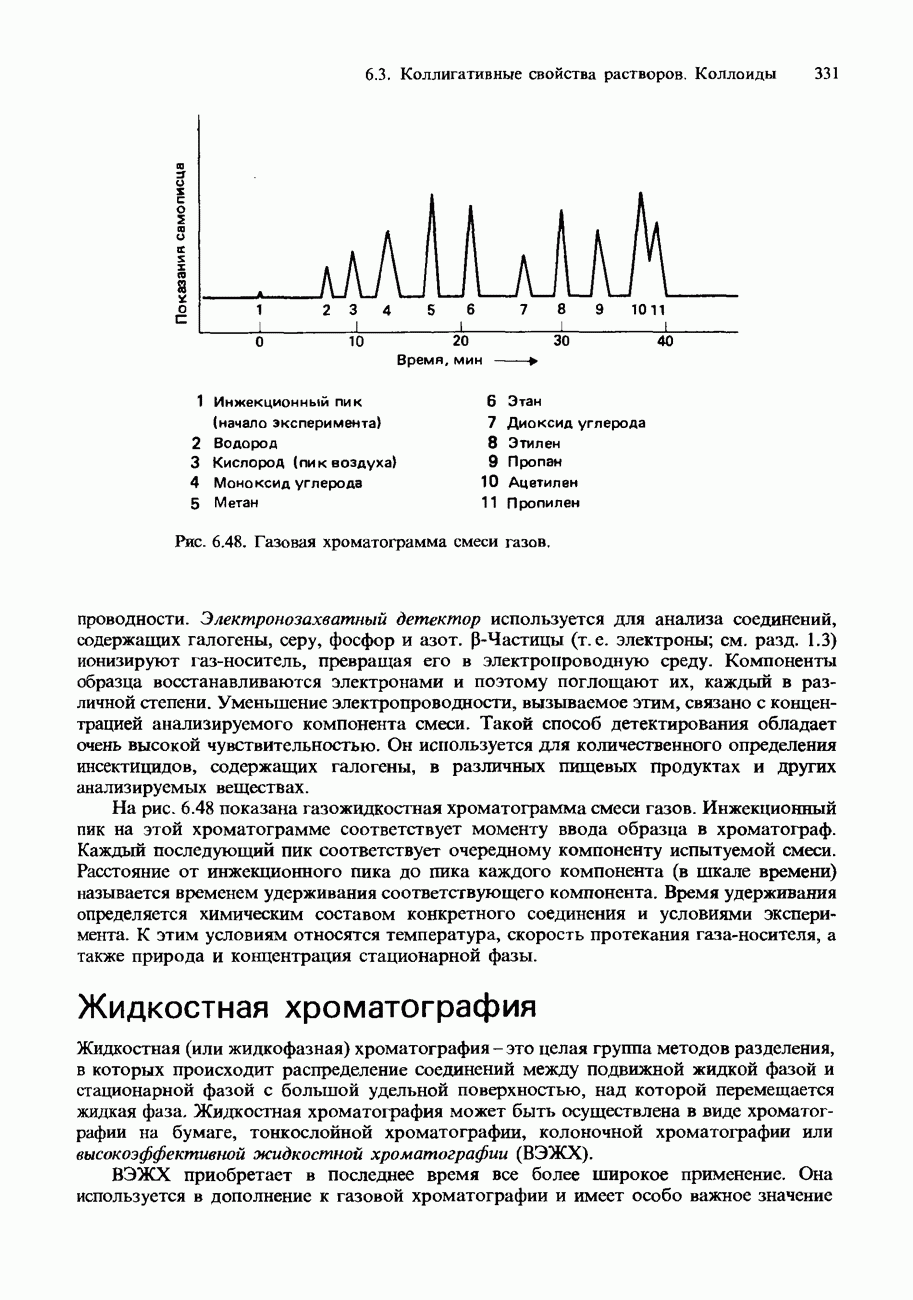
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
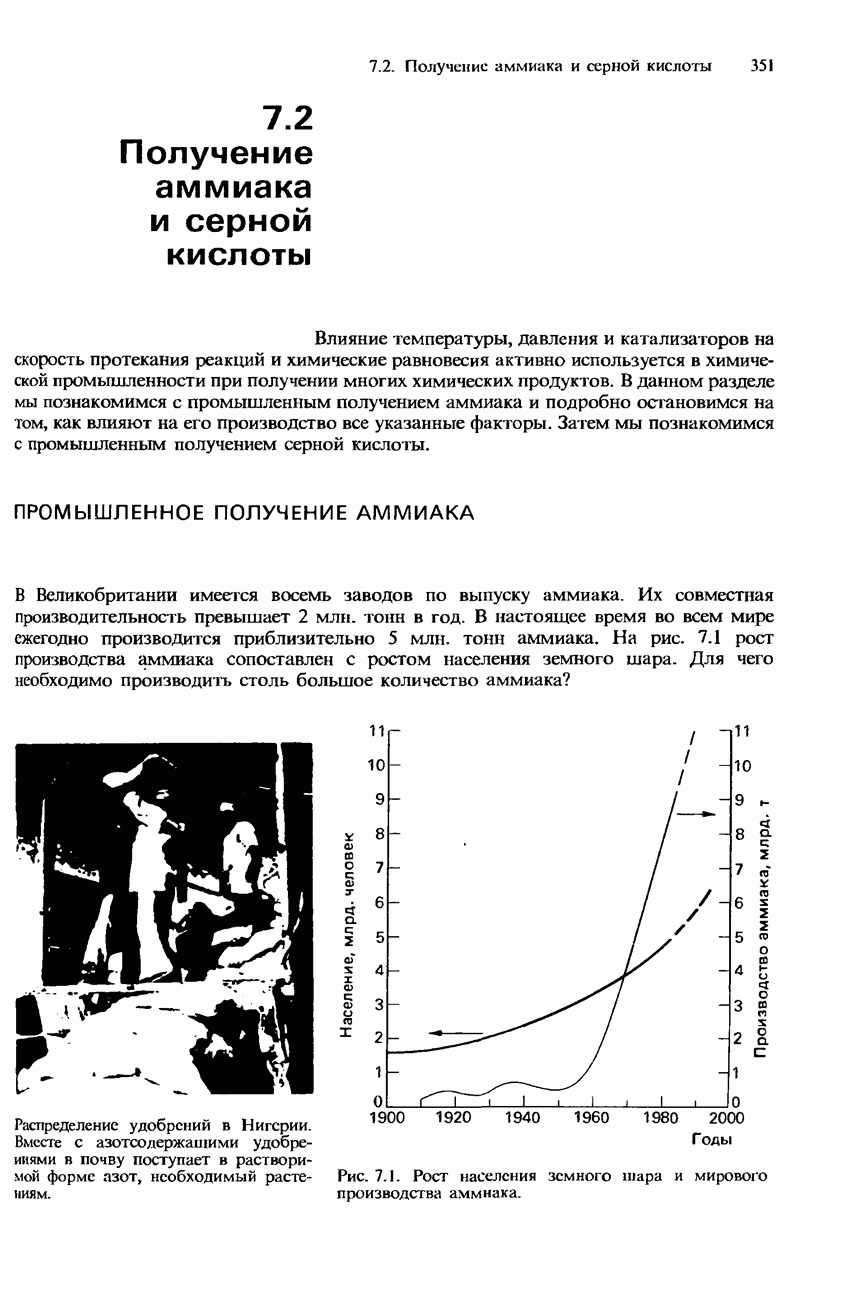
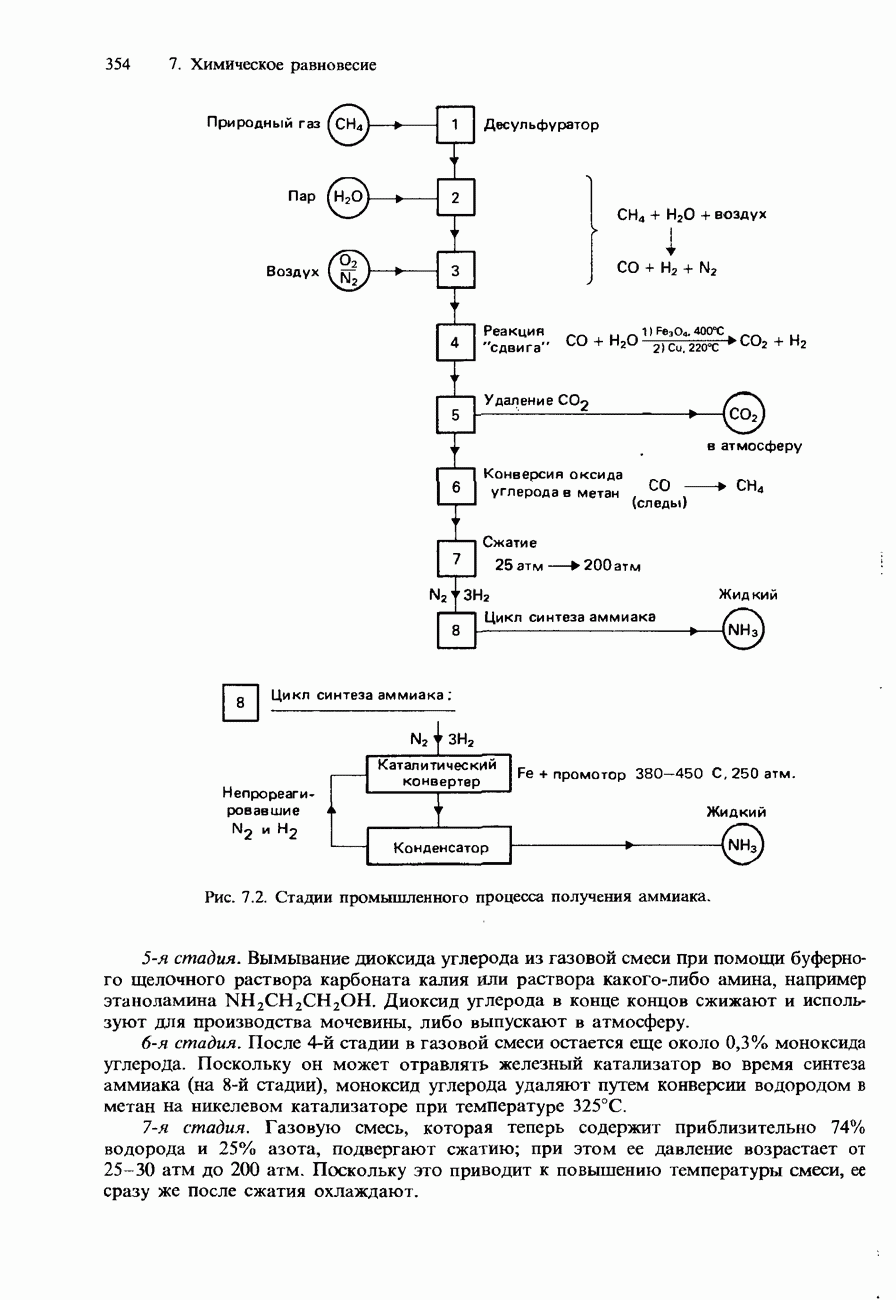
- 7.2. Получение аммиака и серной кислоты
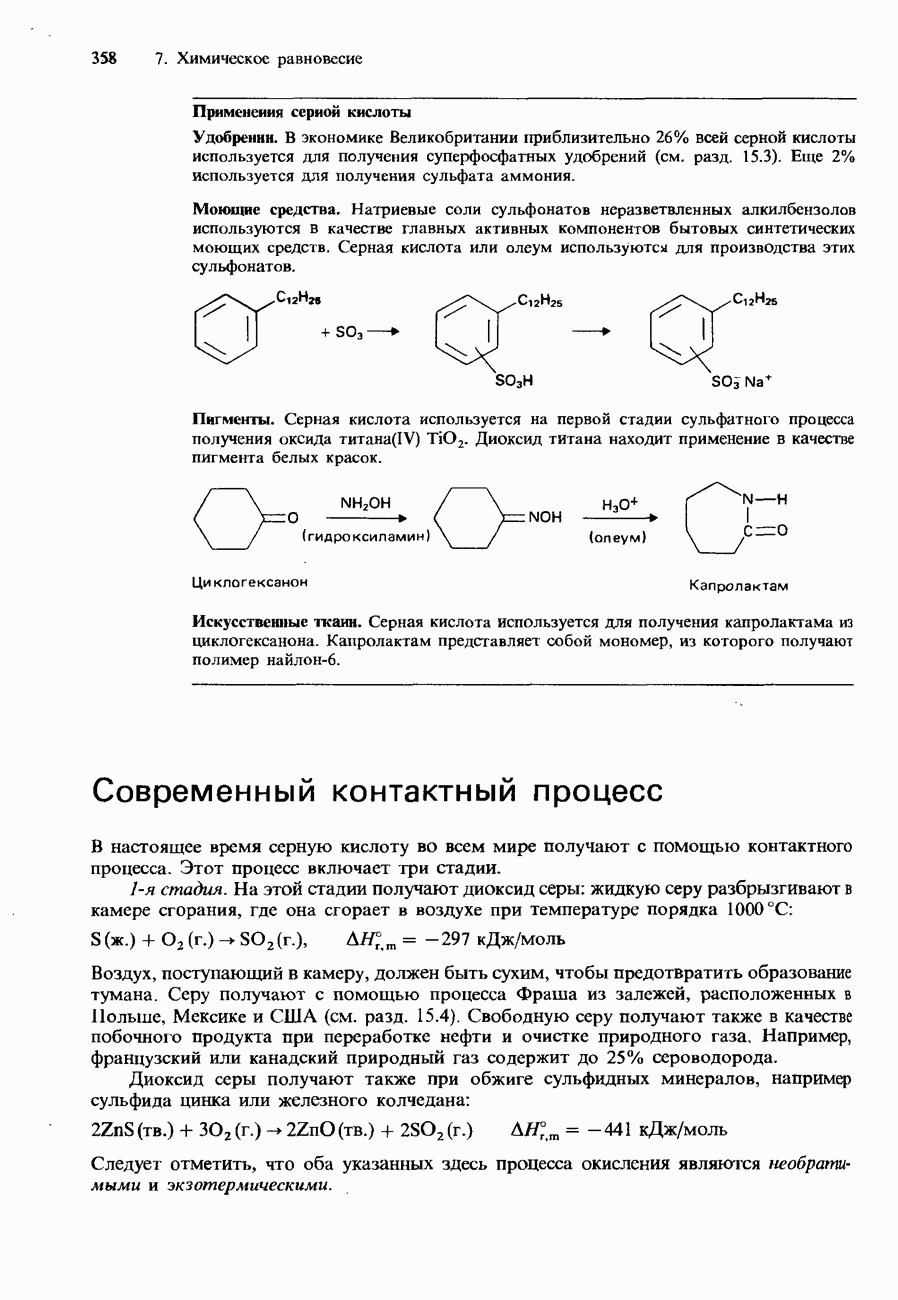
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
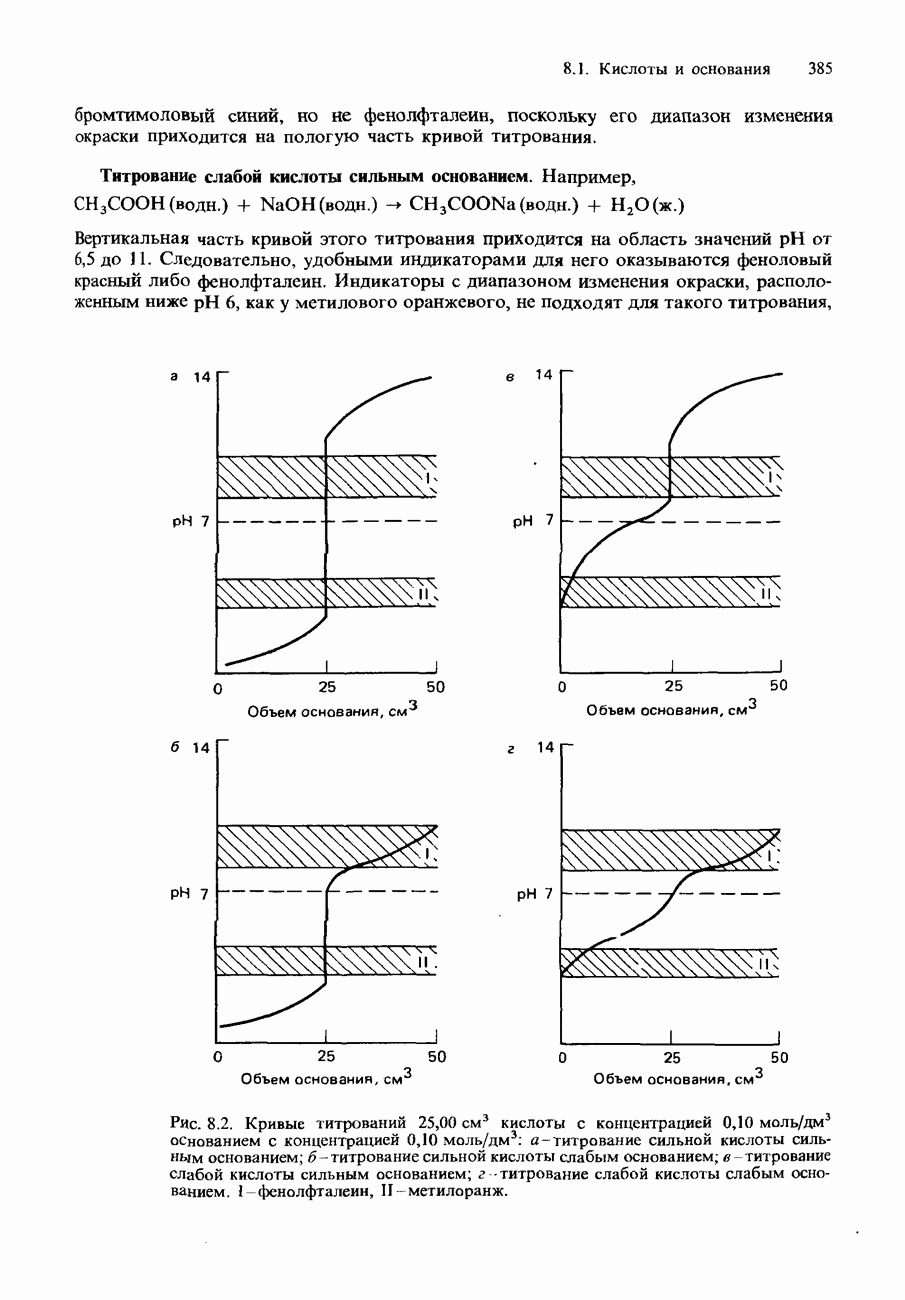
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
- 10.4. Химические источники тока
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
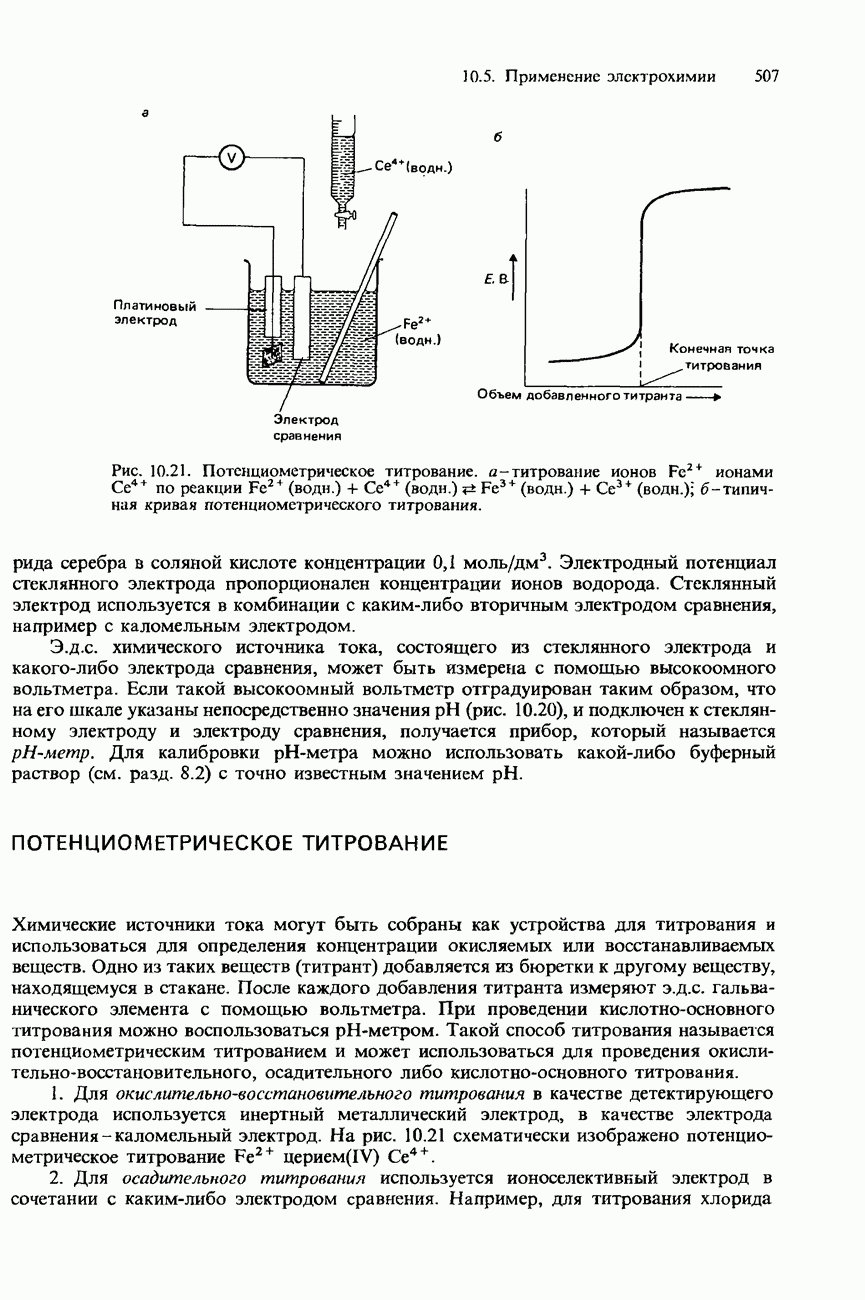
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
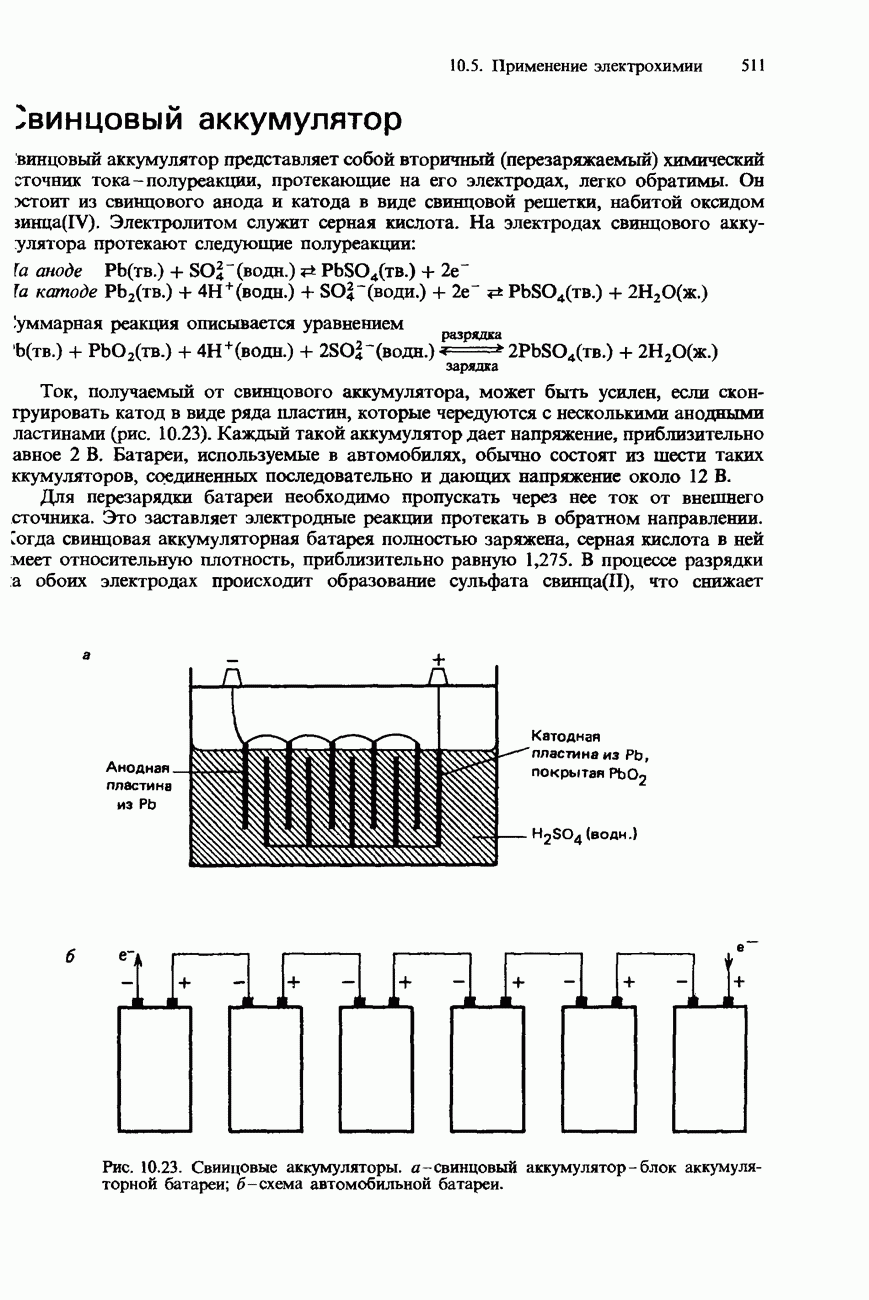
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ