| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОПРОСЫ ДЛЯ ПРОВЕРКИ
1. а) 1) Что означает выражение «изменение внутренней энергии в химической реакции 
Что означает выражение «изменение энтальпии в химической реакции 
Чем объясняется различие между Л U и ЛЯ?
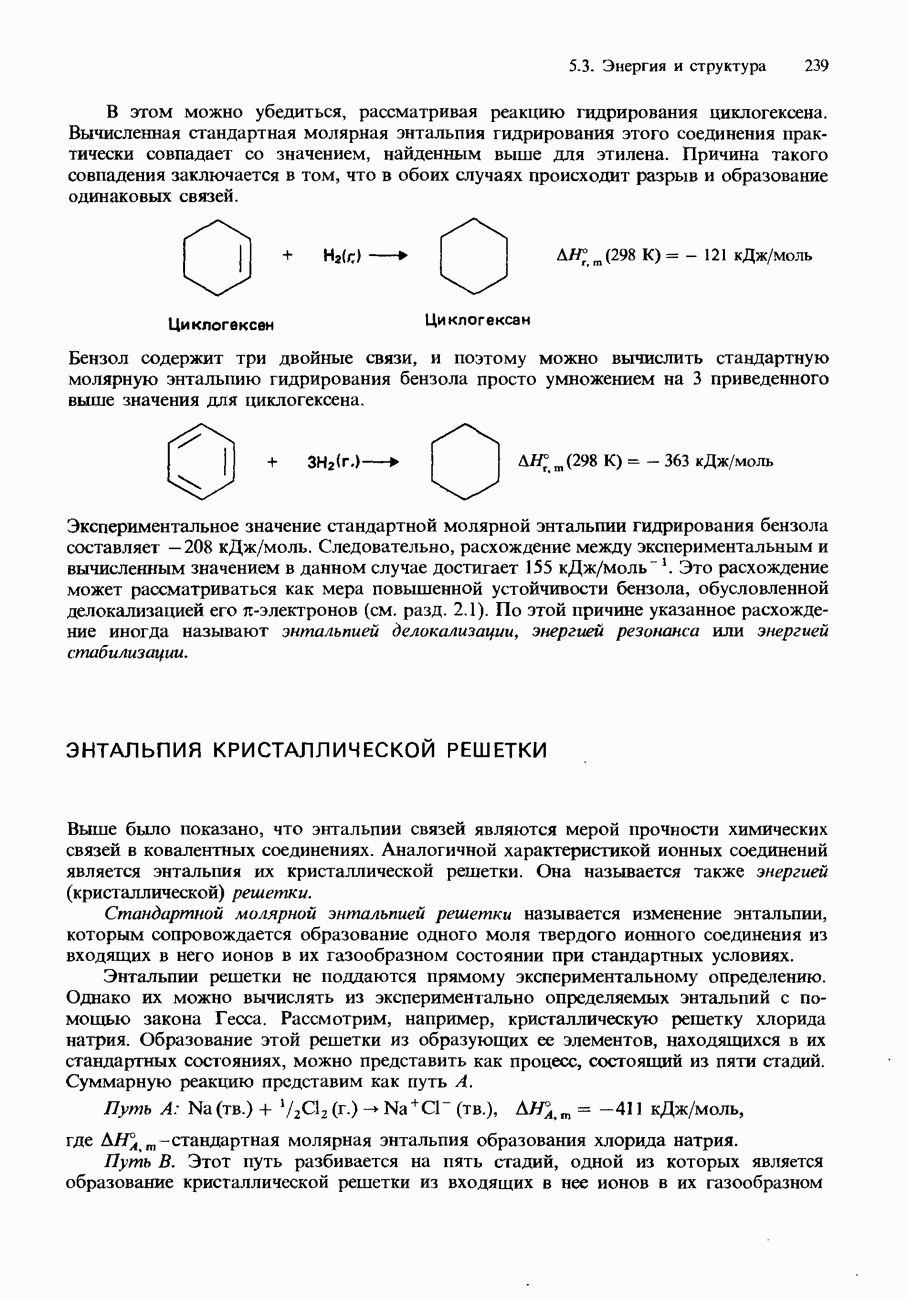
б) К какому выводу о характере химической связи в бензоле  можно прийти на основании следующих данных?
можно прийти на основании следующих данных?

в) Вычислите энтальпию образования метана на основании следующих данных:

2. а) Дайте определения стандартной энтальпии сгорания этана  и стандартной энтальпии образования пропана
и стандартной энтальпии образования пропана 
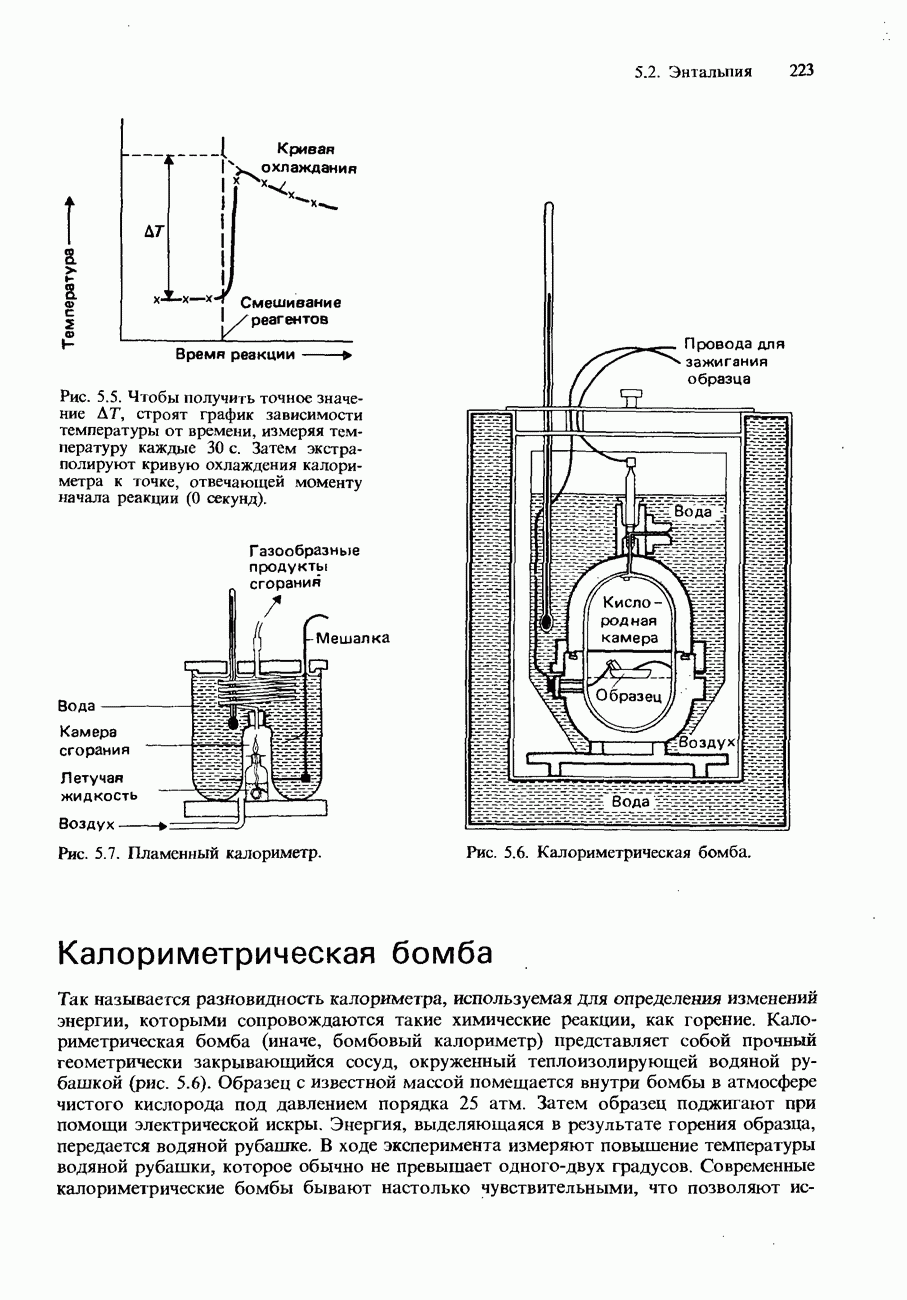
б) 1) Кратко опишите, как осуществляется определение стандартной энтальпии сгорания твердого вещества или жидкости с известной относительной молекулярной массой.
2) Смесь пропана с бутаном объемом 5,6 дм3 (при стандартных условиях) в результате полного сгорания выделила 654 кДж тепловой энергии. Вычислите состав этой смеси в объемных процентах. (Энтальпии сгорания пропана и бутана составляют 2220 и  соответственно; молярный объем при стандартных условиях равен 22,4 дм3.)
соответственно; молярный объем при стандартных условиях равен 22,4 дм3.)
в) Вычислите стандартную энтальпию образования этилена по следующим данным о энергии, выделяющейся при сгорании 1 г указанных веществ в избытке кислорода:


г) Кратко объясните, почему хлорид кальция имеет высокую температуру плавления, либо почему он очень хорошо растворяется в воде.
3. а) 1) Дайте определение понятия стандартная энтальпия сгорания, 
Вычислите изменение стандартной энтальпии для реакции окисления этанола в уксусный альдегид на основании следующих данных о стандартных энтальпиях сгорания:

б) 1) На примере метана  объясните, в чем заключается различие между энтальпией диссоциации связи и средней энтальпией связи.
объясните, в чем заключается различие между энтальпией диссоциации связи и средней энтальпией связи.
2) Вычислите среднюю энтальпию связей  по следующим данным о стандартных энтальпиях атомизации метана и этана:
по следующим данным о стандартных энтальпиях атомизации метана и этана:

3) Первая, вторая и третья энтальпии диссоциации метана равны соответственно  Вычислите четвертую энтальпию диссоциации метана.
Вычислите четвертую энтальпию диссоциации метана.
в) Как объяснить следующие фактьг: 1) иитрат аммония легко растворим в воде, несмотря на то что стандартная энтальпия его растворения имеет положительное значение; 2) хотя энтальпия сгорания тростникового сахара равна приблизительно  окисления тростникового сахара на воздухе при обычных температурах не наблюдается?
окисления тростникового сахара на воздухе при обычных температурах не наблюдается?
4. а) Сформулируйте закон Гесса.
б) Стандартную энтальпию образования  бензола (т. е.
бензола (т. е.  для указанной ниже реакции (1) при
для указанной ниже реакции (1) при  и давлении 1 атм), а также
и давлении 1 атм), а также  гидроксида натрия (т. е. АН для реакции
гидроксида натрия (т. е. АН для реакции  ) нельзя определить прямыми экспериментальными методами.
) нельзя определить прямыми экспериментальными методами.

Однако каждое из этих двух значений  можно получить, выразив его через измеримые соответствующими калориметрическими методами значения АН для трех различных процессов или реакций. Опишите эти три процесса или реакции (дайте словесное описание или запишите соответствующие уравнения) для каждого из указанных выше случаев образования бензола и гидроксида натрия (2). (Не требуется указывать, каким образом следует использовать значения АН, чтобы определить
можно получить, выразив его через измеримые соответствующими калориметрическими методами значения АН для трех различных процессов или реакций. Опишите эти три процесса или реакции (дайте словесное описание или запишите соответствующие уравнения) для каждого из указанных выше случаев образования бензола и гидроксида натрия (2). (Не требуется указывать, каким образом следует использовать значения АН, чтобы определить  ).
).
5. а) Сформулируйте закон Гесса.
б) При добавлении 2,76 г (0,02 моля) карбоната калия к 30,0 см3 соляной кислоты, концентрация которой равна приблизительно  произошло повышение температуры на
произошло повышение температуры на 
1) Запишите уравнение этой реакции.
2) Вычислите изменение энтальпии в этой реакции в расчете на один моль карбоната калия, исходя из предположения, что удельная теплоемкость всех растворов равна  и что все растворы имеют плотность 1,0 г/см3.
и что все растворы имеют плотность 1,0 г/см3.
3) Объясните, почему концентрация соляной кислоты должна быть лишь приблизительно равной 
в) При добавлении 2,00 г (0,020 моля) гидрокарбоната калия к  соляной кислоты с указанной выше концентрацией произошло понижение температуры на
соляной кислоты с указанной выше концентрацией произошло понижение температуры на 
1) Запишите уравнение этой реакции.
2) Вычислите изменение энтальпии в этой реакции в расчете на один моль гидрокарбоната калия.
г) При нагревании гидрокарбоната калия он разлагается на карбонат калия, воду и диоксид углерода. Воспользовавшись законом Гесса и результатами, полученными вами при ответе на вопросы (б) и (в), вычислите изменение энтальпии для термического разложения гидрокарбоната калия. Приведите все выкладки с объяснениями, отмечая в них, какие изменения энтальпии являются экзотермическими либо эндотермическими.
6. а) Сформулируйте закон Гесса и дайте определения:
1) стандартного состояния вещества;
2) стандартного изменения энтальпии в химической реакции.
б) Кратко опишите, как провести экспериментальное определение энтальпии нейтрализации разбавленного раствора соляной кислоты разбавленным раствором гидроксида натрия.
в) Стандартная энтальпия сгорания пропана  при 298 К равна
при 298 К равна  Вычислите стандартную энтальпию образования
Вычислите стандартную энтальпию образования  пропана при 298 К исходя из того, что при этой температуре
пропана при 298 К исходя из того, что при этой температуре

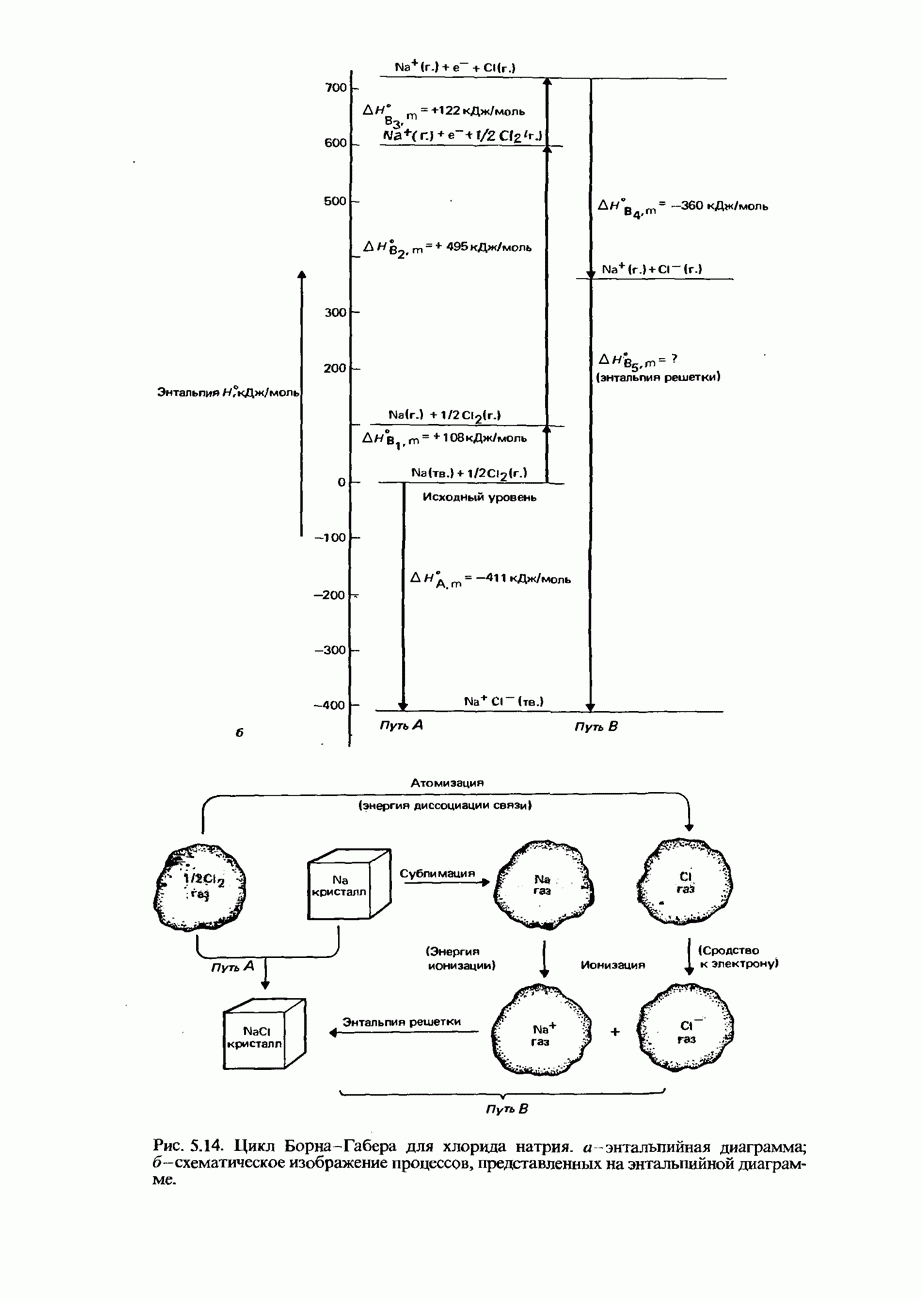
7. Дайте определения понятиям энтальпии образования вещества и энергии решетки кристаллического вещества.
Укажите, какими факторами определяется величина энергии решетки. Нарисуйте циклы Борна Габера для образования: а) кристаллического хлорида калия; б) водного раствора хлорида калия. Воспользуйтесь этими циклами и приведенными ниже данными, чтобы вычислить: 1) энтальпию образования хлорида калия, 2) энтальпию растворения хлорида калия.

На основании полученного ответа на вопрос (2) кратко укажите свое мнение относительно растворимости хлорида калия в воде.
8. Ниже перечислены энтальпии некоторых связей при 298 К.

а) На примере метана поясните различие между средней энтальпией связи и энтальпией диссоциации связи.
б) С помощью приведенных выше энтальпий связи вычислите энтальпию реакции

в) Как изменяется энтропия в реакции (б): уменьшается, увеличивается или остается неизменной? Поясните ответ.
г) 1) Воспользуйтесь результатом вашего расчета в пункте  и вычислите энтальпию гидрирования бутадиена исходя из его формулы
и вычислите энтальпию гидрирования бутадиена исходя из его формулы  Экспериментальное значение этого изменения энтальпии равно
Экспериментальное значение этого изменения энтальпии равно  Объясните причину расхождения между этим значением и полученным вами расчетным результатом.
Объясните причину расхождения между этим значением и полученным вами расчетным результатом.
9. а) Нарисуйте термодинамический цикл, показывающий соотношение между энтальпией образования галогенида металла  металл,
металл,  галоген)
галоген)
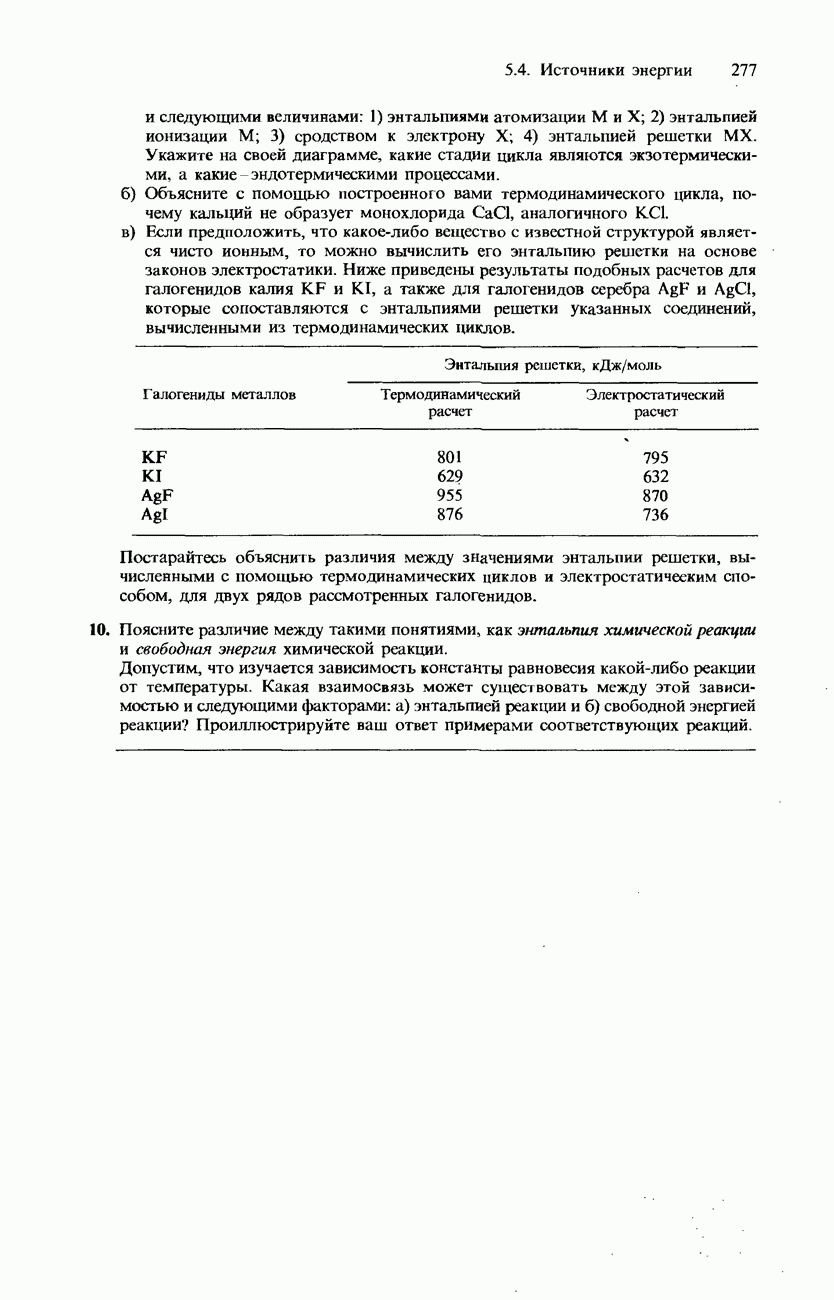
и следующими величинами: 1) энтальпиями атомизации М и X; 2) энтальпией ионизации М; 3) сродством к электрону X; 4) энтальпией решетки MX. Укажите на своей диаграмме, какие стадии цикла являются экзотермическими, а какие - эндотермическими процессами.
б) Объясните с помощью построенного вами термодинамического цикла, почему кальций не образует монохлорида  аналогичного
аналогичного 
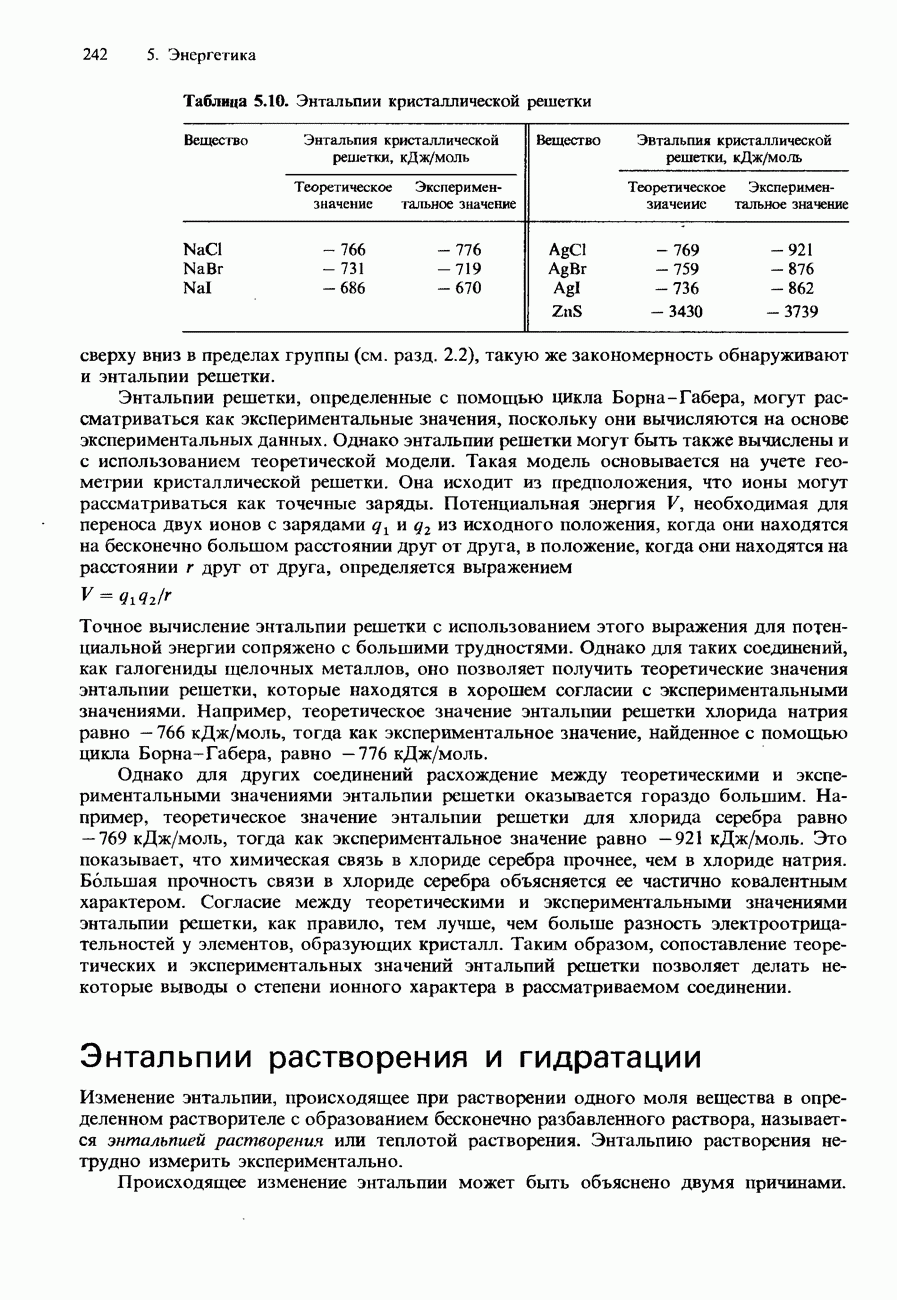
в) Если предположить, что какое-либо вещество с известной структурой является чисто ионным, то можно вычислить его энтальпию решетки на основе законов электростатики. Ниже приведены результаты подобных расчетов для галогенидов калия KF и KI, а также для галогенидов серебра  которые сопоставляются с энтальпиями решетки указанных соединений, вычисленными из термодинамических циклов.
которые сопоставляются с энтальпиями решетки указанных соединений, вычисленными из термодинамических циклов.

Постарайтесь объяснить различия между значениями энтальпии решетки, вычисленными с помощью термодинамических циклов и электростатическим способом, для двух рядов рассмотренных галогенидов.
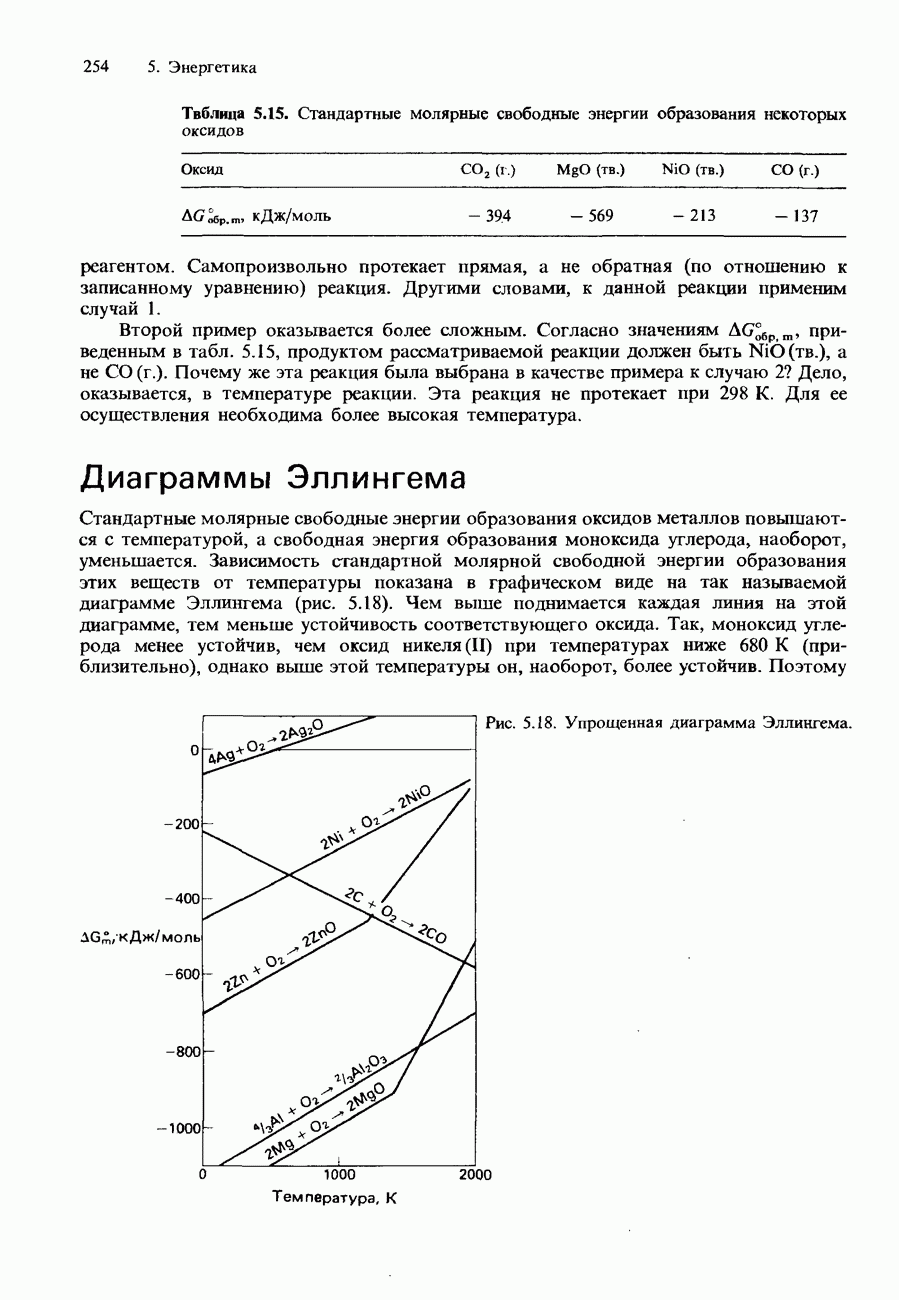
10. Поясните различие между такими понятиями, как энтальпия химической реакции и свободная энергия химической реакции.
Допустим, что изучается зависимость константы равновесия какой-либо реакции от температуры. Какая взаимосвязь может существовать между этой зависимостью и следующими факторами: а) энтальпией реакции и б) свободной энергией реакции? Проиллюстрируйте ваш ответ примерами соответствующих реакций.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
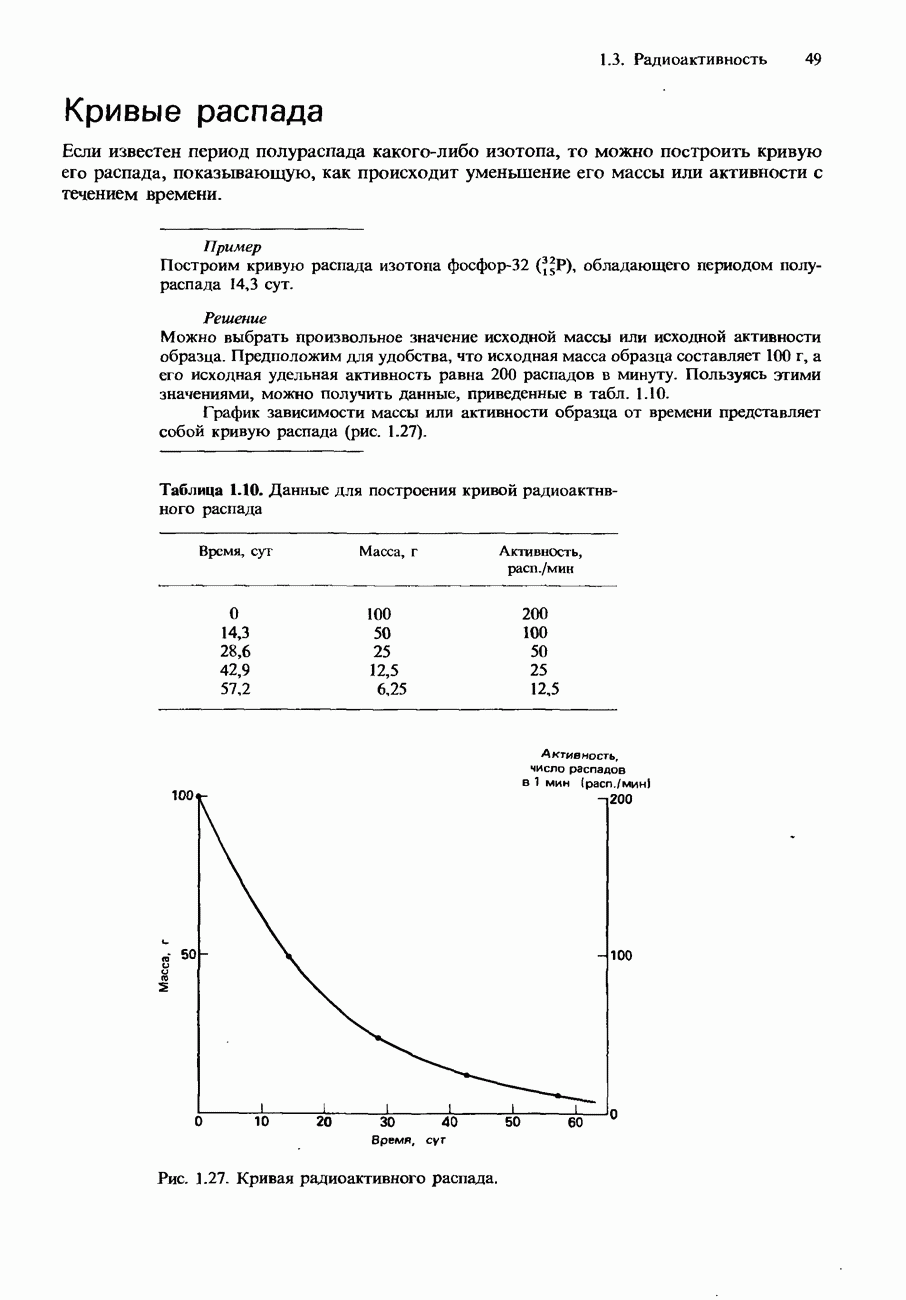
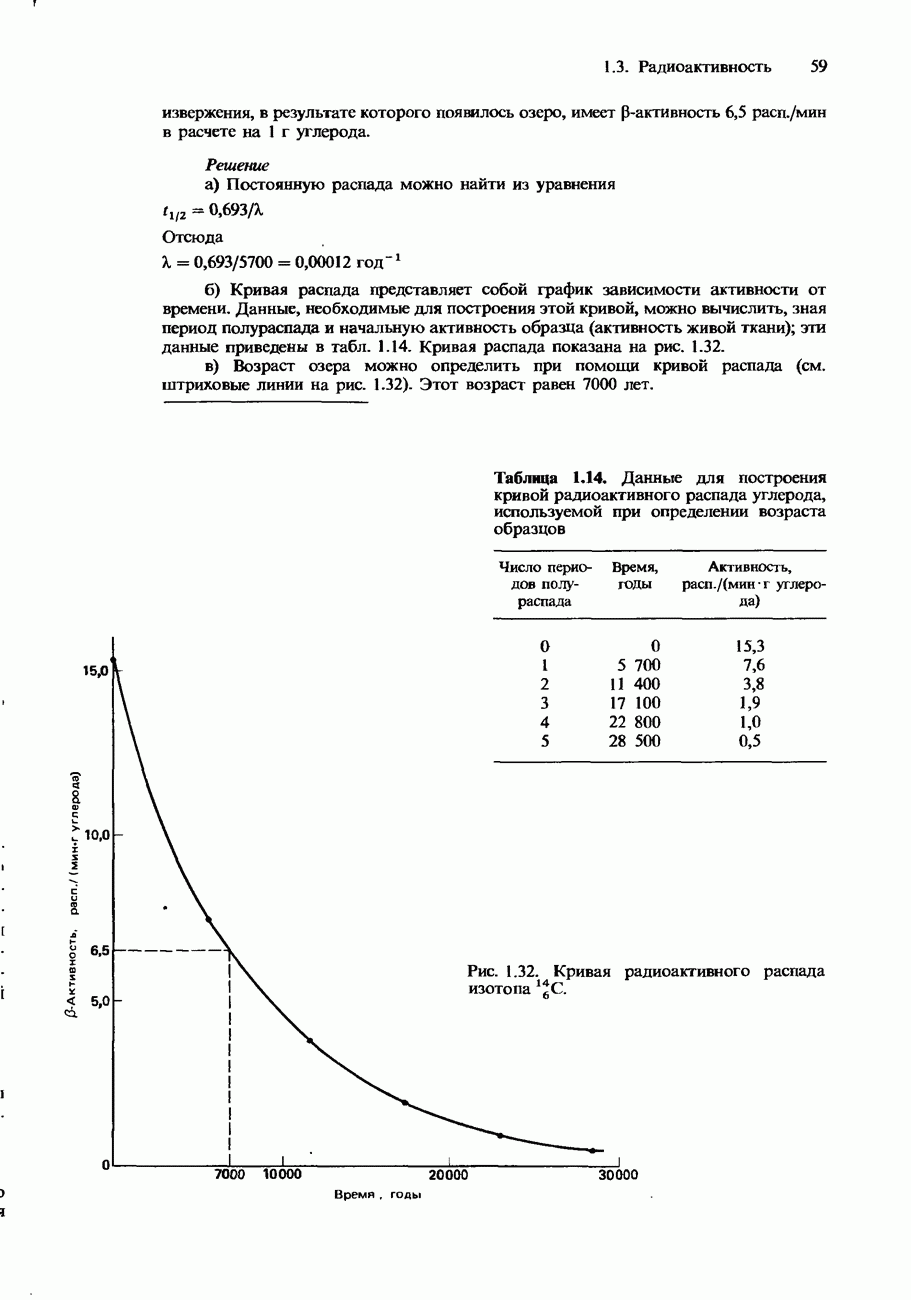
- Кривые распада
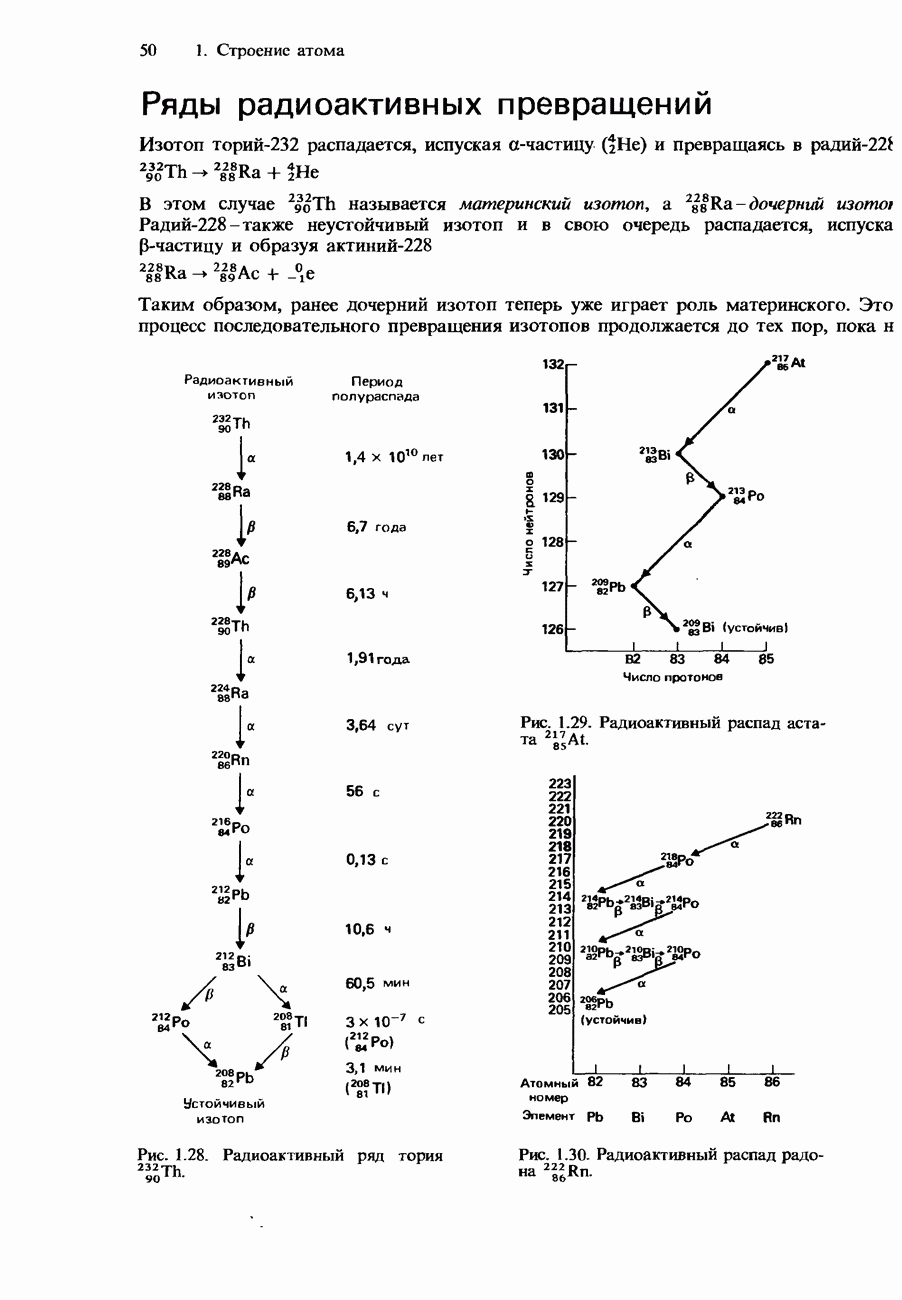
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
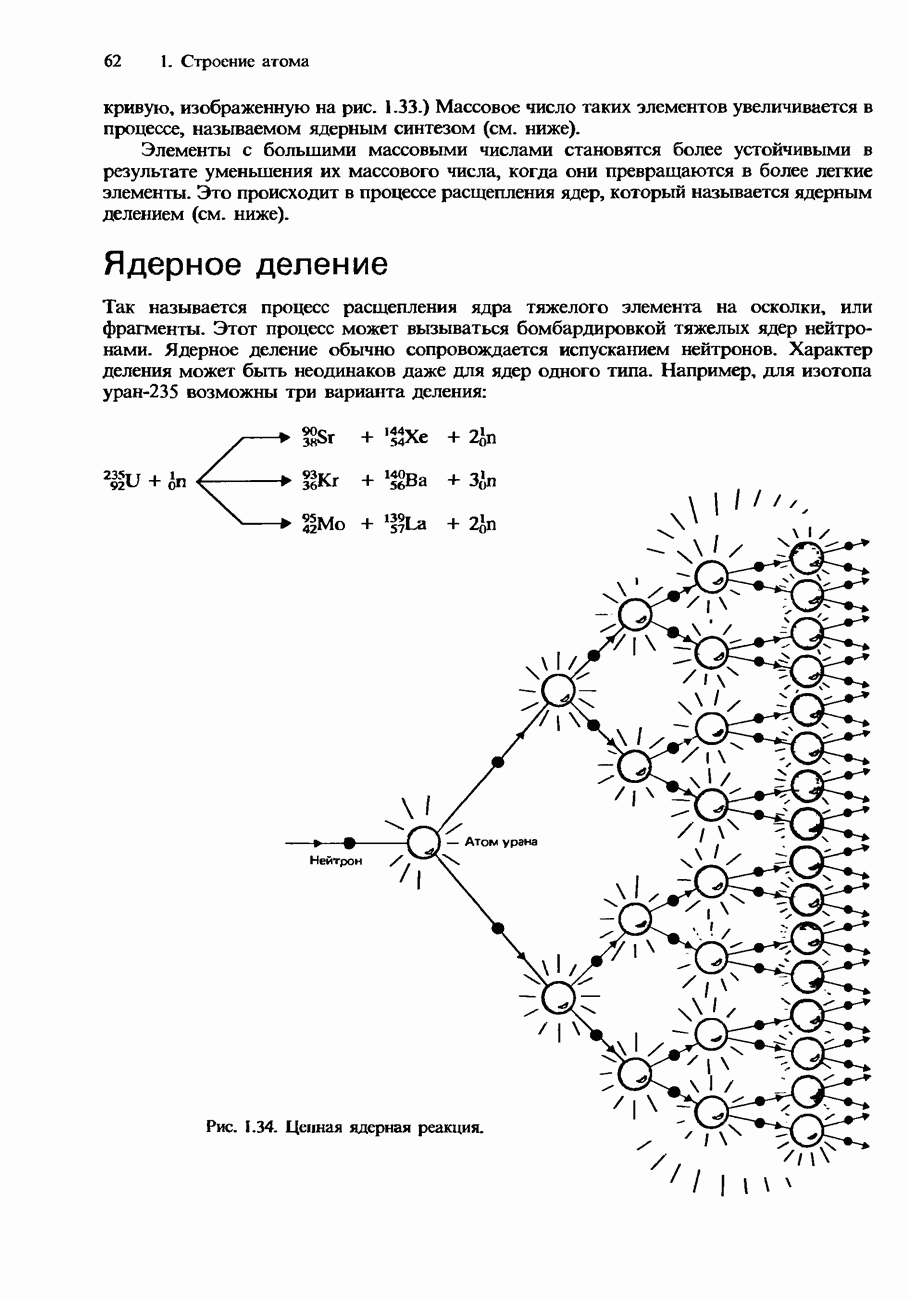
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
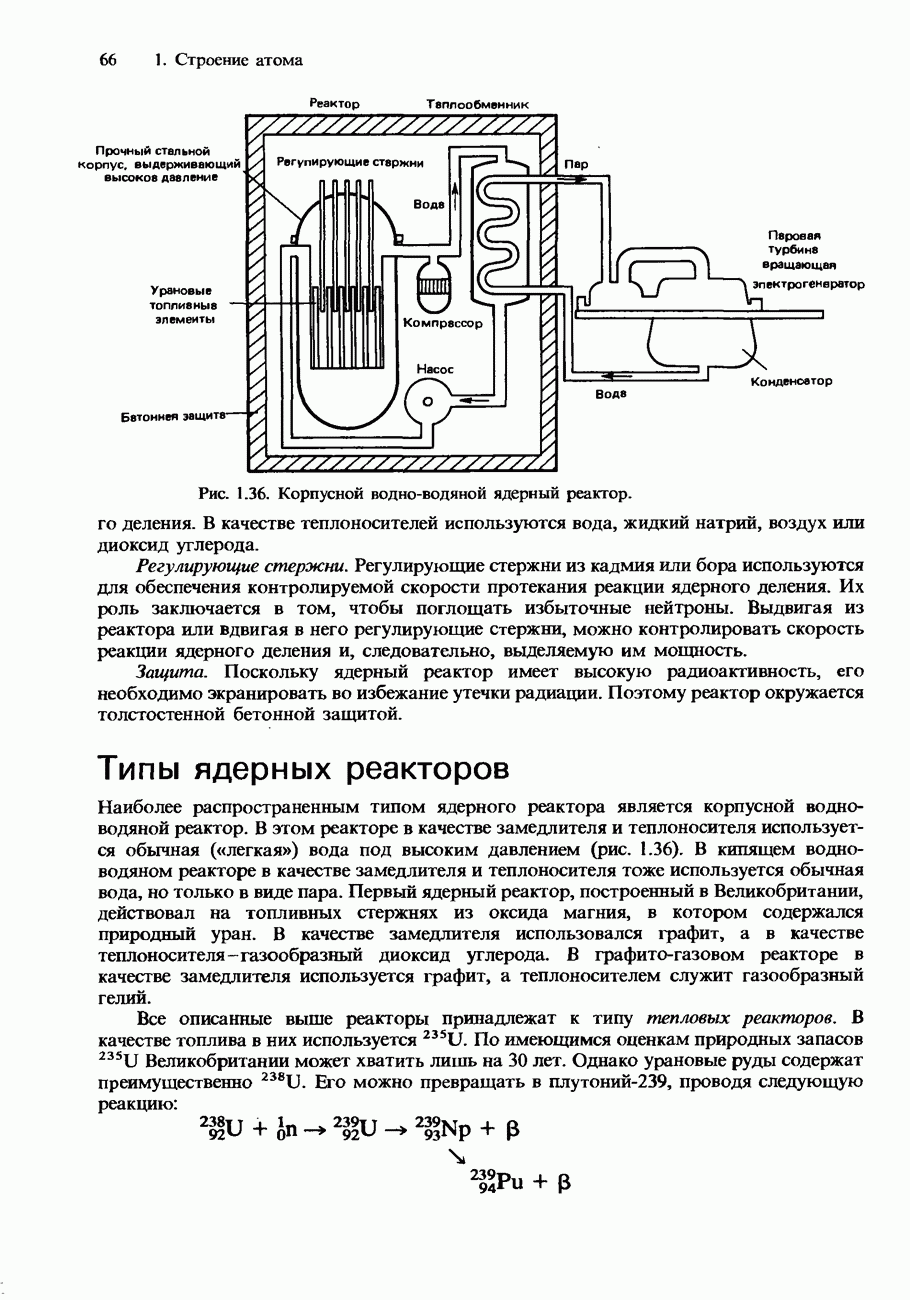
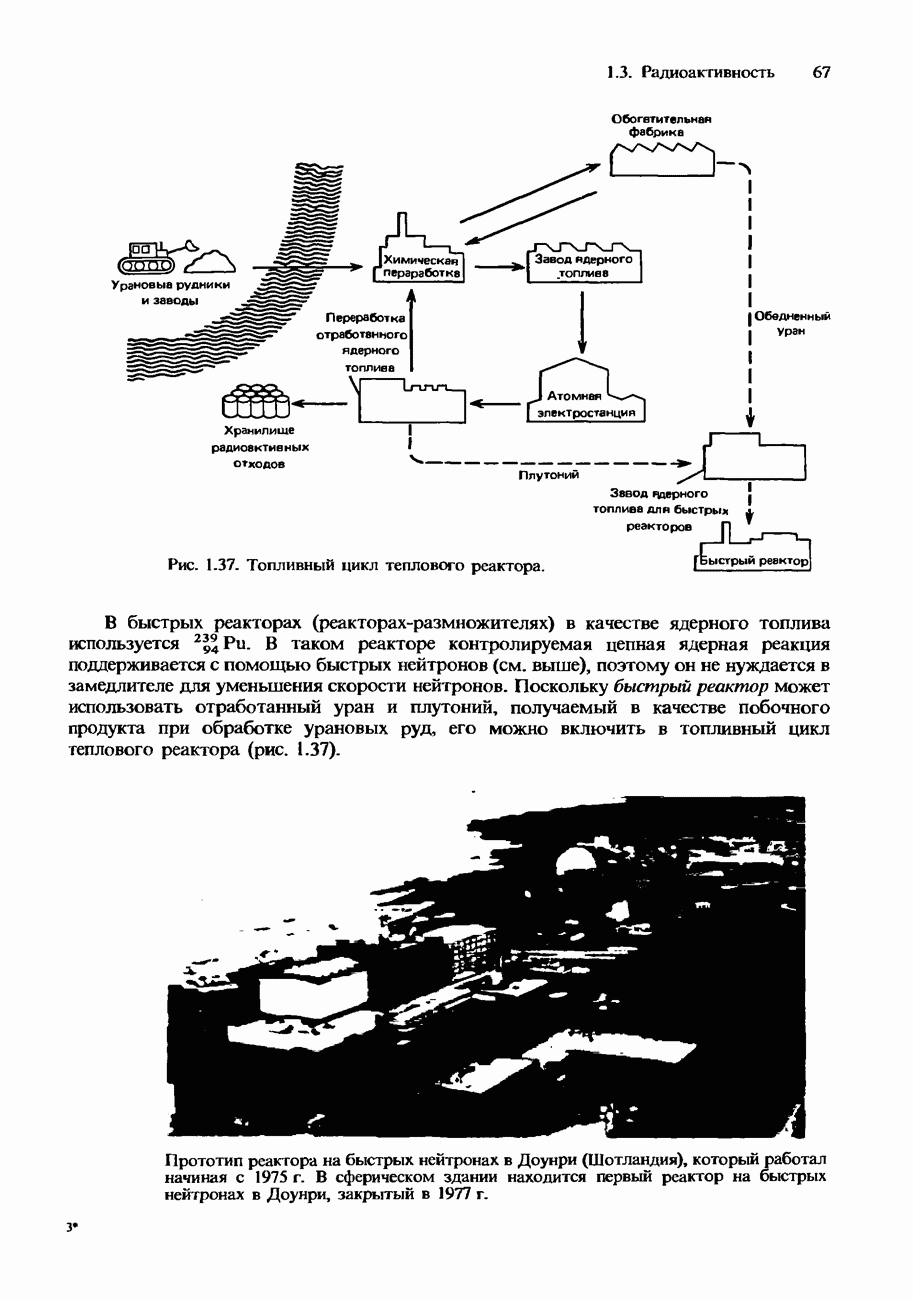
- Типы ядерных реакторов
- Радиоактивные ядерные отходы и их переработка
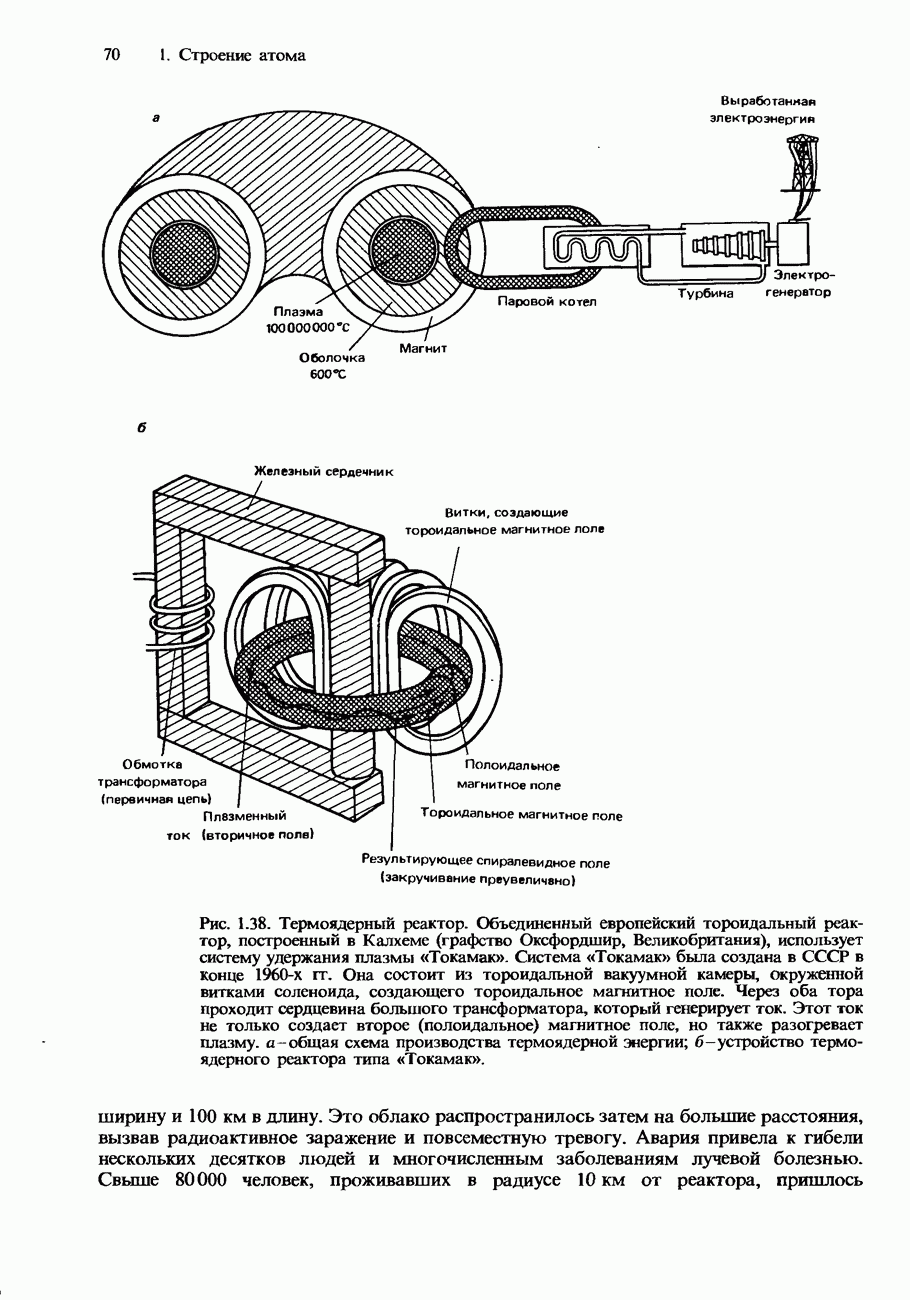
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
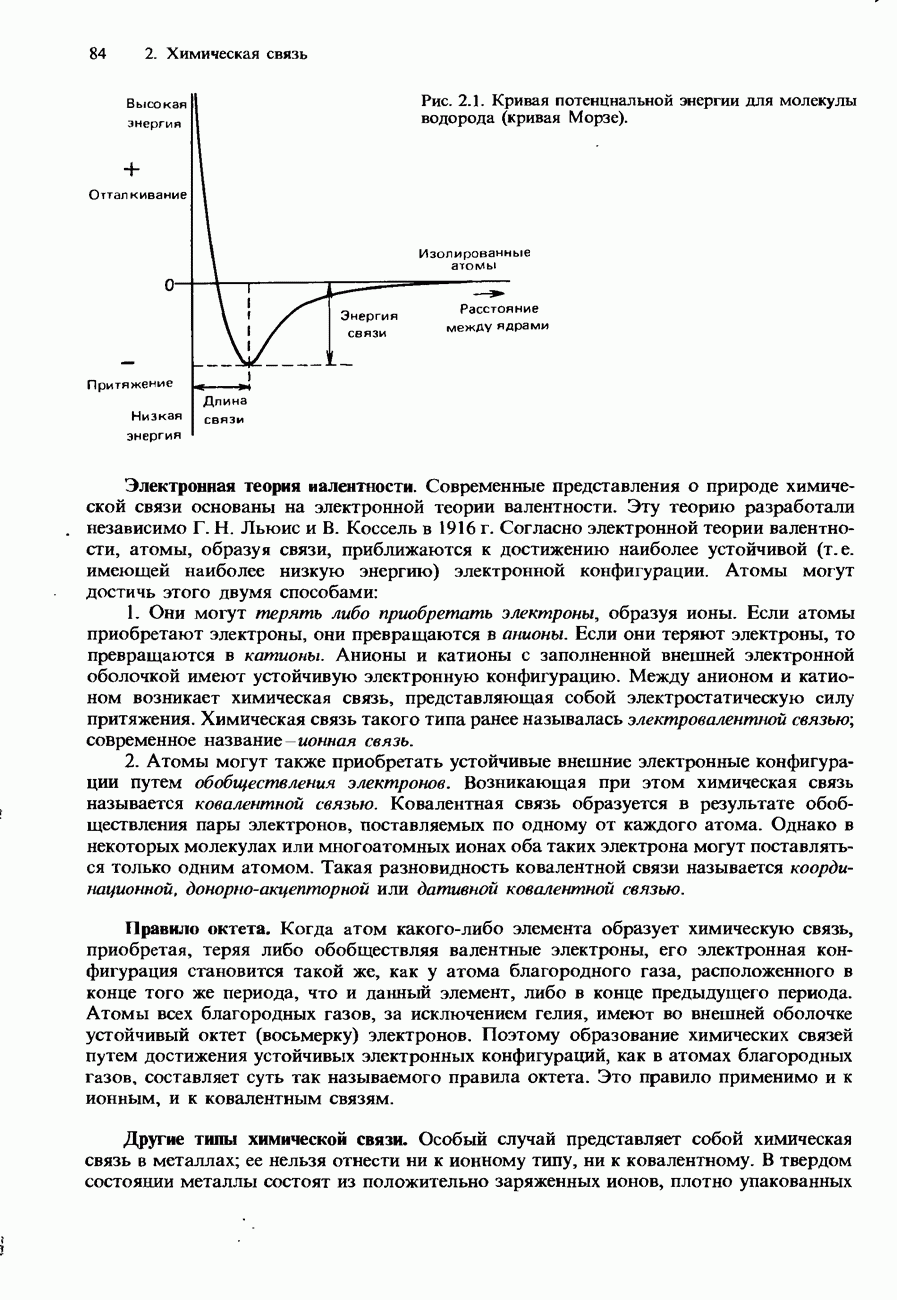
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
- Молекулярные орбитали
- Гибридные атомные орбитали
- Делокализованные орбитали
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
- Сжижение газов
- ЖИДКОСТИ
- Свойства жидкостей
- 3.2. Твердые вещества
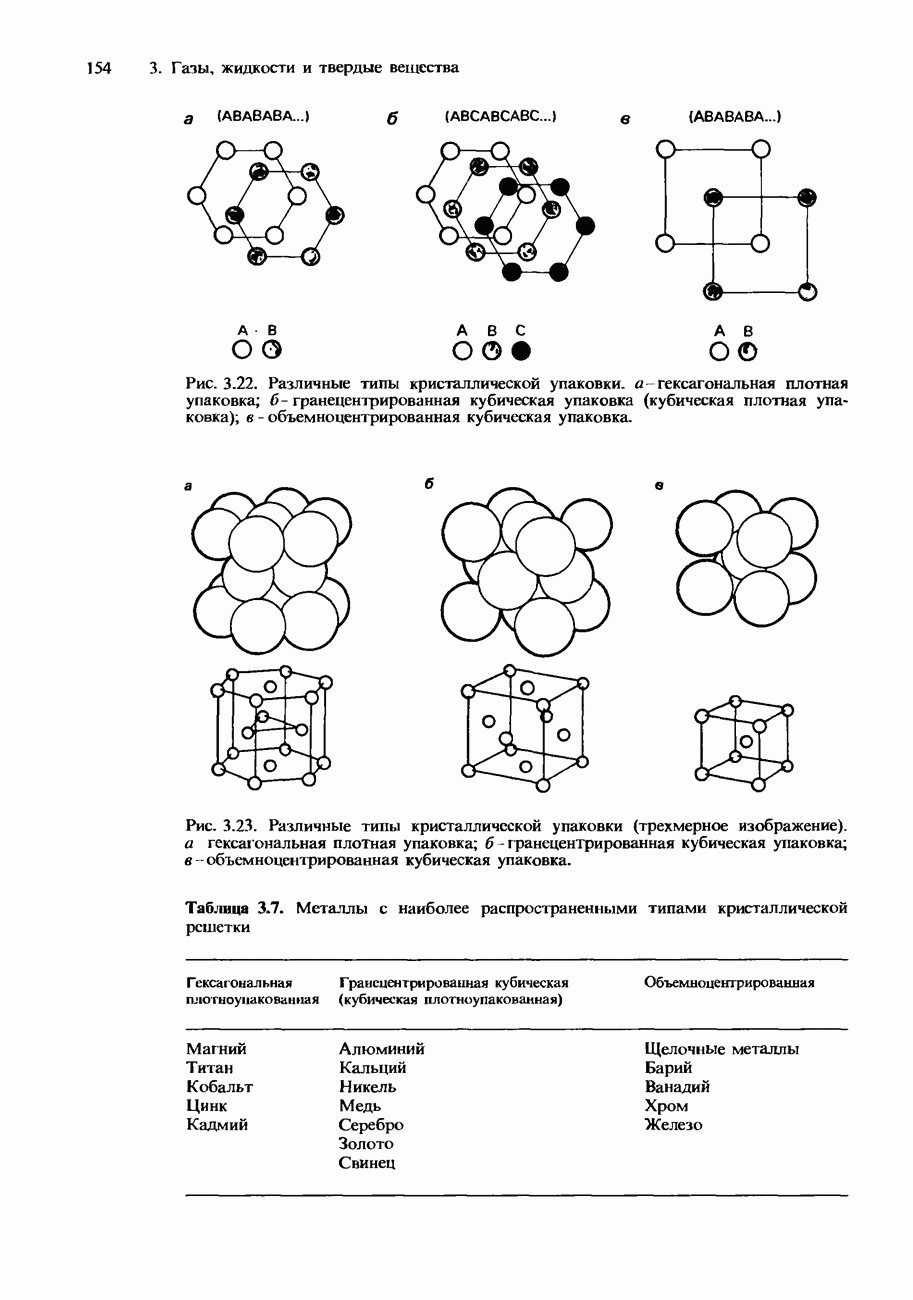
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
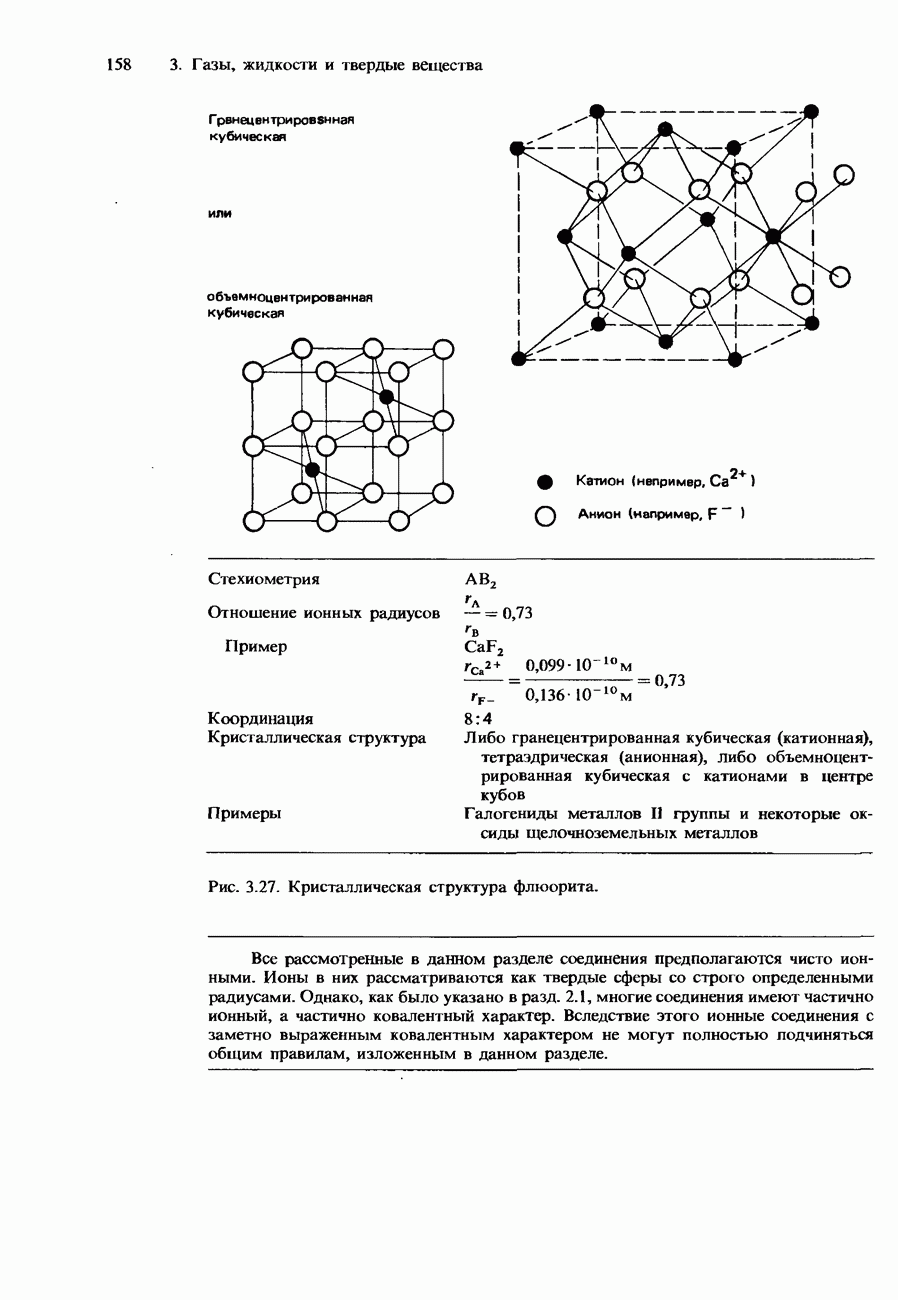
- Ионные кристаллы
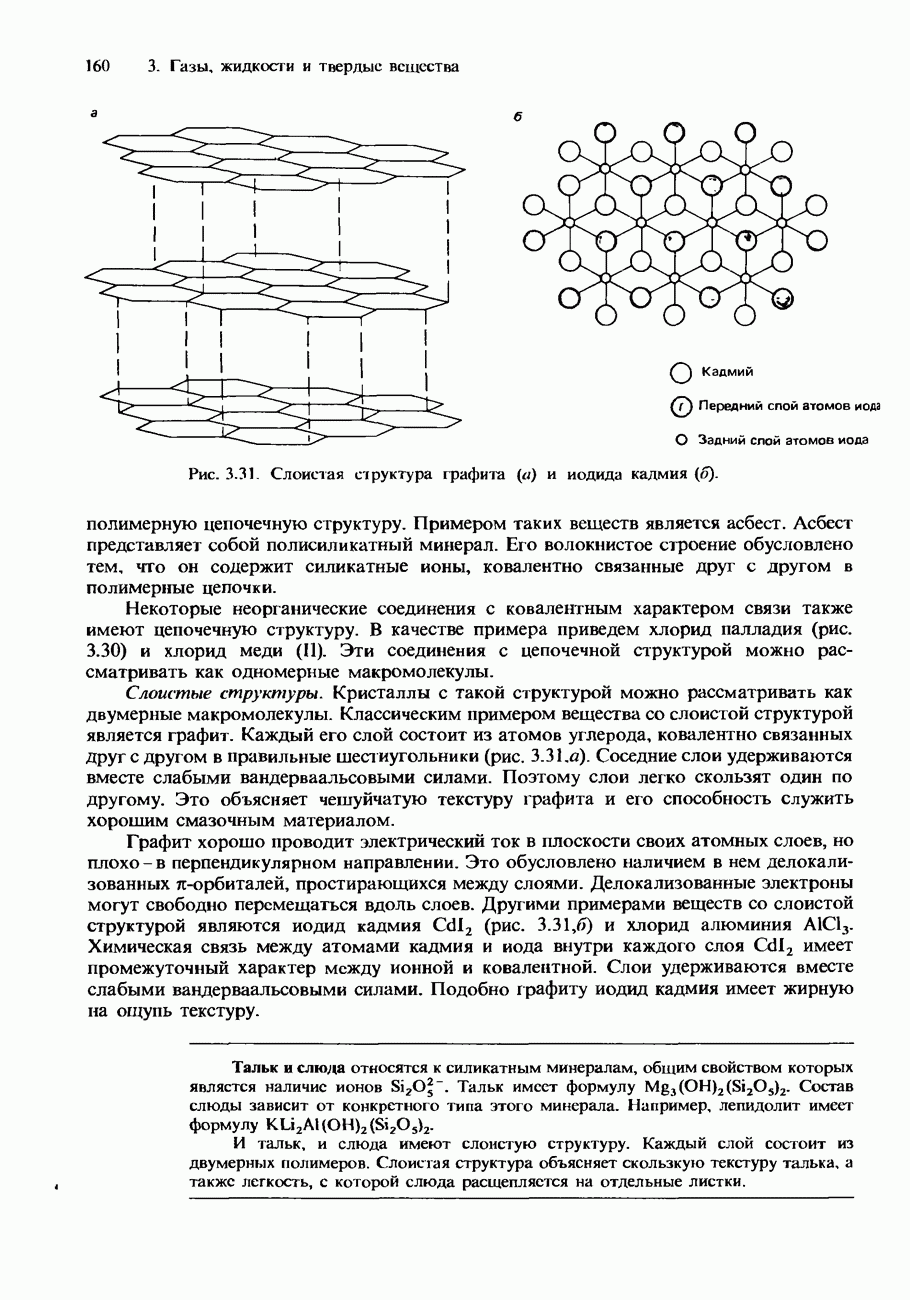
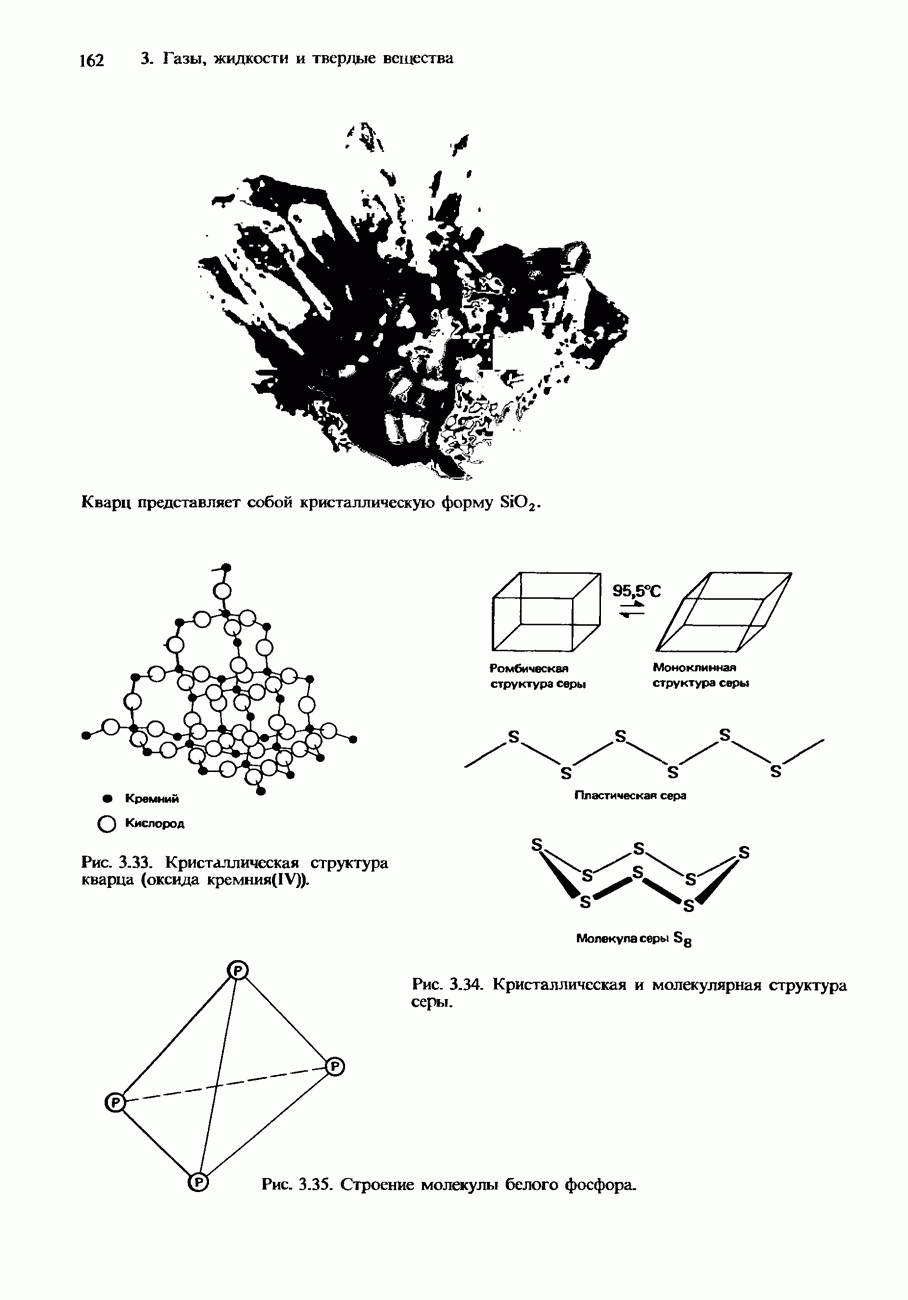
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
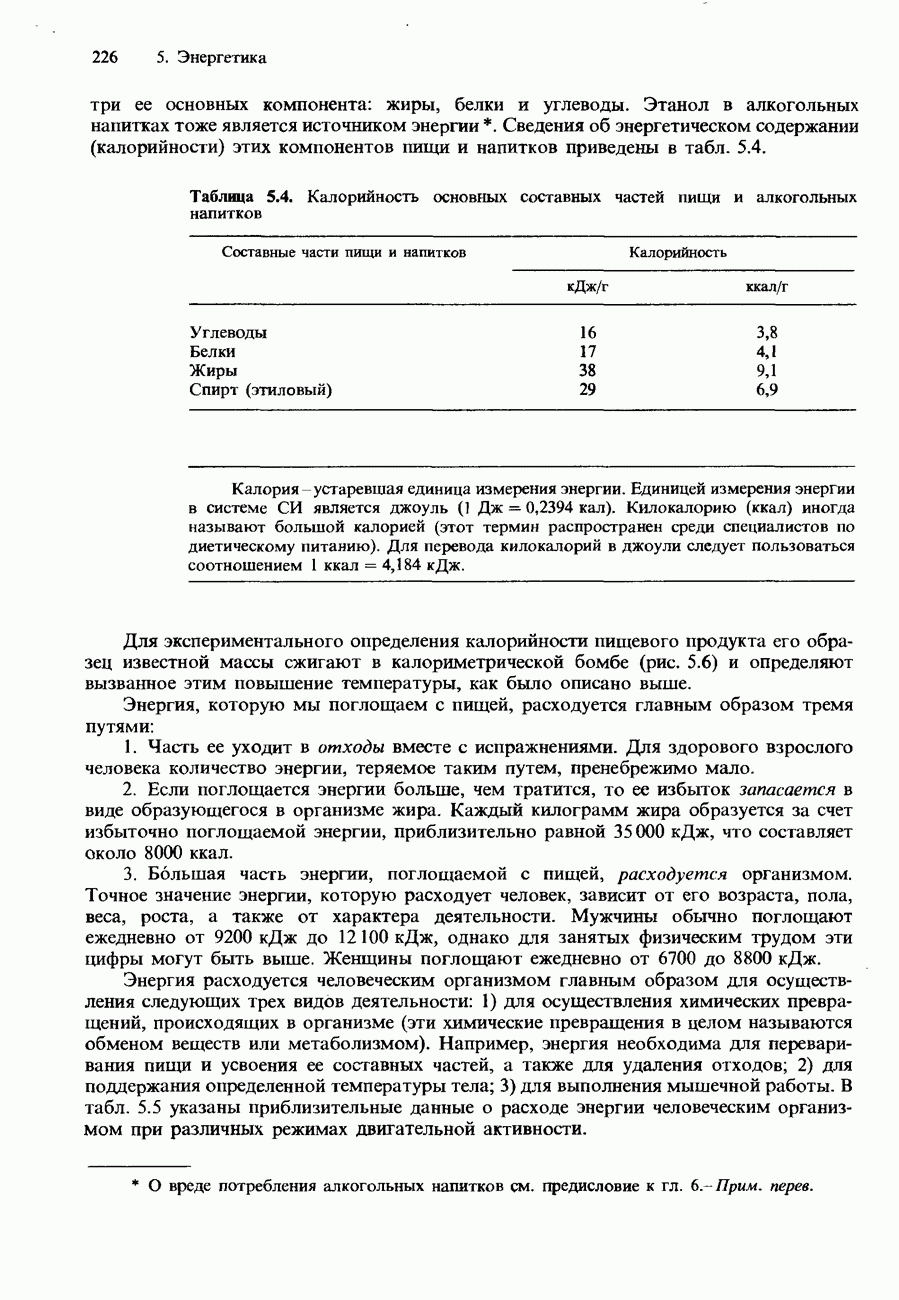
- КАЛОРИЙНОСТЬ ПИЩИ
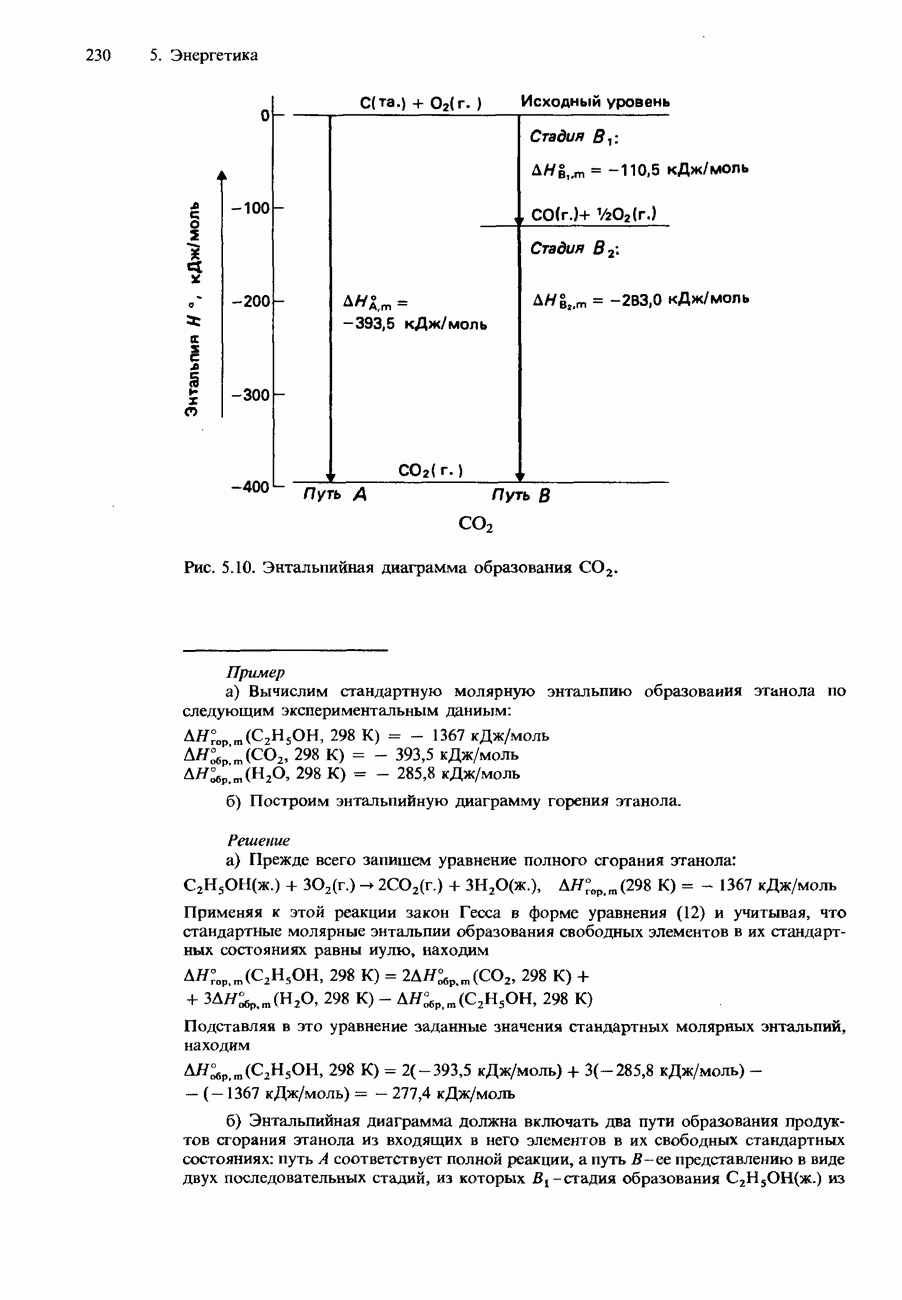
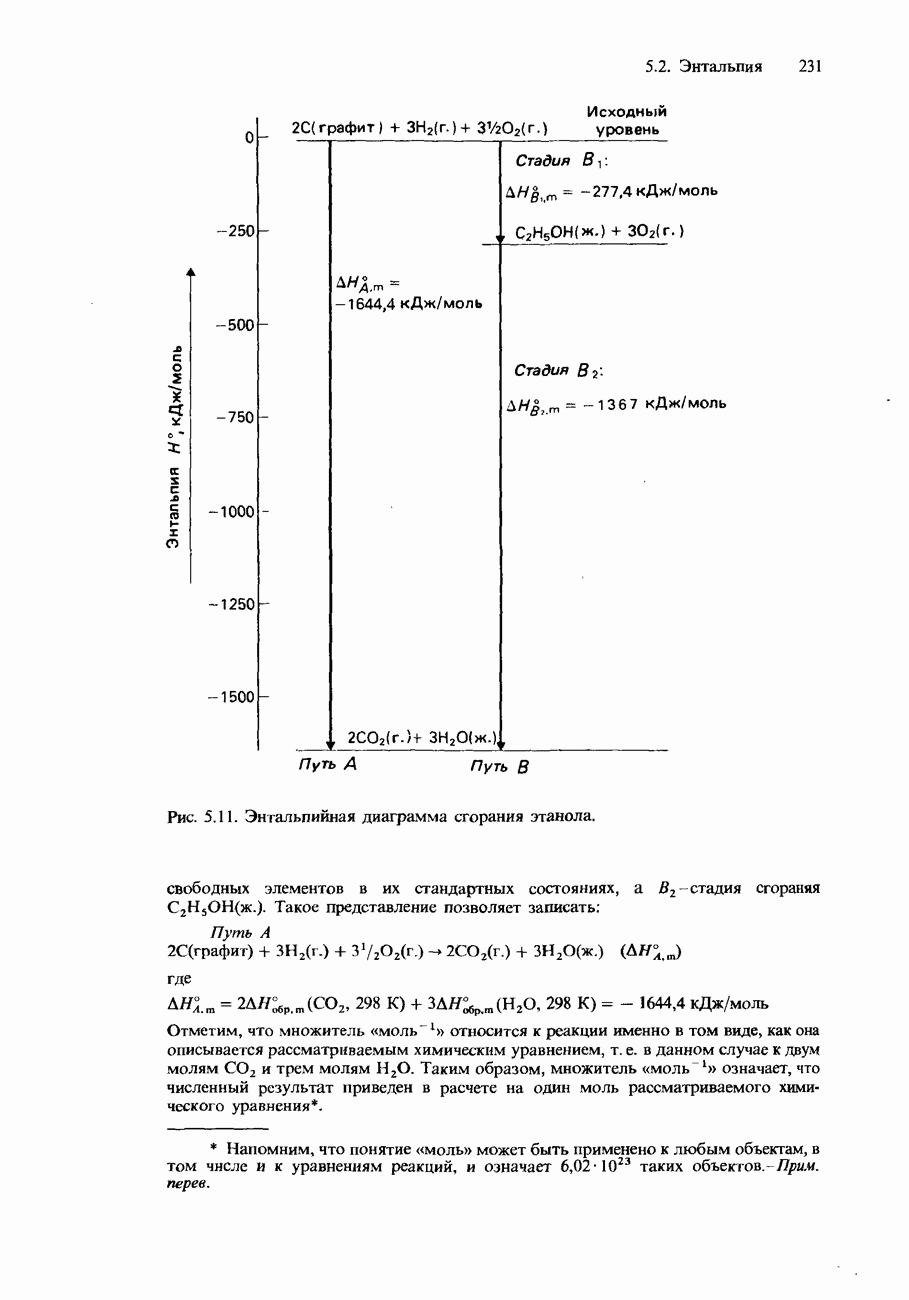
- ЗАКОН ГЕССА
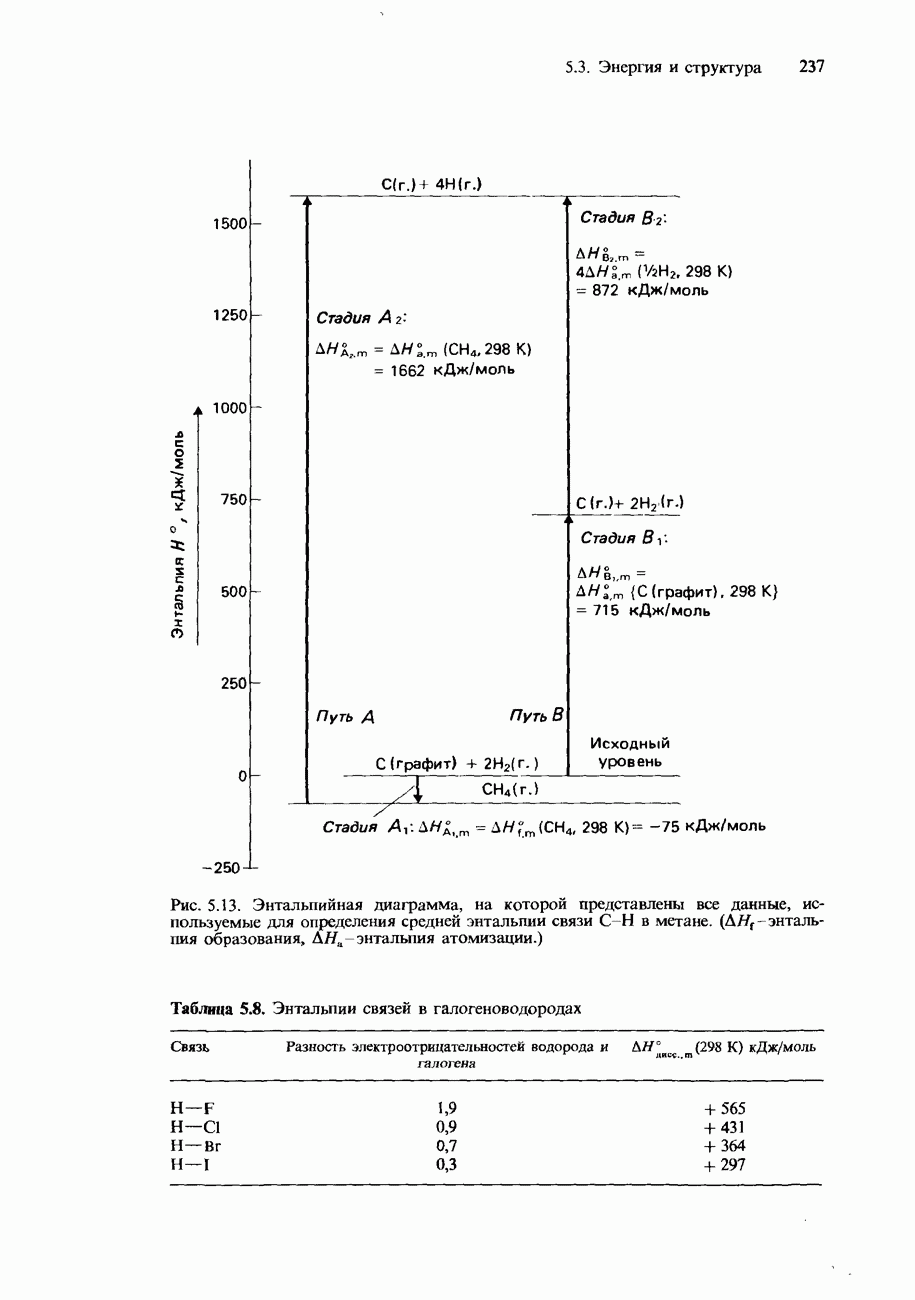
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
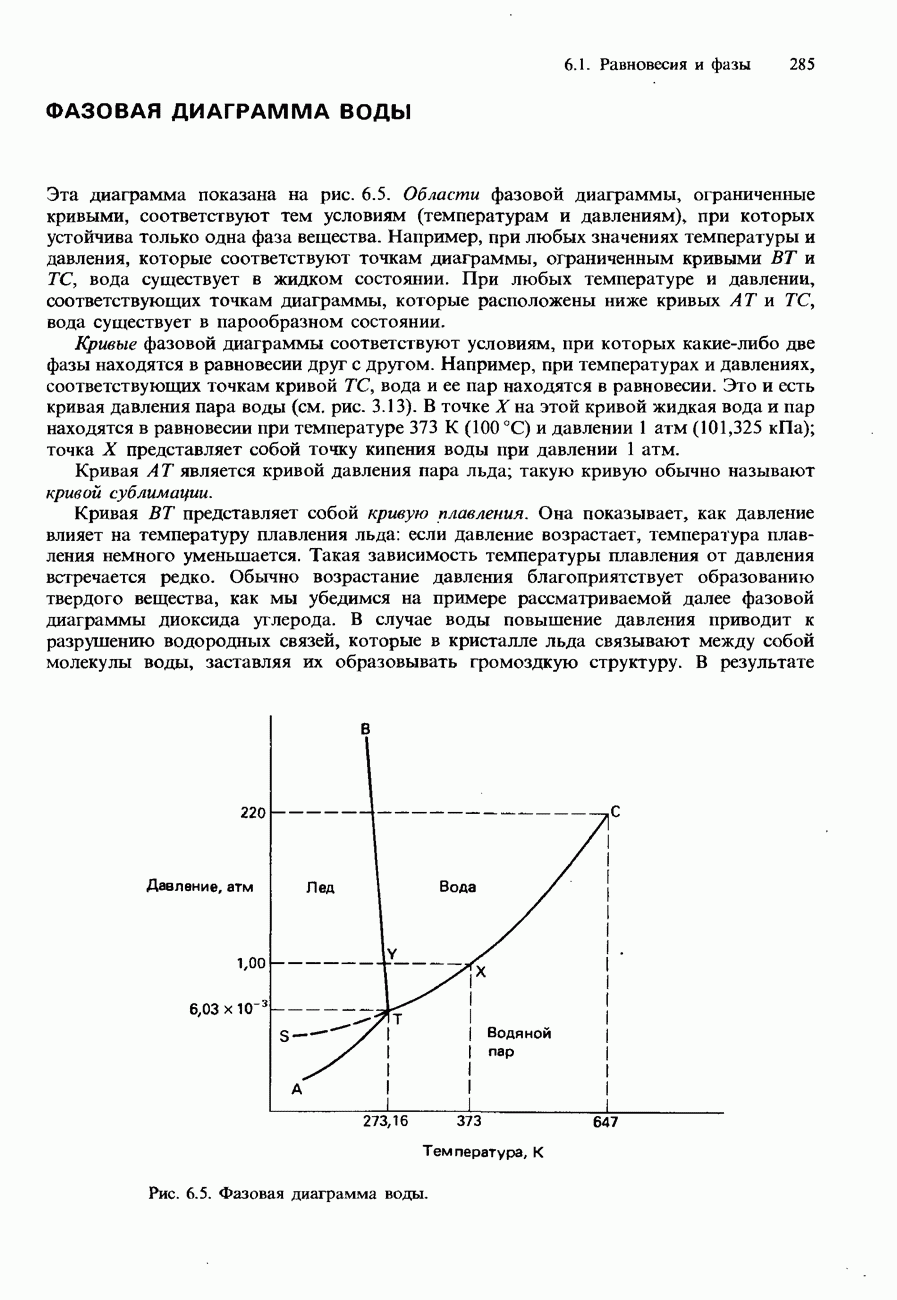
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
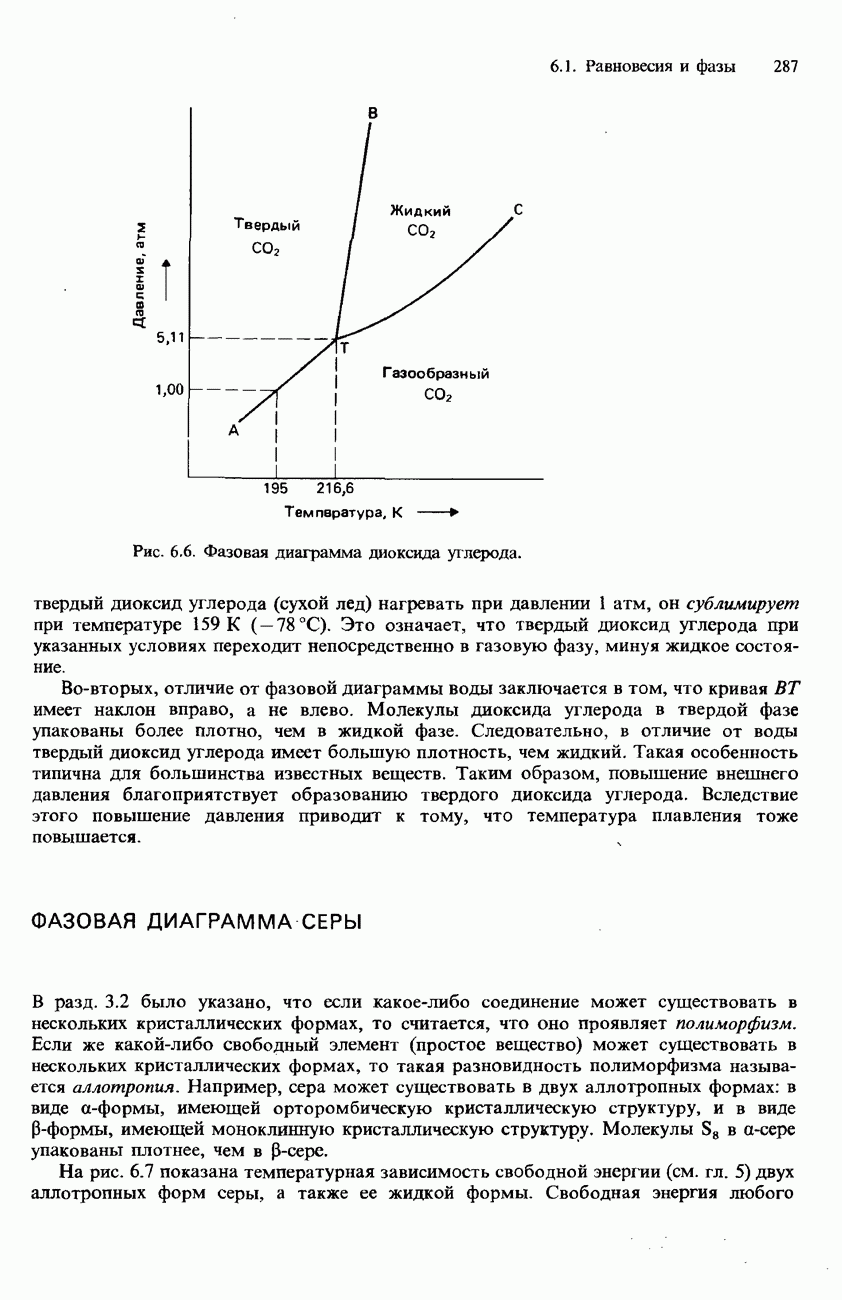
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
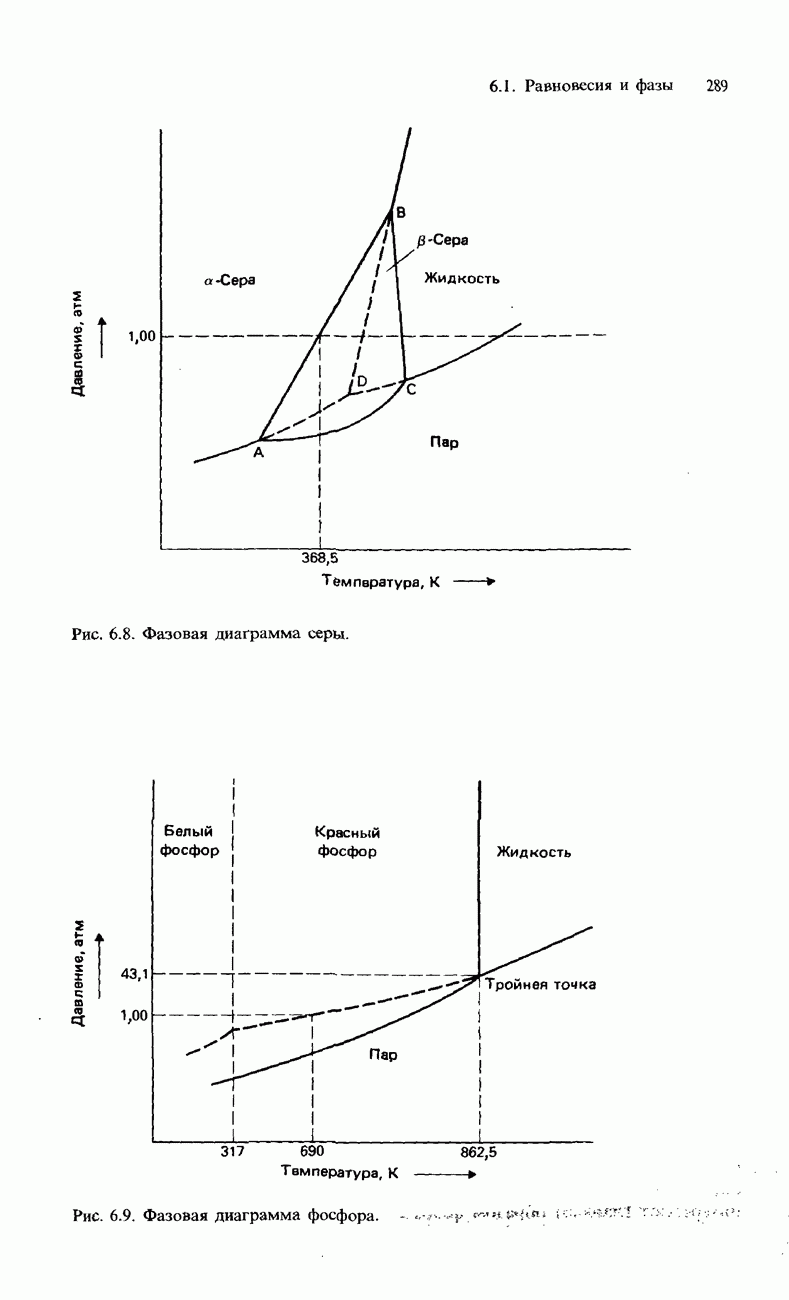
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
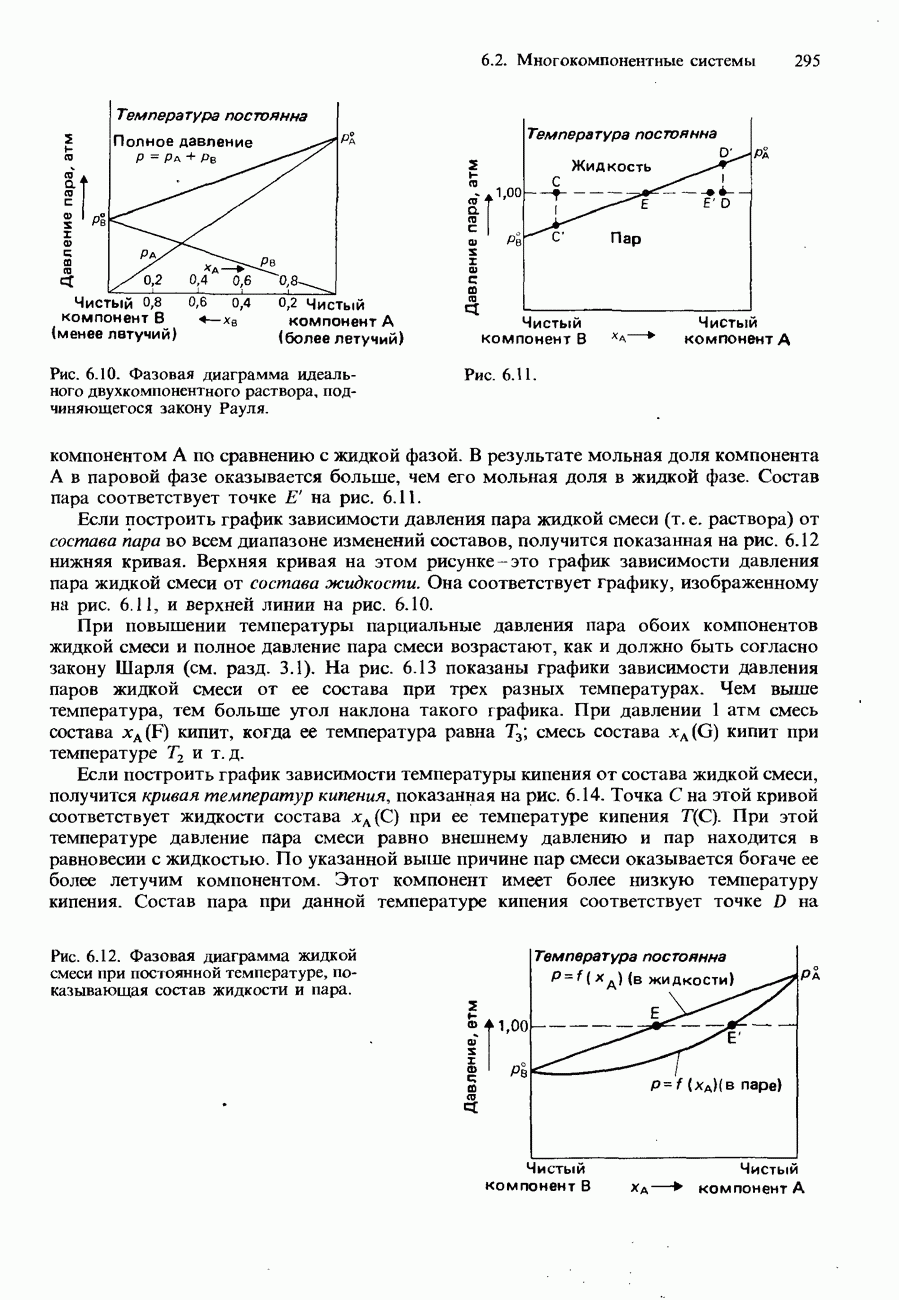
- Фазовые диаграммы полностью смешивающихся жидкостей
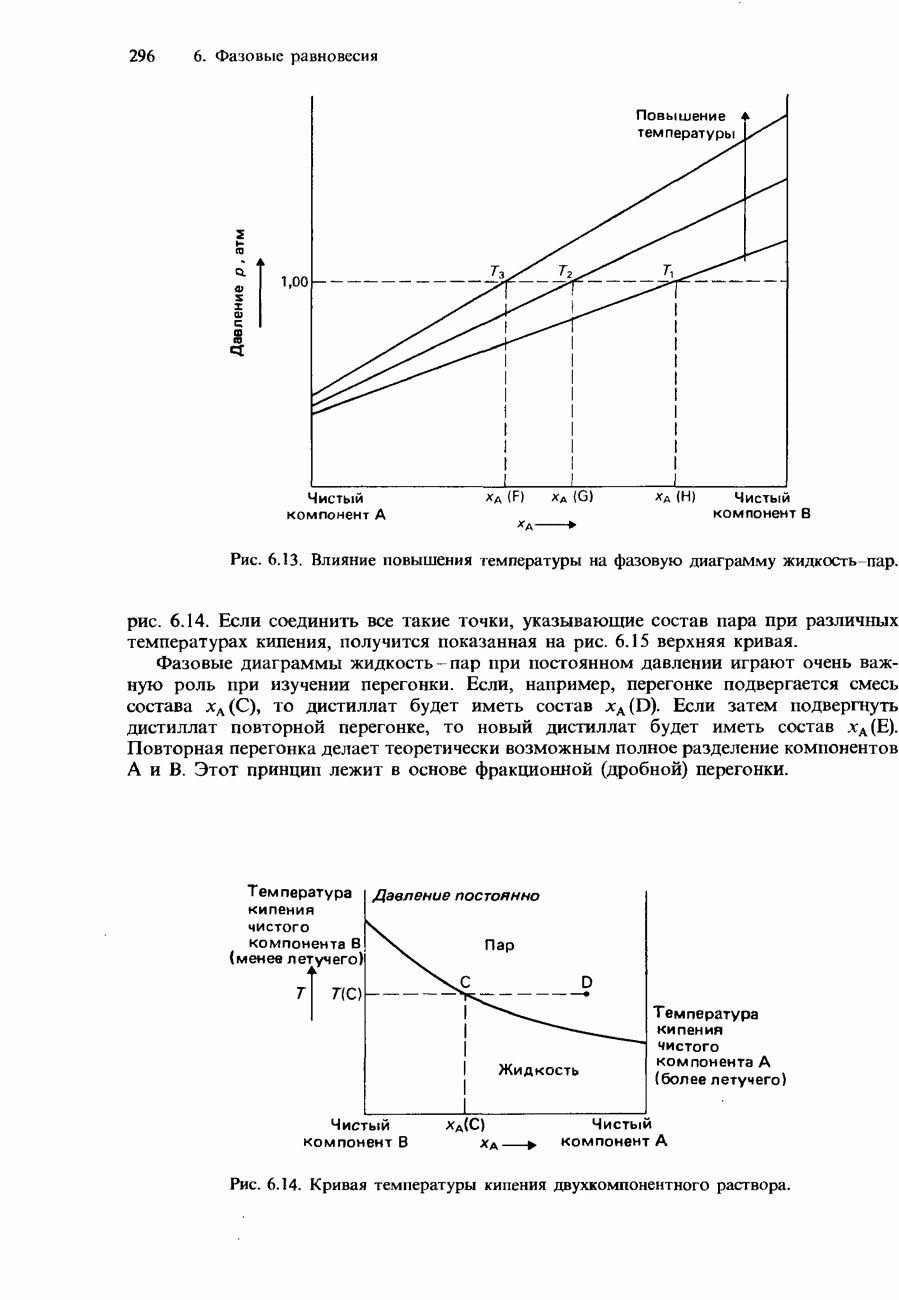
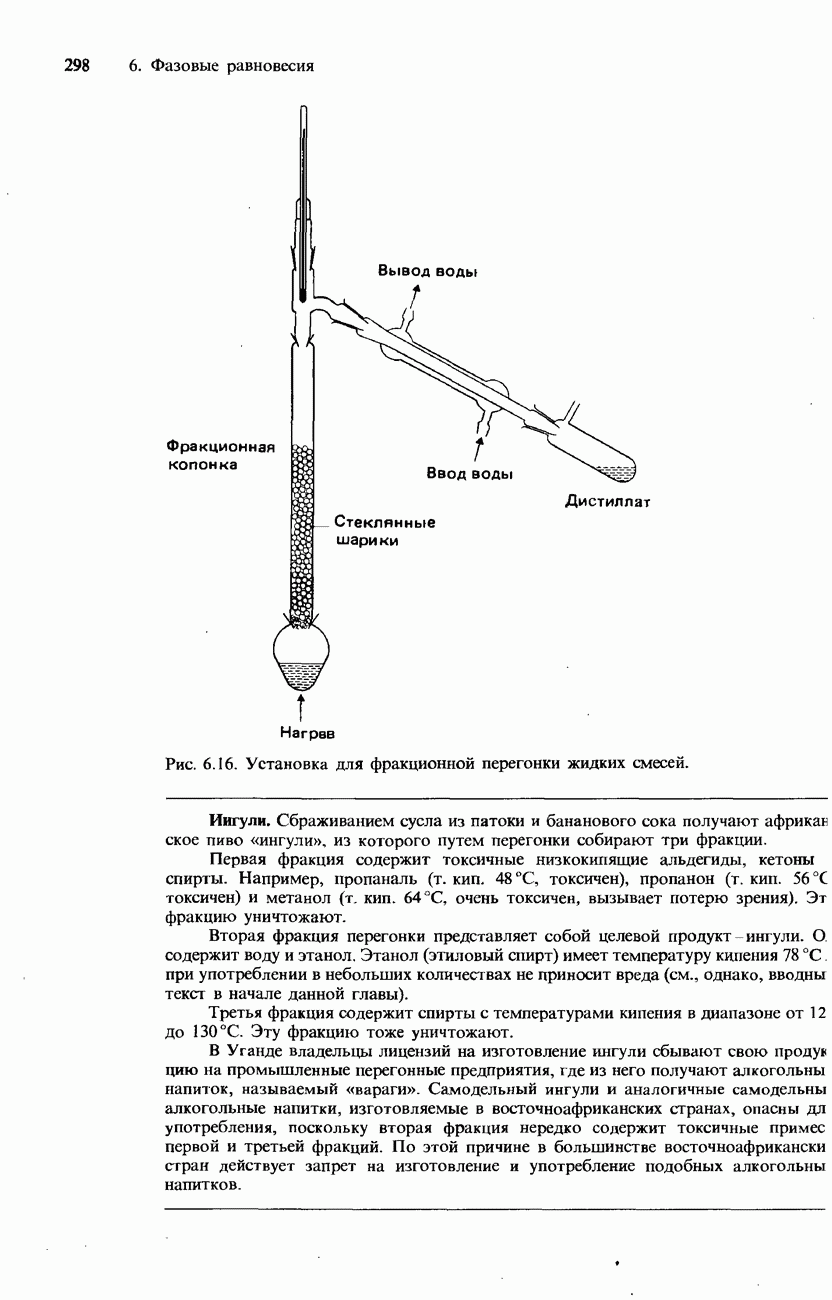
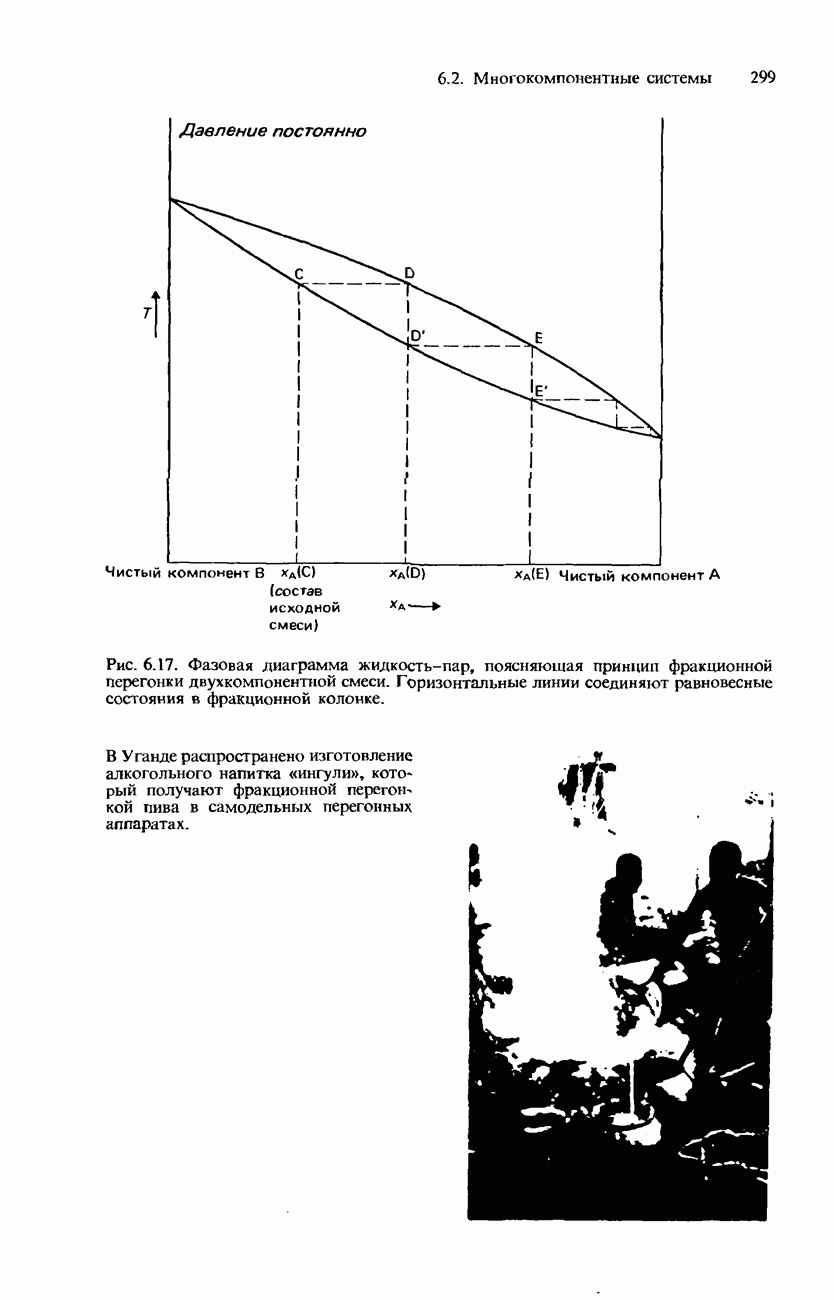
- Фракционная перегонка
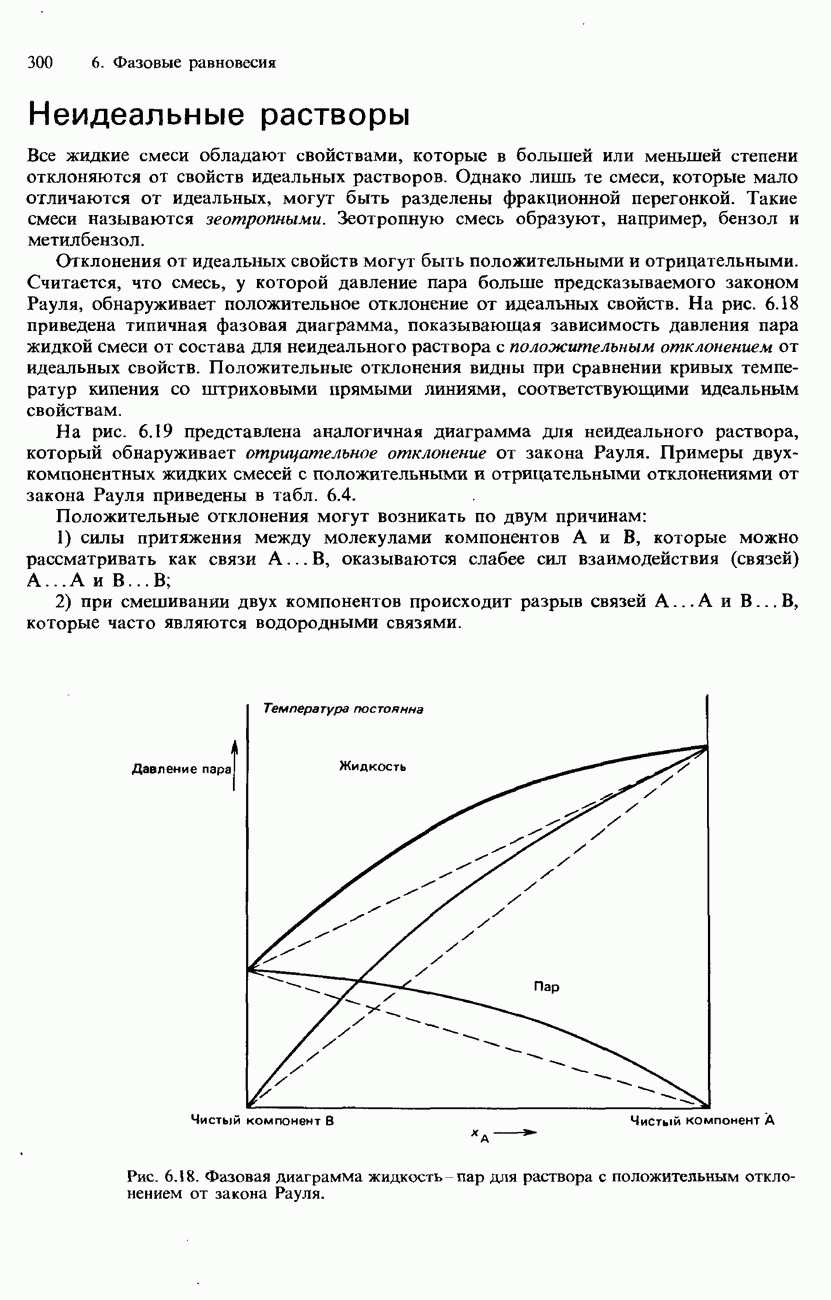
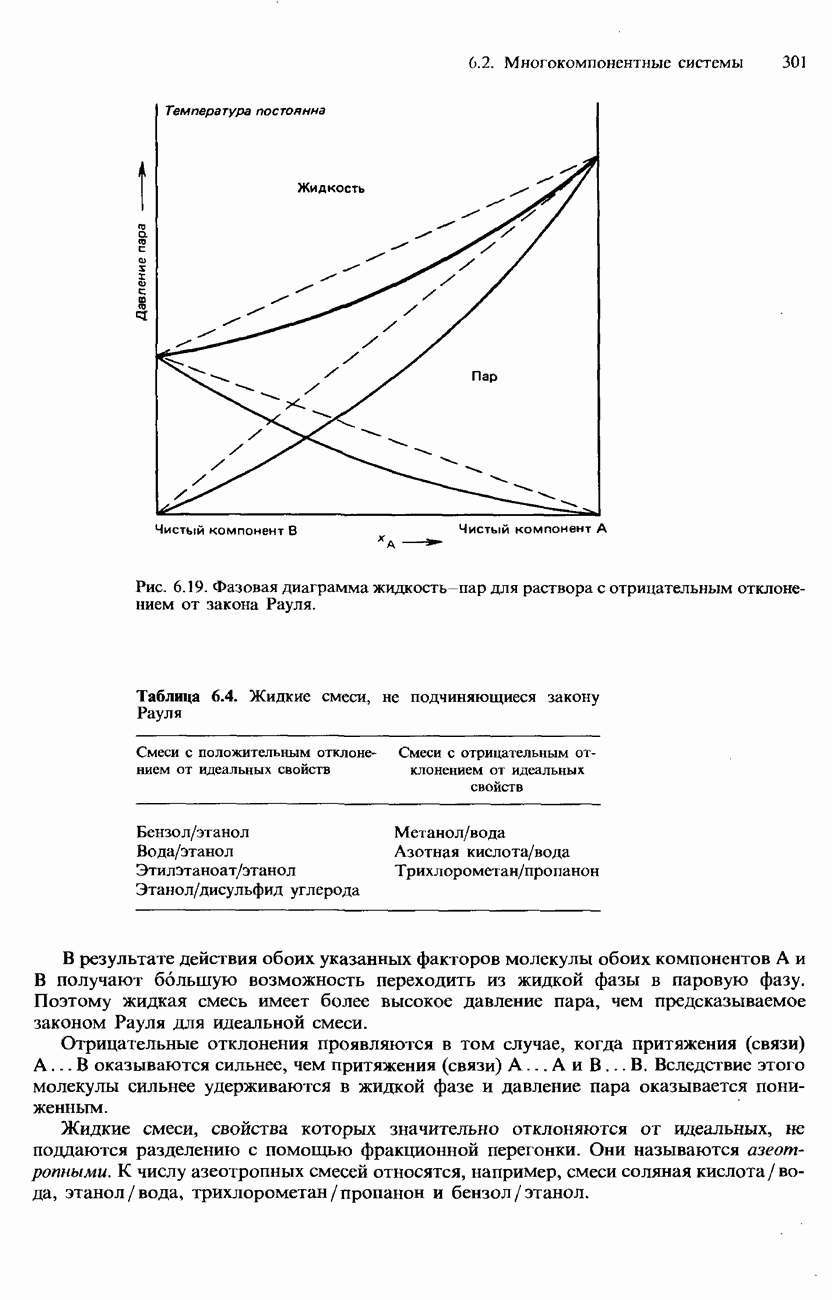
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
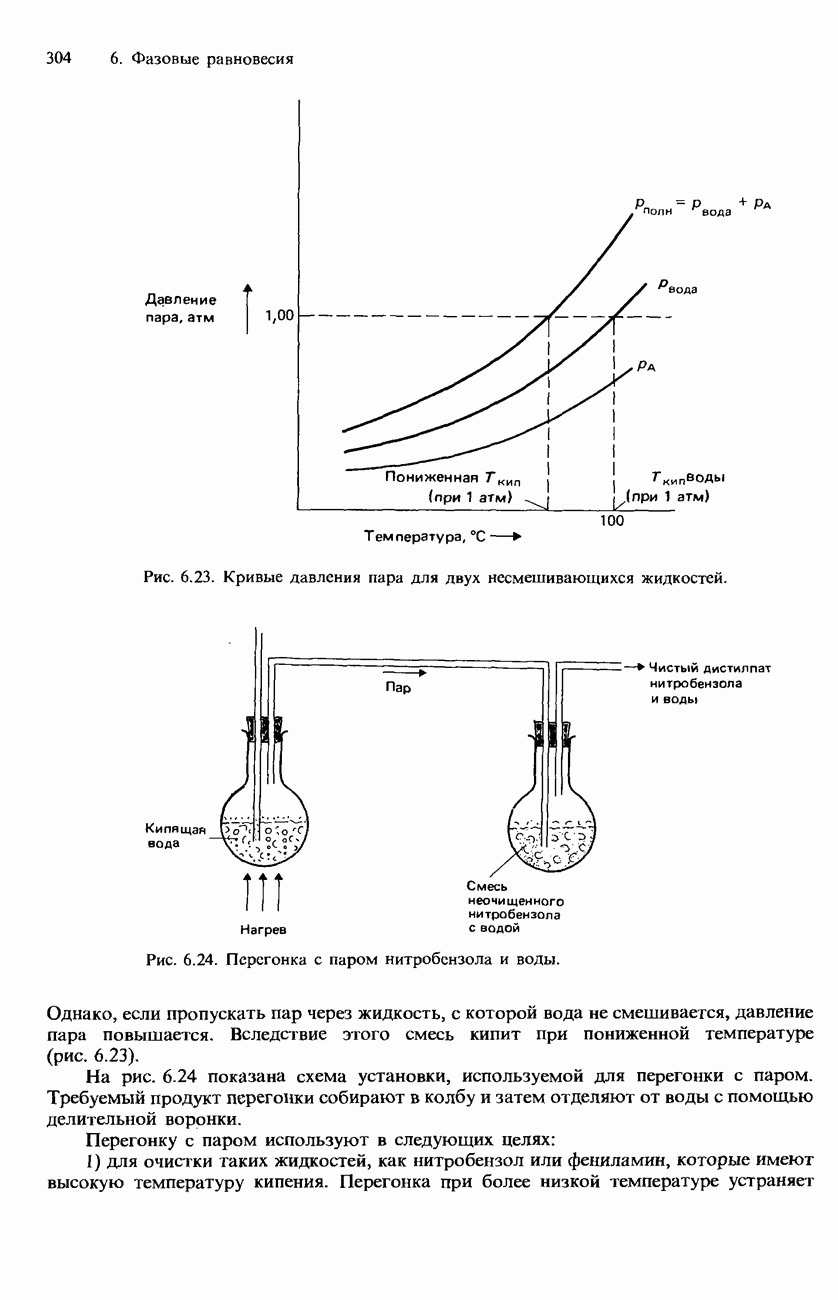
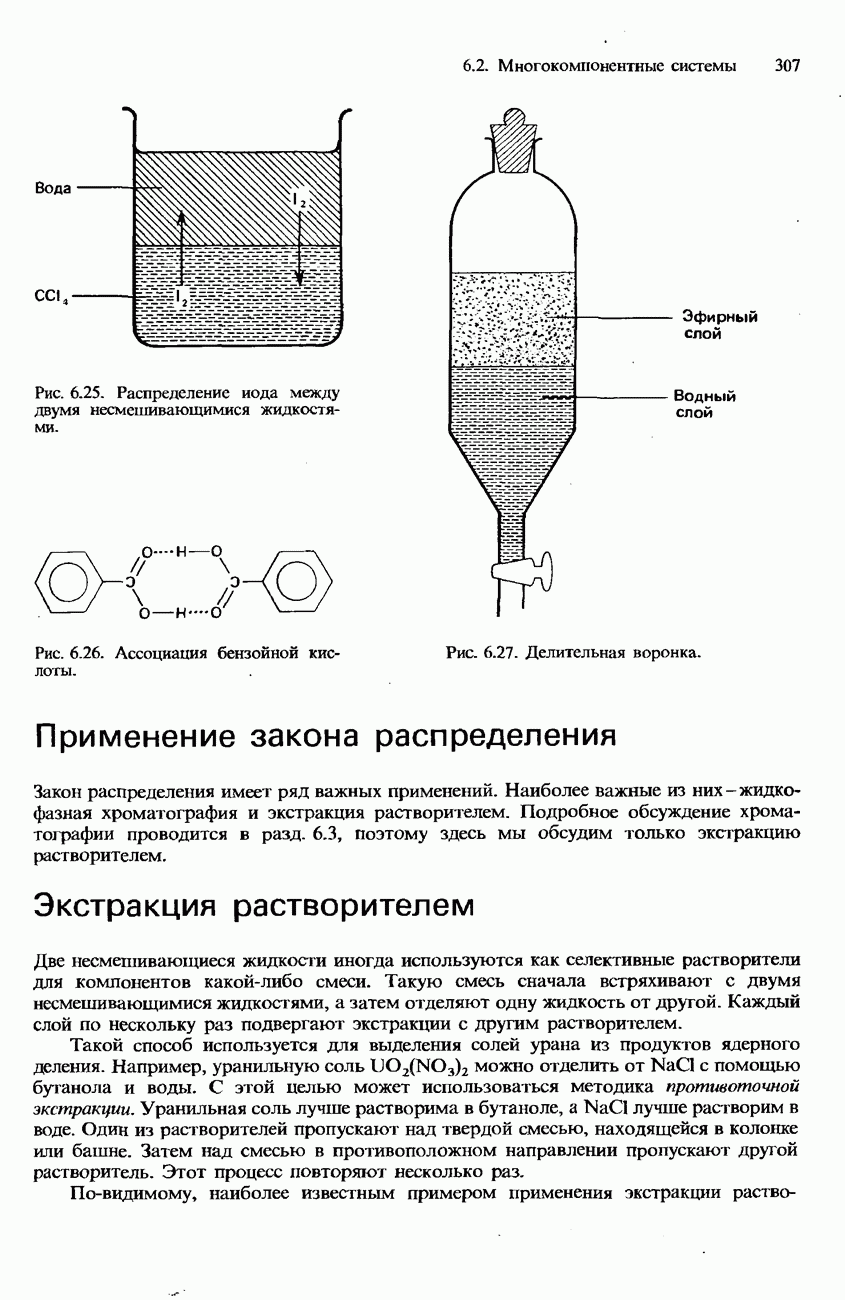
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
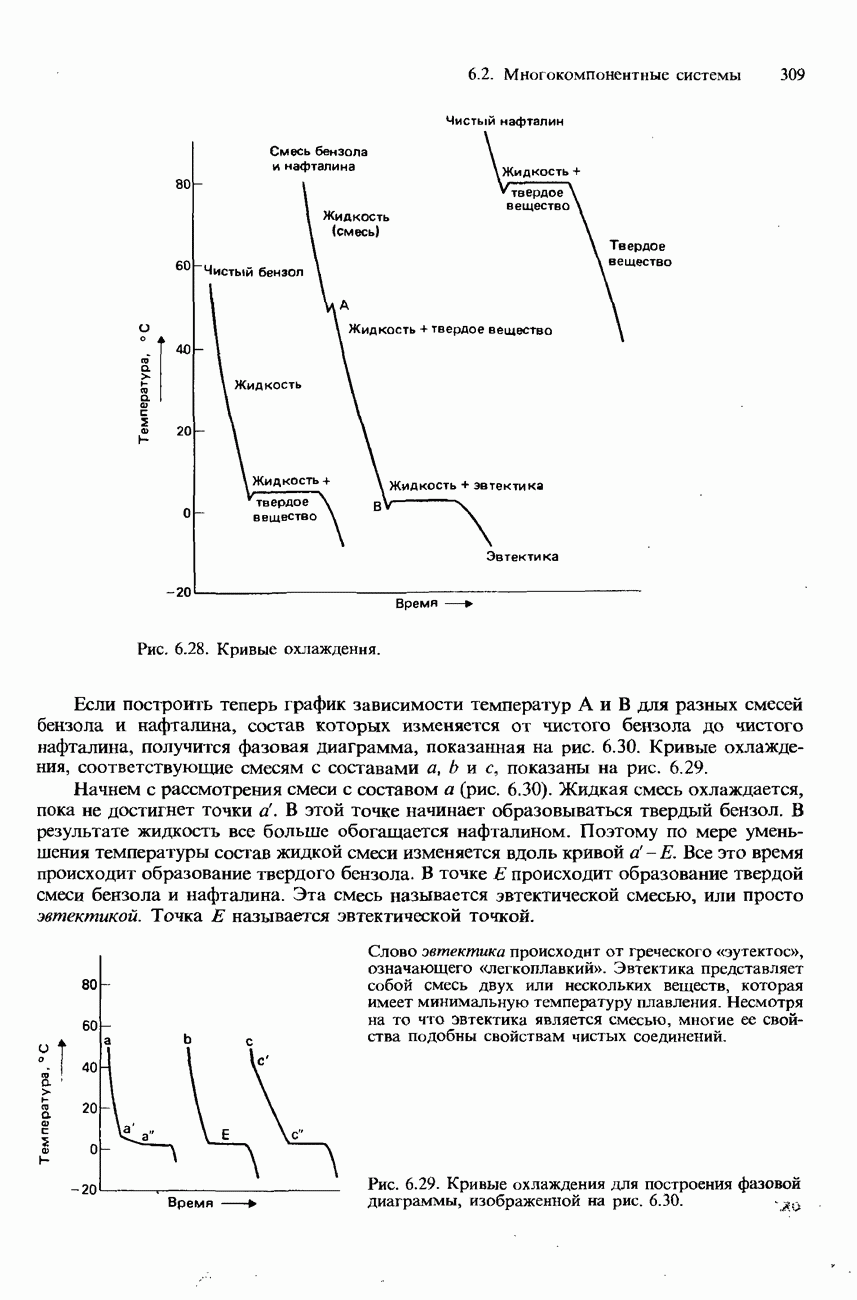
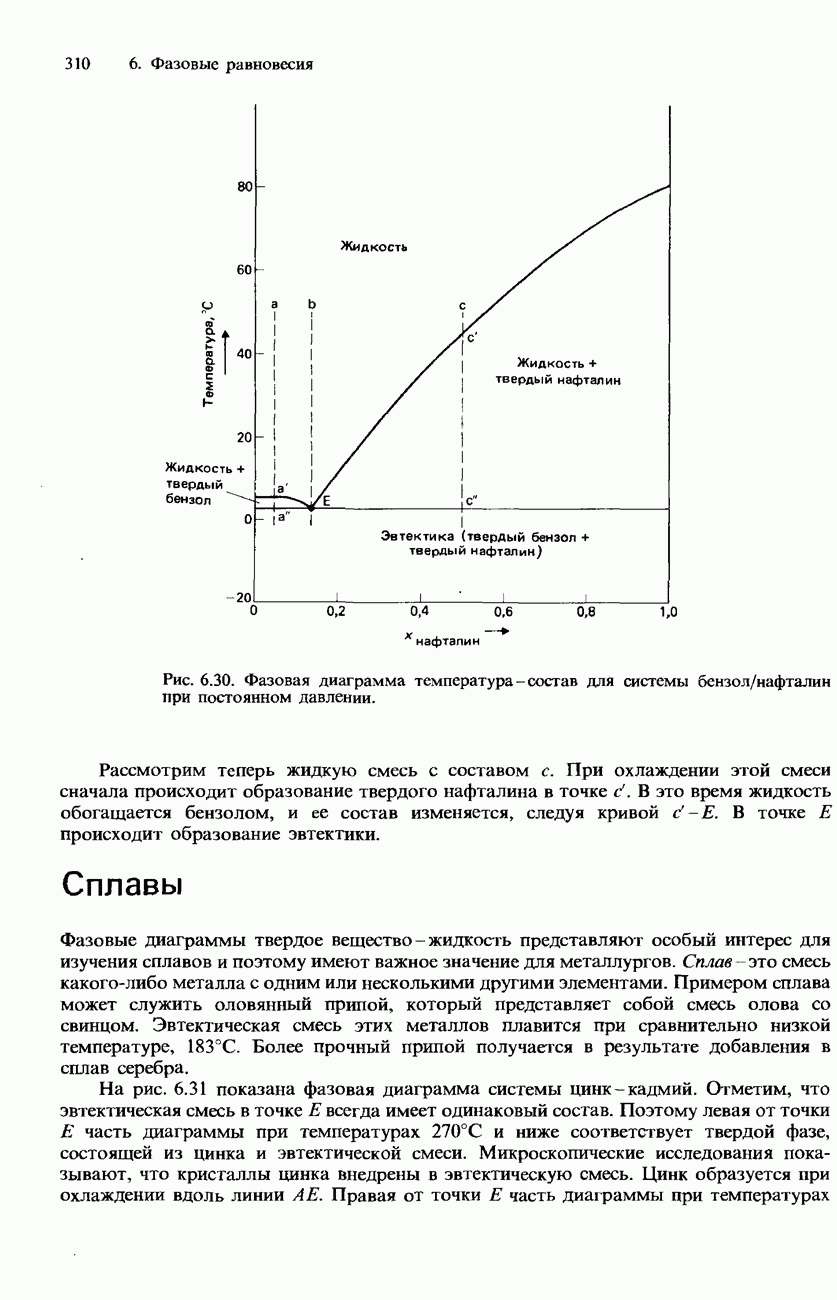
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
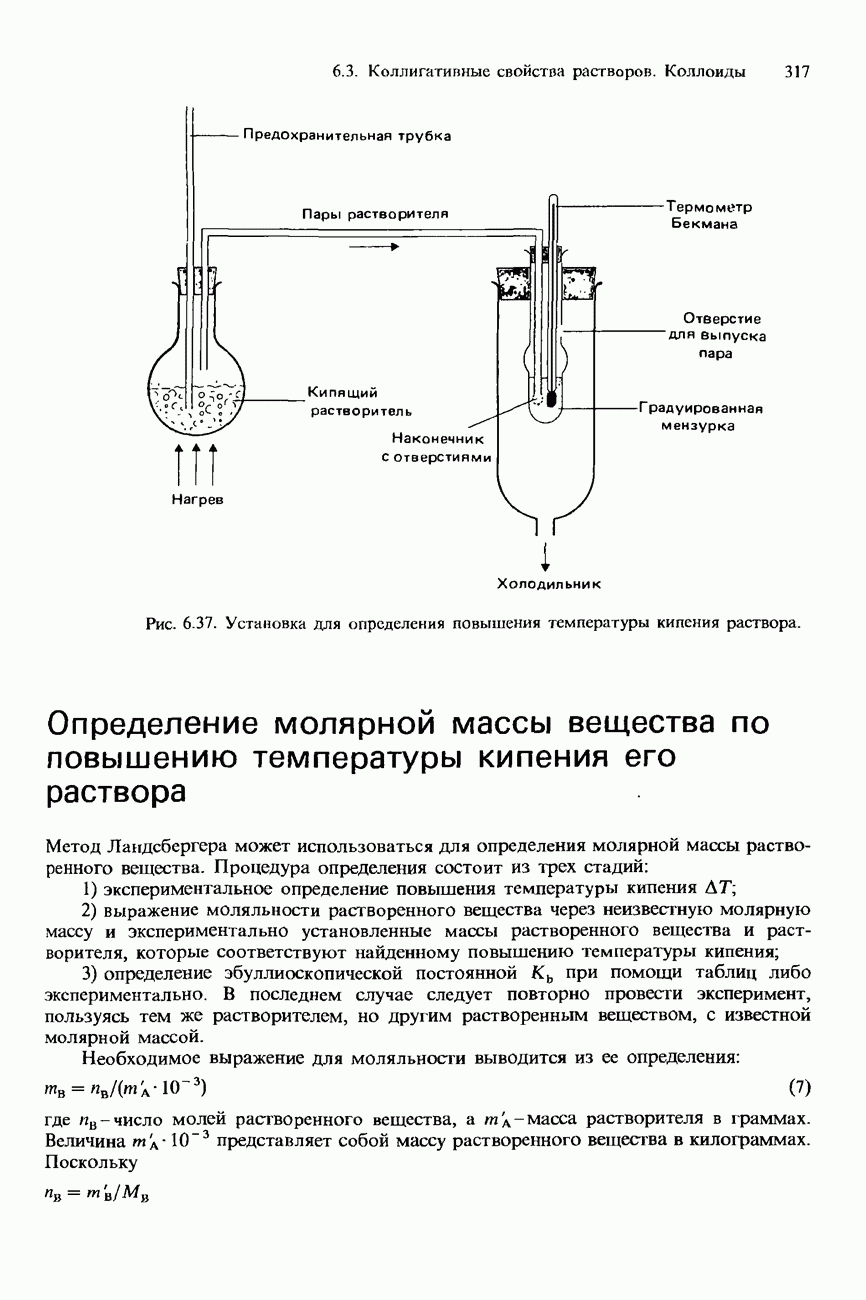
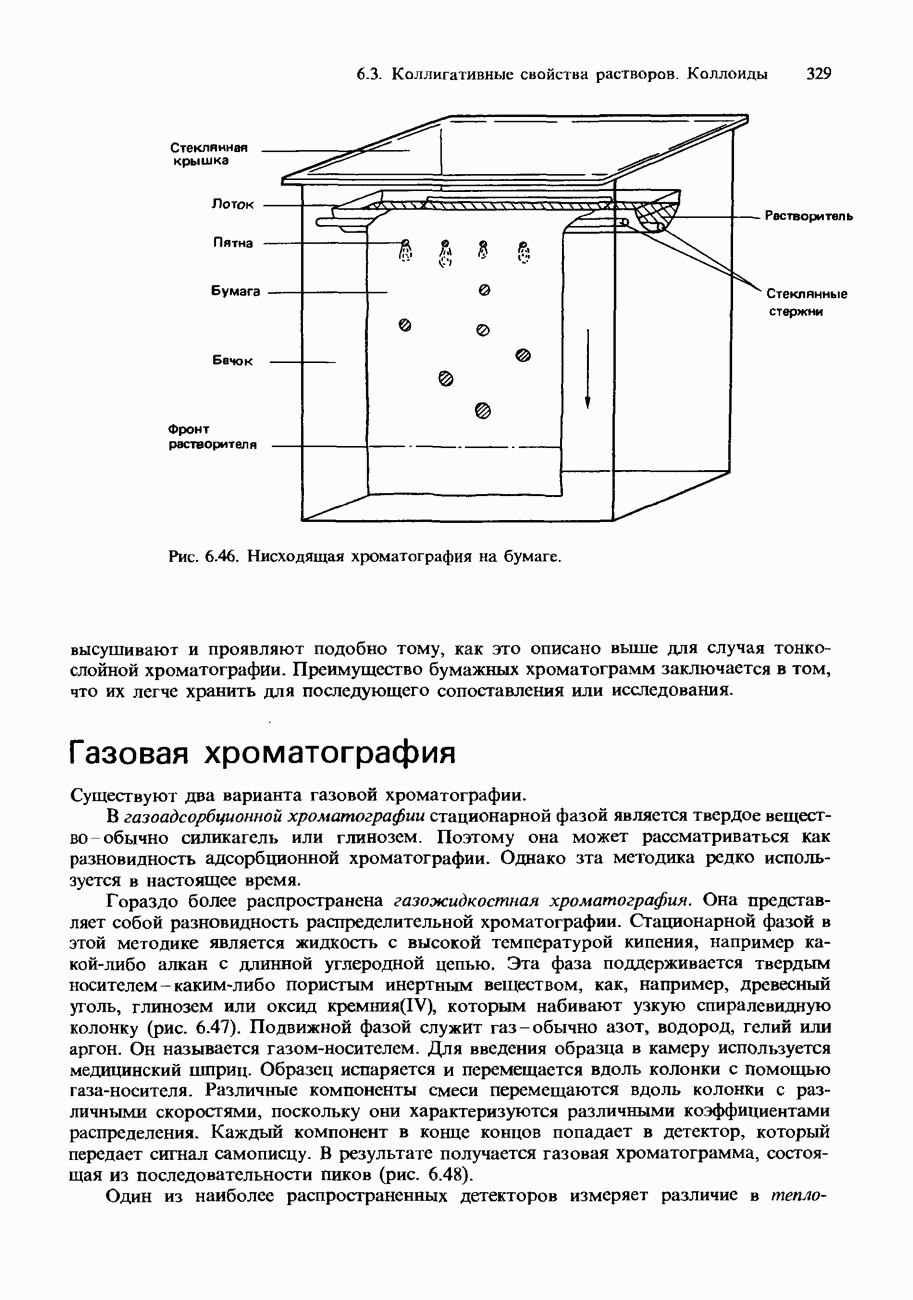
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
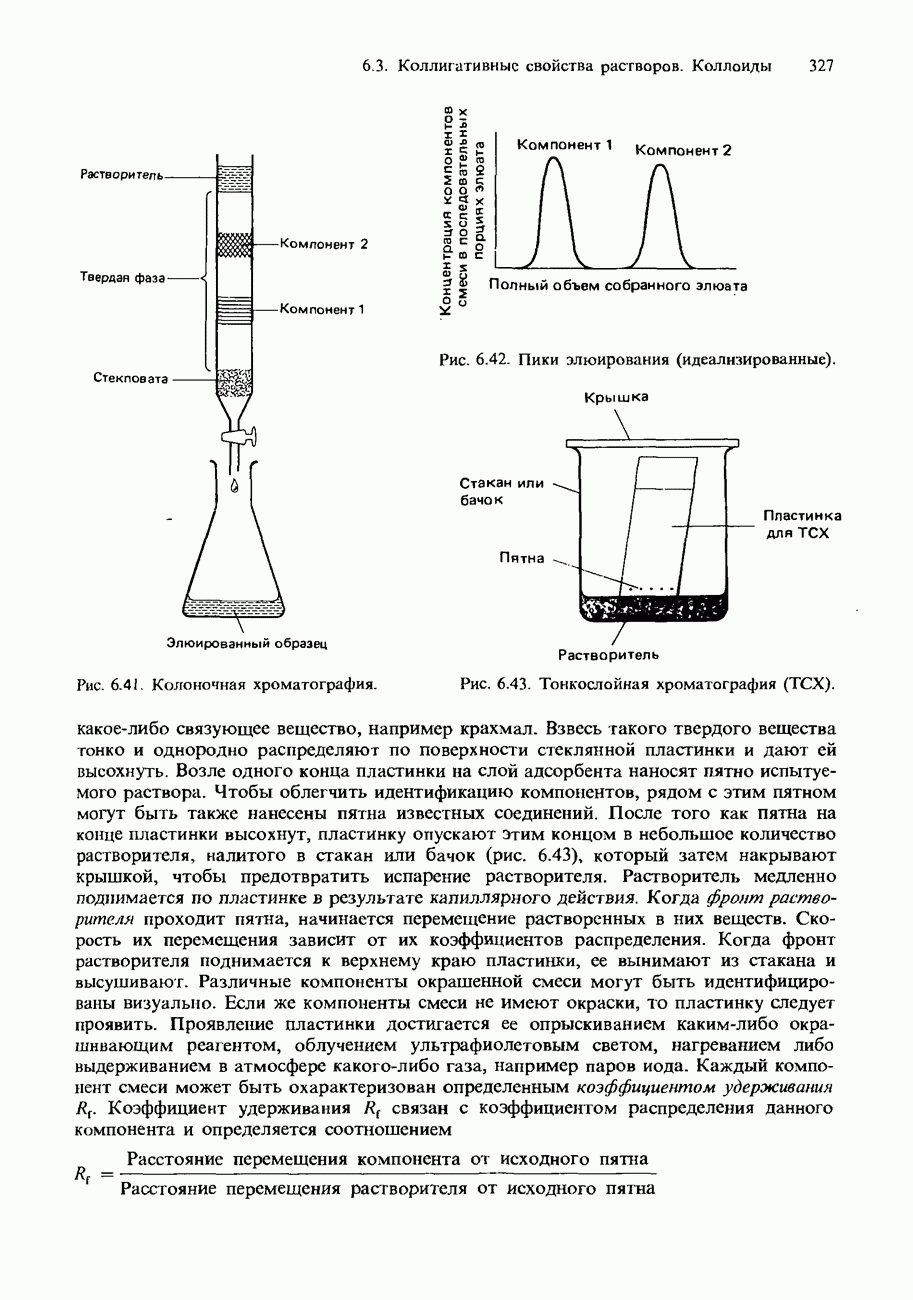
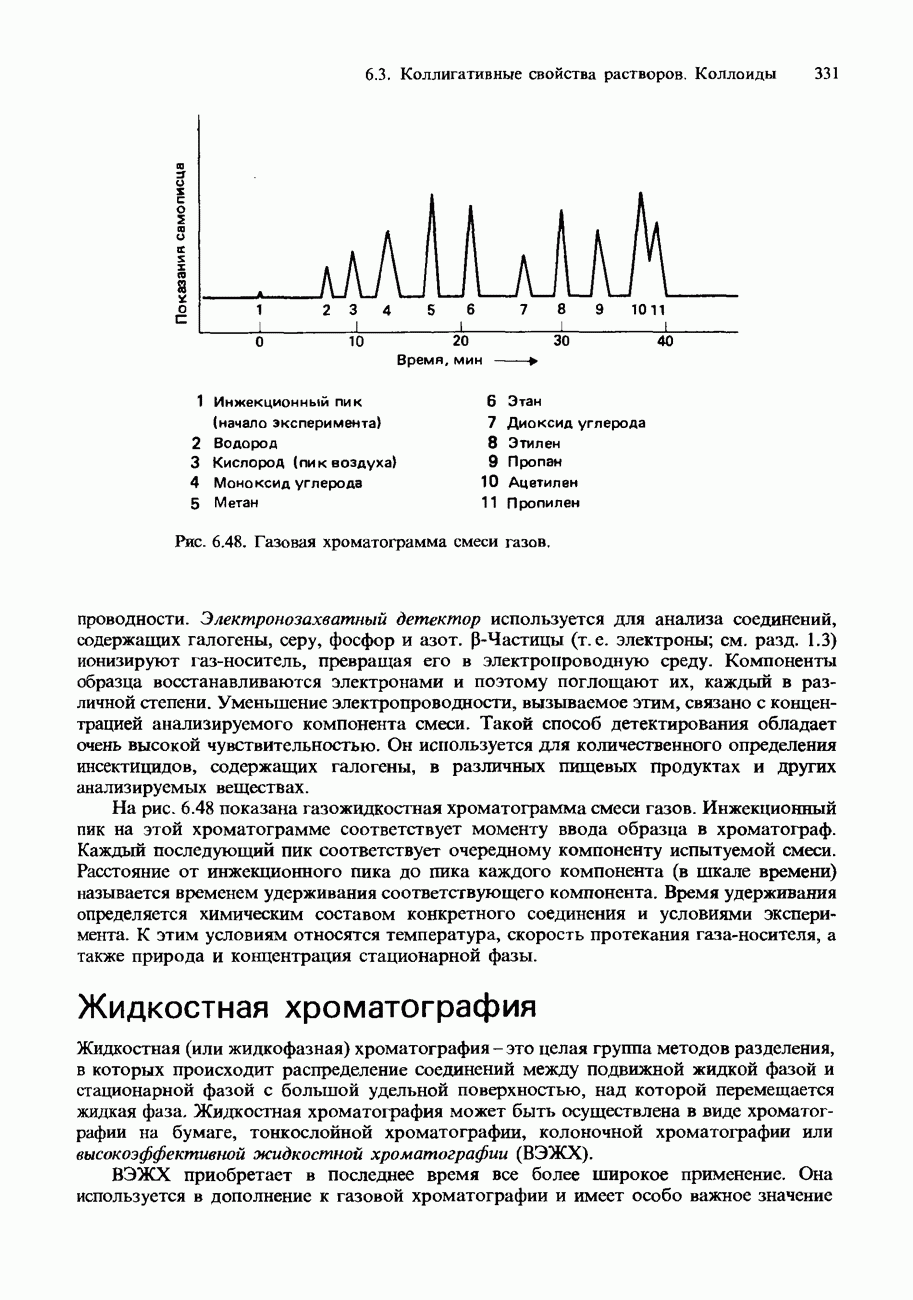
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
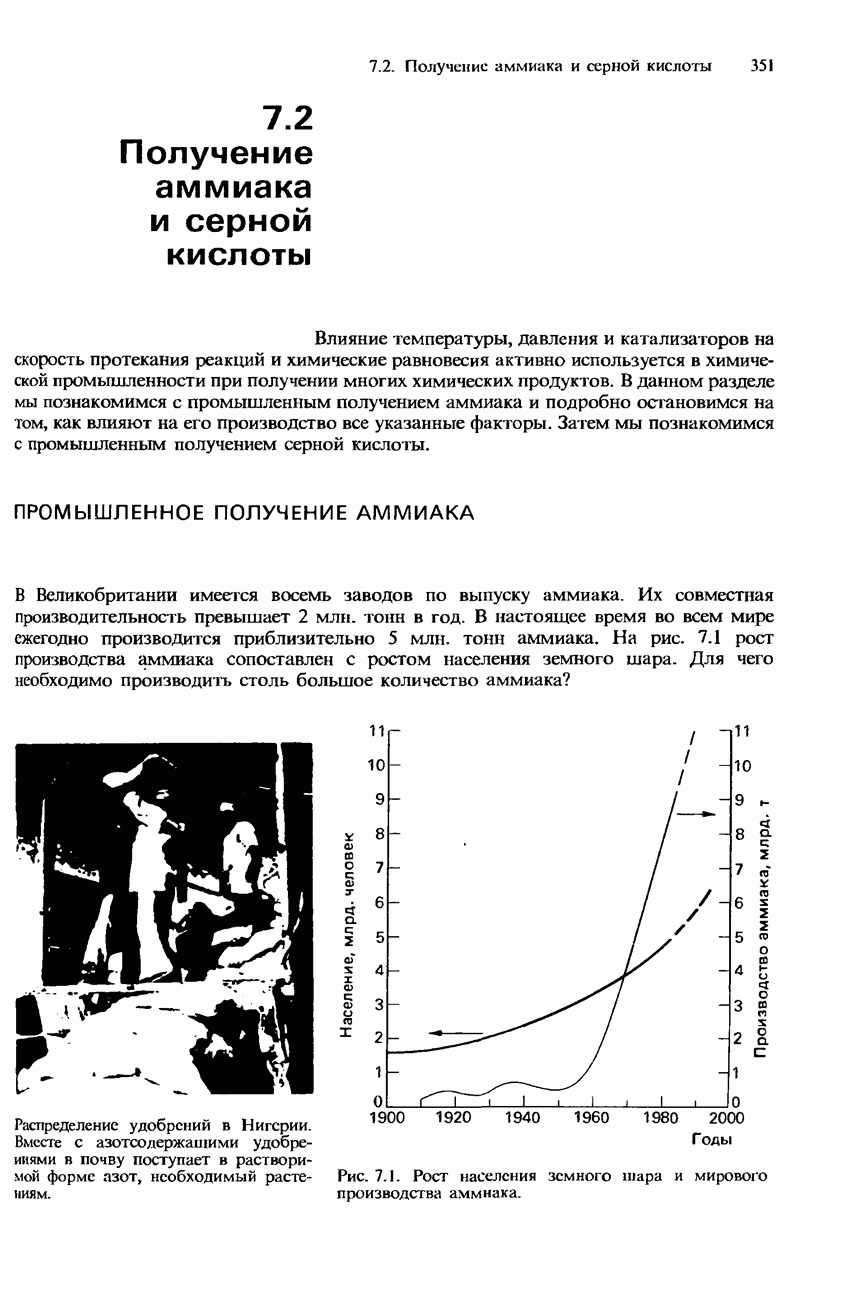
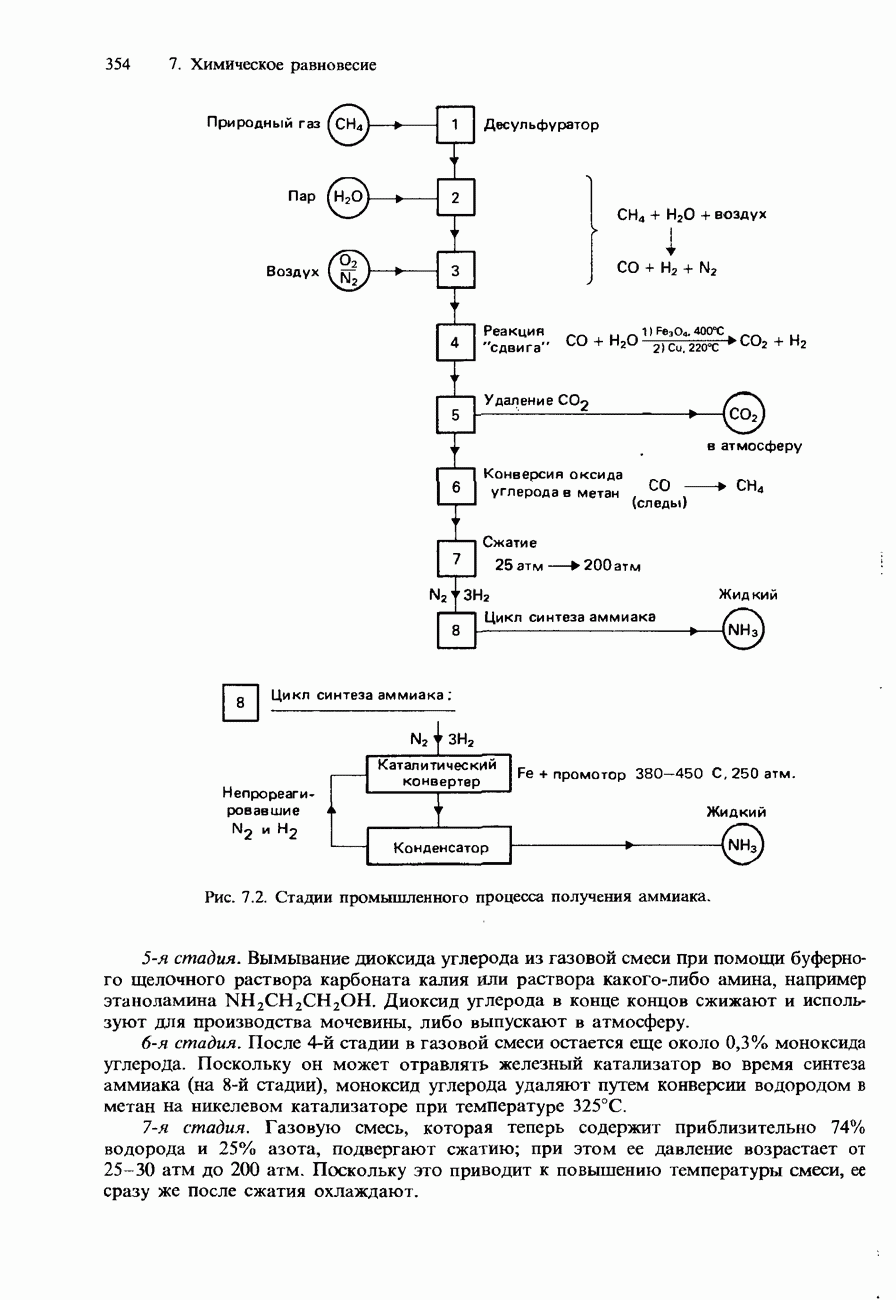
- 7.2. Получение аммиака и серной кислоты
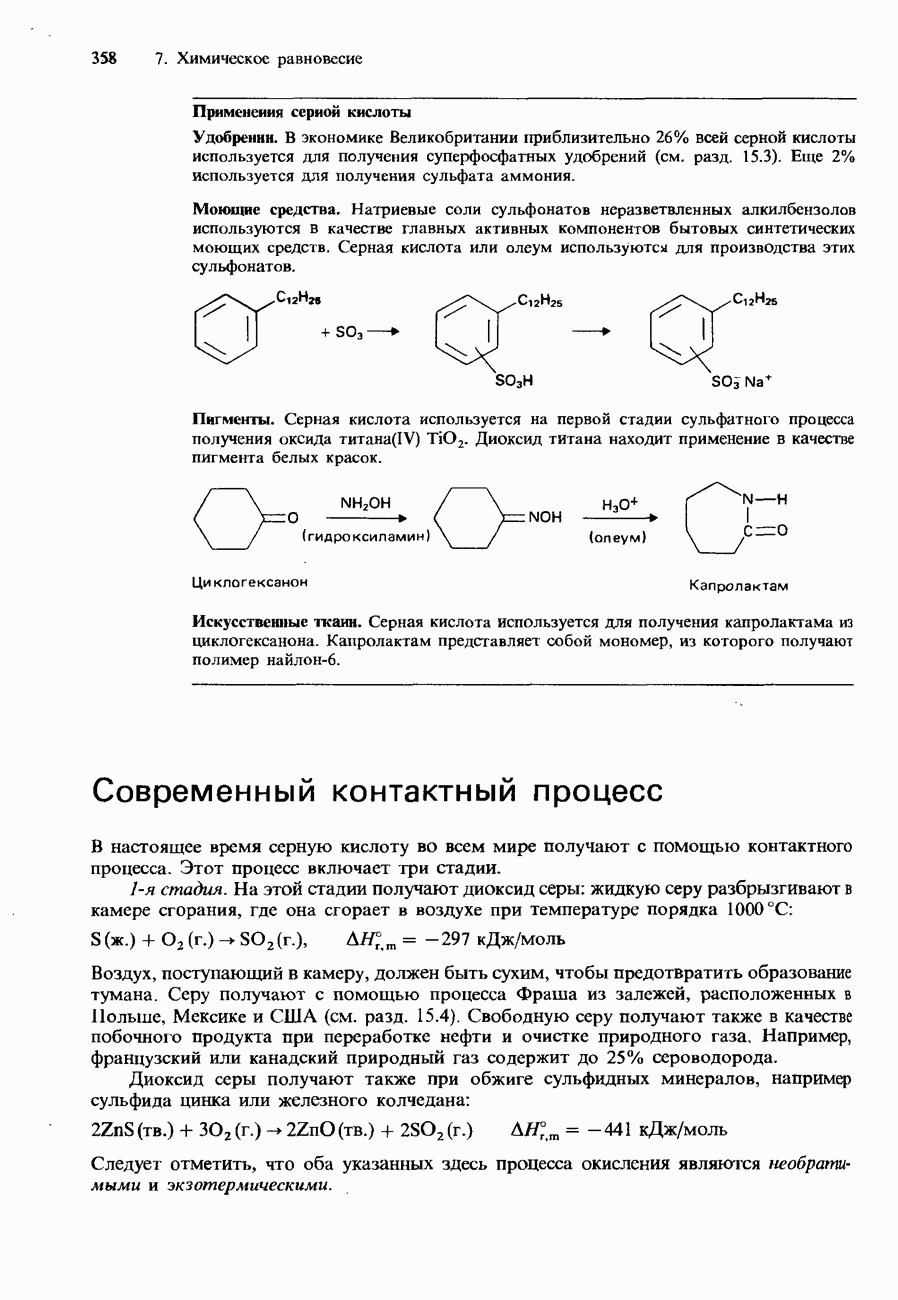
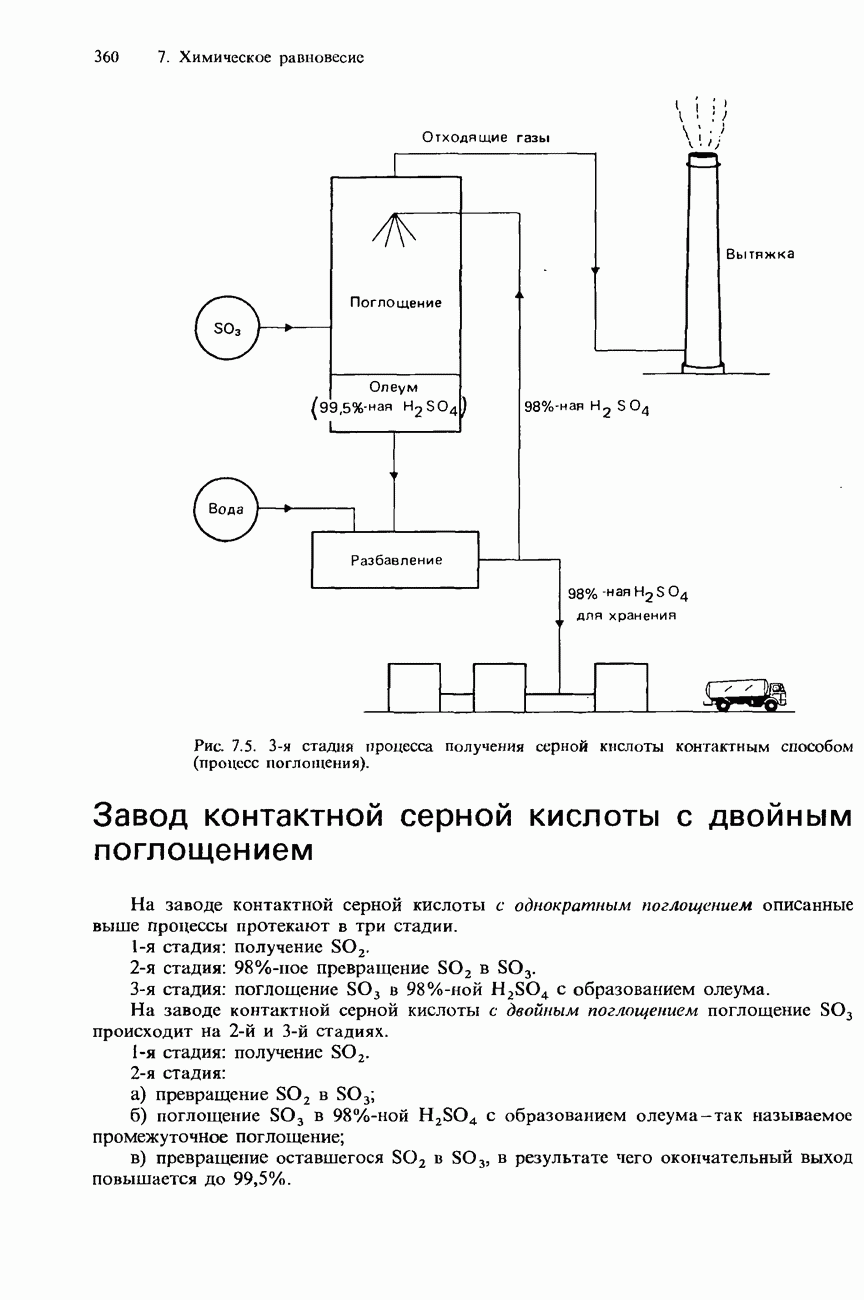
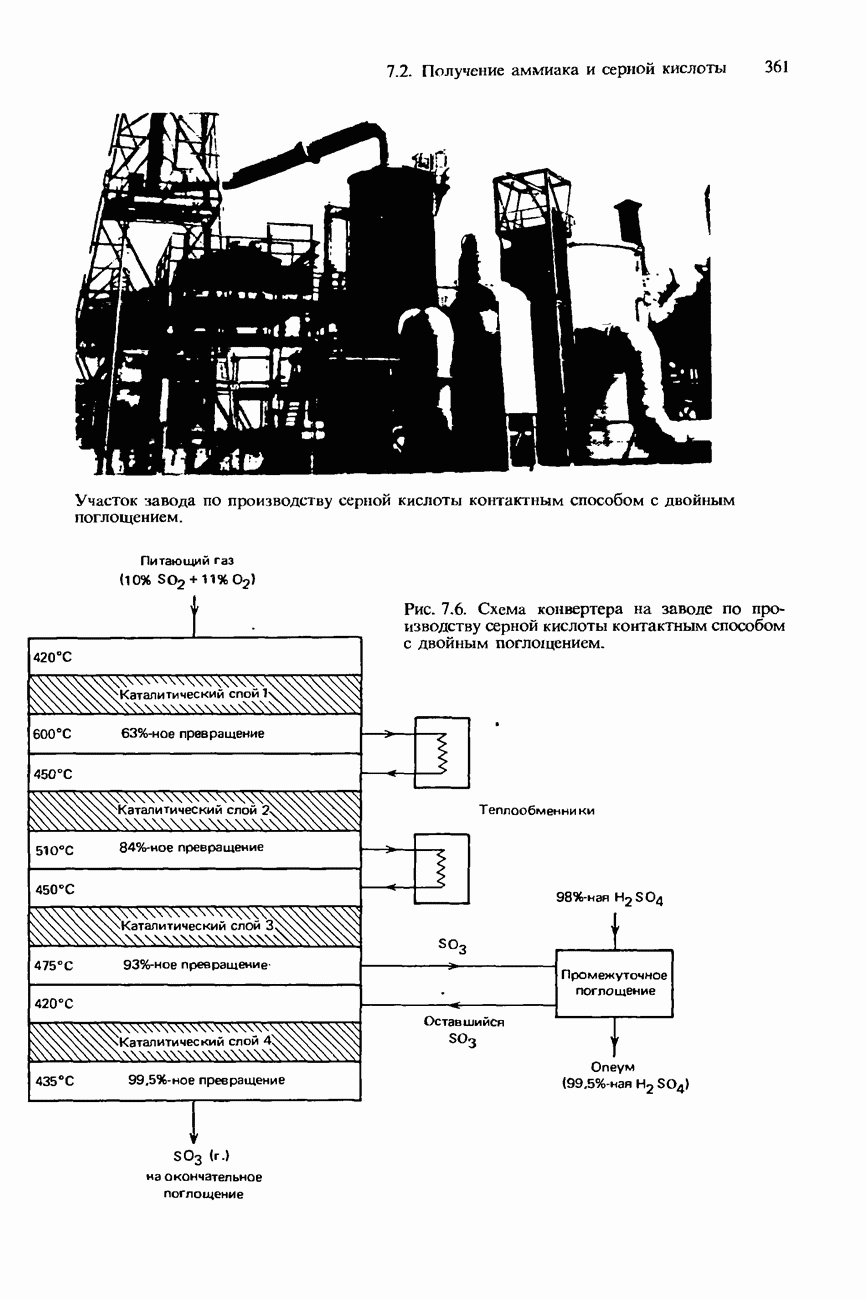
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
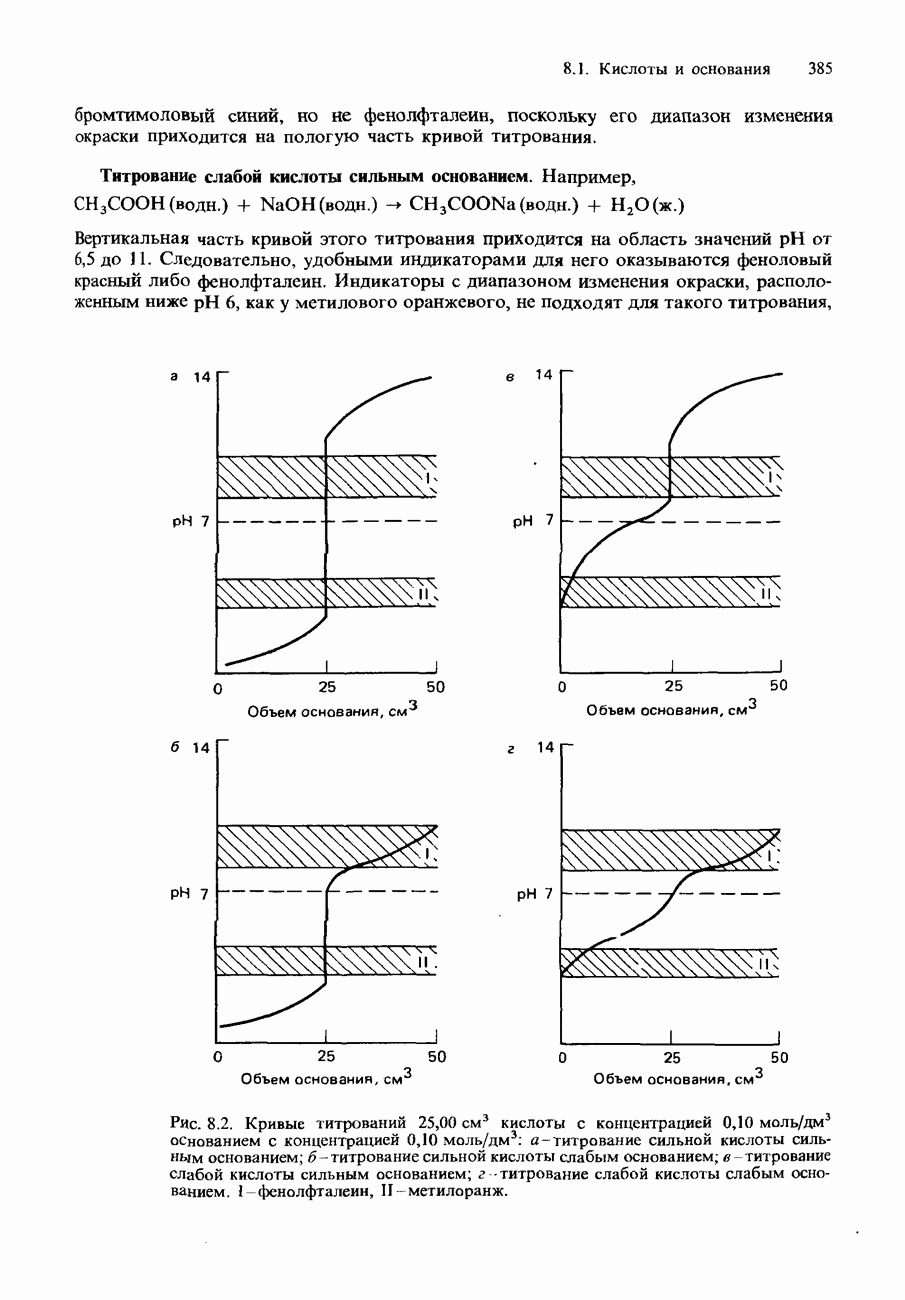
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
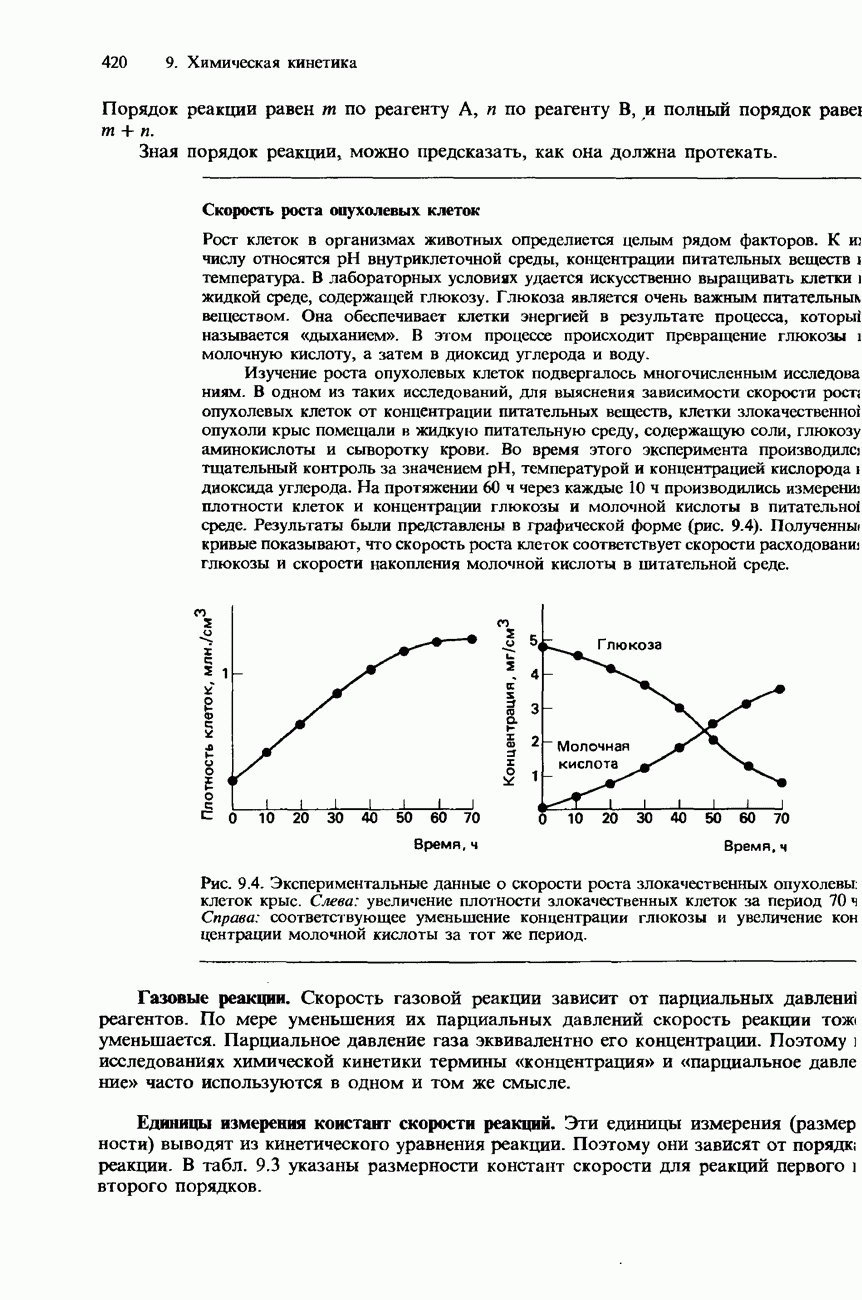
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
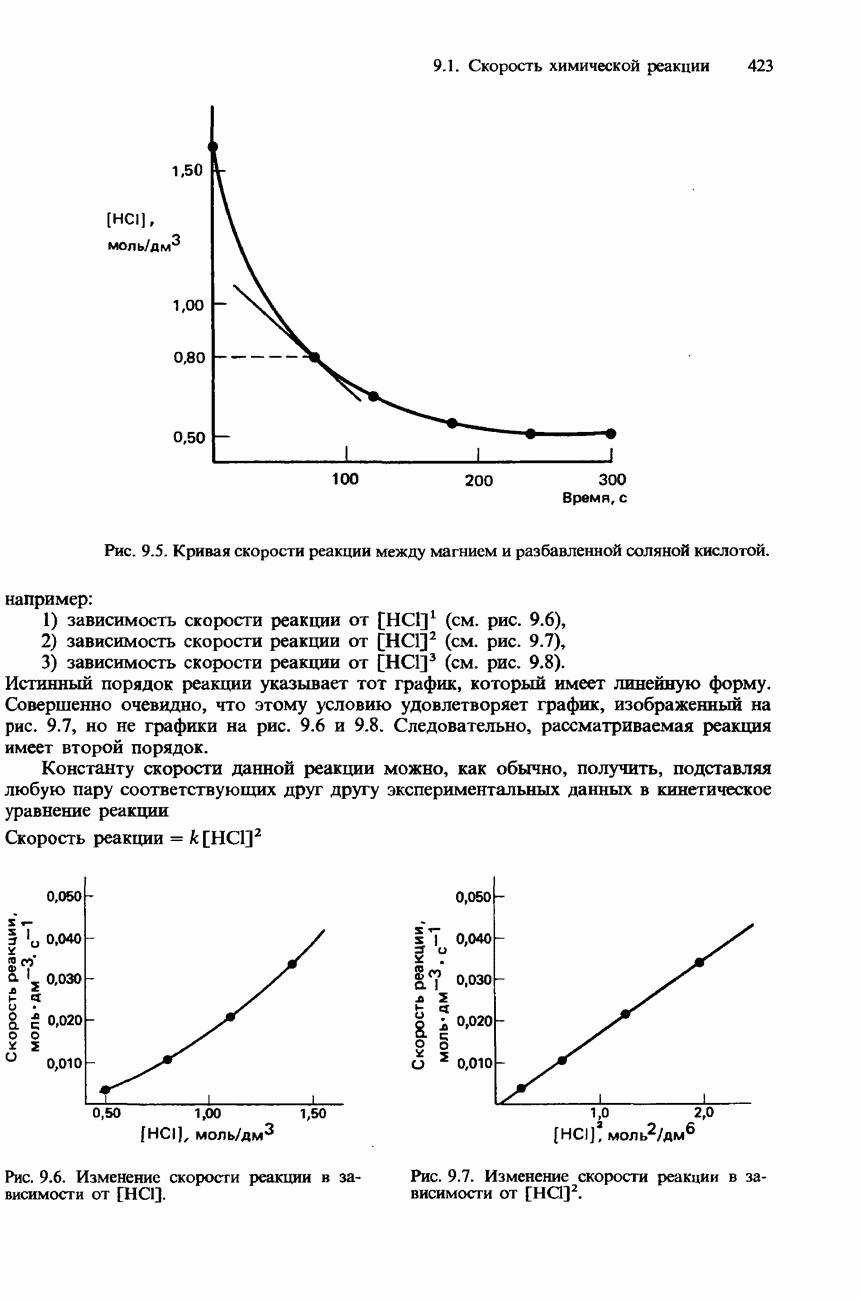
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
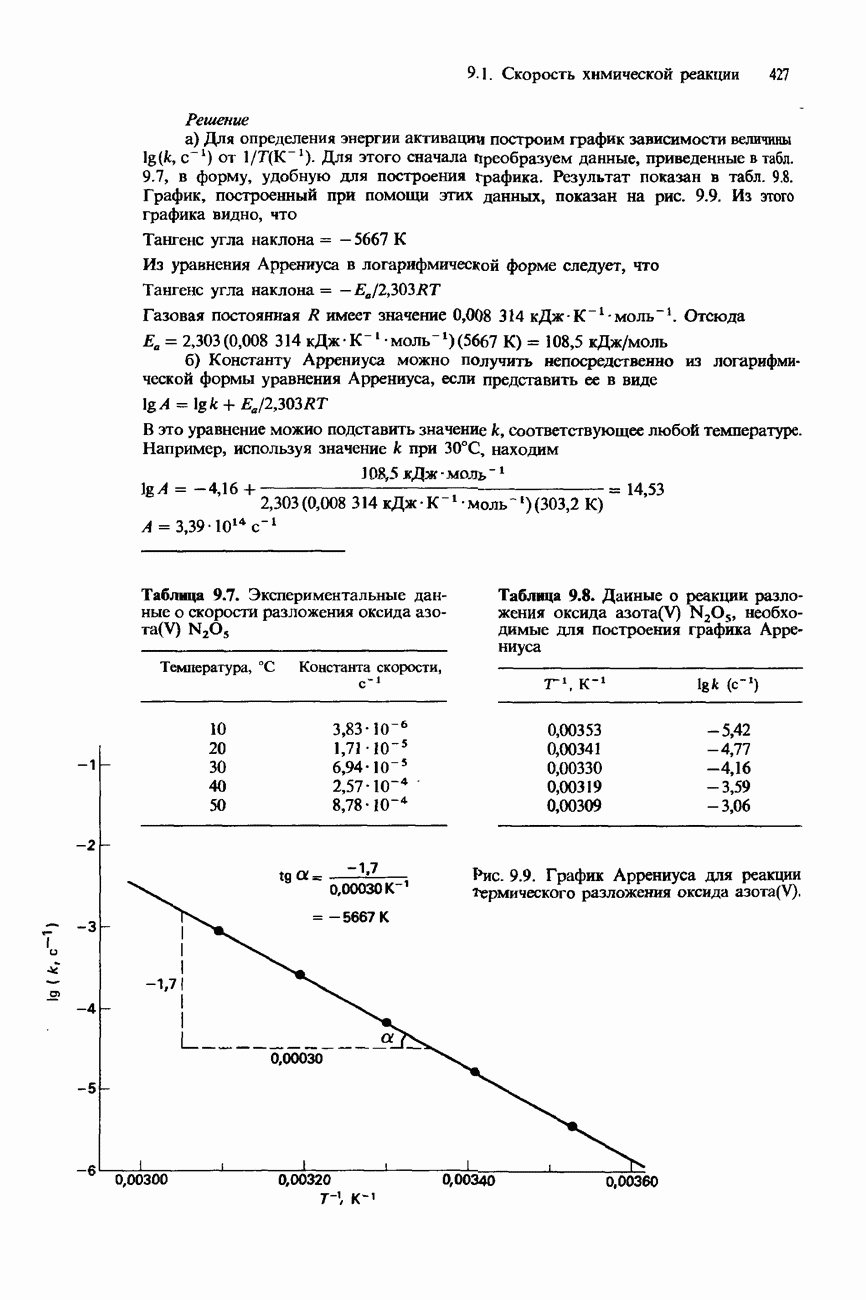
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
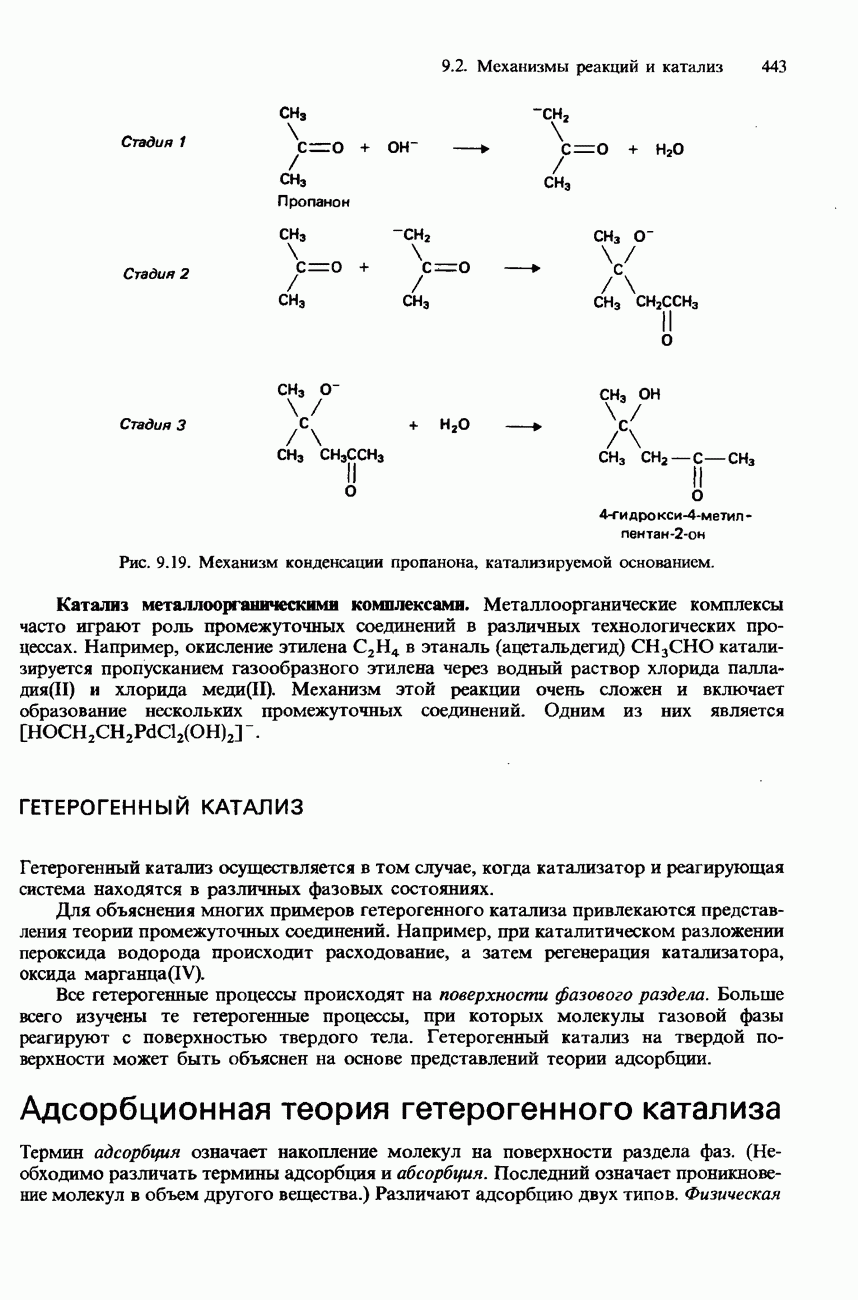
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
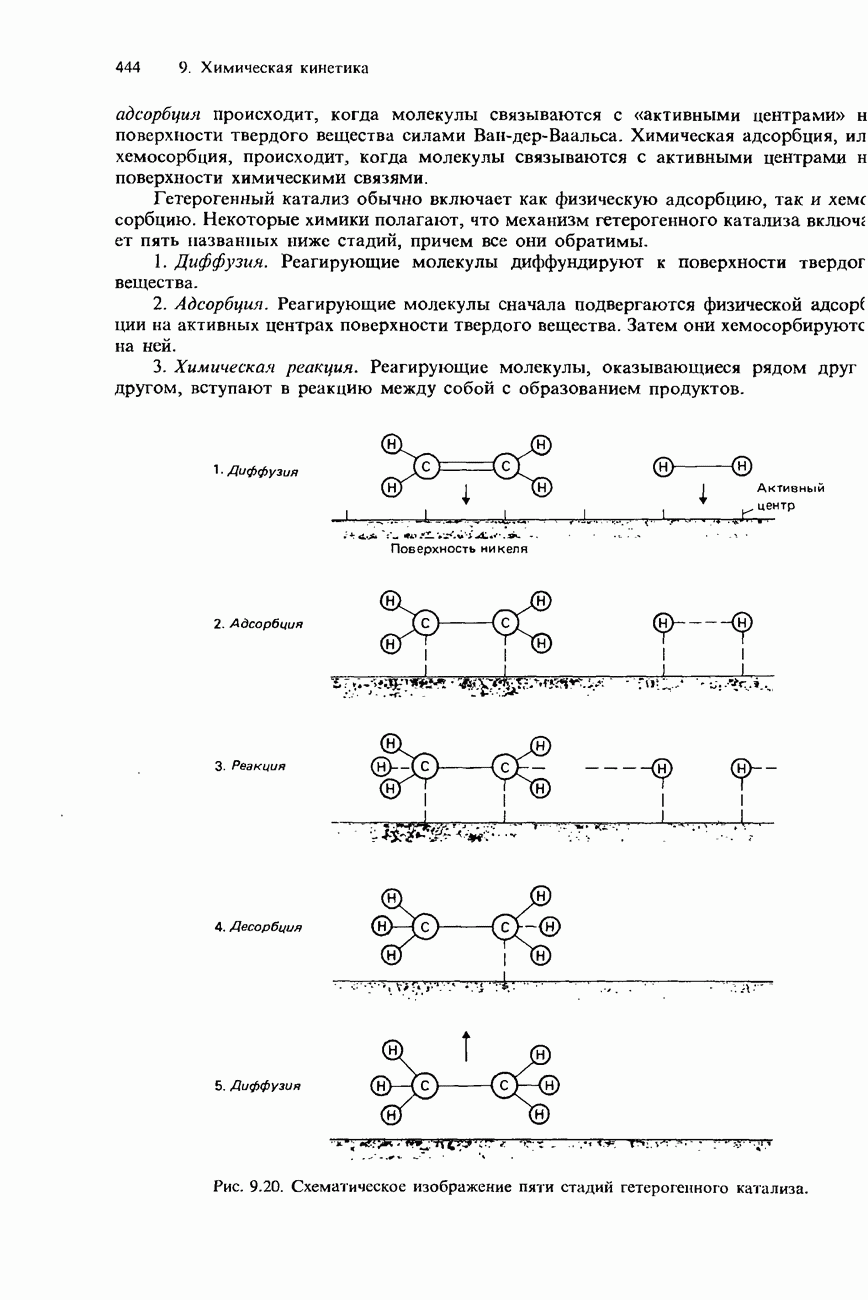
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
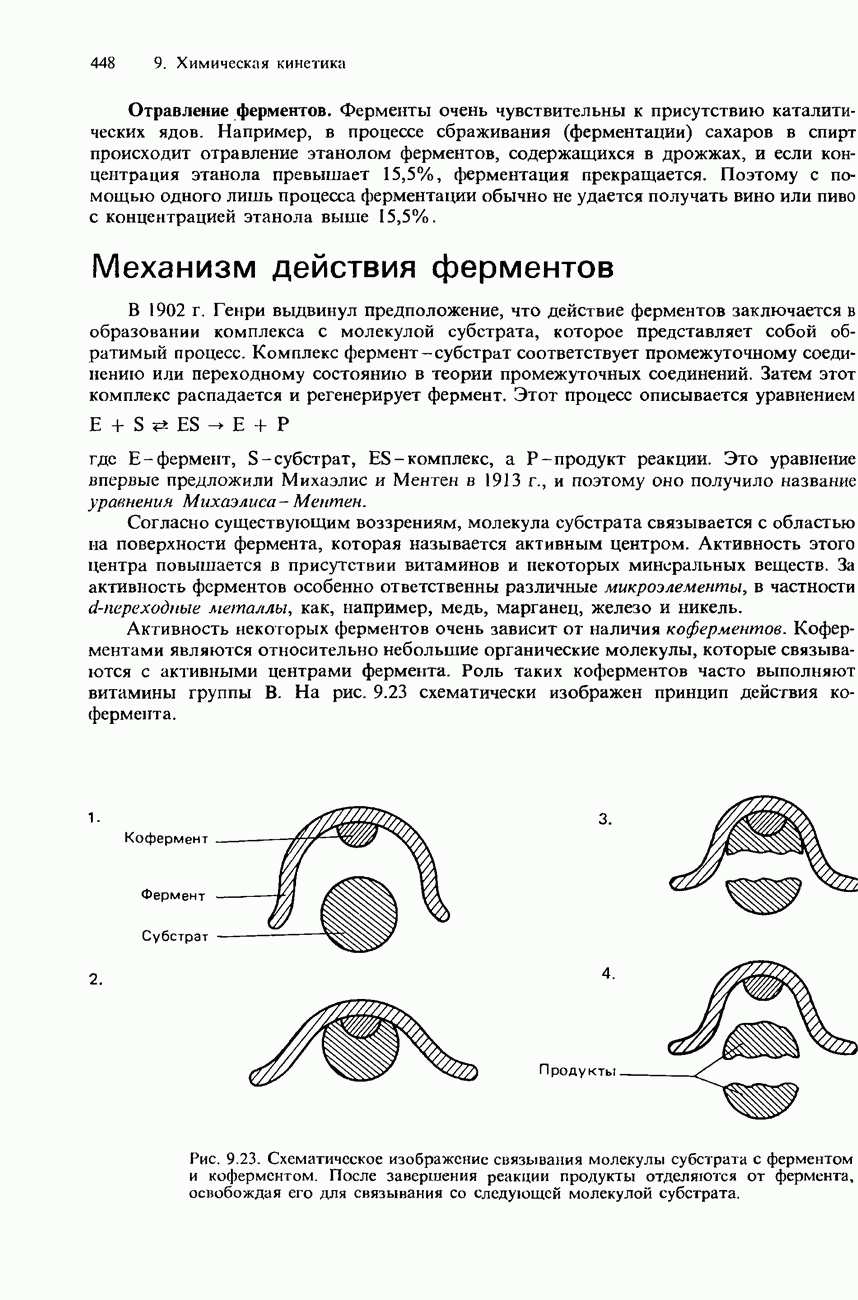
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
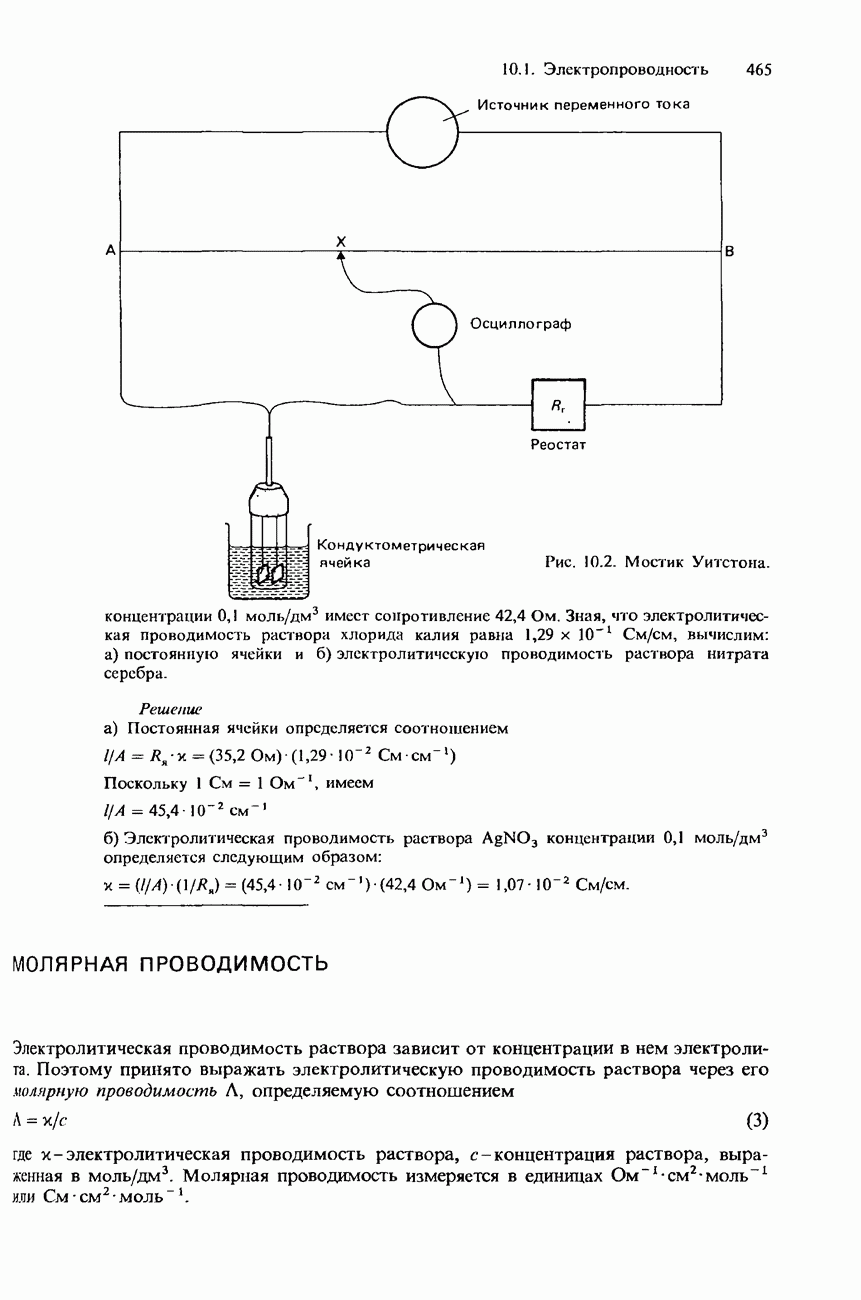
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
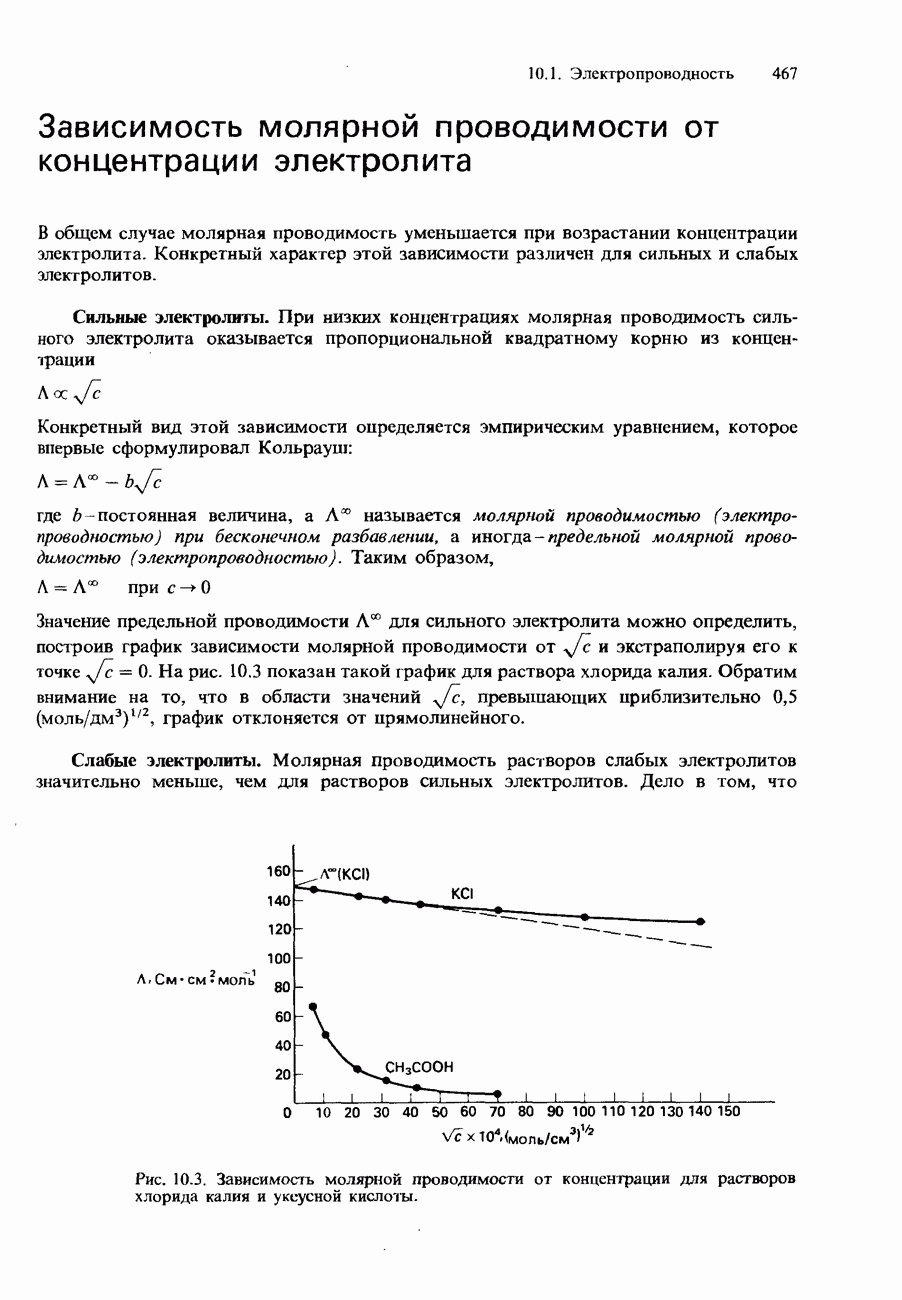
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
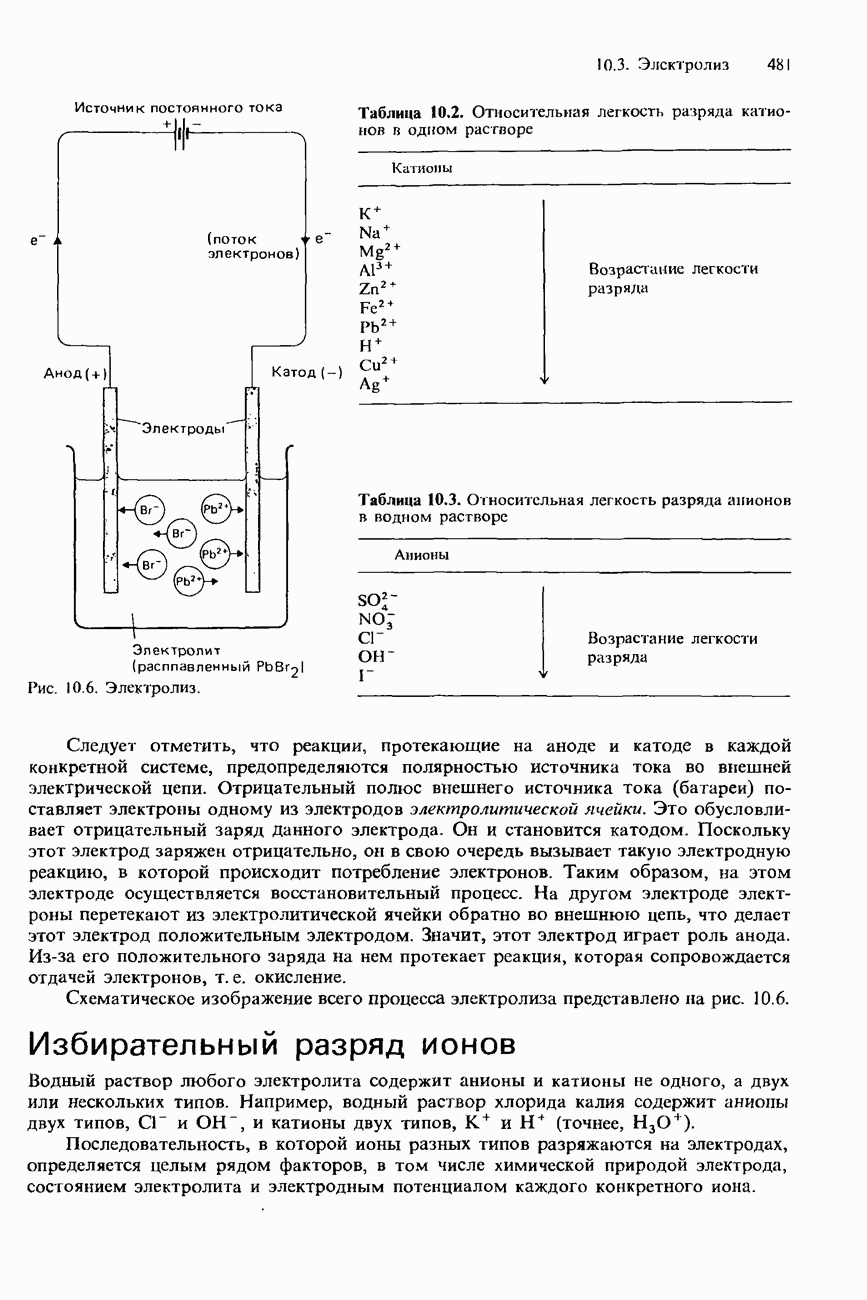
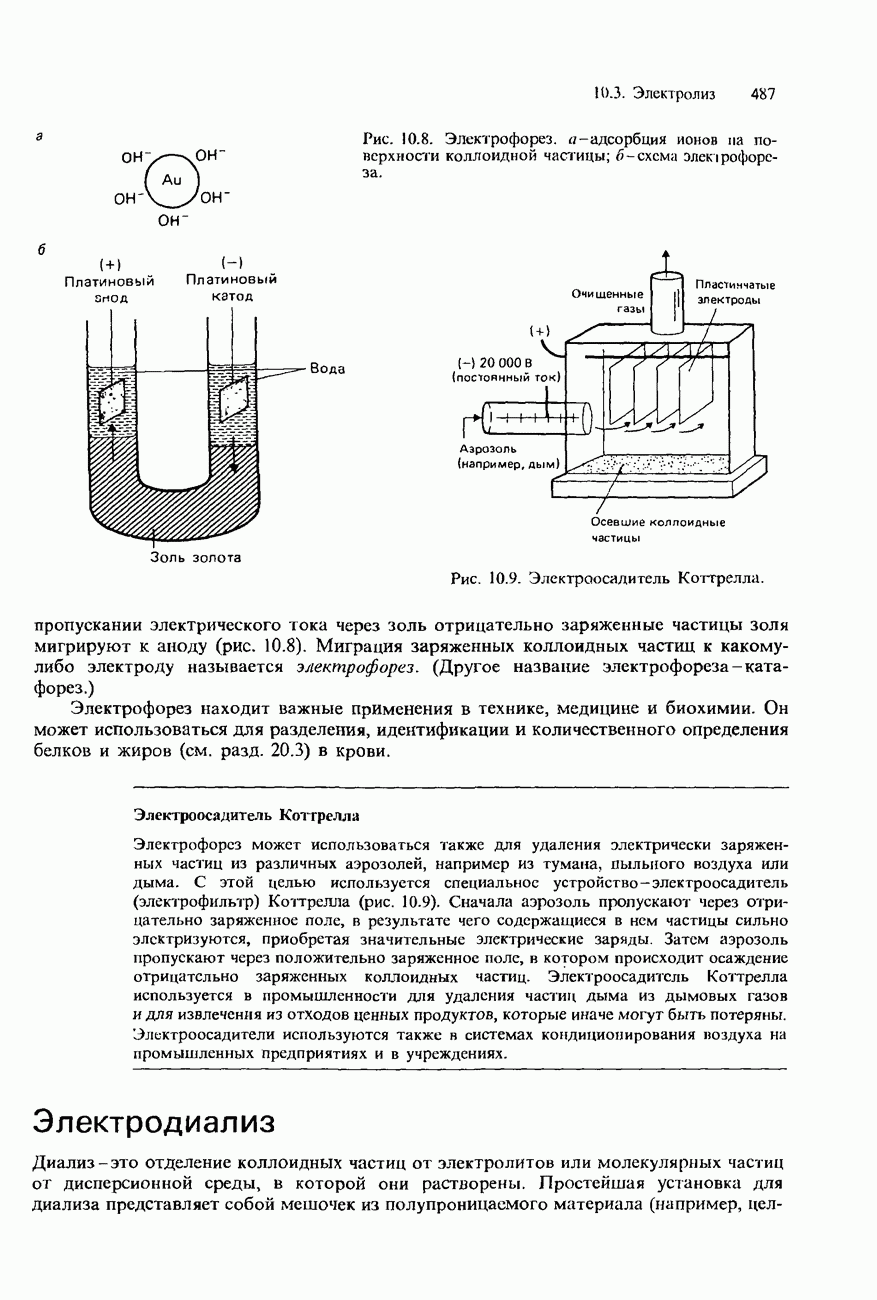
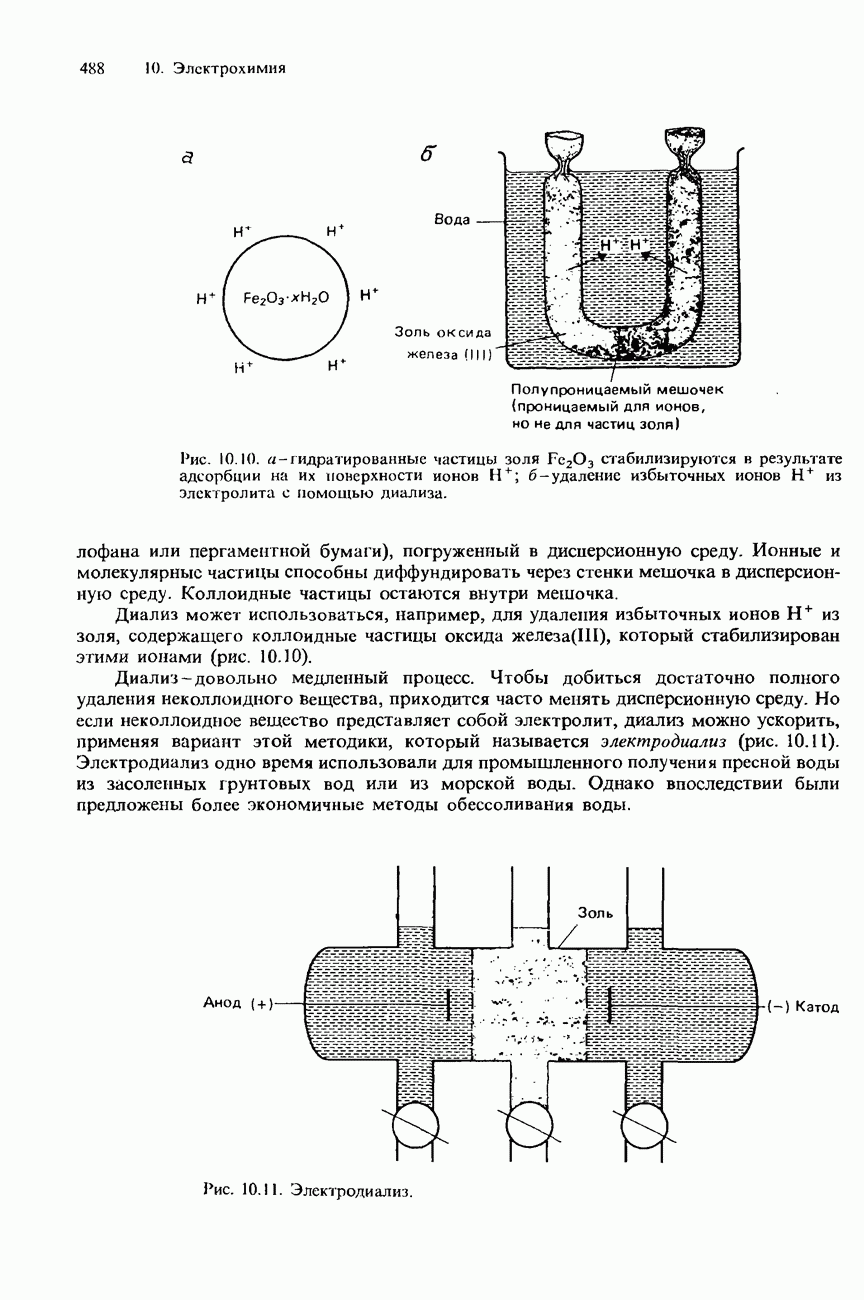
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
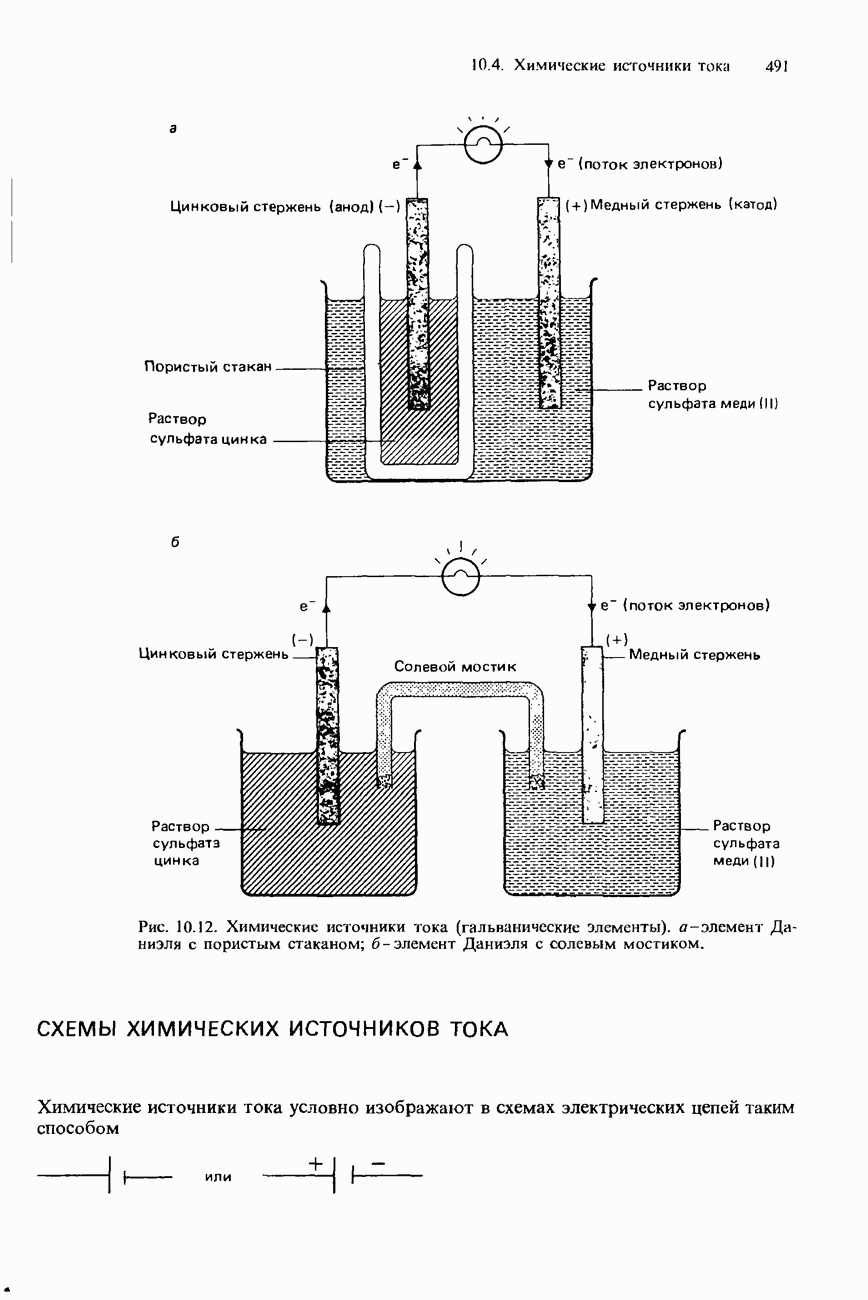
- 10.4. Химические источники тока
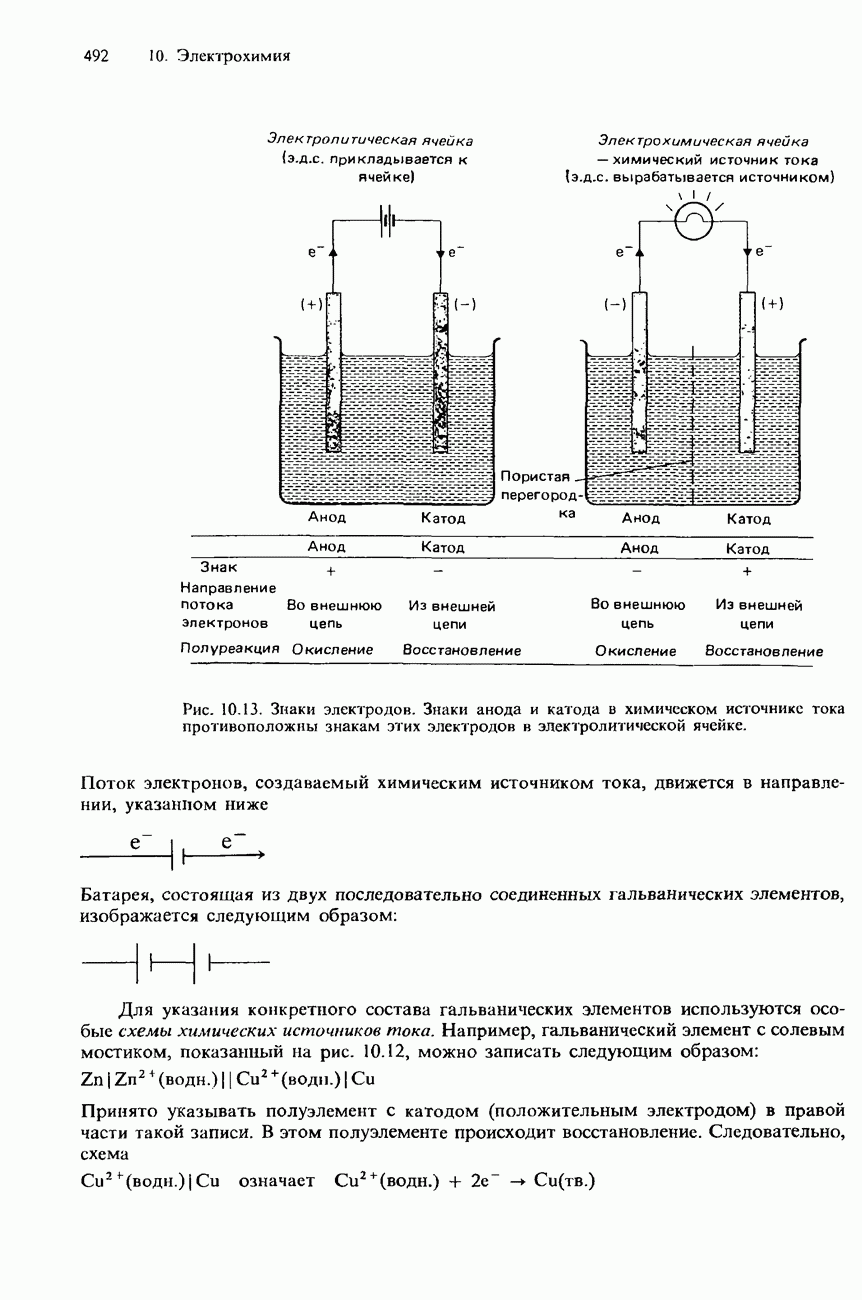
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
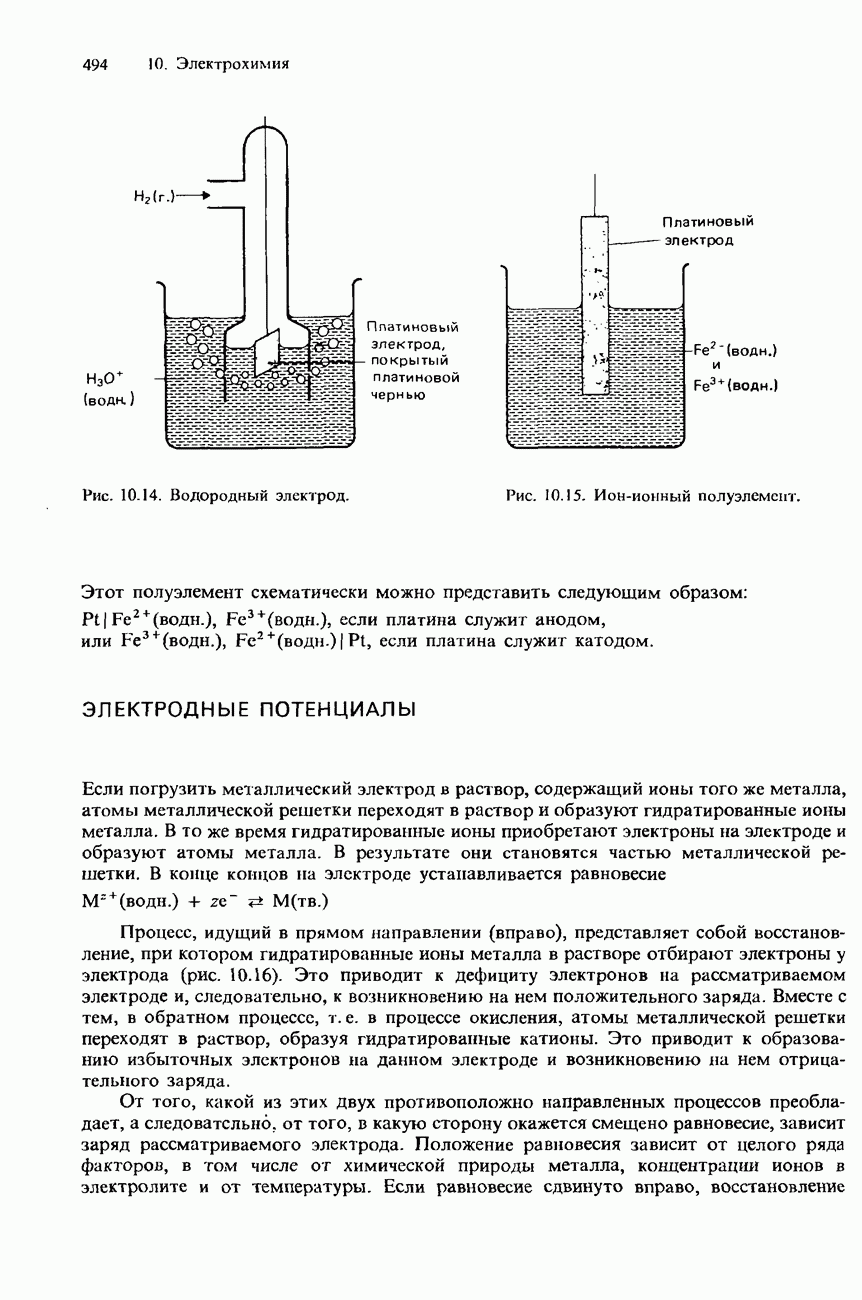
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
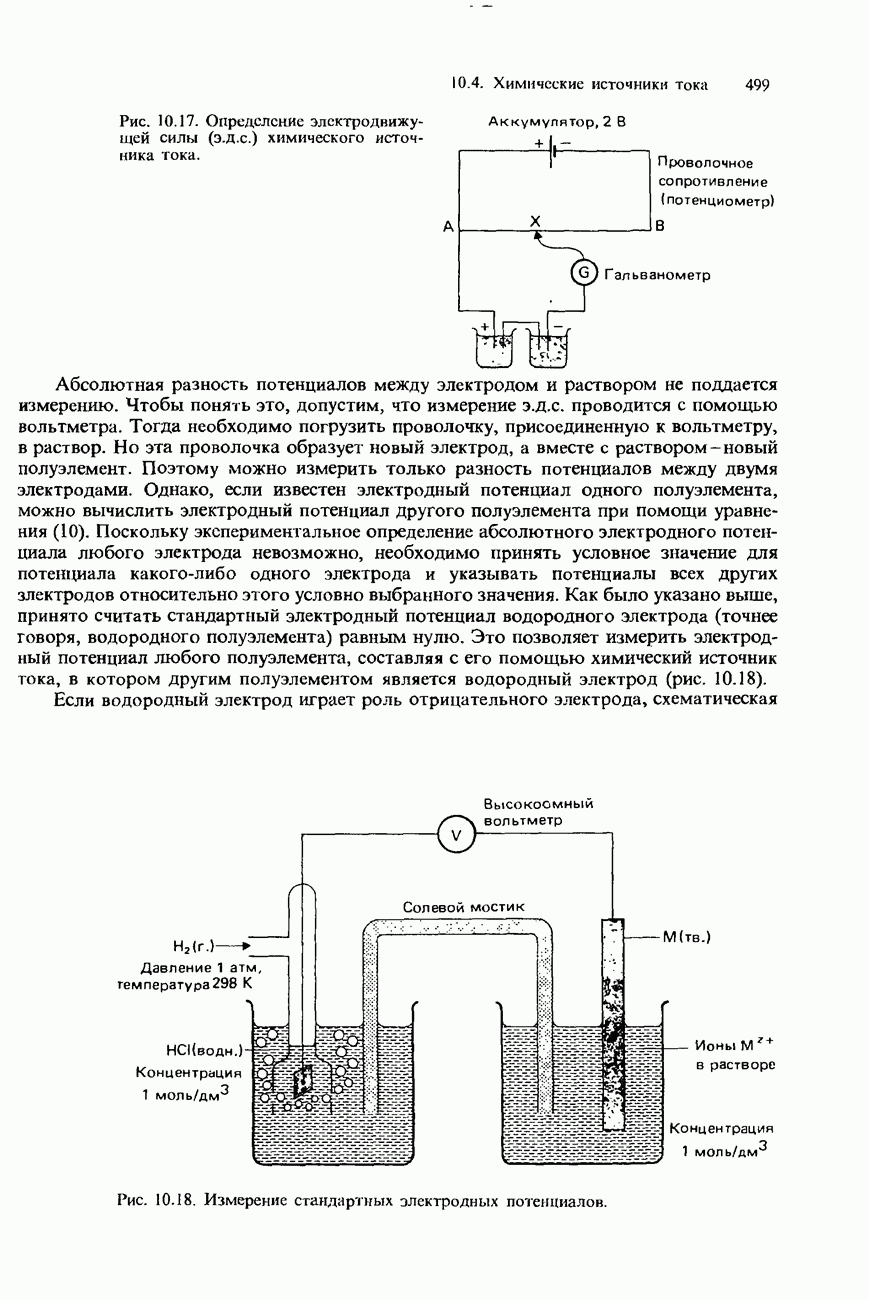
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
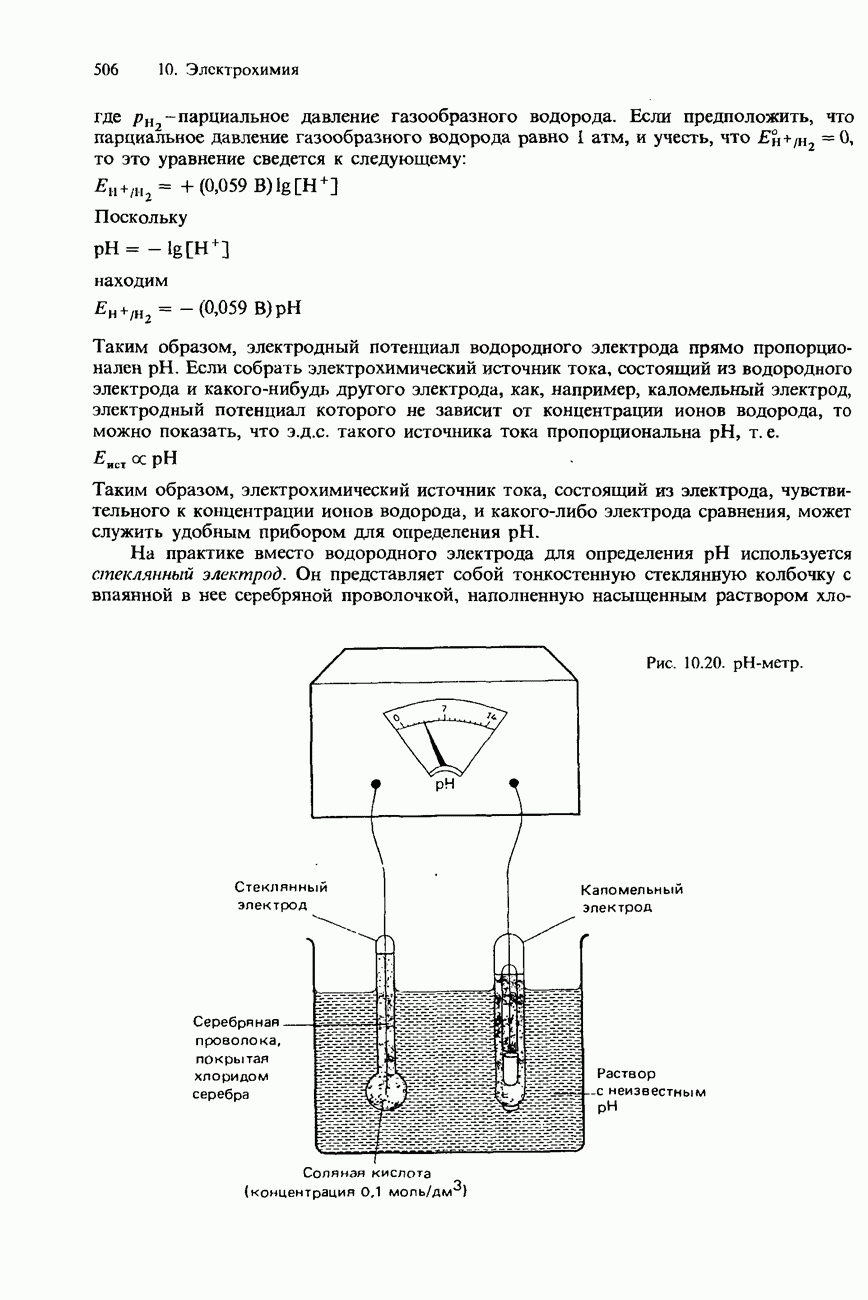
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
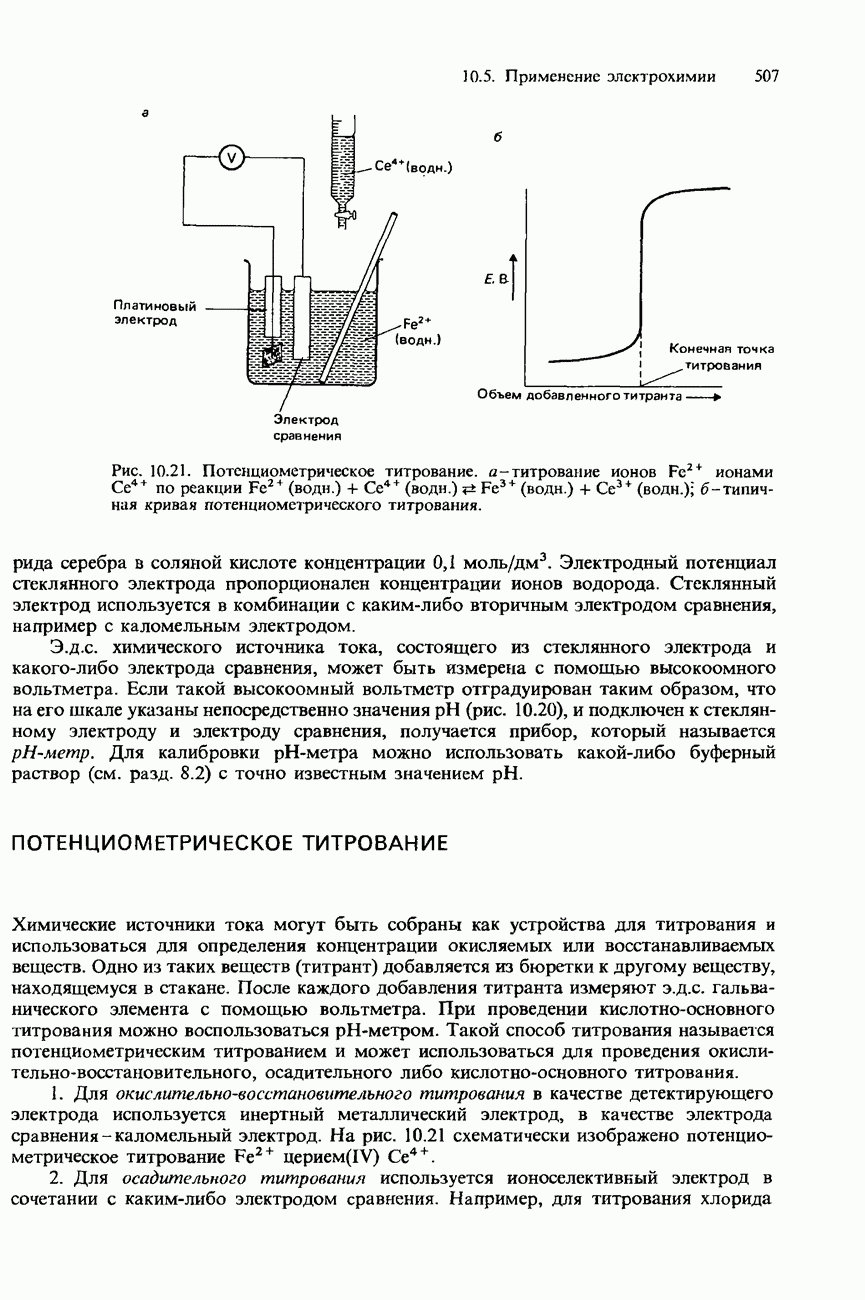
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
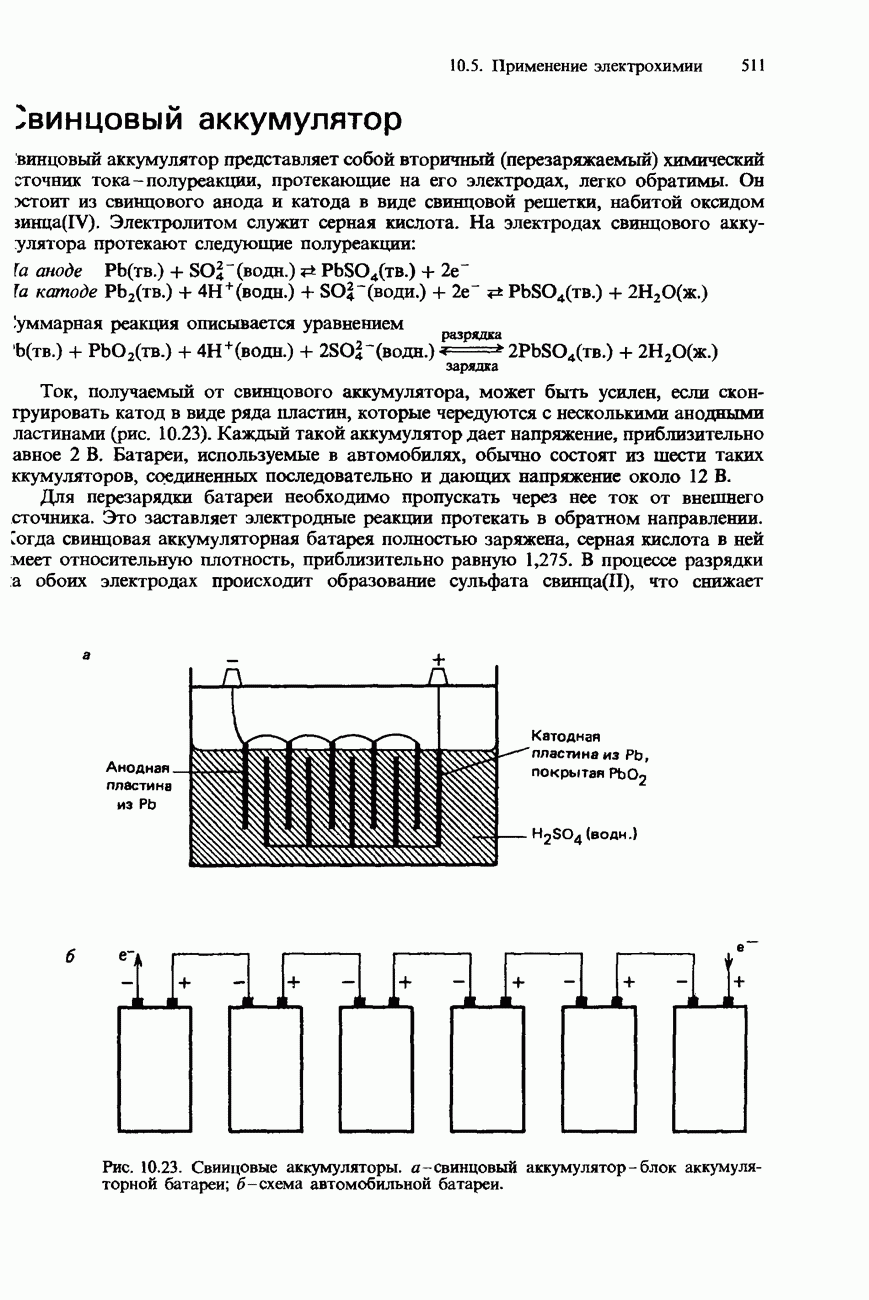
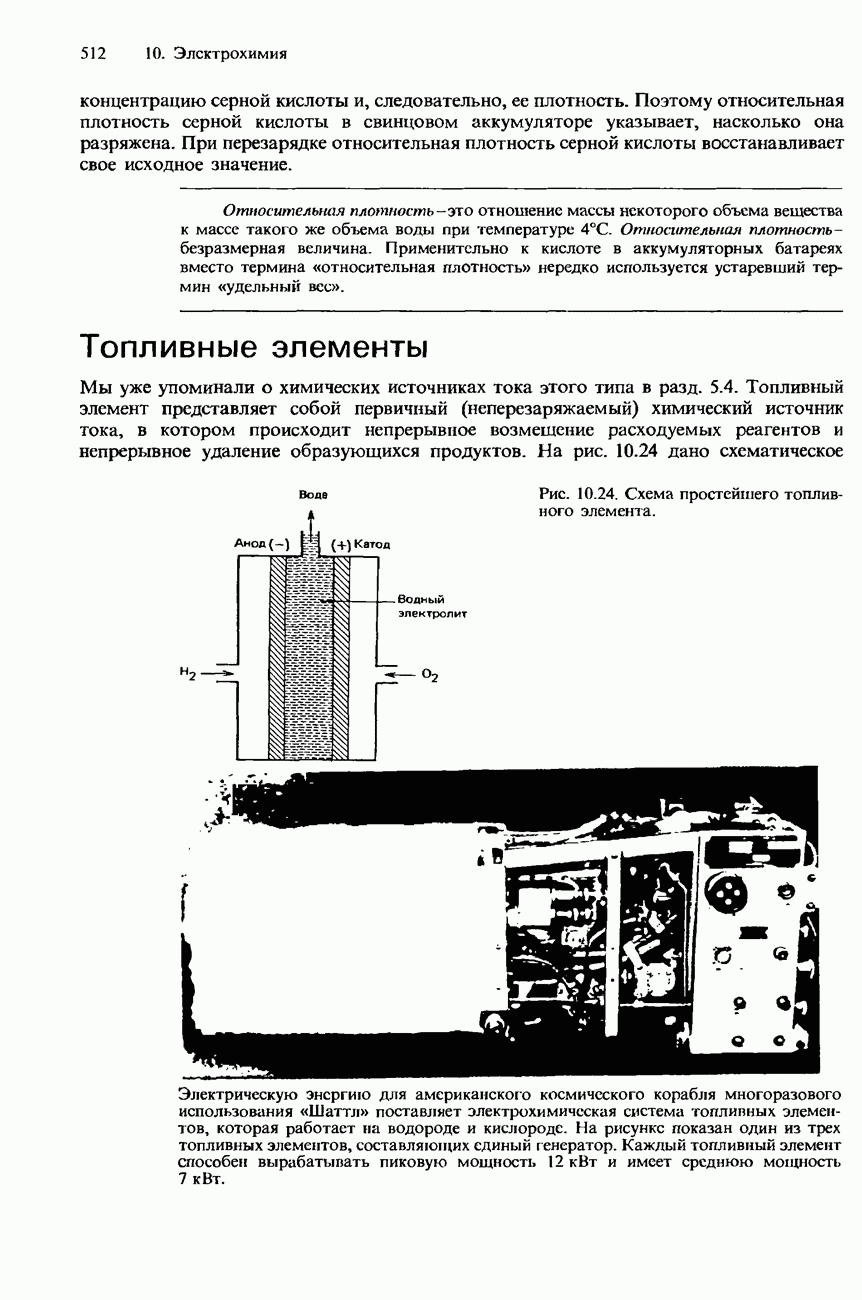
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ