| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
В качестве приближенного правила можно запомнить, что скорость любой химической реакции становится вдвое больше при повышении температуры на каждые 10 К. Это правило позволяет предположить, что между скоростью реакций и температурой

Шведский физикохимик Сванте Аррениус получил Нобелевскую премию по химии в 1903 г. за созданную им теорию электролитической диссоциации. В своей докторской диссертации (Уппсальский университет) Аррениус высказал предположение, что такие «молекулы» как хлорид натрия, самопроизвольно распадаются в растворе, образуя ионы, которые выполняют роль реагентов при электролизе. Однако более всего Аррениус известен своим уравнением, определяющим температурную зависимость константы скорости реакции
должна существовать экспоненциальная зависимость. Точное соотношение межд скоростью реакций и температурой впервые установил шведский химик Аррениус 1889 г. Это соотношение, получившее название уравнения Аррениуса, имеет вид

где к - константа скорости реакции;  - постоянная, характеризующая каждую конкретную реакцию (константа Аррениуса);
- постоянная, характеризующая каждую конкретную реакцию (константа Аррениуса);  - еще одна постоянная, характерная
- еще одна постоянная, характерная  каждой реакции и называемая энергией активации;
каждой реакции и называемая энергией активации;  - газовая постоянная и Т - абсс лютная температура в кельвинах. Отметим, что это уравнение связывает температур не со скоростью реакции, а с константой скорости.
- газовая постоянная и Т - абсс лютная температура в кельвинах. Отметим, что это уравнение связывает температур не со скоростью реакции, а с константой скорости.
В логарифмической форме уравнение Аррениуса приобретает вид

Если перейти от натуральных логарифмов к десятичным, последнее соотношени сводится к виду

Именно эта форма уравнения Аррениуса наиболее употребительна.
Для определения констант А и  характеризующих конкретную реакцию, строя график зависимости
характеризующих конкретную реакцию, строя график зависимости  к от величины 1/Т. (Напомним, что температура должна быт выражена в абсолютной шкале.) Тангенс угла наклона графика к оси абсцисс дает величину
к от величины 1/Т. (Напомним, что температура должна быт выражена в абсолютной шкале.) Тангенс угла наклона графика к оси абсцисс дает величину  Для определения константы Аррениуса А следует подставить уравнение Аррениуса все остальные известные значения.
Для определения константы Аррениуса А следует подставить уравнение Аррениуса все остальные известные значения.
Пример
В табл. 9.7 указаны константы скорости, полученные при разных температурах  реакции
реакции

Определим: а) энергию активации и б) константу Аррениуса для зтой реакции.
Решение
а) Для определения энергии активации построим график зависимости величины  от
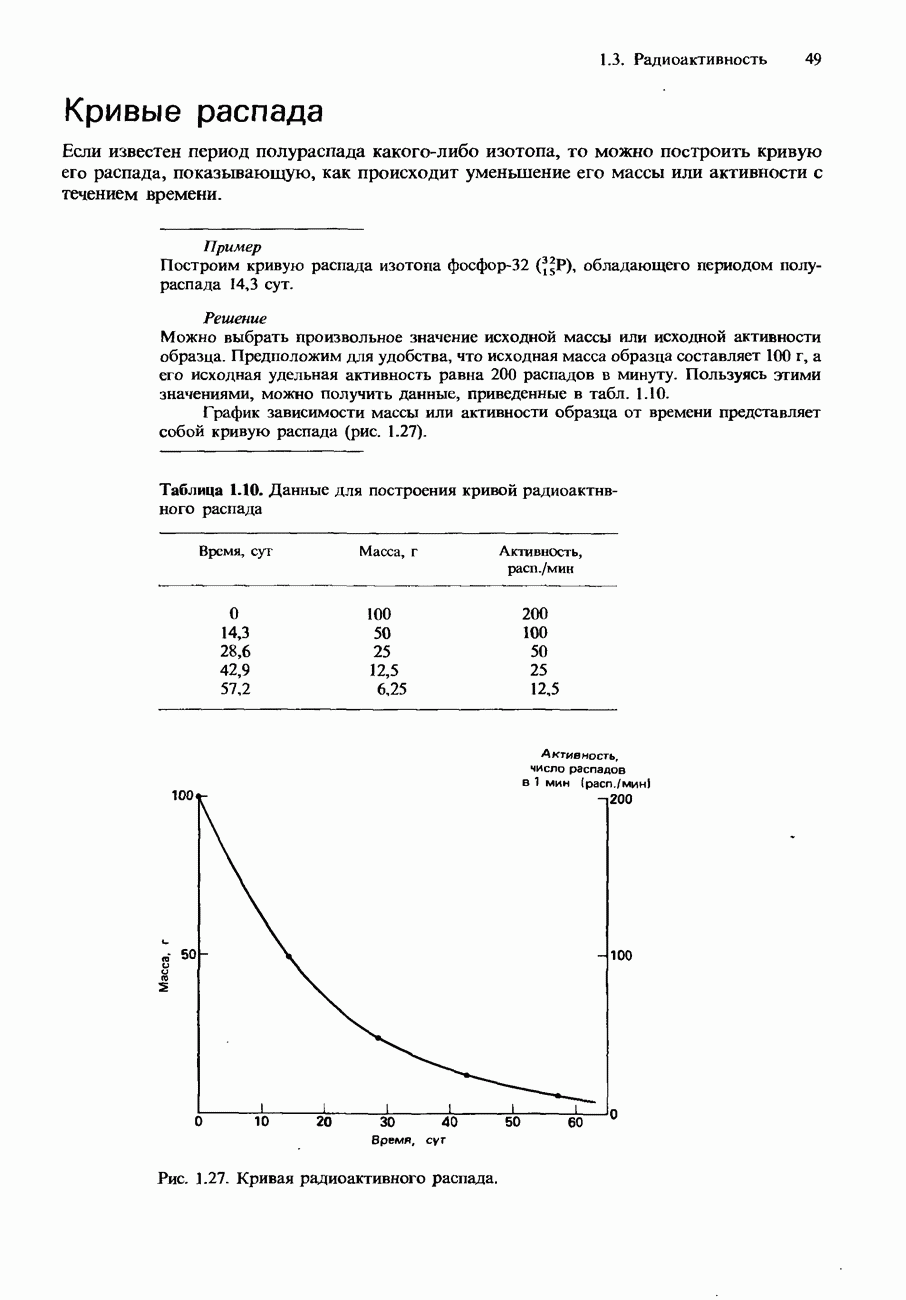
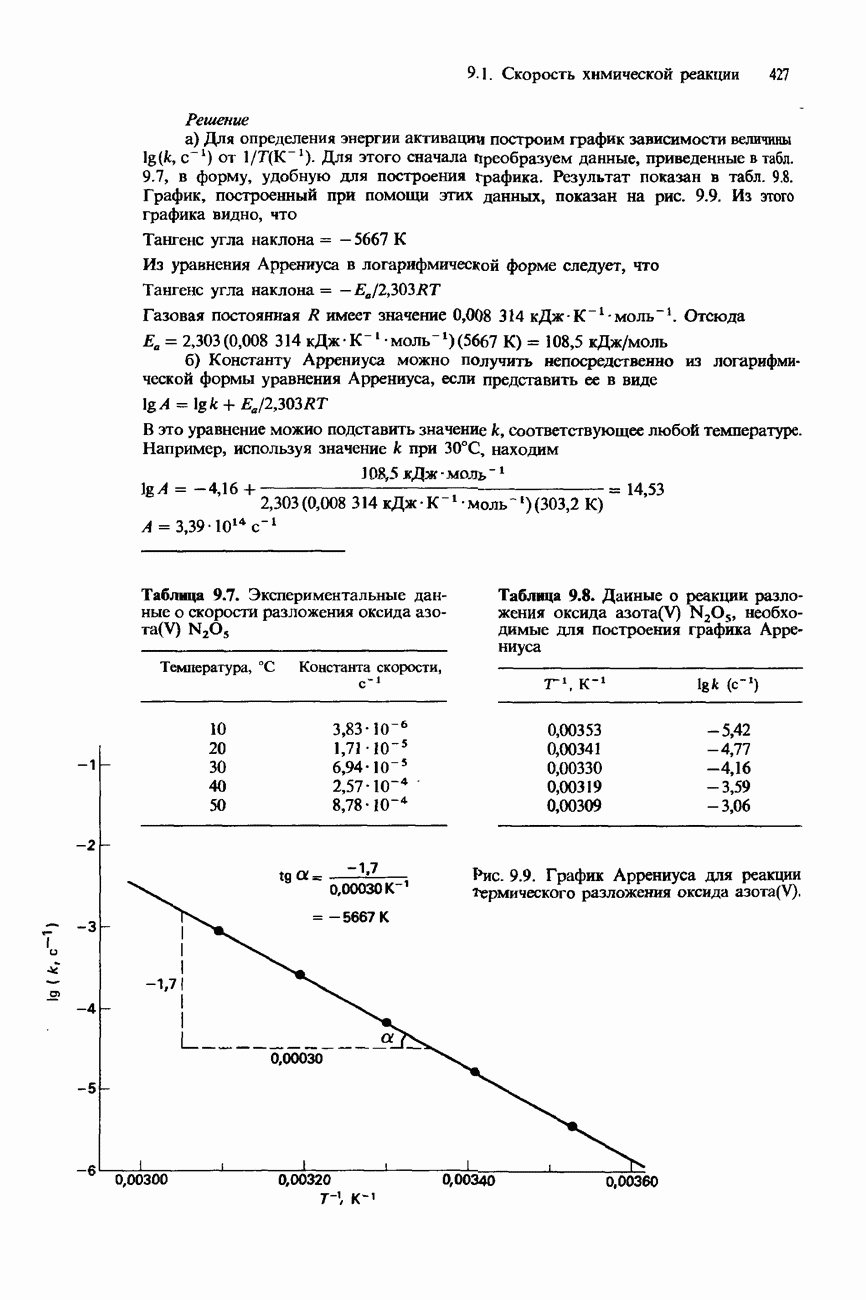
от  Для этого сначала Преобразуем данные, приведенные в табл. 9.7, в форму, удобную для построения графика. Результат показан в табл. 9.8. График, построенный при помощи этих данных, показан на рис. 9.9. Из этого графика видно, что
Для этого сначала Преобразуем данные, приведенные в табл. 9.7, в форму, удобную для построения графика. Результат показан в табл. 9.8. График, построенный при помощи этих данных, показан на рис. 9.9. Из этого графика видно, что
Тангенс угла наклона 
Из уравнения Аррениуса в логарифмической форме следует, что Тангенс угла наклона 
Газовая постоянная R имеет значение 0,008 314 кДж  моль
моль  . Отсюда
. Отсюда

б) Константу Аррениуса можно получить непосредственно из логарифмической формы уравнения Аррениуса, если представить ее в виде

В это уравнение можно подставить значение k, соответствующее любой температуре. Например, используя значение к при  находим
находим

Таблица 9.7. Экспериментальные данные о скорости разложения оксида 

Таблица 9.8. Даиные о реакции разложения оксида  необходимые для построения графика Аррениуса
необходимые для построения графика Аррениуса

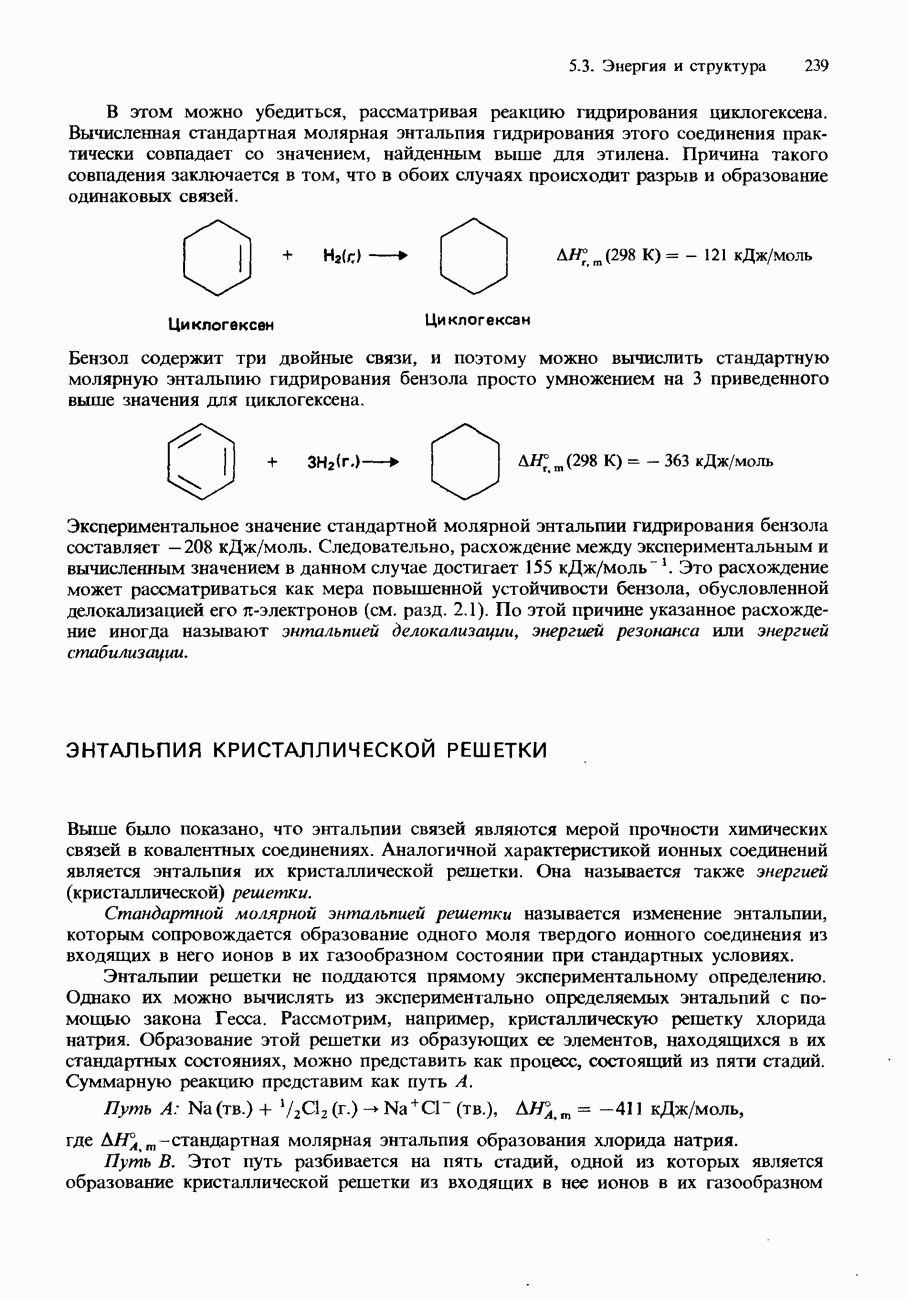
(см. скан)
Рис. 9.9. График Аррениуса для реакции термического разложения оксида 
Почему важно исследовать влияние температуры на скорость химических реакций?
Температура оказывает заметное влияние на сложные биологические и химические процессы, протекающие в растениях и организмах животных. В качестве примера укажем на влияние температуры на скорость дыхания, которое имеет важное значение в медицине. Во время некоторых хирургических операций тело пациента подвергают охлаждению, чтобы замедлить протекание метаболических процессов, понизить скорость циркуляции крови и частоту дыхания.
Температура оказывает также заметное влияние на биохимические процессы, протекающие в пише при ее хранении или в ходе ее приготовления. Скорость порчи пищевых продуктов может быть понижена разными способами, включая замораживание (рис. 9.10), использование консервантов, как, например, сорбиновой кислоты, диоксида серы или нитритов, а также соблюдением надлежащих условий хранения. Так, свежесть и аромат чая зависят от содержания в нем ряда химических веществ, принадлежащих к группе флавинов. При хранении чая содержание в нем флавинов постепенно уменьшается. Скорость разрушения флавинов в час приблизительно в равной мере зависит от влажности и температуры.
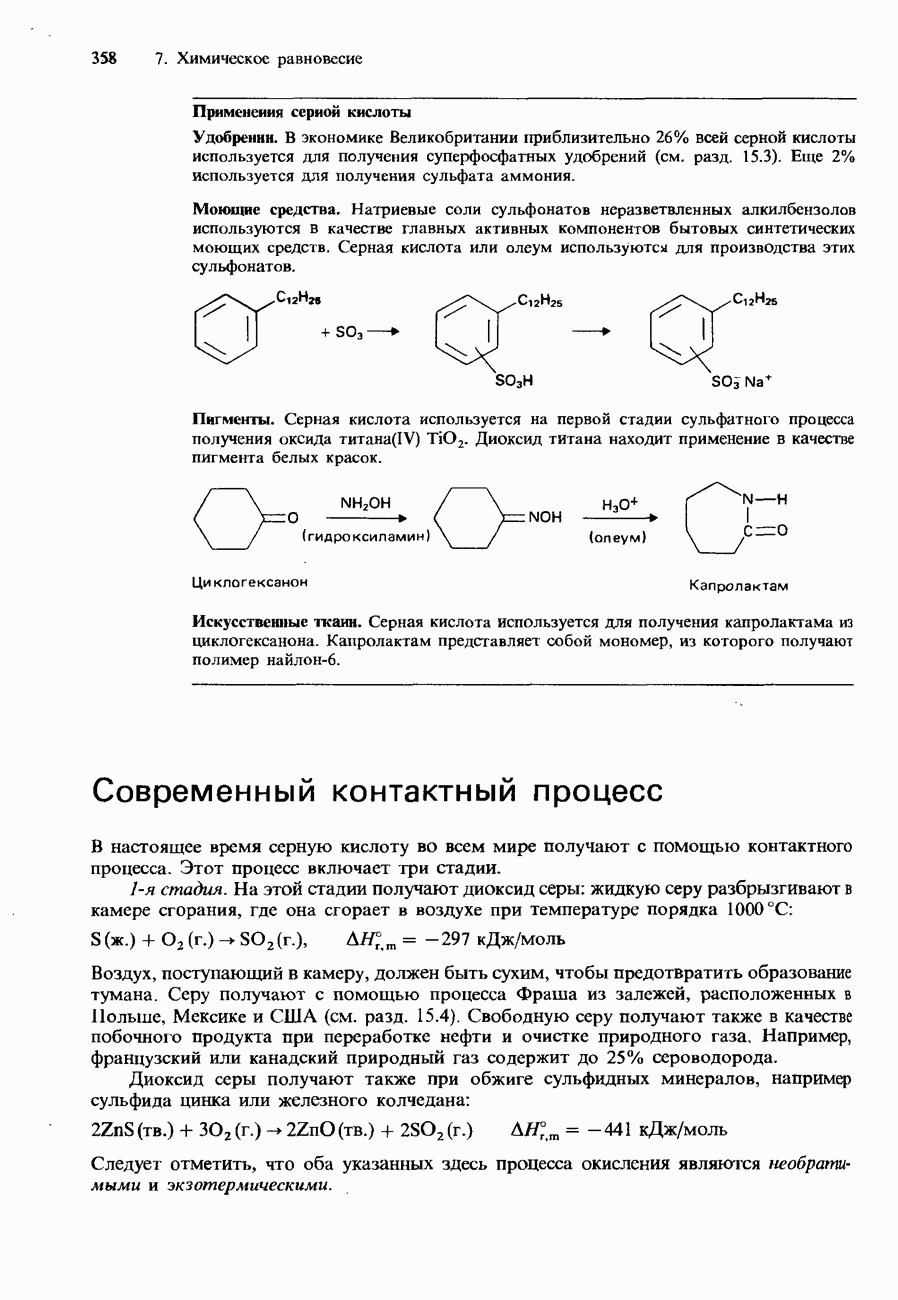
Оптимальная эффективность многих технологических химических процессов тоже зависит от температуры. В качестве примера укажем на вторую стадию контактного процесса получения серной кислоты (см. разд. 7.2)

Поскольку эта реакция экзотермична, выход триоксида серы можно повысить, понижая температуру. Однако понижение температуры приводит к замедлению процесса. Поэтому необходимо найти оптимальный баланс между выходом и скоростью реакции. Это достигается путем проведения данной стадии процесса при температуре от 450 до 500°С и использовании катализатора - оксида ванадия (V).

Рис. 9.10. Торговая этикетка на упаковке замороженных сосисок. На ней указаны способ приготовления, состав и инструкция по хранению при разных режимах: в морозильнике с одной звездочкой в течение 1 нед, с двумя звездочками -1 мес, с тремя и четырьмя звездочками - 3 мес. Таким образом, хранение пищевых продуктов при температуре 5°С (обычная температура внутри холодильника) допустимо в течение нескольких дней; хранение замороженных продуктов при температуре от - 5°С до - 2°С - в течение нескольких недель. Глубоко замороженные продукты в морозильной камере при температуре около -18°С можно хранить в течение пескопьких месяцев.
Температура влияет не только на скорость химических реакций; она может влиять и на путь протекания реакции. Например, при нагревании нитрата аммония не выше 200°С происходит следующая реакция, которая протекает с умеренной скоростью

Эта реакция часто используется для получения  в лабораторных условиях. Однако, если нагревать нитрат аммония до высоких температур в замкнутом
в лабораторных условиях. Однако, если нагревать нитрат аммония до высоких температур в замкнутом
объеме, происходит следующая взрывная реакция

Таким образом, термическое разложение нитрата аммония может протекать, i зависимости от температуры, двумя совершенно различными путями. В следующем разделе будет показано, как экспериментальное определение скоростей реакцию позволяет предсказать путь протекания химической реакции.
Итак, повторим еще раз!
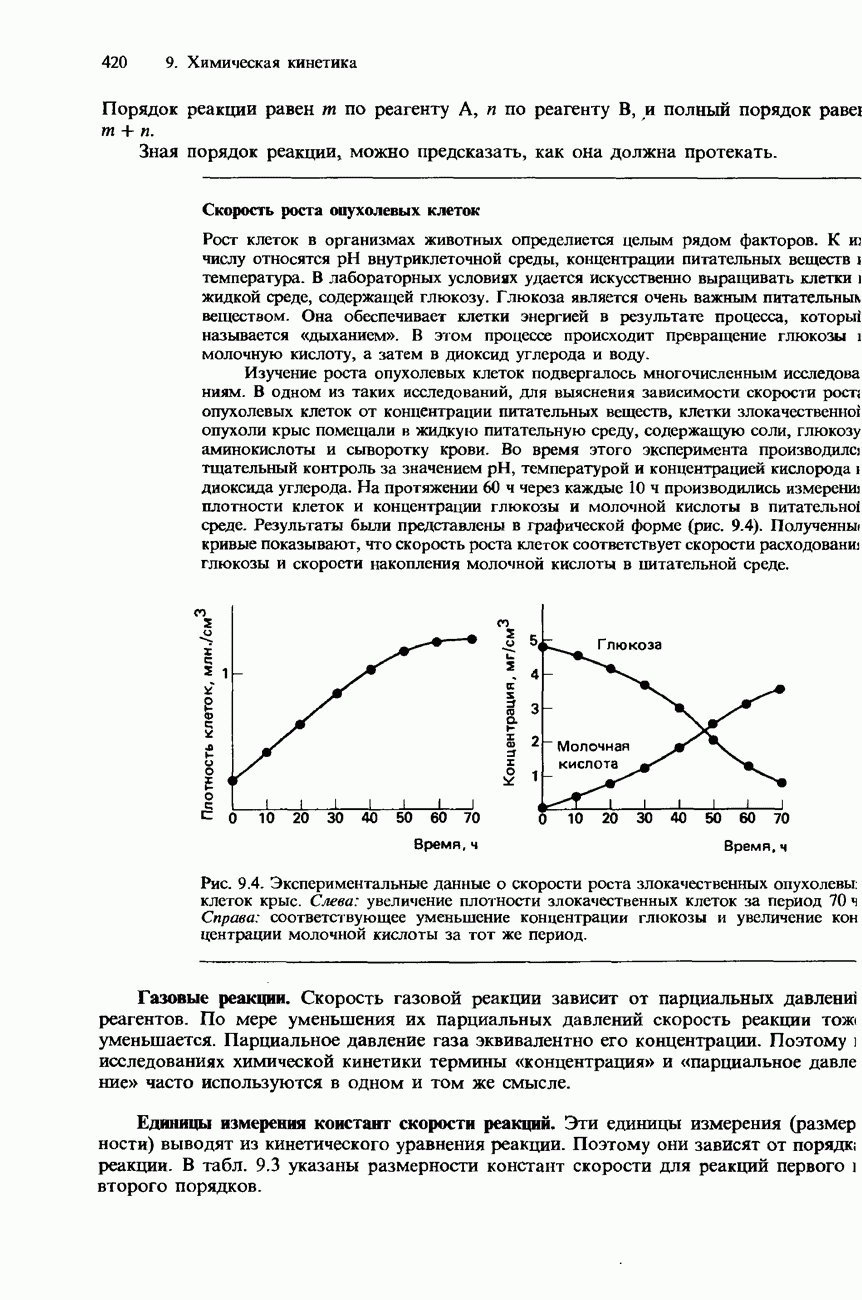
1. Скорость реакции определяется как скорость образования продуктов либо скорость расходования реагентов, о которой можно судить по изменению концентрации.
2. Скорость реакции может зависеть от а) концентрации или давления реагентов, б) температуры, в) присутствия катализаторов, г) доступности реагентов, в том числе от степени измельчения твердых реагентов и площади их поверхности.
3. Начальная скорость реакции обычно имеет наибольшую величину. Затем по мере продвижения реакции ее скорость, как правило, уменьшается.
4. Скорость реакции возрастает при увеличении степени измельчения твердых реагентов.
5. Кинетическое уравнение реакции в общем виде записывается так:

где к - константа скорости,  - порядок реакции, с - концентрация реагента.
- порядок реакции, с - концентрация реагента.
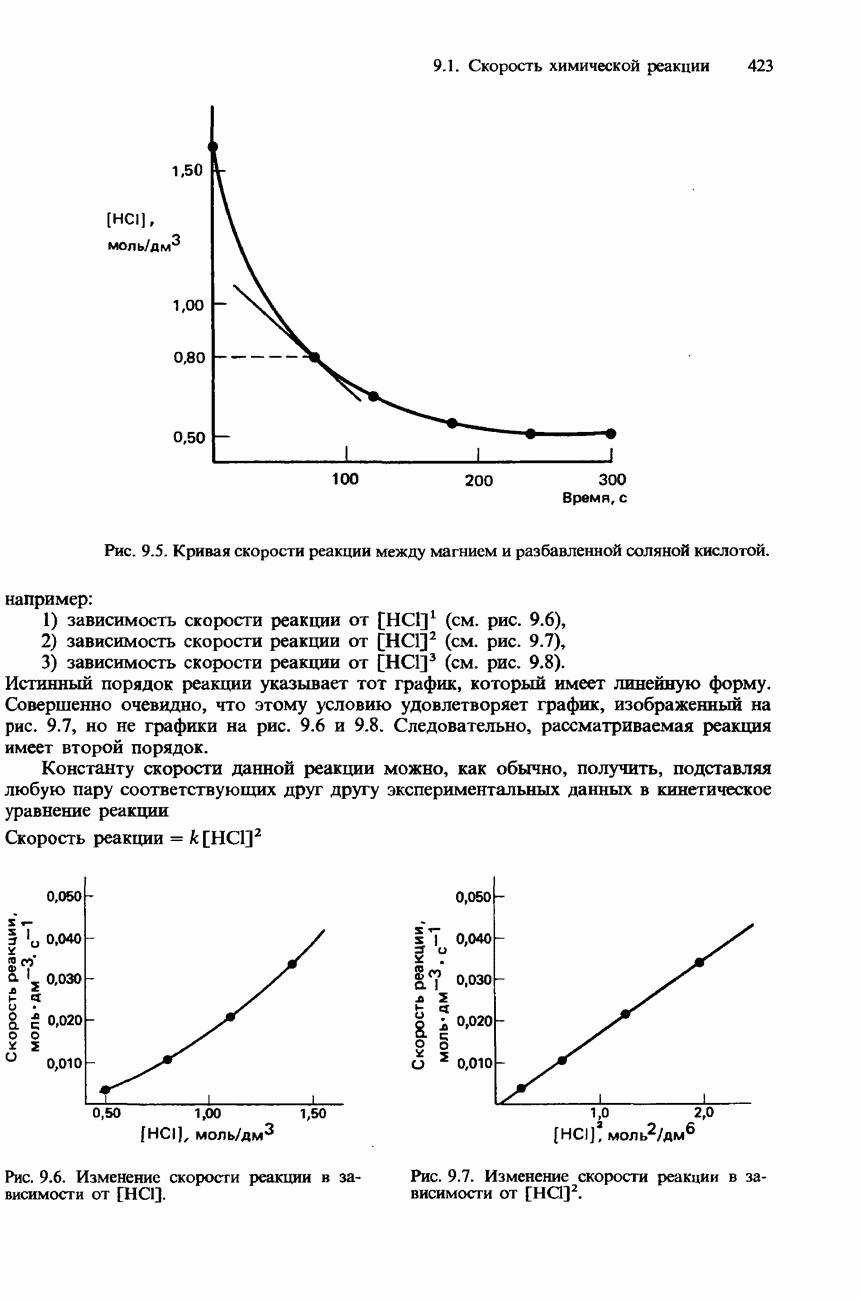
6. Порядок реакции и константу скорости можно определить из экспериментальных данных следующими способами:
а) методом анализа экспериментальных данных,
б) методом анализа кривой скорости реакции,
в) методом интегрирования кинетического уравнения реакции.
7. Период полупревращения - это время, необходимое для уменьшения начальной концентрации реагента в два раза. Период полупревращения для реакции первого порядка связан с константой скорости соотношением

8. Скорости большинства химических реакций возрастают при увеличении температуры.
9. Уравнение Аррениуса связывает константу скорости к с абсолютной температурой Т. В наиболее употребительной форме  уравнение имеет вид
уравнение имеет вид

где А и  постоянные, характеризующие конкретную реакцию;
постоянные, характеризующие конкретную реакцию;  называется энергией активации, а А - константой Аррениуса.
называется энергией активации, а А - константой Аррениуса.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
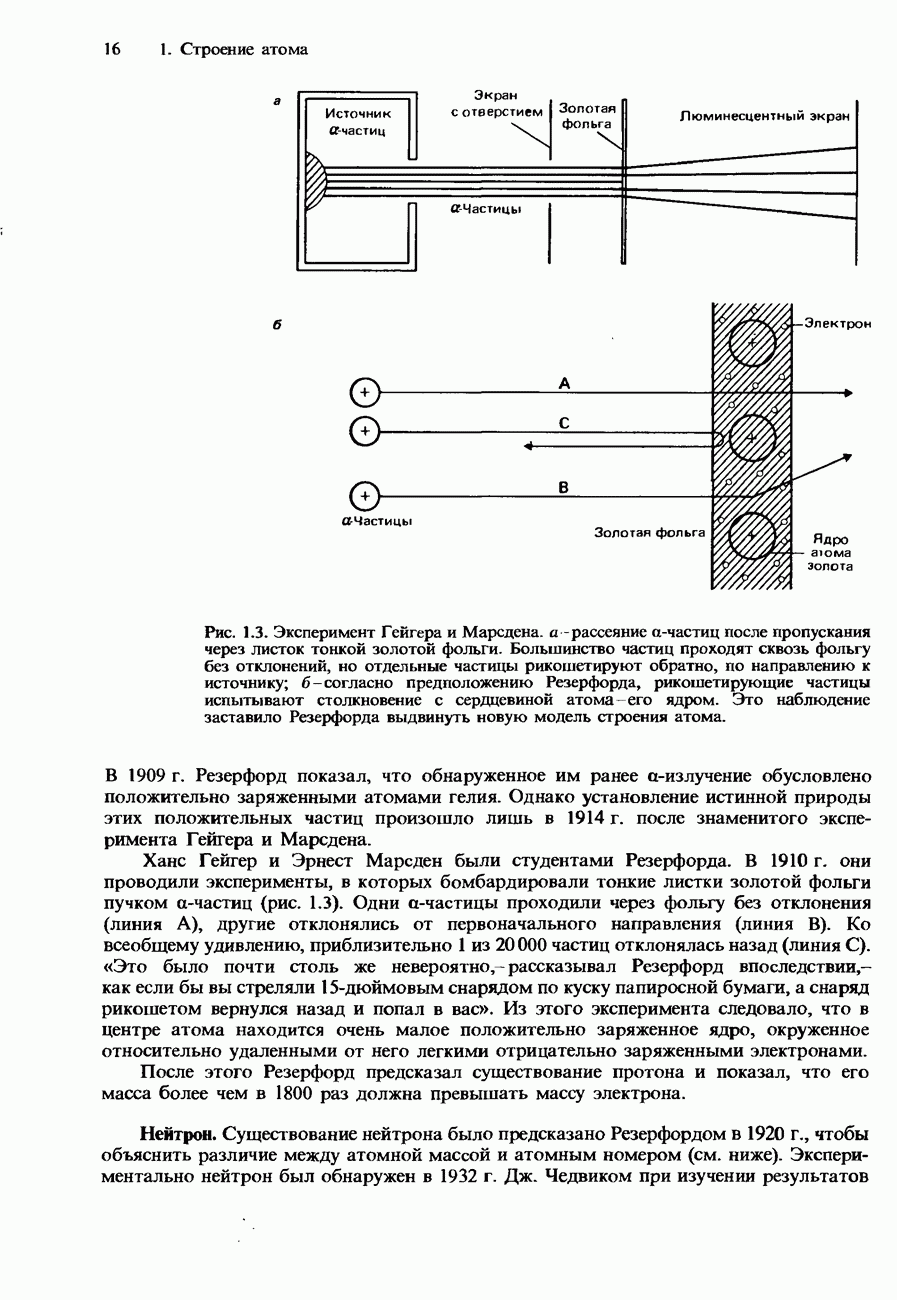
- 1.1. Субатомные частицы
- Модели атома
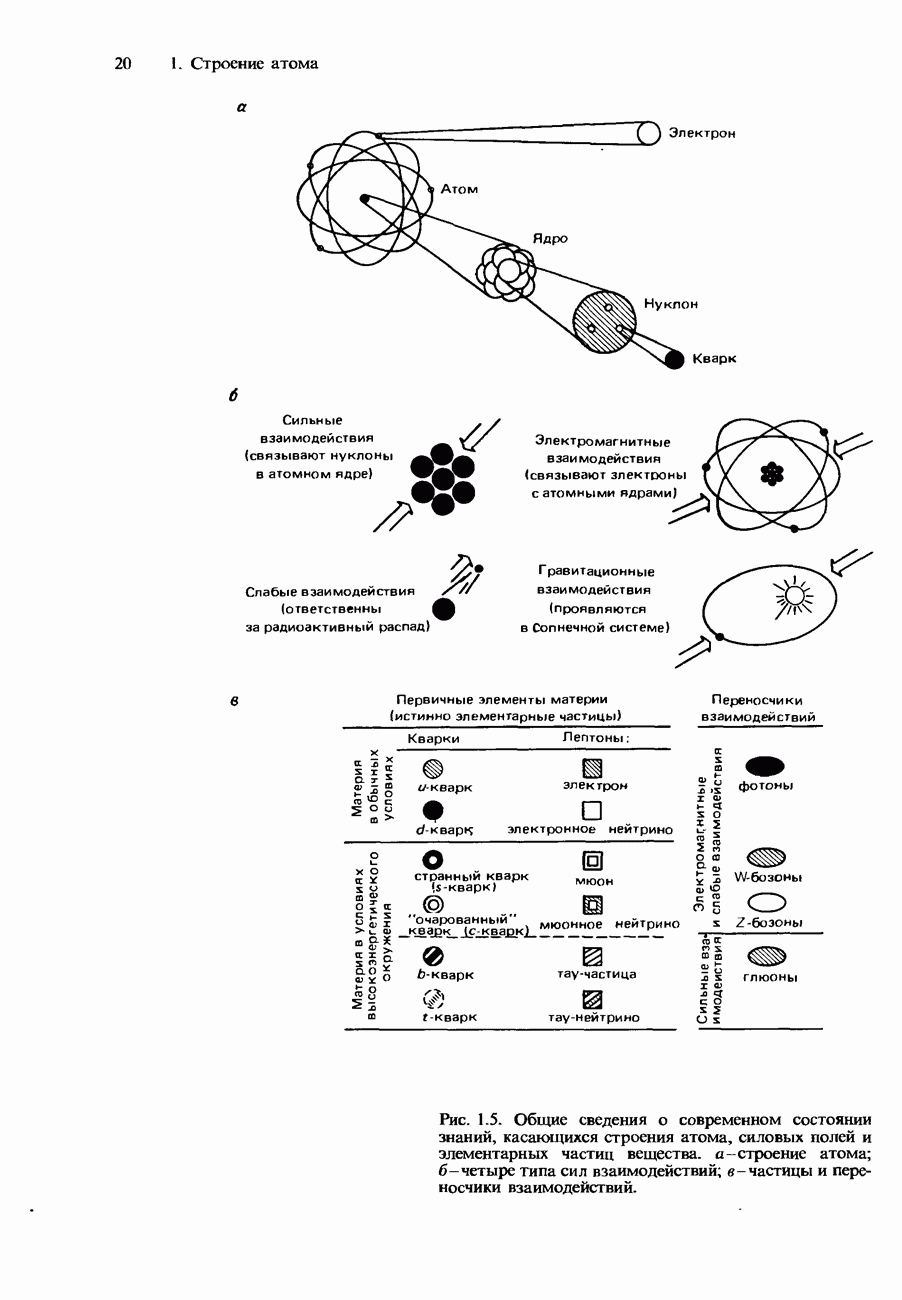
- Новые элементарные частицы
- МАССА АТОМА
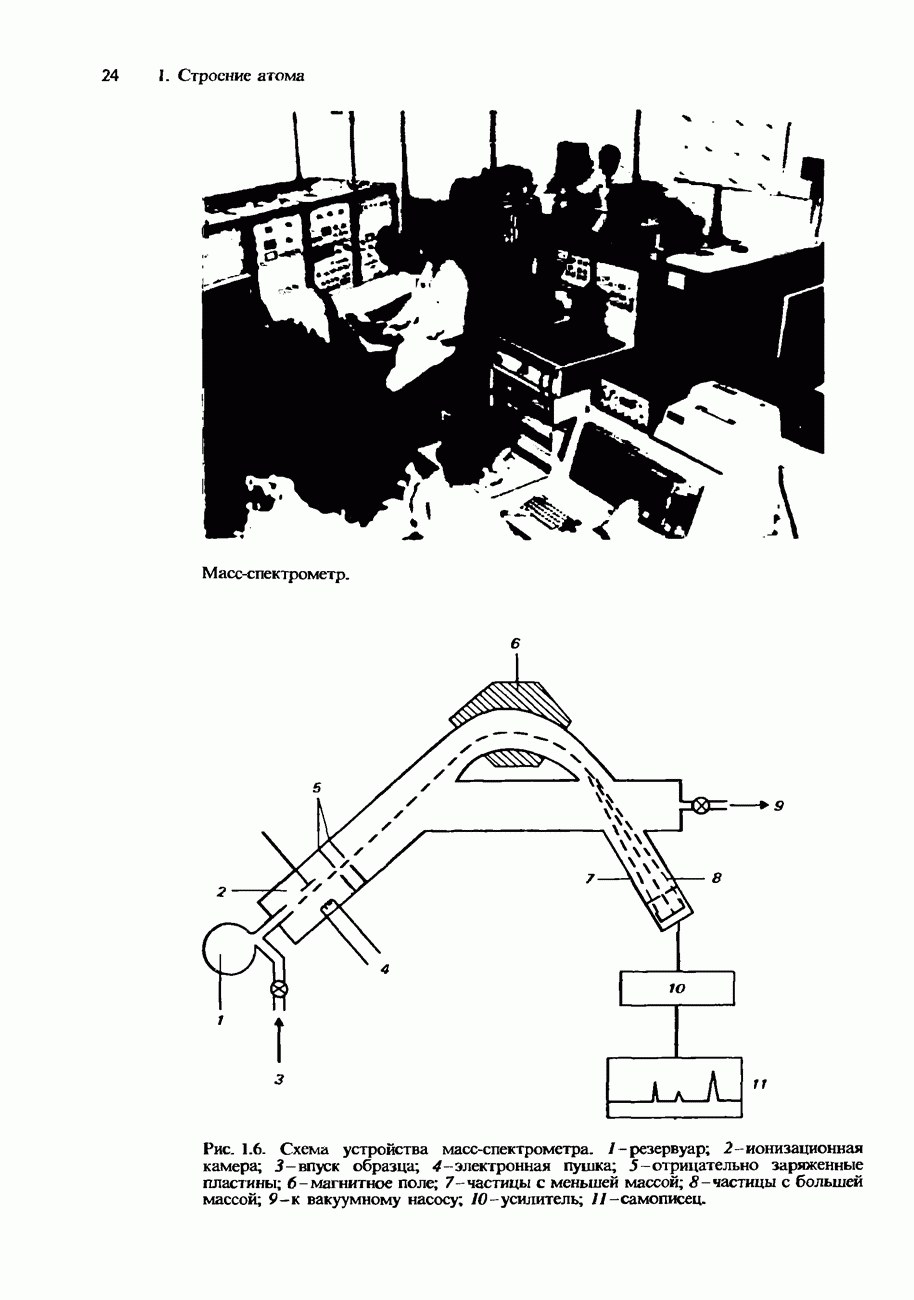
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
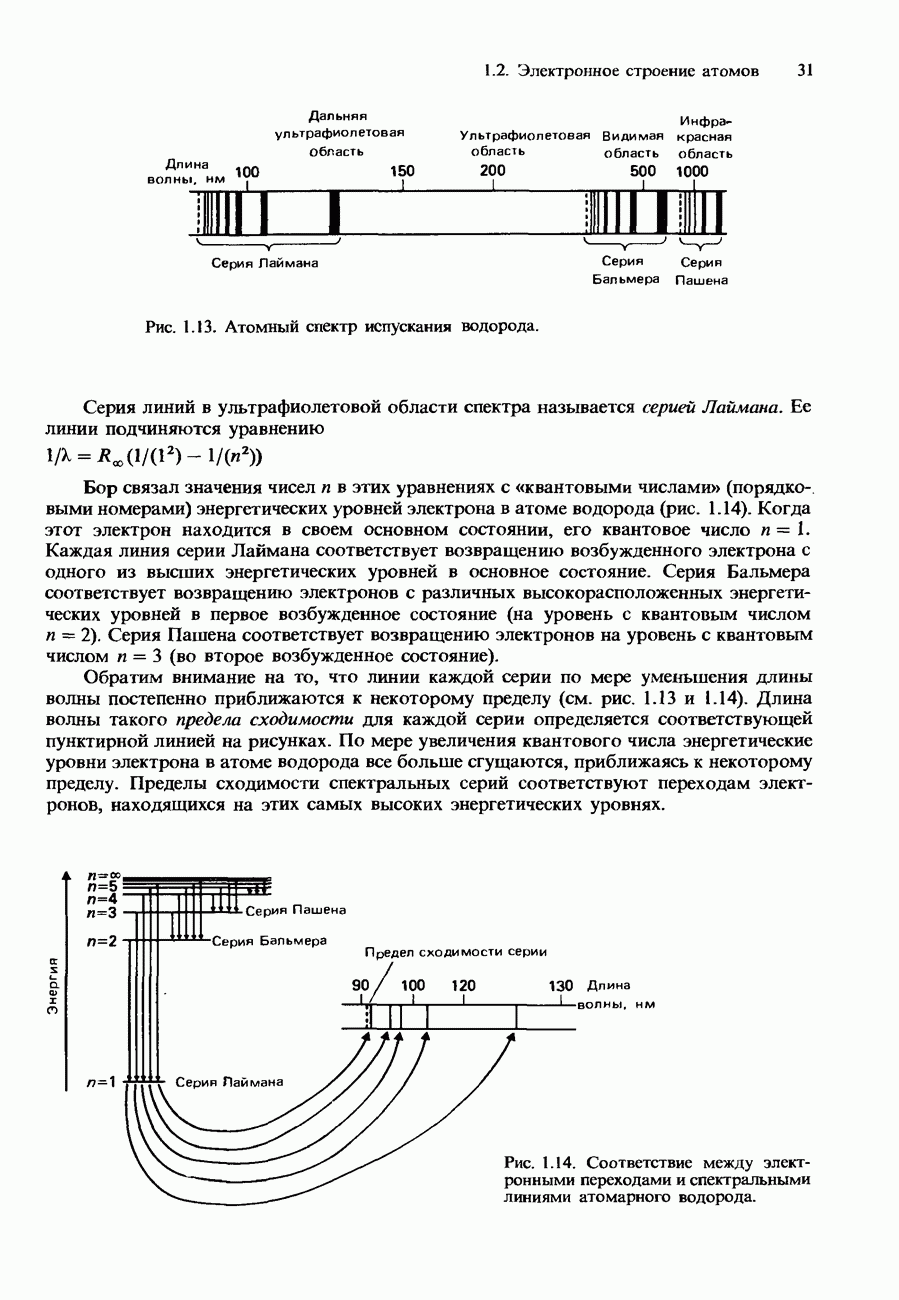
- Атомный спектр испускания водорода
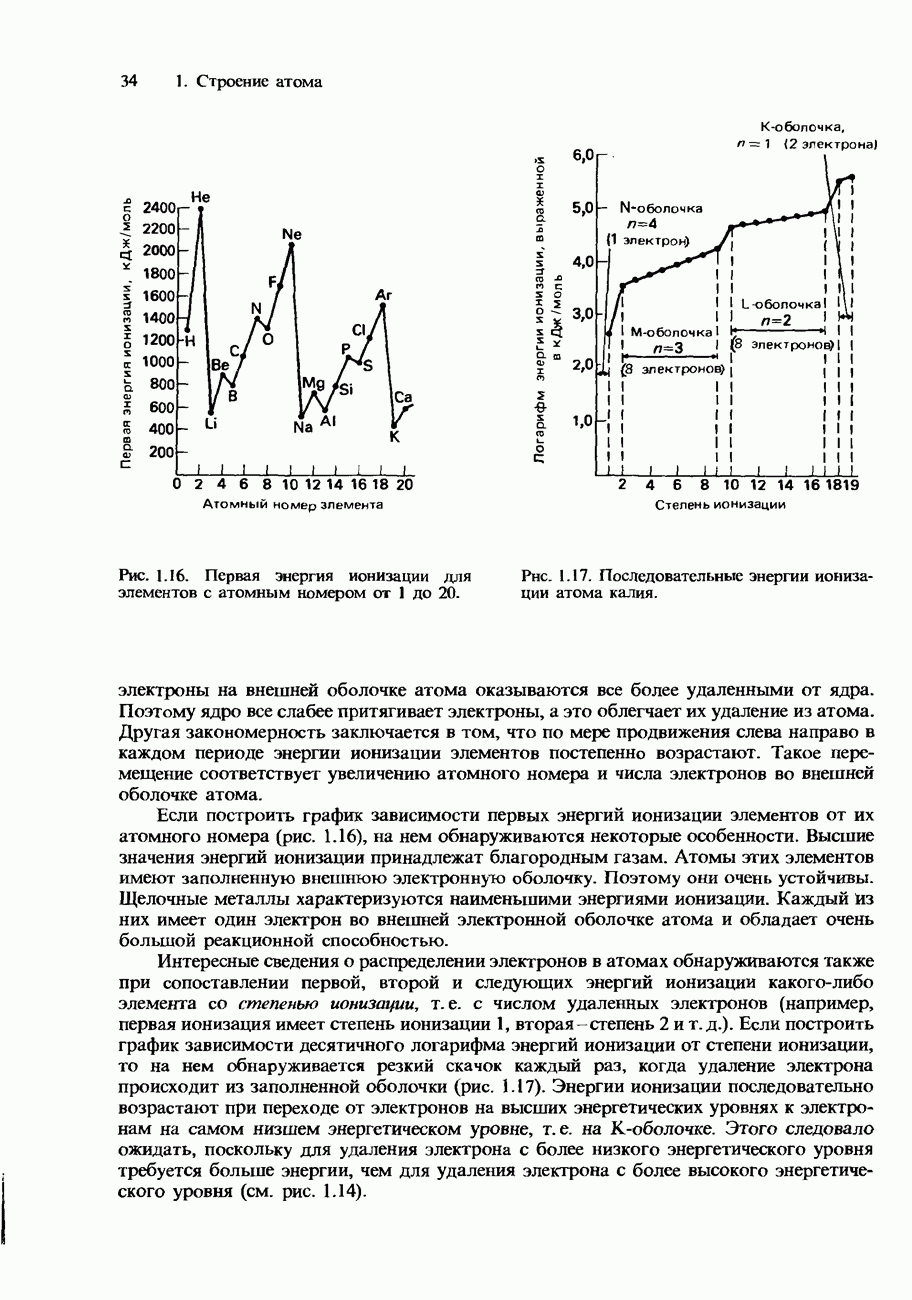
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
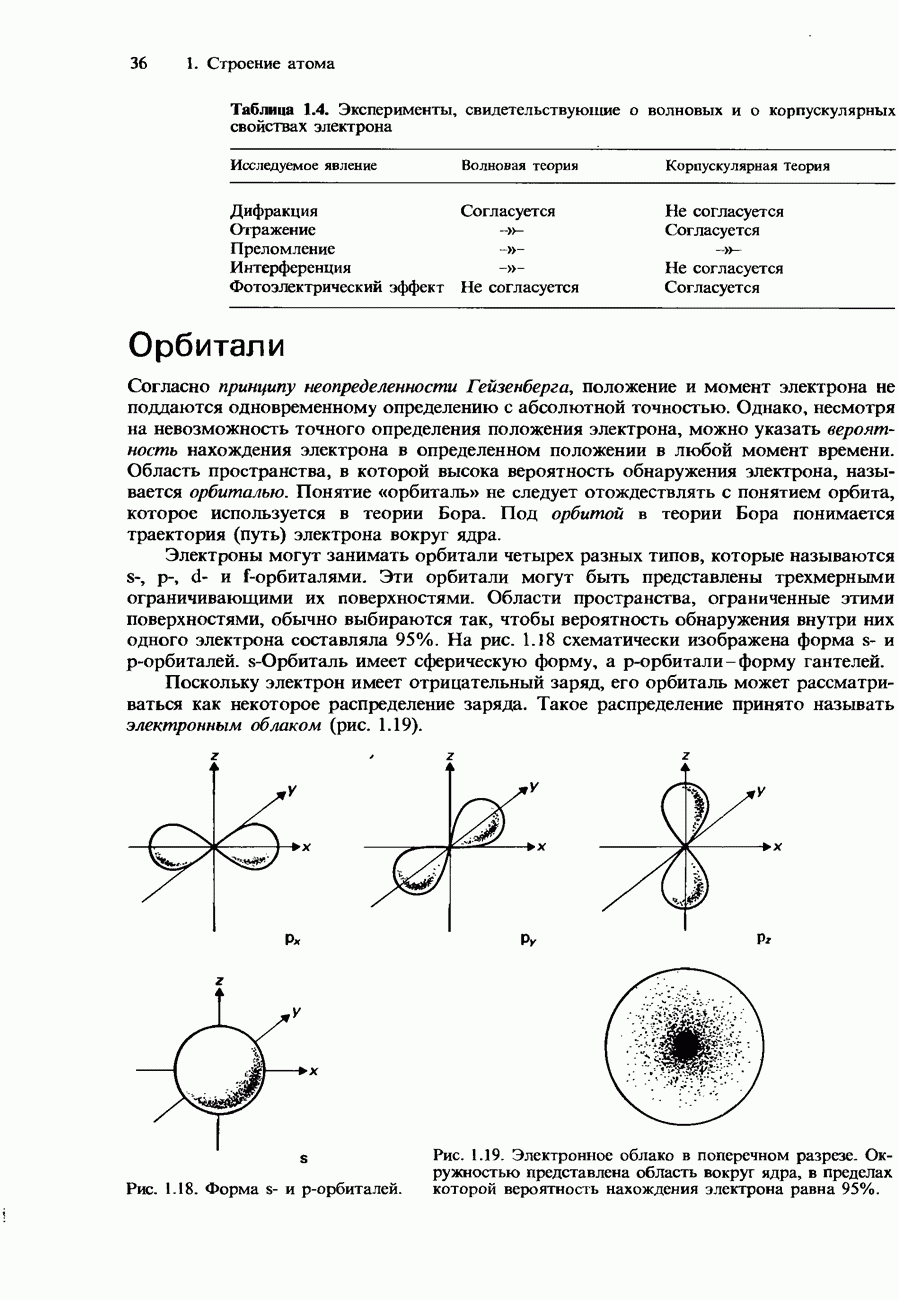
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
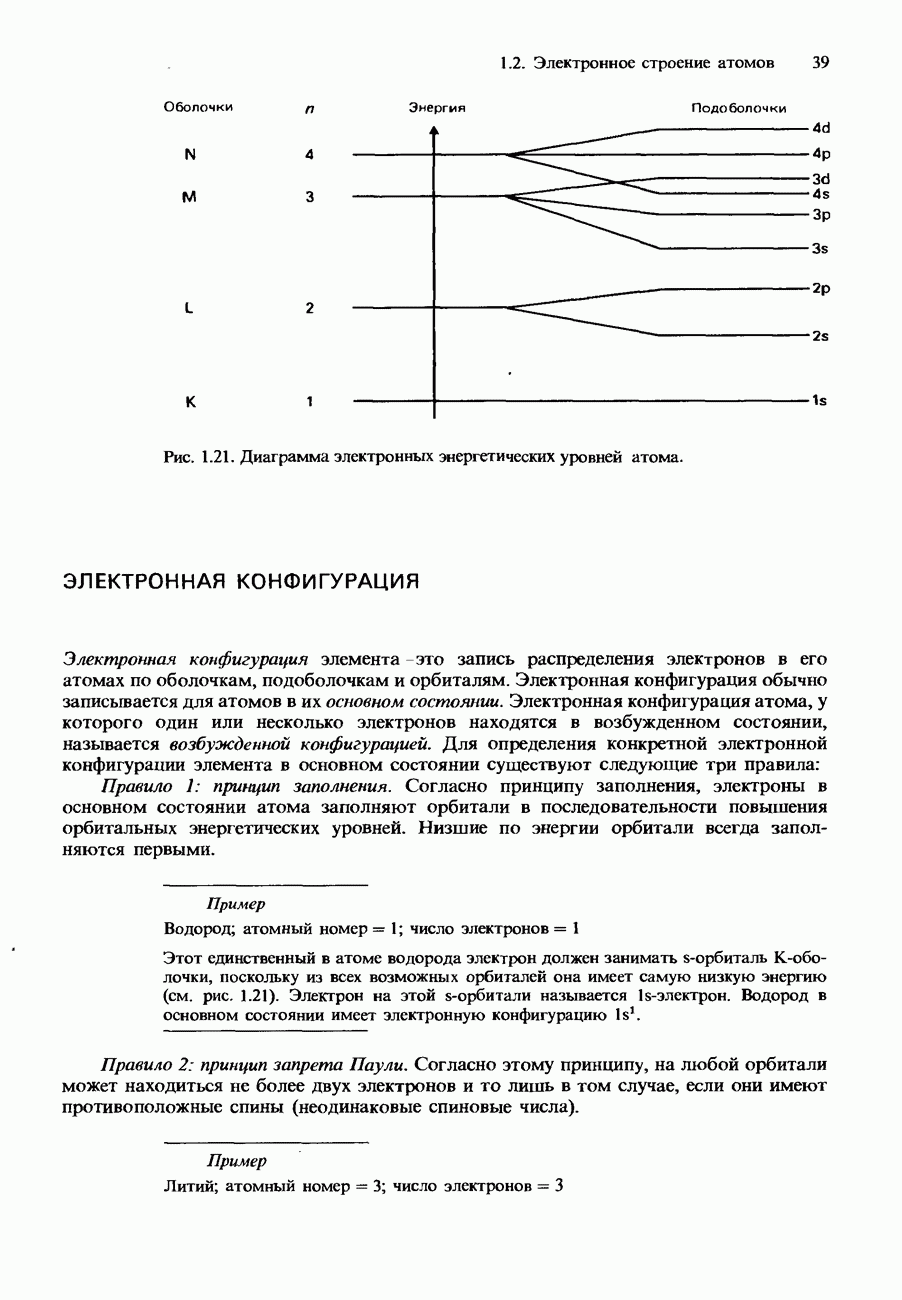
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
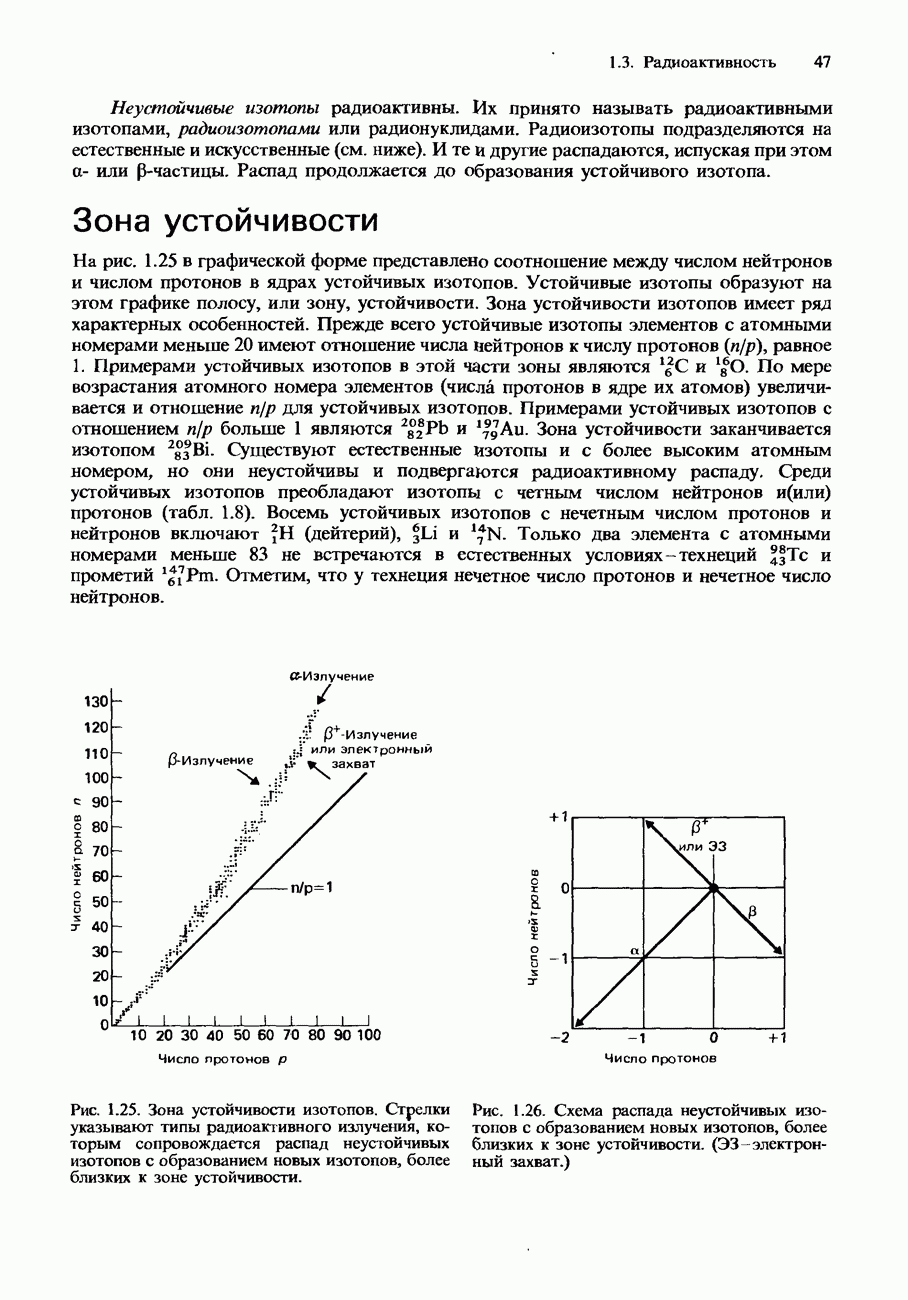
- Зона устойчивости
- Период полураспада
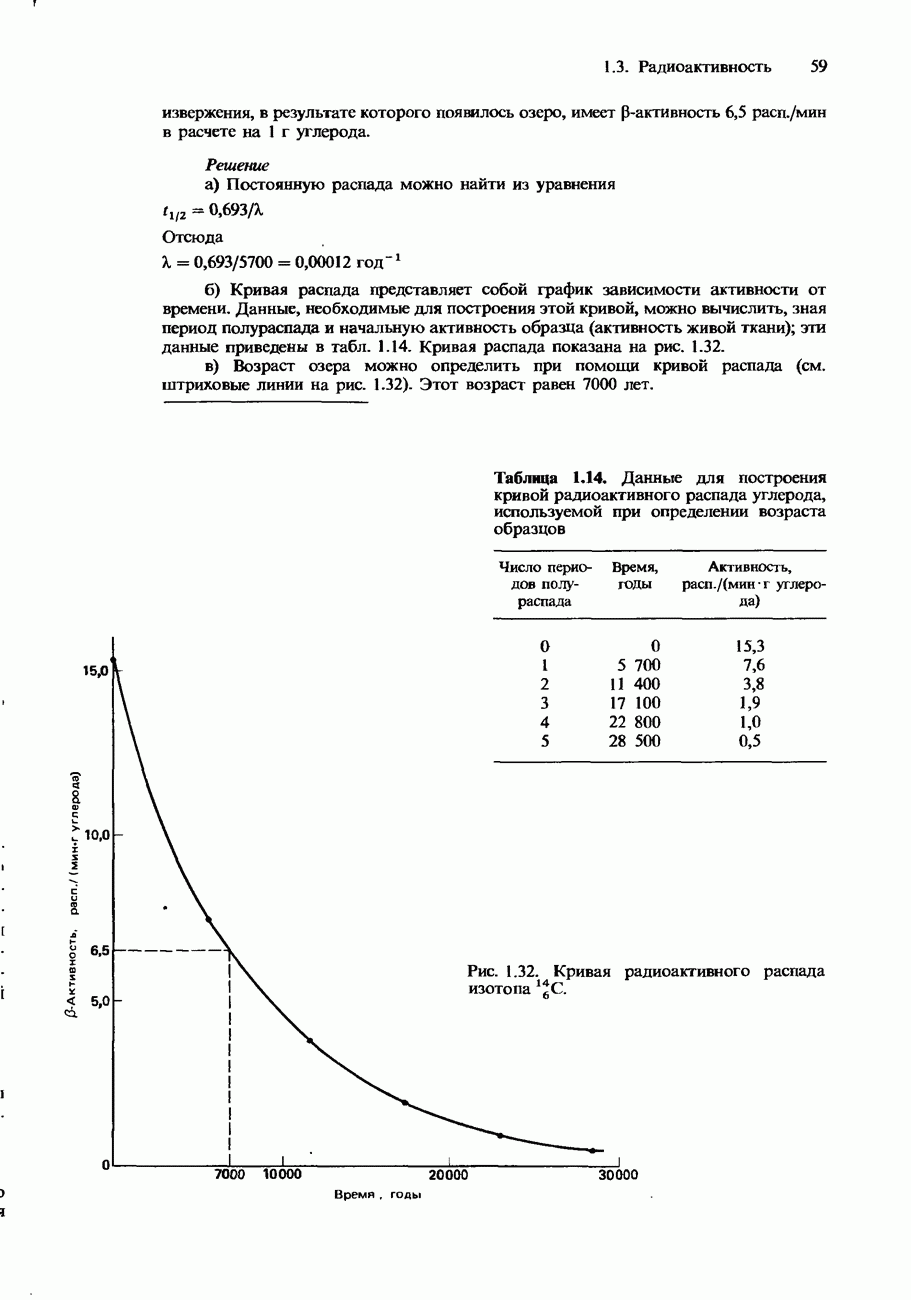
- Кривые распада
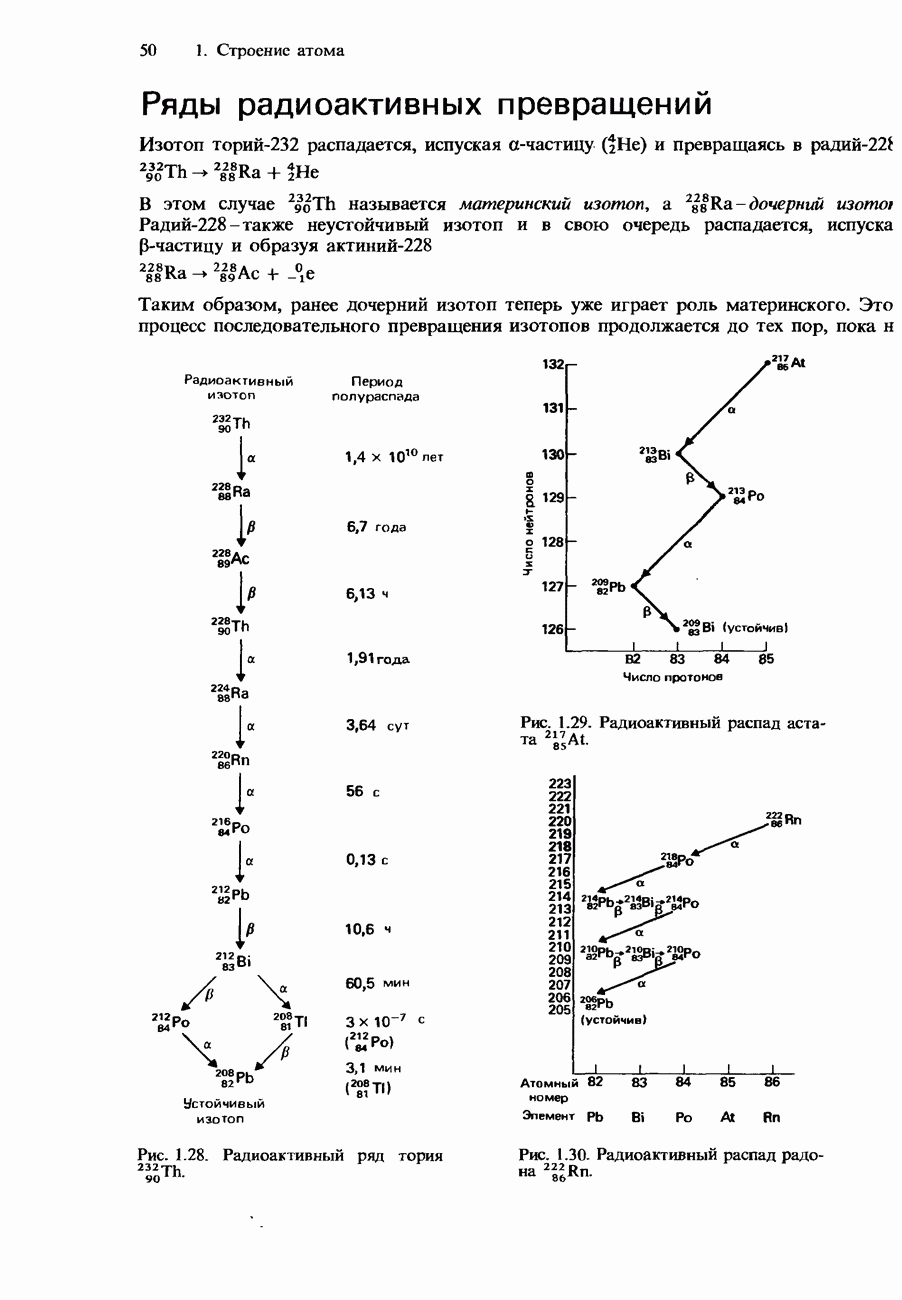
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
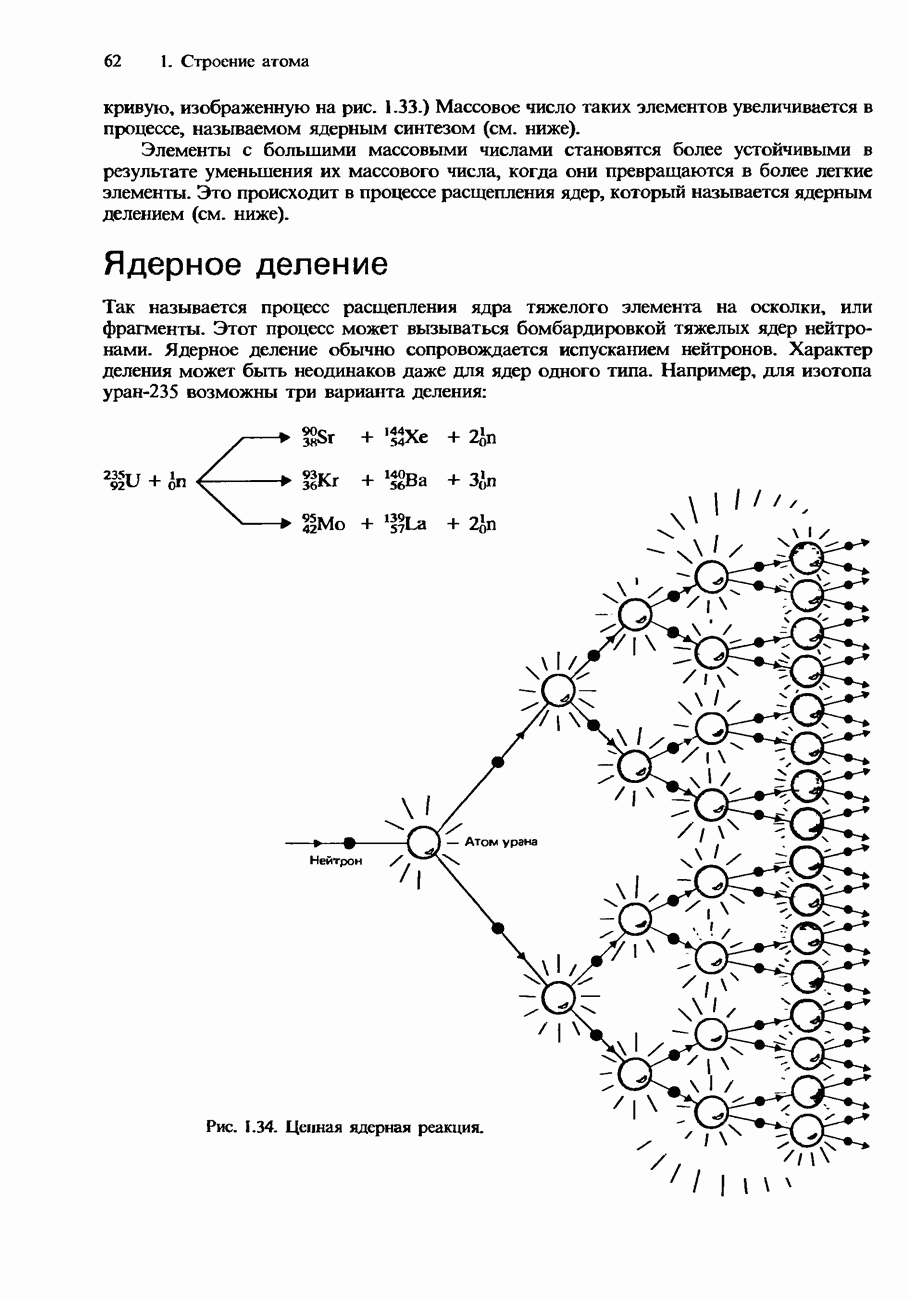
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
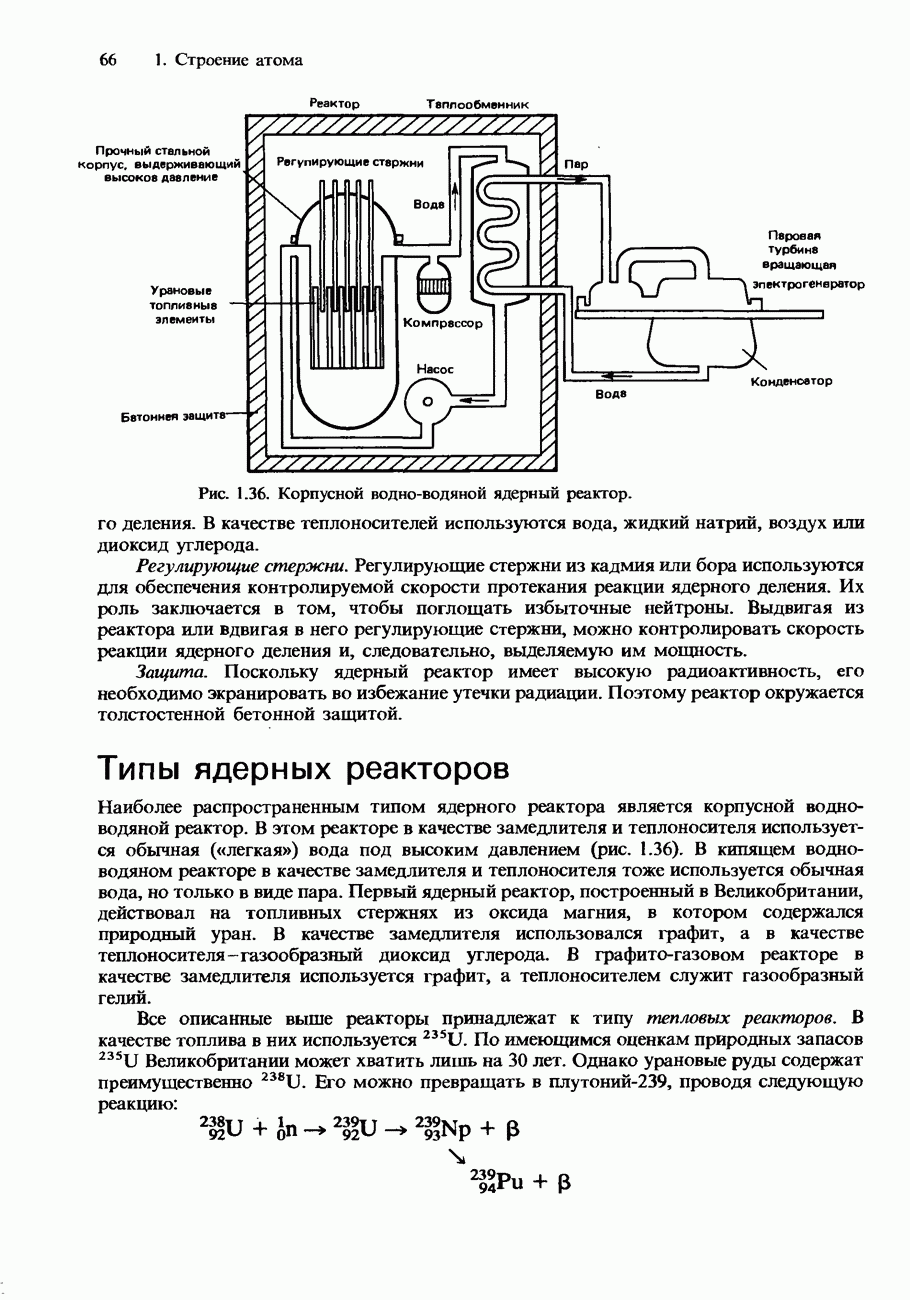
- Типы ядерных реакторов
- Радиоактивные ядерные отходы и их переработка
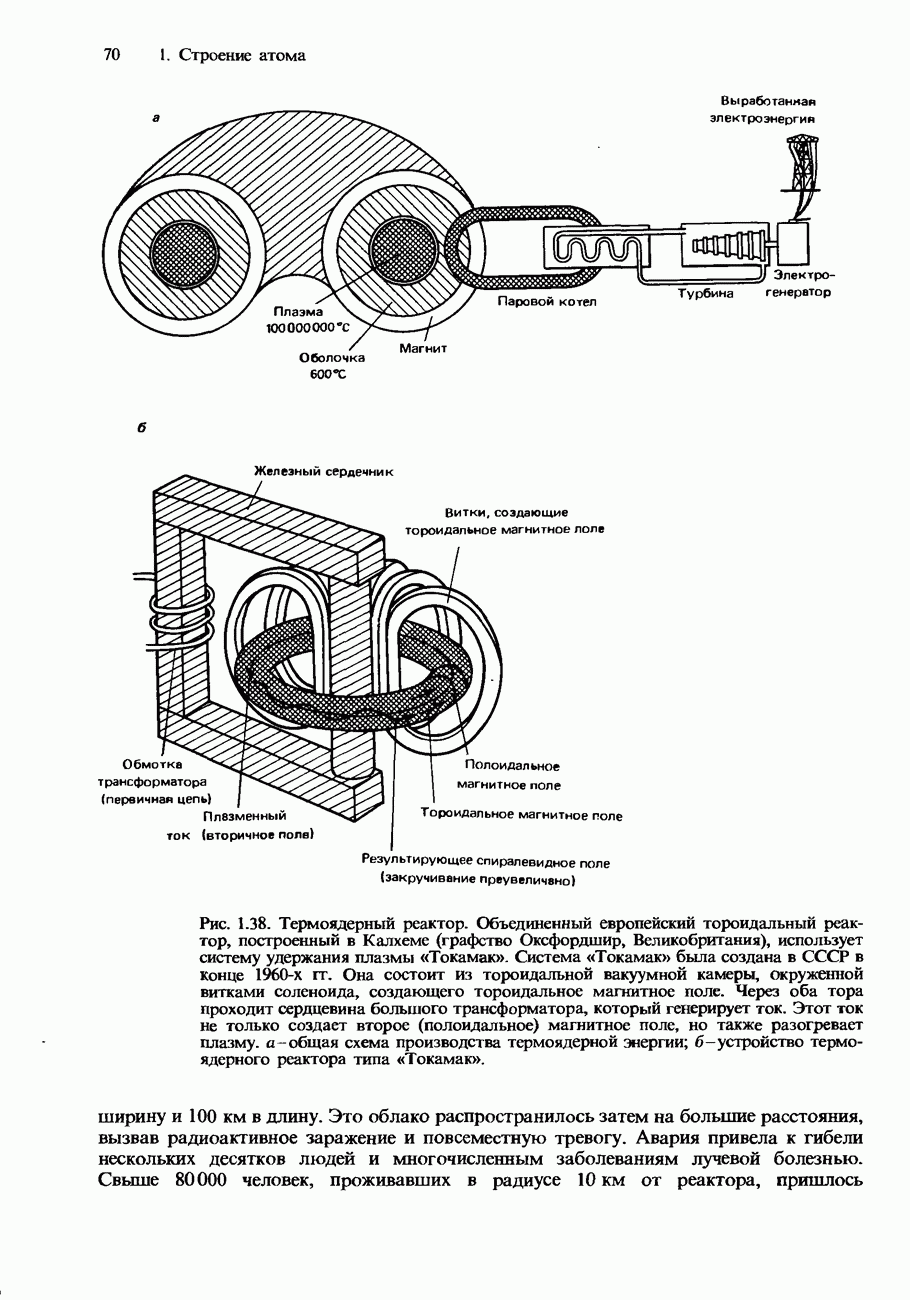
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
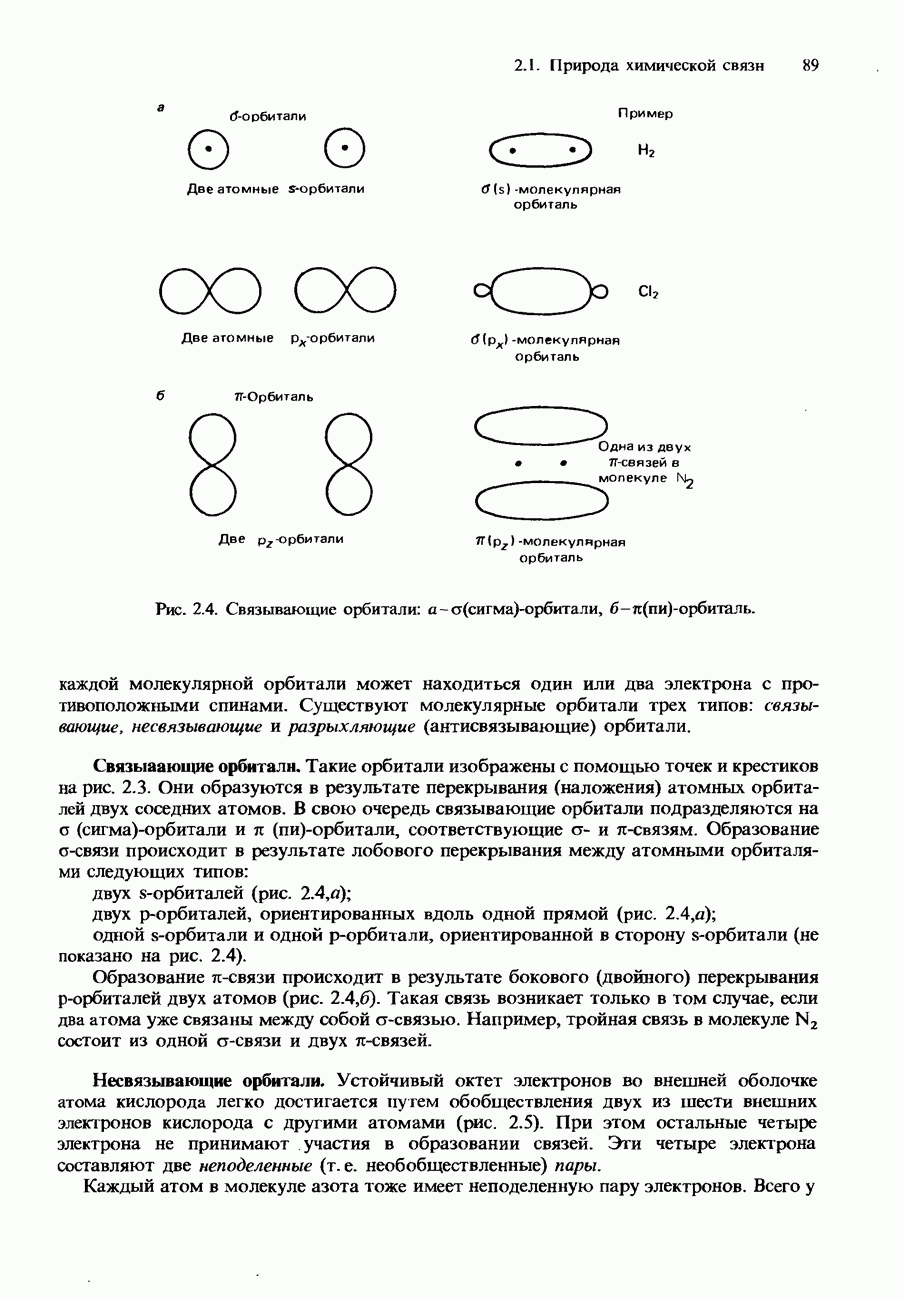
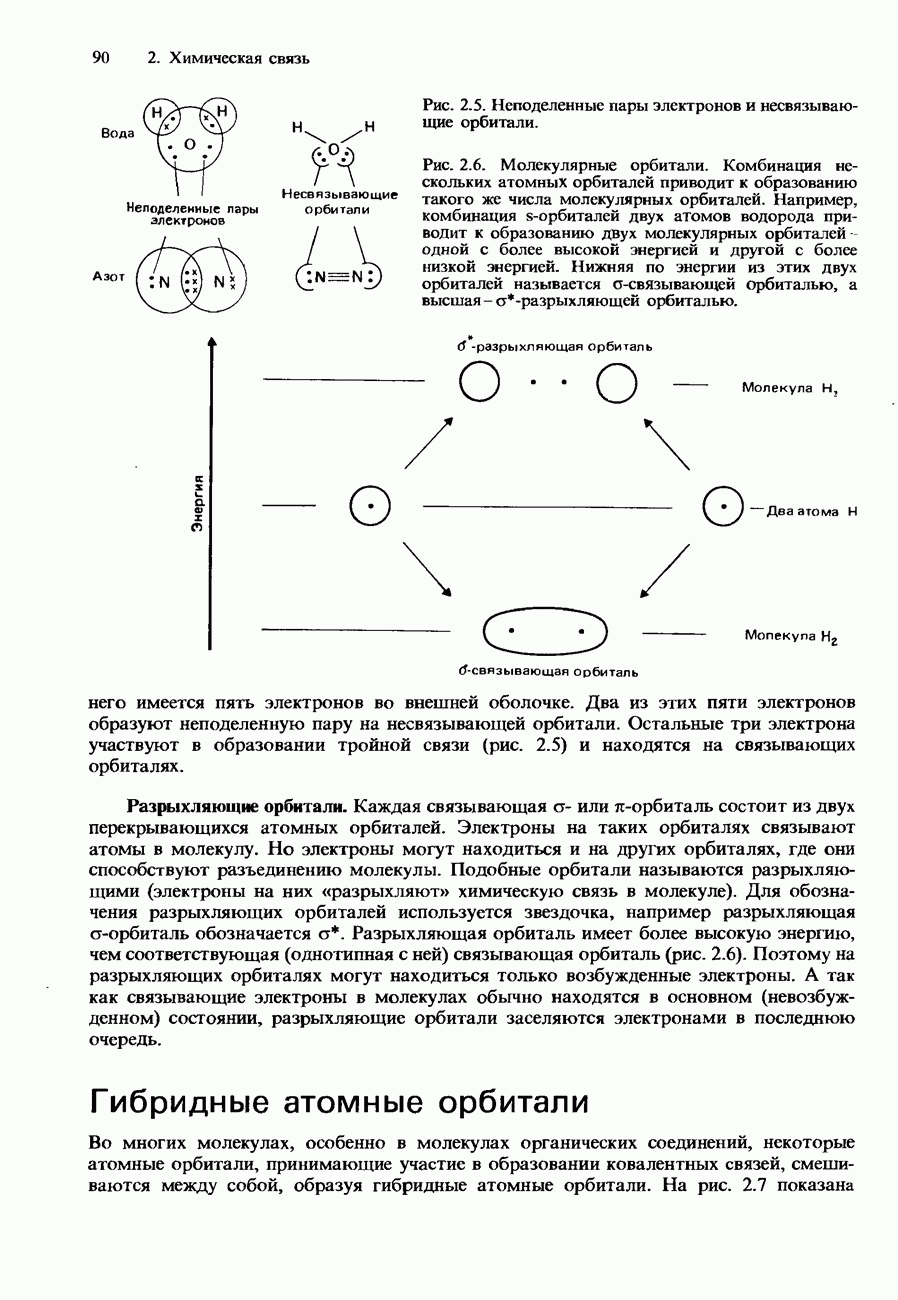
- Молекулярные орбитали
- Гибридные атомные орбитали
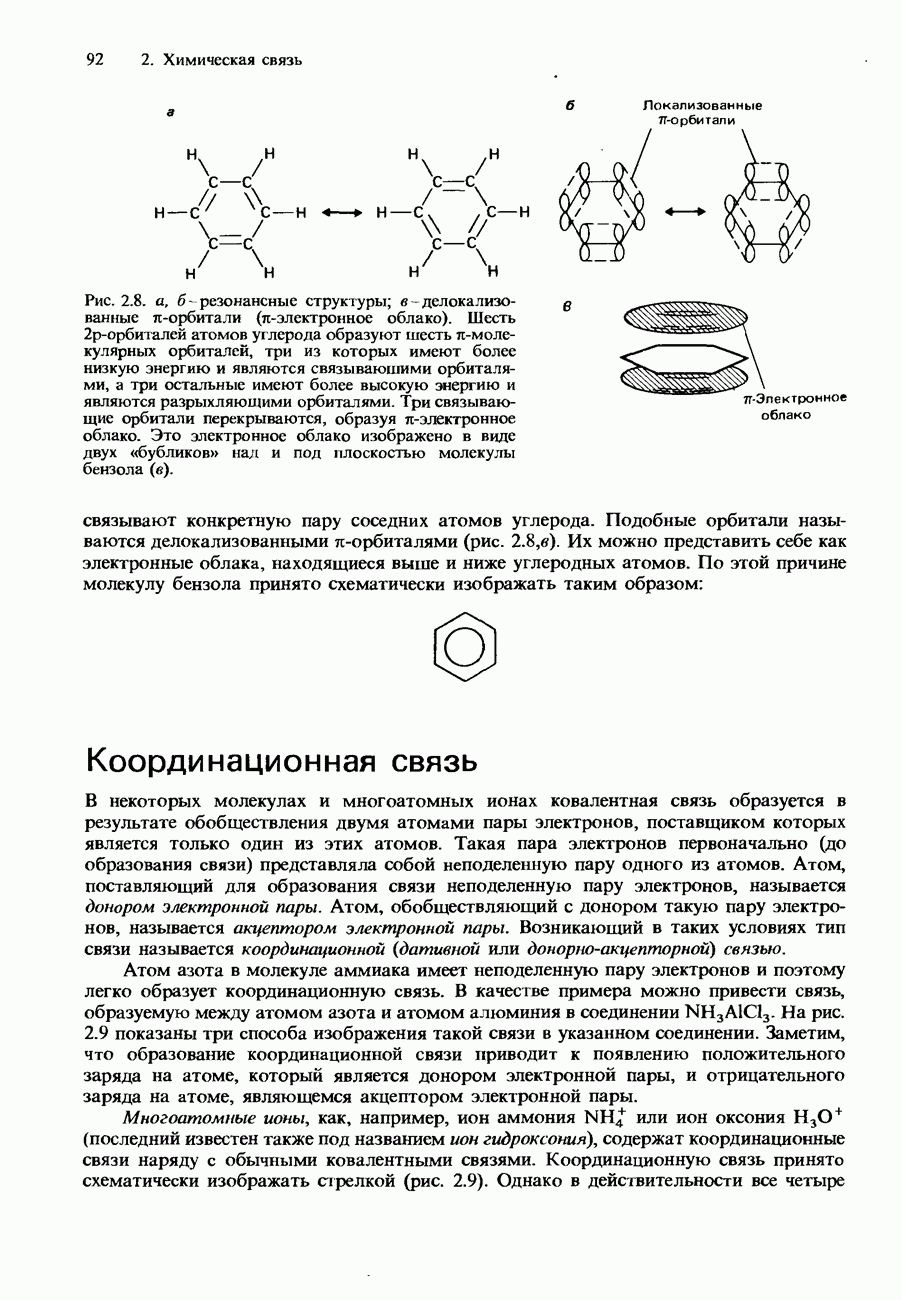
- Делокализованные орбитали
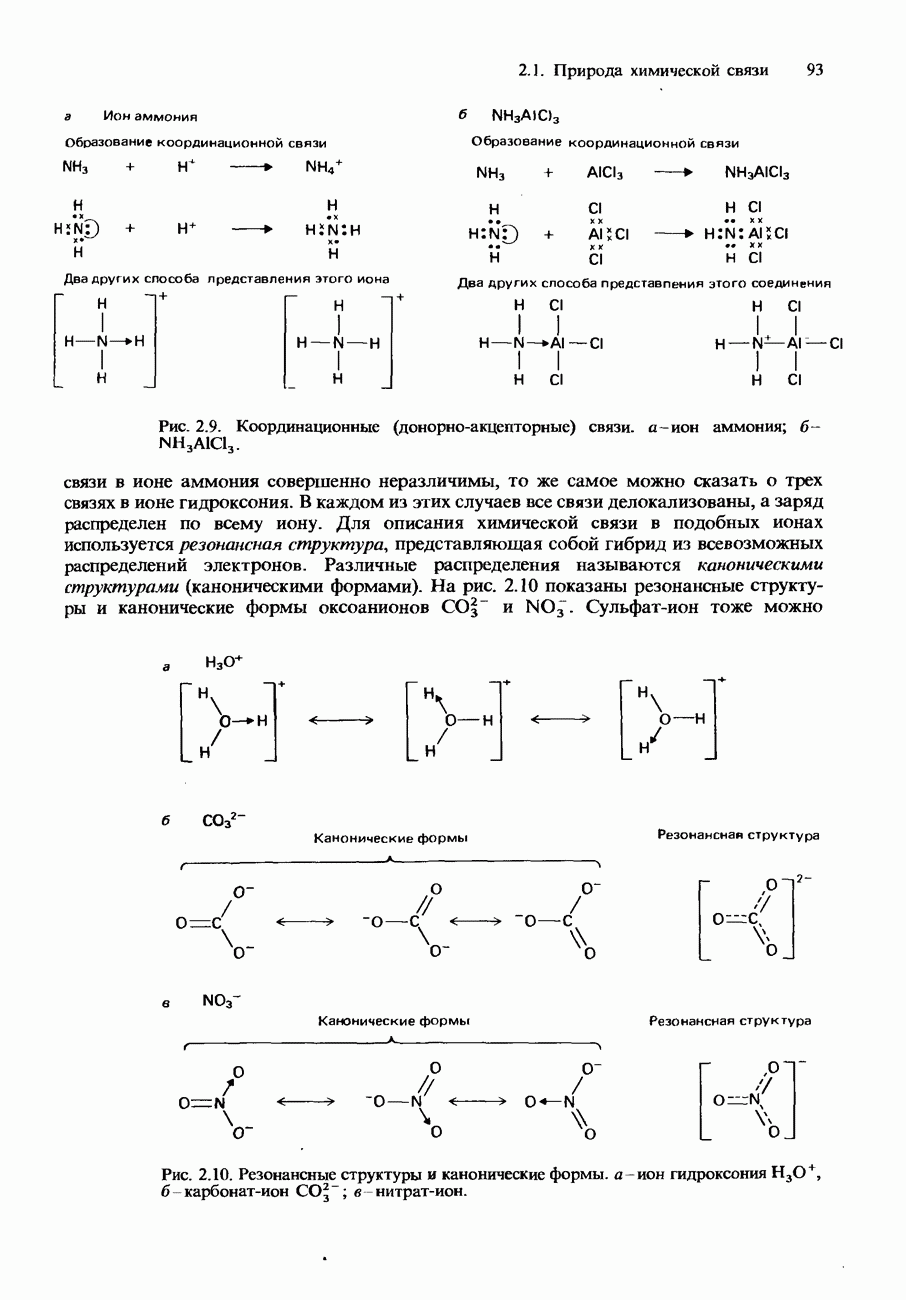
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
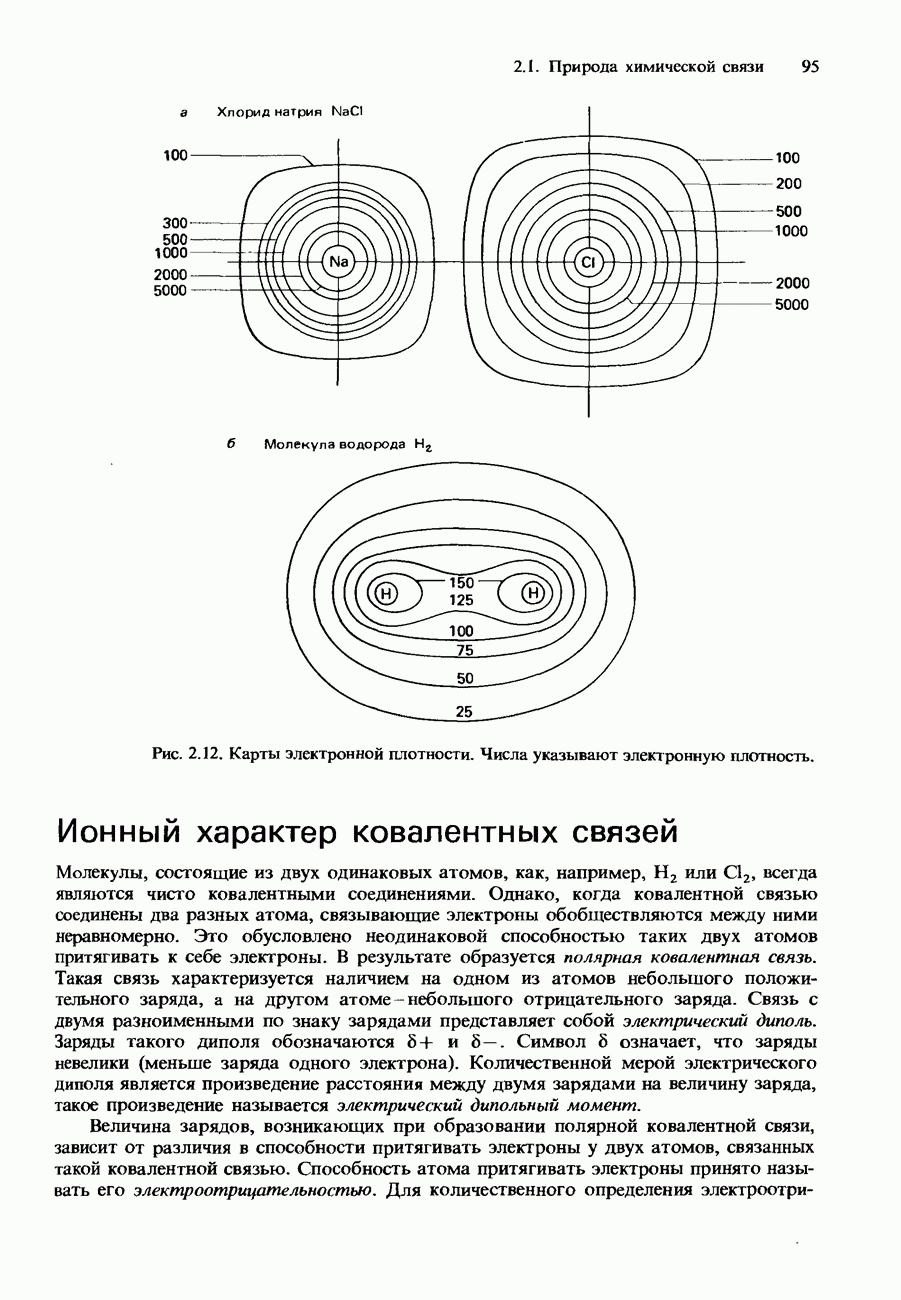
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
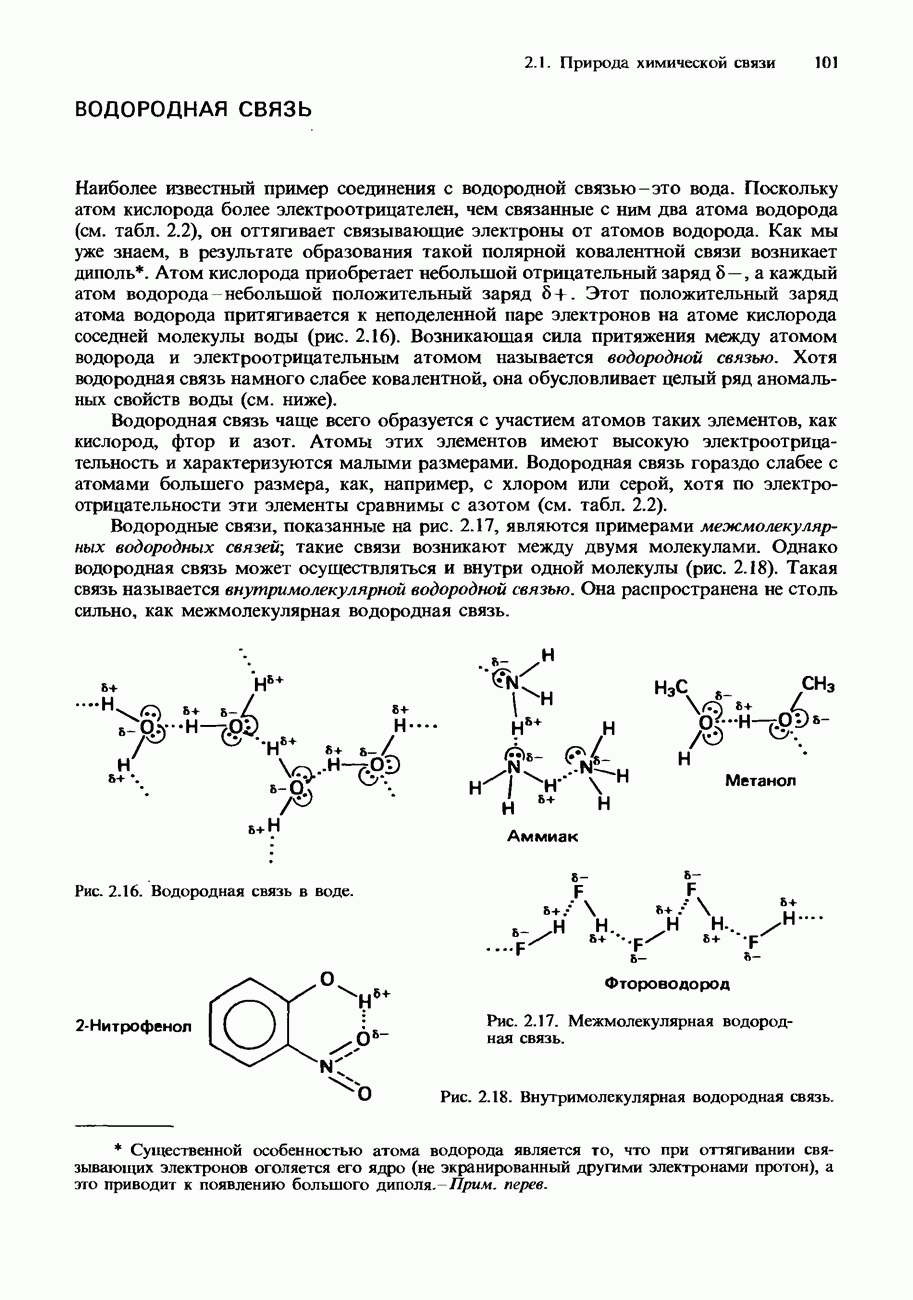
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
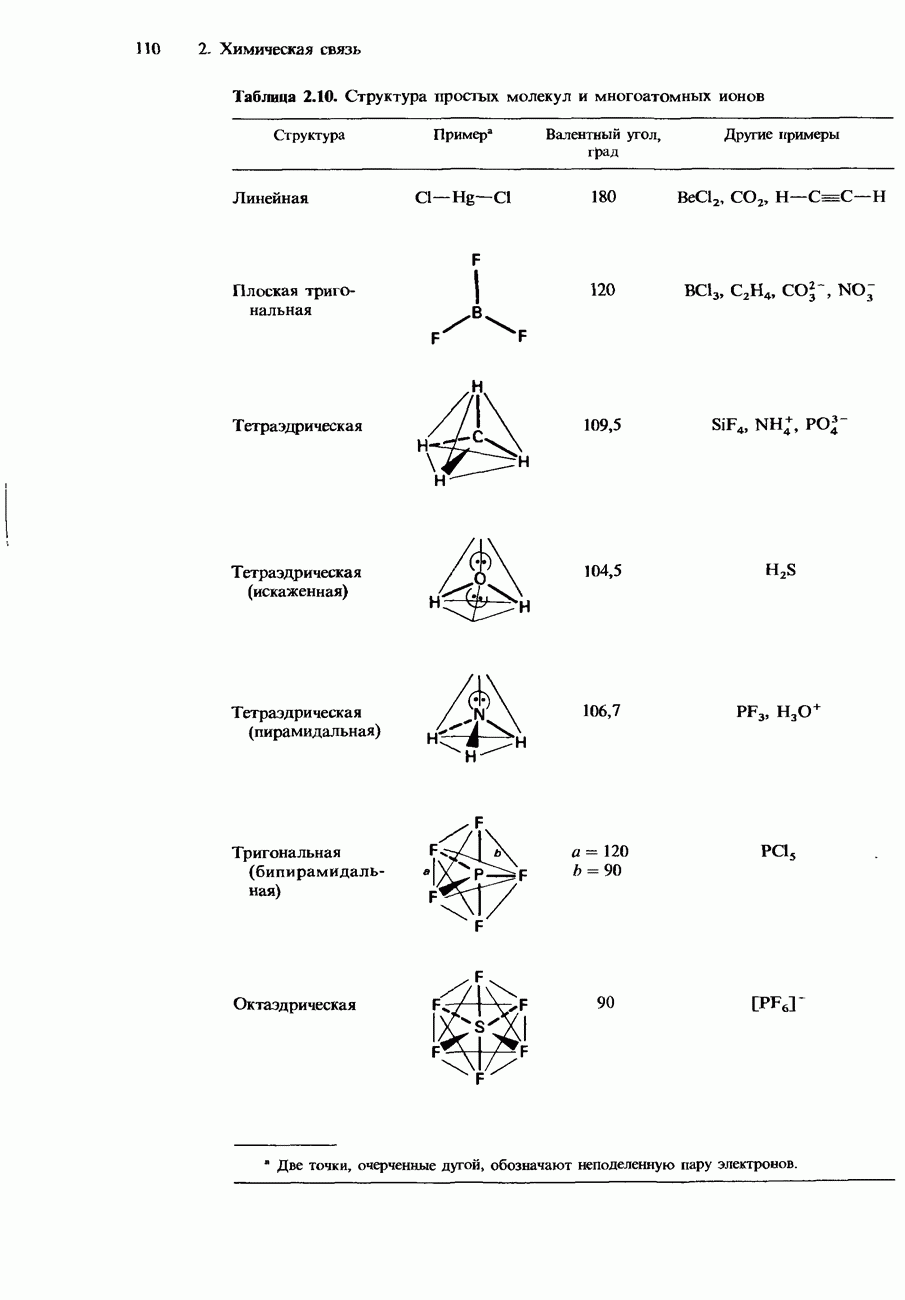
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
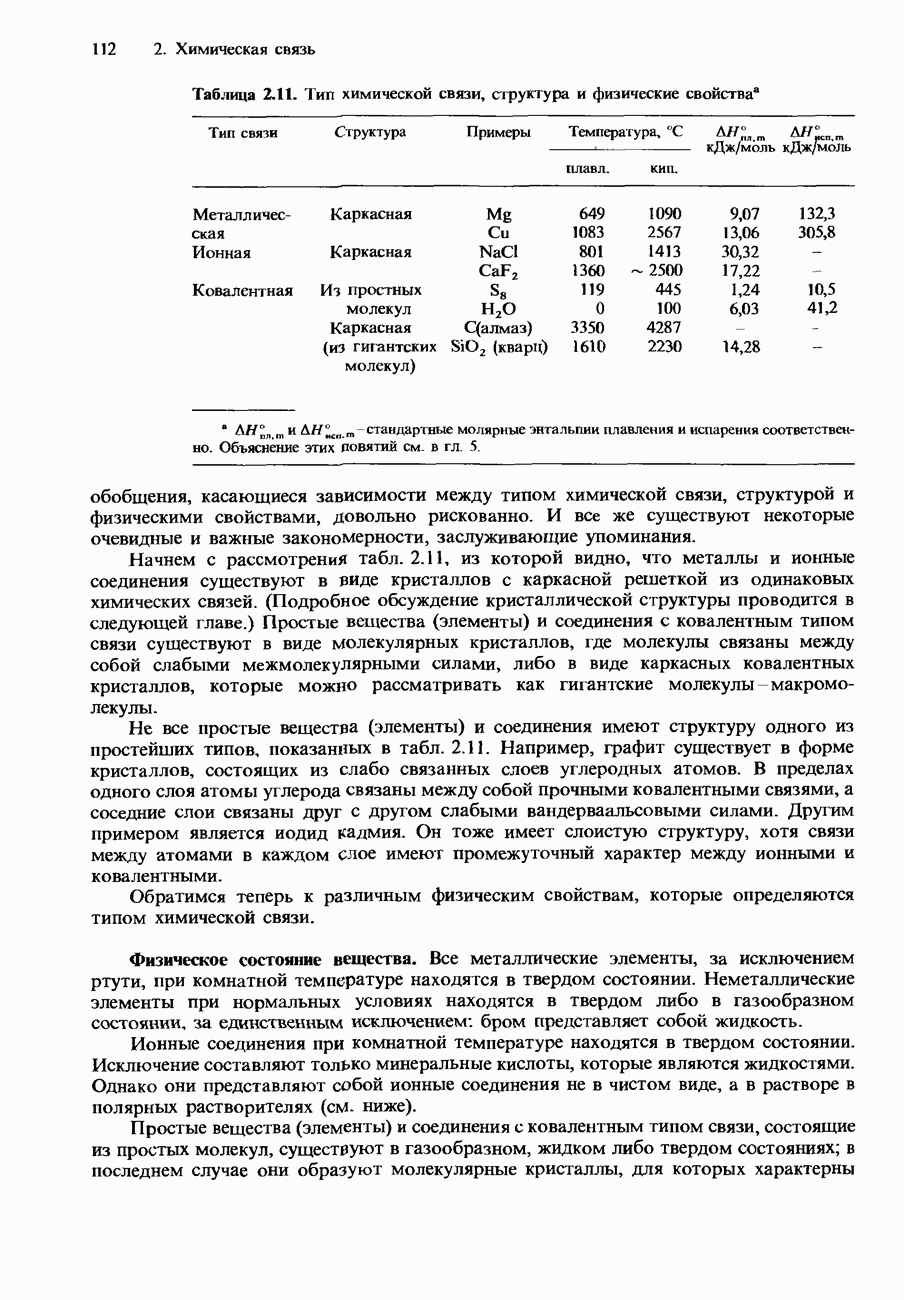
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
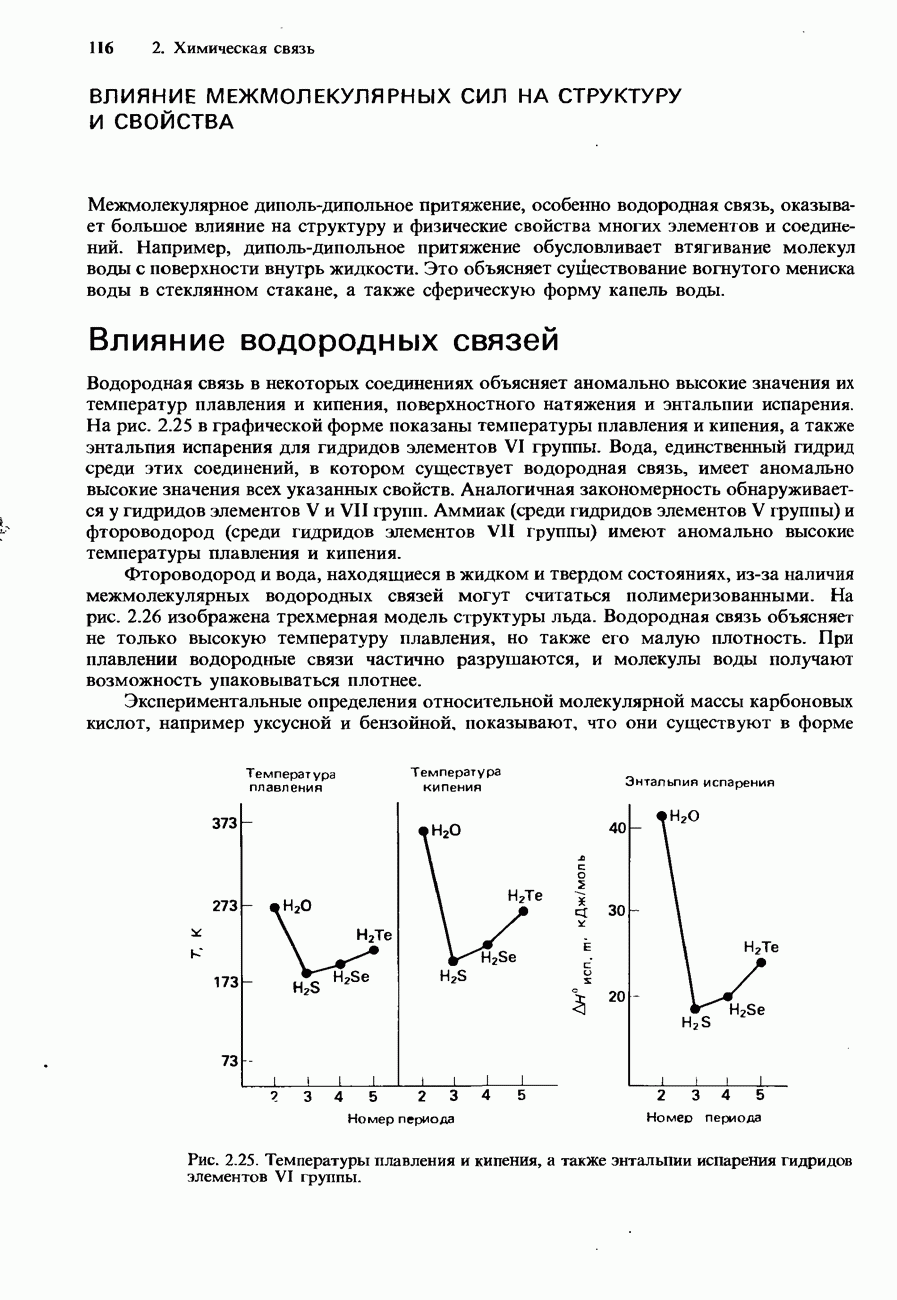
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
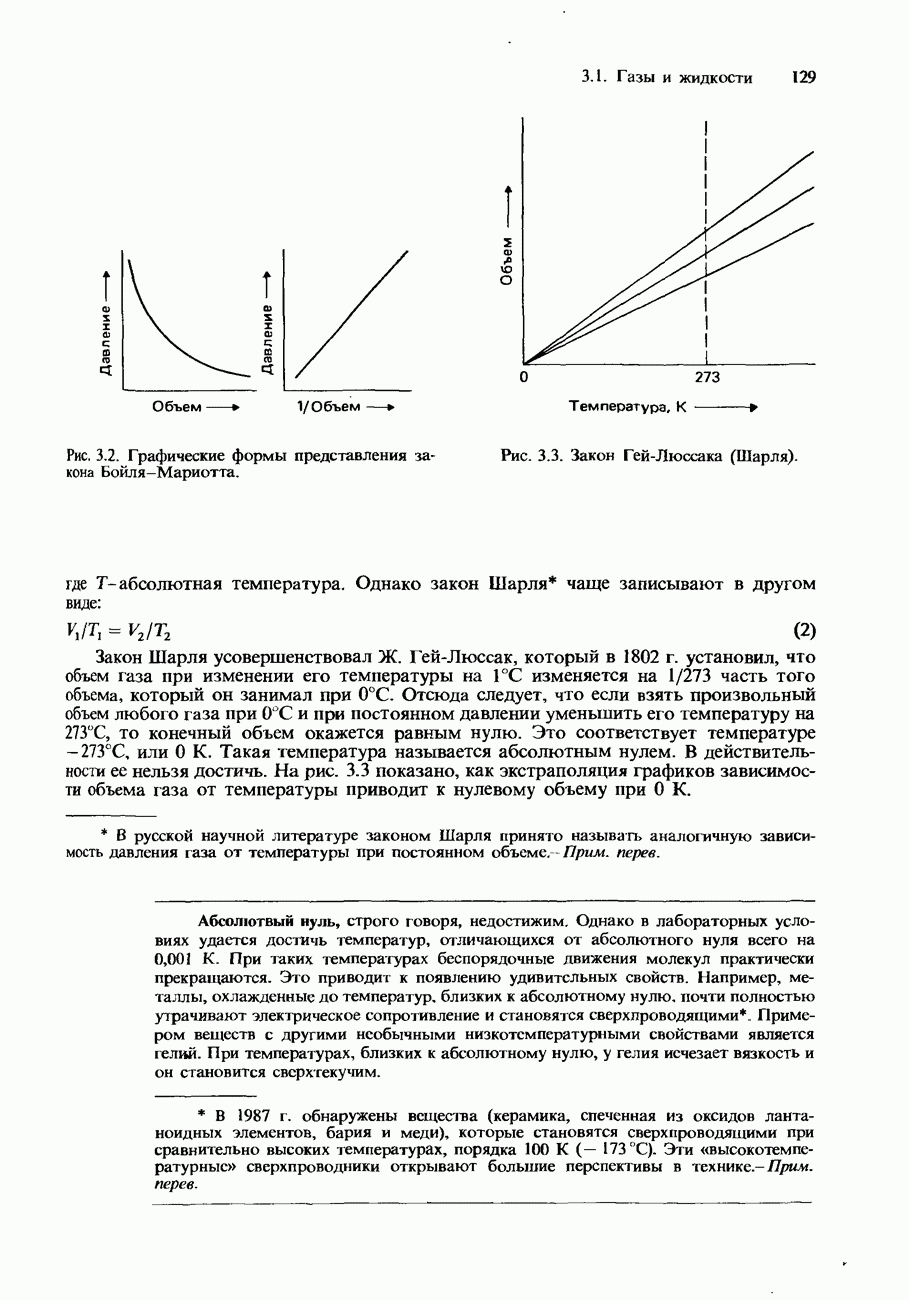
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
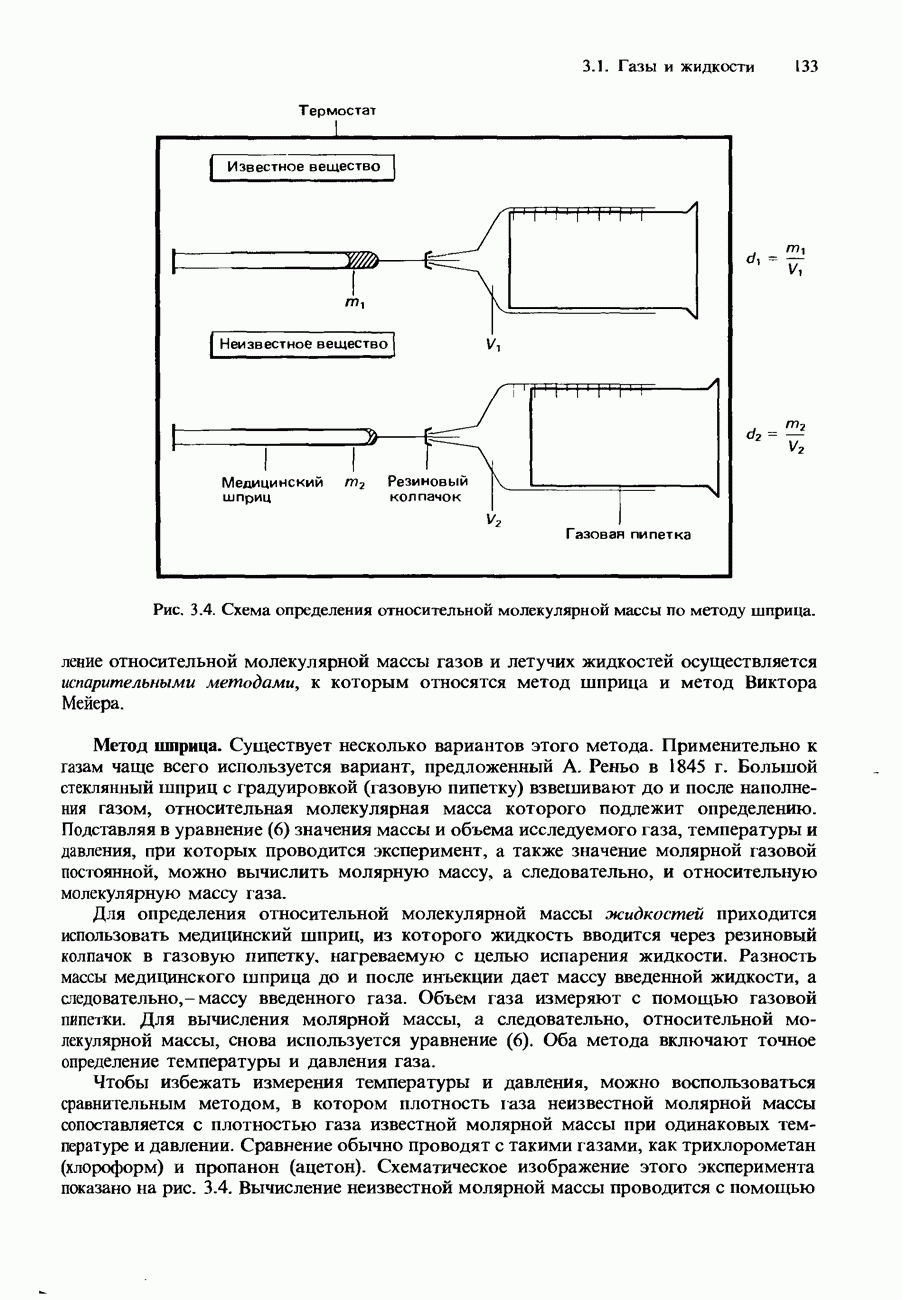
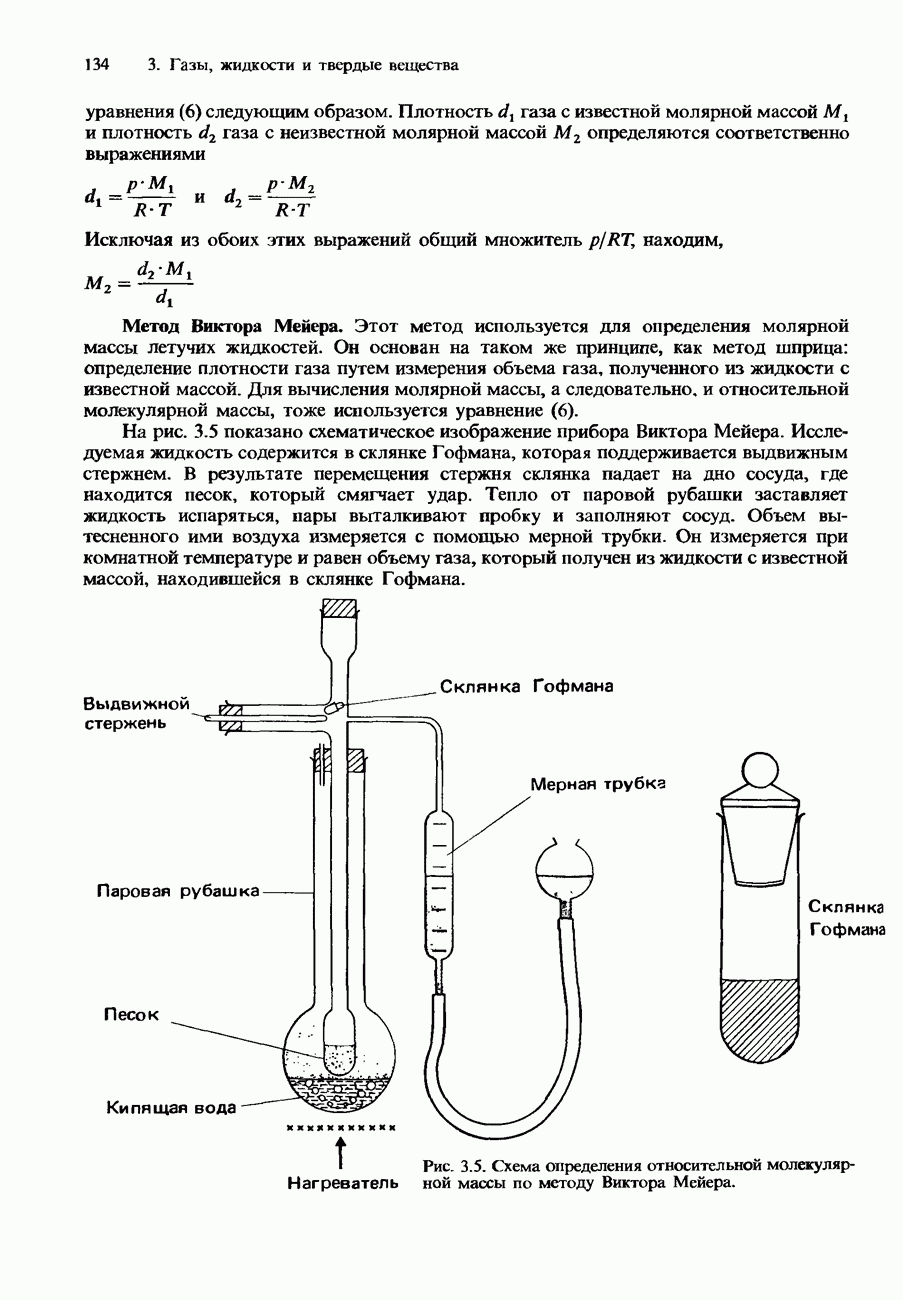
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
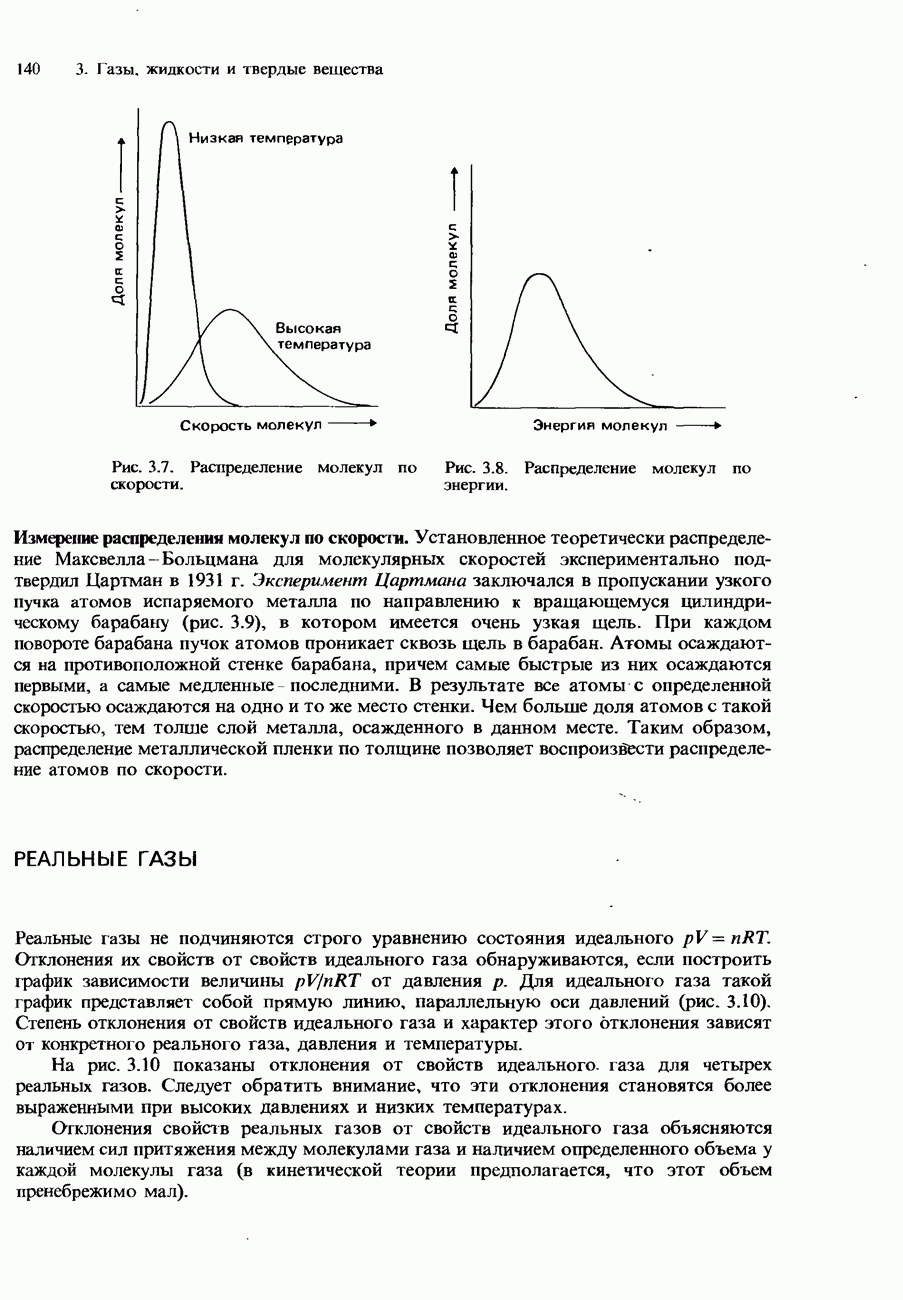
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
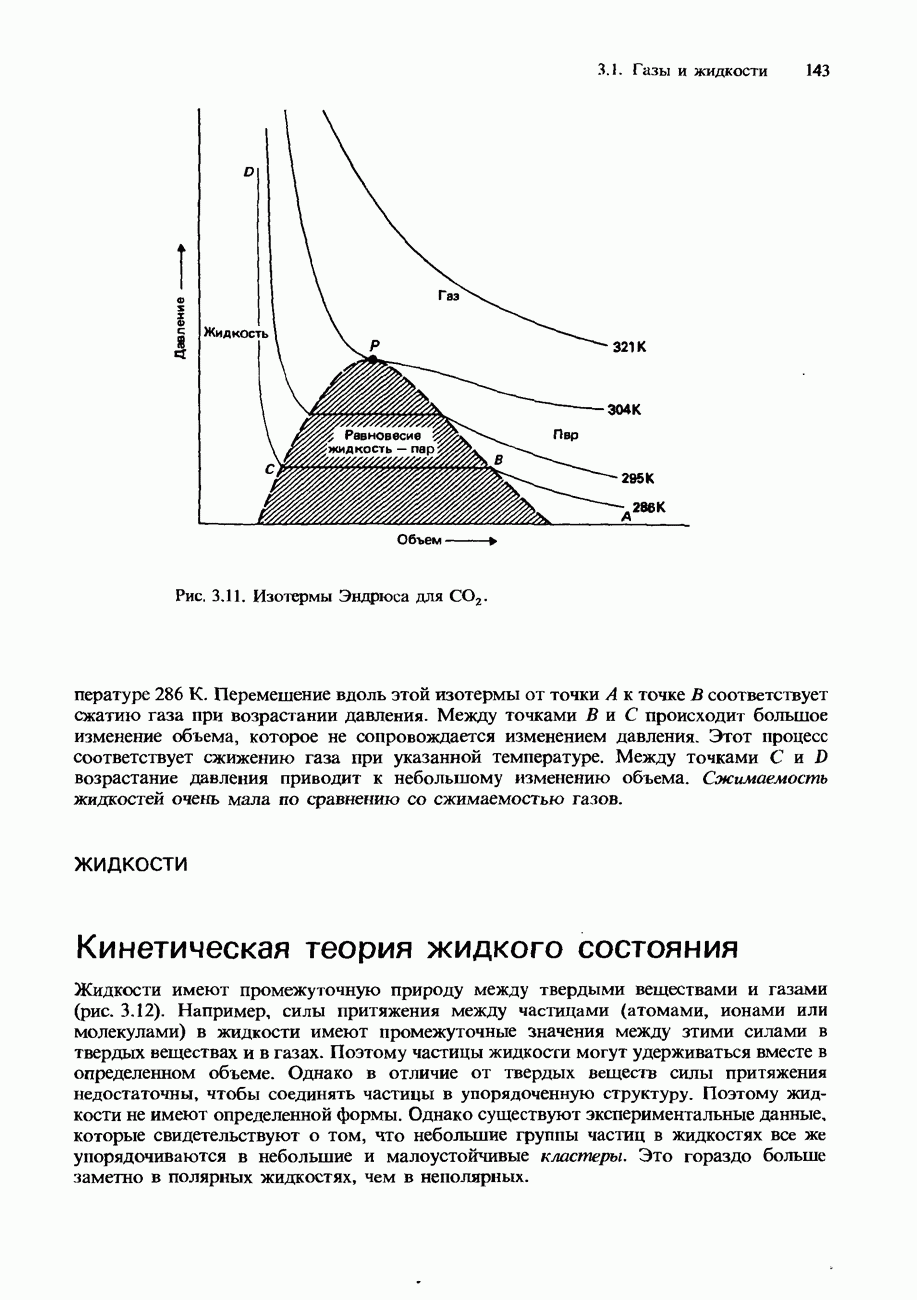
- Сжижение газов
- ЖИДКОСТИ
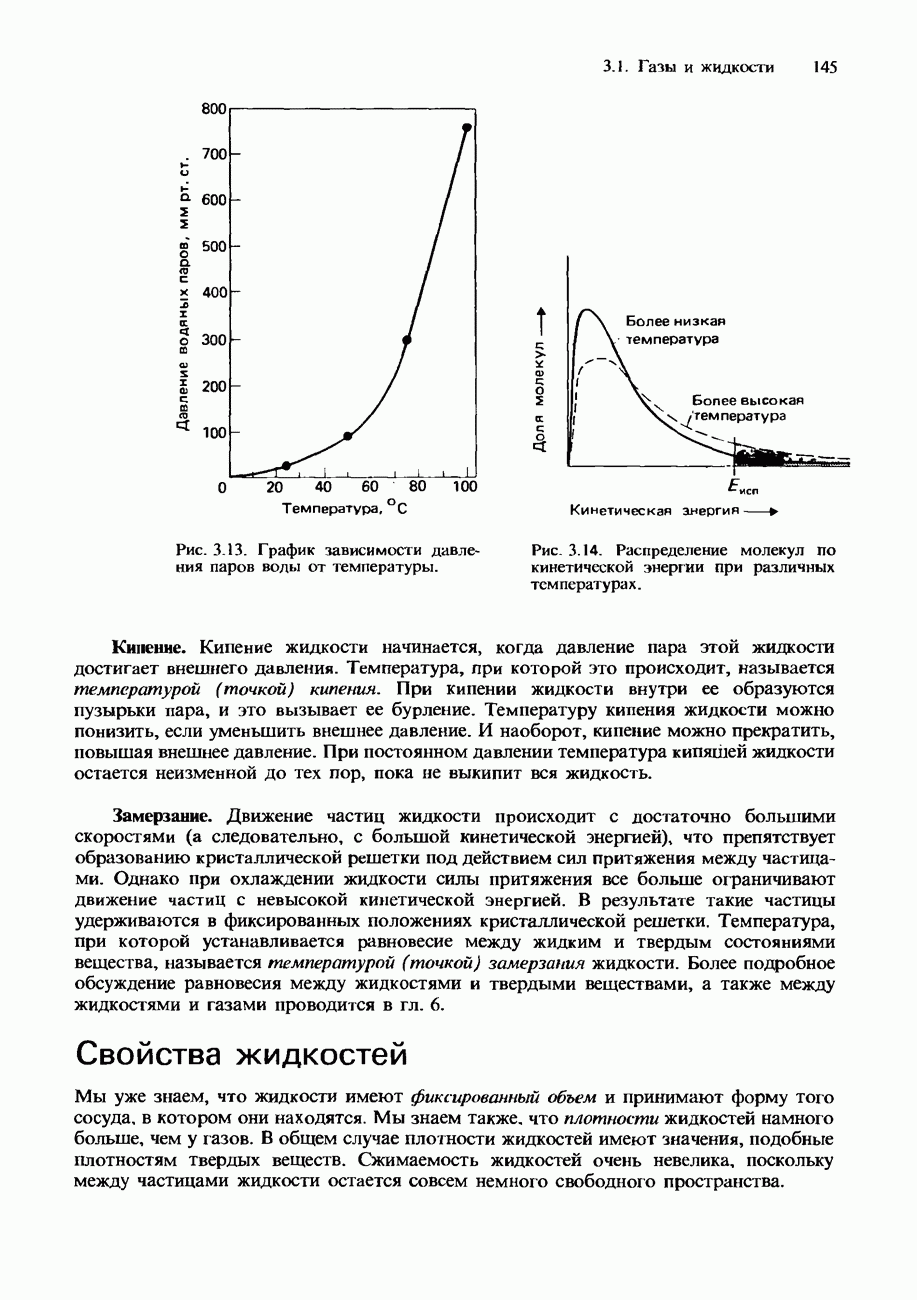
- Свойства жидкостей
- 3.2. Твердые вещества
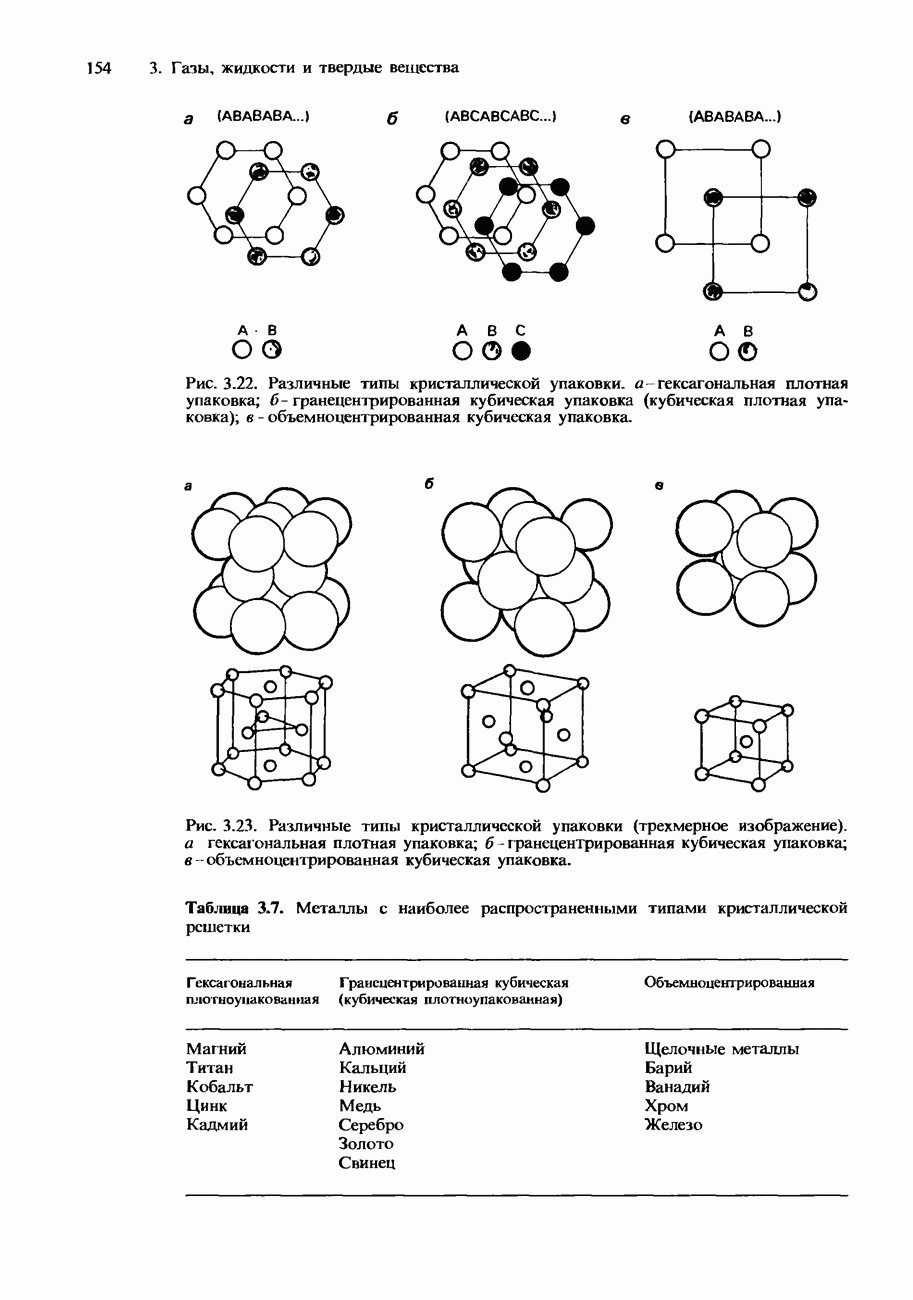
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
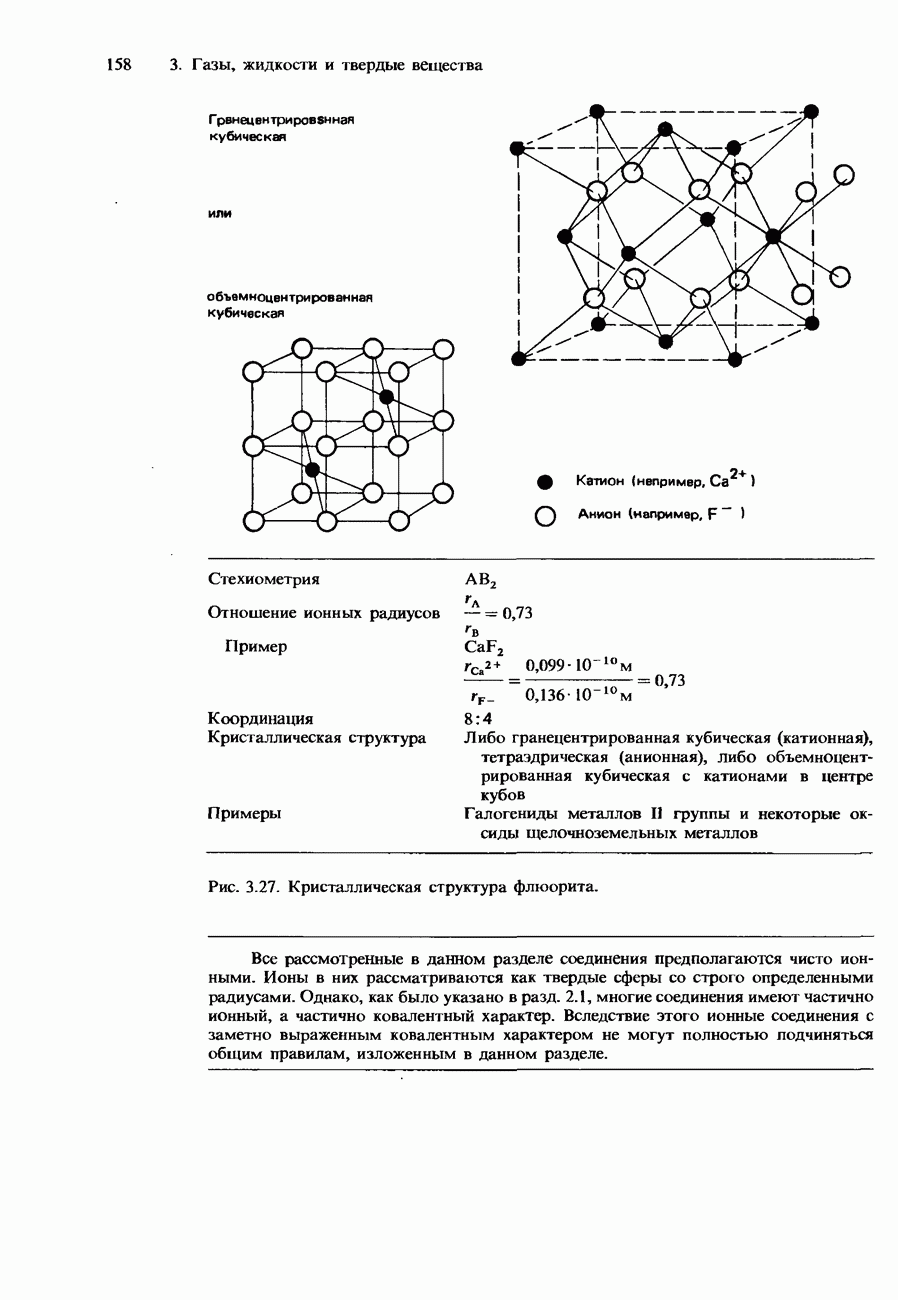
- Ионные кристаллы
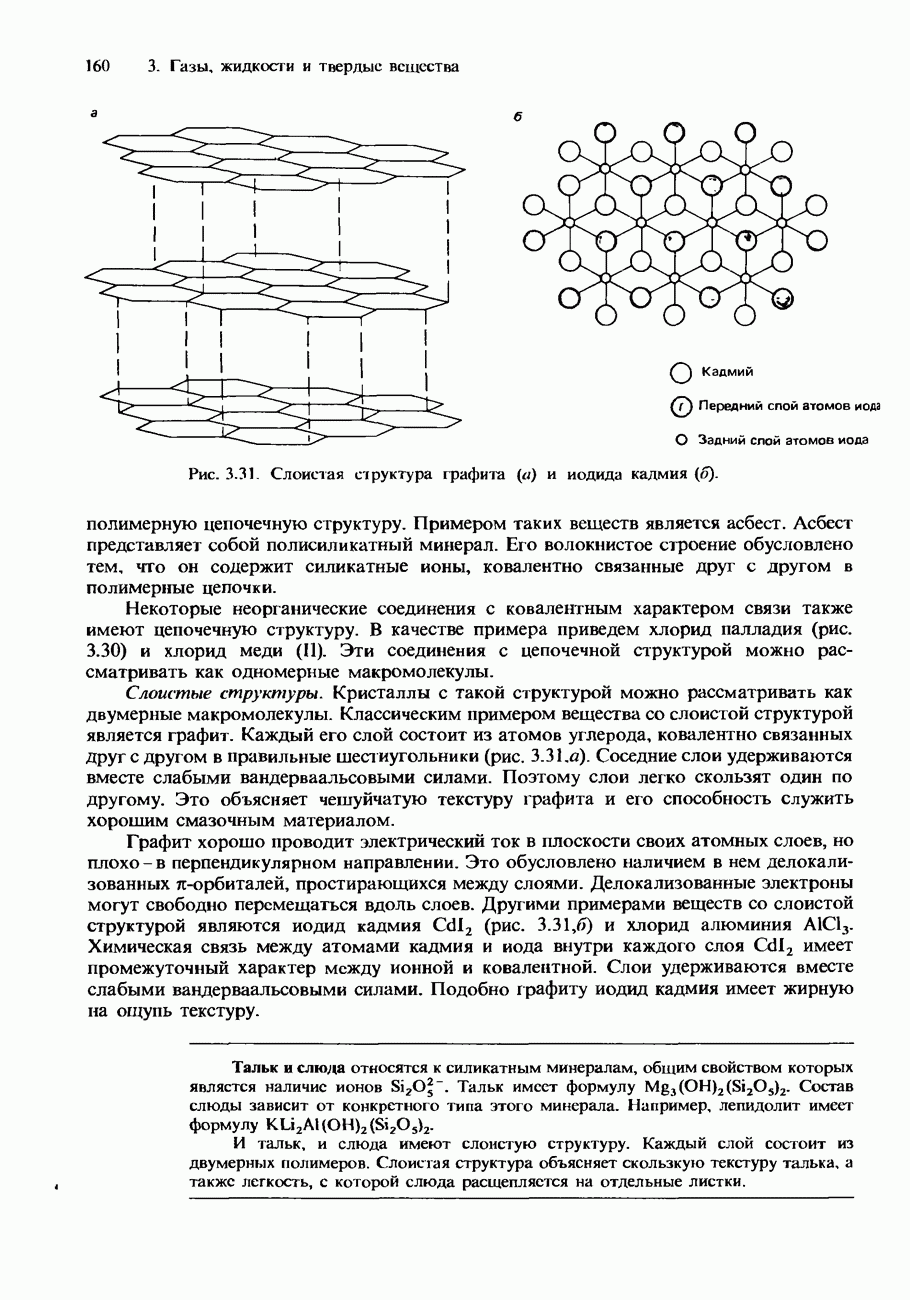
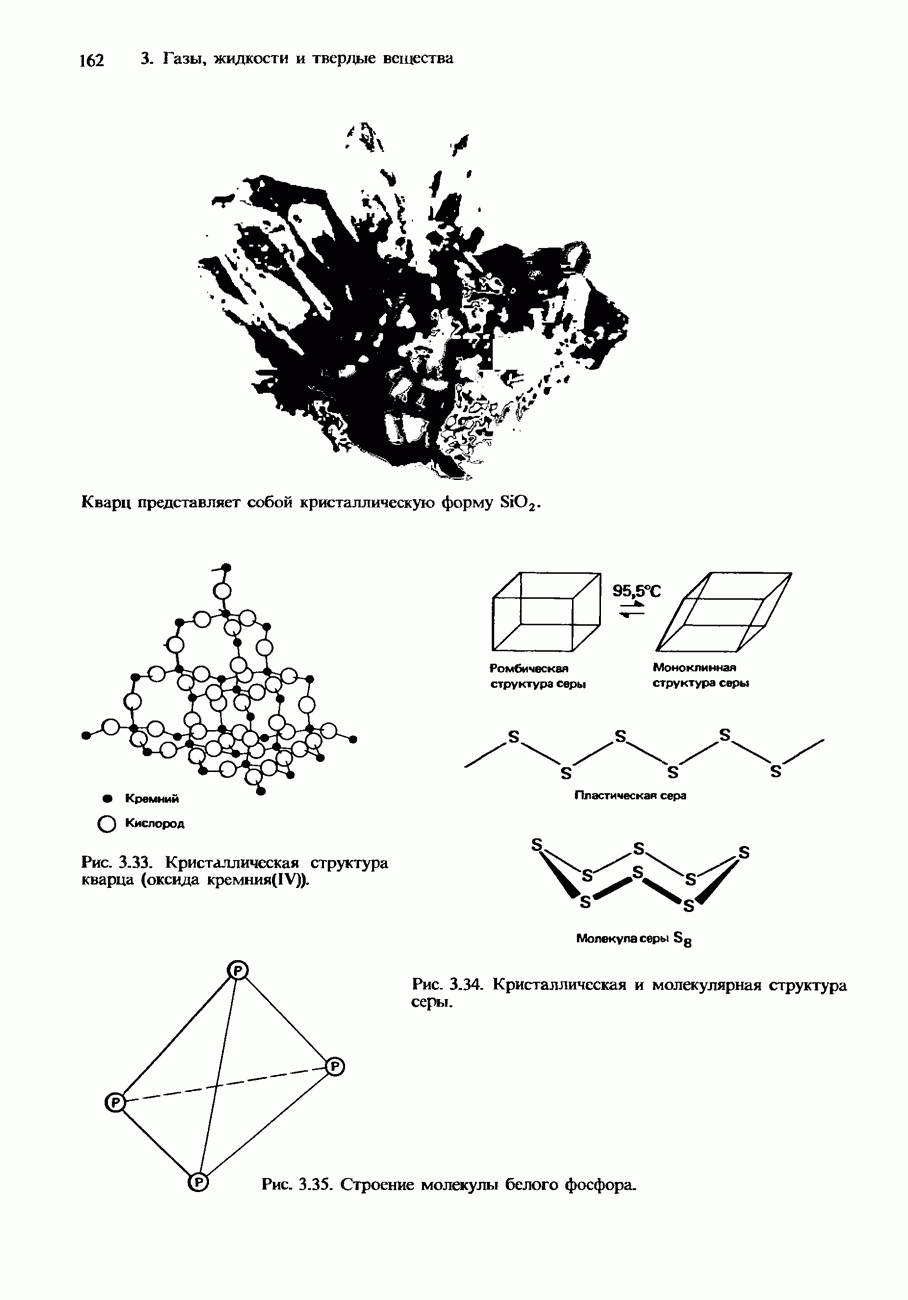
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
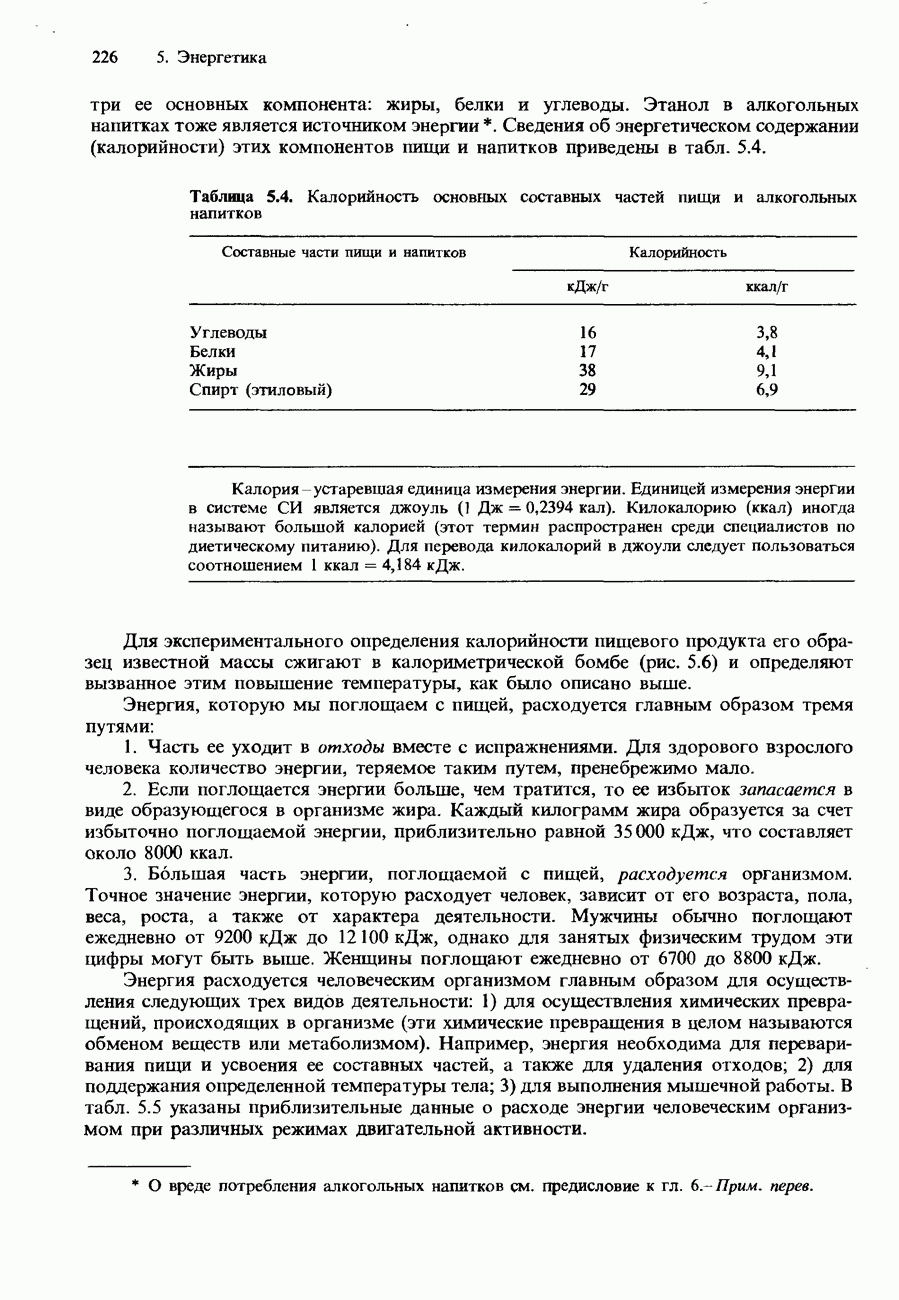
- КАЛОРИЙНОСТЬ ПИЩИ
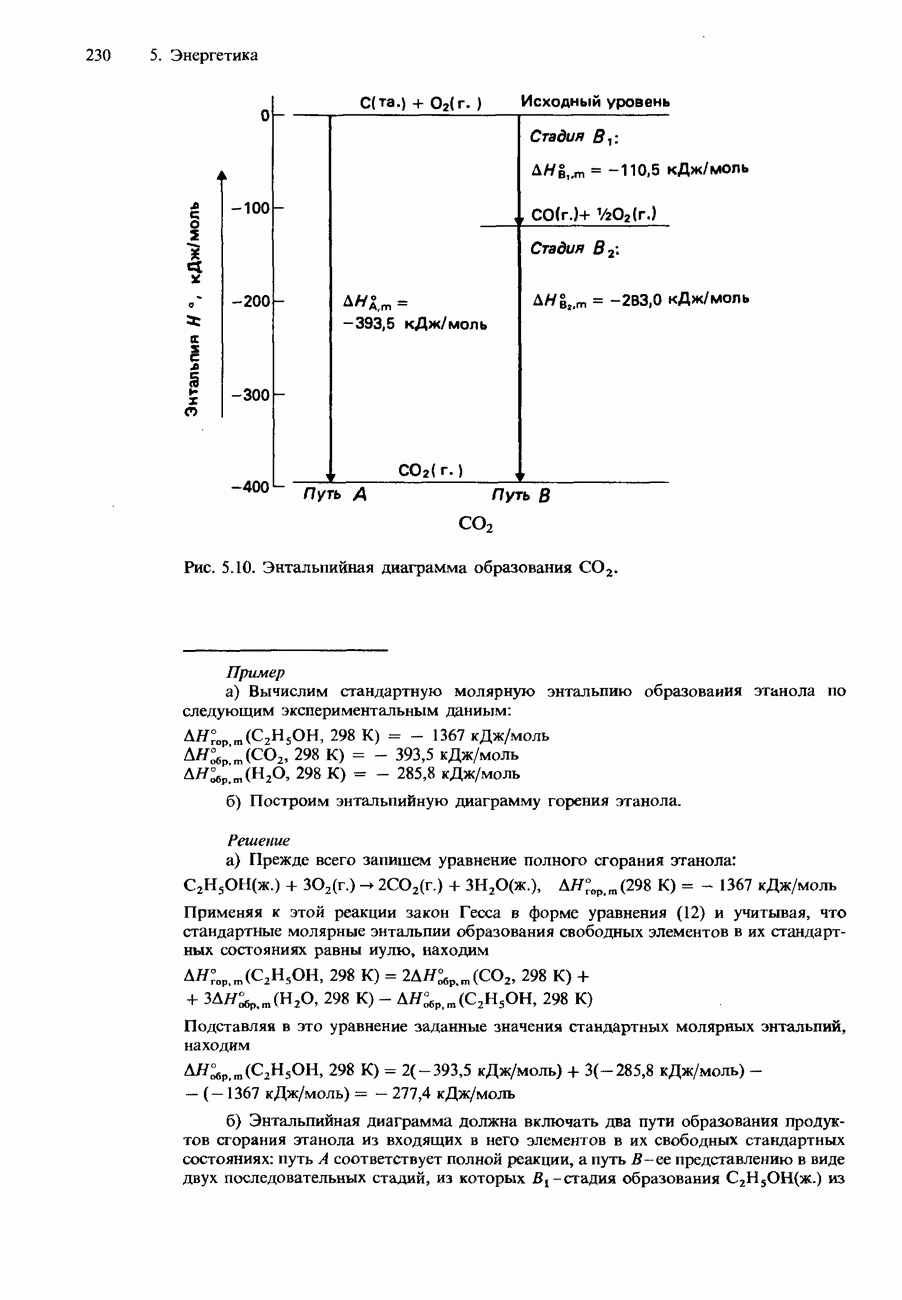
- ЗАКОН ГЕССА
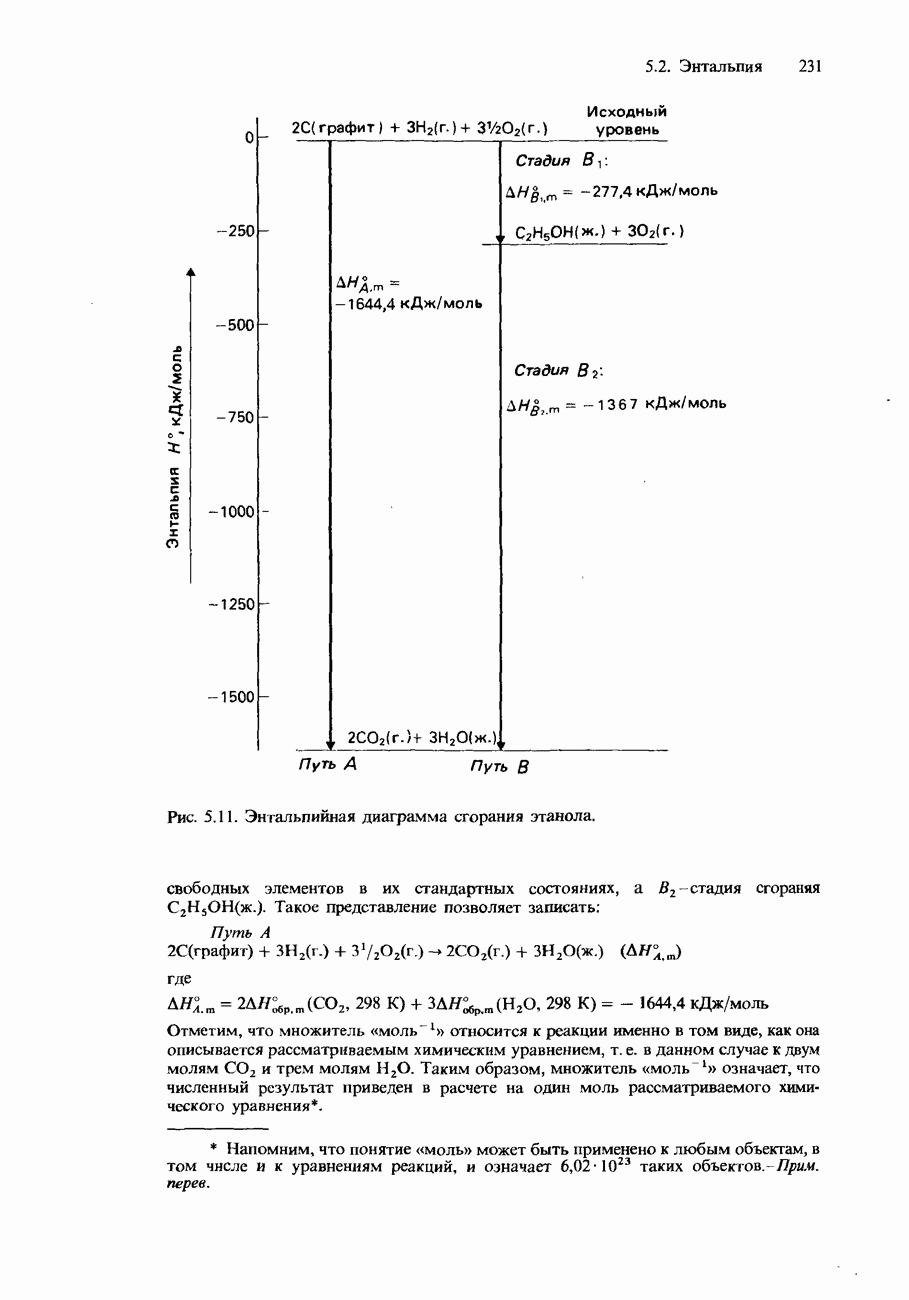
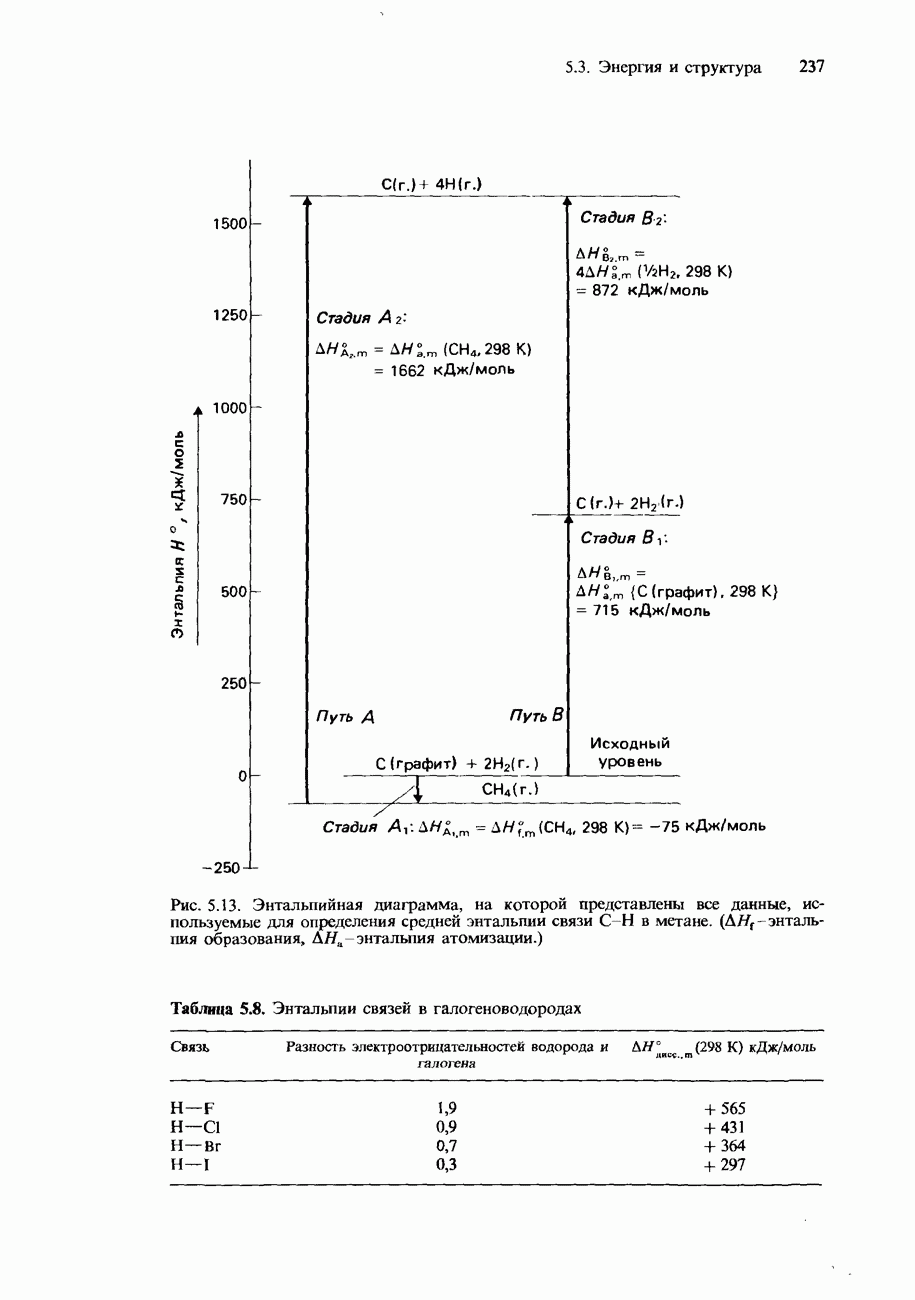
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
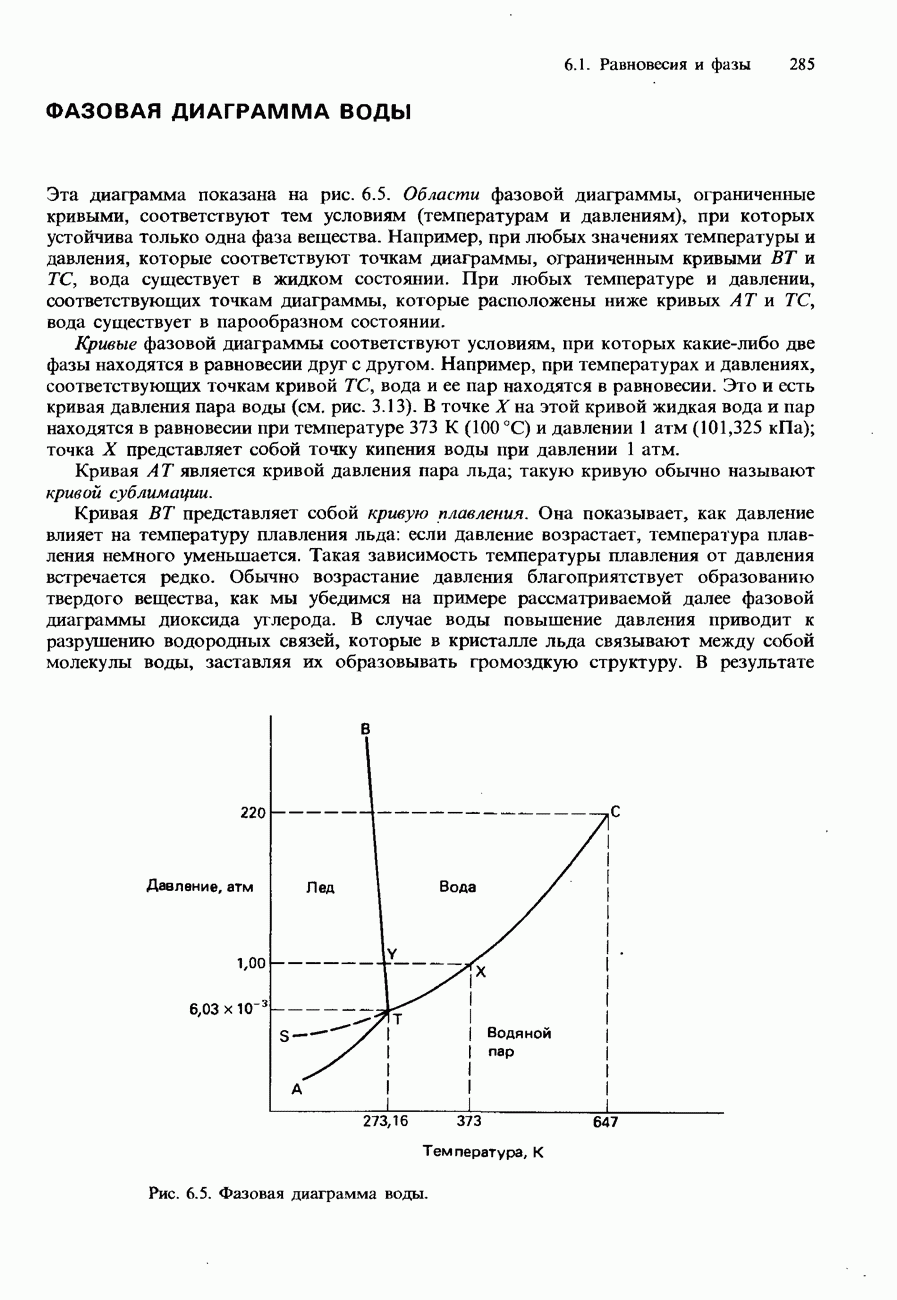
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
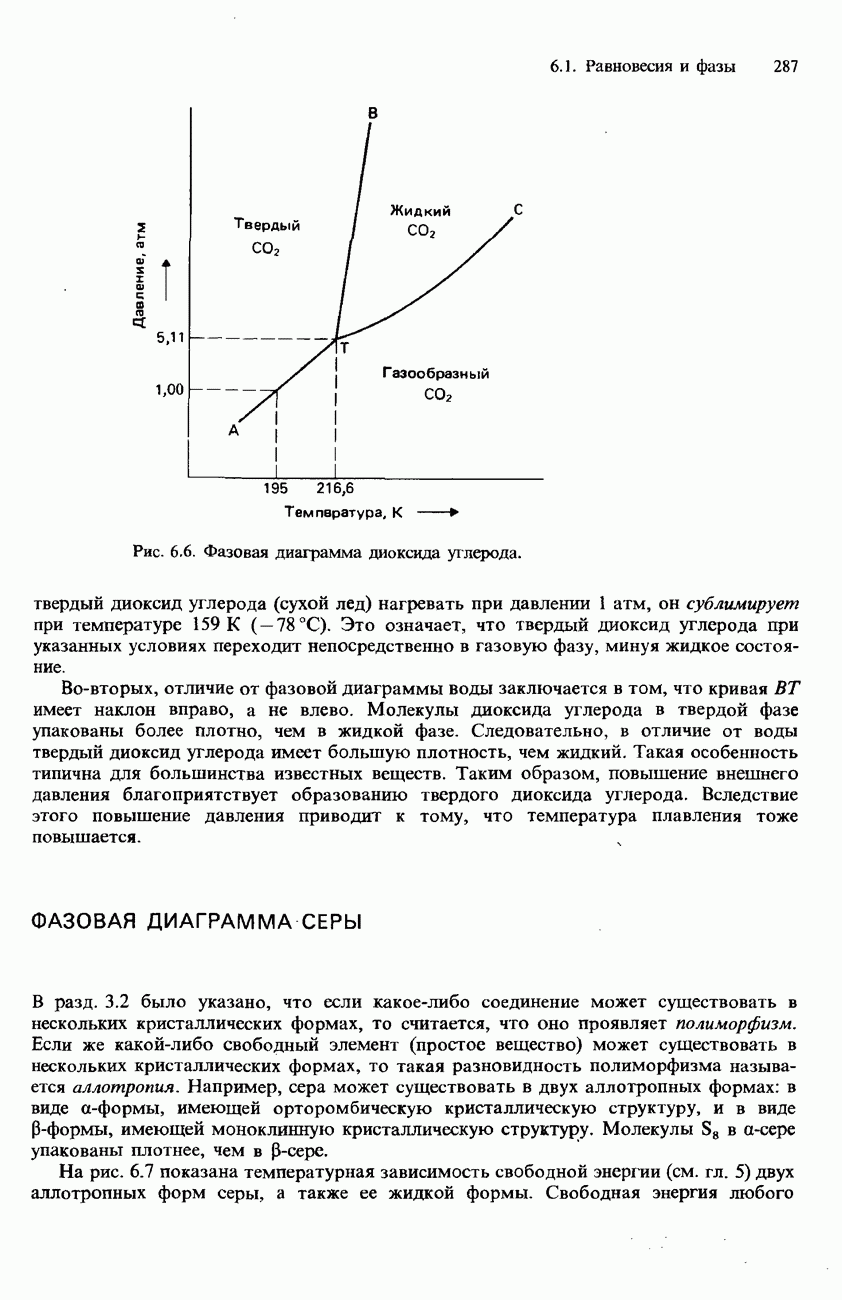
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
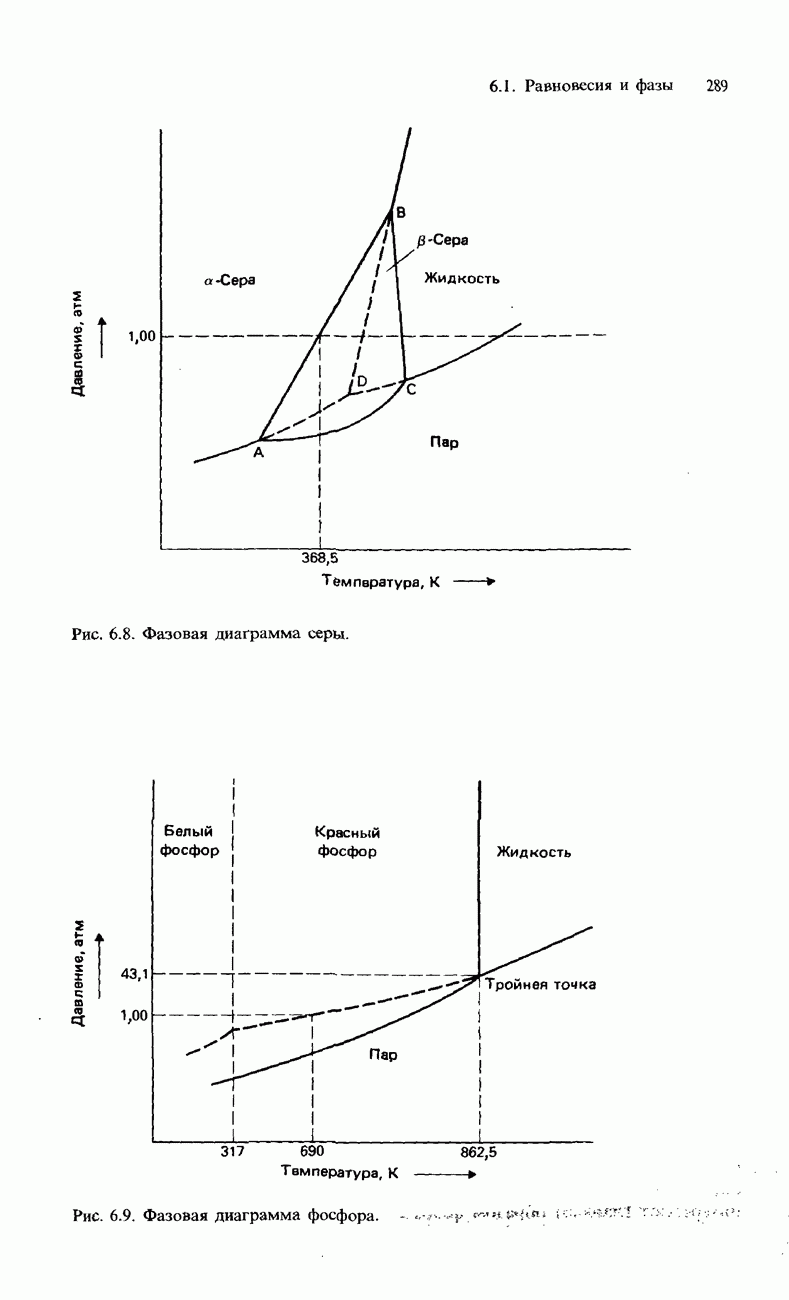
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
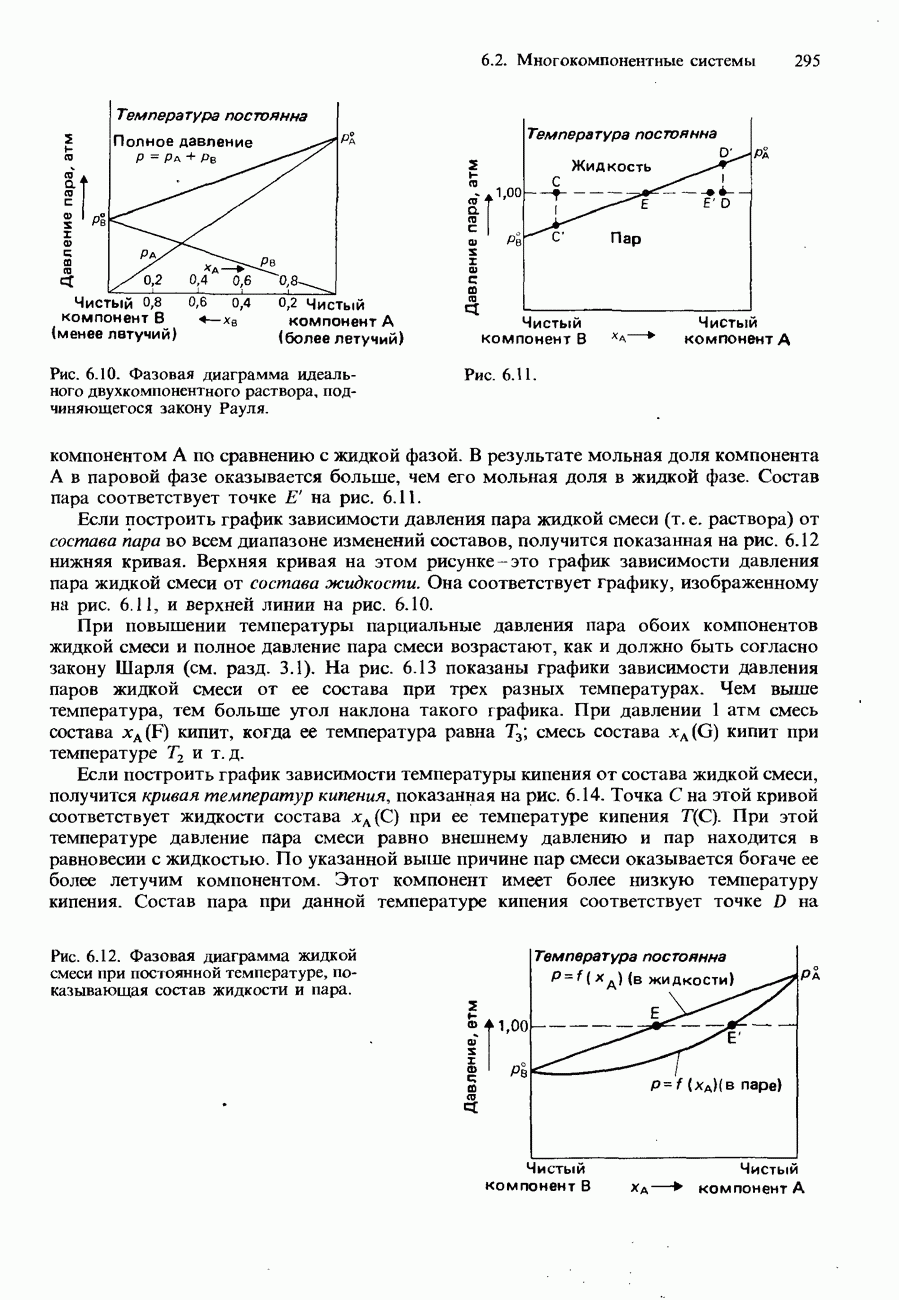
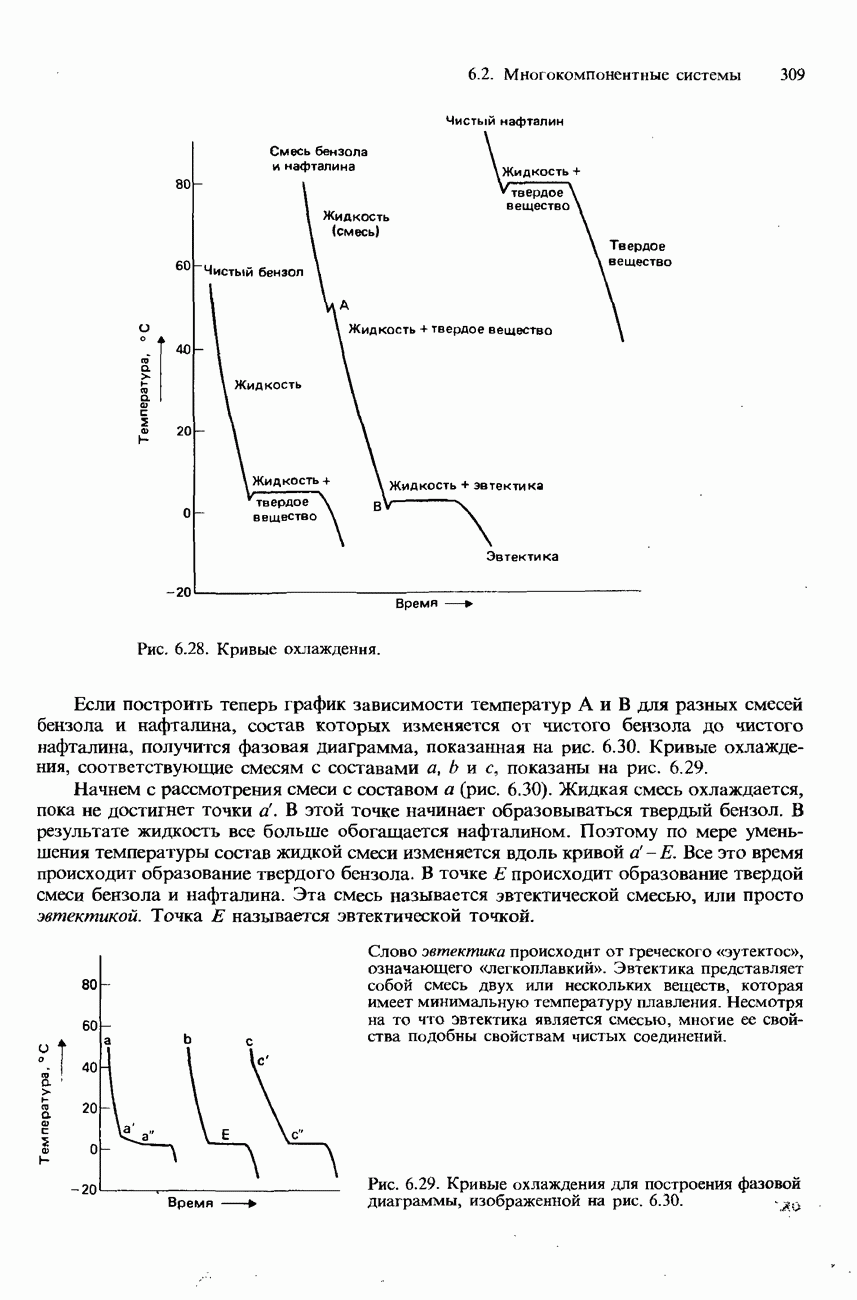
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- Фазовые диаграммы полностью смешивающихся жидкостей
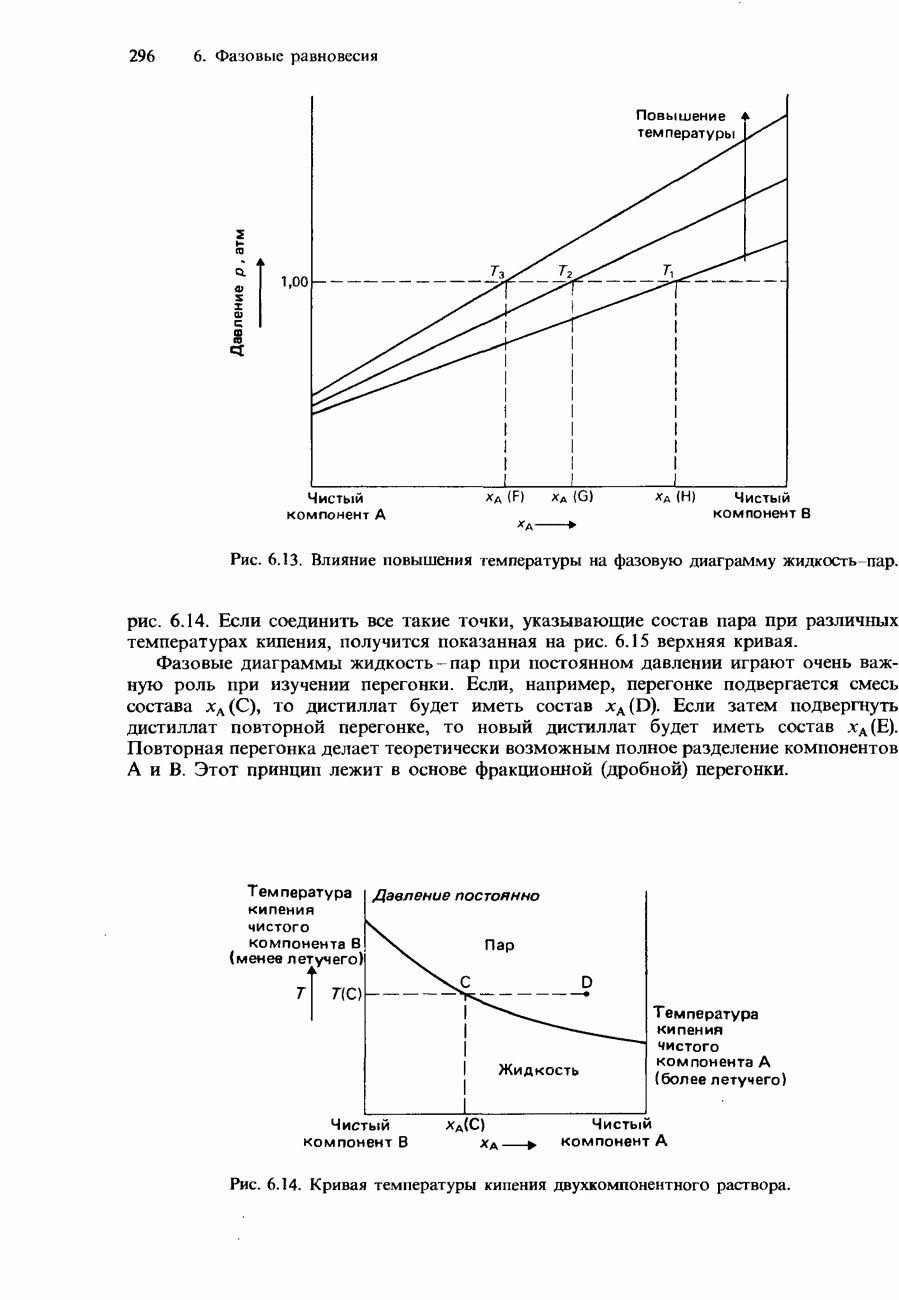
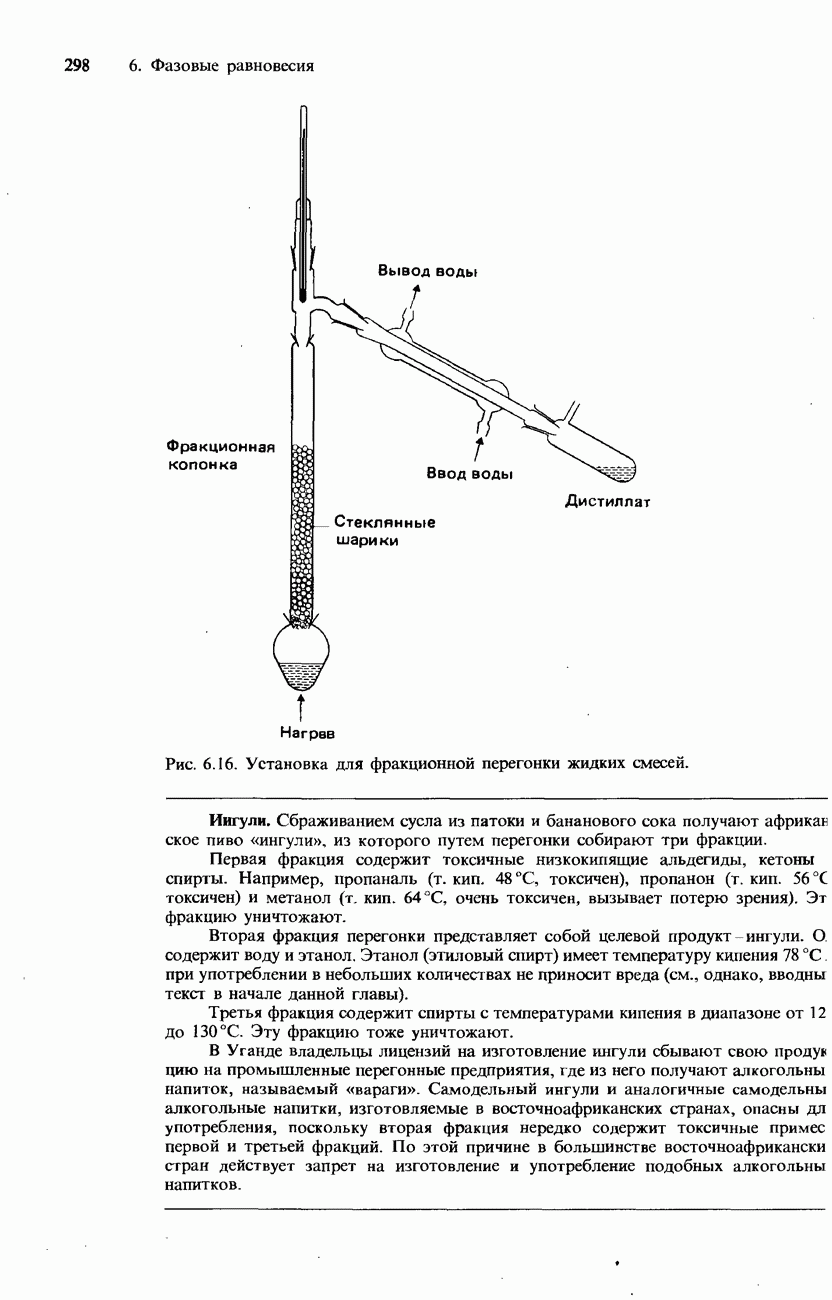
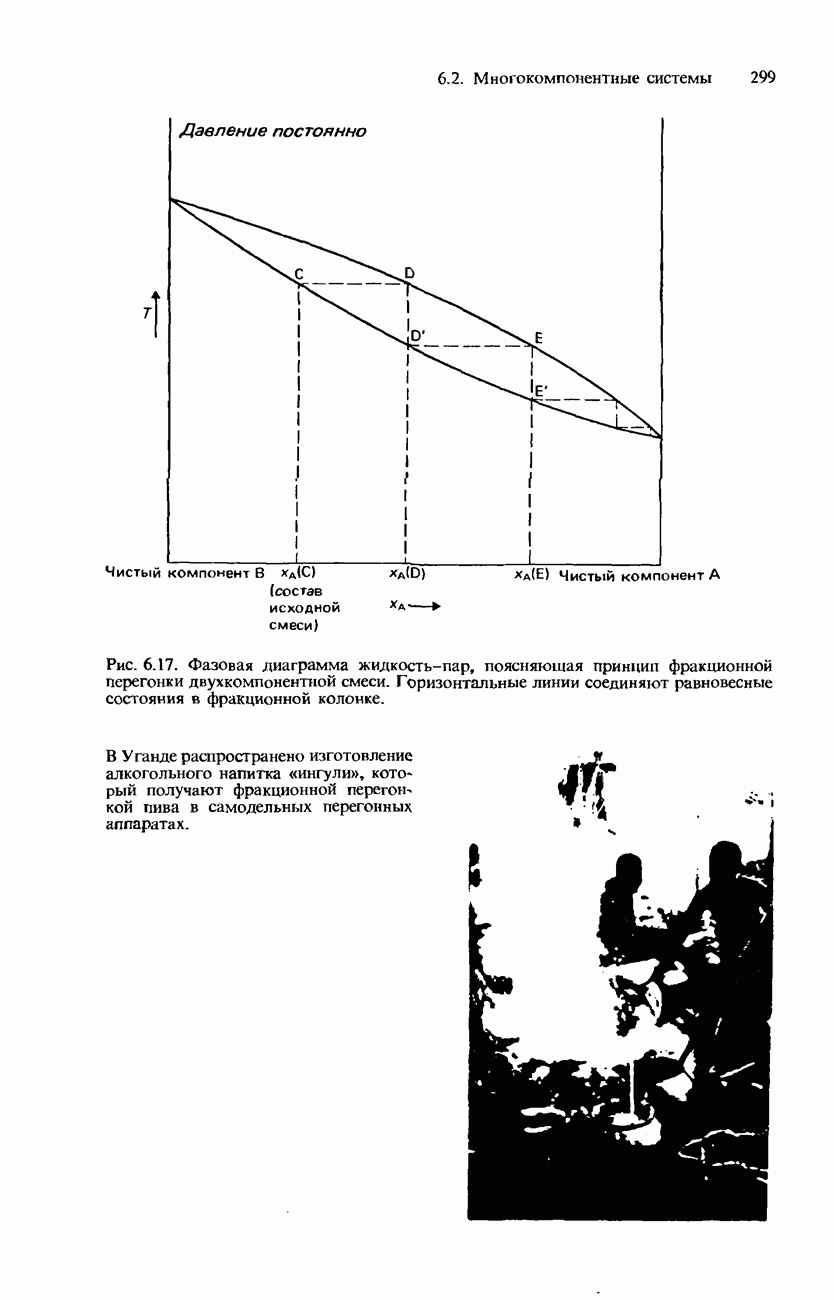
- Фракционная перегонка
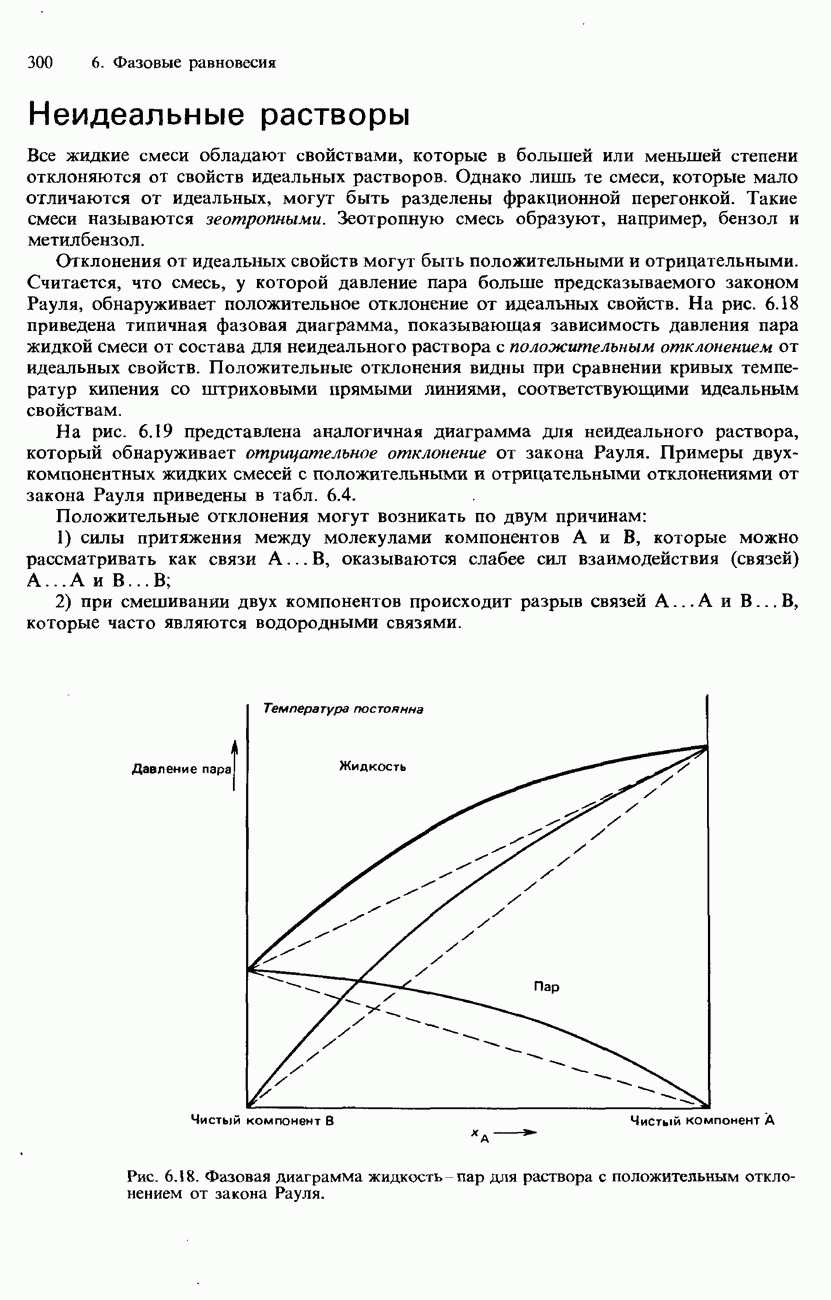
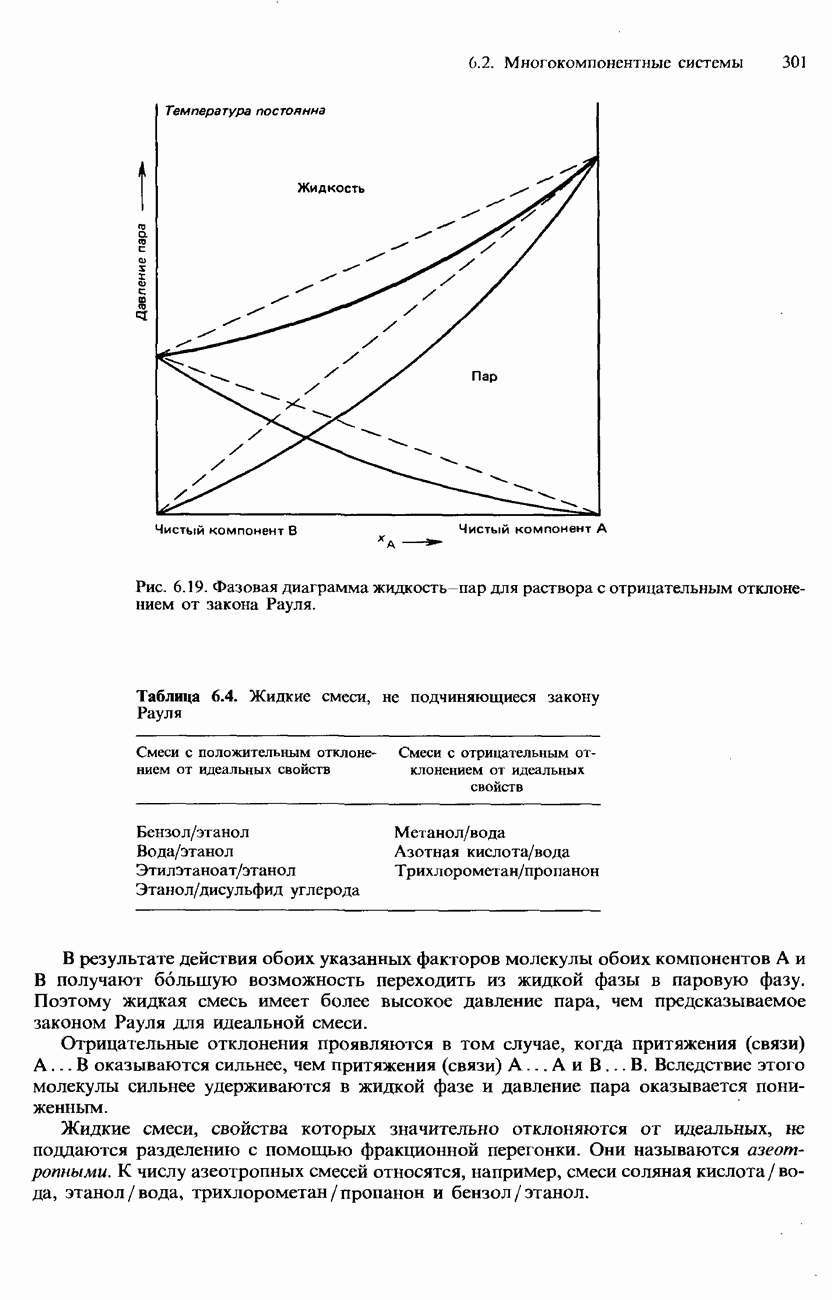
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
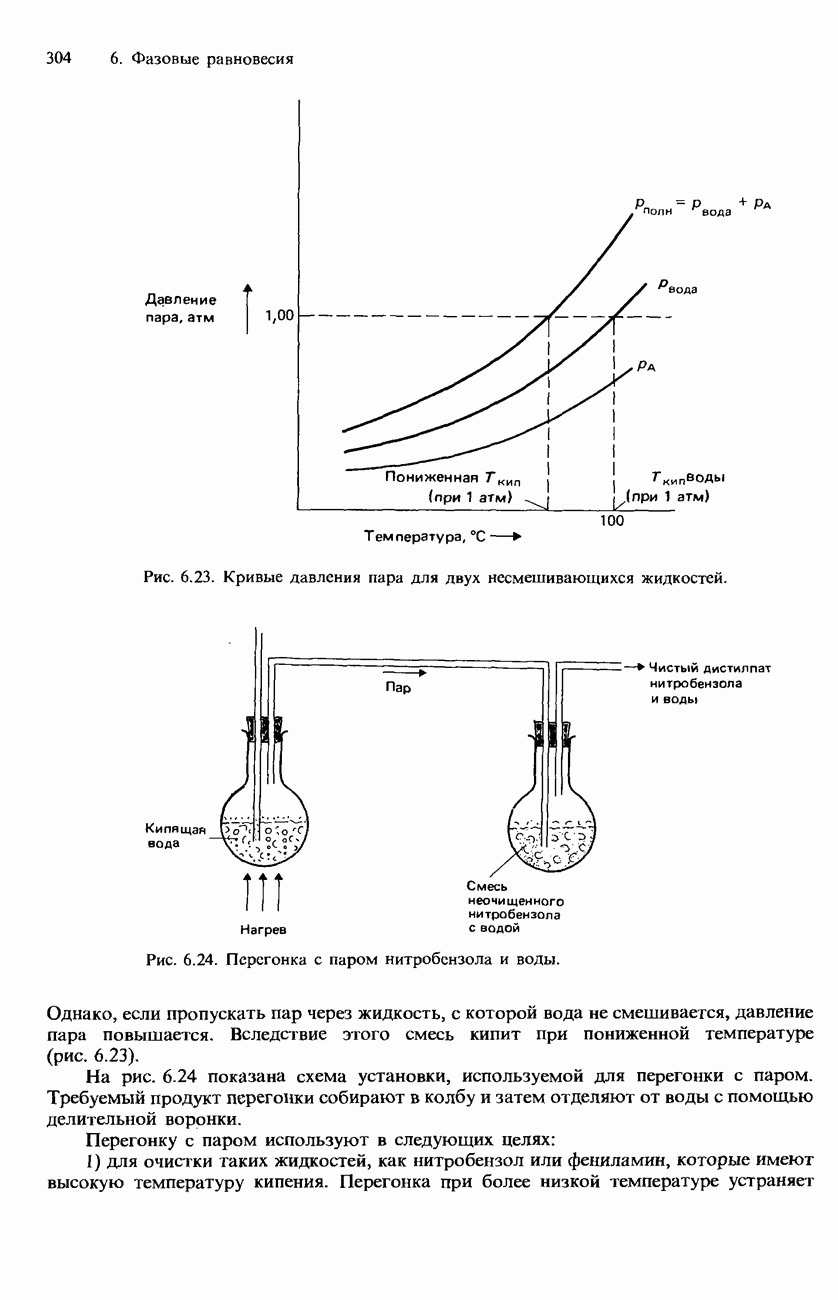
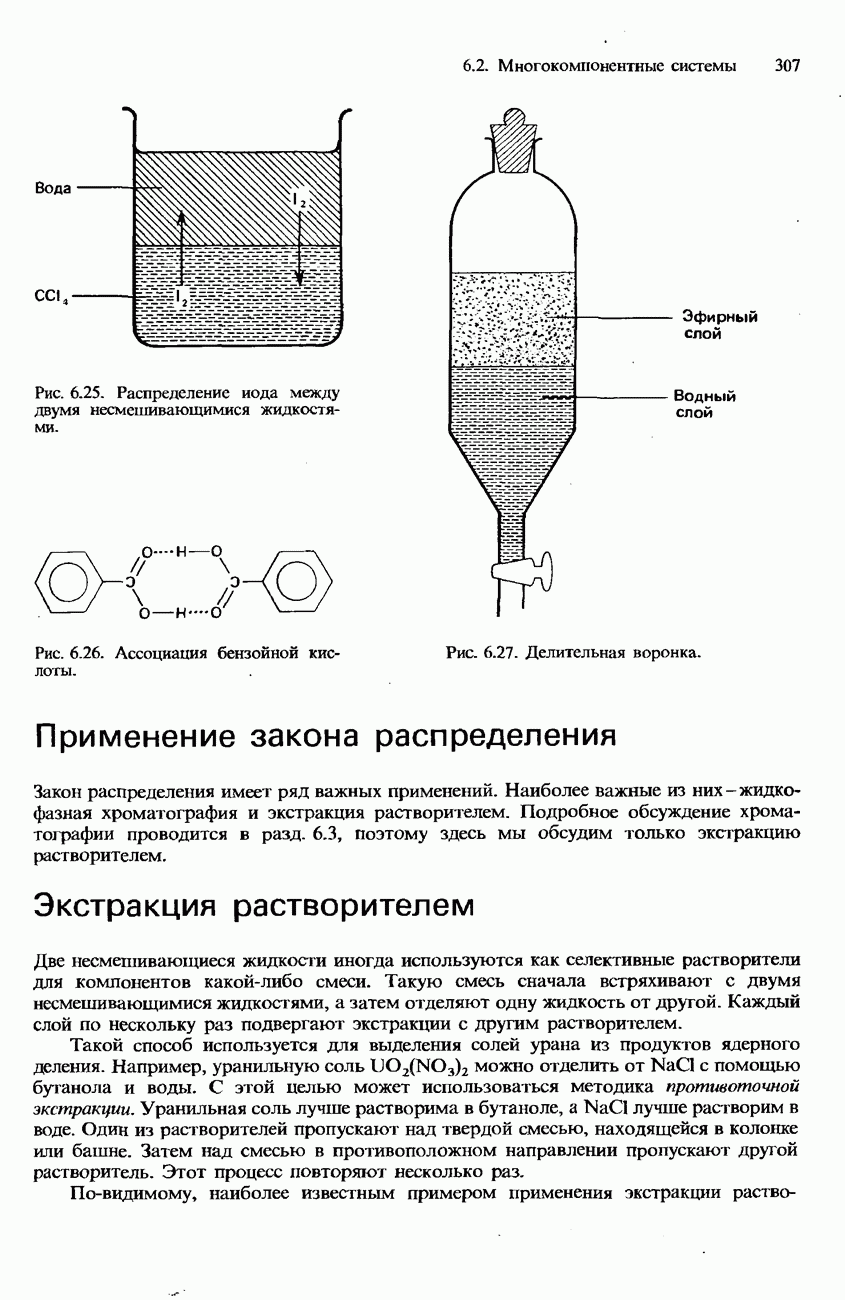
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
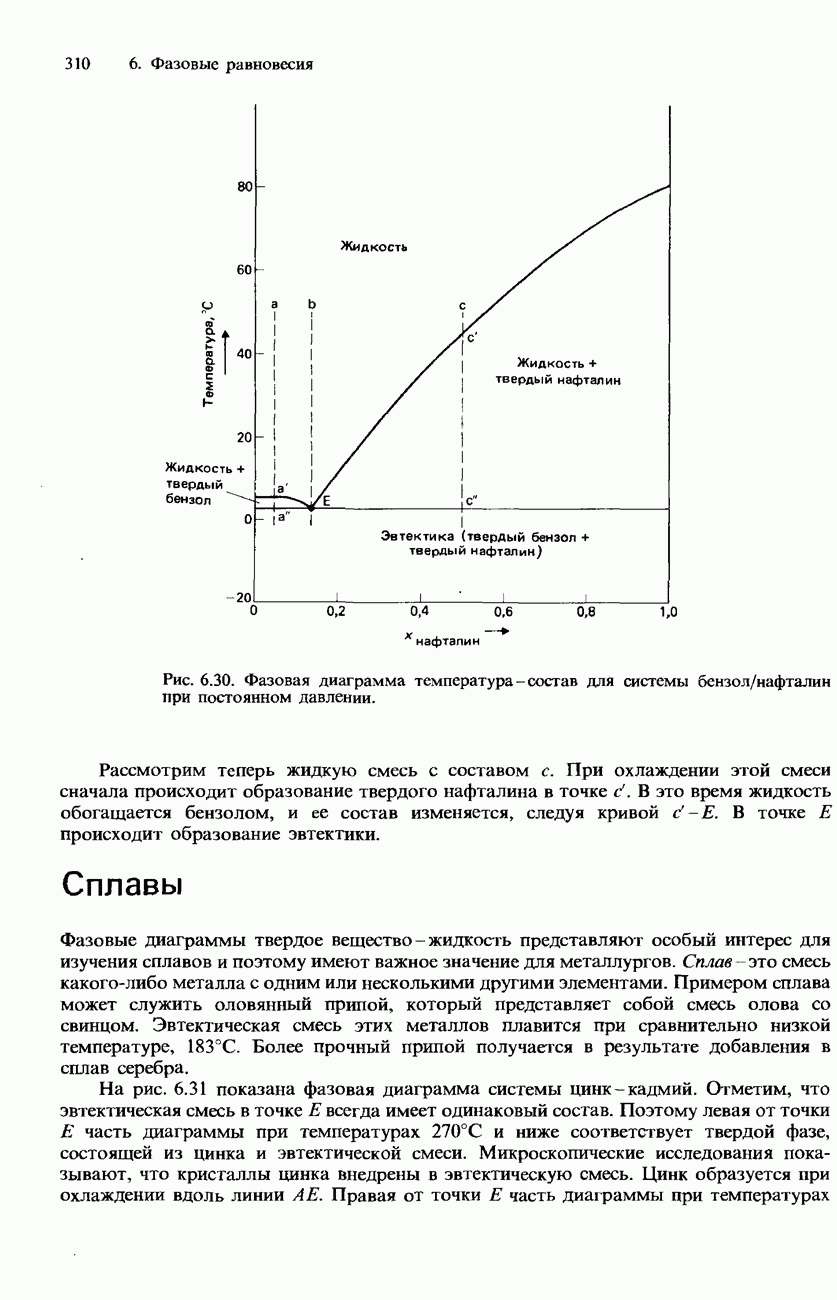
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
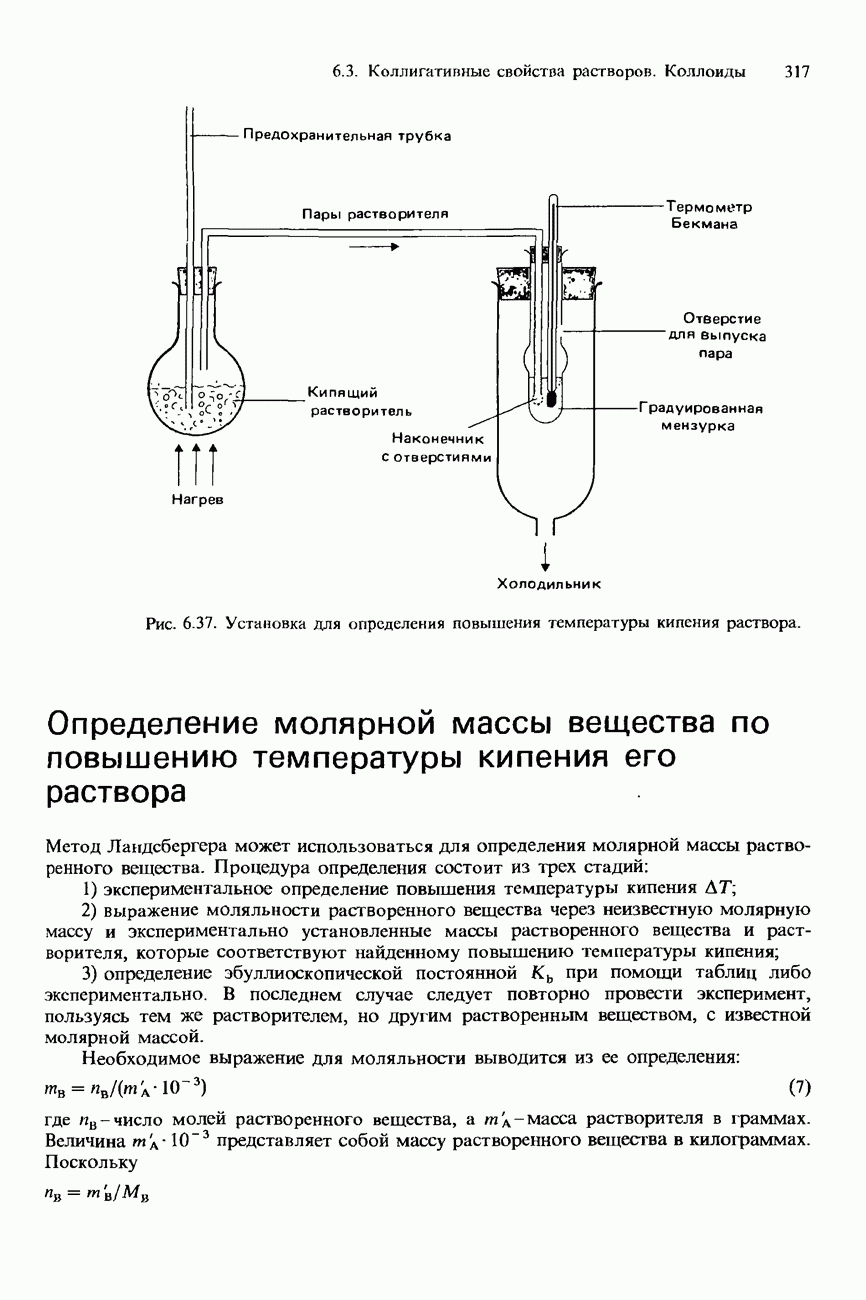
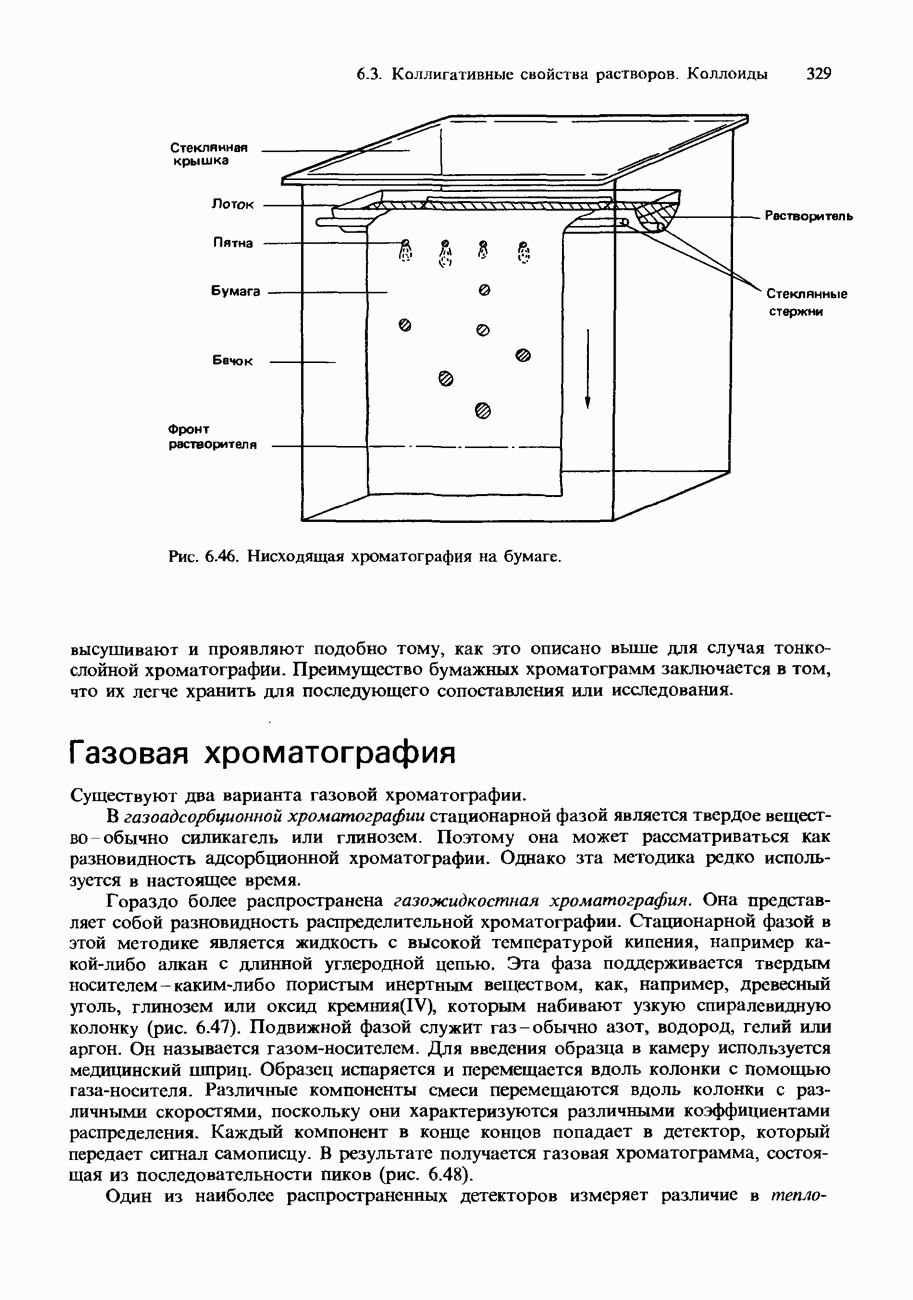
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
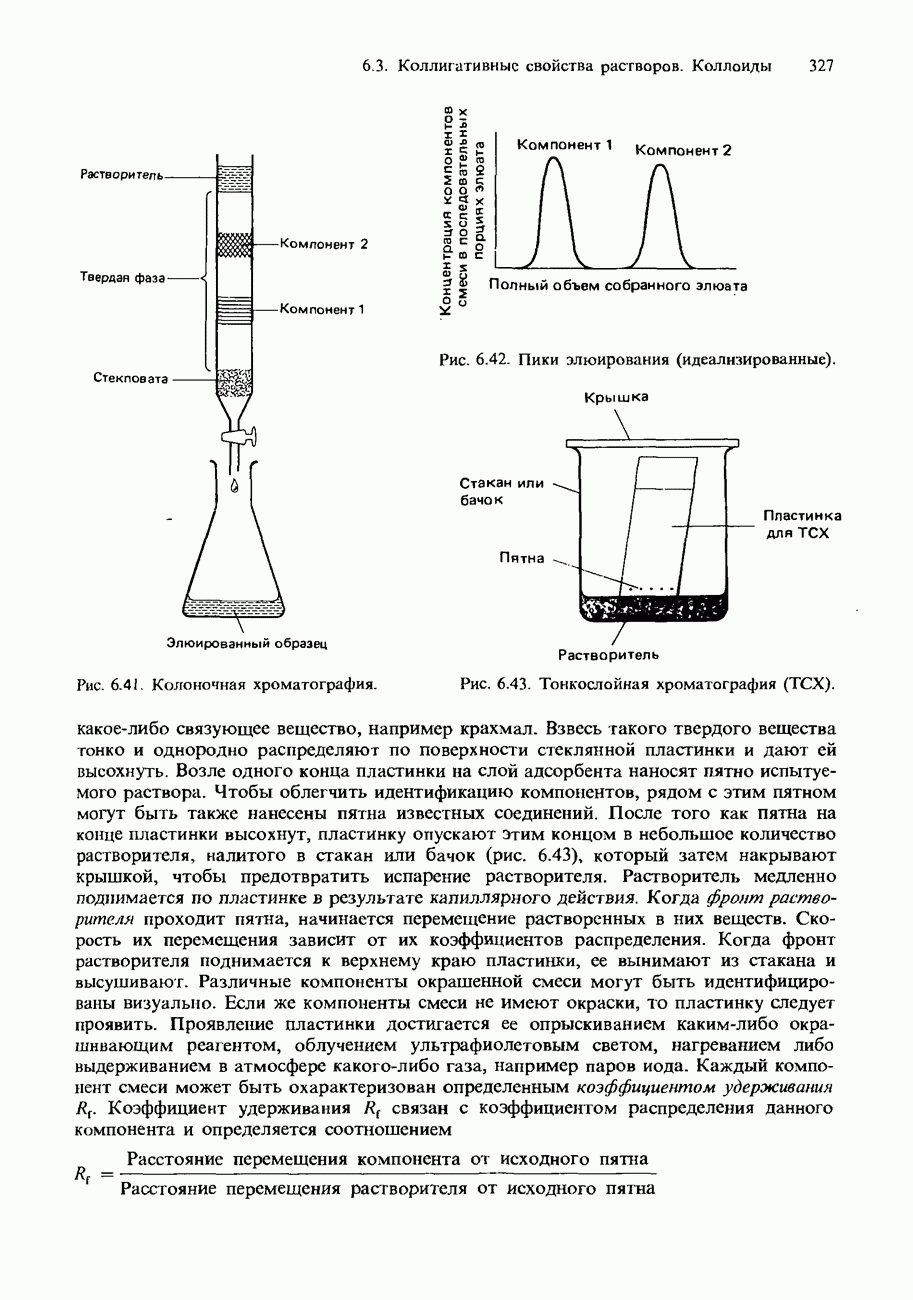
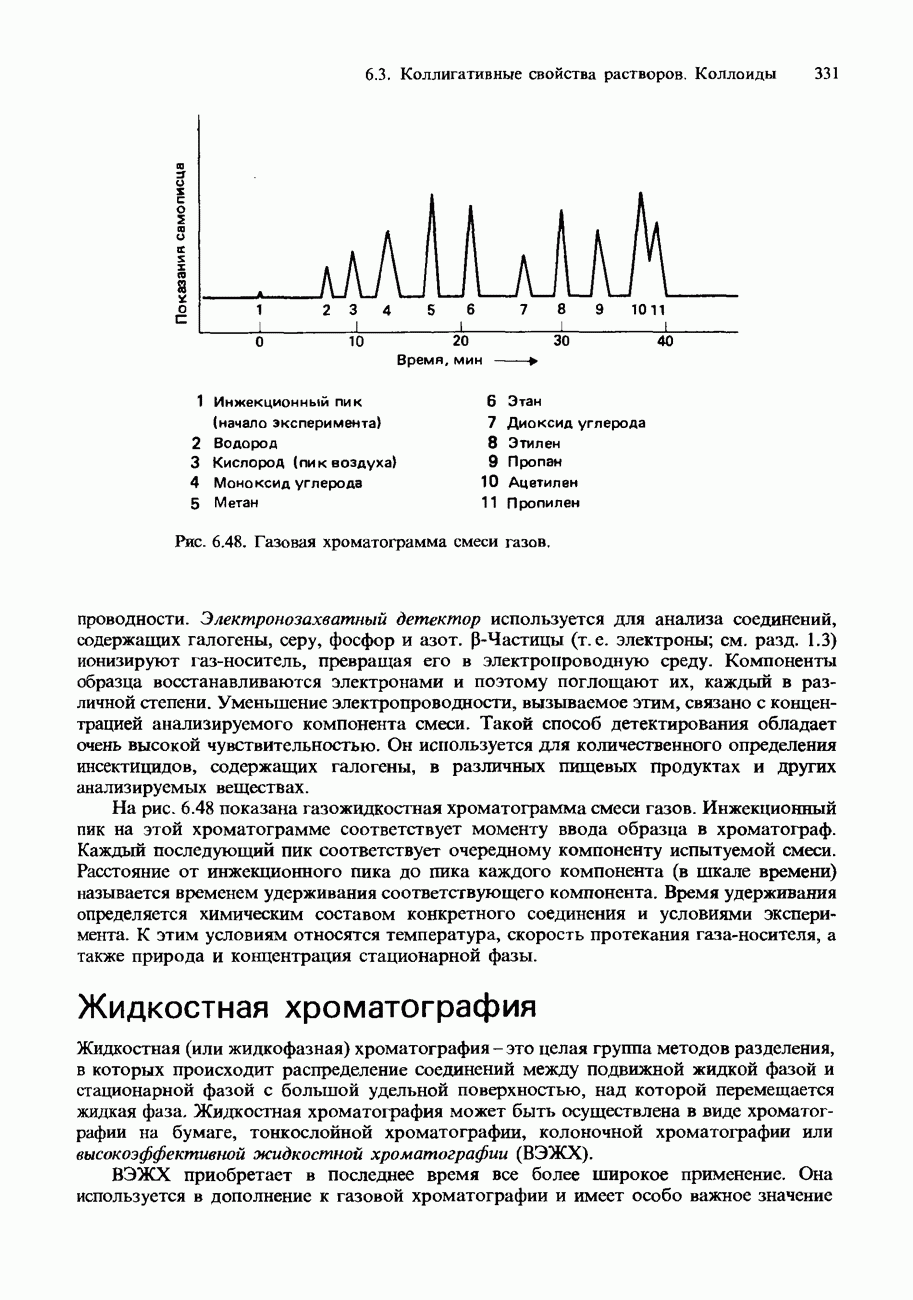
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
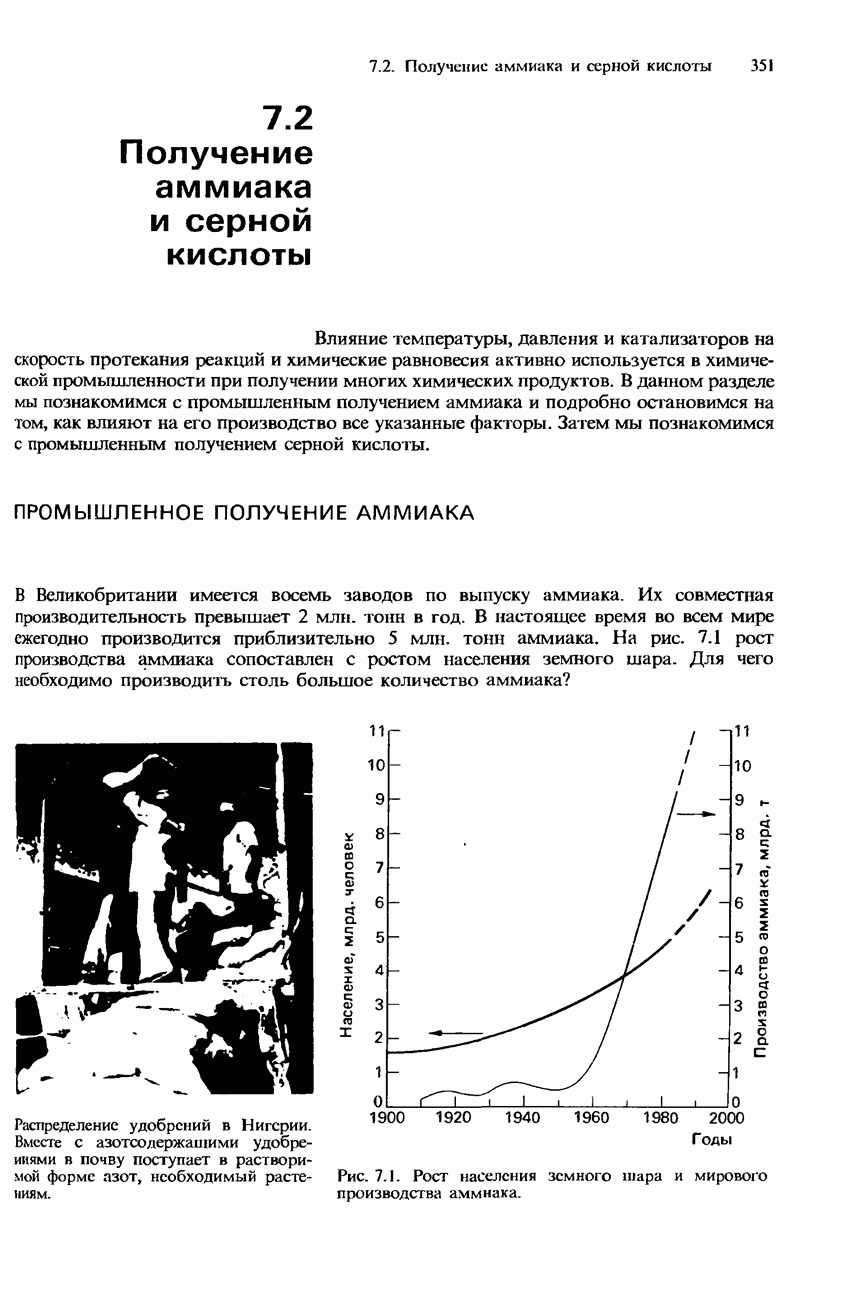
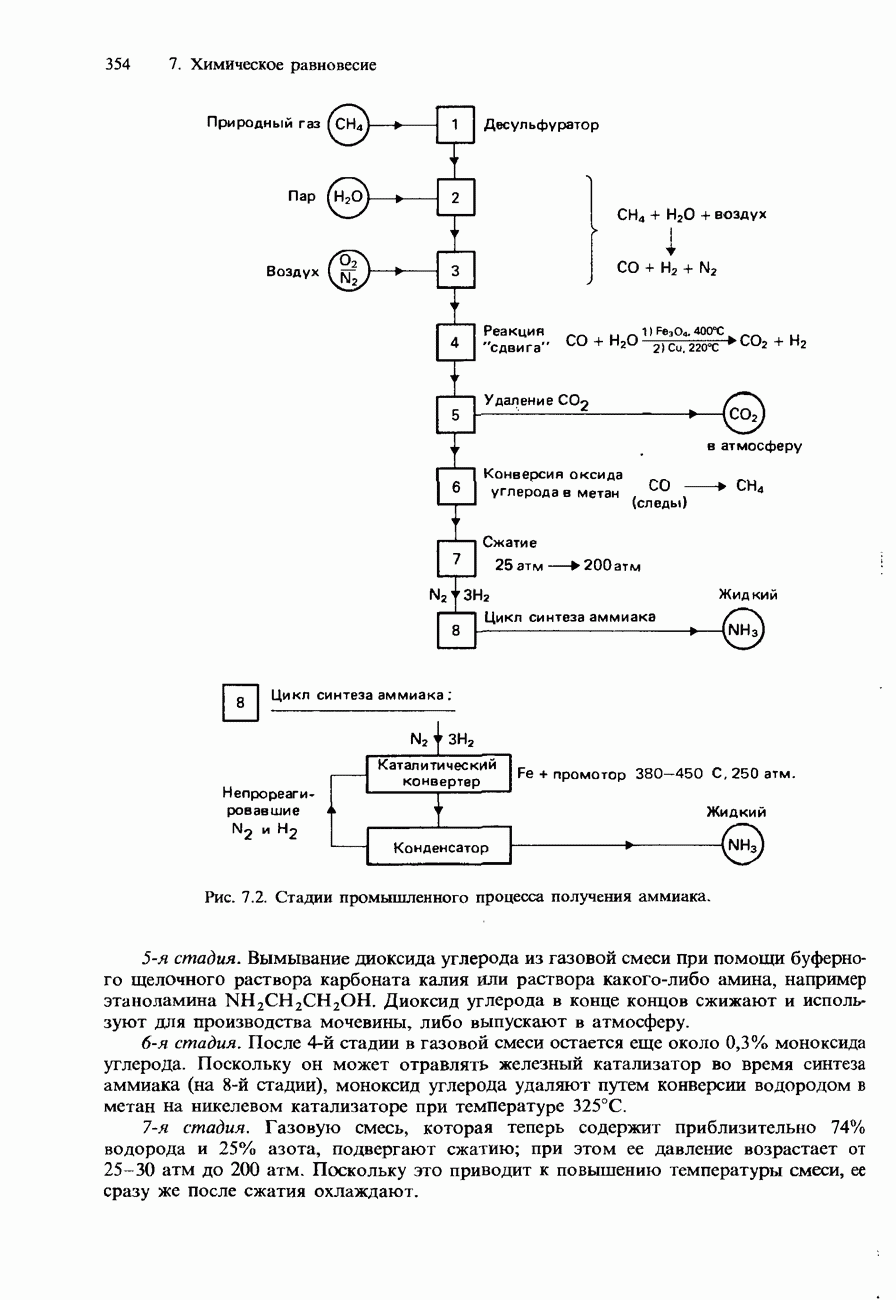
- 7.2. Получение аммиака и серной кислоты
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
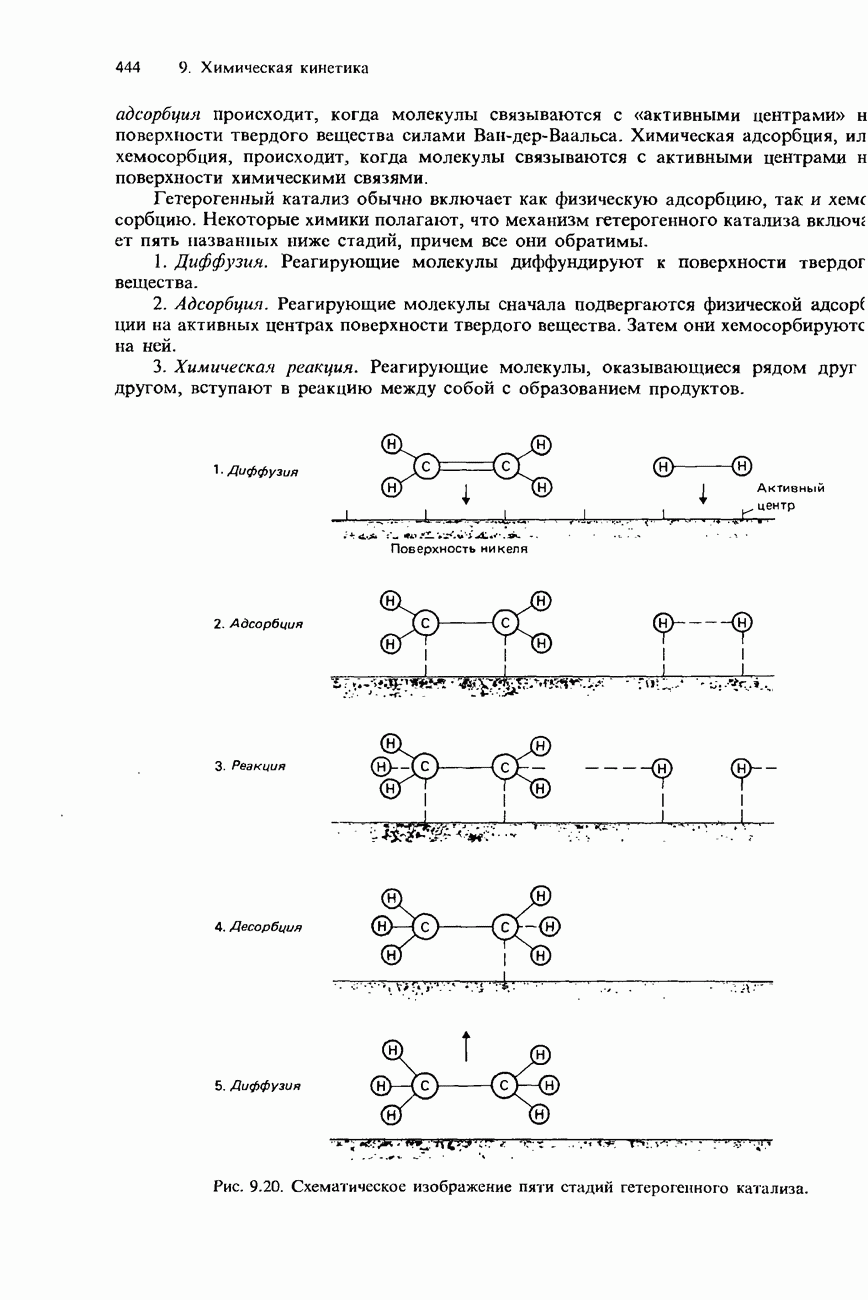
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
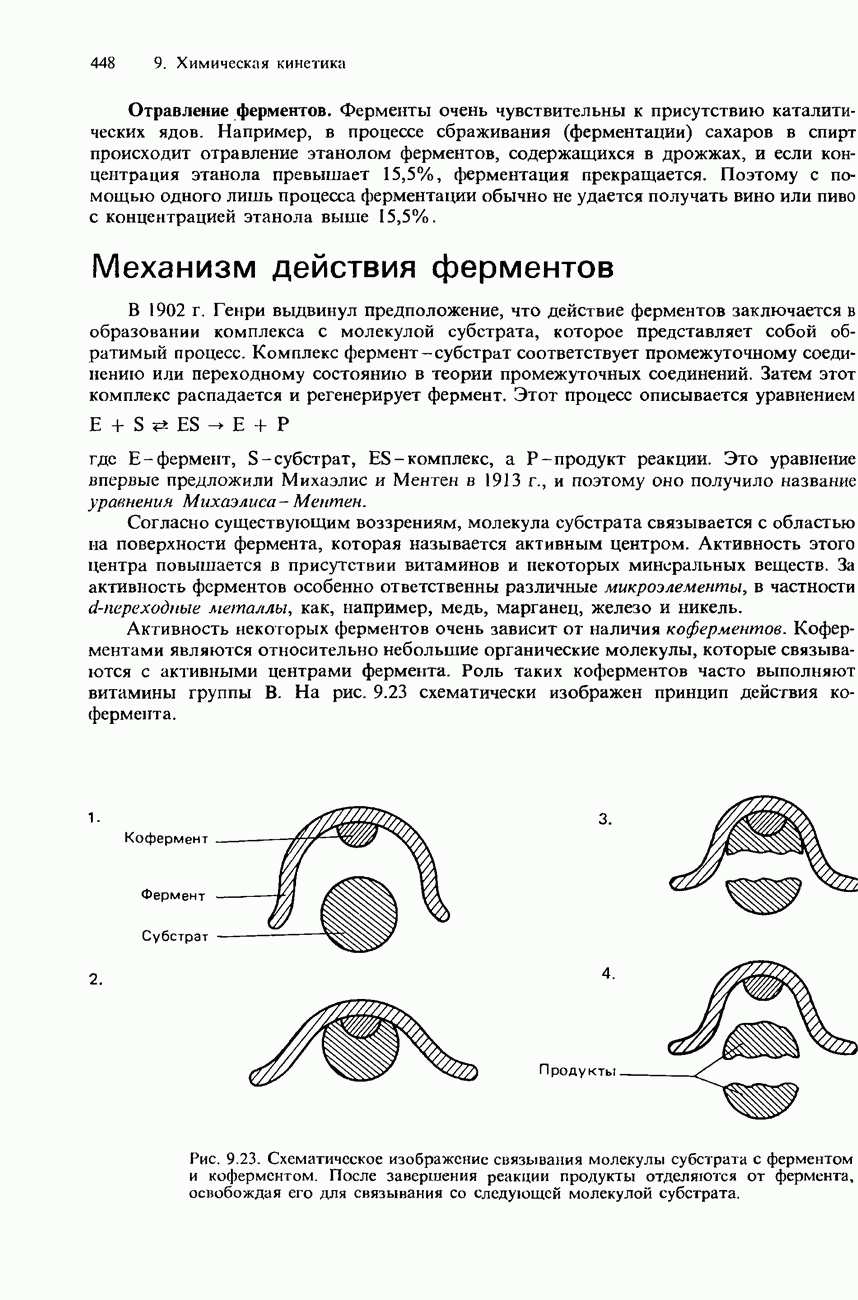
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
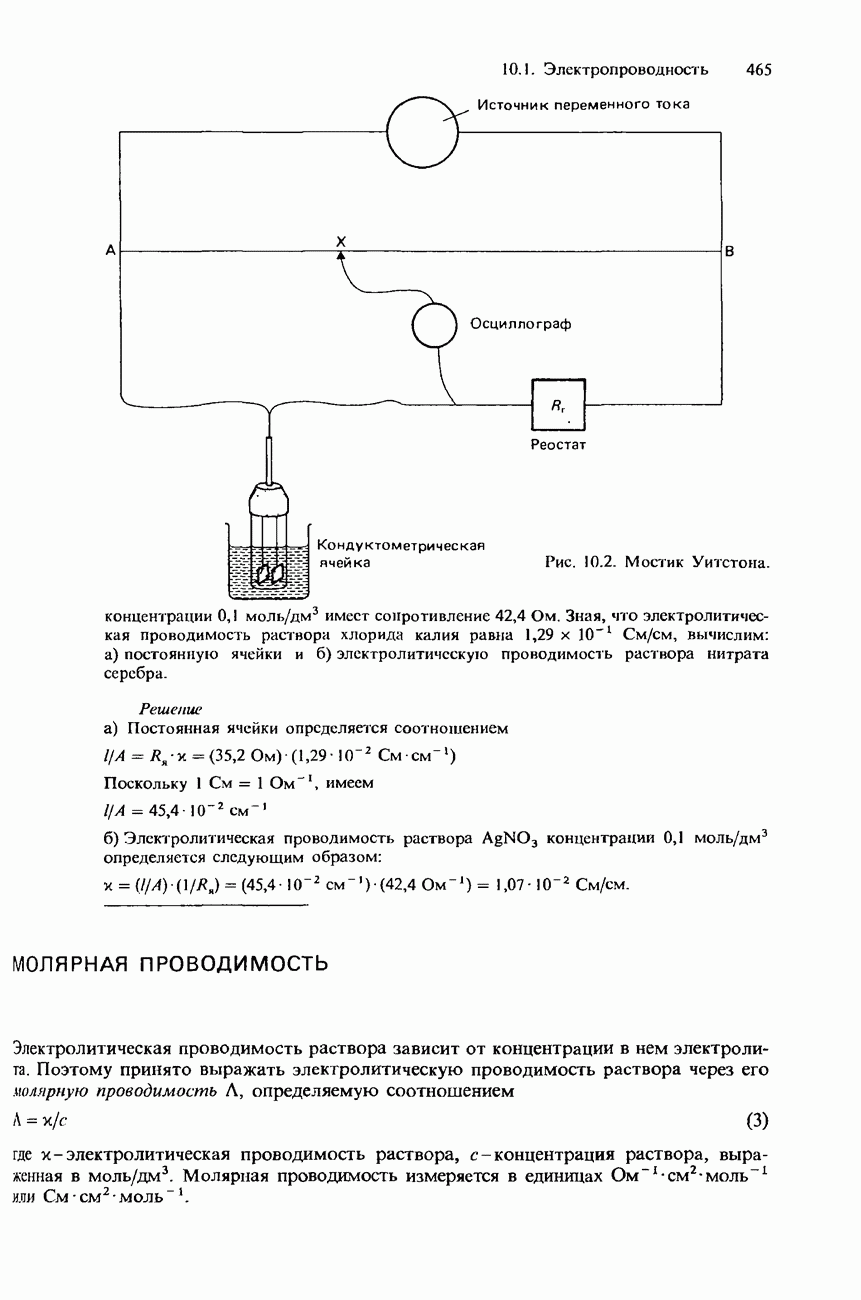
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
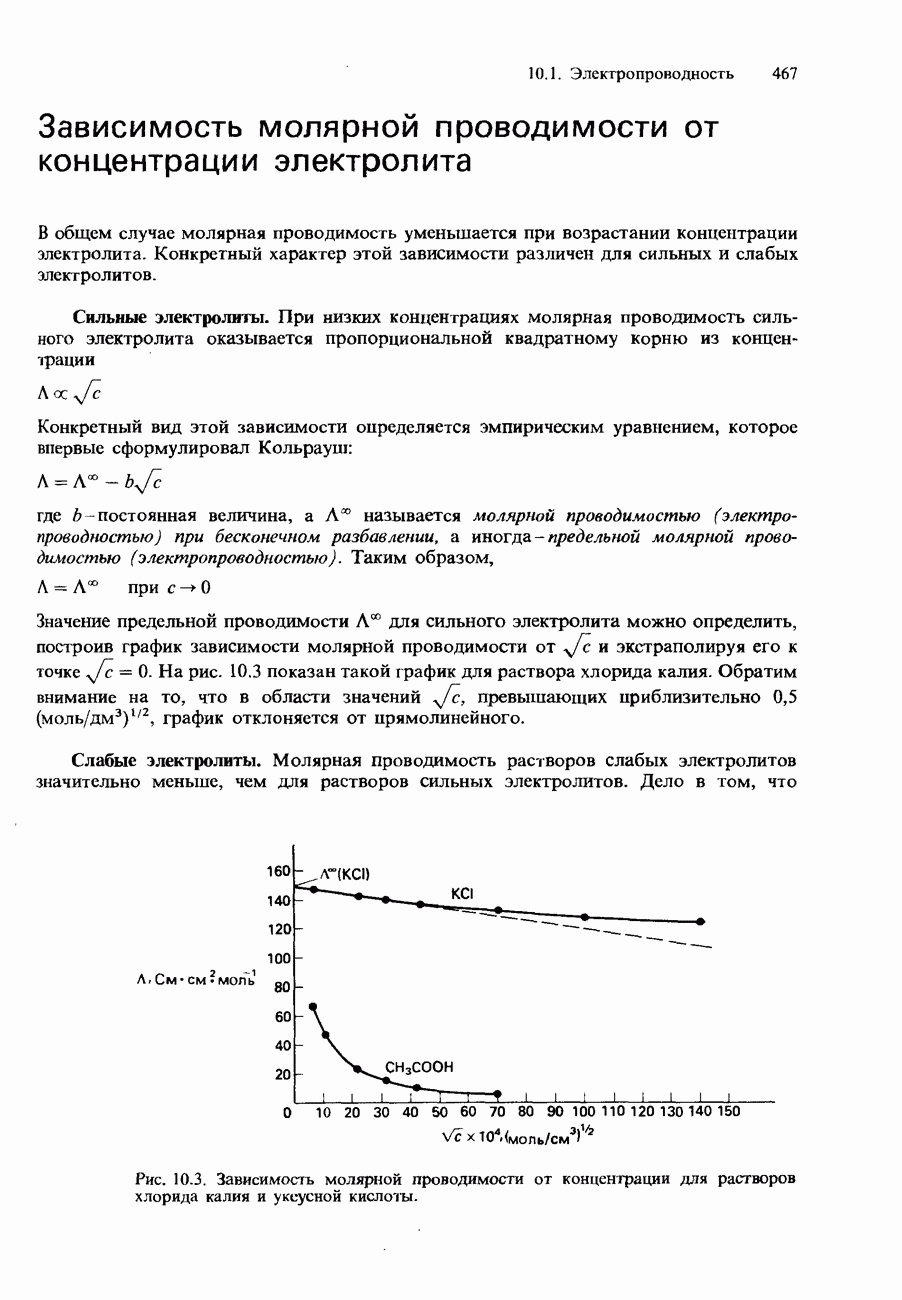
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
- 10.4. Химические источники тока
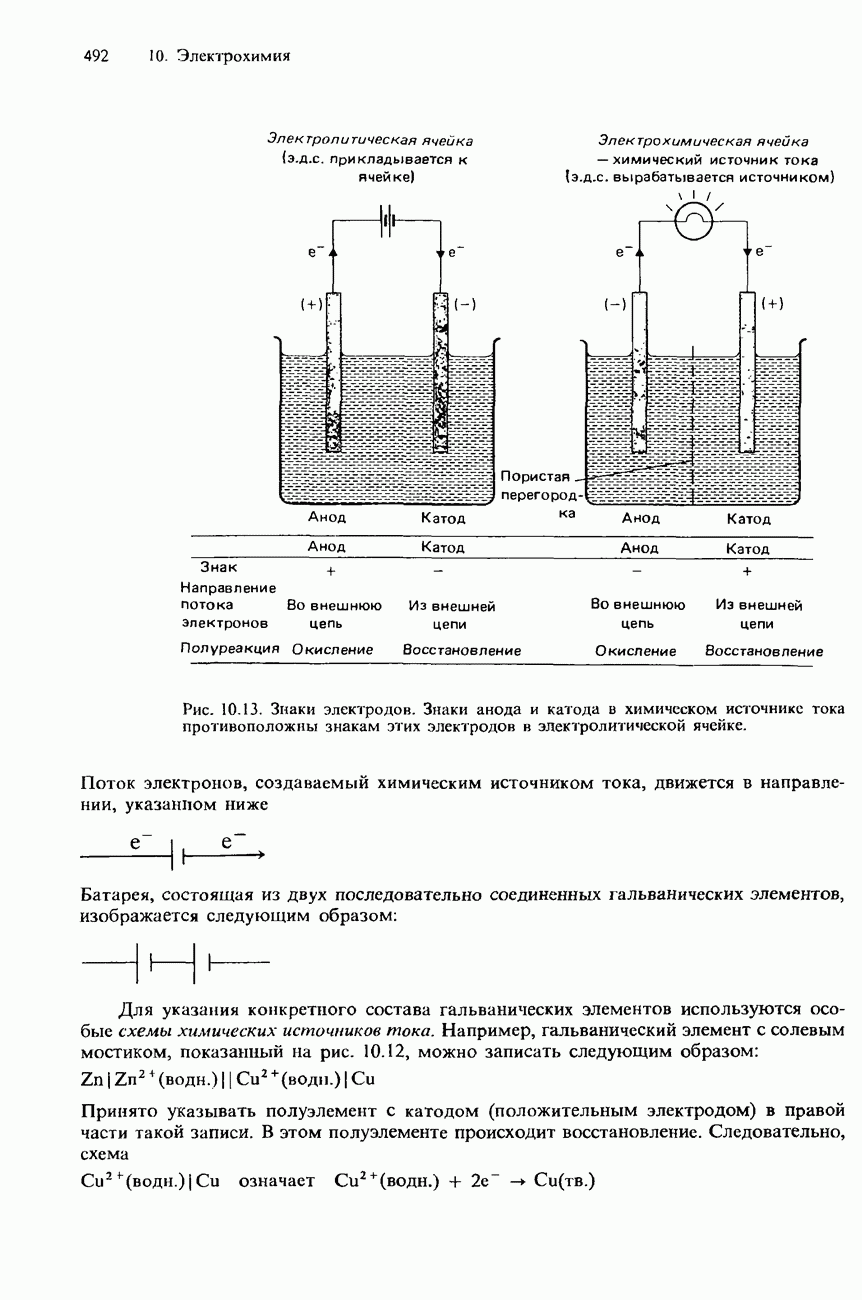
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
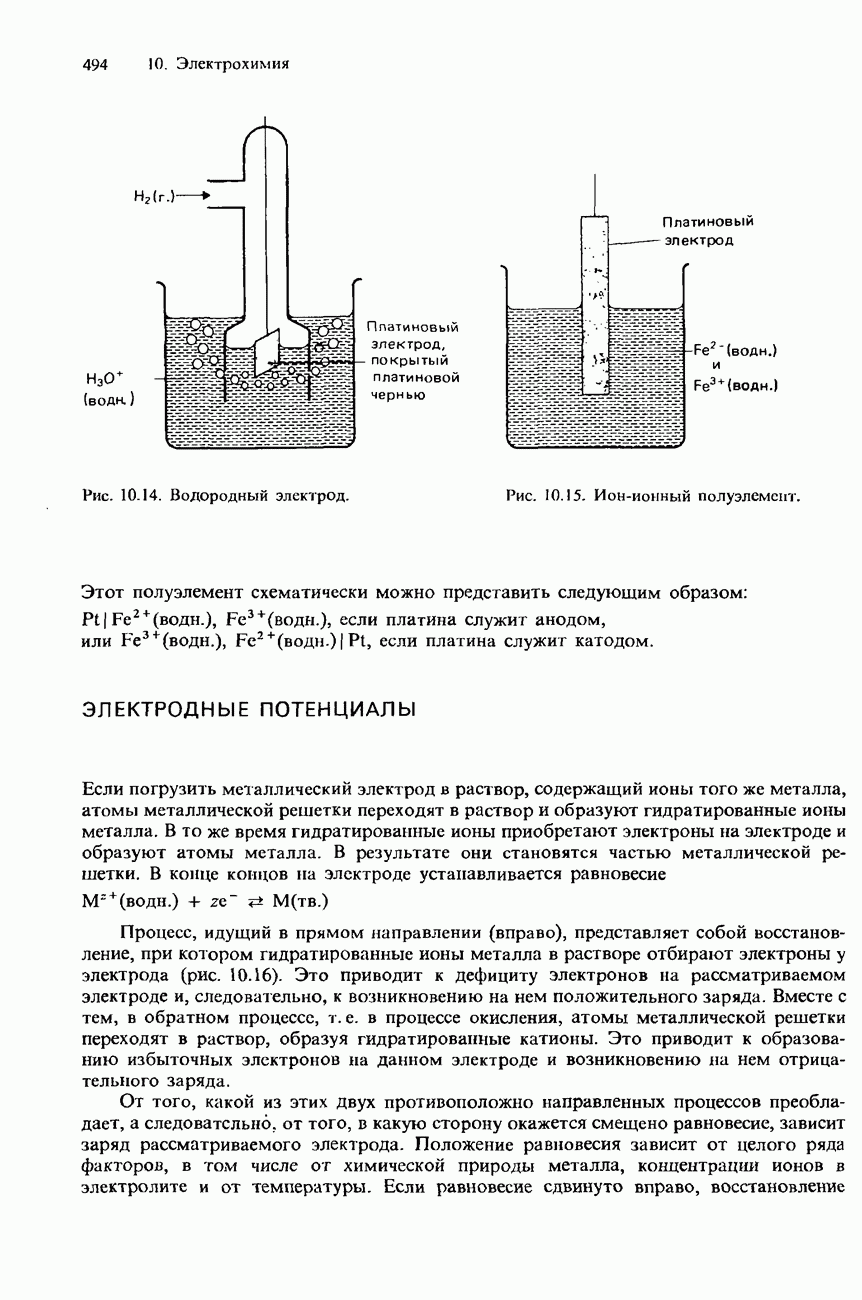
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
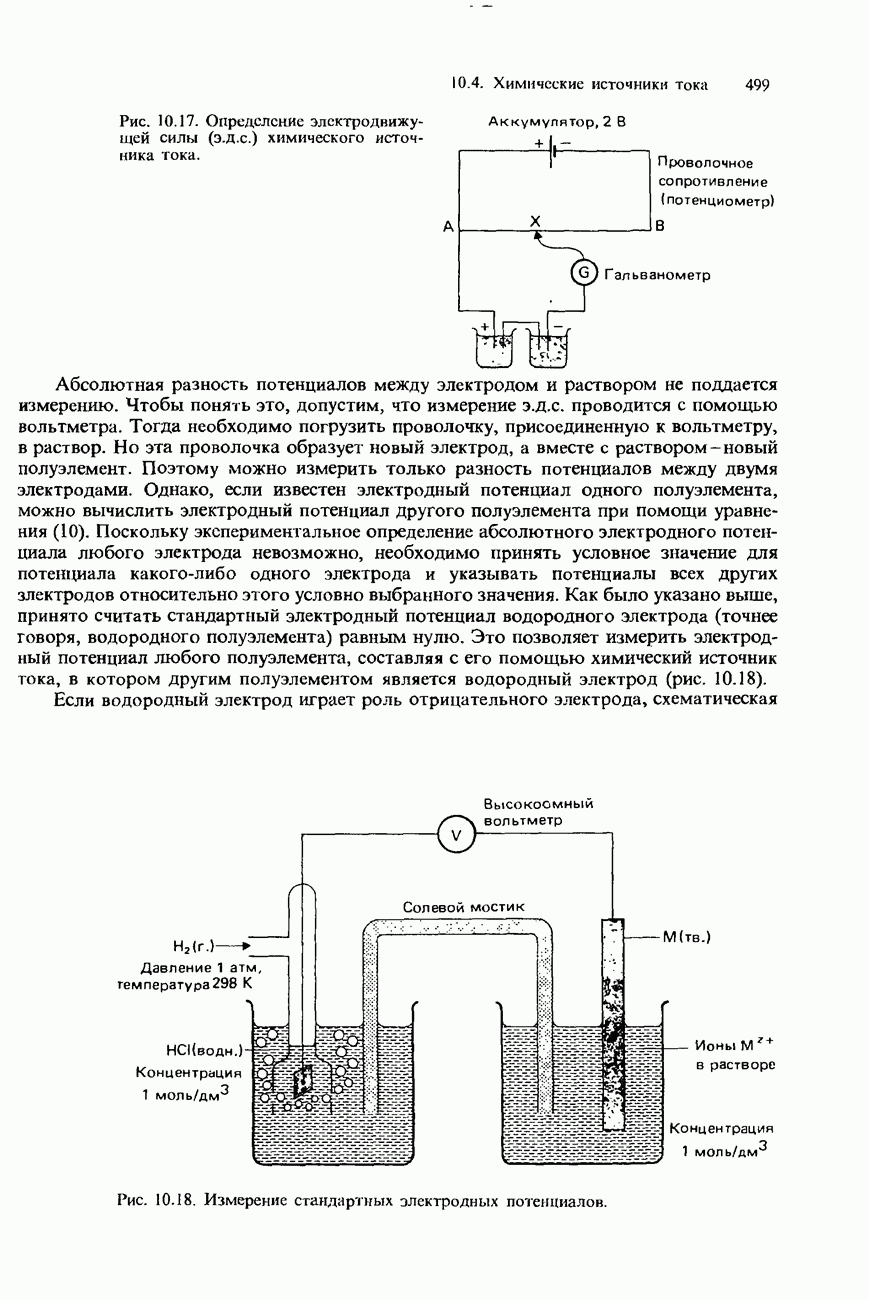
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
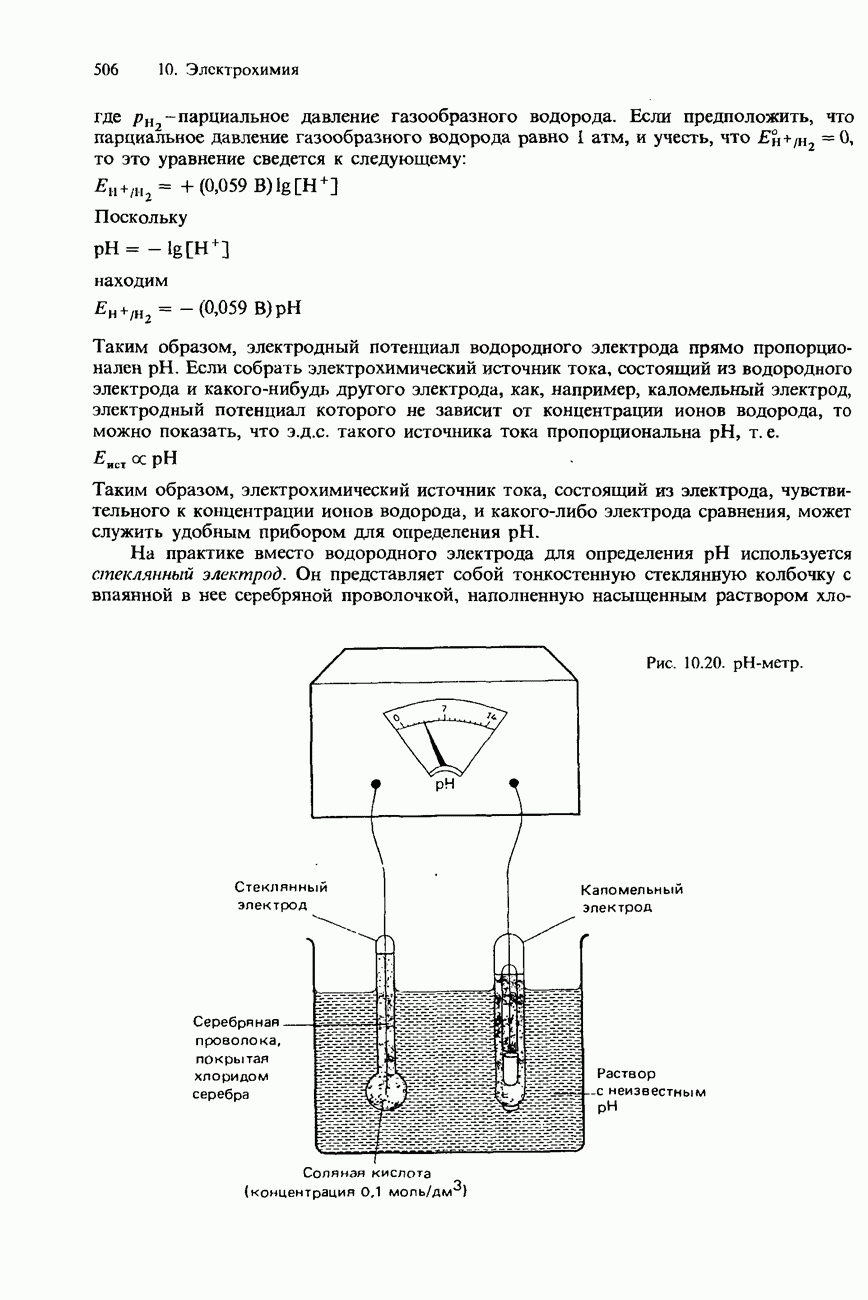
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
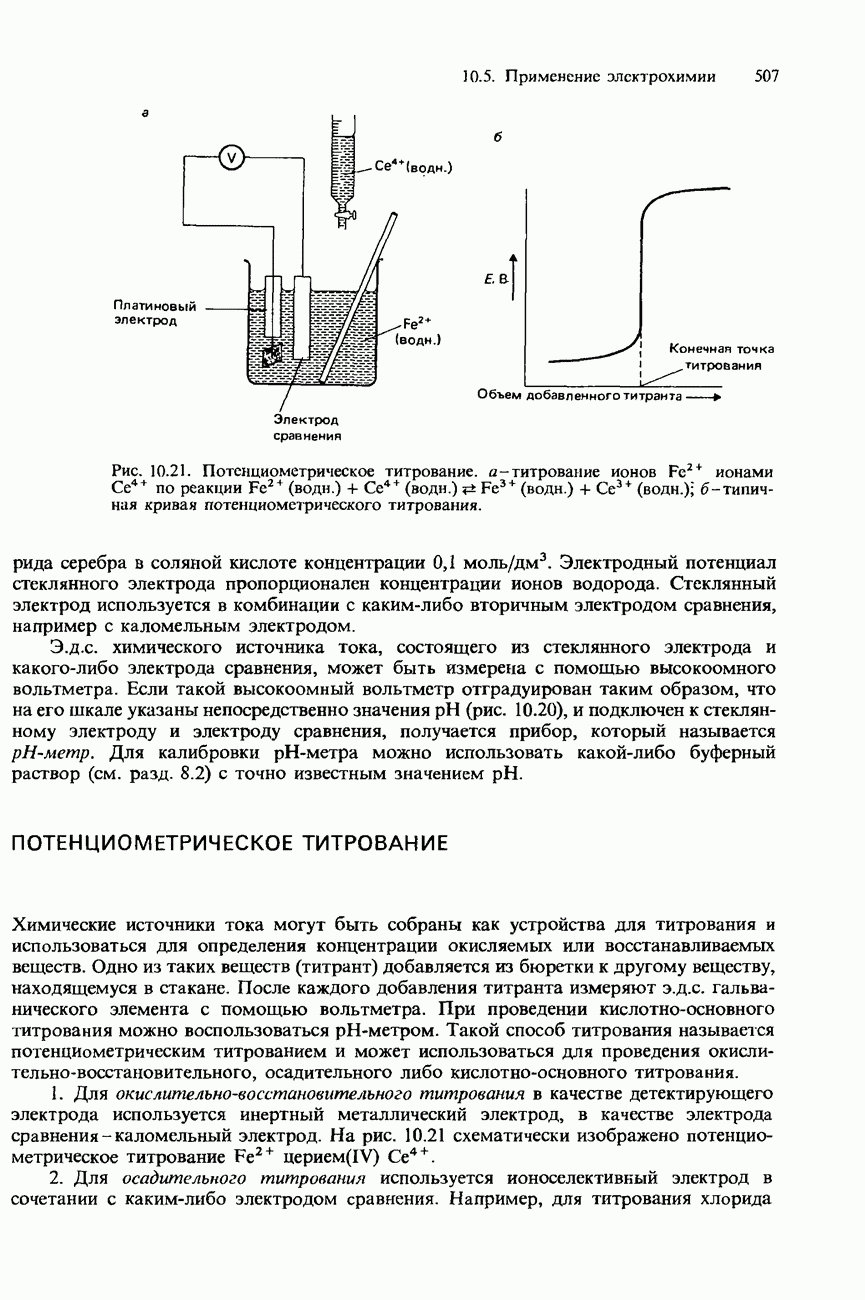
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
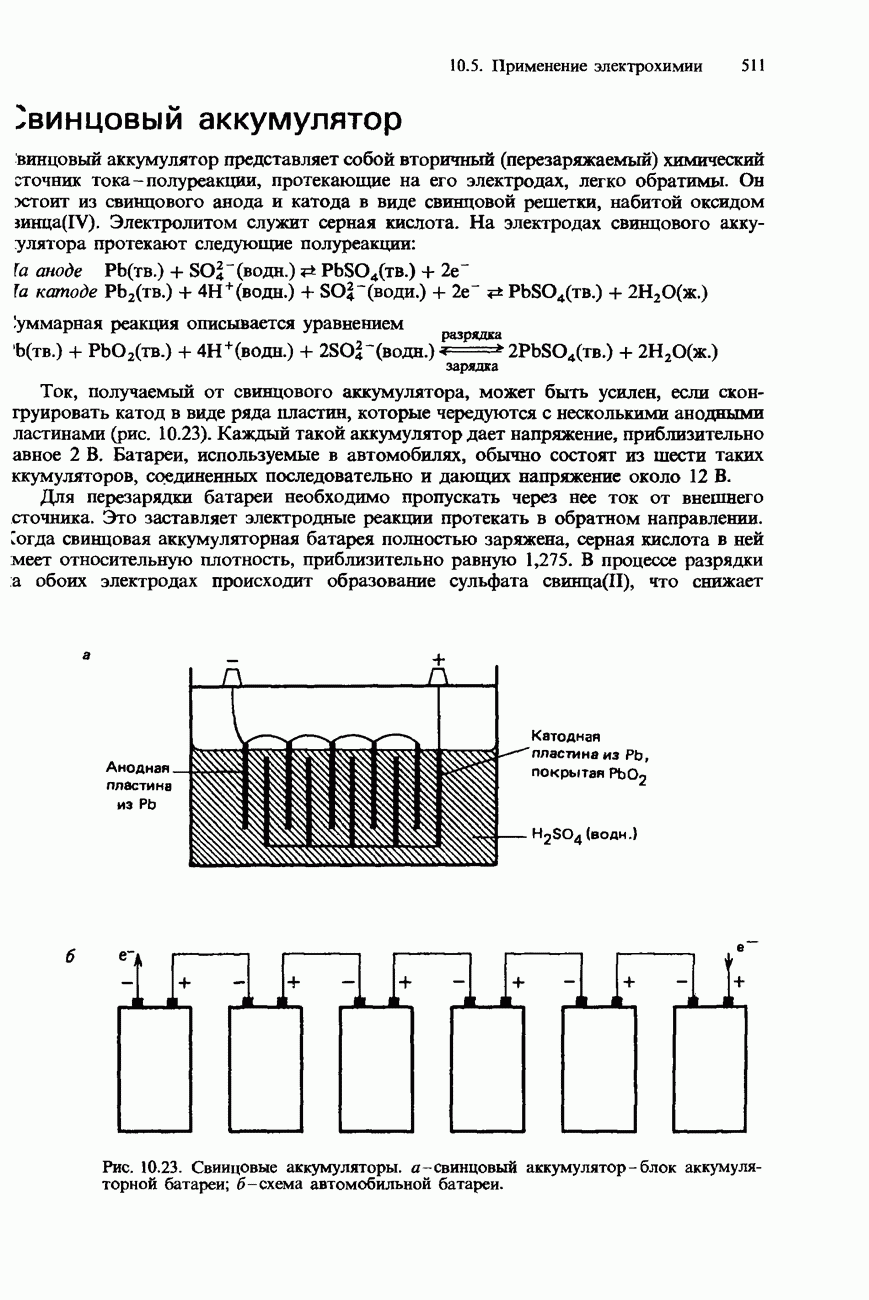
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ