| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РАСТВОРИМОСТЬ
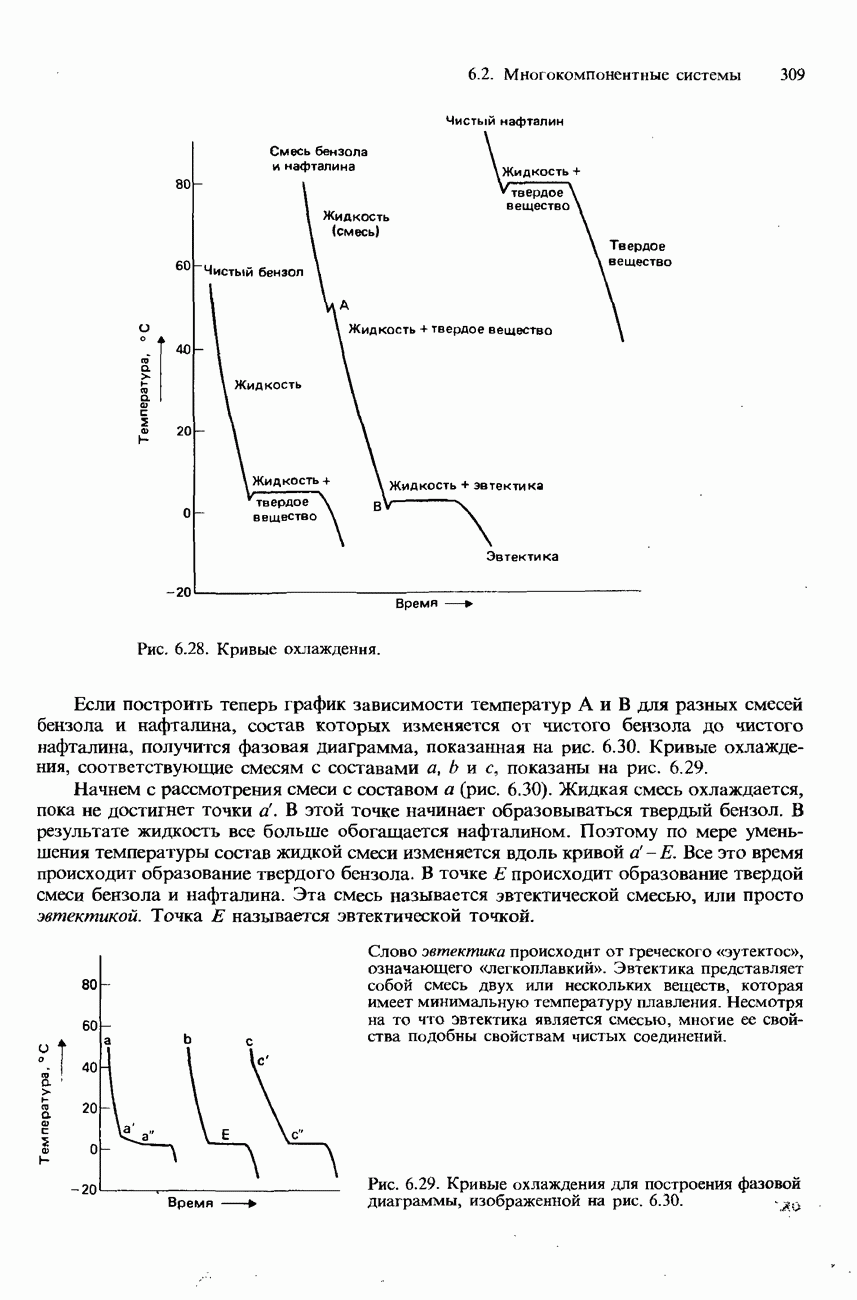
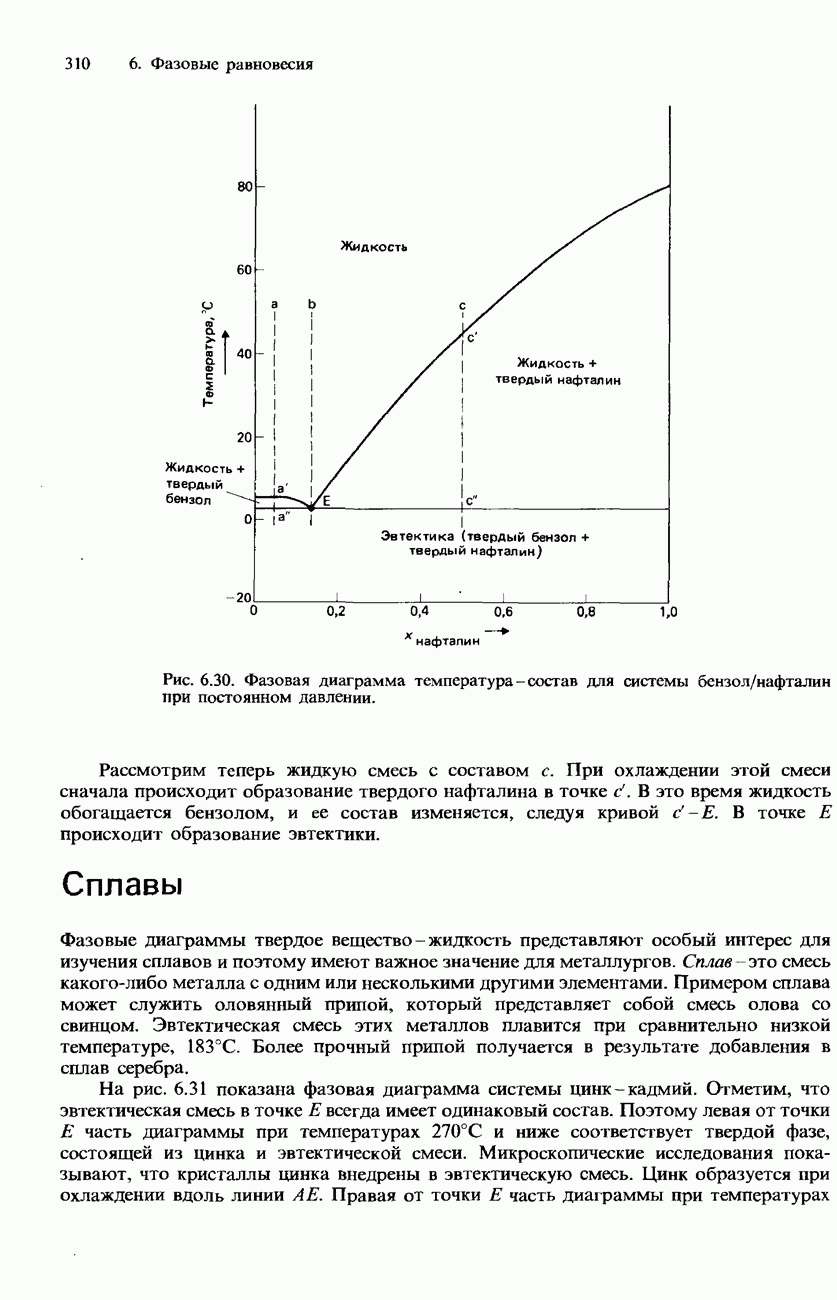
В гл. 2 было рассказано о том, что ионные соединения, как правило, растворяются в полярных растворителях, например в воде. Растворимость в таких случаях обусловлена сольватацией (в случае воды ее называют гидратацией) ионов полярными молекулами растворителя. Изменения энтальпии, которыми сопровождаются растворение и гидратация, обсуждались в гл. 5. Затем в гл. 6 было рассказано о том, что кривая растворимости какой-либо соли в воде представляет собой часть фазовой диаграммы для двухкомпонентной смеси.
Обратимся теперь к рассмотрению ионных равновесий, которые устанавливаются при растворении ионных соединений в воде.
Произведение растворимости
Насыщенный раствор образуется в том случае, когда растворяемое вещество больше уже не может растворяться в нем. Если растворяемое вещество представляет собой ионное соединение, то ионы в насыщенном растворе находятся в динамическом равновесии с избыточным, нерастворившимся твердым веществом. Например, в насыщенном растворе хлорида серебра устанавливается следующее равновесие:

Константа этого равновесия определяется выражением

Константа  называется произведением растворимости хлорида серебра.
называется произведением растворимости хлорида серебра.
Растворимость хлорида серебра можно выразить через концентрацию с растворенного  в воде. Эта концентрация совпадает с концентрацией обоих ионов в растворе:
в воде. Эта концентрация совпадает с концентрацией обоих ионов в растворе:

Таким образом, растворимость хлорида серебра может быть связана с его произведением растворимости следующим соотношением:

В насыщенном растворе соли, имеющей общую формулу  устанавливается равновесие
устанавливается равновесие

Произведение растворимости такой соли определяется выражением

Произведение растворимости  в таком случае имеет размерность (концентрация)
в таком случае имеет размерность (концентрация)  . Например, в насыщенном водном растворе
. Например, в насыщенном водном растворе  устанавливается равновесие
устанавливается равновесие

Следовательно,

Размерность произведения растворимости фосфата кальция (концентрация), или 
Значения  обычно приводятся только для электролитов, которые слабо растворимы в воде. Электролит считается слабо растворимым в воде, если его растворимость не превышает
обычно приводятся только для электролитов, которые слабо растворимы в воде. Электролит считается слабо растворимым в воде, если его растворимость не превышает  воды). Произведения растворимости некоторых слаборастворимых электролитов при 25 °С указаны в табл. 8.7. Отметим, что значения Кир представляют собой постоянные лишь применительно к определенному растворяемому веществу и при указанной температуре.
воды). Произведения растворимости некоторых слаборастворимых электролитов при 25 °С указаны в табл. 8.7. Отметим, что значения Кир представляют собой постоянные лишь применительно к определенному растворяемому веществу и при указанной температуре.
Для экспериментального определения произведений растворимости солей могут использоваться различные методы, в том числе титрование, ионный обмен (см. ниже) и электрохимические методы (см. гл. 10). Для определения произведений растворимости можно использовать и такой метод, как полное выпаривание насыщенного раствора с последующим взвешиванием сухого остатка.
Таблица 8.7. Произведения растворимости различных солей в воде при 

Растворимость солей металлов
Растворимость принято выражать, указывая массу растворяемого вещества, которая необходима для насыщения 100 г растворителя при заданной температуре. Кроме того, растворимость иногда выражают как количество растворяемого вещества в молях, необходимое для насыщения 1 кг воды. Ни один из этих способов не использует представления о концентрации, поскольку они не связаны с выражением растворимости через объем.
Следует отметить, что такие характеристики, как растворимое или нерастворимое вещество, являются лишь относительными, качественными понятиями. Например, если к 100 г воды при комнатной температуре добавить 50 г карбоната магния  то произойдет растворение лишь 0,06 г этой соли. Поэтому карбонат магния обычно считается нерастворимой солью. Вместе с тем, если к 100 г воды при комнатной температуре добавить 50 г гидрата сульфата магния
то произойдет растворение лишь 0,06 г этой соли. Поэтому карбонат магния обычно считается нерастворимой солью. Вместе с тем, если к 100 г воды при комнатной температуре добавить 50 г гидрата сульфата магния  то произойдет растворение 36,4 г этой соли. Поэтому сульфат магния считается растворимой солью. Не существует солей металлов, которые совершенно нерастворимы в воде. Например, карбонат
то произойдет растворение 36,4 г этой соли. Поэтому сульфат магния считается растворимой солью. Не существует солей металлов, которые совершенно нерастворимы в воде. Например, карбонат  обычно считается очень плохо растворимым в воде. И все же в 100 г воды при комнатной температуре растворяется 0,000 017 г
обычно считается очень плохо растворимым в воде. И все же в 100 г воды при комнатной температуре растворяется 0,000 017 г 
Пример
Установлено, что насыщенный водный раствор фторида кальция  при 25 °С содержит
при 25 °С содержит  растворенного вещества. Вычислим
растворенного вещества. Вычислим  для
для 
Решение
В насыщенном растворе фторида кальция устанавливается равновесие

Следовательно, 
Начнем с вычисления концентрации с растворенного  Поскольку
Поскольку  г/моль,
г/моль,

Из стехиометрического уравнения, описывающего равновесие растворения фторида кальция, следует, что

Подставляя эти значения в выражение для  находим
находим

Условия осаждения солей
Произведения растворимостей могут использоваться для предсказания условий осаждения солей из раствора. Допустим, например, что разбавленный раствор хлорида бария смешивают с разбавленным раствором сульфата натрия. Как узнать, будет ли происходить осаждение сульфата бария из полученной смеси? Прежде всего необходимо рассмотреть равновесие

Произведение растворимости сульфата бария определяется выражением

При 25 °С произведение растворимости сульфата бария имеет постоянное значение  Если произведение концентраций ионов
Если произведение концентраций ионов  в двух смешиваемых растворах превосходит произведение растворимости сульфата бария, то после смешивания раствора будет происходить осаждение сульфата бария до тех пор, пока произведение концентраций ионов бария и сульфата не станет меньше произведения растворимости. Но если в растворю после смешивания произведение концентраций этих ионов меньше, чем произведение растворимости сульфата бария, то осаждение вообще не будет происходить. В этом случае положение равновесия полностью находится в правой части уравнения (11). Сказанное выше можно сформулировать с помощью следующих математических соотношений:
в двух смешиваемых растворах превосходит произведение растворимости сульфата бария, то после смешивания раствора будет происходить осаждение сульфата бария до тех пор, пока произведение концентраций ионов бария и сульфата не станет меньше произведения растворимости. Но если в растворю после смешивания произведение концентраций этих ионов меньше, чем произведение растворимости сульфата бария, то осаждение вообще не будет происходить. В этом случае положение равновесия полностью находится в правой части уравнения (11). Сказанное выше можно сформулировать с помощью следующих математических соотношений:

Эффект общего иона
При растворении хлорида серебра в воде после образования насыщенного раствора устанавливается равновесие

Если добавить в раствор дополнительное количество хлорид-ионов, например в виде хлорида натрия, то равновесие сдвинется влево. В этом заключается эффект общего иона. В рассматриваемом случае хлорид-ион является общим ионом как для хлорида серебра, так и для хлорида натрия.
Поскольку добавление общего иона приводит к смещению равновесия влево, из раствора должно начаться осаждение хлорида серебра. Таким образом, добавление общего иона приводит к уменьшению растворимости хлорида серебра. Такое же воздействие окажет на раствор и добавление к нему раствора нитрата серебра, только при этом общим ионом будет ион серебра 
Эффект общего иона приводит к тому, что растворимость всякого электролита в водном растворю, содержащем общий с данным электролитом ион, меньше растворимости этого электролита в воде. Например, при 25 °С растворимость  в воде приблизительно равна
в воде приблизительно равна  Однако в растворе
Однако в растворе  с концентрацией 0,1 моль/дм3 растворимость сульфата бария составляет всего
с концентрацией 0,1 моль/дм3 растворимость сульфата бария составляет всего  Это значение можно проверить, пользуясь уравнением (11). Зная произведение растворимости какого-либо электролита, можно вычислить, какое количество этого электролита подвергнется осаждению из раствора после добавления общего иона.
Это значение можно проверить, пользуясь уравнением (11). Зная произведение растворимости какого-либо электролита, можно вычислить, какое количество этого электролита подвергнется осаждению из раствора после добавления общего иона.
Эффект общего иона приводит также к снижению степени диссоциации слабых электролитов. Вернемся к равновесию, которое устанавливается в водном растворе уксусной кислоты:

Если в этот раствор добавить ацетат натрия, то положение равновесия сместится влево. Другими словами, в результате добавления общего иона  произойдет уменьшение степени диссоциации уксусной кислоты. Аналогичный эффект будет достигнут в результате добавления небольшого количества какой-либо сильной кислоты. В этом случае общим ионом окажется ион гидроксония
произойдет уменьшение степени диссоциации уксусной кислоты. Аналогичный эффект будет достигнут в результате добавления небольшого количества какой-либо сильной кислоты. В этом случае общим ионом окажется ион гидроксония 
Применения эффекта общего иона
Гравиметрический анализ. Концентрацию сульфата в водном растворе можно определить гравиметрически, добавляя раствор хлорида бария с целью осаждения сульфата бария. Осадок отфильтровывают и затем промывают, но не водой, а разбавленной серной кислотой. Наличие ионов  в промывном растворе обеспечивает сохранение в осадке максимального количества сульфата бария.
в промывном растворе обеспечивает сохранение в осадке максимального количества сульфата бария.
Качественный анализ. В классических схемах качественного неорганического анализа обнаружение ионов различных металлов в водном растворе основано на применении эффекта общего иона. Ионы некоторых металлов осаждаются из раствора в виде сульфидных солей в результате продувания сероводорода через раствор. Например, чтобы осадить из раствора ион металла  в виде сульфидной соли, нужно создать условия, при которых
в виде сульфидной соли, нужно создать условия, при которых

Таким образом, если концентрация сульфид-ионов  невелика, из раствора будет происходить осаждение в виде сульфидов только тех металлов, сульфиды которых имеют низкие значения
невелика, из раствора будет происходить осаждение в виде сульфидов только тех металлов, сульфиды которых имеют низкие значения  Концентрация ионов
Концентрация ионов  в растворе зависит от его
в растворе зависит от его  потому что сероводород в водном растворе обладает свойствами слабой кислоты:
потому что сероводород в водном растворе обладает свойствами слабой кислоты:

При добавлении в раствор некоторого количества кислоты это равновесие смещается влево. В результате происходит уменьшение концентрации сульфидных ионов. Это означает, что из кислого раствора должно происходить осаждение только тех металлов, сульфиды которых имеют самые низкие значения  . В эту группу металлов попадают
. В эту группу металлов попадают 
Однако, если раствор сделать щелочным, рассматриваемое равновесие сместится вправо. В результате произойдет возрастание концентрации сульфидных ионов. В этих условиях из раствора будут осаждаться металлы, сульфиды которых характеризуются более высокими значениями  К этой группе металлов относятся цинк,
К этой группе металлов относятся цинк, 
Высаливание
Термин высаливание часто используется в промышленности и означает удаление соли из раствора. Высаливание применяется, например, в производстве мыла. Главной составной частью мыла является стеарат натрия  иначе называемый октадеканоат натрия. Его высаливание осуществляется добавлением концентрированного раствора хлорида натрия. Это приводит к тому, что произведение концентраций стеарат-иона и иона натрия оказывается больше произведения растворимости стеарата натрия. В данном случае высаливание обусловлено эффектом общего иона, роль которого играет ион натрия
иначе называемый октадеканоат натрия. Его высаливание осуществляется добавлением концентрированного раствора хлорида натрия. Это приводит к тому, что произведение концентраций стеарат-иона и иона натрия оказывается больше произведения растворимости стеарата натрия. В данном случае высаливание обусловлено эффектом общего иона, роль которого играет ион натрия  .
.
Для высаливания из раствора хлорида натрия, сильного электролита, можно воспользоваться добавлением концентрированной соляной кислоты либо продуванием газообразного хлороводорода через раствор соли. В данном случае высаливание обусловливается не только эффектом общего иона, но также высокой степенью гидратации ионов, образующихся при диссоциации кислоты. Последнее обстоятельство приводит к уменьшению количества воды, которая может служить растворителем для хлорида натрия.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
- Кривые распада
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
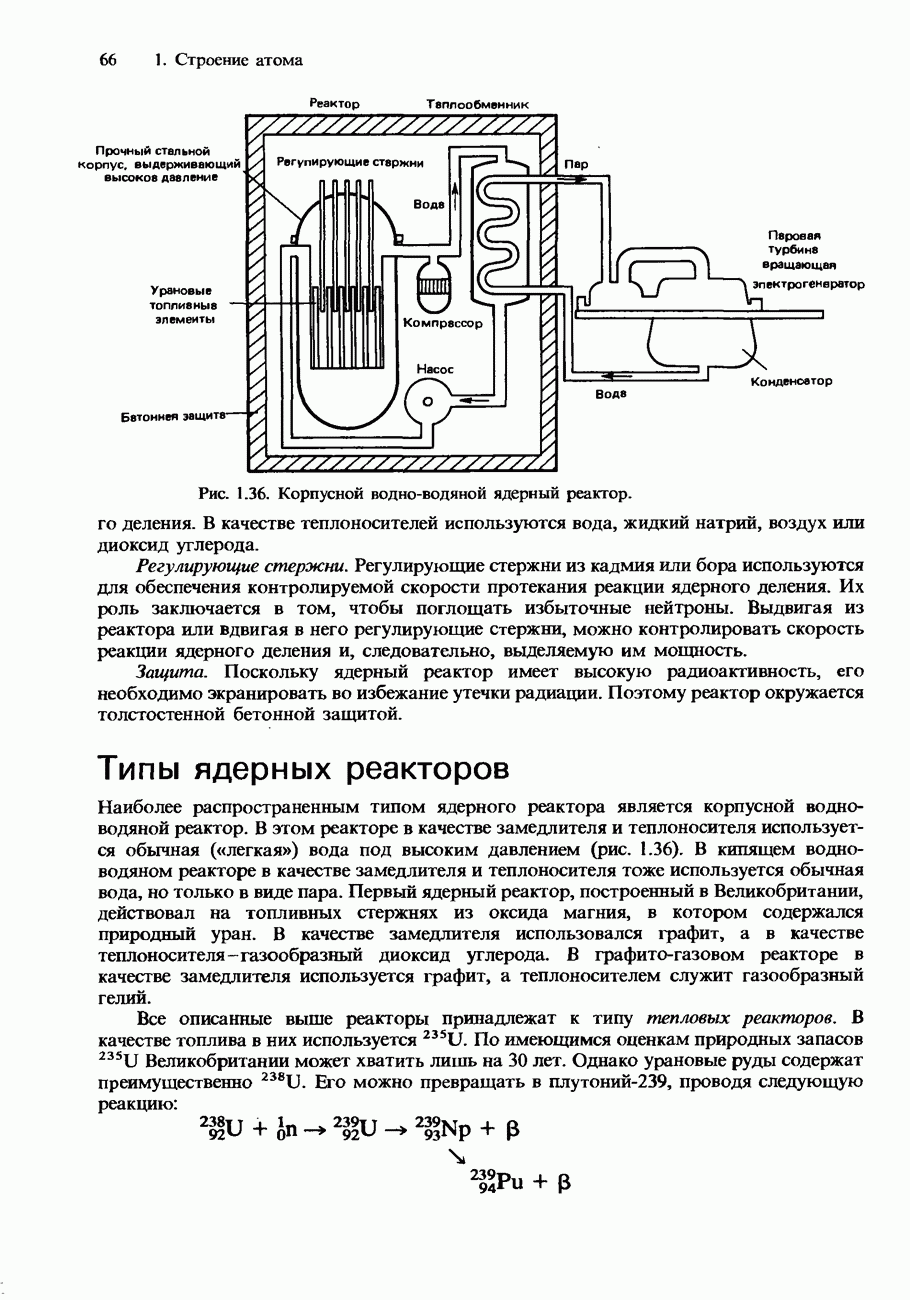
- Типы ядерных реакторов
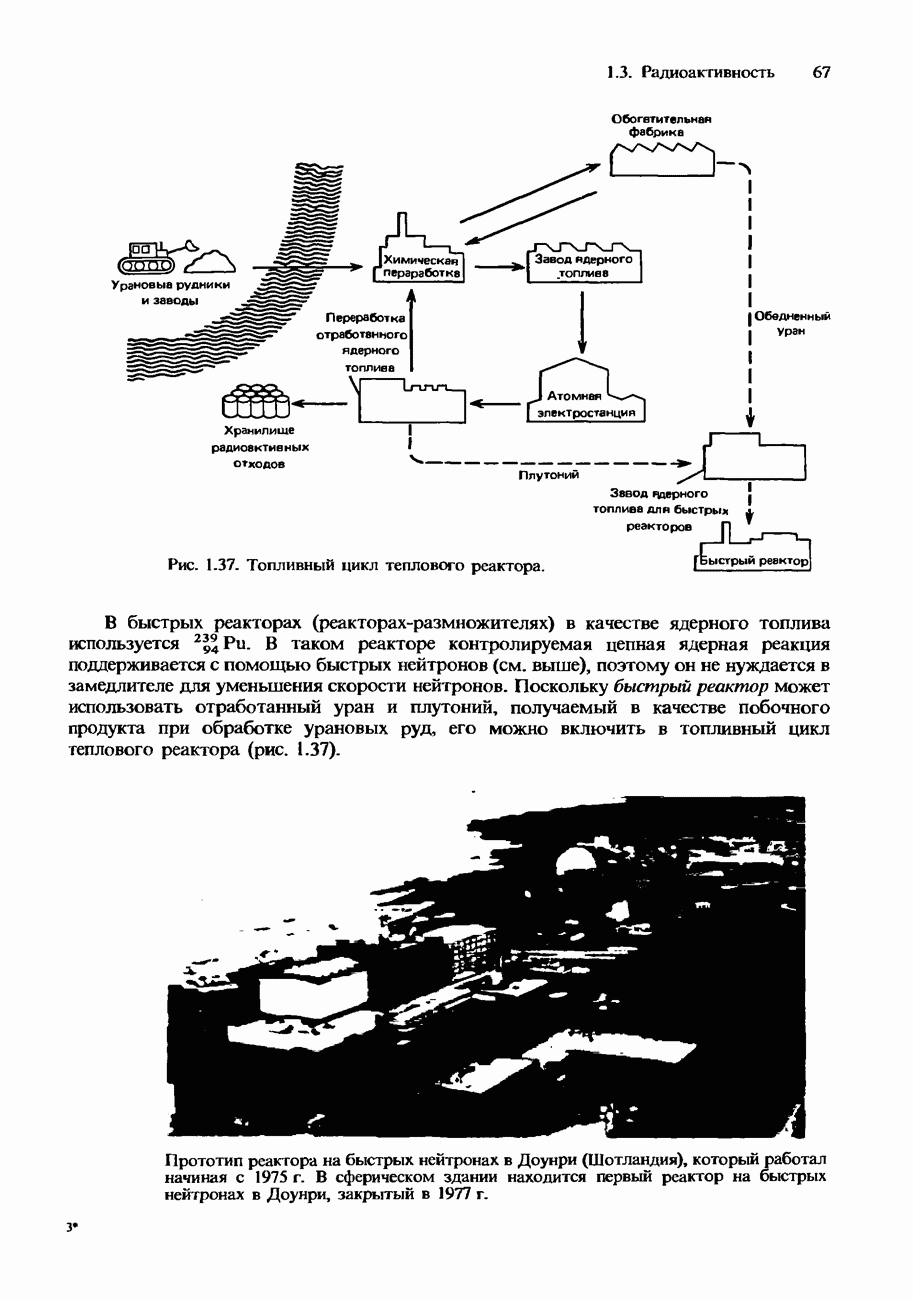
- Радиоактивные ядерные отходы и их переработка
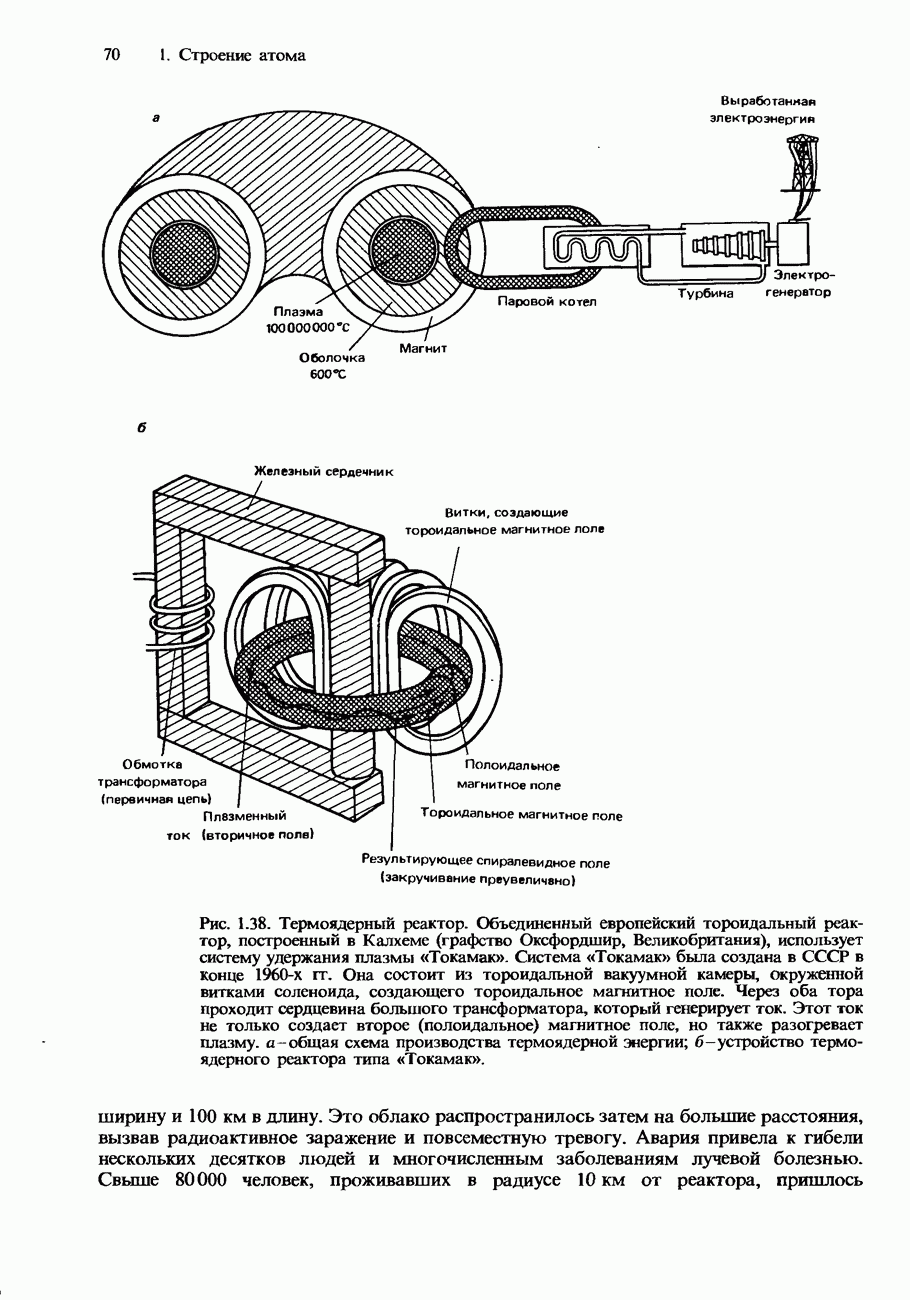
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
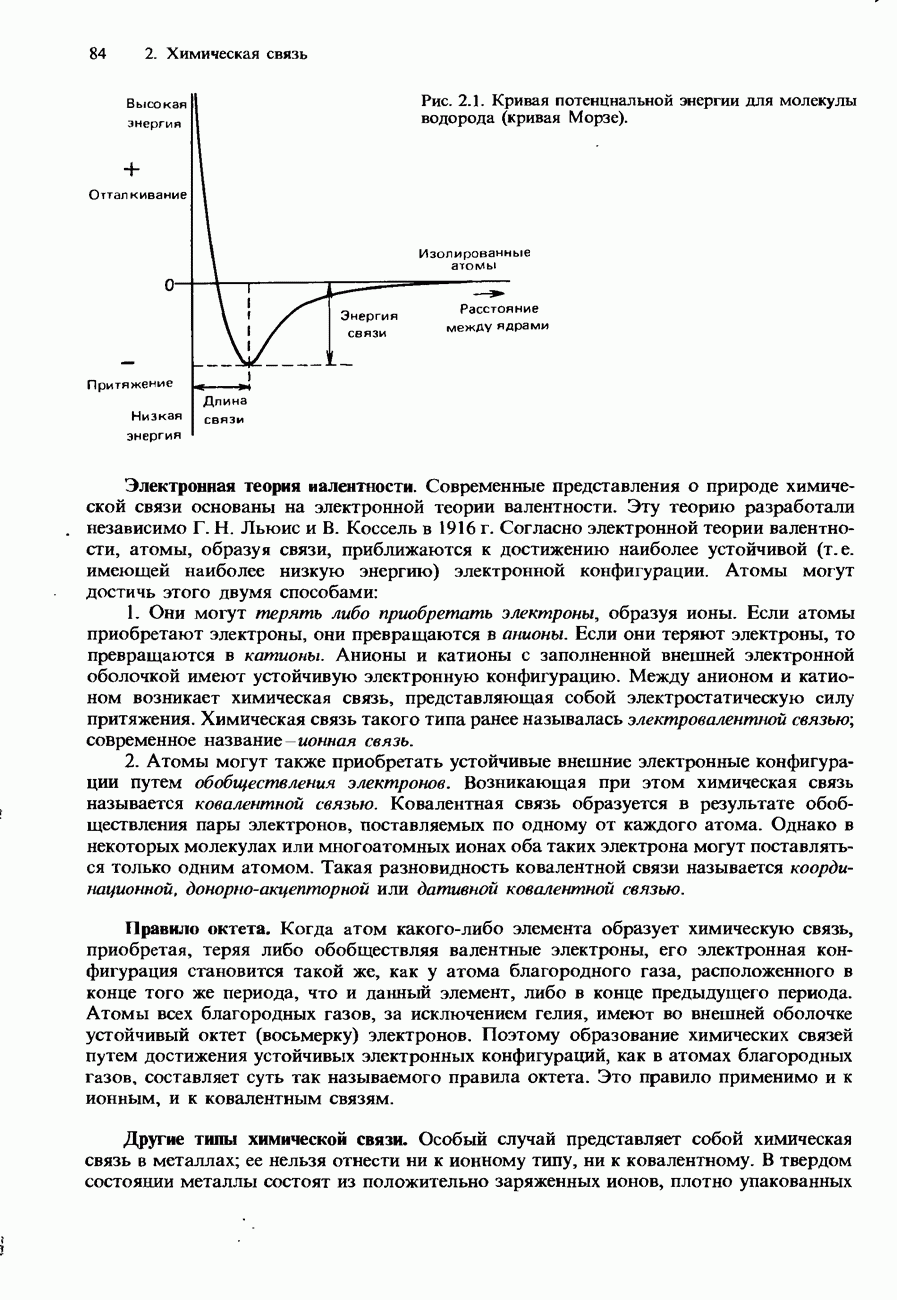
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
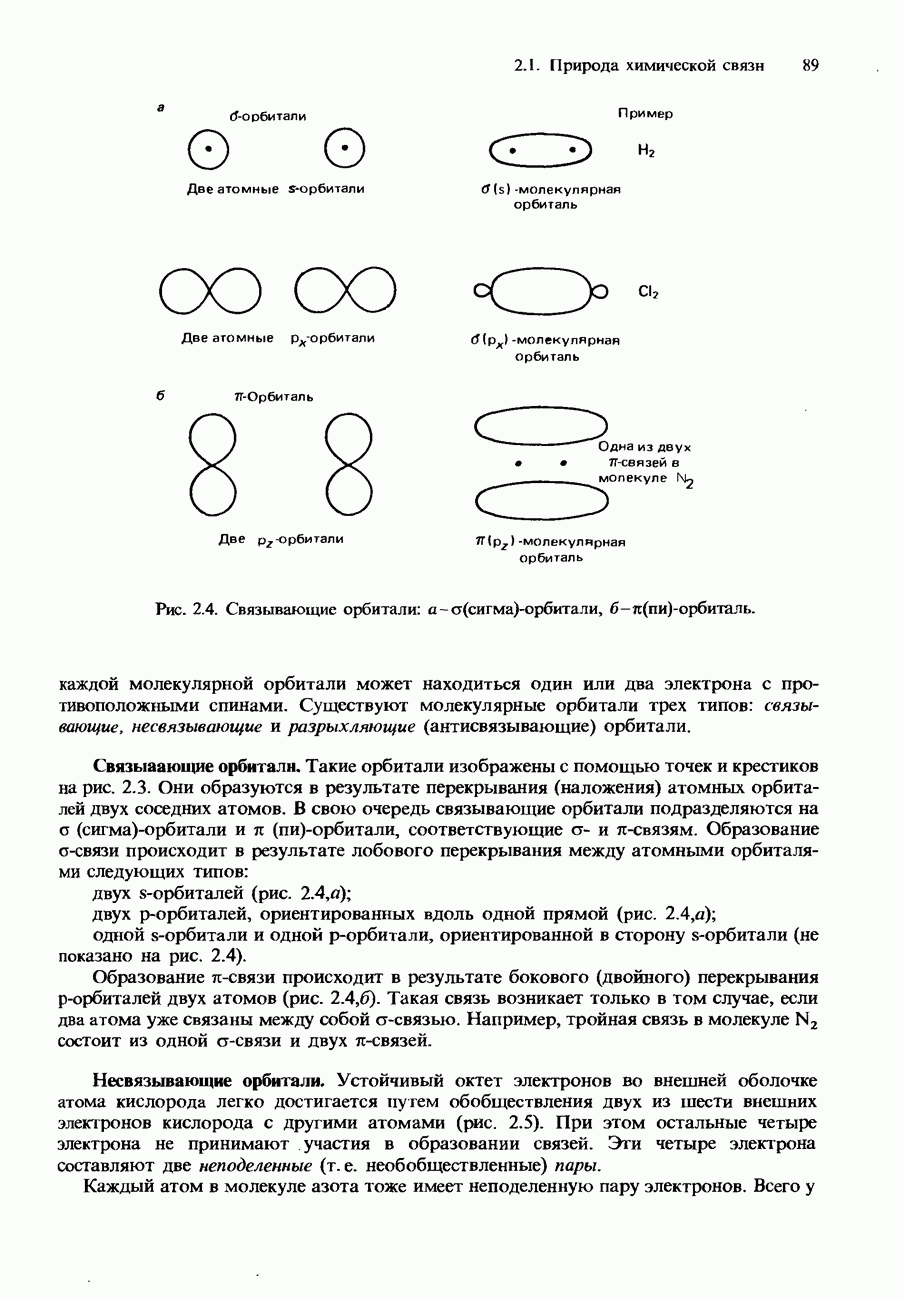
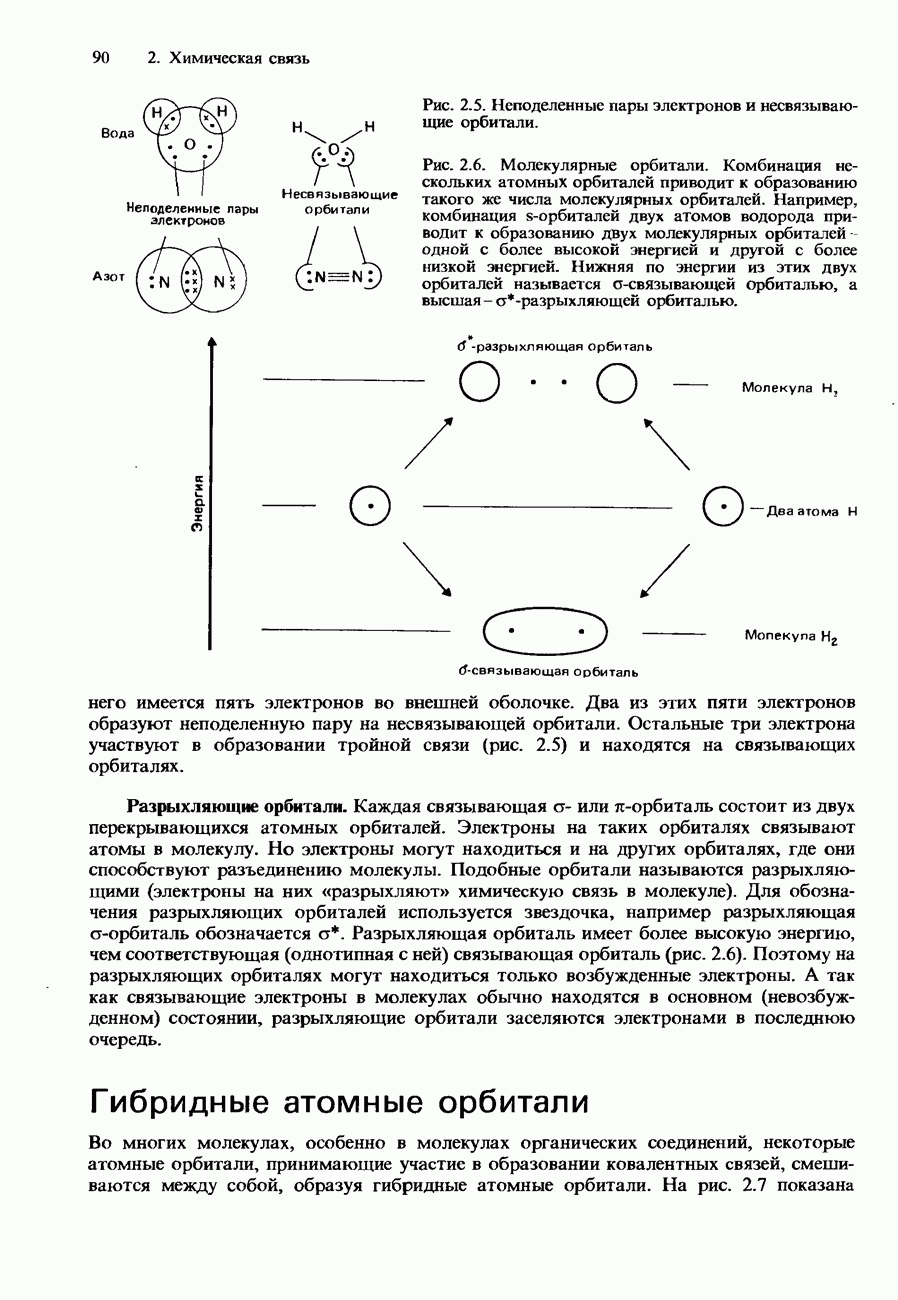
- Молекулярные орбитали
- Гибридные атомные орбитали
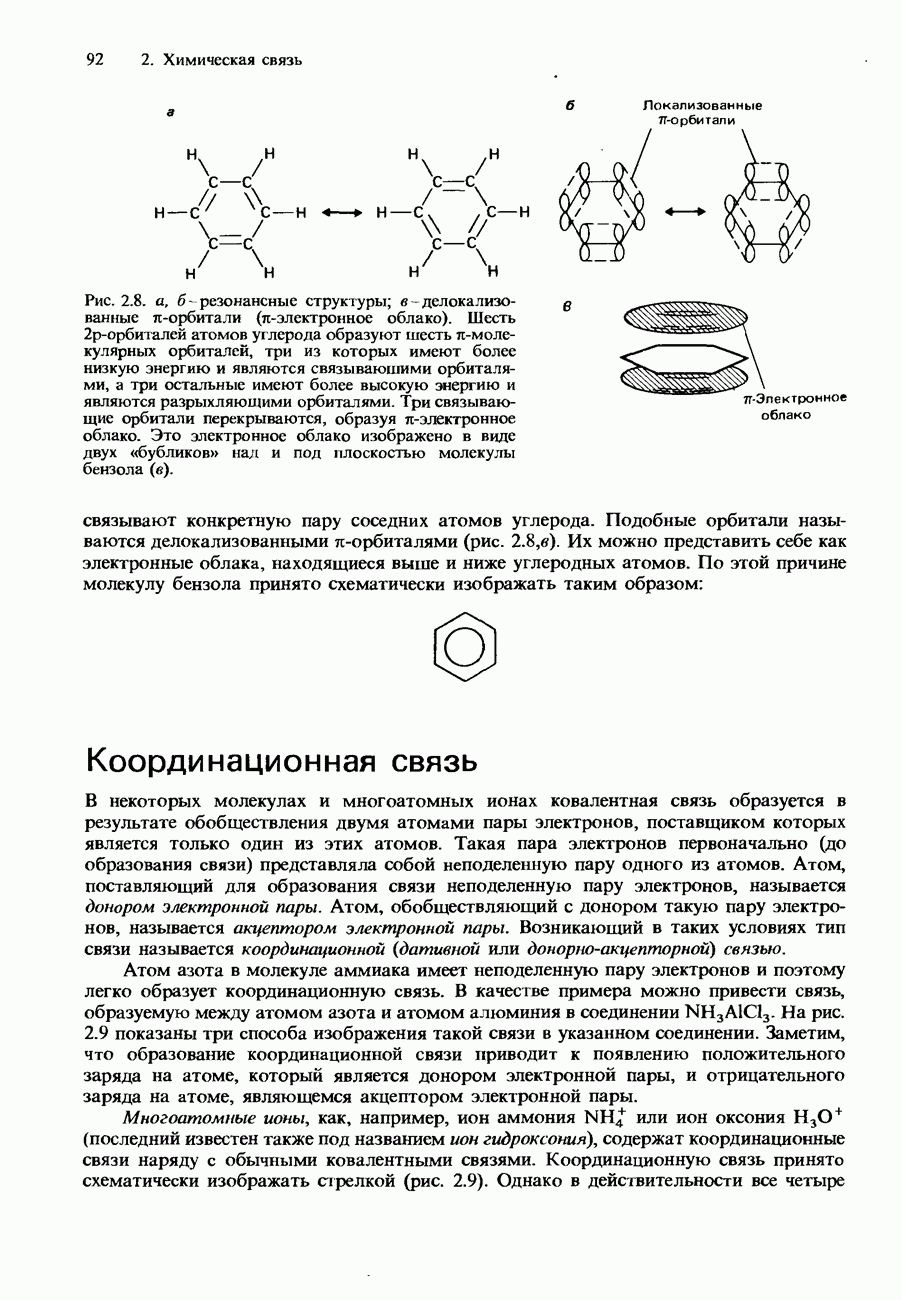
- Делокализованные орбитали
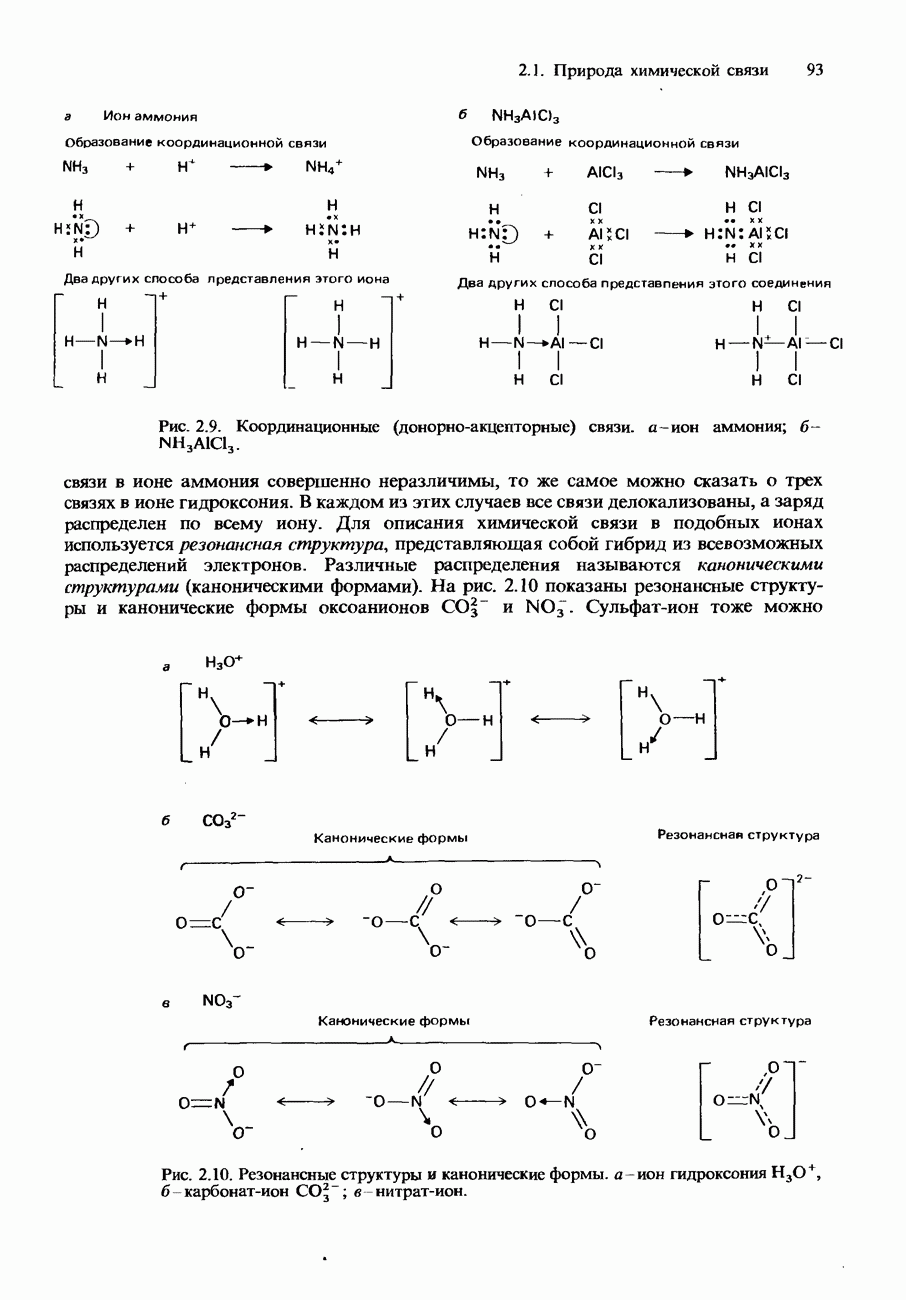
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
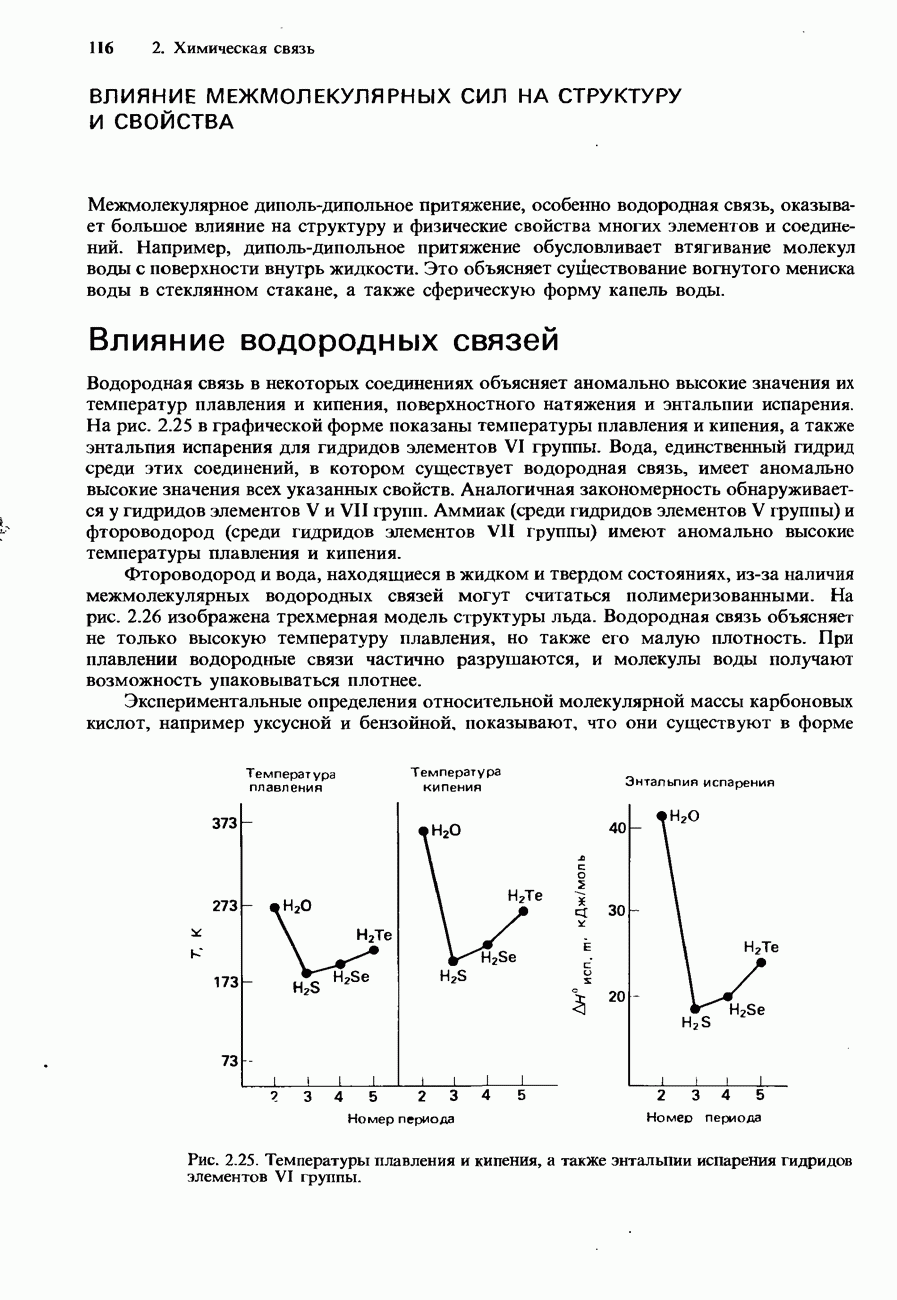
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
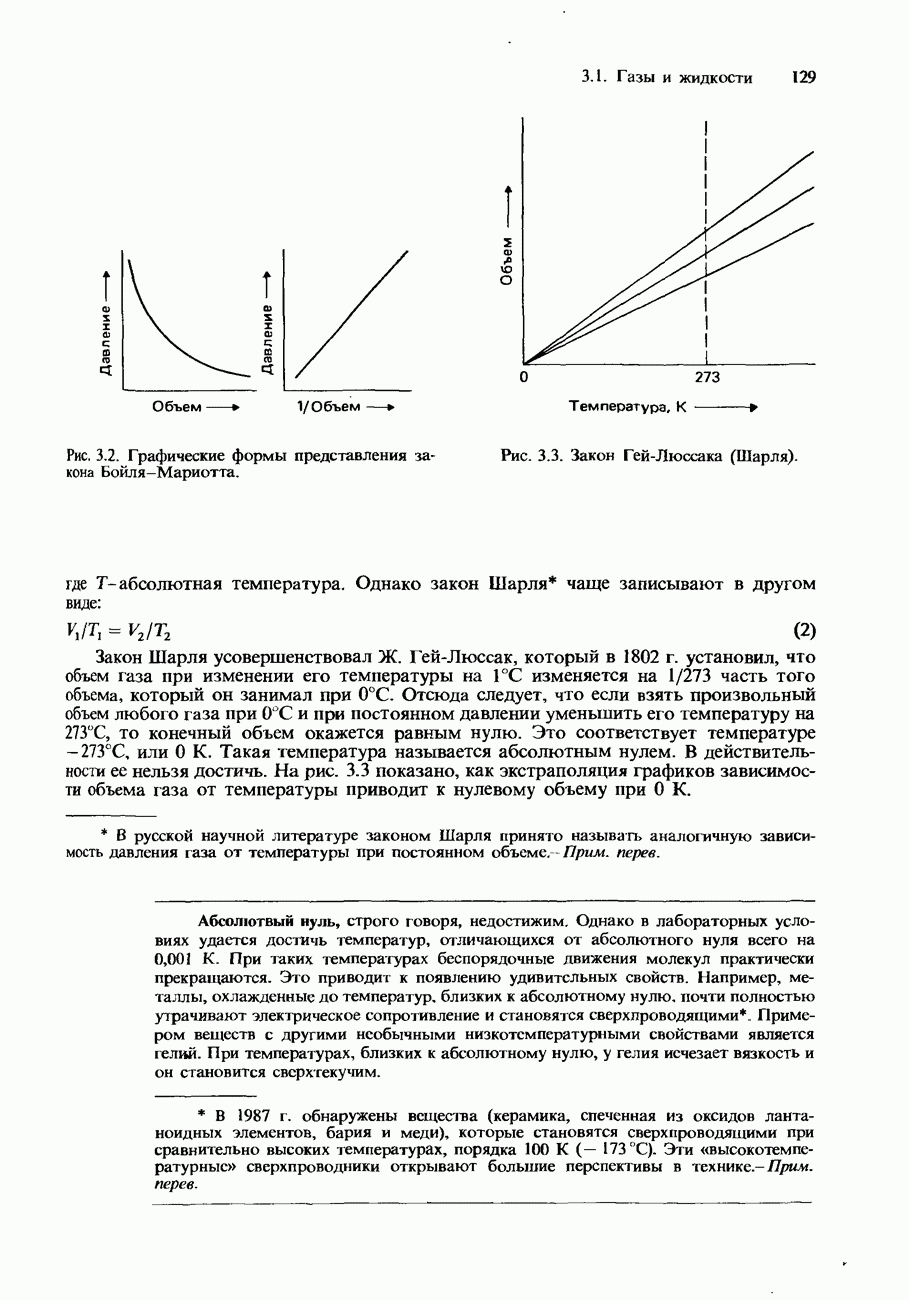
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
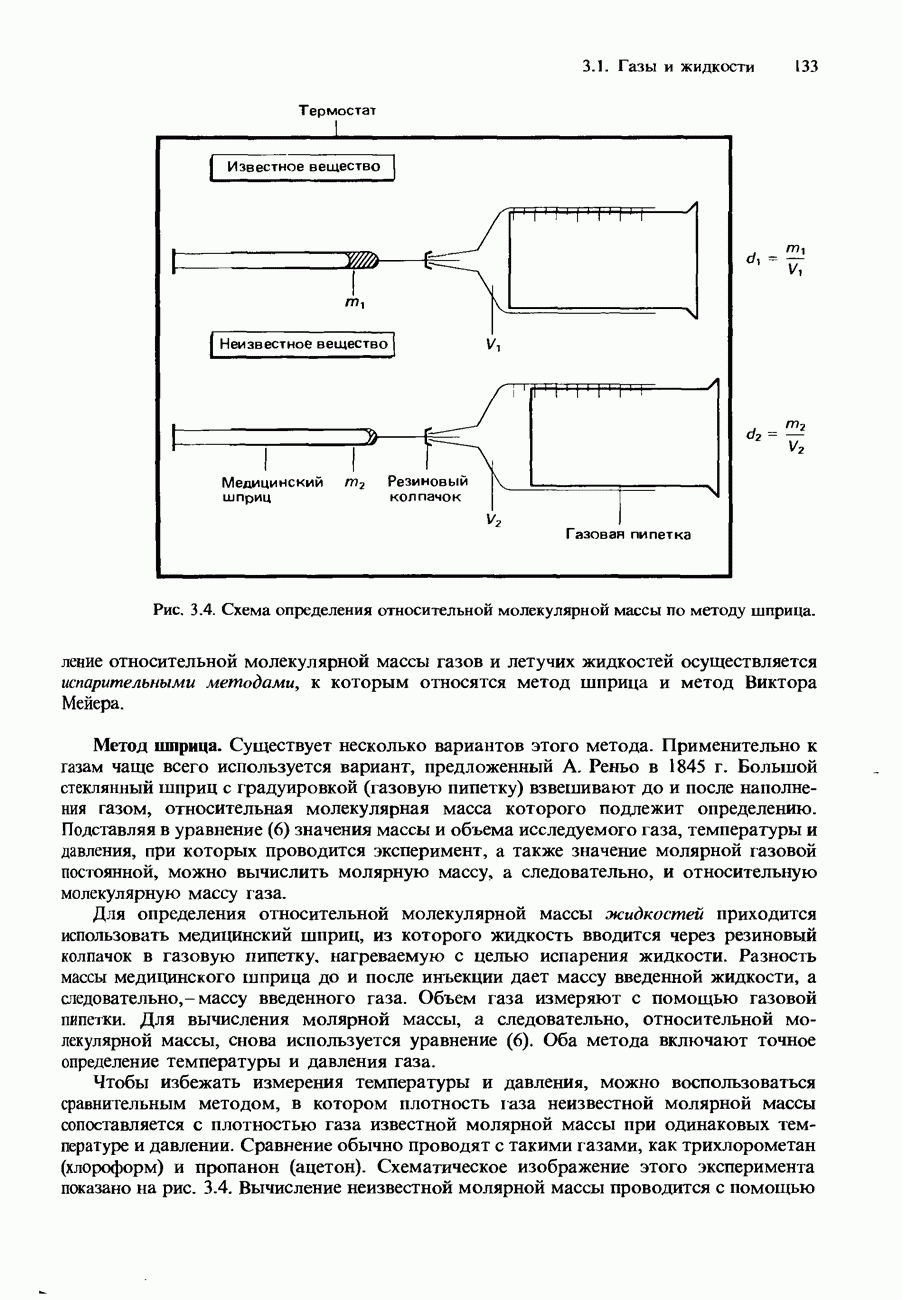
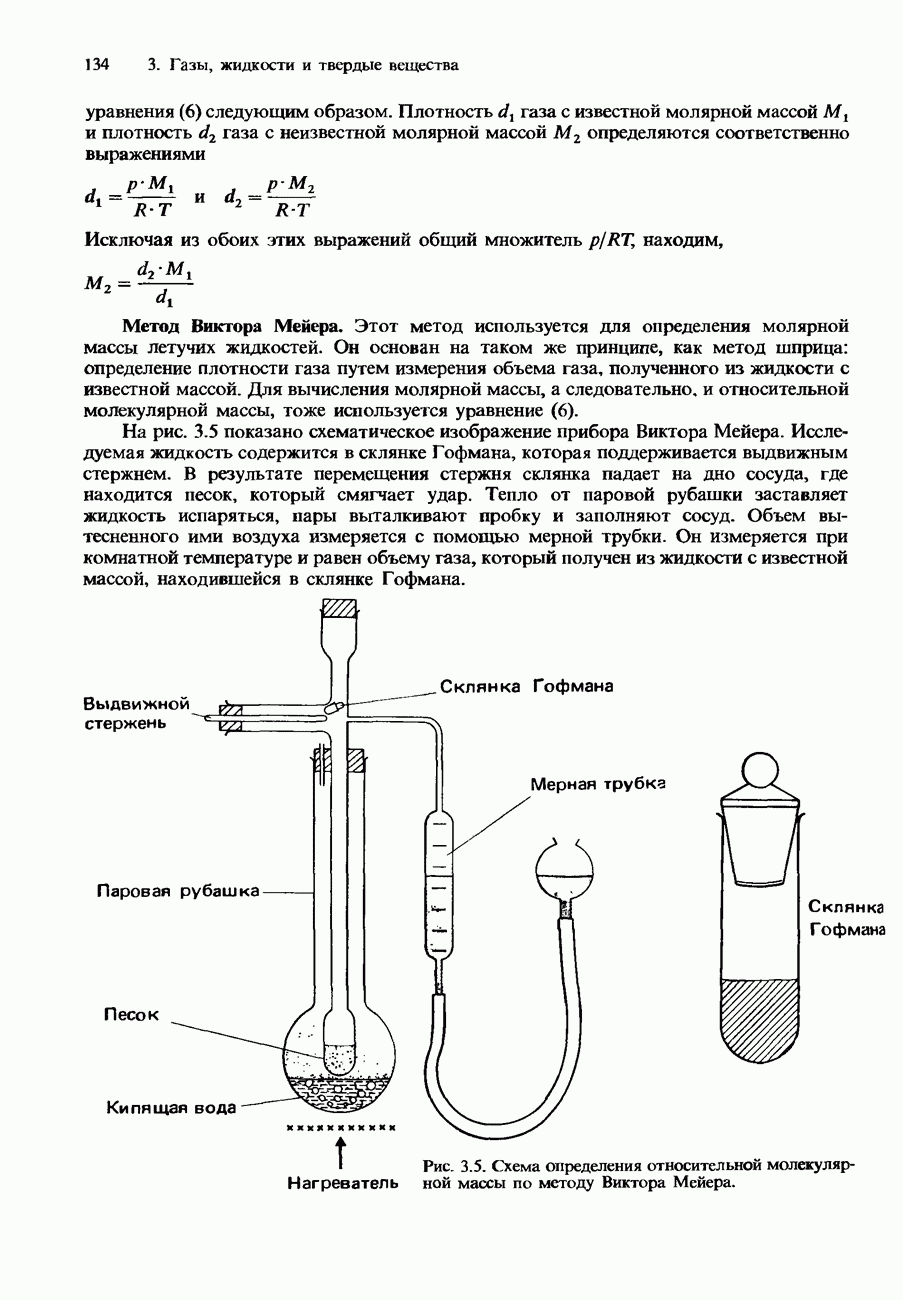
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
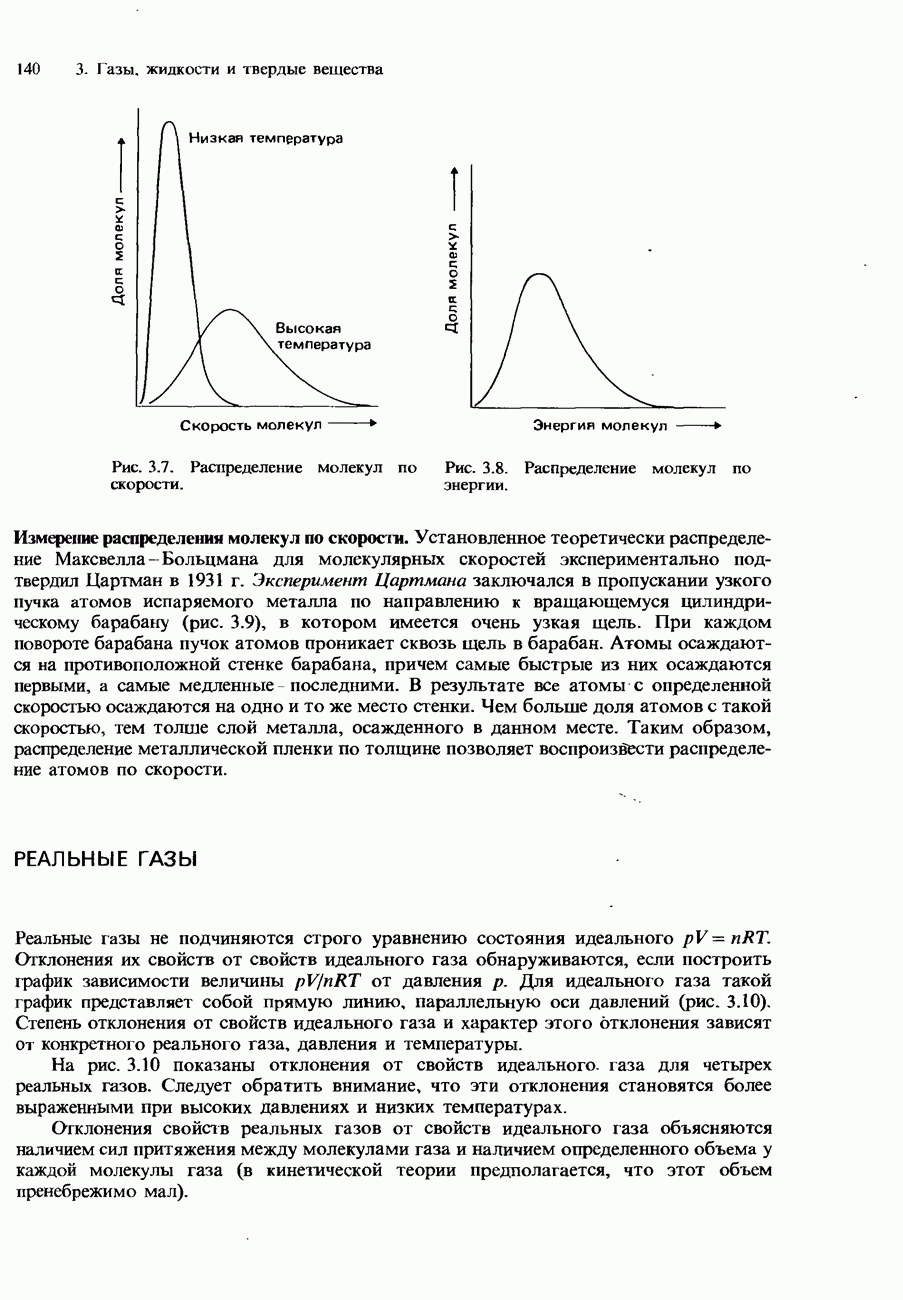
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
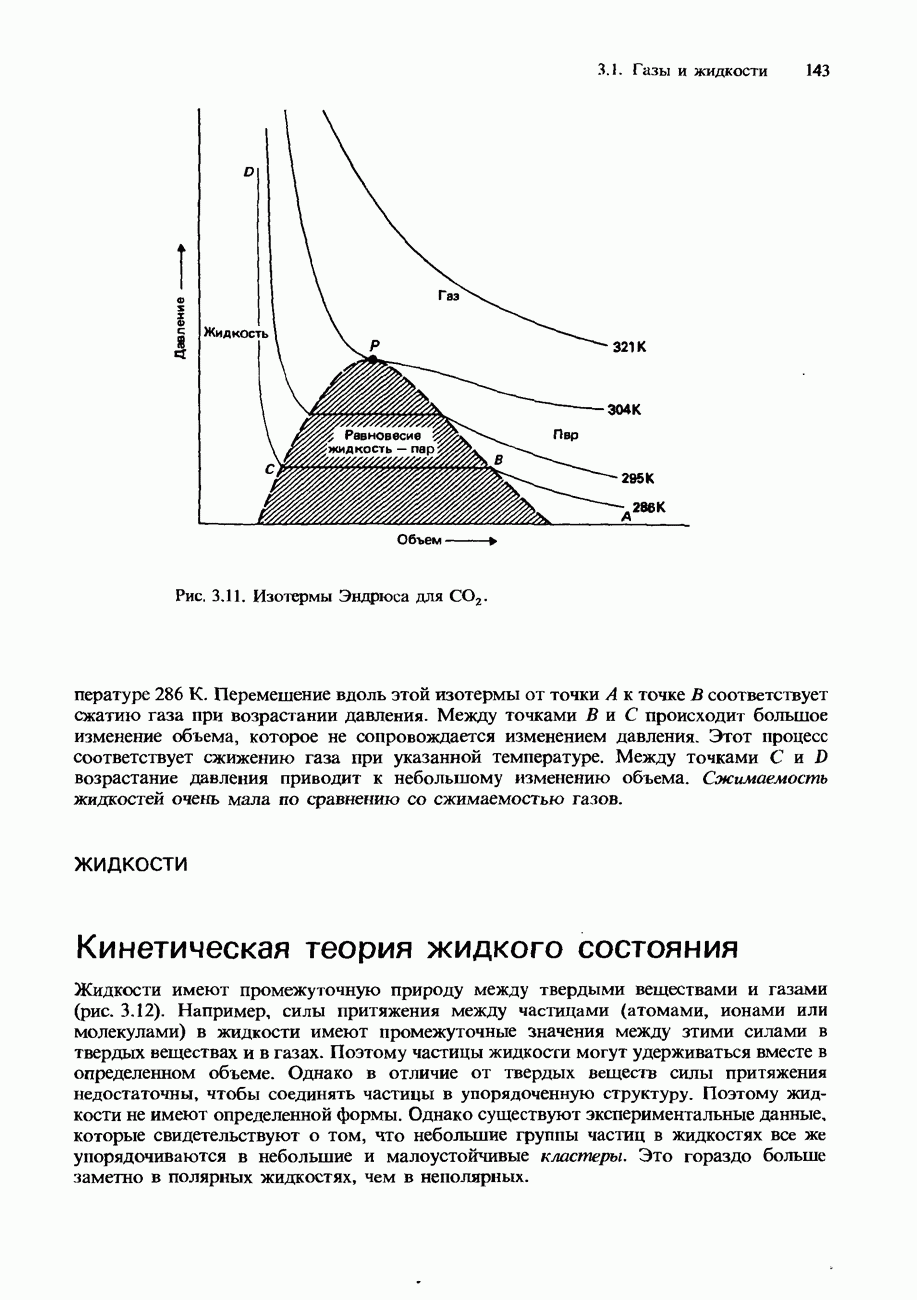
- Сжижение газов
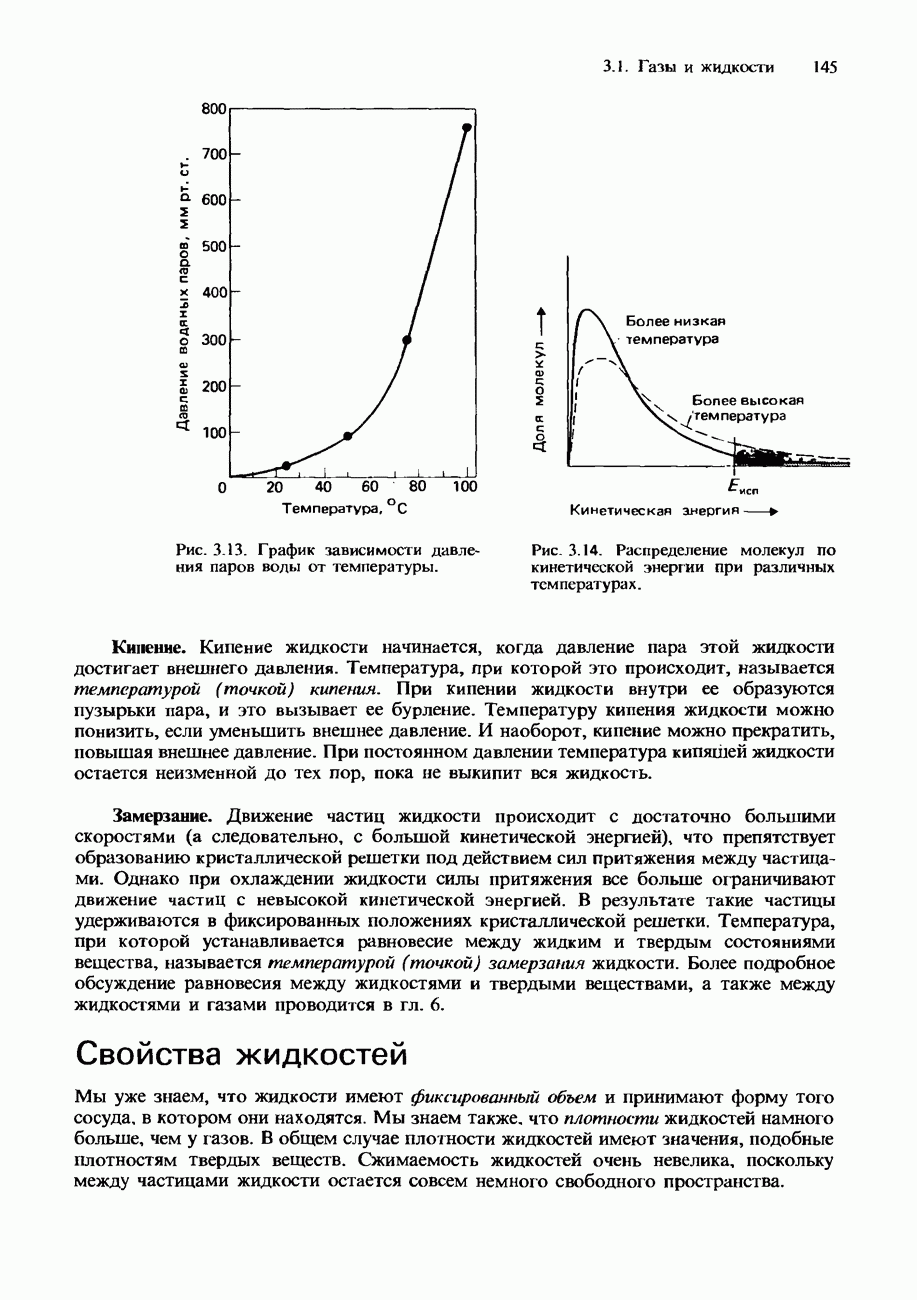
- ЖИДКОСТИ
- Свойства жидкостей
- 3.2. Твердые вещества
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
- Ионные кристаллы
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
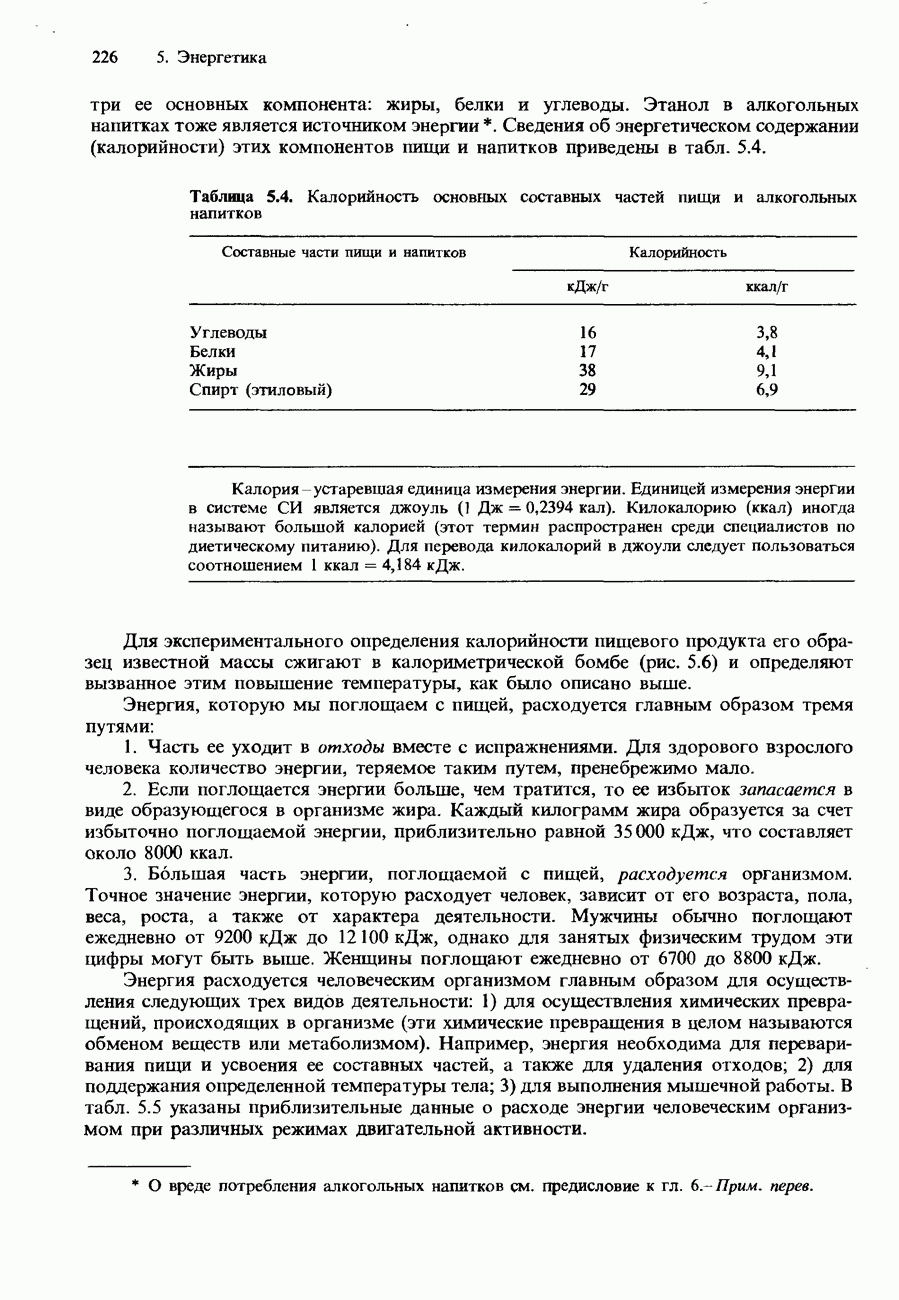
- КАЛОРИЙНОСТЬ ПИЩИ
- ЗАКОН ГЕССА
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
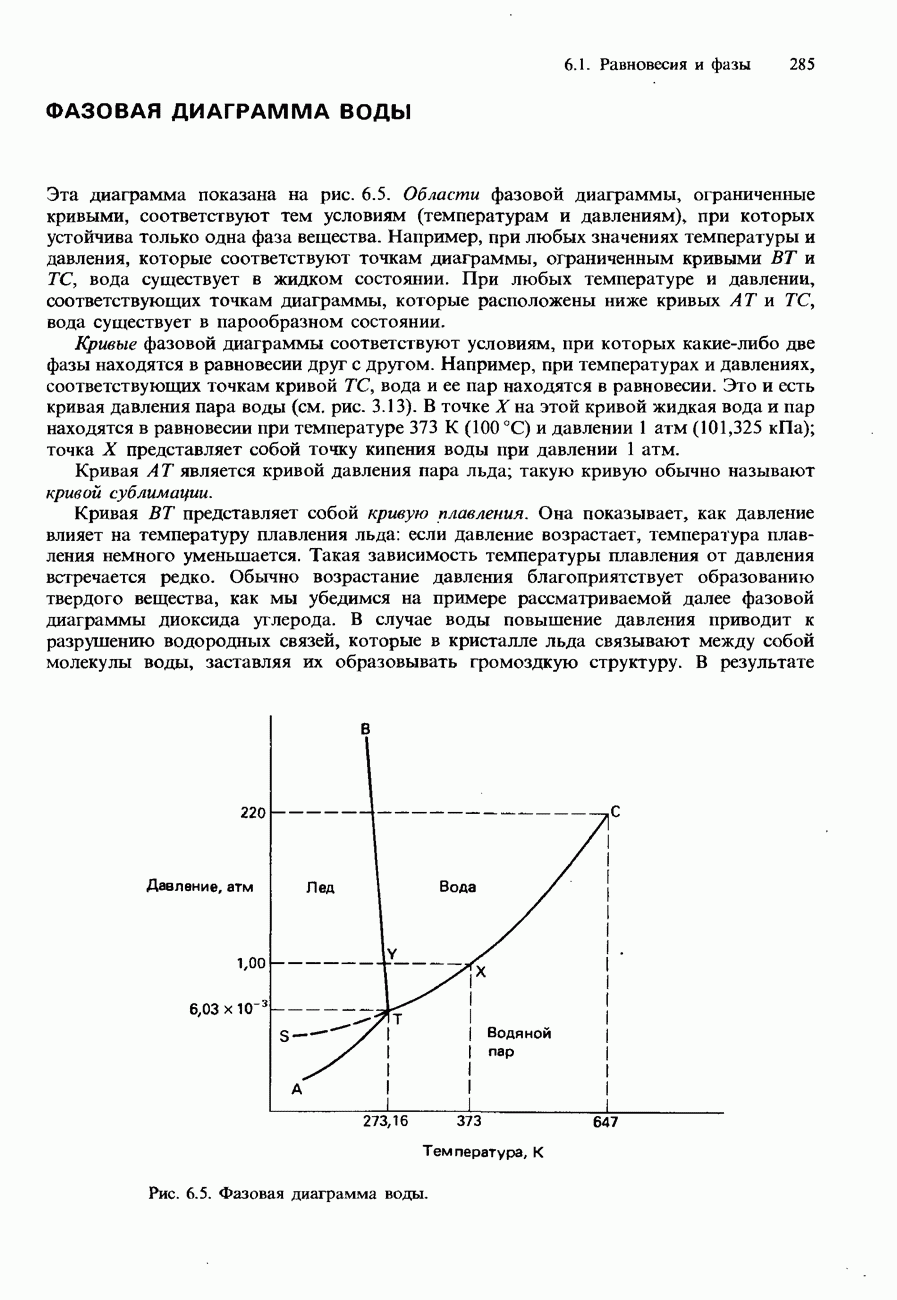
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
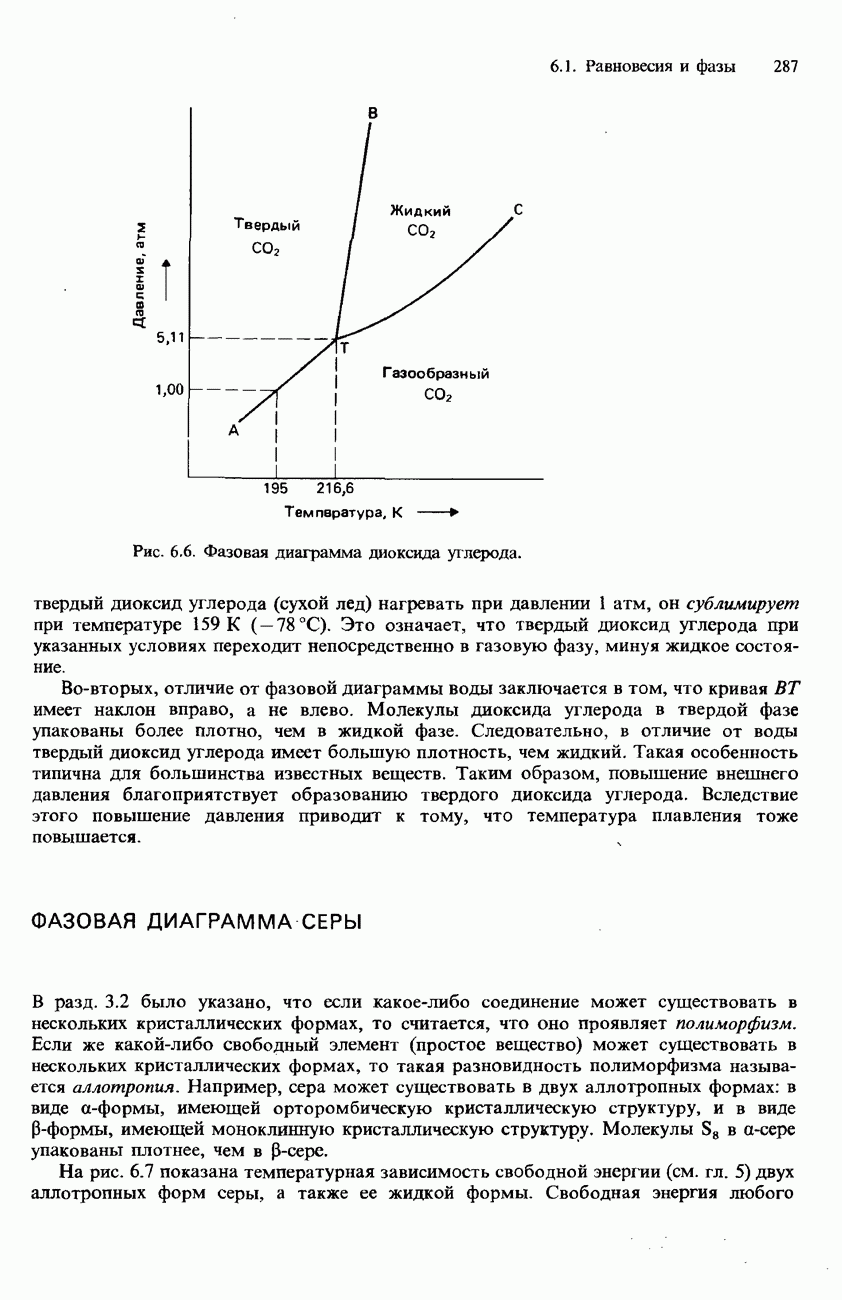
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
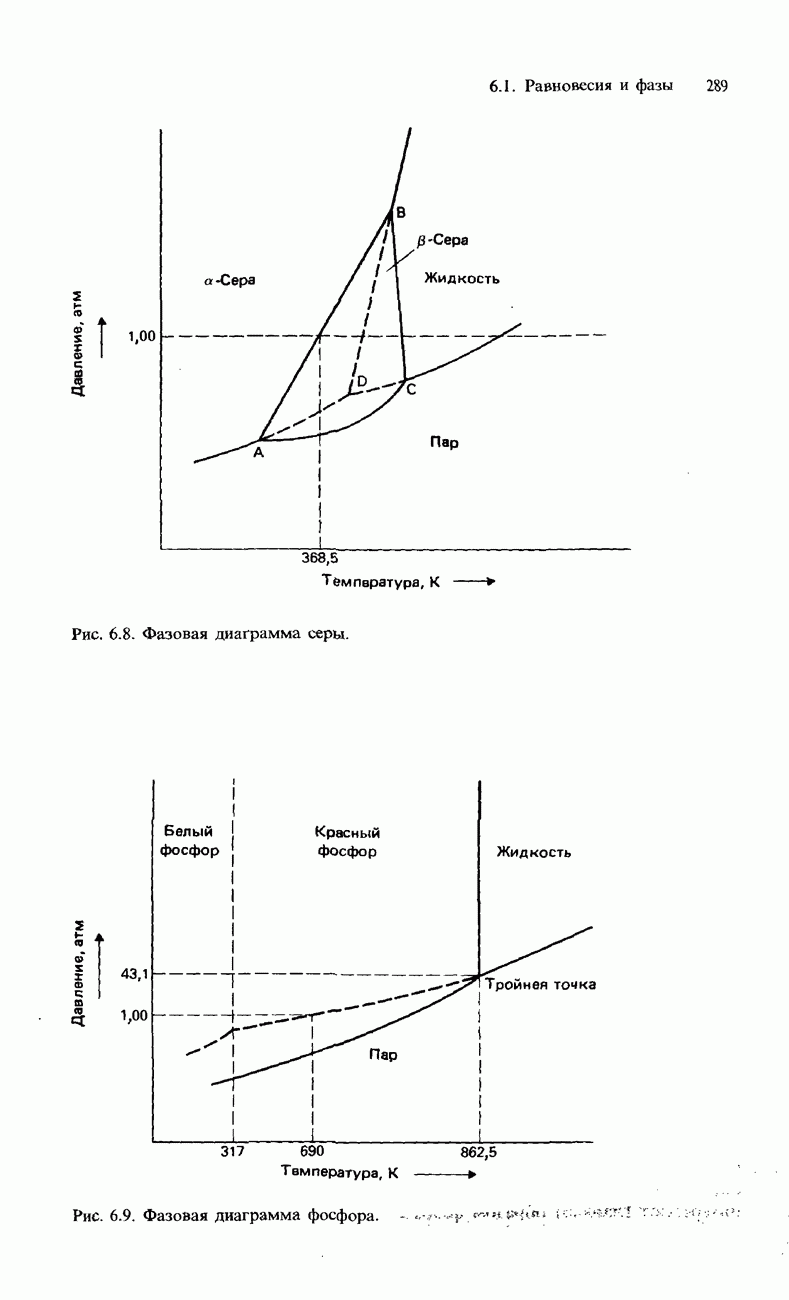
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- Фазовые диаграммы полностью смешивающихся жидкостей
- Фракционная перегонка
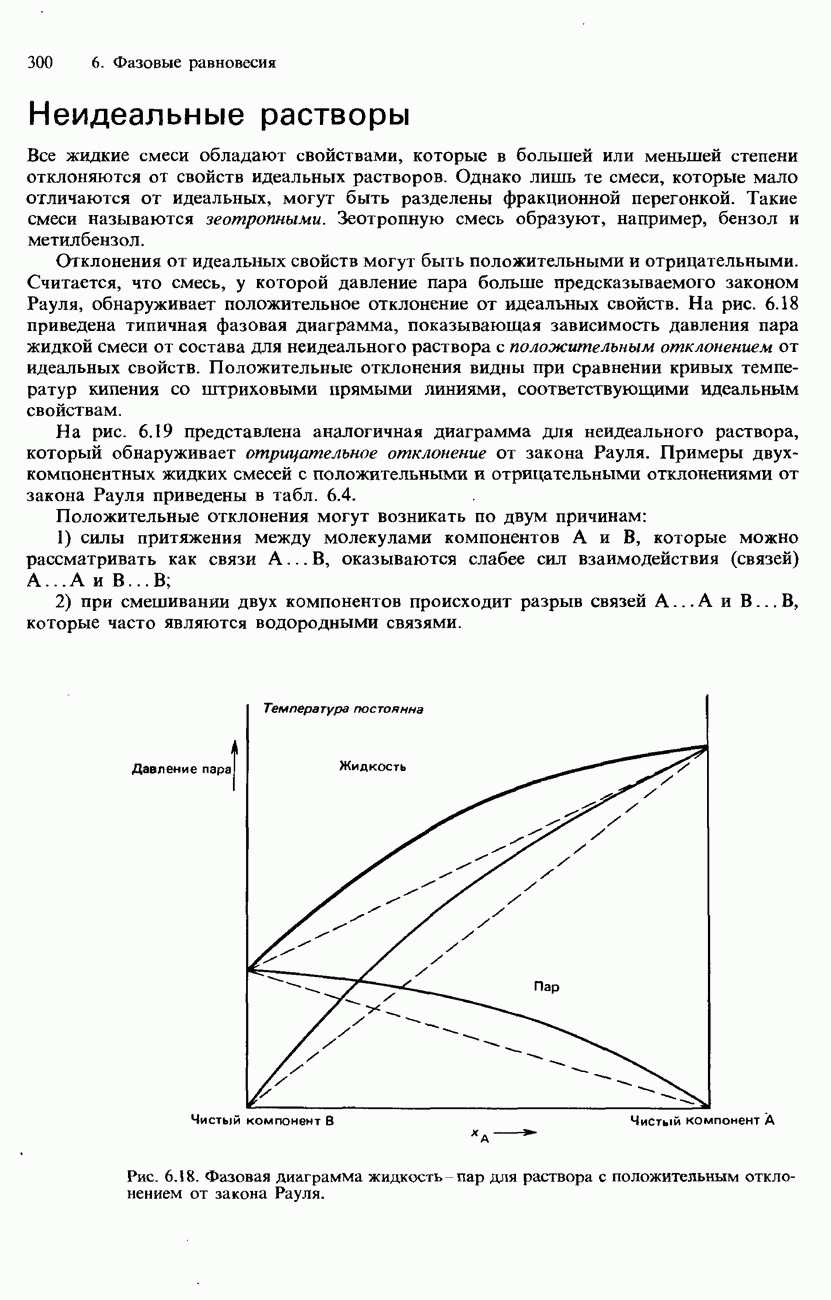
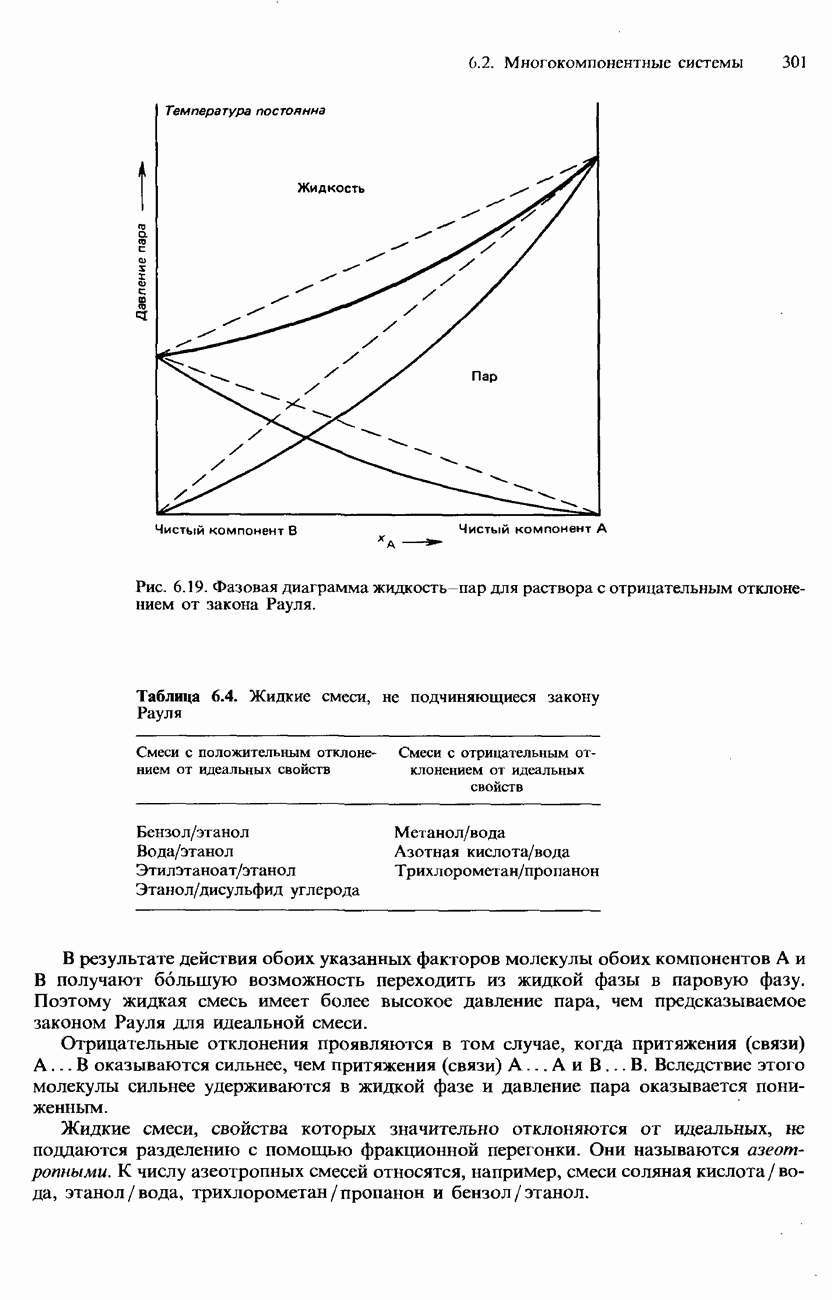
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
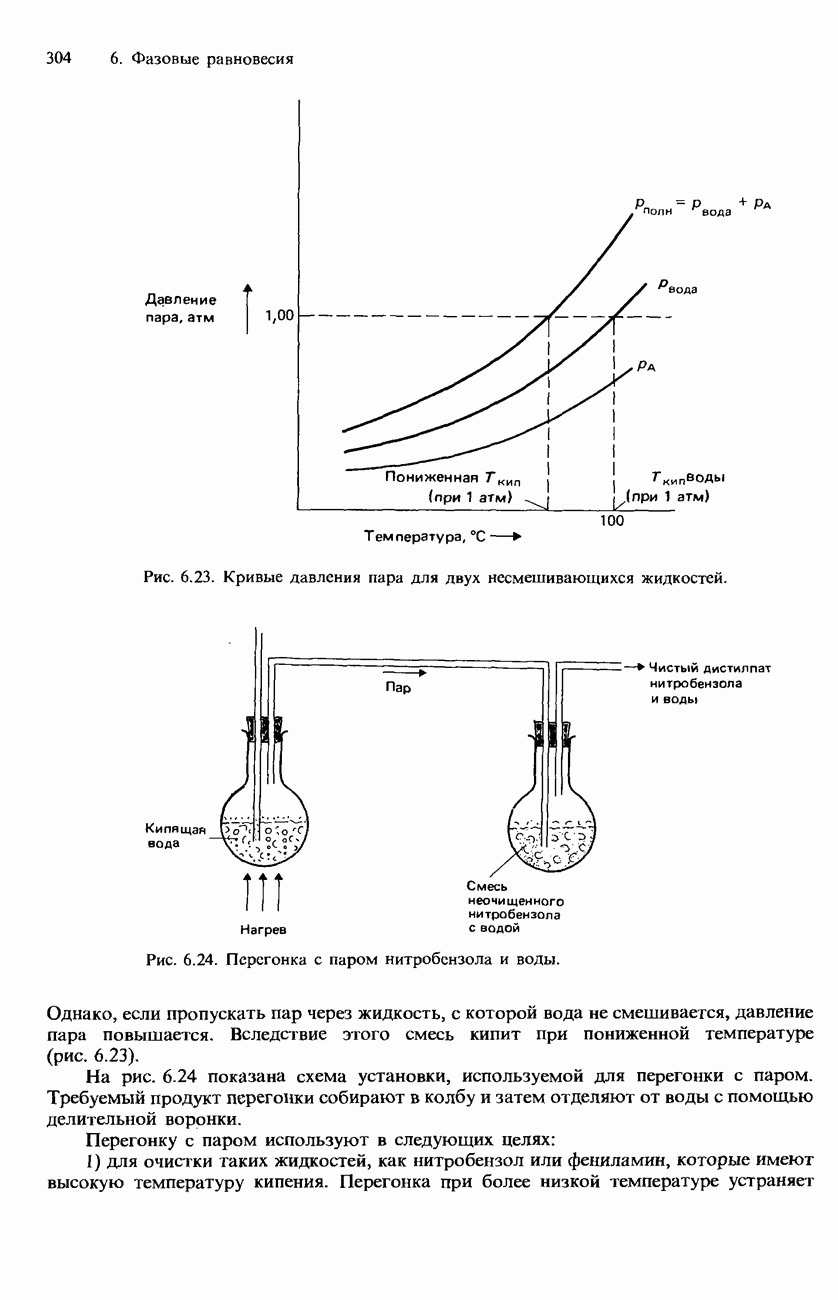
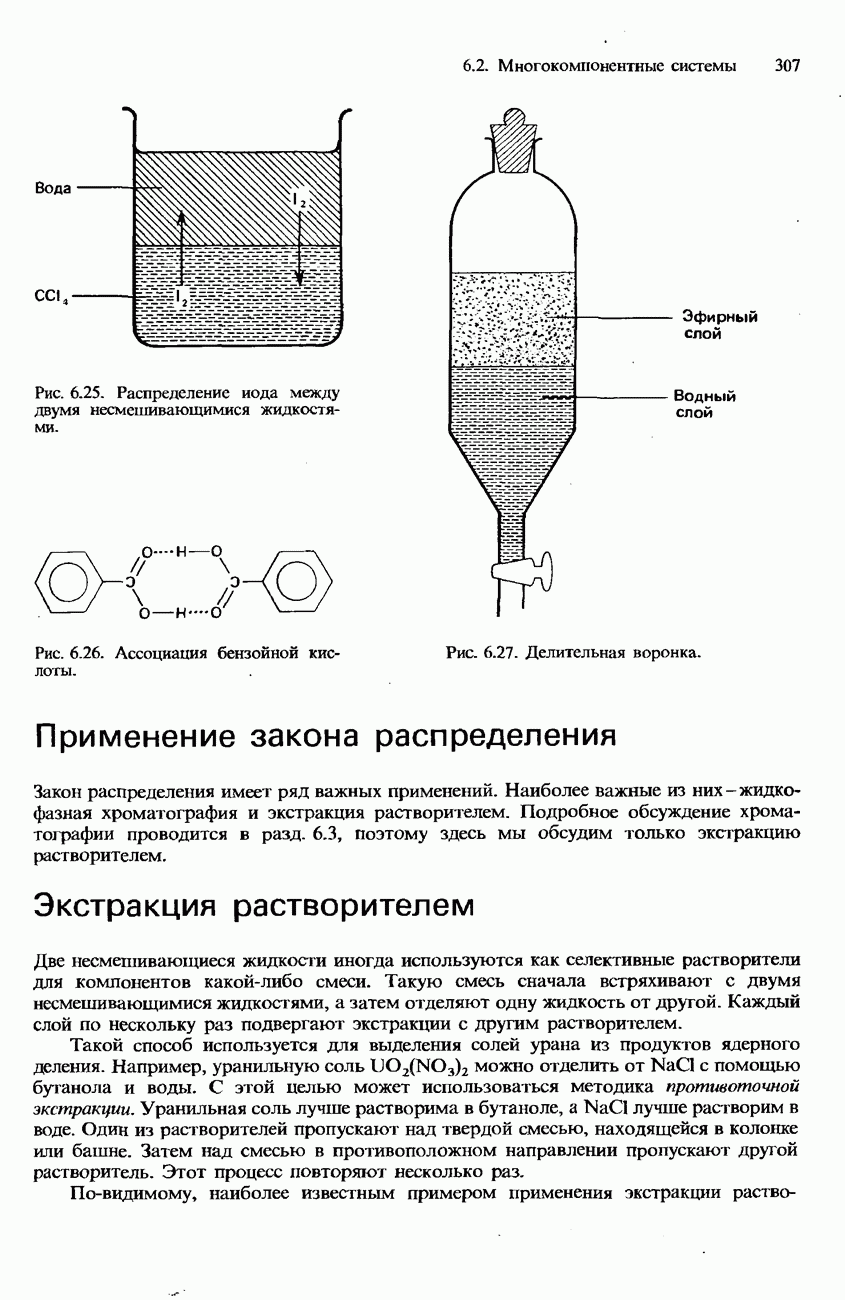
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
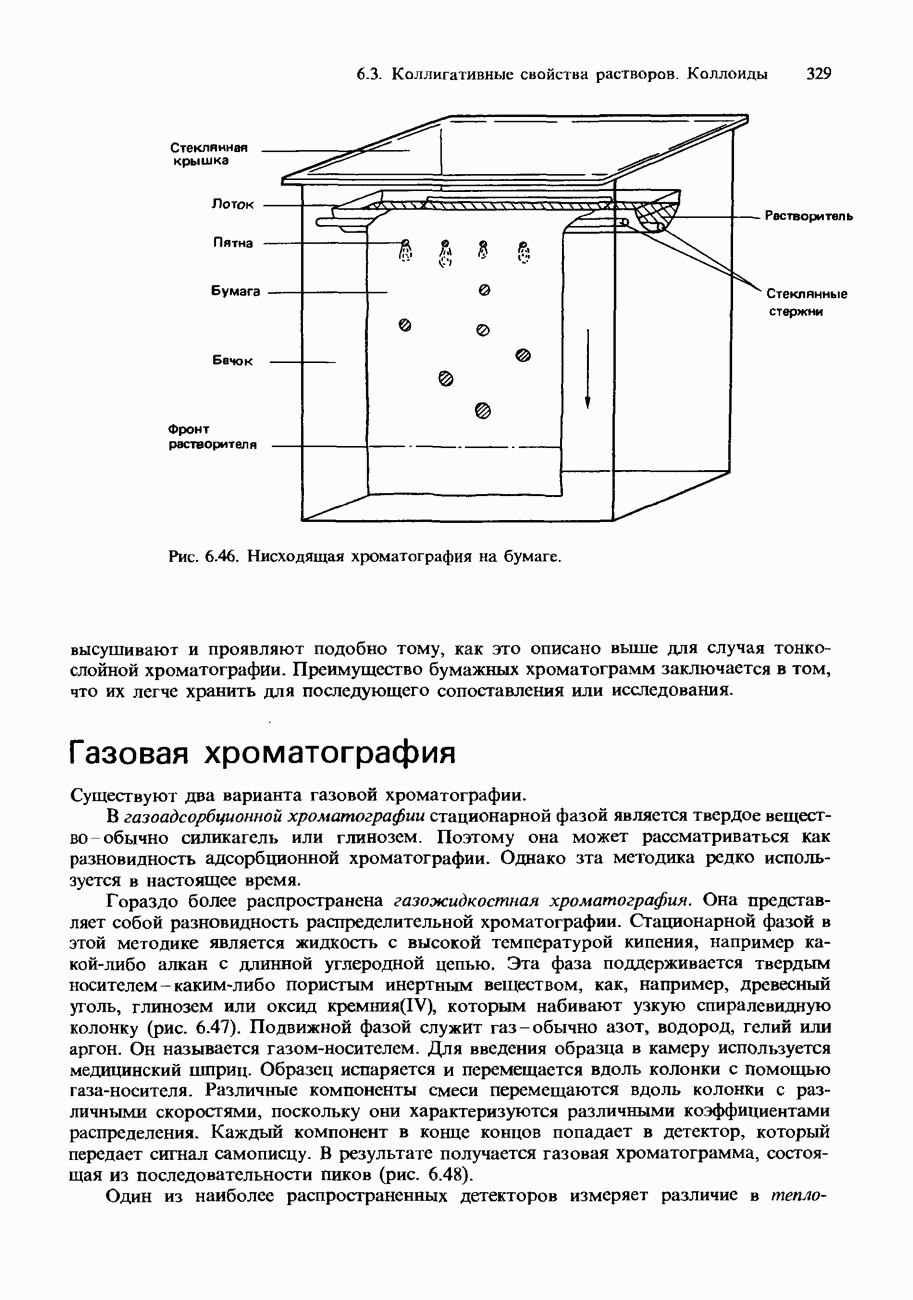
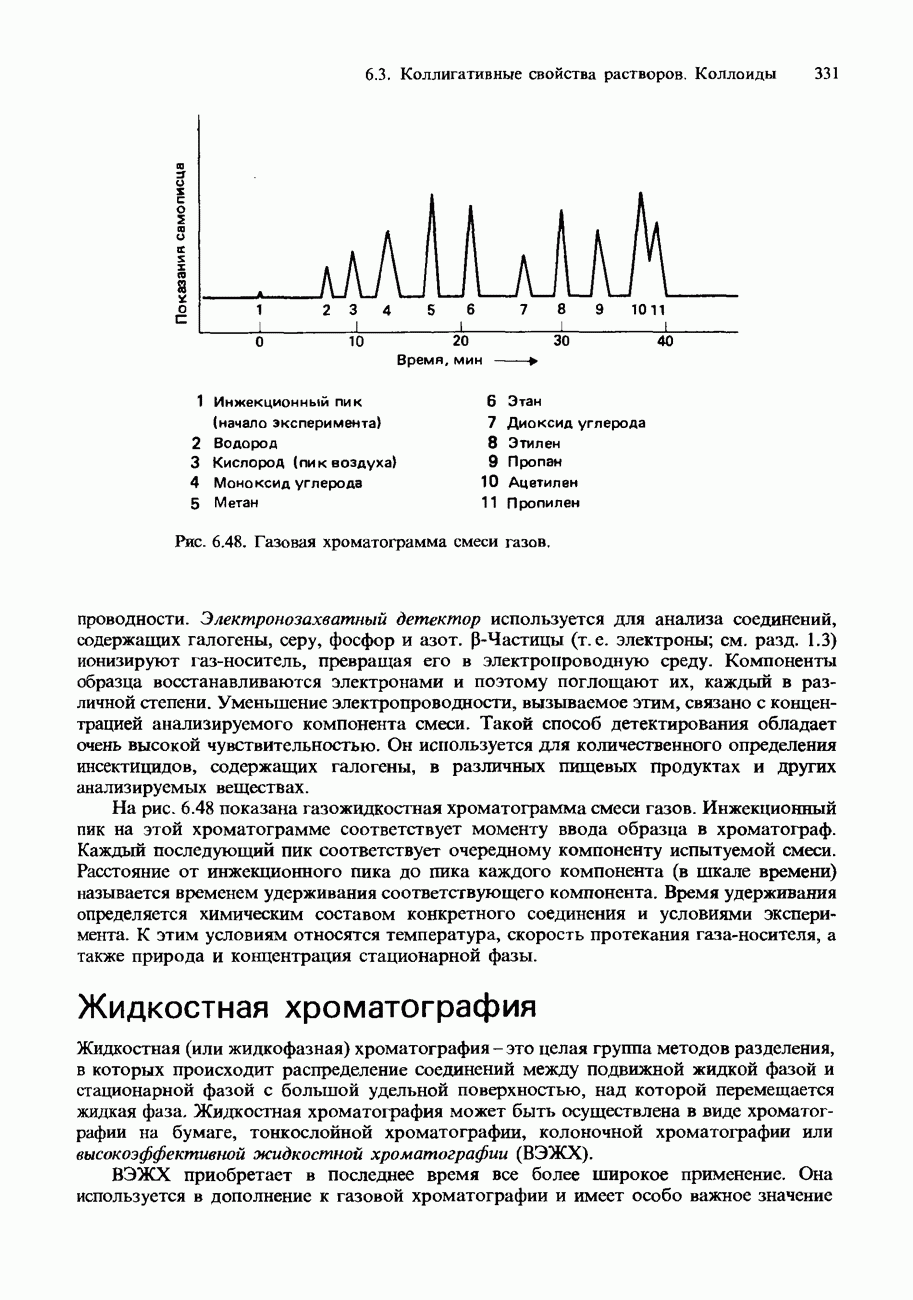
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
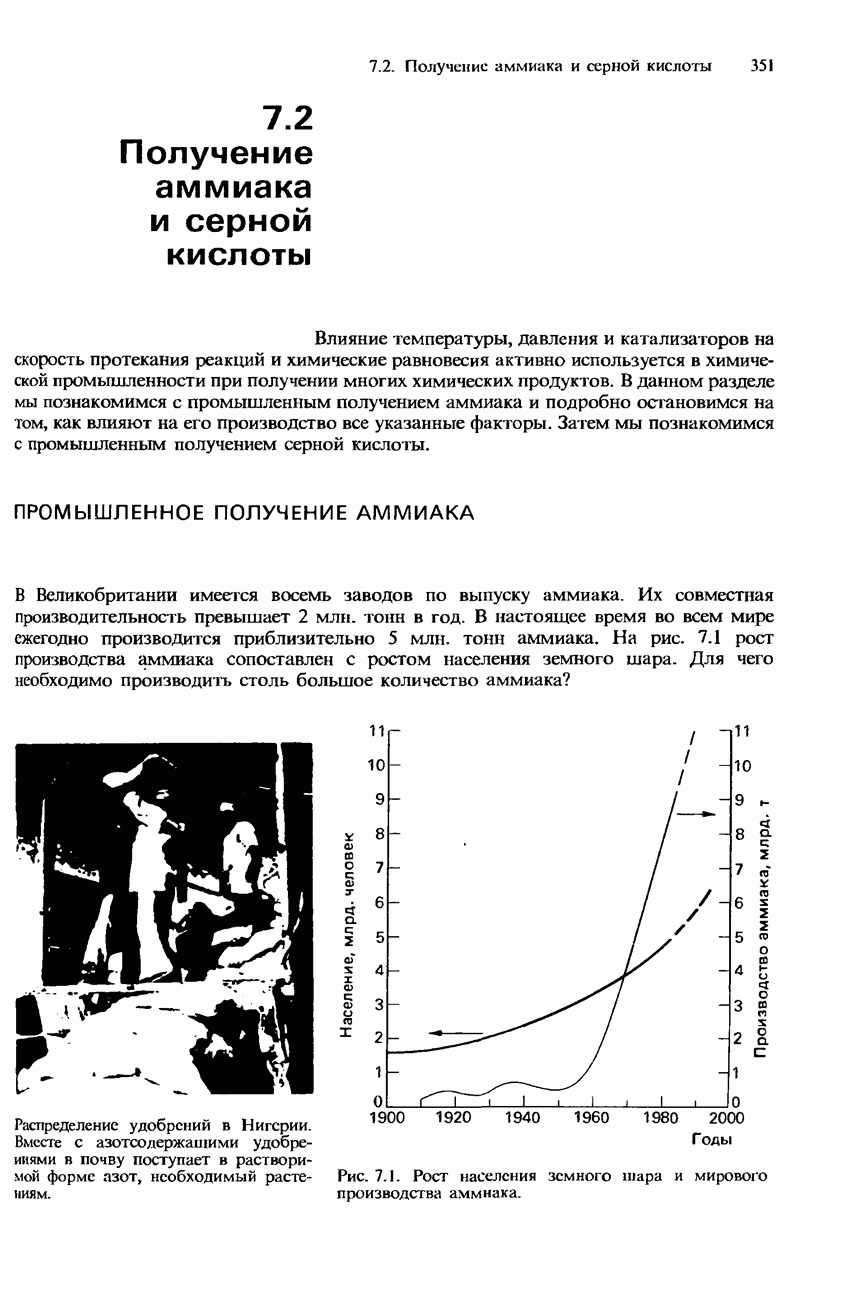
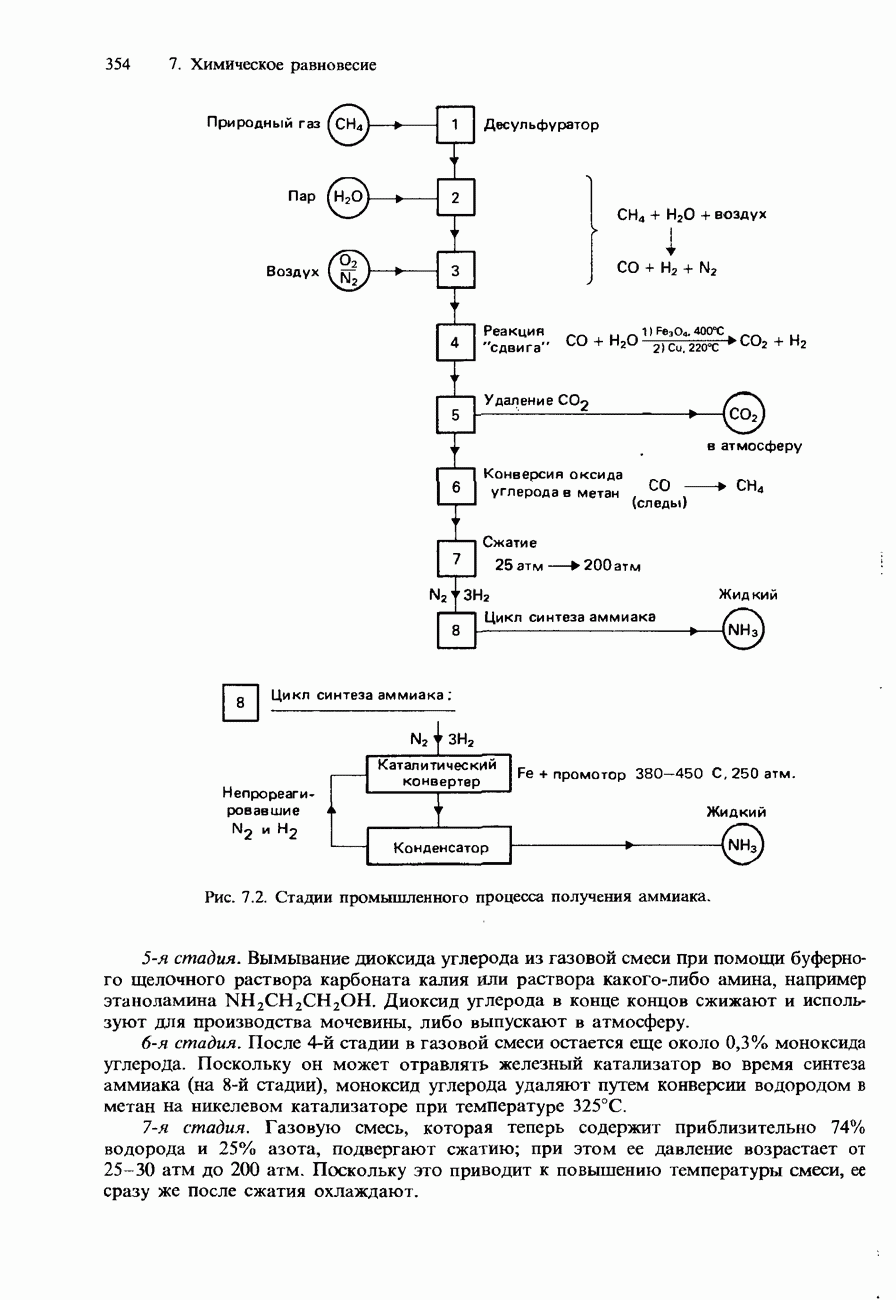
- 7.2. Получение аммиака и серной кислоты
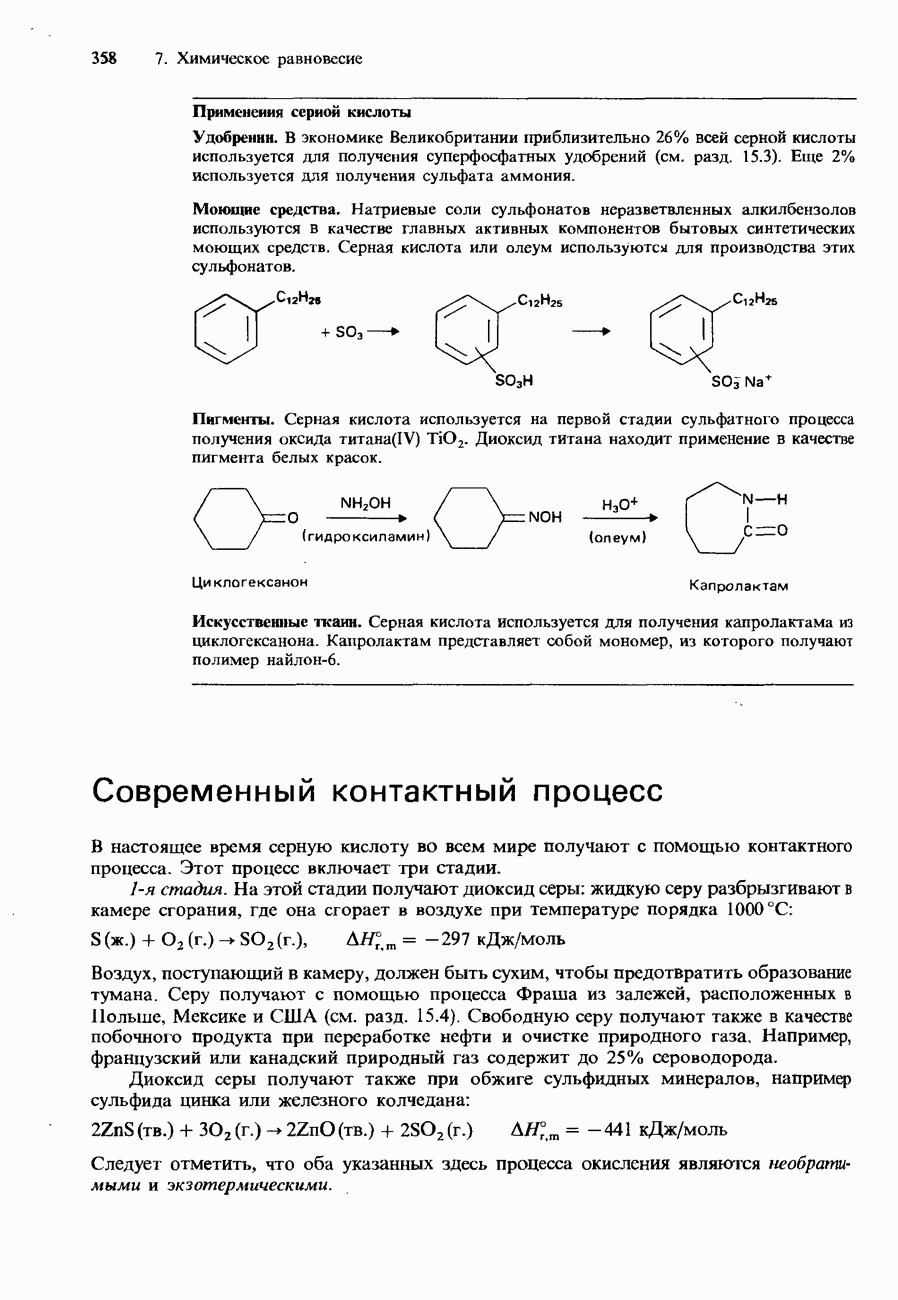
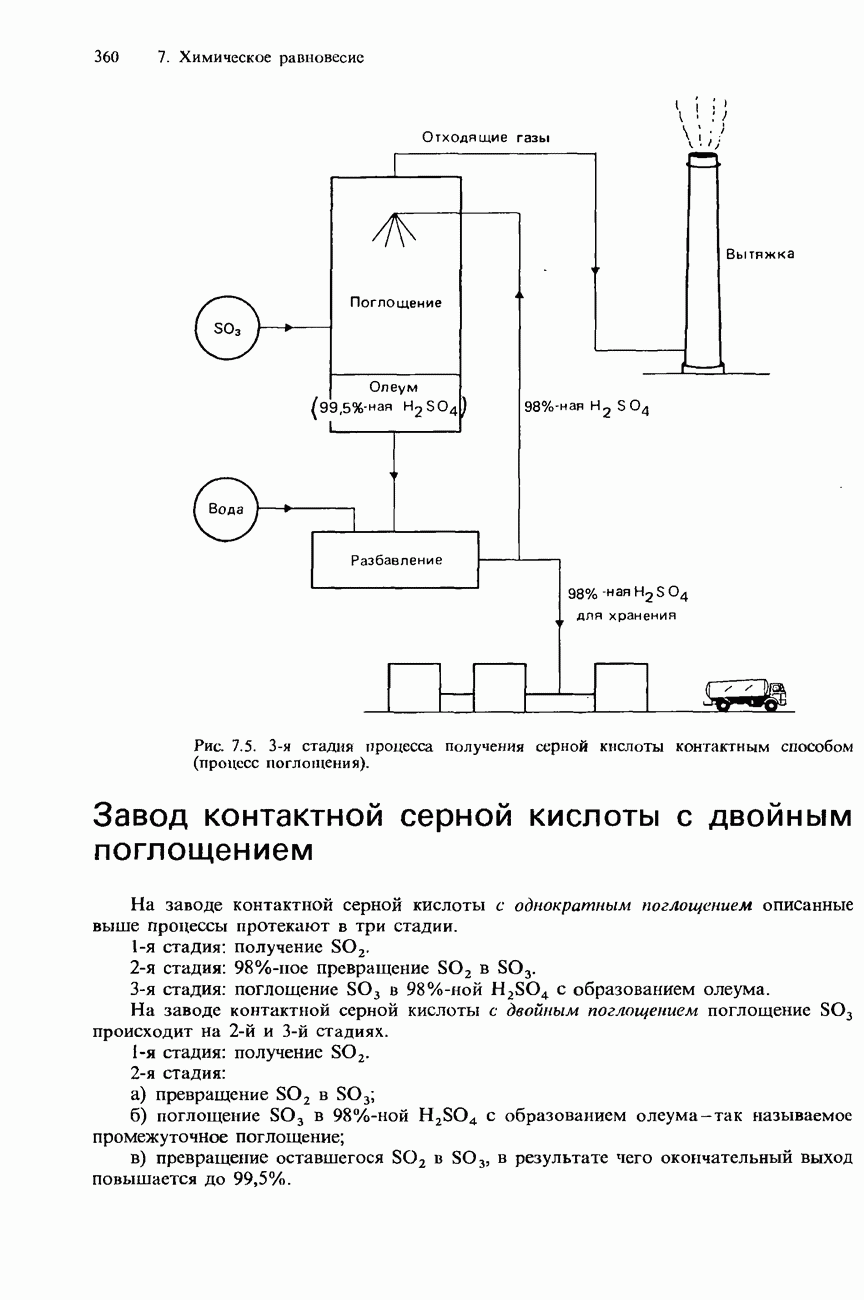
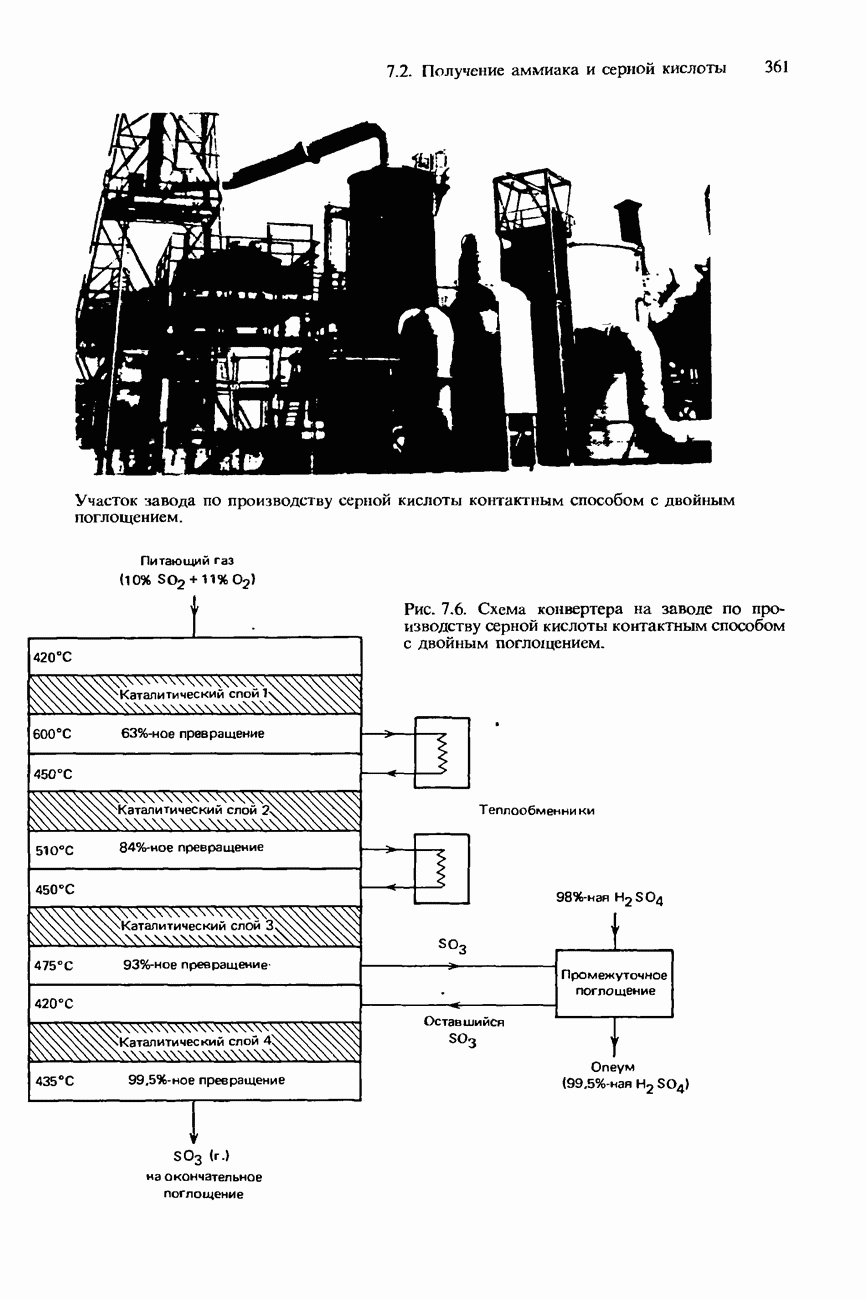
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
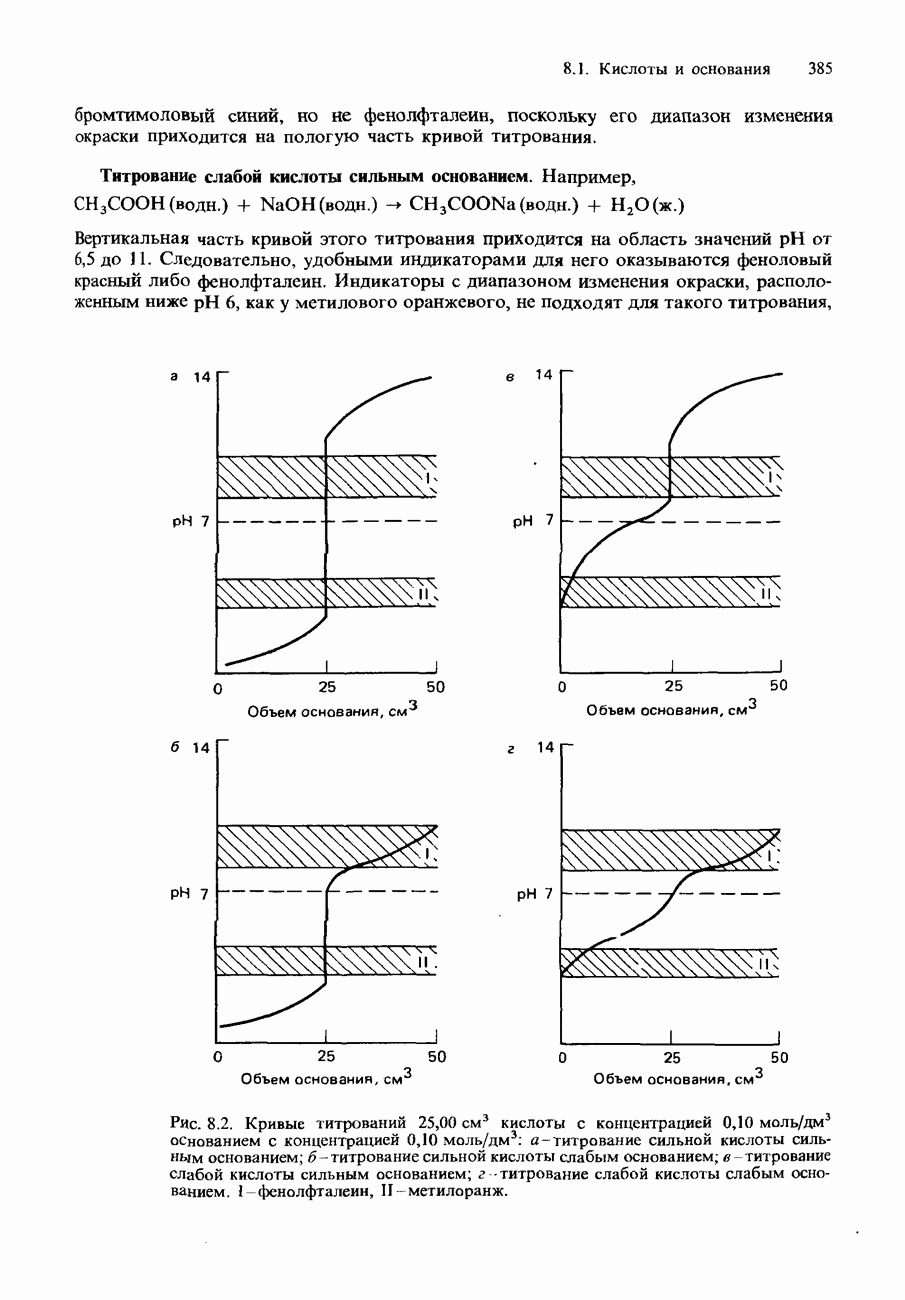
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
- 10.4. Химические источники тока
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
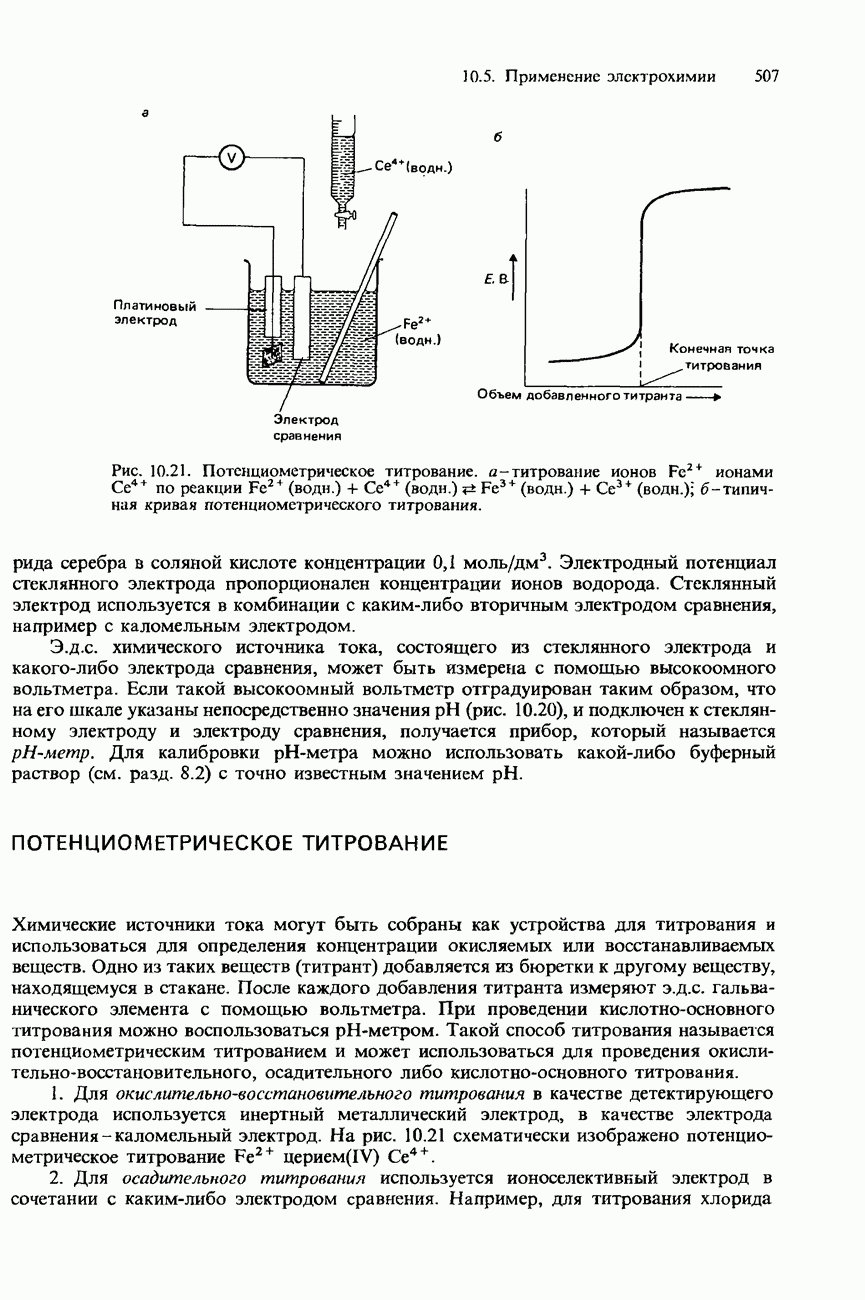
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
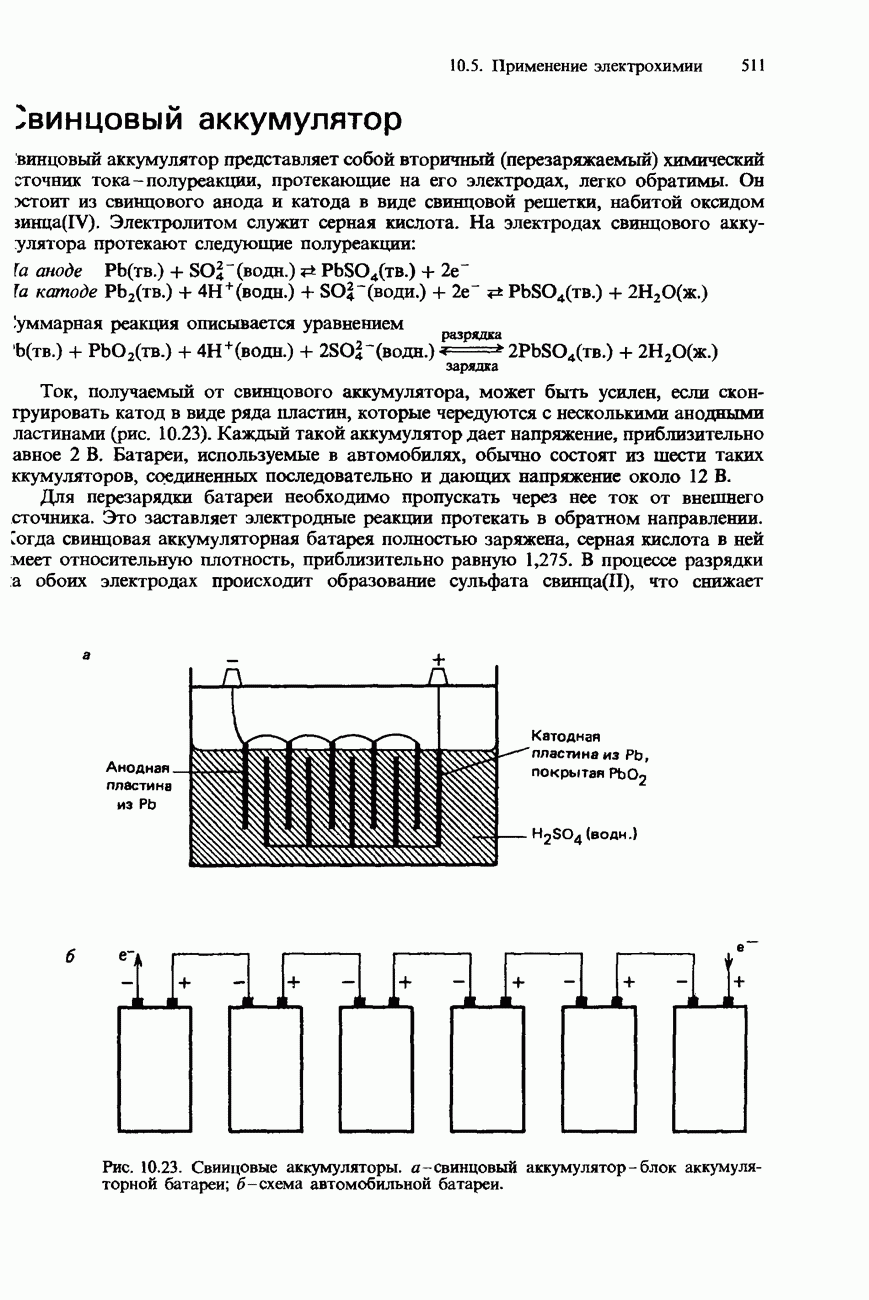
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ