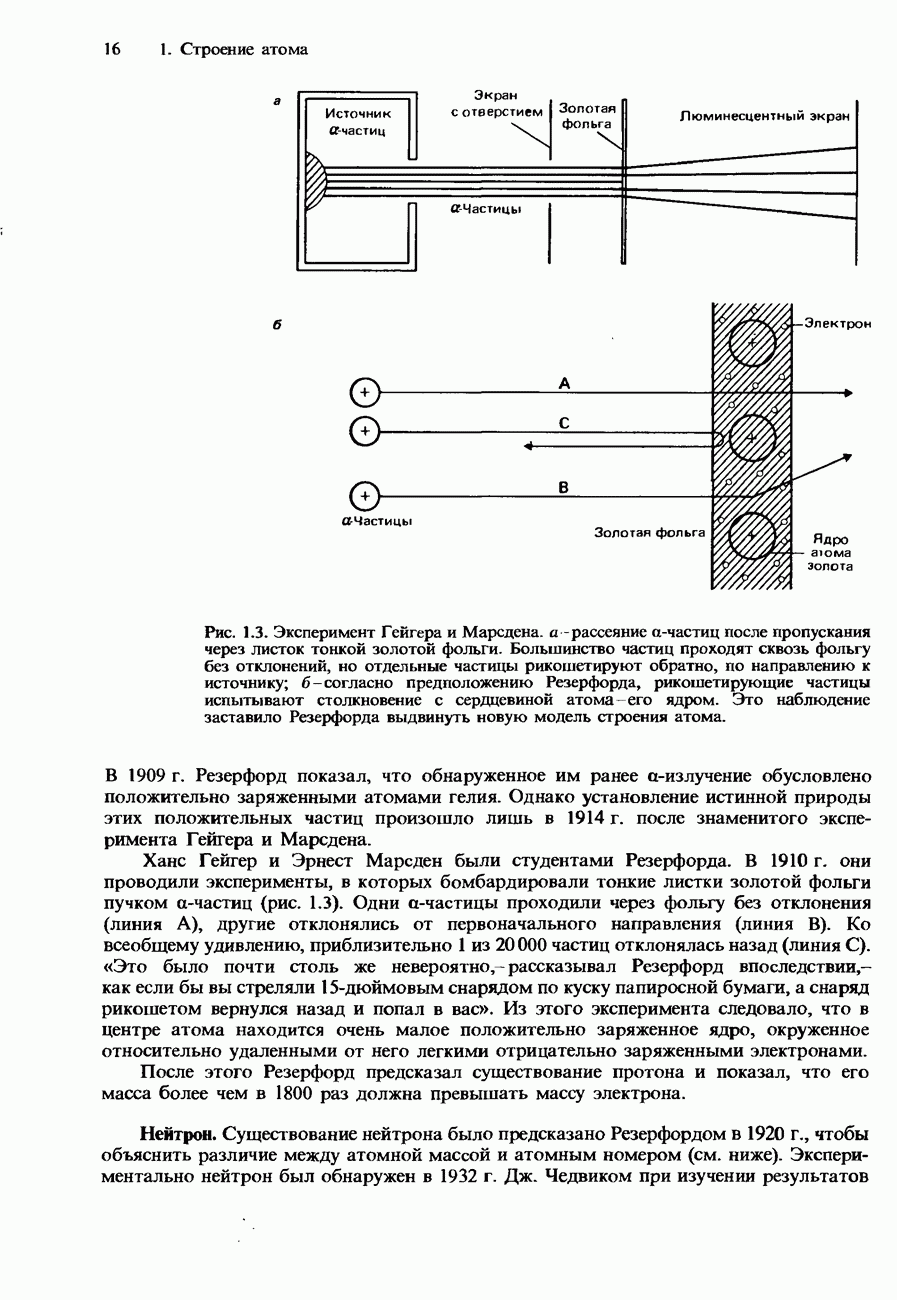
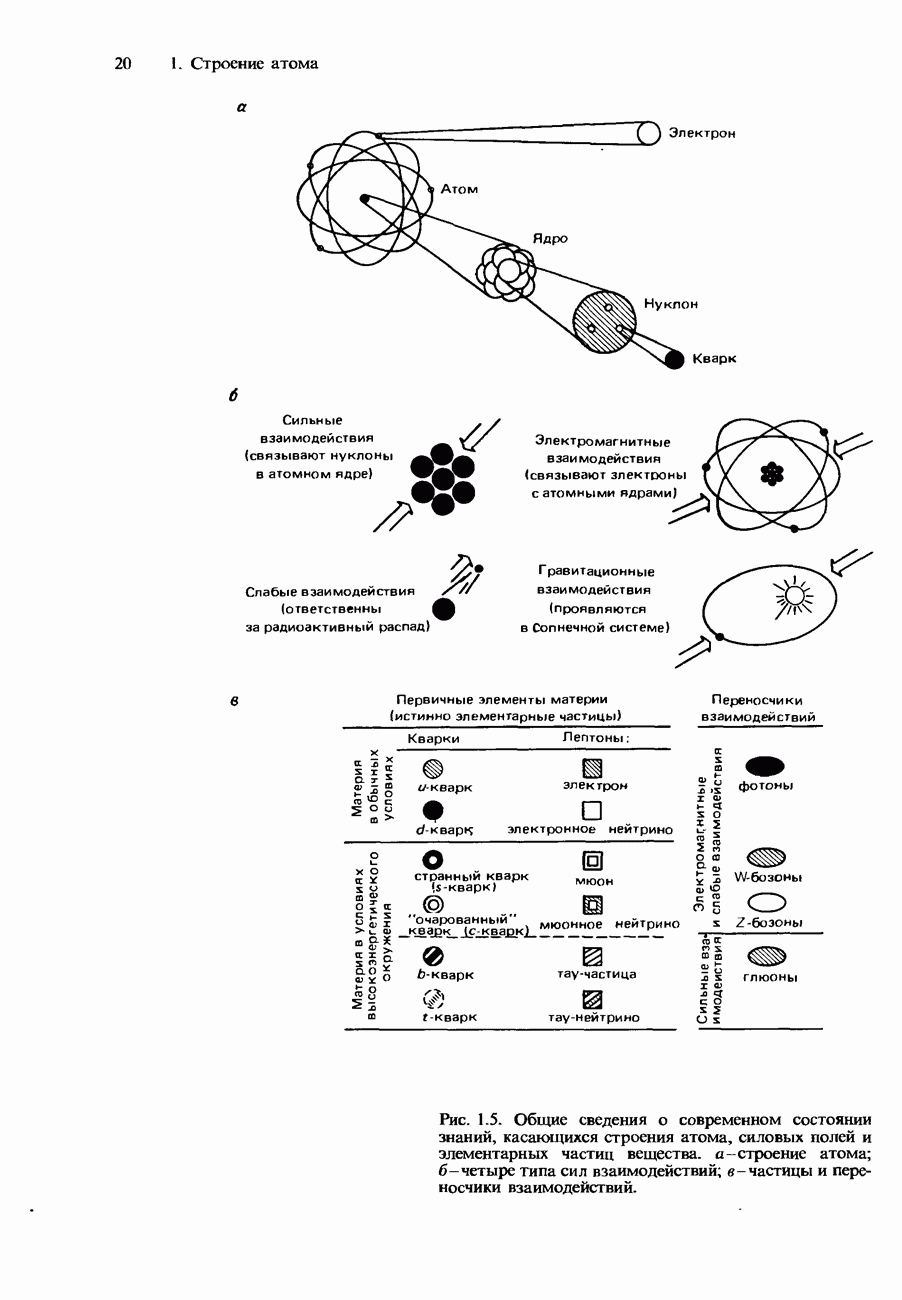
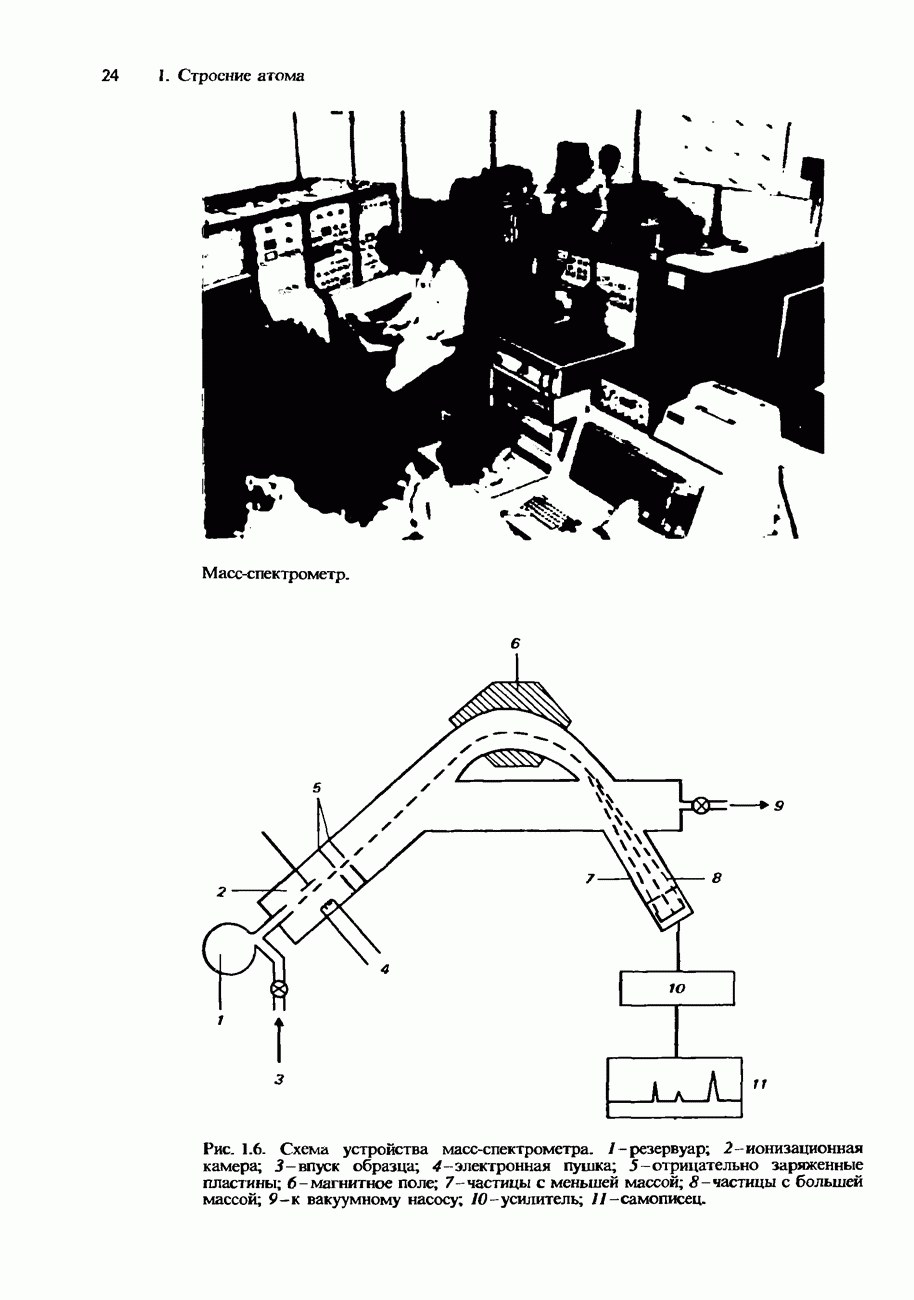
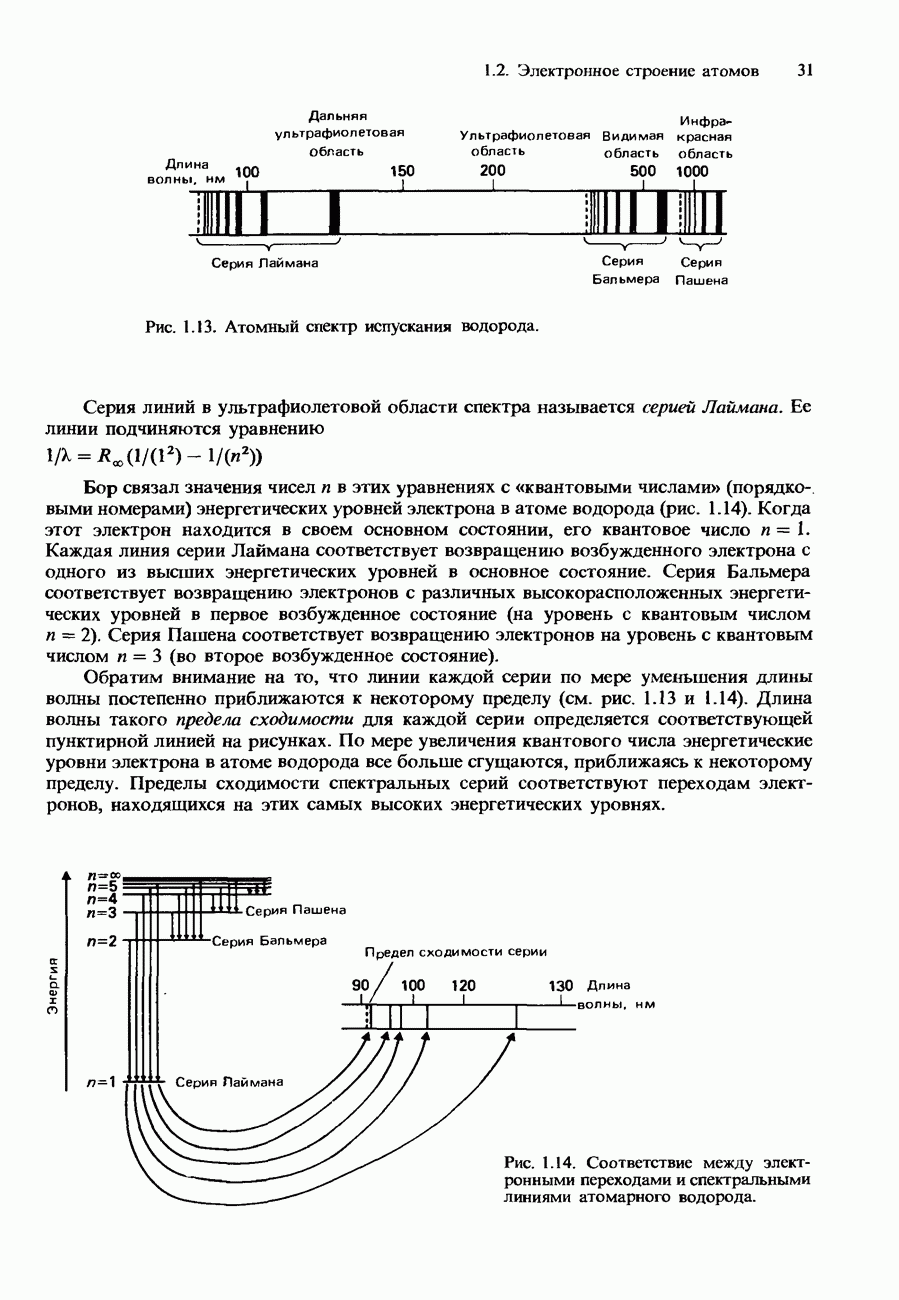
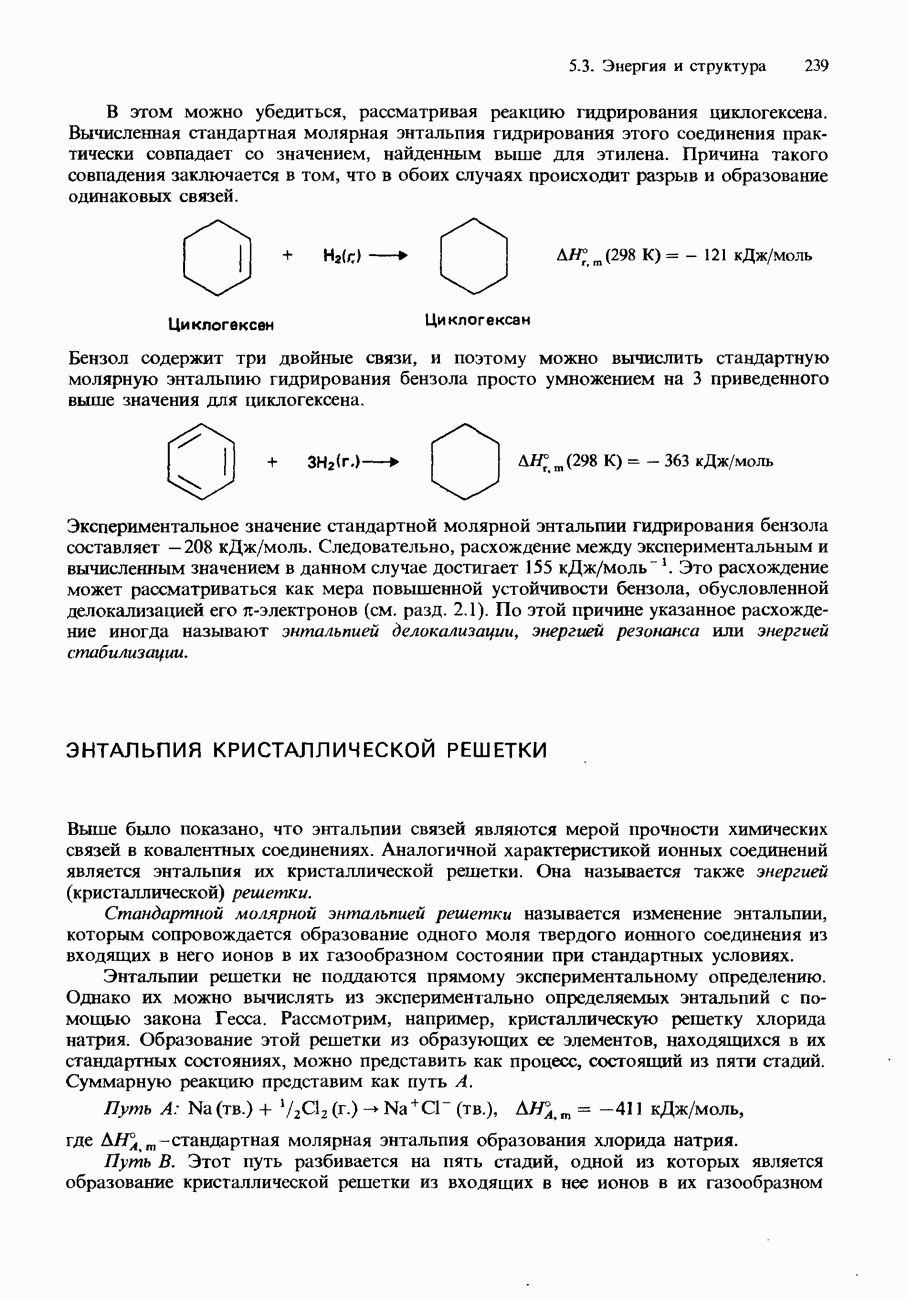
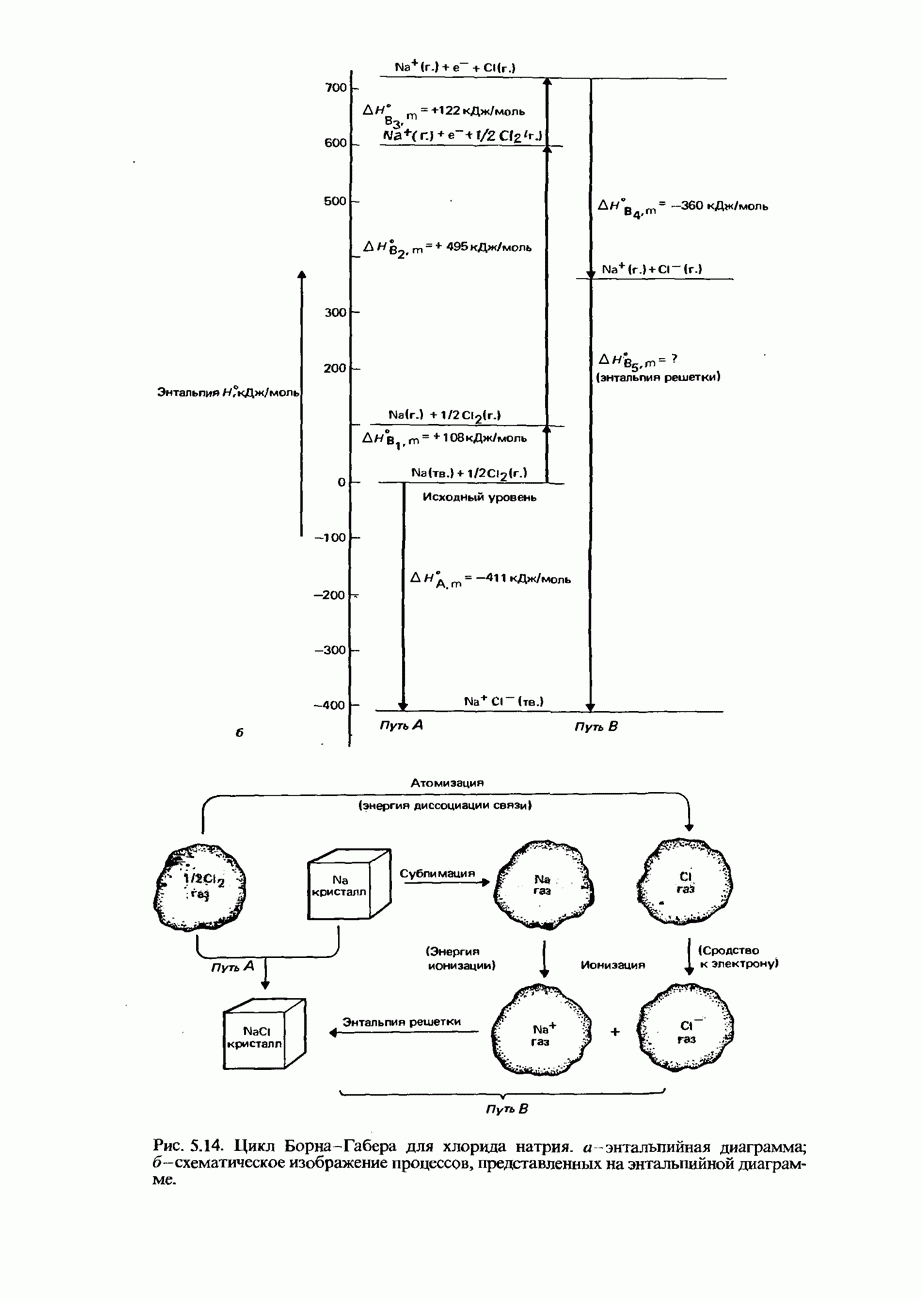
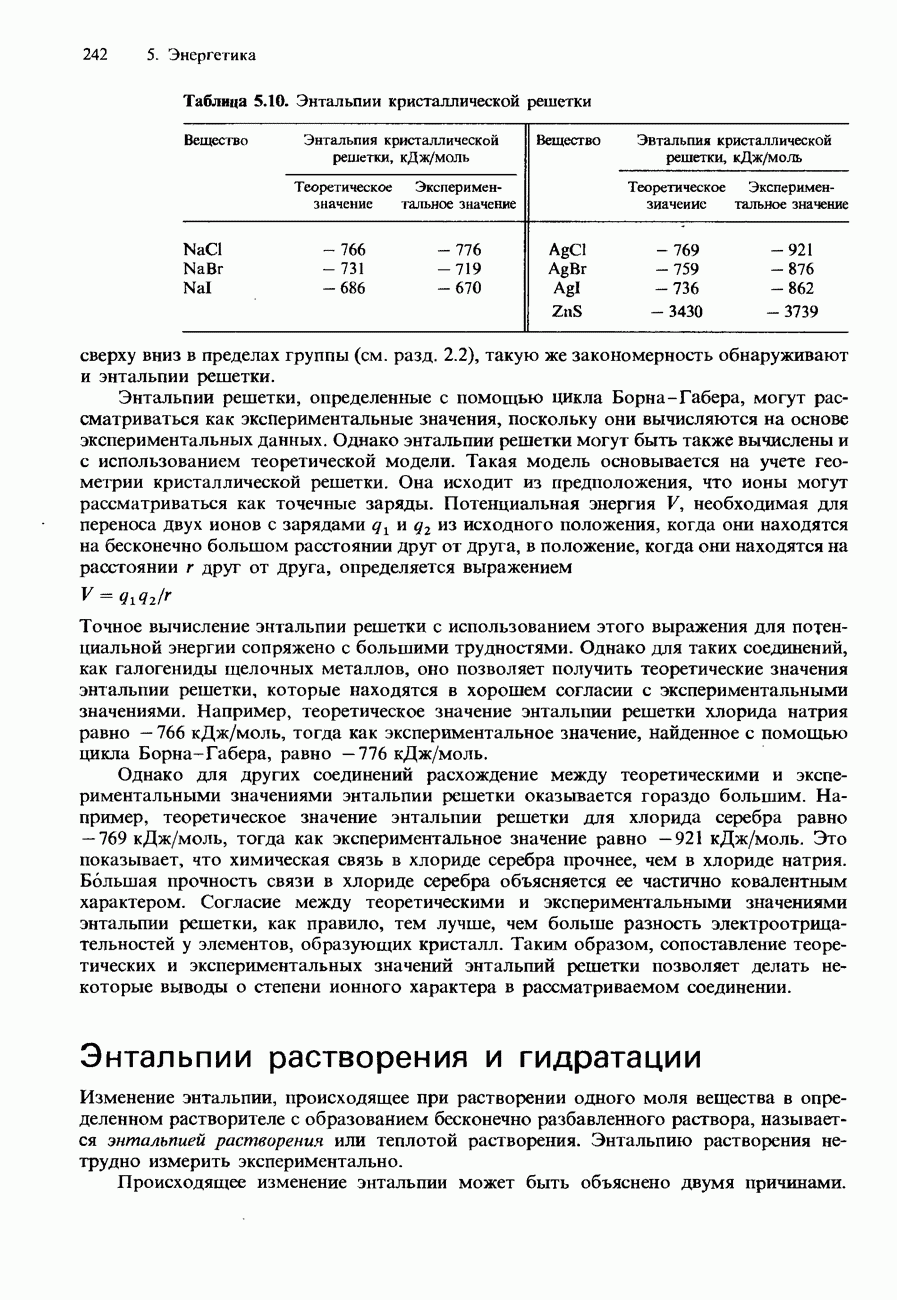
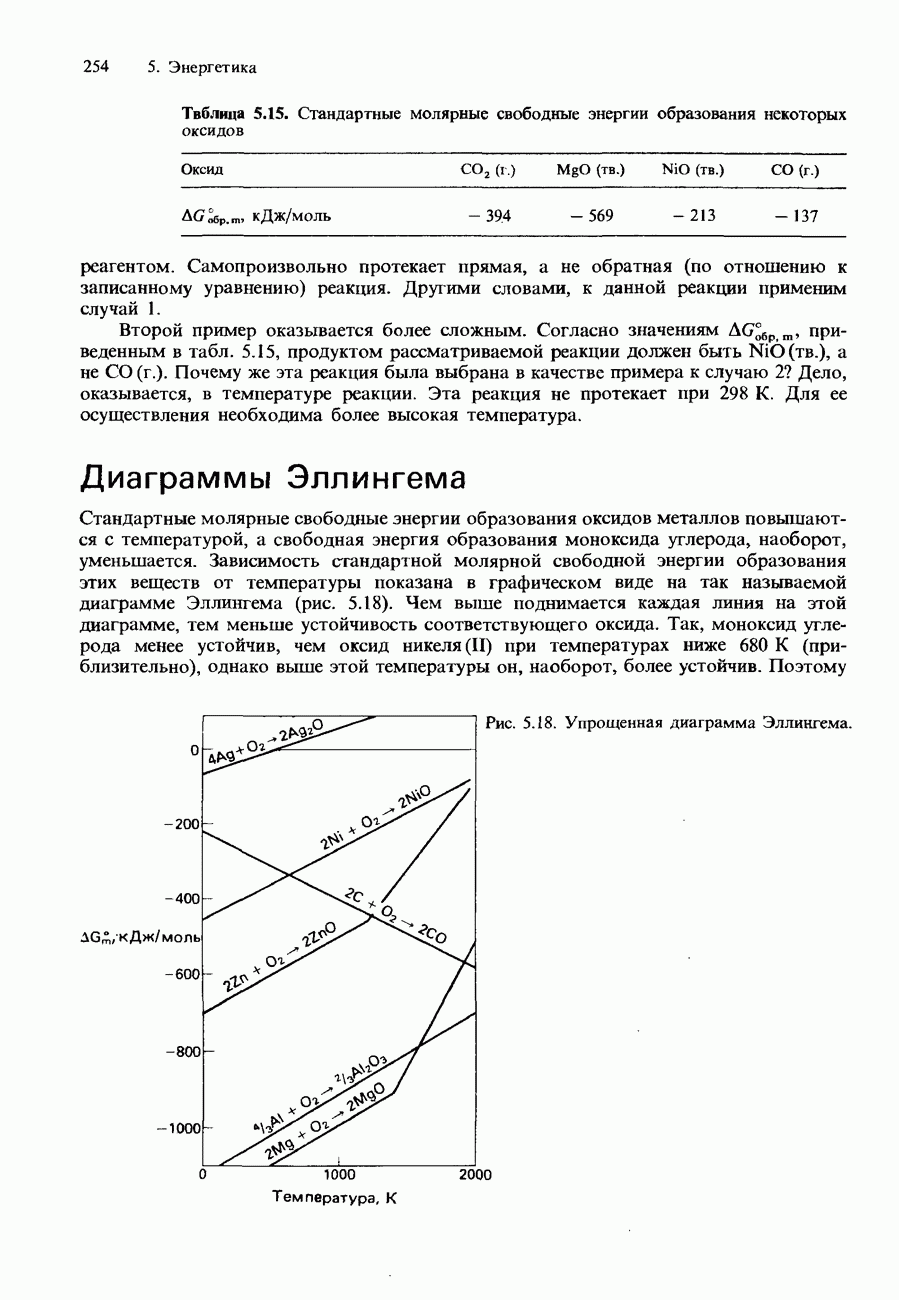
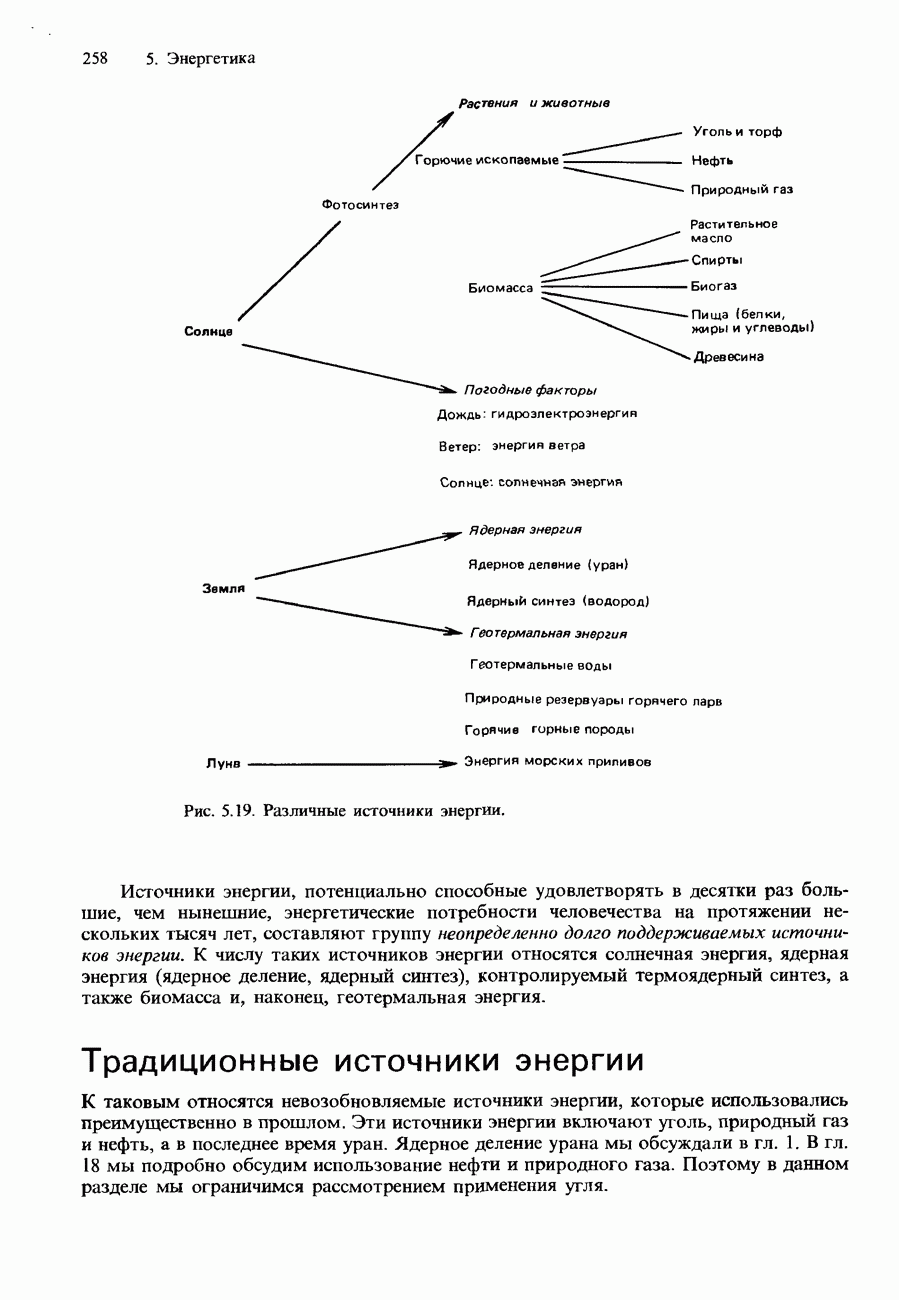
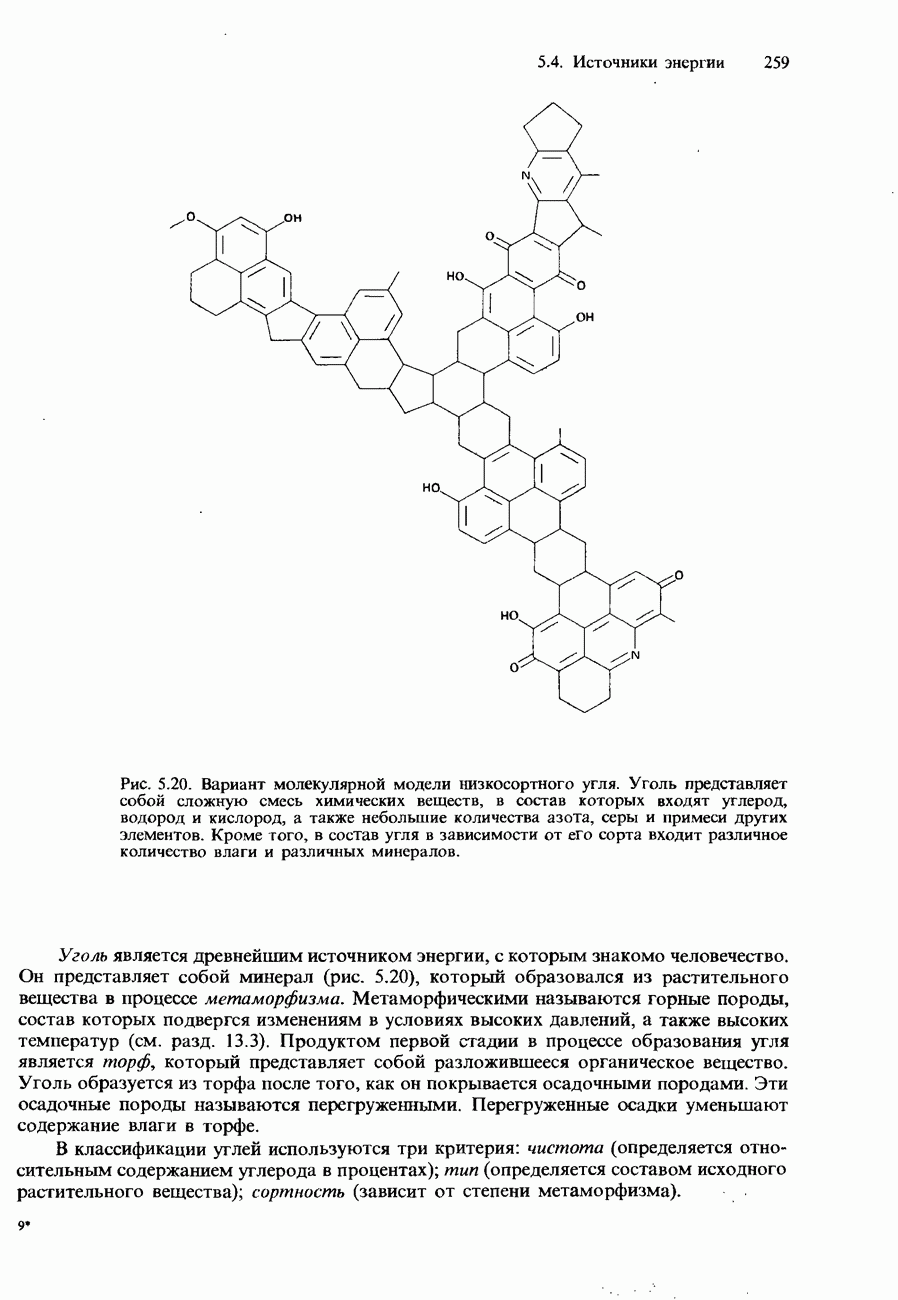
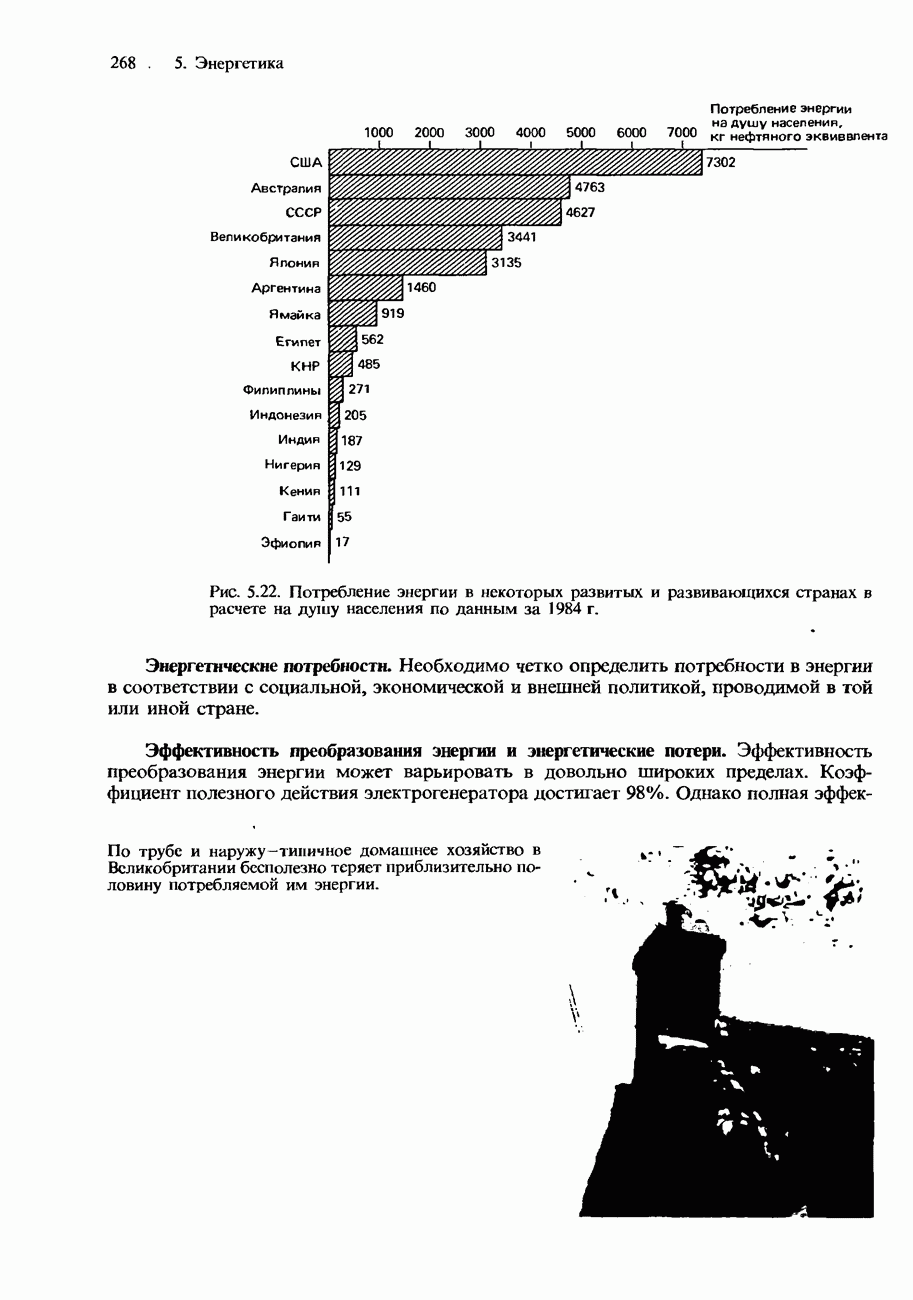
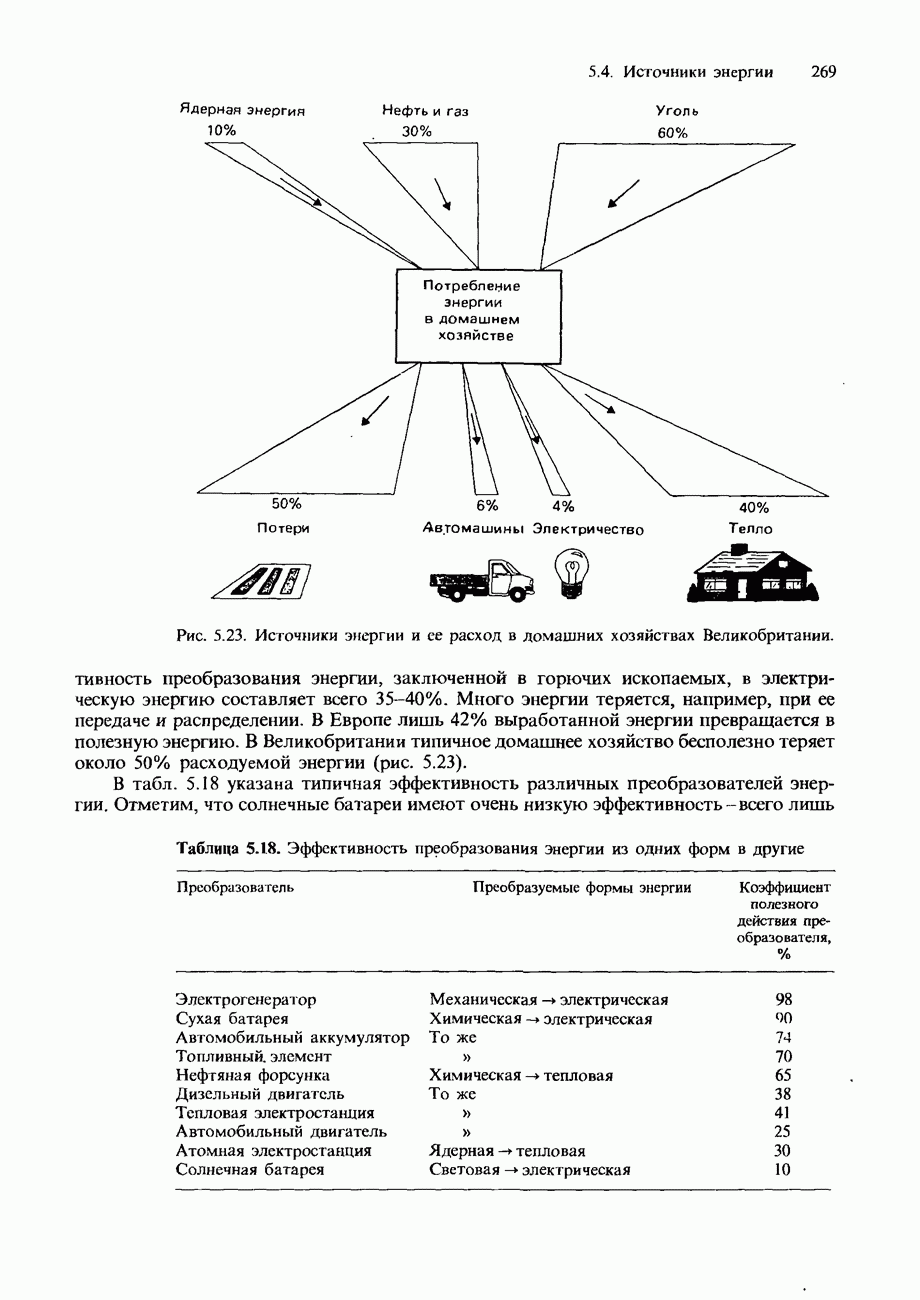
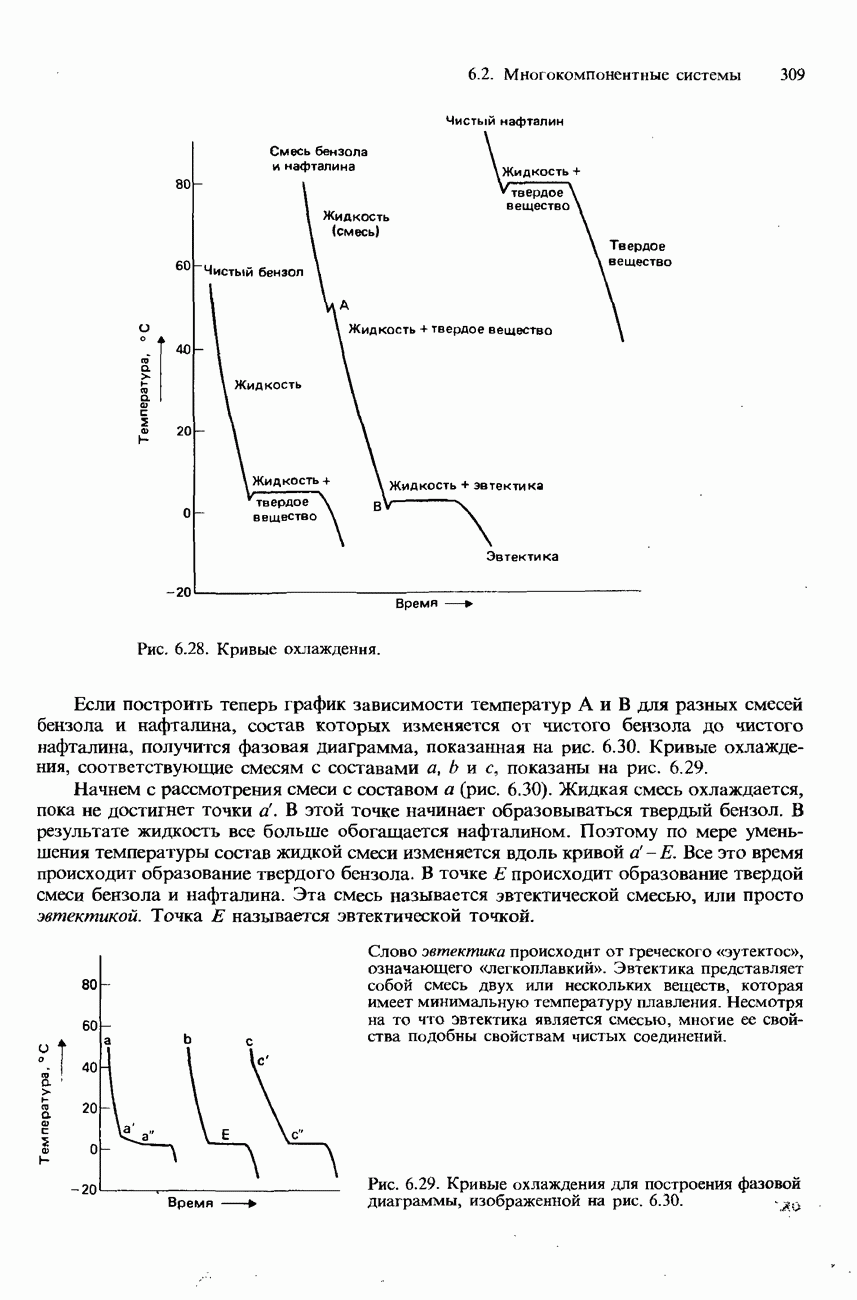
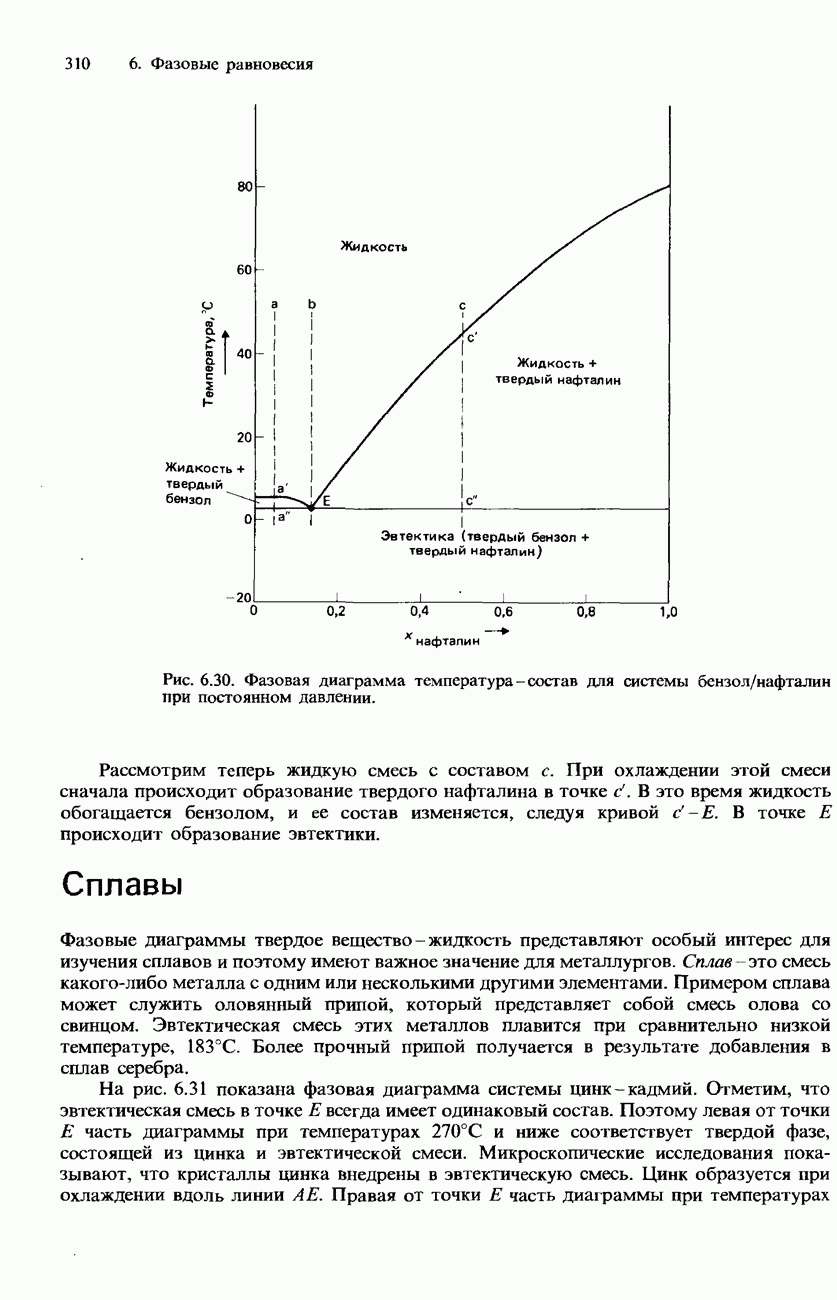
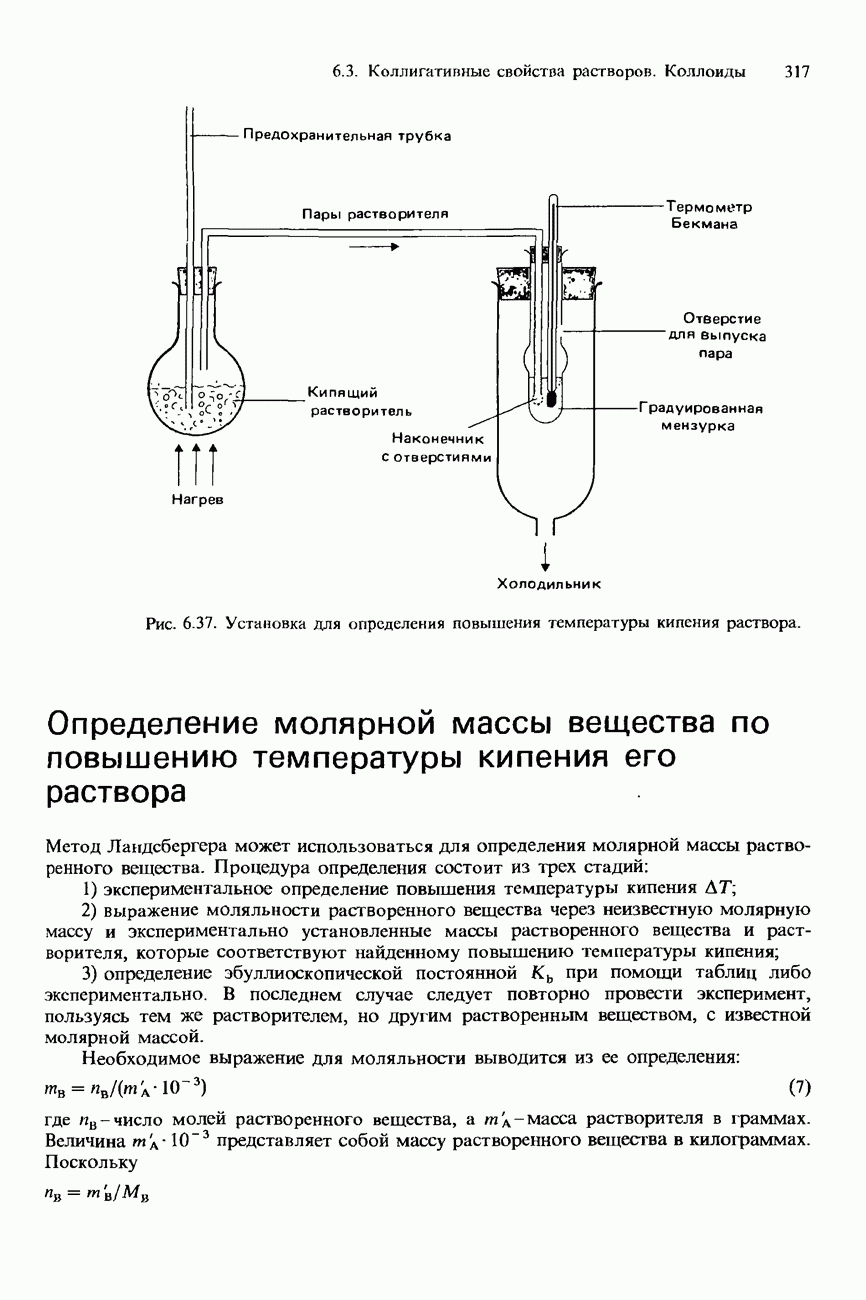
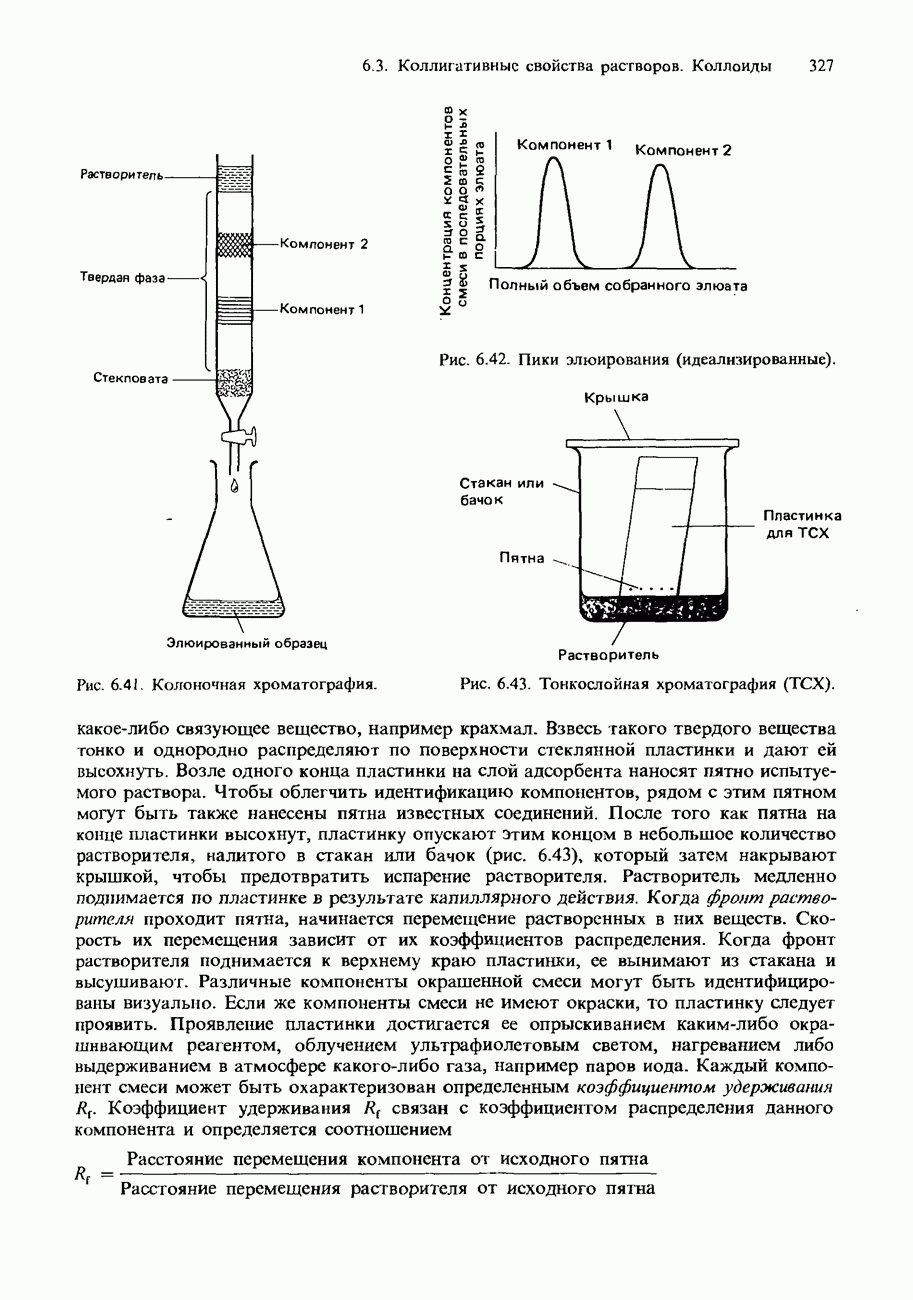
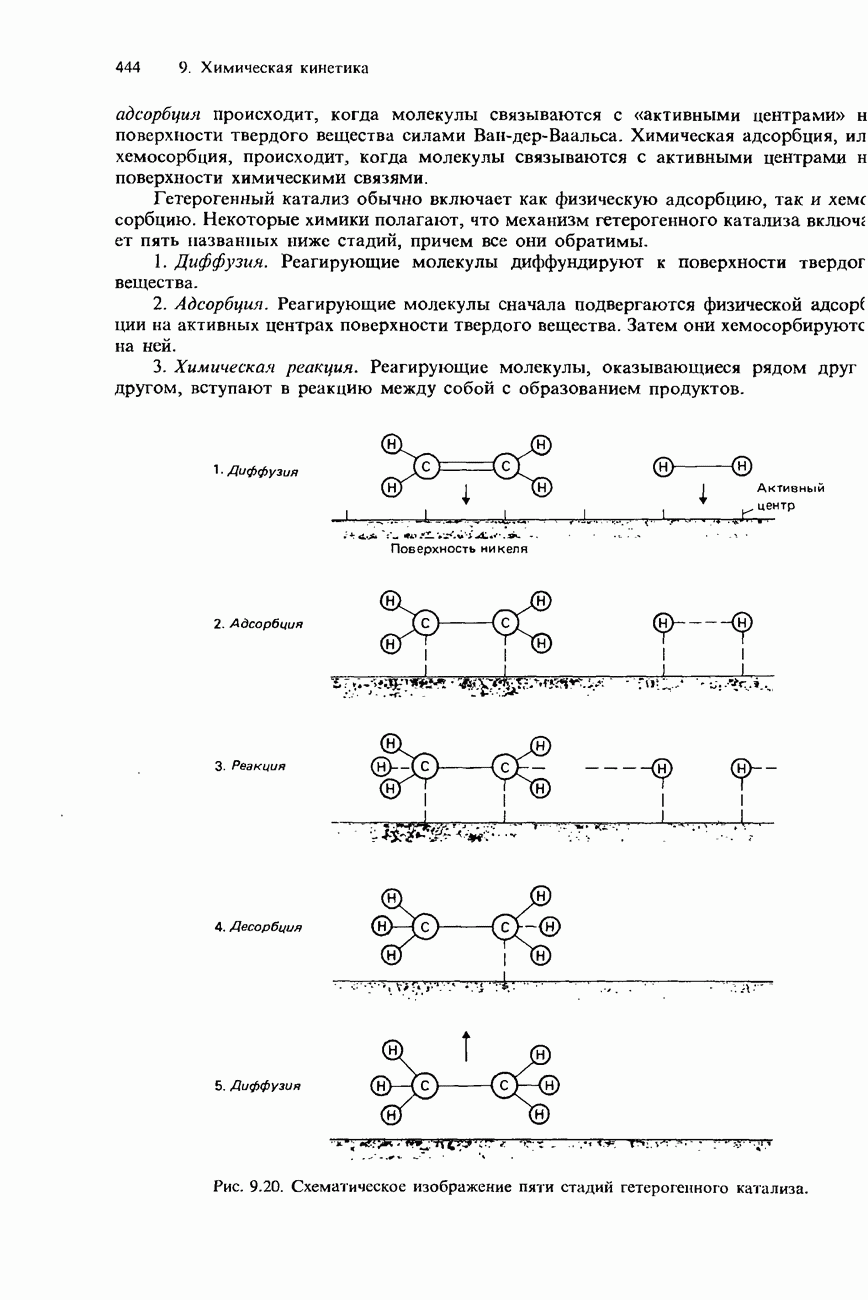
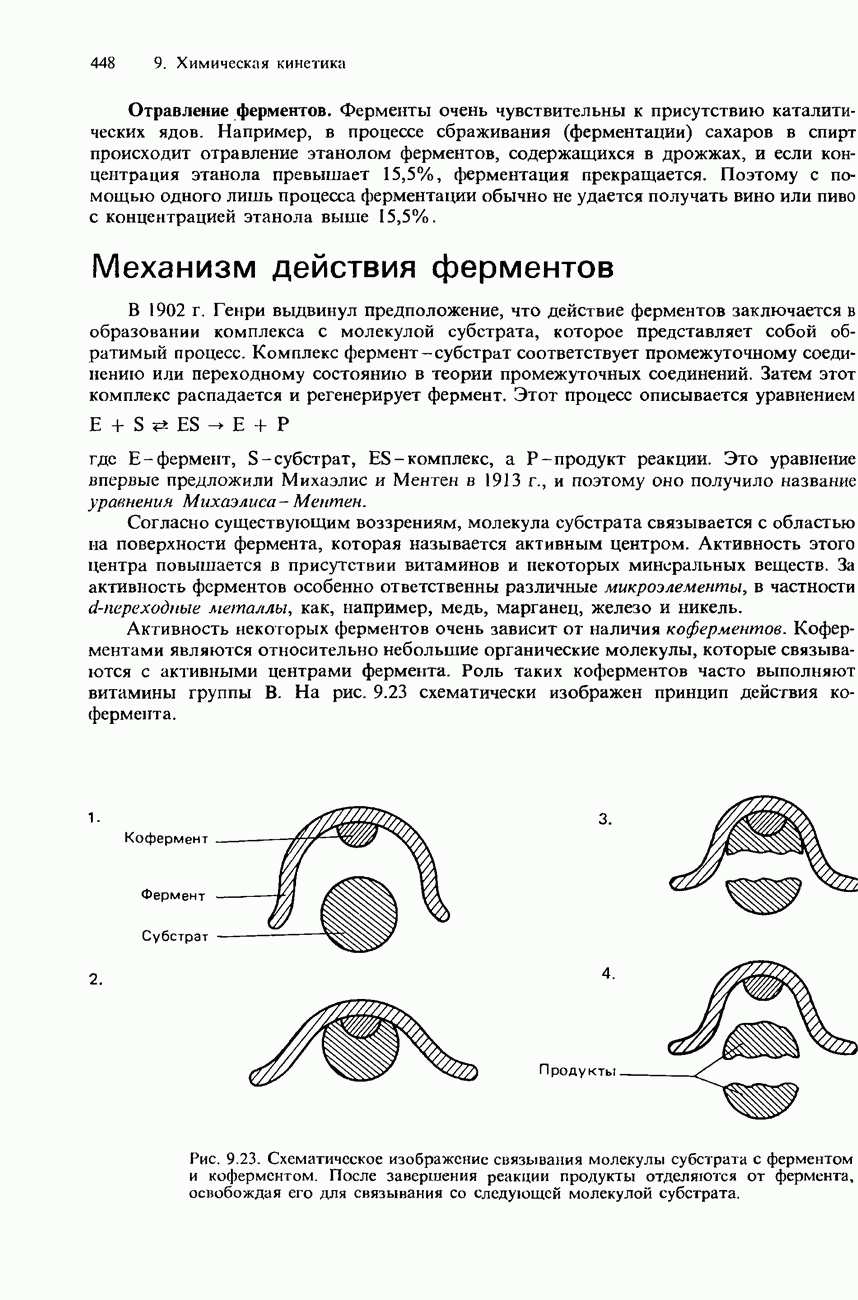
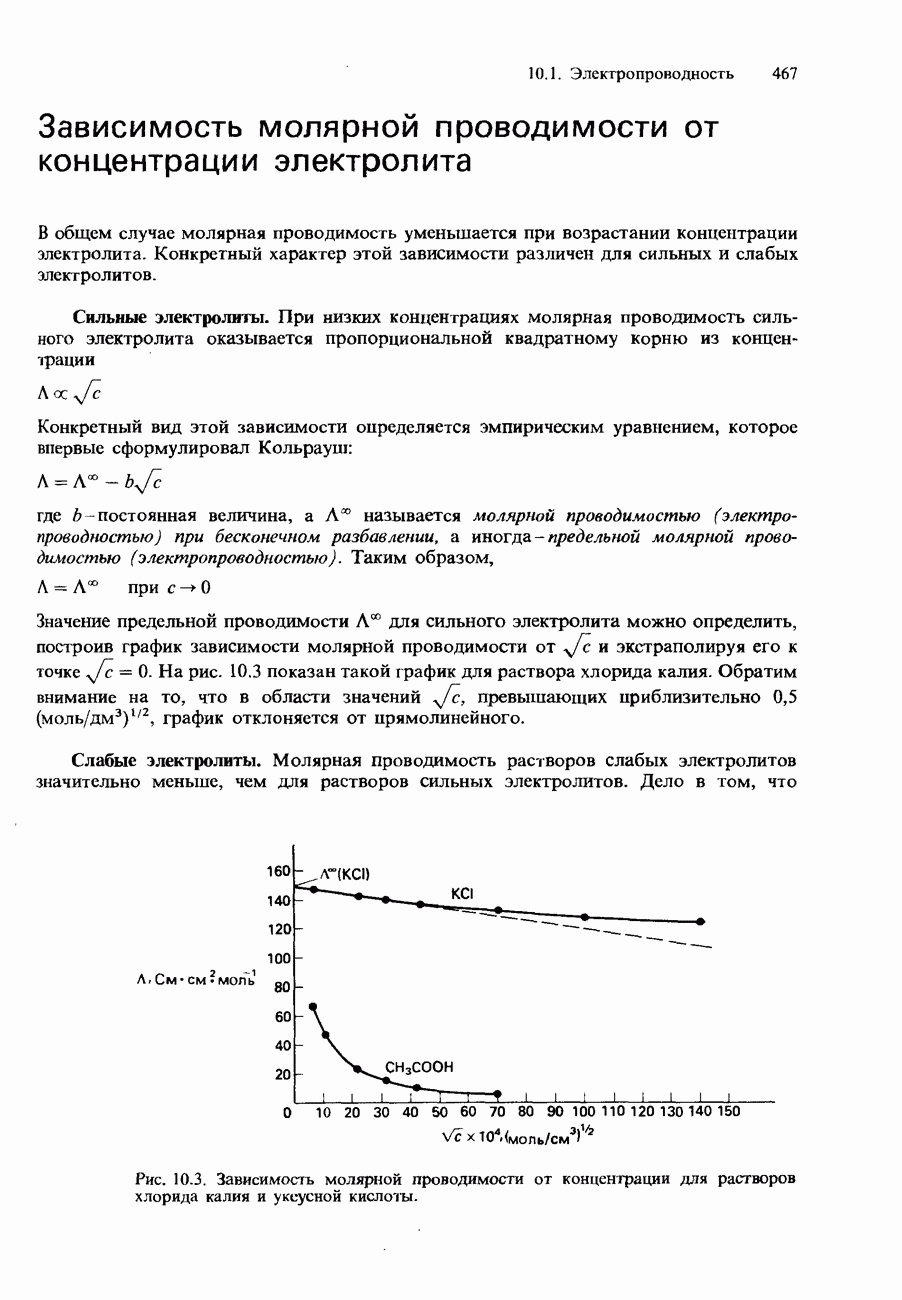
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
БУФЕРНЫЕ РАСТВОРЫ
Буферным раствором или просто буфером называют такой раствор, pH которого не претерпевает значительных изменений при добавлении небольших количеств кислоты либо основания.
Буферные растворы можно подразделить на четыре типа.
Буферные растворы, содержащие сильную кислоту
Всякая сильная кислота, например азотная, может использоваться как буфер с низким значением pH. Сильные кислоты полностью диссоциированы в водных растворах, и поэтому их растворы характеризуются высокой концентрацией ионов гидроксония. Добавление небольшого количества кислоты или основания к сильной кислоте оказывает поэтому лишь незначительное влияние на pH раствора сильной кислоты.
Например, если к 100 см3 раствора азотной кислоты с концентрацией 0,01 моль/дм3 добавить 1 см3 соляной кислоты с концентрацией 0,1 моль/дм3, то  уменьшится от 2,00 до 1,96. Изменение pH на 0,04 может считаться пренебрежимо малым. Чтобы проверить указанные выше значения pH раствора до и после добавления соляной кислоты, следует воспользоваться уравнением
уменьшится от 2,00 до 1,96. Изменение pH на 0,04 может считаться пренебрежимо малым. Чтобы проверить указанные выше значения pH раствора до и после добавления соляной кислоты, следует воспользоваться уравнением

Сопоставим теперь указанное пренебрежимо малое уменьшение pH с результатом добавления  раствора
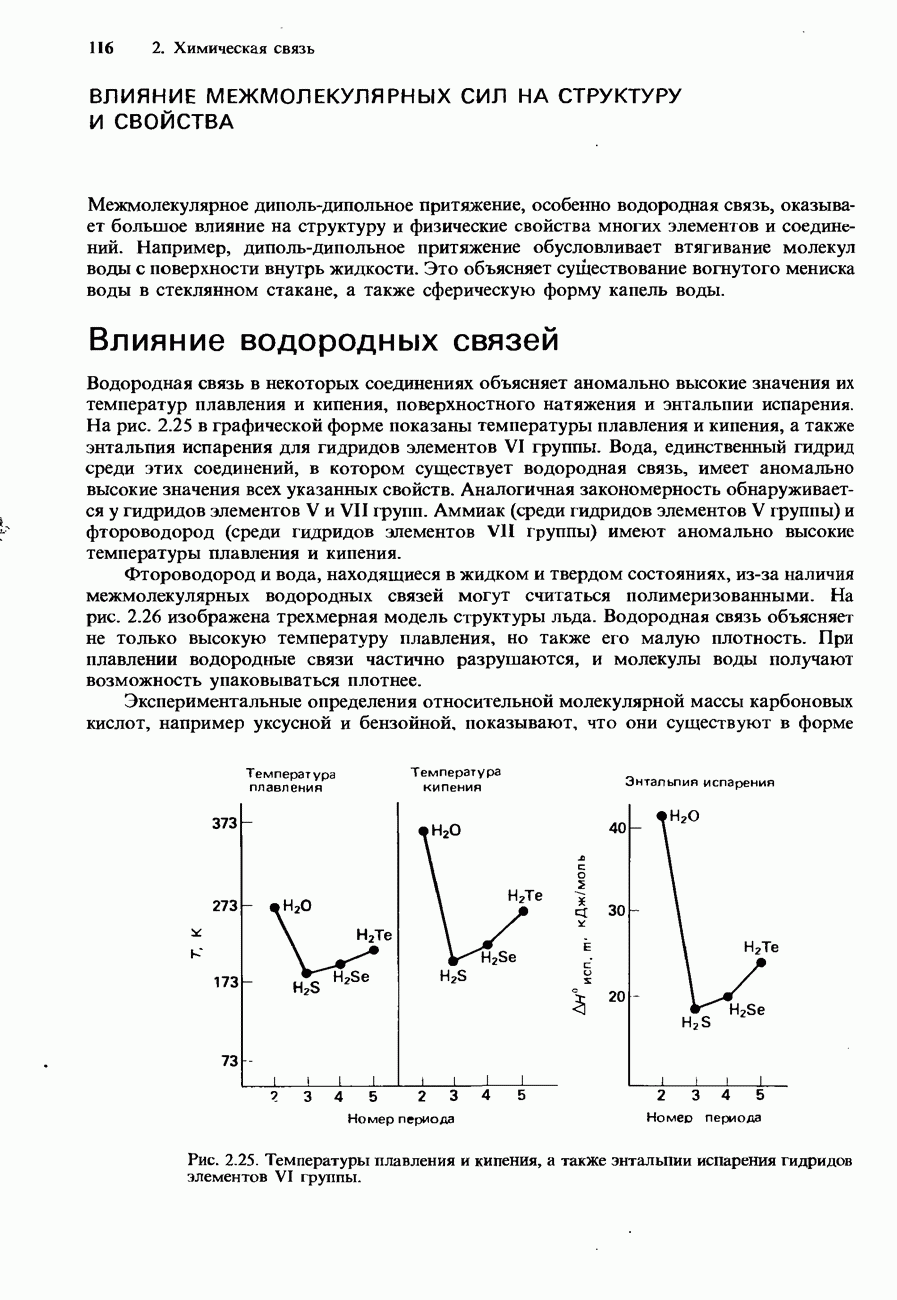
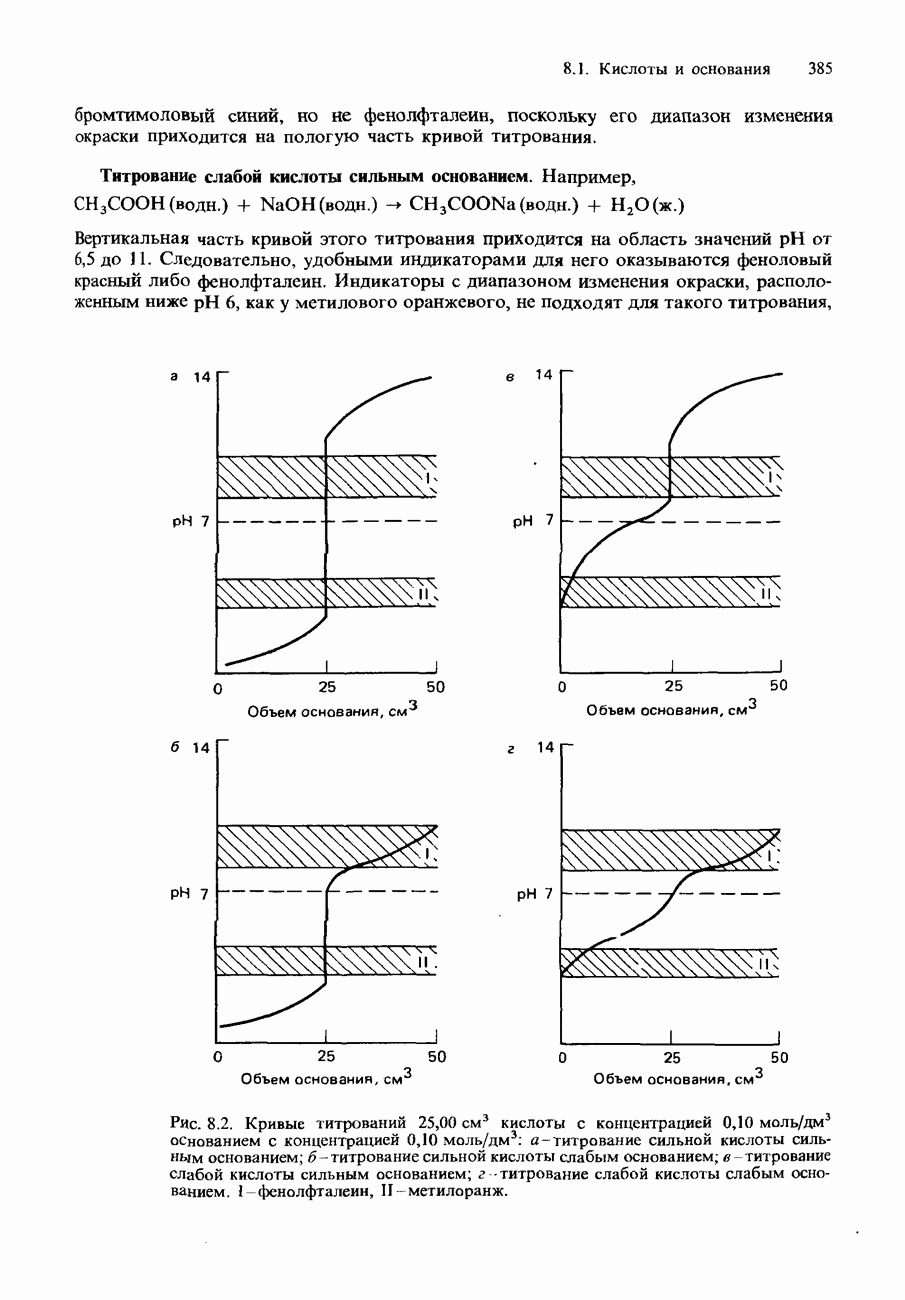
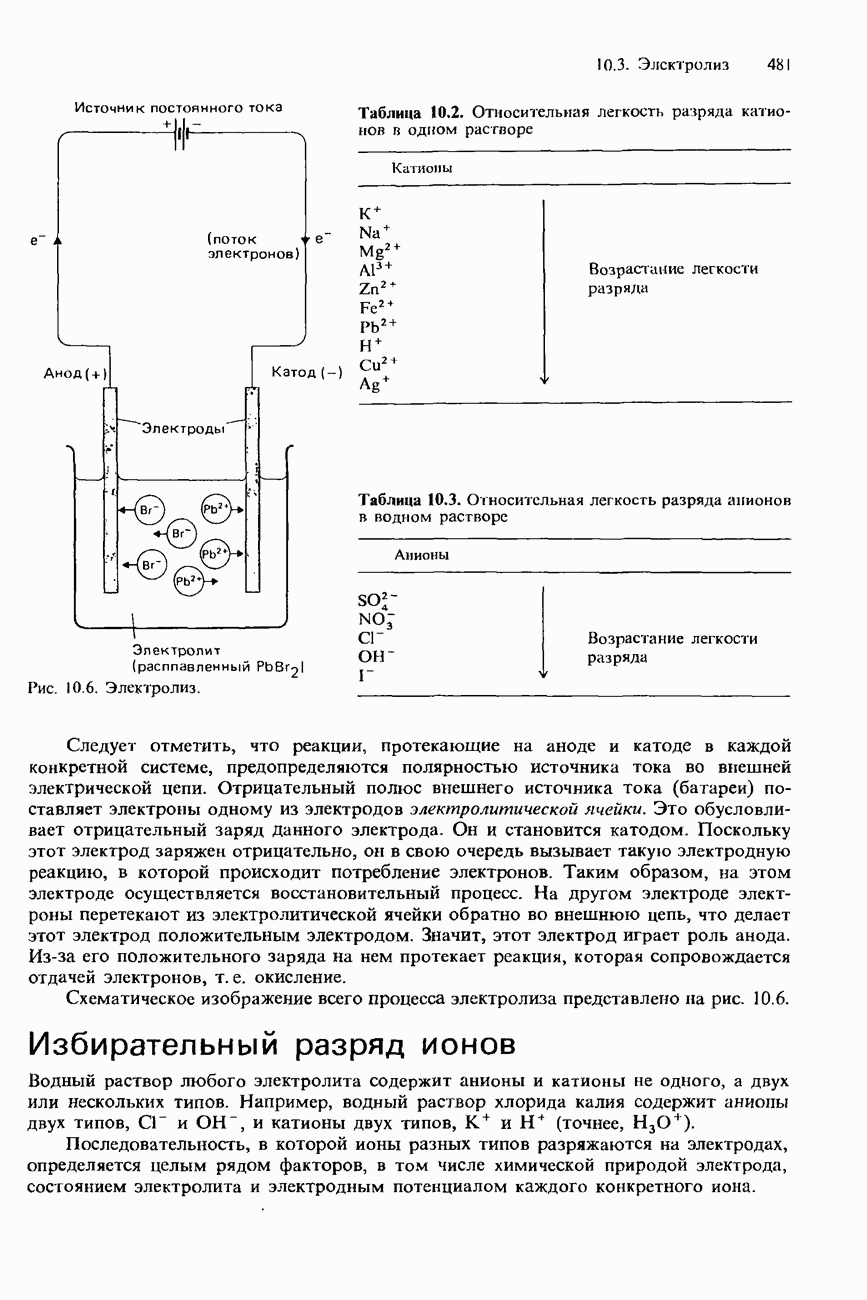
раствора  с концентрацией 0,1 моль/дм3 к 100 см3 чистой воды. В этом случае pH резко уменьшается от 7,00 до 4,00. Очевидно, чистая вода не действует как буферный раствор, поскольку она не поддерживает pH приблизительно на прежнем уровне. Концентрации буферных растворов соответствуют пологим частям кривых титрования, показанных на рис. 8.2. Эти части кривых титрования называются буферными областями. В буферной области значения pH нечувствительны к небольшим изменениям концентрации кислоты или основания.
с концентрацией 0,1 моль/дм3 к 100 см3 чистой воды. В этом случае pH резко уменьшается от 7,00 до 4,00. Очевидно, чистая вода не действует как буферный раствор, поскольку она не поддерживает pH приблизительно на прежнем уровне. Концентрации буферных растворов соответствуют пологим частям кривых титрования, показанных на рис. 8.2. Эти части кривых титрования называются буферными областями. В буферной области значения pH нечувствительны к небольшим изменениям концентрации кислоты или основания.
Буферные растворы, содержащие сильное основание
Всякое сильное основание может использоваться в качестве буфера с высоким значением  Добавление к такому буферу небольшого количества кислоты либо основания оказывает пренебрежимо малое влияние на
Добавление к такому буферу небольшого количества кислоты либо основания оказывает пренебрежимо малое влияние на  Например, при добавлении
Например, при добавлении  раствора соляной кислоты с концентрацией
раствора соляной кислоты с концентрацией  раствора
раствора  с концентрацией
с концентрацией  происходит изменение
происходит изменение  от 12,00 до 11,96. Изменение
от 12,00 до 11,96. Изменение  в этом случае составляет всего 0,04. Проверить этот результат можно с помощью уравнения (6) и соотношения
в этом случае составляет всего 0,04. Проверить этот результат можно с помощью уравнения (6) и соотношения

Буферные растворы, содержащие слабую кислоту
Буферные растворы с устойчивыми значениями  в пределах от 4 до 7 можно получить с помощью какой-либо слабой кислоты и одной из ее солей. С этой целью часто пользуются смесью уксусной кислоты и ацетата натрия. Ацетат натрия в водном растворе полностью ионизирован
в пределах от 4 до 7 можно получить с помощью какой-либо слабой кислоты и одной из ее солей. С этой целью часто пользуются смесью уксусной кислоты и ацетата натрия. Ацетат натрия в водном растворе полностью ионизирован

В отличие от него уксусная кислота ионизирована лишь частично

При добавлении кислоты это равновесие смещается влево, содержание добавленных ионов  уменьшается и восстанавливается первоначальное значение
уменьшается и восстанавливается первоначальное значение  Наличие ацетата натрия в буферном растворе обеспечивает большой запас ионов
Наличие ацетата натрия в буферном растворе обеспечивает большой запас ионов  способный компенсировать действие добавляемых порций кислоты.
способный компенсировать действие добавляемых порций кислоты.
При добавлении основания оно нейтрализуется ионами гидроксония

Удаление ионов  в результате протекания этой реакции приводит к тому, что равновесие (7) смещается вправо. Концентрация ионов
в результате протекания этой реакции приводит к тому, что равновесие (7) смещается вправо. Концентрация ионов  и, следовательно, значение
и, следовательно, значение  раствора остаются постоянными. Наличие уксусной кислоты в буферном растворе обеспечивает большой запас недиссоциированных молекул
раствора остаются постоянными. Наличие уксусной кислоты в буферном растворе обеспечивает большой запас недиссоциированных молекул  способных диссоциировать и, таким образом, при необходимости компенсировать добавление порций основания.
способных диссоциировать и, таким образом, при необходимости компенсировать добавление порций основания.
Действие буферных растворов можно рассмотреть количественно на основе закона действующих масс. Как было показано в предыдущем разделе, применение этого закона к равновесию диссоциации уксусной кислоты приводит к следующему выражению для константы диссоциации уксусной кислоты:

Логарифмирование этого выражения приводит к следующему результату: 

где  полные концентрации соответствующих частиц в буферном растворе. Константа диссоциации уксусной кислоты равна
полные концентрации соответствующих частиц в буферном растворе. Константа диссоциации уксусной кислоты равна  табл. 8.1). Это означает, что равновесие диссоциации уксусной кислоты, описываемое
табл. 8.1). Это означает, что равновесие диссоциации уксусной кислоты, описываемое
уравнением (7), значительно сдвинуто влево. По этой причине относительный вклад уксусной кислоты в общее количество ионов  в буферном растворе невелик. Величина
в буферном растворе невелик. Величина  в уравнении (8) почти полностью обусловлена вкладом соли, т.е. ацетата натрия, который полностью диссоциирован на ионы
в уравнении (8) почти полностью обусловлена вкладом соли, т.е. ацетата натрия, который полностью диссоциирован на ионы  Следовательно,
Следовательно,

Поскольку уксусная кислота мало диссоциирована в буферном растворю, концентрация кислоты  в равновесной смеси (7) приблизительно совпадает с ее исходной концентрацией в буферном растворе. Это позволяет записать
в равновесной смеси (7) приблизительно совпадает с ее исходной концентрацией в буферном растворе. Это позволяет записать

Подставляя полученные результаты в уравнение (8), получаем

Полученное соотношение называется уравнением Гендерсона для буферного раствора, состоящего из слабой кислоты и ее соли. Его можно использовать для различных вычислений, а именно для вычисления:  буферного раствора;
буферного раствора;
количества кислоты или соли, необходимого для получения буферного раствора с требуемым значением 
изменений  буферного раствора при добавлении к нему небольших порций кислоты либо основания.
буферного раствора при добавлении к нему небольших порций кислоты либо основания.
Пример
а) Сколько ацетата натрия следует растворить в  уксусной кислоты, имеющей концентрацию
уксусной кислоты, имеющей концентрацию  чтобы получить буферный раствор с
чтобы получить буферный раствор с 
б) Как изменится  этого буферного раствора, если к
этого буферного раствора, если к  буфера добавить
буфера добавить  раствора
раствора  имеющего концентрацию
имеющего концентрацию 
Решение
а) Из уравнения (9) нетрудно найти

По условию  и
и 
По данным табл. 8.1  .
.
Подстановка всех этих значений в полученное уравнение дает

Следовательно,

Это означает, что для получения буферного раствора с  следует растворить в
следует растворить в  уксусной кислоты
уксусной кислоты  моль ацетата натрия.
моль ацетата натрия.
Относительная молярная масса ацетата натрия:

Следовательно, масса  моль ацетата натрия составляет
моль ацетата натрия составляет

Таким образом, чтобы получить буферный раствор с  нужно растворить в
нужно растворить в  уксусной кислоты 1,46 г ацетата натрия.
уксусной кислоты 1,46 г ацетата натрия.
б) 1 см3 раствора  имеющего концентрацию
имеющего концентрацию  содержит
содержит
0,001 моля  Он реагирует с
Он реагирует с  образуя
образуя  Следовательно, концентрация
Следовательно, концентрация  уменьшится на
уменьшится на  а концентрация
а концентрация  возрастет на 0,001 моль/дм3 (небольшим увеличением объема можно пренебречь). Таким образом,
возрастет на 0,001 моль/дм3 (небольшим увеличением объема можно пренебречь). Таким образом,

Значит,

Итак, при добавлении к  буферного раствора
буферного раствора  щелочи должно произойти пренебрежимо малое изменение
щелочи должно произойти пренебрежимо малое изменение  на величину 0,07.
на величину 0,07.
При рассмотрении буферных растворов, содержащих слабую кислоту, возникает один особый случай. Уравнение Гендерсона показывает, что, когда концентрация соли точно равна концентрации кислоты,  буферного раствора совпадает с
буферного раствора совпадает с  этой кислоты, т.е.
этой кислоты, т.е.

Например, если 100 см3 раствора  с концентрацией 0,1 моль/дм3 добавить к 100 см3 раствора
с концентрацией 0,1 моль/дм3 добавить к 100 см3 раствора  с концентрацией 0,1 моль/дм3, то pH полученного буфера должен быть равен 4,75 при 25 °С.
с концентрацией 0,1 моль/дм3, то pH полученного буфера должен быть равен 4,75 при 25 °С.
Буферные растворы, содержащие слабое основание
Буферные растворы с устойчивыми значениями  в интервале от 7 до 10 можно получить, смешав какое-либо слабое основание с одной из его солей. Типичным буферным раствором такого типа является раствор аммиака и хлорида аммония. В водном растворе хлорид аммония полностью диссоциирует
в интервале от 7 до 10 можно получить, смешав какое-либо слабое основание с одной из его солей. Типичным буферным раствором такого типа является раствор аммиака и хлорида аммония. В водном растворе хлорид аммония полностью диссоциирует

Аммиак диссоциирует в воде лишь частично

При добавлении кислоты в этот буферный раствор она нейтрализуется ионами  Вследствие этого равновесие (10) смещается вправо. Этот сдвиг поддерживает постоянную концентрацию ионов
Вследствие этого равновесие (10) смещается вправо. Этот сдвиг поддерживает постоянную концентрацию ионов  и, следовательно, постоянный
и, следовательно, постоянный 
При добавлении основания равновесие (10) смещается влево, и концентрация ионов ОН поддерживается постоянной. Наличие в буферном растворе хлорида аммония обеспечивает в нем большой запас ионов  позволяющий компенсировать влияние добавляемых порций основания.
позволяющий компенсировать влияние добавляемых порций основания.
Уравнение Гендерсона для буферного раствора, содержащего слабое основание и одну из его солей, имеет вид

Применения буферных растворов
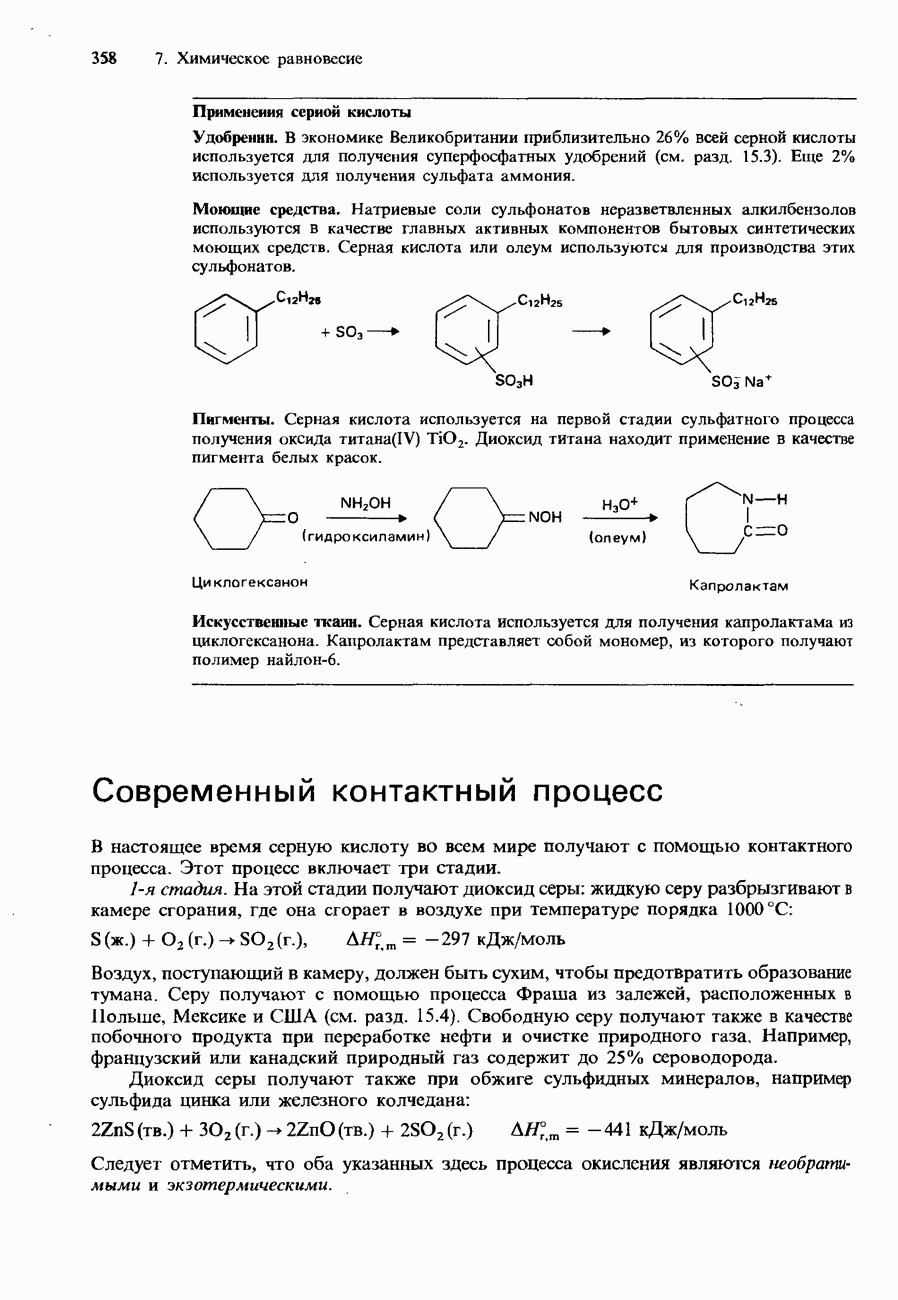
Буферные растворы играют важную роль во многих технологических процессах. Они используются, например, при электрохимическом нанесении защитных покрытий, в производстве красителей, фотоматериалов и кожи. Кроме того, буферные растворы широко используются в химическом анализе и для калибровки рН-метров (см. гл. 10).
Многие биологические и другие системы зависят от содержащихся в них буферных растворов, которые поддерживают постоянство pH. Нормальные значения pH для некоторых из таких систем указаны в табл. 8.6. Например, pH крови в организме человека поддерживается в пределах от 7,35 до 7,45, несмотря на то, что содержание диоксида углерода и, следовательно, угольной кислоты в крови может варьировать в широких пределах. Содержащийся в крови буфер представляет собой смесь фосфата, гидрокарбоната и белков. Буферы, состоящие из белков, поддерживают pH слез равным 7,4. В бактериологических исследованиях для поддержания постоянства pH культурных сред, используемых с целью выращивания бактерий, тоже приходится использовать буферные растворы.
Таблица 8.6, Значения pH для некоторых биологических систем и других растворов

| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
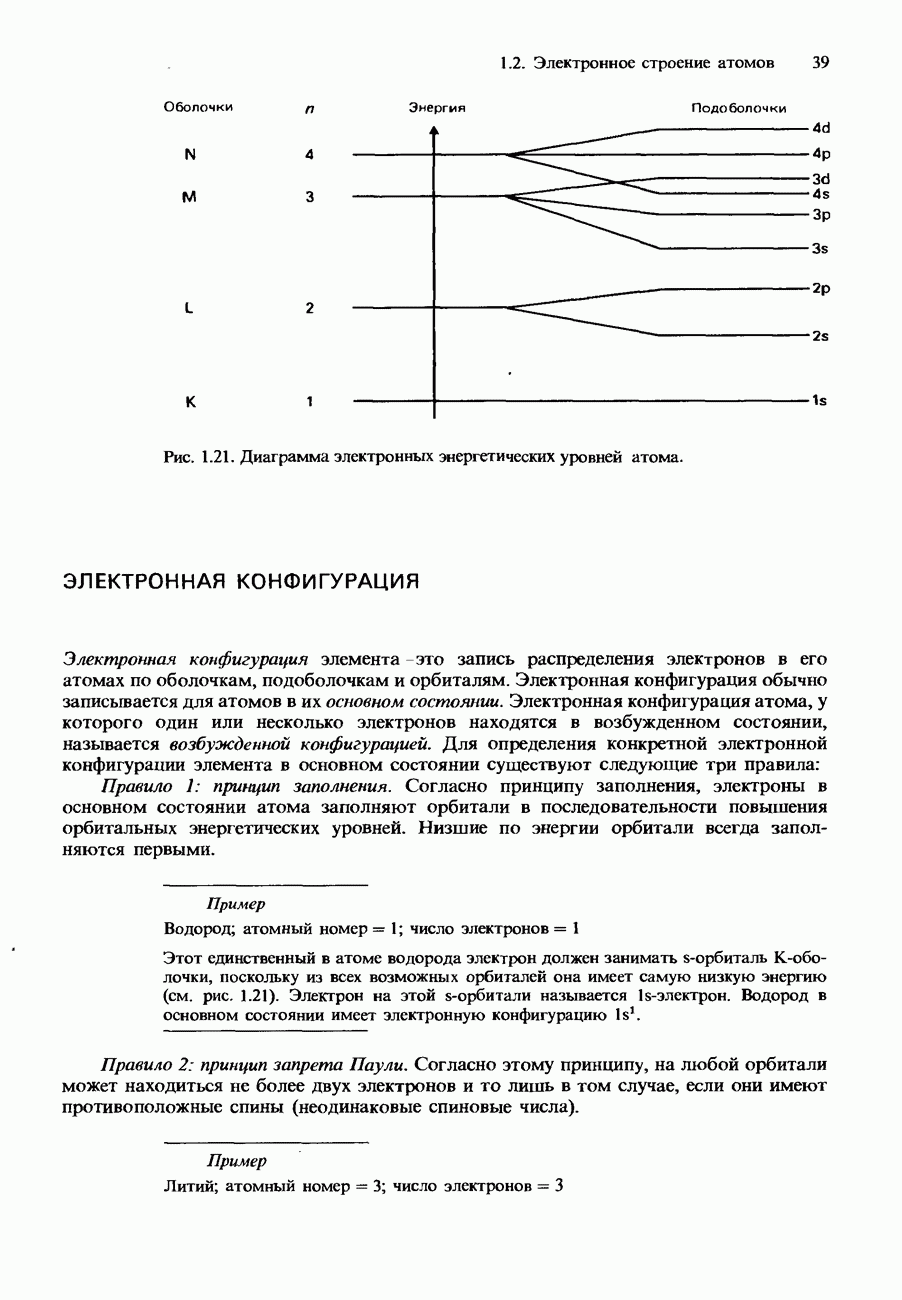
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
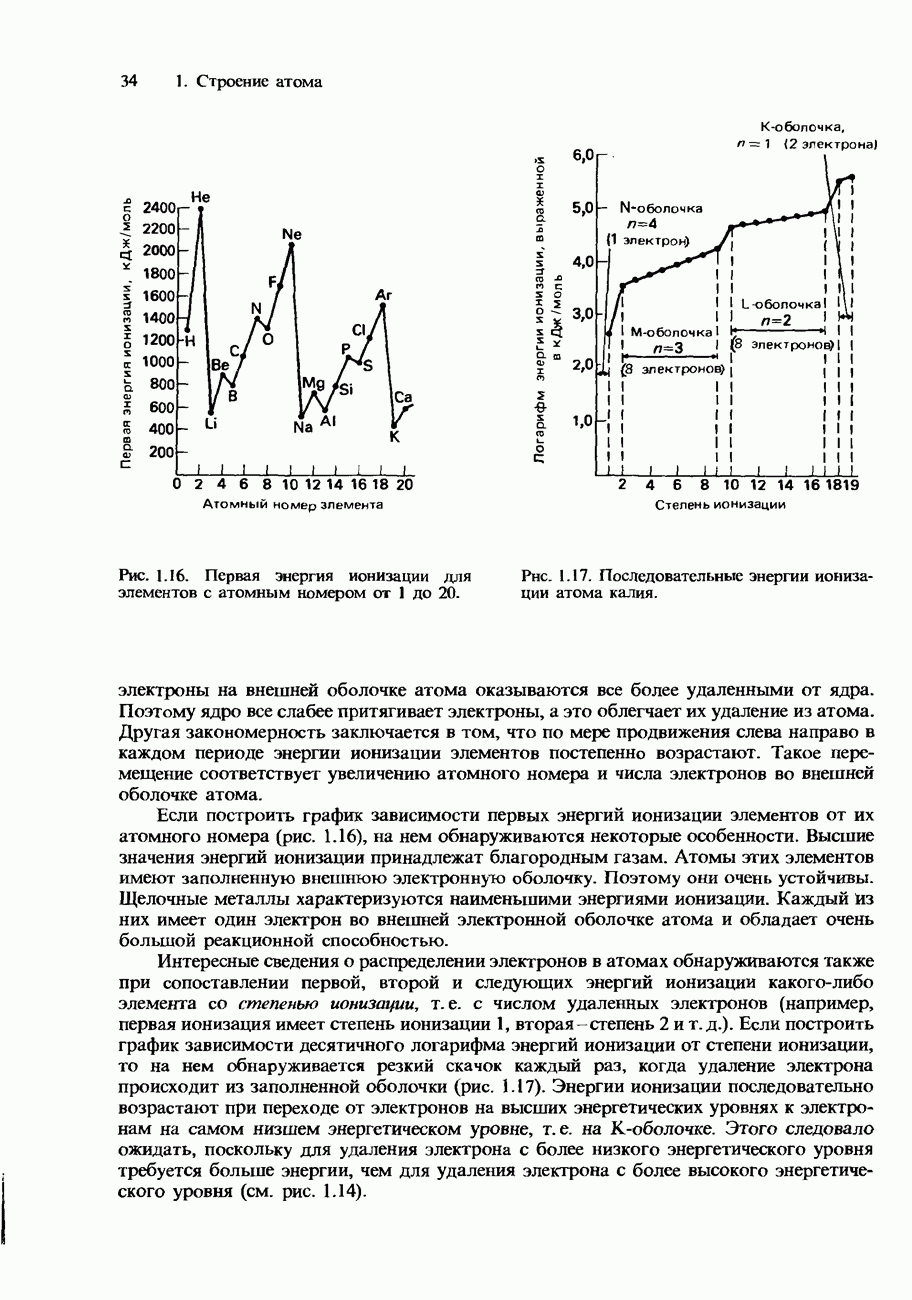
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
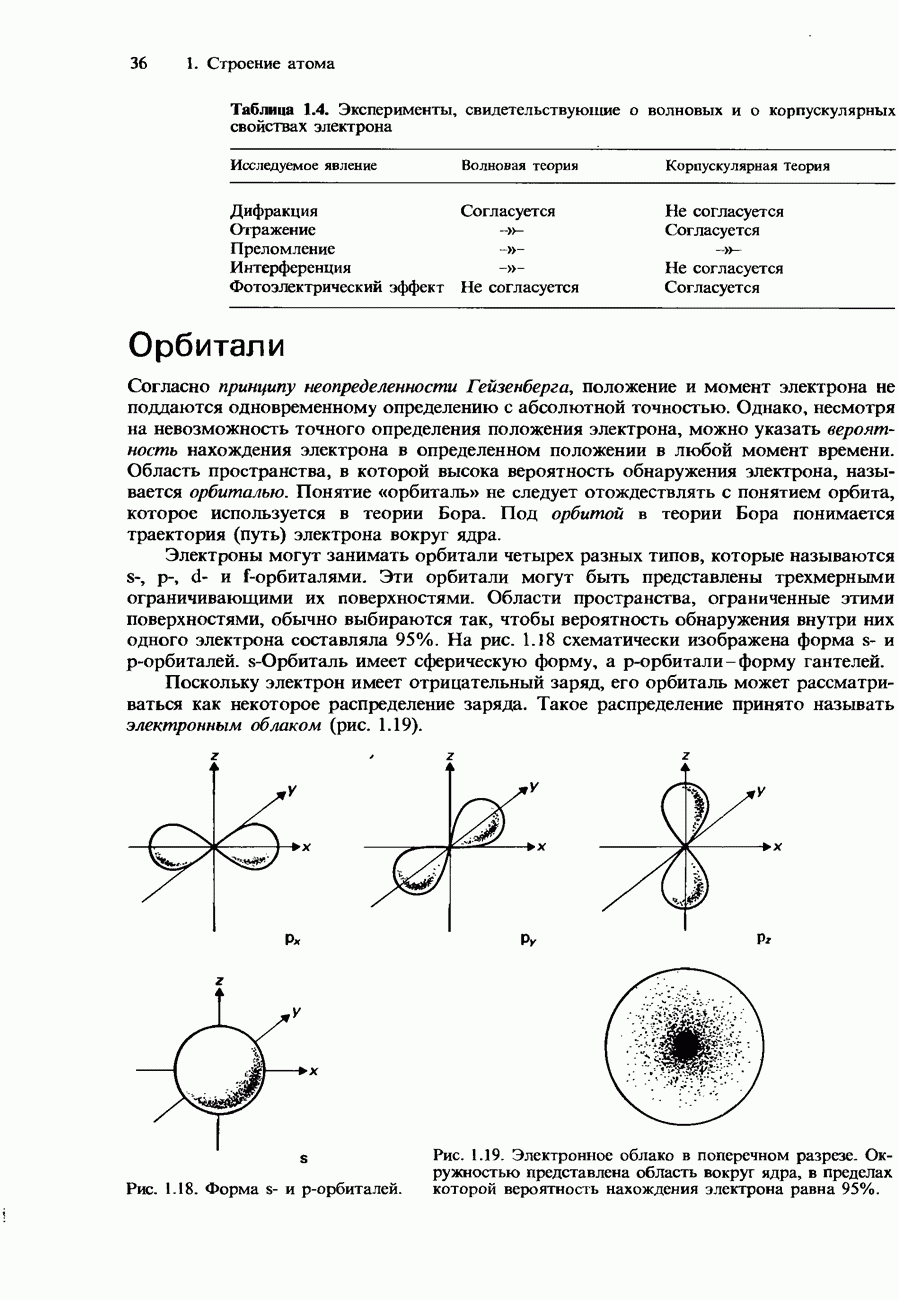
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
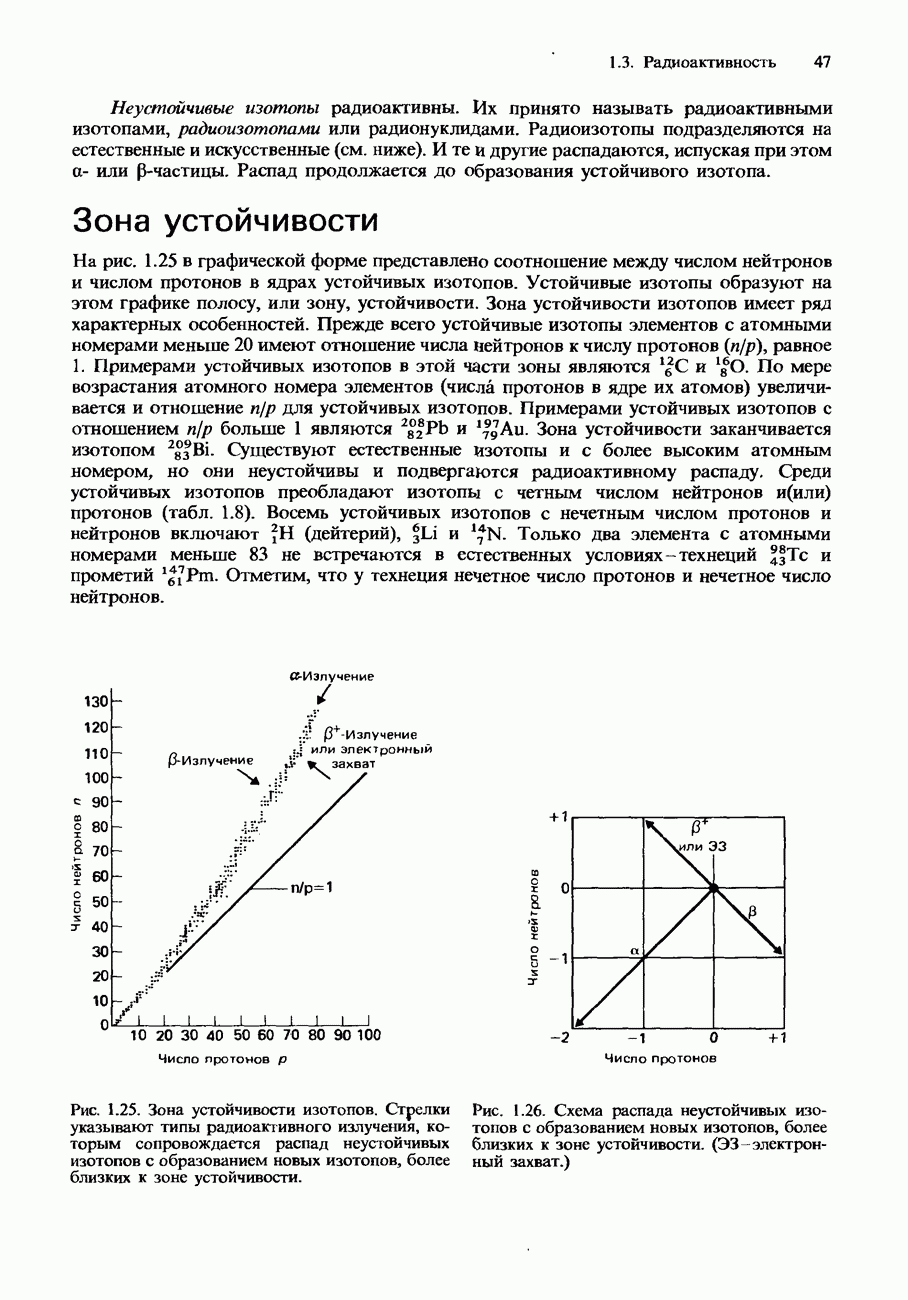
- Зона устойчивости
- Период полураспада
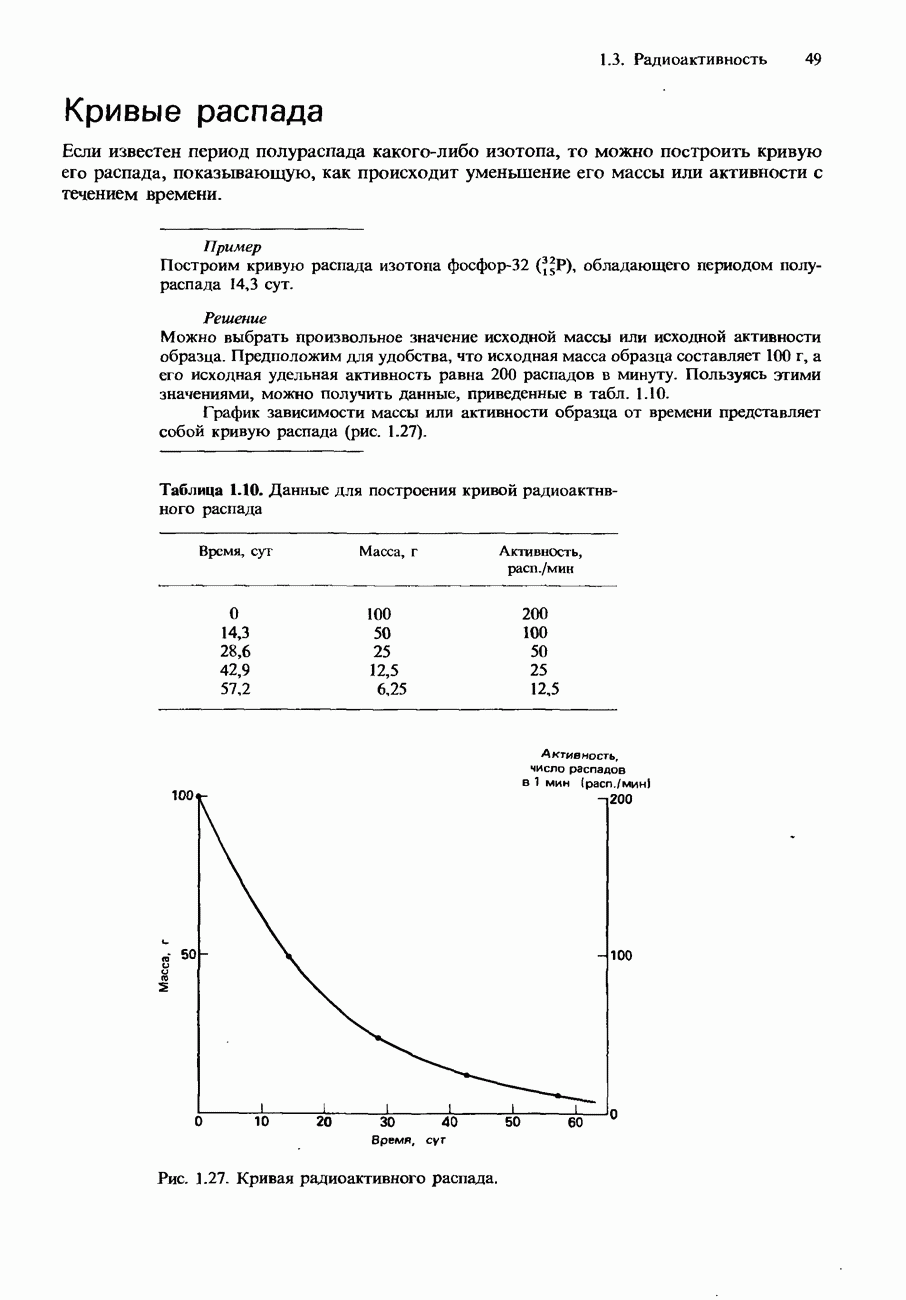
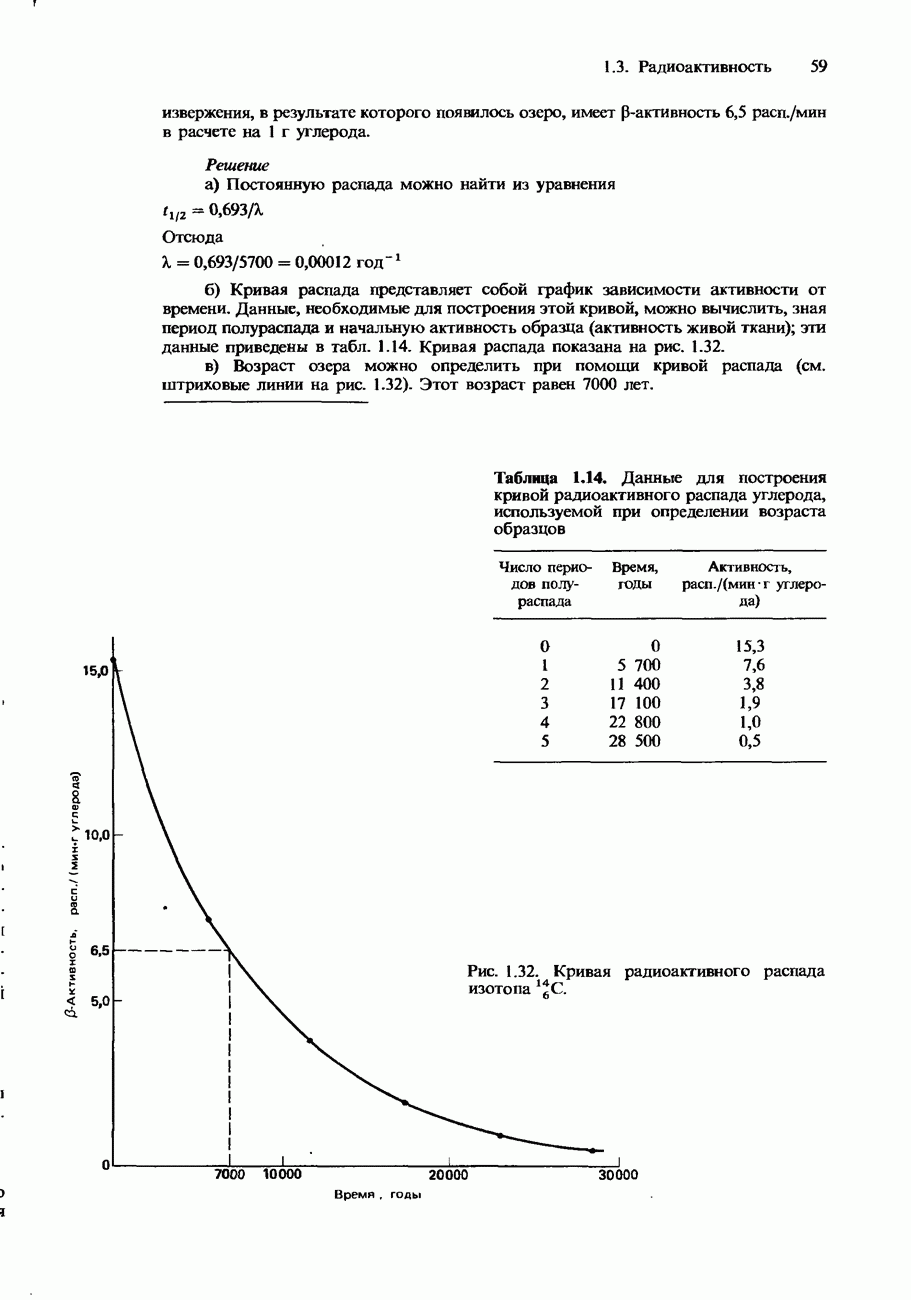
- Кривые распада
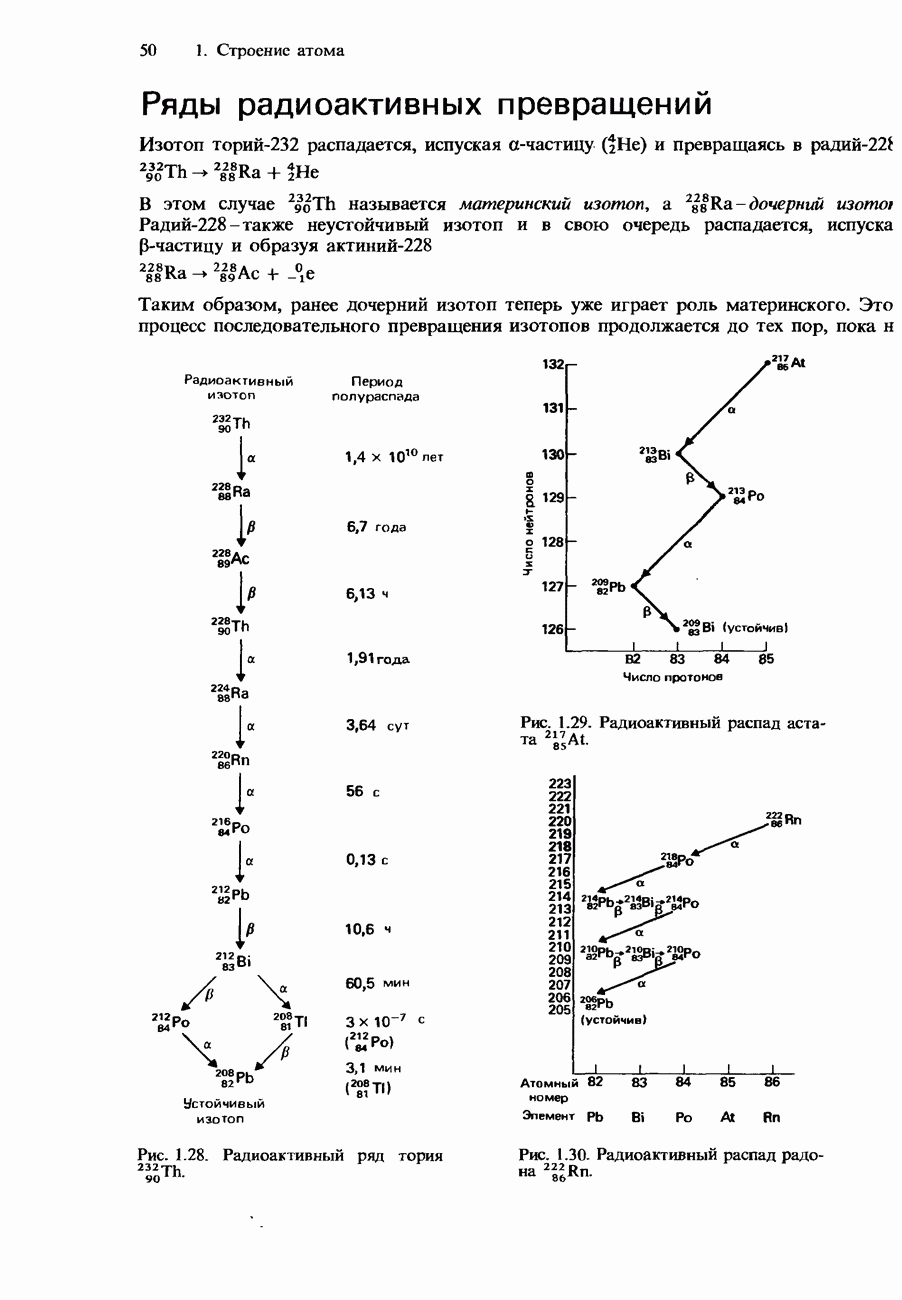
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
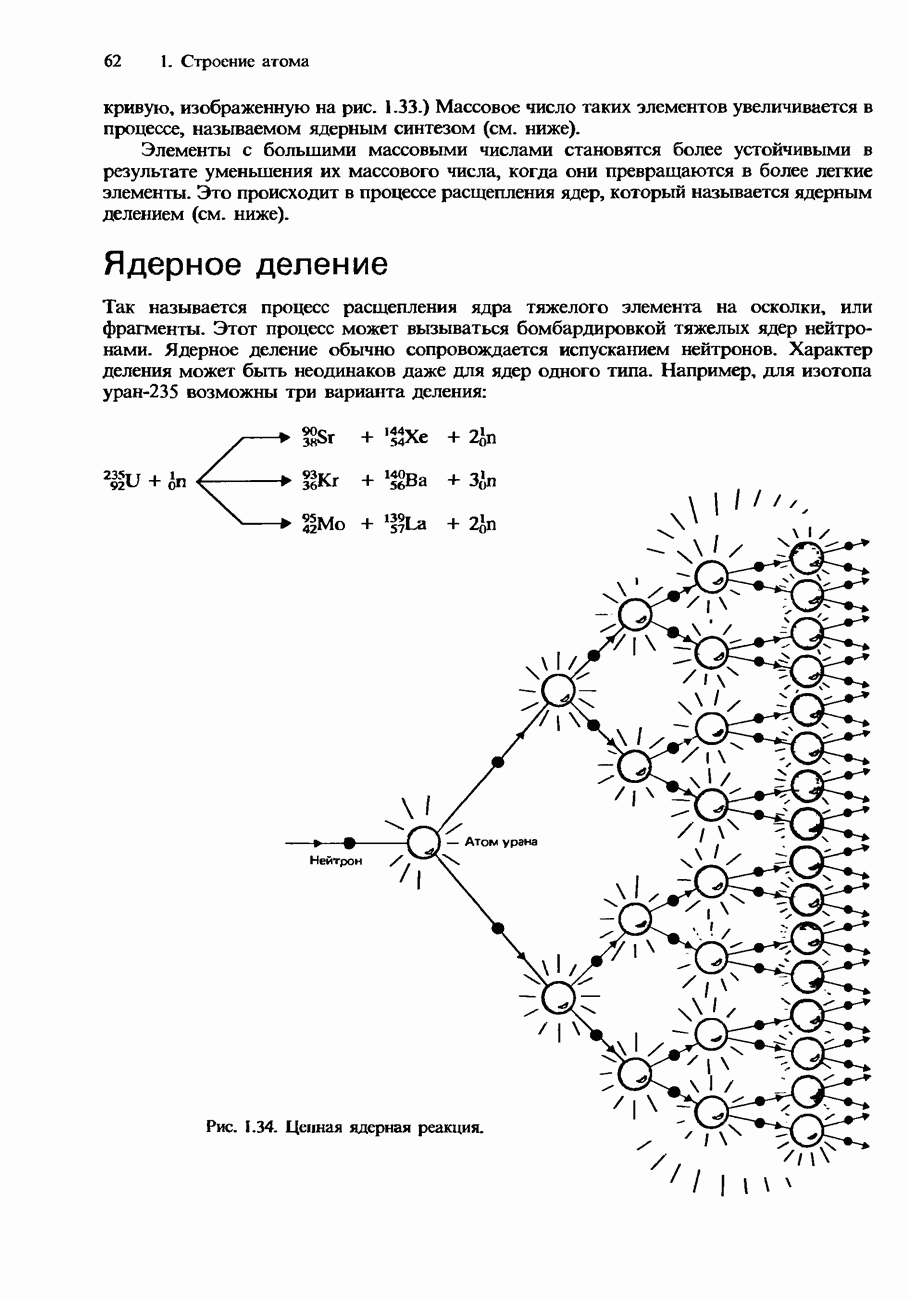
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
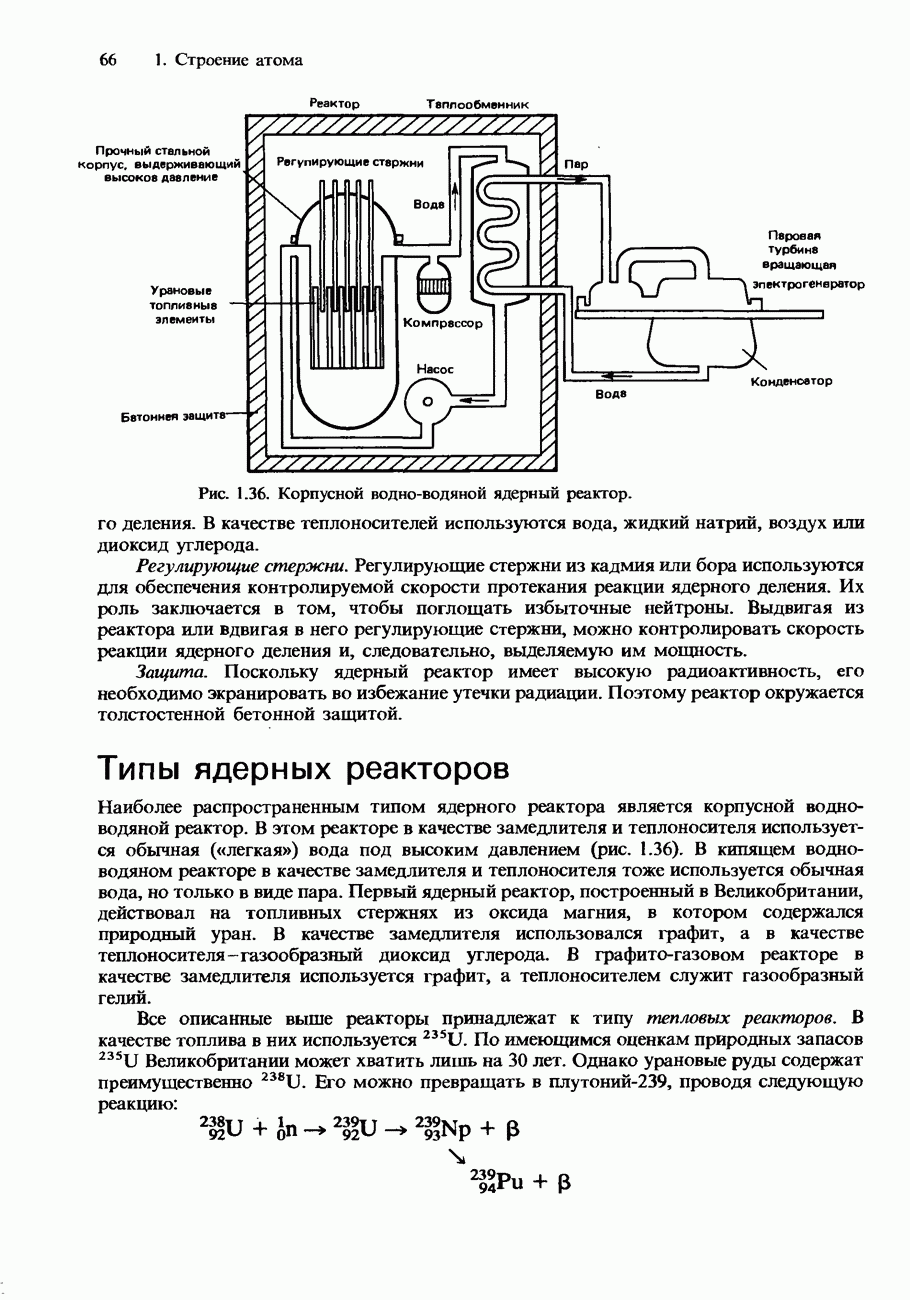
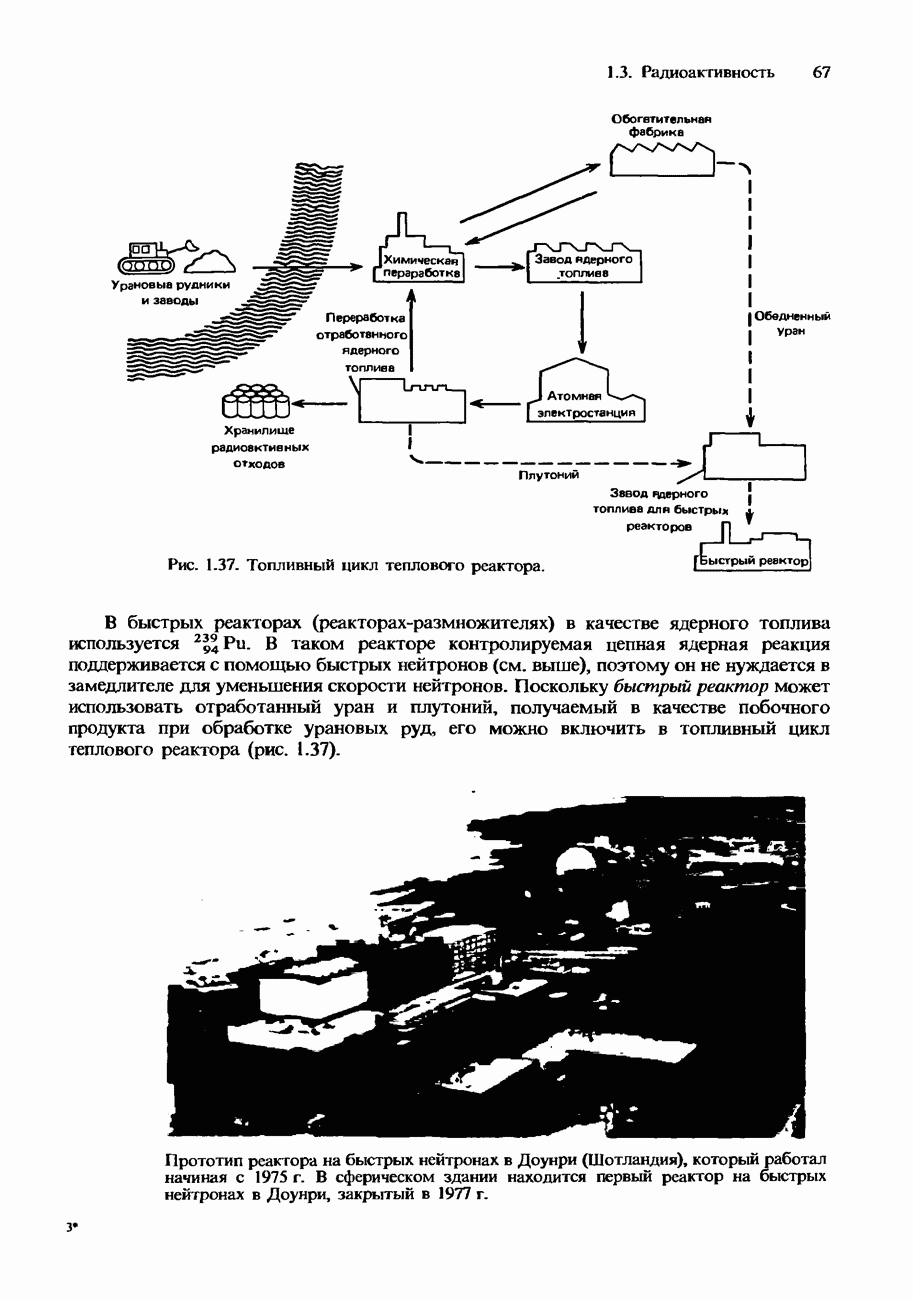
- Типы ядерных реакторов
- Радиоактивные ядерные отходы и их переработка
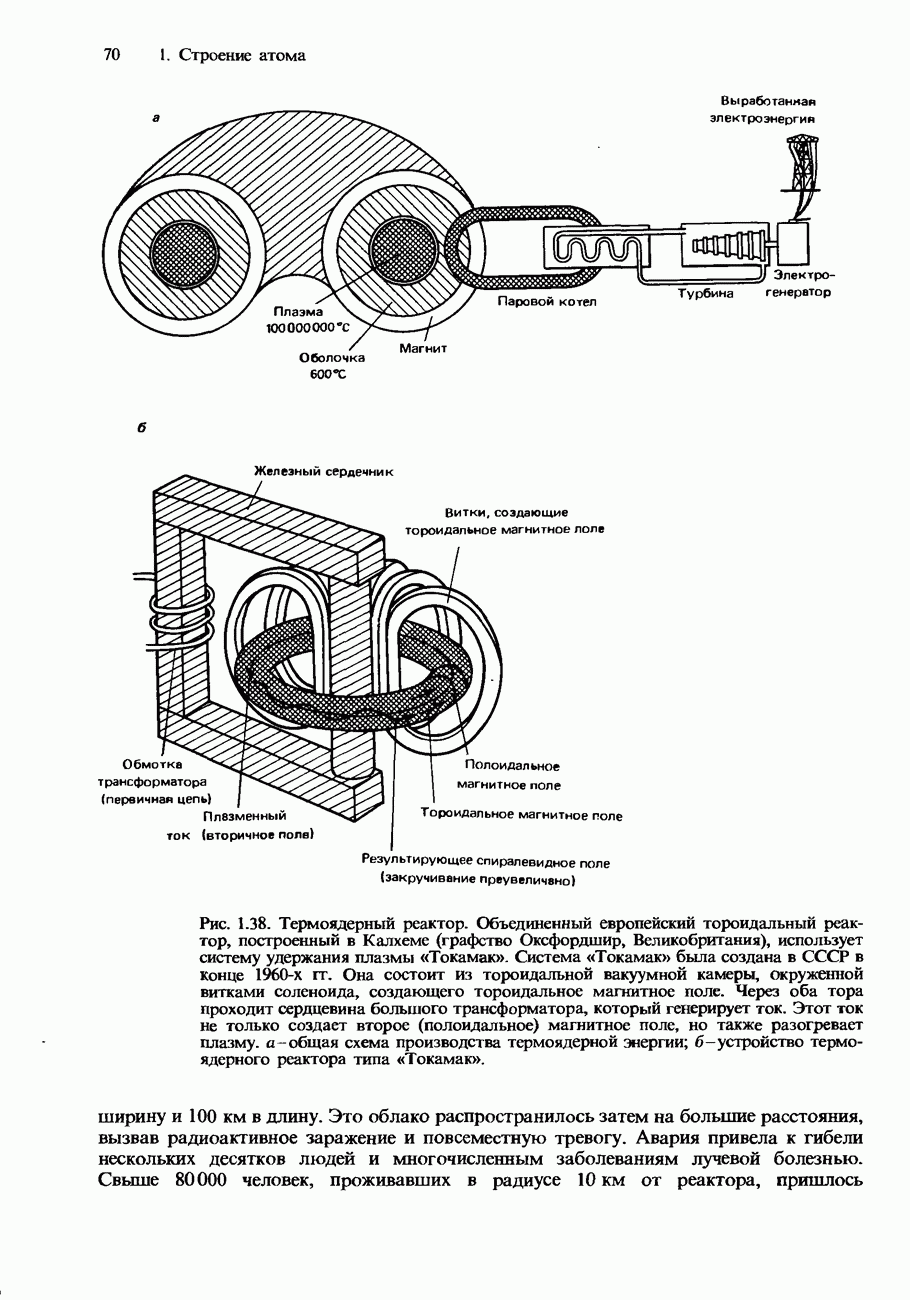
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
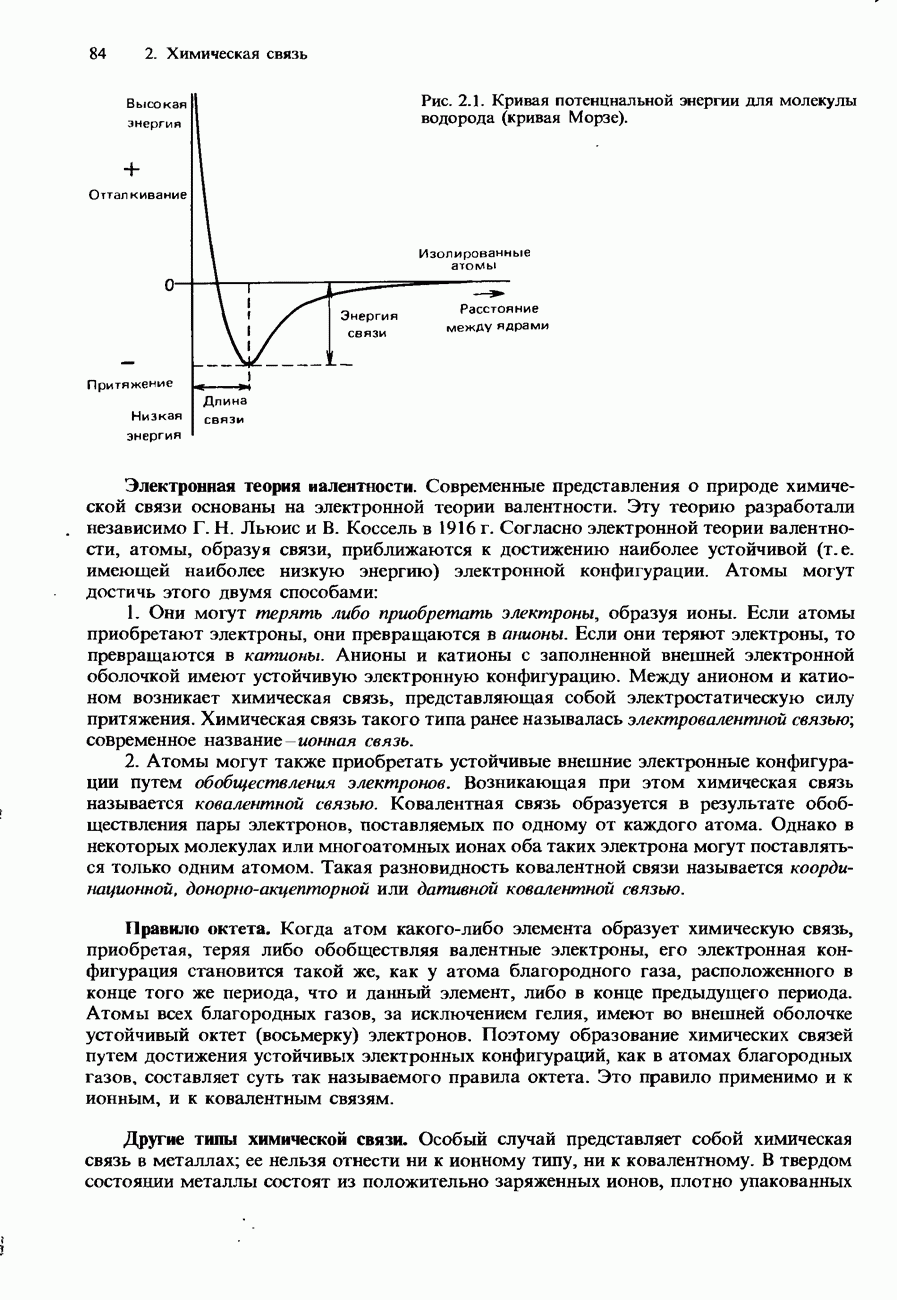
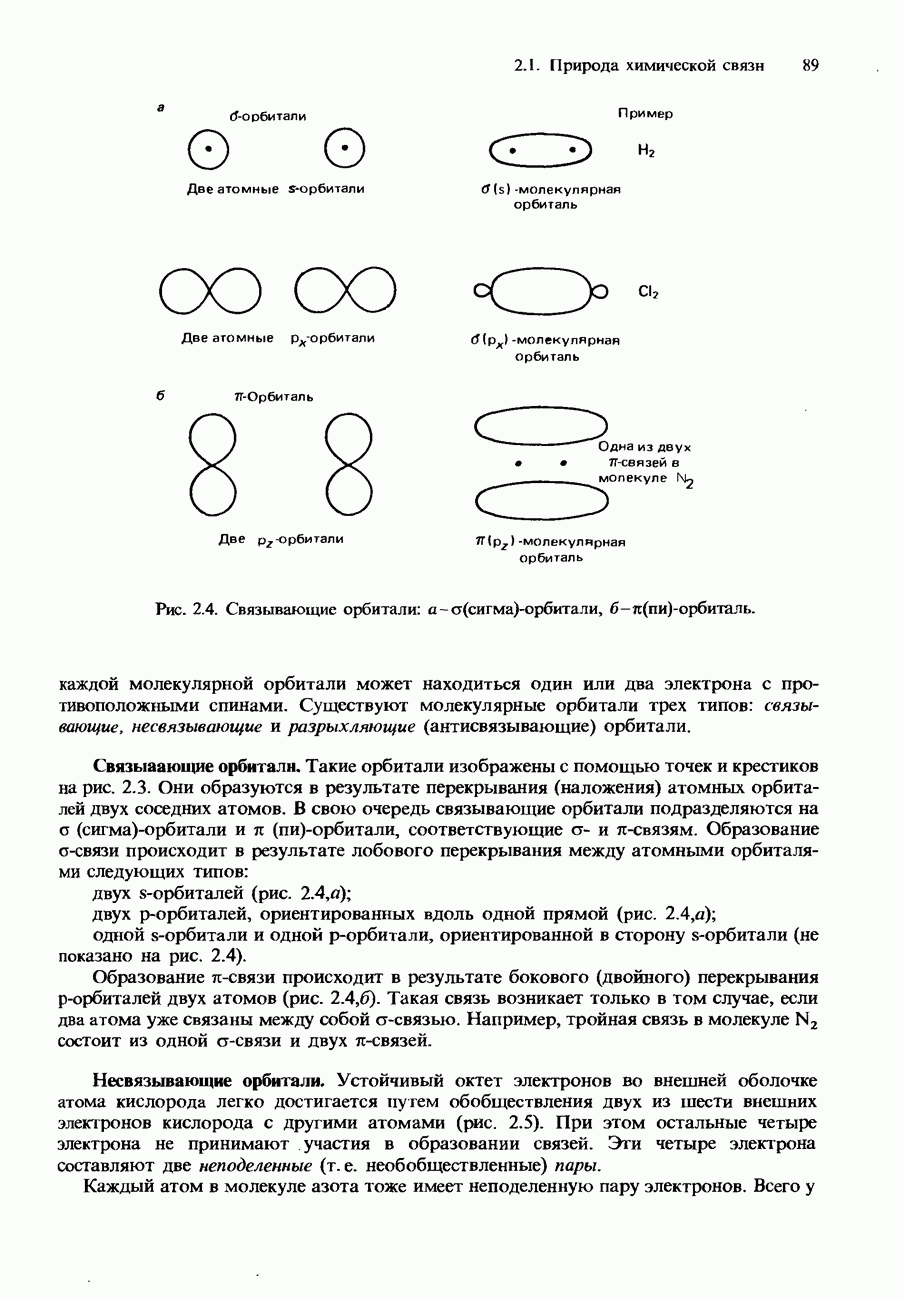
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
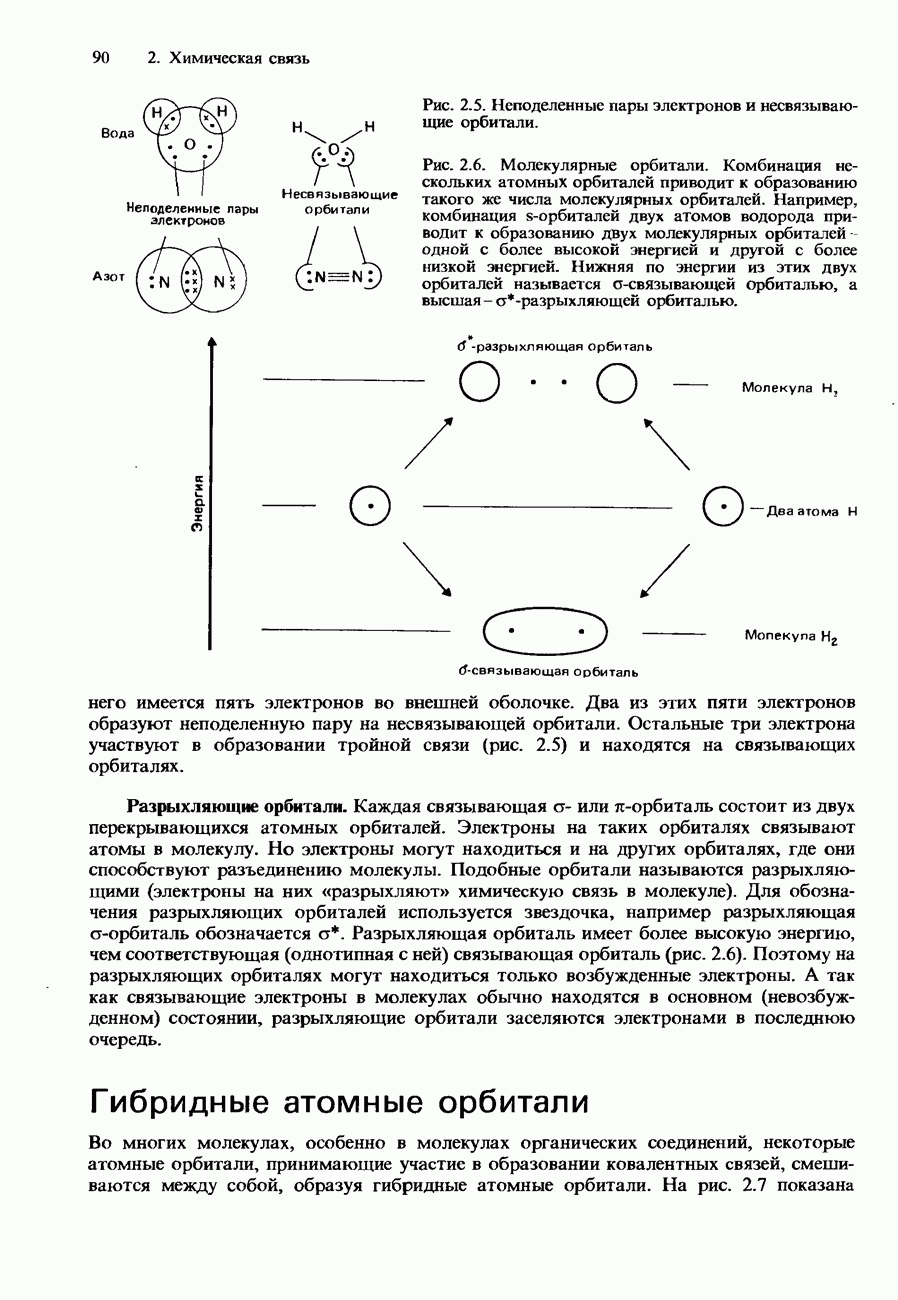
- Молекулярные орбитали
- Гибридные атомные орбитали
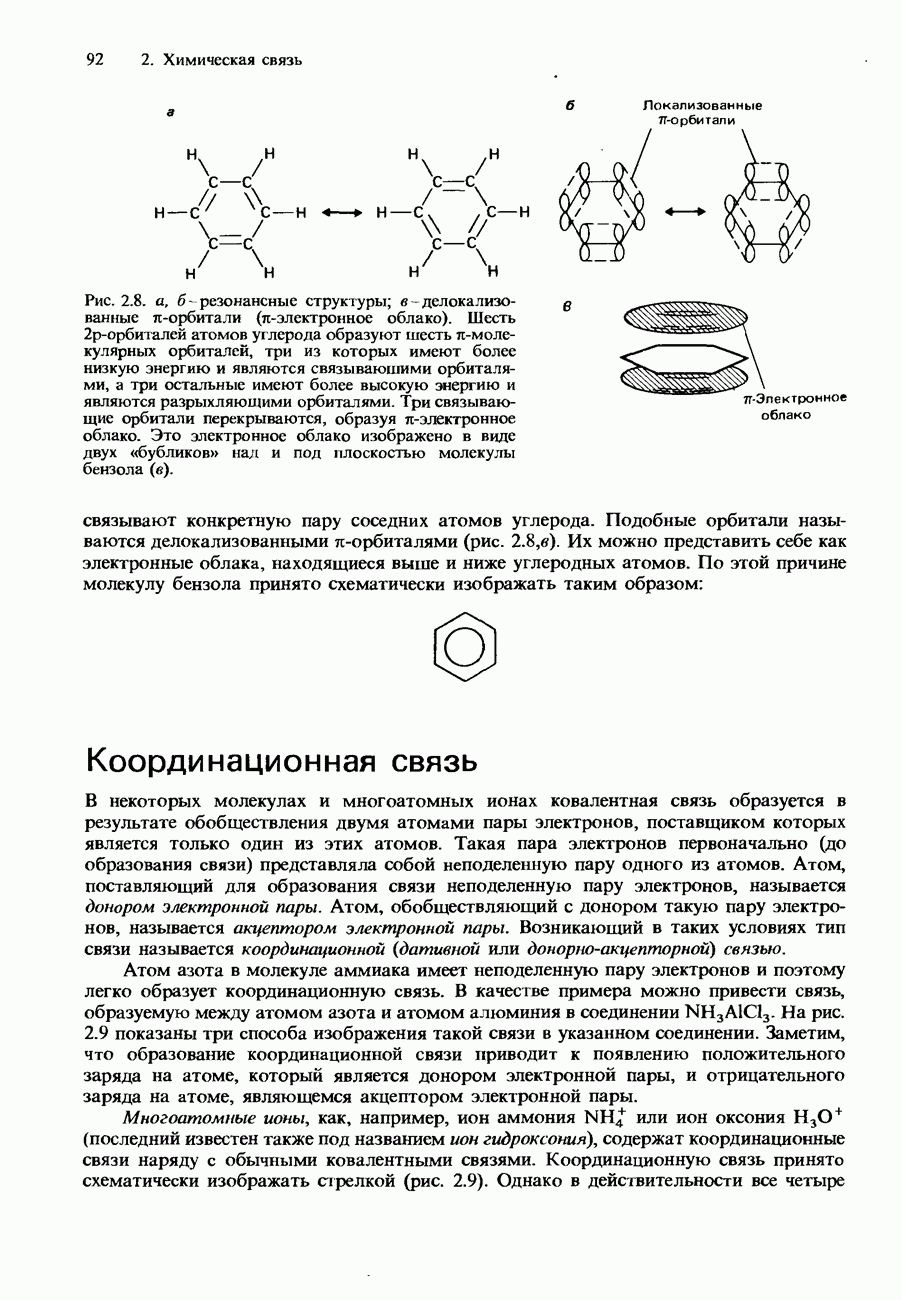
- Делокализованные орбитали
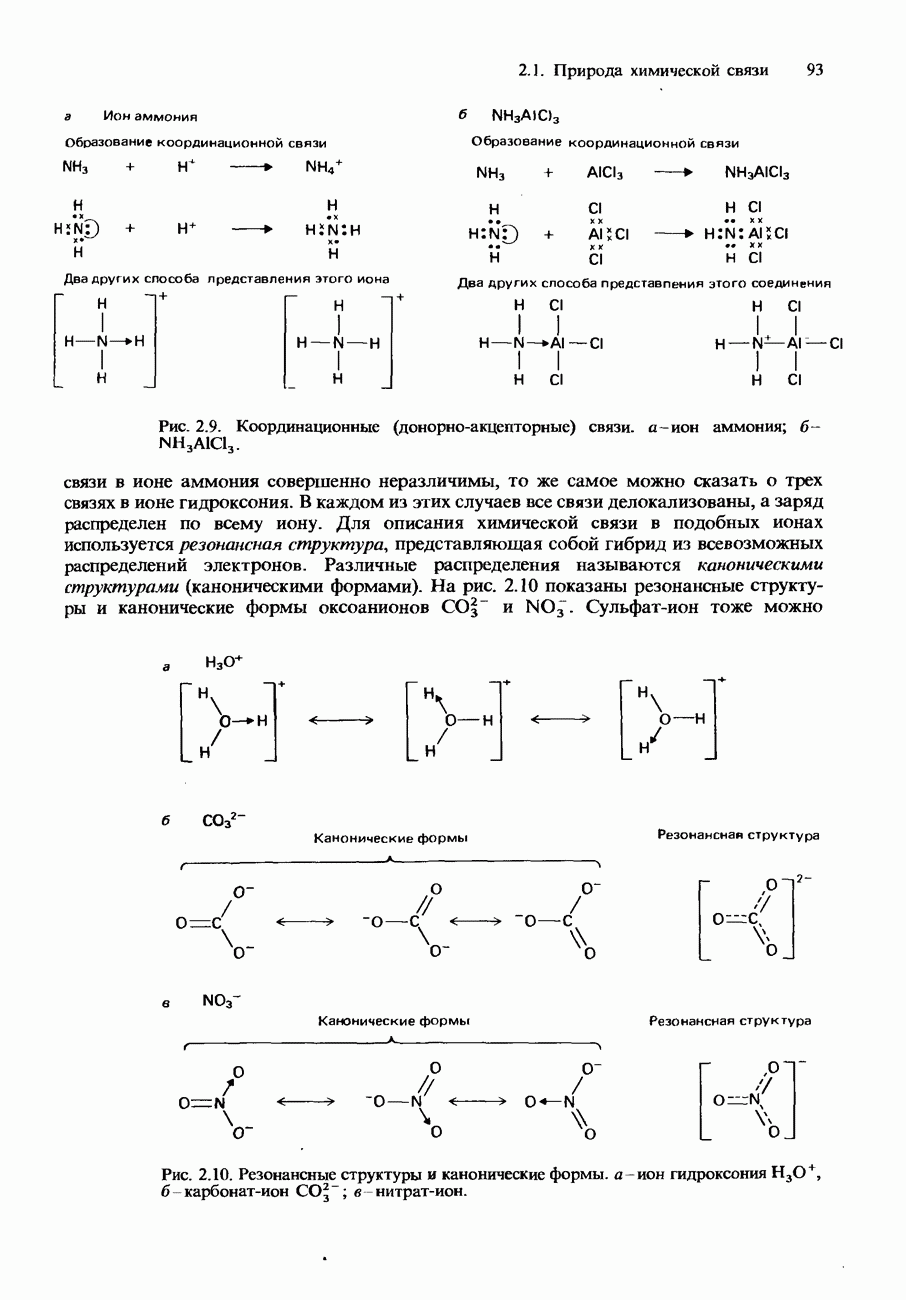
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
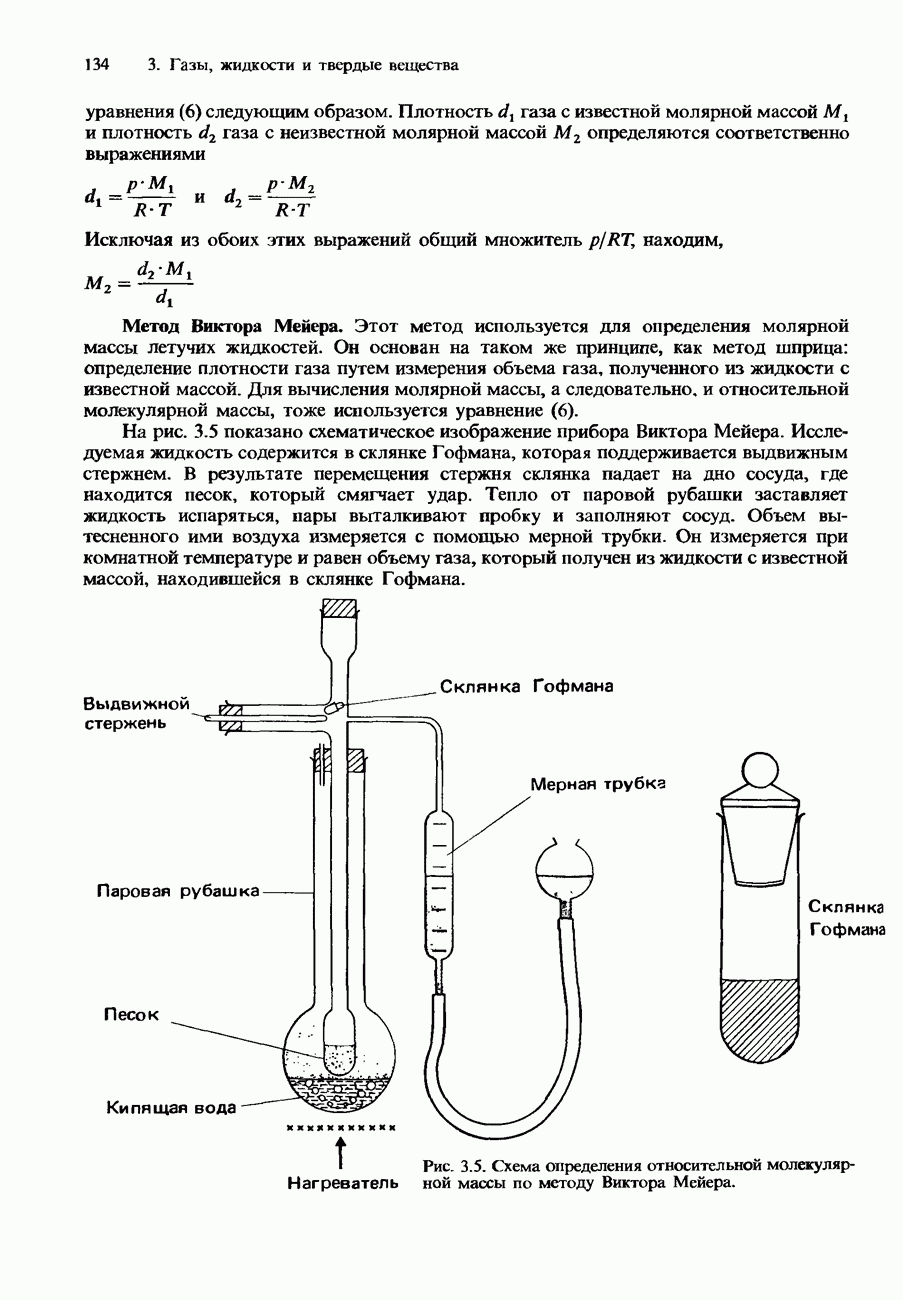
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
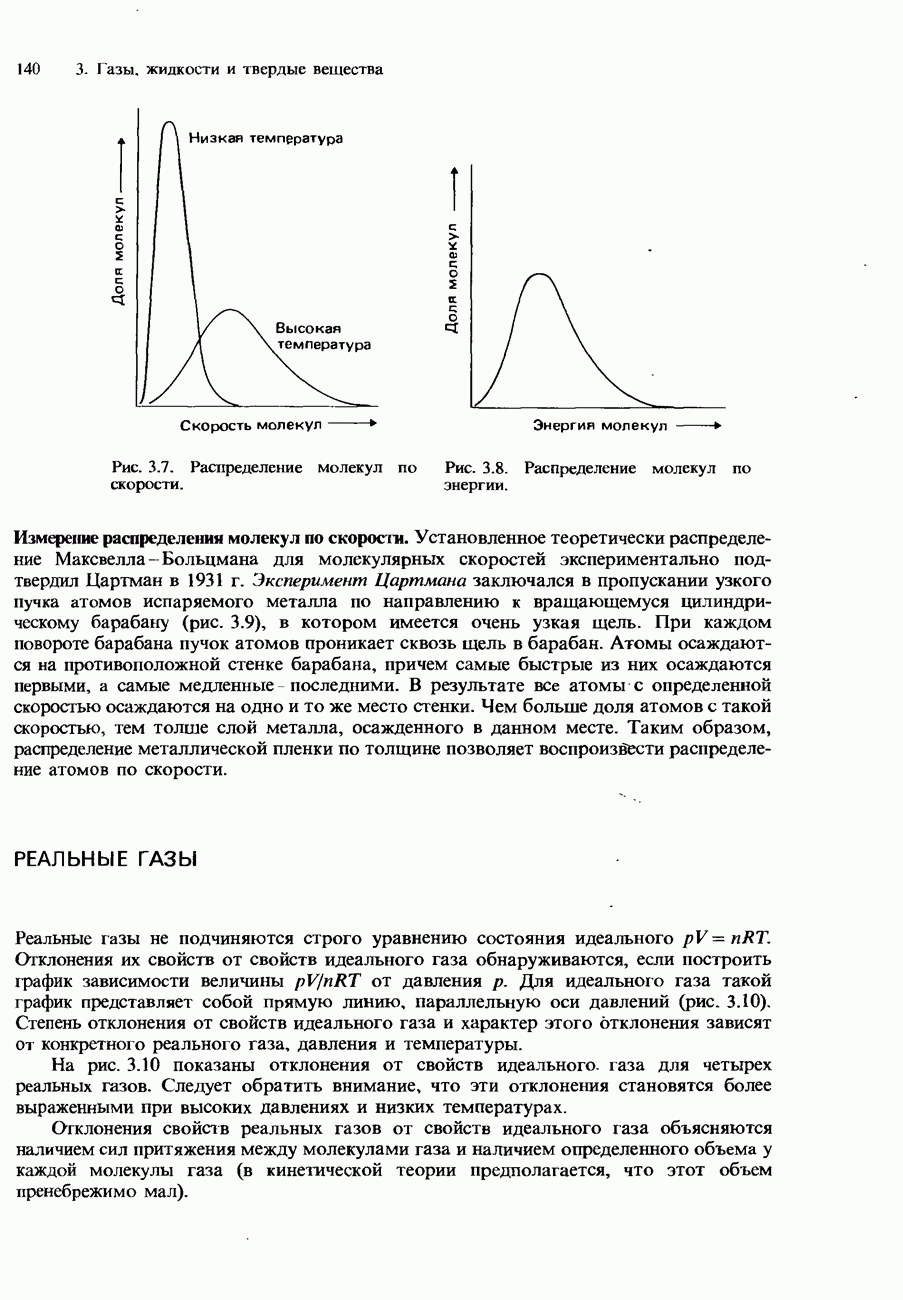
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- Скорости молекул
- Распределение Максвелла-Больцмана
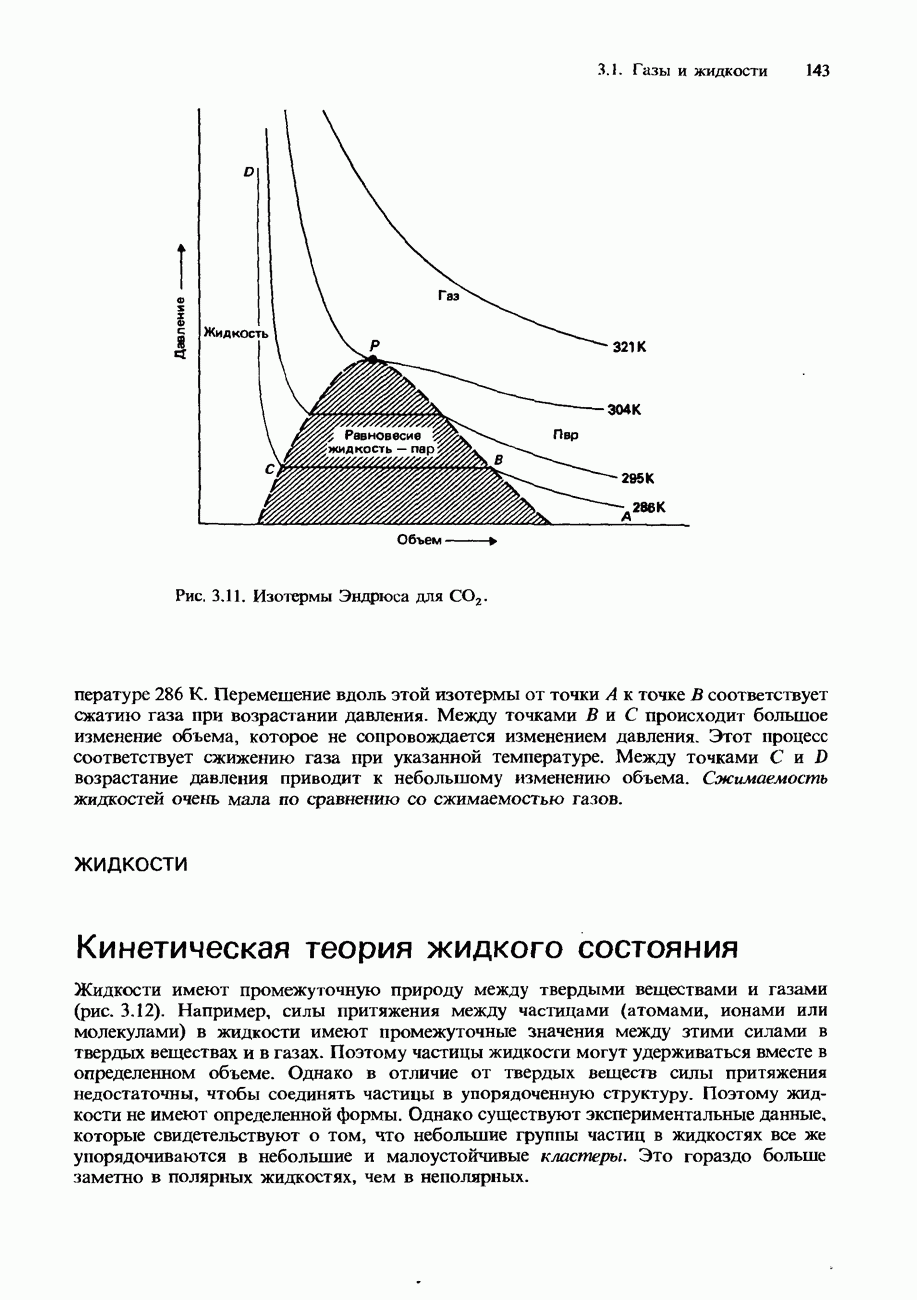
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
- Сжижение газов
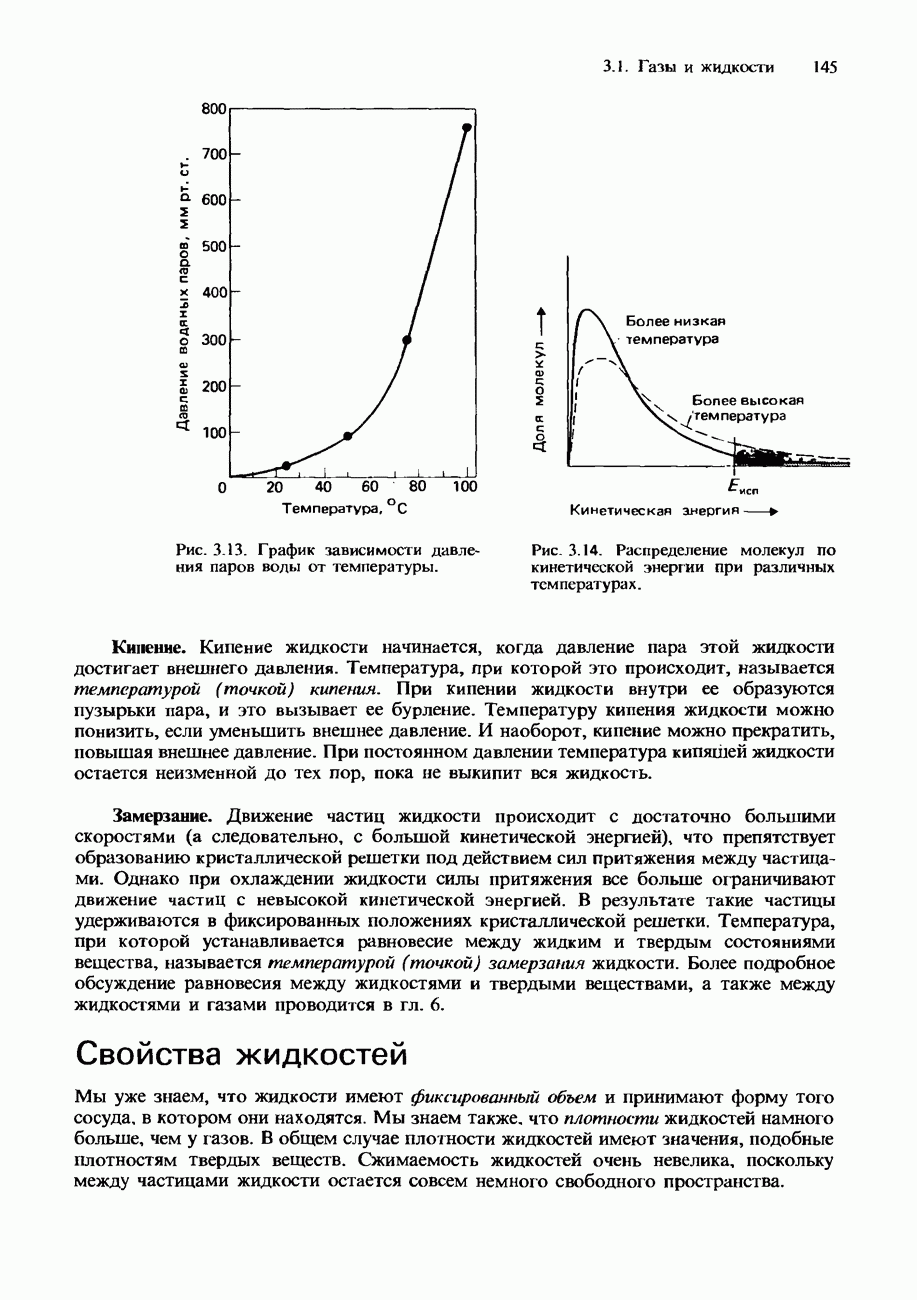
- ЖИДКОСТИ
- Свойства жидкостей
- 3.2. Твердые вещества
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
- Ионные кристаллы
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
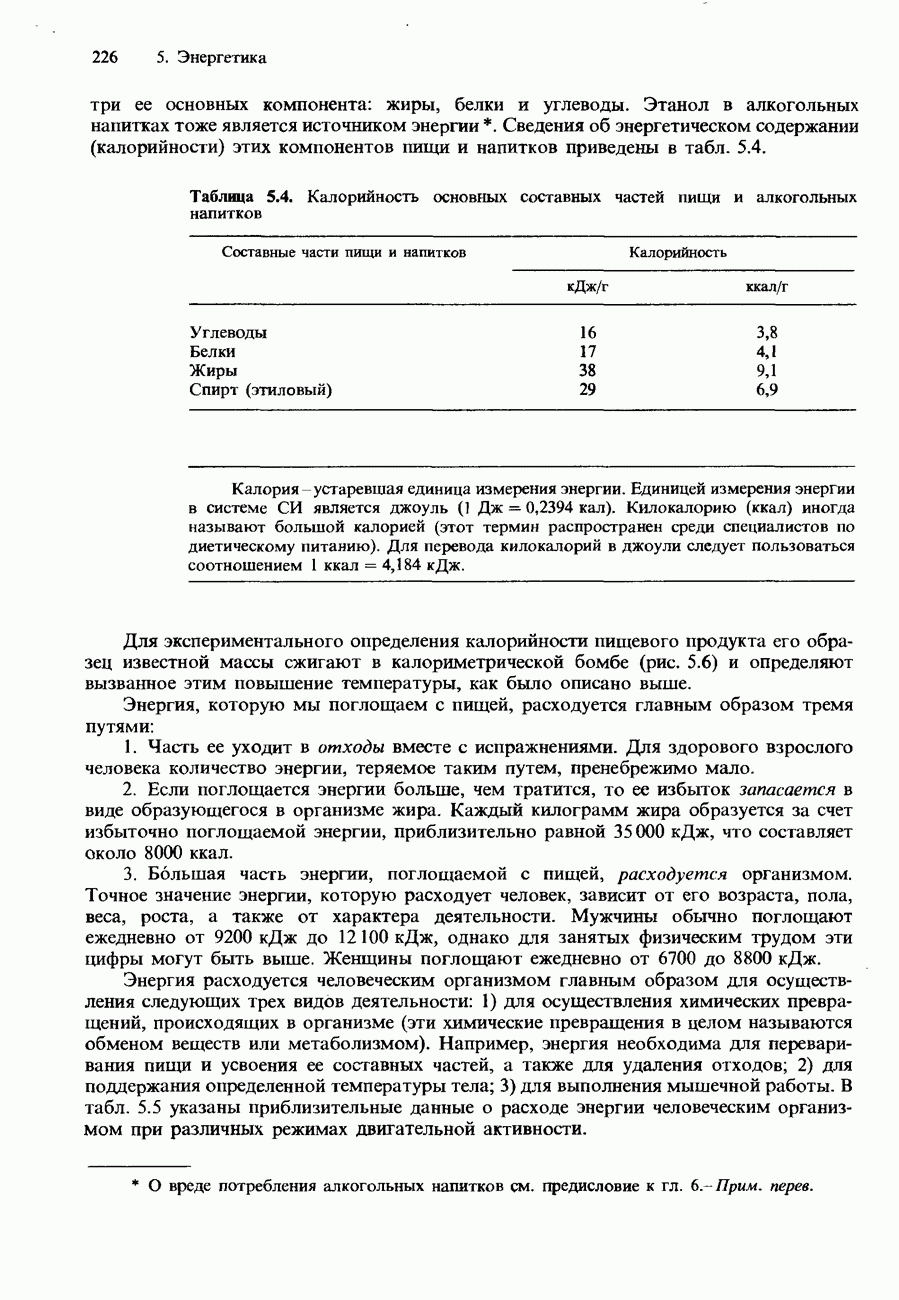
- КАЛОРИЙНОСТЬ ПИЩИ
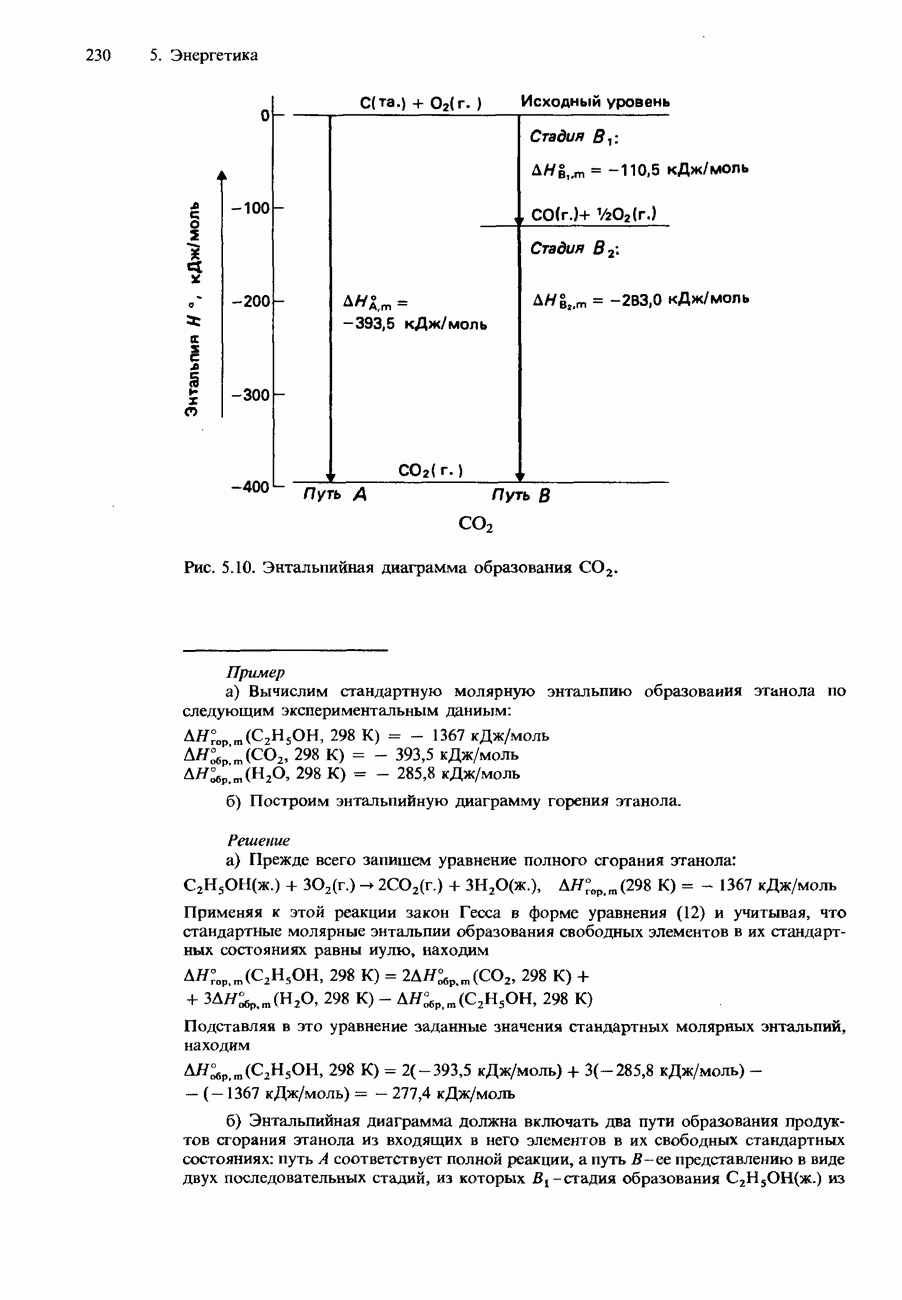
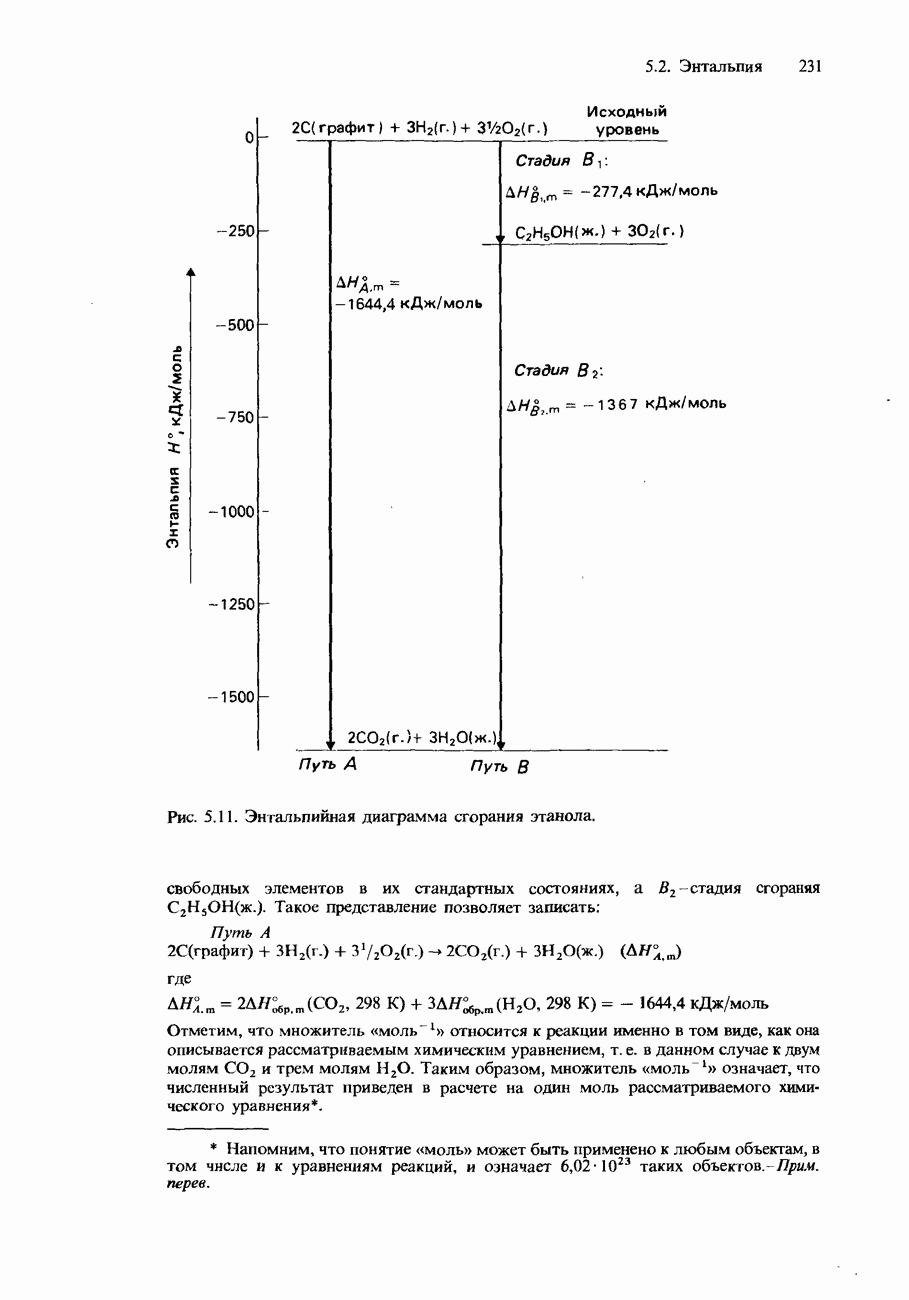
- ЗАКОН ГЕССА
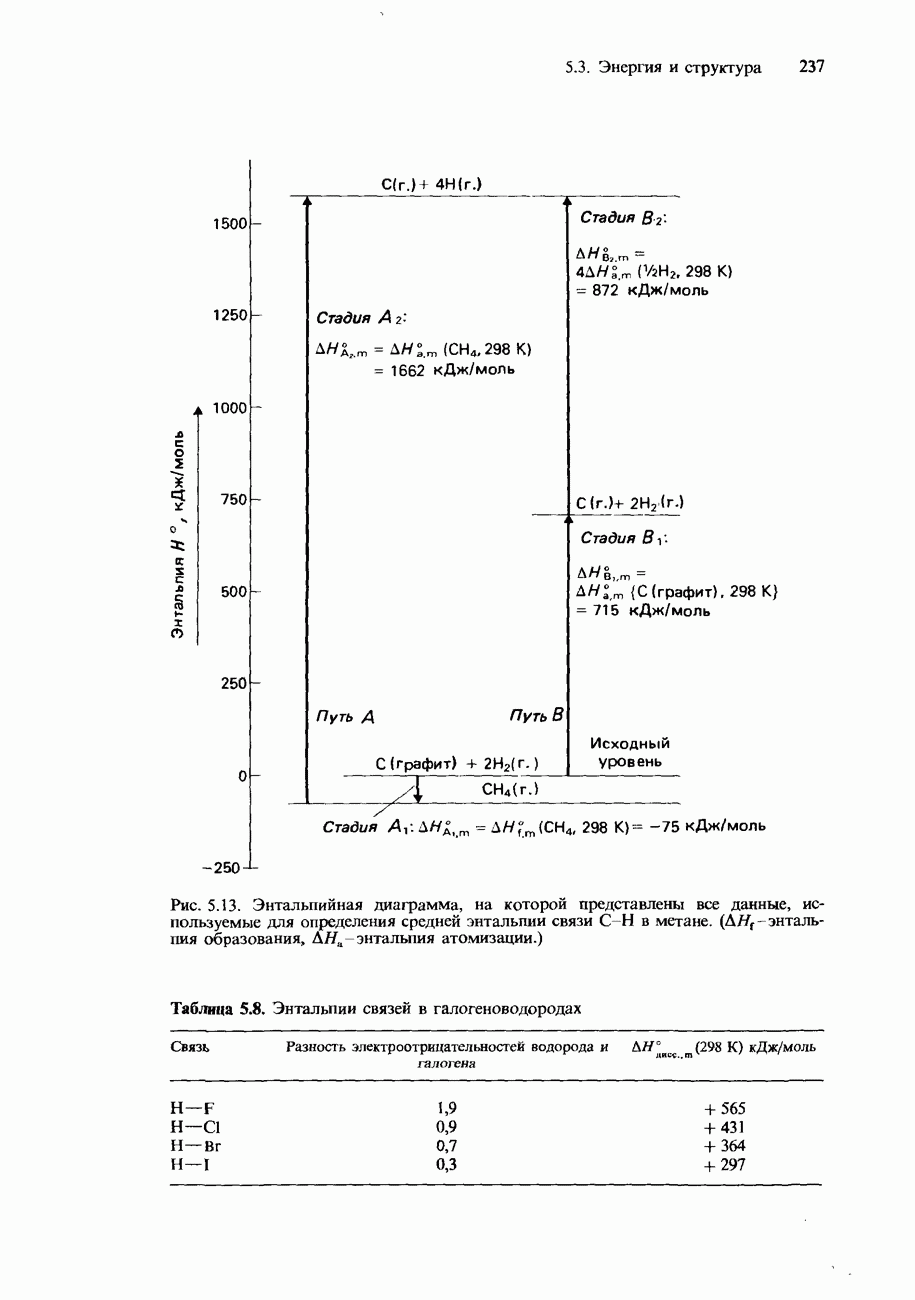
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
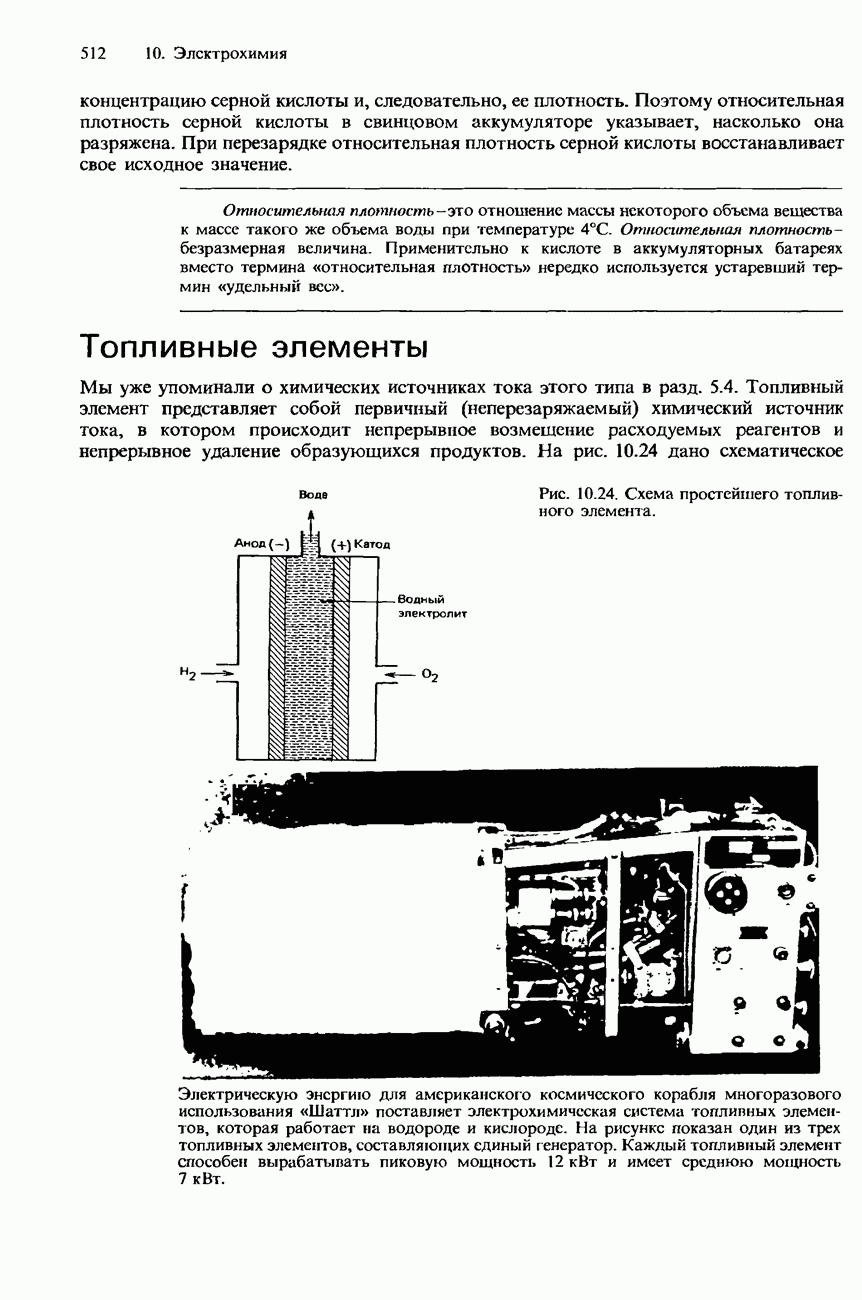
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
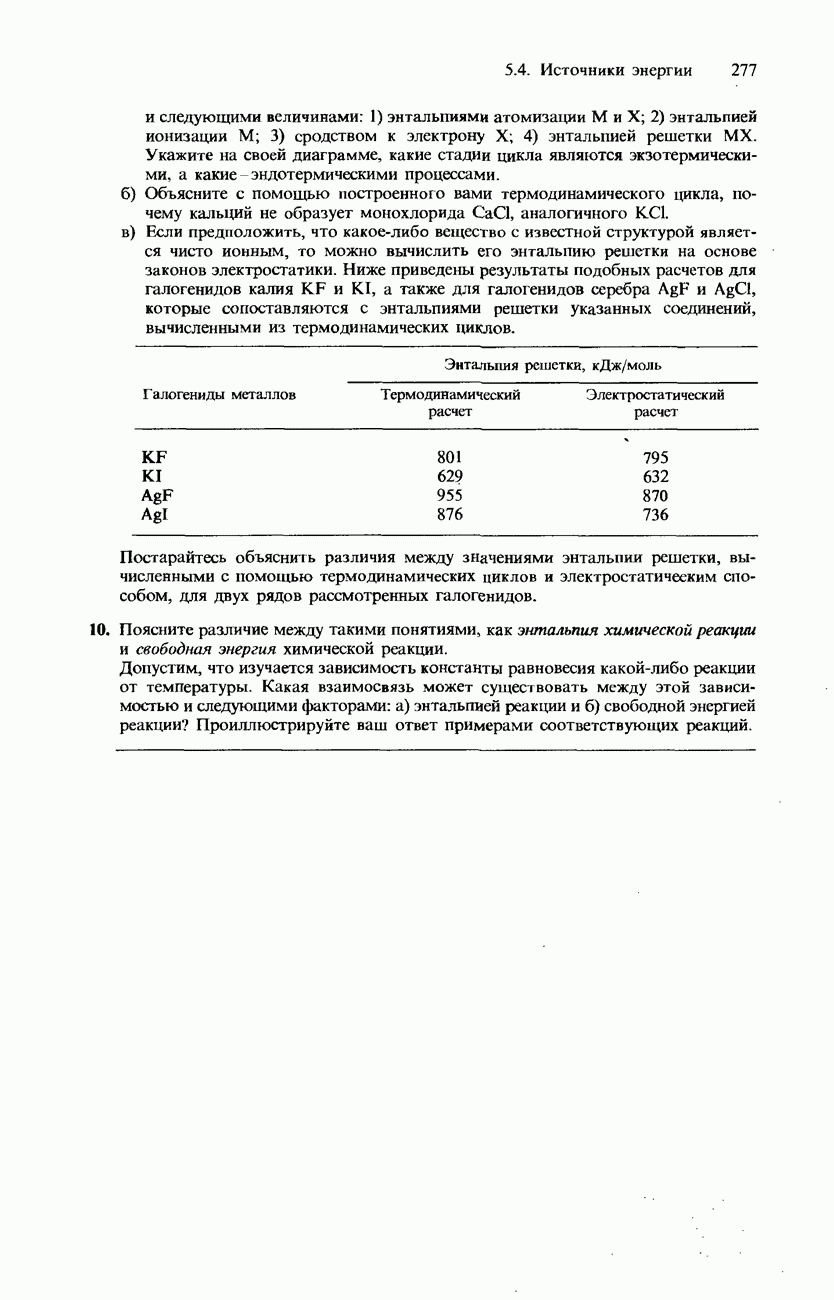
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
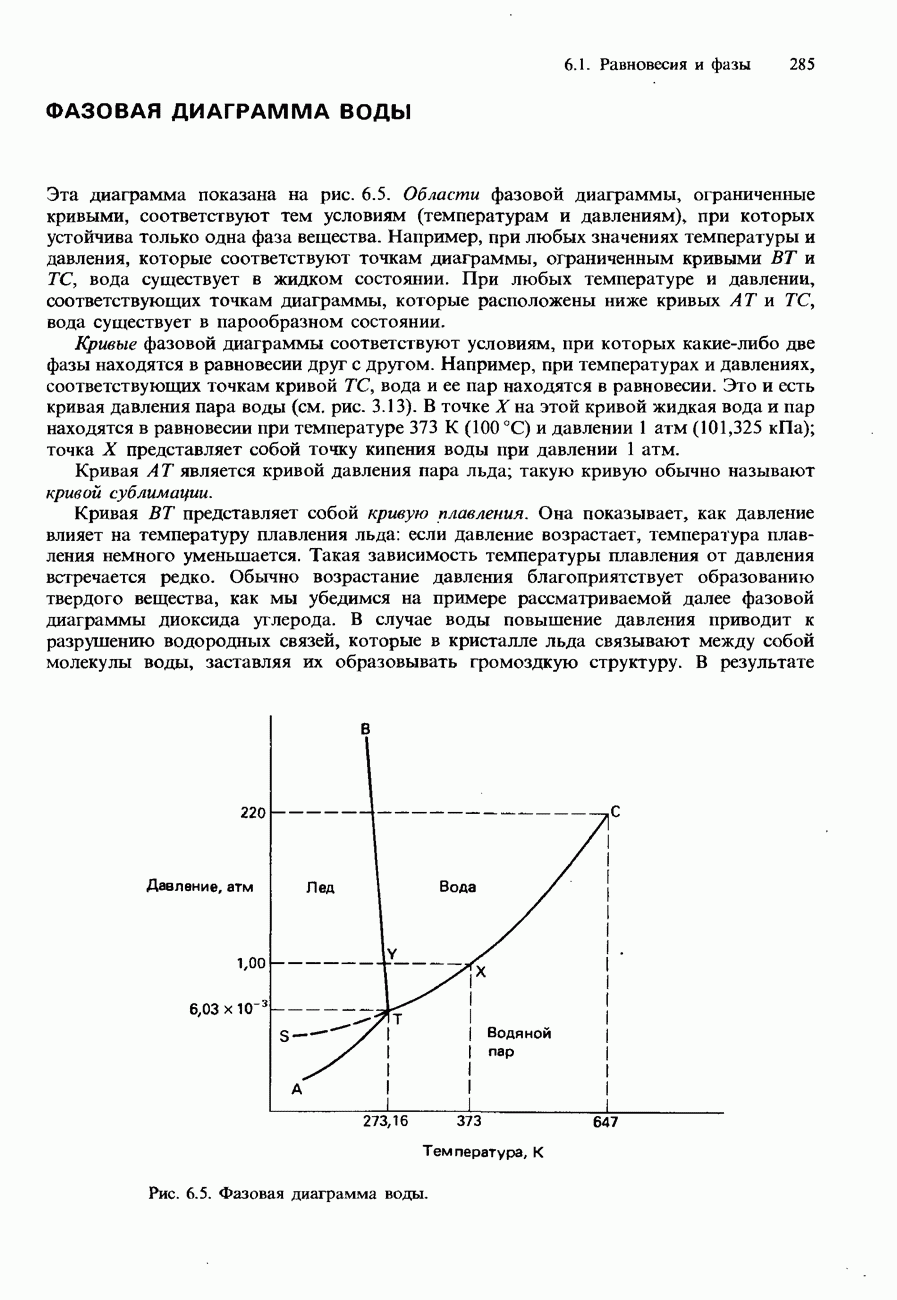
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
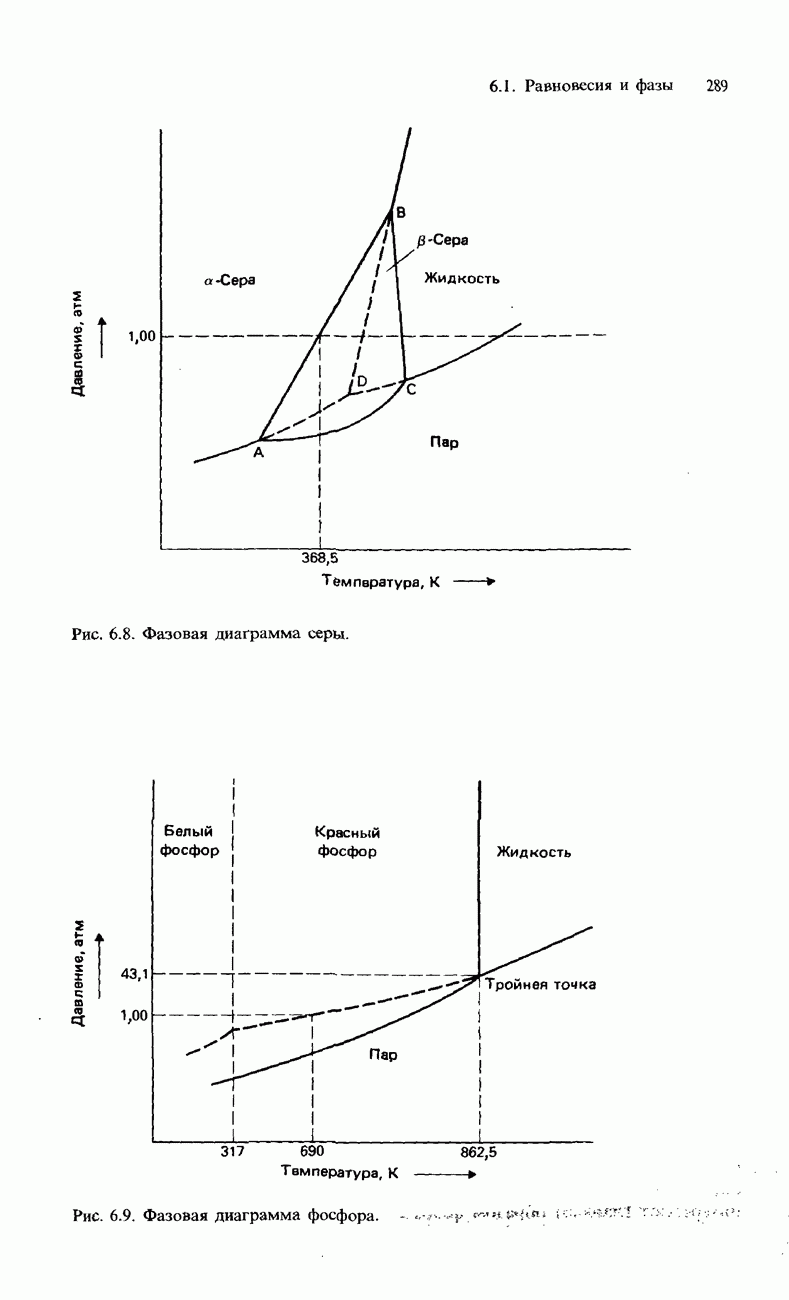
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- Фазовые диаграммы полностью смешивающихся жидкостей
- Фракционная перегонка
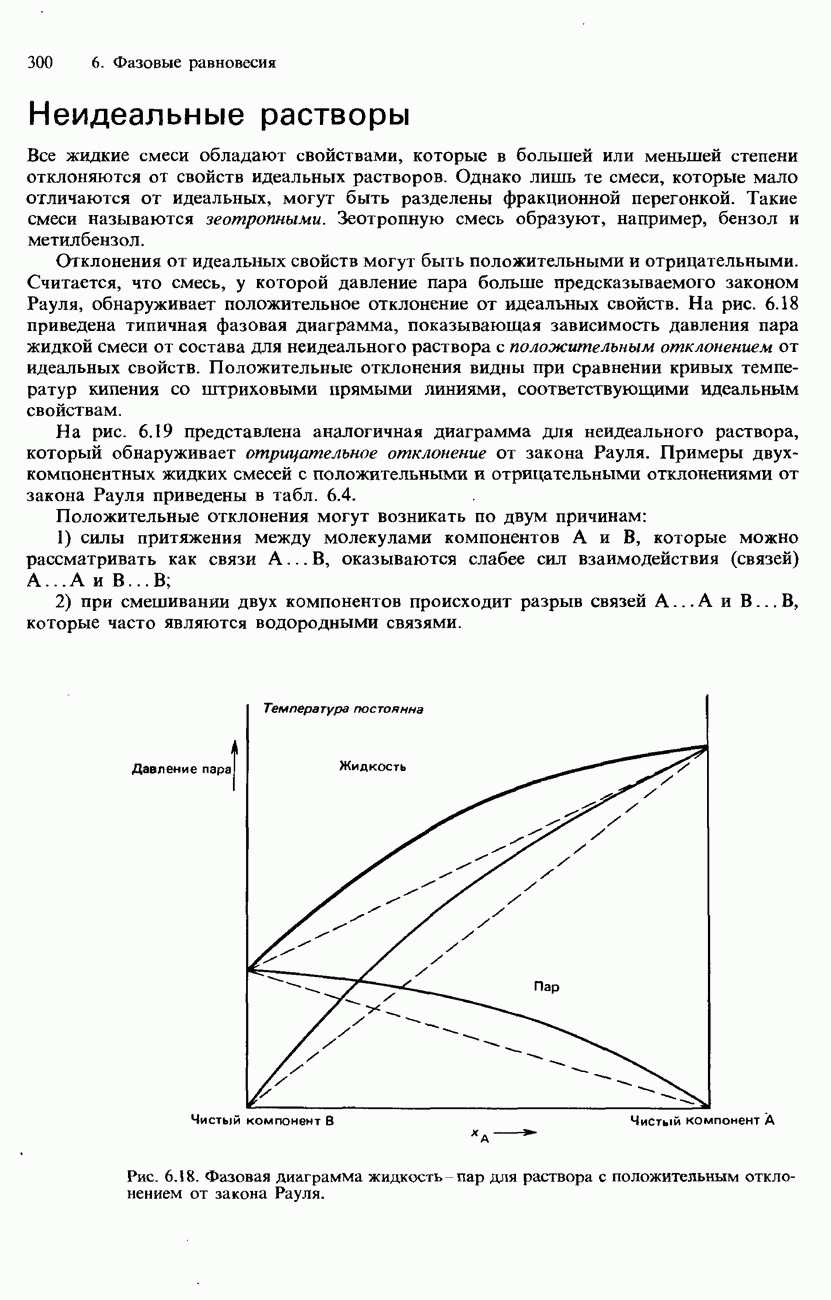
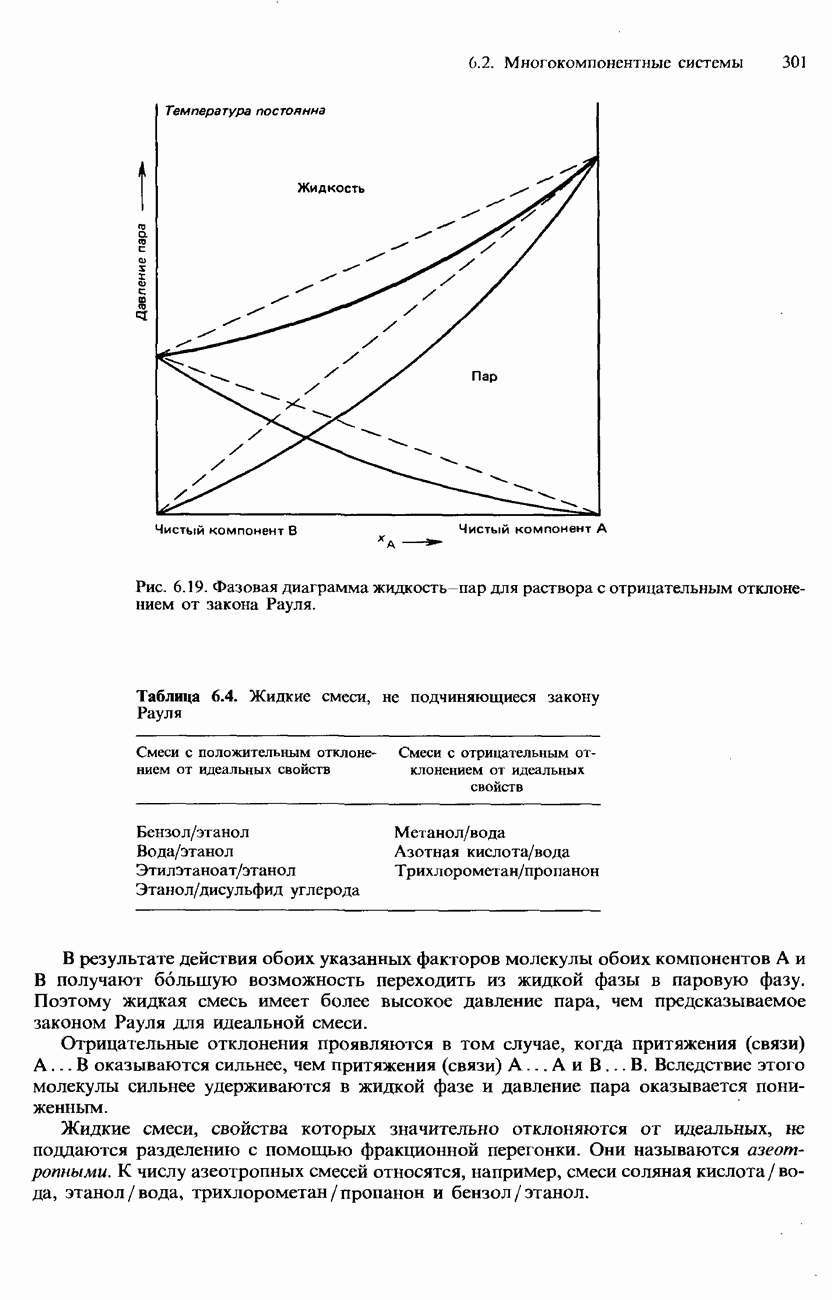
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
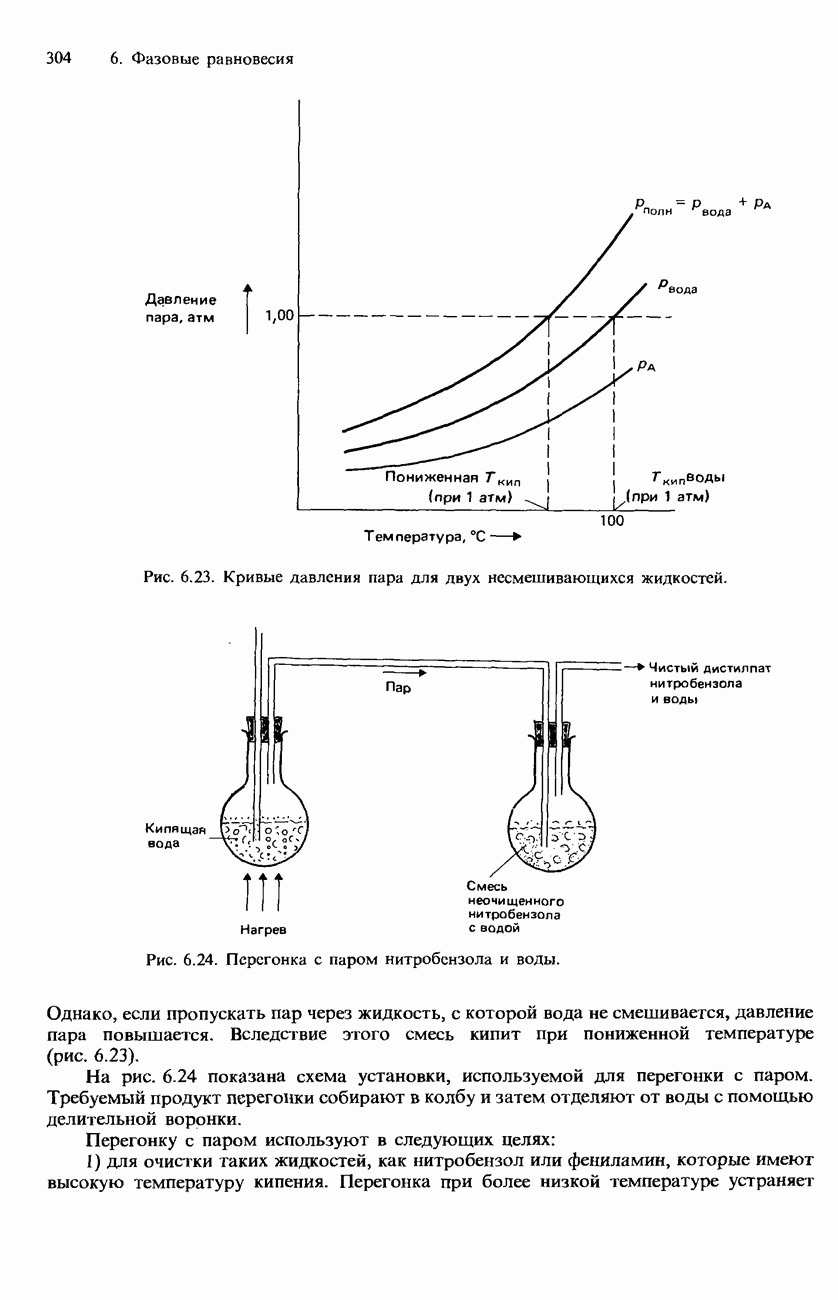
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
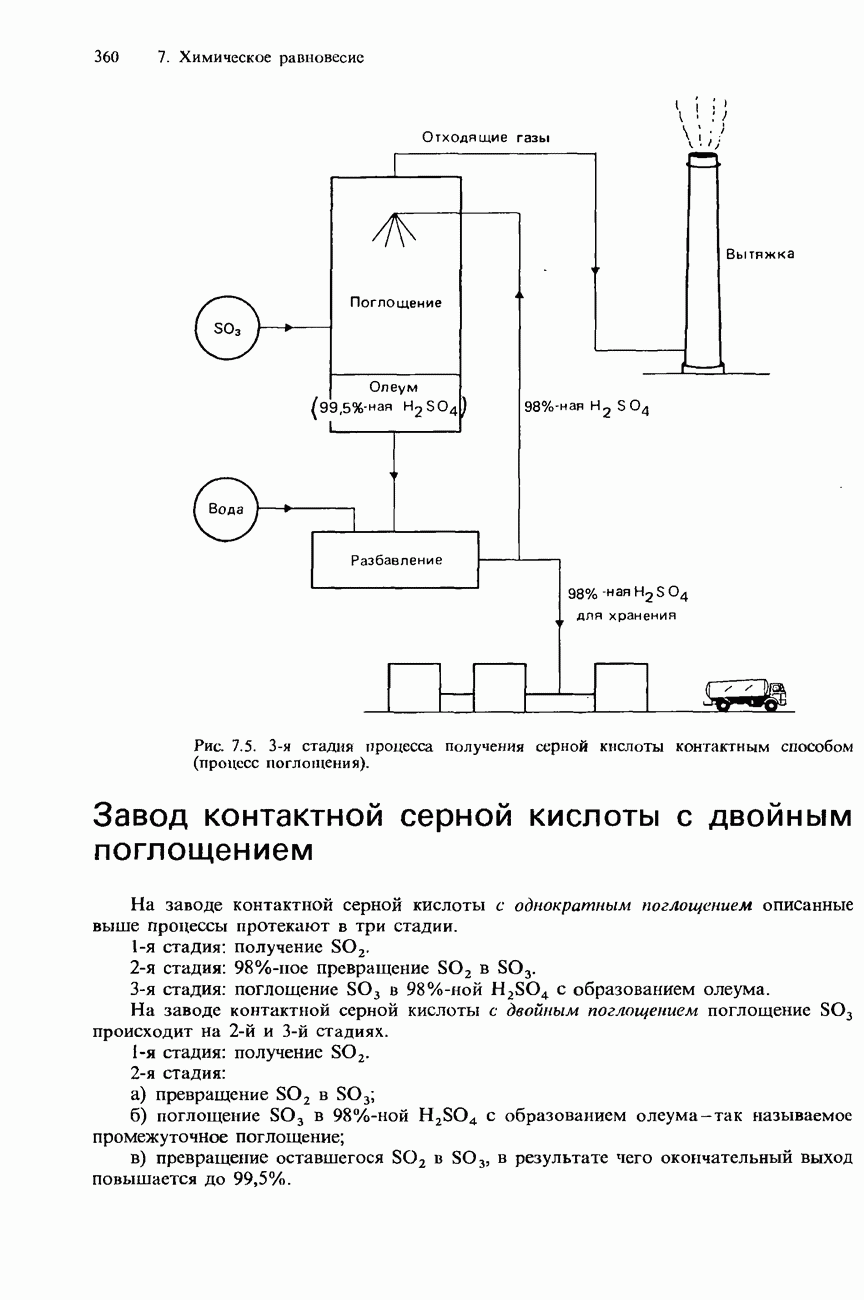
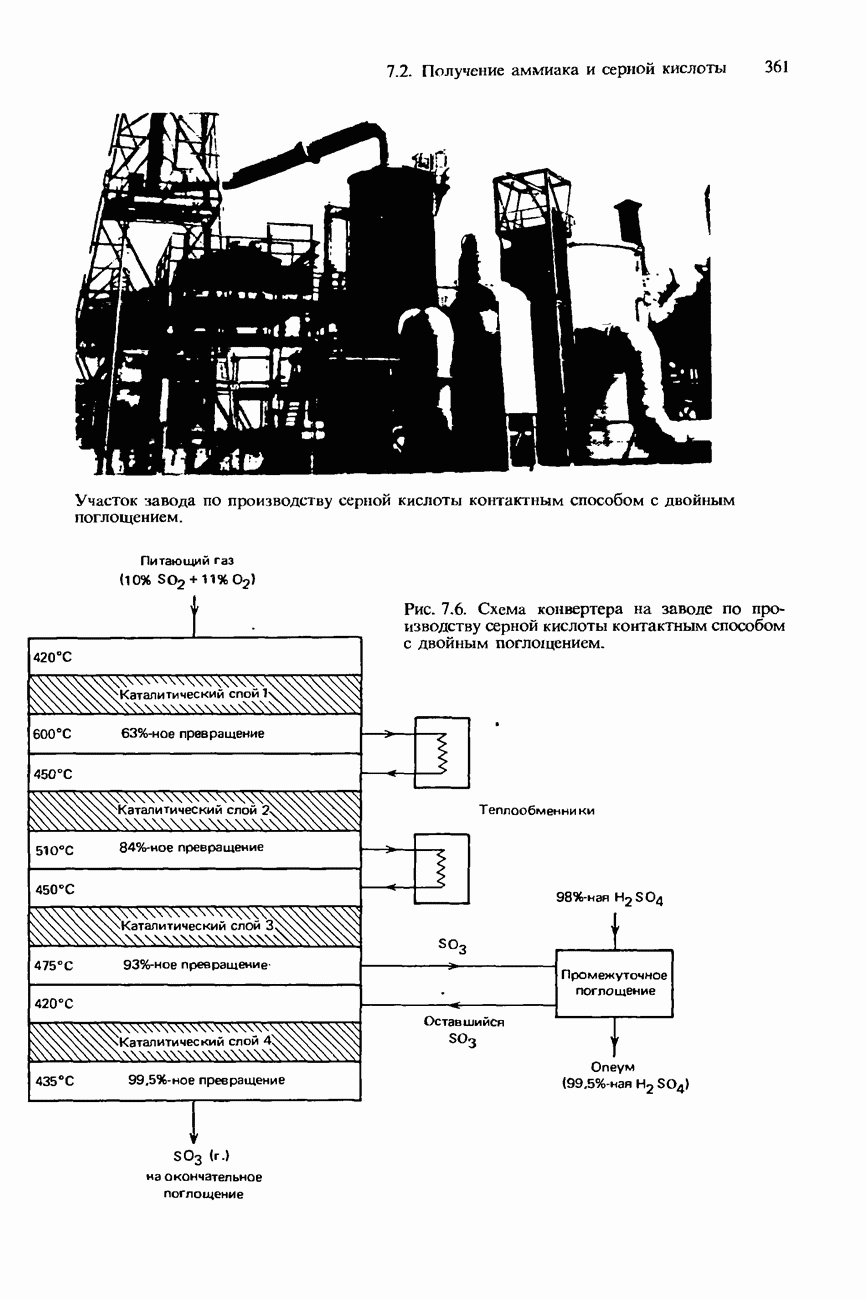
- 7.2. Получение аммиака и серной кислоты
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
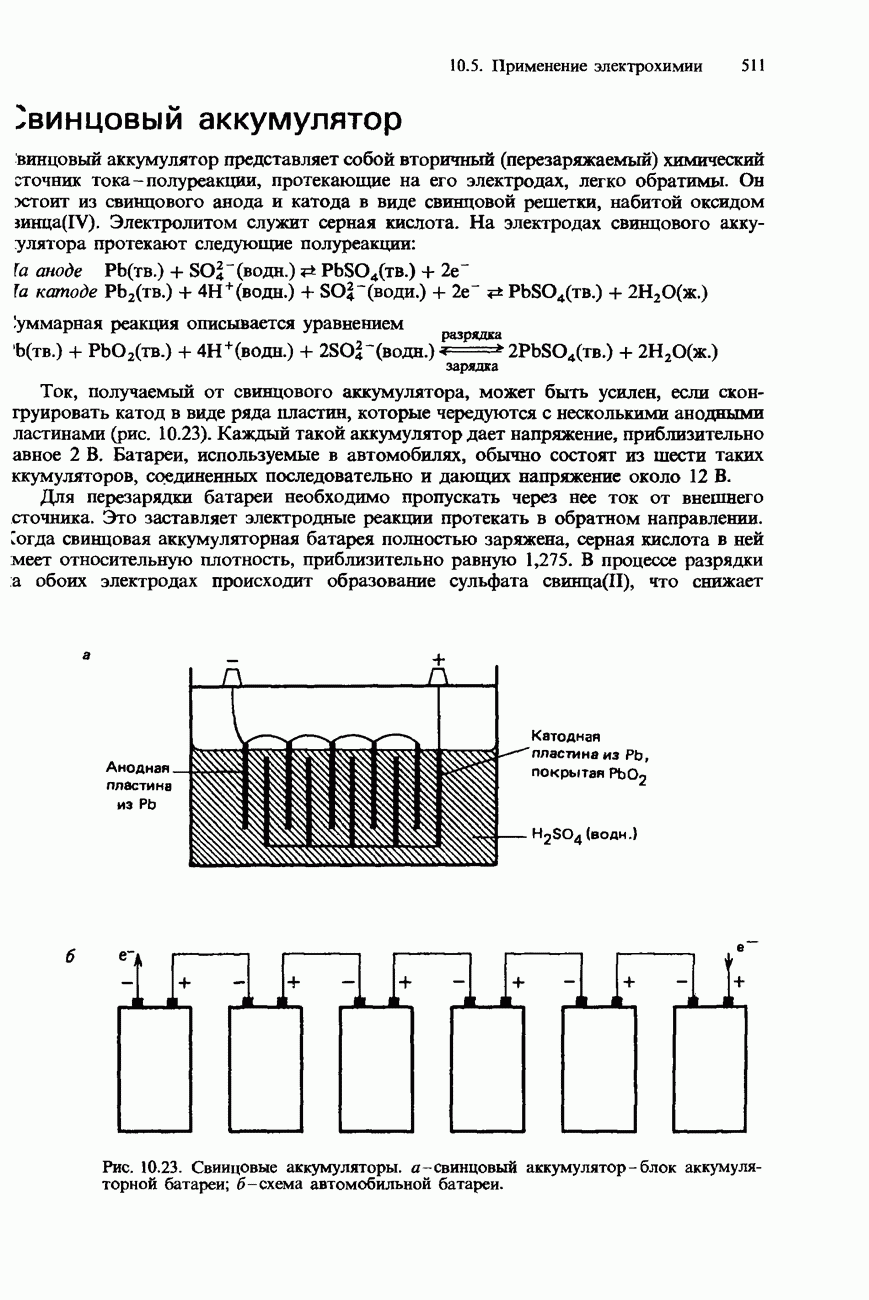
- 10.4. Химические источники тока
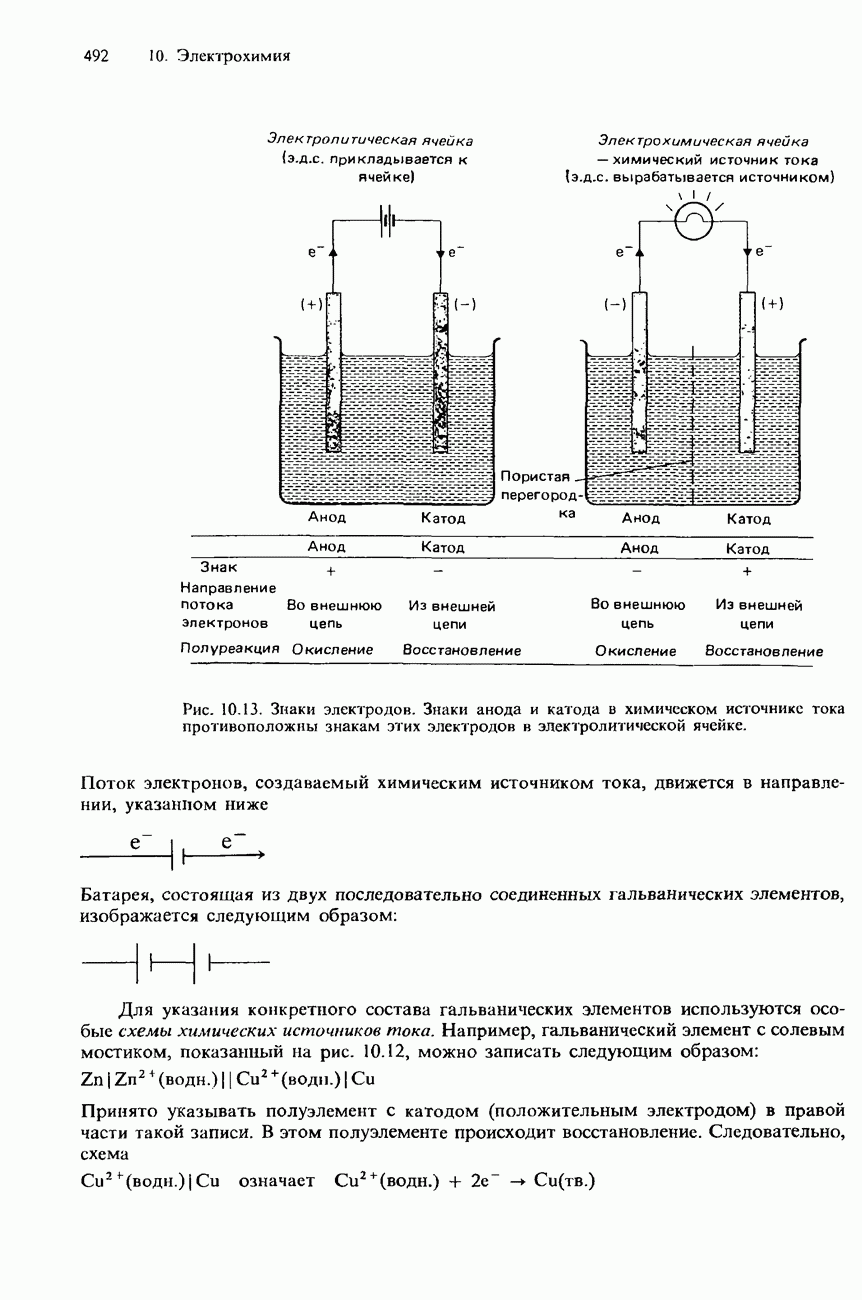
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
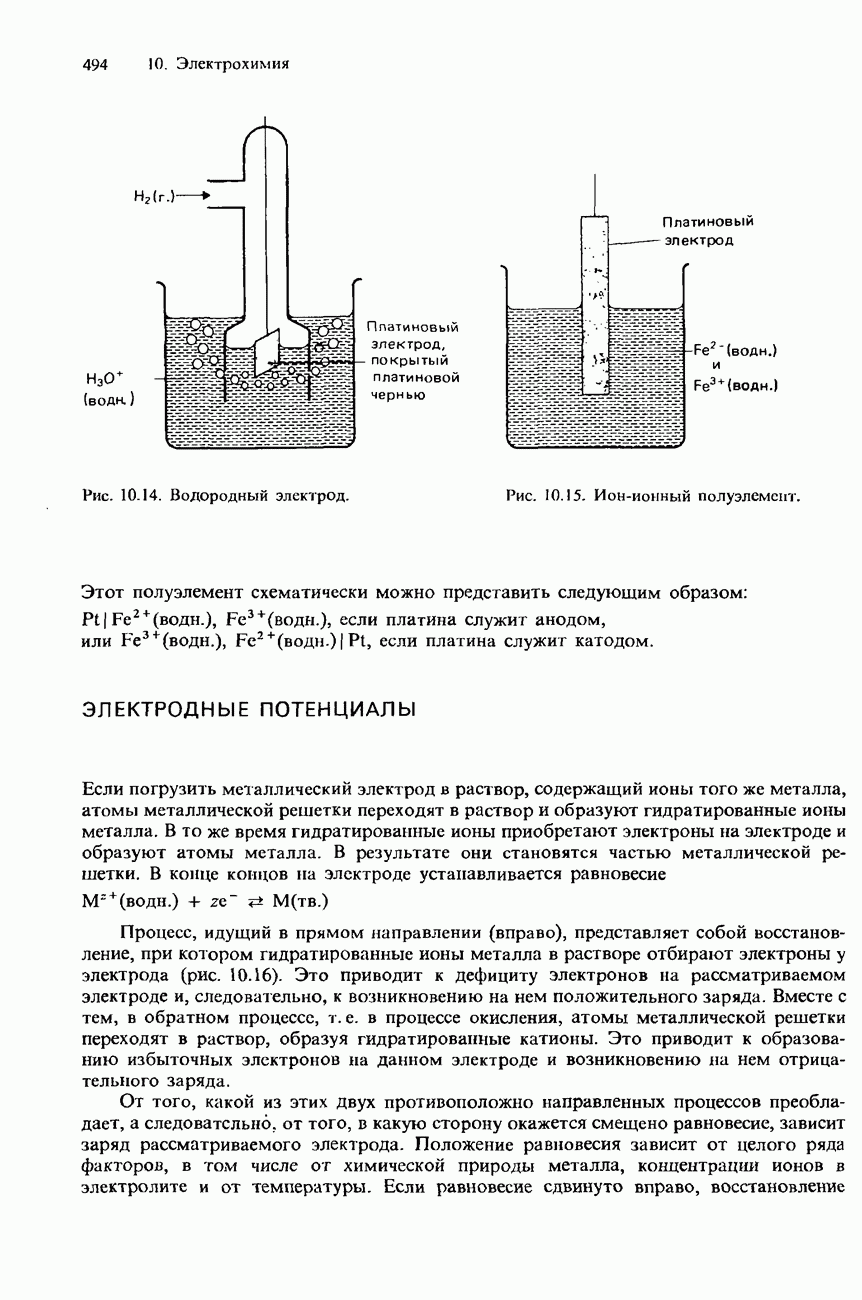
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
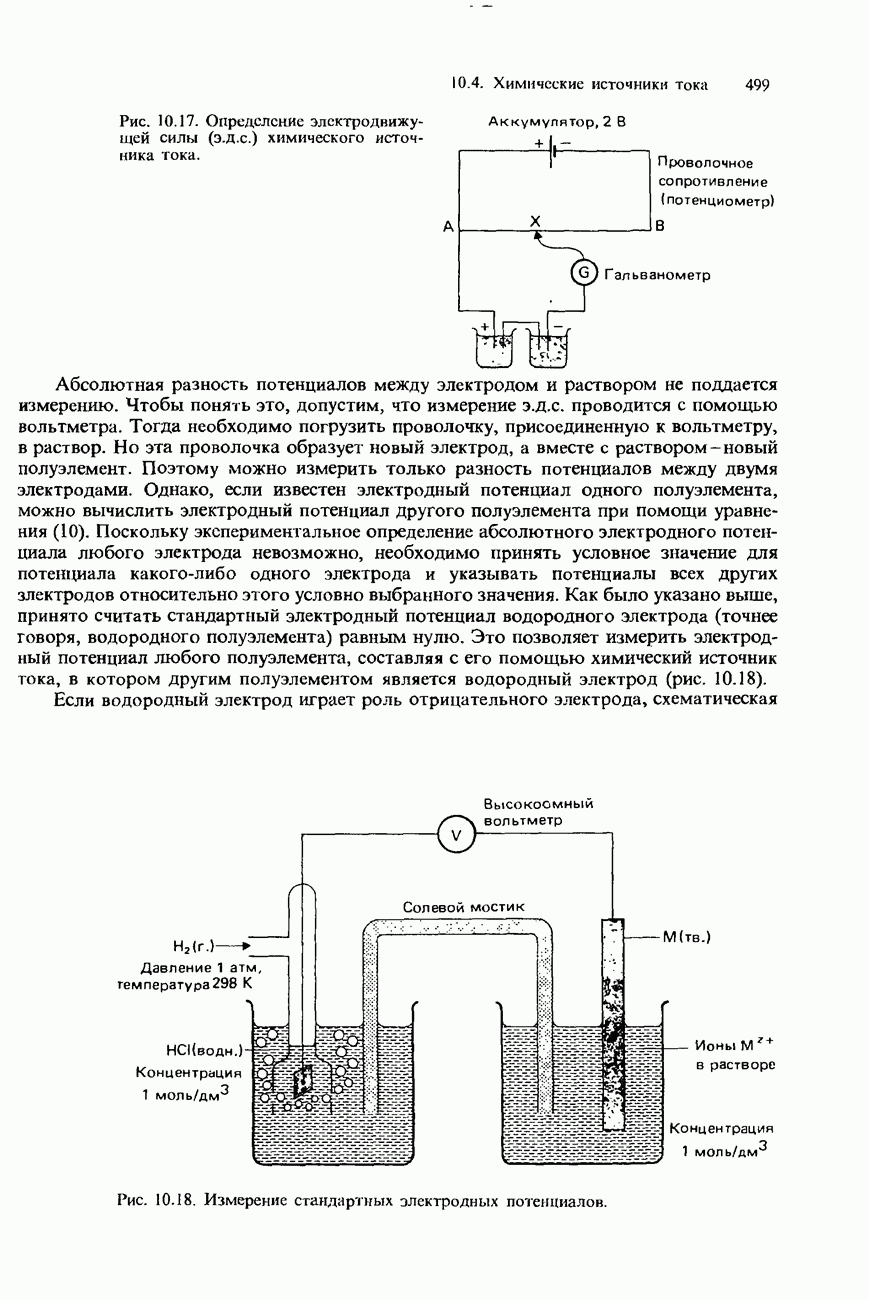
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
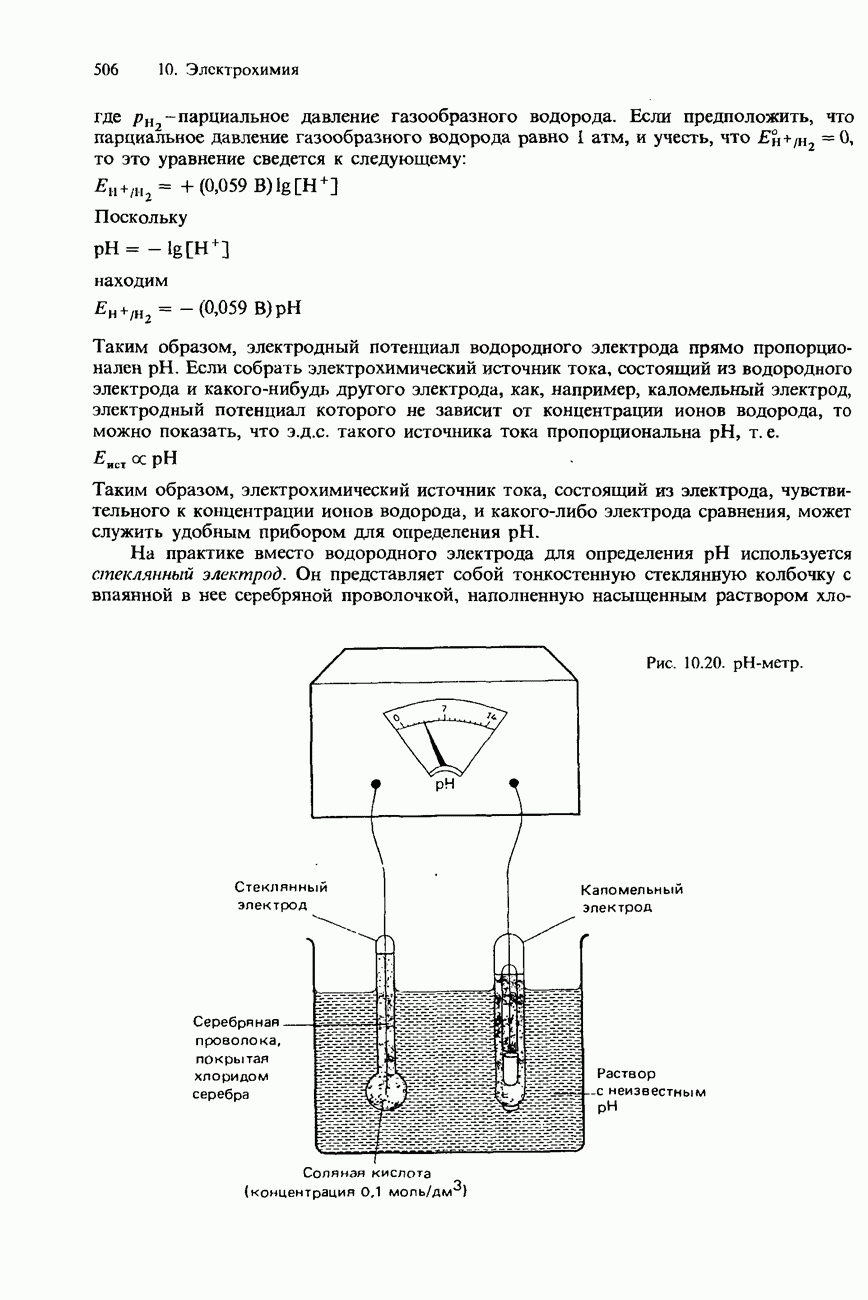
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
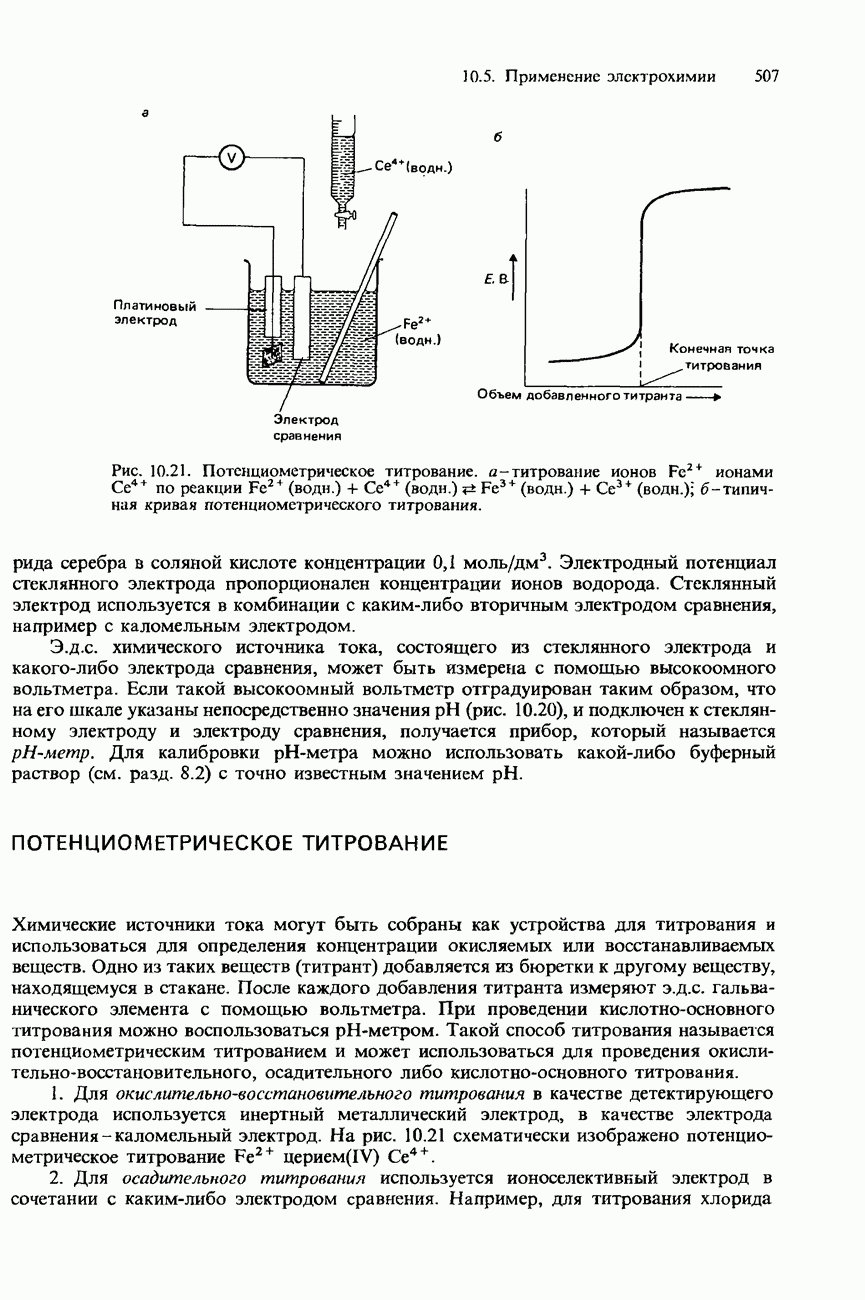
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ