| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОПРОСЫ ДЛЯ ПРОВЕРКИ
1. а) Сформулируйте закон Авогадро.
б) К какому выводу можно прийти на основании того факта, что при нормальных условиях в 22,4 дм3 диоксида углерода содержится намного больше молекул, чем 
в) 1) Сформулируйте закон эффузии Грэхема.
2) Установлено, что отношение скорости эффузии газа Y к скорости эффузии азота равно 0,366. Вычислите на этом основании относительную молекулярную массу газа 
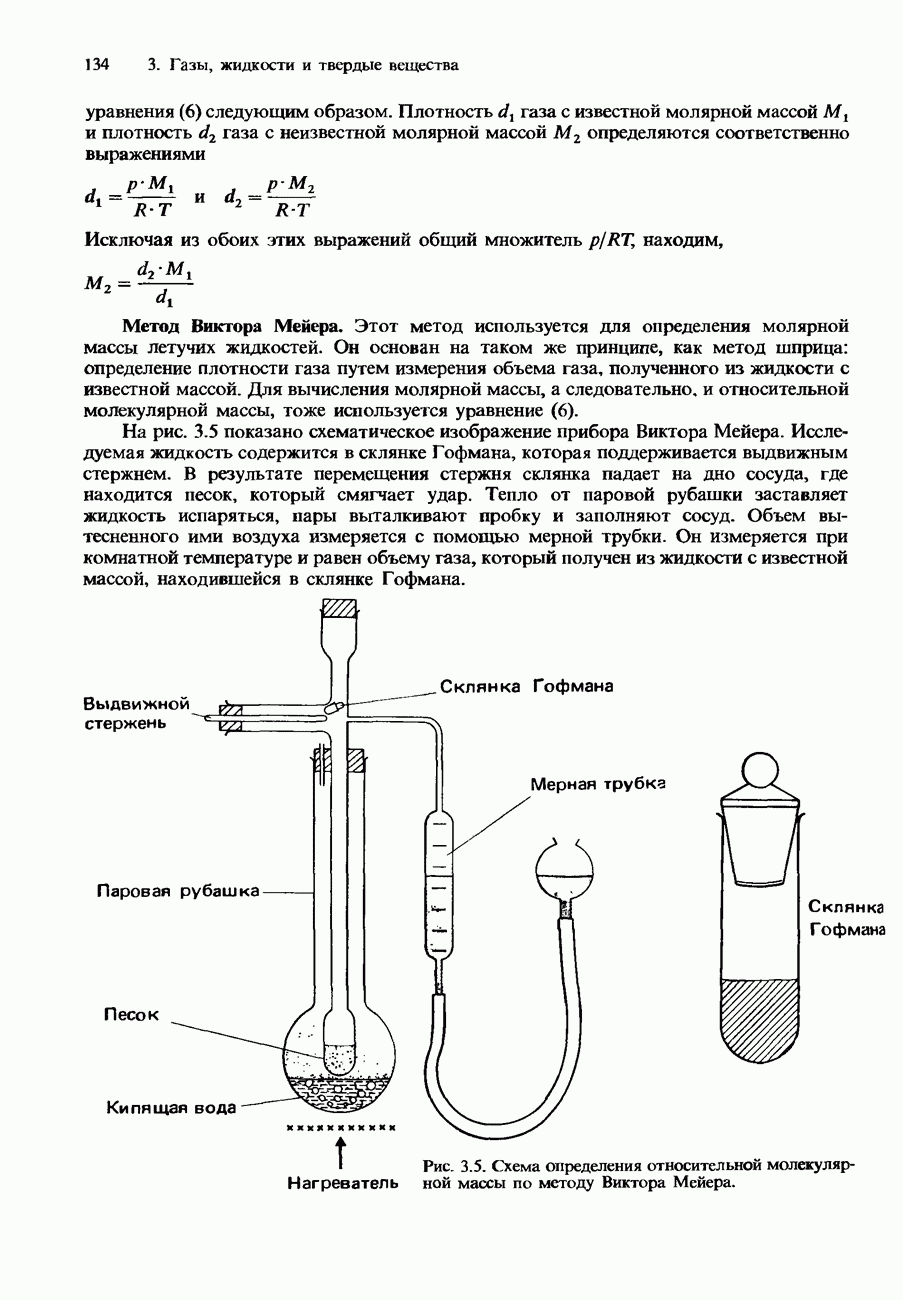
Опишите эксперимент, который позволил бы вам определить относительную молекулярную массу какого-либо газа или пара. Сформулируйте закон парциальных давлений Дальтона и покажите, как его можно вывести из уравнения состояния идеального газа.
Смесь кислорода и азота, в которой мольная доля кислорода равна 0,25, находится под давлением 1,0 атм. Вычислите парциальное давление каждого газа в этой смеси (полагая, что она обладает свойствами идеального газа).
3. а) Дайте определения терминов относительная атомная масса и относительная молекулярная масса. Имеет ли термин «относительная молекулярная масса»
такой же смысл применительно к хлориду калия, какой он имеет применительно к бензолу?
б) Какими двумя переменными определяется средняя скорость молекул идеального газа? Сформулируйте кратко, как эта скорость зависит от указанных вами переменных. (Вывод формулы не требуется.)
в) Реакция  калия (перхлората калия)
калия (перхлората калия)  с фторсульфоновой кислотой
с фторсульфоновой кислотой  приводит к выделению газа X.
приводит к выделению газа X.
1) Установлено, что 0,245 г газа X при температуре 293 К и давлении  Па занимают объем
Па занимают объем  Вычислите относительную молекулярную массу газа X с точностью до трех значащих цифр.
Вычислите относительную молекулярную массу газа X с точностью до трех значащих цифр.
2) С помощью масс-спектрометрии установлено, что газ X содержит только элементы  . Предложите молекулярную формулу для газа X.
. Предложите молекулярную формулу для газа X.
4. а) Сформулируйте закон диффузии газов Грэхема.
б) Вычислите с точностью до четырех значащих цифр отношение скорости диффузии через пористую мембрану газообразного хлороводорода, состоящего полностью из молекул  к скорости диффузии газа, состоящего полностью из молекул
к скорости диффузии газа, состоящего полностью из молекул  при условии, что оба газа находятся при одинаковой температуре и одинаковом давлении. (Для этого расчета воспользуйтесь следующими значениями относительных атомных масс изотопов:
при условии, что оба газа находятся при одинаковой температуре и одинаковом давлении. (Для этого расчета воспользуйтесь следующими значениями относительных атомных масс изотопов: 
а) 1) Воспользуйтесь основными предположениями кинетической теории газов и выведите уравнение  для идеального газа.
для идеального газа.
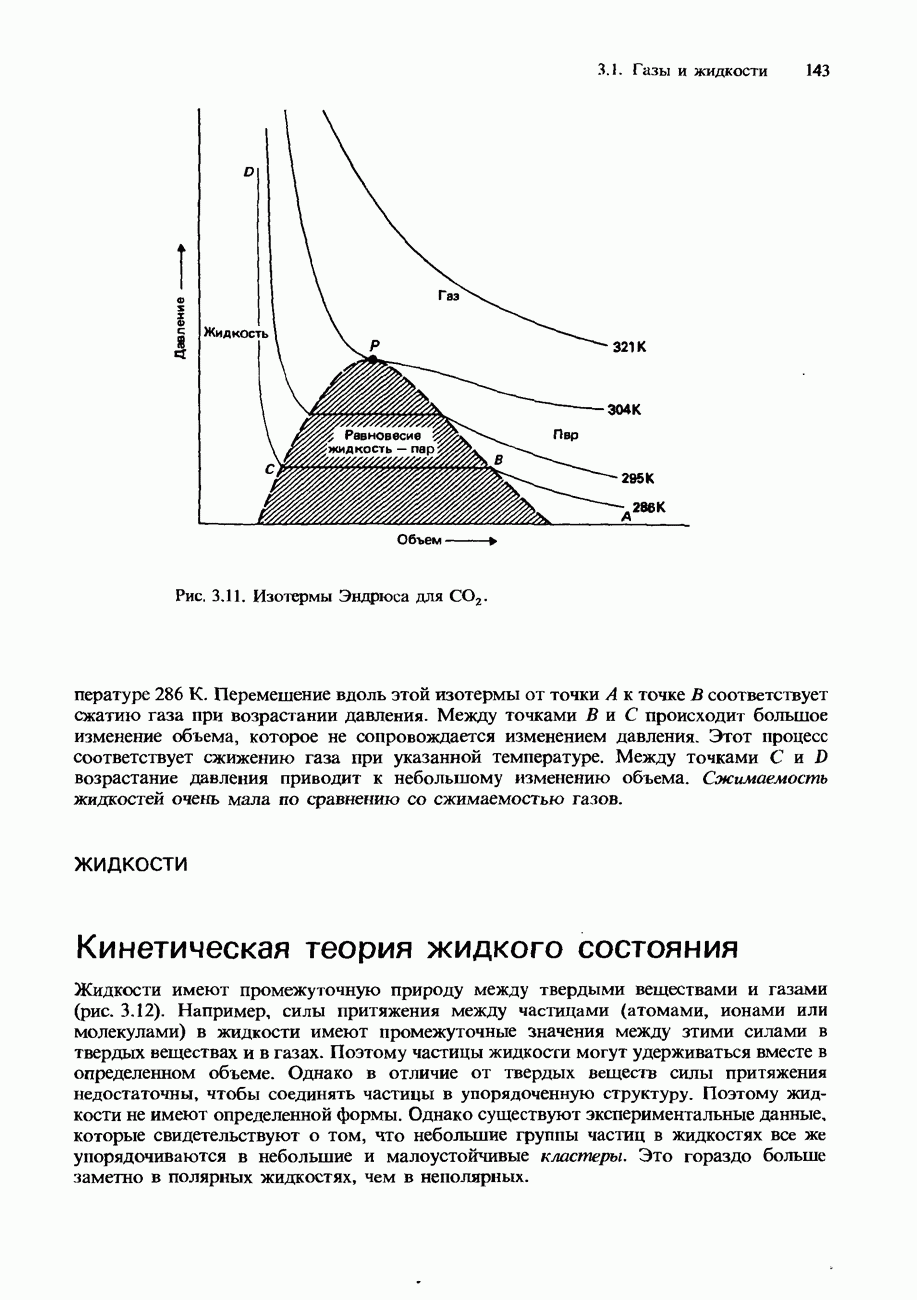
2) Какой смысл имеют термины реальный газ и критическая температура?
б) 1) Постройте график зависимости величины  от
от  для газа Y (имеющего критическую температуру 155 К) при 273 К и повышении давления от 0 до 1,013 -108 Па; укажите, при каких условиях Y ведет себя как идеальный газ, а при каких условиях - как реальный газ.
для газа Y (имеющего критическую температуру 155 К) при 273 К и повышении давления от 0 до 1,013 -108 Па; укажите, при каких условиях Y ведет себя как идеальный газ, а при каких условиях - как реальный газ.
2) Объясните различия между графиками, построенными для реального газа и для идеального газа.
3) Ожидаете ли вы увидеть какие-либо изменения на графике для реального газа при 223 и 323 К?
в) Ниже указано, какие значения имеет произведение  г газа Y при 273 К и различных давлениях
г газа Y при 273 К и различных давлениях  :
:

1) Оцените при помощи графика значение величины  нулевом давлении.
нулевом давлении.
2) При помощи выражения  определите относительную молекулярную массу газа Y.
определите относительную молекулярную массу газа Y.
6. а) Пользуясь кинетическими представлениями о веществе, объясните следующие явления:
1) плавление твердого вещества;
2) испарение жидкости;
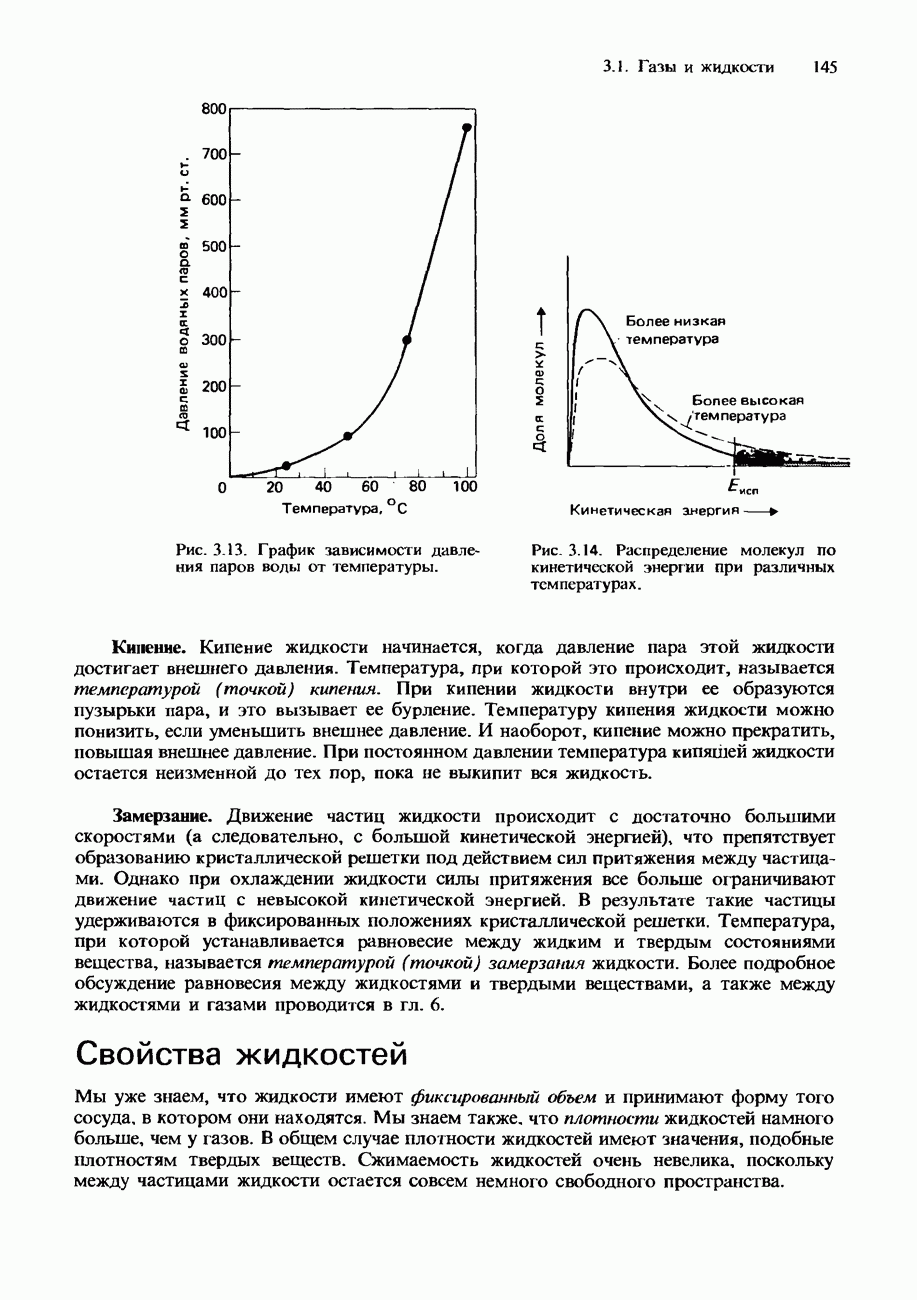
3) существование давления насыщенных паров над жидкостью.
б) 1) Вычислите значение газовой постоянной R (с указанием единиц измерения) исходя из того, что плотность аргона при нормальных условиях равна 
Воспользуйтесь полученным вами в п. (6-1) значением и оцените среднюю кинетическую энергию атома аргона при 273 К исходя из того, что для моля газа суммарная кинетическая энергия молекул газа равна 
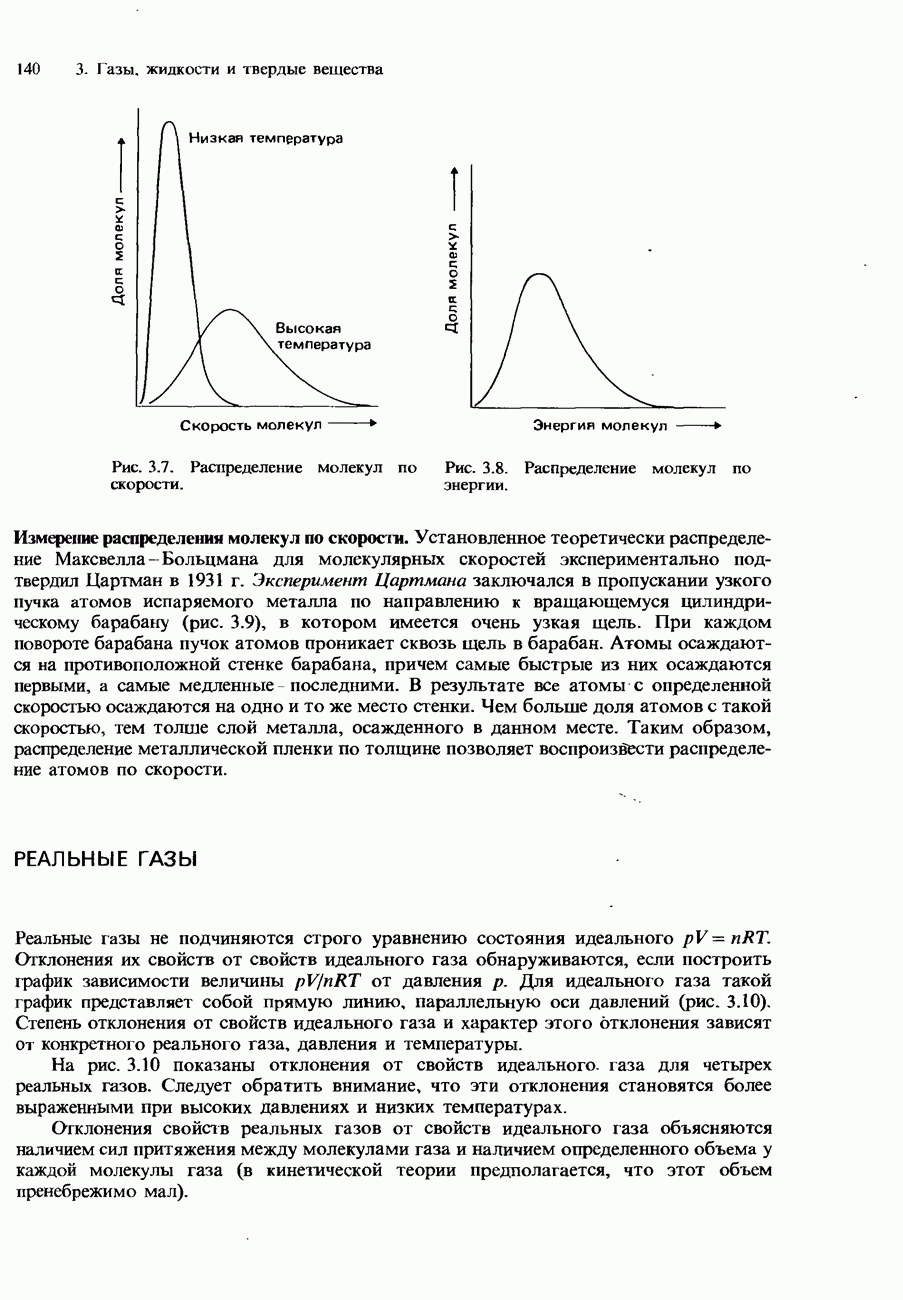
3) Покажите в графической форме, как изменяется распределение по кинетической энергии для молекул в образце газообразного аргона при повышении температуры газа. Сформулируйте закономерность, которой подчиняется площадь под каждой из нарисованных вами кривых.
7. а) 5 г вещества R (с температурой кипения 40 °С) занимают объем  при
при
50 °С и давлении 102,0 кПа.
1) Кратко опишите эксперимент, который необходимо провести для получения этих данных в лабораторных условиях.
2) Вычислите относительную молекулярную массу соединения 
б) Критическая температура бутана равна 425 К, а его критическое давление равно  кПа.
кПа.
Какой смысл имеют эти данные? Объясните, почему бутан удобно хранить в виде жидкости, а метан-неудобно?
в) Некоторое соединение обнаруживает значительные отклонения от свойств идеального газа при нормальных температуре и давлении.
1) Запишите уравнение состояния идеального газа и поясните смысл каждой величины, входящей в это уравнение.
2) Какие изменения температуры и давления должны привести к еще большим отклонениям от свойств идеального газа? Поясните, какую роль должны играть эти изменения.
3) Укажите, какие изменения внес Ван-дер-Ваальс в уравнение состояния идеального газа, чтобы учесть подобные отклонения.
4) Какие выводы о внутримолекулярных и межмолекулярных связях в рассматриваемом соединении при нормальных температуре и давлении позволяют объяснить наблюдаемые отклонения его свойств от свойств идеального газа?
8. а) Кратко перечислите важнейшие свойства рентгеновских лучей и кристаллов, которые позволяют использовать рентгеновские лучи для определения структуры кристаллов.
б) Опишите при помощи схематического рисунка структуру какого-либо кристалла, имеющего ионную решетку и обладающего заметной растворимостью в воде. Кратко объясните: 1) чем отличаются силы, удерживающие эту решетку в единое целое, от сил, обусловливающих целостность кристаллической решетки алмаза, 2) почему выбранный вами ионный кристалл растворяется в воде, а алмаз не растворяется.
в) Кристаллы металлической меди имеют кубическую элементарную ячейку, в которой находятся четыре атома меди. При помощи дифракции рентгеновских лучей установлено, что длина ребра этой элементарной ячейки равна  . Плотность меди равна 8920 кг/м3 (8,920 г/см3), а ее относительная атомная масса равна 63,5. Вычислите на основании этих данных постоянную Авогадро.
. Плотность меди равна 8920 кг/м3 (8,920 г/см3), а ее относительная атомная масса равна 63,5. Вычислите на основании этих данных постоянную Авогадро.
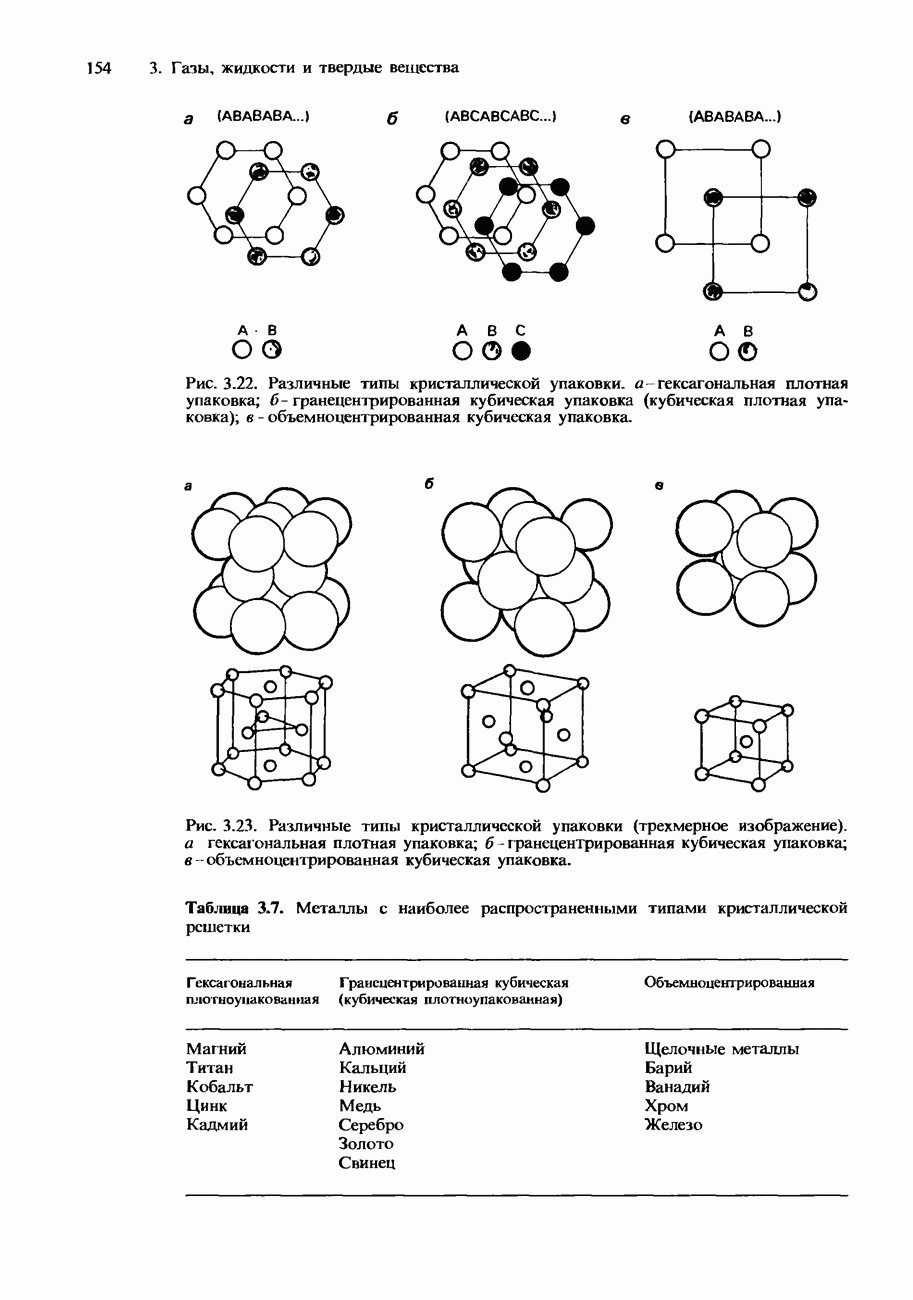
9. Кратко опишите все, что вы знаете о твердом состоянии. Включите в свое описание объяснение различных типов химической связи, которые встречаются в твердых веществах, сопровождая его схематическими рисунками с указанием расположения структурных единиц и соответствующими подписями. В качестве примера можете рассмотреть одно или несколько твердых веществ перечисленных ниже типов: конкретные (с указанием названия) галогениды металлов, аллотропы углерода, типичный металлический элемент, типичный неметаллический элемент (кроме углерода), лед.
Кратко укажите, как зависят физические свойства веществ, выбранных вами в качестве примеров, от типа химической связи в них и от их структуры.
С помощью четких схематических рисунков кратко проиллюстрируйте структурные различия между двумя типами плотной упаковки-кубической и гексагональной.
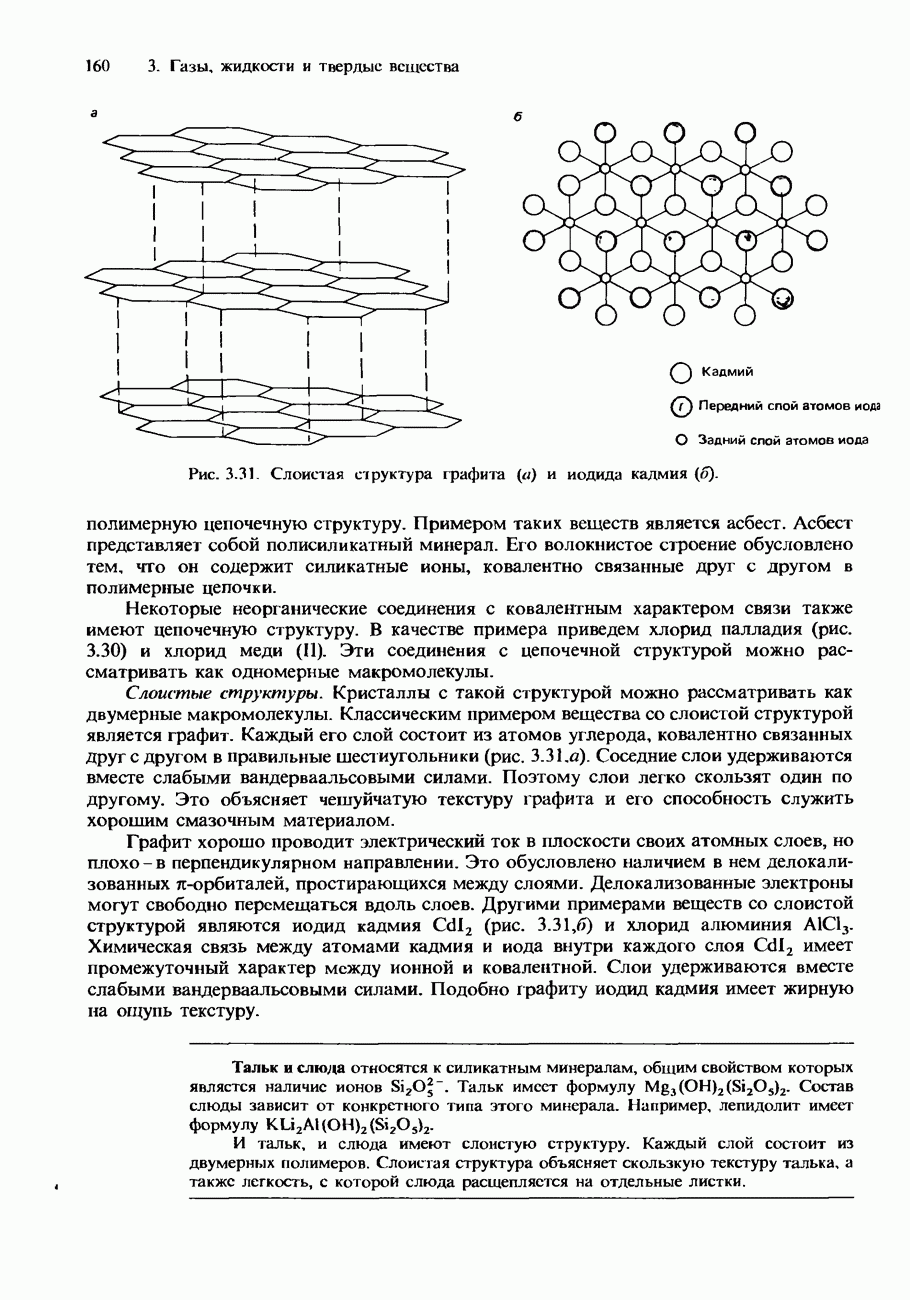
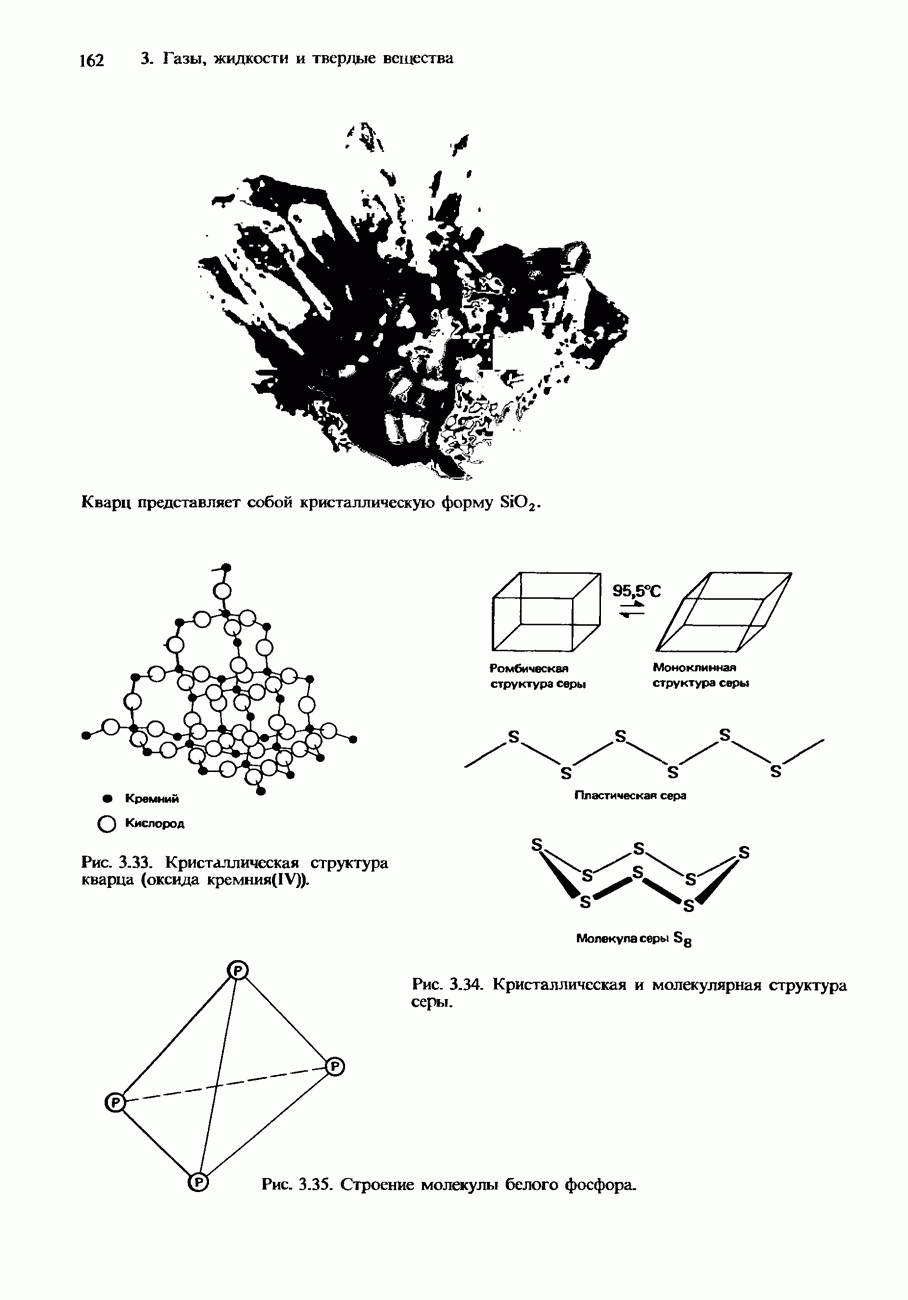
10. Опишите природу химической связи и структуру следующих твердых веществ: а) алмаз, б) иод, в) оксид фосфора (V), г) лед, д) магний (металл с гексагональной плотной упаковкой).
11. а) Какой смысл имеет понятие координационное число применительно к описанию кристаллической структуры?
б) Назовите галогенид какого-либо металла, имеющий 1) координацию 6:6, 2) координацию 8:8. Укажите, почему один из двух названных вами гало-генидов металлов имеет более высокую координацию, чем другой.
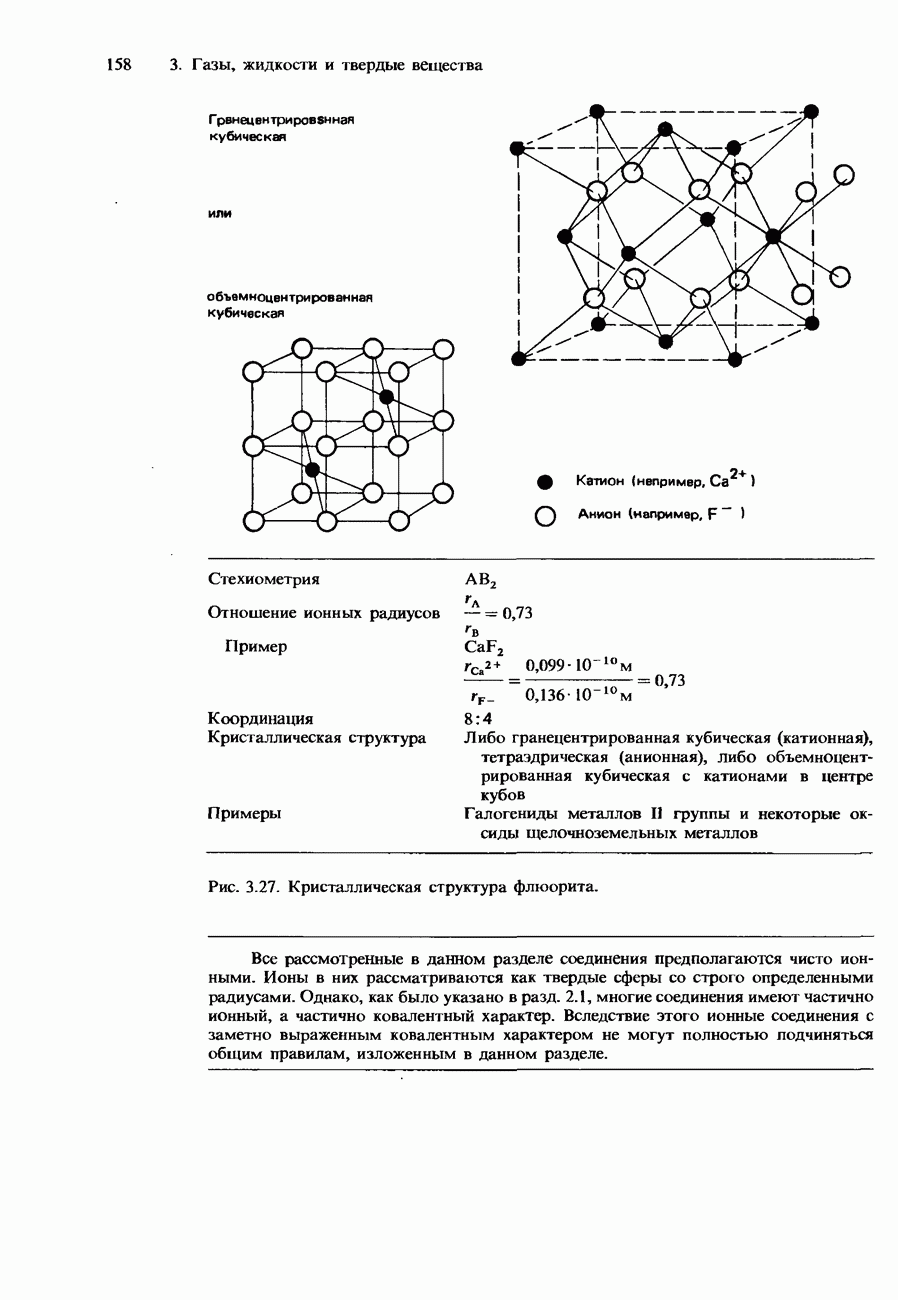
в) Этот пункт поможет вам получить схематическое изображение структуры типа флюорита, которую имеет фторид кальция.
1) Нарисуйте куб с ионами кальция в центре каждой грани и в каждой вершине.
2) Нарисуйте второй куб такого же размера. Разделите этот куб на восемь меньших кубов равного размера. Поместите фторид-ион  в центре каждого из восьми меньших кубов. Получится внутренний куб, имеющий в каждой вершине по одному из этих восьми фторид-ионов. Элементарную ячейку флюорита можно получить наложением рисунков (1) и (2). Кристаллическая решетка фторида кальция получается бесконечным повторением таких элементарных ячеек во всех направлениях пространства.
в центре каждого из восьми меньших кубов. Получится внутренний куб, имеющий в каждой вершине по одному из этих восьми фторид-ионов. Элементарную ячейку флюорита можно получить наложением рисунков (1) и (2). Кристаллическая решетка фторида кальция получается бесконечным повторением таких элементарных ячеек во всех направлениях пространства.
3) Наложите один рисунок на другой и нарисуйте новый рисунок, изображающий элементарную ячейку флюорита.
4) Обобществляются ли фторид-ионы соседними элементарными ячейками кристалла фторида кальция?
5) Сколько элементарных ячеек кристалла фторида кальция обобществляют каждый ион кальция, находящийся в центре грани элементарной ячейки?
6) Сколько элементарных ячеек кристалла фторида кальция обобществляют каждый ион кальция, находящийся в центре грани элементарной ячейки?
7) Выведите на основании ответов на два предыдущих вопроса эмпирическую формулу фторида кальция, сопровождая ответ необходимыми пояснениями.
8) Сколько молей фторида кальция приходится на каждую элементарную ячейку?
9) Объясните, каким образом выведенная вами эмпирическая формула согласуется с положением кальция и фтора в периодической системе элементов.
12. а) Объясните смысл термина аллотропия.
б) Схематически изобразите структуру двух аллотропов углерода и объясните с учетом структурных особенностей физические свойства каждого аллотропа.
в) Укажите, какие данные свидетельствуют о том, что аллотропы, упоминаемые в пункте (б), принадлежат одному элементу.
г) Кратко объясните, почему углерод образует в своих соединениях четыре ковалентные связи и не образует соединений с ионными связями.
д) Схематически изобразите геометрическую форму молекул трех углеводородов: 1) этана, 2) этена (этилена), 3) этина (ацетилена). Дайте необходимые пояснения.
е) Объясните, почему тетрахлорометан (тетрахлорид углерода) имеет полярные связи, но у его молекулы отсутствует дипольный момент.
| << Предыдущий параграф | Следующий параграф >> |
- ОТ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРА К РУССКОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ
- 1. СТРОЕНИЕ АТОМА
- 1.1. Субатомные частицы
- Модели атома
- Новые элементарные частицы
- МАССА АТОМА
- МАСС-СПЕКТРОМЕТРИЯ
- 1.2 Электронное строение атомов
- Связь между спектральными линиями и электронами (открытие Бора)
- Применение возбуждения электронов на практике
- Атомный спектр испускания водорода
- ЭНЕРГИИ ИОНИЗАЦИИ
- Рассмотрение энергий ионизации в рамках модели атома, предложенной Бором
- ВОЛНОВАЯ ПРИРОДА ЭЛЕКТРОНА
- Орбитали
- КВАНТОВЫЕ ЧИСЛА
- ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
- 1.3 Радиоактивность
- ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ
- Обнаружение и измерение радиоактивности
- УСТОЙЧИВЫЕ И НЕУСТОЙЧИВЫЕ ИЗОТОПЫ
- Зона устойчивости
- Период полураспада
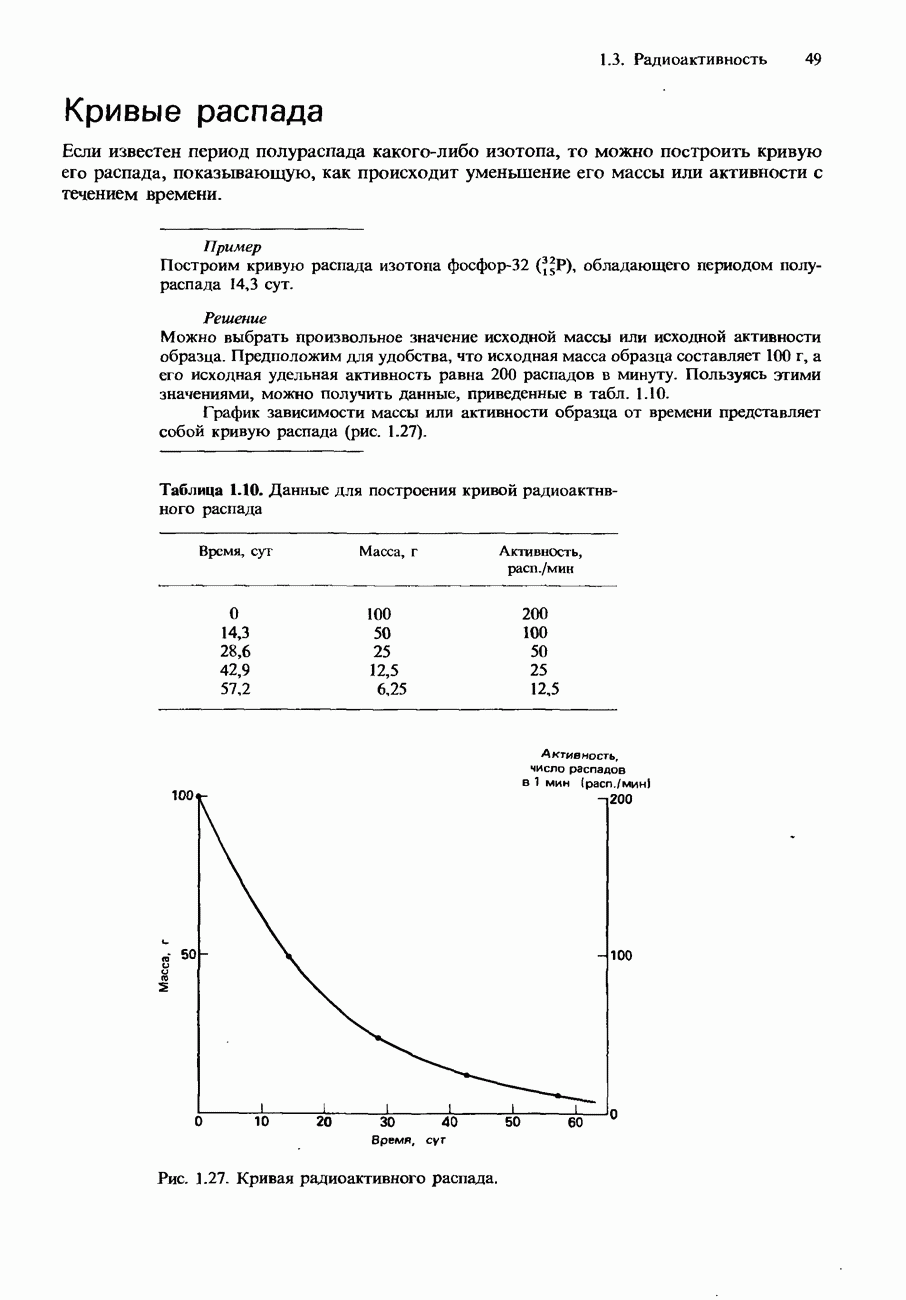
- Кривые распада
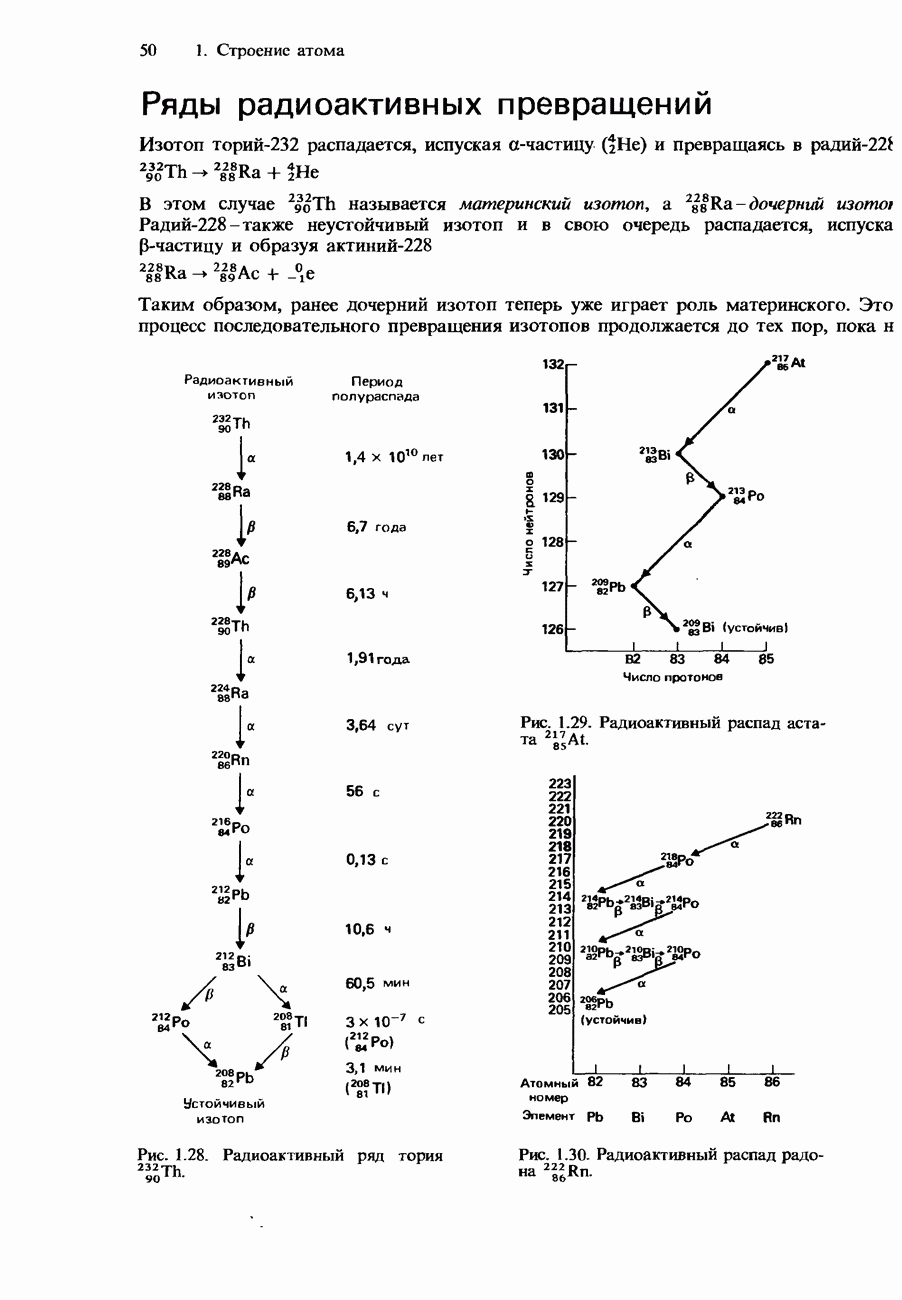
- Ряды радиоактивных превращений
- Естественные радиоизотопы
- ИСКУССТВЕННЫЕ ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
- Ускорители элементарных частиц
- Трансурановые элементы
- ПРИМЕНЕНИЯ ИЗОТОПОВ
- ЯДЕРНОЕ ДЕЛЕНИЕ И ЯДЕРНЫЙ СИНТЕЗ
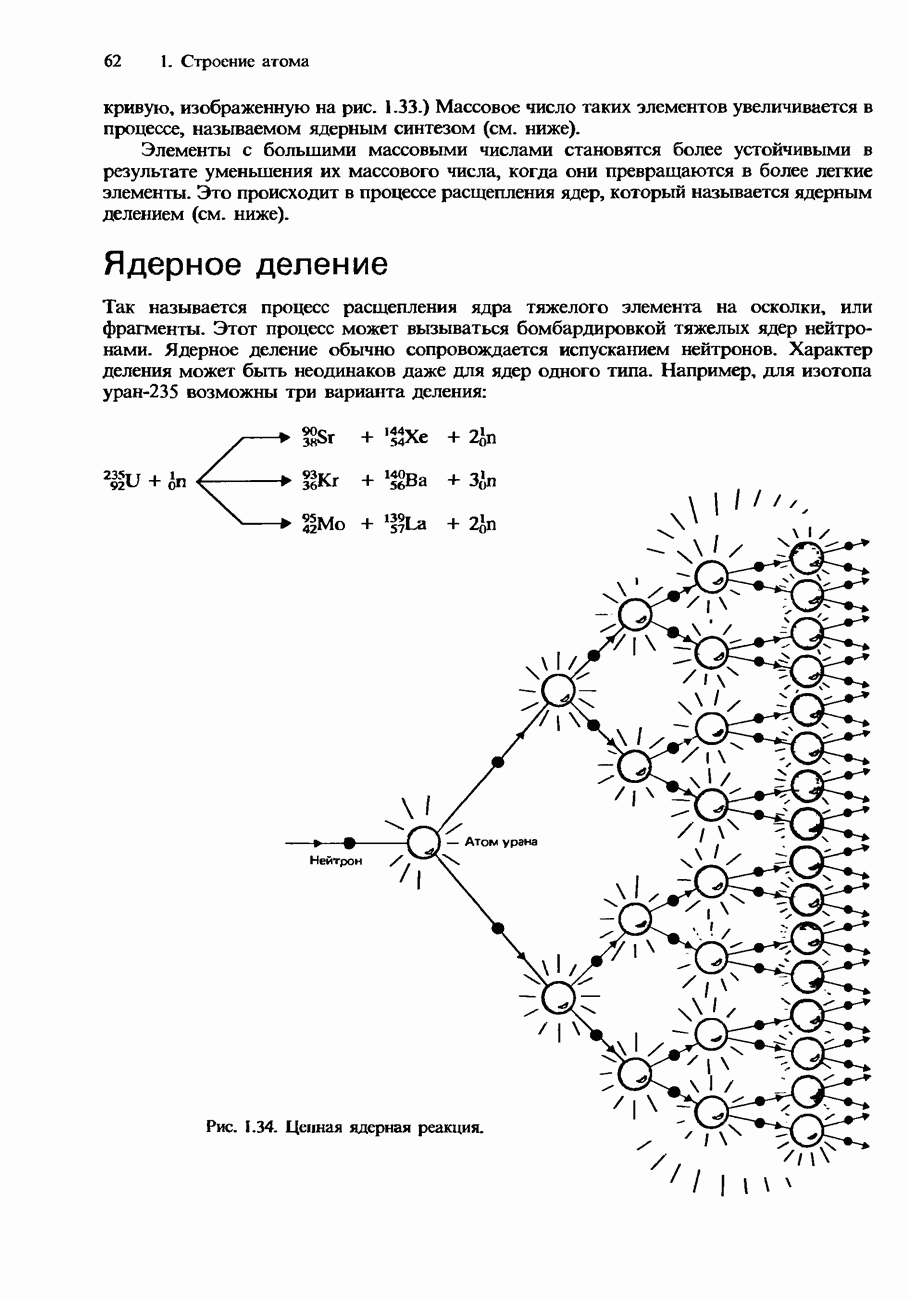
- Ядерное деление
- Ядерный синтез
- Ядерный синтез в звездах
- ЯДЕРНАЯ ЭНЕРГИЯ
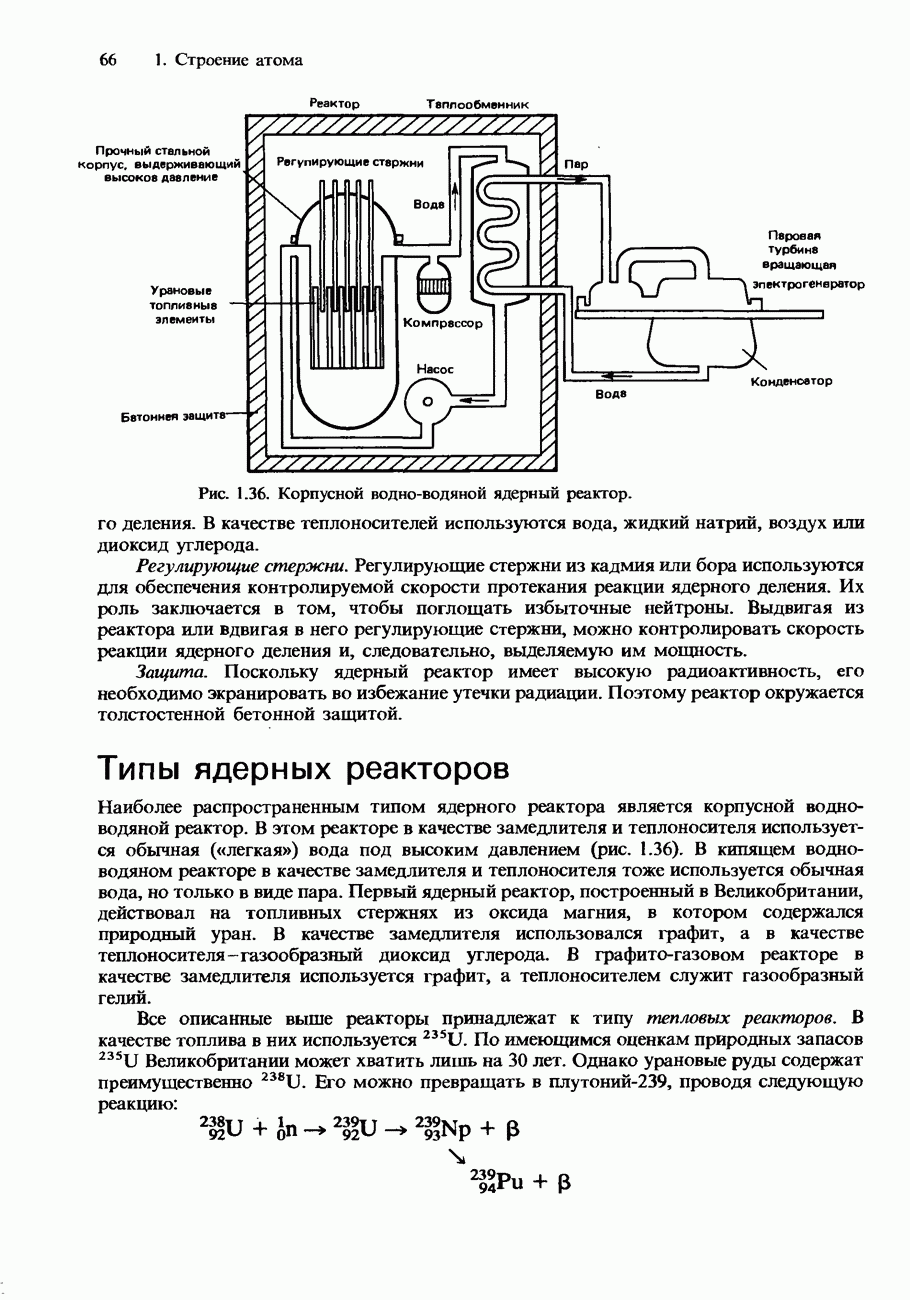
- Типы ядерных реакторов
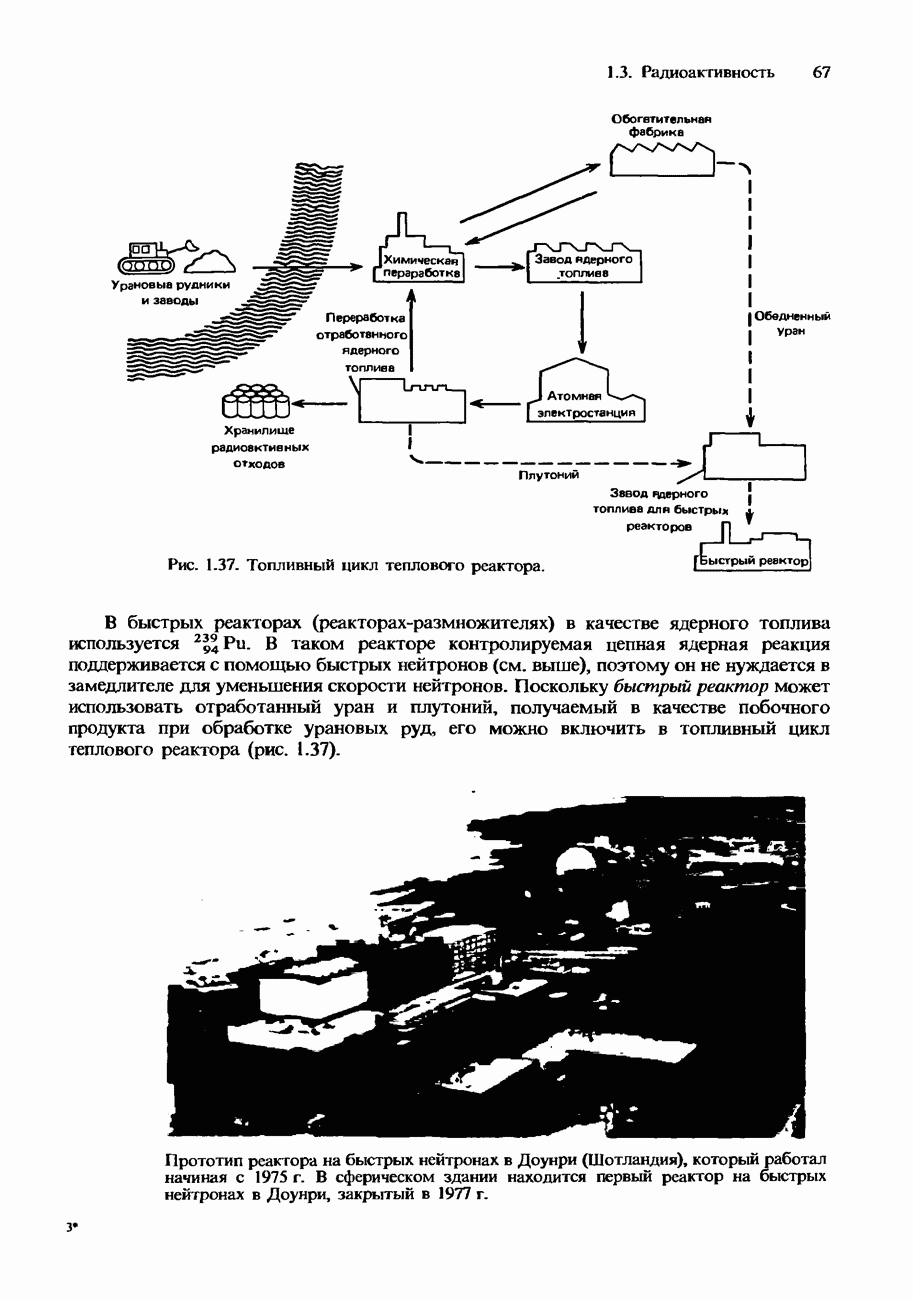
- Радиоактивные ядерные отходы и их переработка
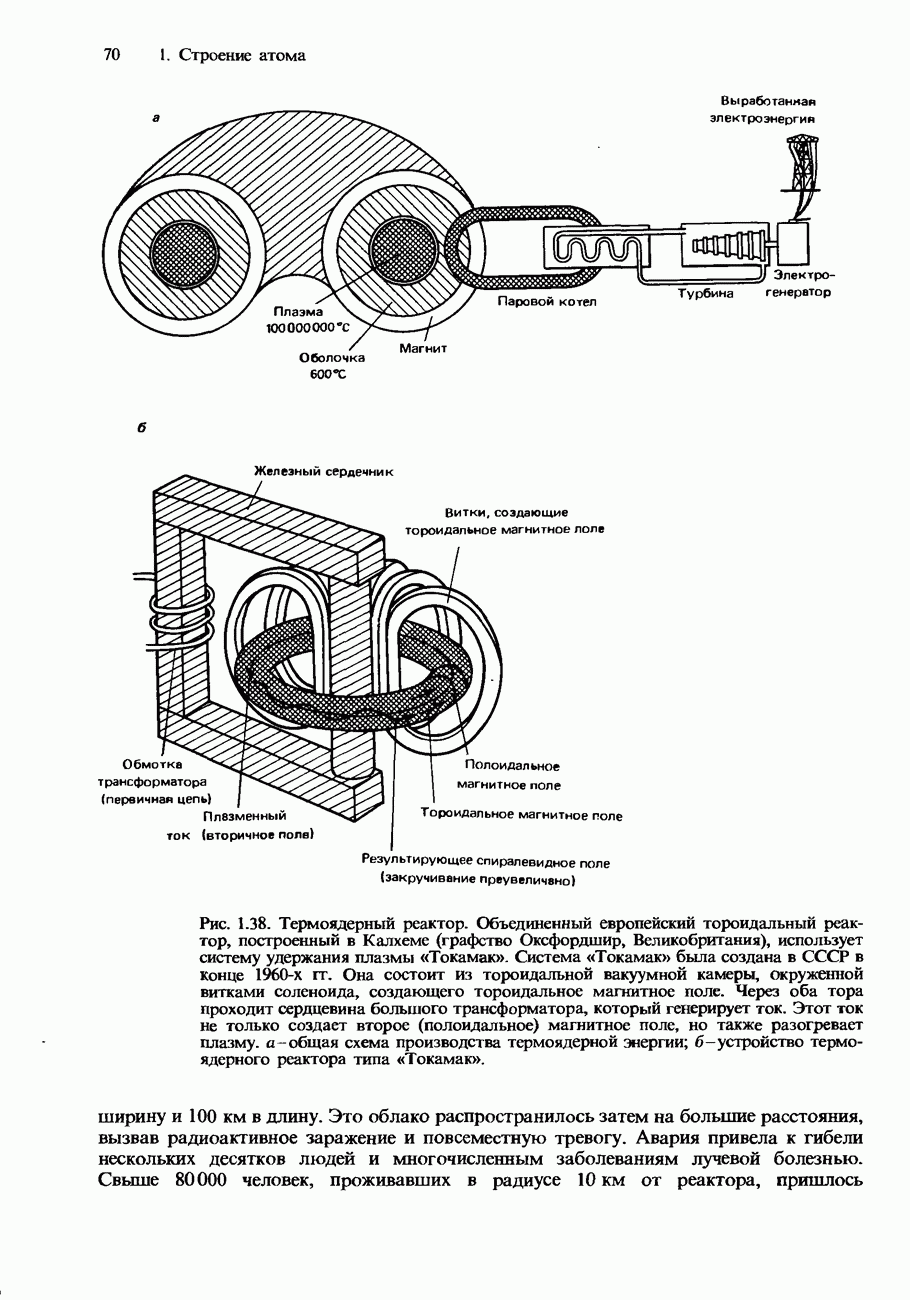
- Термоядерные реакторы
- Аргументы против использования ядерной энергии
- ЯДЕРНОЕ ОРУЖИЕ
- Ядерное разоружение
- ИСТОЧНИКИ РАДИАЦИИ И ЕЕ ВОЗДЕЙСТВИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 2. ХИМИЧЕСКАЯ СВЯЗЬ
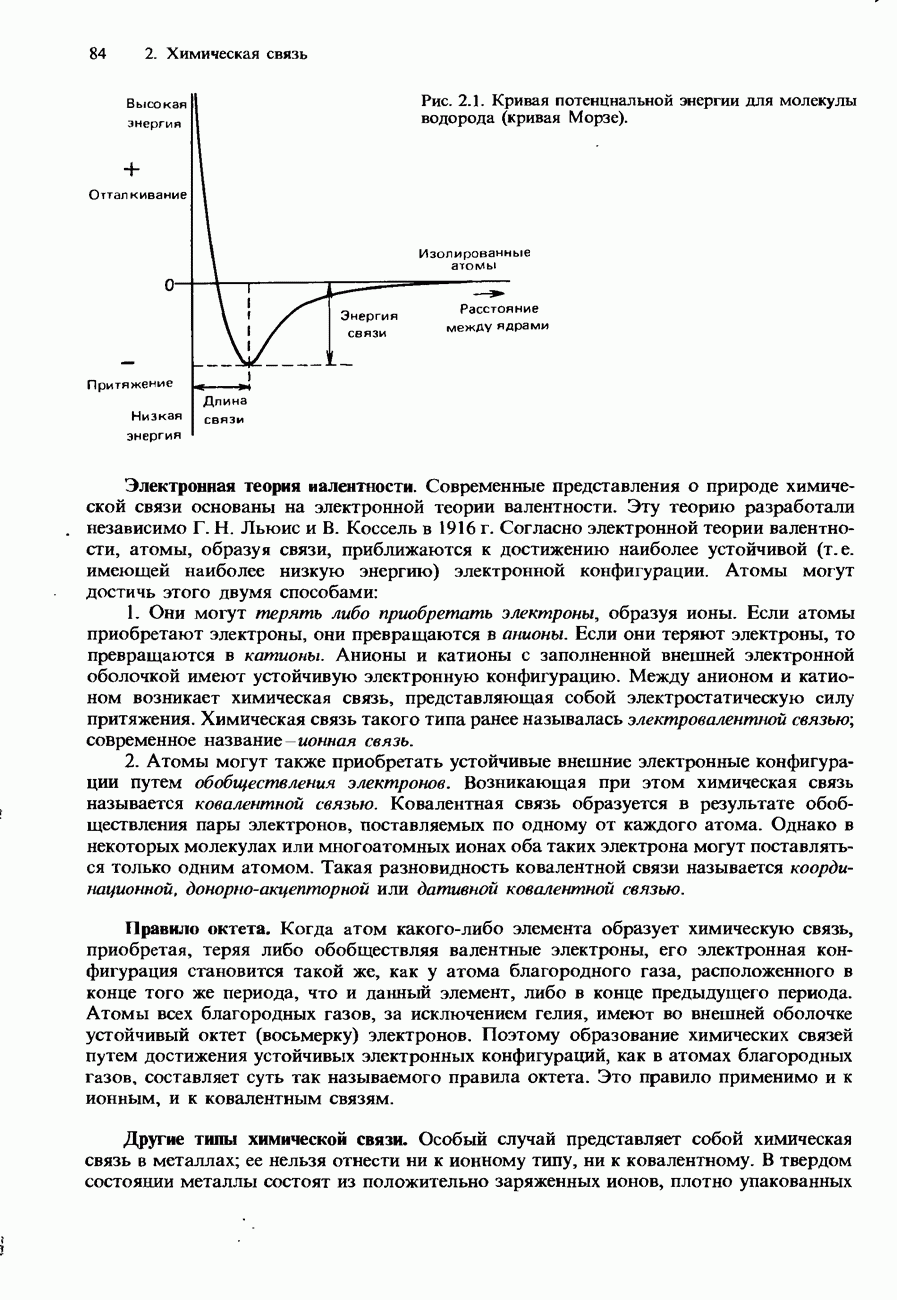
- 2.1. Природа химической связи
- ИОННАЯ СВЯЗЬ
- Устойчивость ионных соединений
- КОВАЛЕНТНАЯ СВЯЗЬ
- Молекулярные орбитали
- Гибридные атомные орбитали
- Делокализованные орбитали
- Координационная связь
- ИОННЫЙ И КОВАЛЕНТНЫЙ ХАРАКТЕР СВЯЗИ
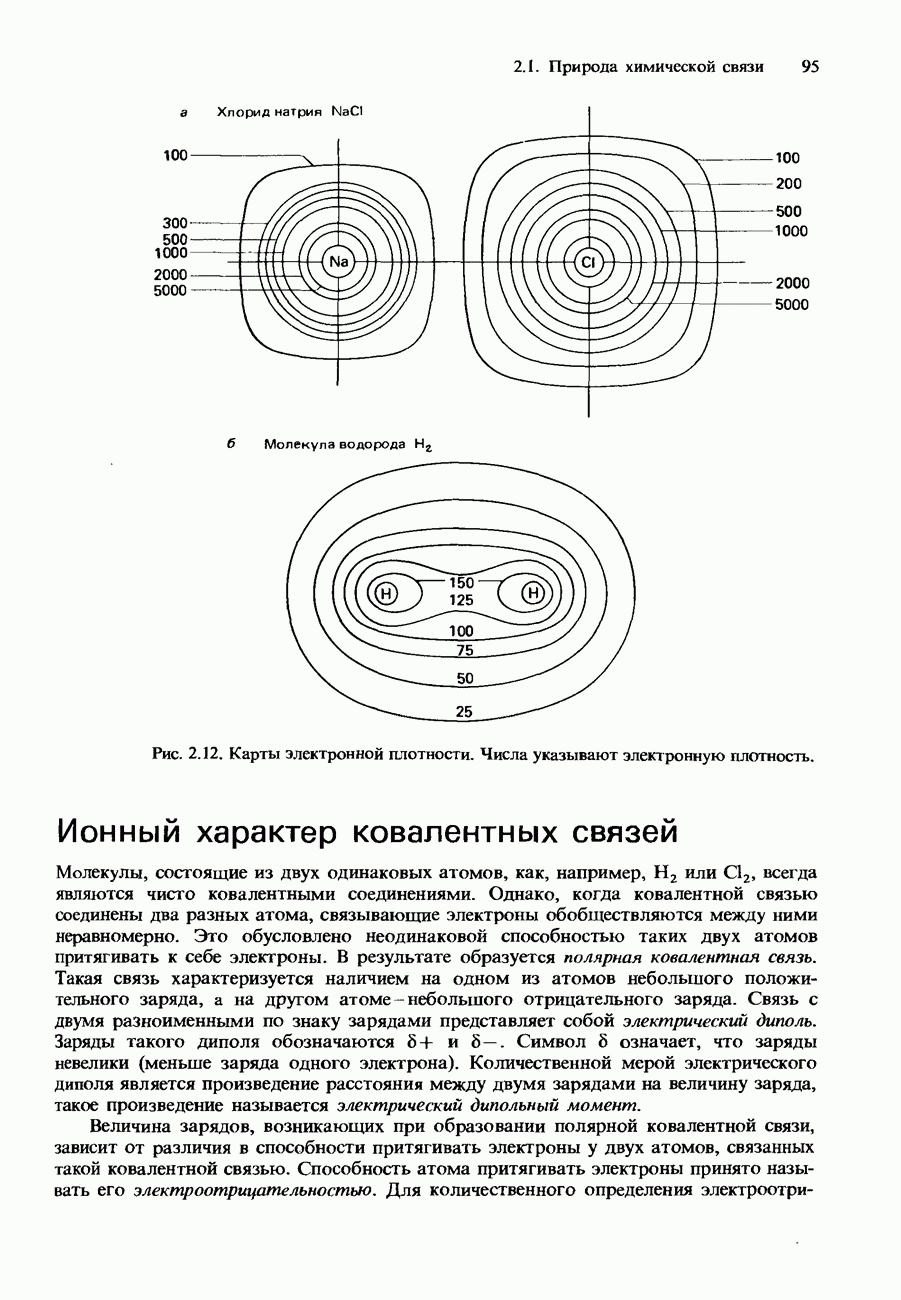
- Ионный характер ковалентных связей
- Ионные и ковалентные соединения
- МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
- Валентная зона и зона проводимости
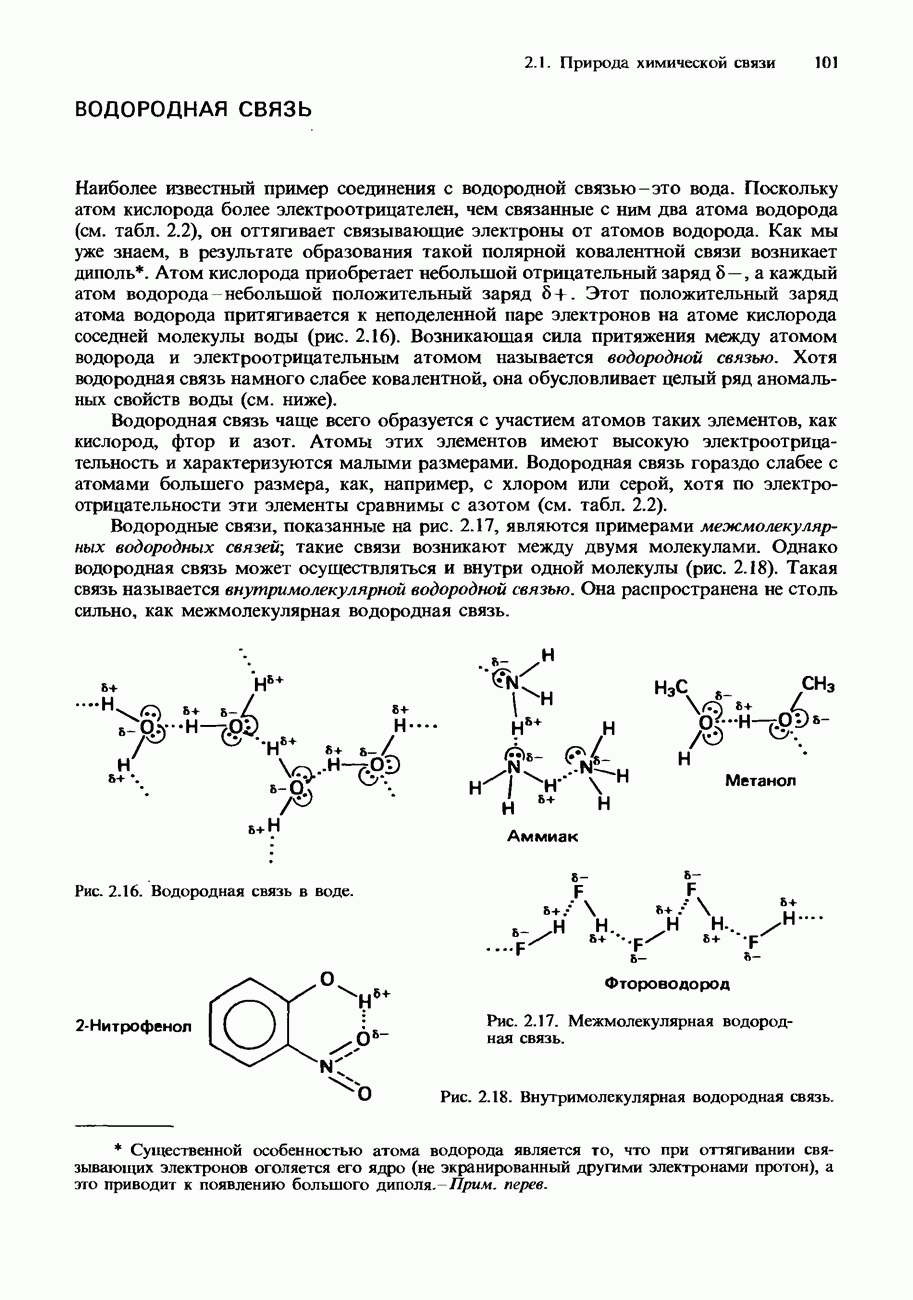
- ВОДОРОДНАЯ СВЯЗЬ
- ВАНДЕРВААЛЬСОВЫ СИЛЫ
- Притяжение типа диполь-индуцированный диполь (индукционное)
- Что понимается под вандерваальсовыми силами
- 2.2. Влияние химической связи на свойства соединений
- Атомные радиусы
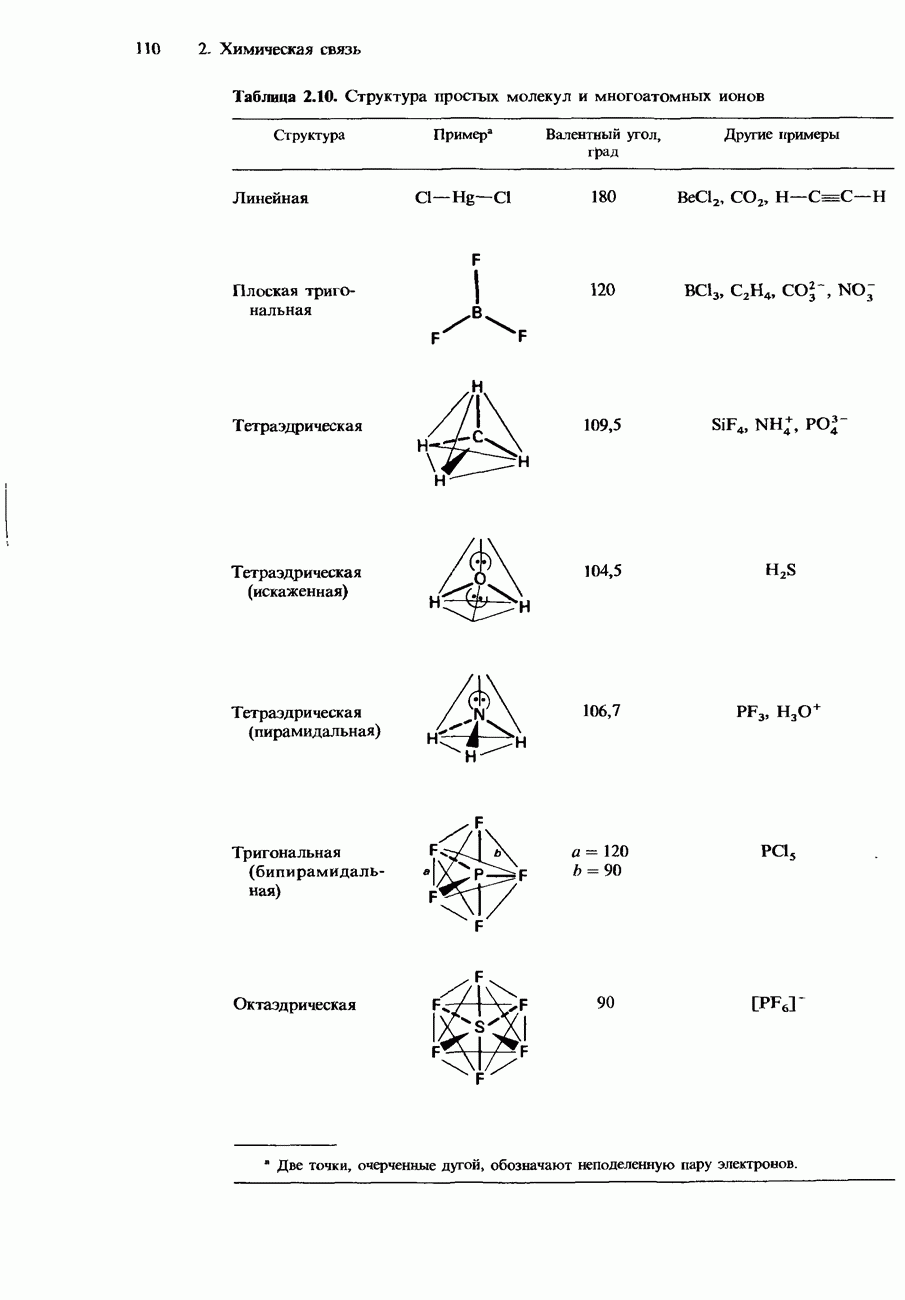
- ФОРМА ПРОСТЫХ МОЛЕКУЛ И МНОГОАТОМНЫХ ИОНОВ
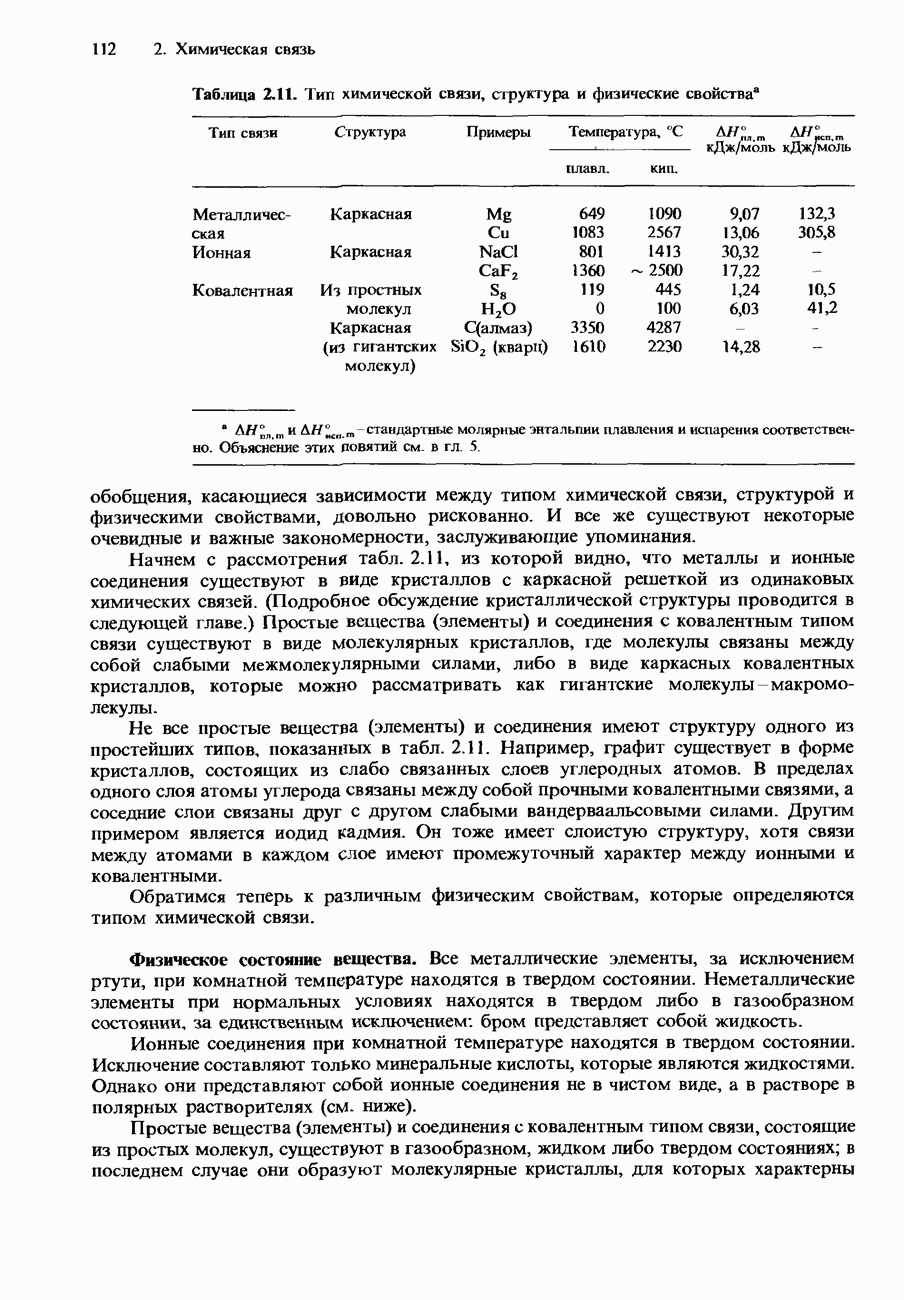
- ТИП ХИМИЧЕСКОЙ СВЯЗИ, СТРУКТУРА И ФИЗИЧЕСКИЕ СВОЙСТВА
- ТИП СВЯЗИ И ХИМИЧЕСКИЕ СВОЙСТВА
- ВЛИЯНИЕ МЕЖМОЛЕКУЛЯРНЫХ СИЛ НА СТРУКТУРУ И СВОЙСТВА
- ВЛИЯНИЕ ВАНДЕРВААЛЬСОВЫХ СИЛ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 3 ГАЗЫ, ЖИДКОСТИ И ТВЕРДЫЕ ВЕЩЕСТВА
- 3.1. Газы и жидкости
- ГАЗОВЫЕ ЗАКОНЫ
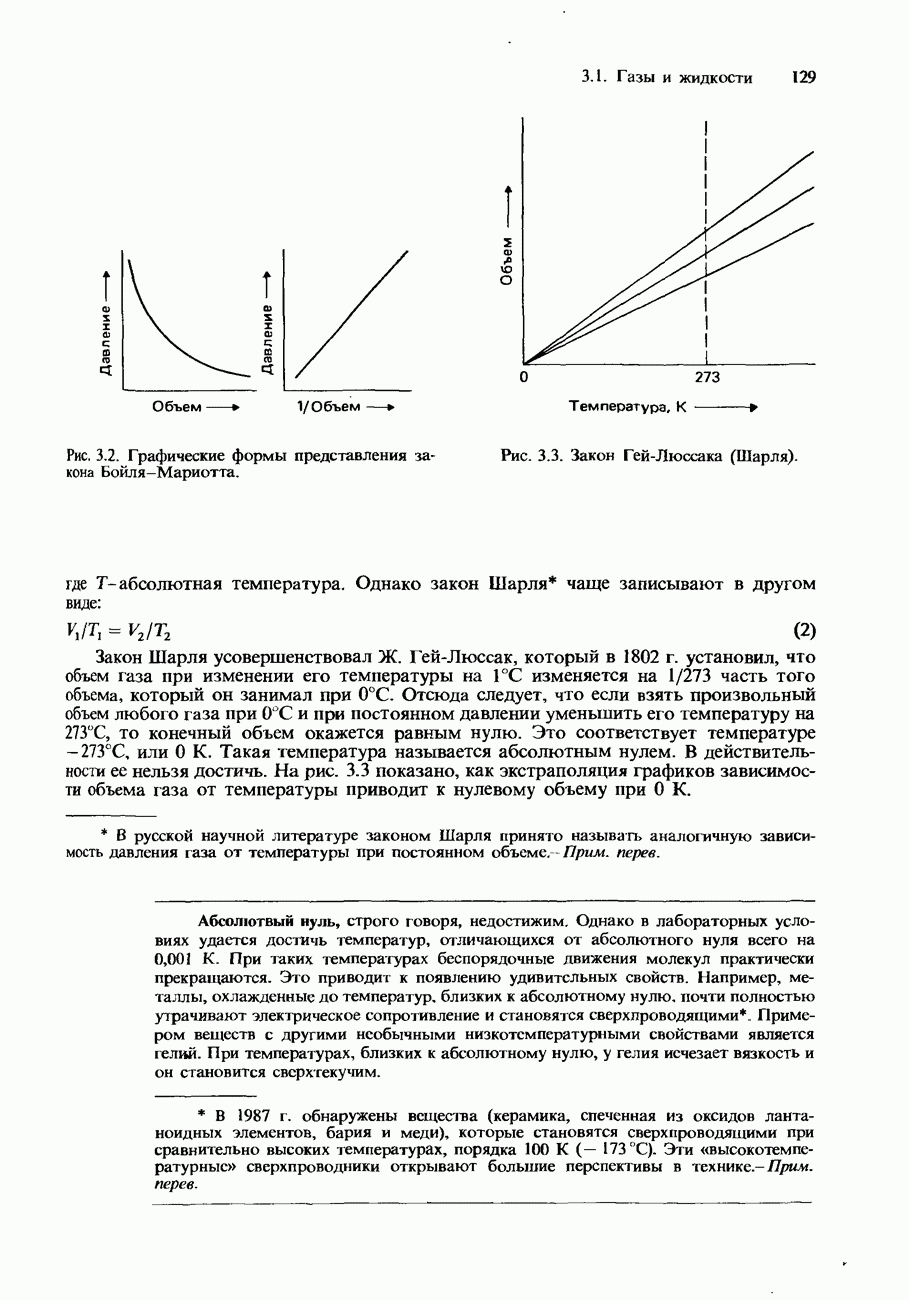
- Закон Бойля-Мариотта
- Закон Гей-Люссака (закон Шарля)
- Объединенный газовый закон
- Закон Авогадро
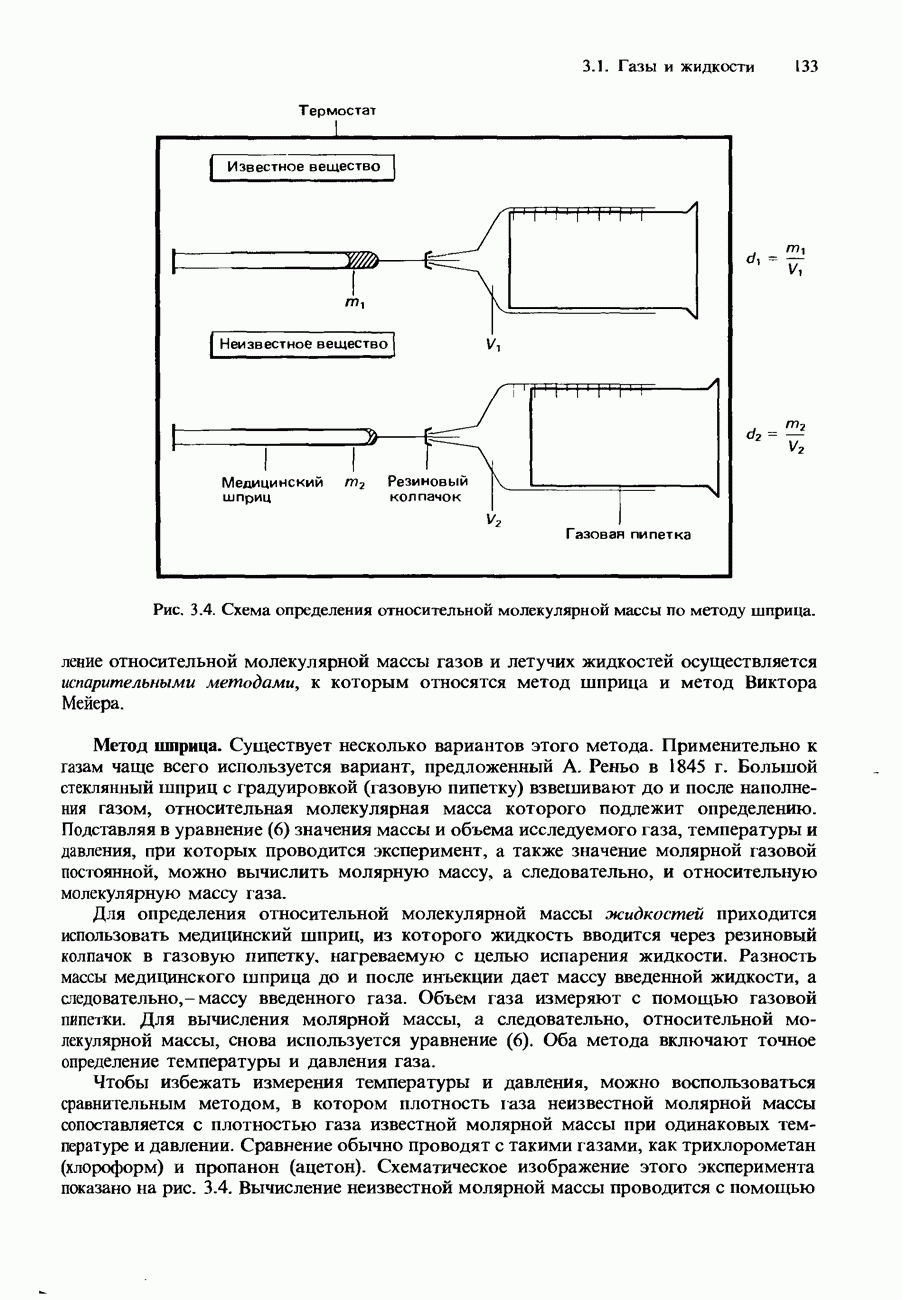
- Экспериментальное определение относительной молекулярной массы
- Закон парциальных давлений газов (закон Дальтона)
- Законы Грэхема
- КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- Скорости молекул
- Распределение Максвелла-Больцмана
- РЕАЛЬНЫЕ ГАЗЫ
- Уравнение Ван-дер-Ваальса
- Сжижение газов
- ЖИДКОСТИ
- Свойства жидкостей
- 3.2. Твердые вещества
- КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
- Металлические кристаллы
- Ионные кристаллы
- Ковалентные кристаллы
- ИЗОМОРФИЗМ. ПОЛИМОРФИЗМ И АЛЛОТРОПИЯ
- СВОЙСТВА ТВЕРДЫХ ВЕЩЕСТВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 4. СТЕХИОМЕТРИЯ
- 4.1. Стехиометрия и номенклатура
- Химические вещества
- Количественные законы химии
- Вес и масса
- НАЗВАНИЯ И ФОРМУЛЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- Химические формулы
- НОМЕНКЛАТУРА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- Степень окисления (состояние окисления)
- Элементы
- Бинарные соединения
- 4.2 Стехиометрические вычисления
- Молярная масса
- Число частиц вещества
- Процентный состав соединения
- Эмпирическая формула соединения
- Молярные постоянные и молярные величины
- Состав гомогенных смесей
- ХИМИЧЕСКИЕ УРАВНЕНИЯ
- ВЫХОД РЕАКЦИИ
- ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 5. ЭНЕРГЕТИКА
- 5.1. Термодинамика
- ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 5.2. Энтальпия
- СТАНДАРТНЫЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- ДРУГИЕ ИЗМЕНЕНИЯ ЭНТАЛЬПИИ
- КАЛОРИМЕТРИЯ
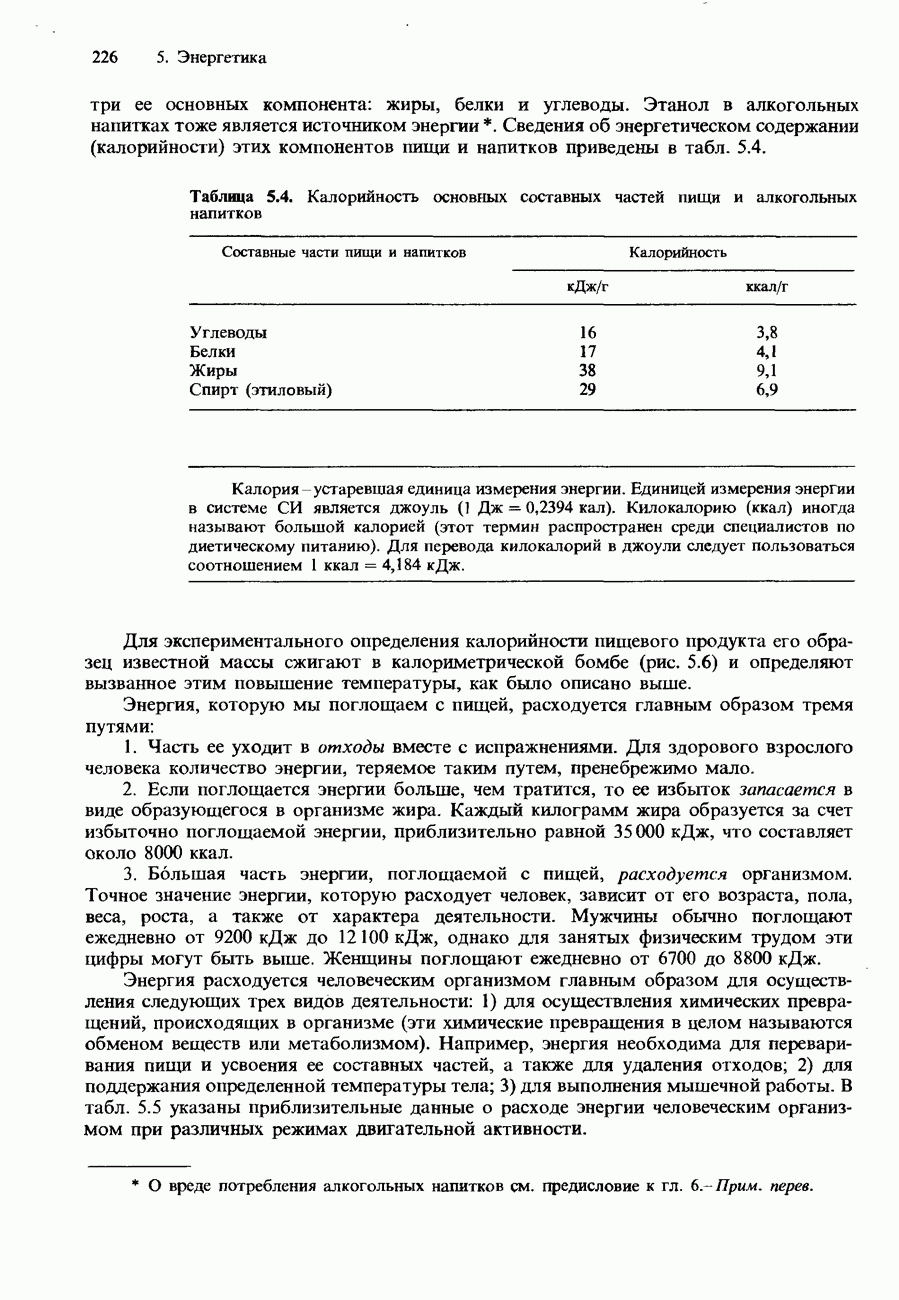
- КАЛОРИЙНОСТЬ ПИЩИ
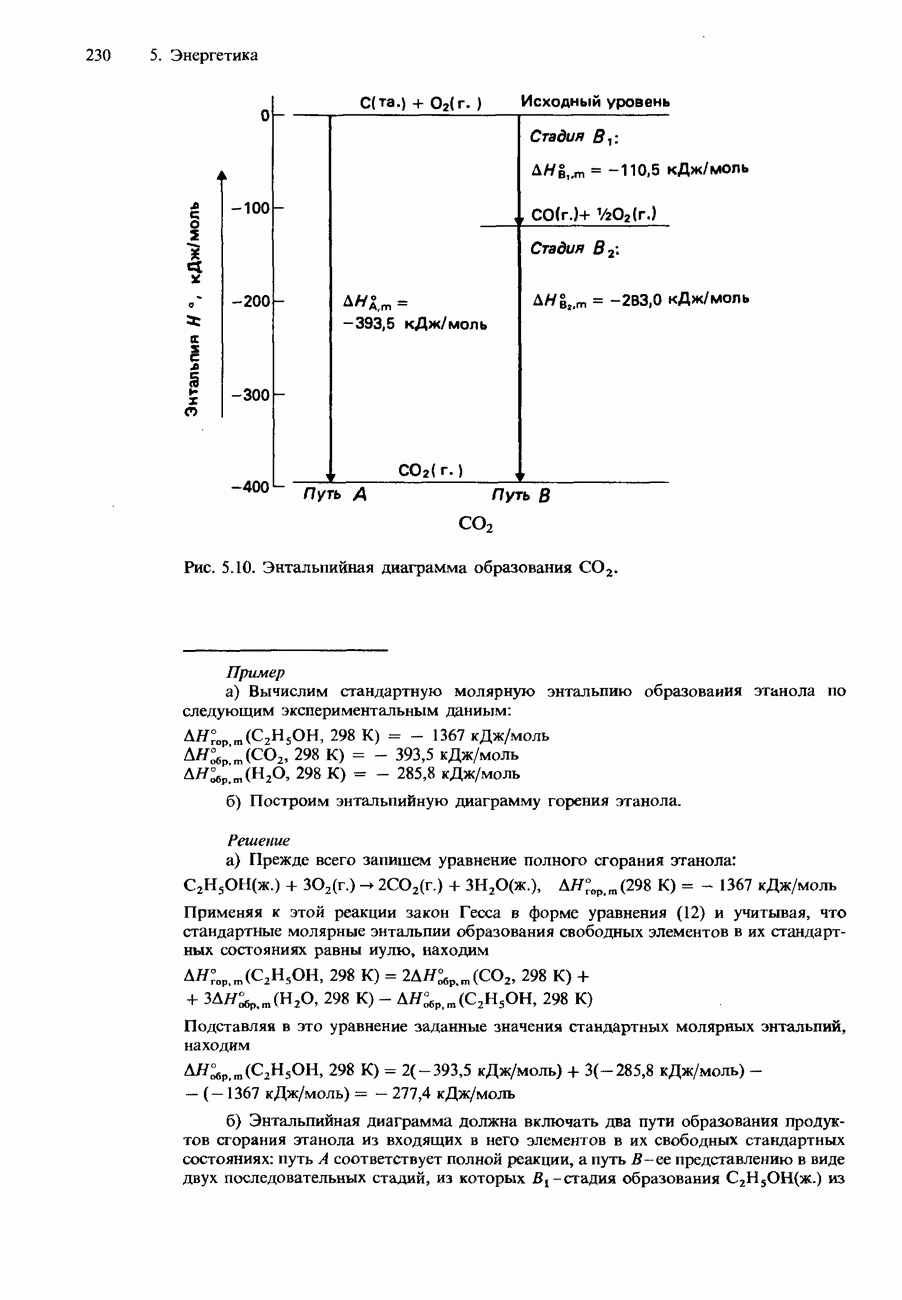
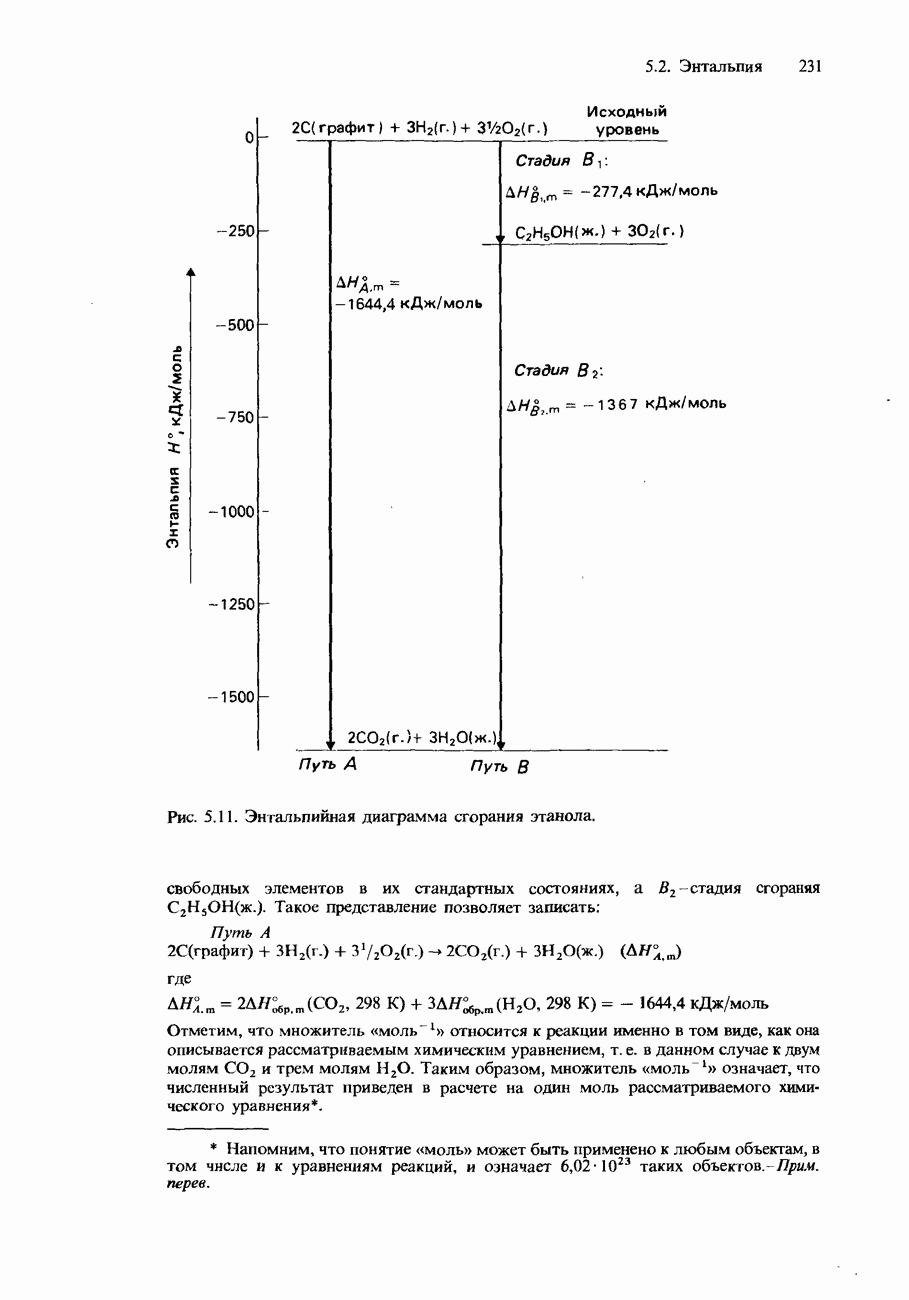
- ЗАКОН ГЕССА
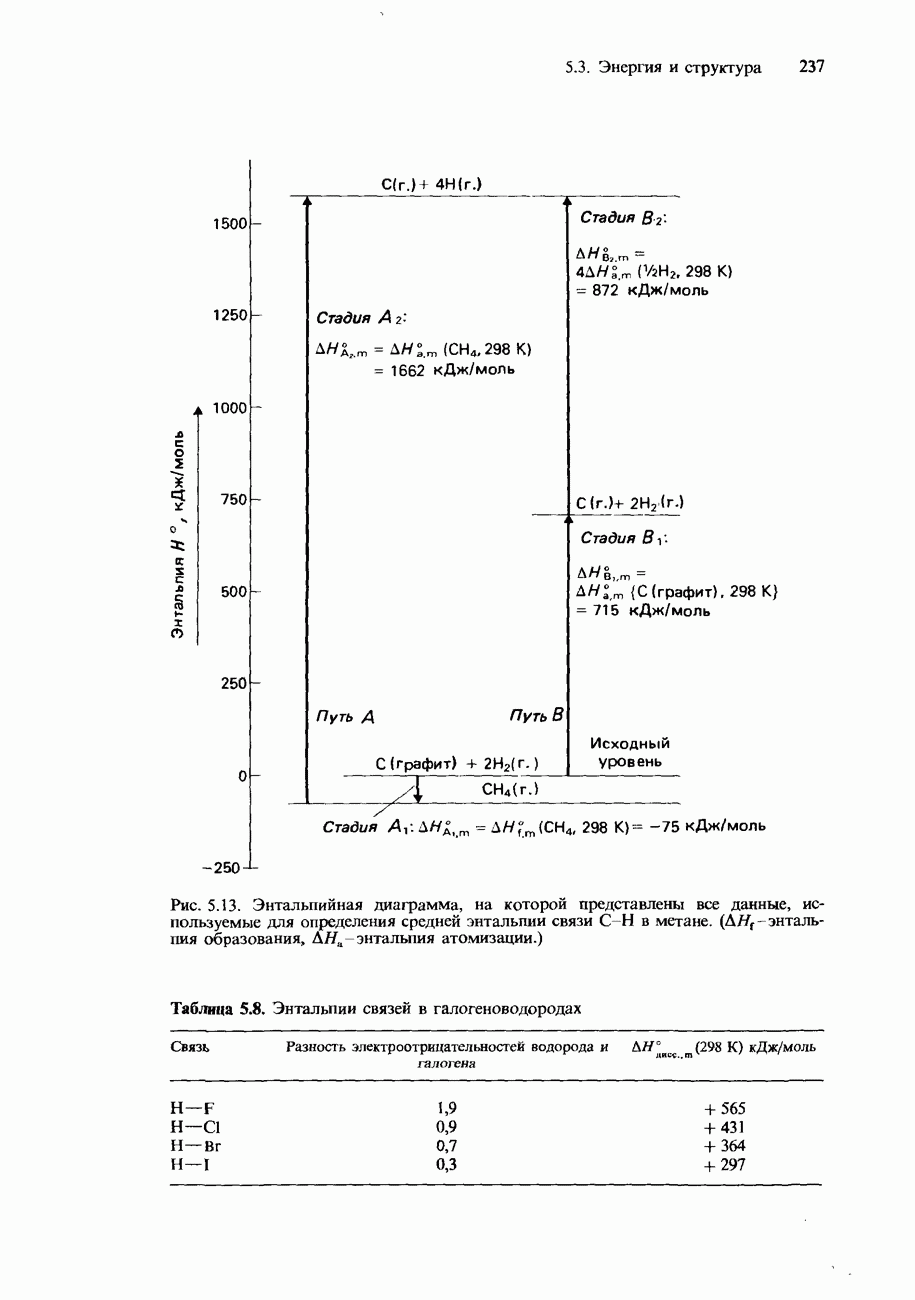
- 5.3 Энергия и структура
- ЭНТАЛЬПИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
- Энтальпии растворения и гидратации
- ЭНТРОПИЯ
- СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
- О ЧЕМ ПОЗВОЛЯЕТ СУДИТЬ ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ СИСТЕМЫ
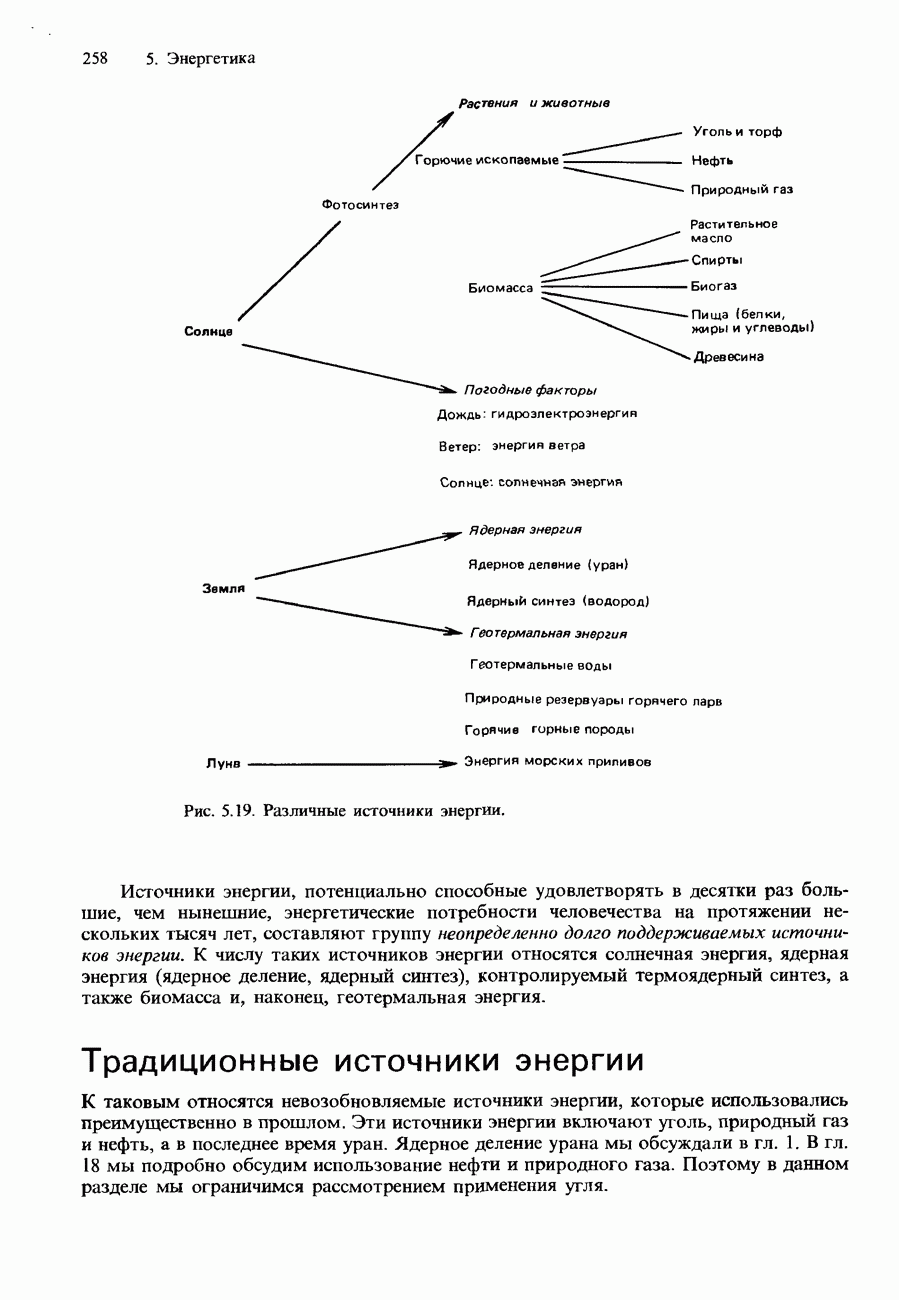
- 5.4. Источники энергии
- НЕТРАДИЦИОННЫЕ ИСТОЧНИКИ ЭНЕРГИИ
- ЗАПАСАНИЕ ЭНЕРГИИ
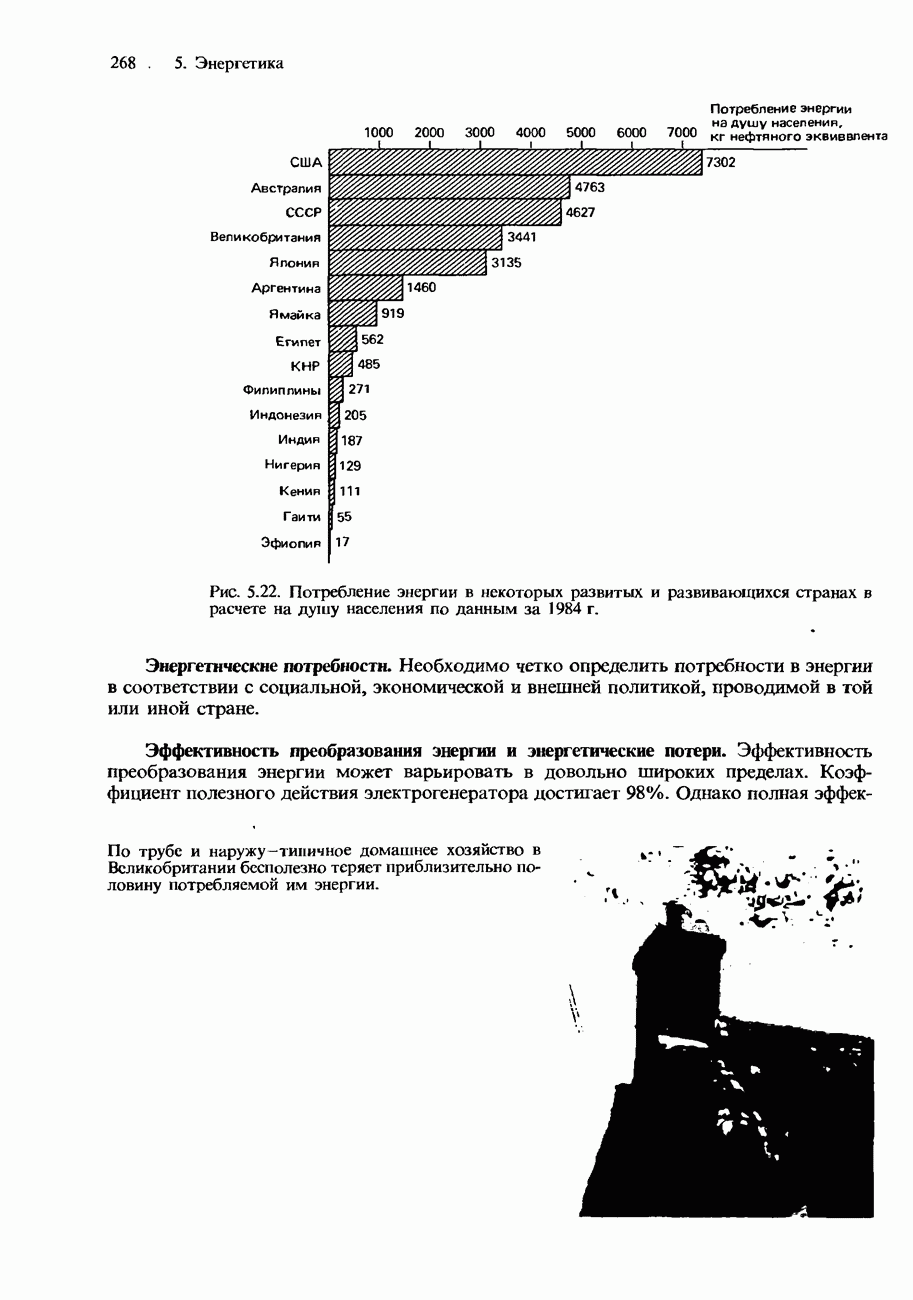
- ПОТРЕБЛЕНИЕ ЭНЕРГИИ В ПРОШЛОМ, НАСТОЯЩЕМ И БУДУЩЕМ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 6. ФАЗОВЫЕ РАВНОВЕСИЯ
- 6.1. Равновесия и фазы
- ФАЗЫ И КОМПОНЕНТЫ
- Фазы
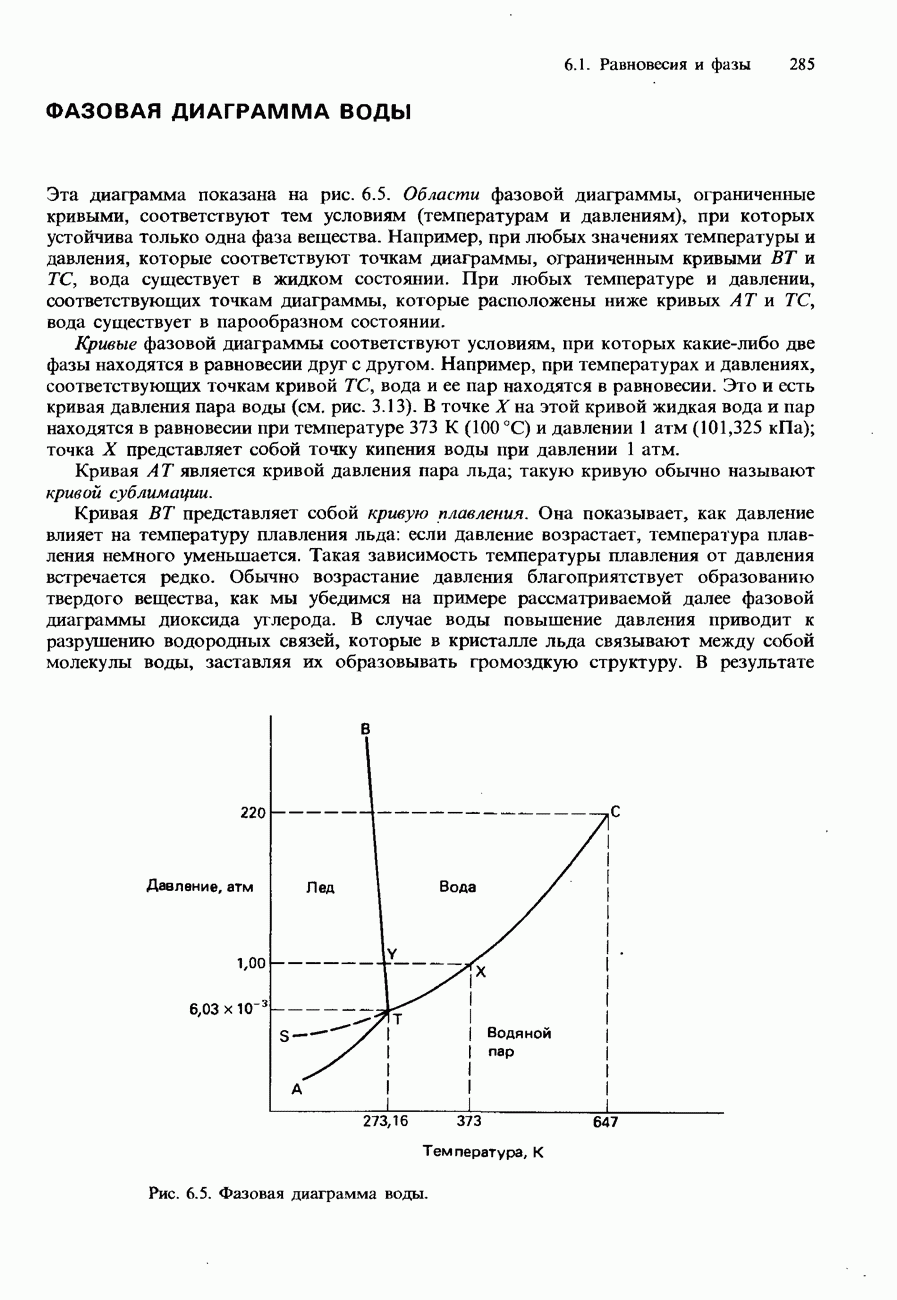
- ФАЗОВАЯ ДИАГРАММА ВОДЫ
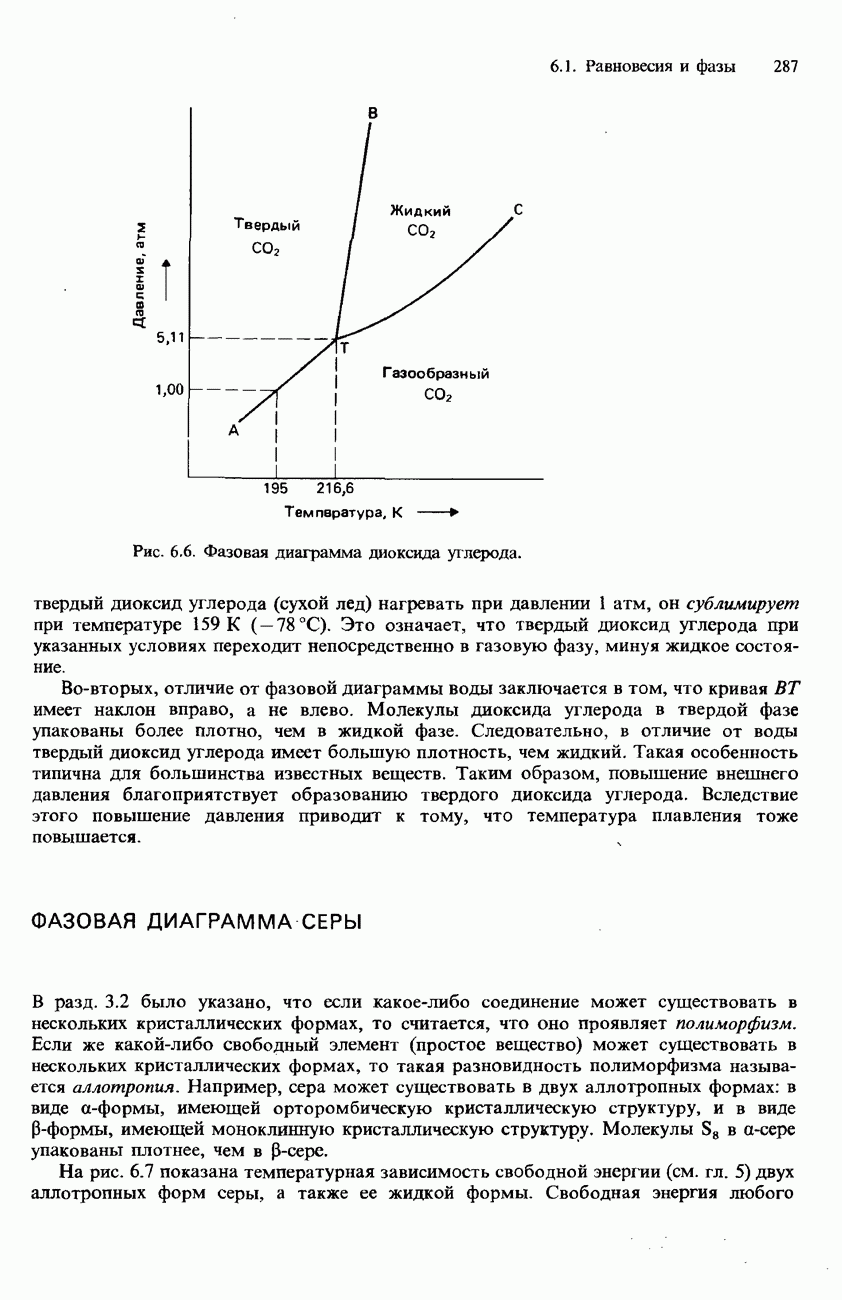
- ФАЗОВАЯ ДИАГРАММА ДИОКСИДА УГЛЕРОДА
- ФАЗОВАЯ ДИАГРАММА СЕРЫ
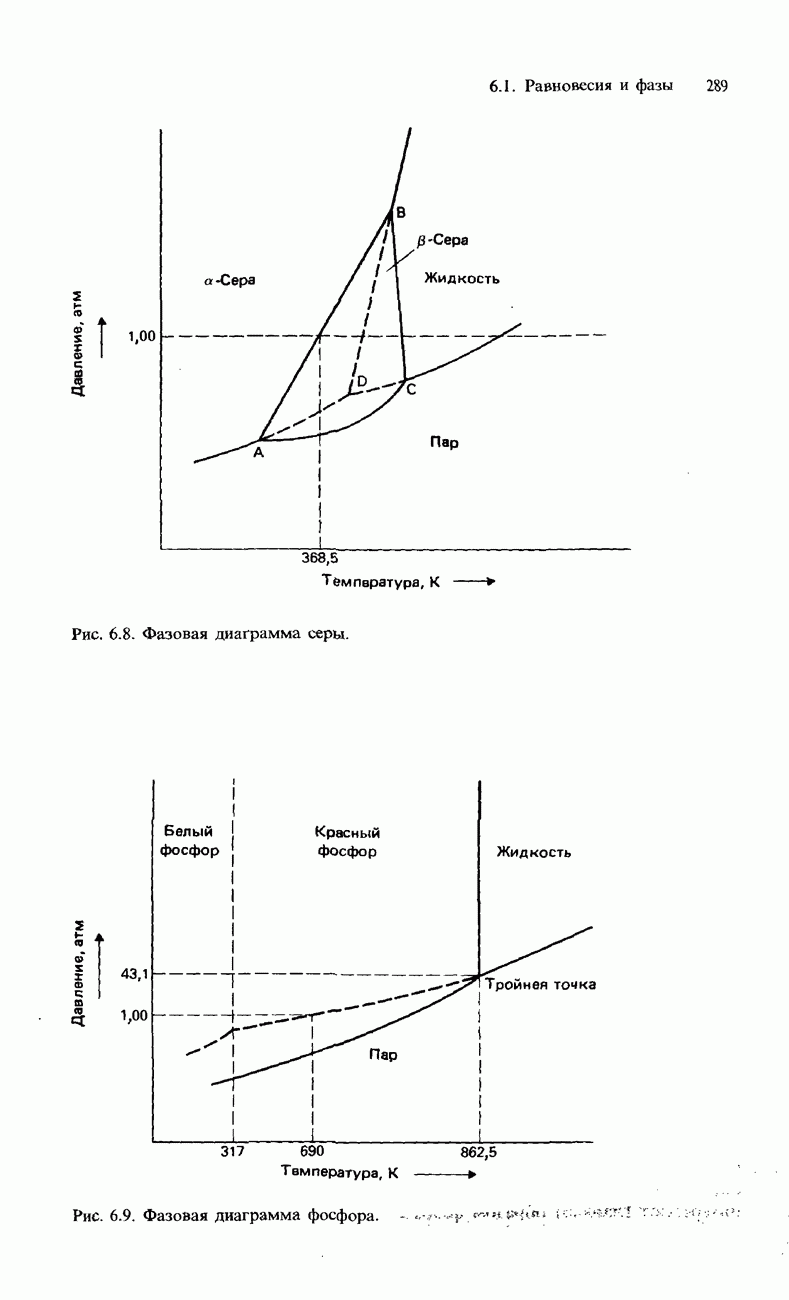
- ФАЗОВАЯ ДИАГРАММА ФОСФОРА
- 6.2. Многокомпонентные системы
- ДВУХКОМПОНЕНТНЫЕ ЖИДКИЕ СМЕСИ
- ПОЛНОСТЬЮ СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
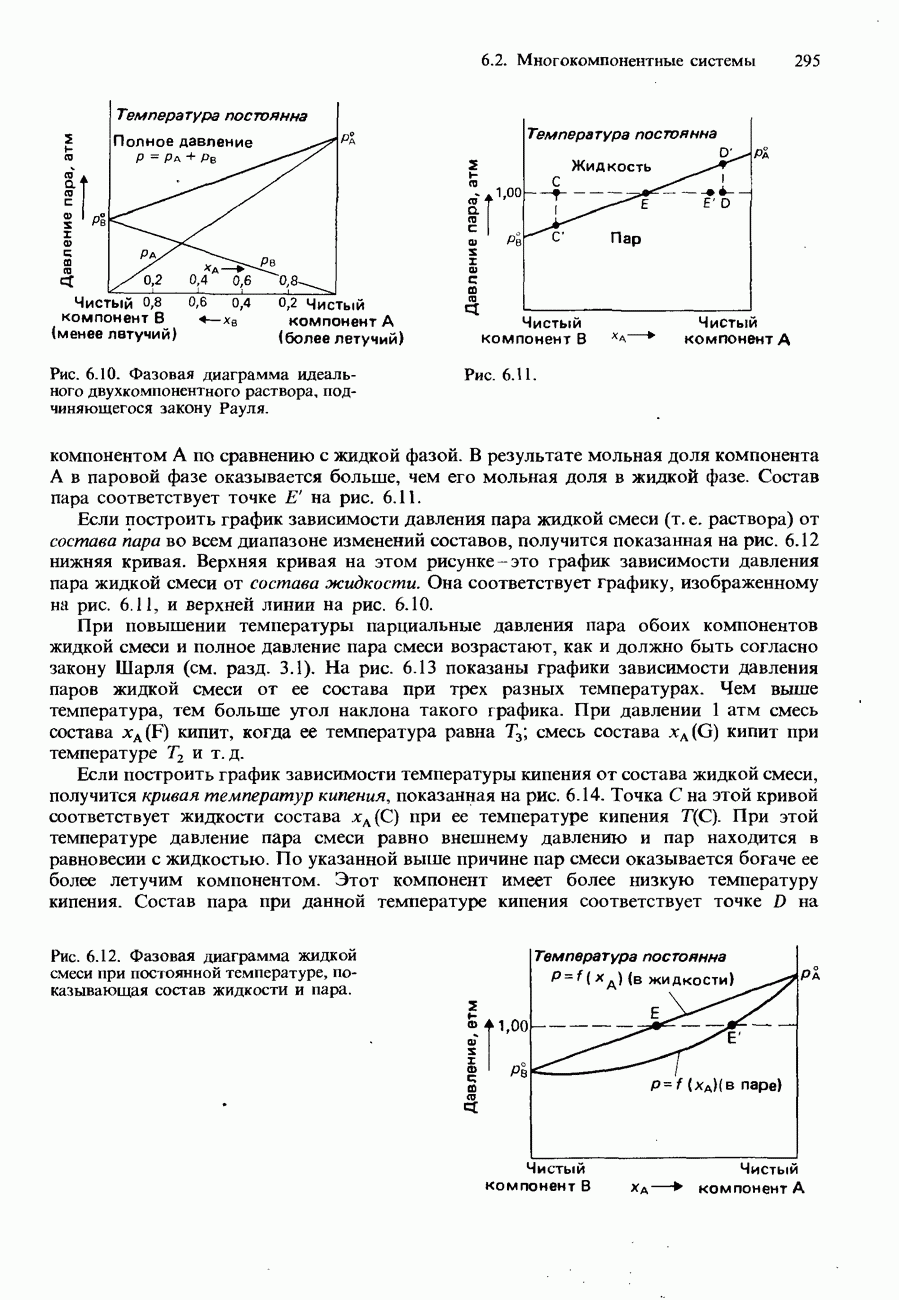
- Фазовые диаграммы полностью смешивающихся жидкостей
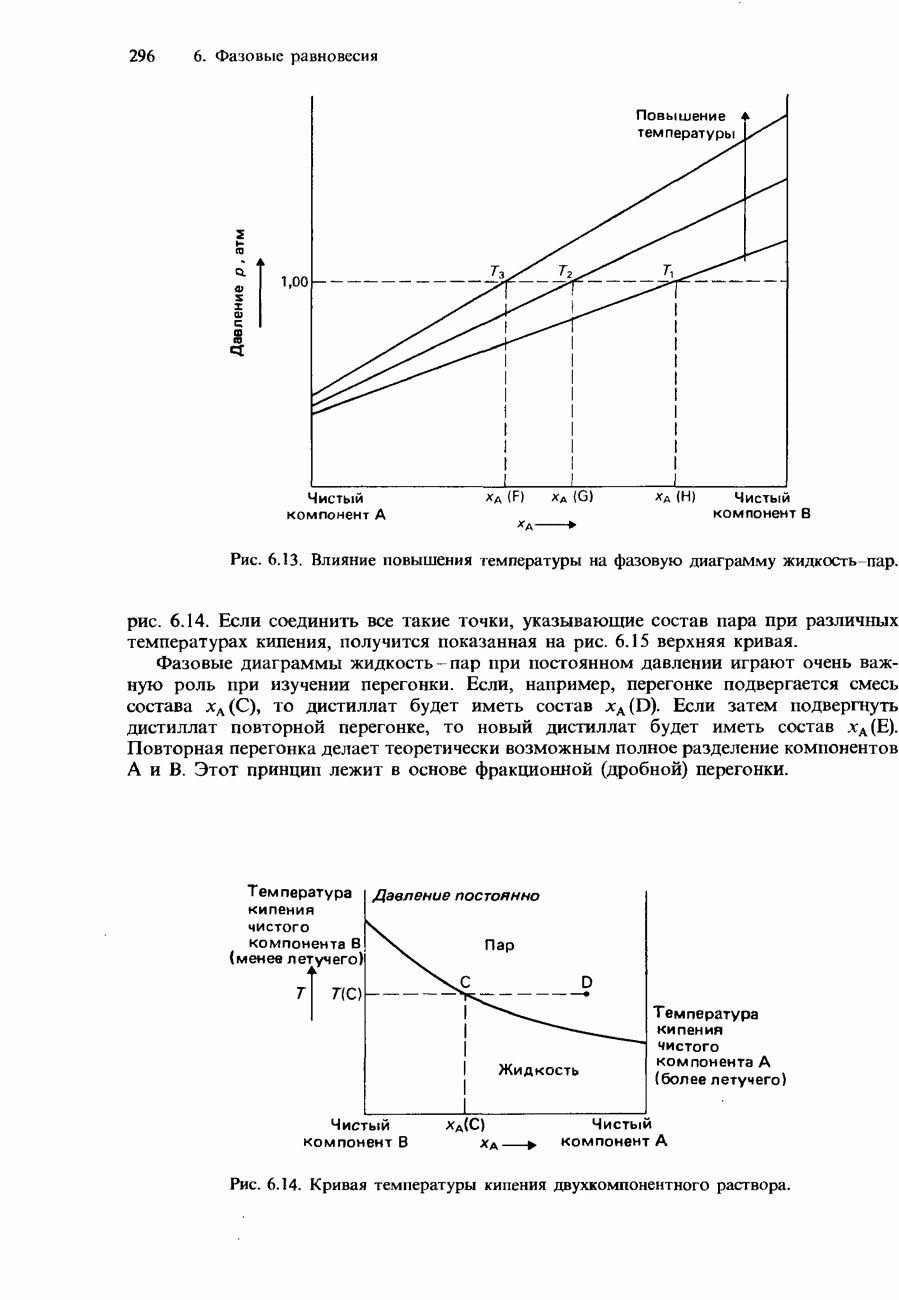
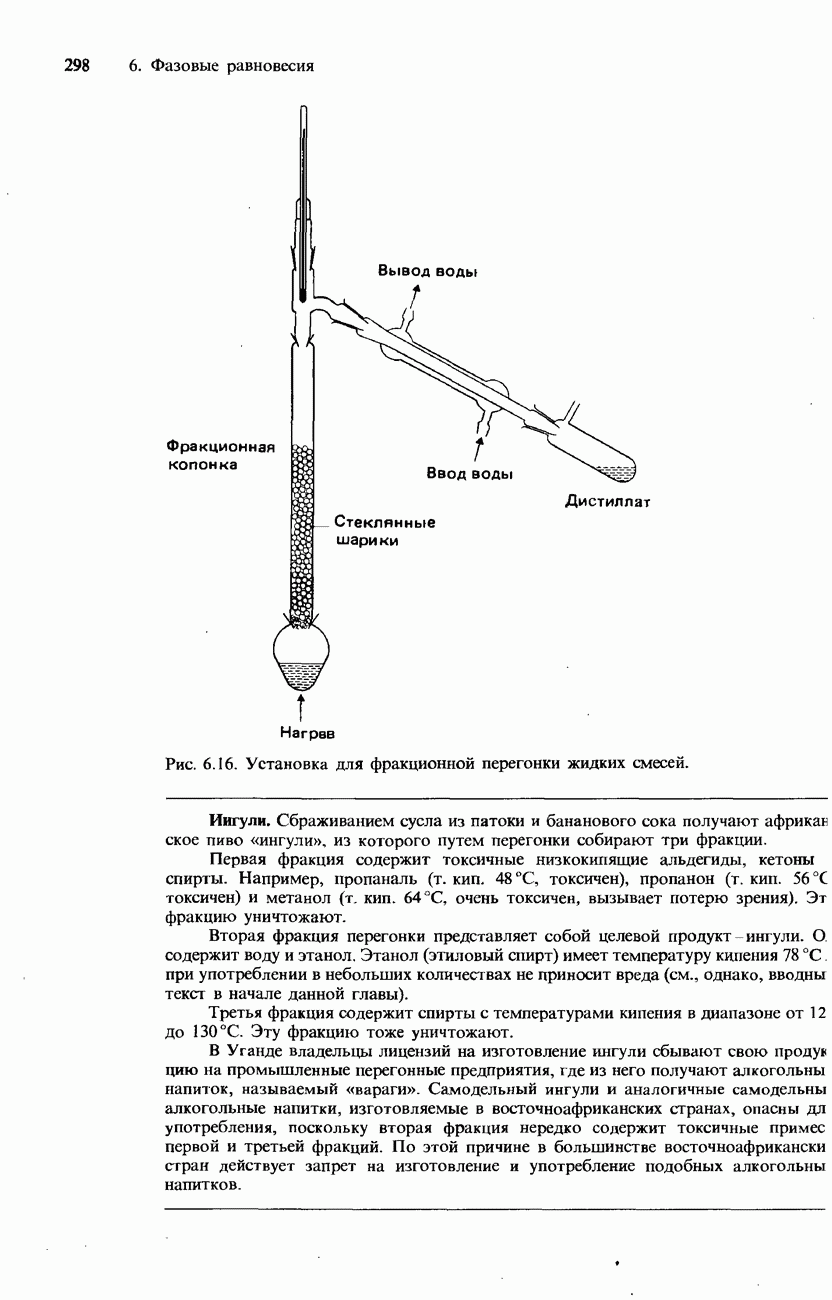
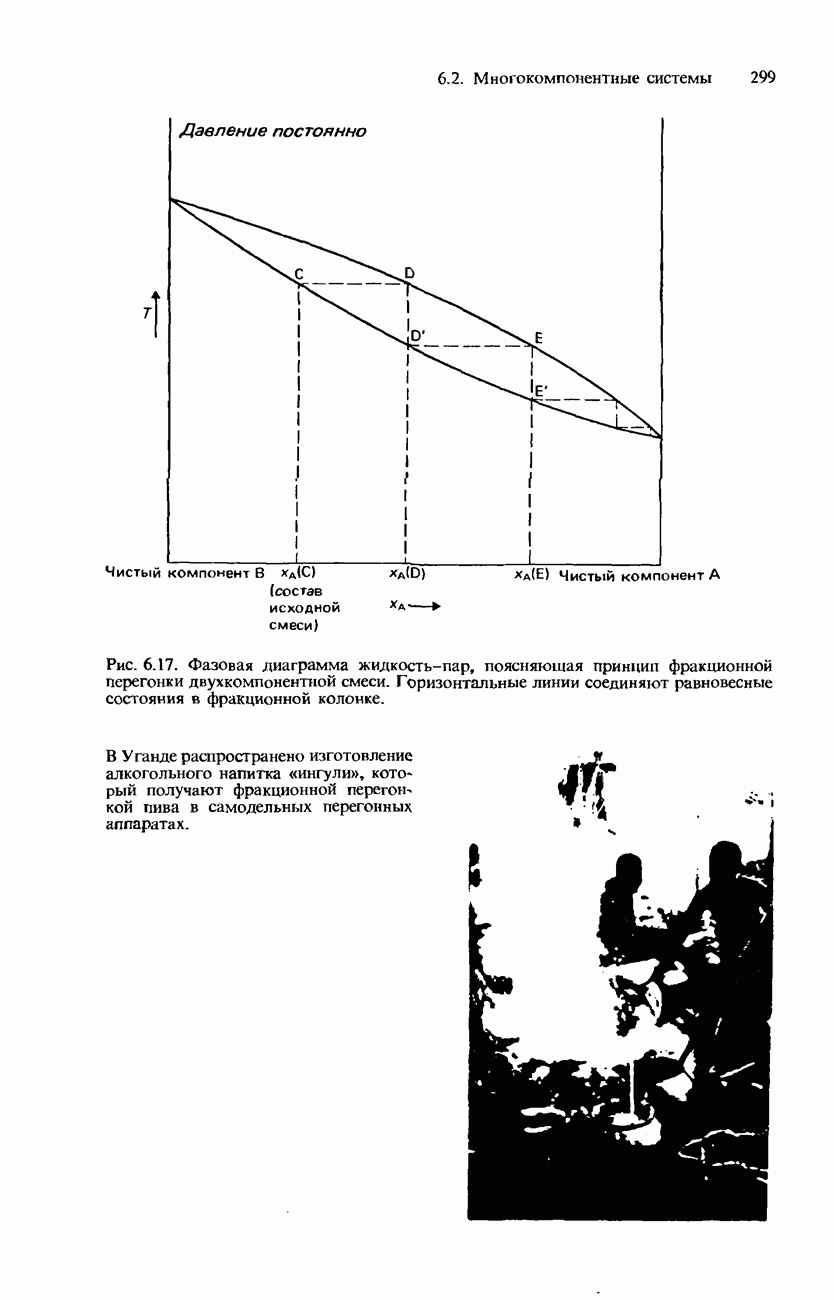
- Фракционная перегонка
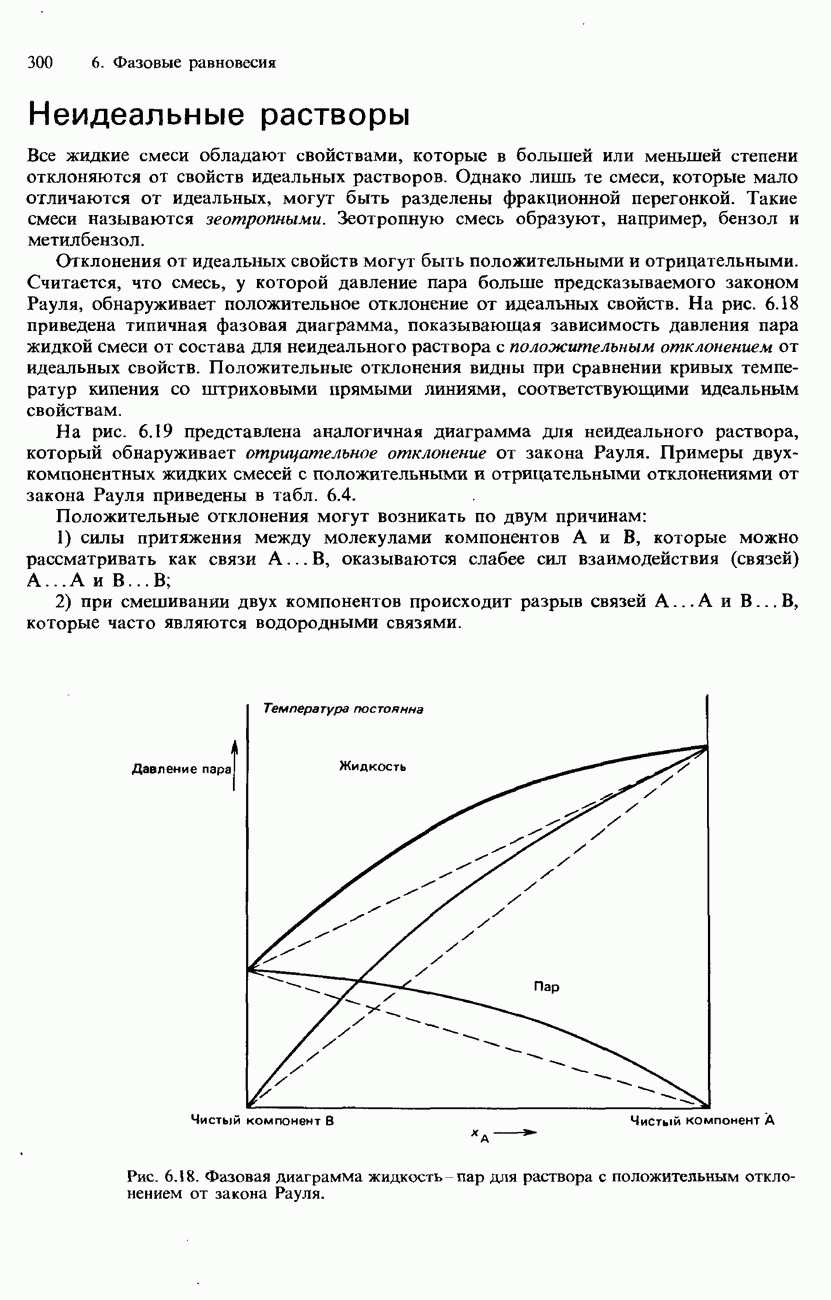
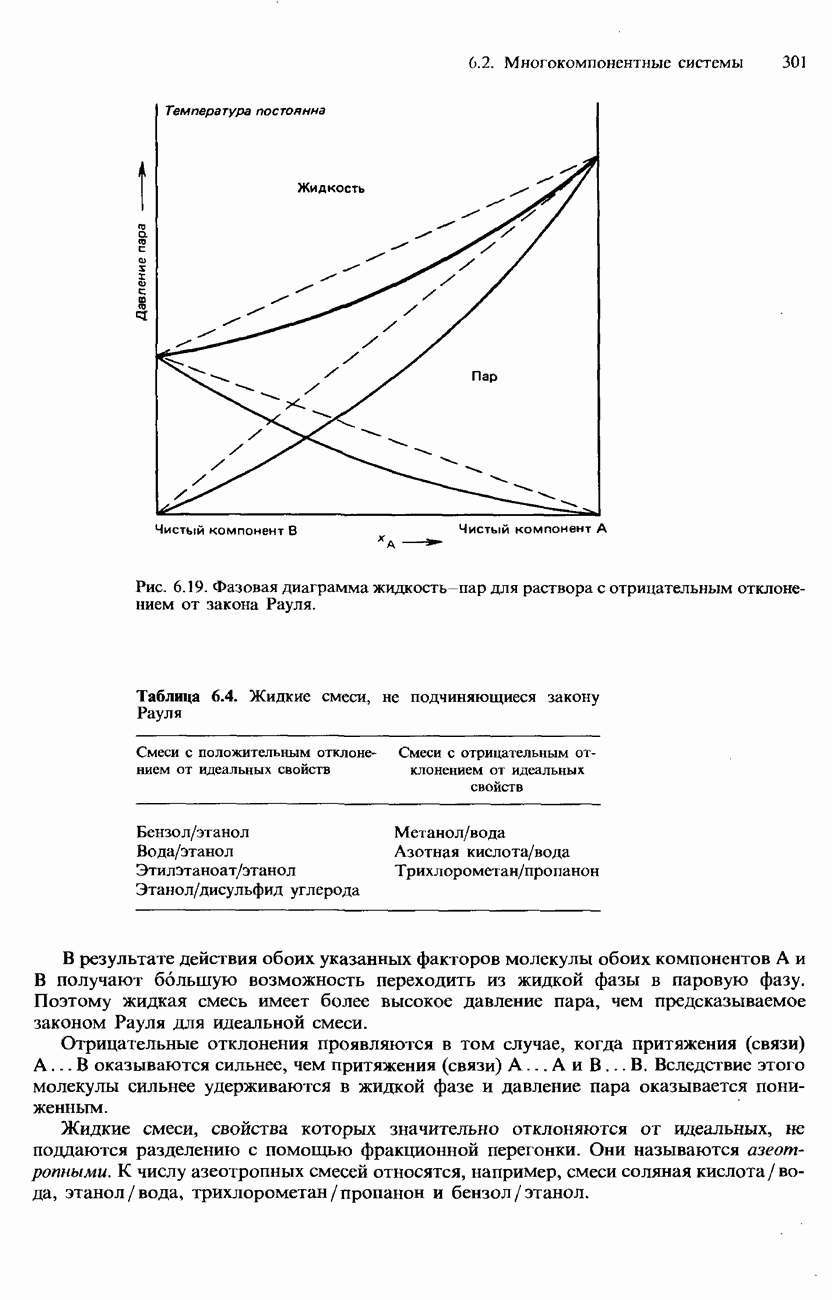
- Неидеальные растворы
- ЧАСТИЧНО СМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
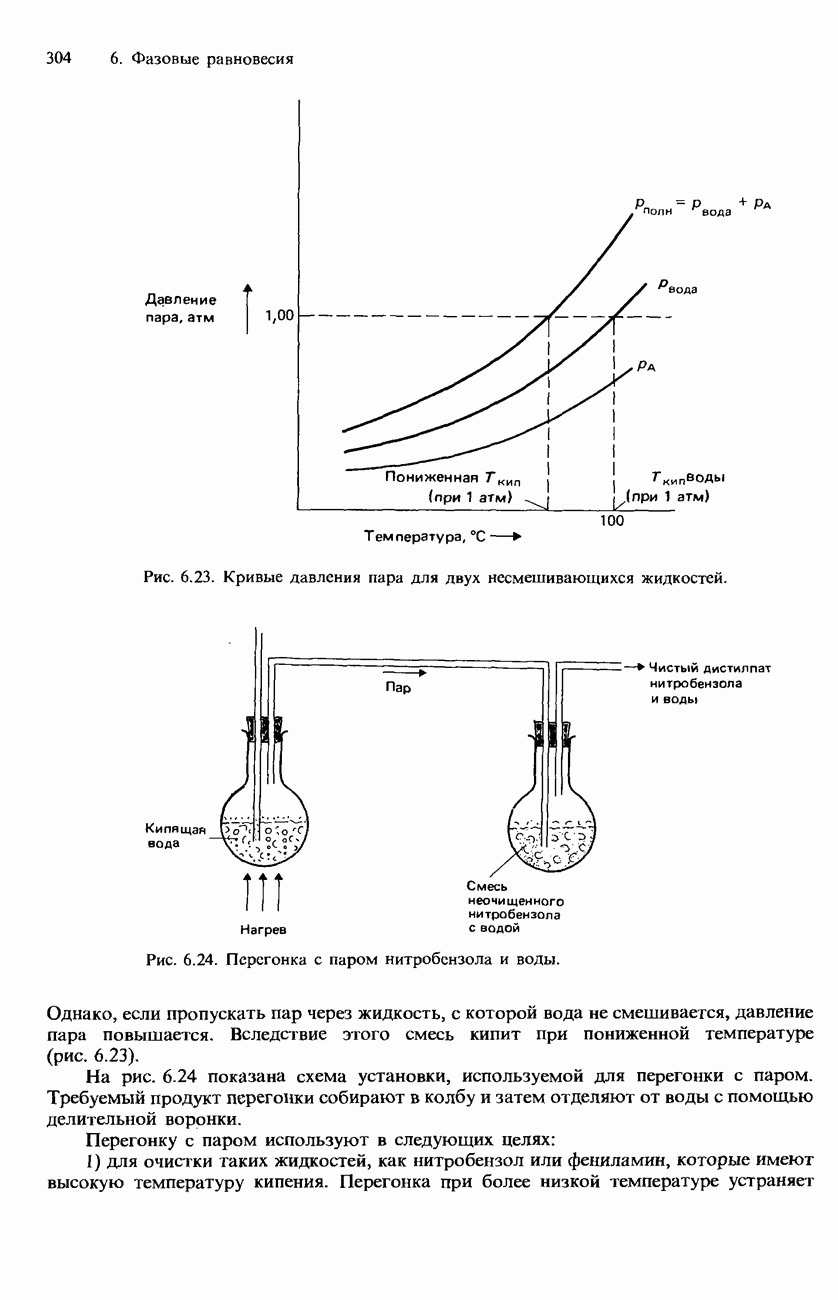
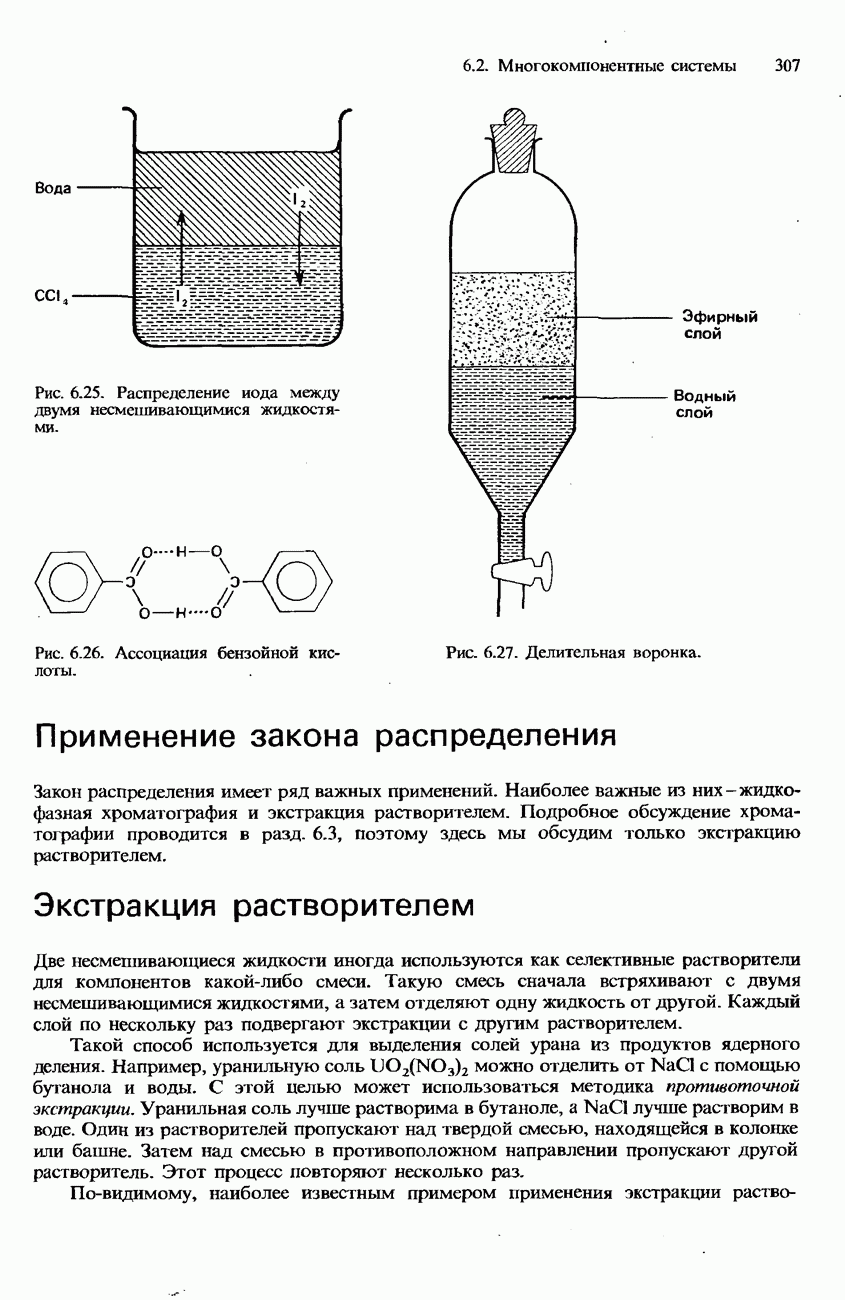
- НЕСМЕШИВАЮЩИЕСЯ ЖИДКОСТИ
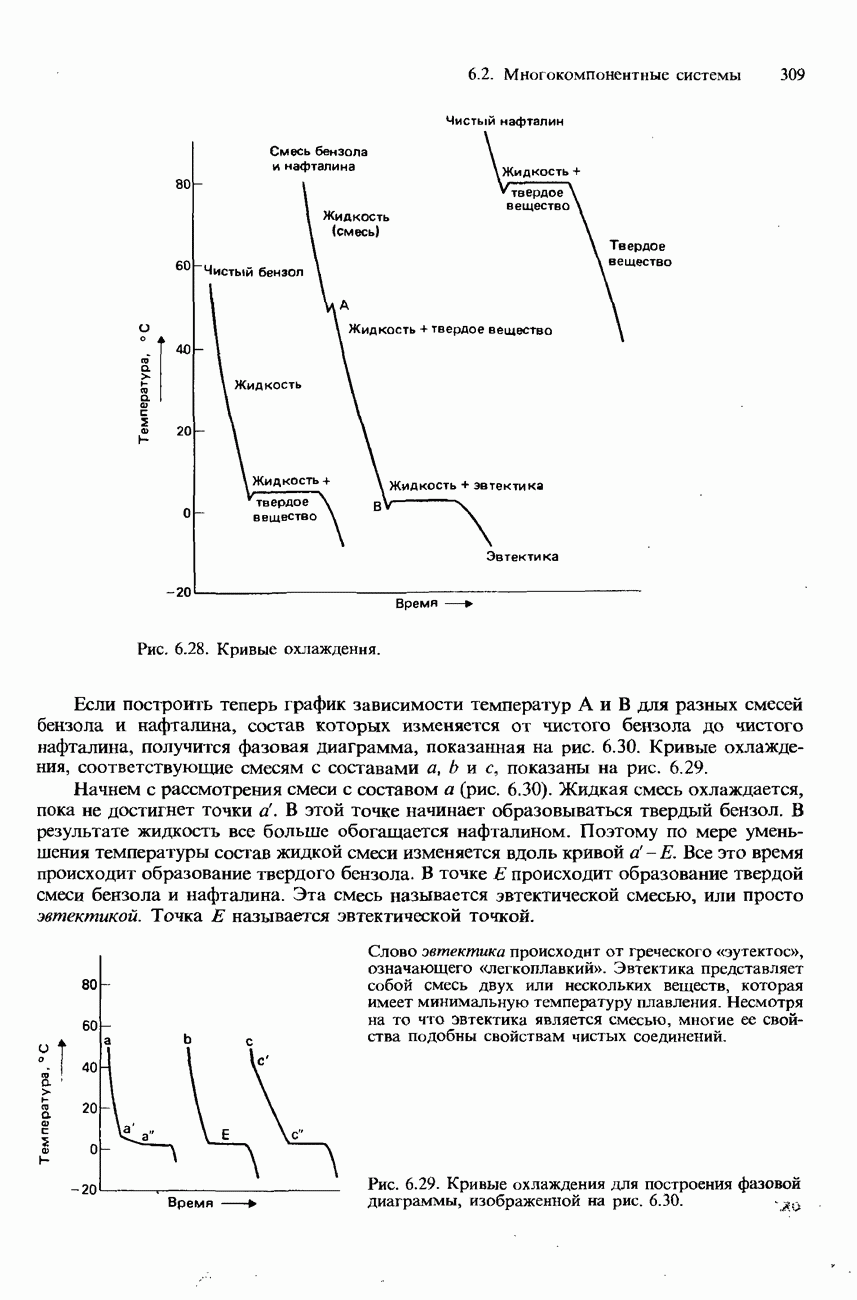
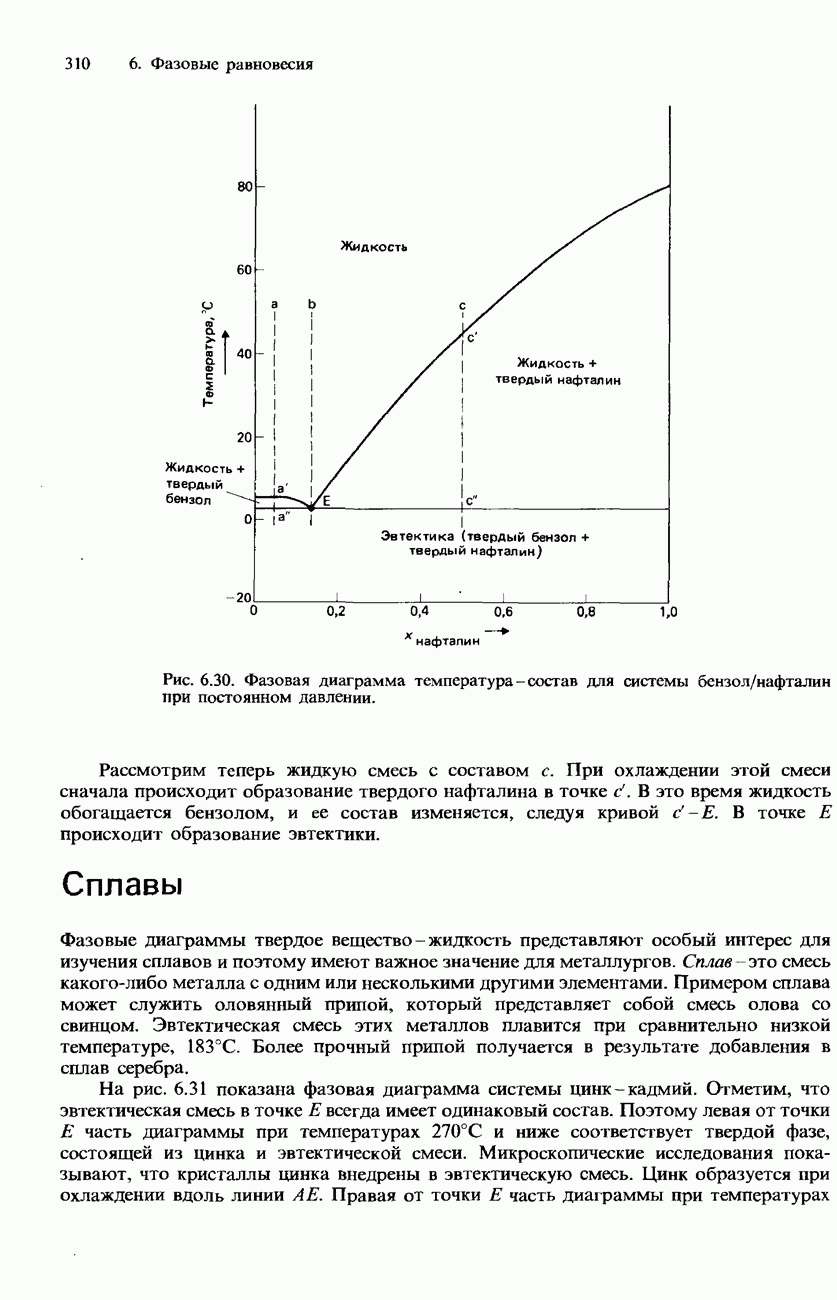
- РАВНОВЕСИЯ ТВЕРДОЕ ВЕЩЕСТВО-ЖИДКОСТЬ
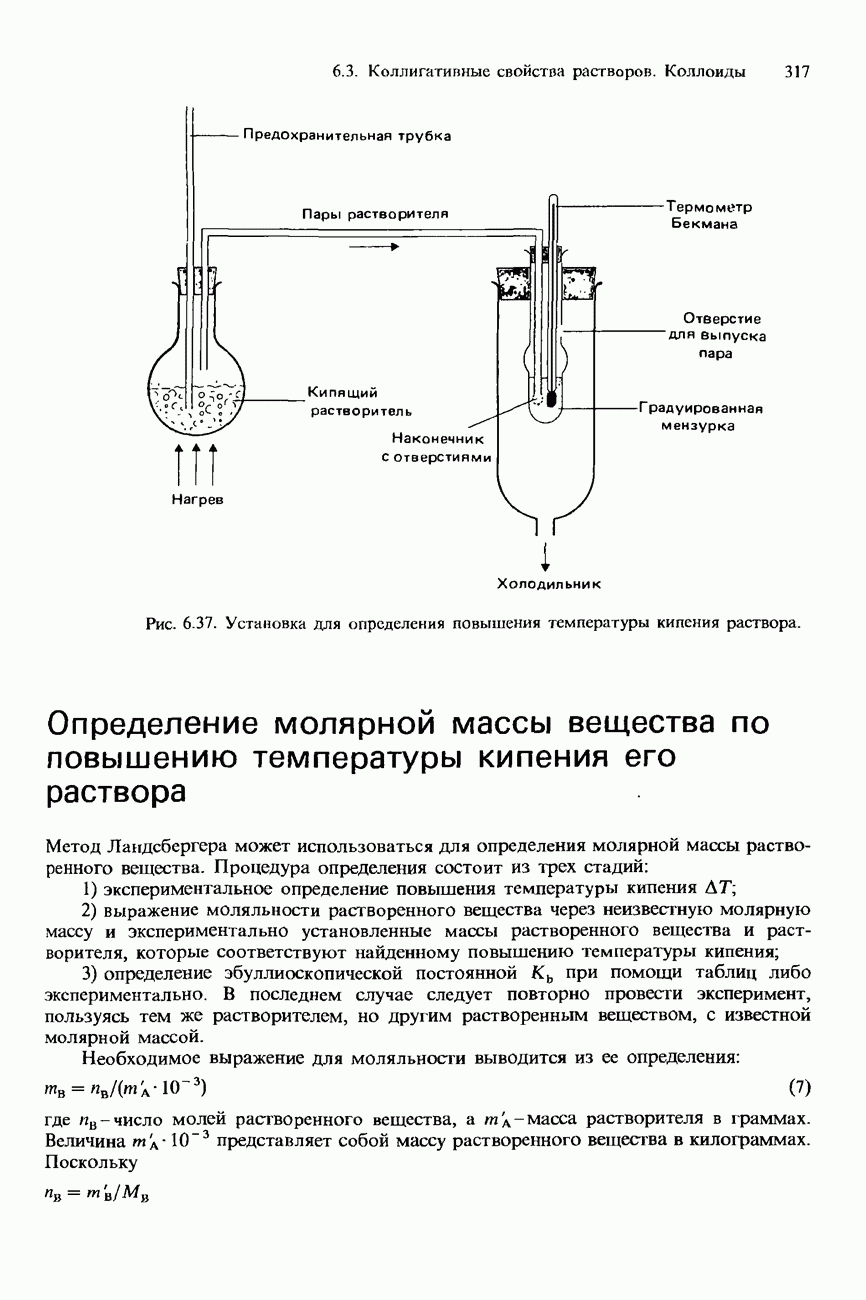
- 6.3. Коллигативные свойства растворов. Коллоиды Хроматография
- КОЛЛОИДЫ
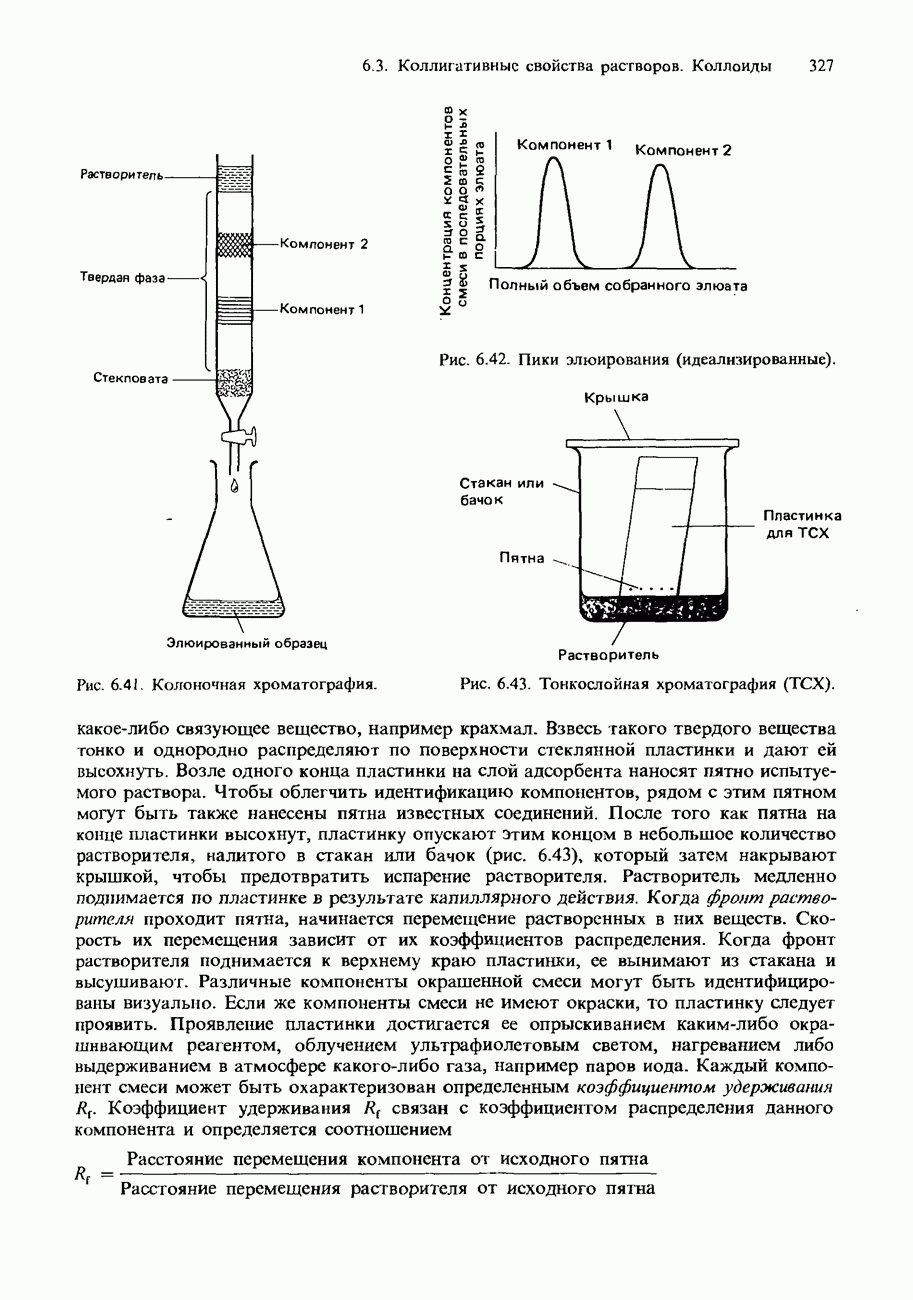
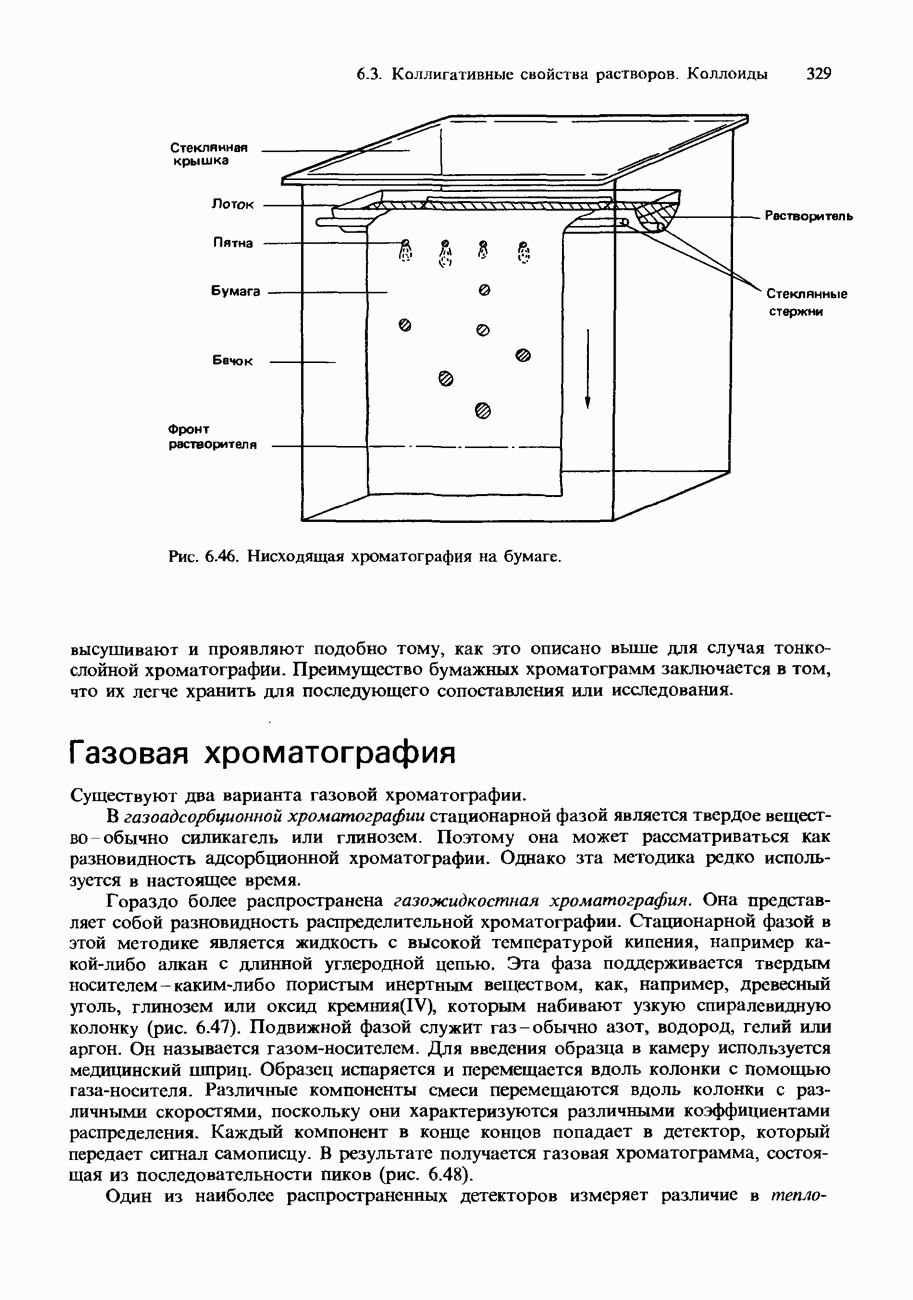
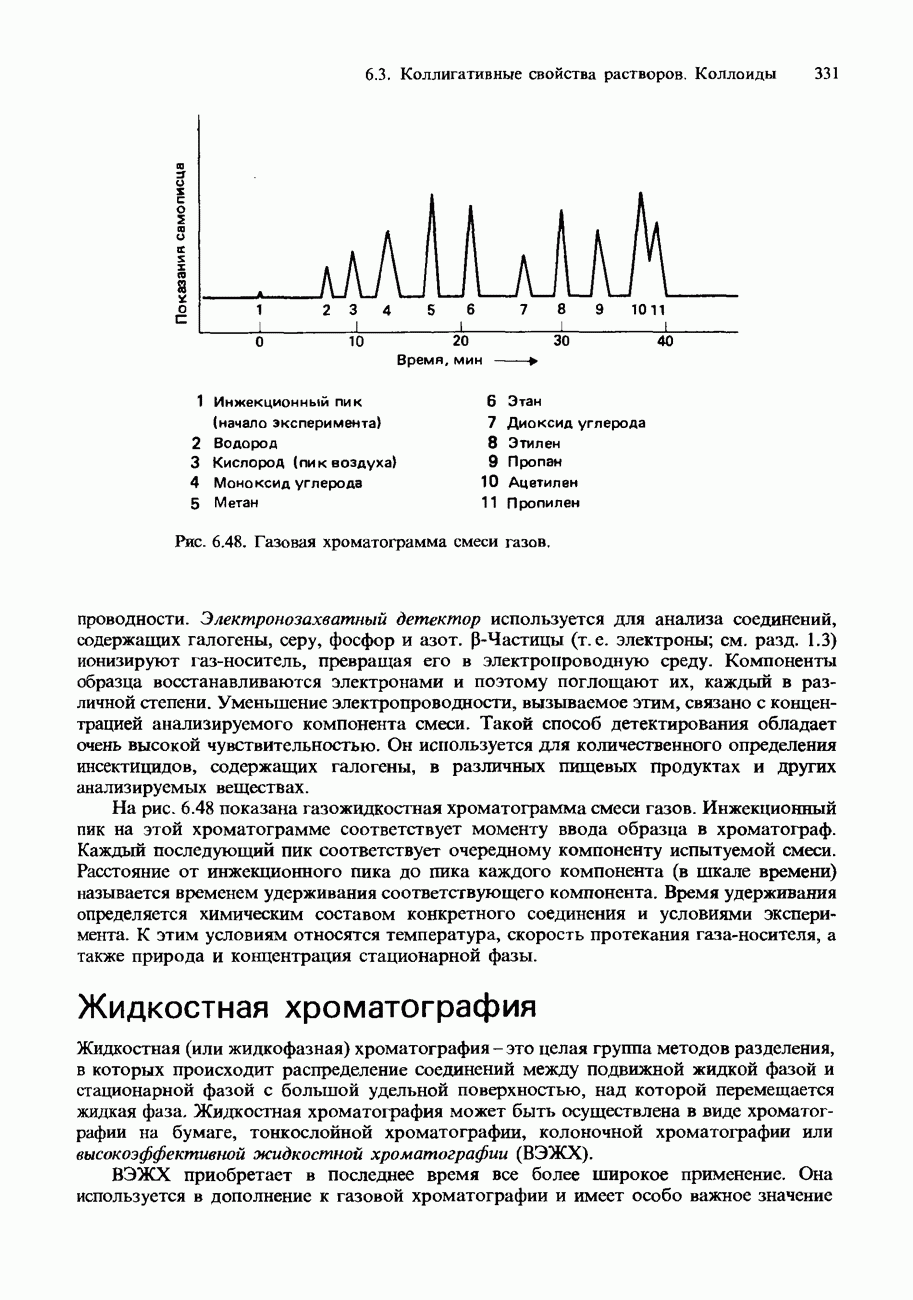
- ХРОМАТОГРАФИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 7.1. Константа равновесия
- ЗАКОН ДЕЙСТВУЮЩИХ МАСС
- ВЛИЯНИЕ УСЛОВИЙ ПРОТЕКАНИЯ РЕАКЦИИ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ
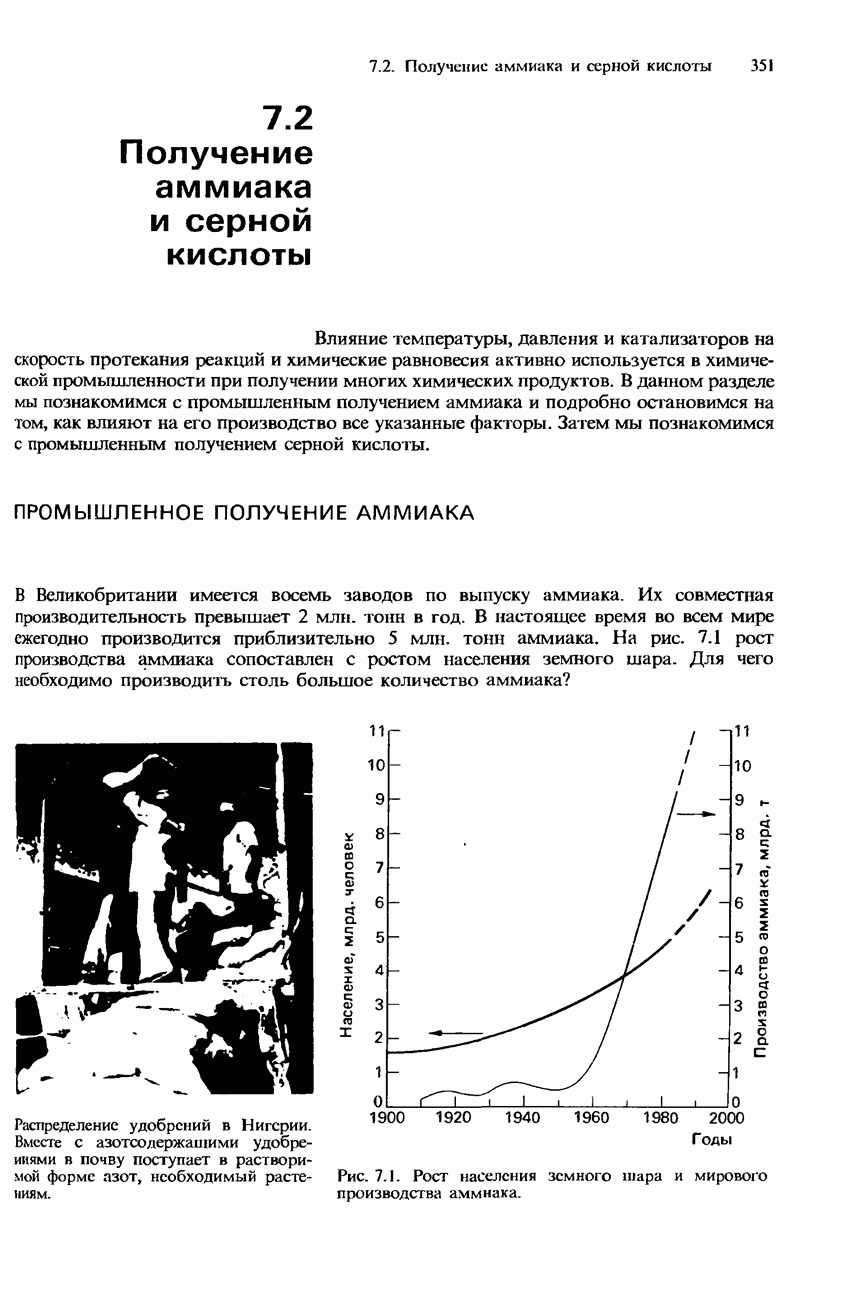
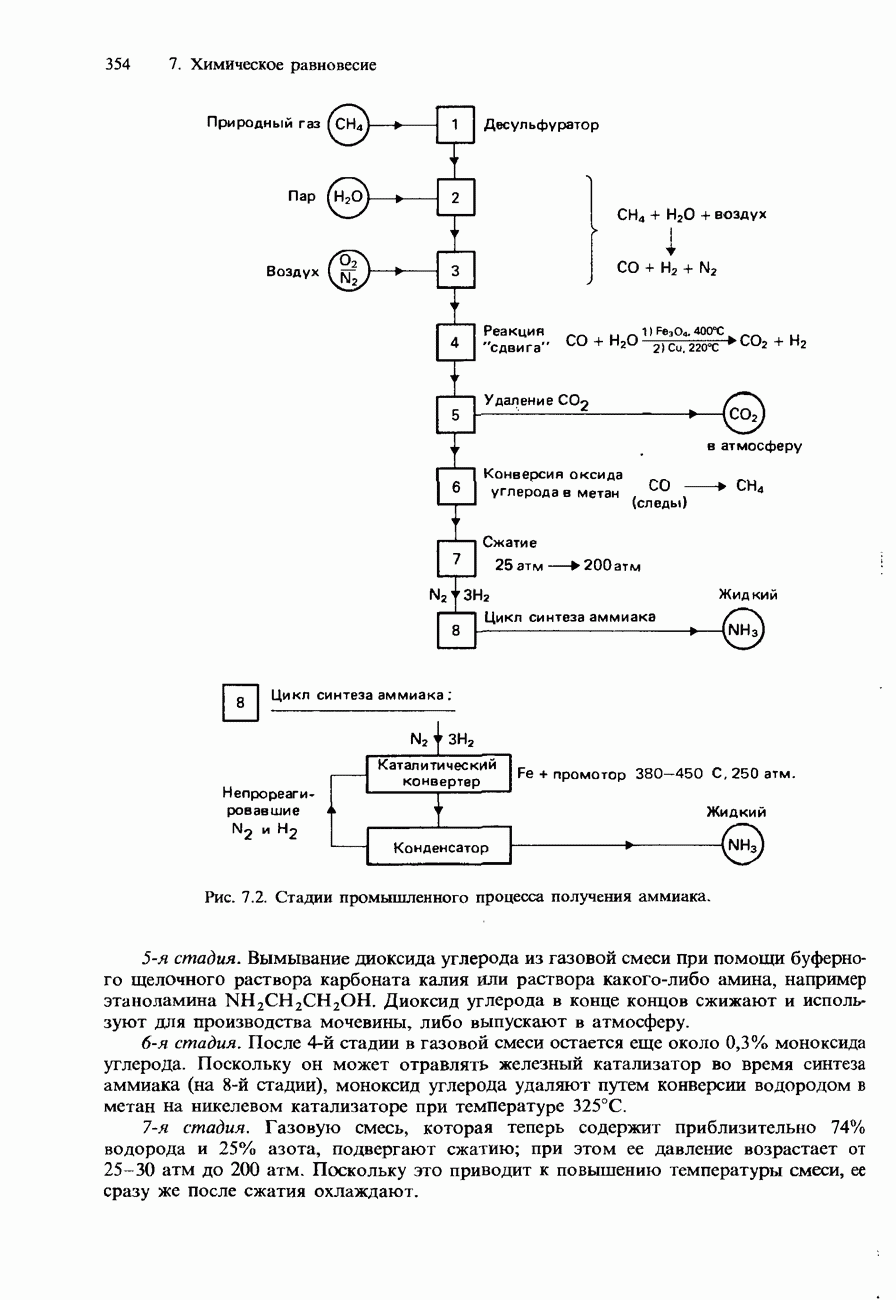
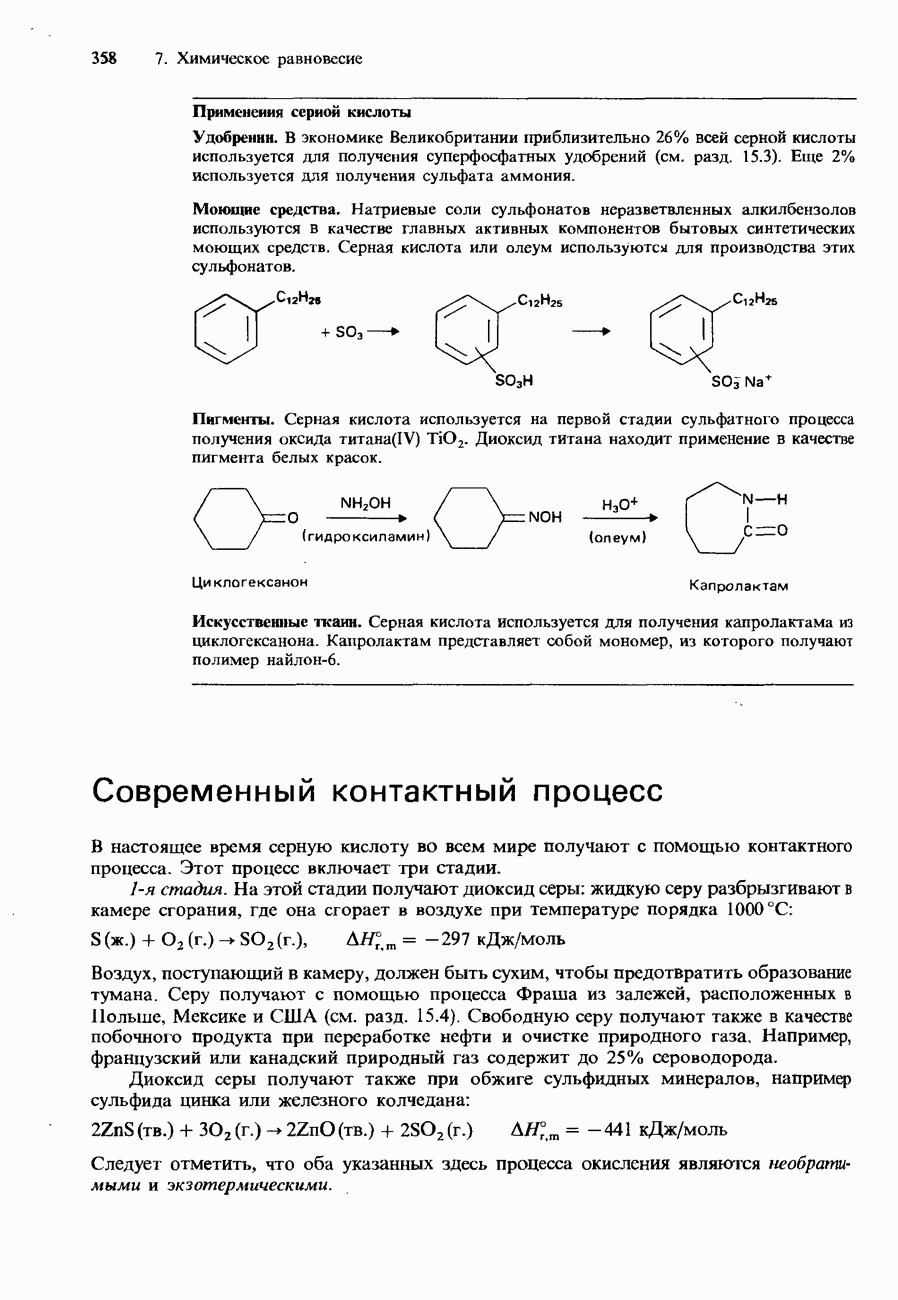
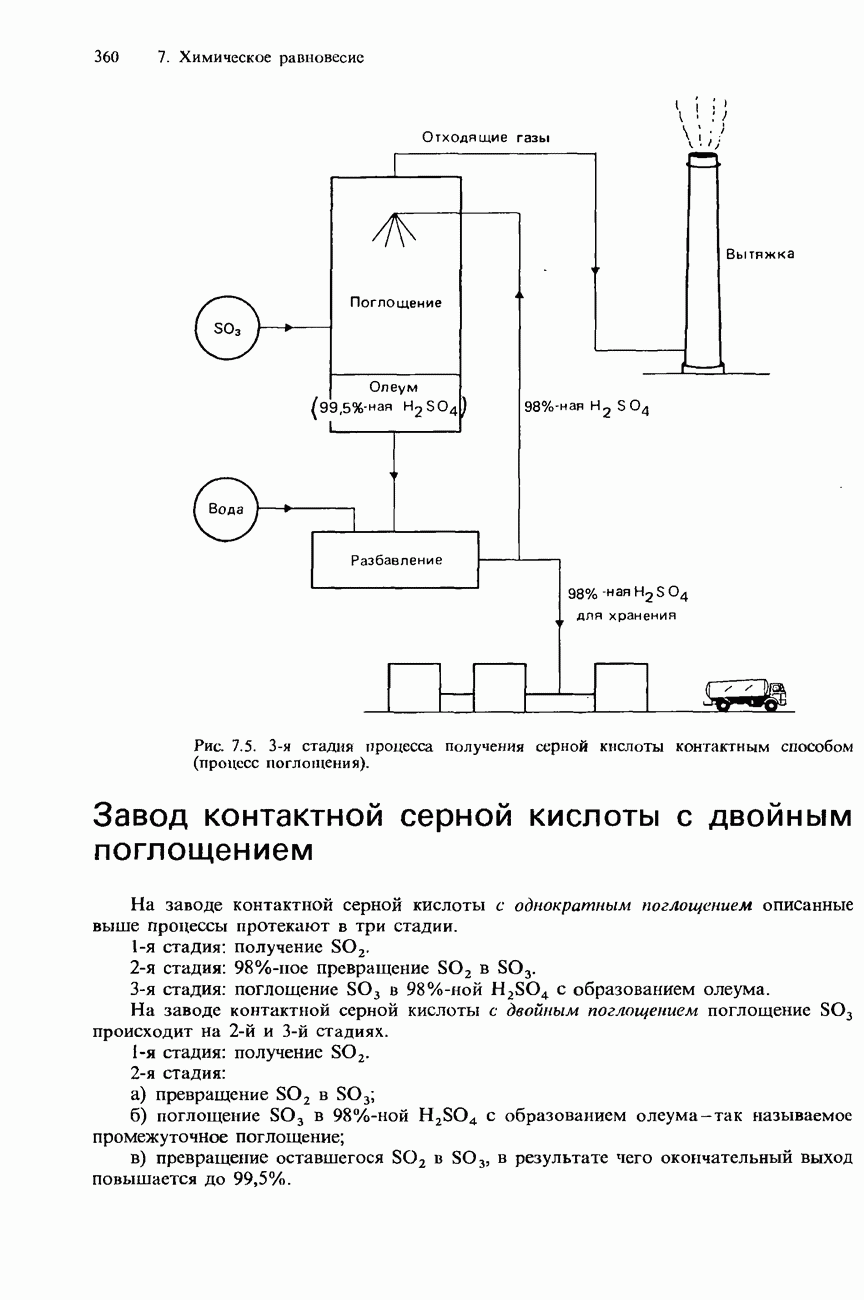
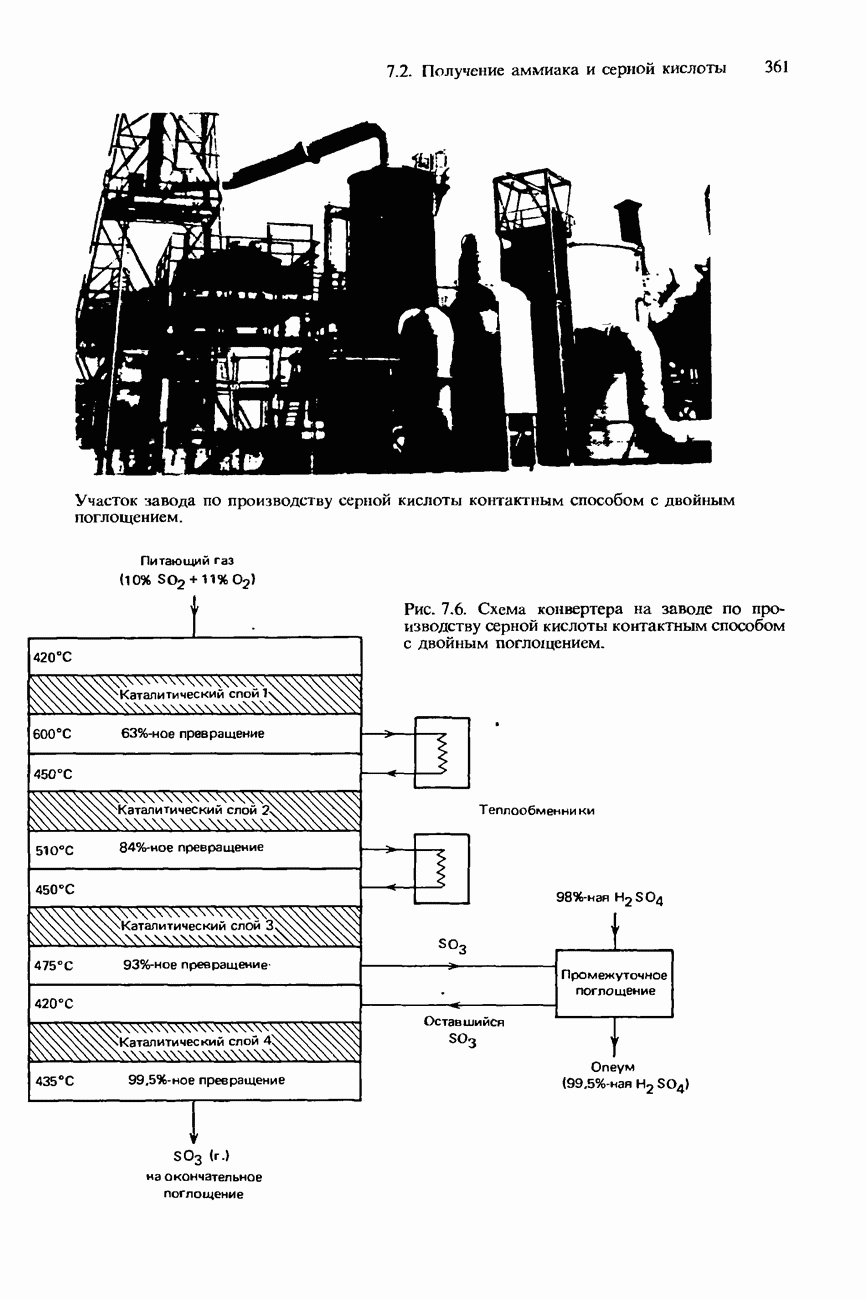
- 7.2. Получение аммиака и серной кислоты
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СЕРНОЙ КИСЛОТЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 8. ИОНЫ
- 8.1. Кислоты и основания
- ЭЛЕКТРОЛИТЫ
- КИСЛОТЫ И ОСНОВАНИЯ
- КОНСТАНТЫ ДИССОЦИАЦИИ
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ pH ШКАЛА ЕГО ЗНАЧЕНИЙ
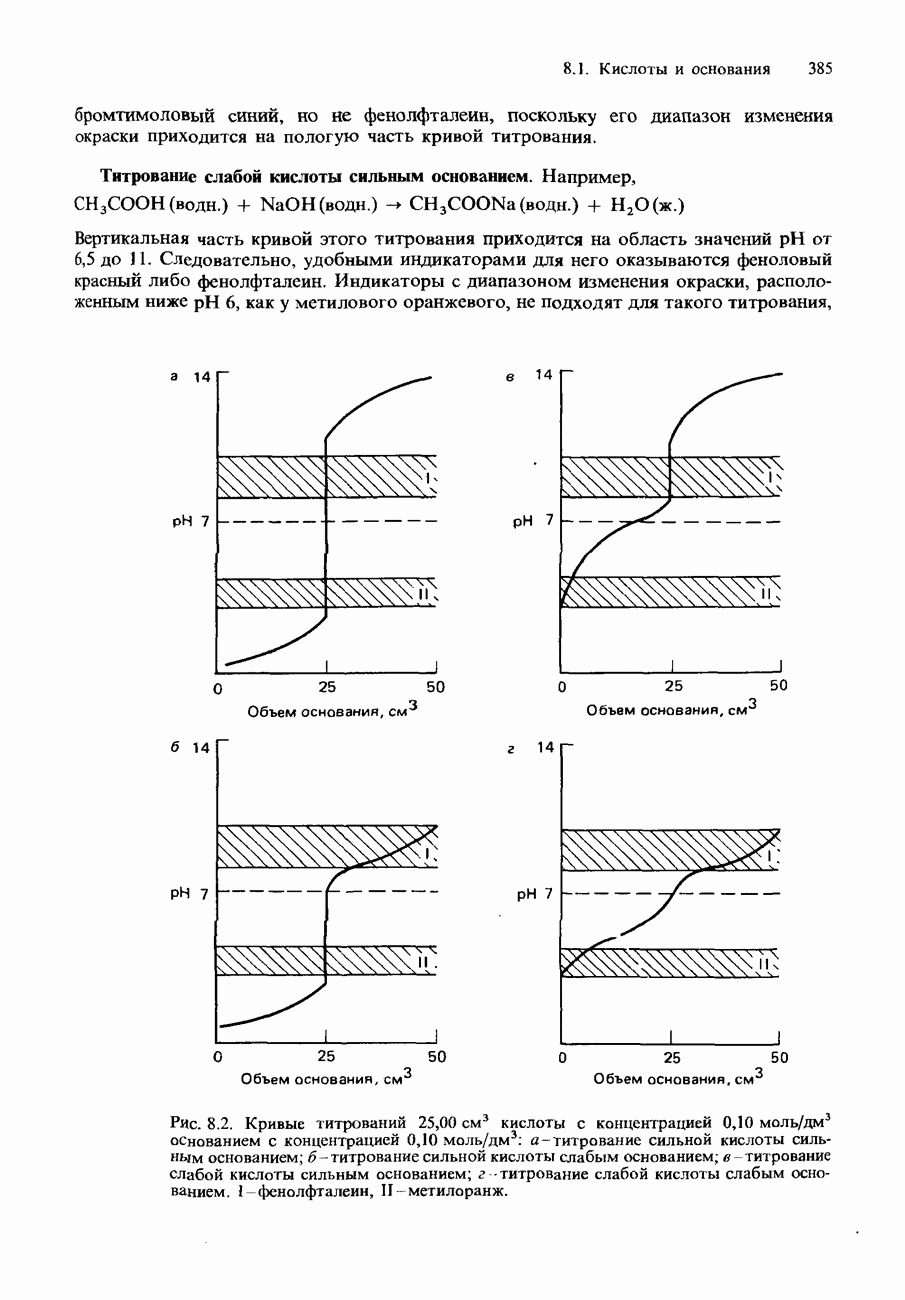
- КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ И ТИТРОВАНИЕ
- 8.2. Соли, растворимость и устойчивость
- БУФЕРНЫЕ РАСТВОРЫ
- РАСТВОРИМОСТЬ
- РАВНОВЕСИЯ С УЧАСТИЕМ КОМПЛЕКСНЫХ ИОНОВ
- ИОННЫЙ ОБМЕН
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 9. ХИМИЧЕСКАЯ КИНЕТИКА
- 9.1. Скорость химической реакции
- МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСТИ РЕАКЦИЙ
- СКОРОСТЬ РЕАКЦИИ И КОНЦЕНТРАЦИИ РЕАГЕНТОВ
- ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ УРАВНЕНИЕ АРРЕНИУСА
- 9.2. Механизмы реакций и катализ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ
- ЦЕПНЫЕ РЕАКЦИИ
- КАТАЛИЗ
- ТИПЫ КАТАЛИЗАТОРОВ
- ГОМОГЕННЫЙ КАТАЛИЗ
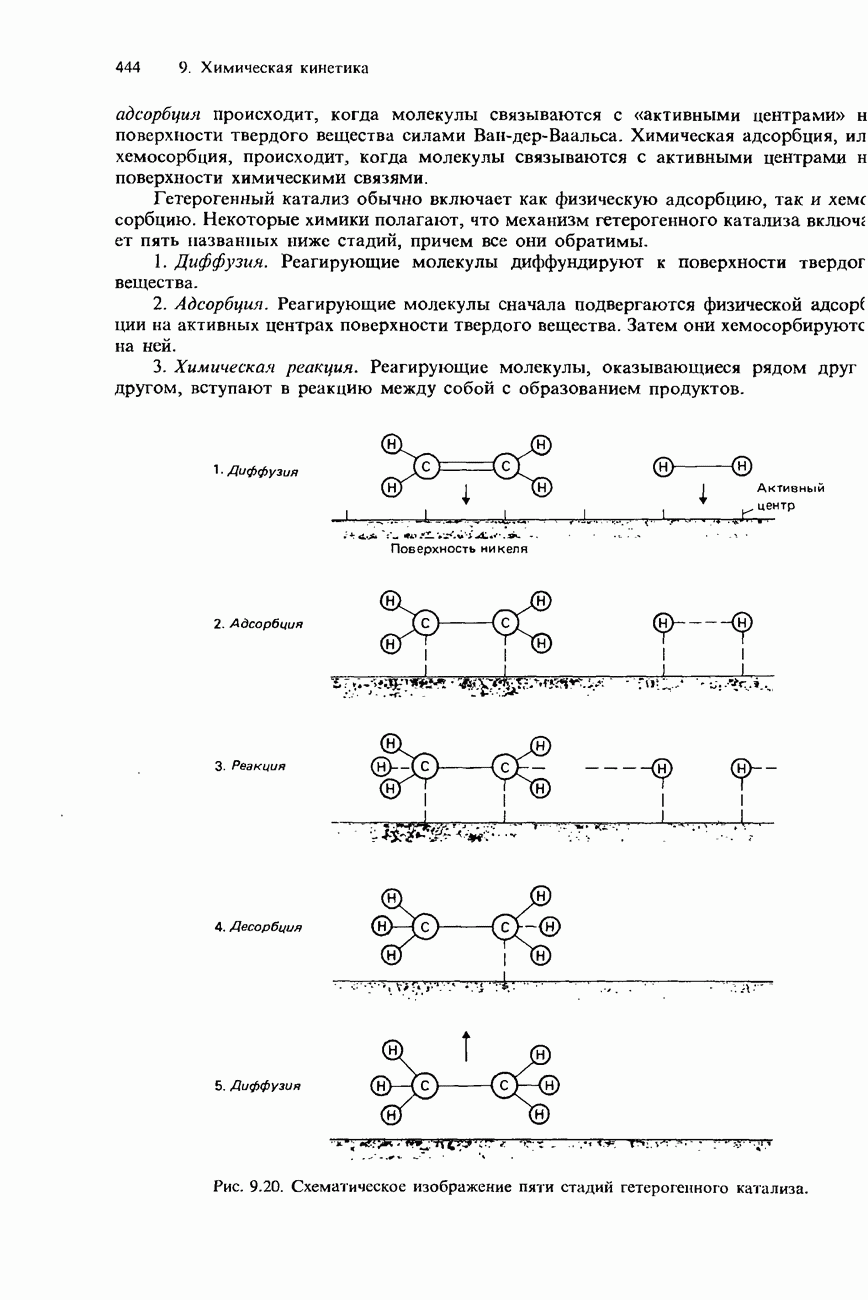
- ГЕТЕРОГЕННЫЙ КАТАЛИЗ
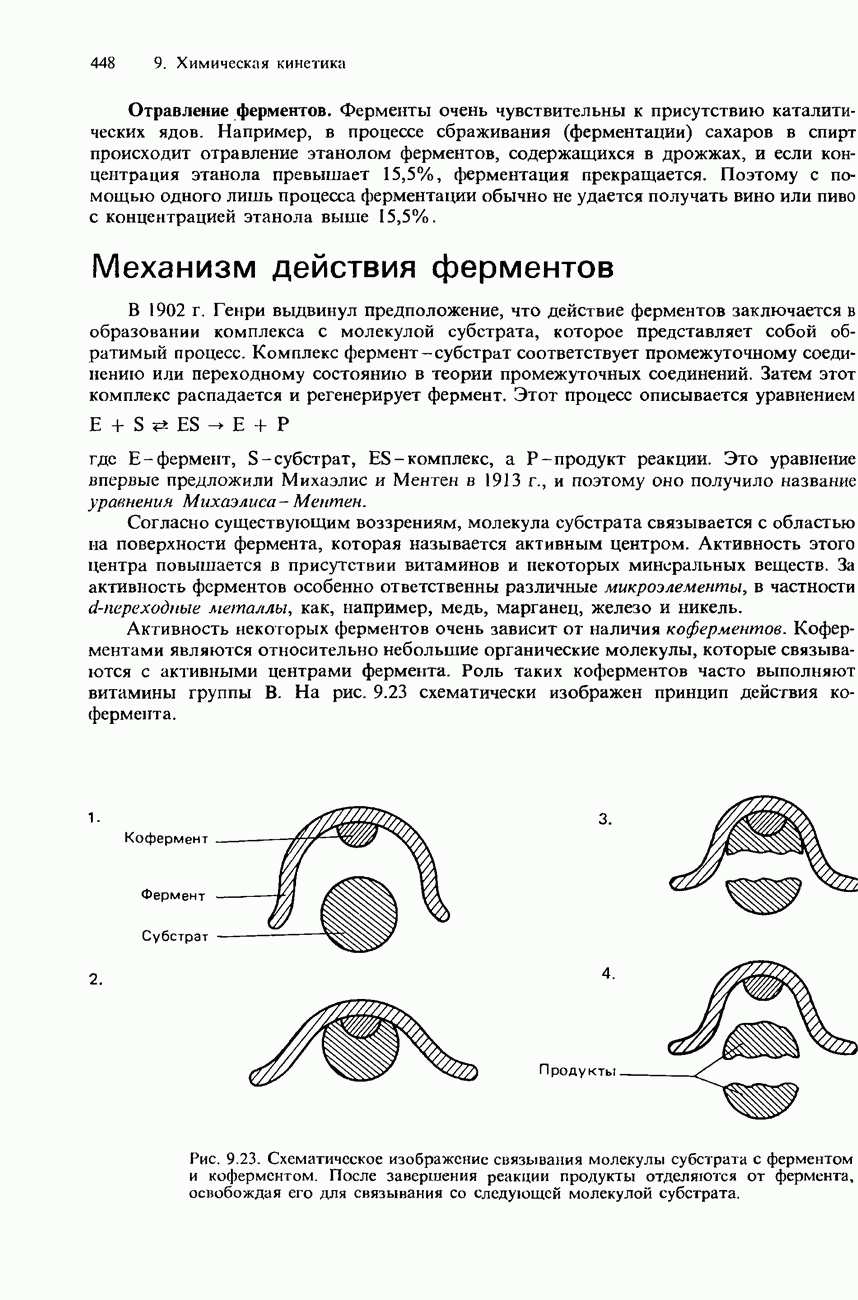
- ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 10. ЭЛЕКТРОХИМИЯ
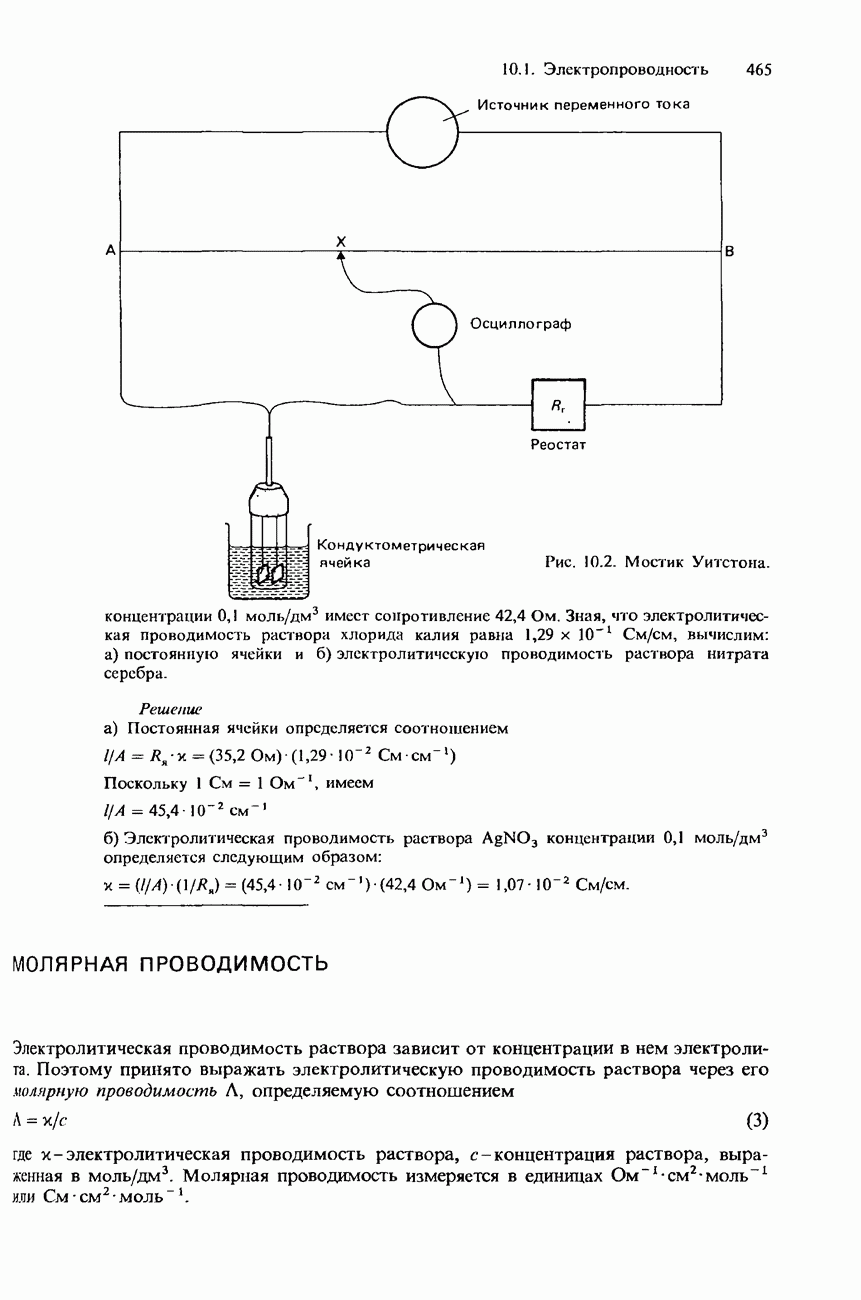
- 10.1. Электропроводность
- ПРОВОДНИКИ ЭЛЕКТРИЧЕСКОГО ТОКА И ЭЛЕКТРОПРОВОДНОСТЬ
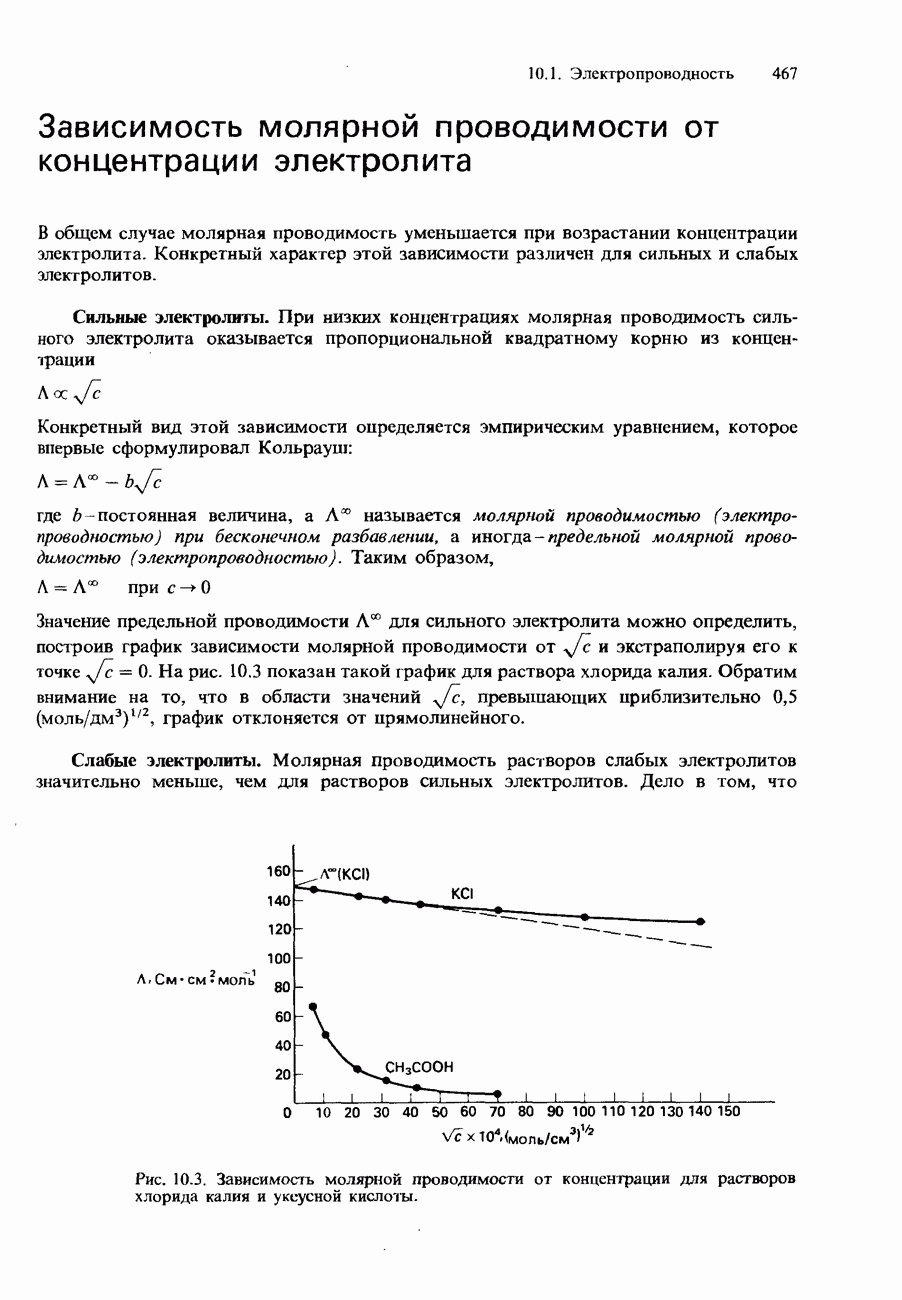
- МОЛЯРНАЯ ПРОВОДИМОСТЬ
- КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 10.2. Окислительно-восстановительные процессы
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ КОЭФФИЦИЕНТОВ
- СТЕПЕНЬ ОКИСЛЕНИЯ
- ОКИСЛИТЕЛИ
- ВОССТАНОВИТЕЛИ
- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ
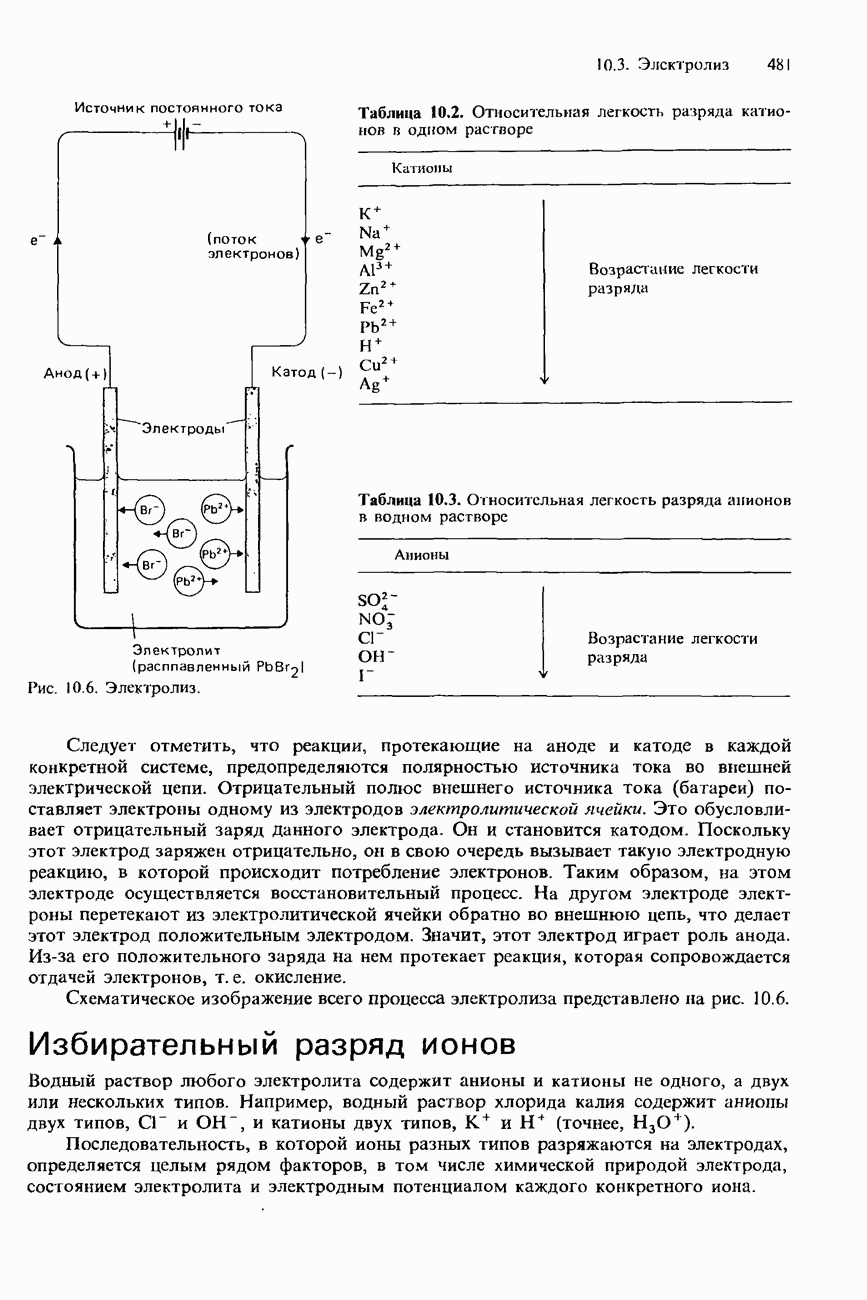
- 10.3. Электролиз
- ЗАКОНЫ ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- ПРОМЫШЛЕННЫЕ ПРИМЕНЕНИЯ ЭЛЕКТРОЛИЗА
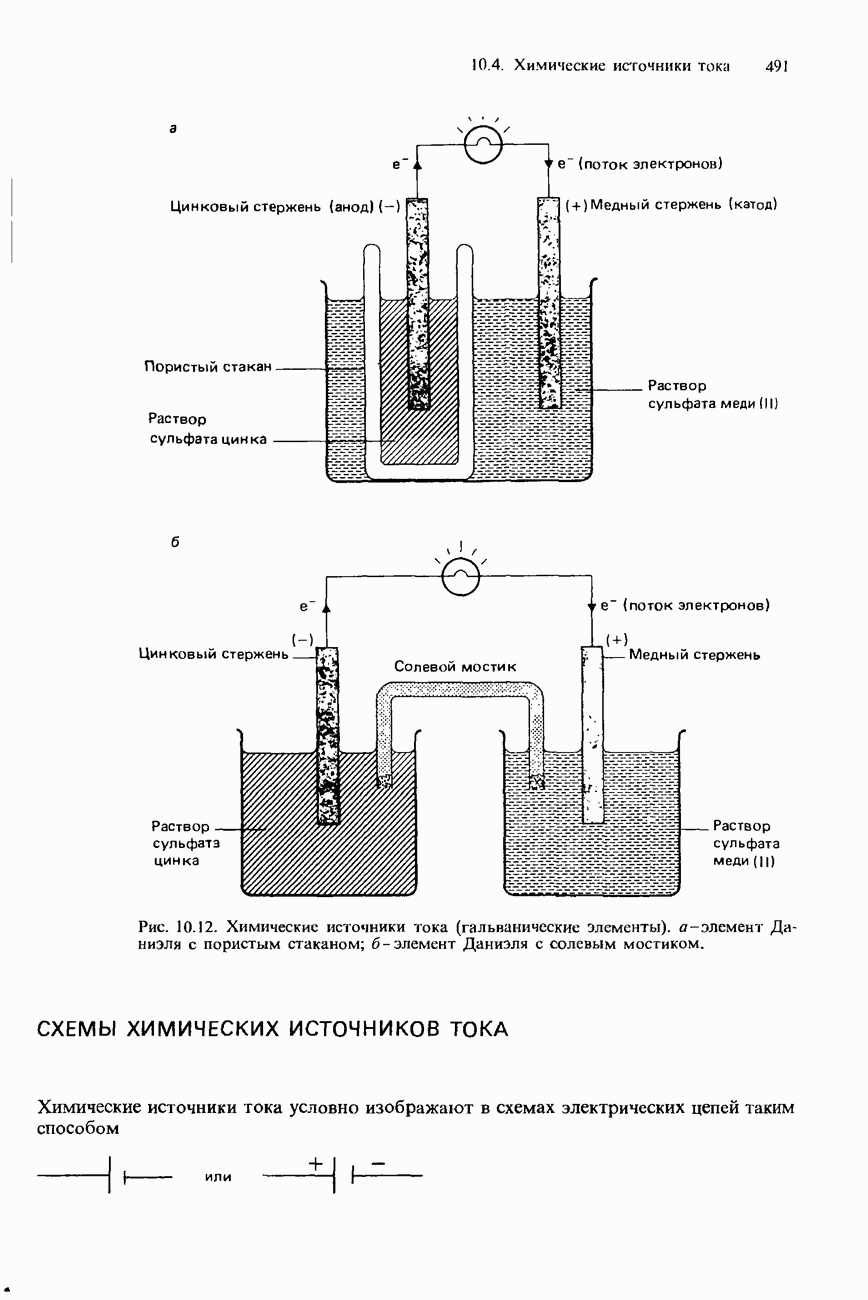
- 10.4. Химические источники тока
- СХЕМЫ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ТИПЫ ПОЛУЭЛЕМЕНТОВ
- ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ
- ЭЛЕКТРОДВИЖУЩАЯ СИЛА ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА
- ИЗМЕРЕНИЕ Э.Д.С. ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА И ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ
- 10.5. Применения электрохимии
- ВЫЧИСЛЕНИЕ КОНСТАНТ РАВНОВЕСИЯ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ pH РАСТВОРА
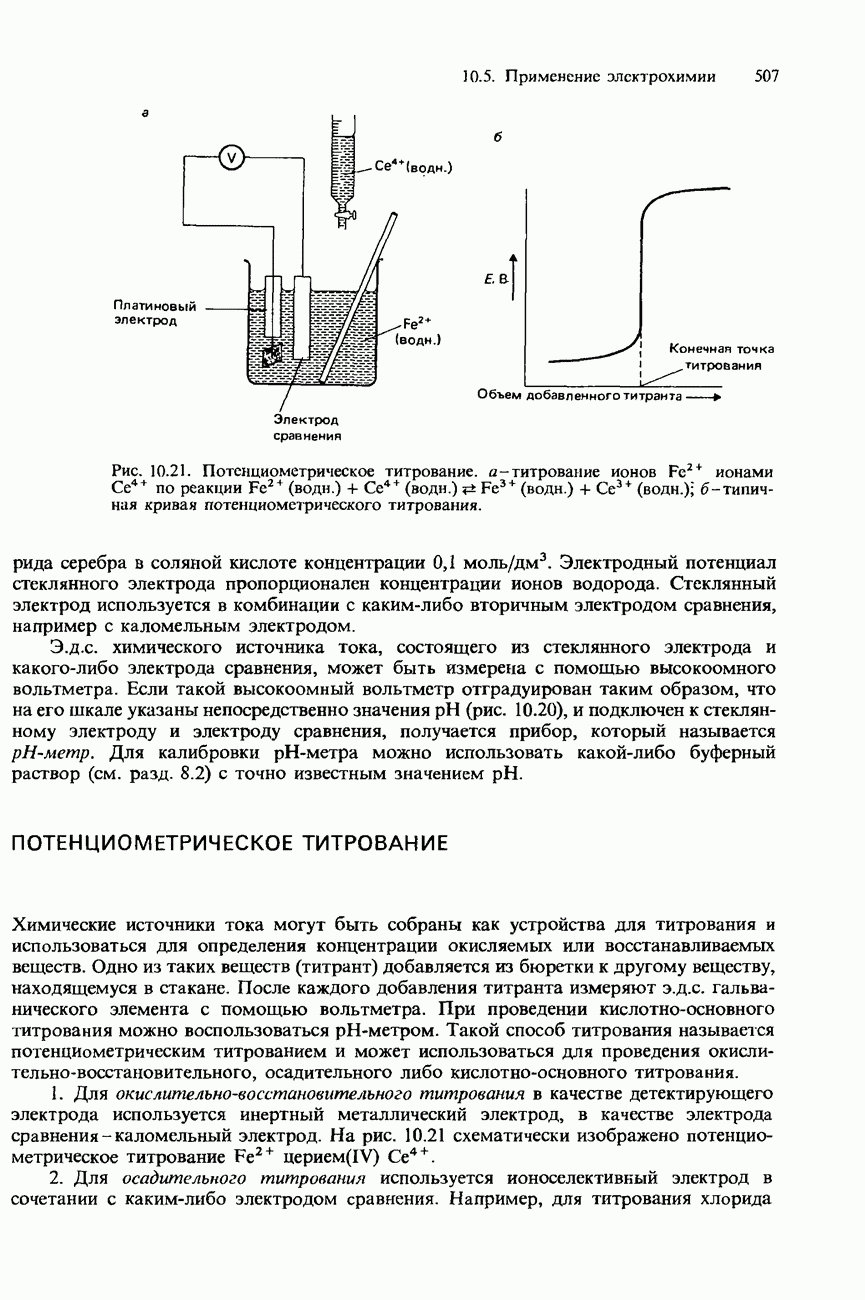
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- ОСУЩЕСТВИМОСТЬ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- ОПРЕДЕЛЕНИЕ ВЕЛИЧИНЫ AG
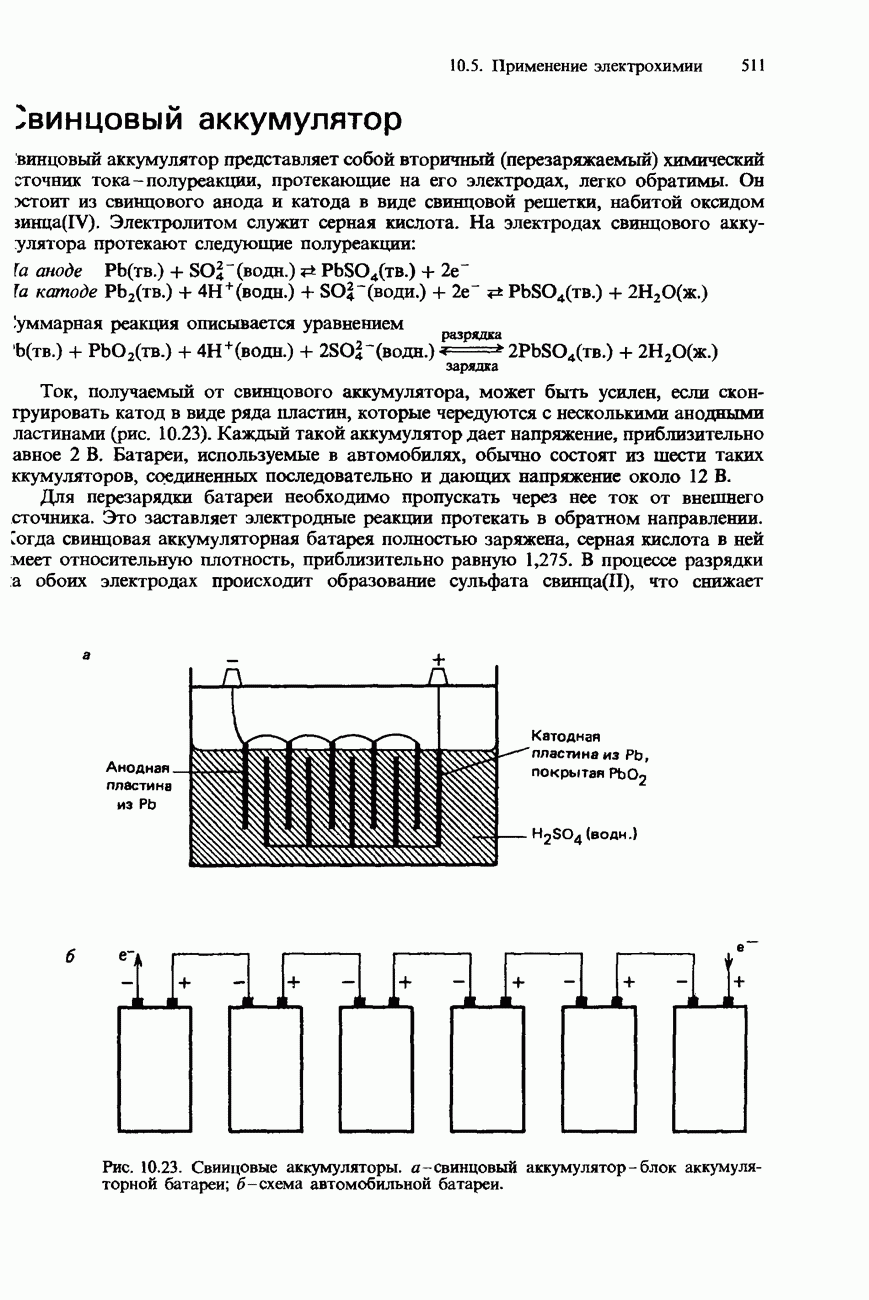
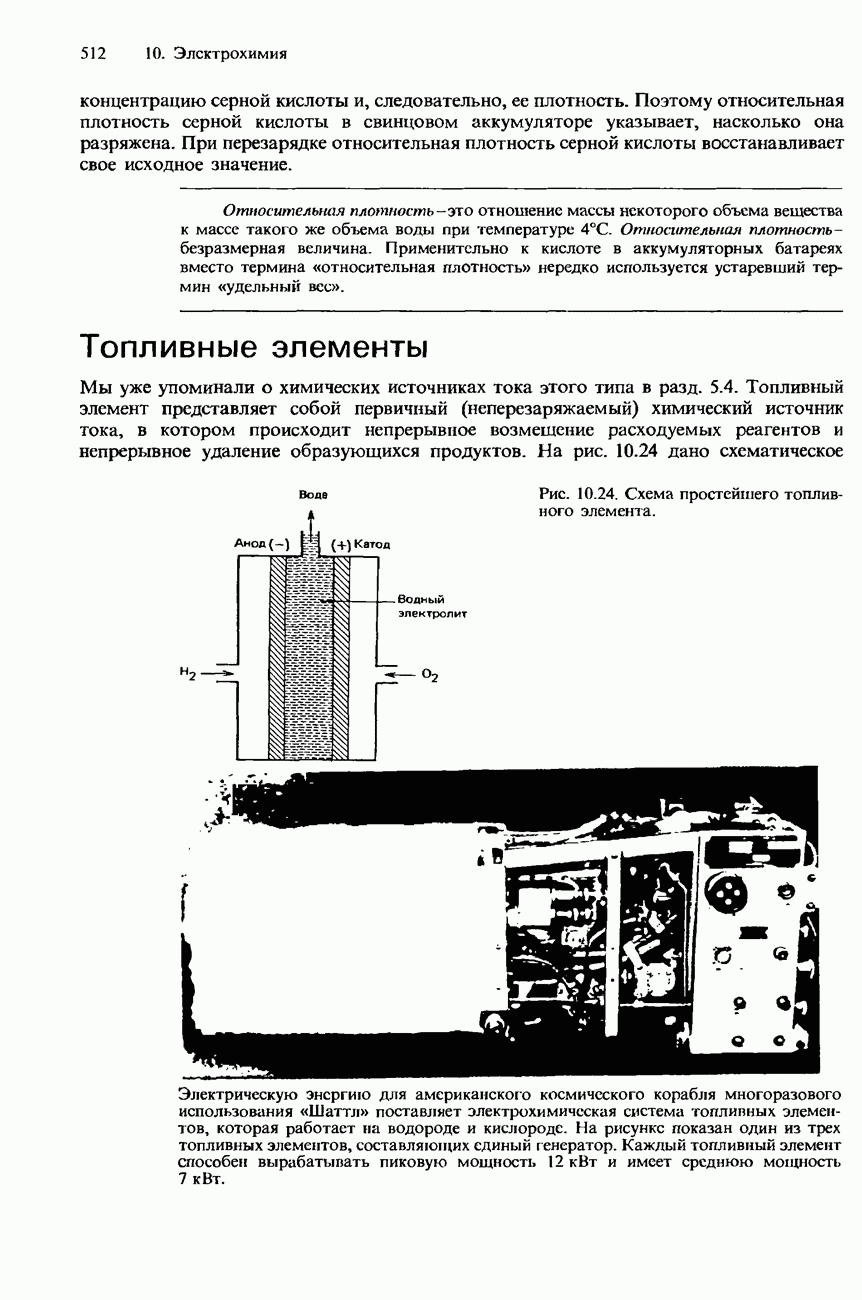
- БАТАРЕИ И ПРОМЫШЛЕННЫЕ ИСТОЧНИКИ ТОКА
- МЕТАЛЛУРГИЯ
- КОРРОЗИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ