| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
121. Изменение концентрации фонового электролита
Во многих случаях концентрация фонового электролита на поверхности электрода выше, чем в глубине раствора. Эта разница

Рис. 121-1. Разность концентраций добавленного электролита, поделенная на концентрацию реагента. Ось абсцисс та же, что и на рис. 120-1 и 120-2. 1 — капля; 2— диск; 3 — нернстовский слой; 4— диск; 5 — капля.
обычно получается как побочный результат при расчетах влияния миграции на предельные токи. Тем не менее величина этой разности представляет значительный интерес в задачах о свободной конвекции, поскольку конвективная скорость обусловлена изменением плотности раствора, возникающим в результате протекания электродной реакции. При этом фоновый электролит дает примерно такой же вклад в изменение плотности, как и сами реагирующие компоненты (разд. 111).

Рис. 121-2. Приповерхностные концентрации в случае анодной реакции в системе  . 1 - диск; 2 — капля; 3 — капля; 4 — диск; 5 — капля; 6 — диск.
. 1 - диск; 2 — капля; 3 — капля; 4 — диск; 5 — капля; 6 — диск.
На рис. 121-1 показаны некоторые из концентраций на поверхности электродов для двух систем (разряд Ag+ из растворов  и разряд
и разряд  из растворов
из растворов  ), находящихся в различных гидродинамических условиях. Для этих одновалентных ионов в случае избытка фонового электролита разностьконцентраций добавленных ионов составляет примерно половину разности концентраций реагирующего иона. Конечно, эта разность стремится к нулю при удалении фонового электролита, однако она быстро возрастает за счет даже малых примесей (напомним, что для абсциссы используется корневая шкала).
), находящихся в различных гидродинамических условиях. Для этих одновалентных ионов в случае избытка фонового электролита разностьконцентраций добавленных ионов составляет примерно половину разности концентраций реагирующего иона. Конечно, эта разность стремится к нулю при удалении фонового электролита, однако она быстро возрастает за счет даже малых примесей (напомним, что для абсциссы используется корневая шкала).
В случае окислительно-восстановительных систем приходится иметь дело как с добавленными ионами, так и с ионами продукта реакции. На рис. 121-2 показаны соответствующие разности концентраций для анодного окисления ионов ферроцианида, а на рис. 121-3 — для катодного восстановления феррицианида. В последнем случае приэлектродная область обеднена ионами гидроксила.

Рис. 121-3. Приповерхностные концентрации в случае катодной реакции в системе  . 1 - диск; 2 — диск; 3 — капля; 4 — капля; 5 — диск.
. 1 - диск; 2 — диск; 3 — капля; 4 — капля; 5 — диск.
На этих рисунках предполагается, что концентрации ферро- и феррицианидов в глубине раствора одинаковы, а противоионом служит  По оси абсцисс отложена та же величина, что и на рис. 120-3.
По оси абсцисс отложена та же величина, что и на рис. 120-3.
Результаты, относящиеся к системе сульфат меди — серная кислота, обсуждаются в следующем разделе.
В разд. 73 рассматривались системы с фоновым электролитом. Там же приводились расчеты концентрационных профилей фонового электролита и компонента с малой концентрацией. Сейчас мы воспользуемся изложенным в разд. 73 методом и рассчитаем поверхностную концентрацию добавленного иона и
иона продукта электродной реакции в пределе  т. е. при большом избытке фонового электролита. В результате будут получены значения ординаты при
т. е. при большом избытке фонового электролита. В результате будут получены значения ординаты при  на рис. 121-1-121-3.
на рис. 121-1-121-3.
Используя соотношение Нернста—Эйнштейна (75-1), перепишем уравнение (119-4) для вращающегося диска:

где  . Обозначим добавленные ионы и противоионы индексами 1 и 2, реагент
. Обозначим добавленные ионы и противоионы индексами 1 и 2, реагент  продукт, также присутствующий в малом количестве, — 4.
продукт, также присутствующий в малом количестве, — 4.
Для реагента в пределе  можно пренебречь миграцией. В этом случае концентрационный профиль будет описываться формулой
можно пренебречь миграцией. В этом случае концентрационный профиль будет описываться формулой

Для продукта также можно пренебречь миграцией, и равенство (121-1) приобретает вид

Граничное условие (119-7) на электроде сводится к равенству

Тогда решение задачи имеет вид

откуда следует

После линеаризации можно получить уравнения для добавленного иона и противоиона:

где  — однородные концентрации этих ионов в отсутствие компонентов реагента и продукта (разд. 73).
— однородные концентрации этих ионов в отсутствие компонентов реагента и продукта (разд. 73).
Концентрации удовлетворяют условию электронейтральности в следующем виде:

Исключая  из уравнений (121-7) и (121-8), получаем
из уравнений (121-7) и (121-8), получаем

где

Уравнение (121-11) служит обобщением уравнения (73-5) на случай двух компонентов с малой концентрацией. Подставляя в него равенства (121-2) и (121-5), находим

Решение этого уравнения, удовлетворяющее граничному условию на бесконечности, имеет вид

Граничное условие на электроде, определяющее равенство нулю потоков ионов (121-1) и (121-2), приобретает вид

С учетом равенства (121-10) можно записать

а из уравнения (121-9) следует

при  . Это позволяет отыскать постоянную В в уравнении (121-14):
. Это позволяет отыскать постоянную В в уравнении (121-14):

Наконец, можно вычислить изменение концентрации компонентов 1 от глубины раствора до поверхности электрода:

Полагая  или
или  получим случай, когда отсутствуют ионы продукта. Соответствующее уравнение для
получим случай, когда отсутствуют ионы продукта. Соответствующее уравнение для  можно вывести из уравнения (121-19), переставляя местами индексы 1 и 2.
можно вывести из уравнения (121-19), переставляя местами индексы 1 и 2.
Для растущей ртутной капли разности концентраций описываются формулами

и

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- ПРЕДИСЛОВИЕ АВТОРА
- Глава 1. ВВЕДЕНИЕ
- 1. Термодинамика, кинетика электродных процессов и процессы переноса
- 2. Вращающиеся цилиндры
- 3. Прохождение тока в электролитах
- 4. Течение жидкости
- 5. Диффузионный слой
- 6. Концентрационные ячейки
- 7. Концентрационное перенапряжение
- 8. Поверхностное перенапряжение
- 9. Потенциал ячейки
- 10. Фоновый электролит
- 11. Свободная конвекция
- СПИСОК ОБОЗНАЧЕНИЙ
- Часть А. ТЕРМОДИНАМИКА ЭЛЕКТРОХИМИЧЕСКИХ ЯЧЕЕК
- Глава 2. ТЕРМОДИНАМИКА НА ЯЗЫКЕ ЭЛЕКТРОХИМИЧЕСКИХ ПОТЕНЦИАЛОВ
- 12. Равновесие фаз
- 13. Химический и электрохимический потенциалы
- 14. Определение некоторых термодинамических функций
- 15. Ячейка с раствором однородной концентрации
- 16. Процессы переноса в областях контакта
- 17. Ячейка с одним электролитом переменной концентрации
- 18. Ячейка с двумя электролитами, концентрация одного из которых почти однородна
- 19. Ячейка с двумя электролитами переменной концентрации
- 20. Стандартный потенциал ячейки и коэффициенты активности
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- СПИСОК ЛИТЕРАТУРЫ
- Глава 3. ЭЛЕКТРИЧЕСКИЙ ПОТЕНЦИАЛ
- 22. Электростатический потенциал
- 23. Межмолекулярные силы
- 24. Внешний и внутренний потенциалы
- 25. Потенциалы электродов сравнения
- 26. Электрический потенциал в термодинамике
- СПИСОК ОБОЗНАЧЕНИЙ
- СПИСОК ЛИТЕРАТУРЫ
- Глава 4. КОЭФФИЦИЕНТЫ АКТИВНОСТИ
- 27. Распределение ионов в разбавленных растворах
- 28. Электрический вклад в свободную энергию
- 29. Недостатки модели Дебая—Хюккеля
- 30. Растворы бинарных электролитов
- 31. Многокомпонентные растворы
- 32. Измерение коэффициентов активности
- 33. Слабые электролиты
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- СПИСОК ЛИТЕРАТУРЫ
- Глава 5. ЭЛЕКТРОДЫ СРАВНЕНИЯ
- 34. Критерии выбора электродов сравнения
- 35. Экспериментальные факторы, влияющие на выбор электродов сравнения
- 36. Водородный электрод
- 37. Каломельный электрод и другие электроды типа ртуть—соль ртути
- 38. Окиснортутный электрод
- 39. Электроды типа серебро—галогенид серебра
- 40. Потенциалы относительно данного электрода сравнения
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 6. ПОТЕНЦИАЛЫ ЯЧЕЕК С ПЕРЕНОСОМ
- 41. Уравнение Нернста
- 42. Типы жидкостных соединений
- 43. Формулы для потенциалов жидкостных соединений
- 44. Определение концентрационных профилей
- 45. Численные результаты
- 46. Ячейки с жидкостным соединением
- 47. Поправки к уравнению Нернста
- 48. Мембранные потенциалы
- СПИСОК ОБОЗНАЧЕНИЙ
- СПИСОК ЛИТЕРАТУРЫ
- Часть Б. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ И ДРУГИЕ ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ
- Глава 7. СТРОЕНИЕ ЭЛЕКТРИЧЕСКОГО ДВОЙНОГО СЛОЯ
- 49. Качественное описание двойных слоев
- 50. Изотерма адсорбции Гиббса
- 51. Уравнение Липпмана
- 52. Диффузная часть двойного слоя
- 53. Емкость двойного слоя в отсутствие специфической адсорбции
- 54. Специфическая адсорбция на границе раздела электрод — раствор
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 8. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ
- 55. Гетерогенные электродные реакции
- 56. Зависимость плотности тока от поверхностного перенапряжения
- 57. Модели в кинетике электродных процессов
- 58. Влияние строения двойного слоя
- 59. Кислородный электрод
- 60. Методы измерения
- 61. Одновременно протекающие реакции
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- СПИСОК ЛИТЕРАТУРЫ
- Глава 9. ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ
- 62. Разрывная скорость на границе раздела
- 63. Электроосмос и потенциал течения
- 64. Электрофорез
- 65. Потенциал осаждения
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 10. ЭЛЕКТРОКАПИЛЛЯРНЫЕ ЯВЛЕНИЯ
- 66. Динамика границы раздела
- 67. Электрокапиллярное движение ртутных капель
- 68. Потенциалы осаждения для падающих ртутных капель
- СПИСОК ОБОЗНАЧЕНИЙ
- Часть В. ПРОЦЕССЫ ПЕРЕНОСА В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- Глава 11. БЕСКОНЕЧНО РАЗБАВЛЕННЫЕ РАСТВОРЫ
- 69. Законы переноса
- 70. Проводимость, диффузионные потенциалы и числа переноса
- 71. Сохранение заряда
- 72. Бинарный электролит
- 73. Фоновый электролит
- 74. Многокомпонентная диффузия, возникающая при исключении электрического поля
- 75. Подвижности и коэффициенты диффузии
- 76. Электронейтральность и уравнение Лапласа
- 77. Умеренно разбавленные растворы
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 12. КОНЦЕНТРИРОВАННЫЕ РАСТВОРЫ
- 78. Законы переноса
- 79. Бинарный электролит
- 80. Стандартные скорости
- 81. Потенциал
- 82. Связь с теорией разбавленных растворов
- 83. Многокомпонентный транспорт
- 84. Потенциалы жидкостного соединения
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 13. ТЕПЛОВЫЕ ЭФФЕКТЫ
- 85. Термодиффузия
- 86. Выделение и перенос тепла
- 87. Тепловыделение на границе раздела фаз
- 88. Термогальванические ячейки
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 14. ХАРАКТЕРИСТИКИ ПЕРЕНОСА
- 89. Бесконечно разбавленные растворы
- 90. Растворы, содержащие одну соль
- 92. Интегральные коэффициенты диффузии
- ЗАДАЧА
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 15. МЕХАНИКА ЖИДКИХ СРЕД
- 94. Напряжение в ньютоновской жидкости
- 95. Граничные условия
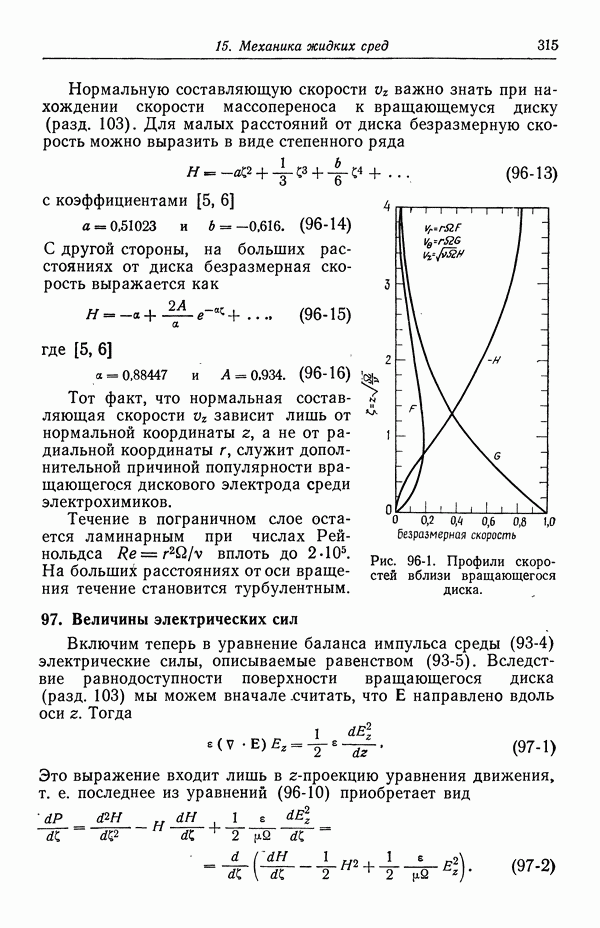
- 96. Течение жидкости к вращающемуся диску
- 97. Величины электрических сил
- 98. Турбулентное течение
- 99. Массоперенос в турбулентном потоке
- СПИСОК ОБОЗНАЧЕНИЙ
- СПИСОК ЛИТЕРАТУРЫ
- Часть Г. РАСПРЕДЕЛЕНИЕ ТОКА И МАССОПЕРЕНОС В ЭЛЕКТРОХИМИЧЕСКИХ СИСТЕМАХ
- Глава 16. ОСНОВНЫЕ УРАВНЕНИЯ
- 100. Перенос в разбавленных растворах
- 101. Кинетика электродных процессов
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 17. ЗАДАЧИ КОНВЕКТИВНОЙ ДИФФУЗИИ
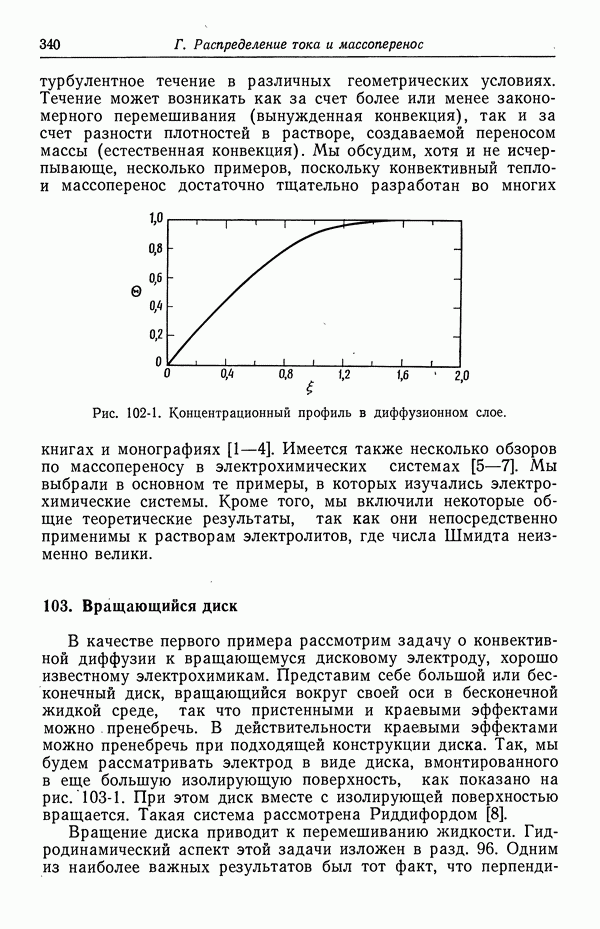
- 102. Упрощенное описание конвективной диффузии
- 103. Вращающийся диск
- 104. Задача Граца
- 105. Кольцевой зазор
- 106. Двумерные диффузионные слои при вынужденной ламинарной конвекции
- 107. Осесимметричные диффузионные слои при вынужденной ламинарной конвекции
- 109. Вращающиеся цилиндры
- 110. Растущие ртутные капли
- 111. Свободная конвекция
- 112. Наложение свободной и вынужденной конвекции
- 113. Ограничения за счет поверхностных реакций
- 114. Бинарные и концентрированные растворы
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 18. ПРИЛОЖЕНИЯ ТЕОРИИ ПОТЕНЦИАЛА
- 115. Упрощения в задачах теории потенциала
- 116. Первичное распределение тока
- 117. Вторичное распределение тока
- 118. Численное решение методом конечных разностей
- СПИСОК ОБОЗНАЧЕНИЙ
- ГЛАВА 19. ВЛИЯНИЕ МИГРАЦИИ НА ПРЕДЕЛЬНЫЕ ТОКИ
- 119. Решение задачи
- 120. Поправочный множитель в случае предельных токов
- 121. Изменение концентрации фонового электролита
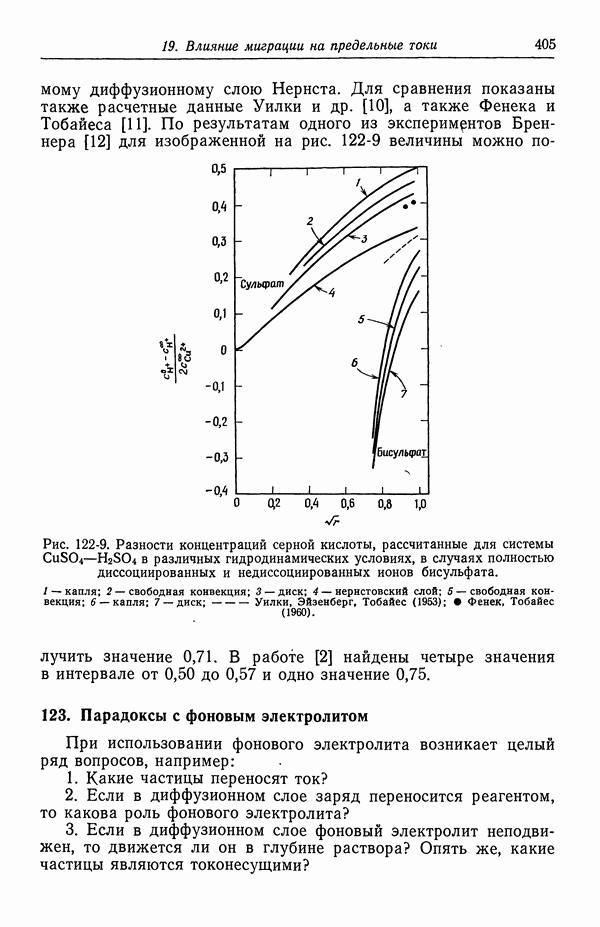
- 122. Роль ионов бисульфата
- 123. Парадоксы с фоновым электролитом
- 124. Предельные токи в случае свободной конвекции
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 20. КОНЦЕНТРАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
- 126. Бинарный электролит
- 127. Фоновый электролит
- 128. Численные расчеты
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Глава 21. ДОПРЕДЕЛЬНЫЕ ТОКИ
- 129. Объем раствора
- 130. Диффузионные слои
- 131. Граничные условия и метод решения
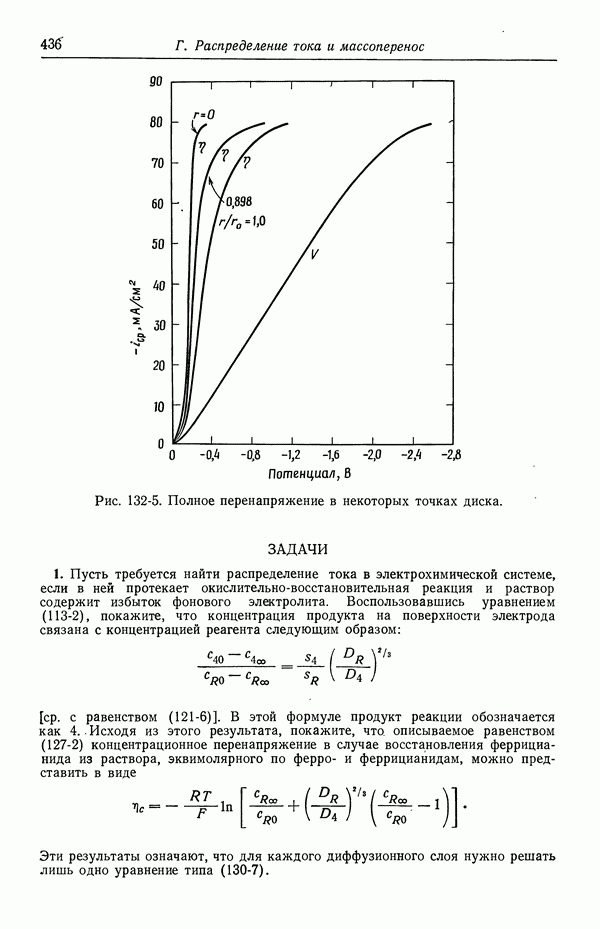
- 132. Результаты для вращающегося диска
- ЗАДАЧИ
- СПИСОК ОБОЗНАЧЕНИЙ
- Приложение А. ПАРЦИАЛЬНЫЕ МОЛЯРНЫЕ ОБЪЕМЫ
- Приложение Б. ВЕКТОРЫ И ТЕНЗОРЫ
- Приложение В. ЧИСЛЕННОЕ РЕШЕНИЕ СИСТЕМЫ ОБЫКНОВЕННЫХ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ