| Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Введение. Эффекты электронной корреляции
О. Синаноглу
В первом томе этой книги была изложена теория локализованных и делокализованных молекулярных орбиталей для  и
и  -электронов в системах с заполненными и незаполненными оболочками. При этом некоторые корреляционные эффекты неявно уже учитывались при оправдании тех или иных приближений в теории.
-электронов в системах с заполненными и незаполненными оболочками. При этом некоторые корреляционные эффекты неявно уже учитывались при оправдании тех или иных приближений в теории.
Второй том посвящается специально теории корреляционных эффектов, причем главное внимание уделяется тем случаям, когда простая теория МО оказывается несостоятельной.
Соответственно трем типам молекулярных систем (с заполненными и незаполненными оболочками из хартри-фоковских молекулярных орбиталей и систем с локализованными орбиталями) имеется три типа теорий корреляционных эффектов. Теория корреляционных эффектов для систем с заполненными оболочками из хартри-фоковских молекулярных орбиталей и для систем с локализованными орбиталями недавно подробно обсуждалась [1]. В этом томе в разд. 1-7 изложен вариант этой теории с молекулярными орбиталями в применении к системам с незаполненными оболочками.
Влияние электронной корреляции на орбитали заполненных оболочек обычно мало. Проведенные в рамках теории МО расчеты распределения зарядов и дипольных моментов для  -систем (т. 1, ч. I) и
-систем (т. 1, ч. I) и  -систем (т. 1, ч. II) оказываются для замкнутых оболочек вполне удовлетворительными, если только нет больших эффектов «почти вырождения». Иначе обстоит дело для систем с незаполненными оболочками. Здесь, напротив, обязательно нужно учитывать как влияние электронной корреляции на молекулярные орбитали, так и особые эффекты «средней поляризации» орбиталей
-систем (т. 1, ч. II) оказываются для замкнутых оболочек вполне удовлетворительными, если только нет больших эффектов «почти вырождения». Иначе обстоит дело для систем с незаполненными оболочками. Здесь, напротив, обязательно нужно учитывать как влияние электронной корреляции на молекулярные орбитали, так и особые эффекты «средней поляризации» орбиталей  Последние эффекты могут существенно изменить распределение зарядов по сравнению с тем, к которому приводит расчет просто по хартри-фоковским орбиталям; они могут также
Последние эффекты могут существенно изменить распределение зарядов по сравнению с тем, к которому приводит расчет просто по хартри-фоковским орбиталям; они могут также
повлиять, например, на дипольные моменты возбужденных состояний.
Если под влиянием электронной корреляции уровни изменяются мало, то применяют обычную теорию возмущений. Вырожденную теорию возмущений (в которой с самого начала производится снятие вырождения и исключение эффектов «почти вырождения») нужно использовать, если уровни пересекаются и меняются местами. До некоторой степени проблема аналогична той, которая возникает в теории систем бесконечно большого числа взаимодействующих частиц, когда адиабатическая теория возмущений в основном состоянии оказывается несостоятельной (см. разд.  настоящего тома). При этом, как известно, надо использовать температурную теорию возмущений (которая при
настоящего тома). При этом, как известно, надо использовать температурную теорию возмущений (которая при  сводится к теории возмущений для основного состояния).
сводится к теории возмущений для основного состояния).
В атомных системах эффекты корреляции внешнего электрона с сильно связанными внутренними электронами включают в понятие «поляризация остова». Такого рода корреляция имеет небольшую величину; например, корреляция  составляет
составляет  Корреляции типа «поляризации остова» проявляются также при рассмотрении ридберговских состояний молекул и взаимодействия электрона с растворителем. В последнем случае указанные корреляционные эффекты типа «поляризации остова», конечно, маскируются более сильными корреляционными эффектами орбитального типа, учитываемыми, например, введением нсевдопотенциала (см. разд. II-2 и II-3 настоящего тома). Когда главные квантовые числа соответствующих электронов совпадают, межорбитальные корреляционные эффекты становятся сильнее. Папример, корреляционная энергия
Корреляции типа «поляризации остова» проявляются также при рассмотрении ридберговских состояний молекул и взаимодействия электрона с растворителем. В последнем случае указанные корреляционные эффекты типа «поляризации остова», конечно, маскируются более сильными корреляционными эффектами орбитального типа, учитываемыми, например, введением нсевдопотенциала (см. разд. II-2 и II-3 настоящего тома). Когда главные квантовые числа соответствующих электронов совпадают, межорбитальные корреляционные эффекты становятся сильнее. Папример, корреляционная энергия  между
между  -электронами примерно равна
-электронами примерно равна  (см. разд. 1-2 настоящего тома); в связи с этим заметную величину должны иметь также корреляционные эффекты между
(см. разд. 1-2 настоящего тома); в связи с этим заметную величину должны иметь также корреляционные эффекты между  и
и  -электронами в
-электронами в  -электронных системах (см. т. 1 разд.
-электронных системах (см. т. 1 разд. 
Проблема взаимодействия свободного электрона с жидкостями проливает свет на многие важные эффекты взаимодействия молекул с растворителем. Кроме того, она непосредственно связана с вопросами химии растворов металлов в аммиаке, жидких металлов и радиационной химии (см. разд. II-1, II-3, II-5, а также разд. III-4 и III-5 этого тома).
Корреляции типа «поляризации остова» можно представить себе как результат некоторого вандерваальсова пртдакения между неперекрывающимися распределениями зарядов [2, 3]. Выражение для сил притяжения между различными связями в молекуле или выражение для межмолекулярных сил между двумя изолированными газовыми молекулами можно получить, преобразуя выражение для корреляционной энергии от системы молекулярных
орбиталей к системе локализованных орбиталей [1, 3]. Основанное на этом рассмотрение кривых потенциальной энергии межмолекулярного взаимодействия эффективно в большом интервале расстояний (см. разд. III-2 настоящего тома). Само понятие кривой или поверхности потенциальной энергии, однако, существенно связано с тем, насколько хорошо можно, следуя борн-опненгеймеровскому приближению, разделить ядерньге и электронные координаты в данной задаче (см. разд. III-1).
В статистической механике простых жидкостей обычно с самого начала предполагается, что межмолекуляриый потенциал аддитивно слагается из потенциалов нарного взаимодействия. В приложениях статистической механики каждый такой парный потенциал принимается обычно равным потенциалу парного взаимодействия в газовой фазе. Однако в действительности для жидкостей и твердых тел необходимо принимать во внимание существенные отклонения от аддитивности, даже если учитывать только вандерваальсовы силы. Некоторые примеры таких многоатомных неаддитивных сил, действующих между атомами с заполненными оболочками, рассмотрены в разд. IIT-2 и III-3 этого тома. С крайним случаем неаддитивности межмолекулярных взаимодействий мы сталкиваемся в металлах. В разд. III-4 и III-5 изложены основные сведения об этих взаимодействиях с точки зрения теории молекулярных орбиталей и корреляционной теории в приложении к металлам и сплавам.
ЛИТЕРАТУРА
(см. скан)
| Следующий параграф >> |
- Введение. Эффекты электронной корреляции
- Часть I. Атомы и молекулы
- I-1. Теория, оперирующая с разложением по степеням 1/Z для многоэлектронных атомов
- 2. Теория возмущений
- 3. Понятие «комплекса»
- 4. Анализ Е2
- 5. Применение теории возмущений к молекулам
- I-2. Изменение внутренних оетовов элементов второго и третьего периодов и зависимость корреляционной энергии от Z
- 2. Элементы второго периода
- 3. Поведение полной корреляционной энергии атомов … в зависимости от Z
- 4. Элементы третьего периода. Изоэлектронные ряды Mg, Аl и Si
- I-3. Многоэлектронная теория возмущений и межмолекулярные взаимодействия
- 2. Молекулярные взаимодействия
- I-4. Сепарабельность в многоэлектронных системах
- 2. Критерий сепарабельности, сепарабельные величины и групповые функции
- 3. Многоэлектронная волновая функция (не сепарабельная величина)
- 4. Примитивные величины для волновой функции и матрицы плотности
- 5. Групповые разложения для волновой функции и матрицы плотности
- 6. Групповое разложение волновой функции
- 7. Групповое разложение для матрицы плотности
- 8. Модели независимых частиц и соответствующие корреляционные теории
- 9. Связное групповое разложение для волновой функции
- 10. Приложение. Использование формализма вторичного квантования в квантовой химии
- I-5. Локализованные и делокализованные орбитали, геминали, биорбитали и электронная структура молекул
- 2. Модели независимых частиц
- 3. Теория локализации электронов
- 4. Сравнение разных методов расчета волновых функций
- I-6. Энергия диссоциации
- I-7. Электронная корреляция в системах с незаполненными оболочками
- 2. Многоэлектронная теория для замкнутых оболочек
- 3. Варианты метода Хартри—Фока для состояний с открытыми оболочками
- 4. Построение многоэлектронной волновой функции в случае открытых оболочек
- 5. Вариационное выражение для энергии
- 6. Примеры
- 7. Выводы
- Часть II. Влияние растворителя
- II-1. Электроны в жидкостях. I
- II-2. Псевдопотенциал для системы электрон—гелий
- II-3. Электроны в жидкостях. II
- 2. Некоторые замечания о модели полярона
- 3. Континуальные модели диэлектрика
- 4. Диэлектрические модели для электронов в полярных растворителях
- 5. Термохимические данные и распределение заряда
- 6. Возбужденные состояния электронов в полярных растворителях
- 7. Концентрированные металл-аммиачные растворы
- 8. Электроны в неполярных системах
- 9. Модель свободного электрона
- 10. Пузырьковая модель
- II-4. Влияние растворителя на реакционную способность
- 2. Константы скорости реакций
- II-5. Влияние растворителя на волновые числа оптического поглощения и испускания
- 2. Классическое рассмотрение системы, состоящей из молекулы растворенного вещества в растворителе
- 3. Квантовомеханическое рассмотрение при помощи теории возмущений системы, состоящей из молекулы растворенного вещества в растворителе
- 4. Влияние растворителя на сдвиг волновых чисел вследствие дисперсионных взаимодействий в растворе
- 5. Сдвиг волновых чисел поглощения и испускания
- 6. Приложения теории
- 7. Обсуждение некоторых более ранних работ
- Часть III. Межмолекулярные силы
- III-1. Межатомное отталкивание и адиабатическое приближение
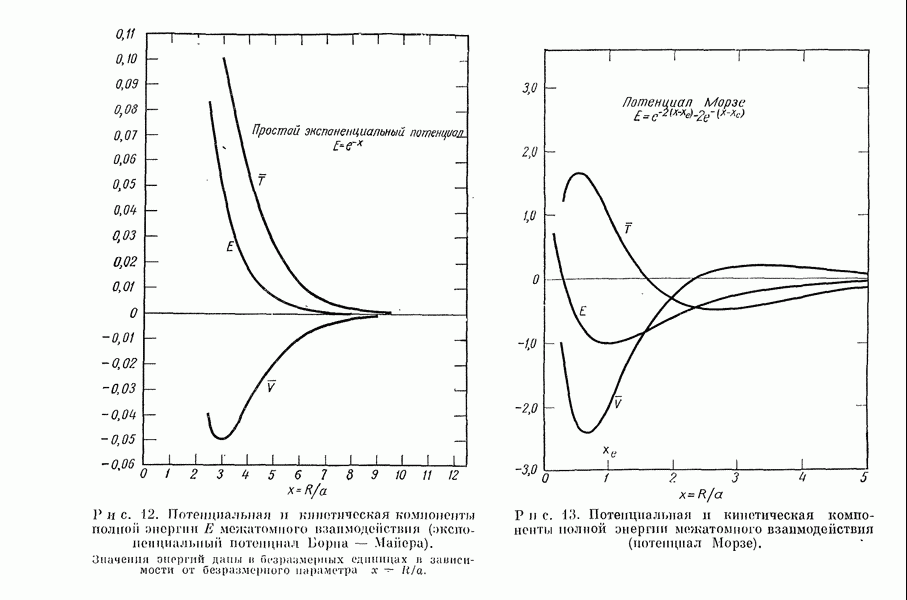
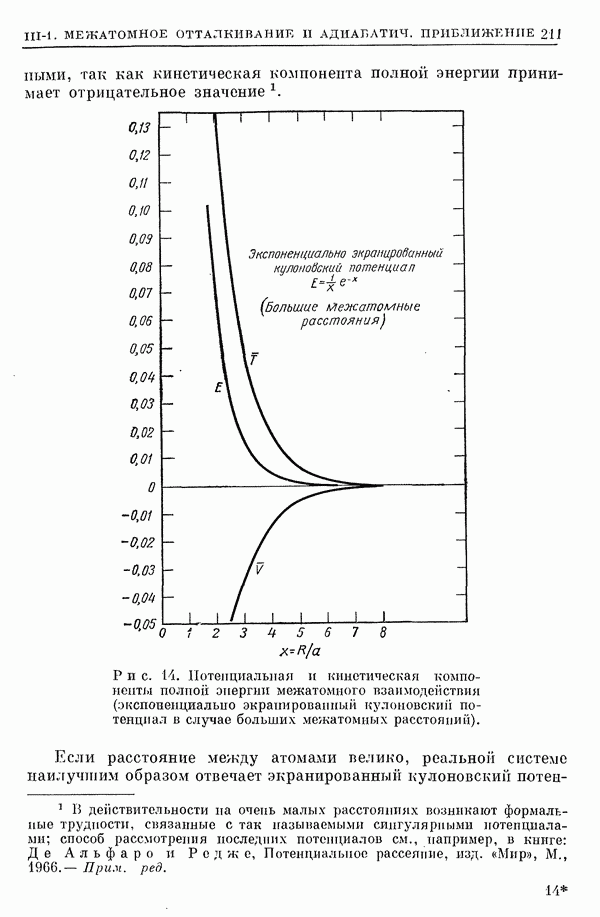
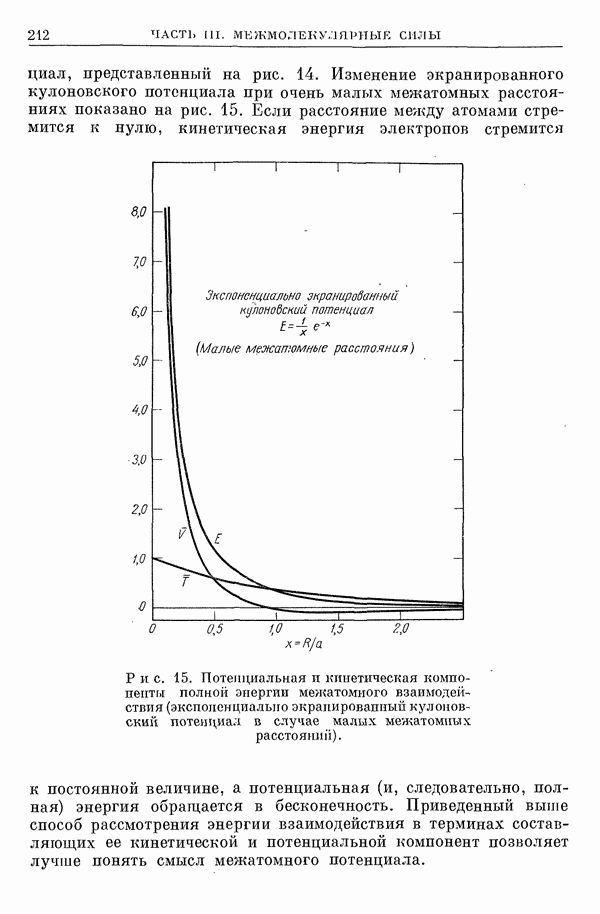
- 2. Кинетическая и потенциальная составляющие энергии межатомного взаимодействия
- 3. Приближение Борна — Оппенгеймера
- 4. Критерий адиабатичности в динамических задачах
- 5. Неадиабатические переходы
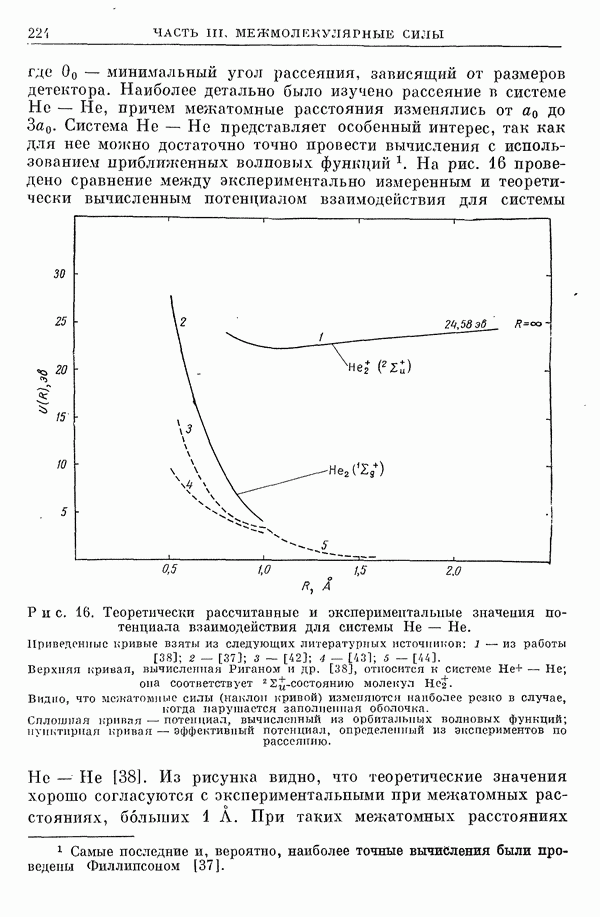
- 6. Межатомные потенциалы и измеряемые величины
- 7. Выводы
- III-2. Межмолекулярные силы в газах и конденсированных средах
- 2. Потенциал взаимодействия двух молекул
- 3. Влияние среды на межмолекулярные потенциалы
- III-3. Многочастичные атомные силы и стабильность кристаллов
- 2. Многочастичные атомные (ионные) взаимодействия в кристаллах
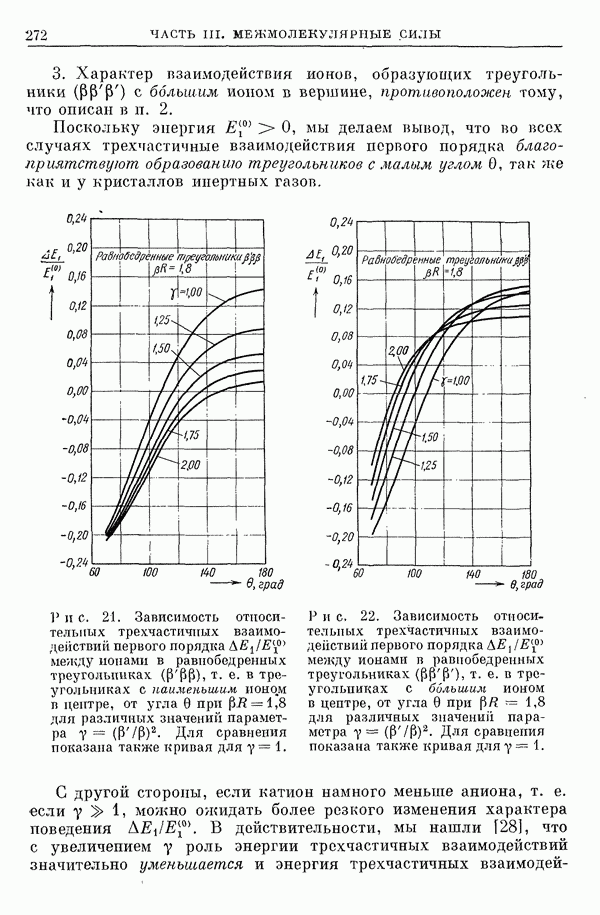
- 3. Атомы инертных газов. Обменные трехчастичные взаимодействия первого и второго порядков
- 4. Полные трехчастичные обменные взаимодействия и стабильность кристаллов
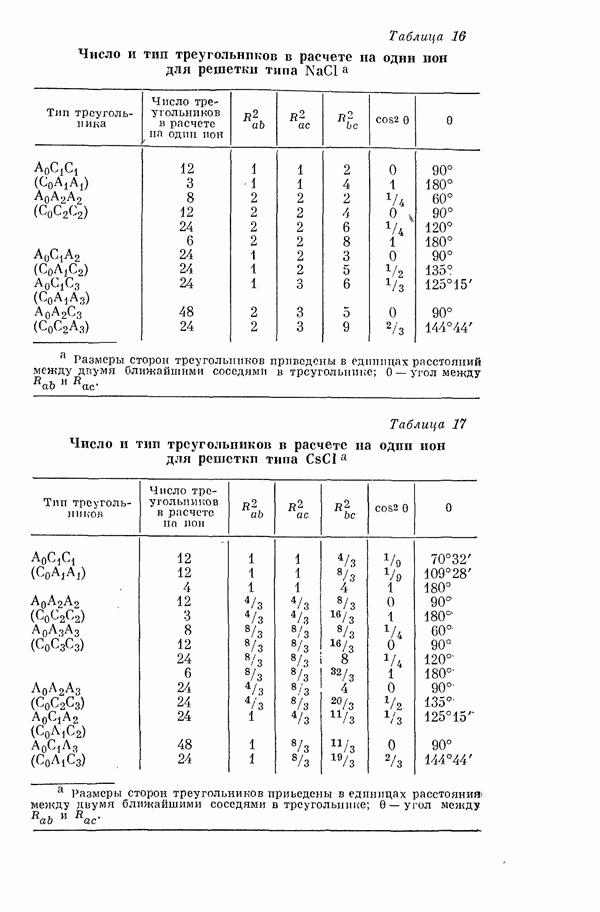
- 5. Галогениды щелочных металлов. Обменные трехчастичные взаимодействия первого и второго порядков [28]
- 6. Стабильность кристаллов галогенидов щелочных металлов
- III-4. Электроны в металлах
- 2. Кристаллические решетки
- 3. Зонная теория электронных орбиталей [1—3]
- 4. Корреляции в электронном газе
- III-5. Силы взаимодействия в металлах
- 2. Энергия основного состояния электронного газа в решетке из положительных зарядов
- 3. Приложение