| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
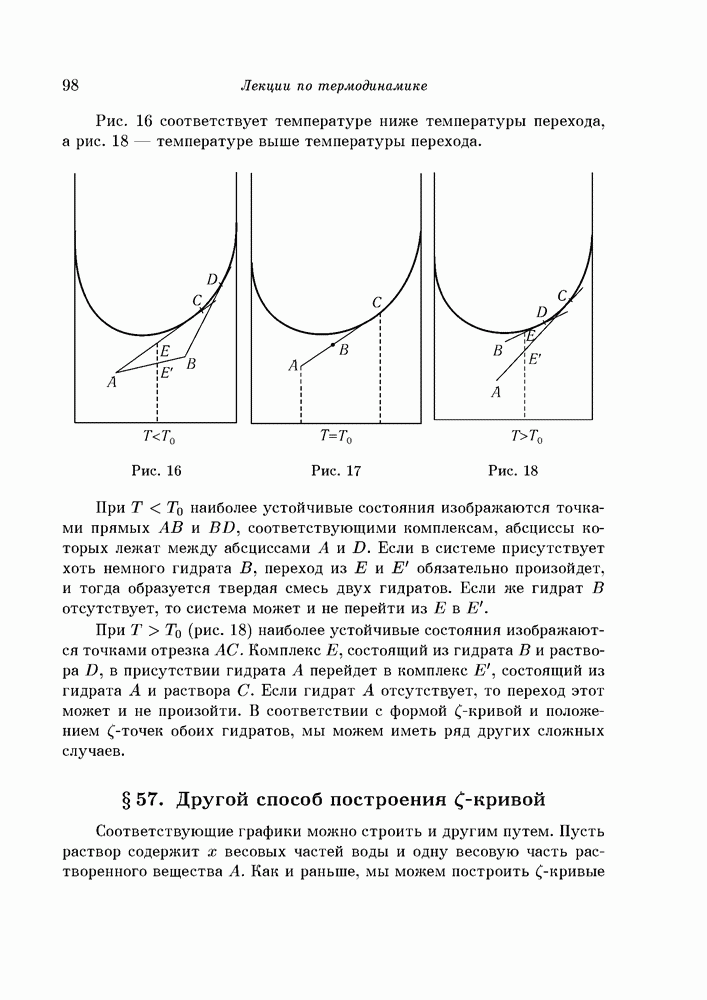
§ 14. Различные обратимые пути между двумя состояниями. Энтропия
Предположим теперь, что из состояния А в состояние В мы можем перейти различными обратимыми путями. Тогда интеграл

должен для любого из этих путей иметь одно и то же значение. Действительно, переходя от А к В по пути  а затем обратно от В к А по пути
а затем обратно от В к А по пути  мы совершим полный цикл, для которого значение интеграла
мы совершим полный цикл, для которого значение интеграла  равно нулю. Значение этого интеграла для перехода от А к В будет, следовательно, равно по абсолютной величине и противоположно по знаку значению его для перехода от В к А. Но поскольку пути
равно нулю. Значение этого интеграла для перехода от А к В будет, следовательно, равно по абсолютной величине и противоположно по знаку значению его для перехода от В к А. Но поскольку пути  оба обратимы, то можно перейти от А к В и по пути
оба обратимы, то можно перейти от А к В и по пути  и
и  будет тогда иметь то же самое значение, что и вдоль
будет тогда иметь то же самое значение, что и вдоль  .
.
Выберем теперь некоторое состояние N, с которым можно будет сравнивать все остальные состояния системы. Если А — одно из этих состояний, то мы можем себе представить, что система переведена из А в N по какому-то обратимому пути. Этому переходу будет соответствовать определенное значение интеграла  которое, как это показано выше, не зависит от пути перехода и, таким образом, поскольку состояние N выбрано раз и навсегда, зависит только от состояния А. Это значение интеграла
которое, как это показано выше, не зависит от пути перехода и, таким образом, поскольку состояние N выбрано раз и навсегда, зависит только от состояния А. Это значение интеграла  и называется энтропиеи системы в состоянии А.
и называется энтропиеи системы в состоянии А.
Мы будем обозначать энтропию всегда через  .
.
Легко видеть, что величина интеграла  для перехода от А к В по обратимому пути равна возрастанию энтропии при этом переходе. Ибо, поскольку этот интеграл не зависит от пути перехода, система может быть сначала переведена в состояние N, а оттуда в состояние В.
для перехода от А к В по обратимому пути равна возрастанию энтропии при этом переходе. Ибо, поскольку этот интеграл не зависит от пути перехода, система может быть сначала переведена в состояние N, а оттуда в состояние В.
Искомый интеграл будет тогда иметь вид:

ибо по определению

Строго говоря, такое определение энтропии имеет силу только для равновесных состояний, так как обратимыми изменениями только эти состояния и достижимы. Но бывают, однако, случаи, в которых, несмотря на отсутствие равновесия, мы все же можем говорить об энтропии. Одним из подобных примеров является вода в присутствии пара, упругость которого ниже максимальной. Если вообразить себе воду и пар отделенными друг от друга перегородкой, то каждая фаза в отдельности будет находиться в состоянии равновесия, и мы можем тогда говорить о сумме энтропий обеих фаз.
Если состояния А и В достаточно мало отличаются друг от друга, то формула (10) получает вид

Таким образом, если  — теплота, полученная телом извне при его переходе из одного равновесного состояния в другое, бесконечно близкое, равновесное состояние, то есть полный дифференциал.
— теплота, полученная телом извне при его переходе из одного равновесного состояния в другое, бесконечно близкое, равновесное состояние, то есть полный дифференциал.
В этой его форме второе начало находит себе многочисленные применения. Введя соответствующие переменные, значения которых определяют равновесное состояние, можно выразить  через дифференциалы этих переменных, а затем использовать соотношения, которые должны соблюдаться между коэффициентами при этих дифференциалах в выражении для для того, чтобы было полным дифференциалом. Что касяется самого
через дифференциалы этих переменных, а затем использовать соотношения, которые должны соблюдаться между коэффициентами при этих дифференциалах в выражении для для того, чтобы было полным дифференциалом. Что касяется самого  то его мы получим по первому началу, выразив теплоту, полученную системой, в виде суммы приращения внутренней энергии и работы, произведенной системой.
то его мы получим по первому началу, выразив теплоту, полученную системой, в виде суммы приращения внутренней энергии и работы, произведенной системой.
Что  — полный дифференциал, это следует, согласно сказанному выше, из равенства нулю
— полный дифференциал, это следует, согласно сказанному выше, из равенства нулю  для всякого обратимого цикла. Обратно, если есть дифференциал некоторой величины [однозначной функции состояния], то мы можем заключить, что
для всякого обратимого цикла. Обратно, если есть дифференциал некоторой величины [однозначной функции состояния], то мы можем заключить, что  для всякого обратимого цикла.
для всякого обратимого цикла.
Величина  сама по себе не является дифференциалом, а представляет собой лишь некоторое бесконечно малое количество теплоты.
сама по себе не является дифференциалом, а представляет собой лишь некоторое бесконечно малое количество теплоты.
Для всего цикла  отличен от нуля и равен работе системы.
отличен от нуля и равен работе системы.
Температура Т есть интегрирующий делитель выражения для  . Существует, конечно, бесконечное число интегрирующих делителей для выражения
. Существует, конечно, бесконечное число интегрирующих делителей для выражения  но замечательно то, что один из них может играть роль температуры, т. е. величины, определяющей возможность перехода теплоты от одного тела к другому.
но замечательно то, что один из них может играть роль температуры, т. е. величины, определяющей возможность перехода теплоты от одного тела к другому.
Не все интегрирующие делители имеют это физическое значение.
Если для какого-то тела, скажем, будет полным дифференциалом, где  — некоторая функция переменных, определяющих состояние тела, и аналогично
— некоторая функция переменных, определяющих состояние тела, и аналогично  — такая же функция для другого тела, то эти тела могут находиться в равновесии друг с другом и при условии, что
— такая же функция для другого тела, то эти тела могут находиться в равновесии друг с другом и при условии, что  не равняется
не равняется 
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редактора к первому изданию
- § 1. Основные понятия термодинамики
- § 2. Первое начало термодинамики
- § 3. Другой пример вычисления работы
- § 4. Приложение к идеальным газам
- § 5. Стационарный ток жидкости через трубу с переменным сечением
- § 6. Однородное тело
- § 7. Применение первого начала к химии: теплота реакции и температура
- § 8. Второе начало термодинамики
- § 9. Цикл Карно
- § 10. Коэффициент полезного действия. Универсальная функция температуры
- § 11. Другой способ определения универсальной функции температуры
- § 12. Второе начало для обратимых процессов
- § 13. Второе начало для обратимых процессов [общий случай]
- § 14. Различные обратимые пути между двумя состояниями. Энтропия
- § 15. Несколько простейших приложений
- § 16. Отношение теплоемкостей
- § 17. Система с произвольным числом параметров
- § 18. Значение полученных общих формул
- § 19. Значение второго начала
- § 20. Приложения второго начала к адиабатическим процессам
- § 21. Сжатие жидкостей
- § 22. Опыты по адиабатическому растяжению проволок
- § 23. Непосредственный вывод уравнения адиабатических процессов
- § 24. Применение к жидким пленкам
- § 25. Применение к гальваническому элементу
- § 26. Уравнение Клапейрона
- § 27. Опытная проверка уравнения Клапейрона (Клаузиус)
- § 28. Опыты де-Виссера с уксусной кислотой
- § 29. Режеляция льда
- § 30. Закон Стефана-Больцмана
- § 31. Другие выражения второго начала
- § 32. Свойства энтропии
- § 33. Свободная энергия
- § 34. Термодинамический потенциал
- § 35. Свободная энергия идеального газа
- § 36. Неравновесные состояния
- § 37. Необратимые процессы
- § 38. Изотермический процесс
- § 39. Свободная энергия и работа
- § 40. Обобщенные силы
- § 41. Условия равновесия
- § 42. Система в поле консервативных сил
- § 43. Газ или жидкость в поле силы тяжести
- § 44. Решение того же вопроса с помощью энтропии
- § 45. Система жидкость-пар
- § 46. Равновесие трехфазной системы
- § 47. Упругость пара над разбавленным раствором
- § 48. Различие в давлении пара над чистой водой и над раствором
- § 49. Смеси
- § 50. Двухкомпонентная система
- § 51. Устойчивые и неустойчивые жидкие фазы; равновесие между двумя жидкими фазами
- § 52. Равновесие между твердой и жидкой фазами; переохлаждение
- § 53. Равновесие трехфазной системы, состоящей из двух компонент
- § 54. Равновесие раствора соли с ее твердым гидратом
- § 55. Равновесие между двумя растворами различной концентрации
- § 56. Система из двух гидратов
- § 57. Другой способ построения кривой
- § 58. Трехкомпонентные системы
- § 59. Трехфазная система из трех компонент
- § 60. Форма поверхности
- § 61. Условия равновесия между твердой и жидкой фазами
- § 62. Равновесие двух твердых фаз с жидкими фазами
- § 63. Равновесие между двумя жидкими фазами
- § 64. Другие способы построения поверхности
- § 65. Смешанные кристаллы
- § 66. Равновесие между смесями и растворами
- § 67. Неопределенность в выражении термодинамического потенциала
- § 68. Смесь газов в поле силы тяжести
- § 69. Смешение и разделение двух газов
- § 70. Парадокс Гиббса
- § 71. Обобщение теоремы Гиббса на случай трех и более газов
- § 72. Уменьшение свободной энергии при смешении двух газов
- § 73. Свободная энергия жидкой смеси
- § 74. Общее выражение для свободной энергии смеси
- § 75. Случай, когда одна из компонент присутствует в весьма малом количестве
- § 76. Равновесие двух фаз, каждая из которых состоит из двух компонент
- § 77. Смесь под действием внешних сил
- § 78. Вывод уравнений равновесия
- § 79. Второй пример системы под действием внешних сил
- § 80. Осмотическое давление. Закон вант-Гоффа
- § 81. Другой вывод закона вант-Гоффа
- § 82. Общие условия равновесия многофазных систем
- § 83. Равновесие трех фаз
- § 84. Вывод условий равновесия с помощью термодинамического потенциала
- § 85. Число независимых условий равновесия
- § 86. Сравнение между собой двух состояний равновесия
- § 87. Общее соотношение между двумя состояниями равновесия
- § 88. Смысл полученного соотношения
- § 89. Добавление некоторого весьма малого количества новой компоненты
- § 90. Несколько заключительных замечаний
- § 91. Диссоциация газа
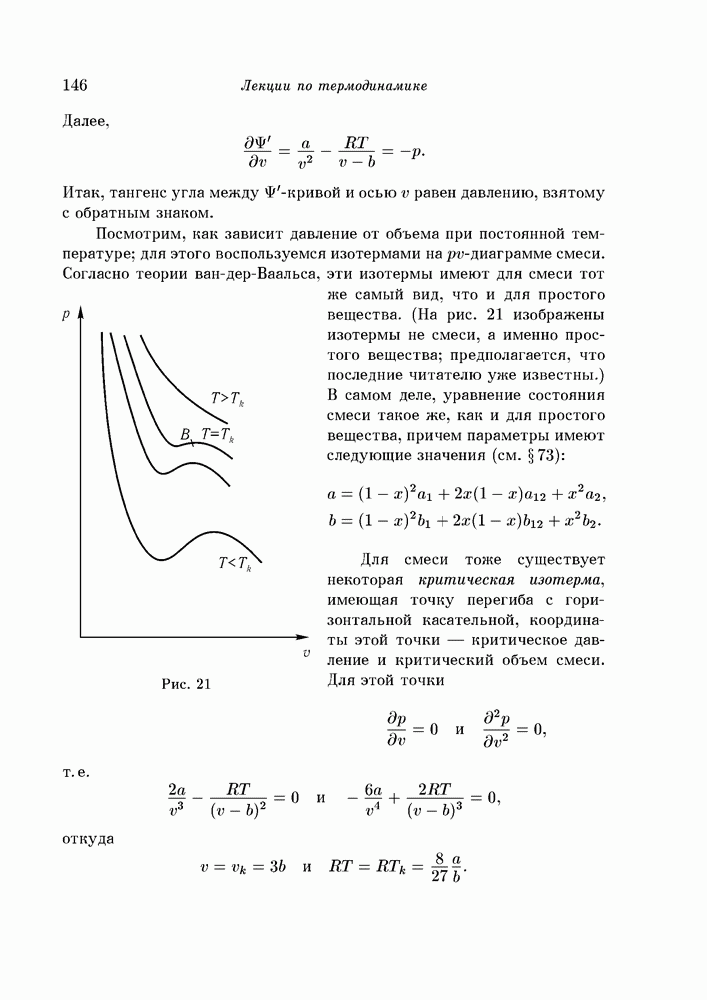
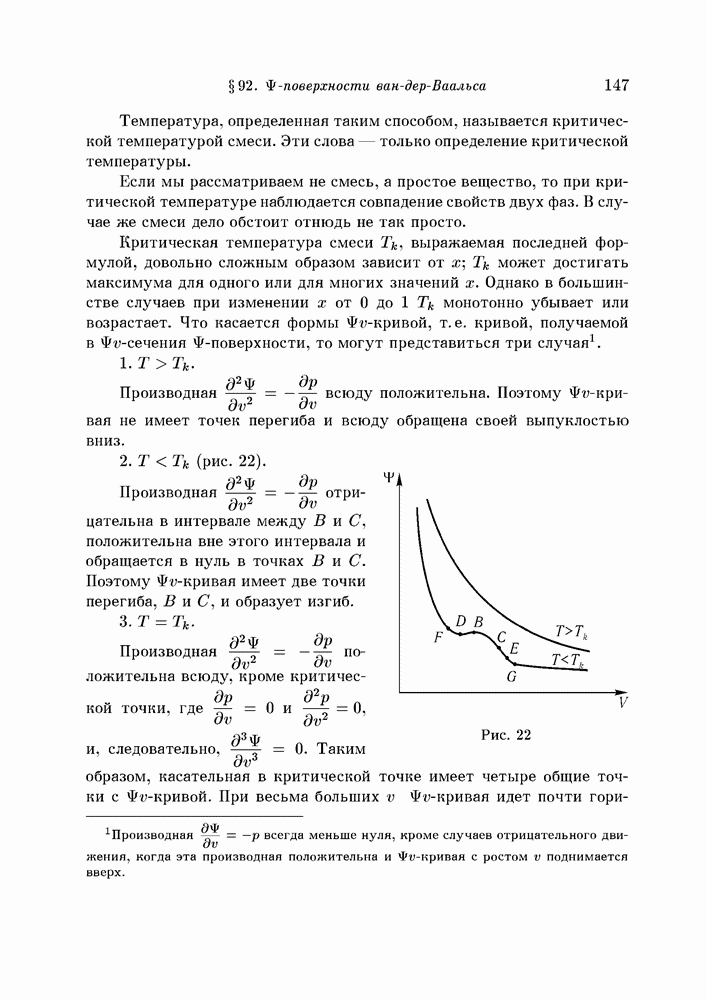
- § 92. поверхности ван-дер-Ваальса
- § 93. Изменение формы поверхности с температурой
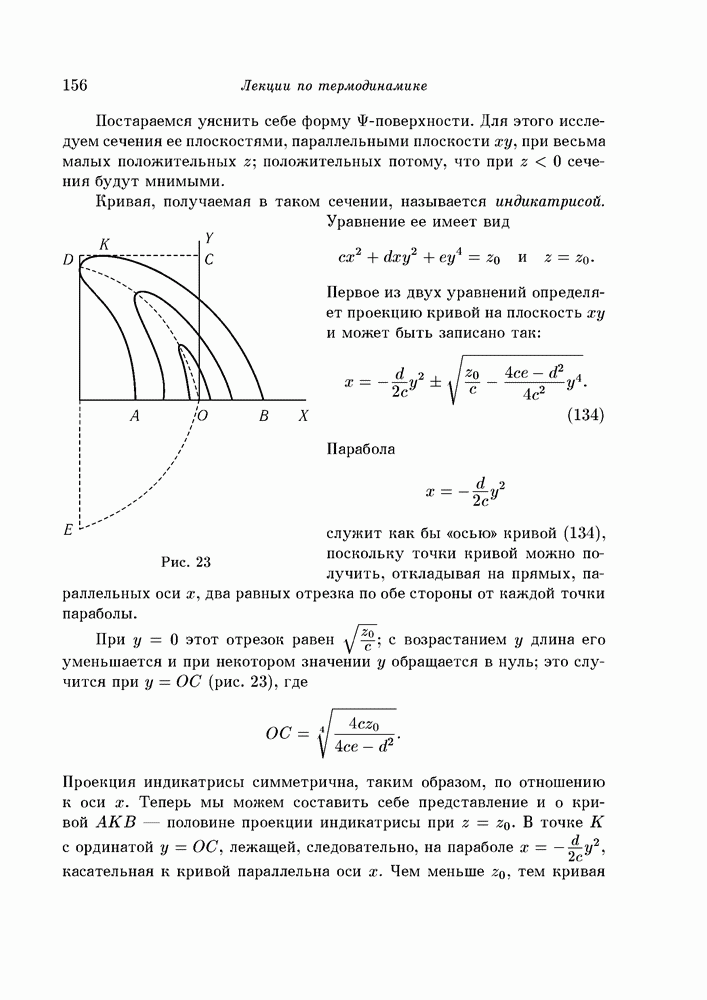
- § 94. Сечения Ф-поверхности
- § 95. Условия равновесия
- § 96. Сосуществующие фазы
- § 97. Математическая теория конечных точек складки
- § 98. Исследование Ф-поверхности в окрестности конечной точки складки
- § 99. Конечная точка складки первого рода
- § 100. Индикатриса, бинодаль и спинодаль
- § 101. Определение координат конечной точки складки непосредственно из самого уравнения Ф-поверхности
- § 102. Кривая конечных точек складки
- § 103. Изменение давления при бесконечно малом изменении состояния
- § 104. Зависимость давления от состава смеси
- § 105. Изобары
- § 106. Изотермическое сжатие смесей
- § 107. Обратная конденсация