| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 85. Число независимых условий равновесия
Определим теперь число взаимно независимых условий равновесия и посмотрим, какой результат можно отсюда извлечь. При заданном Т свободная энергия каждой фазы — однородная функция первого порядка от величины  . Если Тир постоянны, то термодинамический потенциал представляет собой также однородную функцию первого измерения от величин
. Если Тир постоянны, то термодинамический потенциал представляет собой также однородную функцию первого измерения от величин  . В самом деле, если нам задана некоторая фаза, то мы можем себе представить другую фазу с теми же
. В самом деле, если нам задана некоторая фаза, то мы можем себе представить другую фазу с теми же  , но
, но  второй фазы в
второй фазы в  раз больше тех же величин для первой фазы. Поэтому все производные типа
раз больше тех же величин для первой фазы. Поэтому все производные типа  суть функции отношений
суть функции отношений

т. е. функции плотностей компонент в каждой фазе.
Точно так же все производные  зависят от отношении
зависят от отношении

Нужно иметь в виду, что некоторые компоненты присутствуют не во всех фазах и что есть такие фазы, в которых не может присутствовать та или иная компонента. Наличие подобного рода фаз, очевидно, уменьшит число условий равновесия типа уравнений (108) и (109).
Разберем общий случай, когда первая компонента присутствует в  фазах, вторая — в
фазах, вторая — в  фазах и т. д. Для равновесия по отношению к первой компоненте мы получим
фазах и т. д. Для равновесия по отношению к первой компоненте мы получим  взаимно независимых уравнений типа (108), для равновесия по отношению ко второй компоненте
взаимно независимых уравнений типа (108), для равновесия по отношению ко второй компоненте  уравнений и т. д. Но у нас уже есть
уравнений и т. д. Но у нас уже есть  взаимно независимых уравнений типа (107), так что всего будет
взаимно независимых уравнений типа (107), так что всего будет

уравнений между производными от  по v и по m.
по v и по m.
Если первая фаза содержит  компонент, вторая
компонент, вторая  и т.д., то число отношений (112) — плотностей отдельных компонент в каждой фазе — равно
и т.д., то число отношений (112) — плотностей отдельных компонент в каждой фазе — равно

или

Итак, если  , т. е. число фаз на единицу больше числа компонент, то уравнений столько же, сколько неизвестных. Задание температуры полностью определяет тогда все плотности любой из компонент в каждой фазе, а следовательно, и давление, зависящее от этих плотностей. Температуру мы можем задать по желанию. Меняя ее, получим равновесие при другом давлении и с другим составом фаз, соответствующими новой температуре. При
, т. е. число фаз на единицу больше числа компонент, то уравнений столько же, сколько неизвестных. Задание температуры полностью определяет тогда все плотности любой из компонент в каждой фазе, а следовательно, и давление, зависящее от этих плотностей. Температуру мы можем задать по желанию. Меняя ее, получим равновесие при другом давлении и с другим составом фаз, соответствующими новой температуре. При  имеем
имеем  , удовлетворить всем уравнениям при любой температуре нельзя;
, удовлетворить всем уравнениям при любой температуре нельзя;  фазы находятся в равновесии только при определенном значении температуры, которое мы находим, как и плотности (112), из уравнений равновесия.
фазы находятся в равновесии только при определенном значении температуры, которое мы находим, как и плотности (112), из уравнений равновесия.
Для системы вода-пар или вода-лед  . Для системы, состоящей из соли, содержащей воду, ее водного раствора и водяного пара,
. Для системы, состоящей из соли, содержащей воду, ее водного раствора и водяного пара,  . В этом случае равновесие возможно при различных температурах, но лишь при вполне определенном давлении. С другой стороны, существование воды, льда и водяного пара или же двух твердых гидратов какой-либо соли, ее водного раствора и водяного пара возможно лишь при некоторой определенной температуре.
. В этом случае равновесие возможно при различных температурах, но лишь при вполне определенном давлении. С другой стороны, существование воды, льда и водяного пара или же двух твердых гидратов какой-либо соли, ее водного раствора и водяного пара возможно лишь при некоторой определенной температуре.
Те же выводы можно получить, пользуясь и термодинамическим потенциалом. Тогда число уравнений типа (109) будет

и эти уравнения, кроме p и Т, содержат еще отношения (113), из них

отношений, взаимно независимых. Если  , а потому
, а потому  , то при заданной температуре все эти отношения можно определить из уравнений равновесия. Если же число фаз на два больше числа компонент, так что
, то при заданной температуре все эти отношения можно определить из уравнений равновесия. Если же число фаз на два больше числа компонент, так что  , то определится также и температура.
, то определится также и температура.
n веществ, распределенных между числом фаз, меньшим  , могут давать при заданной температуре множество различных состояний равновесия, отличающихся друг от друга давлением, плотностью и составом ряда фаз. Но если известны
, могут давать при заданной температуре множество различных состояний равновесия, отличающихся друг от друга давлением, плотностью и составом ряда фаз. Но если известны  и масса каждой компоненты во всей системе, то состояние равновесия системы полностью определено и в этом случае. Ибо условия последнего типа дают еще
и масса каждой компоненты во всей системе, то состояние равновесия системы полностью определено и в этом случае. Ибо условия последнего типа дают еще  уравнений между величинами
уравнений между величинами  . Всего уравнений будет
. Всего уравнений будет

т.е. столько же, сколько и неизвестных величин  число которых есть
число которых есть

Пусть число фаз в системе меньше, чем  . Если при заданной температуре известны объем системы и количество каждой компоненты, то состояние равновесия системы полностью определится. Это положение доказывается аналогично предыдущему.
. Если при заданной температуре известны объем системы и количество каждой компоненты, то состояние равновесия системы полностью определится. Это положение доказывается аналогично предыдущему.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редактора к первому изданию
- § 1. Основные понятия термодинамики
- § 2. Первое начало термодинамики
- § 3. Другой пример вычисления работы
- § 4. Приложение к идеальным газам
- § 5. Стационарный ток жидкости через трубу с переменным сечением
- § 6. Однородное тело
- § 7. Применение первого начала к химии: теплота реакции и температура
- § 8. Второе начало термодинамики
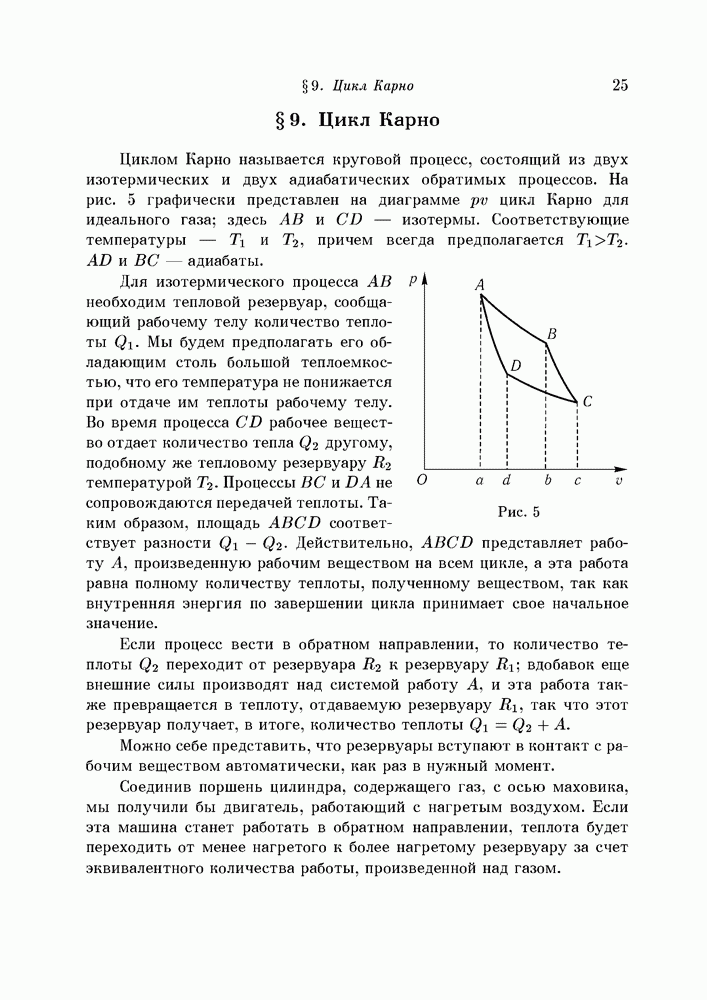
- § 9. Цикл Карно
- § 10. Коэффициент полезного действия. Универсальная функция температуры
- § 11. Другой способ определения универсальной функции температуры
- § 12. Второе начало для обратимых процессов
- § 13. Второе начало для обратимых процессов [общий случай]
- § 14. Различные обратимые пути между двумя состояниями. Энтропия
- § 15. Несколько простейших приложений
- § 16. Отношение теплоемкостей
- § 17. Система с произвольным числом параметров
- § 18. Значение полученных общих формул
- § 19. Значение второго начала
- § 20. Приложения второго начала к адиабатическим процессам
- § 21. Сжатие жидкостей
- § 22. Опыты по адиабатическому растяжению проволок
- § 23. Непосредственный вывод уравнения адиабатических процессов
- § 24. Применение к жидким пленкам
- § 25. Применение к гальваническому элементу
- § 26. Уравнение Клапейрона
- § 27. Опытная проверка уравнения Клапейрона (Клаузиус)
- § 28. Опыты де-Виссера с уксусной кислотой
- § 29. Режеляция льда
- § 30. Закон Стефана-Больцмана
- § 31. Другие выражения второго начала
- § 32. Свойства энтропии
- § 33. Свободная энергия
- § 34. Термодинамический потенциал
- § 35. Свободная энергия идеального газа
- § 36. Неравновесные состояния
- § 37. Необратимые процессы
- § 38. Изотермический процесс
- § 39. Свободная энергия и работа
- § 40. Обобщенные силы
- § 41. Условия равновесия
- § 42. Система в поле консервативных сил
- § 43. Газ или жидкость в поле силы тяжести
- § 44. Решение того же вопроса с помощью энтропии
- § 45. Система жидкость-пар
- § 46. Равновесие трехфазной системы
- § 47. Упругость пара над разбавленным раствором
- § 48. Различие в давлении пара над чистой водой и над раствором
- § 49. Смеси
- § 50. Двухкомпонентная система
- § 51. Устойчивые и неустойчивые жидкие фазы; равновесие между двумя жидкими фазами
- § 52. Равновесие между твердой и жидкой фазами; переохлаждение
- § 53. Равновесие трехфазной системы, состоящей из двух компонент
- § 54. Равновесие раствора соли с ее твердым гидратом
- § 55. Равновесие между двумя растворами различной концентрации
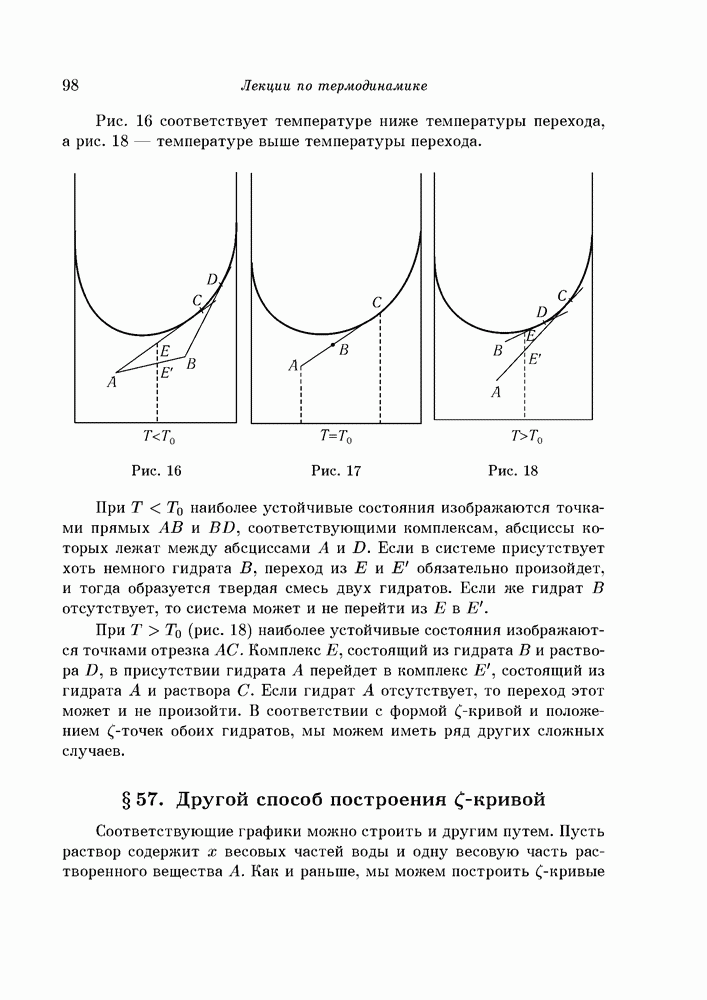
- § 56. Система из двух гидратов
- § 57. Другой способ построения кривой
- § 58. Трехкомпонентные системы
- § 59. Трехфазная система из трех компонент
- § 60. Форма поверхности
- § 61. Условия равновесия между твердой и жидкой фазами
- § 62. Равновесие двух твердых фаз с жидкими фазами
- § 63. Равновесие между двумя жидкими фазами
- § 64. Другие способы построения поверхности
- § 65. Смешанные кристаллы
- § 66. Равновесие между смесями и растворами
- § 67. Неопределенность в выражении термодинамического потенциала
- § 68. Смесь газов в поле силы тяжести
- § 69. Смешение и разделение двух газов
- § 70. Парадокс Гиббса
- § 71. Обобщение теоремы Гиббса на случай трех и более газов
- § 72. Уменьшение свободной энергии при смешении двух газов
- § 73. Свободная энергия жидкой смеси
- § 74. Общее выражение для свободной энергии смеси
- § 75. Случай, когда одна из компонент присутствует в весьма малом количестве
- § 76. Равновесие двух фаз, каждая из которых состоит из двух компонент
- § 77. Смесь под действием внешних сил
- § 78. Вывод уравнений равновесия
- § 79. Второй пример системы под действием внешних сил
- § 80. Осмотическое давление. Закон вант-Гоффа
- § 81. Другой вывод закона вант-Гоффа
- § 82. Общие условия равновесия многофазных систем
- § 83. Равновесие трех фаз
- § 84. Вывод условий равновесия с помощью термодинамического потенциала
- § 85. Число независимых условий равновесия
- § 86. Сравнение между собой двух состояний равновесия
- § 87. Общее соотношение между двумя состояниями равновесия
- § 88. Смысл полученного соотношения
- § 89. Добавление некоторого весьма малого количества новой компоненты
- § 90. Несколько заключительных замечаний
- § 91. Диссоциация газа
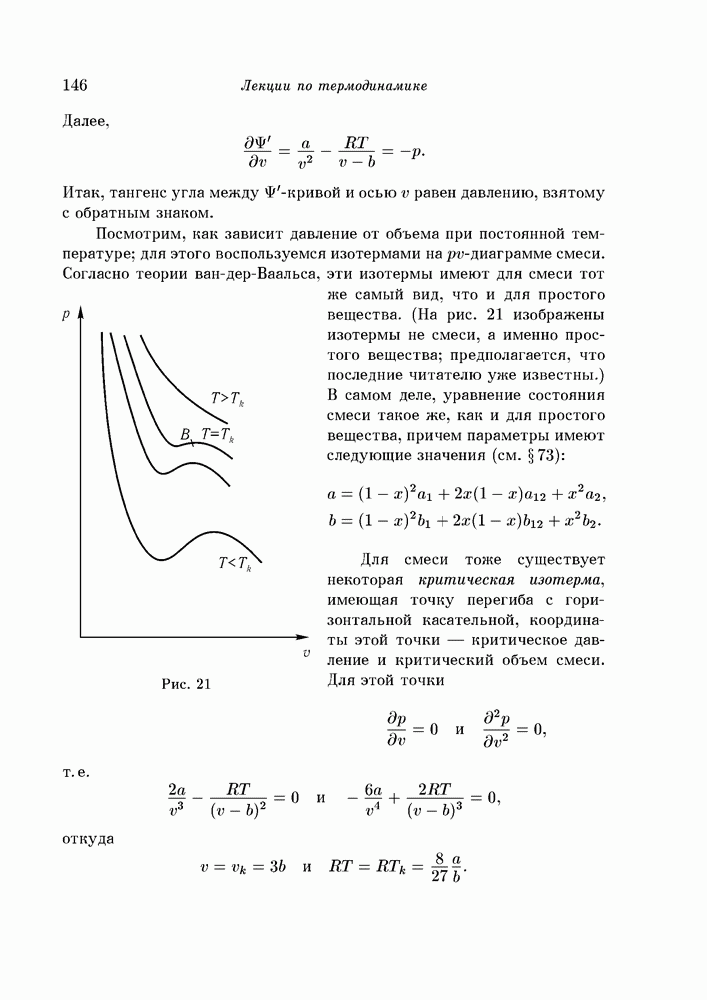
- § 92. поверхности ван-дер-Ваальса
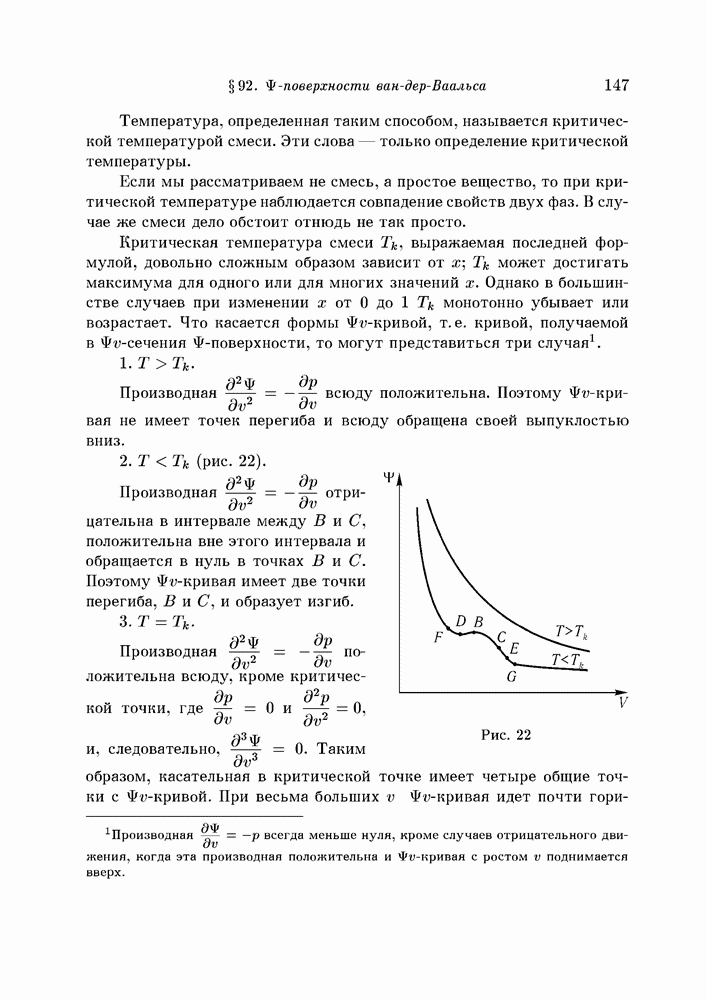
- § 93. Изменение формы поверхности с температурой
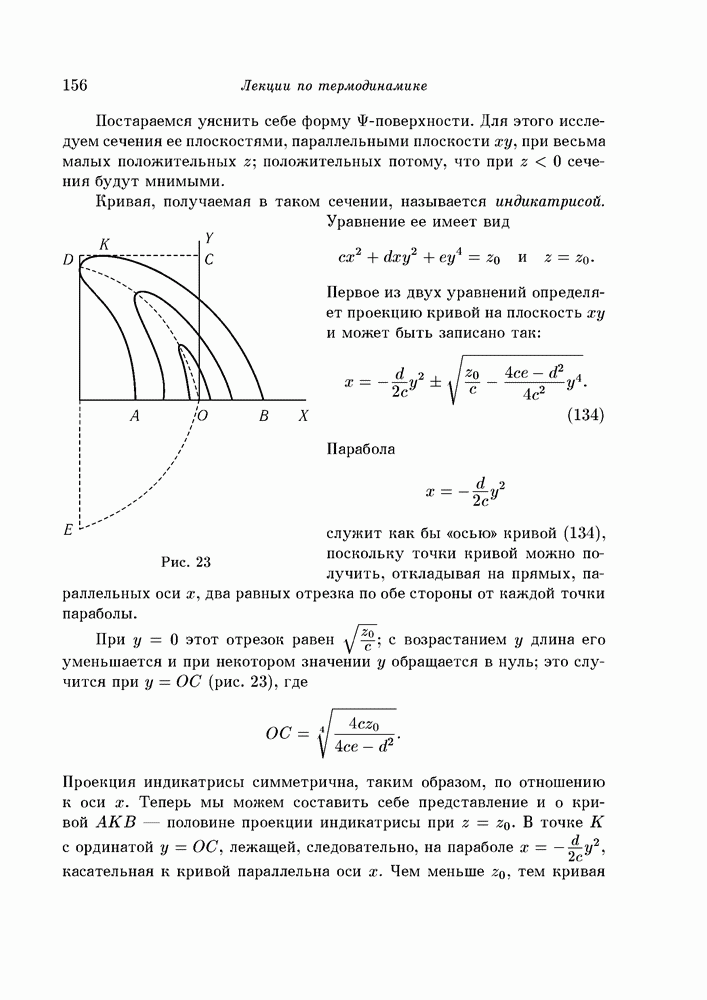
- § 94. Сечения Ф-поверхности
- § 95. Условия равновесия
- § 96. Сосуществующие фазы
- § 97. Математическая теория конечных точек складки
- § 98. Исследование Ф-поверхности в окрестности конечной точки складки
- § 99. Конечная точка складки первого рода
- § 100. Индикатриса, бинодаль и спинодаль
- § 101. Определение координат конечной точки складки непосредственно из самого уравнения Ф-поверхности
- § 102. Кривая конечных точек складки
- § 103. Изменение давления при бесконечно малом изменении состояния
- § 104. Зависимость давления от состава смеси
- § 105. Изобары
- § 106. Изотермическое сжатие смесей
- § 107. Обратная конденсация