| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 38. Изотермический процесс
Легко показать, что для изотермических процессов  . Это можно, впрочем, вывести и из неравенства
. Это можно, впрочем, вывести и из неравенства  (§ 13), положив
(§ 13), положив 
Представим себе систему М, совершающую изотермический круговой процесс. Резервуар R пусть имеет ту же температуру, что и система. Чтобы сообщить или отнять у системы теплоту, не потребуется тогда никаких циклов Карно (см. § 13), ибо теплообмен можно осуществить попросту приведя в соприкосновение систему и резервуар. Мы утверждаем, что  . В самом деле, если
. В самом деле, если  , то система получит от резервуара R за весь цикл некоторое количество теплоты; но поскольку, закончив цикл, система возвращается в начальное состояние, то эта теплота, очевидно, целиком превращена в работу, что противоречит принципу Кельвина. Отсюда заключаем, что
, то система получит от резервуара R за весь цикл некоторое количество теплоты; но поскольку, закончив цикл, система возвращается в начальное состояние, то эта теплота, очевидно, целиком превращена в работу, что противоречит принципу Кельвина. Отсюда заключаем, что  .
.
При обратимом процессе знак  исключается. Иными словами, при обратимом изотермическом круговом процессе алгебраическая сумма количеств теплоты, сообщенных системе, а следовательно, и работа системы равны нулю. Уже издавна известно, что невозможно осуществить вечный двигатель, т. е. машину, дающую работу без всякого воздействия извне. Теперь мы убедились, что невозможно осуществить и такое устройство, все части которого имели бы одинаковую температуру и которое производило бы работу за счет энергии, заимствованной у теплового резервуара той же самой температуры. Это положение выражают обычно словами: невозможно построить вечный двигатель второго рода.
исключается. Иными словами, при обратимом изотермическом круговом процессе алгебраическая сумма количеств теплоты, сообщенных системе, а следовательно, и работа системы равны нулю. Уже издавна известно, что невозможно осуществить вечный двигатель, т. е. машину, дающую работу без всякого воздействия извне. Теперь мы убедились, что невозможно осуществить и такое устройство, все части которого имели бы одинаковую температуру и которое производило бы работу за счет энергии, заимствованной у теплового резервуара той же самой температуры. Это положение выражают обычно словами: невозможно построить вечный двигатель второго рода.
Пользуясь только что доказанной теоремой, можно прийти к новому представлению о свободной энергии. Представим себе опять обратимый изотермический процесс с тепловым резервуаром R той же температуры, что и система. Резервуар этот находится в контакте с рассматриваемой системой. Раз работа для всякого обратимого изотермического цикла равна нулю, то и работа, произведенная при переходе системы из одного состояния в другое, не зависит от пути перехода. Это приводит нас к заключению, что в каждом своем состоянии А система обладает способностью произвести некоторое количество работы. Выбрав некоторое состояние N за нормальное, мы назовем работу, которую произведет система при переходе из А в N по обратимому изотермическому пути, свободной энергией системы в состоянии А. Такое определение сходно с определением внутренней энергии, но эти два определения нельзя смешивать друг с другом. Для этого достаточно вспомнить роль резервуара R. Работа, произведенная системой при переходе из А в N, не равна, вообще говоря, энергии, потерянной системой при этом переходе, так как работа эта производится, частью или целиком, за счет теплоты, заимствованной системой у резервуара.
Разница между внутренней и свободной энергией особенно бросается в глаза в случае идеального газа. Представим себе, что стенки сосуда, куда заключен идеальный газ, составляют часть теплового резервуара. Сосуд с газом пусть закрывается поршнем. Чем меньше его объем, тем большую работу может произвести газ при своем расширении, тем больше, значит, и его свободная энергия. С другой стороны, внутренняя энергия зависит только от температуры, а не от объема. Таким образом, при обратимом изотермическом расширении идеальный газ совершает работу целиком за счет теплоты, потерянной резервуаром.
Для системы вода-пар при уменьшении внутренней энергии свободная энергия даже возрастает, а при возрастании внутренней энергии — уменьшается. Действительно, при испарении воды свободная энергия уменьшается, ибо уменьшается способность производить работу, в то же время внутренняя энергия при испарении увеличивается.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редактора к первому изданию
- § 1. Основные понятия термодинамики
- § 2. Первое начало термодинамики
- § 3. Другой пример вычисления работы
- § 4. Приложение к идеальным газам
- § 5. Стационарный ток жидкости через трубу с переменным сечением
- § 6. Однородное тело
- § 7. Применение первого начала к химии: теплота реакции и температура
- § 8. Второе начало термодинамики
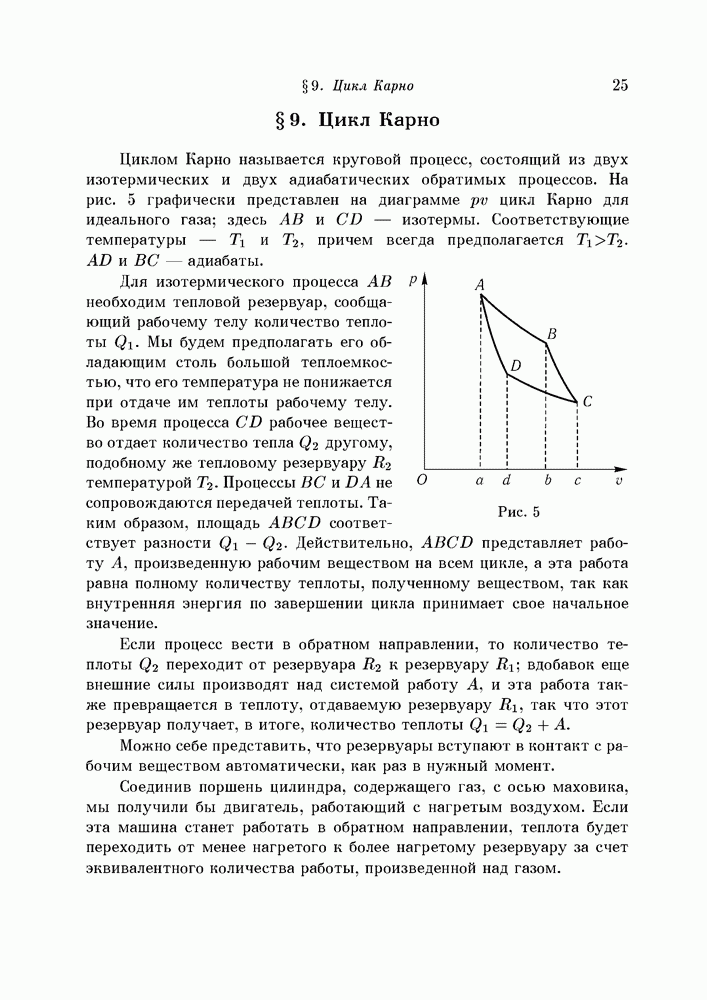
- § 9. Цикл Карно
- § 10. Коэффициент полезного действия. Универсальная функция температуры
- § 11. Другой способ определения универсальной функции температуры
- § 12. Второе начало для обратимых процессов
- § 13. Второе начало для обратимых процессов [общий случай]
- § 14. Различные обратимые пути между двумя состояниями. Энтропия
- § 15. Несколько простейших приложений
- § 16. Отношение теплоемкостей
- § 17. Система с произвольным числом параметров
- § 18. Значение полученных общих формул
- § 19. Значение второго начала
- § 20. Приложения второго начала к адиабатическим процессам
- § 21. Сжатие жидкостей
- § 22. Опыты по адиабатическому растяжению проволок
- § 23. Непосредственный вывод уравнения адиабатических процессов
- § 24. Применение к жидким пленкам
- § 25. Применение к гальваническому элементу
- § 26. Уравнение Клапейрона
- § 27. Опытная проверка уравнения Клапейрона (Клаузиус)
- § 28. Опыты де-Виссера с уксусной кислотой
- § 29. Режеляция льда
- § 30. Закон Стефана-Больцмана
- § 31. Другие выражения второго начала
- § 32. Свойства энтропии
- § 33. Свободная энергия
- § 34. Термодинамический потенциал
- § 35. Свободная энергия идеального газа
- § 36. Неравновесные состояния
- § 37. Необратимые процессы
- § 38. Изотермический процесс
- § 39. Свободная энергия и работа
- § 40. Обобщенные силы
- § 41. Условия равновесия
- § 42. Система в поле консервативных сил
- § 43. Газ или жидкость в поле силы тяжести
- § 44. Решение того же вопроса с помощью энтропии
- § 45. Система жидкость-пар
- § 46. Равновесие трехфазной системы
- § 47. Упругость пара над разбавленным раствором
- § 48. Различие в давлении пара над чистой водой и над раствором
- § 49. Смеси
- § 50. Двухкомпонентная система
- § 51. Устойчивые и неустойчивые жидкие фазы; равновесие между двумя жидкими фазами
- § 52. Равновесие между твердой и жидкой фазами; переохлаждение
- § 53. Равновесие трехфазной системы, состоящей из двух компонент
- § 54. Равновесие раствора соли с ее твердым гидратом
- § 55. Равновесие между двумя растворами различной концентрации
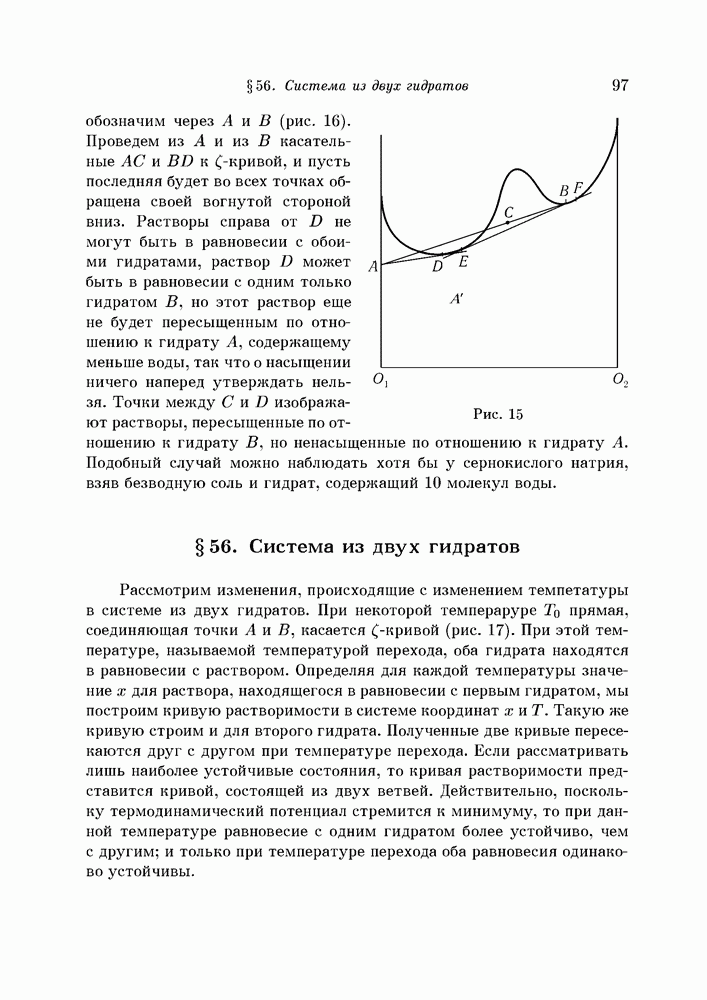
- § 56. Система из двух гидратов
- § 57. Другой способ построения кривой
- § 58. Трехкомпонентные системы
- § 59. Трехфазная система из трех компонент
- § 60. Форма поверхности
- § 61. Условия равновесия между твердой и жидкой фазами
- § 62. Равновесие двух твердых фаз с жидкими фазами
- § 63. Равновесие между двумя жидкими фазами
- § 64. Другие способы построения поверхности
- § 65. Смешанные кристаллы
- § 66. Равновесие между смесями и растворами
- § 67. Неопределенность в выражении термодинамического потенциала
- § 68. Смесь газов в поле силы тяжести
- § 69. Смешение и разделение двух газов
- § 70. Парадокс Гиббса
- § 71. Обобщение теоремы Гиббса на случай трех и более газов
- § 72. Уменьшение свободной энергии при смешении двух газов
- § 73. Свободная энергия жидкой смеси
- § 74. Общее выражение для свободной энергии смеси
- § 75. Случай, когда одна из компонент присутствует в весьма малом количестве
- § 76. Равновесие двух фаз, каждая из которых состоит из двух компонент
- § 77. Смесь под действием внешних сил
- § 78. Вывод уравнений равновесия
- § 79. Второй пример системы под действием внешних сил
- § 80. Осмотическое давление. Закон вант-Гоффа
- § 81. Другой вывод закона вант-Гоффа
- § 82. Общие условия равновесия многофазных систем
- § 83. Равновесие трех фаз
- § 84. Вывод условий равновесия с помощью термодинамического потенциала
- § 85. Число независимых условий равновесия
- § 86. Сравнение между собой двух состояний равновесия
- § 87. Общее соотношение между двумя состояниями равновесия
- § 88. Смысл полученного соотношения
- § 89. Добавление некоторого весьма малого количества новой компоненты
- § 90. Несколько заключительных замечаний
- § 91. Диссоциация газа
- § 92. поверхности ван-дер-Ваальса
- § 93. Изменение формы поверхности с температурой
- § 94. Сечения Ф-поверхности
- § 95. Условия равновесия
- § 96. Сосуществующие фазы
- § 97. Математическая теория конечных точек складки
- § 98. Исследование Ф-поверхности в окрестности конечной точки складки
- § 99. Конечная точка складки первого рода
- § 100. Индикатриса, бинодаль и спинодаль
- § 101. Определение координат конечной точки складки непосредственно из самого уравнения Ф-поверхности
- § 102. Кривая конечных точек складки
- § 103. Изменение давления при бесконечно малом изменении состояния
- § 104. Зависимость давления от состава смеси
- § 105. Изобары
- § 106. Изотермическое сжатие смесей
- § 107. Обратная конденсация