| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
На разрыв и образование связей, а следовательно, на реакционную способность органических соединений, влияет целый ряд факторов. Мы уже указывали, что химические свойства целых классов соединений часто определяются наличием у них общей функциональной группы. Однако даже в какой-либо конкретной реакции с одним соединением реакционная способность другого соединения может варьировать в широких пределах. В гл. 9 было рассказано о том, что скорость протекания реакции может зависеть от температуры, давления, степени измельчения вещества и наличия катализатора, а в гл. 7 было показано, что температура может влиять и на константу равновесия.
Растворители тоже могут оказывать существенное влияние на химический процесс и на его константу равновесия. Классическим примером является хлороводород. При растворении в воде он ионизируется, образуя сильную кислоту (см. разд. 8.1). Полученный раствор - соляная кислота - представляет собой сильный электролит. Однако раствор хлороводорода в метилбензоле (толуоле) не обладает электропроводностью. Влияние такого типа называется эффектом растворителя. К числу эффектов растворителя относятся образование водородной связи или возникновение диполь-дипольного взаимодействия между молекулами растворителя и растворенного вещества (см. гл. 2).
Влияние растворителя на слабые карбоновые кислоты иллюстрируются данными табл. 17.9, в которой указаны значения константы диссоциации этановой (уксусной) кислоты в различных растворителях. Максимальное значение константа диссоциации имеет в чистой воде, которая является полярным растворителем. Если концентрация менее полярного растворителя в смеси, каким является метанол или диоксан, возрастает, константа диссоциации кислоты уменьшается.

Таблица 17.9. Влияние растворителя на константу диссоциации уксусной кислоты при 25°С

Эффекты растворителя могут рассматриваться как влияние окружающей среды на реакционную способность молекулы. Но на реакционную способность какой-либо функциональной группы в молекуле может оказывать влияние и непосредственное окружение этой функциональной группы в самой молекуле (так называемое химическое окружение). Влияние такого типа называется структурным эффектом.
Структурные эффекты в самой молекуле в свою очередь подразделяются на две разновидности: электронные эффекты и стерические эффекты.
Электронные эффекты
Электронные эффекты тоже бывают нескольких типов. Наиболее важными из них являются два: индуктивный эффект и мезомерный  эффект.
эффект.
Индуктивный эффект. Этот эффект возникает только в простых ковалентных связях между неодинаковыми атомами. Из-за различной электроотрицательности таких атомов подобные связи обычно поляризованы. Ранее мы уже показывали, что ковалентная связь между атомами углерода и хлора оказывается поляризованной. Такую связь можно схематически изобразить следующим образом:

Вместо этого поляризацию связи можно указывать стрелкой:

В данном случае стрелка показывает, что атом углерода отталкивает связывающие электроны, а атом хлора из-за своей большей электроотрицательности притягивает связывающие электроны. Поэтому на атоме хлора сосредоточивается большая электронная плотность, а на атоме углерода создается недостаточная электронная плотность. Это смещение (сдвиг) электронной плотности от одного атома к другому и возникающая в результате поляризация связи называются индуктивным эффектом. Те атомы и группы атомов, которые обладают большей электроотрицательностью
ностью, чем углерод, в связях с углеродом оттягивают от него электроны. Это оттягивание электронов называется отрицательным индуктивным эффектом или  -эффектом. Другие атомы и группы, которые менее электроотрицательны по сравнению с углеродом, наоборот, уступают электроны атому углерода в связях с ним. Такая ситуация (она встречается реже) называется положительным индуктивным эффектом или +/- эффектом. Положительным индуктивным эффектом обладают алкильные группы. Этот эффект тем больше, чем больше число алкильных групп, присоединенных к атому углерода, например
-эффектом. Другие атомы и группы, которые менее электроотрицательны по сравнению с углеродом, наоборот, уступают электроны атому углерода в связях с ним. Такая ситуация (она встречается реже) называется положительным индуктивным эффектом или +/- эффектом. Положительным индуктивным эффектом обладают алкильные группы. Этот эффект тем больше, чем больше число алкильных групп, присоединенных к атому углерода, например

Увеличение положительного индуктивного эффекта
Мезомерный эффект. Эти эффекты возникают в молекулах с кратными связями и распространяются по  -орбиталям. Мезомерный эффект проявляется в перераспределении
-орбиталям. Мезомерный эффект проявляется в перераспределении  -электронов и приводит к стабилизации молекул и некоторых радикалов, а также карбанионов или карбкатионов. В качестве примера рассмотрим гидролиз
-электронов и приводит к стабилизации молекул и некоторых радикалов, а также карбанионов или карбкатионов. В качестве примера рассмотрим гидролиз  в водно-спиртовом растворе гидроксида натрия. Продуктом этой реакции является
в водно-спиртовом растворе гидроксида натрия. Продуктом этой реакции является  (аллиловый спирт):
(аллиловый спирт):

Согласно современным воззрениям, эта реакция протекает через образование промежуточного продукта-пропенового карбкатиона. Последний можно рассматривать как резонансный гибрид двух предельных (резонансных) структур (см. гл. 2):

Двусторонняя стрелка  этой схеме указывает, что реальный карбкатион представляет собой нечто промежуточное между этими двумя структурами.
этой схеме указывает, что реальный карбкатион представляет собой нечто промежуточное между этими двумя структурами.
Стабилизация этого резонансного гибрида обусловлена делокализацией  -электронов, которую можно представить себе следующим образом. С одной стороны, два
-электронов, которую можно представить себе следующим образом. С одной стороны, два  -электрона ненасыщенной связи в одной резонансной структуре притягиваются к положительно заряженному атому углерода:
-электрона ненасыщенной связи в одной резонансной структуре притягиваются к положительно заряженному атому углерода:

С другой стороны, два  -электрона в другой резонансной структуре тоже притягиваются к положительно заряженному атому углерода в этой структуре:
-электрона в другой резонансной структуре тоже притягиваются к положительно заряженному атому углерода в этой структуре:

Однако следует подчеркнуть, что резонансный гибрид вовсе не является равновесной смесью двух резонансных структур, а представляет собой нечто среднее из двух этих структур.
Мезомерный эффект имеет особенно важное значение для сопряженных систем, т.е. таких систем, в молекулах которых чередуются простые и двойные связи. Примером соединения, имеющего сопряженную систему связей, является  . В такой системе мезомерный эффект передается по сопряженной цепи атомов
. В такой системе мезомерный эффект передается по сопряженной цепи атомов
углерода. Электронное строение бута-1,3-диена можно представить как гибрид двух резонансных структур:

Мезомерный эффект характерен также для соединений, содержащих карбонильную группу:

Стерические эффекты
Наиболее важным примером влияния стерических факторов на реакционную способность органических соединений является стерическое препятствие. Стерическое препятствие может возникнуть в тех случаях, когда молекула имеет объемистые группы, которые механически препятствуют протеканию реакции. В качестве примера укажем 2,6-дизамещенные производные бензойные кислоты:

Из-за наличия двух метальных групп вблизи карбоксильной группы она не может свободно вращаться вокруг связи между атомом углерода и бензольным кольцом. Поэтому карбоксильная группа оказывается фиксированной в одном положении, перпендикулярном к бензольному кольцу. В результате наличия такого стерического фактора 2,6-дизамещенные бензойные кислоты плохо поддаются обычным методам этерификации (превращения в сложные эфиры).
Стерическое препятствие исключает свободное внутримолекулярное вращение вокруг большинства простых углерод-углеродных связей.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
- ПЕРИОДИЧНОСТЬ
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
- 13.3. Распространенность в природе, получение и применение
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
- 16.3. Распространенность, получение и применение галогенов и их соединений
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
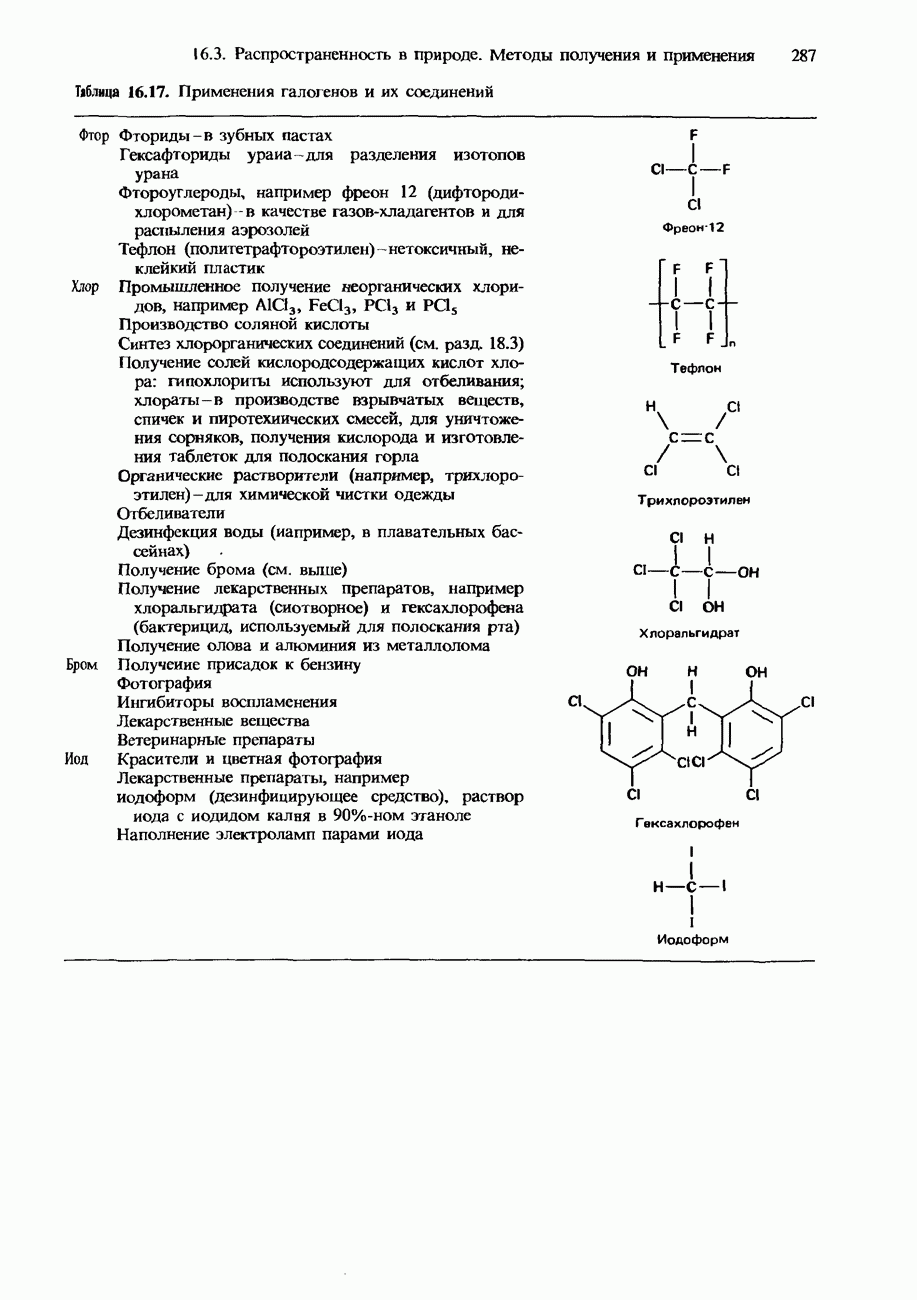
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
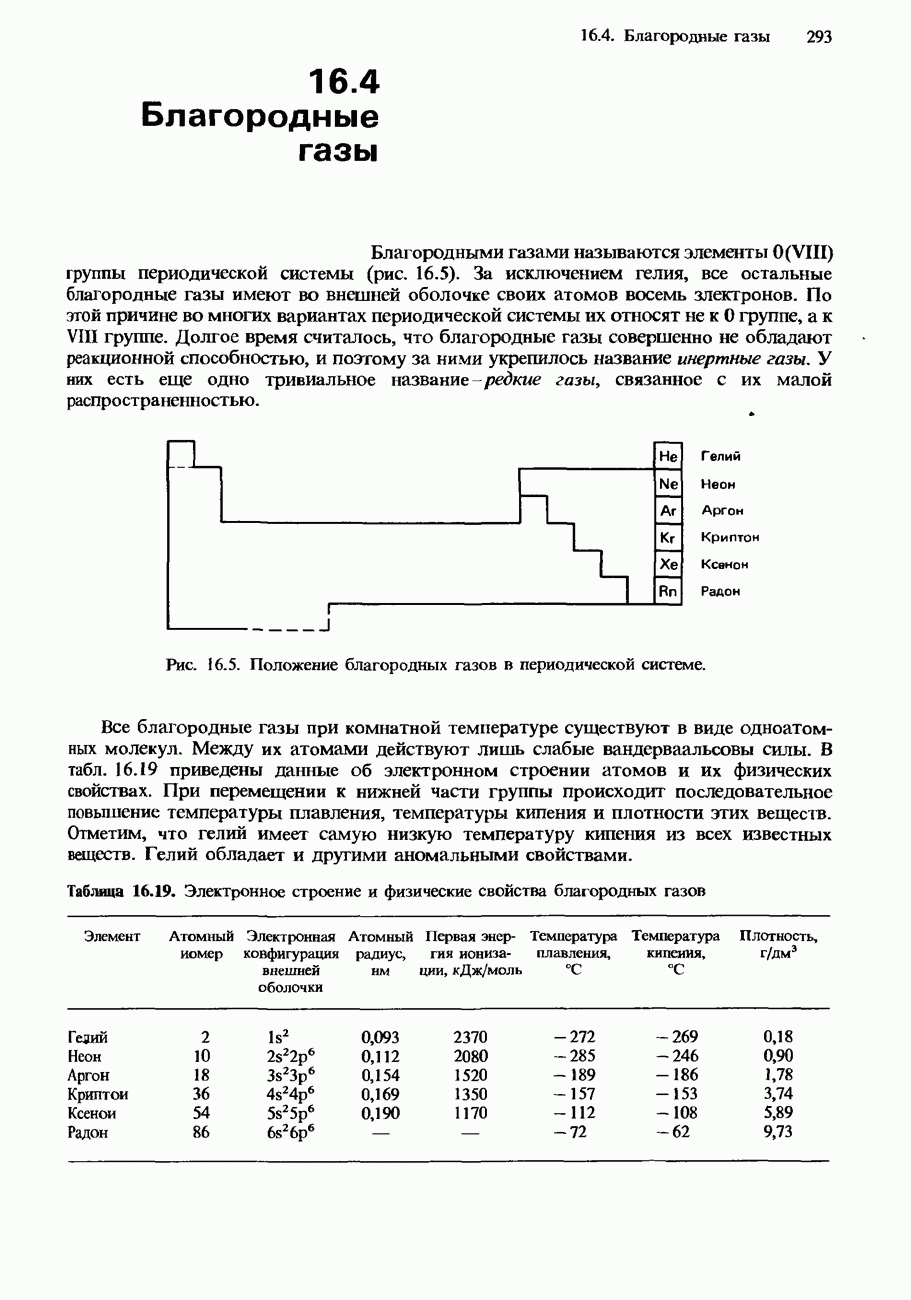
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
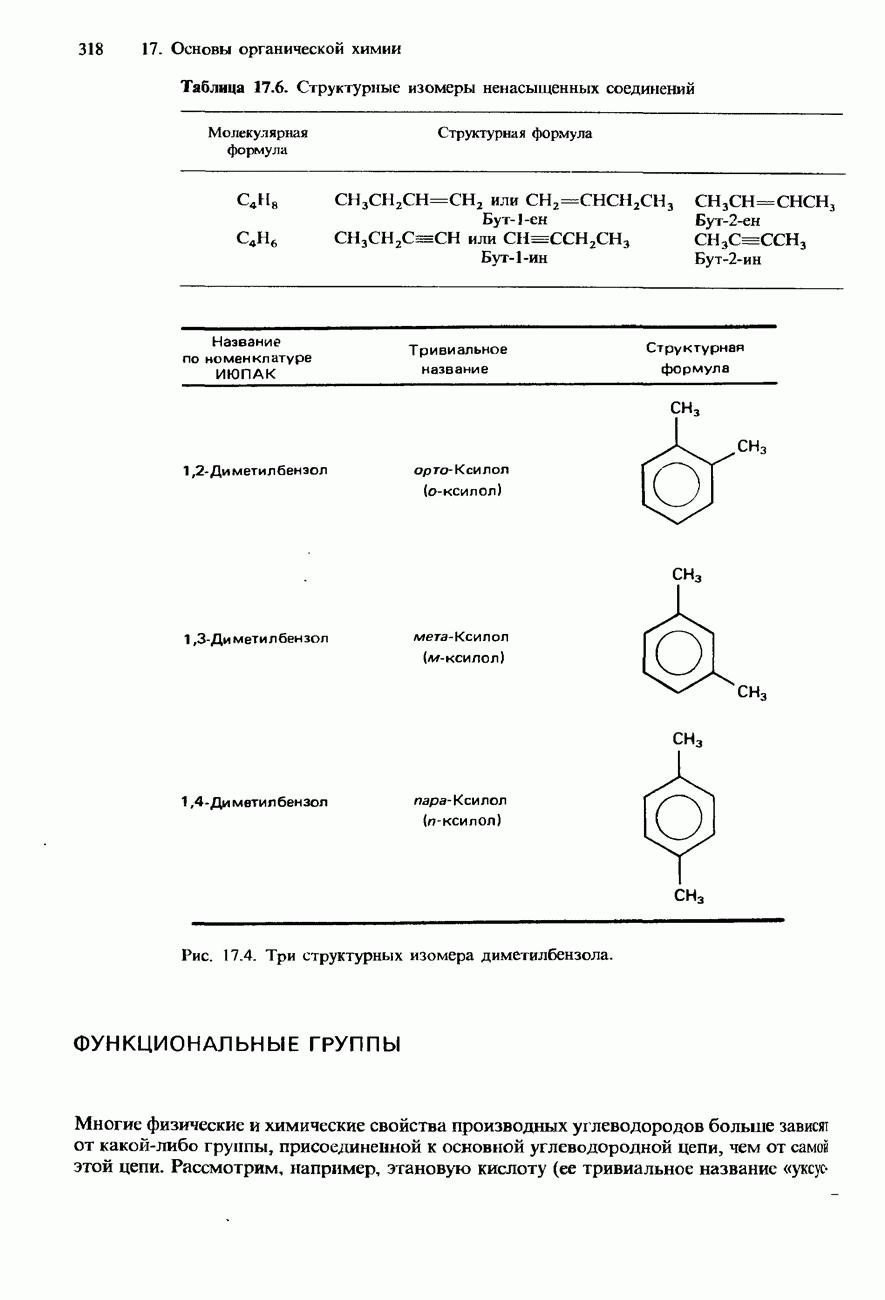
- УГЛЕВОДОРОДЫ
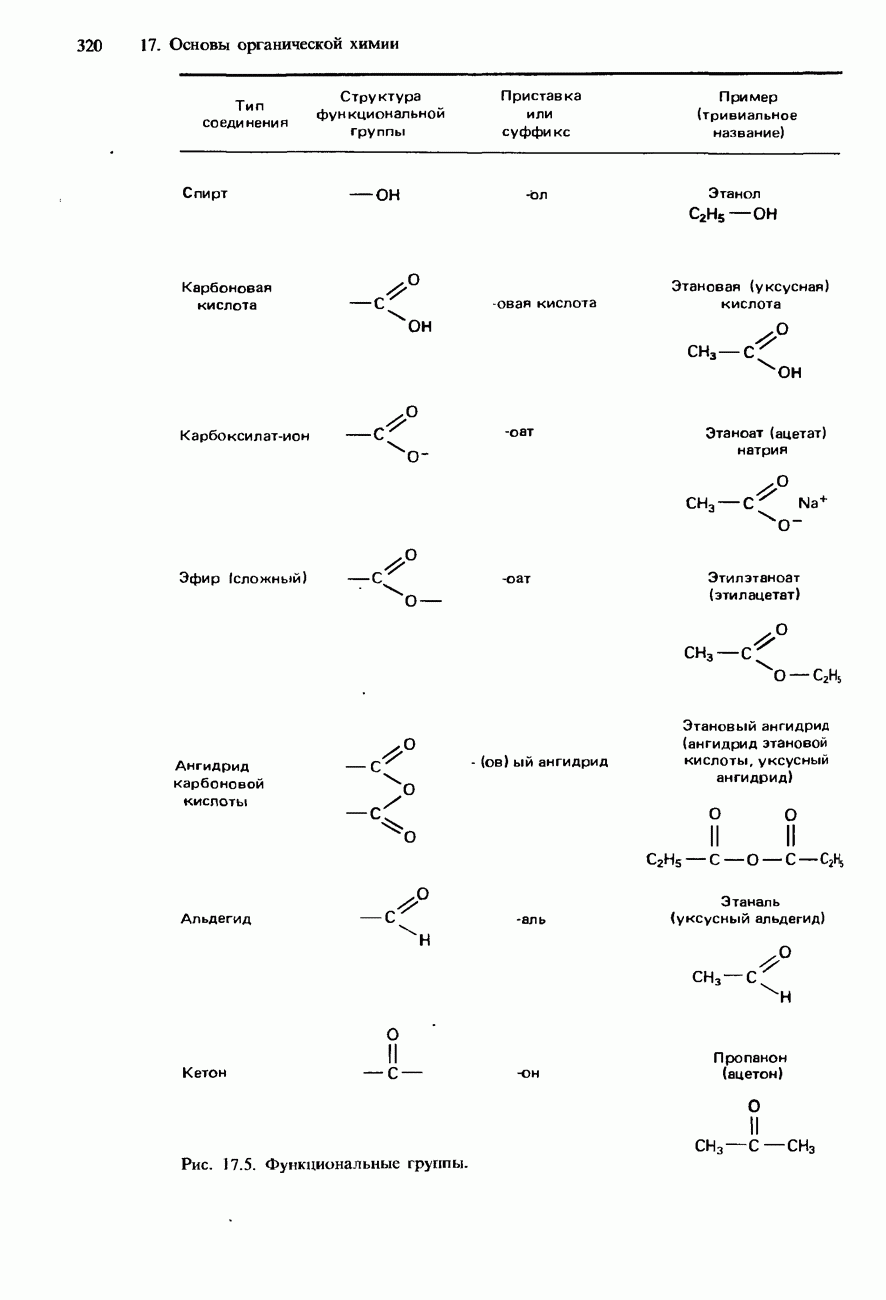
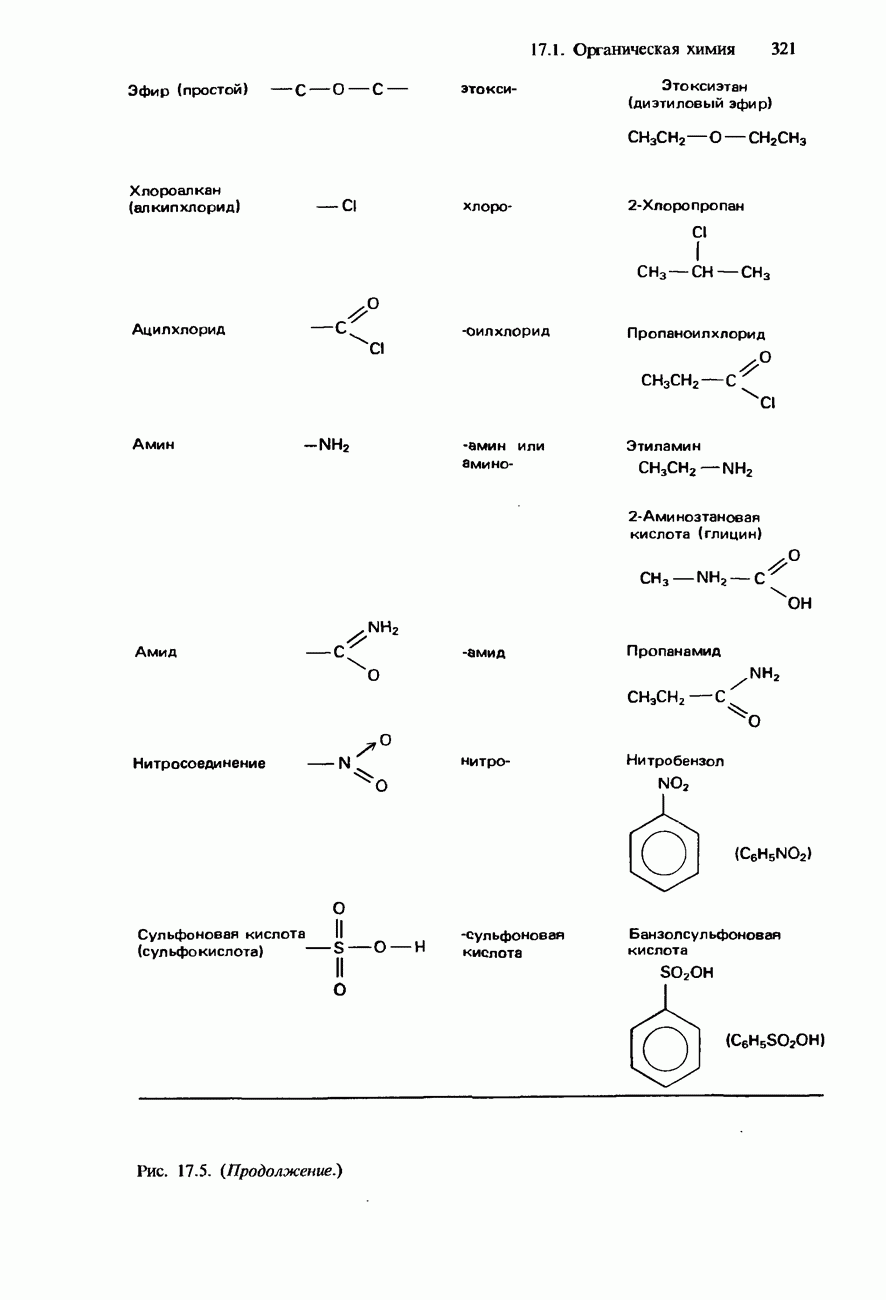
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
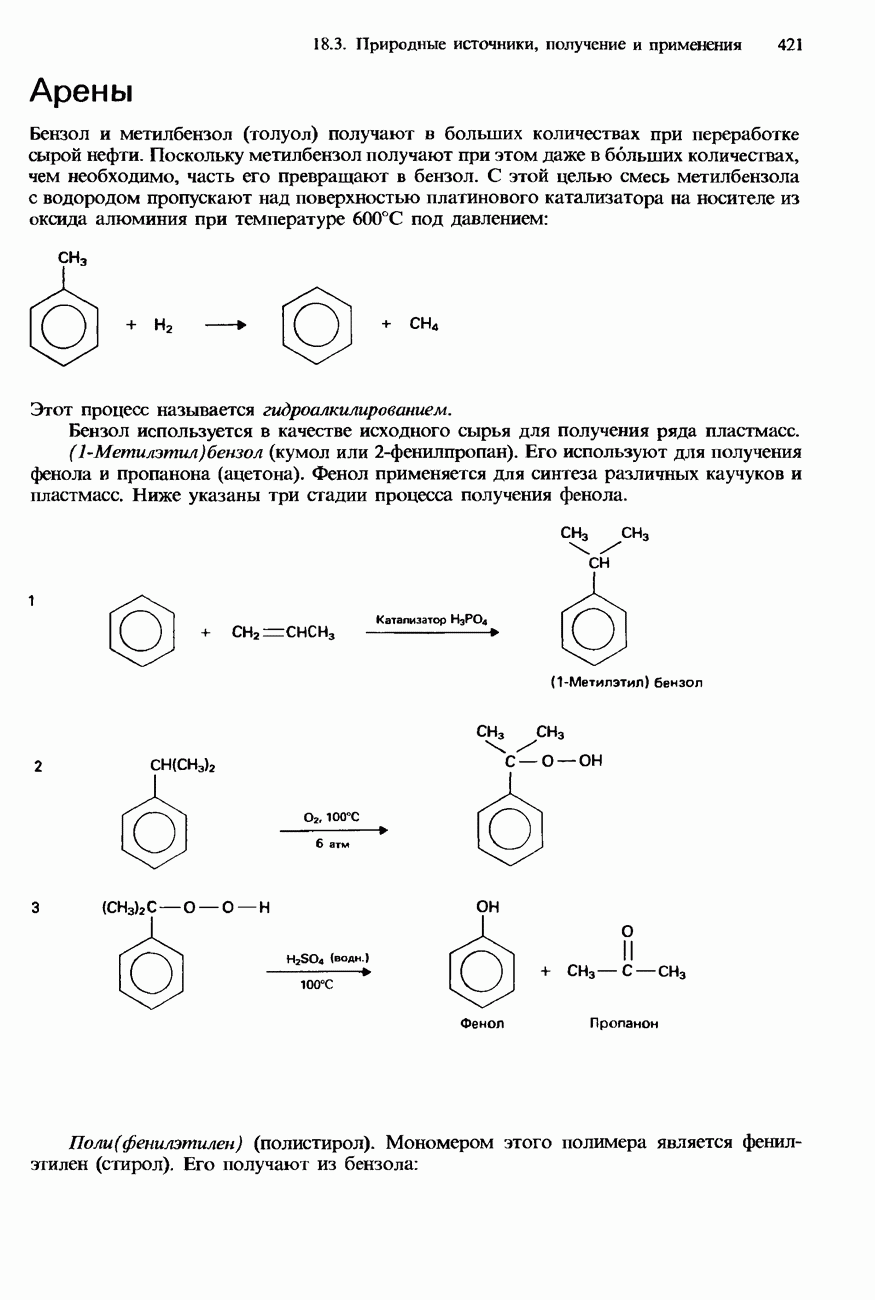
- 18.2. Арены
- БЕНЗОЛ
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
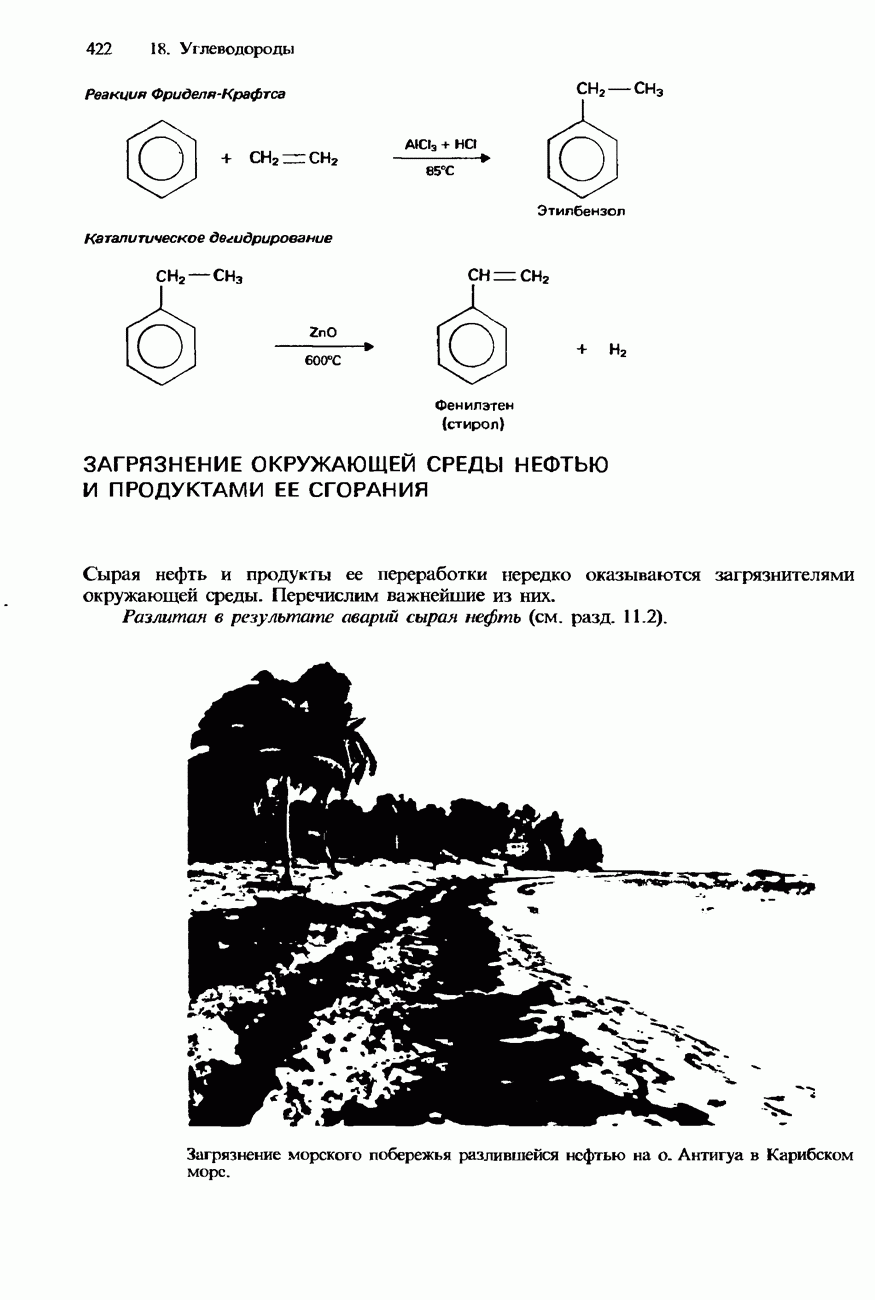
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
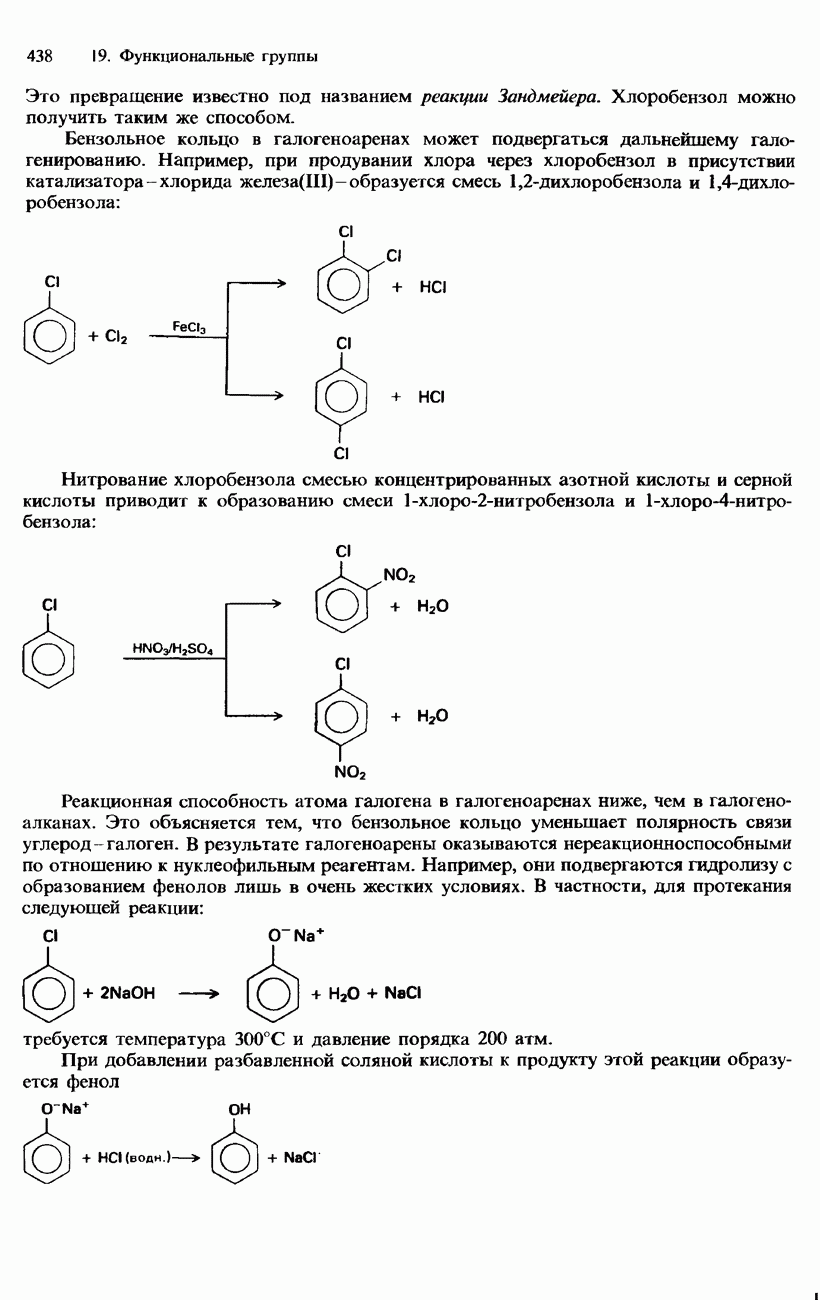
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
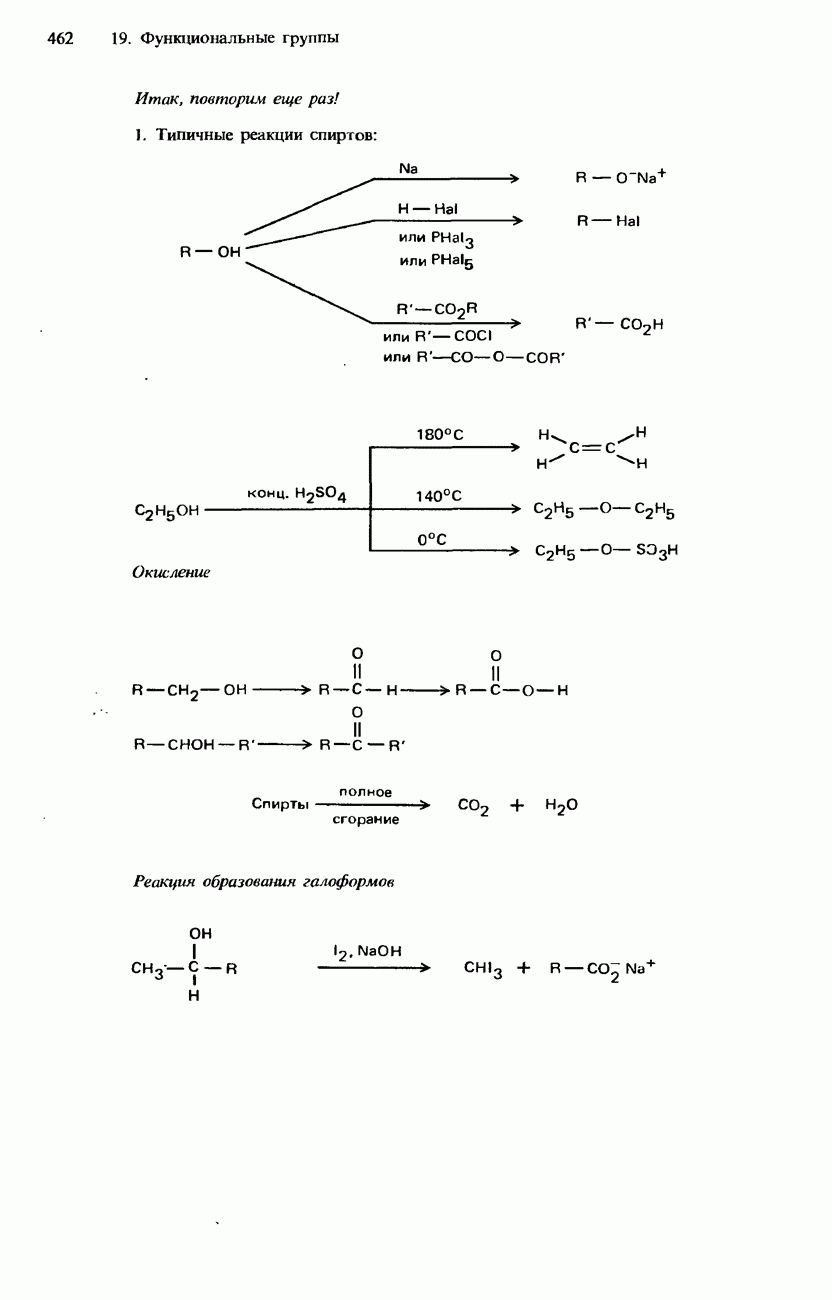
- 19.2. Спирты, фенолы и эфиры
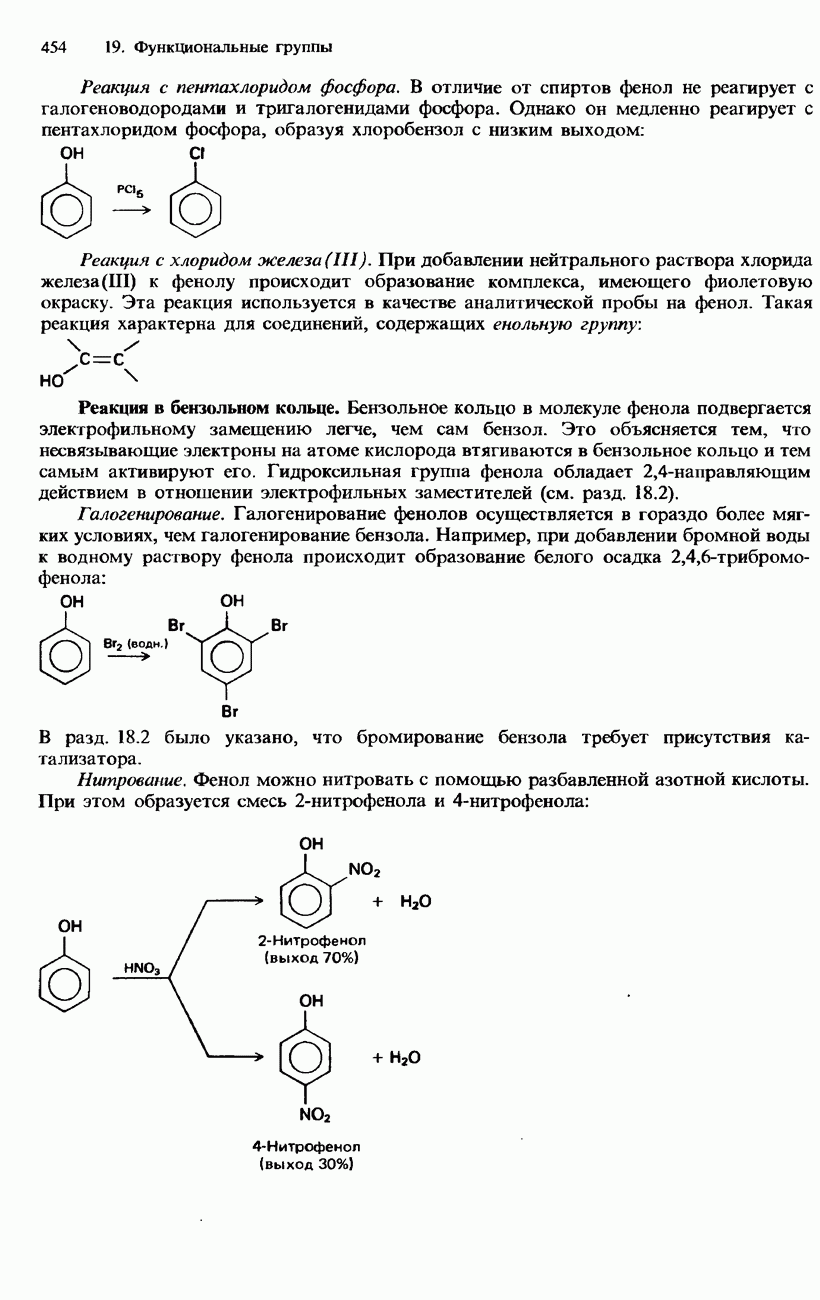
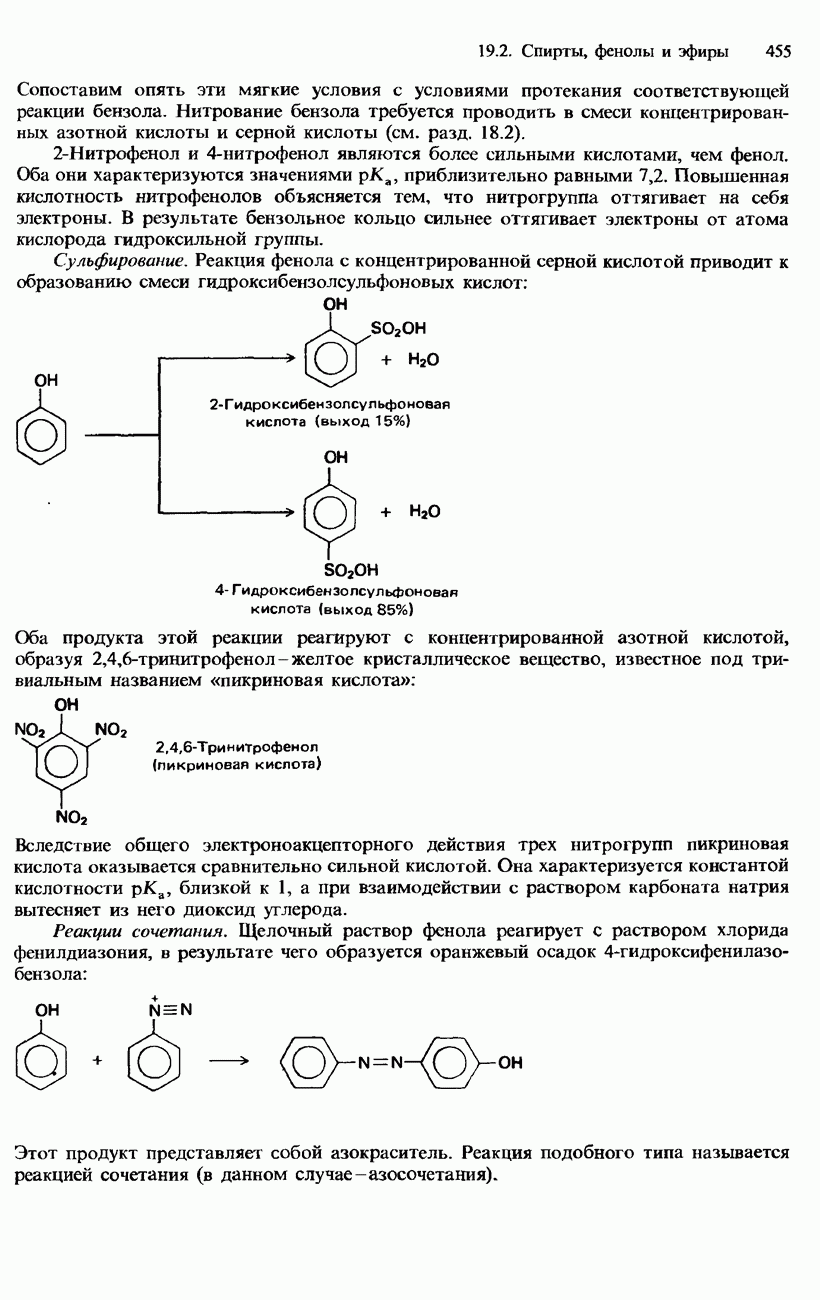
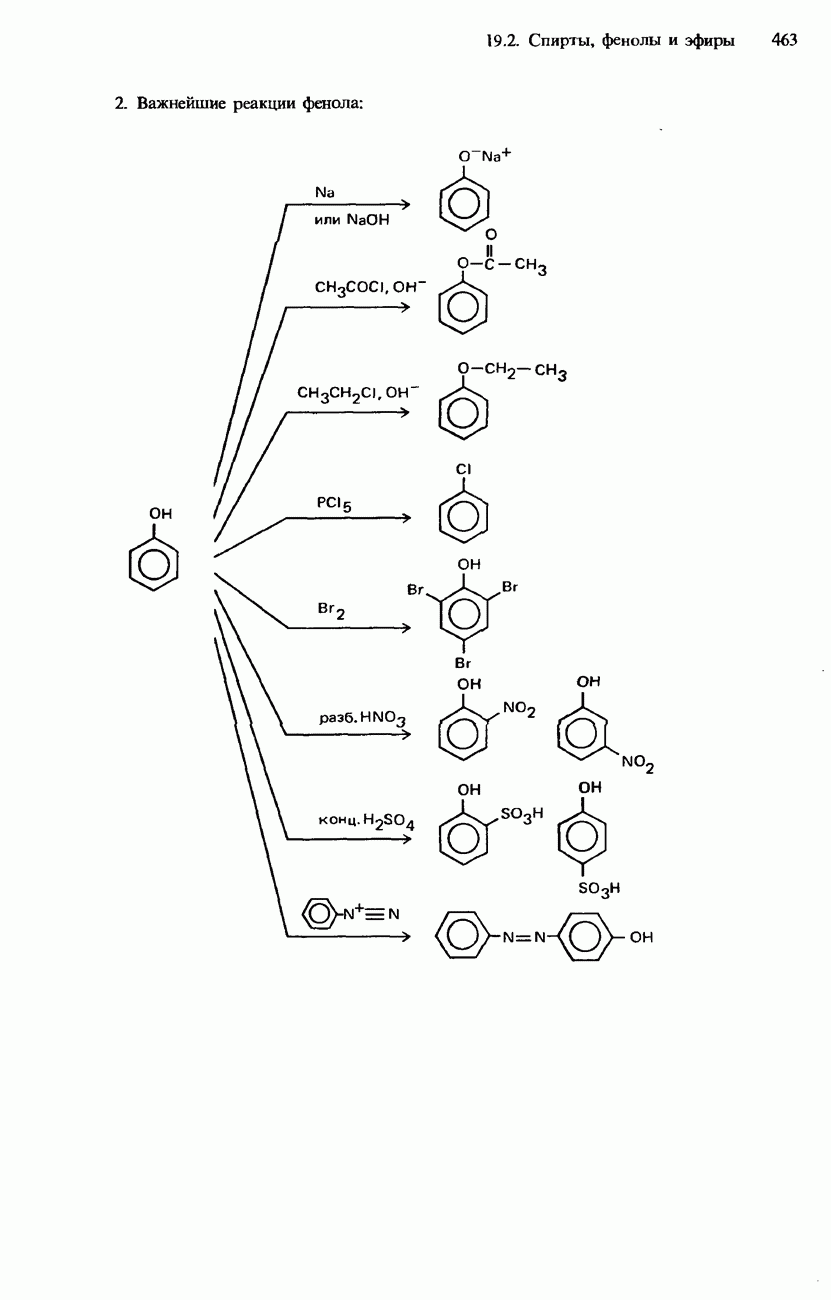
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- КАРБОНОВЫЕ КИСЛОТЫ
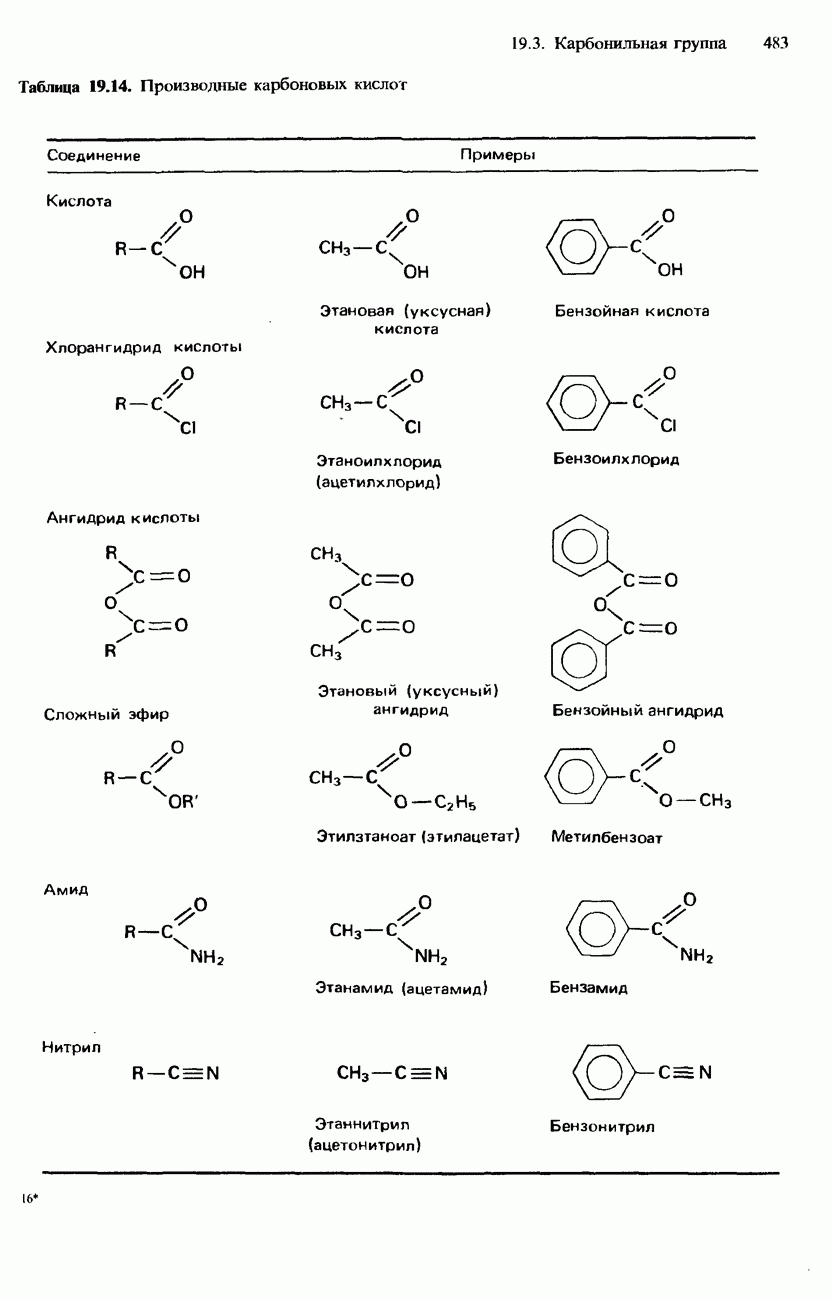
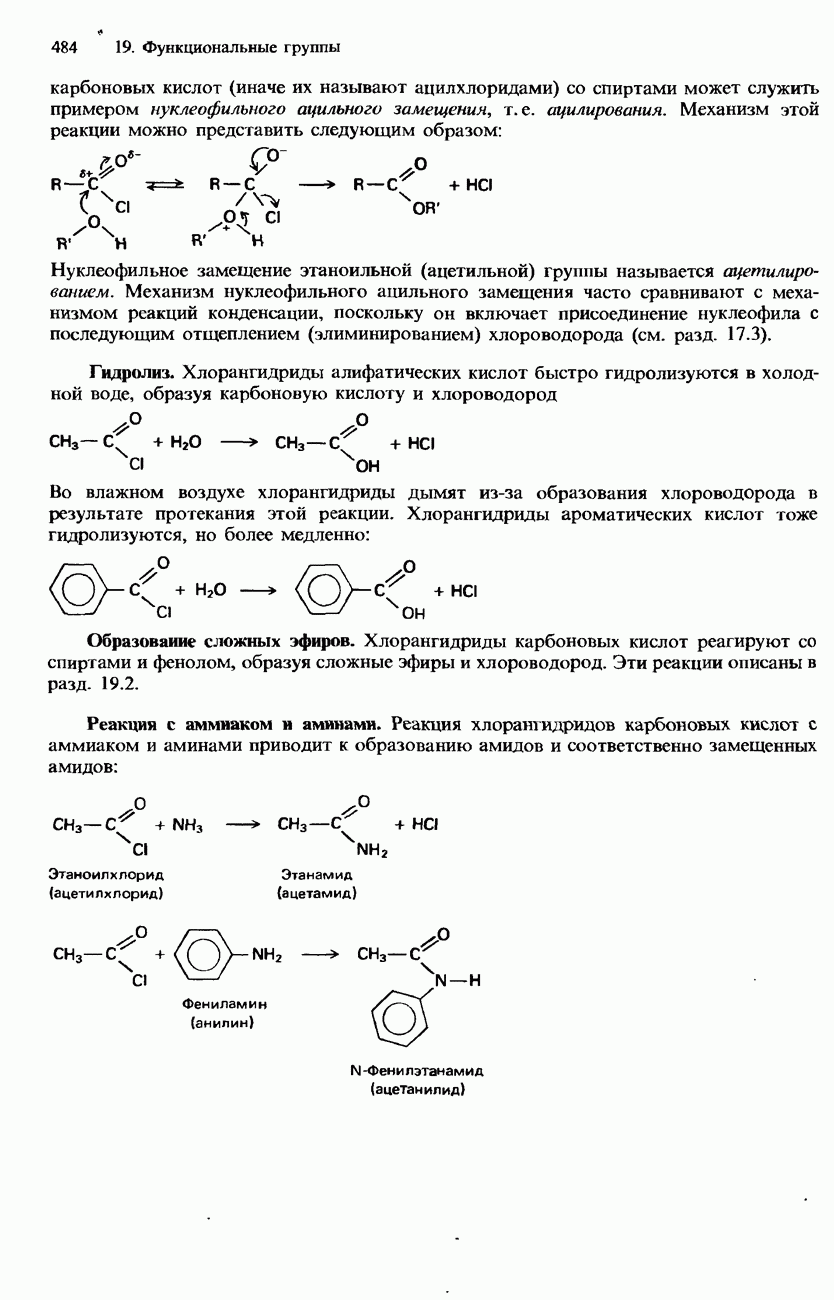
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
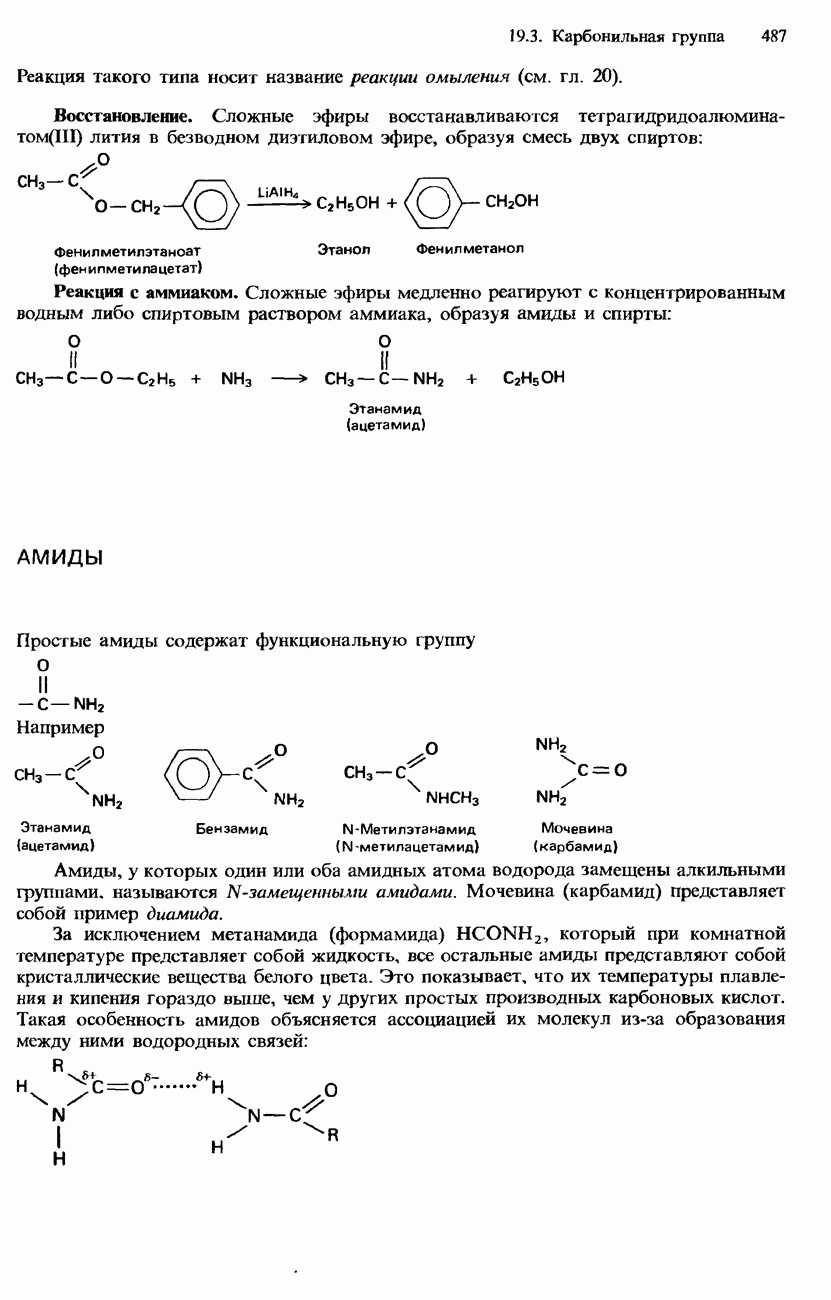
- АМИДЫ
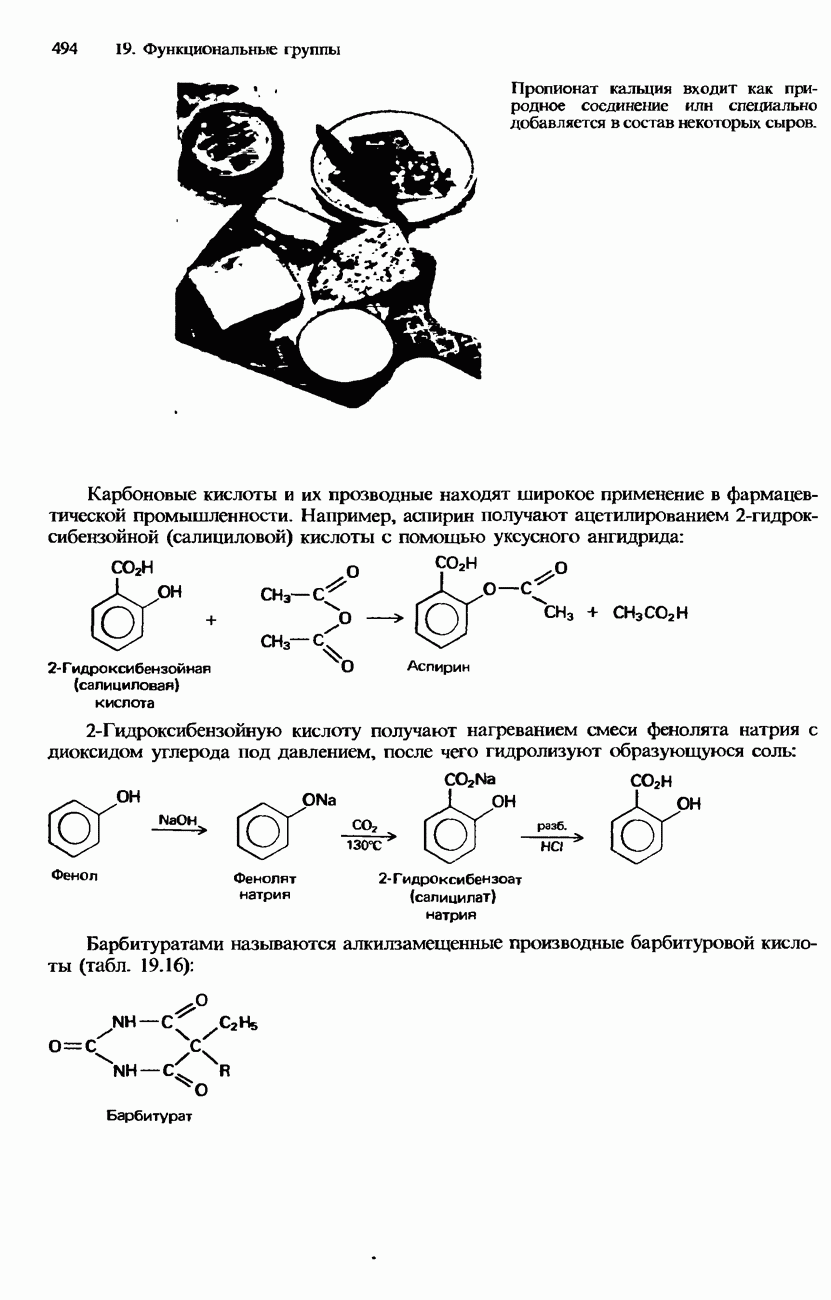
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
- 19.4 Амины и родственные соединения
- СОЛИ ДИАЗОНИЯ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
- 20.2. Углеводы и нуклеиновые кислоты
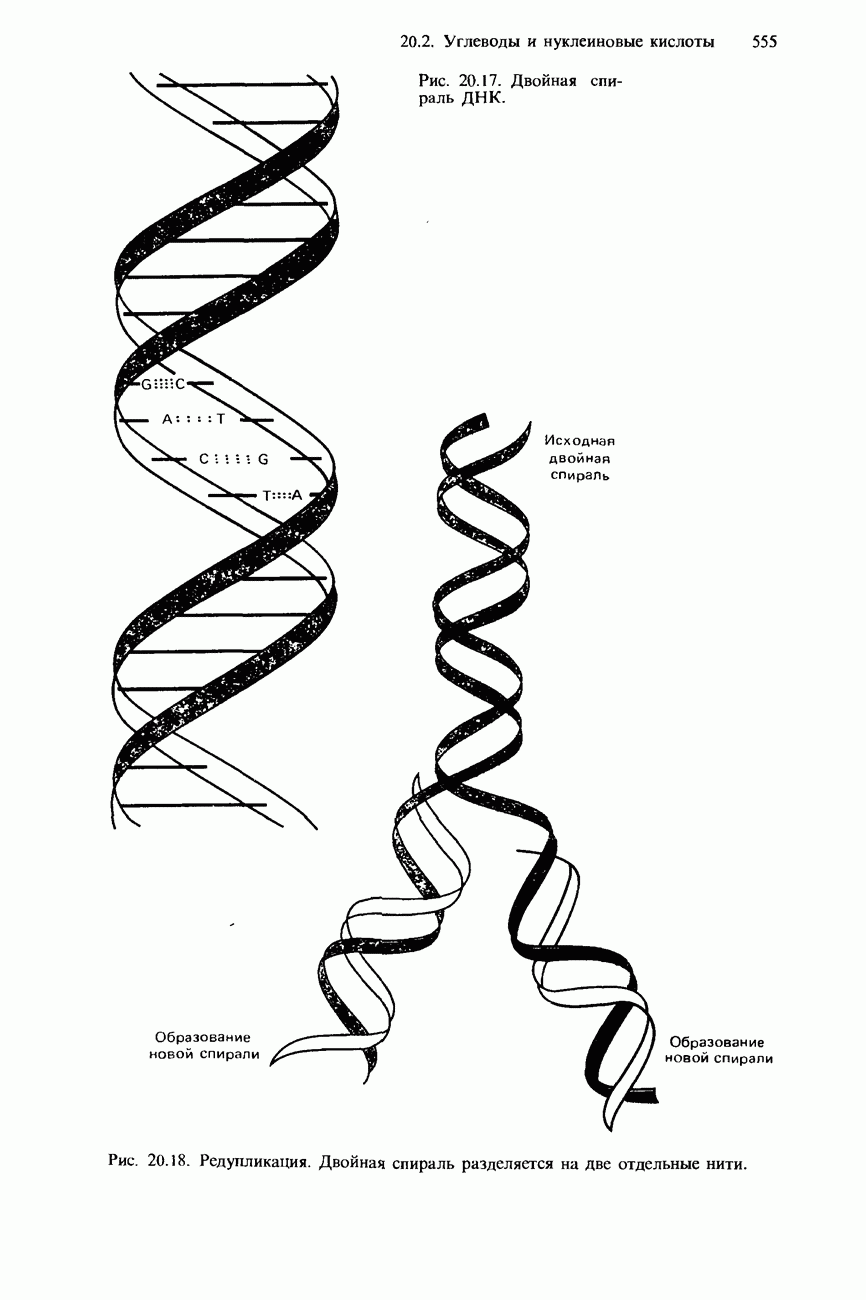
- НУКЛЕИНОВЫЕ КИСЛОТЫ
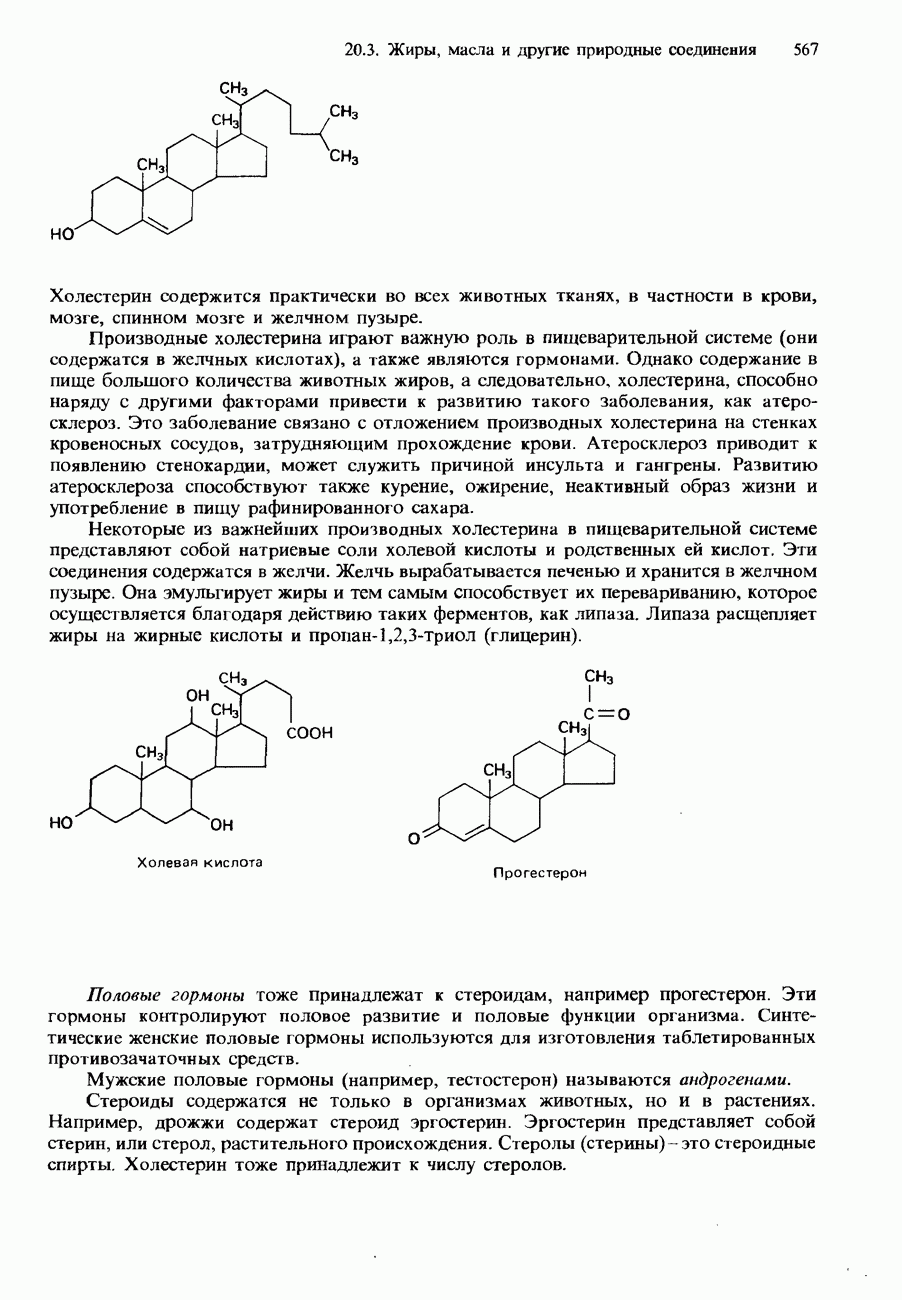
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
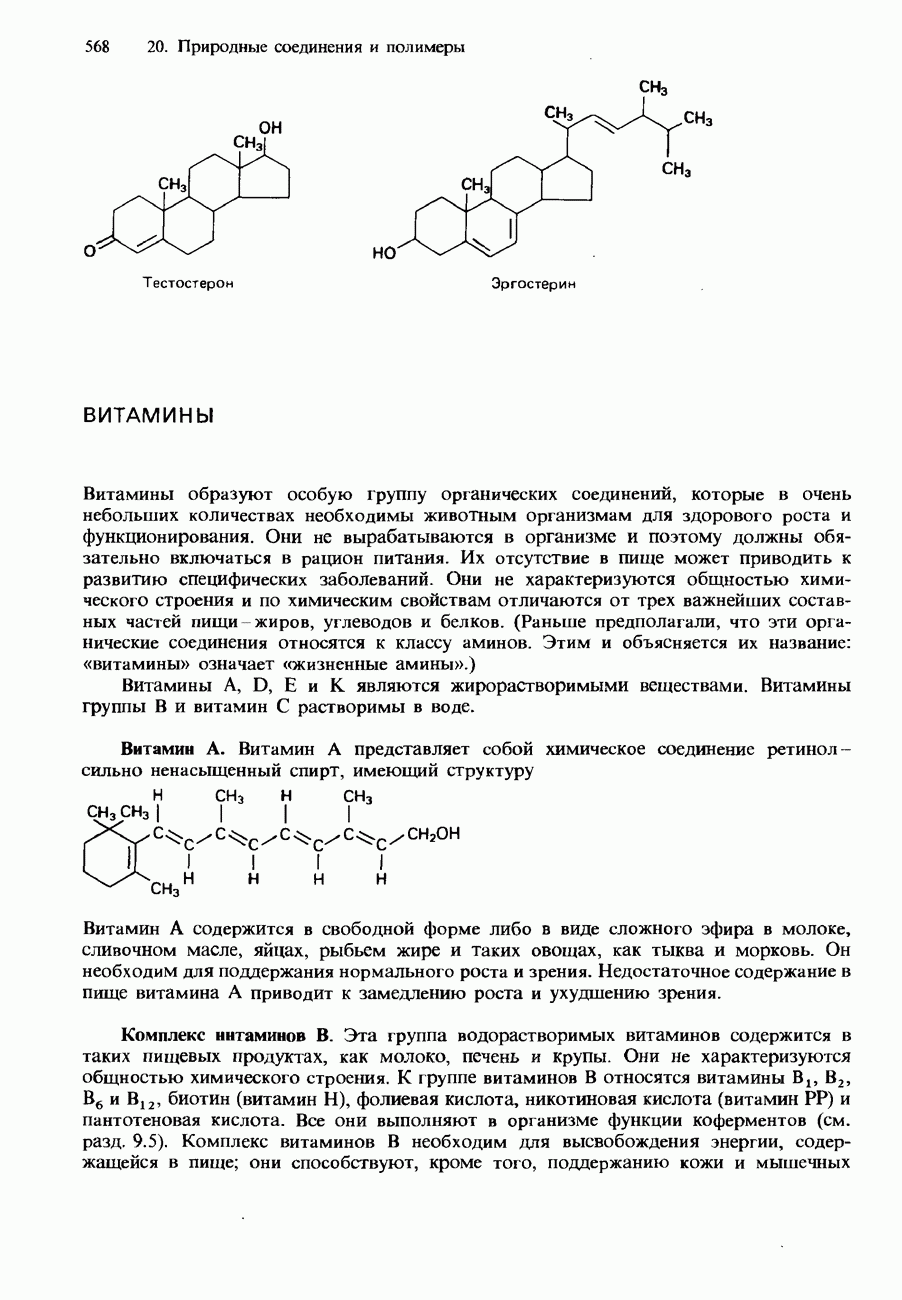
- ВИТАМИНЫ
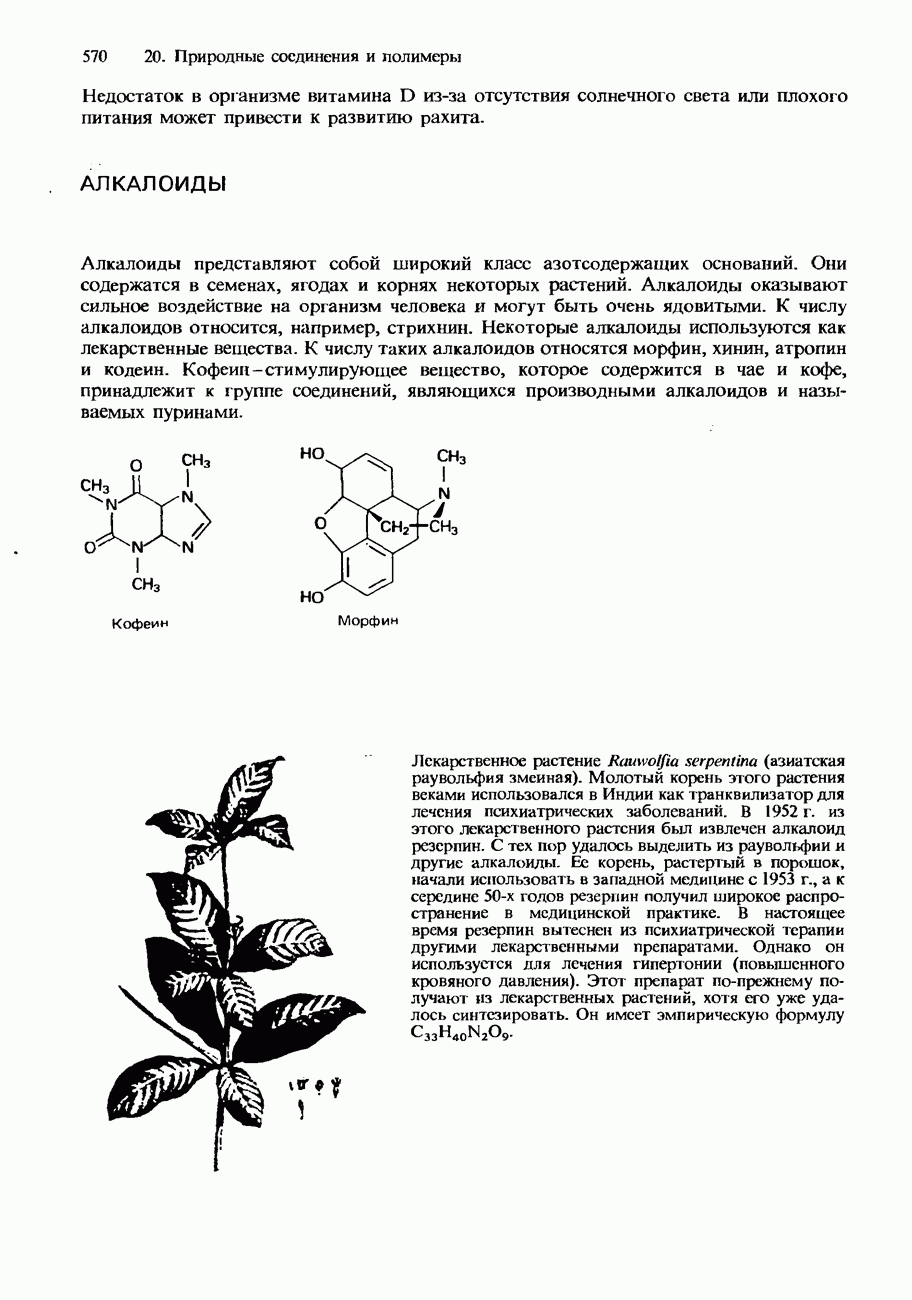
- АЛКАЛОИДЫ
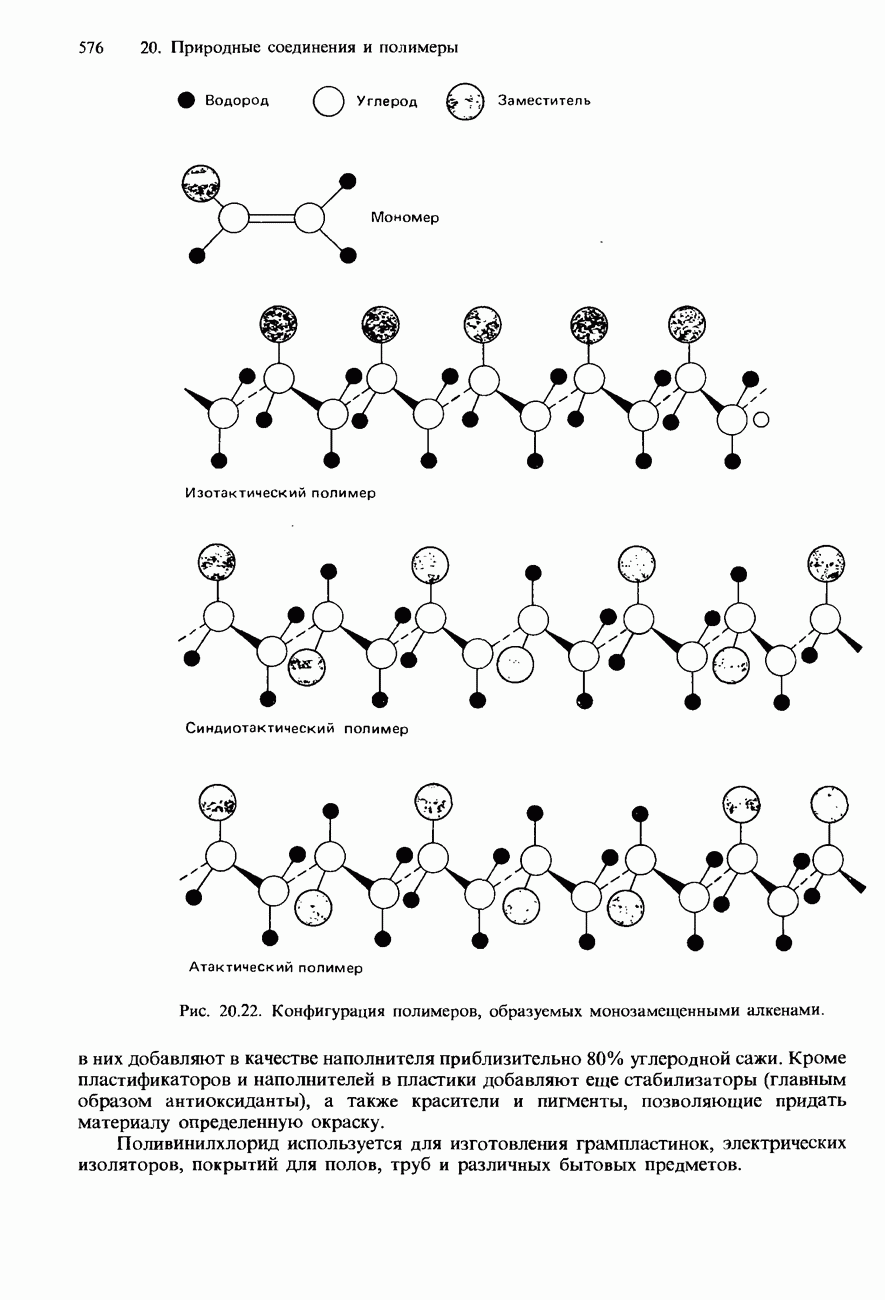
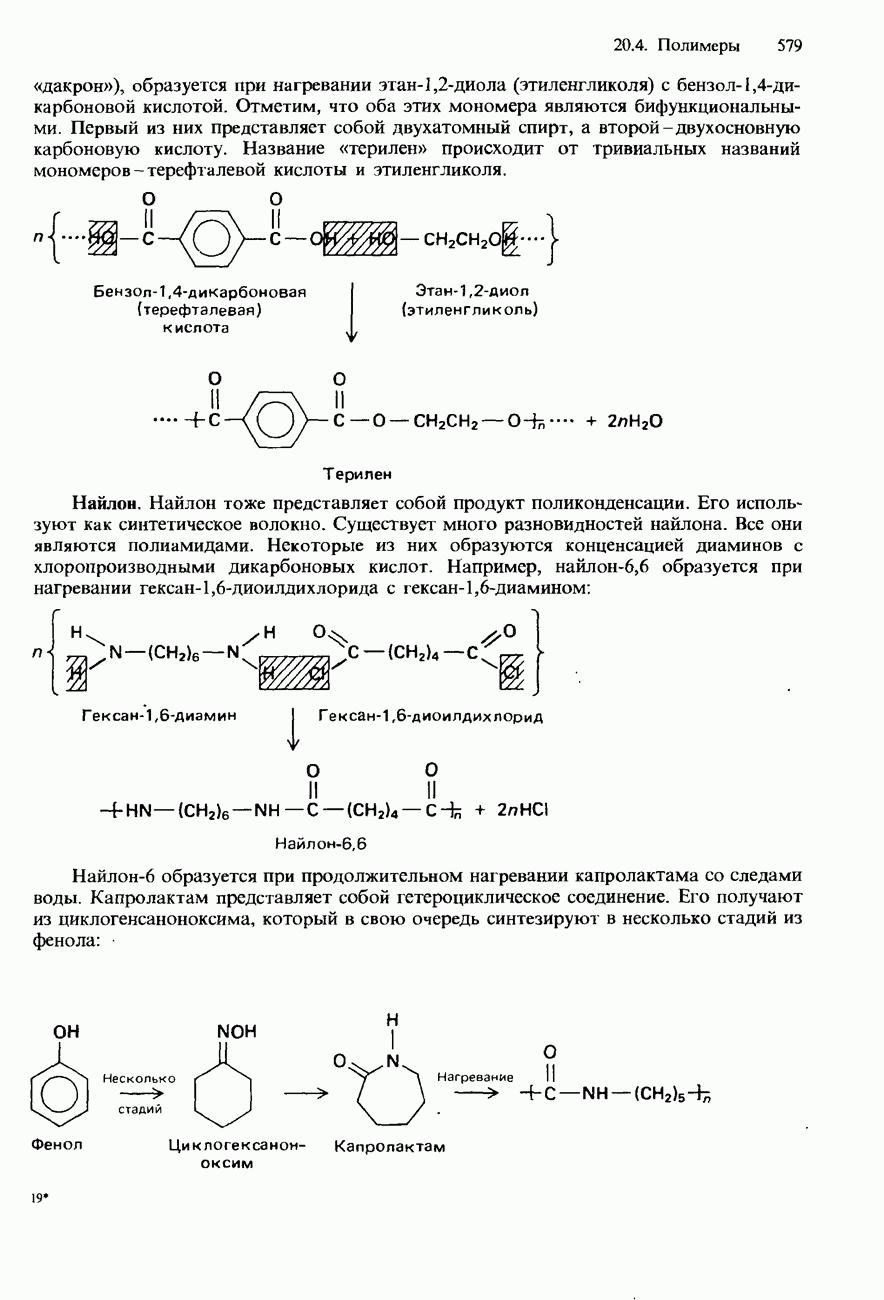
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
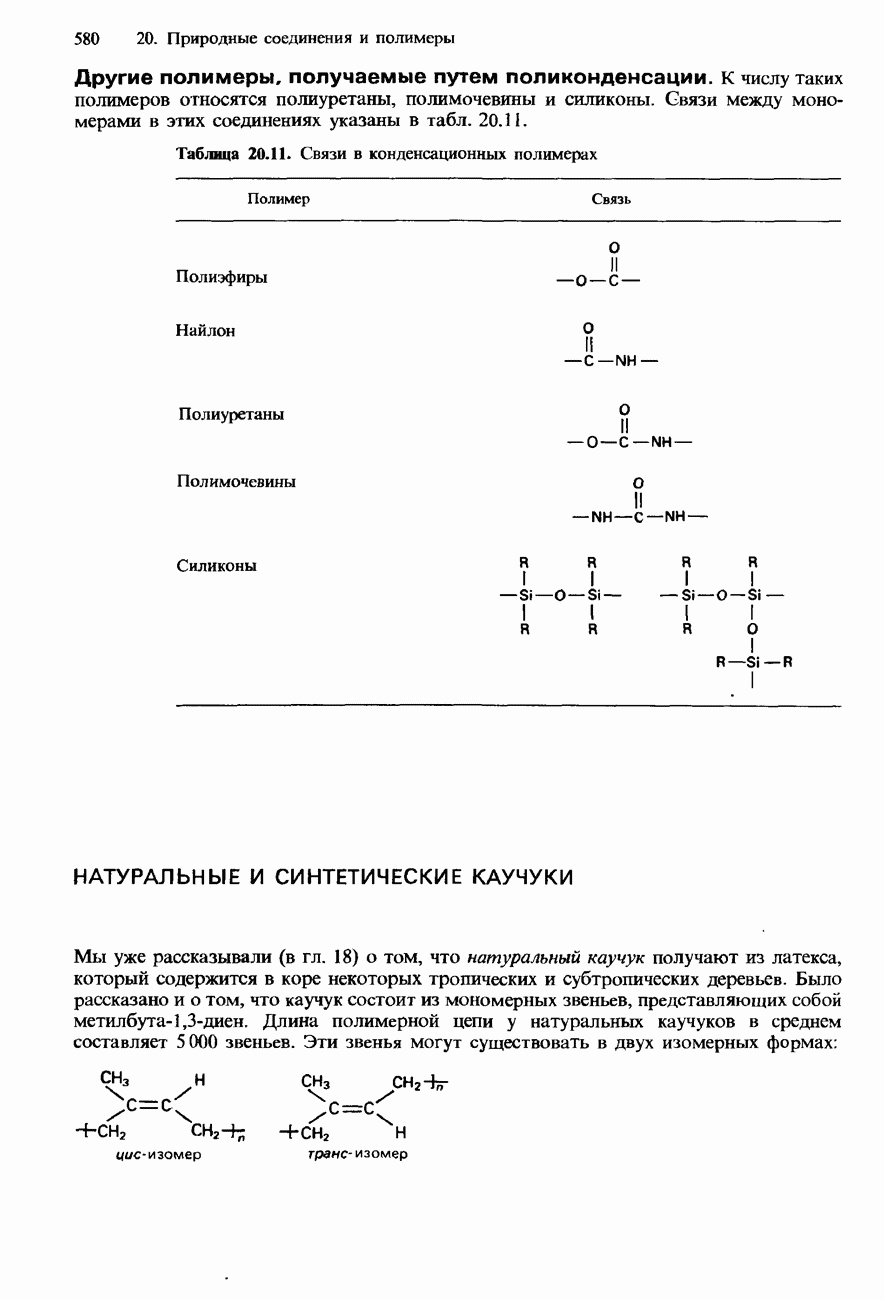
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ