| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
СЕРА
При нормальных условиях сера представляет собой твердое вещество желтого цвета, нерастворимое в воде. В такой форме она нетоксична.
Сера имеет несколько аллотропов, важнейшими из которых являются  -сера и
-сера и  -сера (см. также разд. 3.2 и рис. 6.8). а-Сера (ромбическая сера) устойчива при
-сера (см. также разд. 3.2 и рис. 6.8). а-Сера (ромбическая сера) устойчива при
температурах ниже 95,5°С.  -Сера (моноклинная сера) устойчива при температурах выше
-Сера (моноклинная сера) устойчива при температурах выше  Аллотропия такого типа, как у серы, называется энантиотропией (см. разд. 15.2).
Аллотропия такого типа, как у серы, называется энантиотропией (см. разд. 15.2).
Кристаллы  -серы имеют лимонно-желтую окраску, а игольчатые кристаллы
-серы имеют лимонно-желтую окраску, а игольчатые кристаллы  -серы-более темную медово-желтую окраску. Оба аллотропа состоят из гофрированных колец молекулярной серы
-серы-более темную медово-желтую окраску. Оба аллотропа состоят из гофрированных колец молекулярной серы  .
.
Существует еще много других форм серы. Черенковая сера состоит главным образом из  -серы. Серный цвет представляет собой форму аморфной серы и получается при оседании паров серы на холодную поверхность. Коллоидную серу можно получить, добавляя концентрированную соляную кислоту к раствору тиосульфата натрия, в результате чего протекает реакция
-серы. Серный цвет представляет собой форму аморфной серы и получается при оседании паров серы на холодную поверхность. Коллоидную серу можно получить, добавляя концентрированную соляную кислоту к раствору тиосульфата натрия, в результате чего протекает реакция

При плавлении кристаллической а- или  -серы образуется желтая жидкость. При дальнейшем нагревании жидкая сера сначала становится красно-коричневой, а затем сильно темнеет. Повышение температуры приблизительно до
-серы образуется желтая жидкость. При дальнейшем нагревании жидкая сера сначала становится красно-коричневой, а затем сильно темнеет. Повышение температуры приблизительно до  приводит к повышению вязкости (густоты) жидкой серы. При дальнейшем повышении температуры вплоть до точки кипения серы при
приводит к повышению вязкости (густоты) жидкой серы. При дальнейшем повышении температуры вплоть до точки кипения серы при  ее вязкость уменьшается. При выливании кипящей серы в воду образуется пластическая сера. Это мягкое коричневое эластичное вещество, состоящее из беспорядочно ориентированных цепочек атомов серы. Пластическая сера неустойчива. Постепенно цепочки атомов разрываются, и они перестраиваются, образуя молекулы
ее вязкость уменьшается. При выливании кипящей серы в воду образуется пластическая сера. Это мягкое коричневое эластичное вещество, состоящее из беспорядочно ориентированных цепочек атомов серы. Пластическая сера неустойчива. Постепенно цепочки атомов разрываются, и они перестраиваются, образуя молекулы  ромбической серы.
ромбической серы.
Сера реагирует с большинством металлов, образуя сульфиды. Некоторые из них представляют собой нестехиометрические соединения (см. разд. 4.1). Сера соединяется также с некоторыми неметаллами, например с хлором и кислородом:

Диоксид серы образуется также при действии концентрированной серной кислоты на серу:

Распространенность в природе, получение и применения серы
Сера встречается в природных условиях в виде залежей почти чистой самородной серы, крупнейшие из которых находятся в Италии, Мексике, Японии, Польше и США. Кроме того, сера входит в состав различных сульфидных руд: железного колчедана  цинковой обманки
цинковой обманки  и галенита
и галенита  а также сульфатных руд - гипса
а также сульфатных руд - гипса  и барита
и барита  Соединения серы содержатся также в горючих ископаемых, например в
Соединения серы содержатся также в горючих ископаемых, например в
нефти. Природный газ содержит примесь сероводорода. Морская вода содержит сульфат-ионы. Сера входит в состав биологических тканей всех растений и животных в форме аминокислот цистеина, цистина и метионина.
Действие соединений серы на органы чувстн. Специфические запахи чеснока, горчицы, лука и капусты вызываются органическими соединениями серы. Например, источником запаха чеснока является соединение аллицин, которое имеет следующую структуру:

Слезоточивое, вещество, выделяющееся при нарезании лука, тоже является соединением серы. Оно называется лакриматорный фактор. Это соединение существует в двух формах, в виде син-формы и дюйм-формы, из которых вторая преобладает:

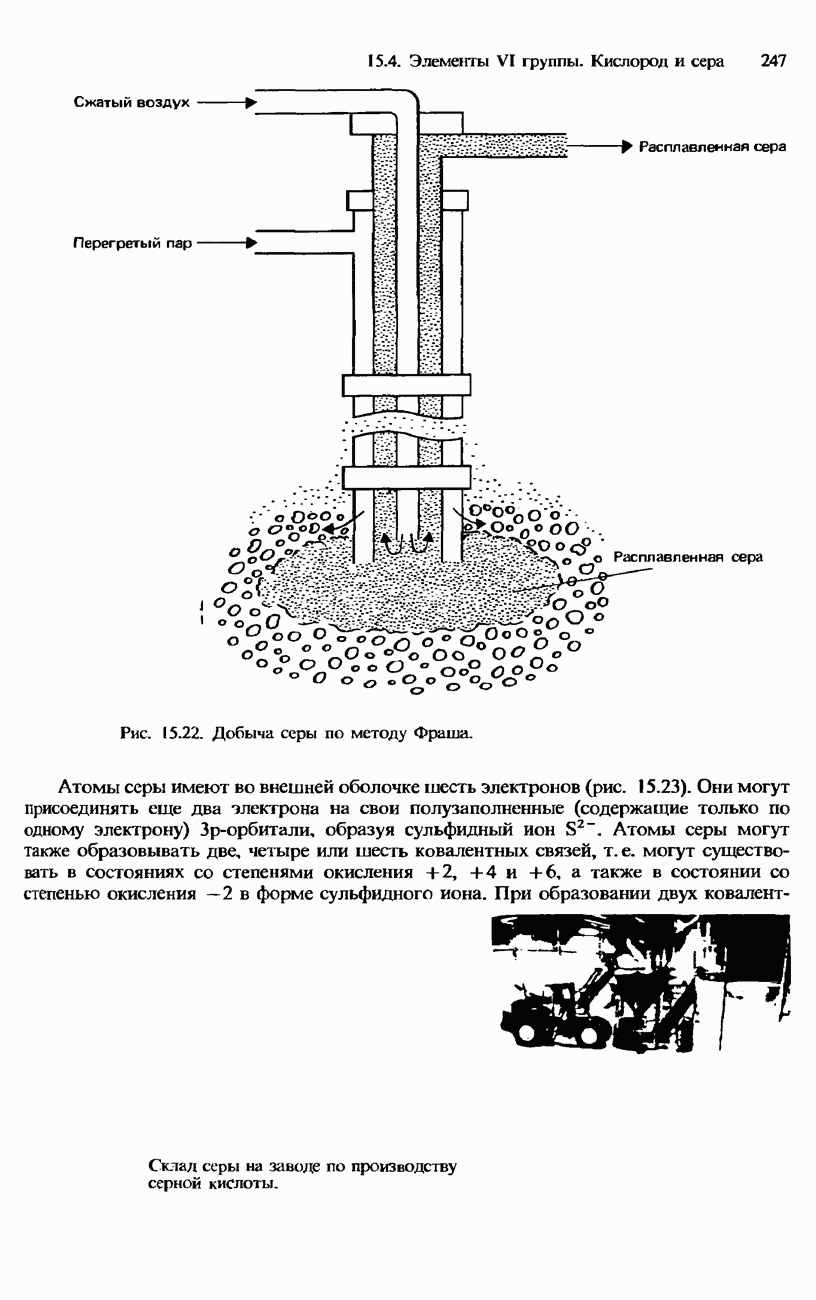
Процесс Фраша. Серу извлекают из подземных залежей с помощью процесса Фраша (рис. 15.22). Для этого под землю по трубам нагнетают горячий сжатый воздух и перегретый пар. Расплавленная сера вместе с водой под давлением выносится на поверхность, где она остывает и отверждается. Полученная таким способом сера имеет чистоту 99,5% и пригодна для непосредственного использования. Добыча серы по методу Фраша осуществляется в США, Ираке и Мексике. Однако в последние годы сокращение ее запасов, а также повышение цен на энергию привели к резкому свертыванию добычи серы таким способом.
Одно время серу добывали, опуская рабочих в клетях в жерла спящих вулканов, где они соскабливали серу с внутренних стенок вулканов.
Элементную серу получают также из сульфидов, которые извлекают из нефти и природного газа. Таким способом в западных странах получают приблизительно 75% всей элементной серы. Главными производителями серы, получаемой из природного газа, являются Канада, Франция, ФРГ, Мексика, Саудовская Аравия и США. В социалистических странах серу получают расплавлением подземных залежей и обычными горнодобывающими методами; кроме того, ее получают также из природного газа и нефти. Польша, главный экспортер серы, эксплуатирует самую большую в мире серную шахту. Другими источниками серы в социалистических странах являются колчедановые и иные сульфидные руды; этот источник серы имеет особенно важное значение в Китае, СССР и некоторых европейских странах.
Сера имеет множество важных применений, среди которых укажем следующие:
получение диоксида серы, серной кислоты, сероводорода и сероуглерода;
вулканизация резины, получение химических веществ, используемых в производстве синтетических моющих средств;
производство пороха;
изготовление косметических кремов и лекарственных препаратов; производство инсектицидов и фунгицидов.

Рис. 15.22. Добыча серы по методу Фраша.
Атомы серы имеют во внешней оболочке шесть электронов (рис. 15.23). Они могут присоединять еще два электрона на свои полузаполненные (содержащие только по одному электрону) 3р-орбитали, образуя сульфидный ион  . Атомы серы могут также образовывать две, четыре или шесть ковалентных связей, т. е. могут существовать в состояниях со степенями окисления +2, +4 и +6, а также в состоянии со степенью окисления —2 в форме сульфидного иона. При образовании двух ковалентных
. Атомы серы могут также образовывать две, четыре или шесть ковалентных связей, т. е. могут существовать в состояниях со степенями окисления +2, +4 и +6, а также в состоянии со степенью окисления —2 в форме сульфидного иона. При образовании двух ковалентных

Рис. 15.23. Орбитальная схема электронного строения атома серы в различных состояниях окисления.
связей атомы серы обобществляют с другими атомами два своих электрона на полузаполненных 3р-орбиталях. Образование четырех ковалентных связей становится возможным, когда один из спаренных 3р-электронов промотируется на любую из вакантных  -орбиталей. В случае образования шести ковалентных связей один из 3s-электронов промотируется на другую 3d-орбиталь.
-орбиталей. В случае образования шести ковалентных связей один из 3s-электронов промотируется на другую 3d-орбиталь.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
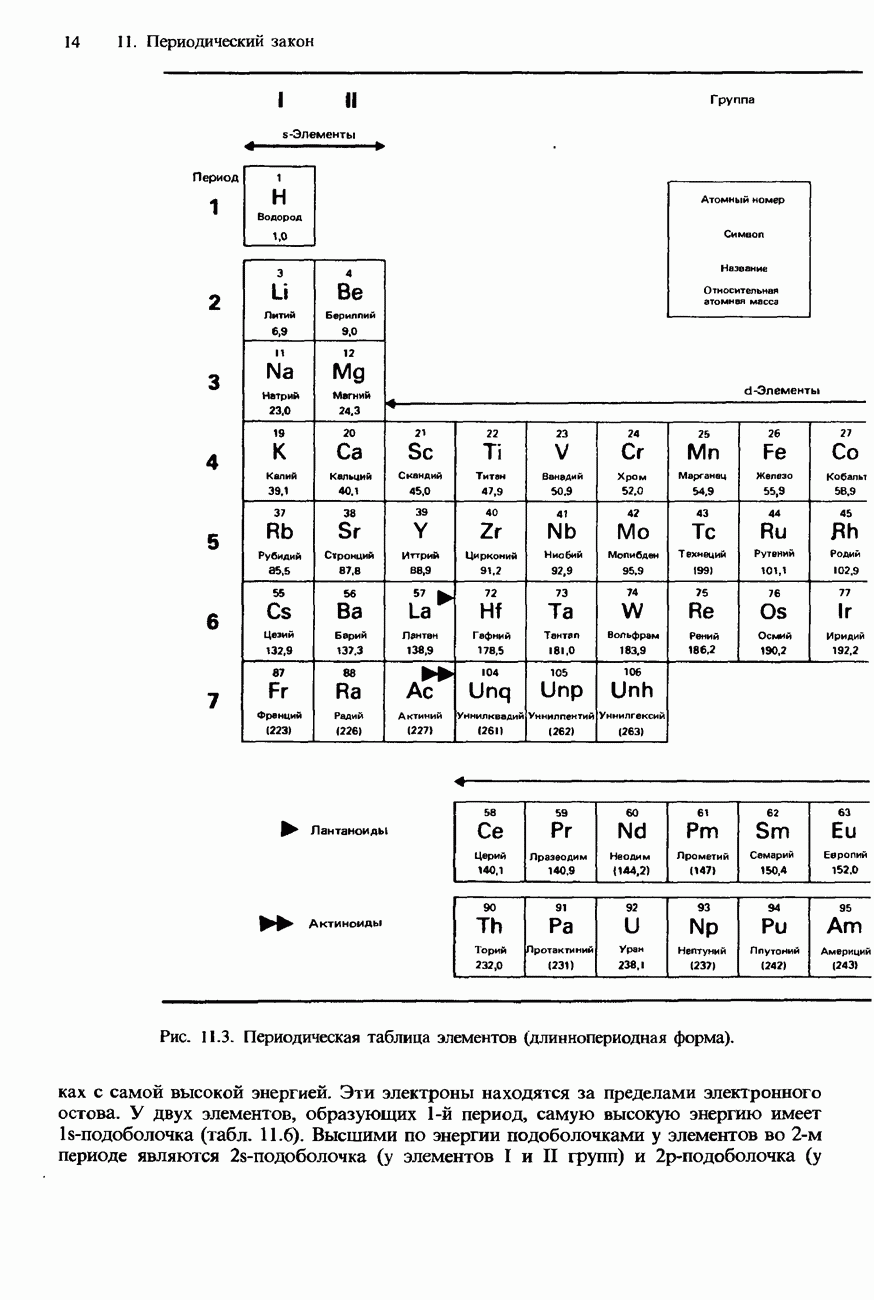
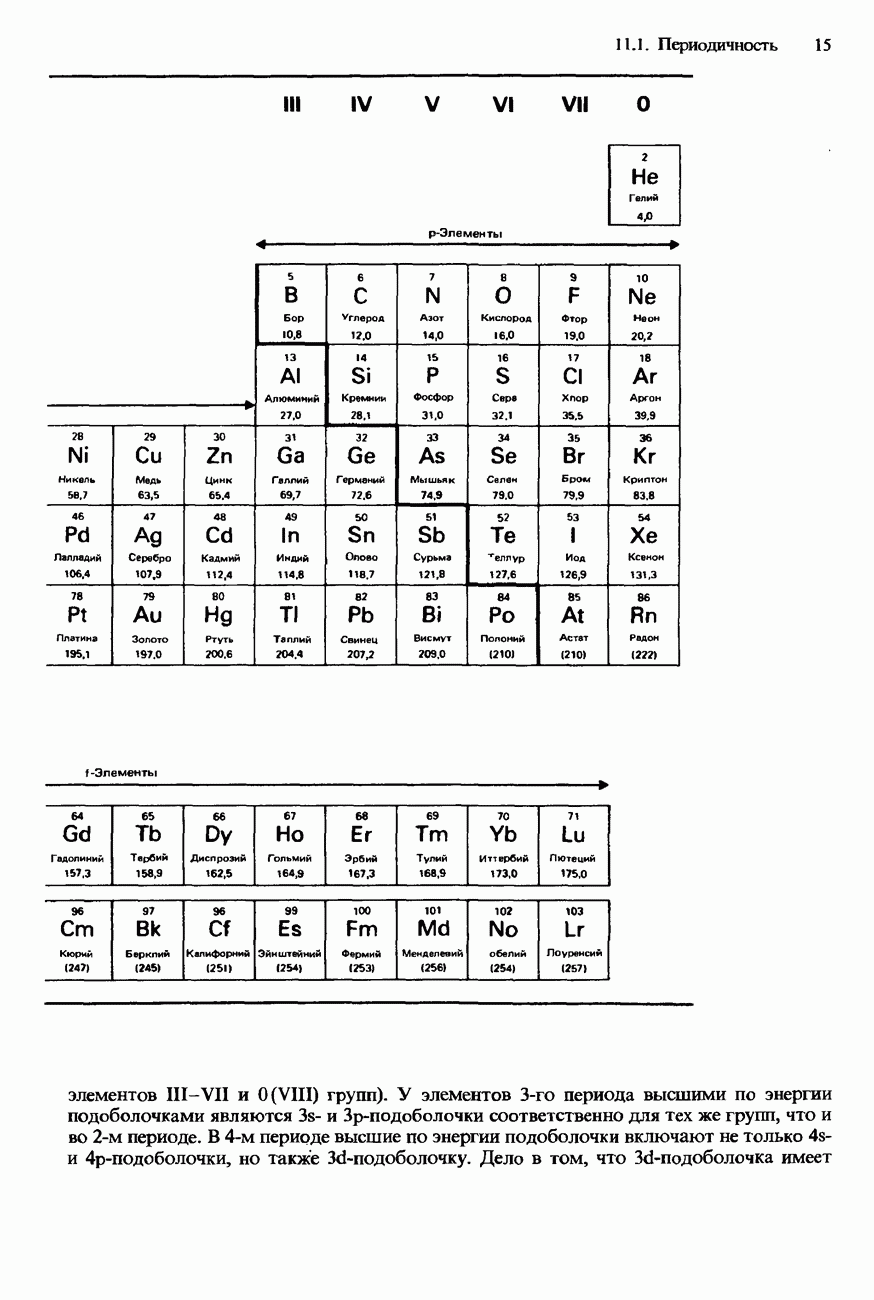
- 11.1 Периодичность
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
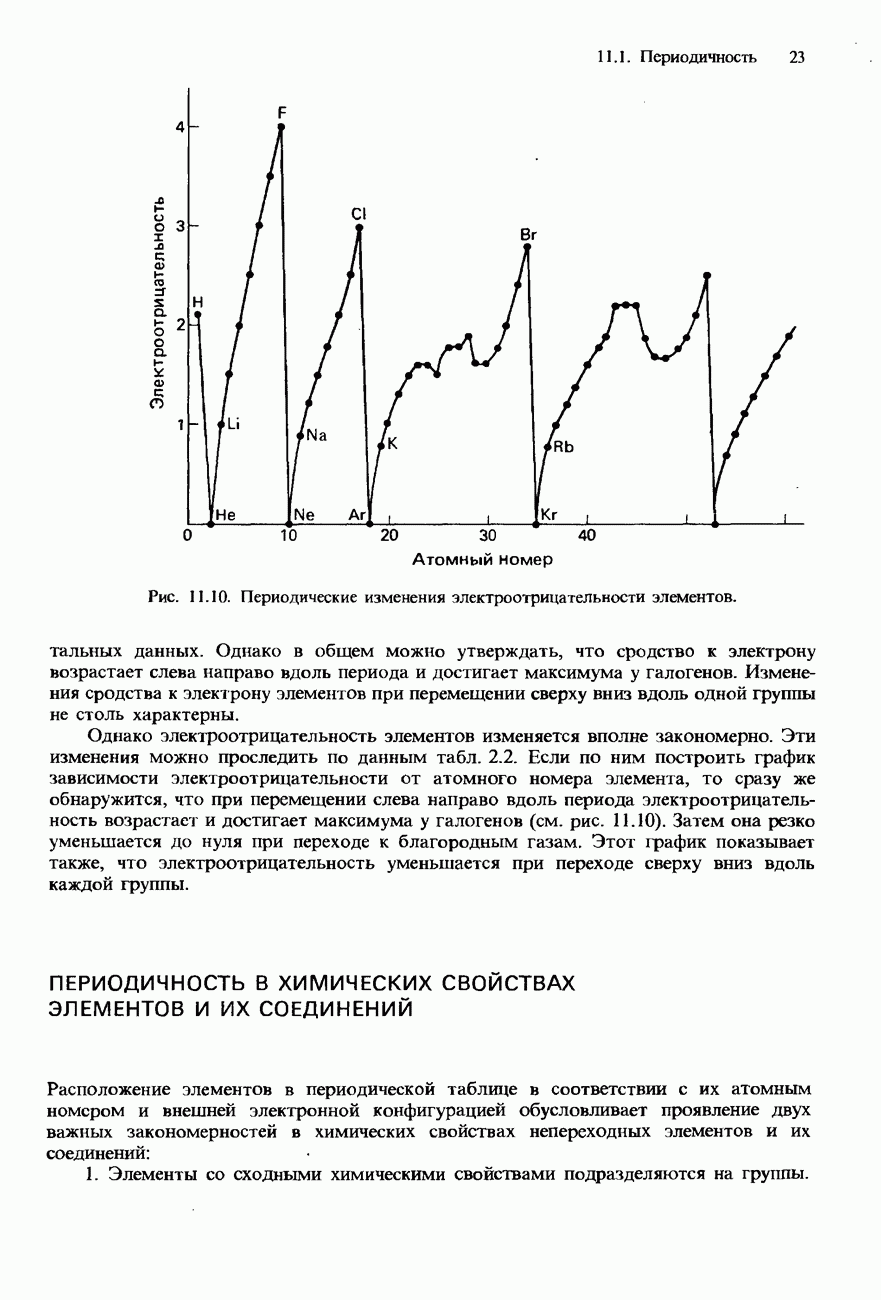
- ПЕРИОДИЧНОСТЬ
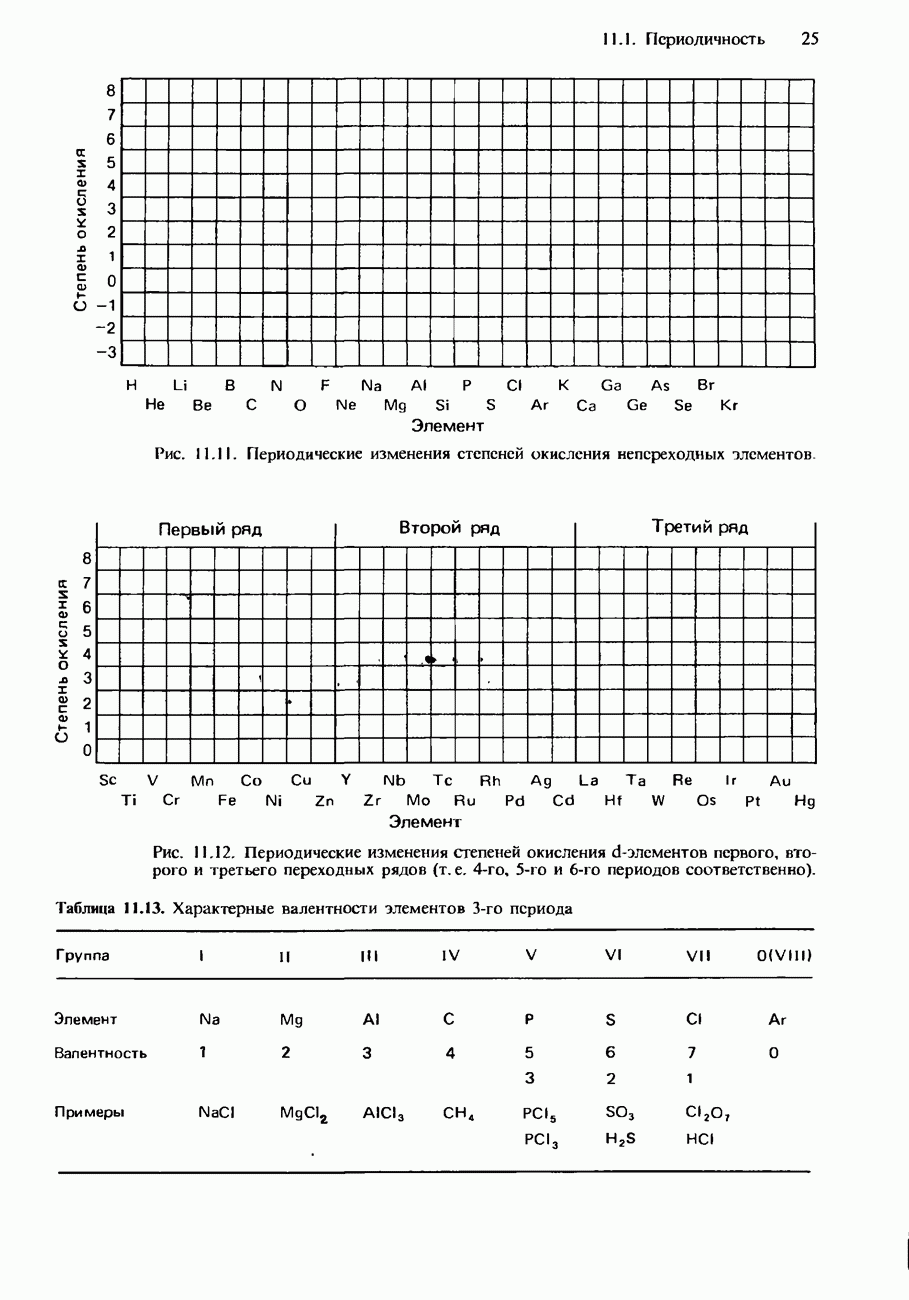
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
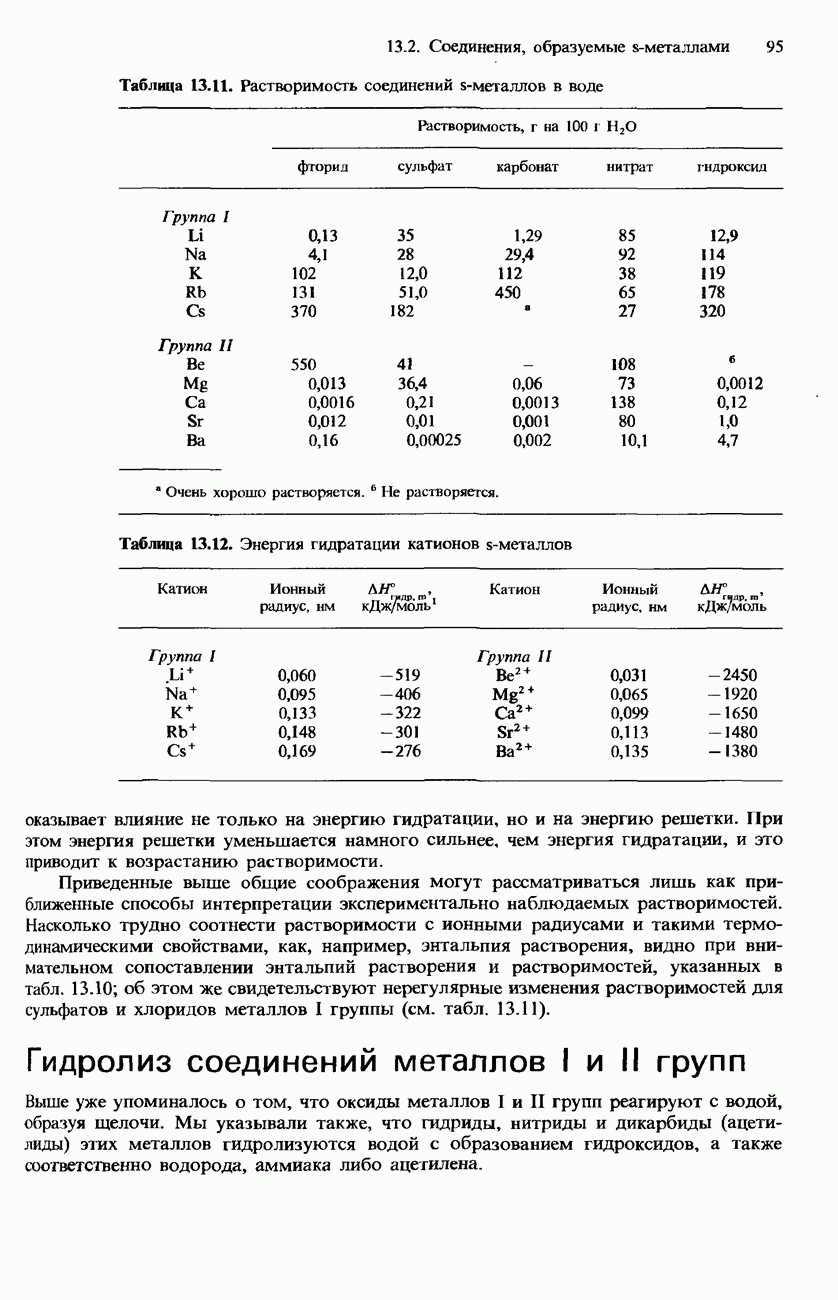
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
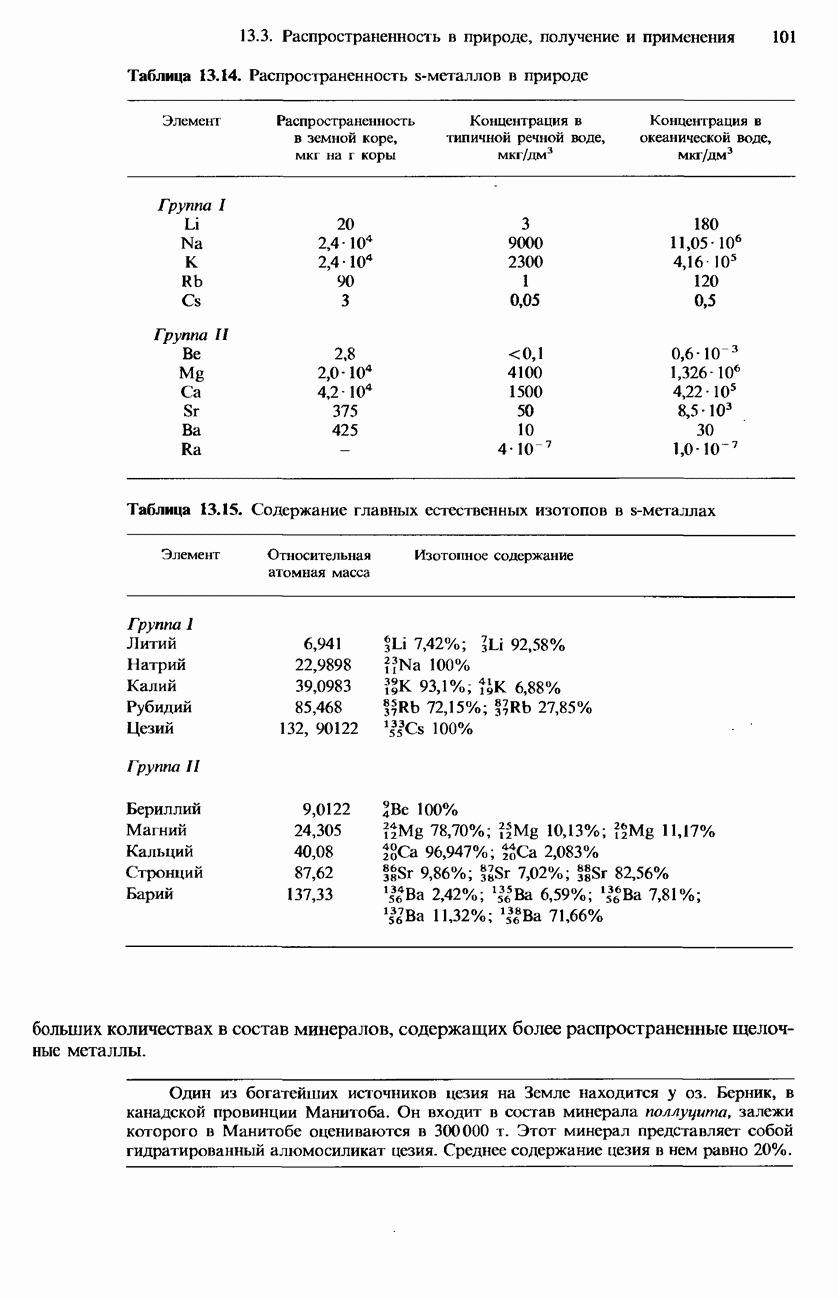
- 13.3. Распространенность в природе, получение и применение
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
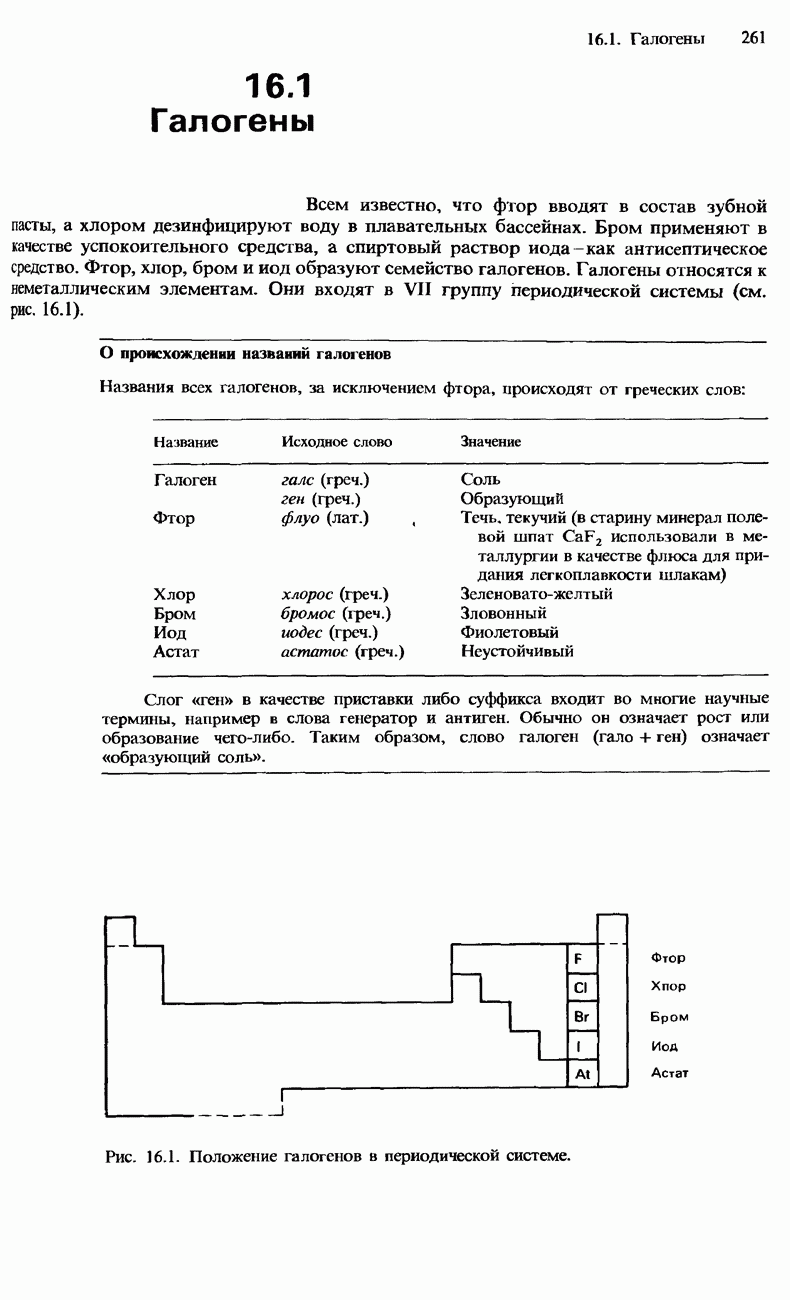
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
- 16.3. Распространенность, получение и применение галогенов и их соединений
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
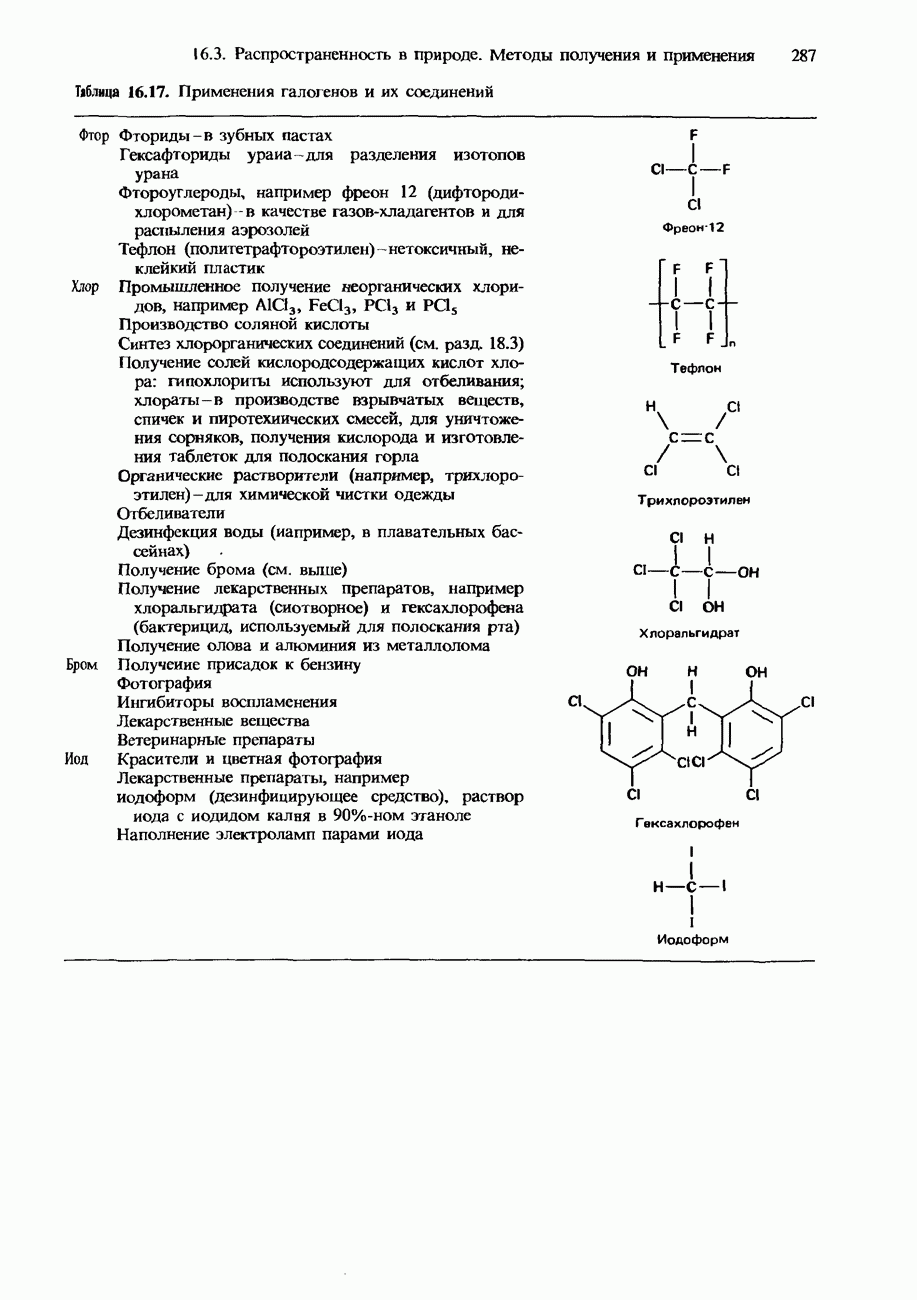
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
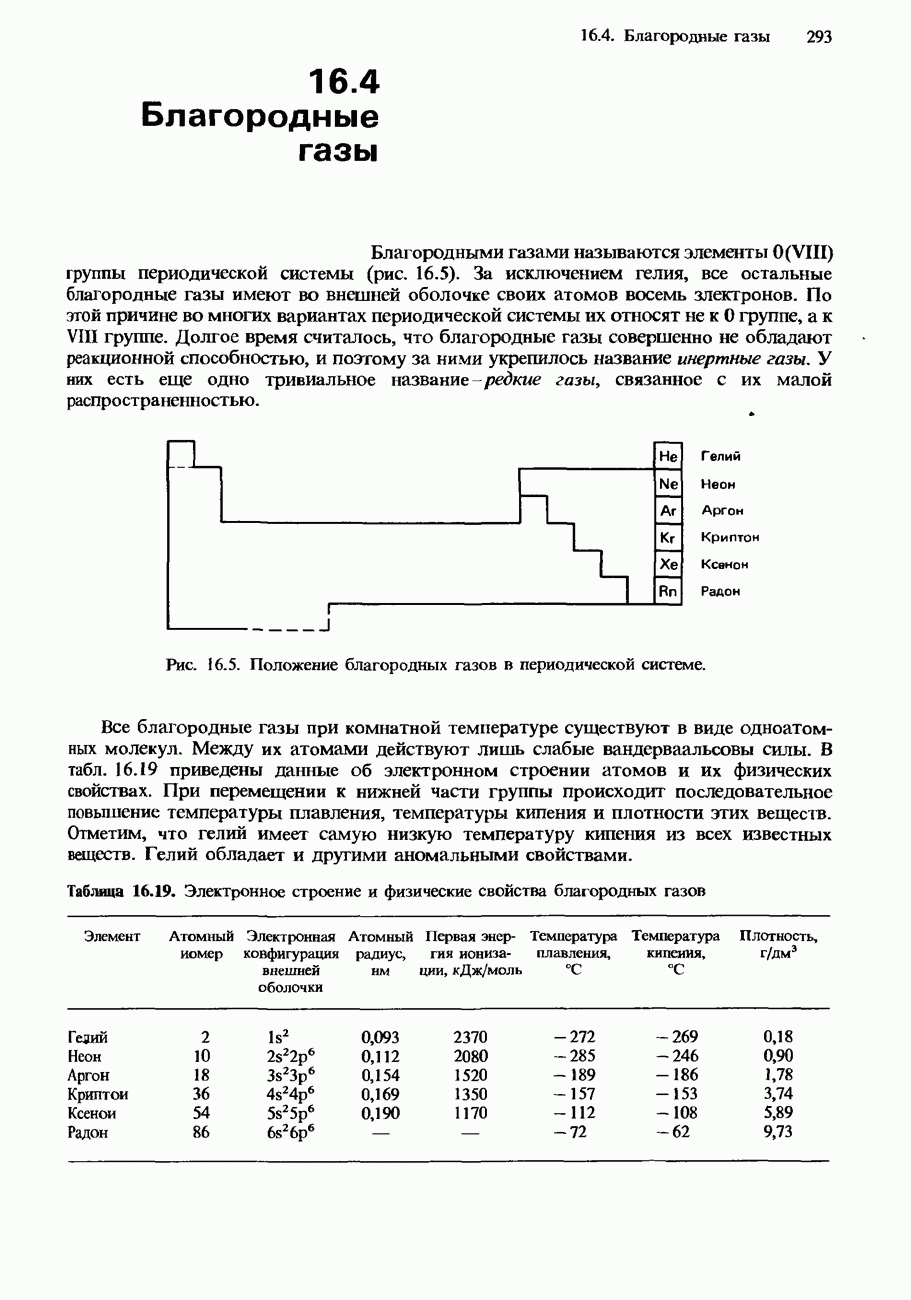
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- УГЛЕВОДОРОДЫ
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
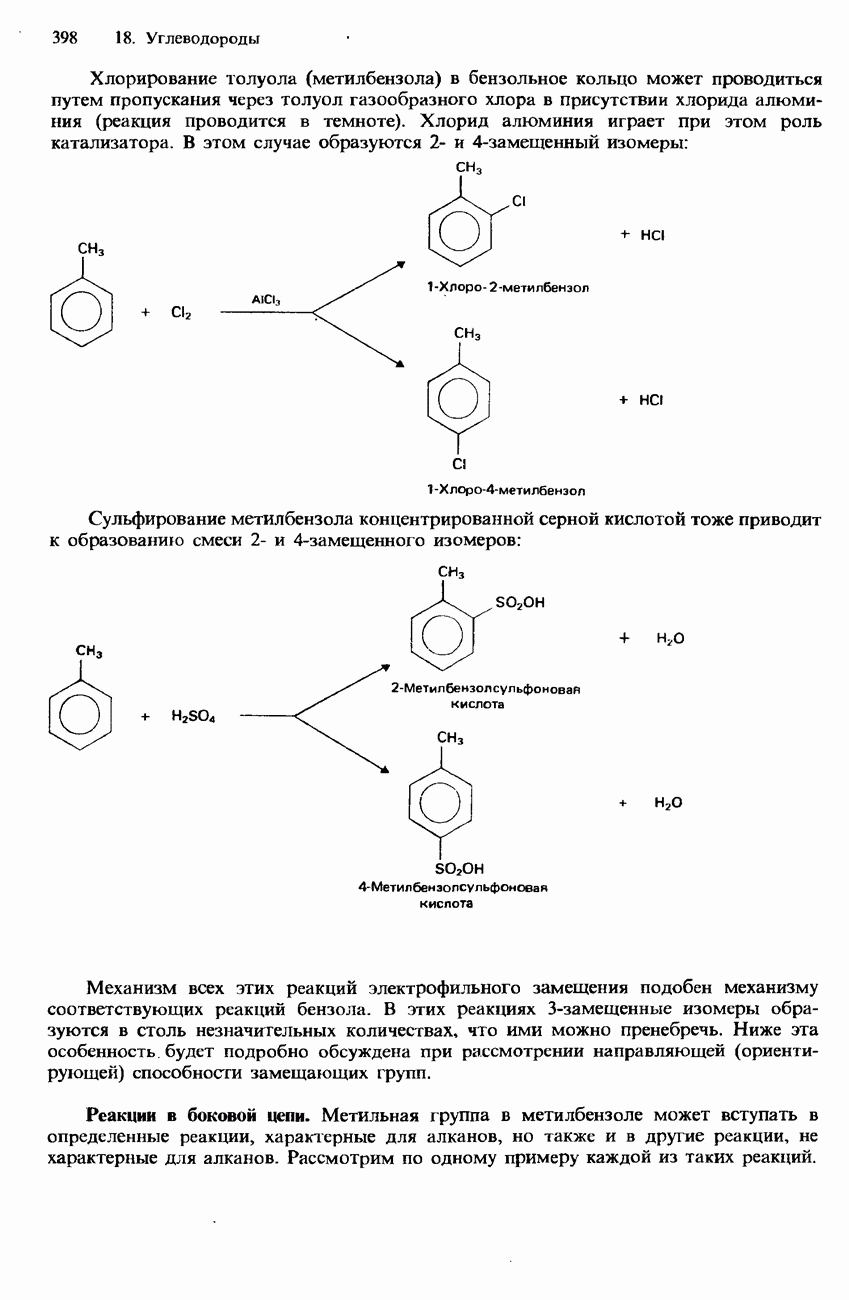
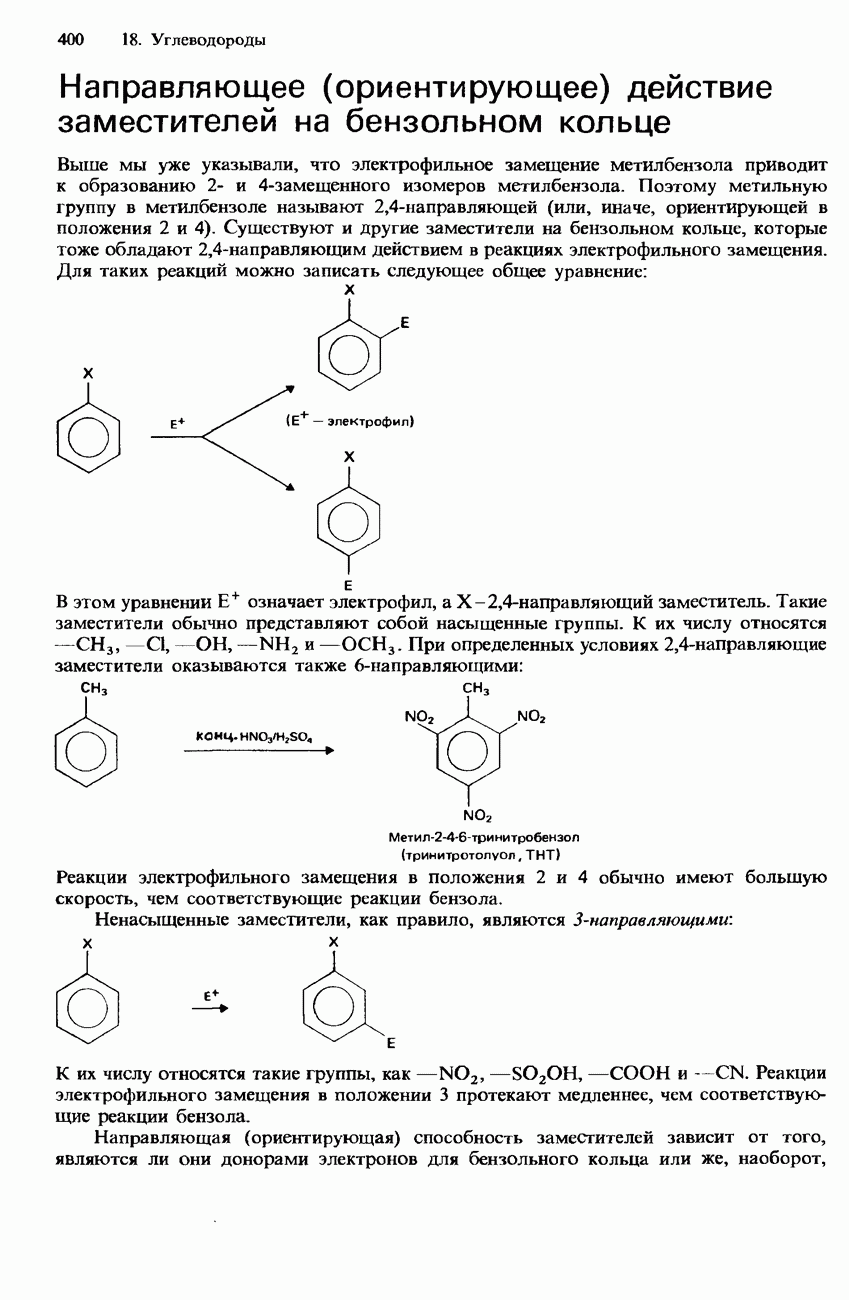
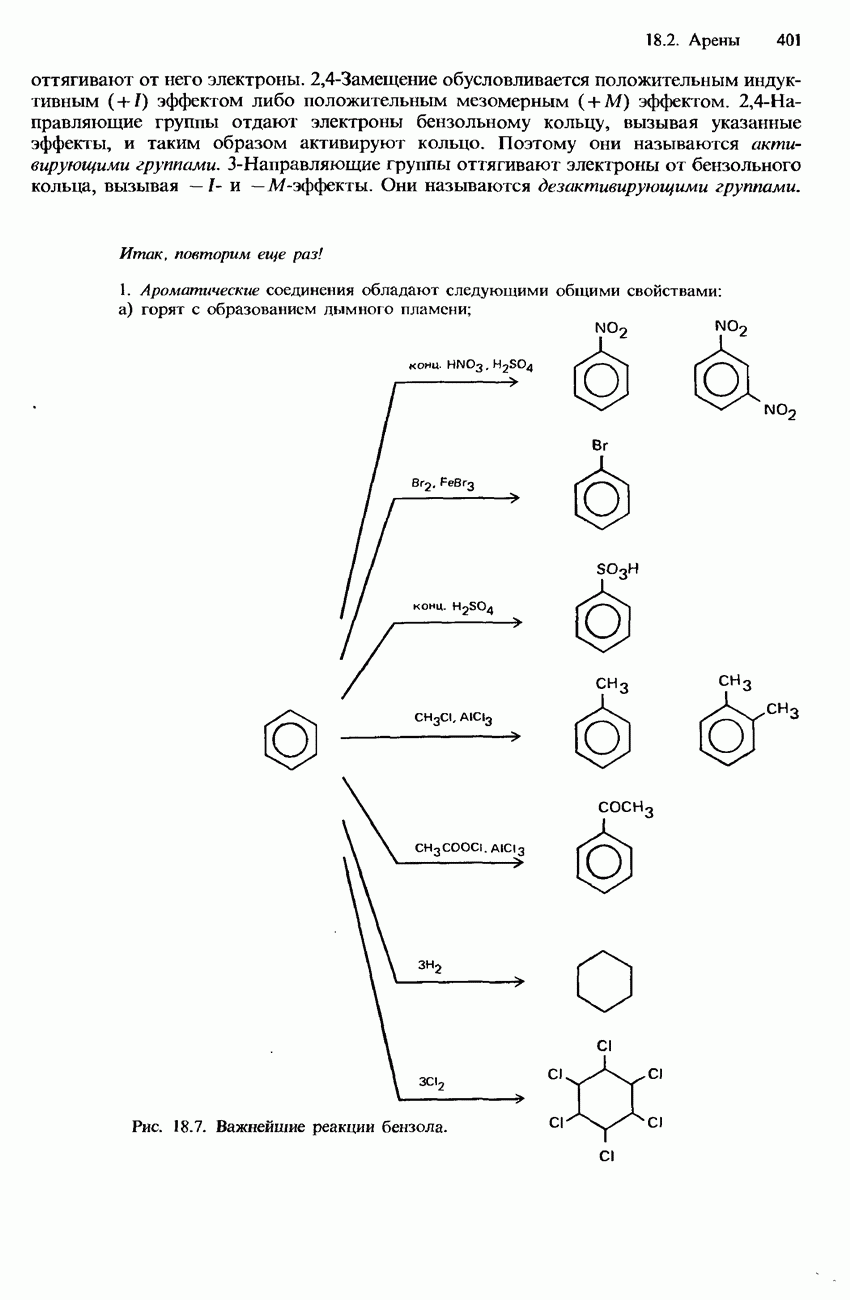
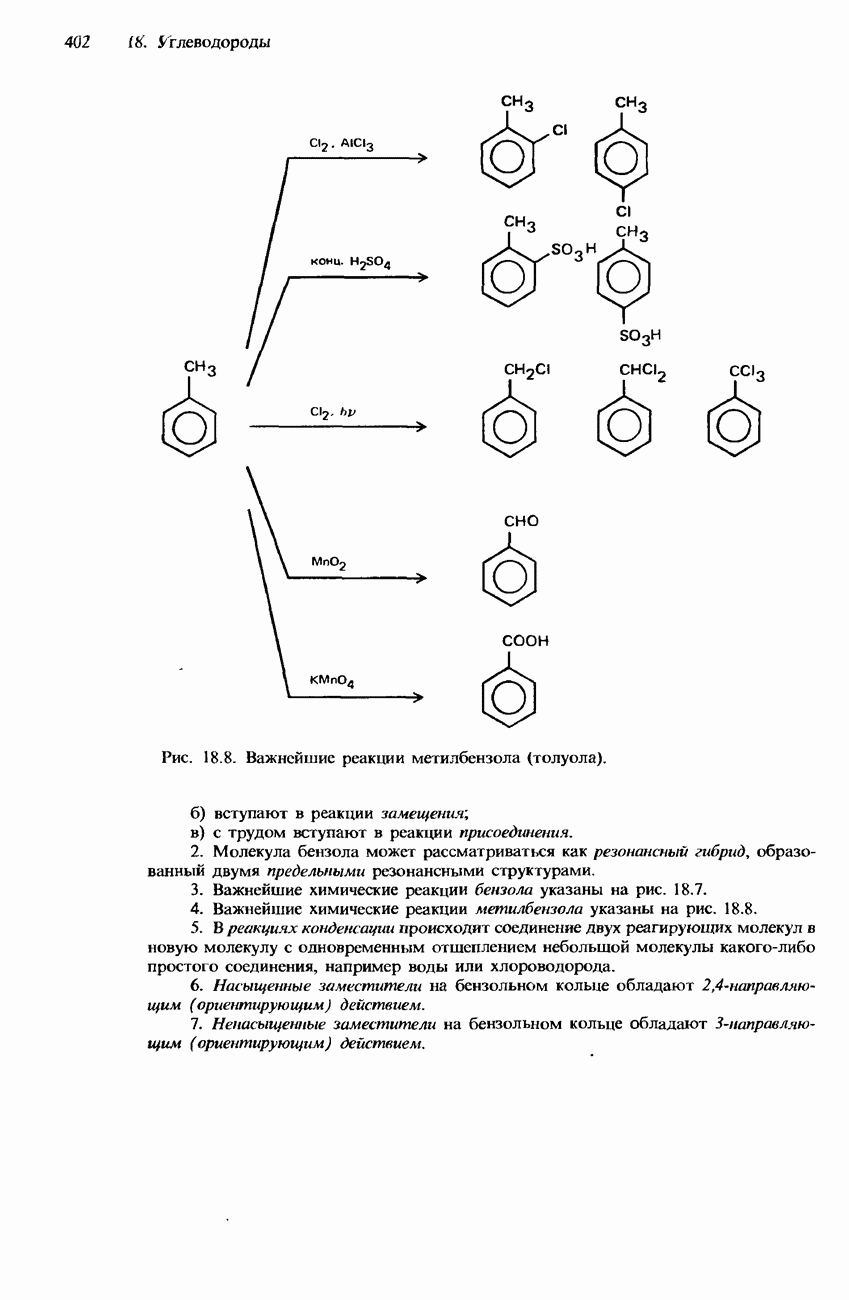
- 18.2. Арены
- БЕНЗОЛ
- МЕТИЛБЕНЗОЛ
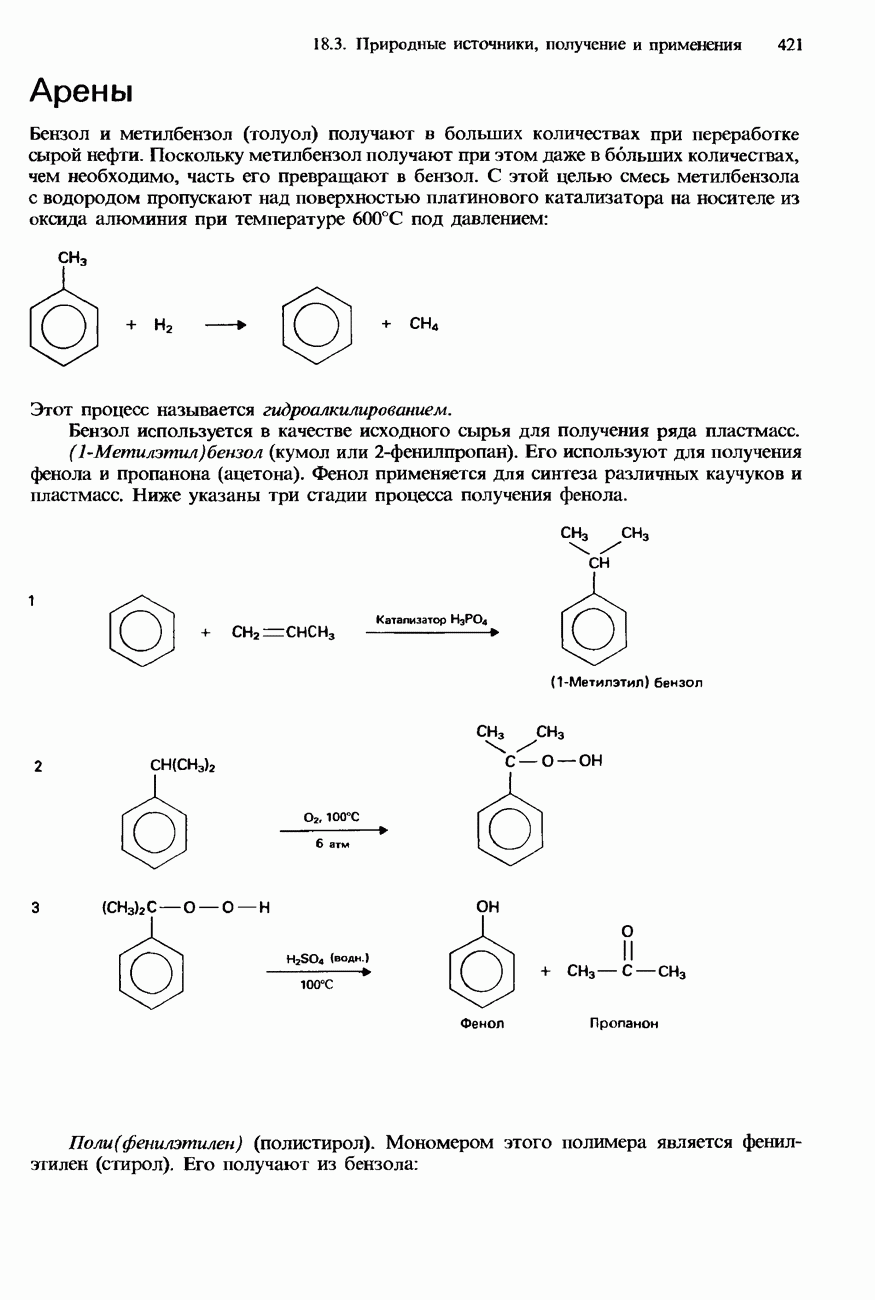
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
- 19.2. Спирты, фенолы и эфиры
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- КАРБОНОВЫЕ КИСЛОТЫ
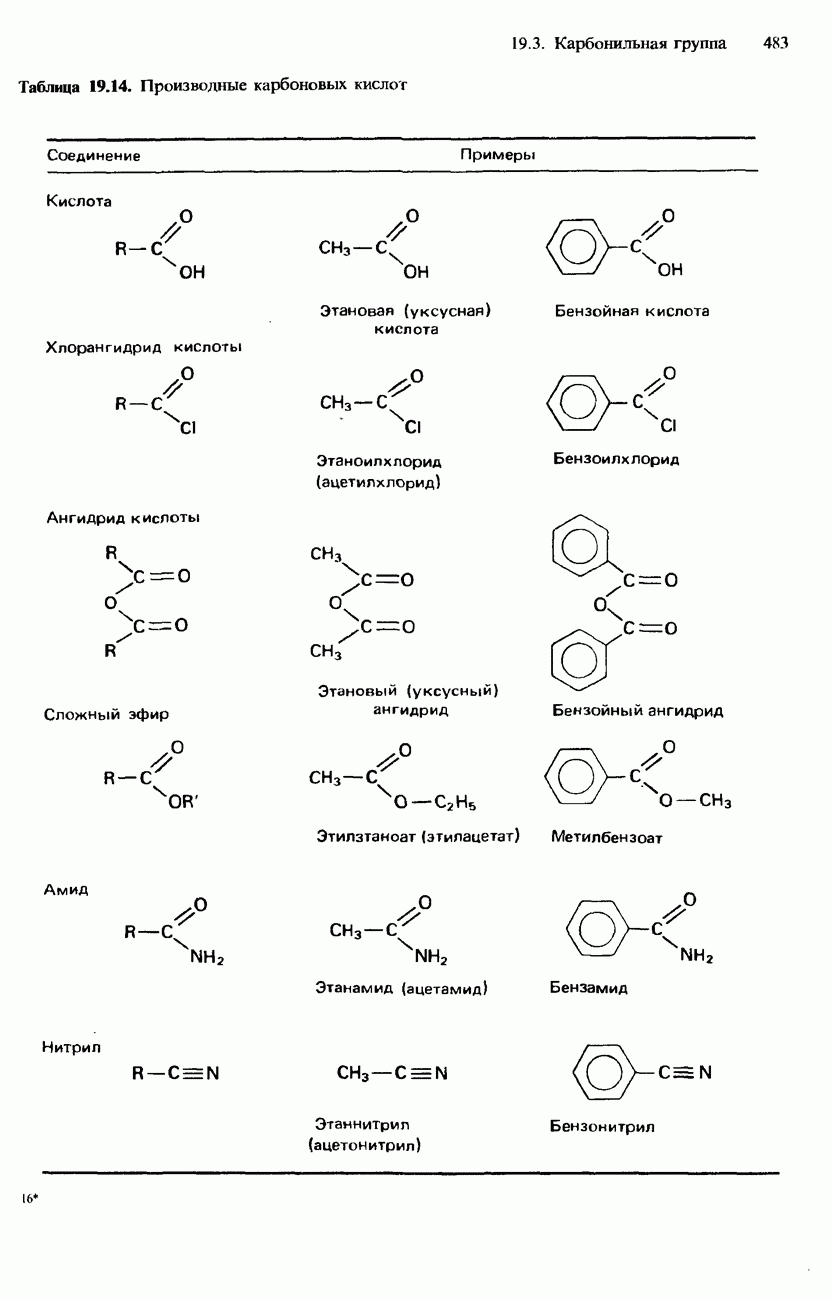
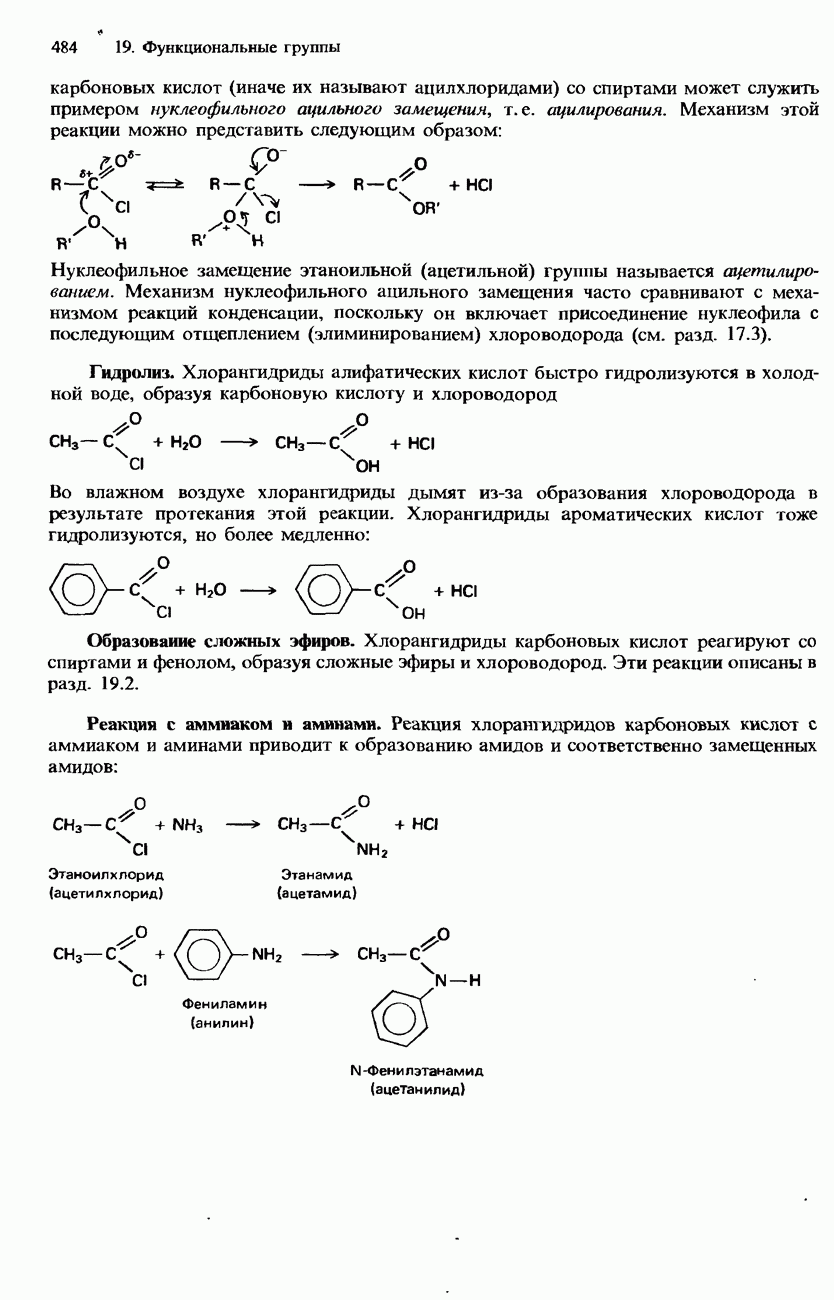
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
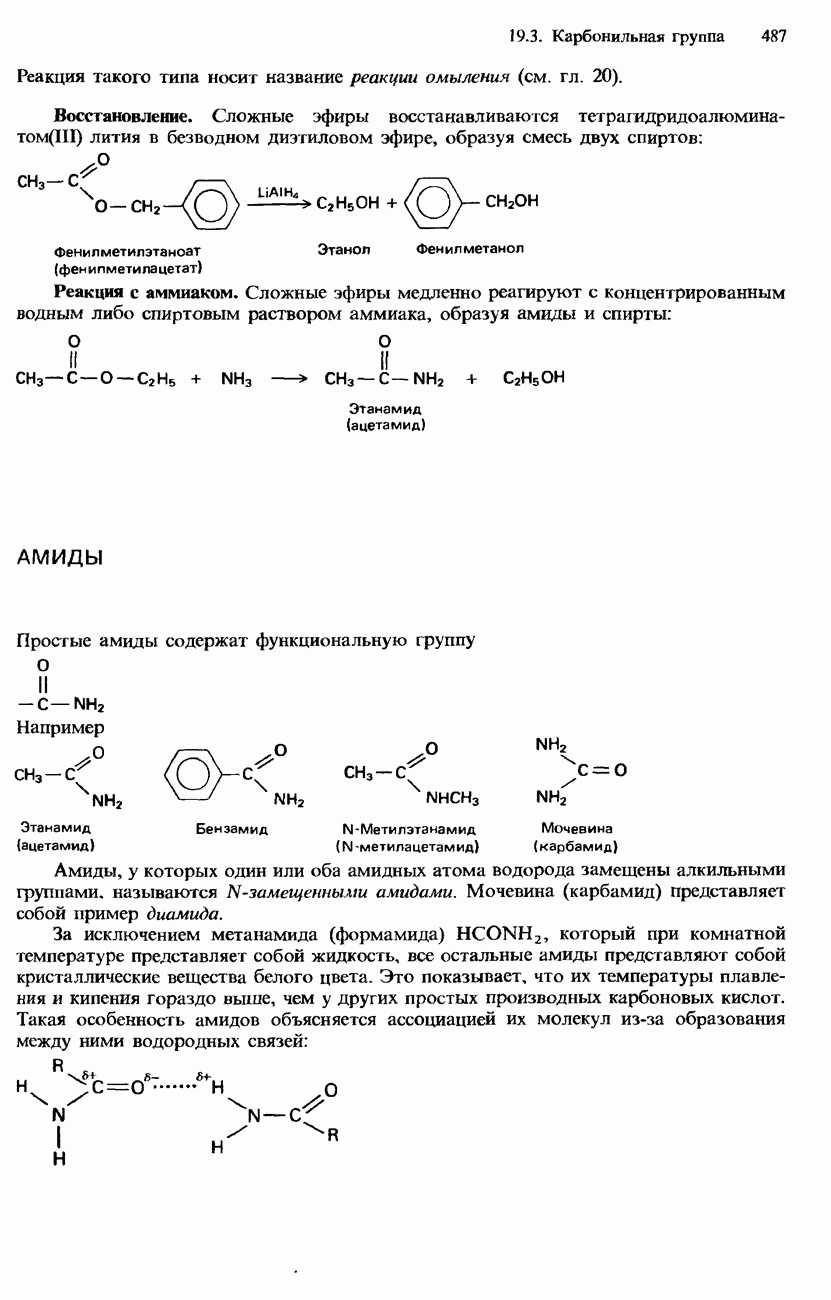
- АМИДЫ
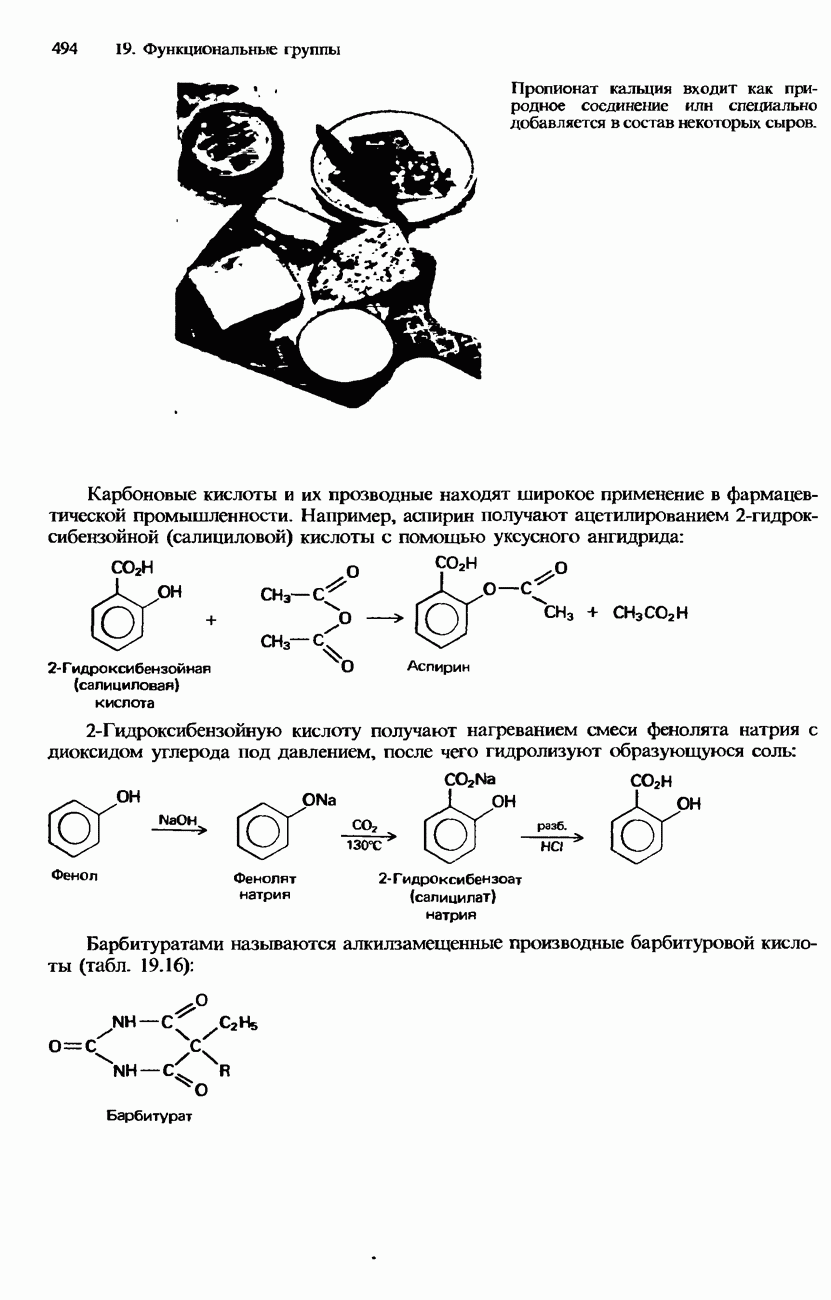
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
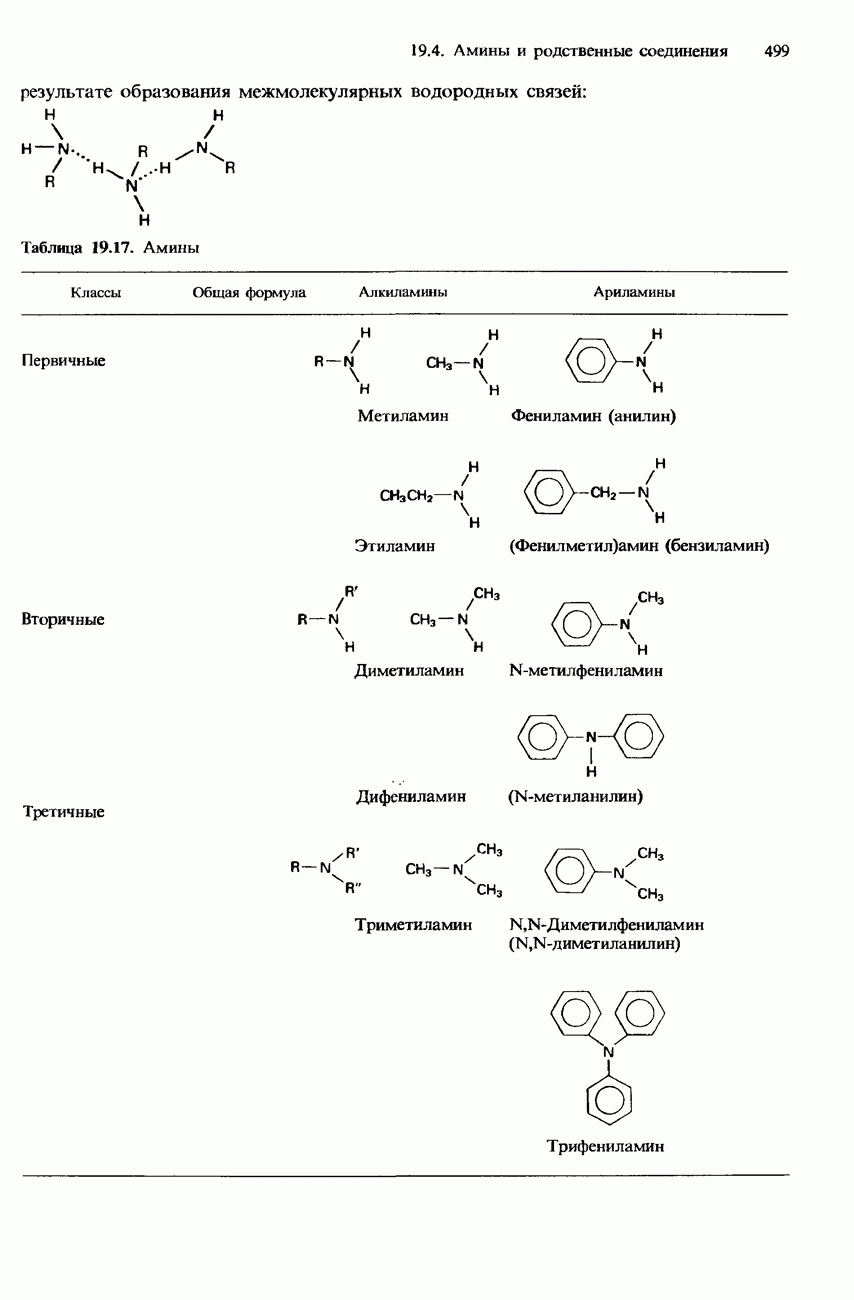
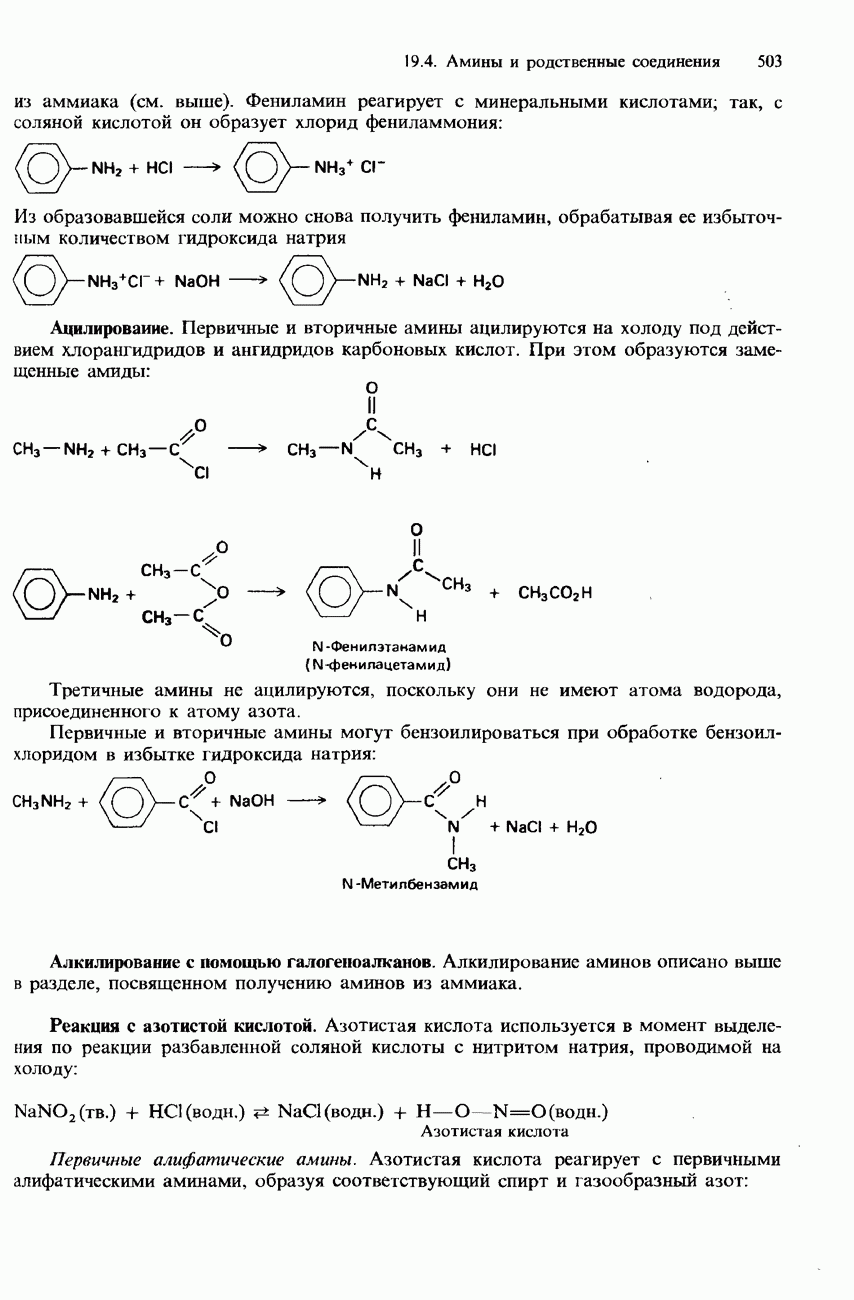
- 19.4 Амины и родственные соединения
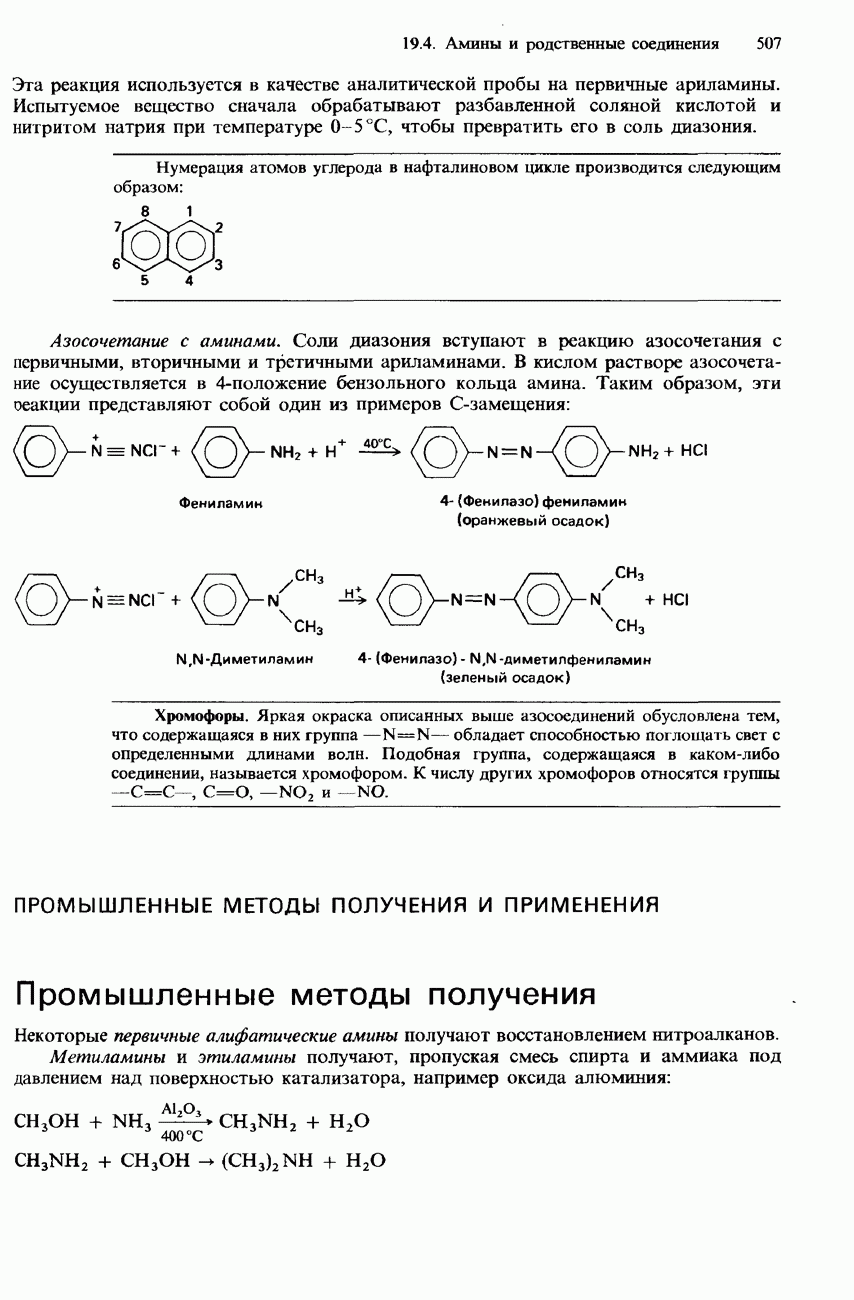
- СОЛИ ДИАЗОНИЯ
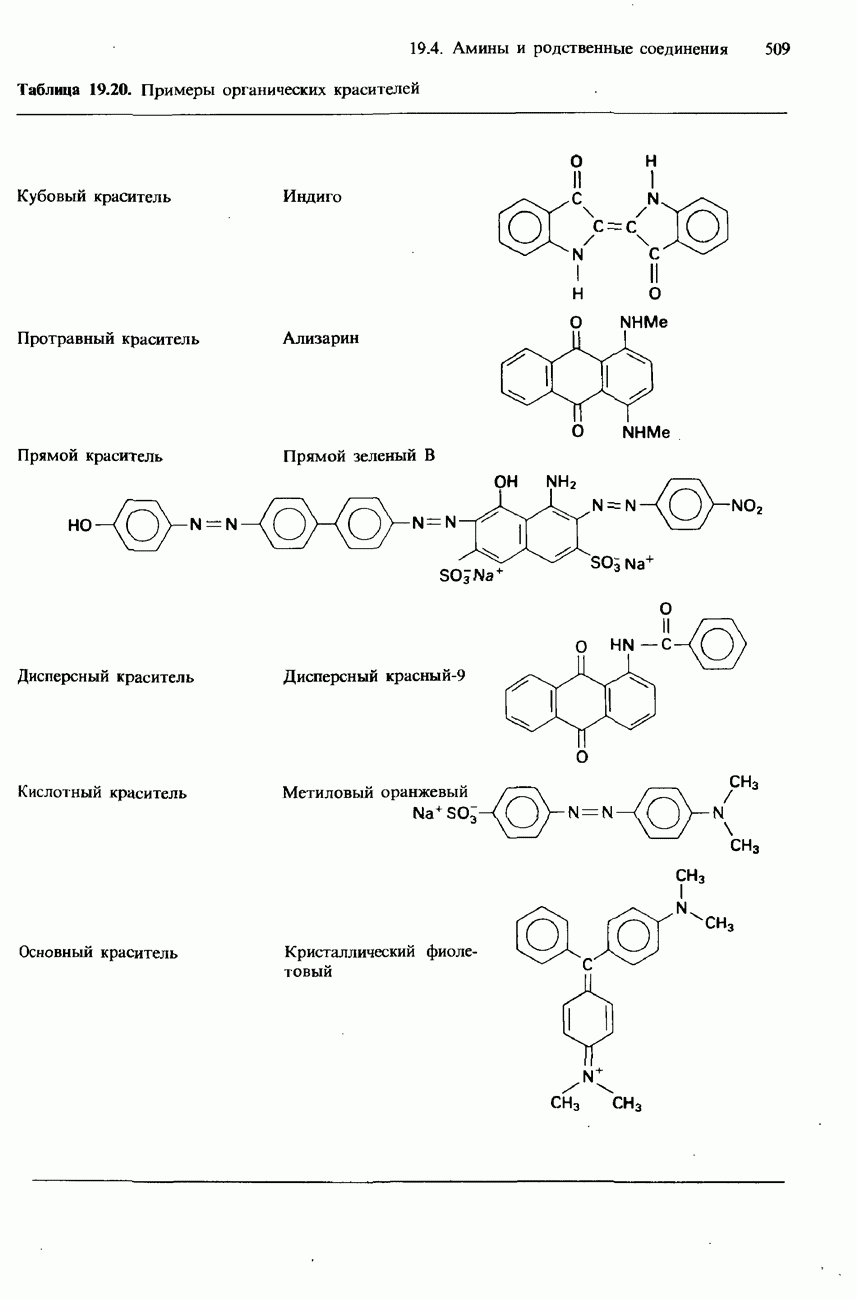
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
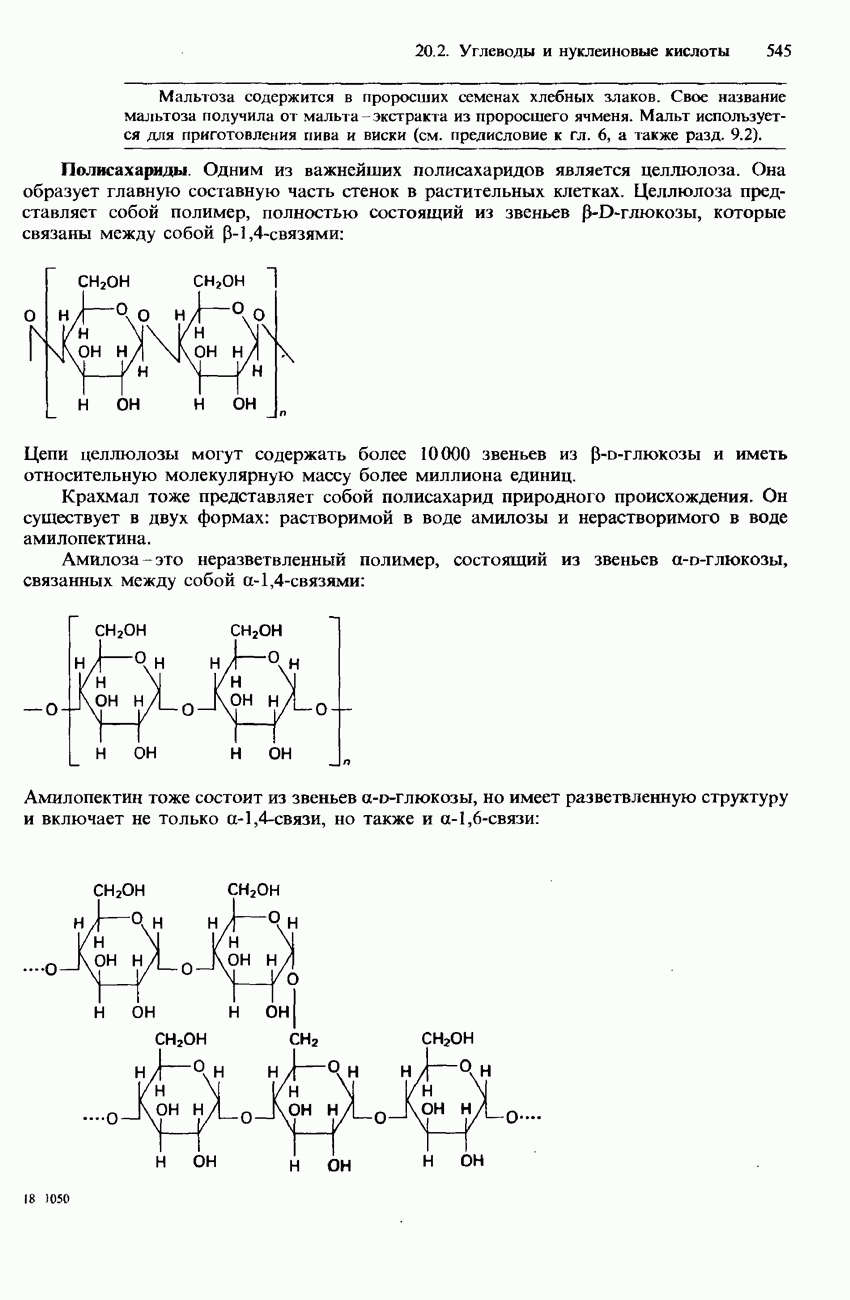
- 20.2. Углеводы и нуклеиновые кислоты
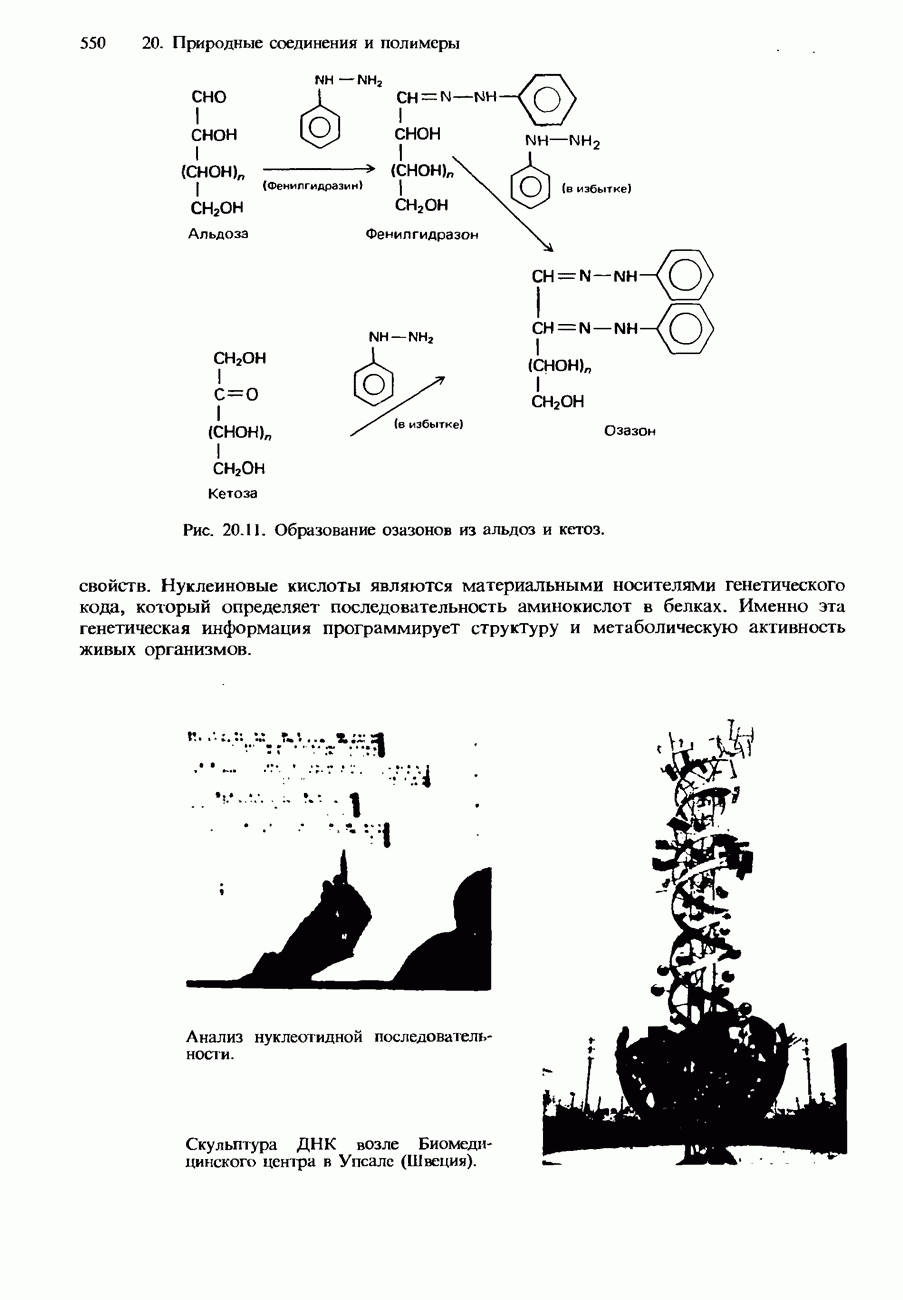
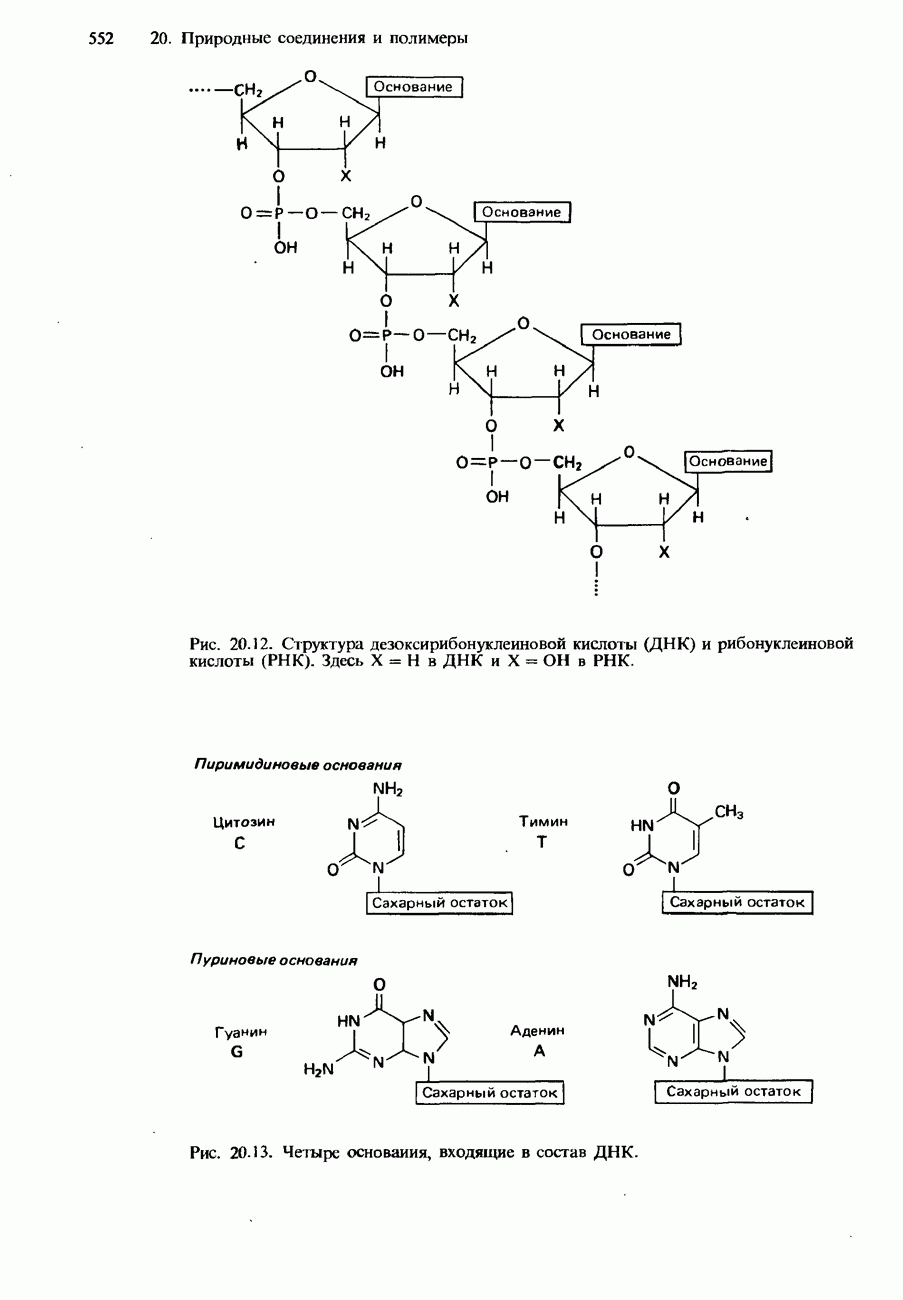
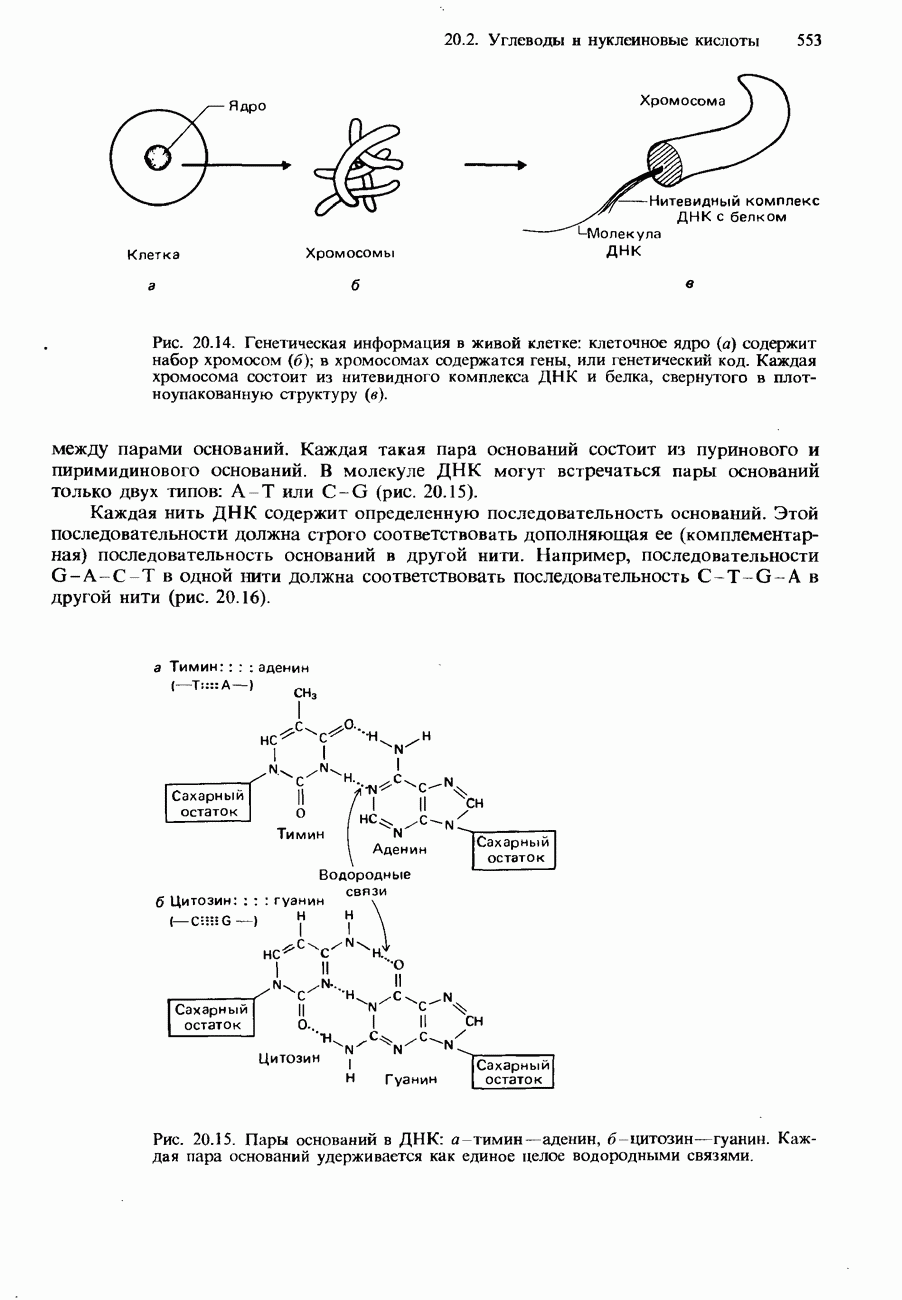
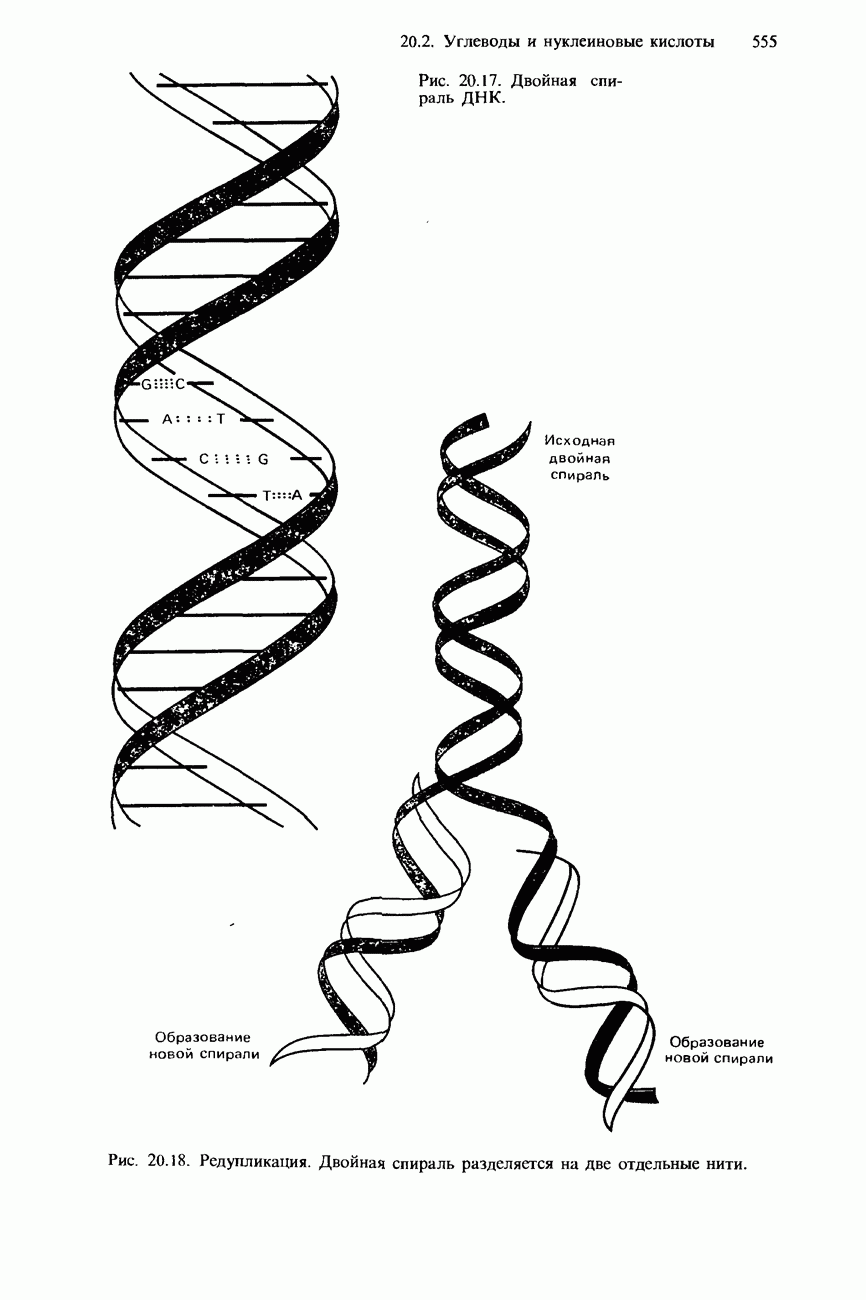
- НУКЛЕИНОВЫЕ КИСЛОТЫ
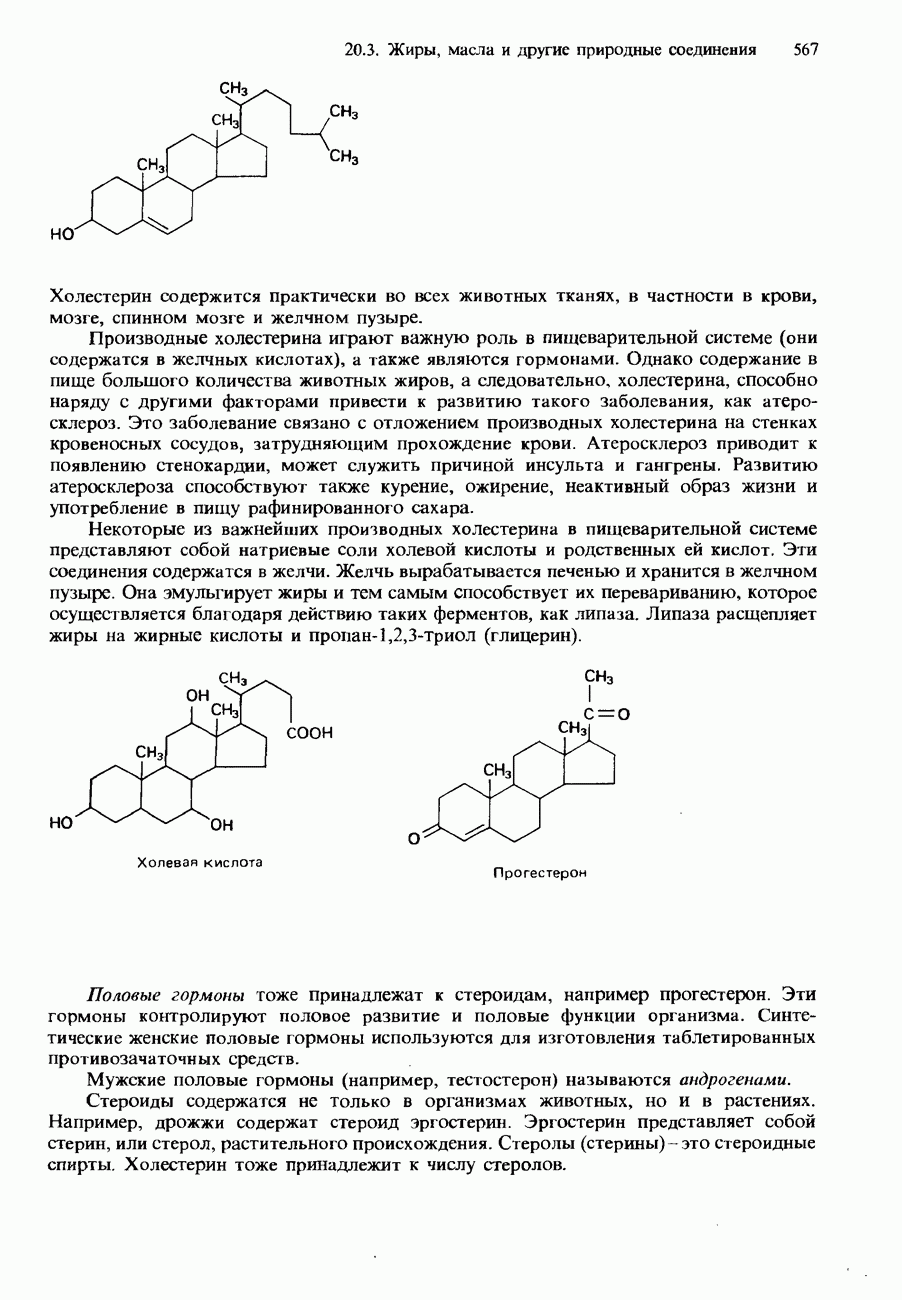
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
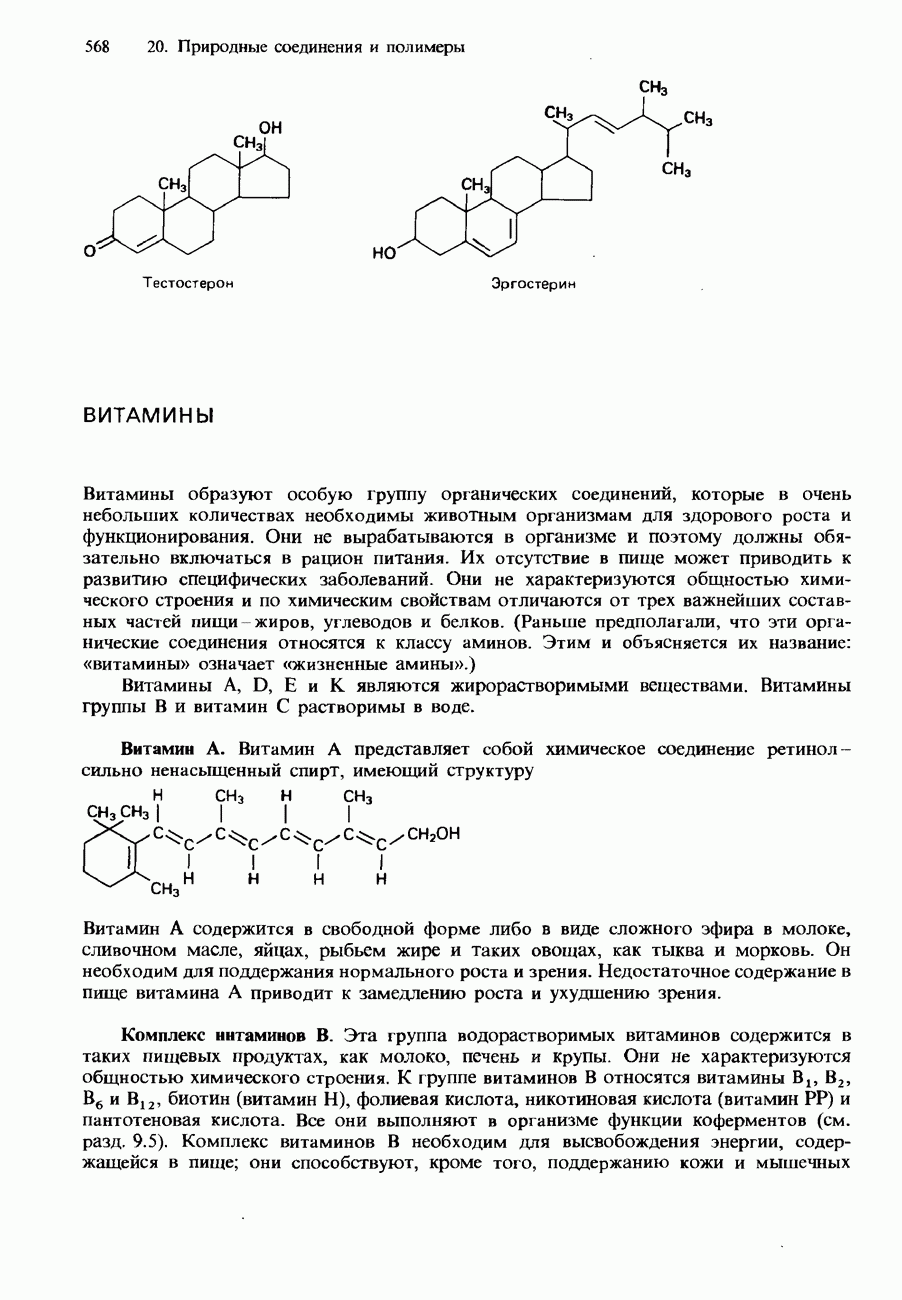
- ВИТАМИНЫ
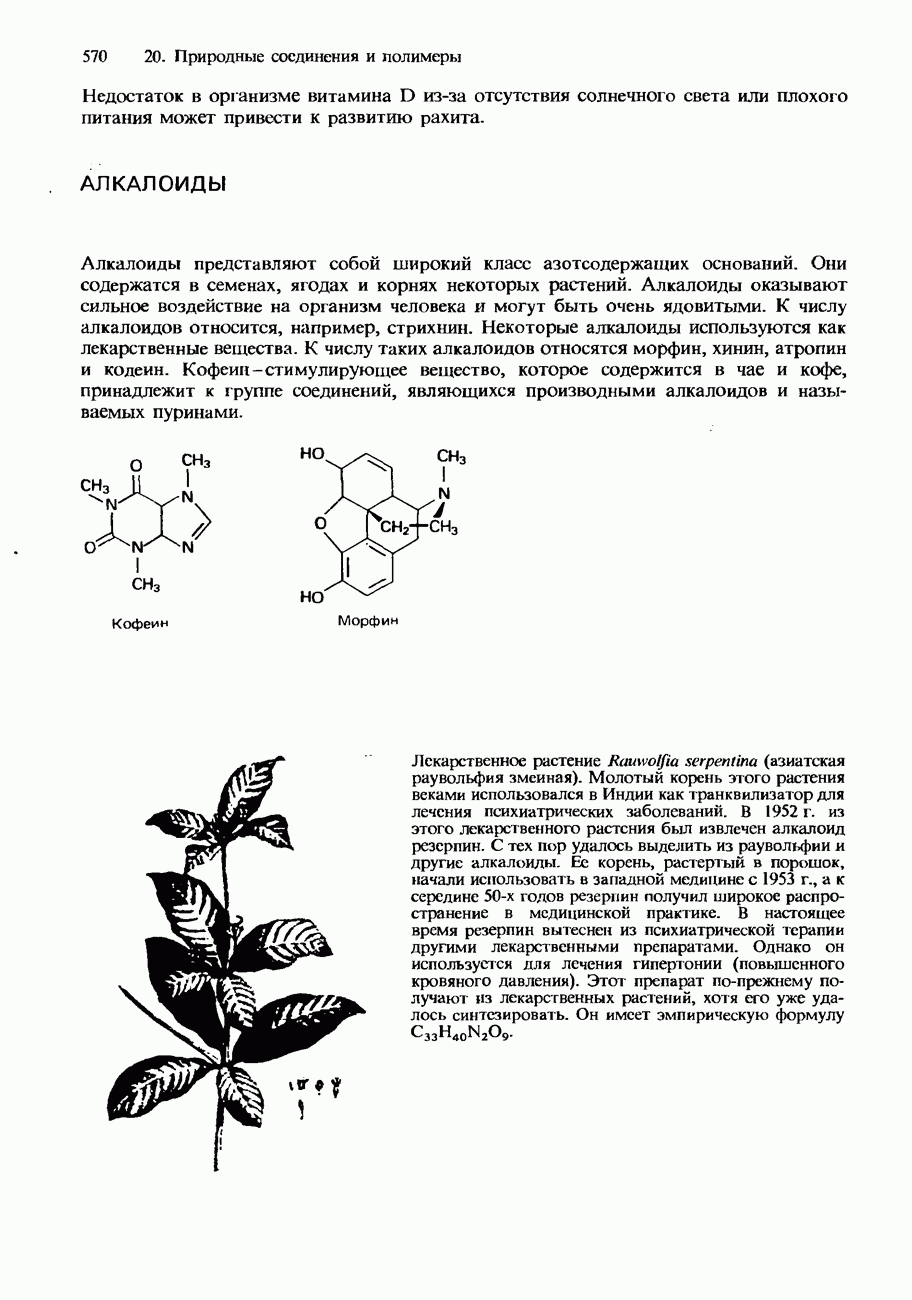
- АЛКАЛОИДЫ
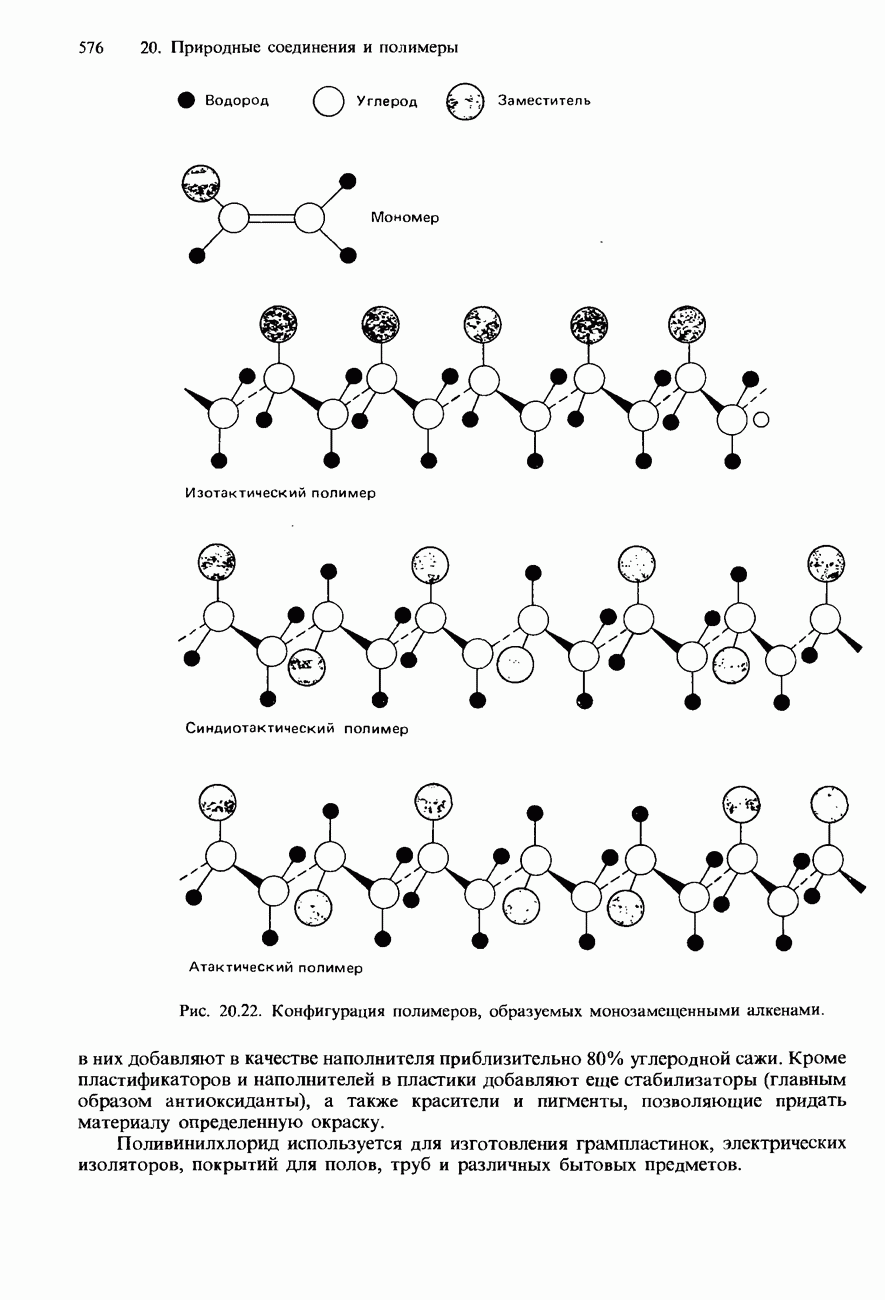
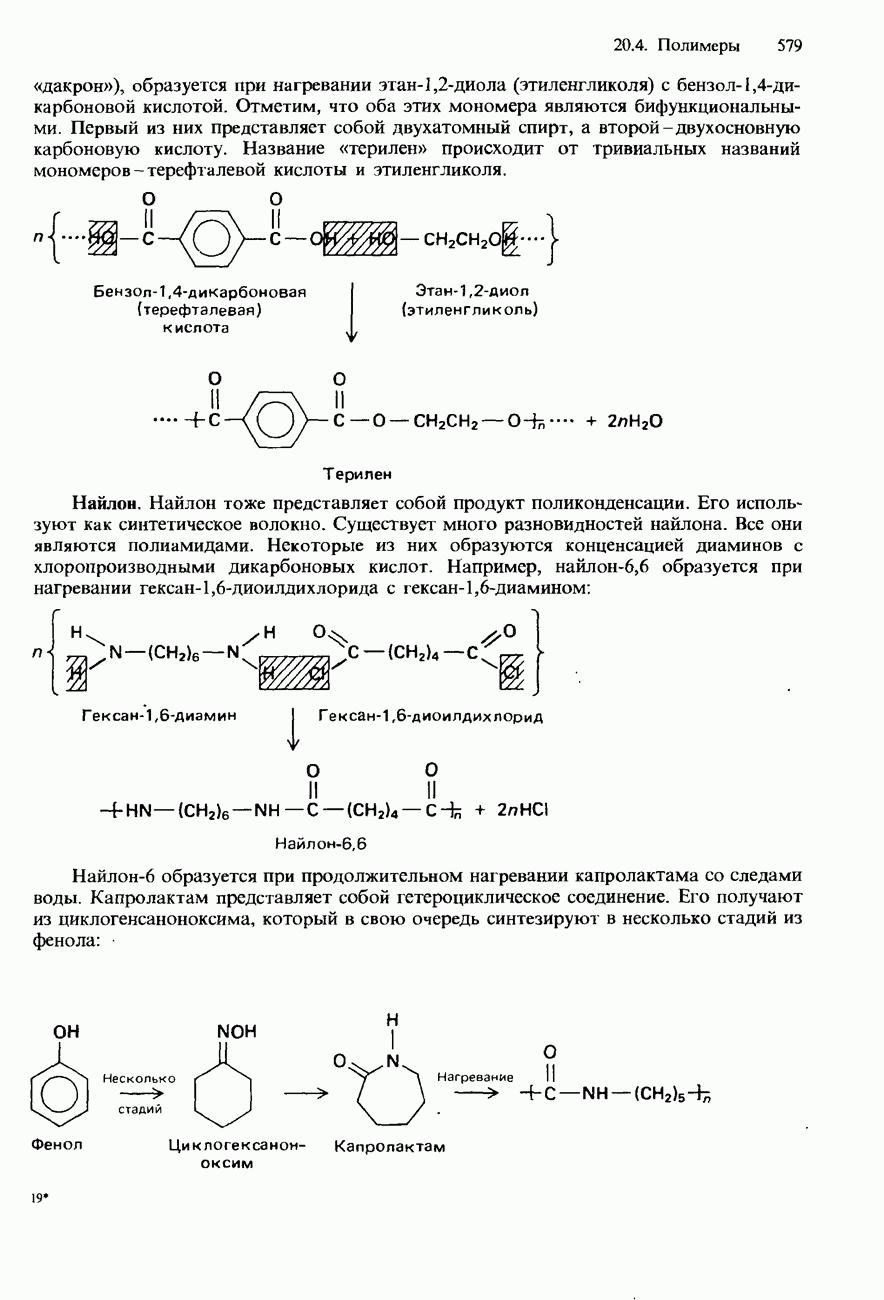
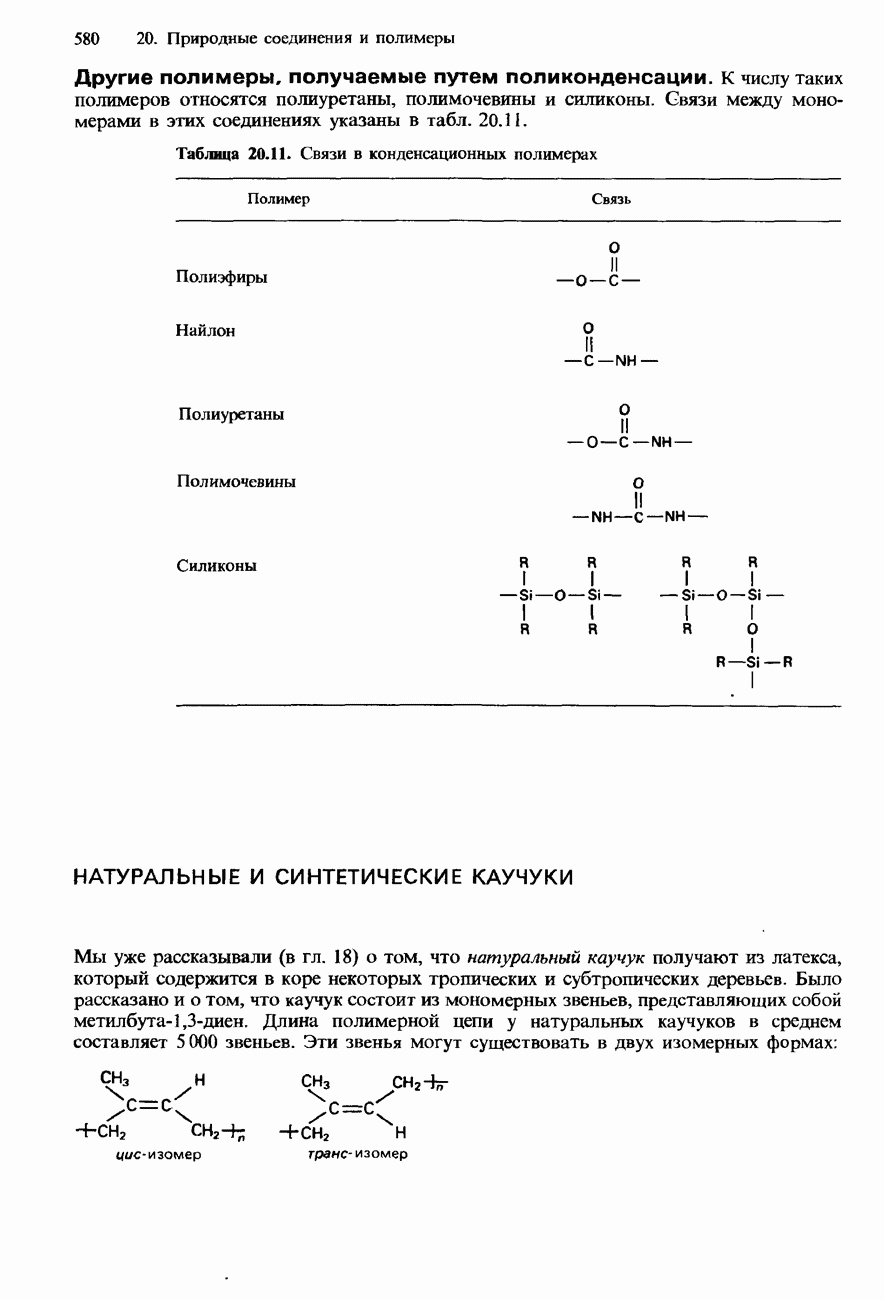
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ