| << Предыдущий параграф | Следующий параграф >> |
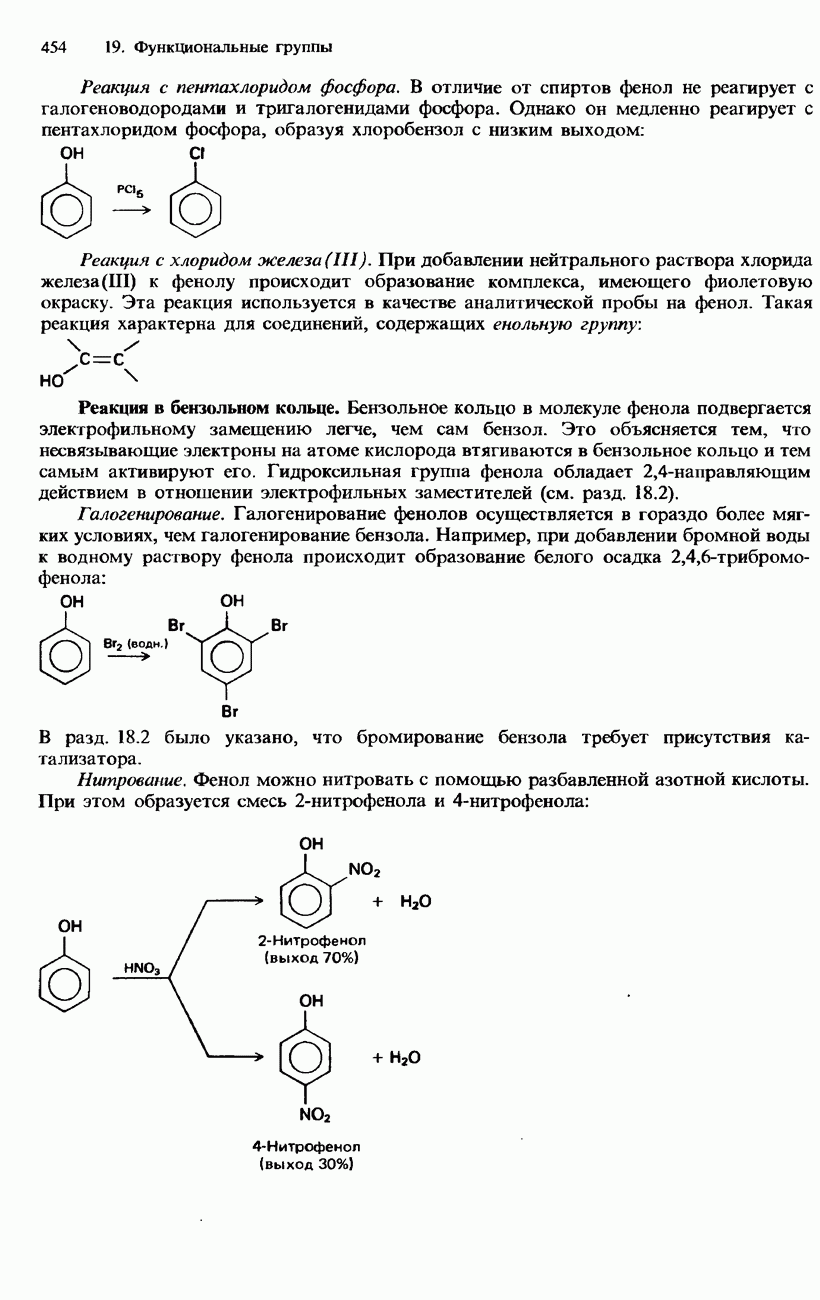
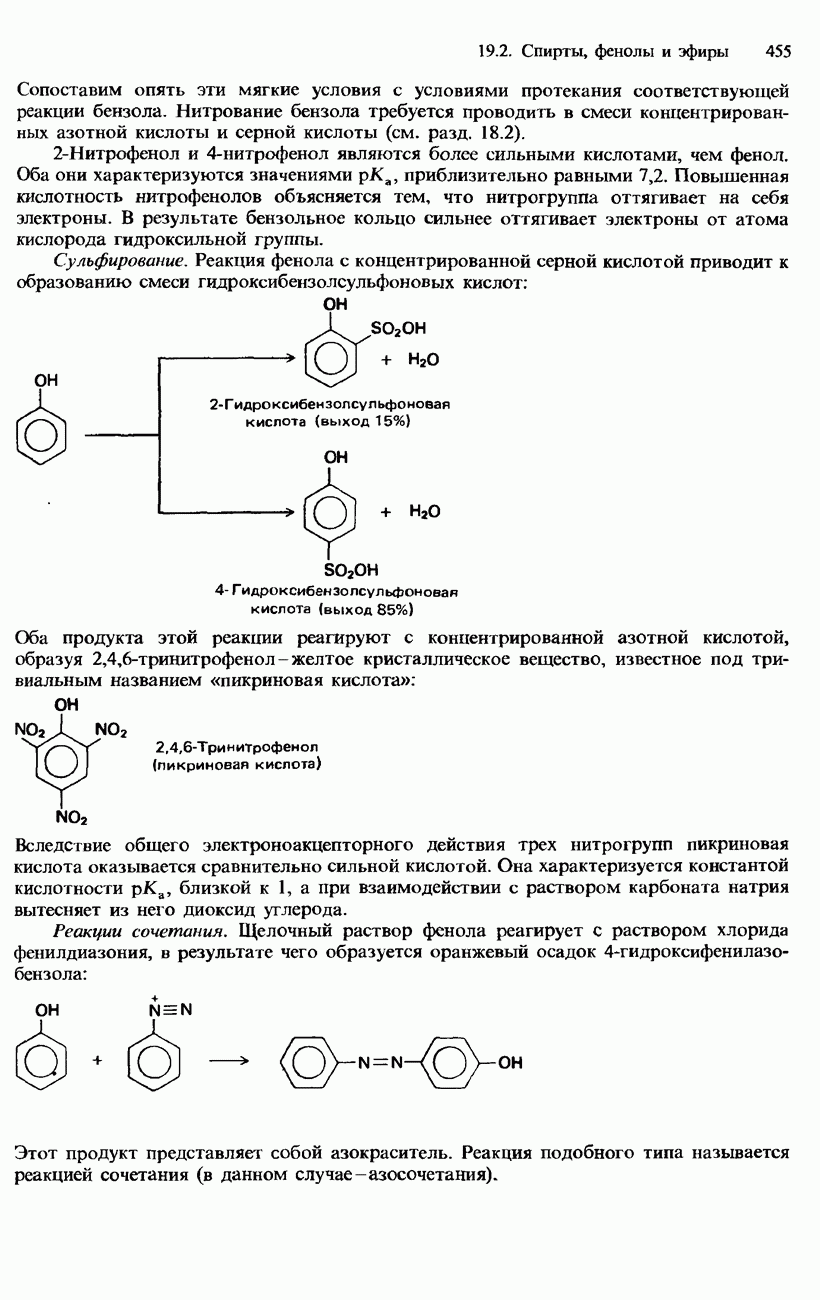
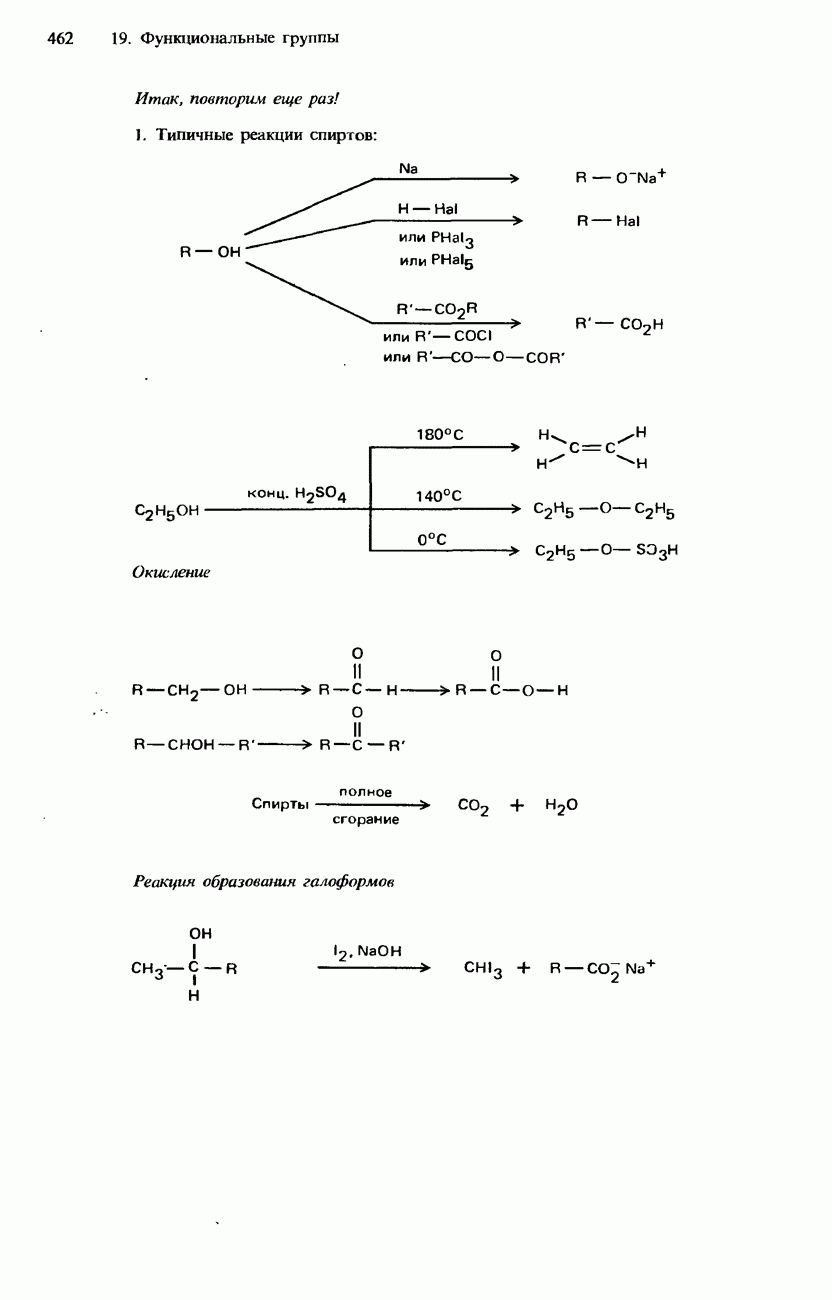
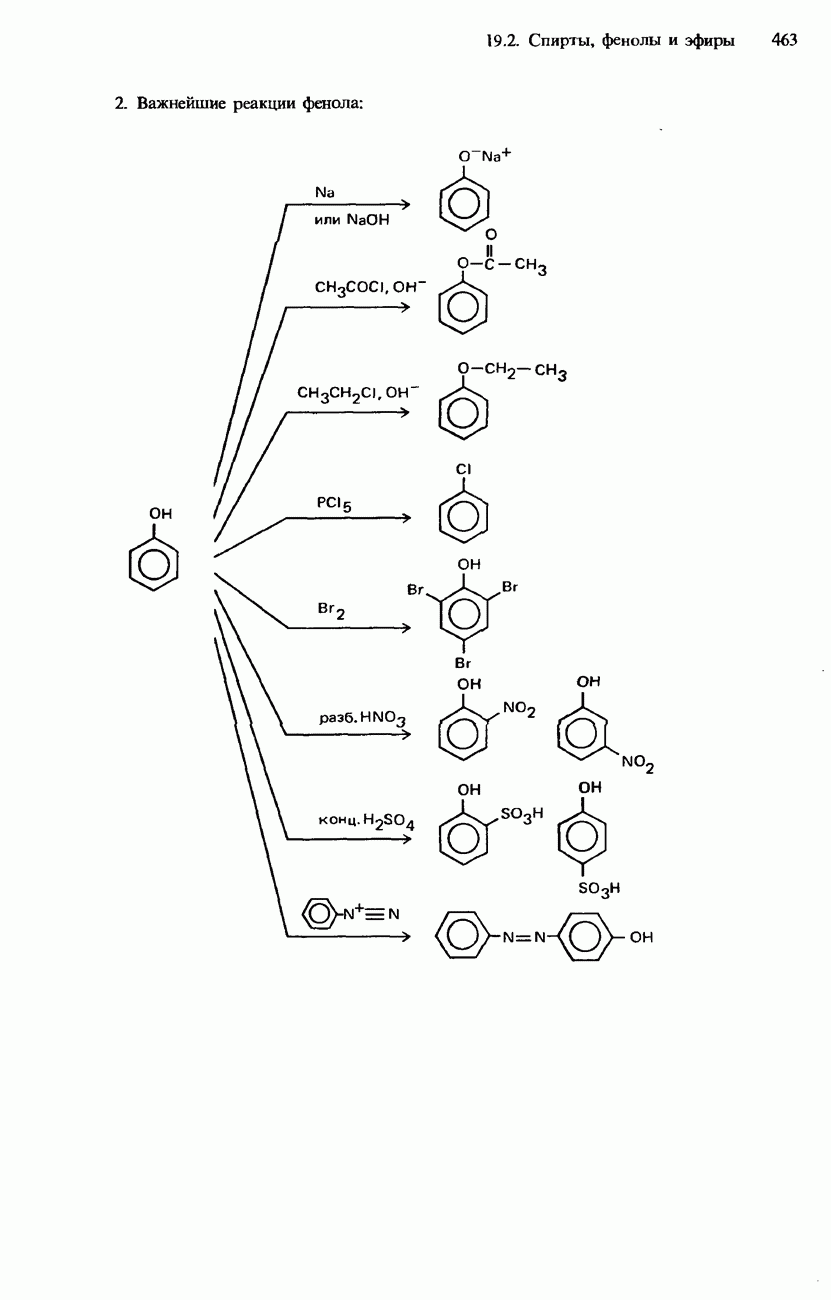
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОПРОСЫ ДЛЯ ПРОВЕРКИ
1. Этот вопрос касается периодической таблицы и электронного строения элементов.

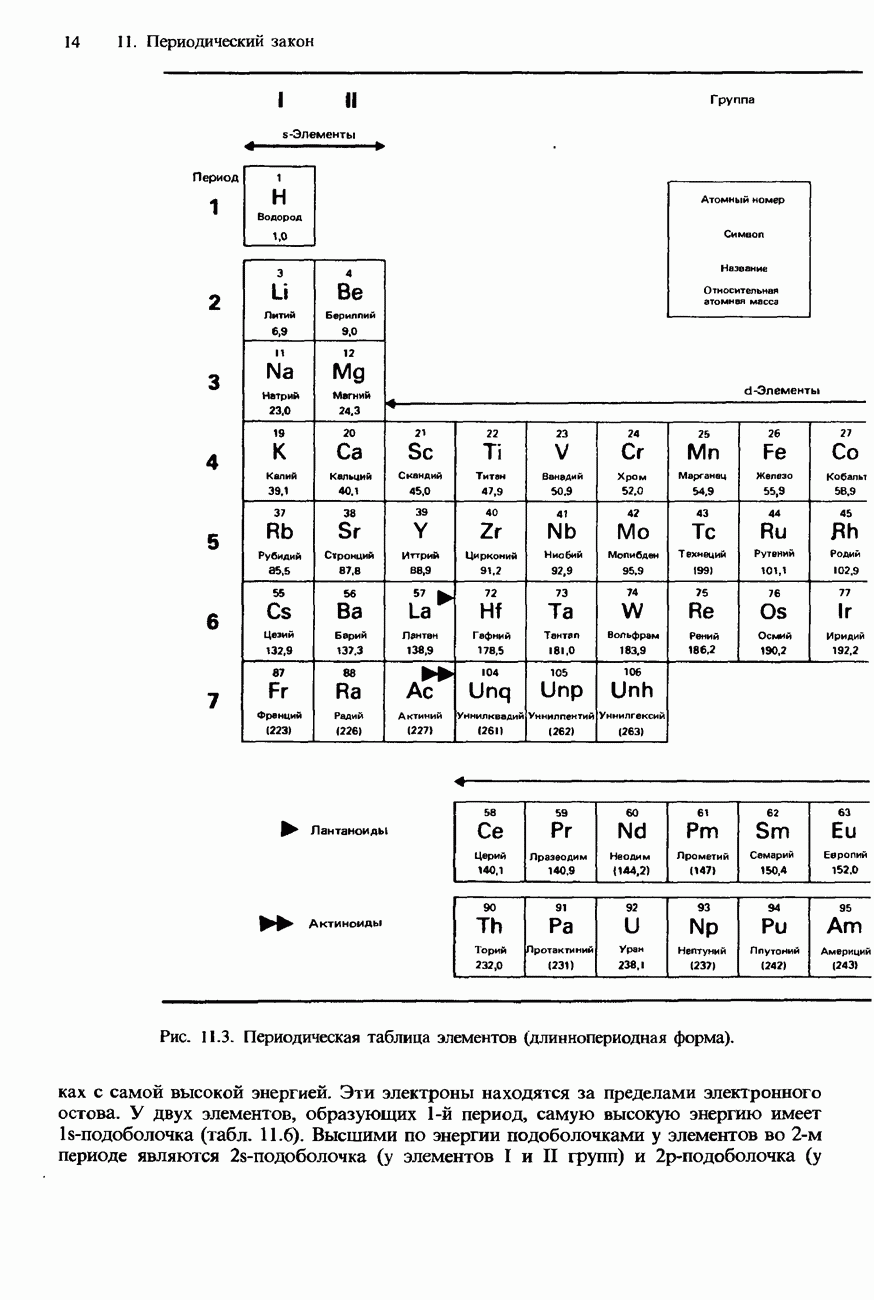
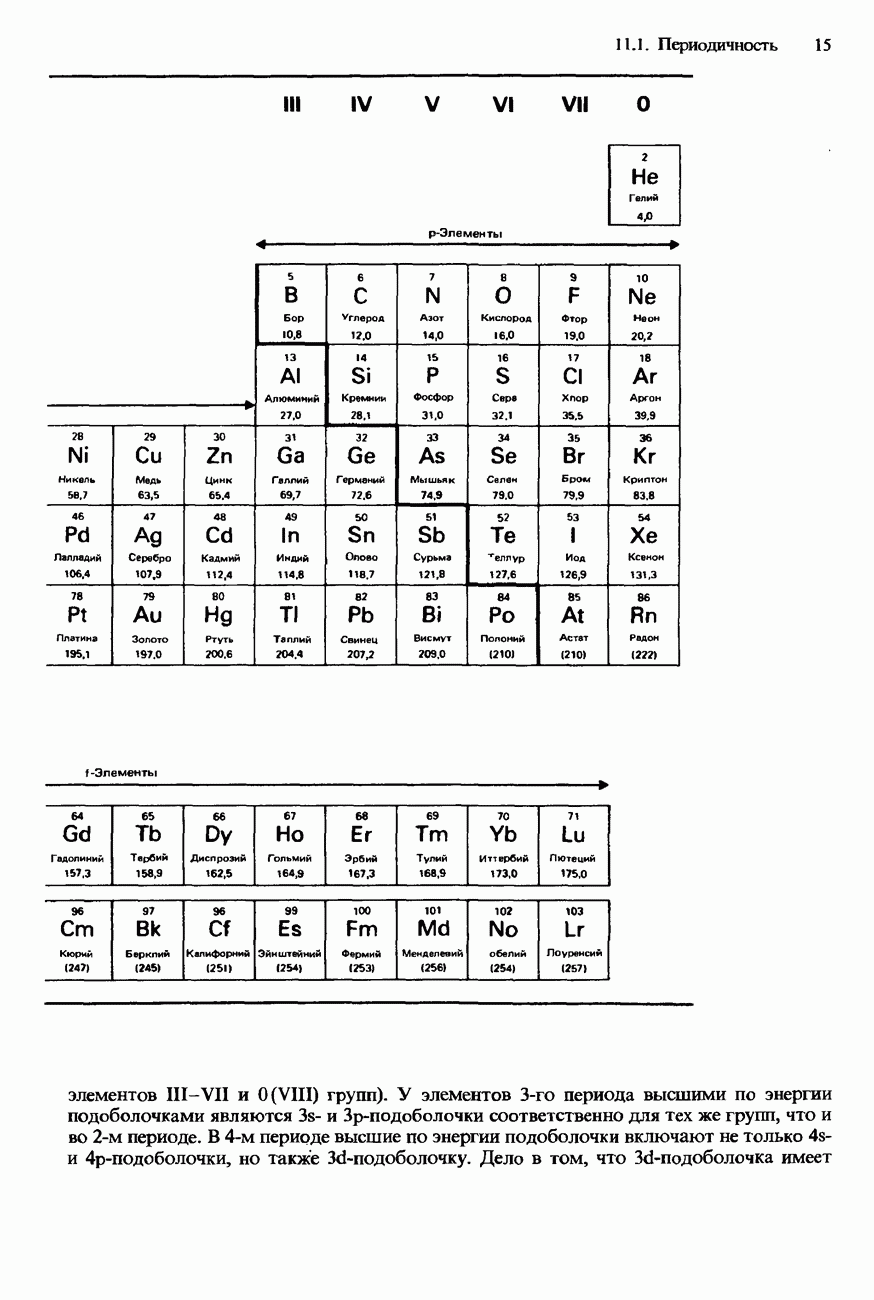
На приведенной здесь схеме изображена часть периодической таблицы элементов; положения гелия, лития и бора указаны их символами. (Остальные буквы представляют собой не химические символы, а лишь указывают положение некоторых обсуждаемых ниже элементов.)
а) Укажите, в каких областях таблицы расположены: 1) s-элементы, 2) р-элементы, 3) d-элементы.
б) 1) Укажите электронное строение элемента Т, обозначив заселенность всех его s- и р-уровней.
2) Больше или меньше первая энергия ионизации элемента Т, чем у лития? Кратко поясните ответ.
в) Каждый из элементов U и X образует соединения, в которых они имеют степень окисления +3. Укажите, как изменяется электронная конфигурация свободных элементов U и X при изменении степени окисления до +3.
г) Какой из элементов - U, W или Q вероятнее всего имеет наибольшее число степеней окисления?
д) 1) Какой из  или
или  -должен иметь наибольшую первую энергию ионизации и почему?
-должен иметь наибольшую первую энергию ионизации и почему?
е) Каждый из элементов X и Y имеет валентность, равную трем.
1) Какую форму должны иметь молекулы газообразных мономерных трихлоридов этих элементов?
2) В чем причина различия  формы?
формы?
2. Объясните, от каких важнейших факторов зависят закономерности изменения физических и химических свойств элементов в пределах одной и той же группы периодической таблицы.
Основываясь на известных вам свойствах элементов с небольшими атомными номерами, предскажите, какими должны быть:
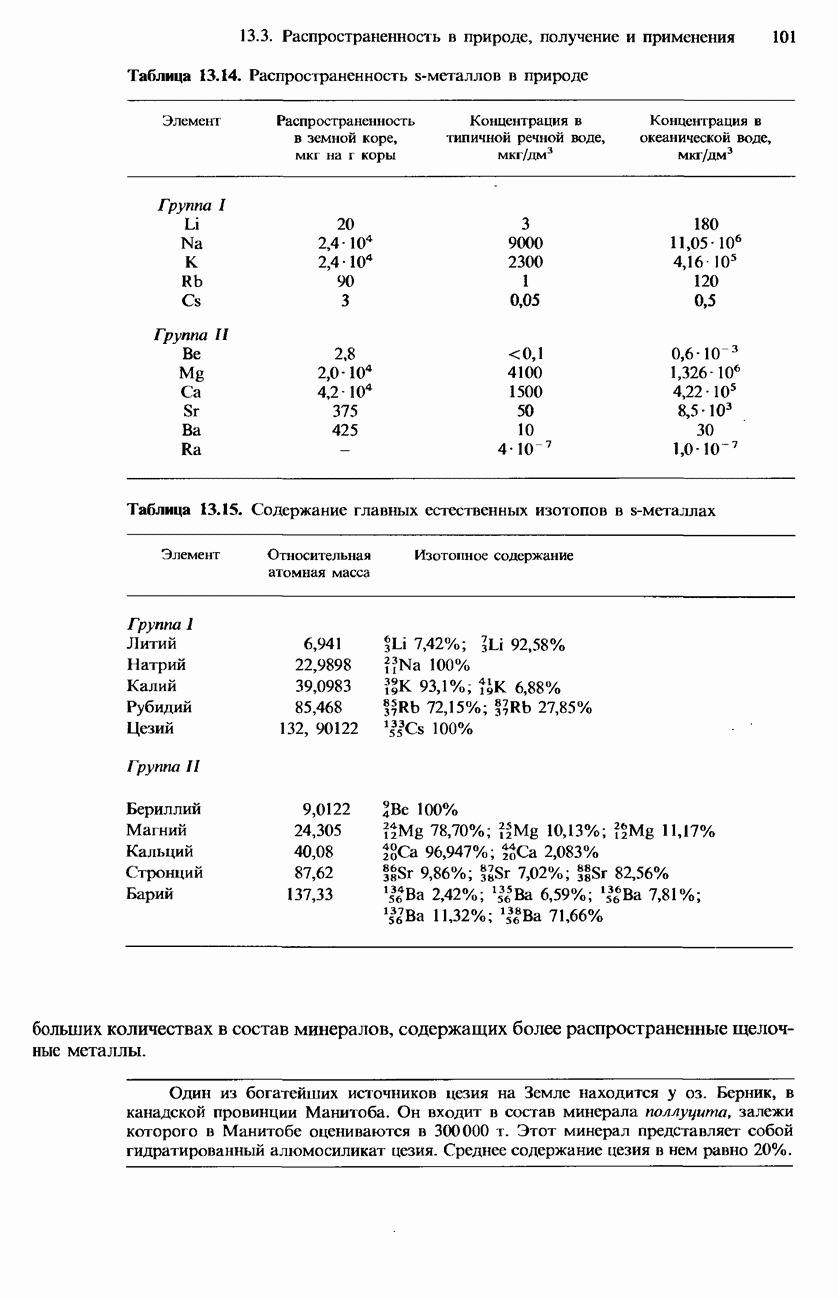
а) физические свойства цезия - пятого элемента в группе I, а также его реакция с водой;
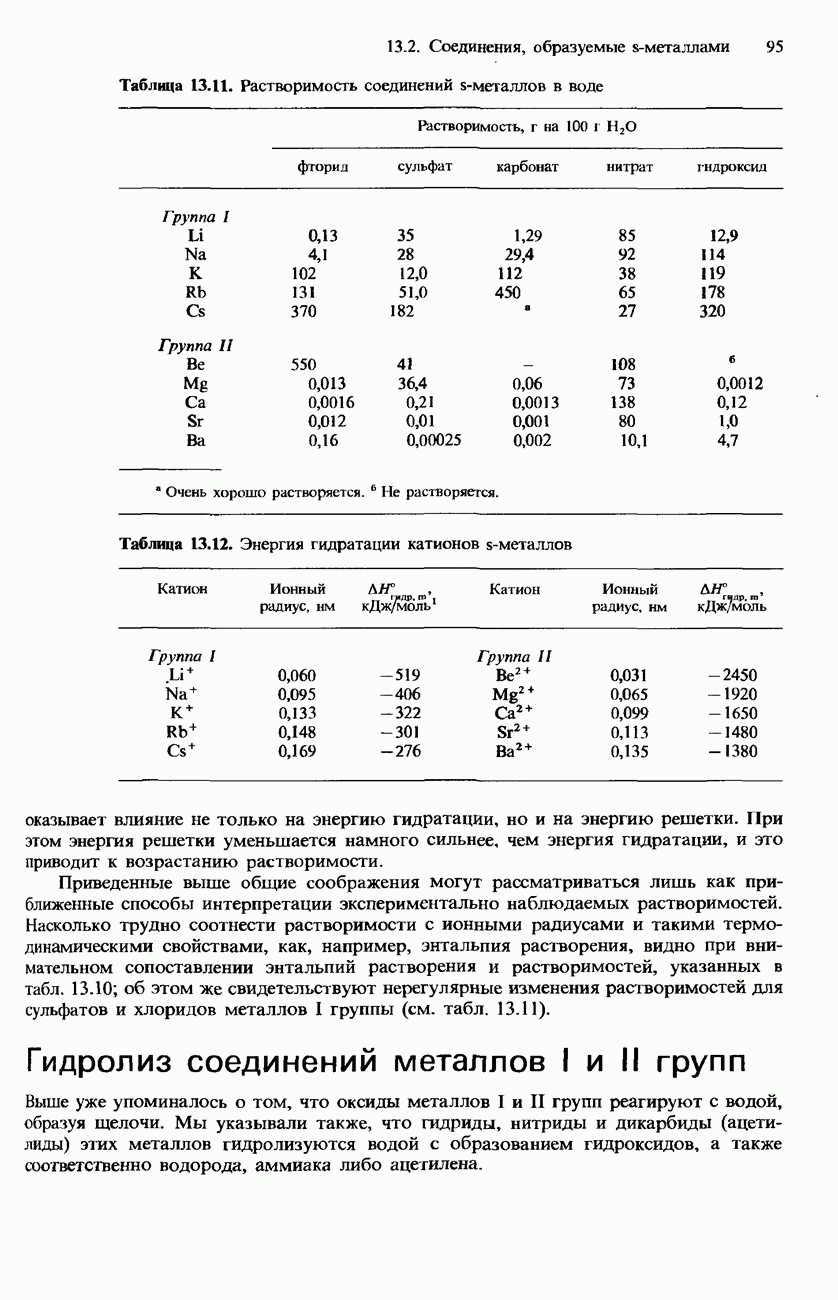
б) растворимость солей бария в воде (барий является пятым элементом в группе II
в) металлический характер висмута - пятого элемента в группе V.
3. а) Кратко опишите, на каком принципе основана последовательность расположения химических элементов в периодической таблице. Какова закономерность изменения у элементов первых двух периодов: I) атомного радиуса и 2) первой энергии ионизации?
Можно ли по положению элемента в периодической таблице отнести его к металлам или неметаллам? Объясните ответ, б) Проиллюстрируйте переход от свойств неметаллических элементов к свойствам металлических элементов, наблюдаемый у элементов IV группы С,  и РЬ, основываясь на свойствах их оксидов и хлоридов.
и РЬ, основываясь на свойствах их оксидов и хлоридов.
4. а) Ниже указаны шесть первых энергий ионизации элемента А:

1) К какой группе периодической таблицы принадлежит элемент А и почему?
2) Какую формулу имеет высший хлорид, образуемый элементом А?
3) Исходя из того, что атомный номер элемента А больше 10, предскажите, какой должна быть реакция высшего хлорида элемента А с водой, и объясните, на чем основан ваш ответ.
б) Для элемента В первая энергия ионизации газообразных ионов  равна
равна 
Каково сродство к электрону газообразных атомов элемента В?
в) К какой группе периодической таблицы должен принадлежать элемент В и почему?
5. Опишите закономерности изменения химических свойств хлоридов указанных ниже элементов: 1) для элементов 3-го периода от  до S; 2) для элементов V группы от N до
до S; 2) для элементов V группы от N до  Рассмотрите такие свойства как структуру, тип химической связи и реакцию с водой.
Рассмотрите такие свойства как структуру, тип химической связи и реакцию с водой.
6. Этот вопрос касается закономерностей изменения свойств и особенностей химических реакций элементов в приведенной части периодической таблицы

а) Укажите символы тех элементов, которые легко реагируют с холодной водой, образуя щелочные растворы, и запишите полное уравнение той из этих реакций, которая, по вашему мнению, протекает наиболее бурно.
б) Укажите символы тех элементов, которые образуют гидриды, имеющие сравнительно низкую температуру кипения. Для наиболее устойчивого гидрида в каждой группе нарисуйте электронную схему связи и схематически изобразите форму его молекулы.
в) Для элементов 3-го периода (в высших состояниях окисления, если их несколько) запишите формулы оксидов, а также соответствующих кислот или гидроксидов, образуемых этими оксидами. Укажите степень окисления рассматриваемого элемента в каждом случае.
г) Укажите символы тех элементов 3-го периода и группы IV, которые образуют нитраты. Объясните, к каким выводам о природе элемента можно прийти на основании сведений о результатах его реакций (если они протекают) с концентрированной азотной кислотой и разбавленной азотной кислотой.
д) В письменной форме представьте сравнительное описание химических свойств фтора и иода, позволяющее проиллюстрировать закономерности изменения свойств элементов в группе VII.
7. Этот вопрос касается только тех элементов, которые находятся в следующей части периодической таблицы:

а) 1) Укажите символы следующих элементов: два металла, которые бурно реагируют с холодной водой;
2) два металла, настолько инертных при комнатной температуре, что они широко используются для нанесения защитных покрытий;
3) один элемент, обладающий физическими и химическими свойствами, которые присущи как металлам, так и неметаллам;
4) элементы, которые существуют в обычных условиях в виде молекул, содержащих 1, 2, 4 или 8 атомов (приведите по одному примеру каждого типа);
5) два элемента, образующие тетрахлориды, которые при комнатной температуре и нормальном давлении находятся в жидком состоянии;
6) два элемента, которые образуют друг с другом соединение, обладающее наиболее ионной кристаллической решеткой (укажите формулу этого соединения);
7) металл, образующий двухзарядный ион, который в водном растворе обладает окраской и легко окисляется (укажите формулу этого иона, а также его окраску);
8) один металл, который образует в водном растворе два окрашенных иона с различными степенями окисления выше 2 (укажите формулы этих ионов, их степени окисления и окраску).
б) 1) Кратко опишите, как происходит последовательное заполнение электронных оболочек атомов у элементов  периода от калия до криптона.
периода от калия до криптона.
2) Какие особенности электронной структуры объясняют то, что элементы от галлия до брома располагаются соответственно в тех же группах периодической таблицы, что и элементы от алюминия до хлора?
8. Литий не является типичным представителем элементов группы 1 (щелочные металлы), а фтор не является типичным представителем элементов группы VII (галогены).
Объясните, на чем основано это утверждение, кратко обсудив для каждого указанного элемента или его соединений два характерных химических свойства. Сопоставьте свойст  хлоридов всех элементов от магния до серы в
хлоридов всех элементов от магния до серы в  периоде. Ваш ответ должен включать следующие свойства: 1) тип связи в указанных хлоридах, 2) геометрическую форму молекул ковалентных хлоридов, 3) реакции с водой или растворимость в воде.
периоде. Ваш ответ должен включать следующие свойства: 1) тип связи в указанных хлоридах, 2) геометрическую форму молекул ковалентных хлоридов, 3) реакции с водой или растворимость в воде.
9. а) Ниже перечислен ряд элементов и ряд свойств. Укажите попарными сочетаниями букв и цифр, какие свойства более всего соответствуют определенному элементу (каждая цифра должна быть использована только один раз).

б) Сопоставьте химические свойства кальция и серы. Для этого достаточно кратко обсудить:
1) степени окисления;
2) тип химической связи в оксидах, хлоридах и гидридах.
Проиллюстрируйте свои ответы построением диаграмм ионной и ковалентной связи.
в) Для кальция и серы обсудите:
1) основные или кислотные свойства их оксидов и гидридов;
2) предельную степень гидролиза, возможную для их хлоридов.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
- ПЕРИОДИЧНОСТЬ
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
- 13.3. Распространенность в природе, получение и применение
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
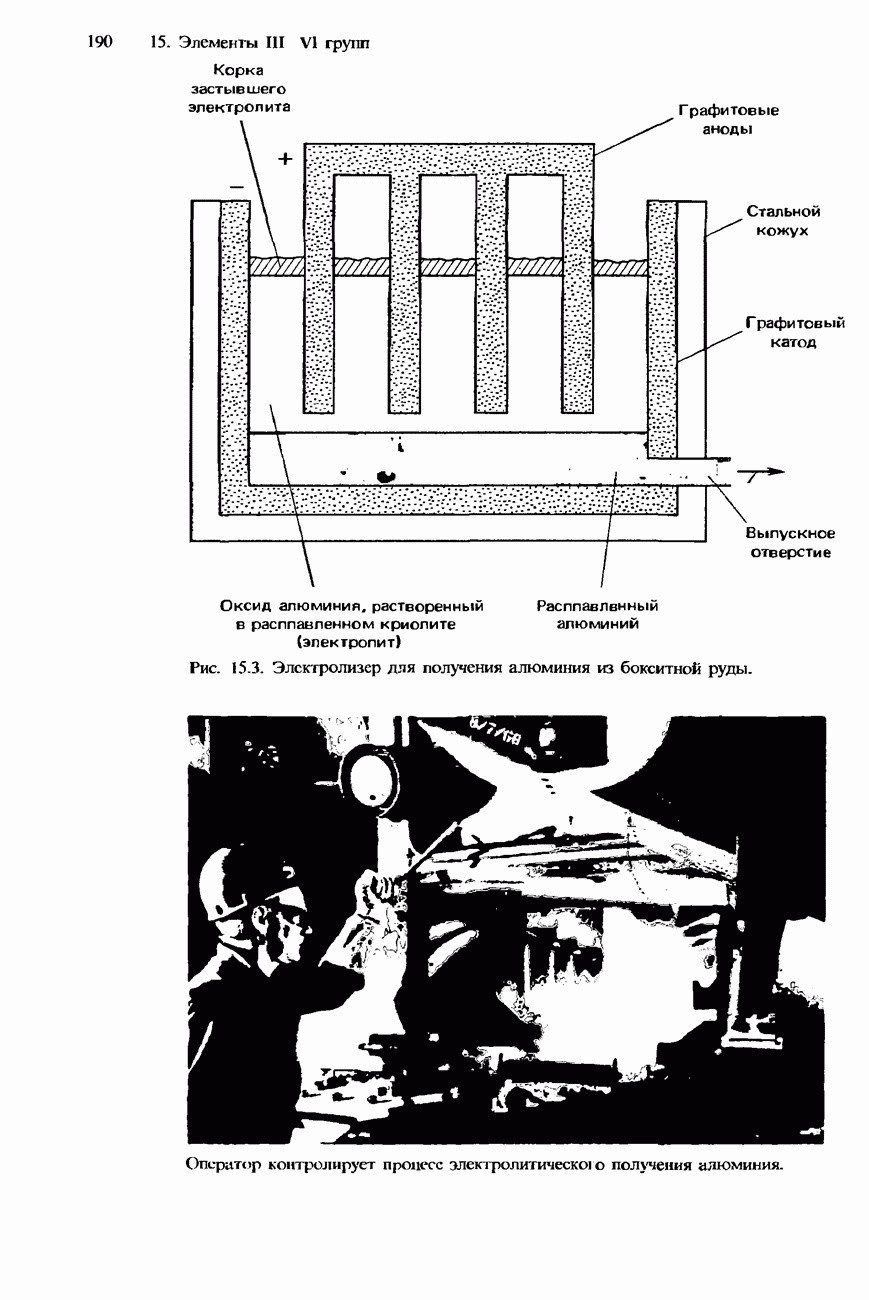
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
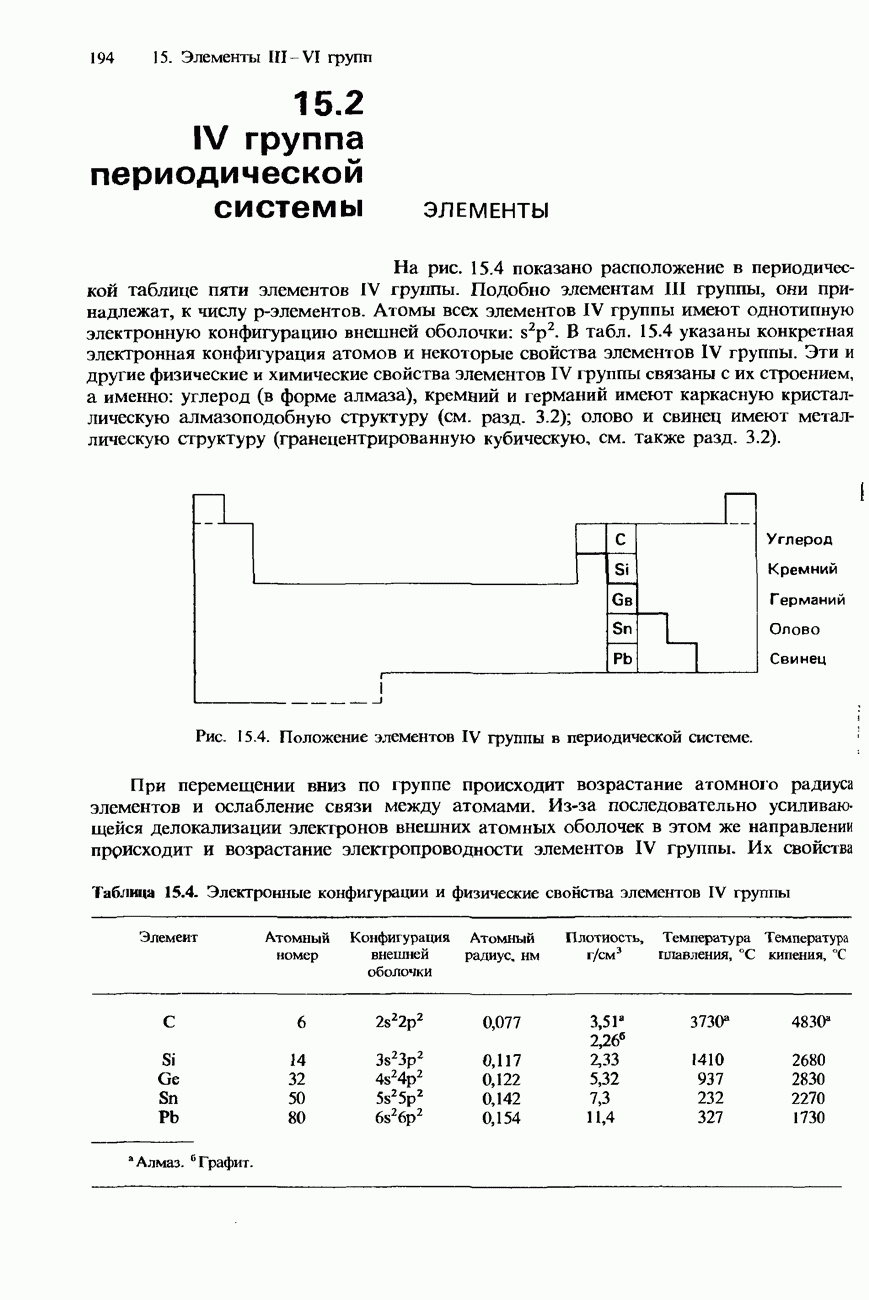
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
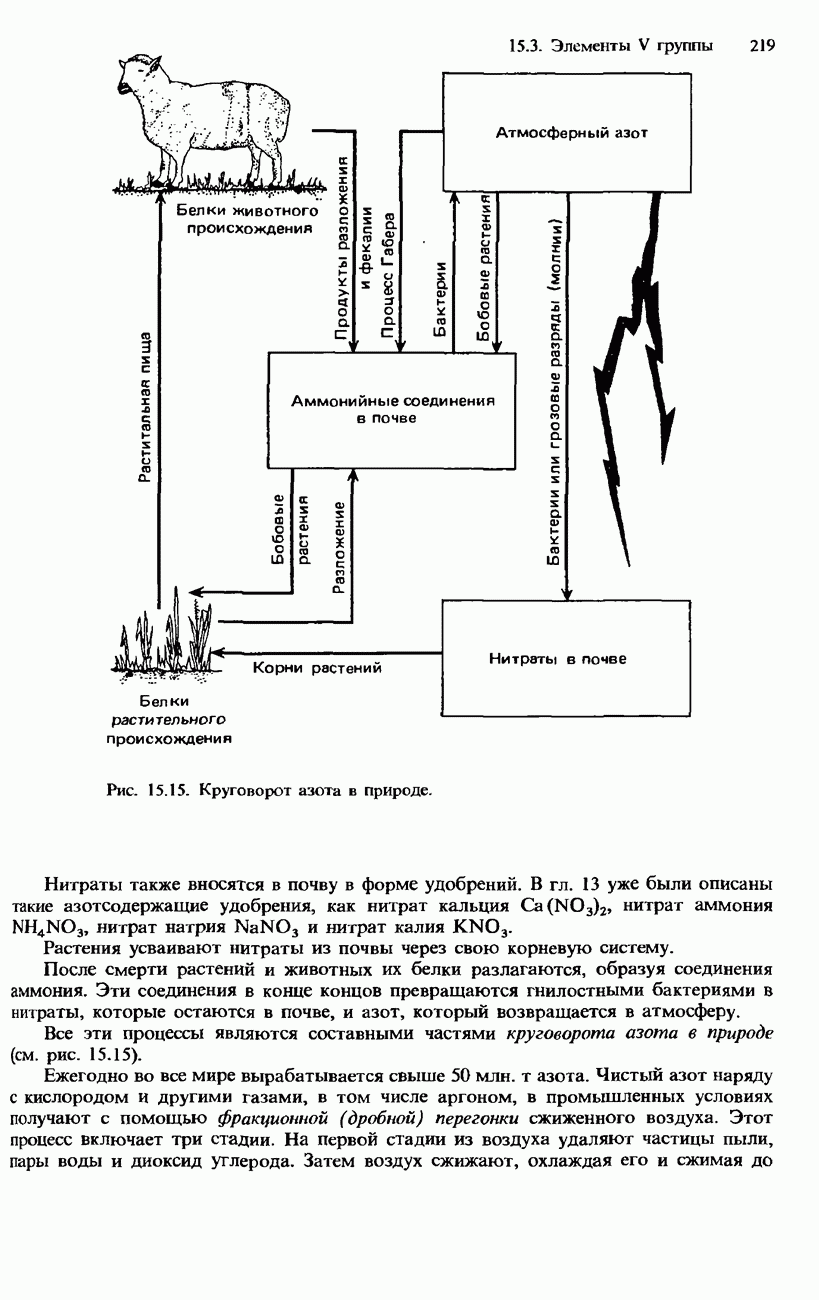
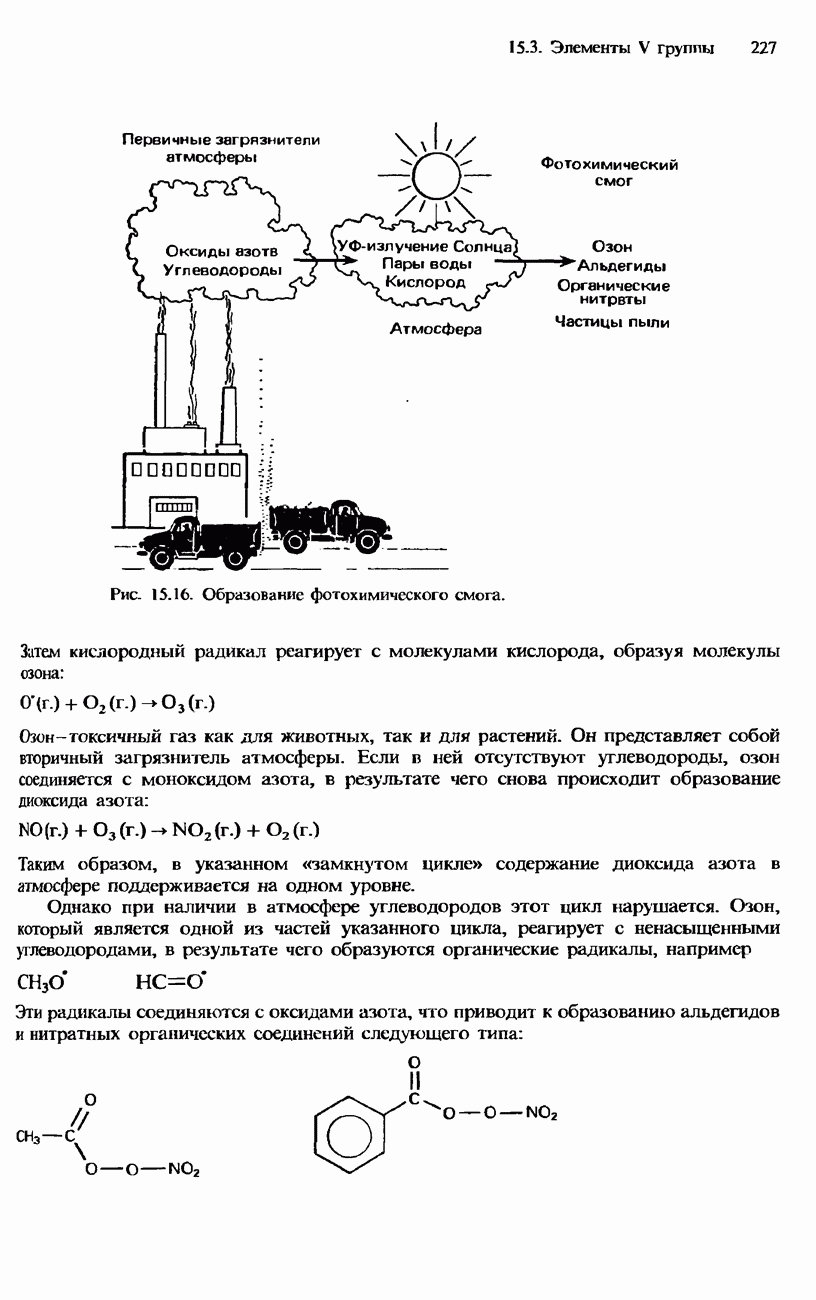
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
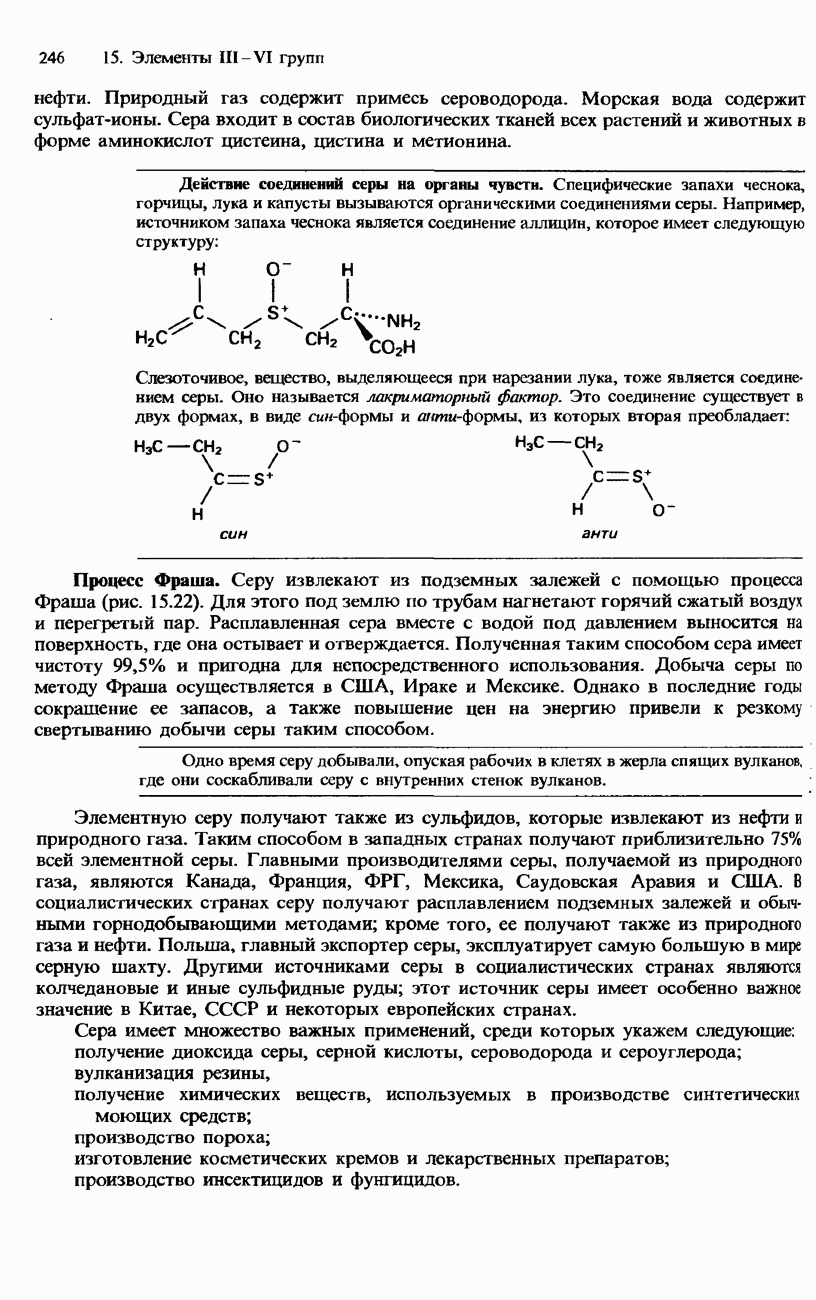
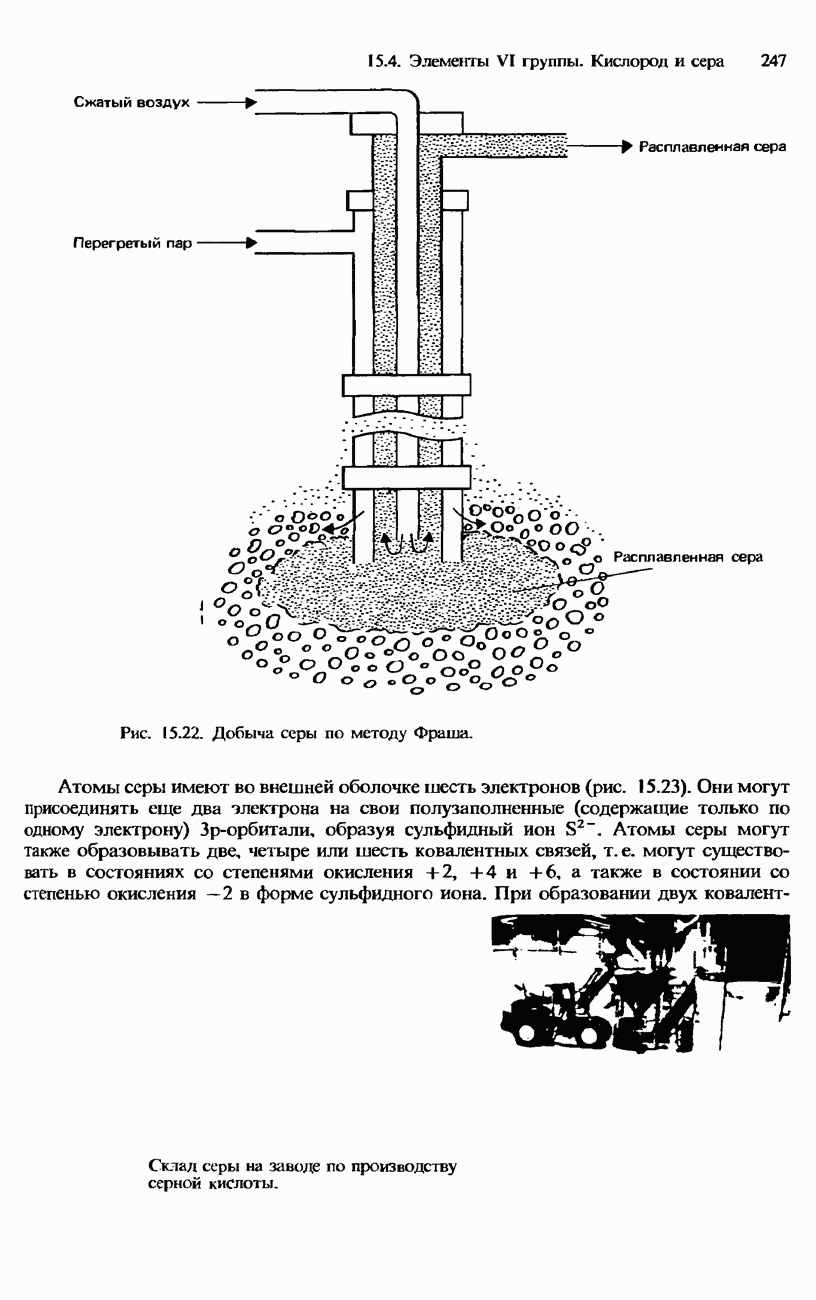
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
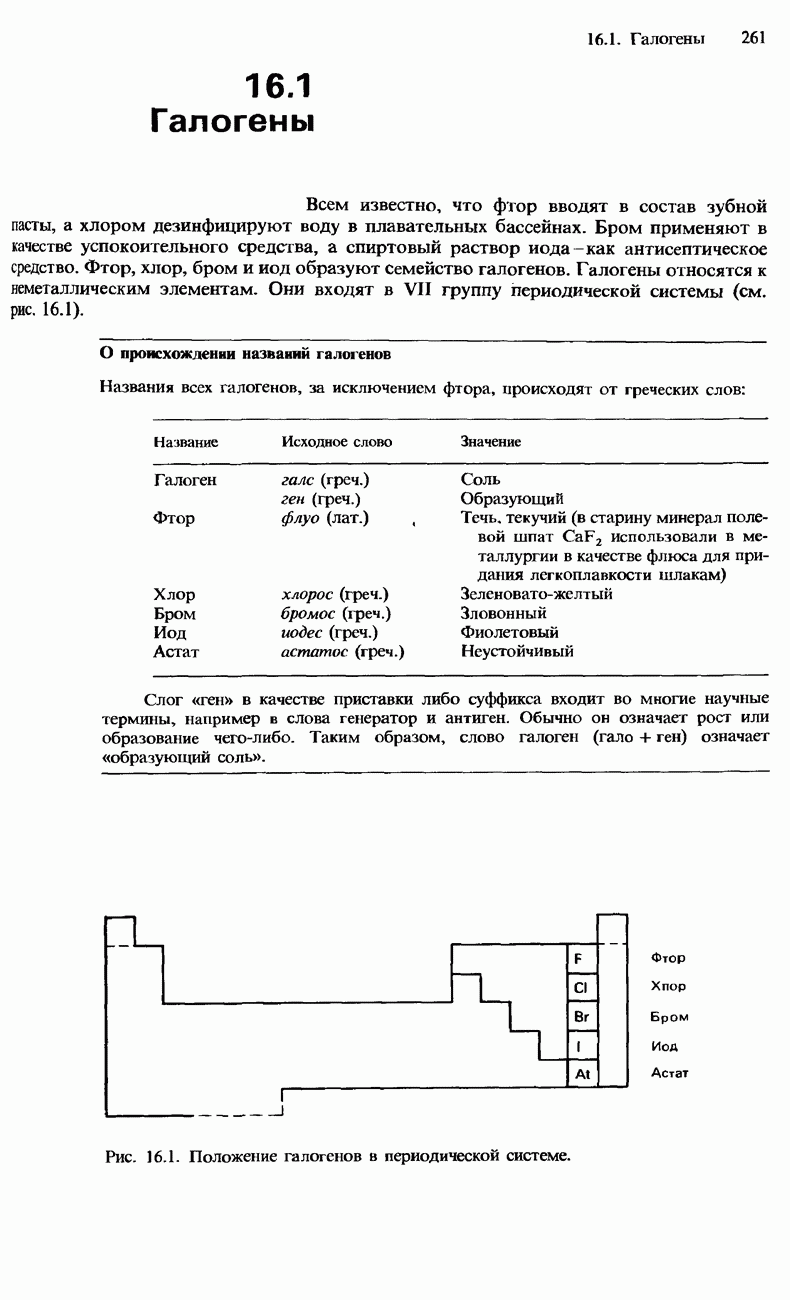
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
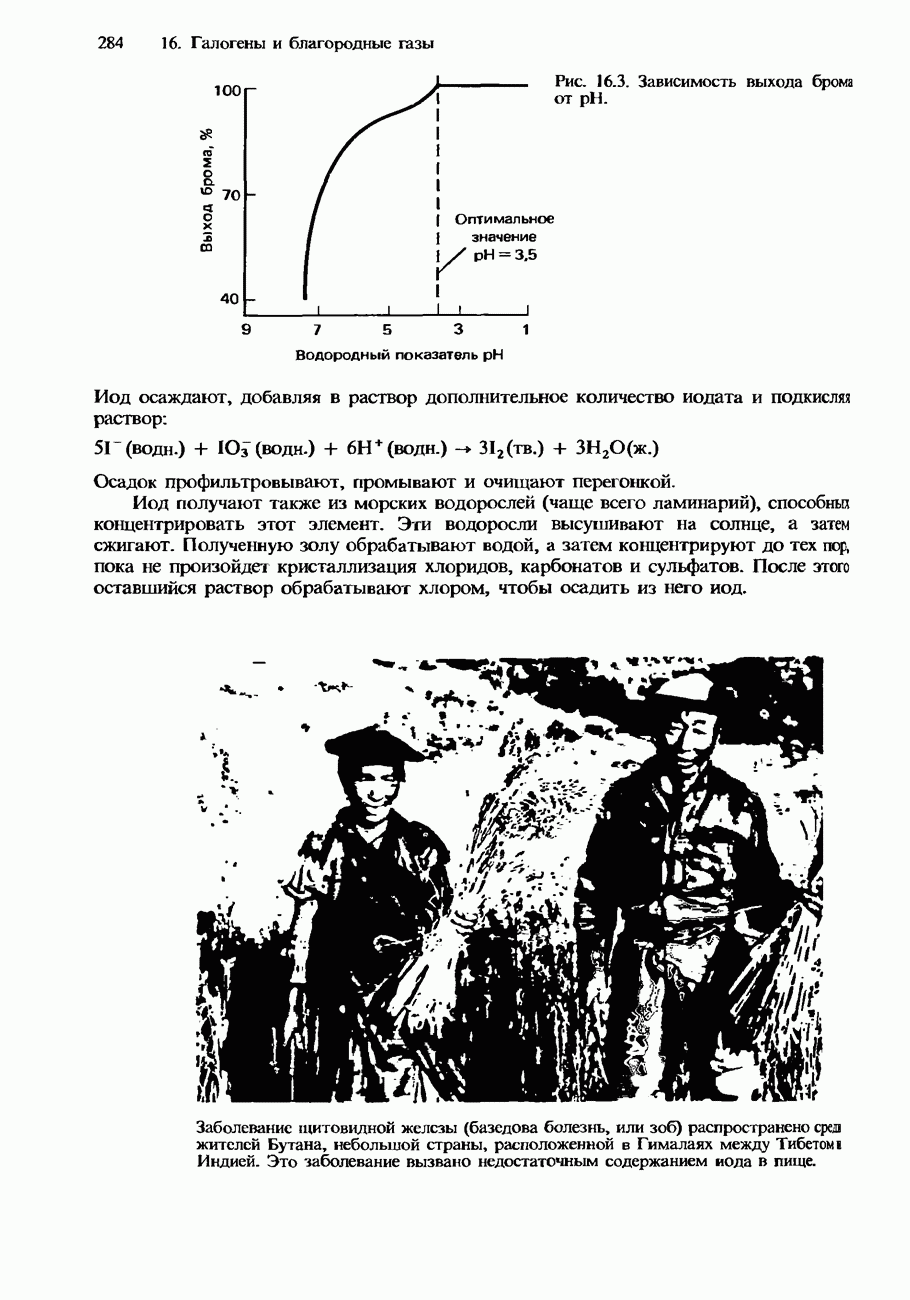
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
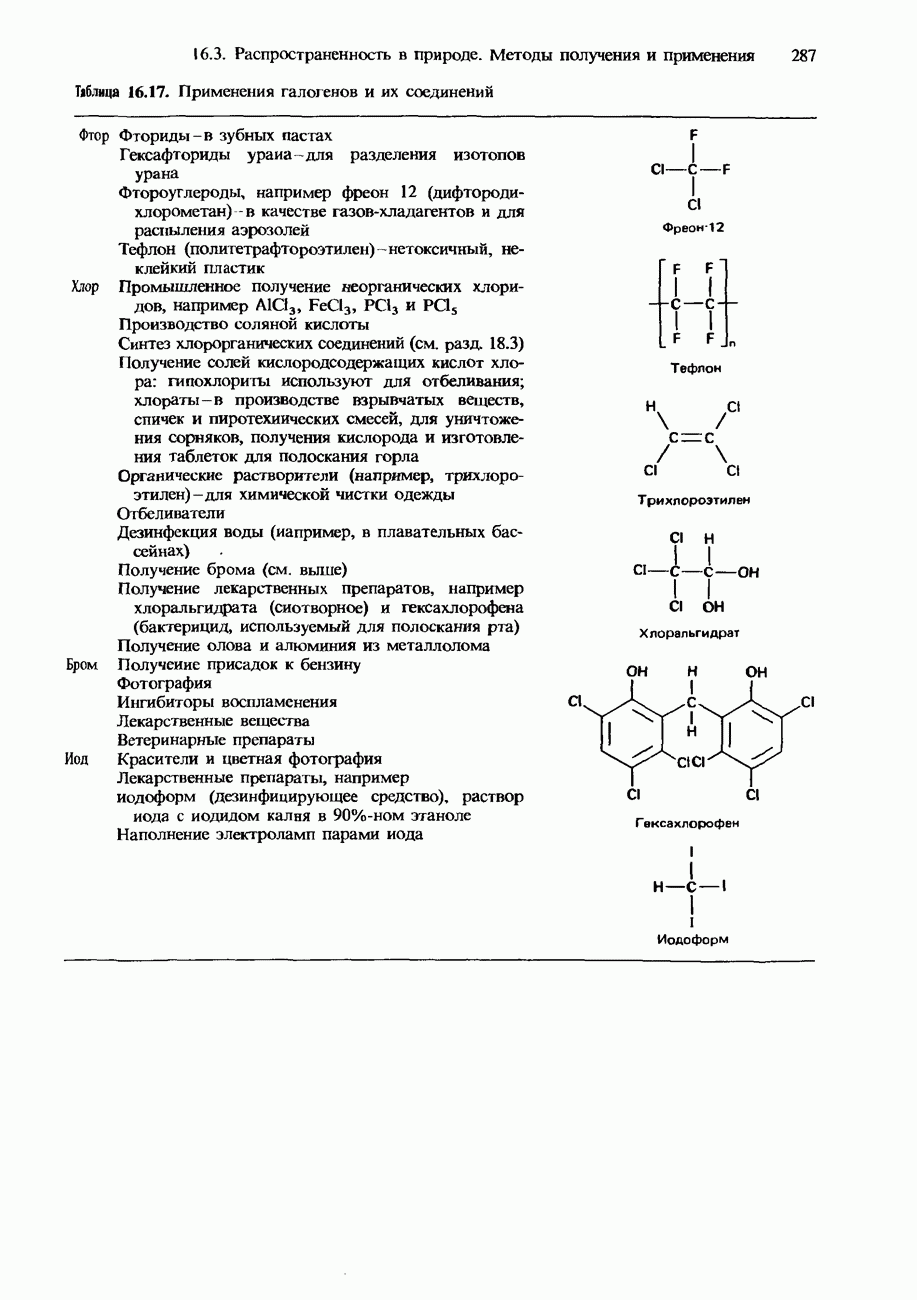
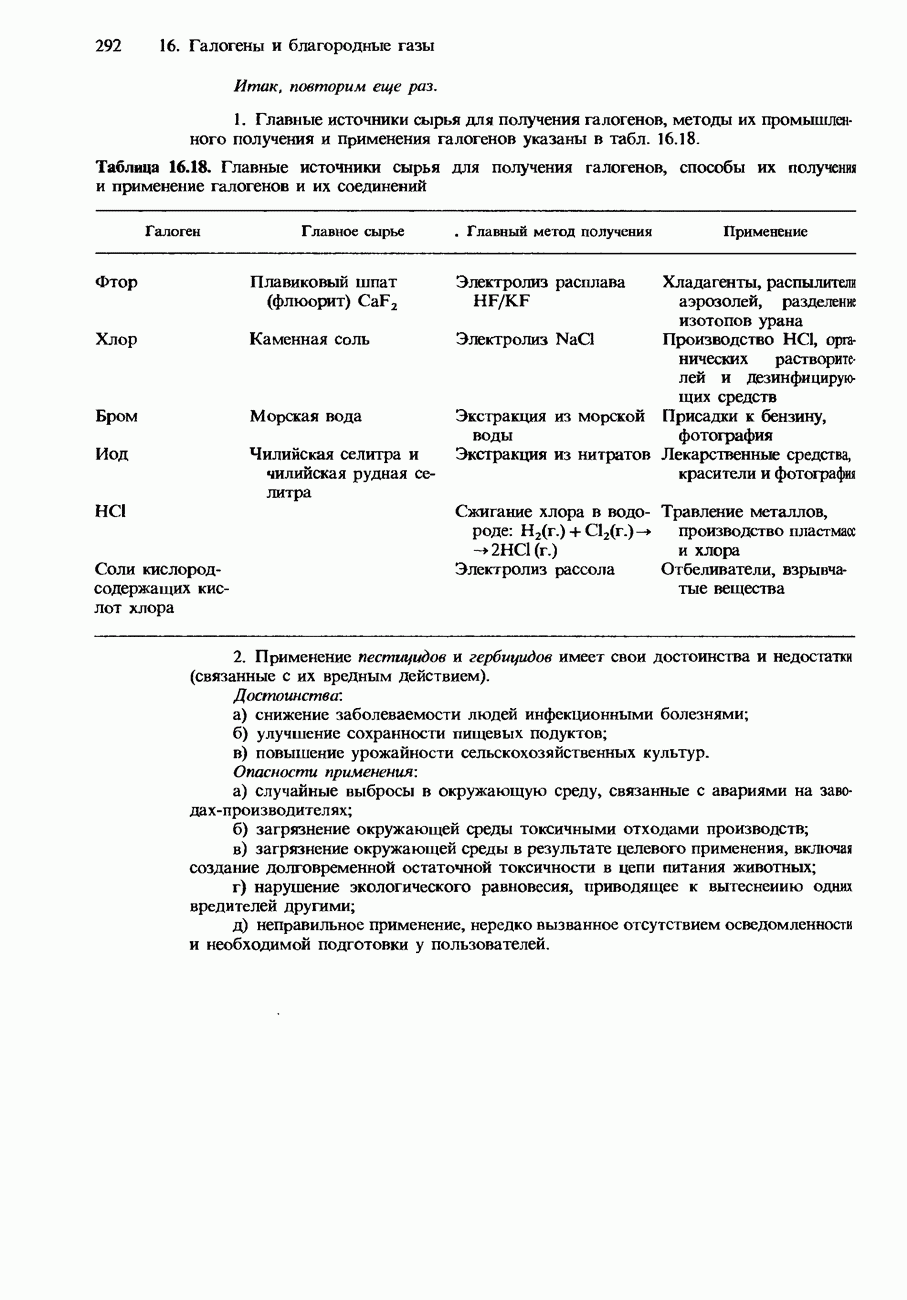
- 16.3. Распространенность, получение и применение галогенов и их соединений
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
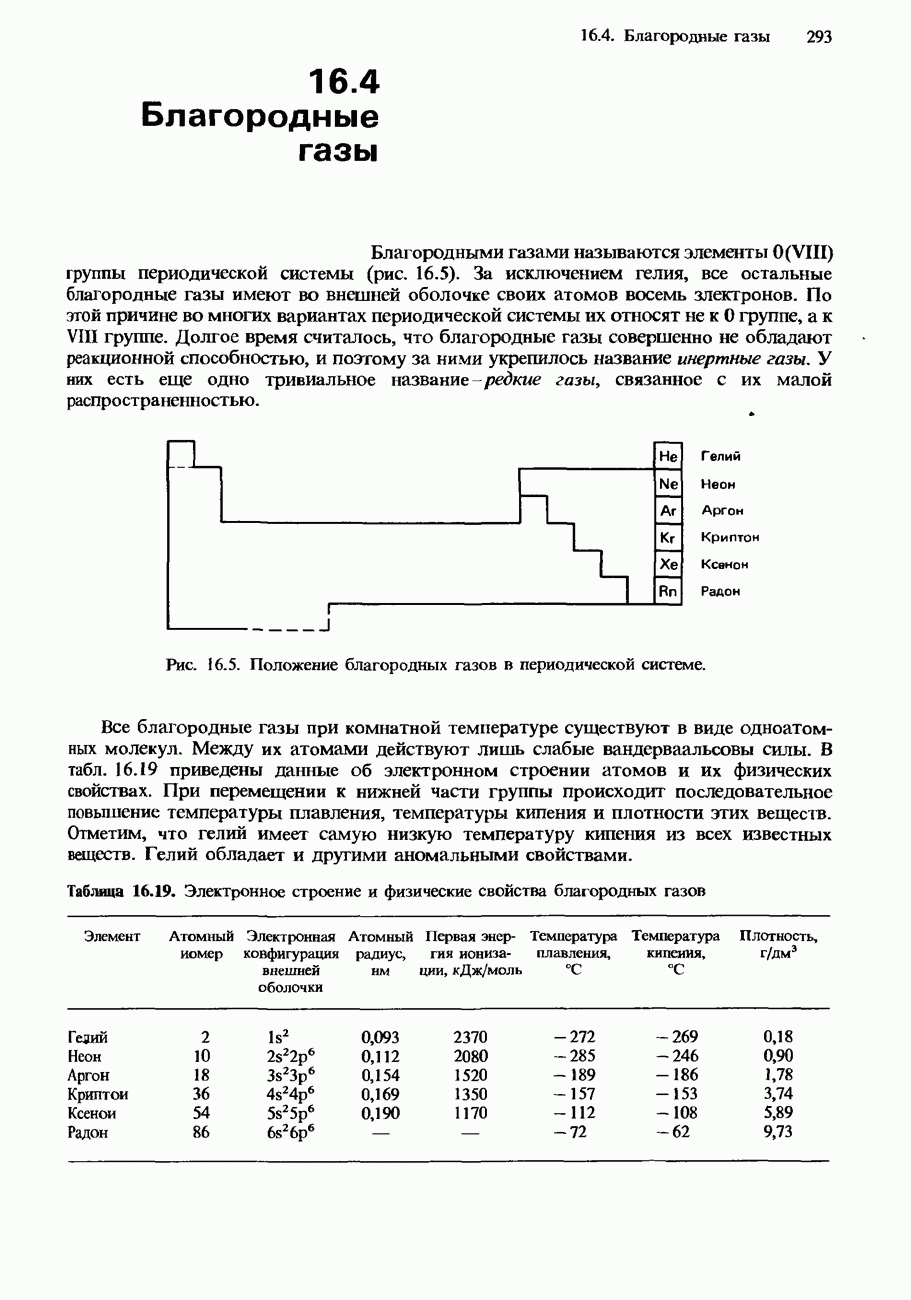
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
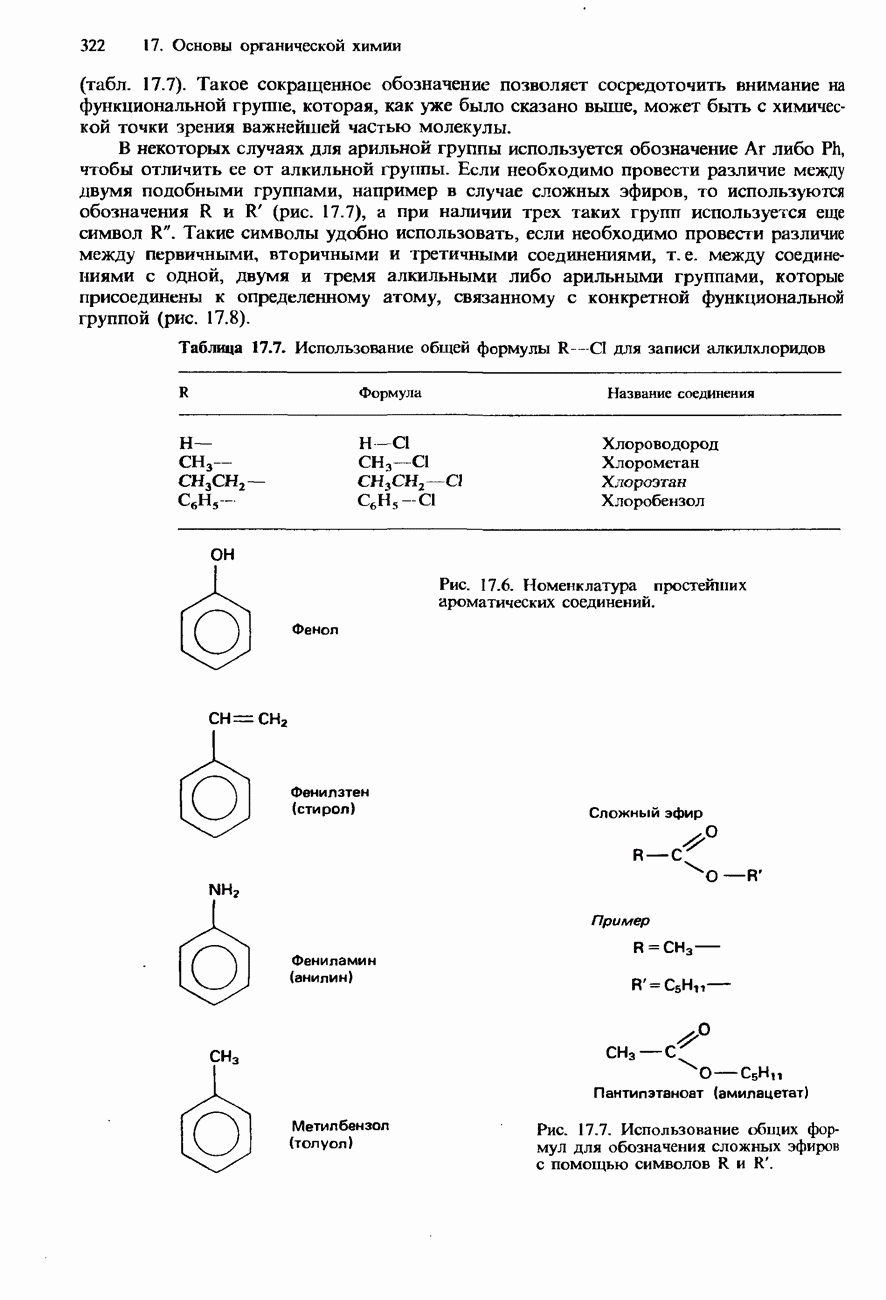
- 7.1. Органическая химия
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
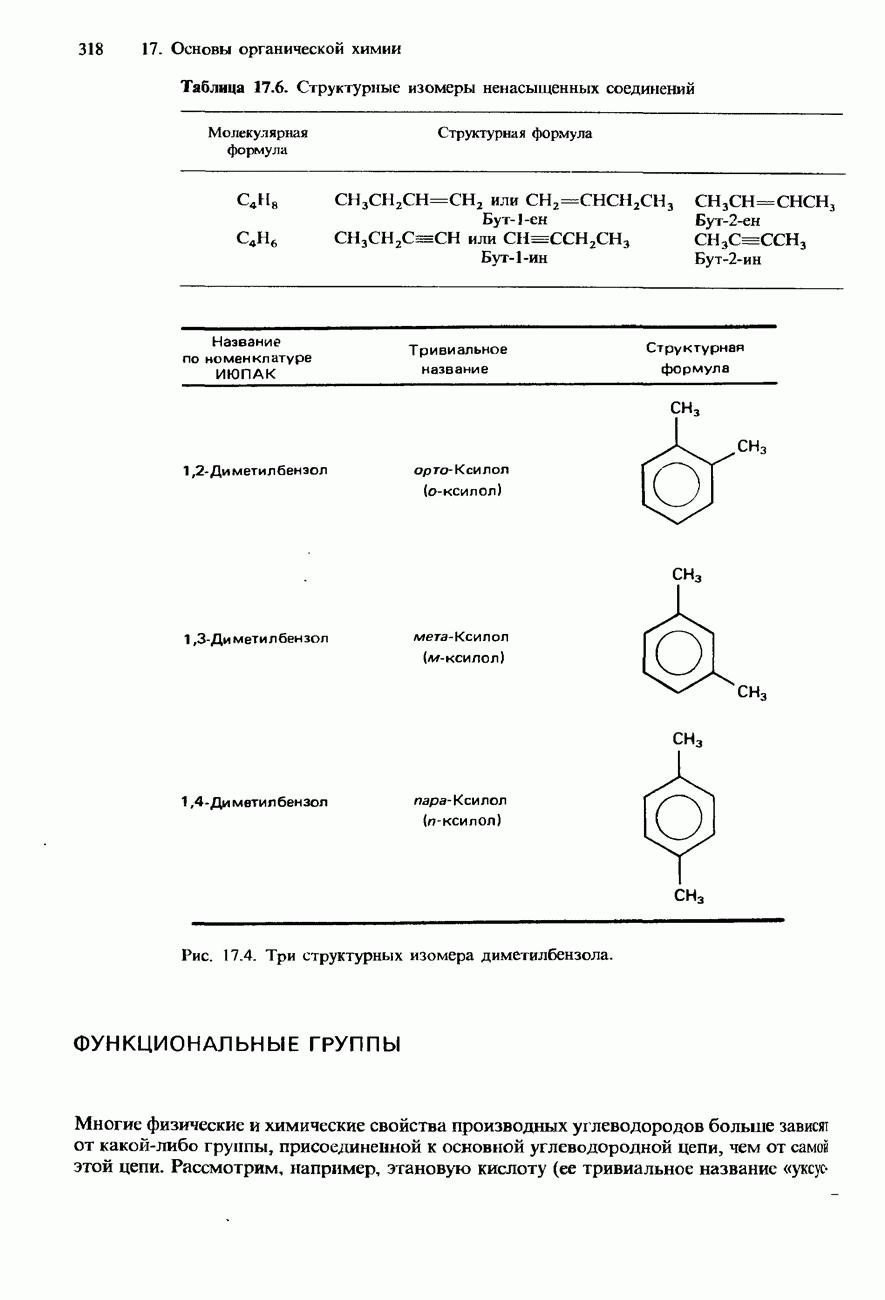
- УГЛЕВОДОРОДЫ
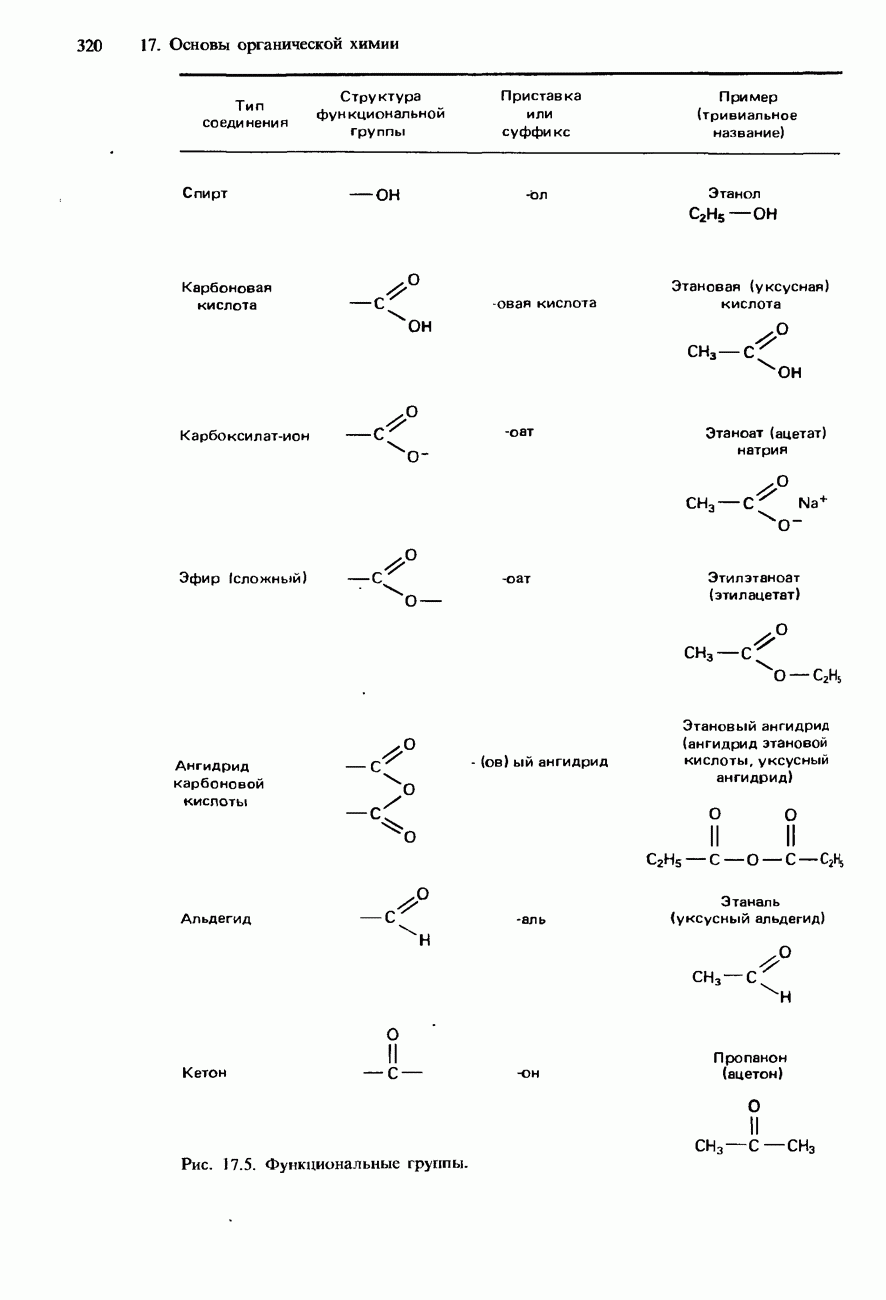
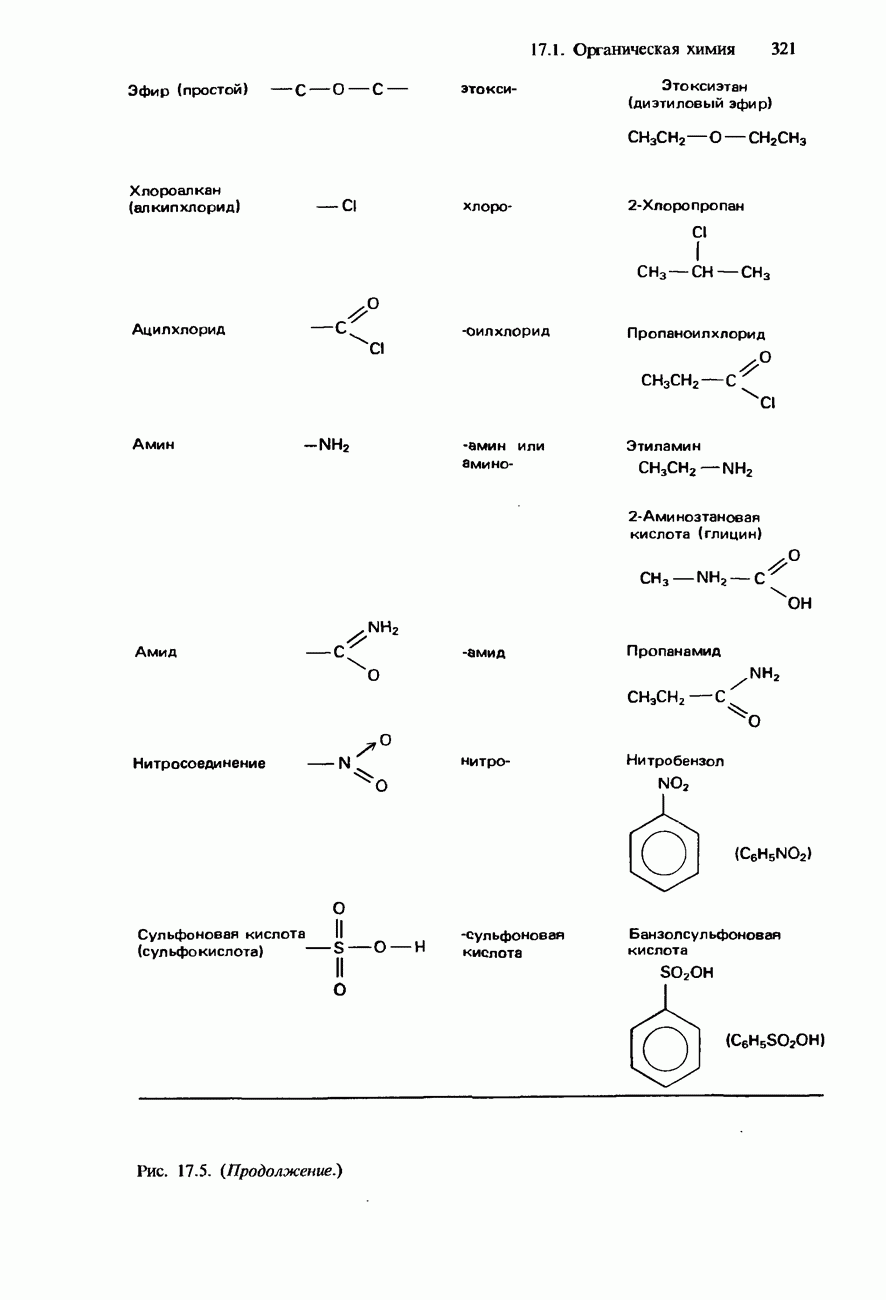
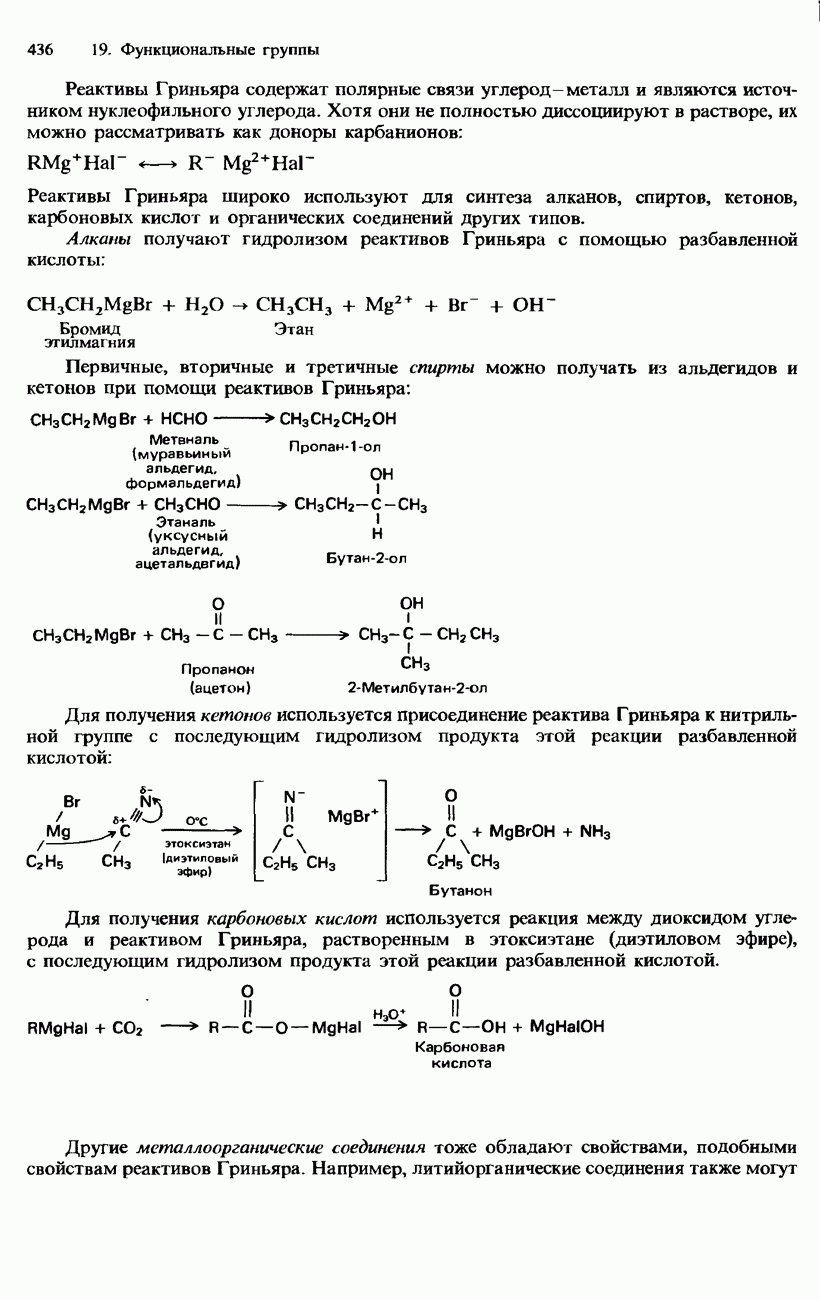
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
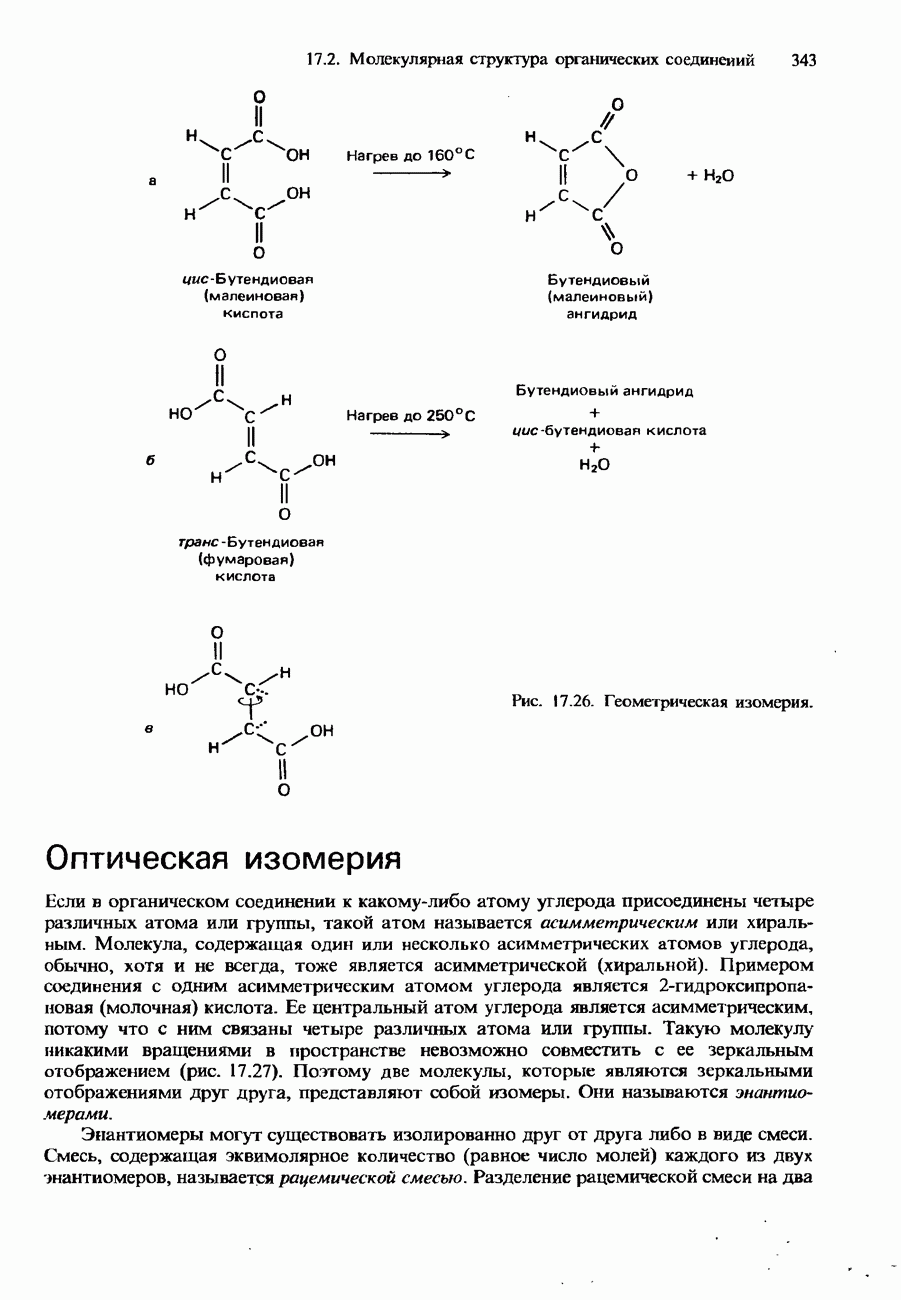
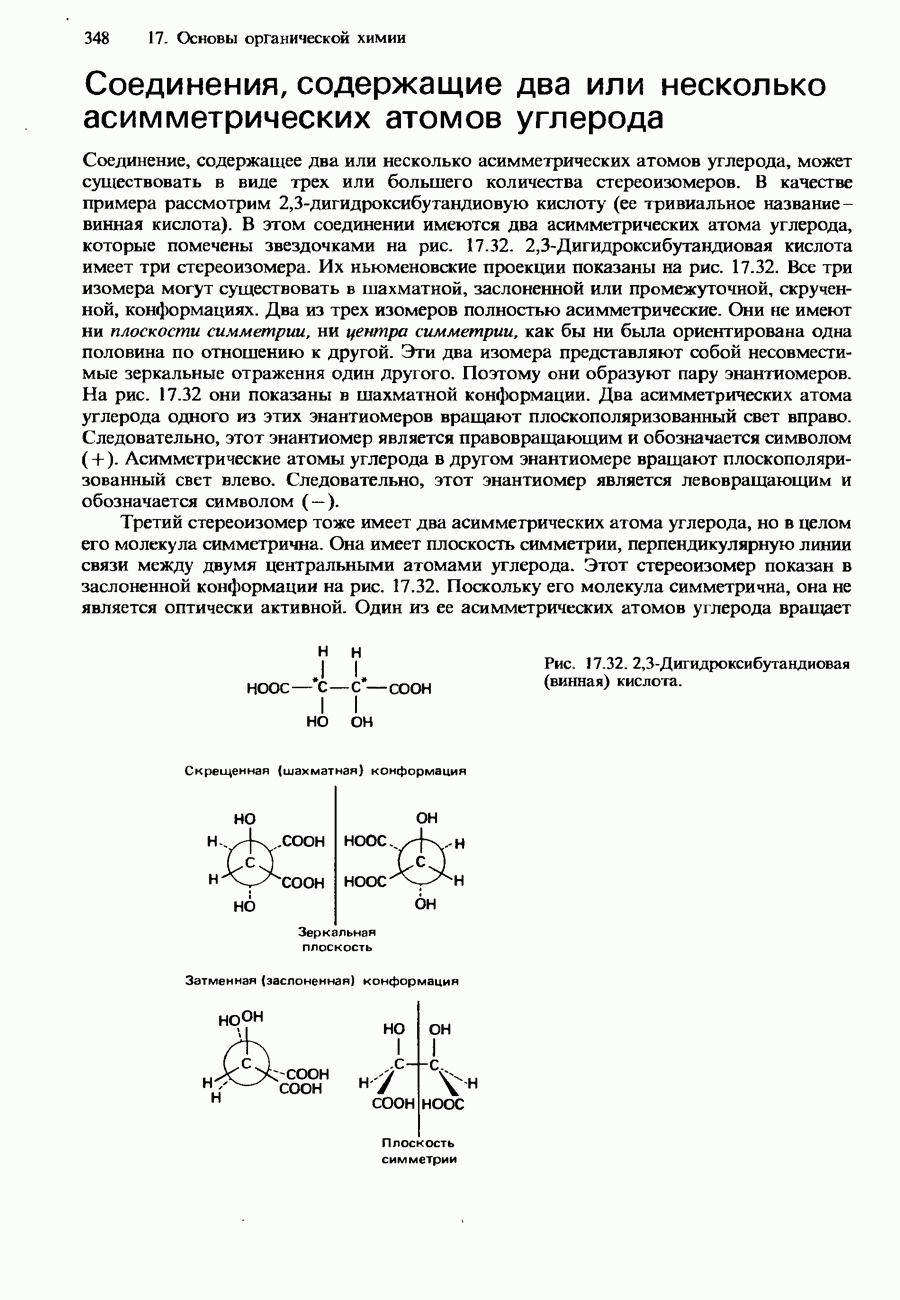
- СТЕРЕОИЗОМЕРИЯ
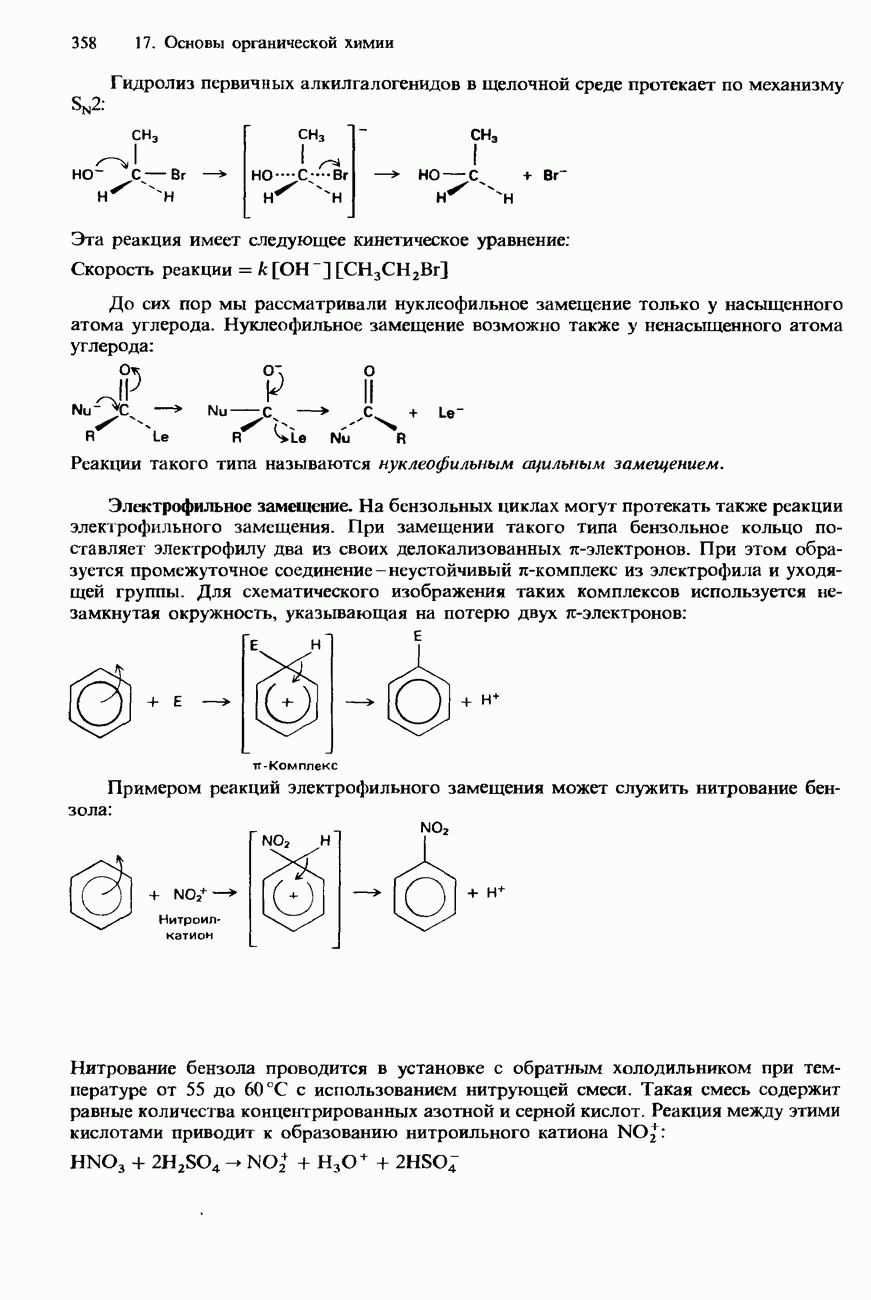
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
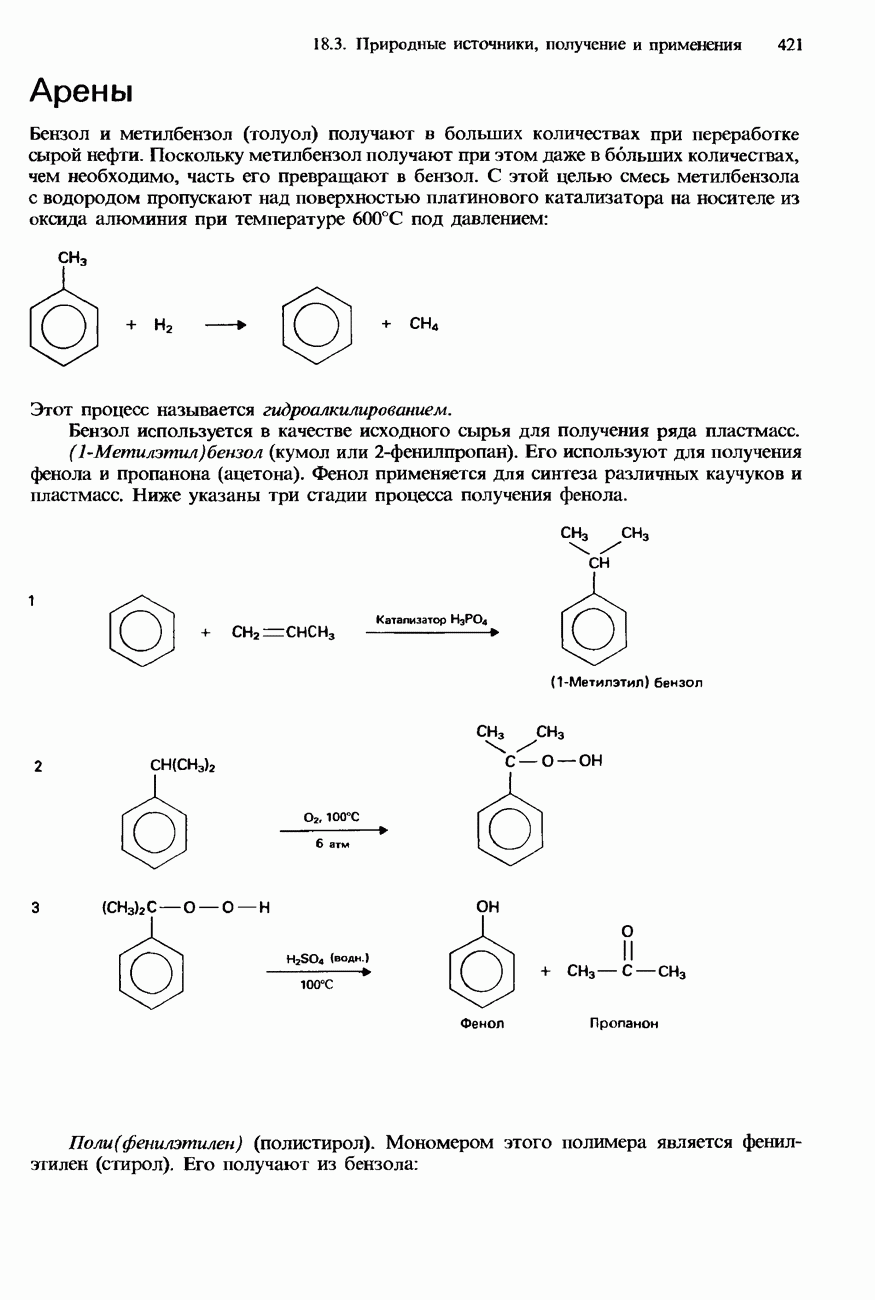
- 18.2. Арены
- БЕНЗОЛ
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
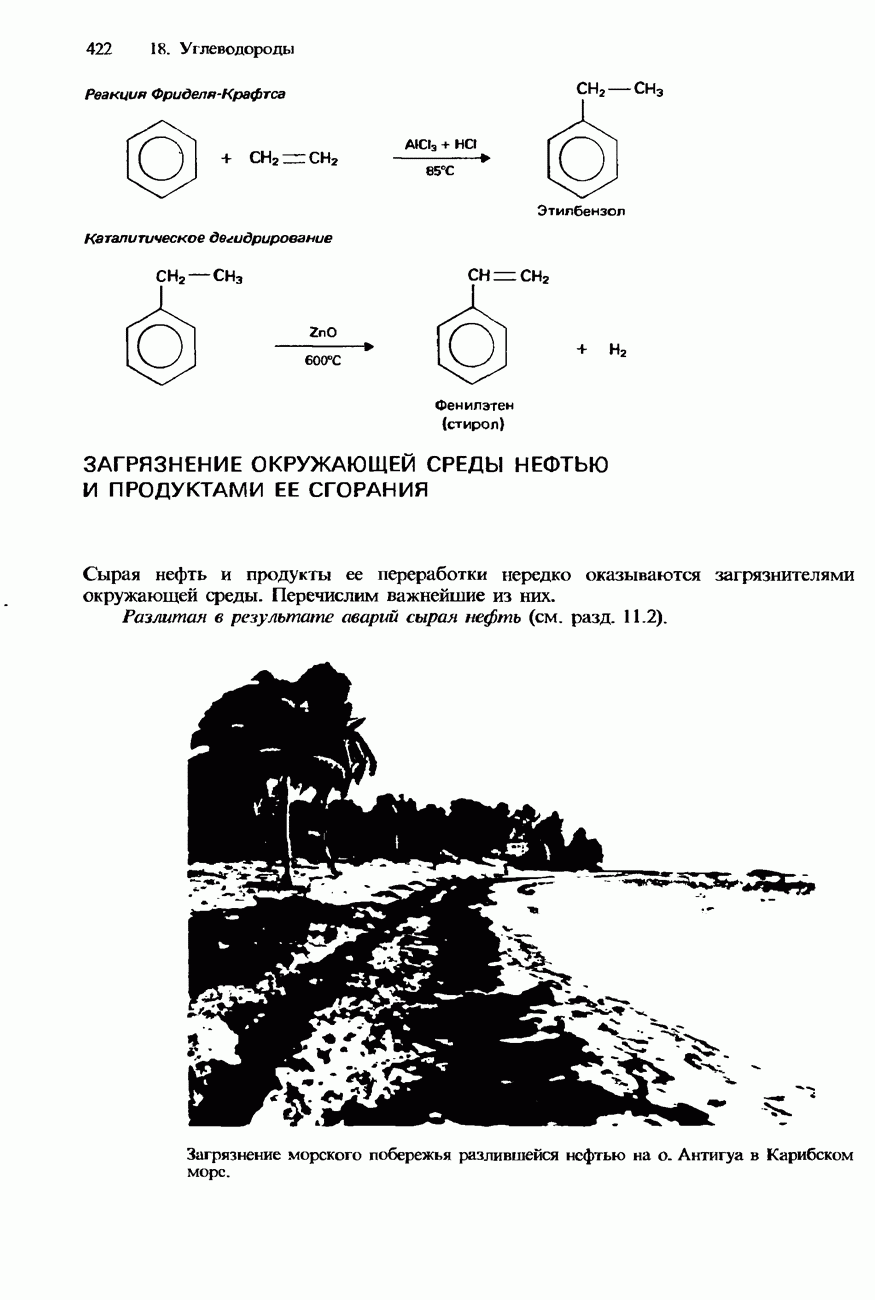
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
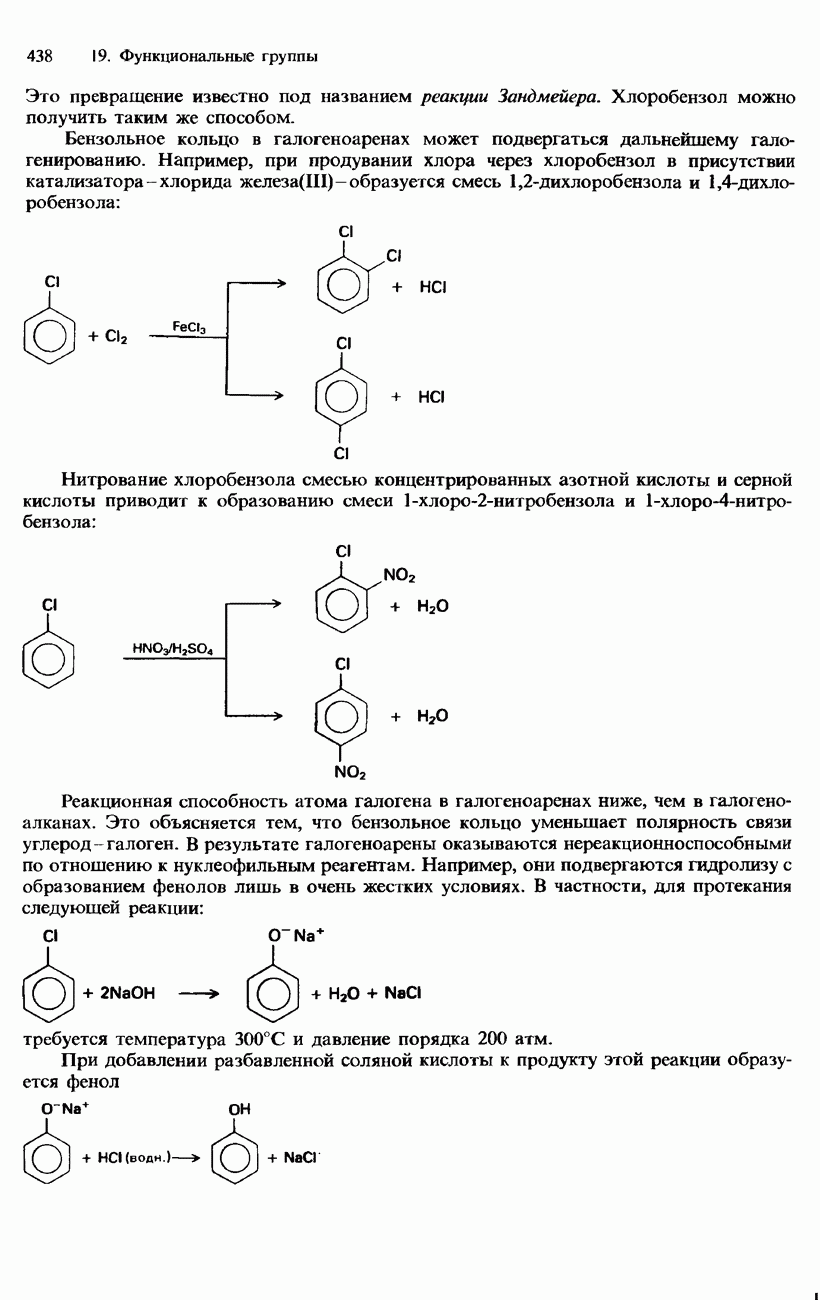
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
- 19.2. Спирты, фенолы и эфиры
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
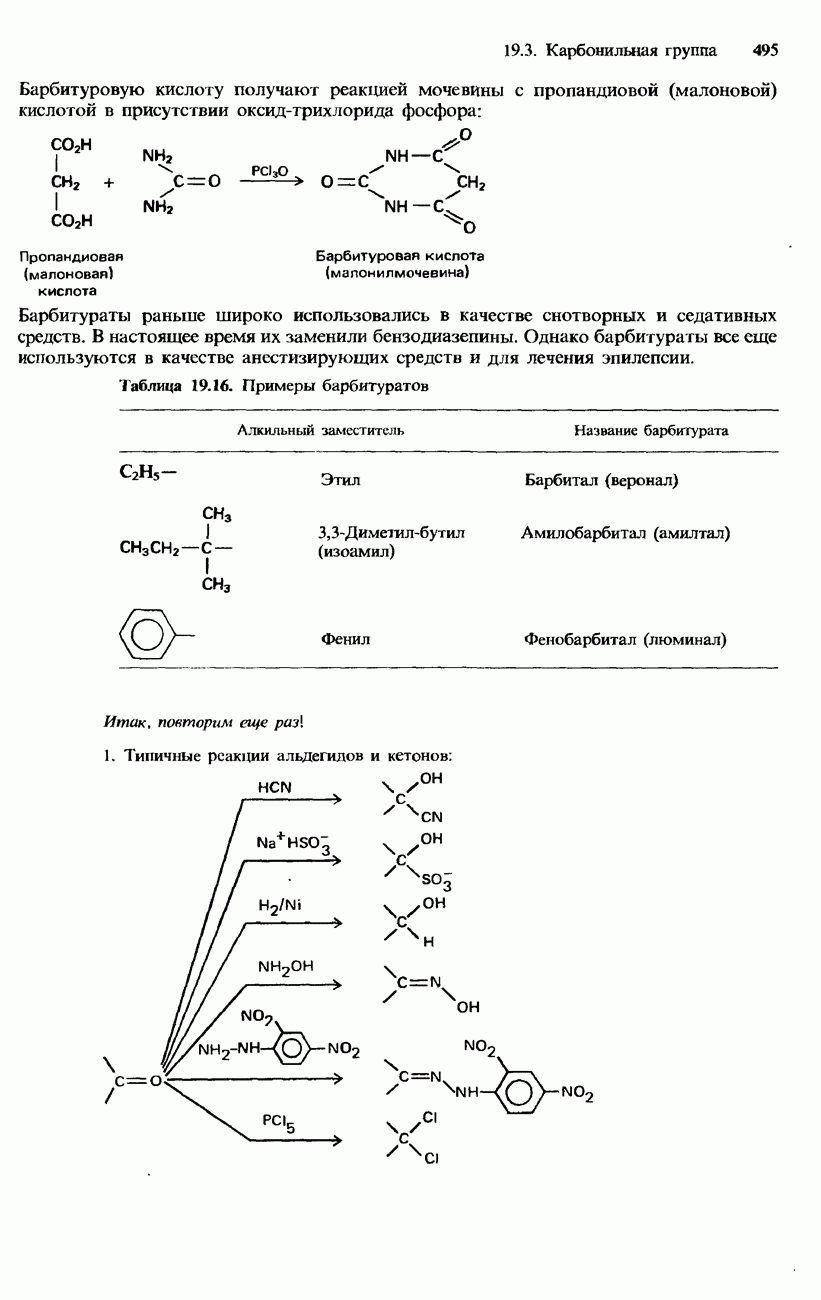
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
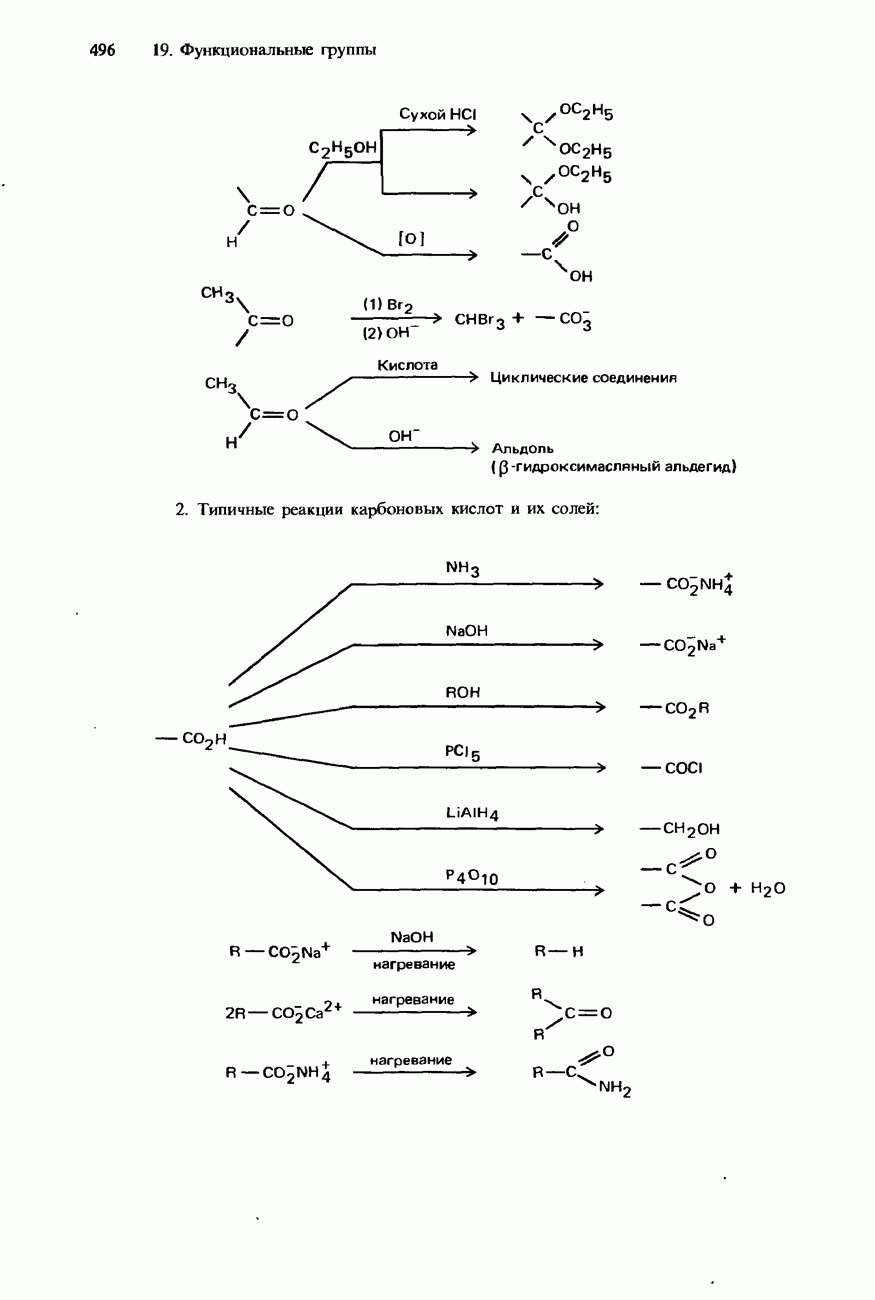
- КАРБОНОВЫЕ КИСЛОТЫ
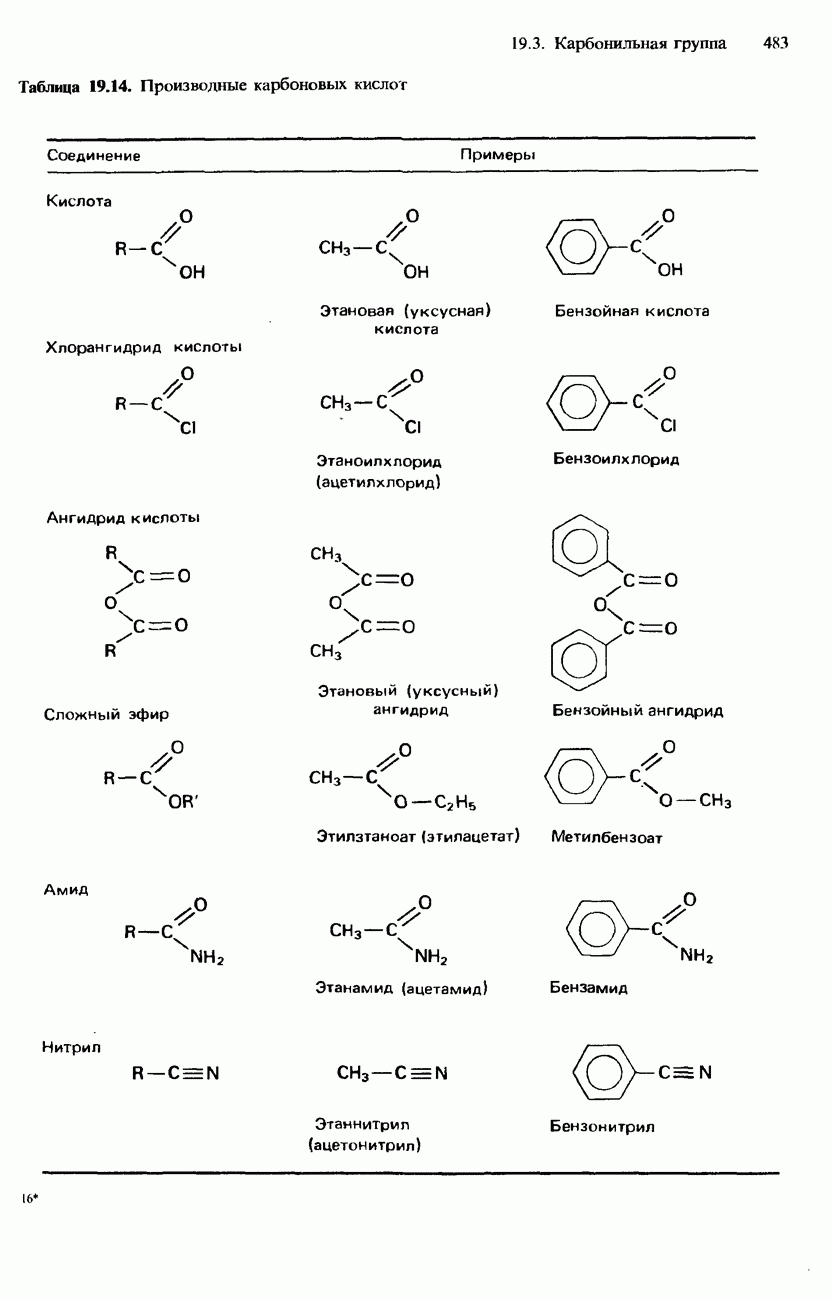
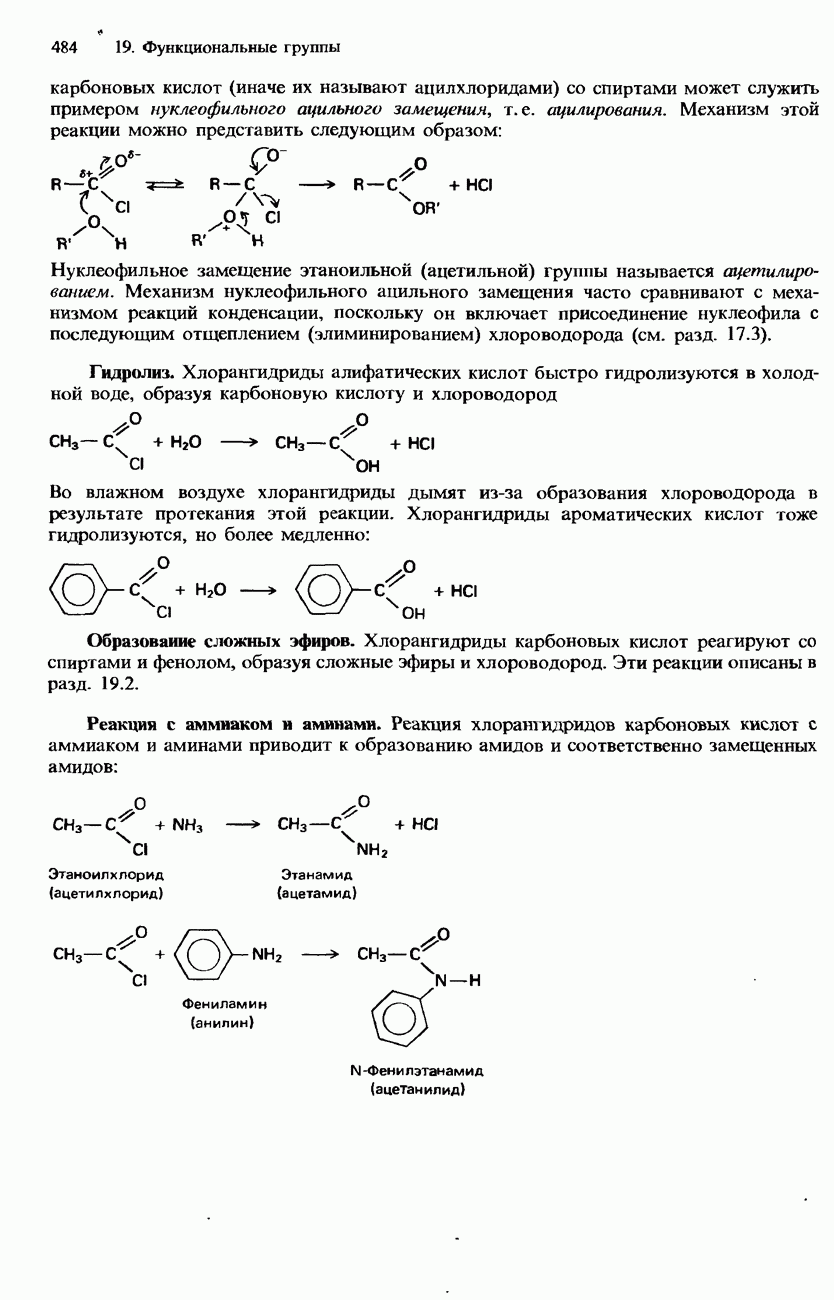
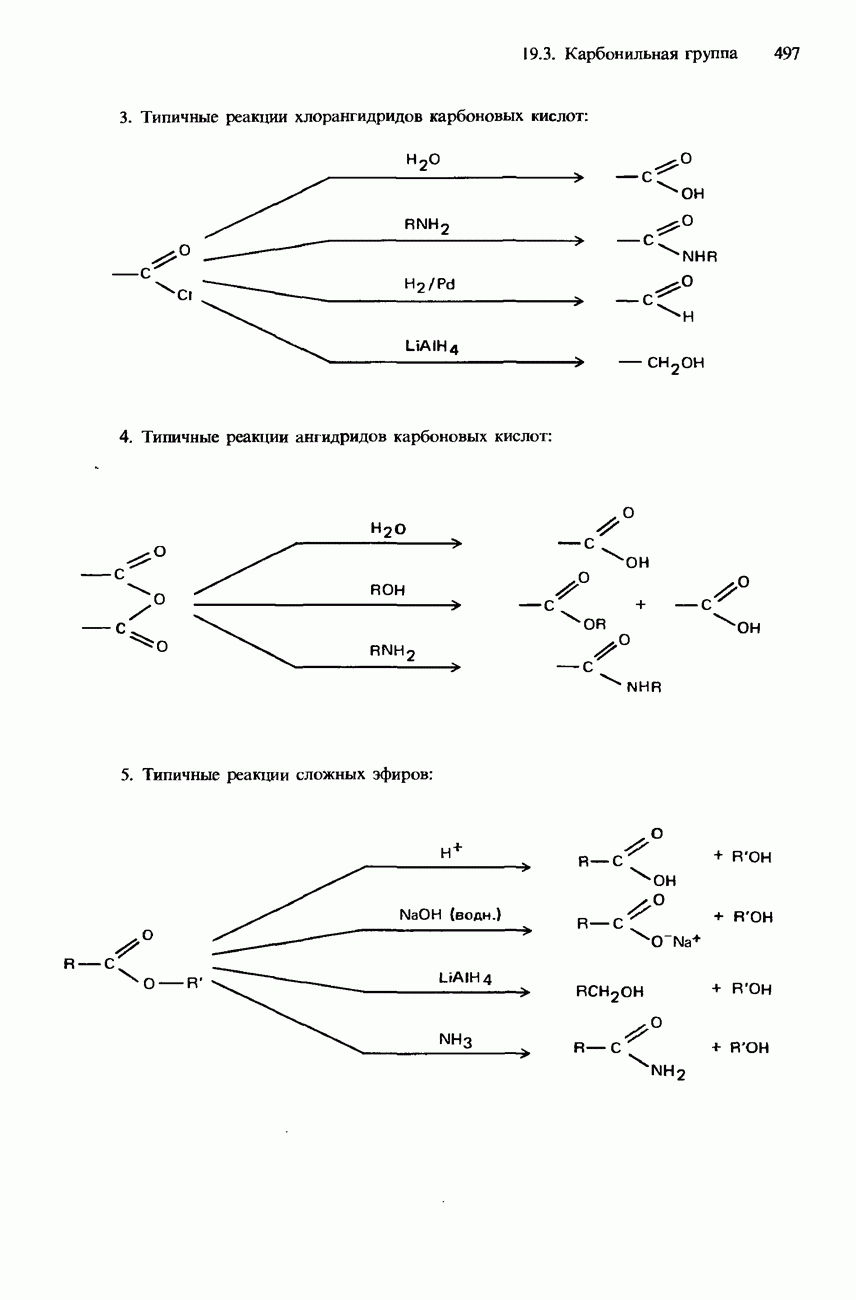
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
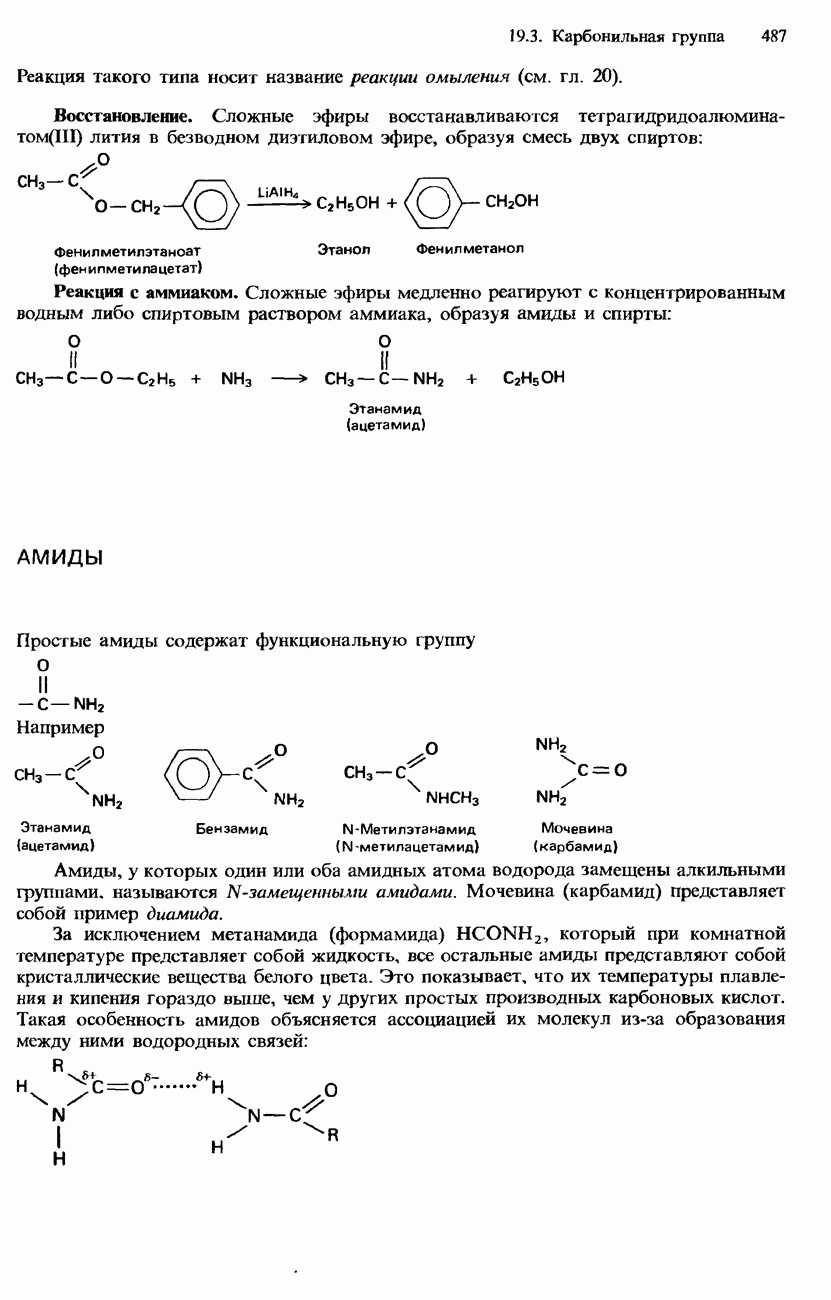
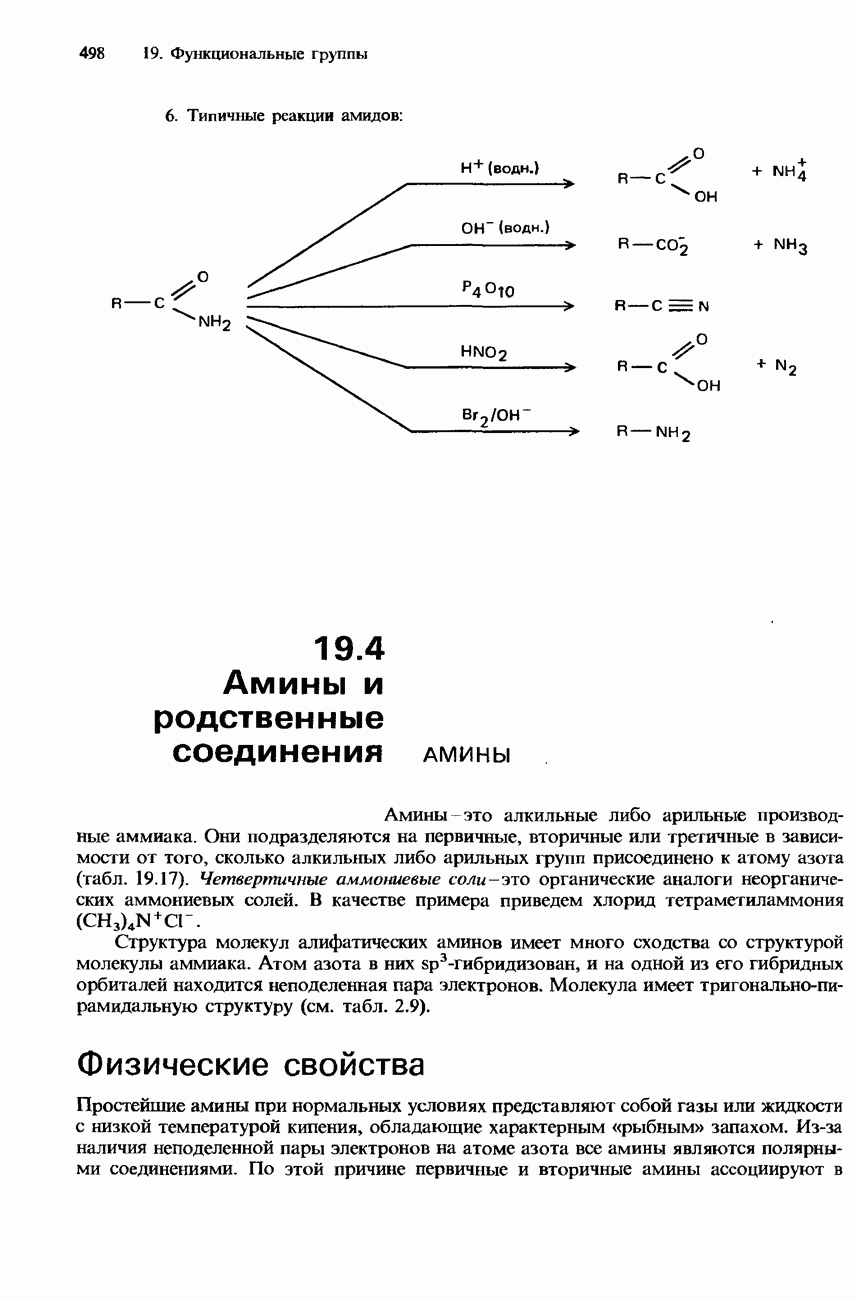
- АМИДЫ
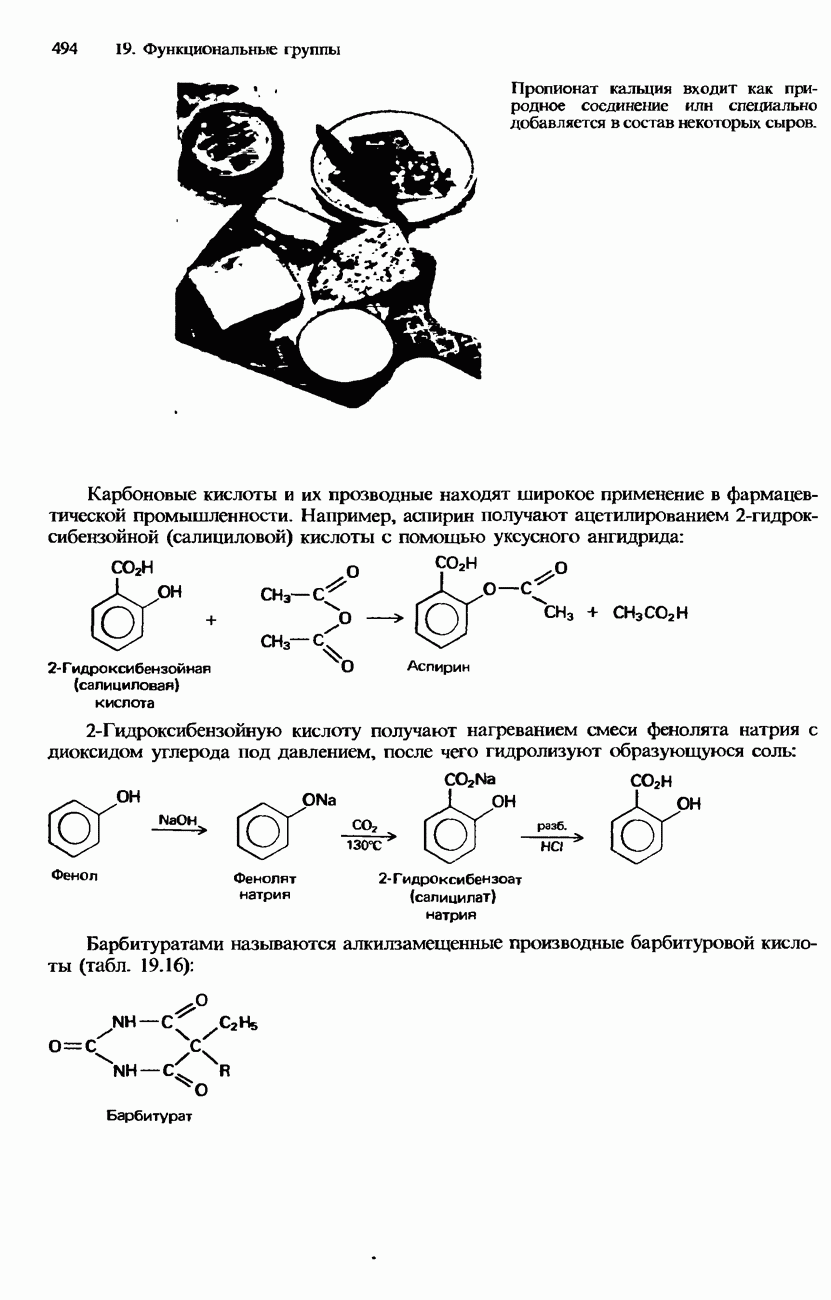
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
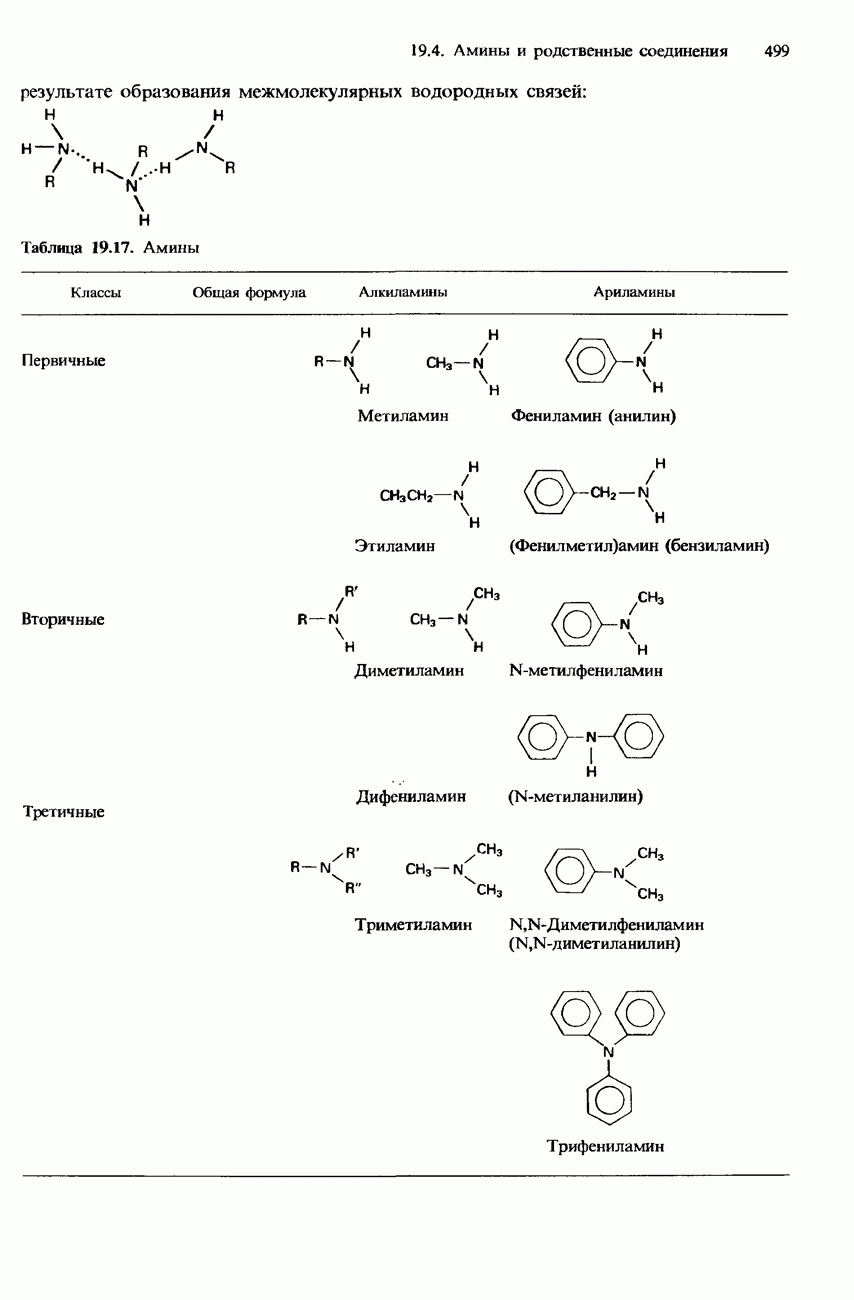
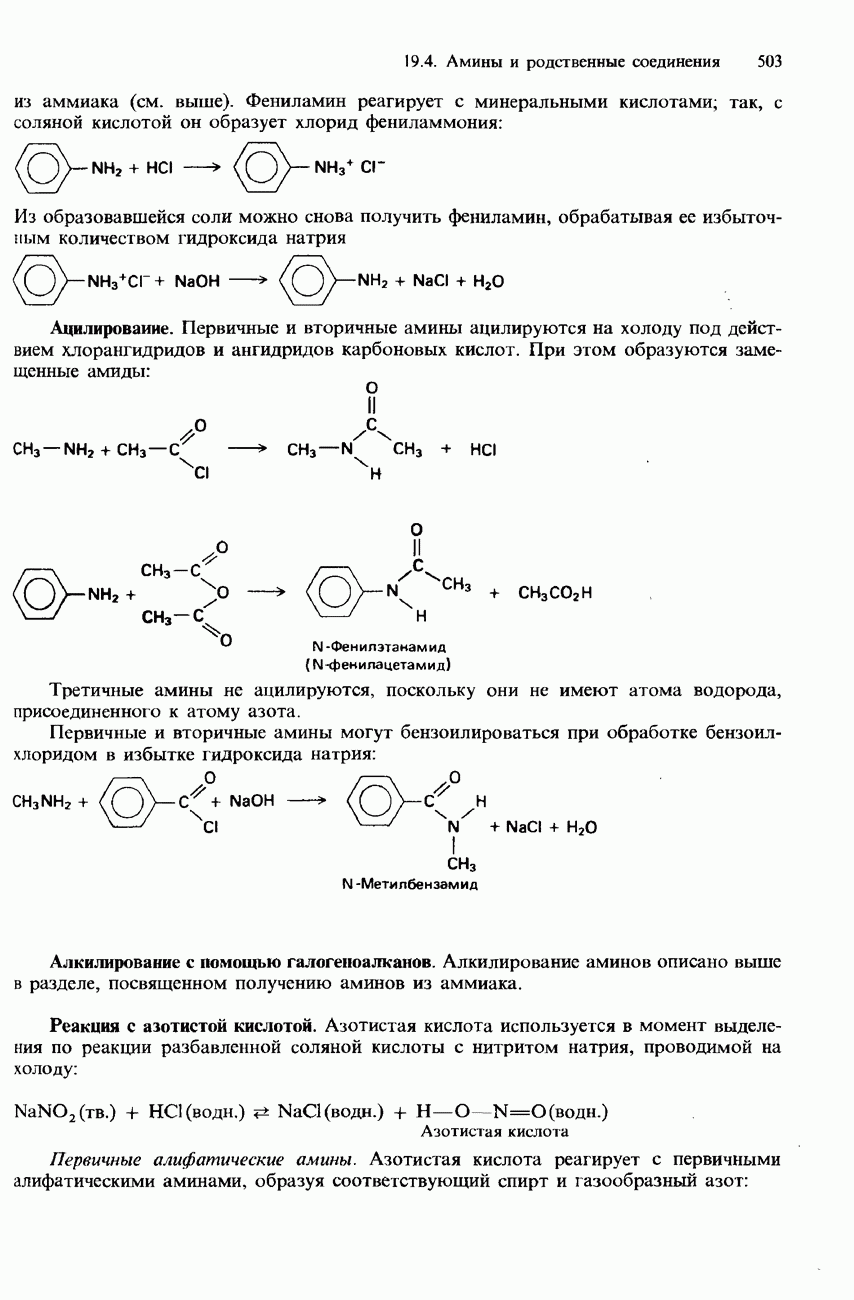
- 19.4 Амины и родственные соединения
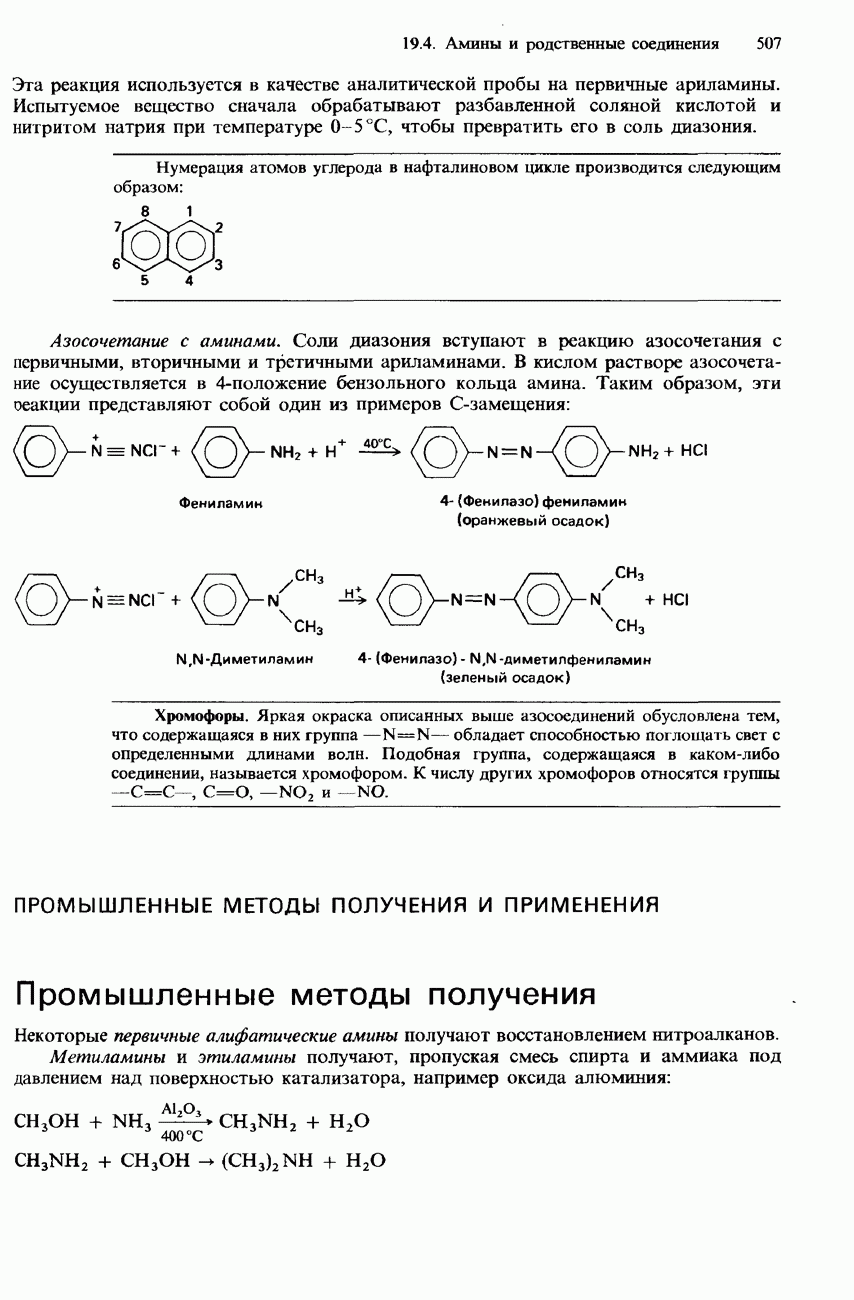
- СОЛИ ДИАЗОНИЯ
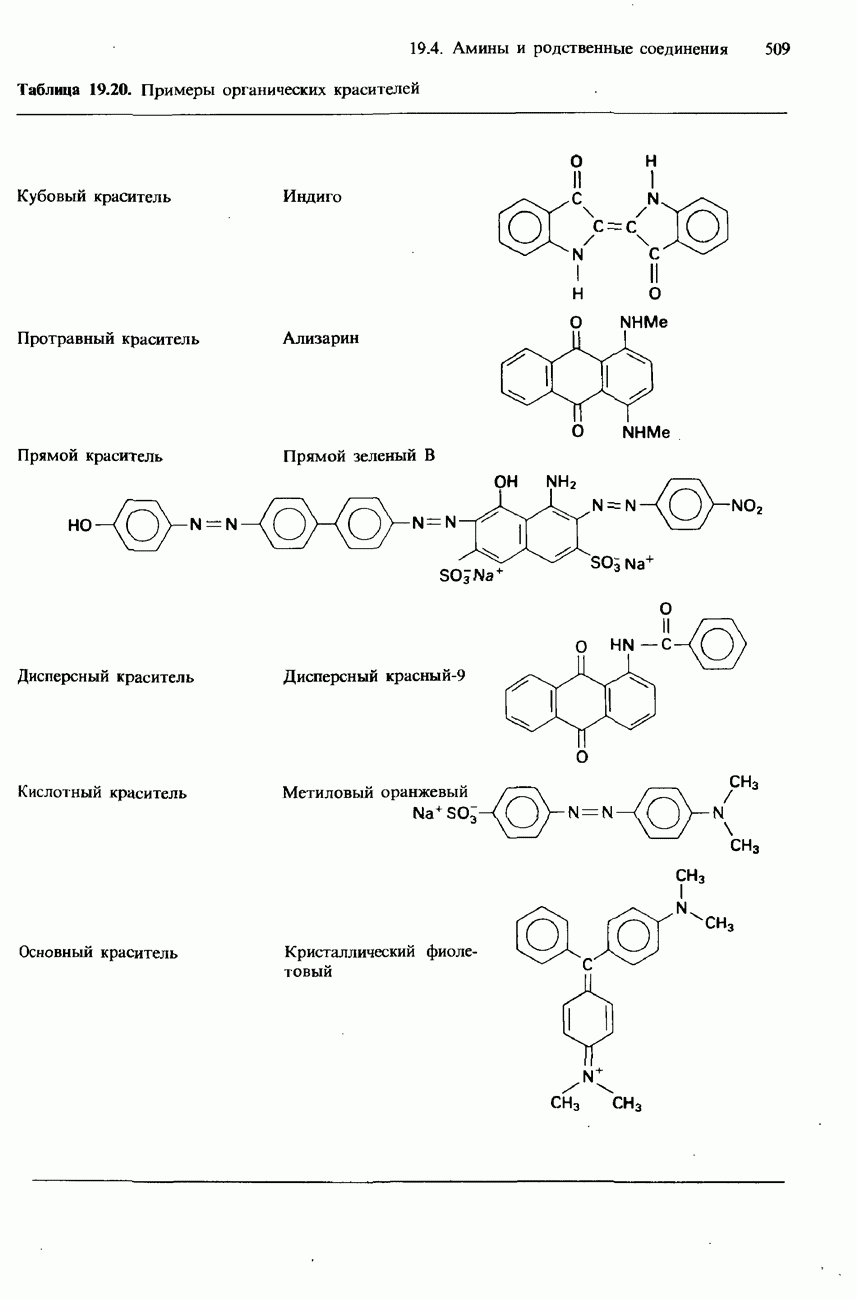
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
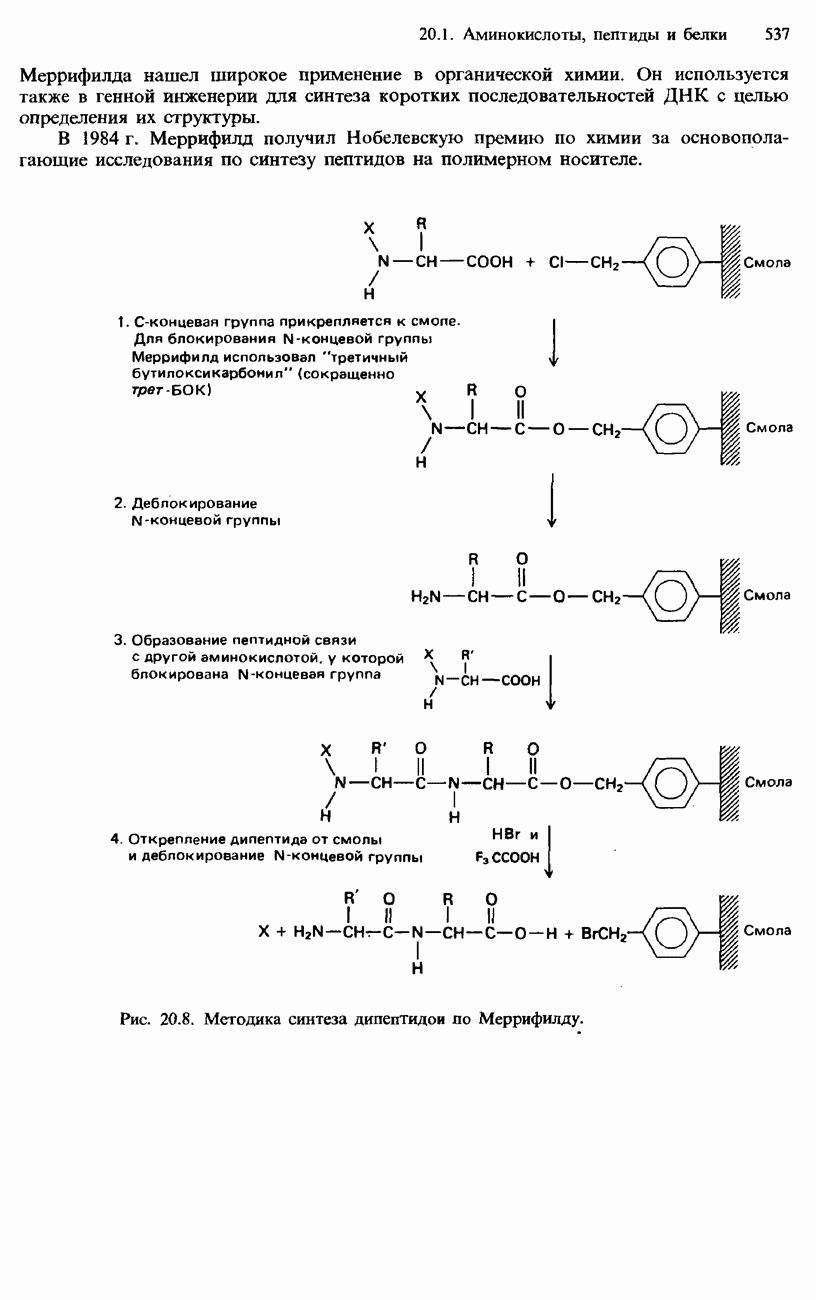
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
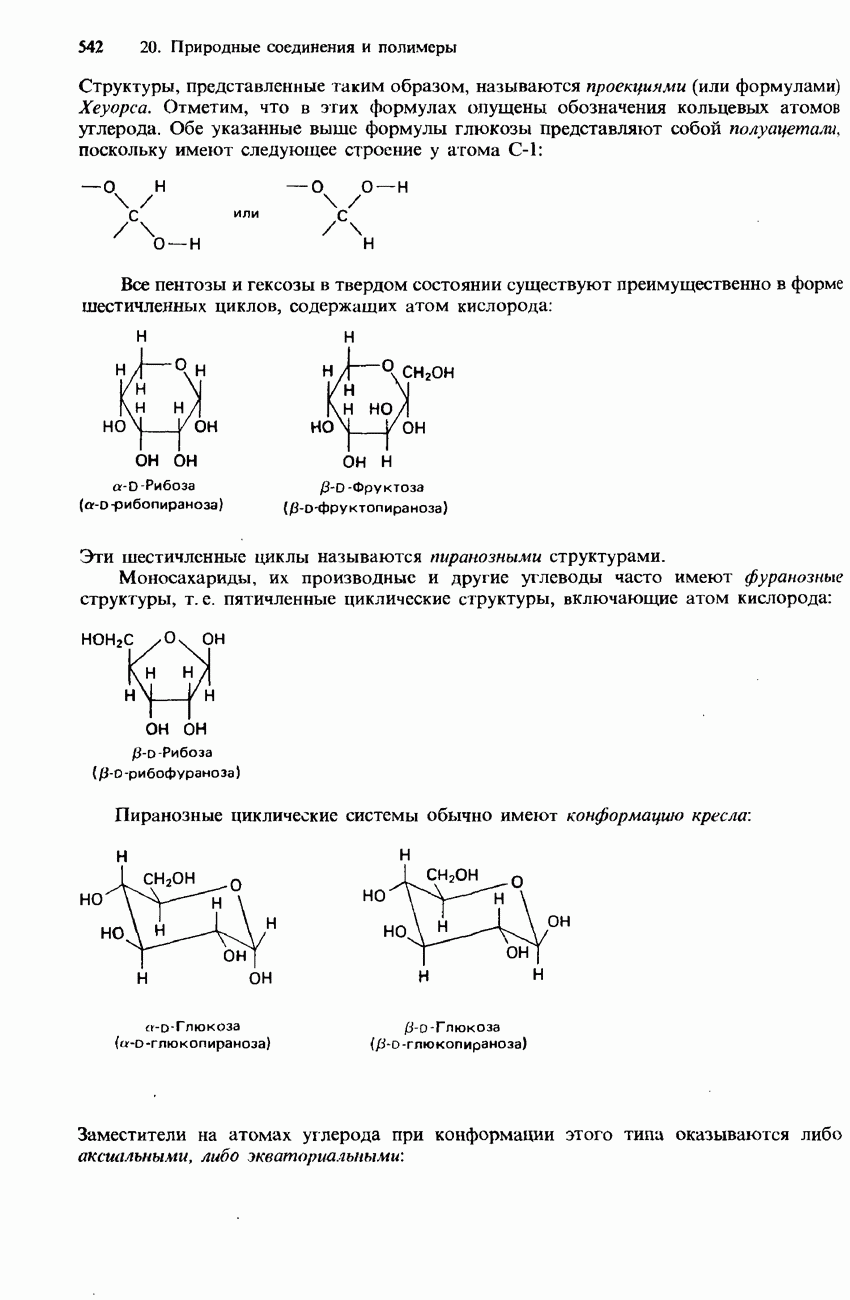
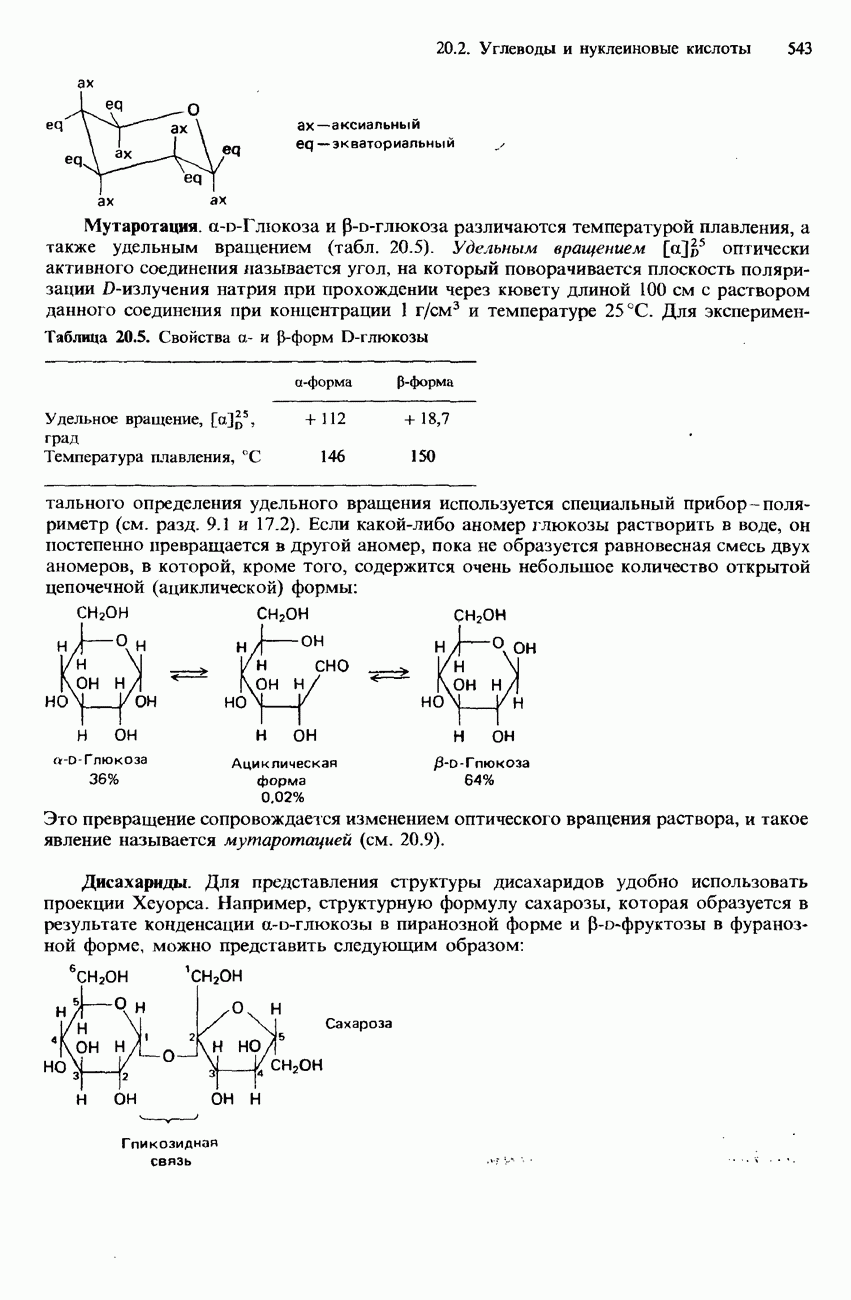
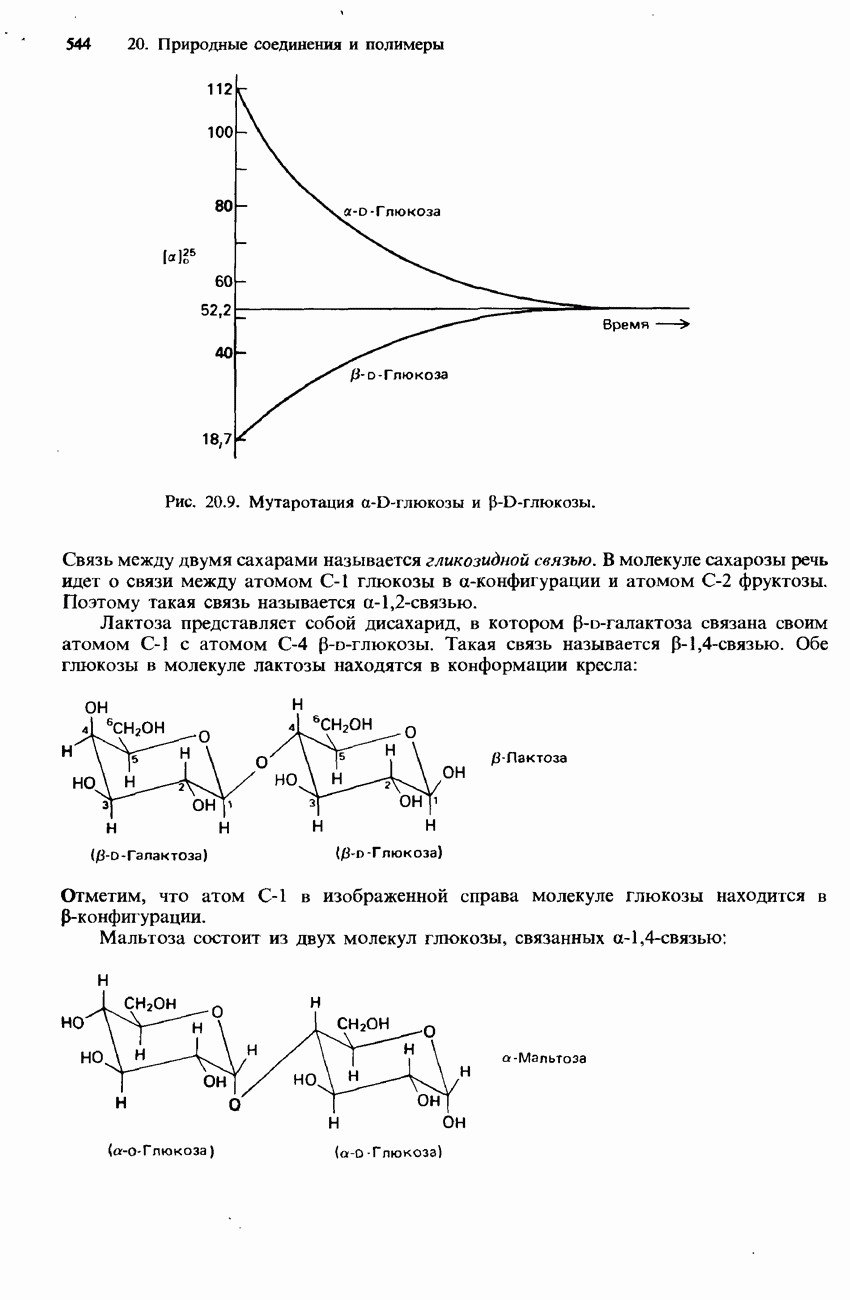
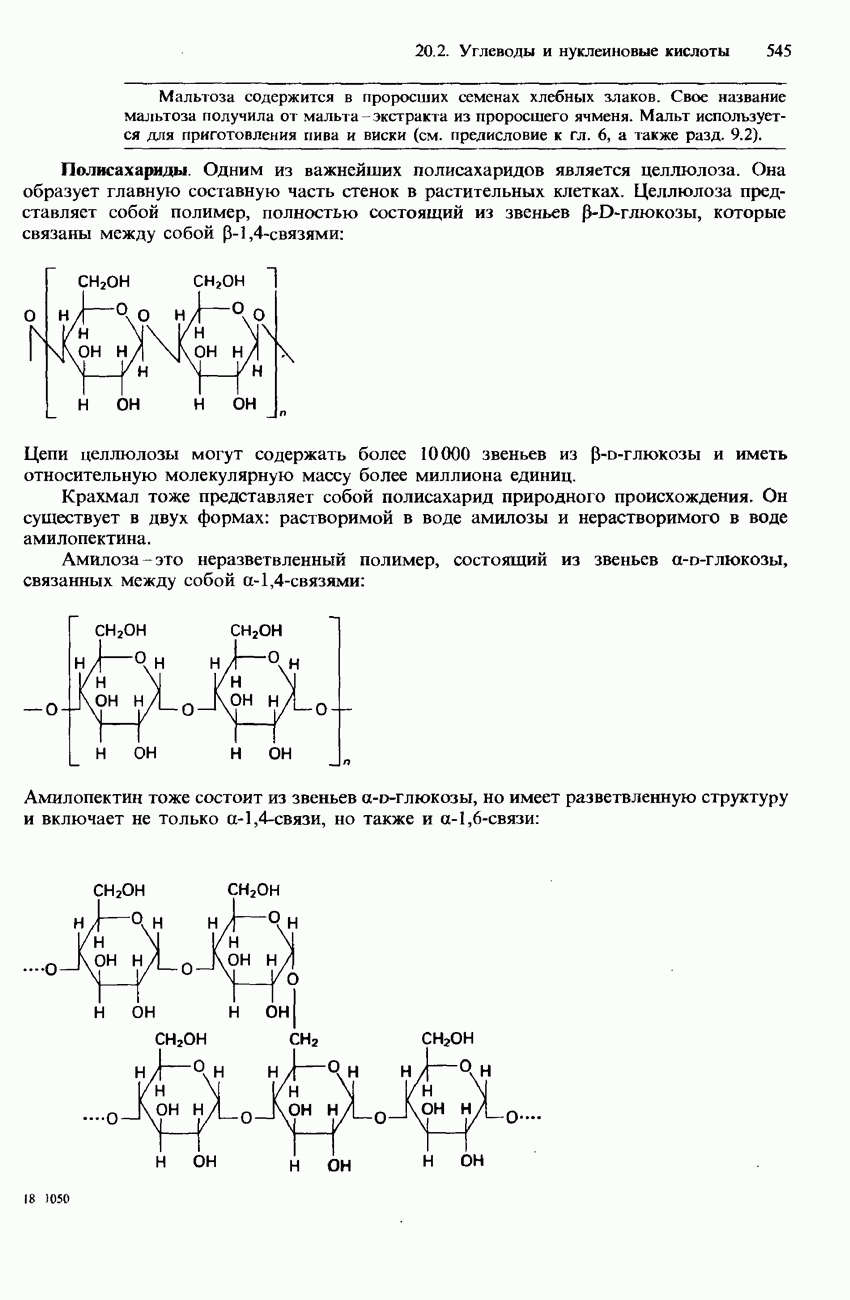
- 20.2. Углеводы и нуклеиновые кислоты
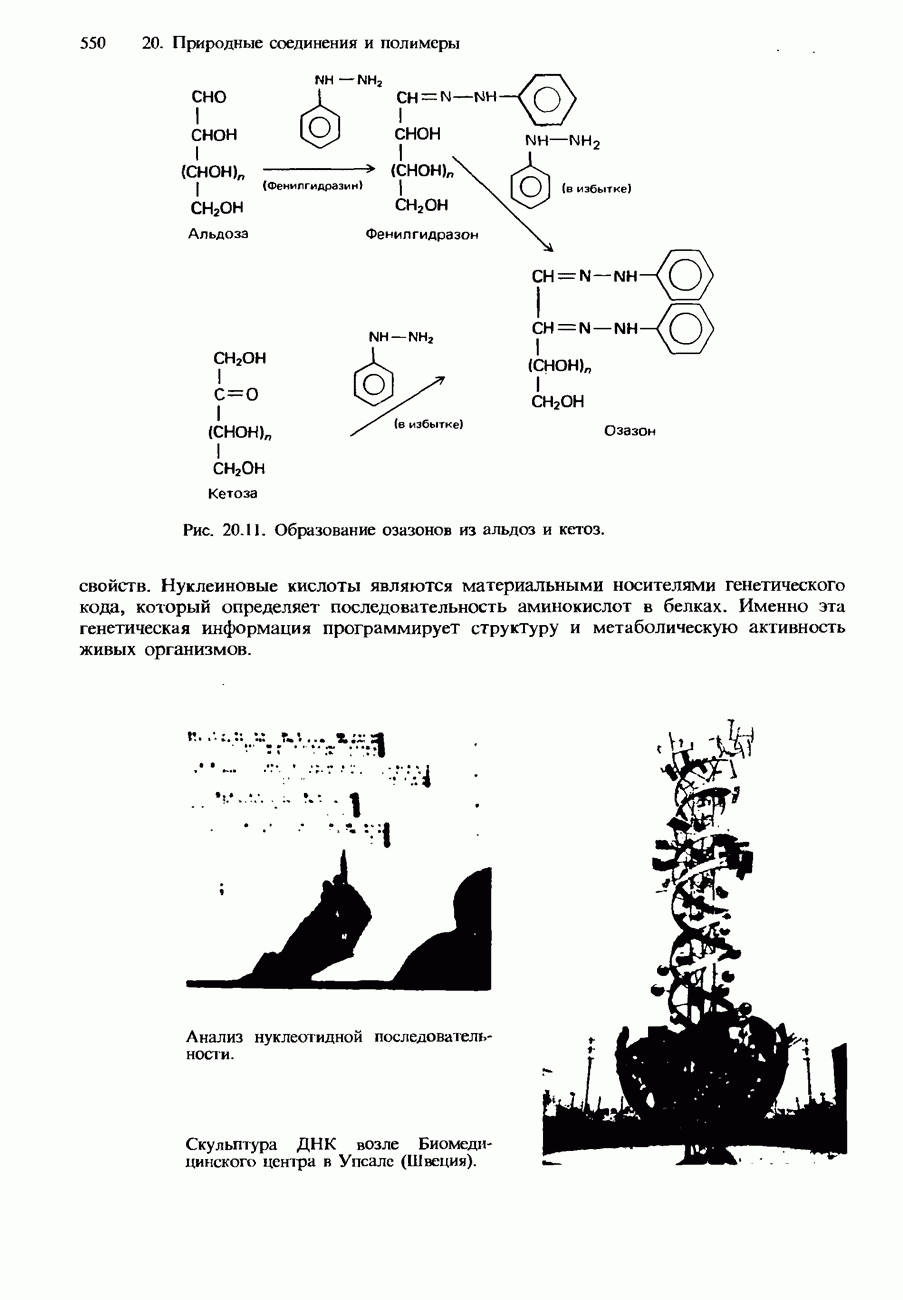
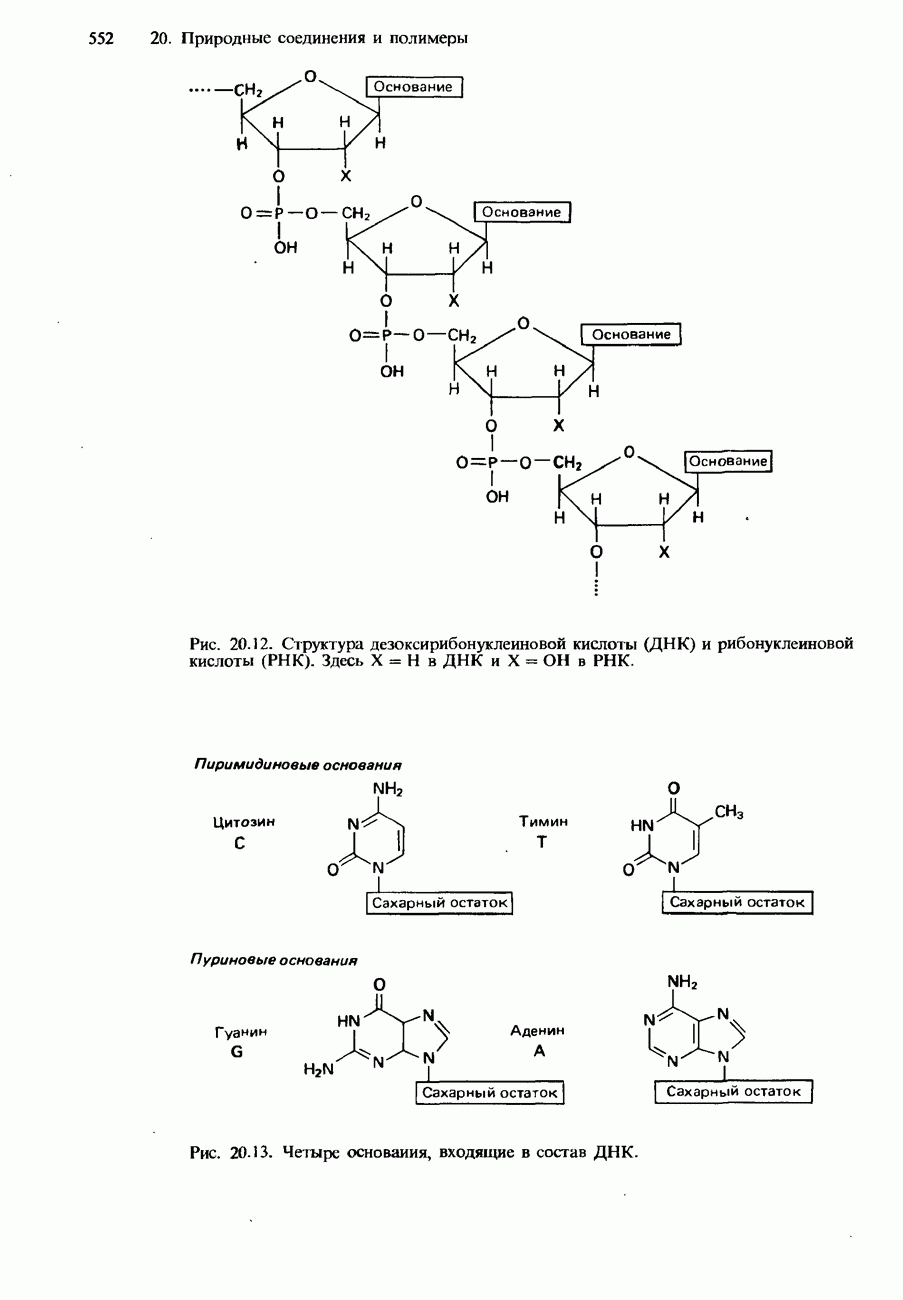
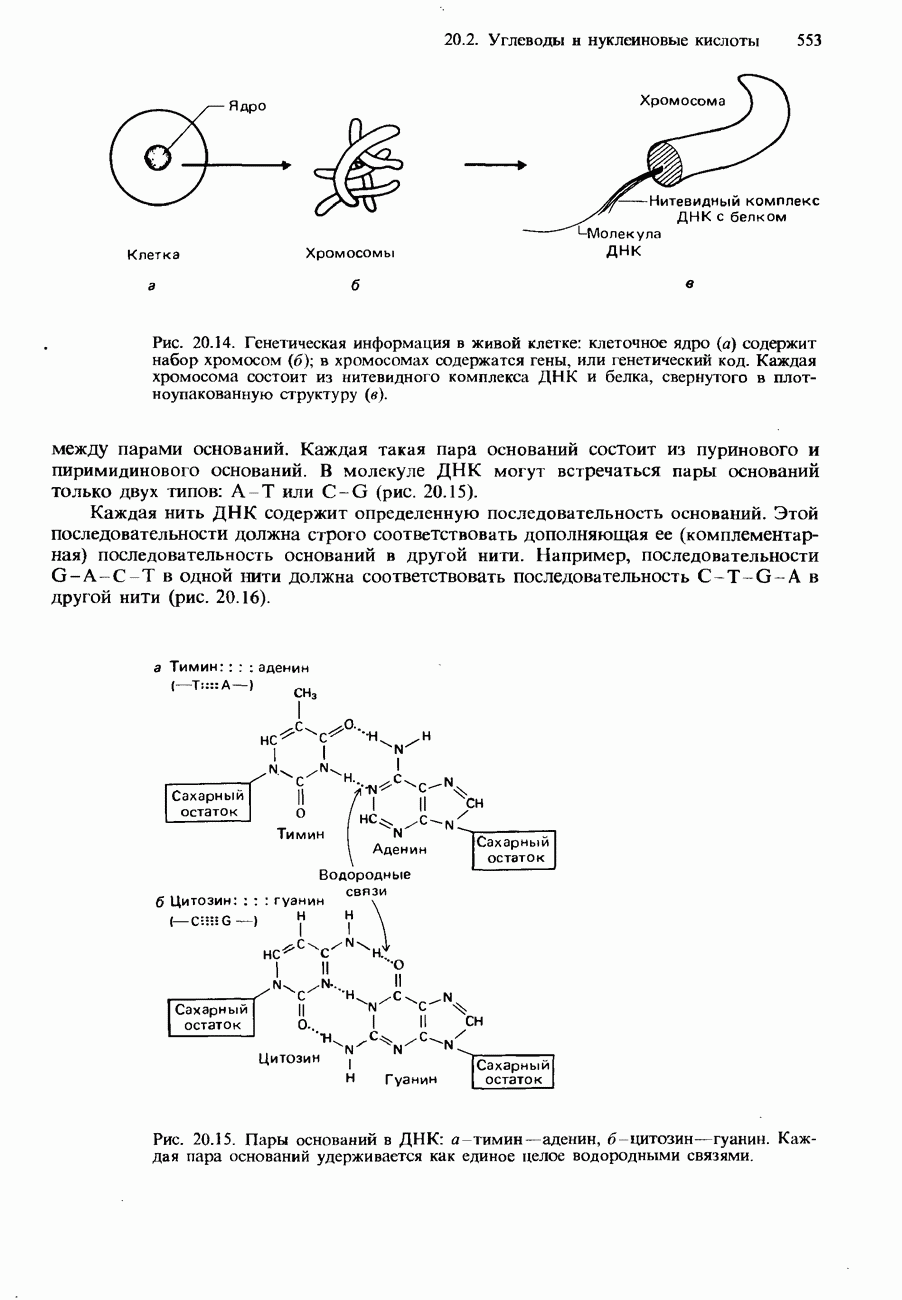
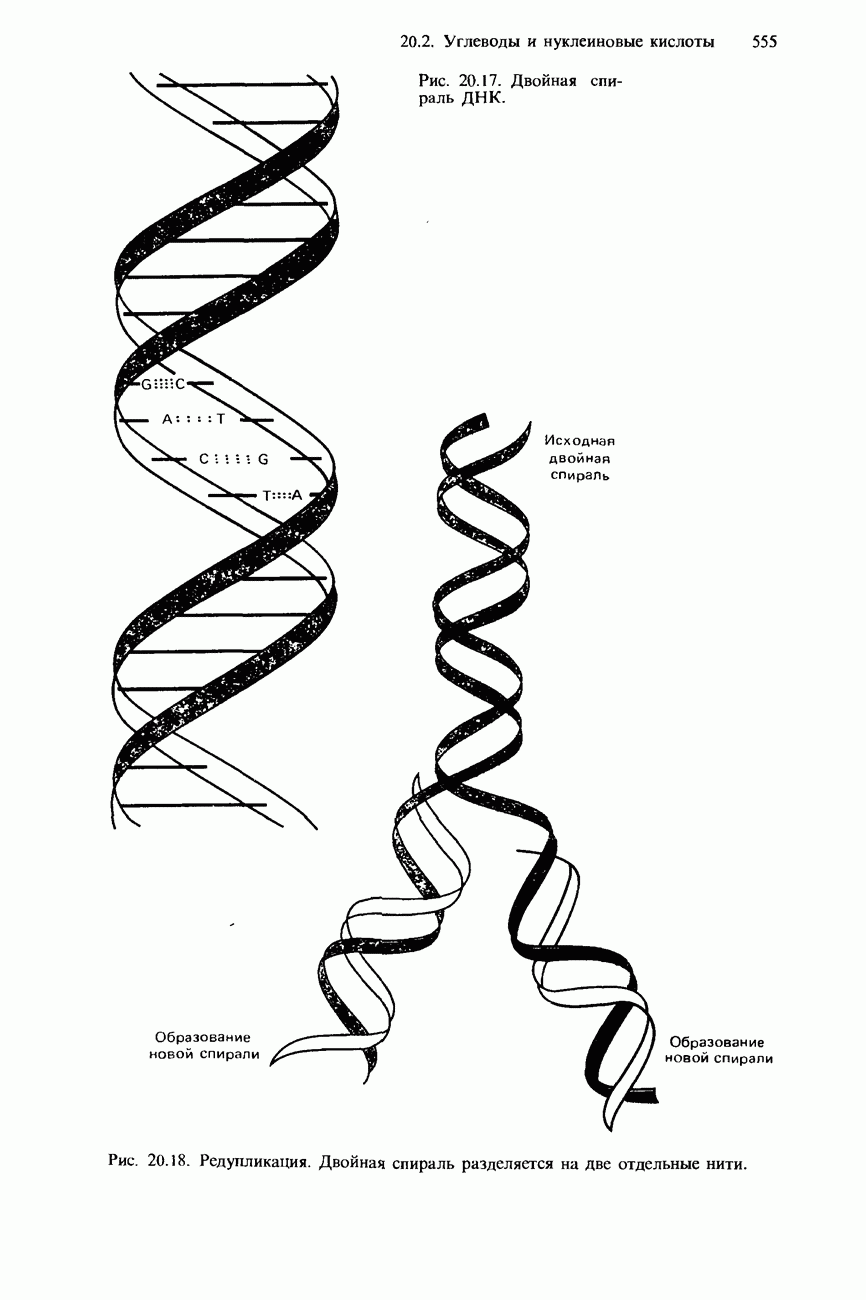
- НУКЛЕИНОВЫЕ КИСЛОТЫ
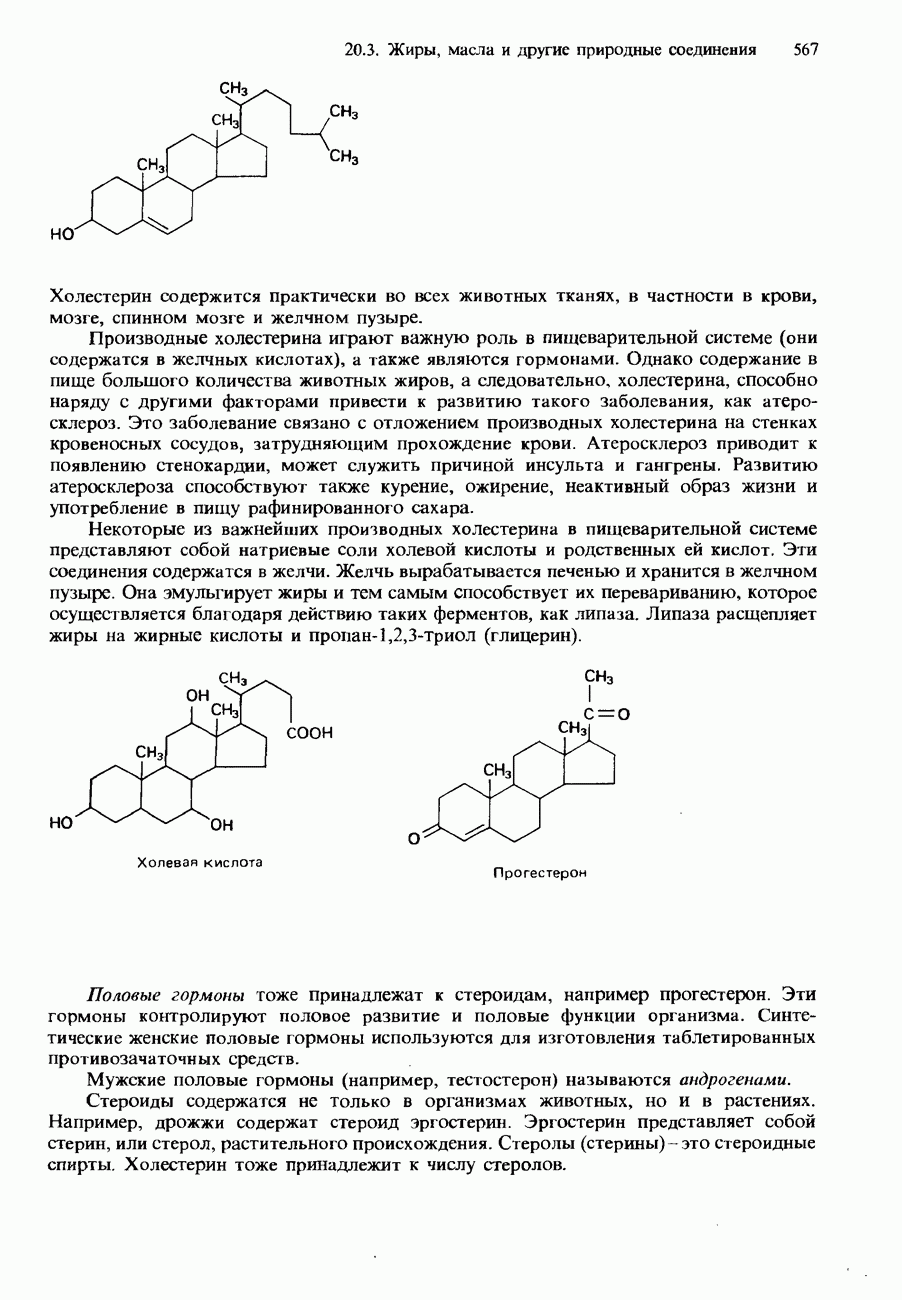
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
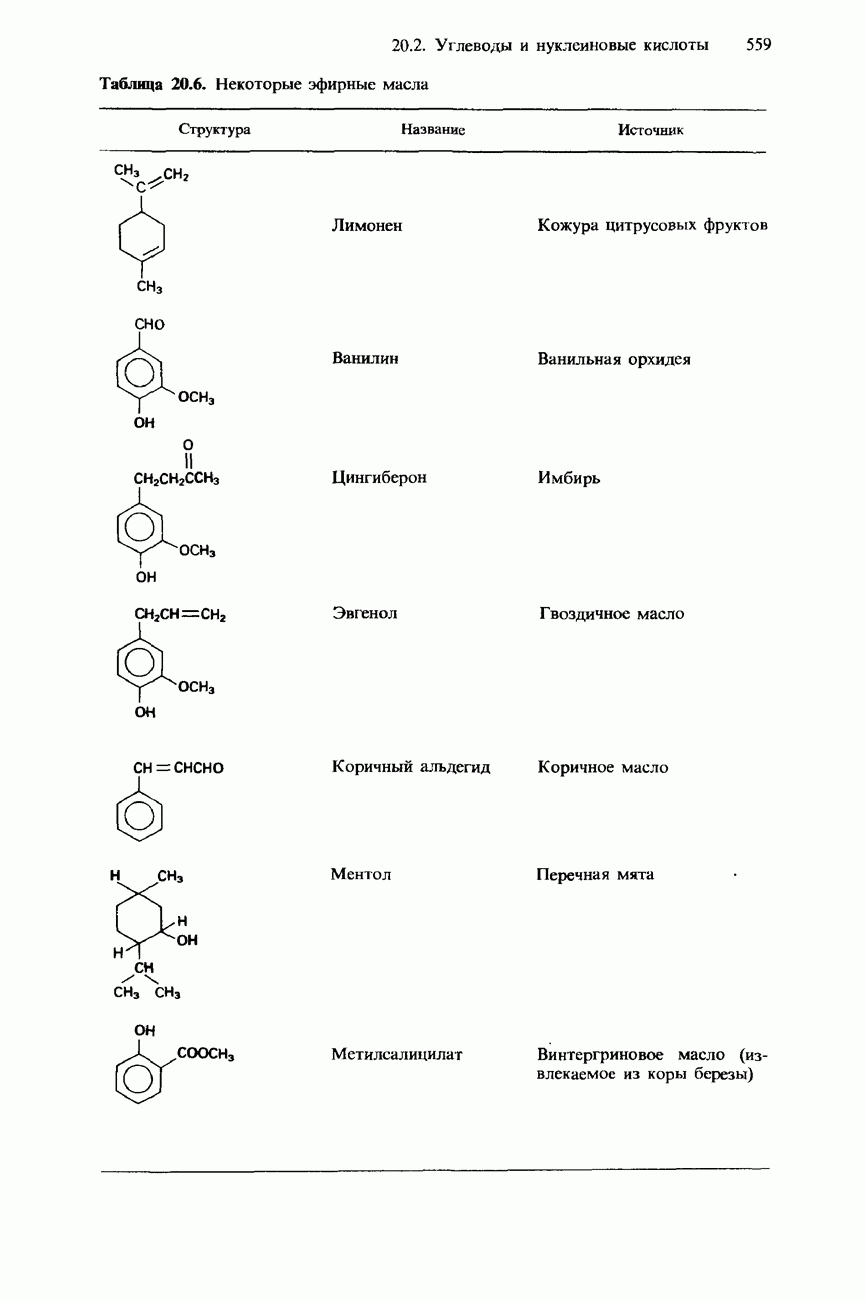
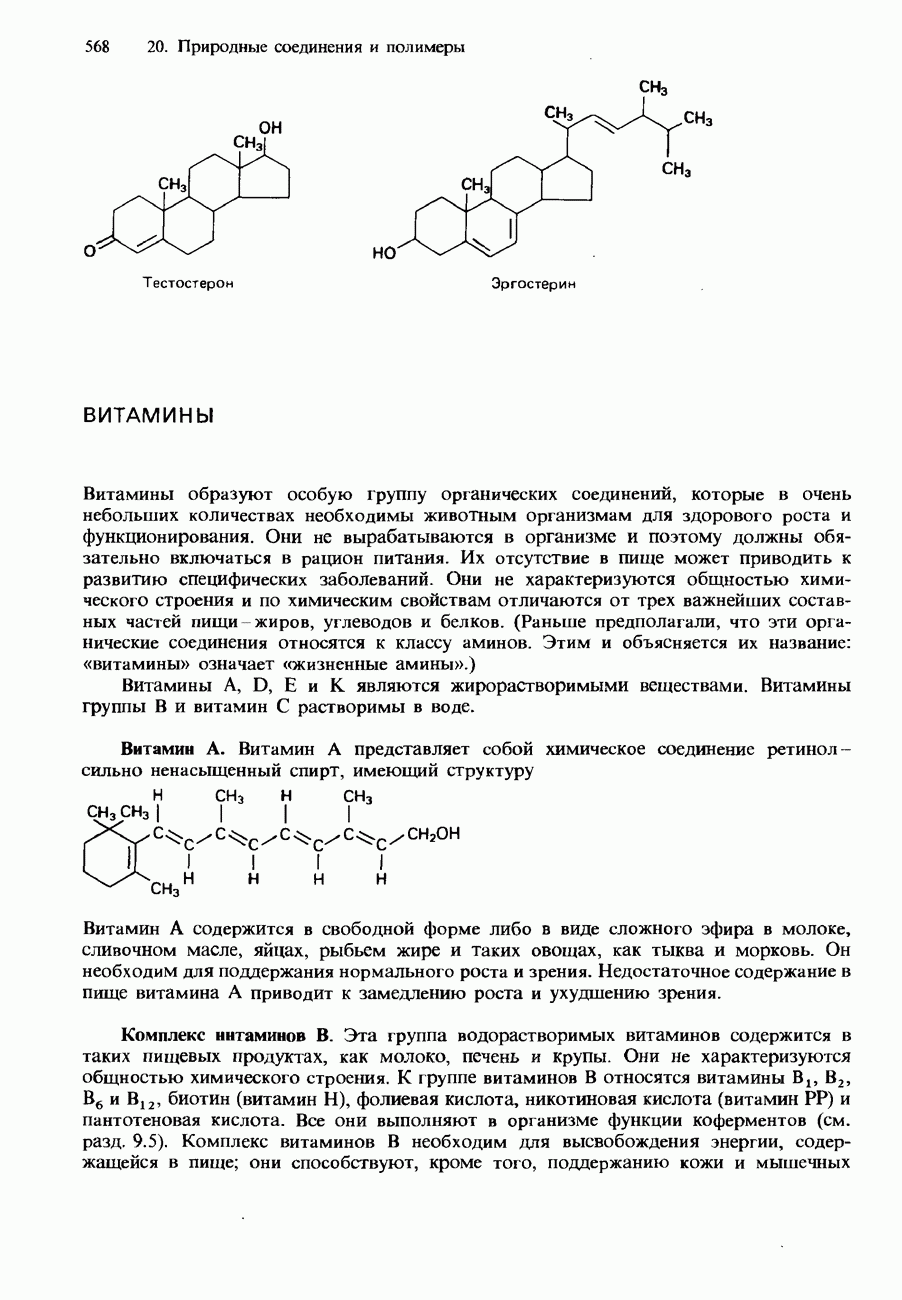
- ВИТАМИНЫ
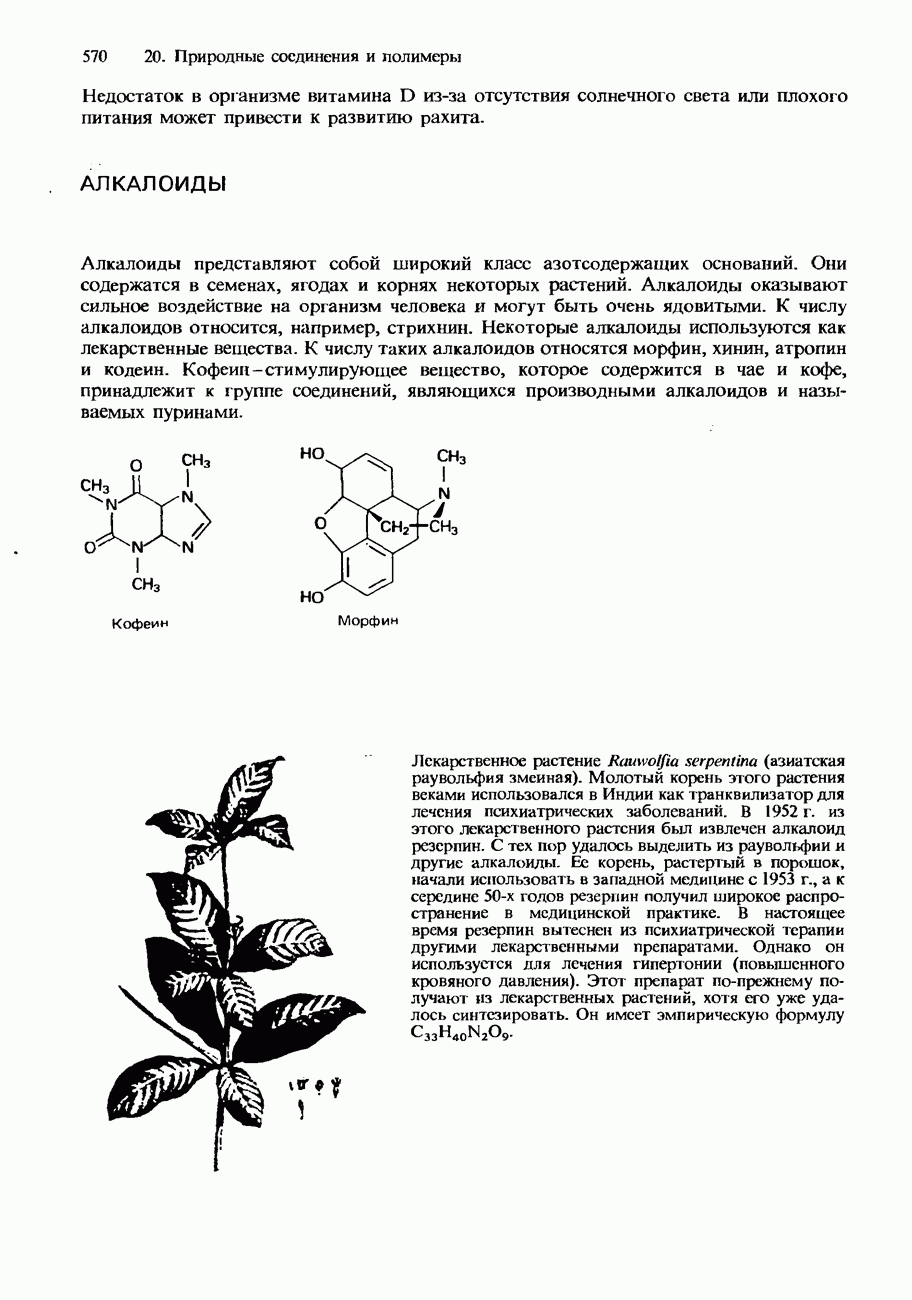
- АЛКАЛОИДЫ
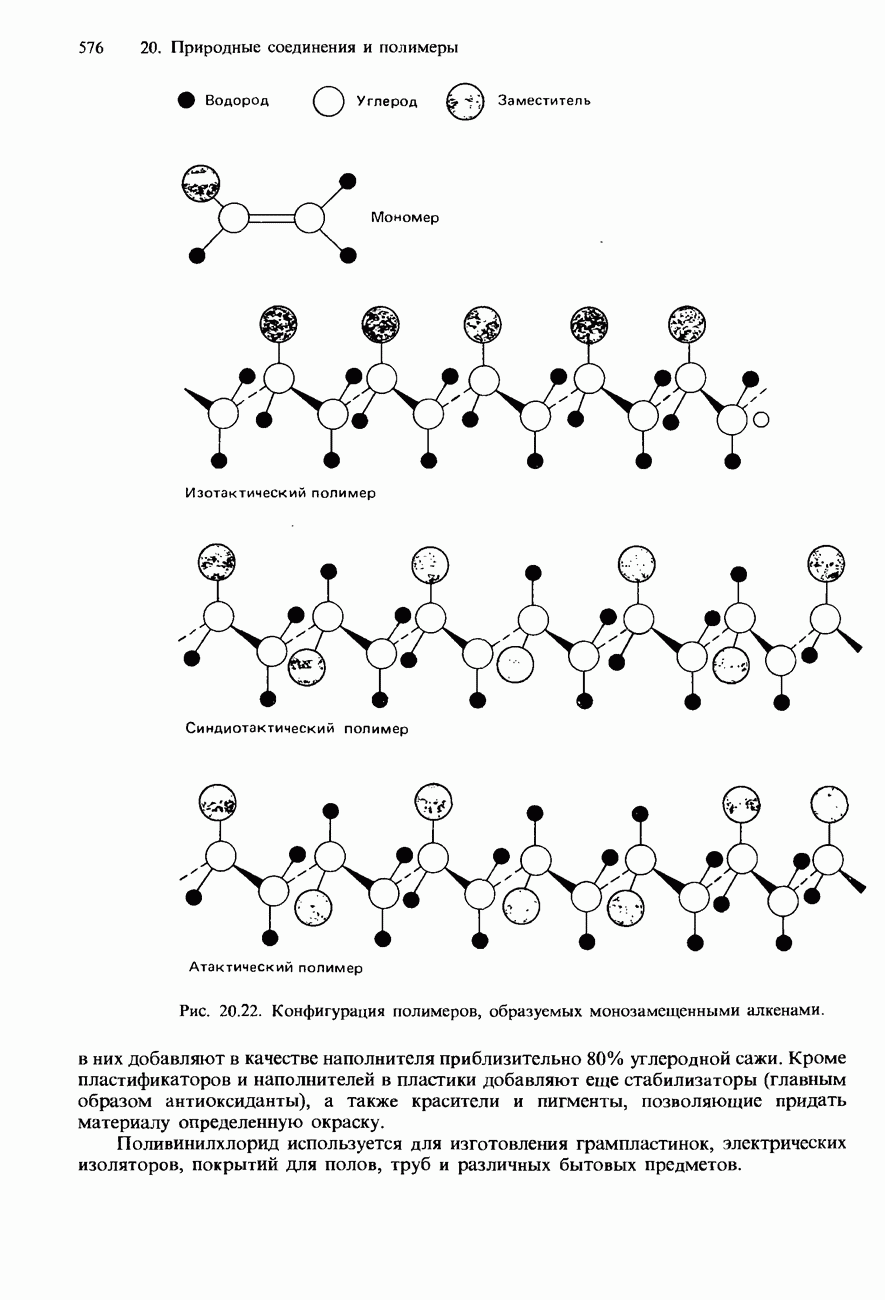
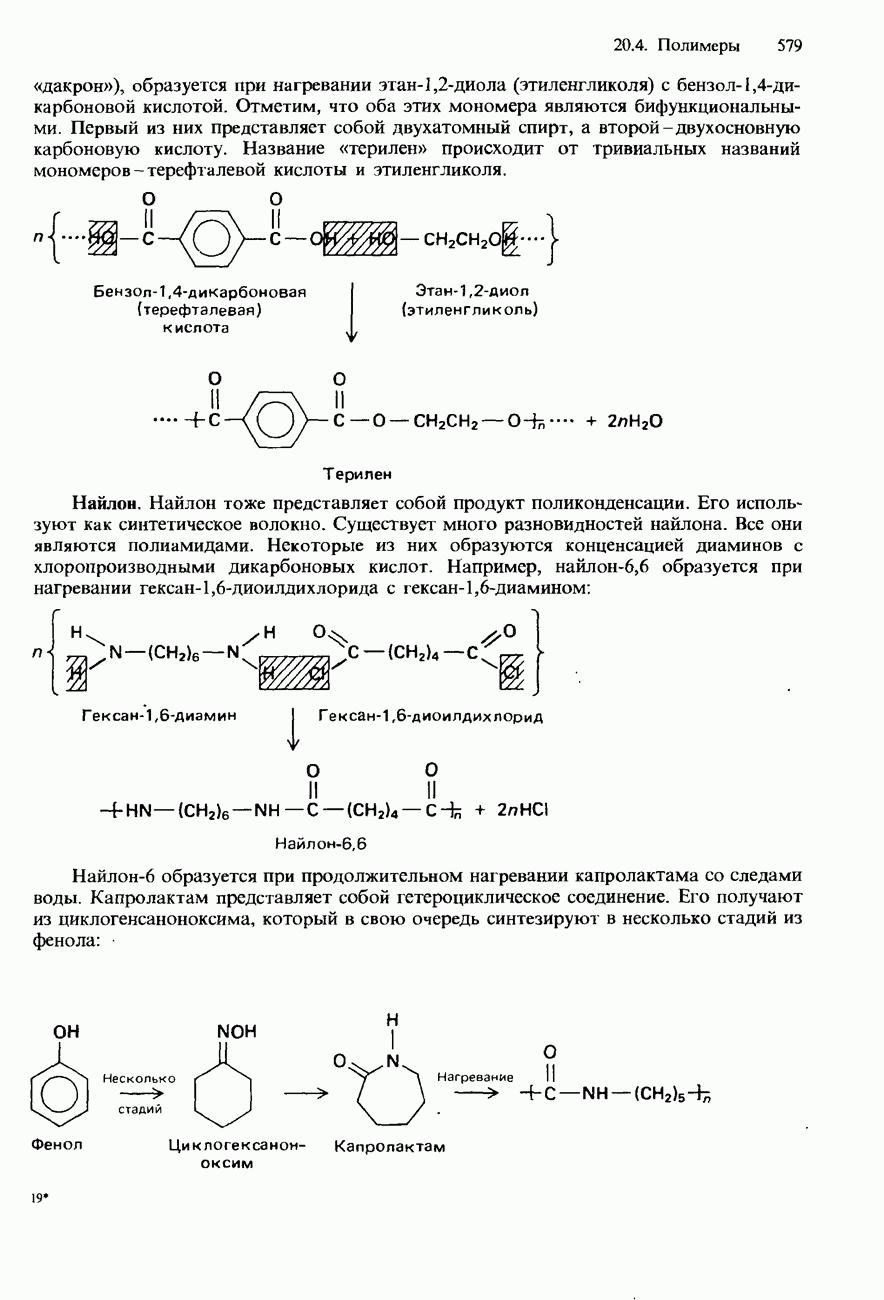
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
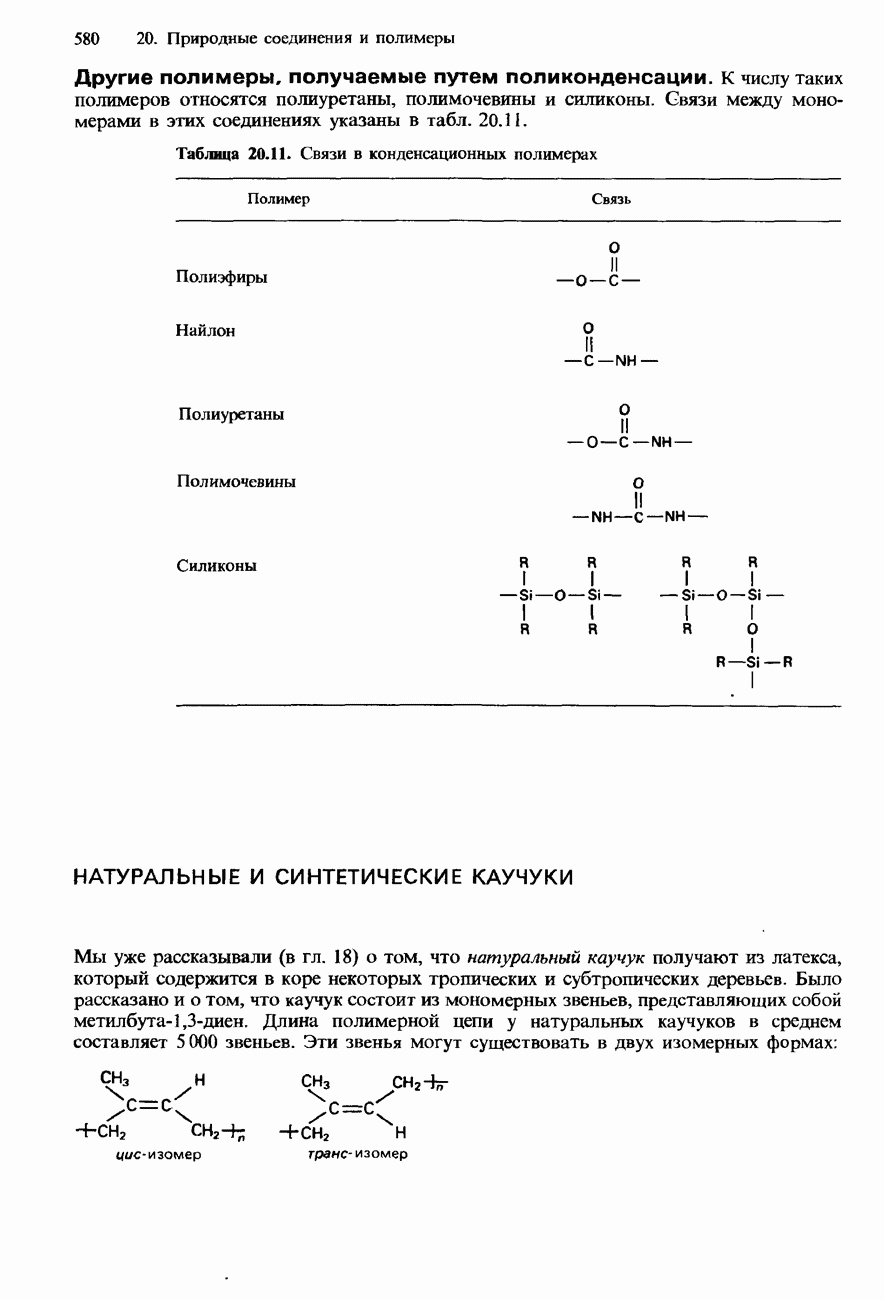
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ