| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
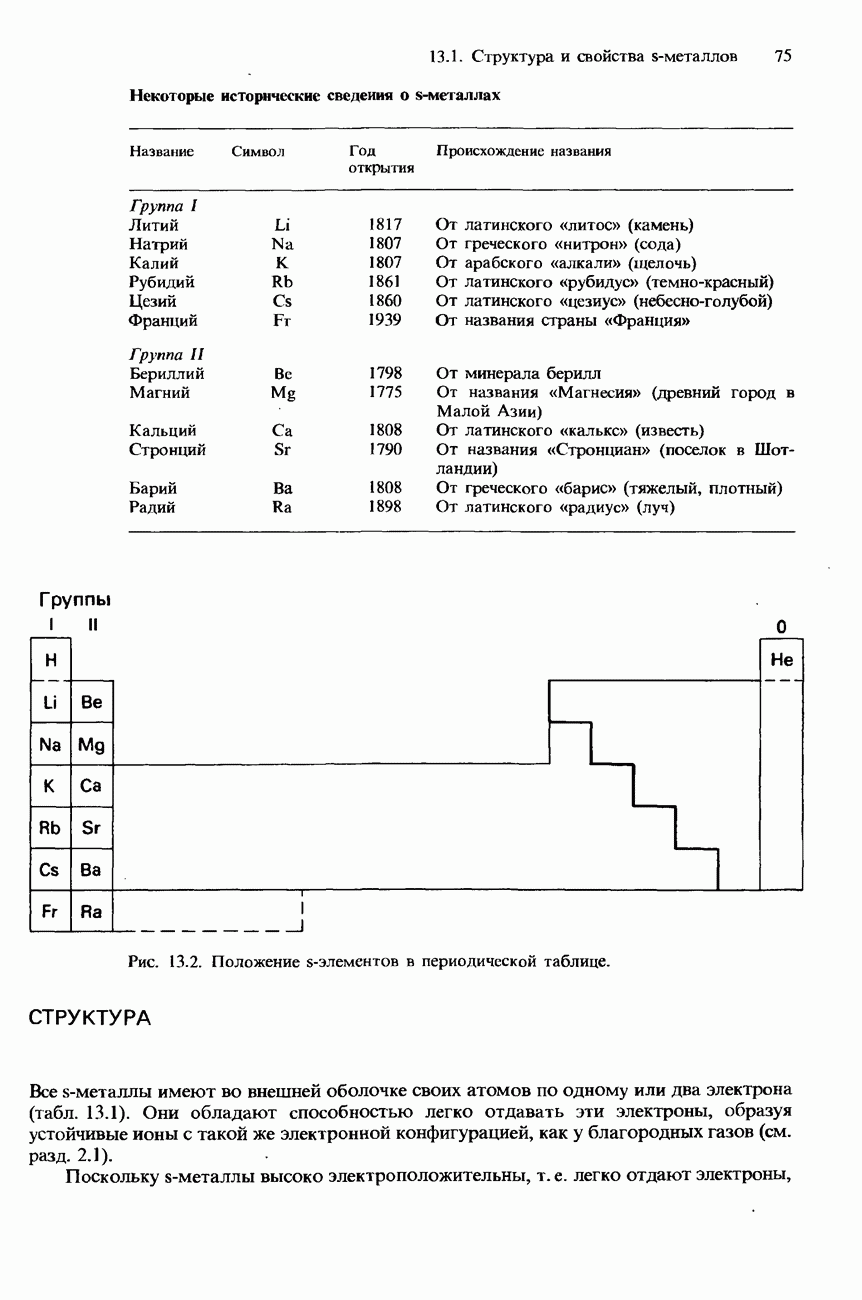
ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
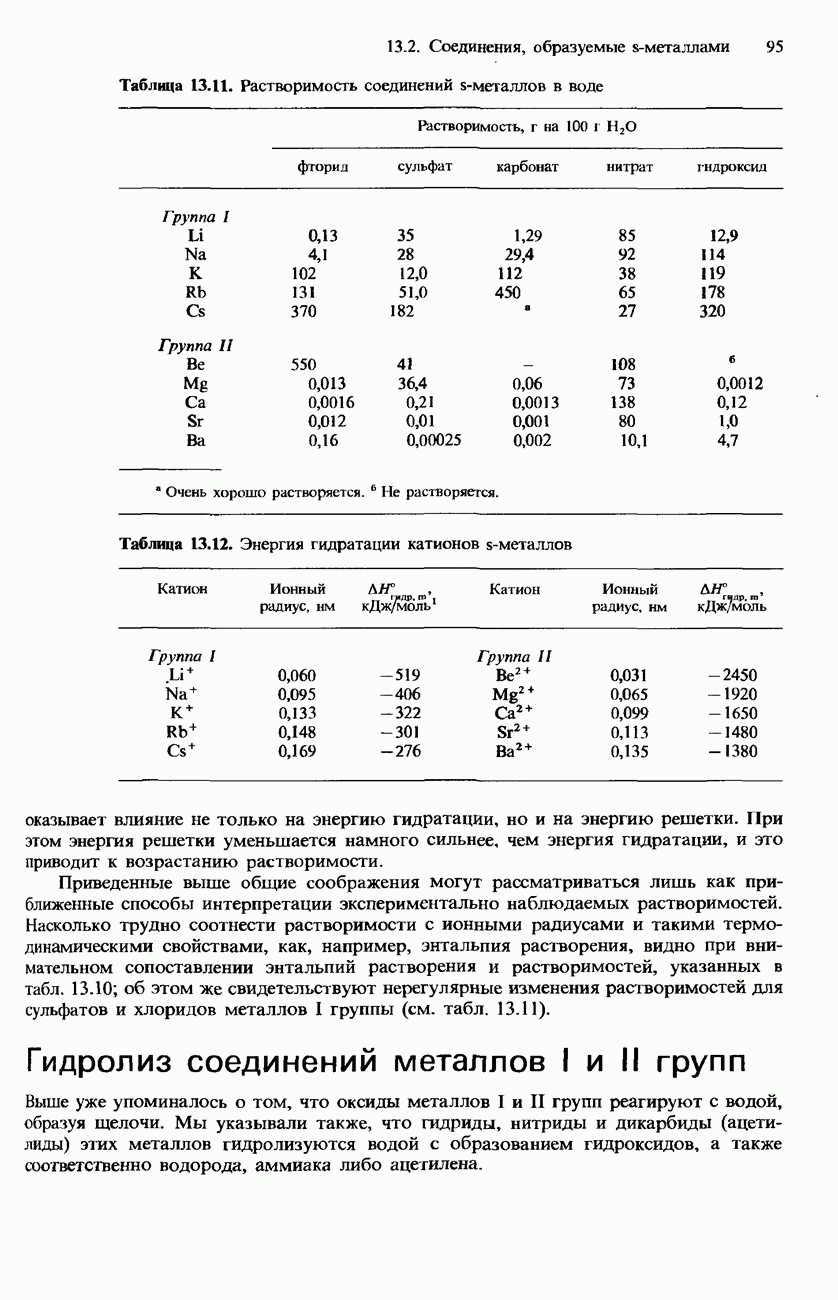
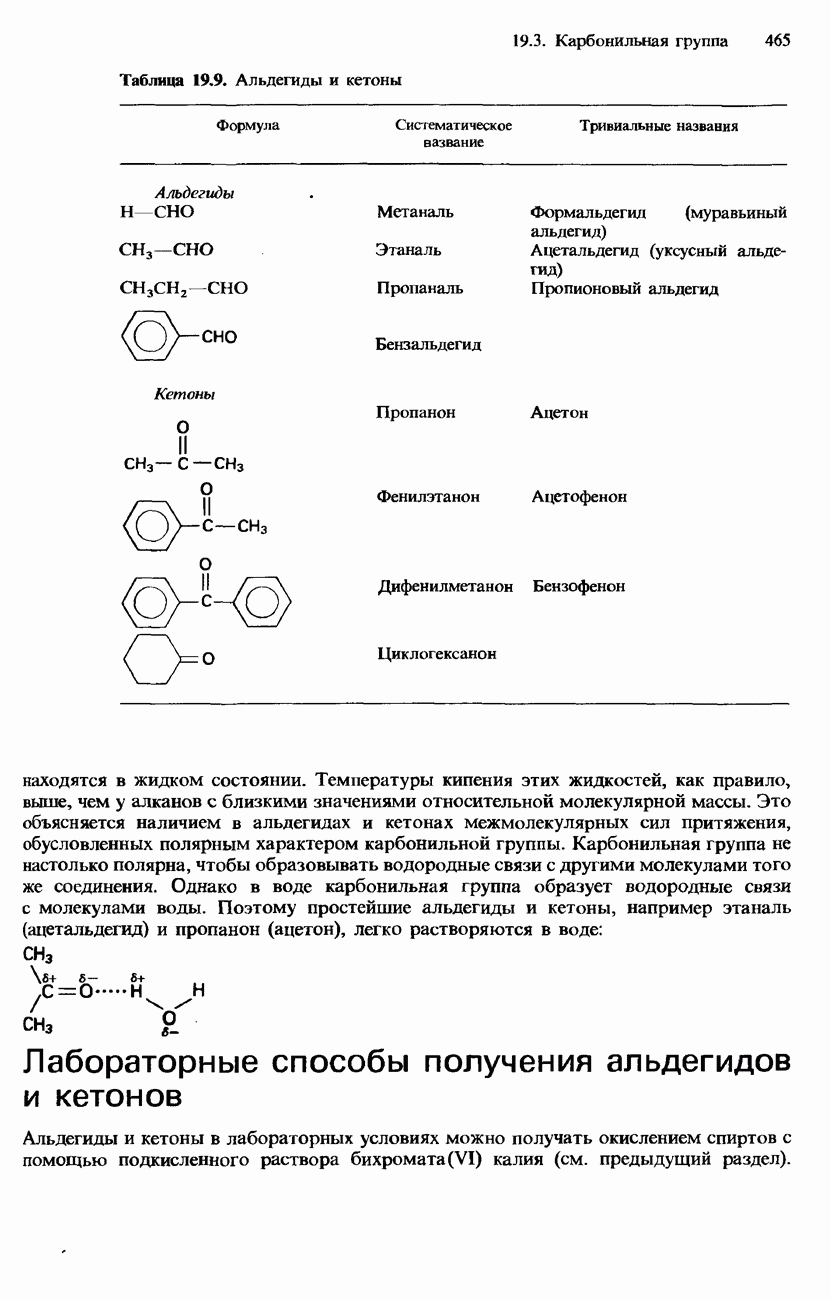
Такие соединения металлов I и II групп, как NaOH, КОН,  имеют огромное промышленное значение и используются в очень больших количествах. Здесь мы рассмотрим некоторые применения этих и других соединений s-металлов, а также кратко опишем производство четырех наиболее важных из них.
имеют огромное промышленное значение и используются в очень больших количествах. Здесь мы рассмотрим некоторые применения этих и других соединений s-металлов, а также кратко опишем производство четырех наиболее важных из них.
Гидроксид натрия
Гидроксид натрия получают путем электролиза рассола в электролизере с ртутным катодом либо в диафрагменном электролизере. Важными побочными продуктами в обоих случаях являются водород и хлор.
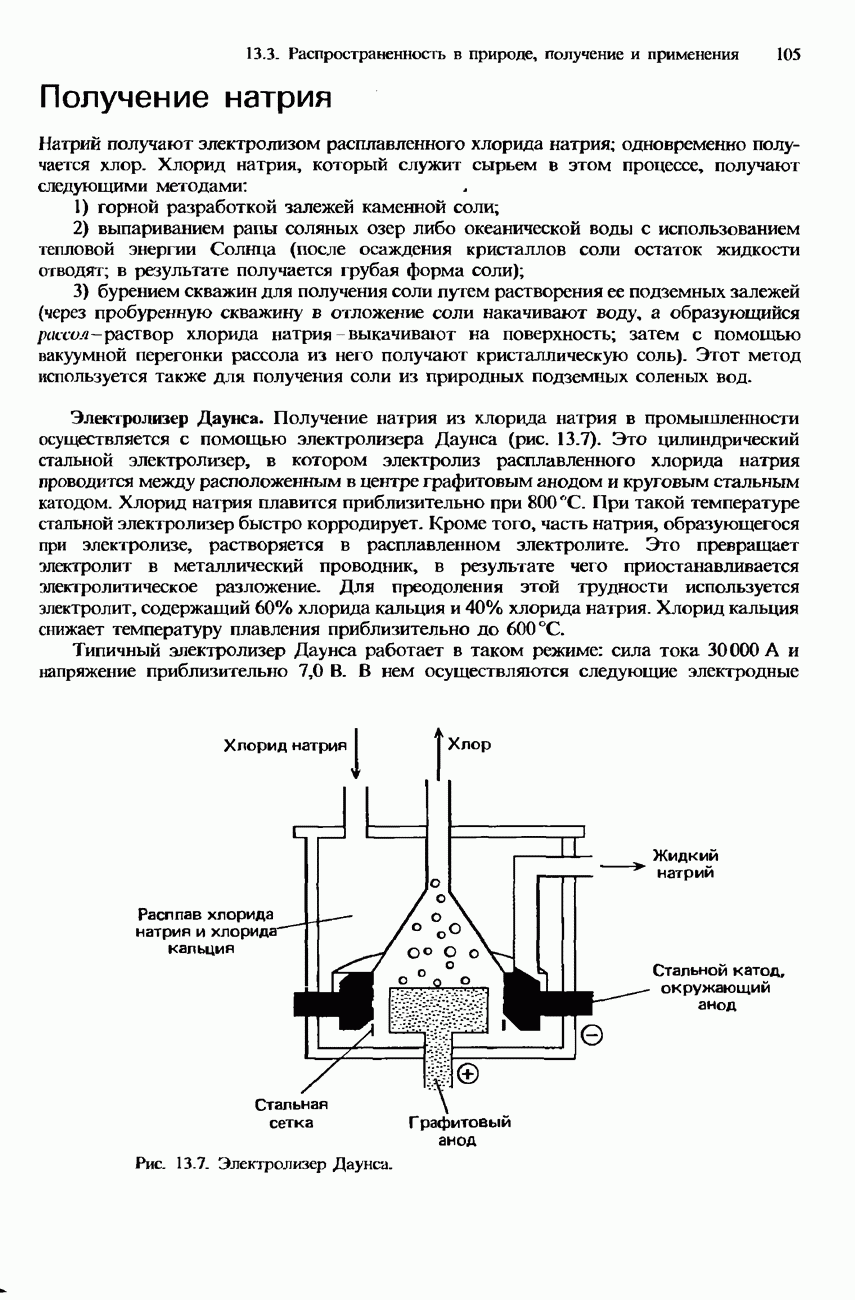
Электролизер с ртутным катодом. Электролизер с ртутным катодом, или электролизер Кестнера-Кельнера, имеет графитовый либо титановый анод и прочный ртутный катод (рис. 13.8). Этот электролизер работает при напряжении 4,3 В и силе тока 300000 А. Химические процессы, протекающие при одновременном получении гидроксида натрия, водорода и хлора в электролизере этого типа, распадаются на три части.
1. Электролиз. В качестве электролита используется концентрированный рассол (раствор хлорида натрия). Благодаря использованию ртутного катода на катоде разряжаются ионы натрия, а не ионы водорода. На аноде разряжаются ионы хлора. Электродные реакции в этом случае совпадают с электродными реакциями в электролизере Даунса.
2. Образование амальгамы. Натрий, образующийся на катоде, растворяется в ртути, образуя амальгаму натрия:

3. Реакция с водой. Амальгама вытекает в отдельную камеру, которая называется содовой камерой (она не показана на рис. 13.8). В этой камере амальгаму смешивают с водой, в результате чего образуется гидроксид натрия и водород. В этом процессе, кроме того, регенерируется чистая ртуть:

Регенерированную ртуть возвращают в электролизер.

Рис. 13.8. Электролизер с ртутным катодом.

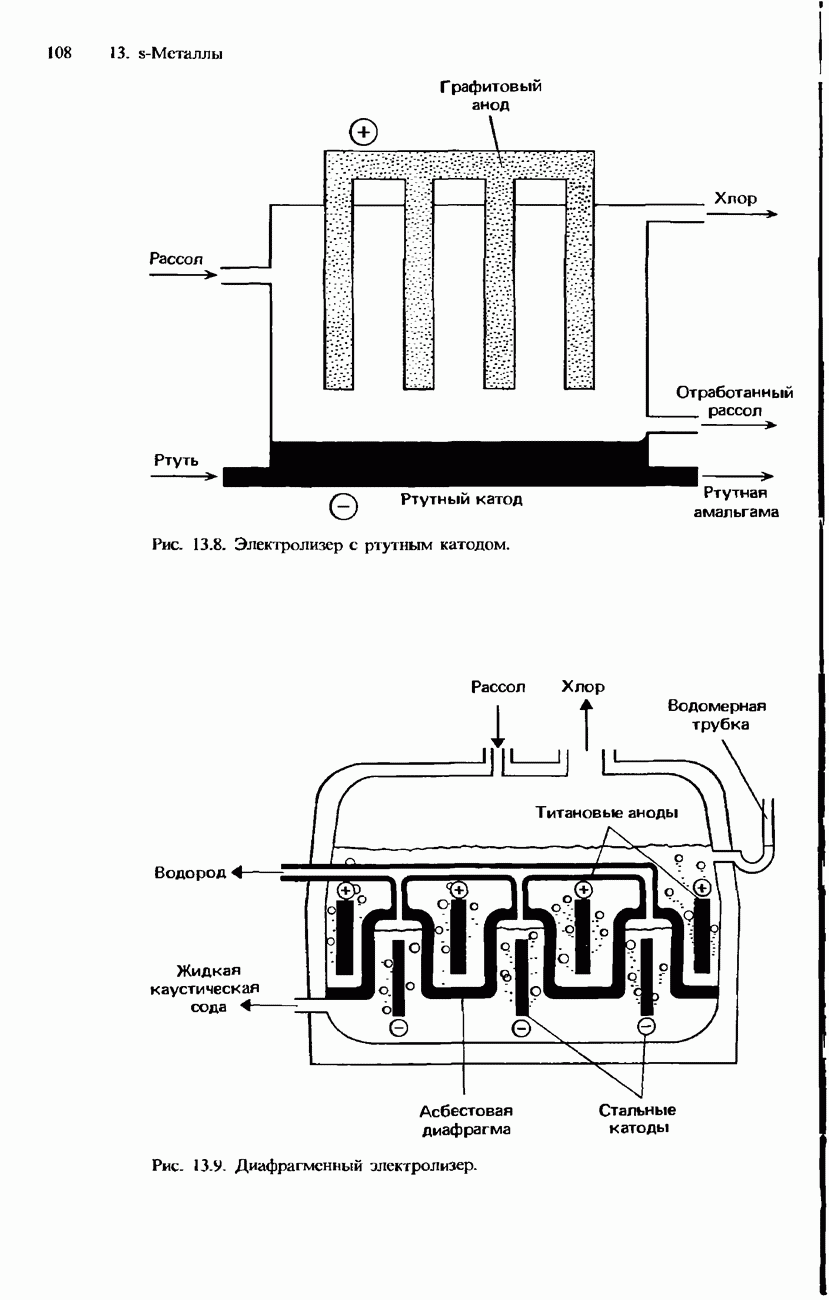
Рис. 13.9. Диафрагмснный электролизер.
Диафрагмснный электролизер. Диафрагменный электролизер имеет графитовый либо титановый анод и стальной катод, отделенные друг от друга асбестовой диафрагмой. Существует несколько разновидностей диафрагменного электролизера. На рис. 13.9 показана принципиальная схема диафрагменного электролизера Хукера. В Великобритании используется только такая разновидность диафрагменного электролизера.
В качестве электролита применяют рассол, подаваемый в электролизер сверху. Разряд ионов хлора происходит на аноде, и газообразный хлор высвобождается в верхней части электролизера. Оставшийся раствор просачивается через асбестовую диафрагму в катодное отделение. На катоде образуются водород и гидроксид натрия:

Раствор, образующийся в катодном отделении, содержит приблизительно равные количества гидроксида натрия и хлорида натрия. Его сливают из электролизера и затем концентрируют выпариванием, в результате чего из него выкристаллизовывается хлорид натрия. Оставшийся раствор содержит приблизительно 50% по массе гидроксида натрия и около 1% хлорида натрия.
Гидроксид калия. Для получения гидроксида калия тоже используются электролизеры двух описанных выше типов. Вместо рассола в этом случае используется концентрированный раствор хлорида калия.
Карбонат натрия
Большую часть карбоната натрия, используемого в Великобритании, получают с помощью аммиачно-содового процесса Сольве. Этот процесс включает две стадии.
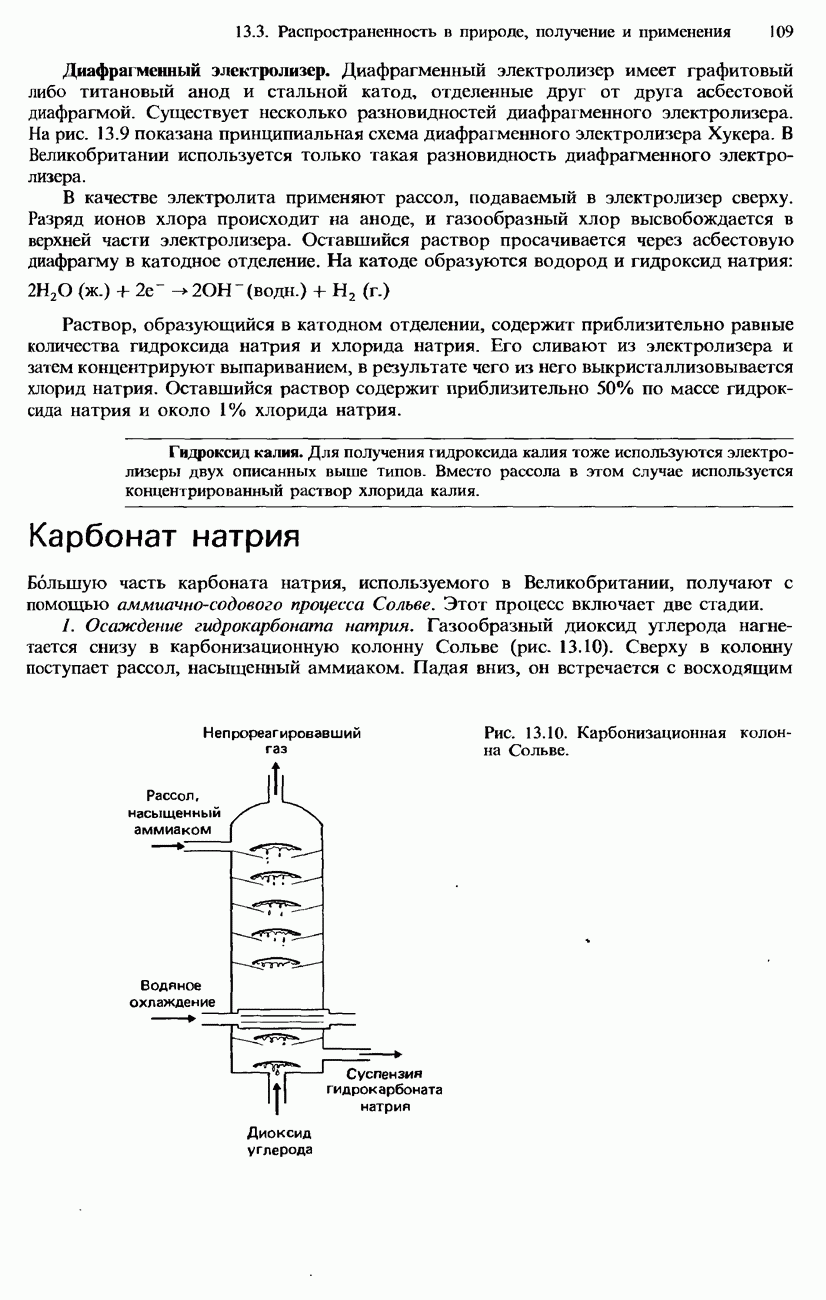
1. Осаждение гидрокарбоната натрия. Газообразный диоксид углерода нагнетается снизу в карбонизационную колонну Сольве (рис. 13.10). Сверху в колонну поступает рассол, насыщенный аммиаком. Падая вниз, он встречается с восходящим

Рис. 13.10. Карбонизационная колонна Сольве.
потоком диоксида углерода. Диоксид углерода растворяется в воде:

Аммиак, содержащийся в растворе, нейтрализует ионы гидроксония, что приводит к смещению вправо указанного выше равновесия:

Гидрокарбонат натрия обладает невысокой растворимостью в воде и поэтому осаждается из раствора:

В растворе остается хлорид аммония.
Суммарное уравнение процесса имеет вид

Поскольку весь этот процесс в целом экзотермичен, для охлаждения колонны приходится использовать воду.
Из нижней части колонны удаляют отстой белого цвета, содержащий гидрокарбонат натрия, взвешенный в растворе хлорида аммония. При помощи вакуумной фильтрации из него отделяют гидрокарбонат натрия.
2. Получение карбоната натрия. Гидрокарбонат натрия, полученный на 1-й стадии, нагревают в длинных железных трубах:

Остаточный хлорид аммония улетучивается на этой стадии. Полученный продукт носит название кальцинированная сода. Он содержит небольшую примесь хлорида натрия.
Сырьевые материалы. Сырьевыми материалами для процесса Сольве служат рассол и карбонат кальция (известняк), относительно недорогие материалы, а также аммиак. Аммиак получают с помощью процесса Габера (см. разд. 7.2).
Карбонат кальция необходим 1) для получения диоксида углерода  используемого на 1-й стадии; 2) для получения гашеной извести
используемого на 1-й стадии; 2) для получения гашеной извести  применяемой с целью повторного использования аммиака (см. ниже).
применяемой с целью повторного использования аммиака (см. ниже).
Для получения 1 т  необходимо такое количество сырьевых материалов:
необходимо такое количество сырьевых материалов:

Отметим, что в процессе Сольве расходуется очень небольшое количество аммиака, потому что в этом процессе его рециклируют (используют повторно).
Рециклирование. В процессе Сольве осуществляется рециклирование диоксида углерода и аммиака. Диоксид углерода, образующийся на 2-й стадии при получении кальцинированной соды, снова направляется в карбонизационную колонну Сольве. Аммиак регенерируют из раствора хлорида аммония, получающегося на  стадии, добавляя в него гашеную известь:
стадии, добавляя в него гашеную известь:


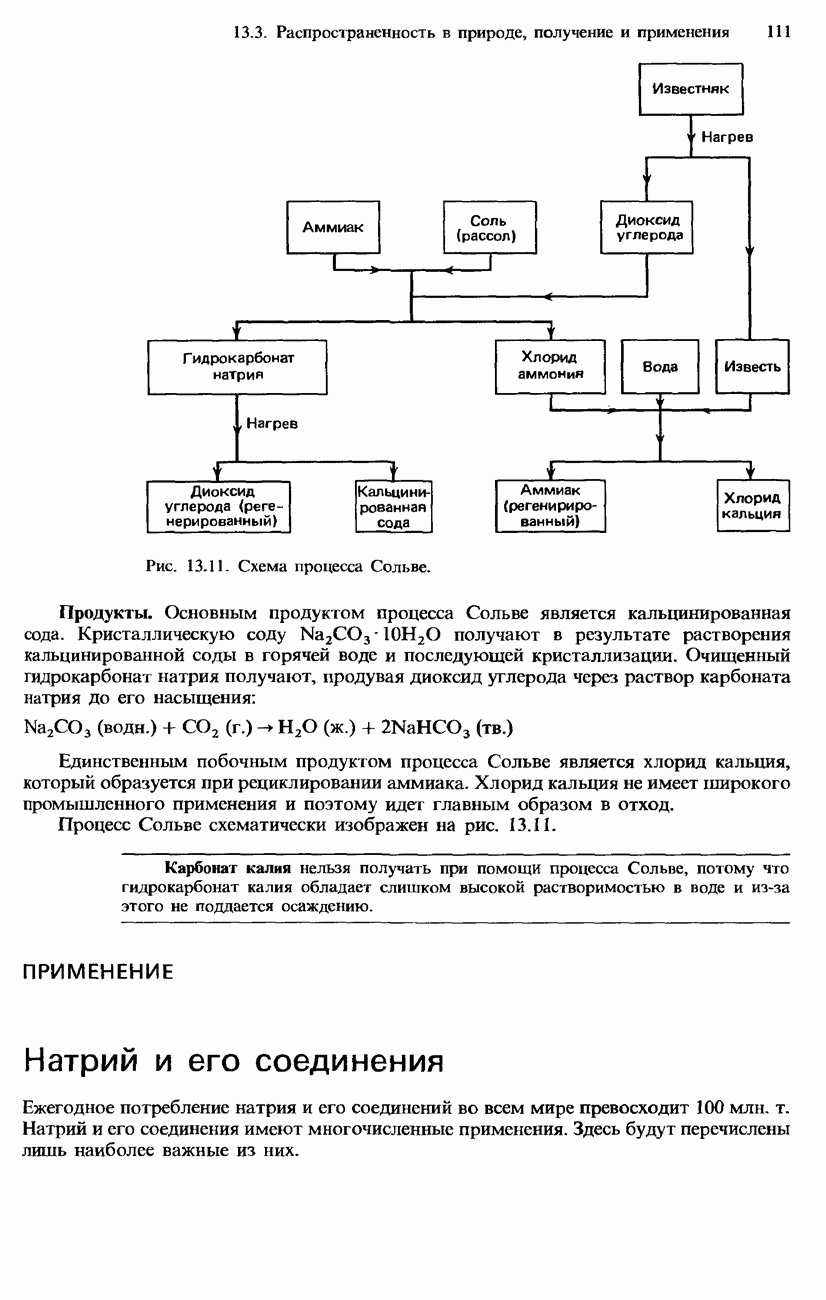
Рис. 13.11. Схема процесса Сольве.
Продукты. Основным продуктом процесса Сольве является кальцинированная сода. Кристаллическую соду  получают в результате растворения кальцинированной соды в горячей воде и последующей кристаллизации. Очищенный гидрокарбонат натрия получают, продувая диоксид углерода через раствор карбоната натрия до его насыщения:
получают в результате растворения кальцинированной соды в горячей воде и последующей кристаллизации. Очищенный гидрокарбонат натрия получают, продувая диоксид углерода через раствор карбоната натрия до его насыщения:

Единственным побочным продуктом процесса Сольве является хлорид кальция, который образуется при рециклировании аммиака. Хлорид кальция не имеет широкого промышленного применения и поэтому идет главным образом в отход.
Процесс Сольве схематически изображен на рис. 13.11.
Карбонат калия нельзя получать при помощи процесса Сольве, потому что гидрокарбонат калия обладает слишком высокой растворимостью в воде и из-за этого не поддается осаждению.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
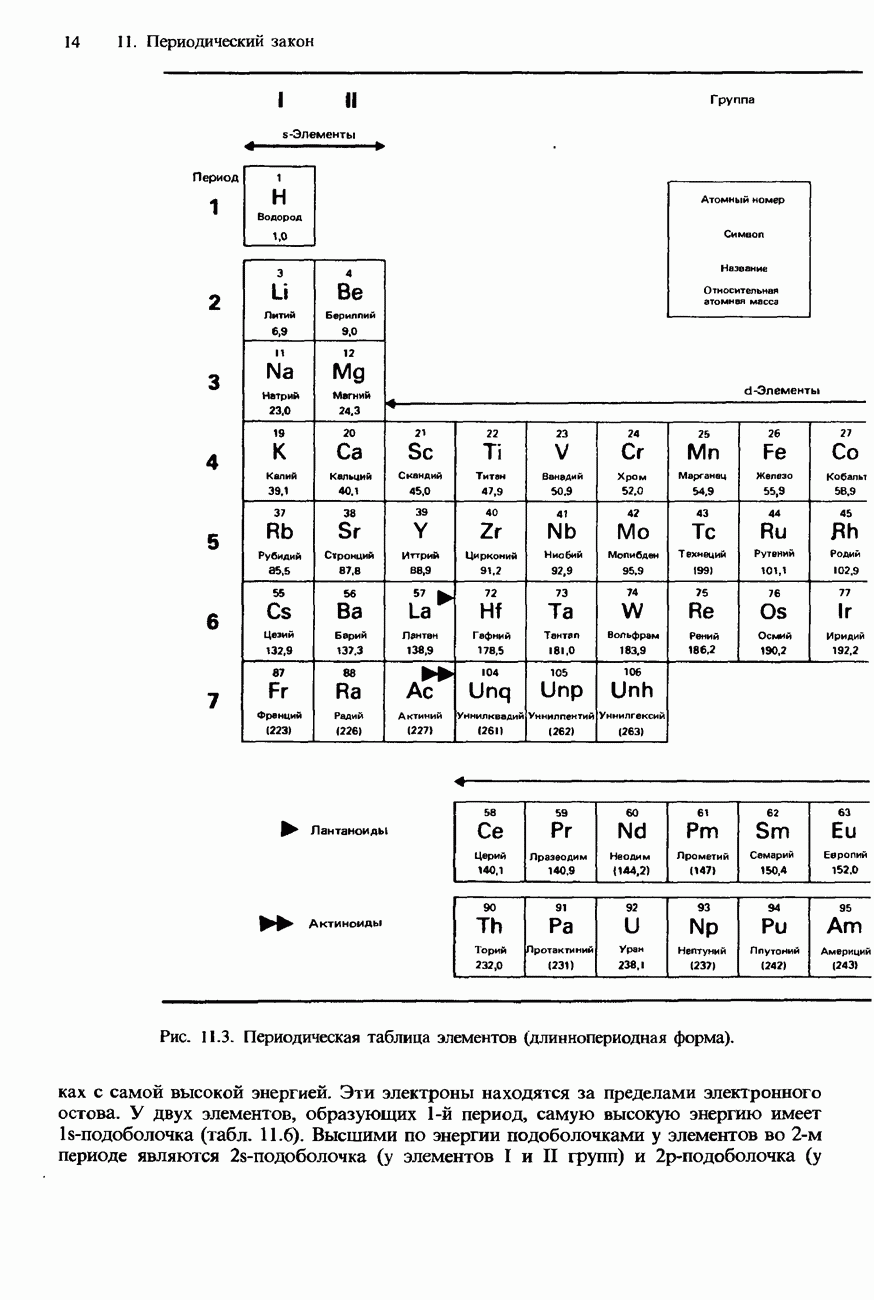
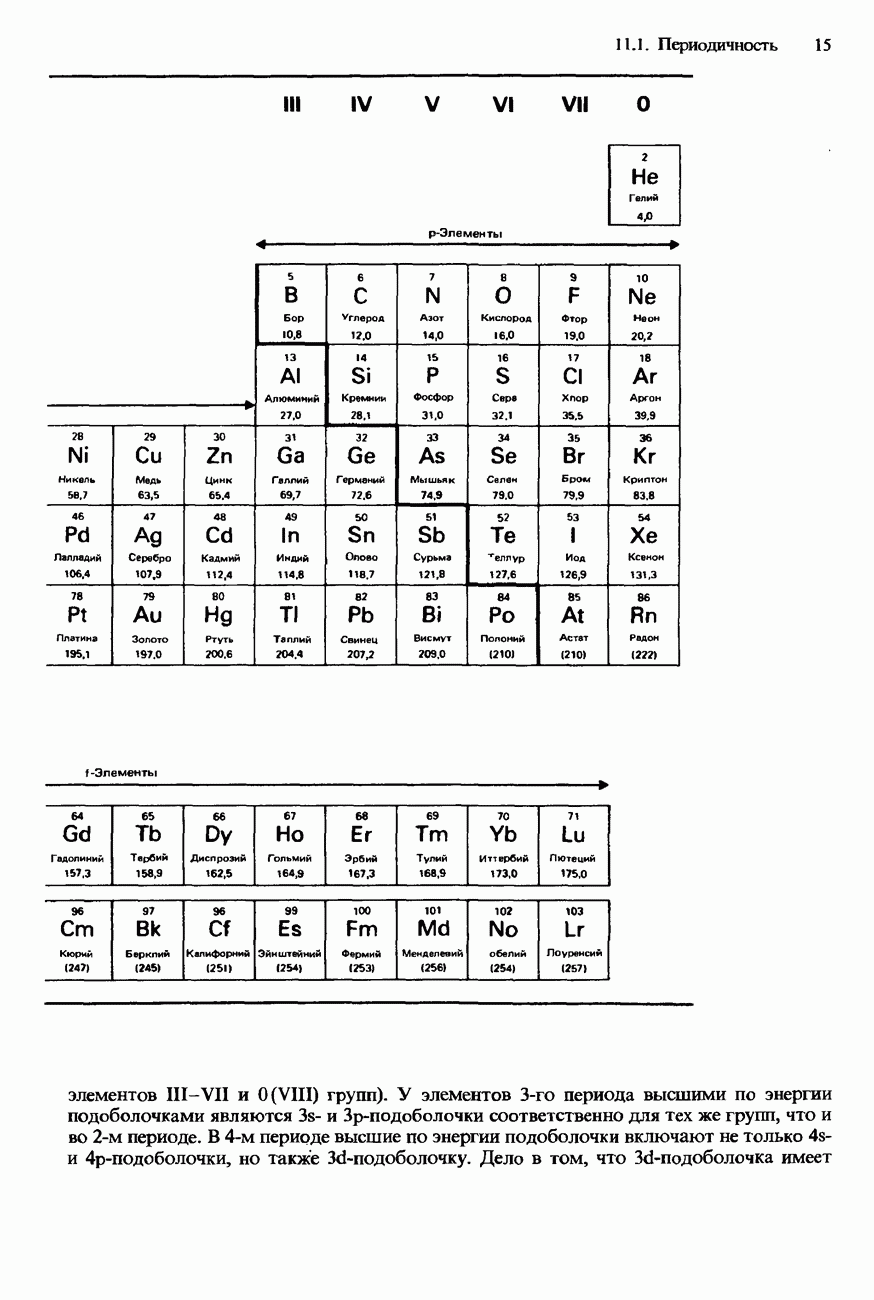
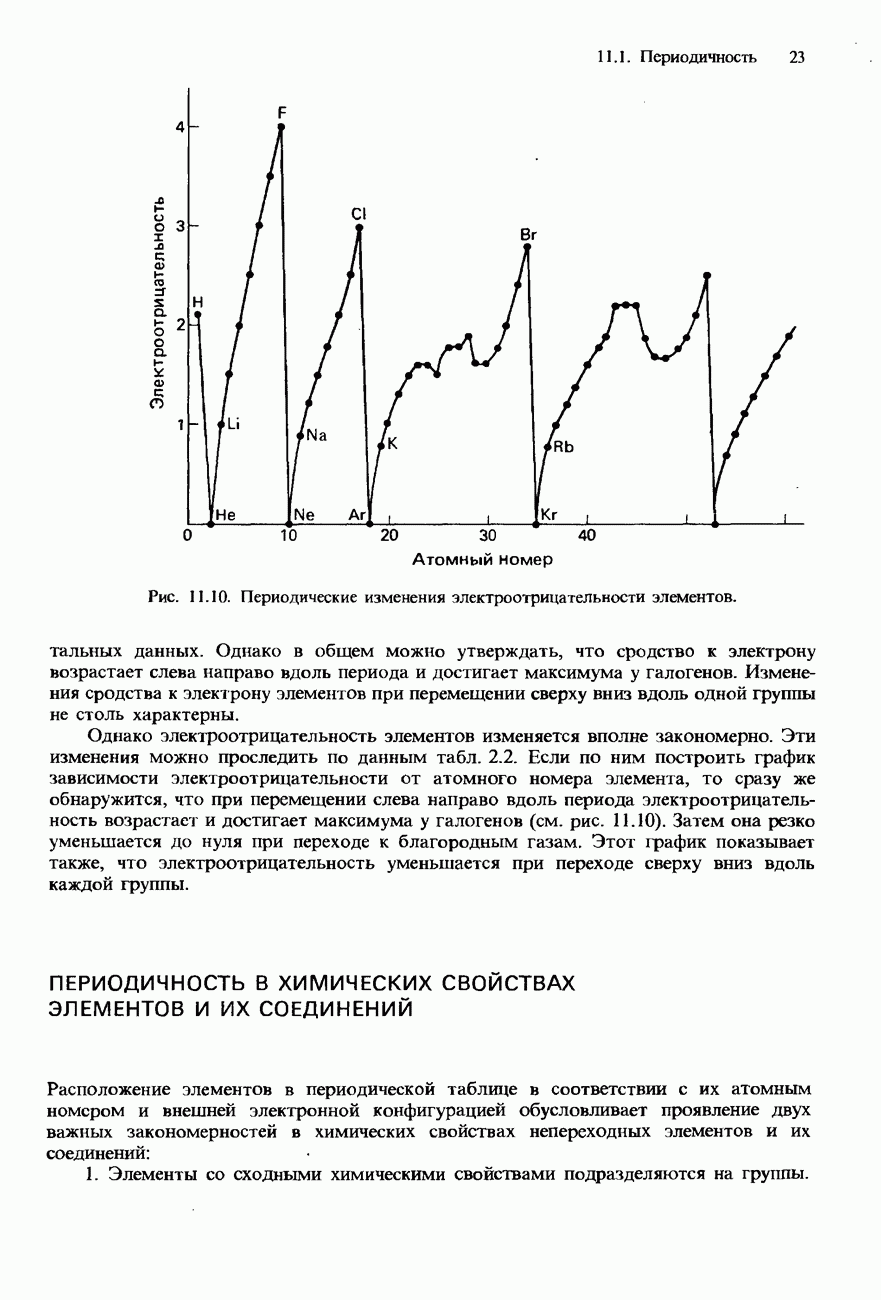
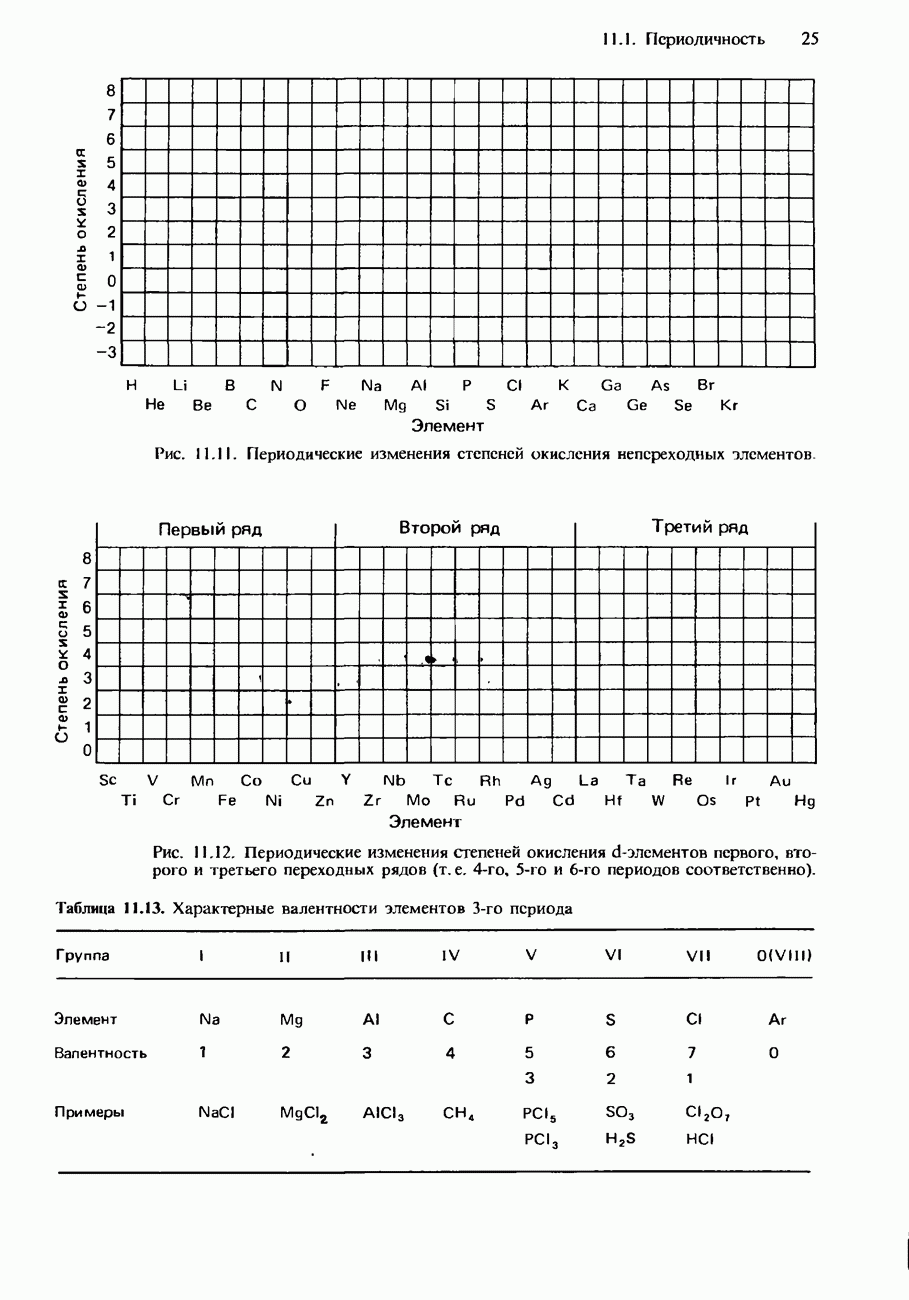
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
- ПЕРИОДИЧНОСТЬ
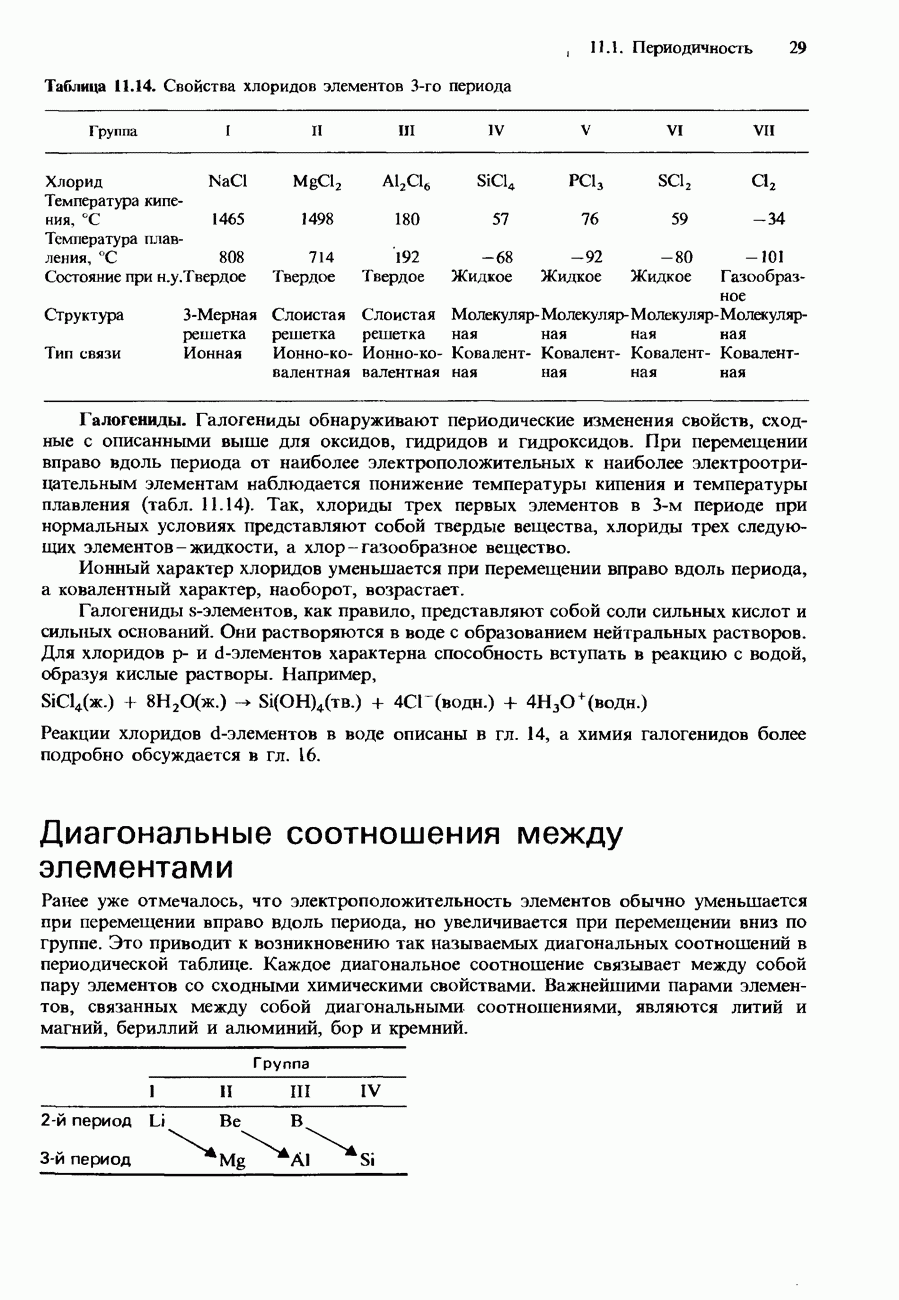
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
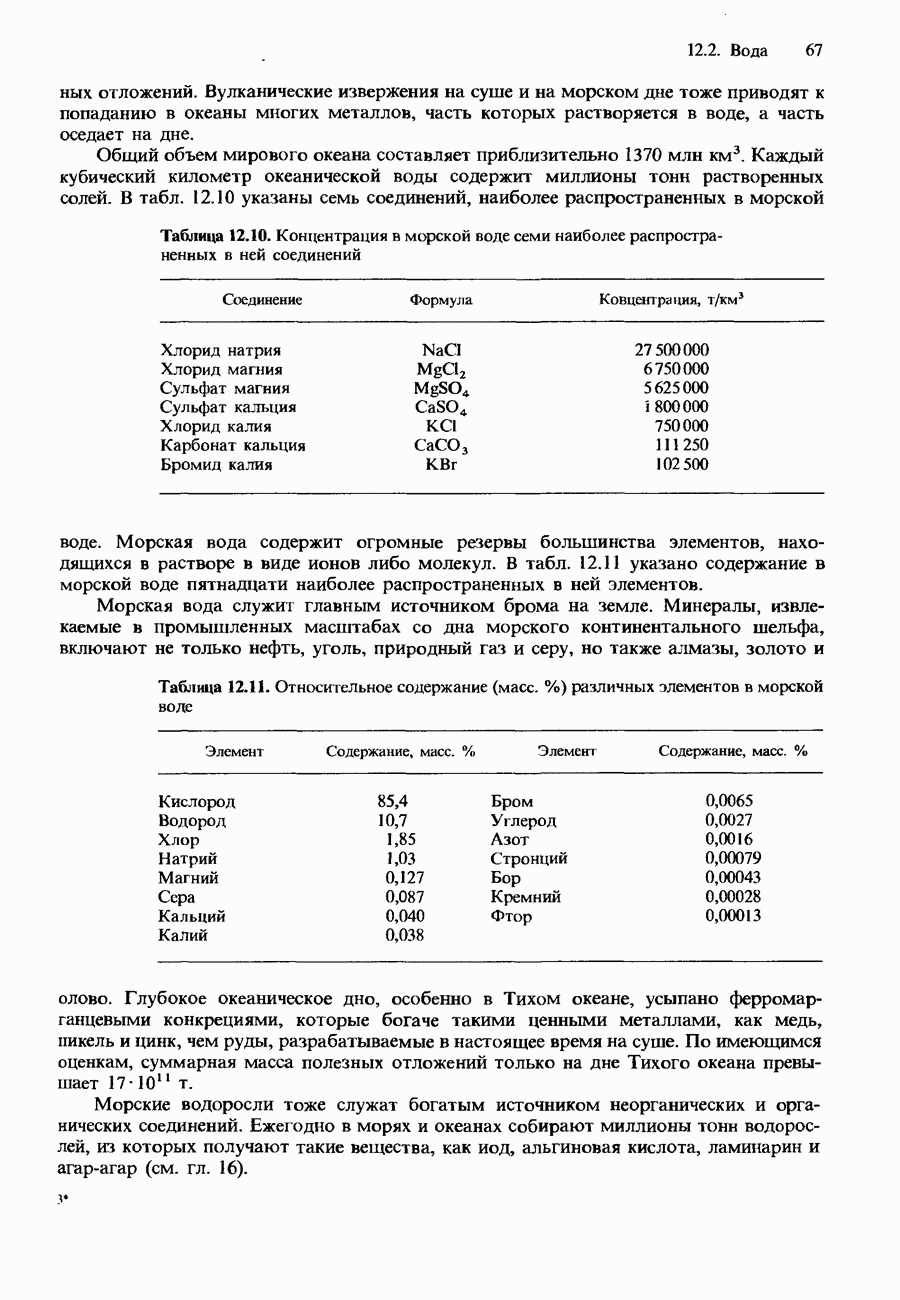
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
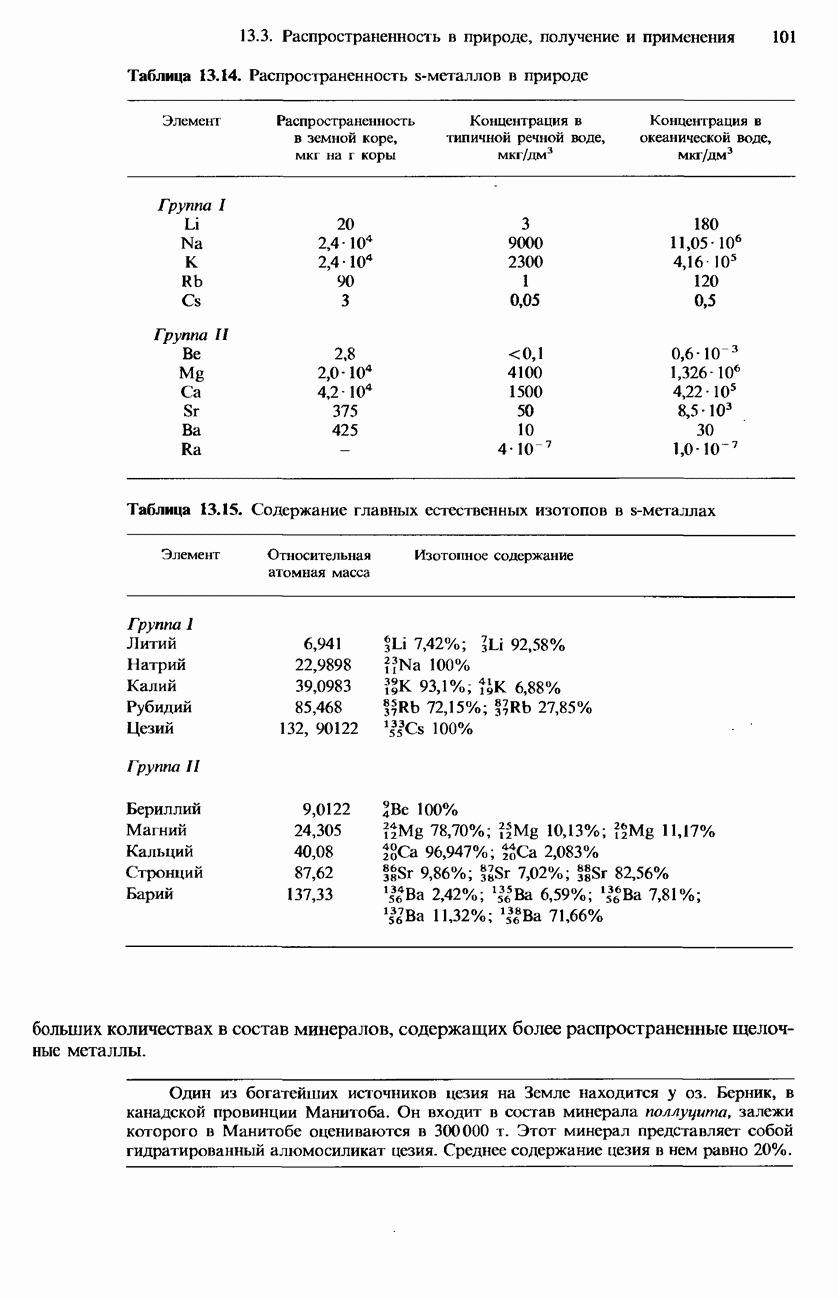
- 13.3. Распространенность в природе, получение и применение
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
- 16.3. Распространенность, получение и применение галогенов и их соединений
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
- 16.4. Благородные газы
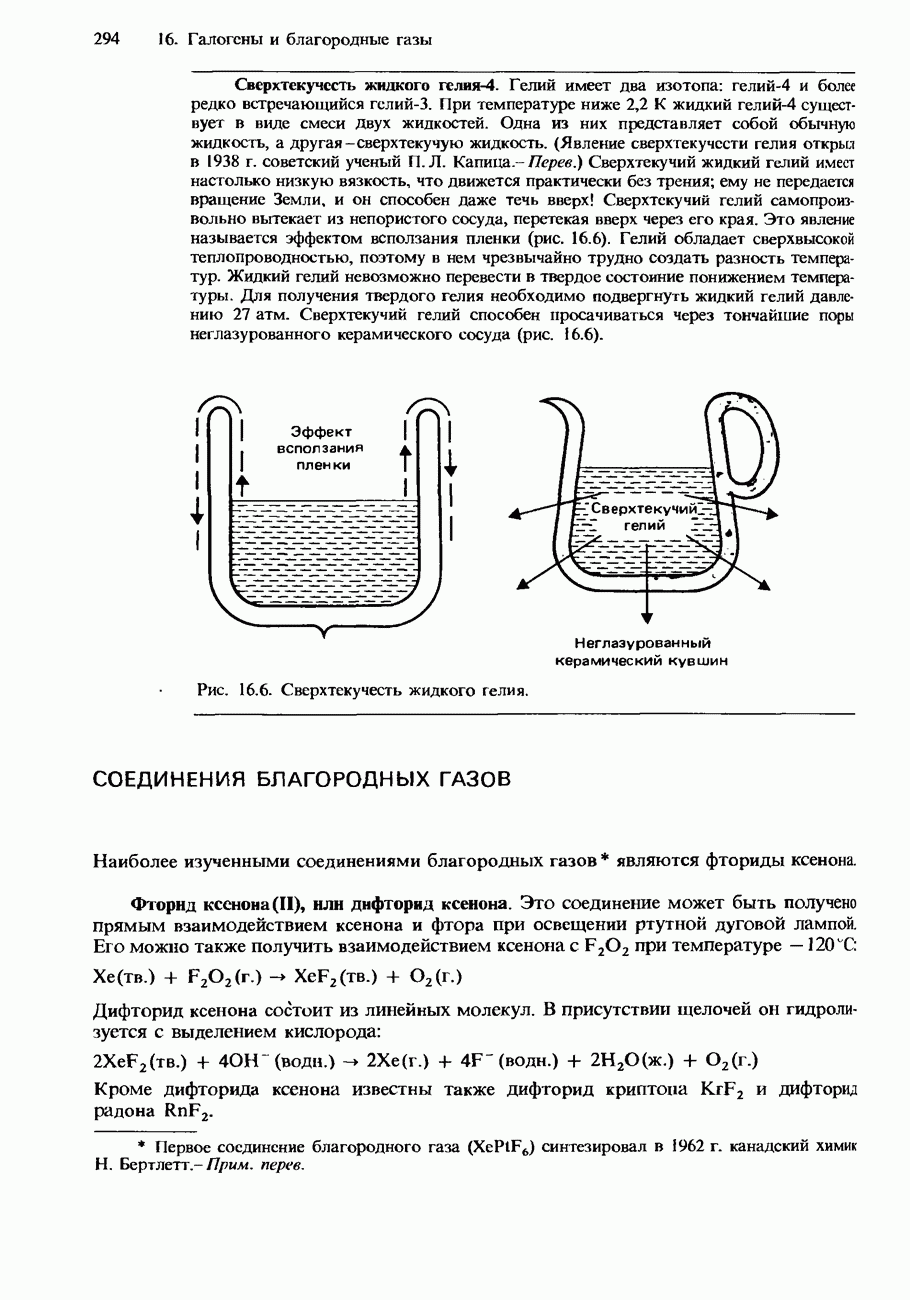
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
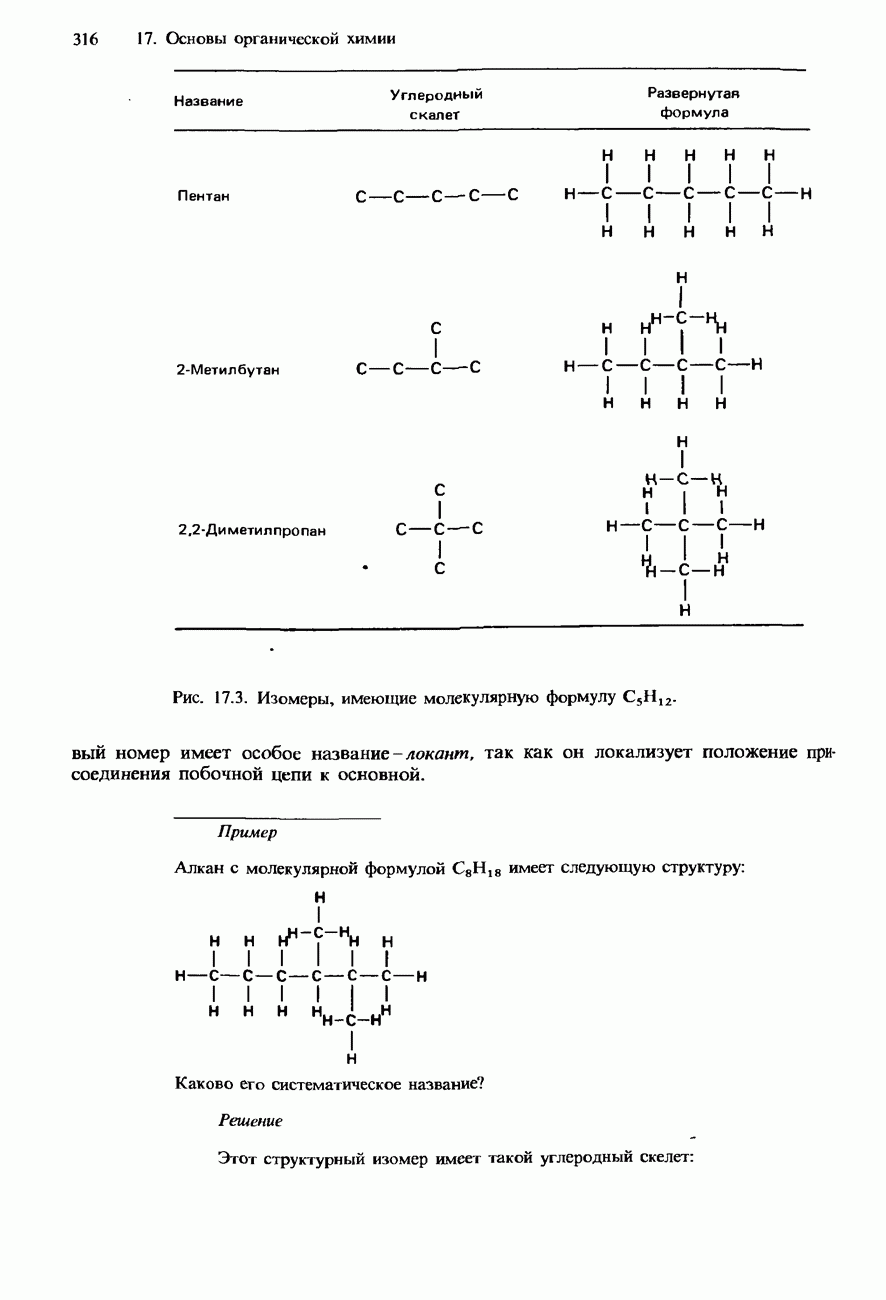
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
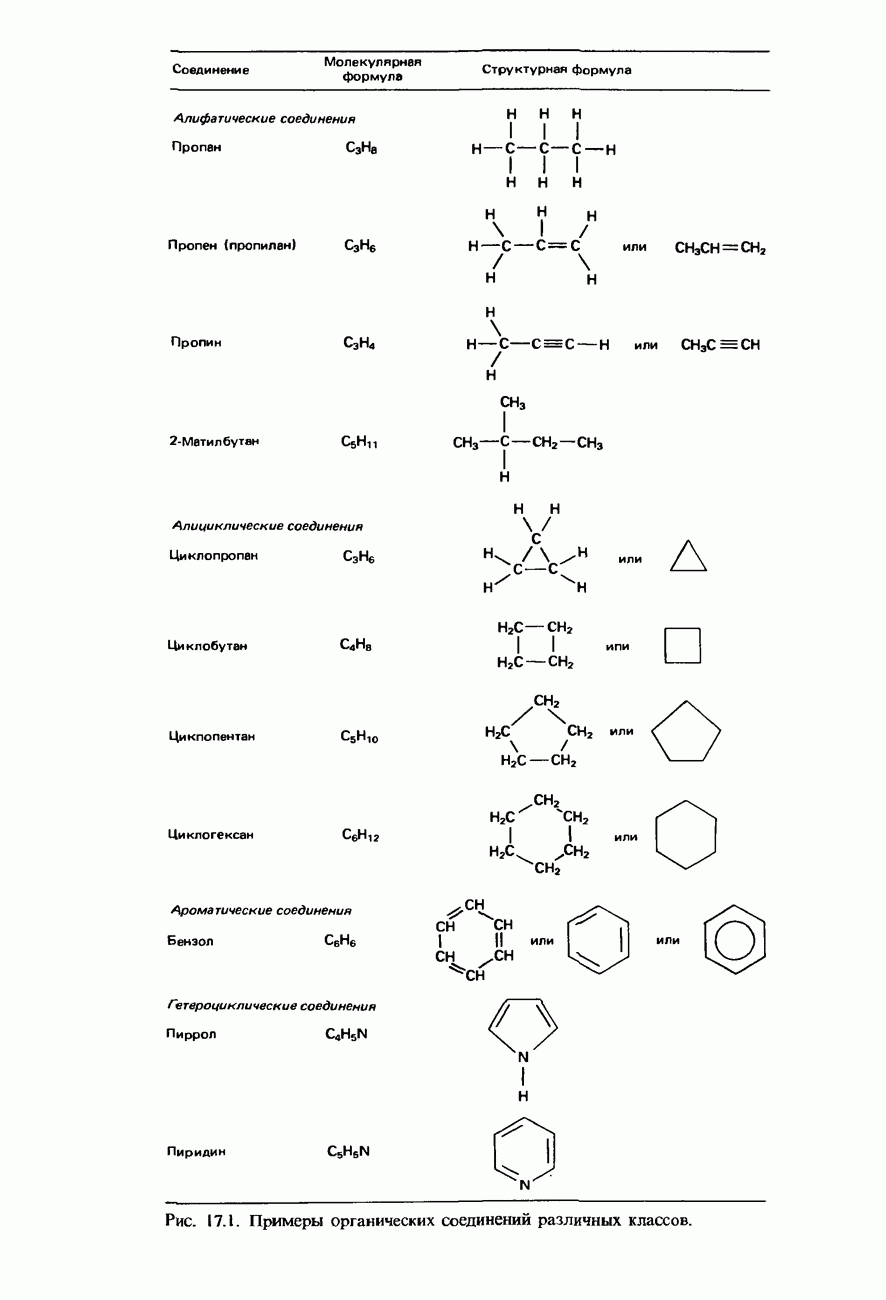
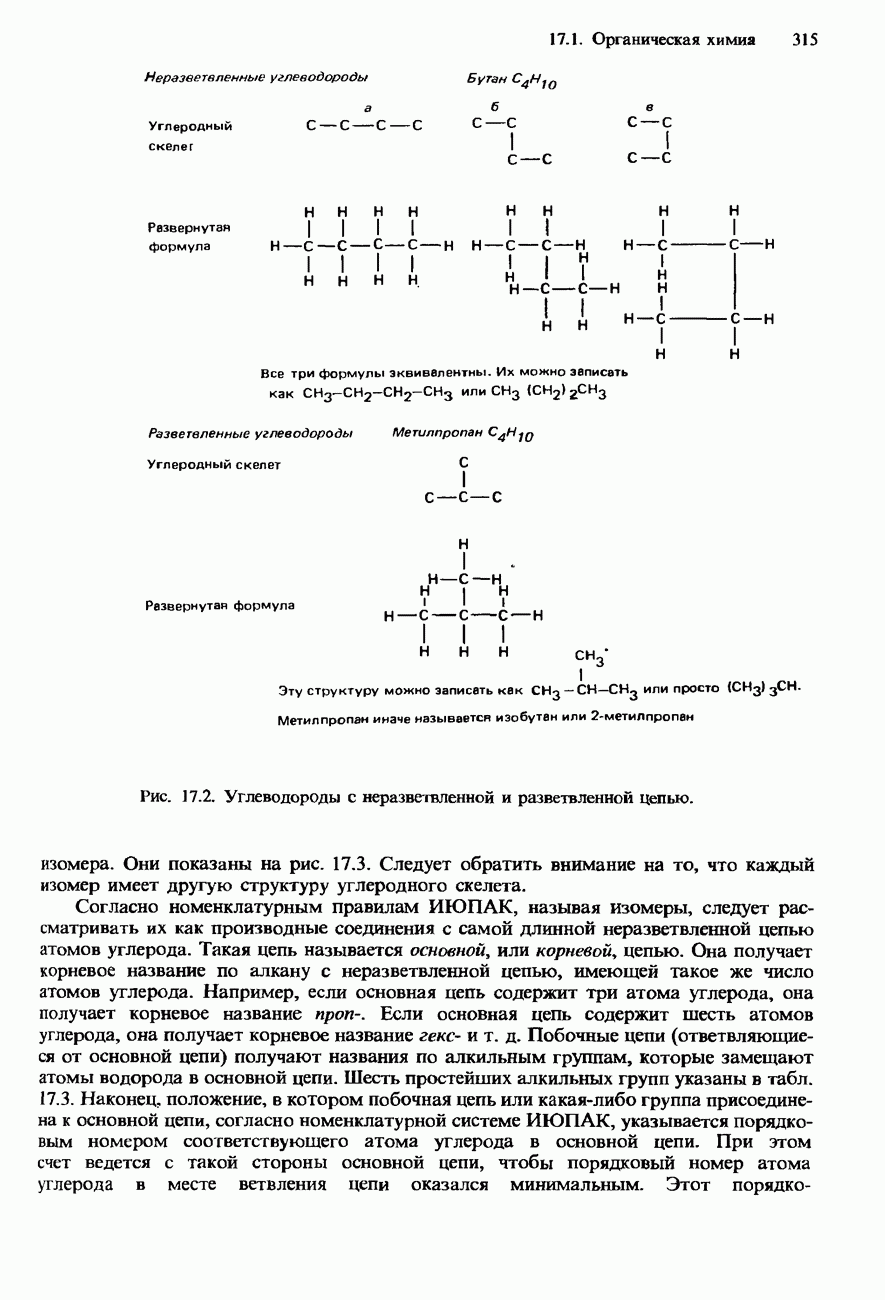
- УГЛЕВОДОРОДЫ
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
- 18.2. Арены
- БЕНЗОЛ
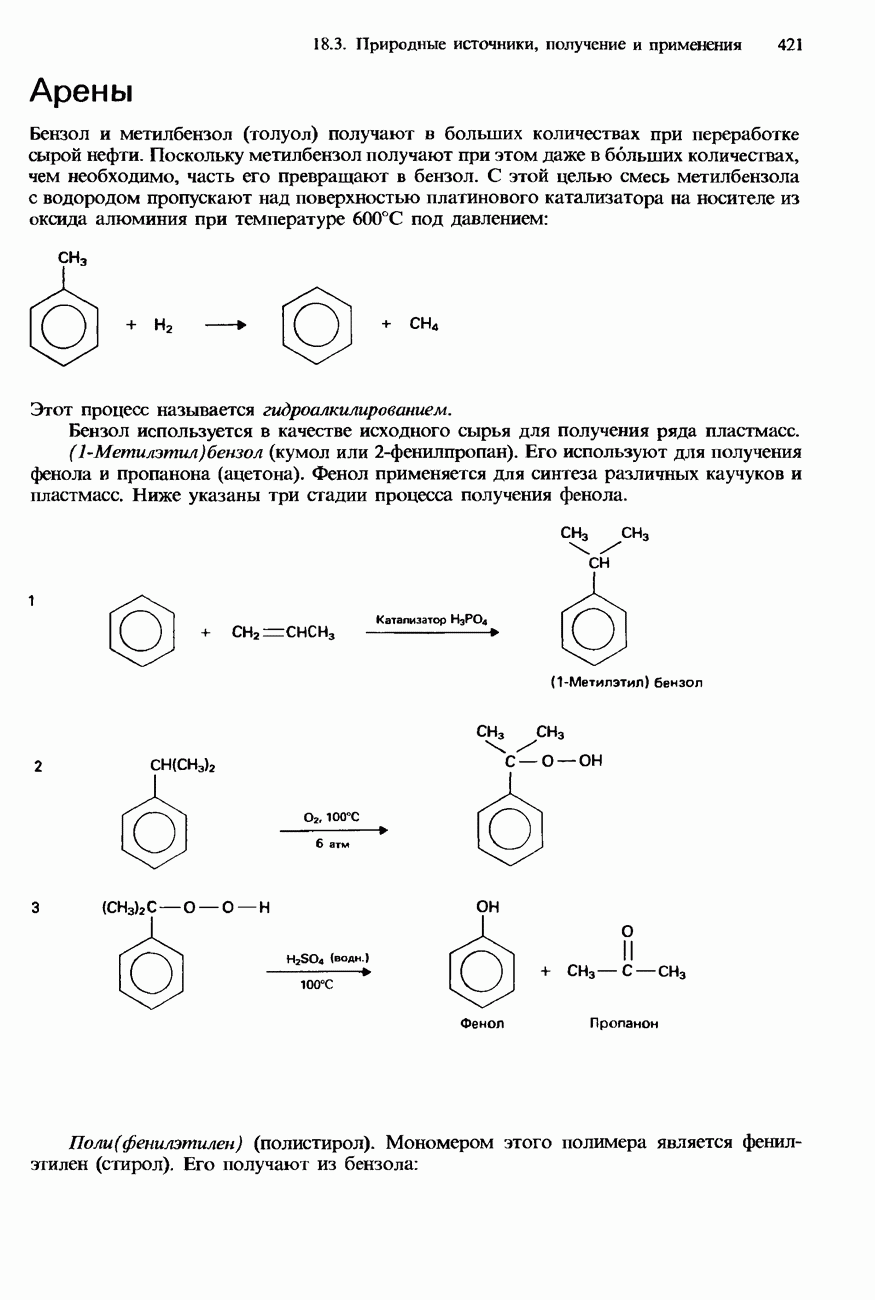
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
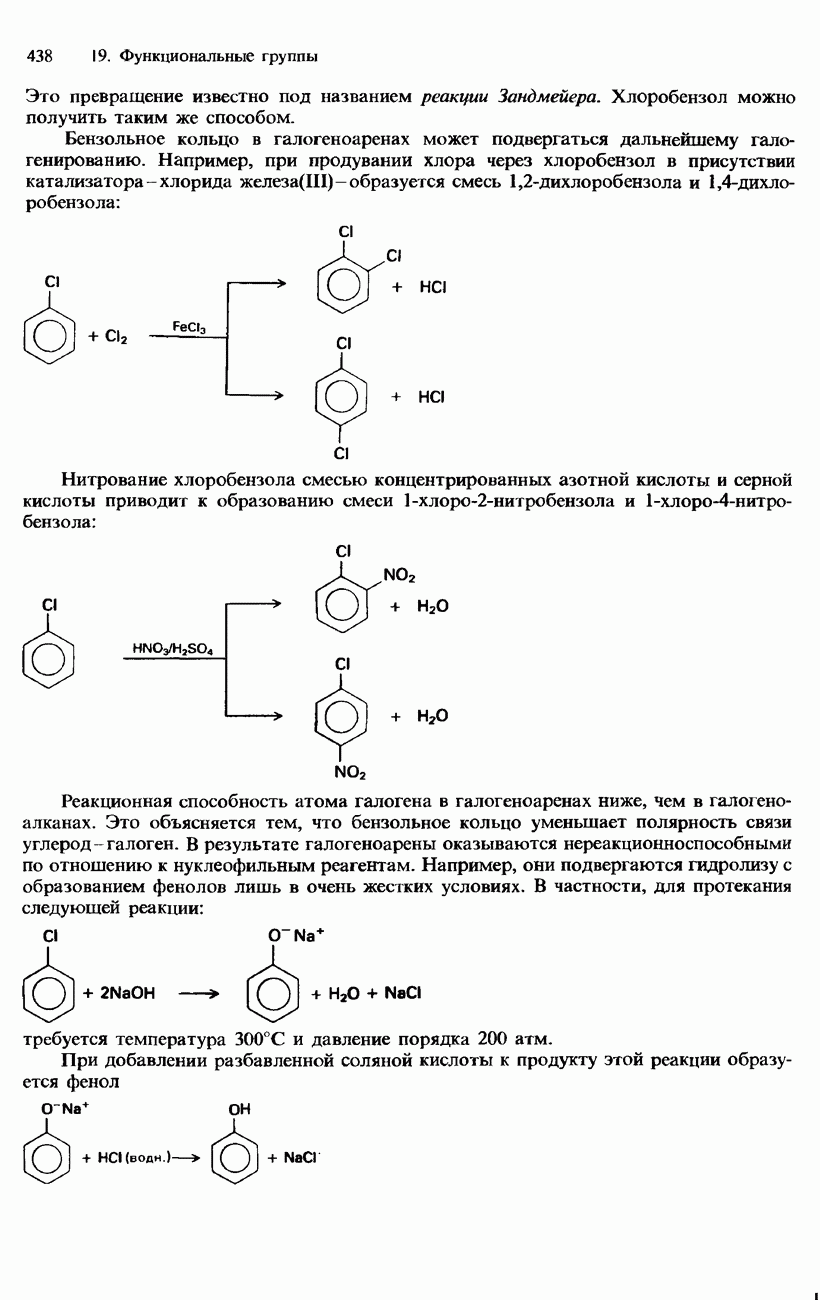
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
- 19.2. Спирты, фенолы и эфиры
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
- 19.3. Карбонильная группа
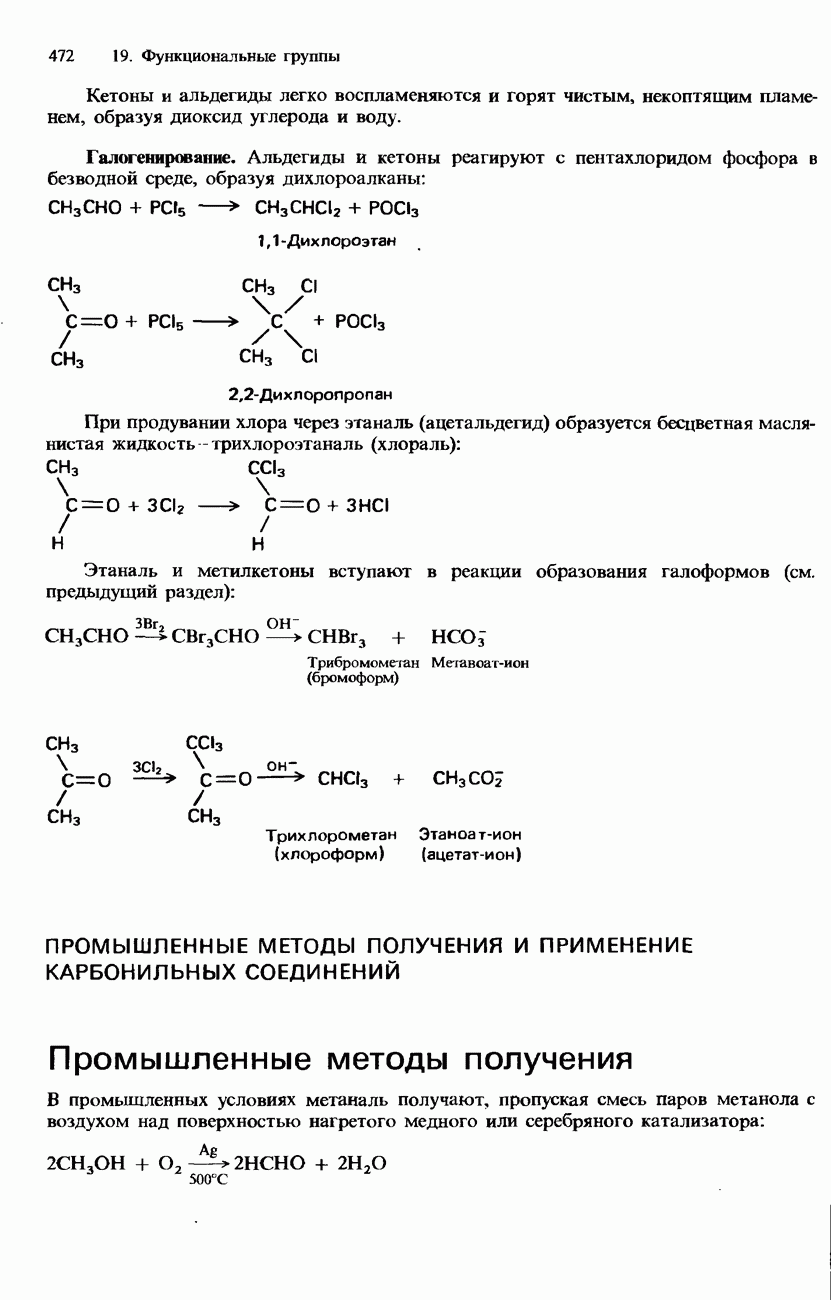
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
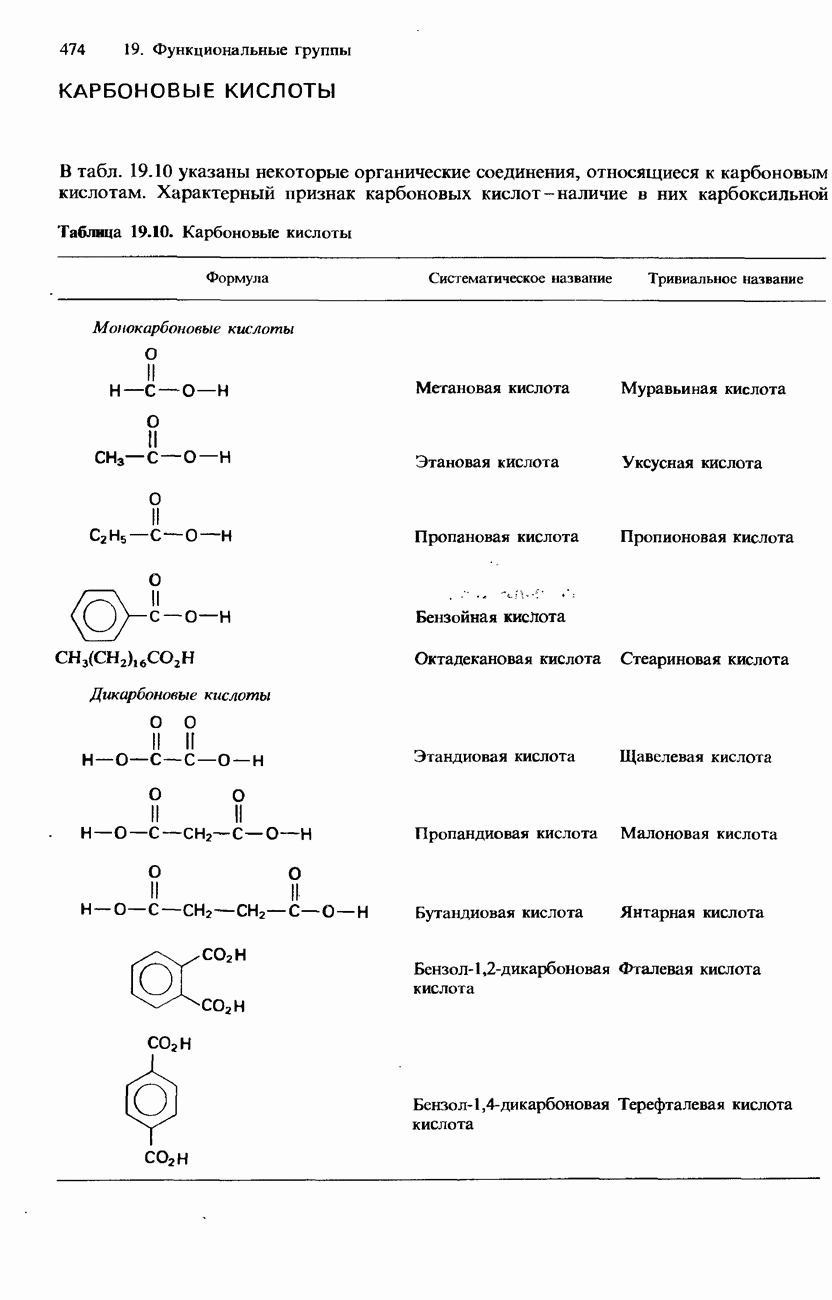
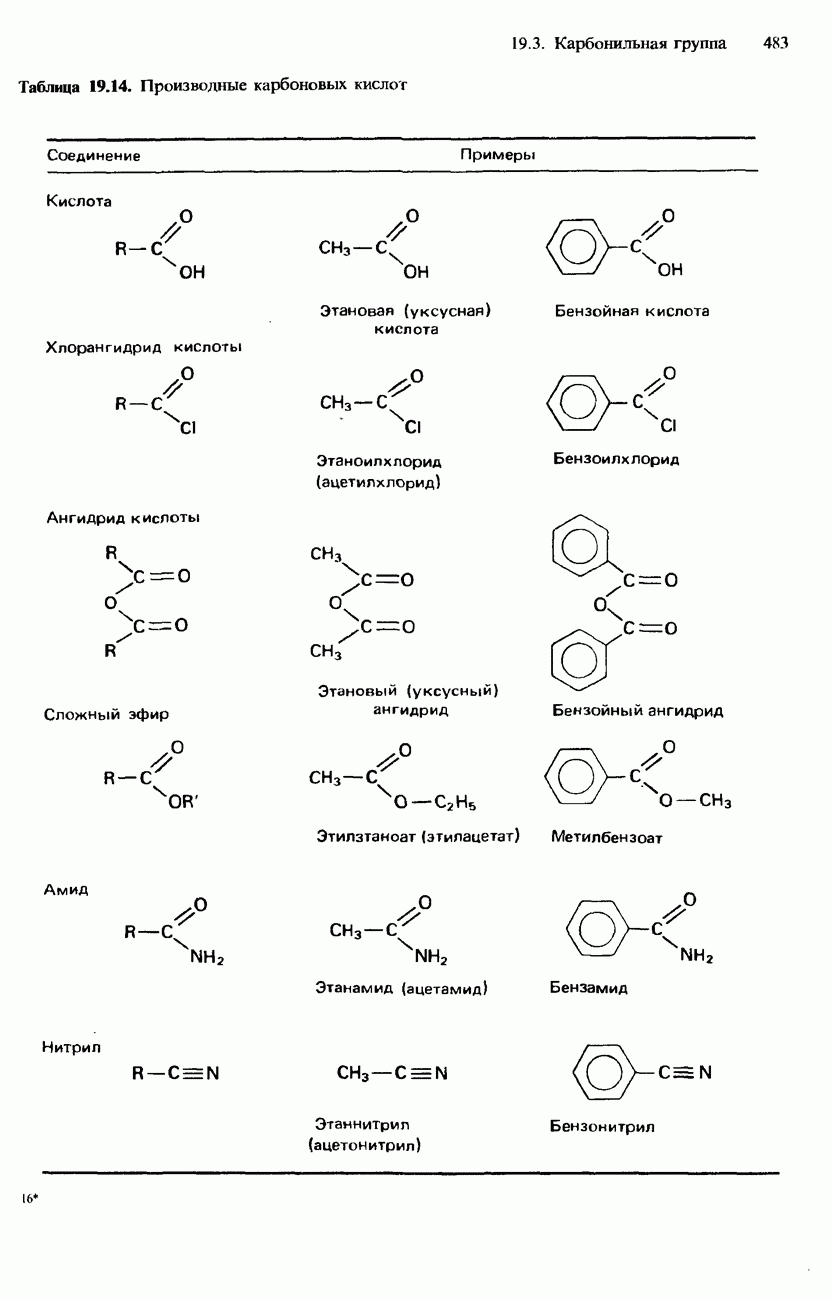
- КАРБОНОВЫЕ КИСЛОТЫ
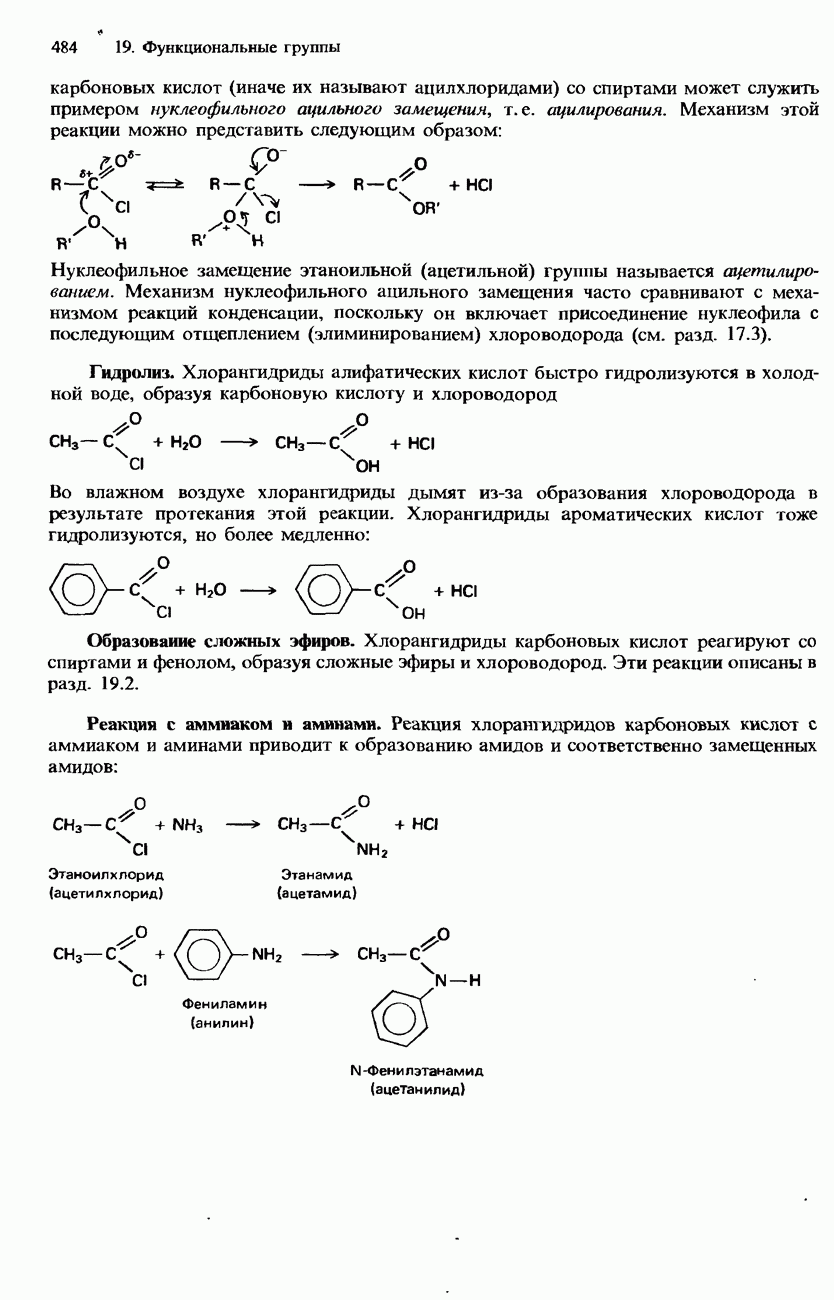
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
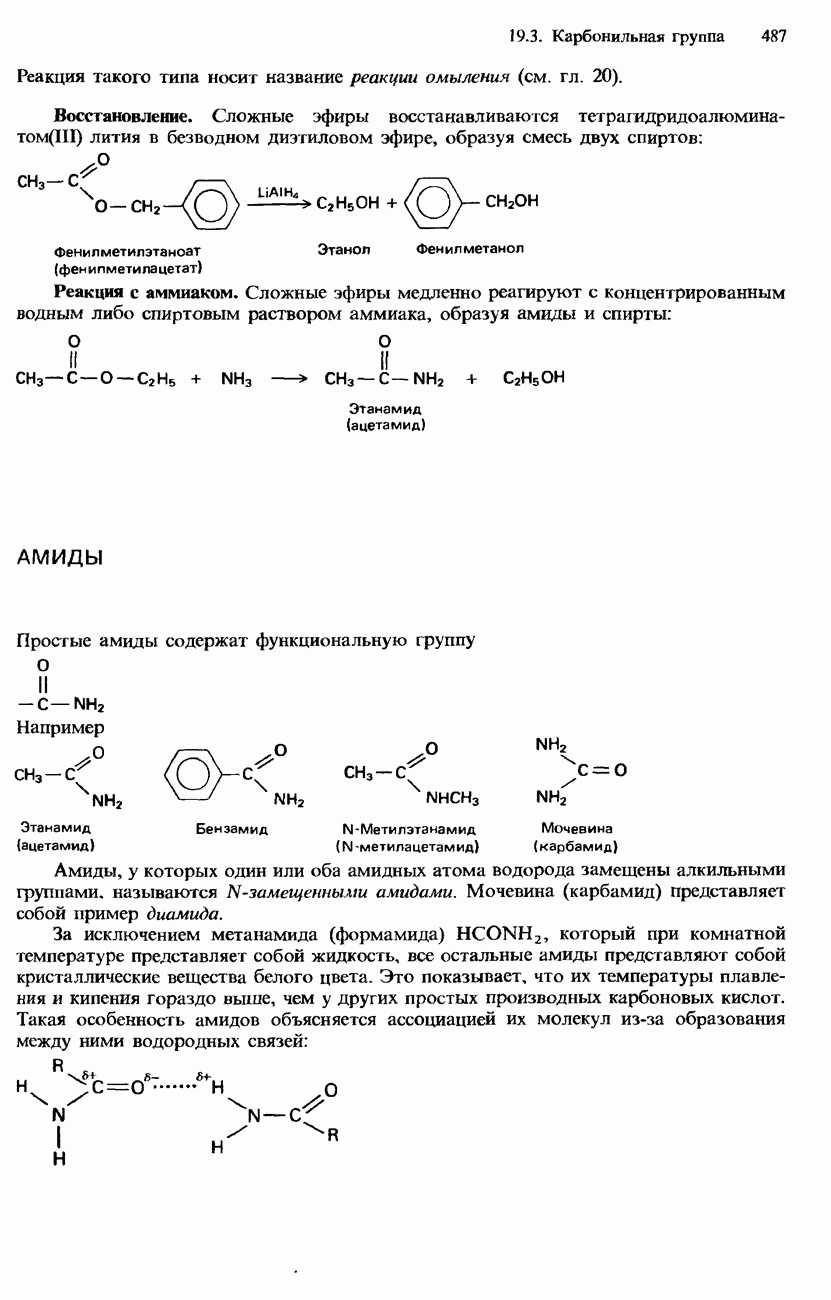
- АМИДЫ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
- 19.4 Амины и родственные соединения
- СОЛИ ДИАЗОНИЯ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
- 20.2. Углеводы и нуклеиновые кислоты
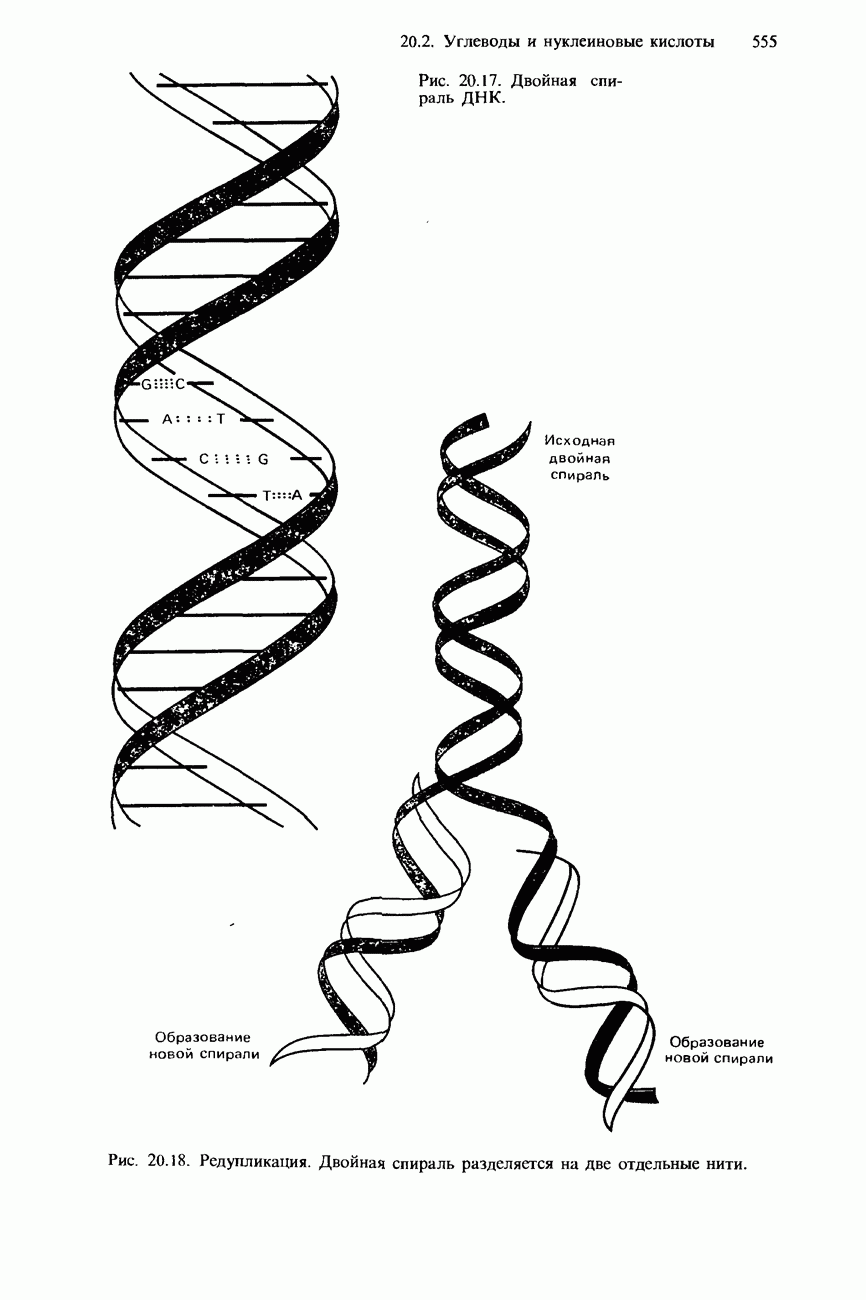
- НУКЛЕИНОВЫЕ КИСЛОТЫ
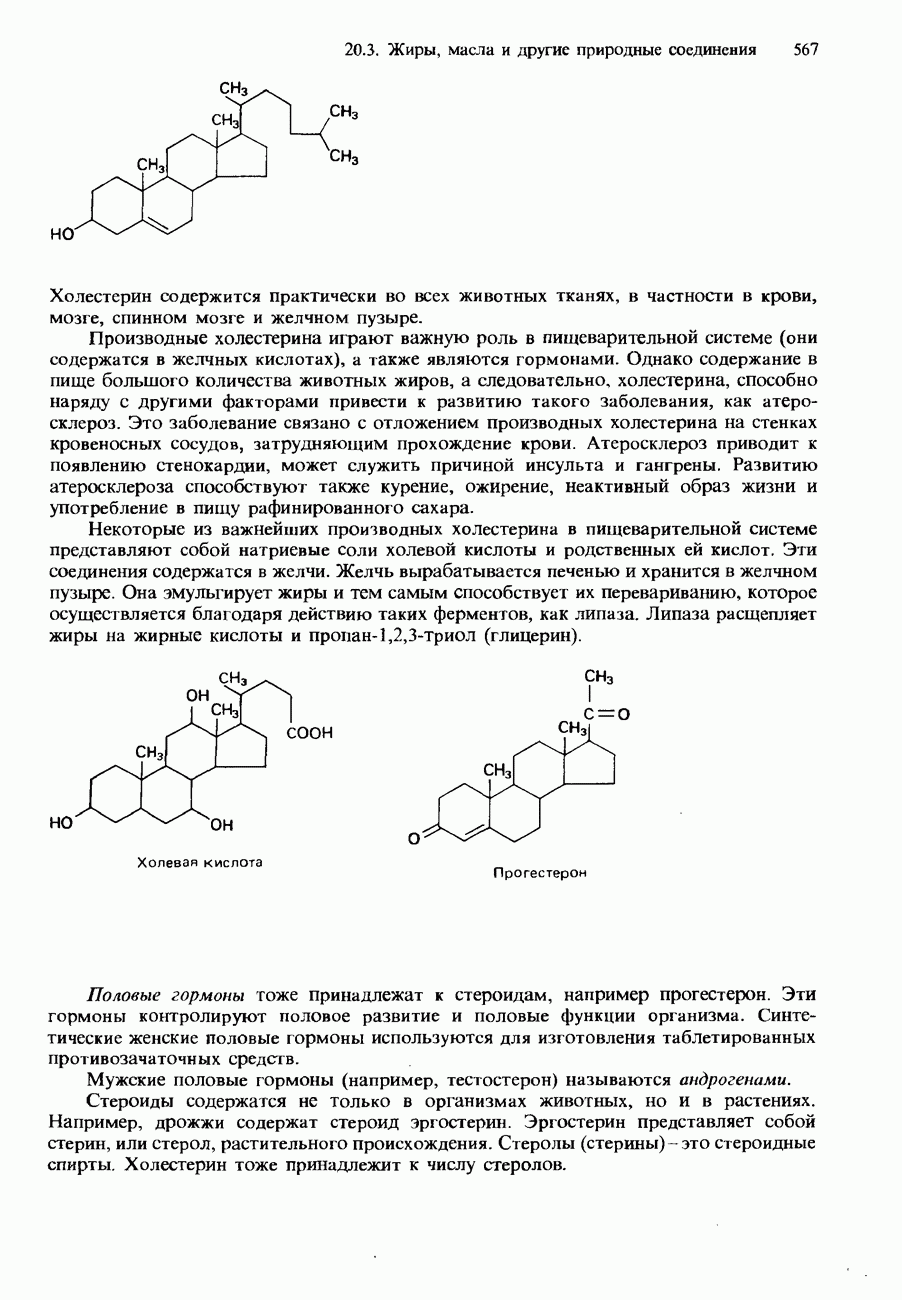
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
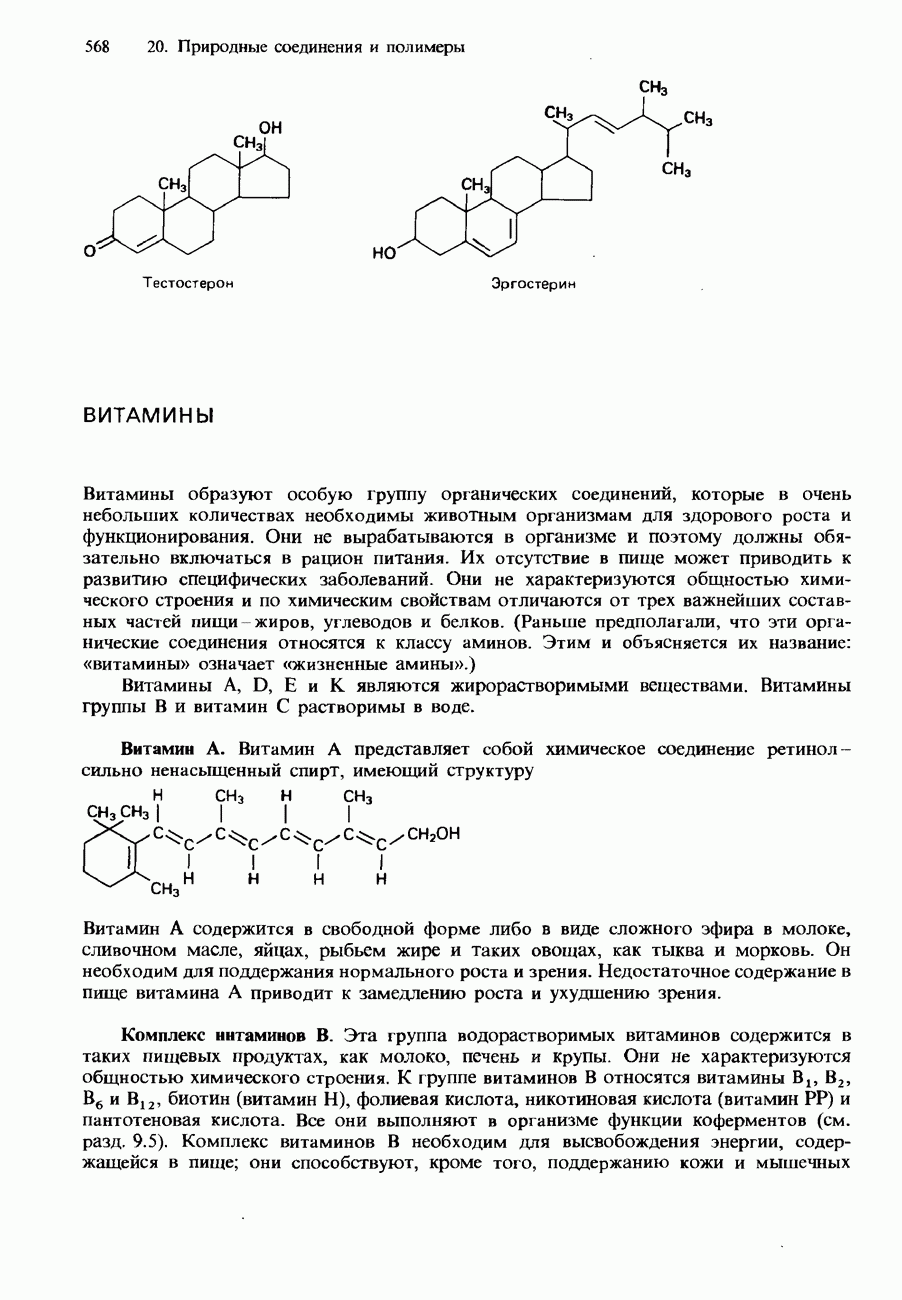
- ВИТАМИНЫ
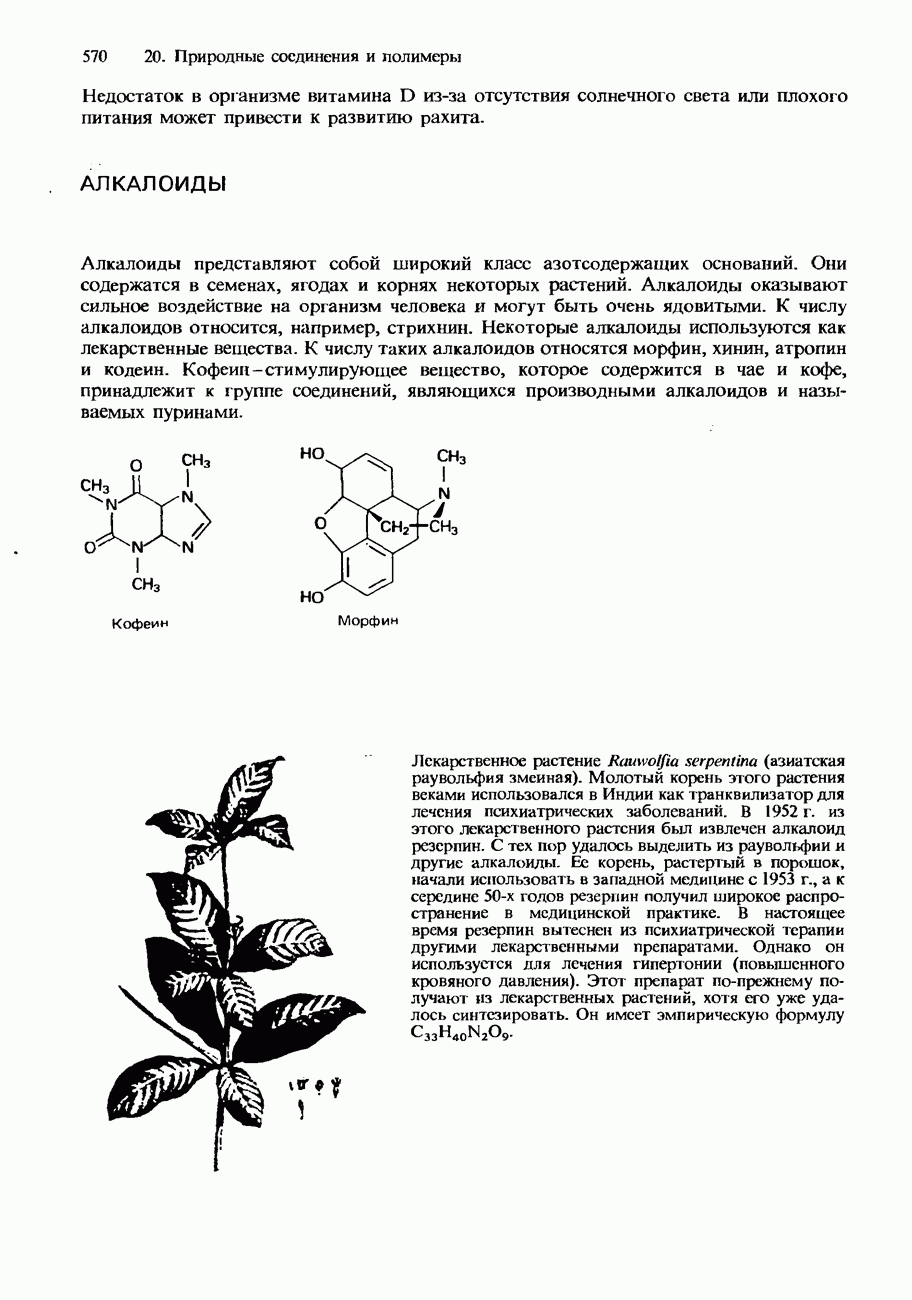
- АЛКАЛОИДЫ
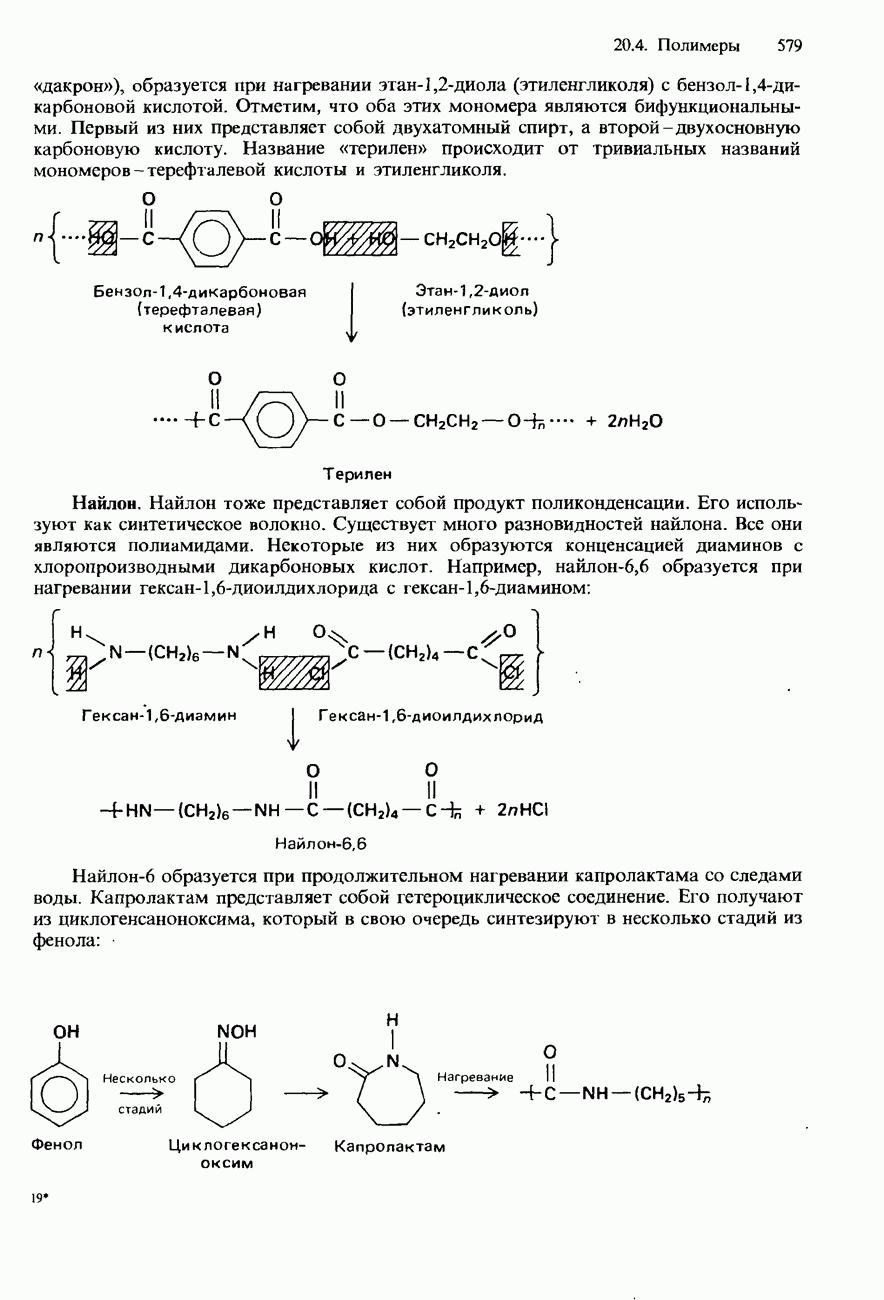
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
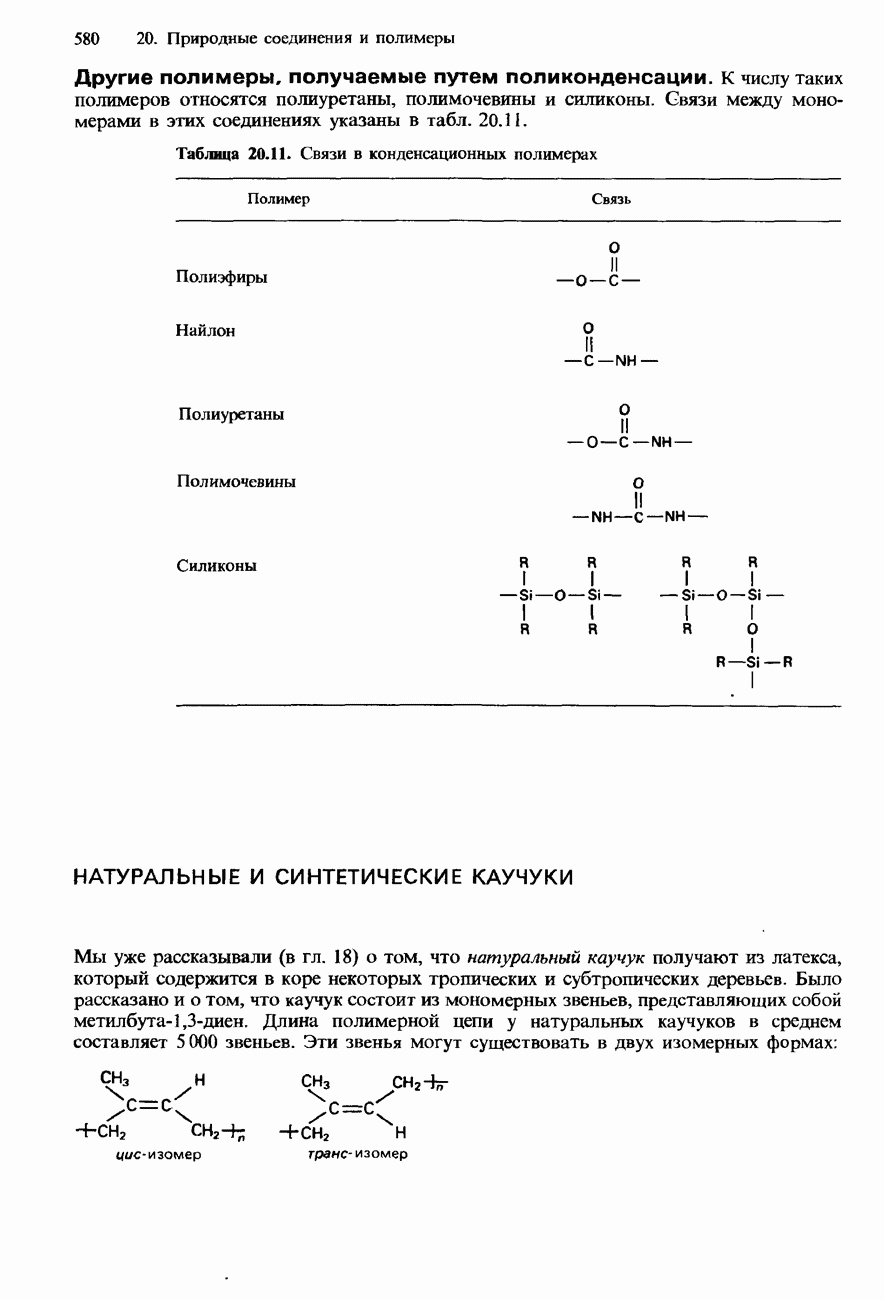
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ