| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
16.3. Распространенность, получение и применение галогенов и их соединений
РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ
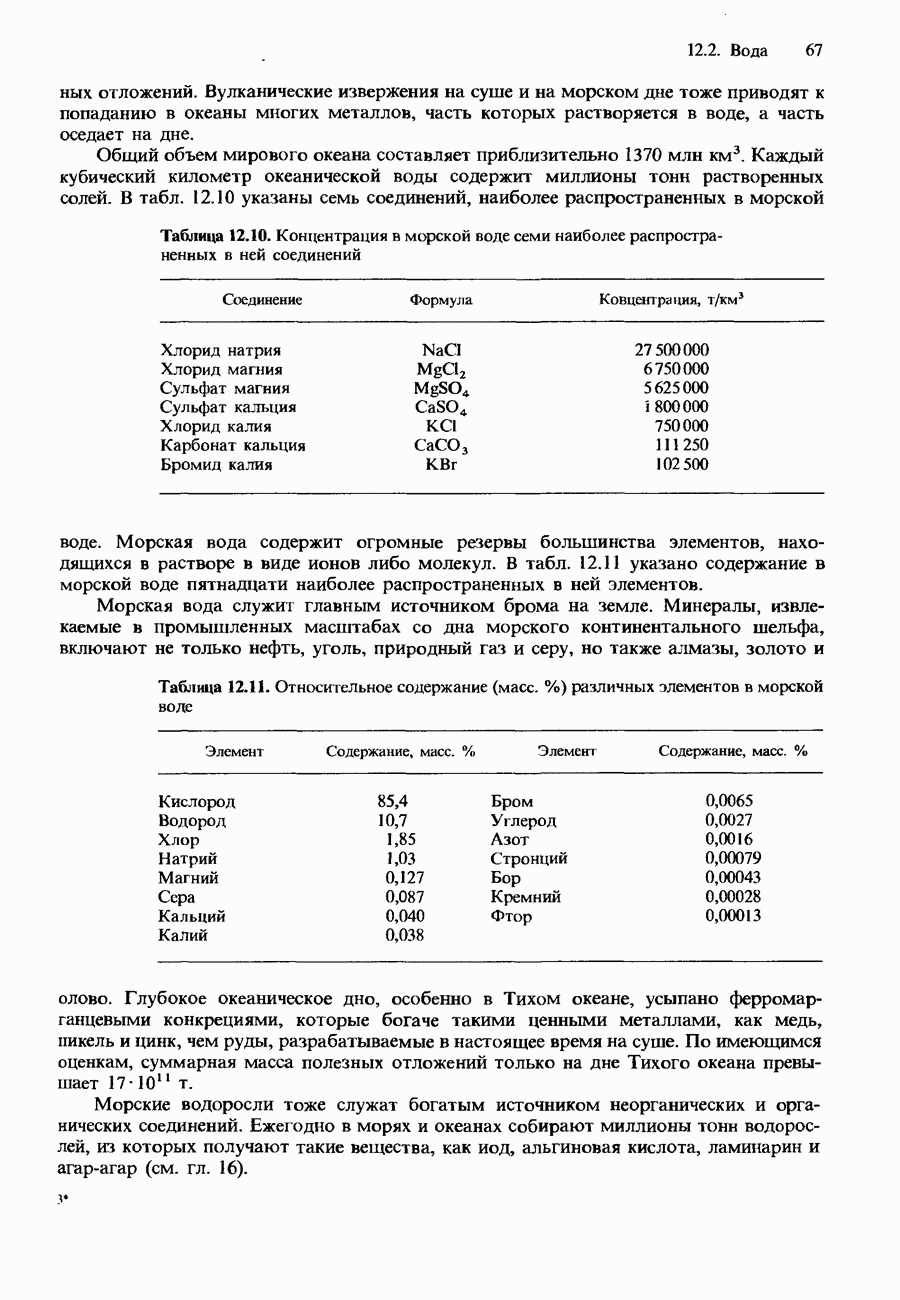
Из-за высокой реакционной способности галогены не встречаются в природе в свободном состоянии. Они существуют в виде солей в земной коре или в виде ионов в морской воде. Их соли очень легко растворимы, особенно при повышенных температурах. Поэтому они обнаруживаются главным образом в тех частях земной коры, которые сформировались при сравнительно невысоких температурах. Со времени образования земной коры огромные количества этих солей растворились в океанической воде. Средняя соленость океанической воды приблизительно равна  промилле - тысячные доли; подробнее о солености см. ниже). В замкнутых морских водоемах или озерах испарение воды приводило
промилле - тысячные доли; подробнее о солености см. ниже). В замкнутых морских водоемах или озерах испарение воды приводило
к повышению концентрации соли. В результате на дне таких водоемов происходило отложение слоев соли. Даже пресноводные озера постепенно становятся солеными вследствие такого же процесса. В качестве примера можно указать Большое Соленое Озеро в США.
Соленость. Соленостью (в промилле.  ) морской воды считается масса в граммах растворенного неорганического вещества в I кг этой воды. На поверхности океанов соленость колеблется от 34,0 до
) морской воды считается масса в граммах растворенного неорганического вещества в I кг этой воды. На поверхности океанов соленость колеблется от 34,0 до  . В тропиках она выше из-за более интенсивного испарения и сравнительно редкого выпадения дождей. В экваториальных регионах соленость оказывается ниже из-за более слабых ветров и более сильного выпадения дождей. Пониженная соленость обнаруживается также в прибрежной зоне континентальных шельфов из-за разбавления морской воды пресными водами рек. Более высокую соленость имеют внутренние, изолированные от океана моря. Например, соленость Средиземного моря достигает
. В тропиках она выше из-за более интенсивного испарения и сравнительно редкого выпадения дождей. В экваториальных регионах соленость оказывается ниже из-за более слабых ветров и более сильного выпадения дождей. Пониженная соленость обнаруживается также в прибрежной зоне континентальных шельфов из-за разбавления морской воды пресными водами рек. Более высокую соленость имеют внутренние, изолированные от океана моря. Например, соленость Средиземного моря достигает  а соленость Красного моря
а соленость Красного моря  Соленость Мертвого моря, имеющего самый низкий уровень на земной поверхности, достигает
Соленость Мертвого моря, имеющего самый низкий уровень на земной поверхности, достигает 
В табл. 16.13 указано содержание галогенов в земной коре, а также в речной и океанической водах. В морской воде, подземных соленых водах и речной воде галогены существуют в виде галогенид-ионов. Иод, кроме того, существует в воде в форме  -ионов.
-ионов.
Фтор обнаруживается во всех природных водах, в костных тканях, зубах, крови и во всех растениях. В земной коре он встречается главным образом в виде полевого шпата  (табл. 16.14). Этот минерал имеет кубическую кристаллическую структуру, известную под названием структура флюорита (см. разд. 3.2). Другим минералом
(табл. 16.14). Этот минерал имеет кубическую кристаллическую структуру, известную под названием структура флюорита (см. разд. 3.2). Другим минералом
Таблица 16.13. Распространенность галогенов в природе

Таблица 16.14. Важнейшие месторождения минералов, содержащих галогены

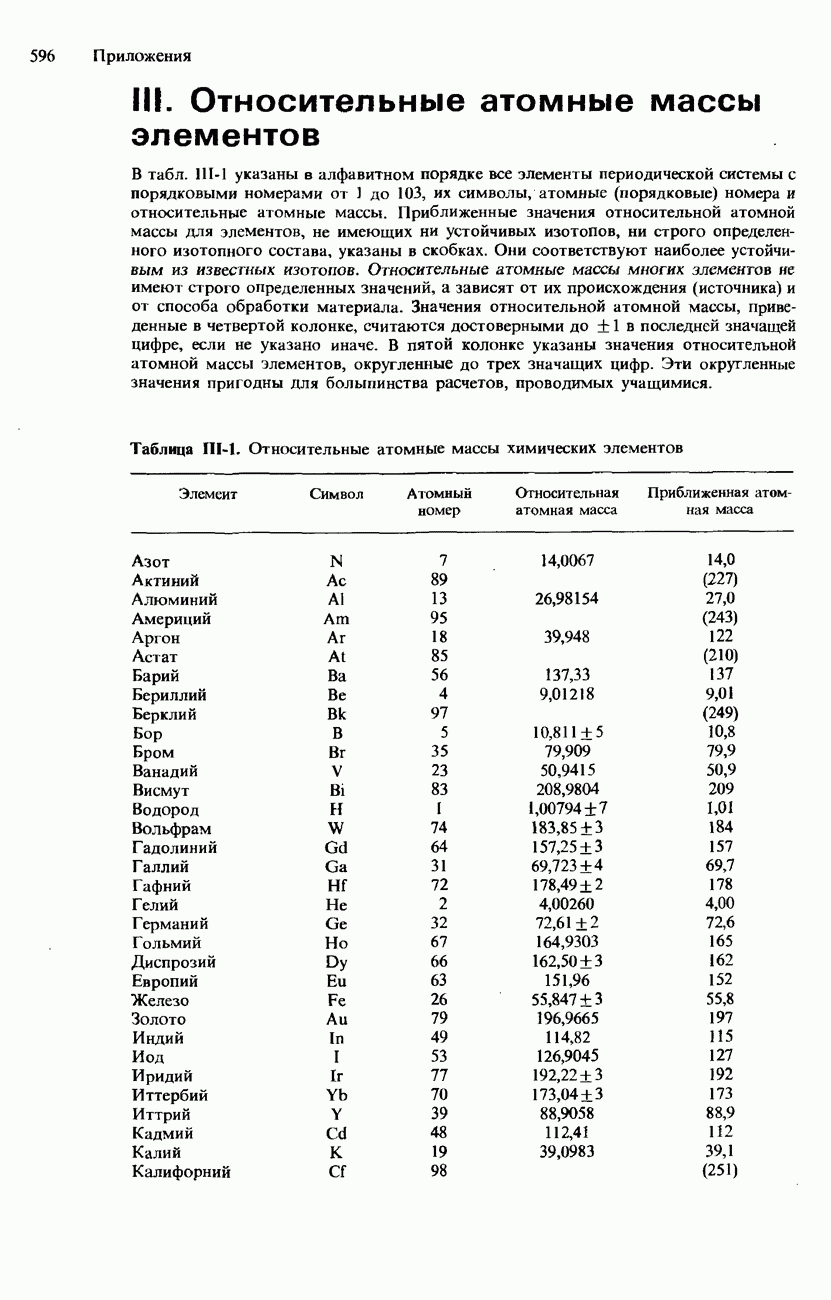
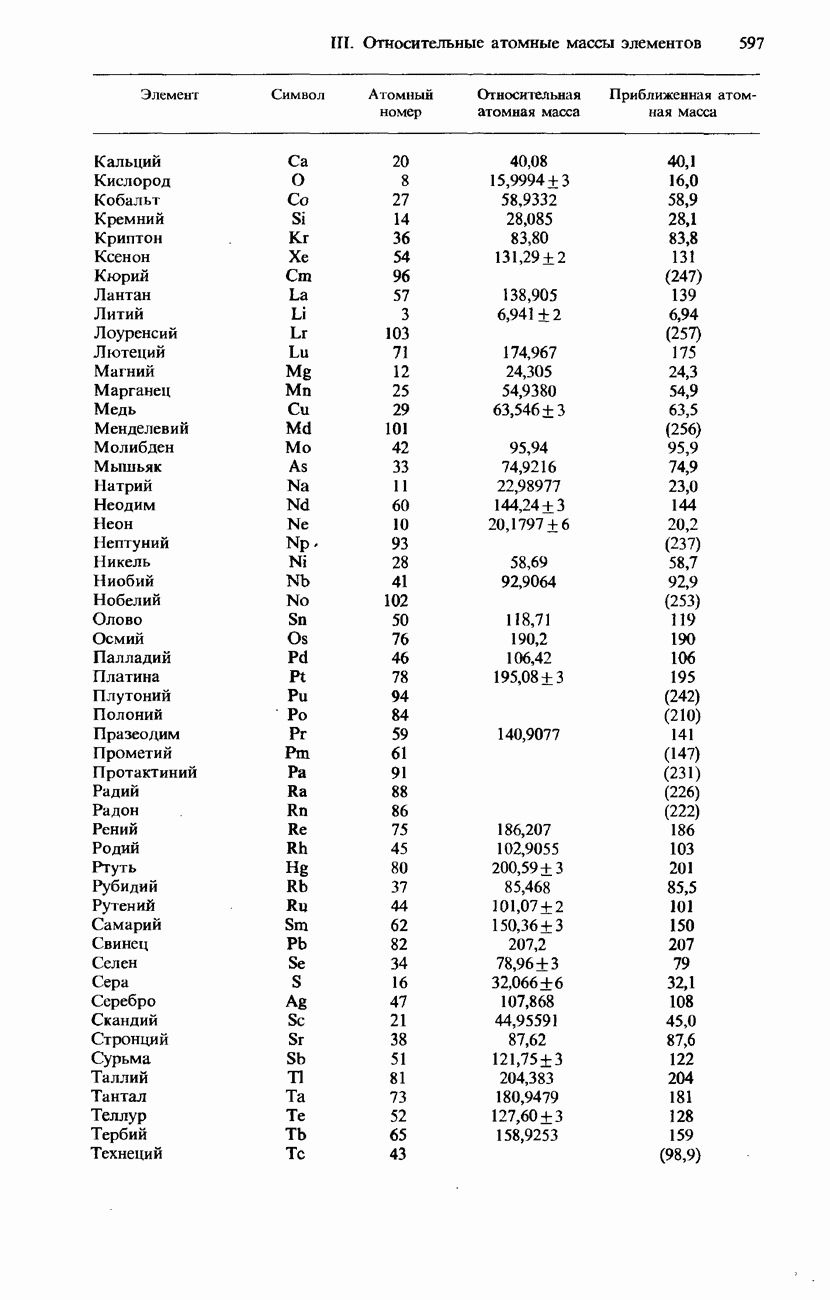
Таблица 16.15. Естественное изотопное содержание галогенов

фтора является криолит  Хлор встречается главным образом в составе именной соли
Хлор встречается главным образом в составе именной соли  имеющей кубическую кристаллическую структуру, известную под названием структуры каменной соли. Главным источником брома является морская вода. Иод в виде иодат-ионов входит в состав чилийской селитры
имеющей кубическую кристаллическую структуру, известную под названием структуры каменной соли. Главным источником брома является морская вода. Иод в виде иодат-ионов входит в состав чилийской селитры  и чилийской рудной селитры
и чилийской рудной селитры  Все четыре галогена встречаются также во многих других минералах, часть из которых обнаруживается лишь в сравнительно малых количествах.
Все четыре галогена встречаются также во многих других минералах, часть из которых обнаруживается лишь в сравнительно малых количествах.
Фтор и бром существуют почти исключительно в виде единственного изотопа. Изотопный состав всех галогенов указан в табл. 16.15.
Астат. В настоящее время известно двадцать изотопов этого элемента. Следы четырех его изотопов  встречаются вместе с естественными изотопами урана, тория и нептуния. Наибольшим периодом полураспада (8,6 ч) обладает изотоп
встречаются вместе с естественными изотопами урана, тория и нептуния. Наибольшим периодом полураспада (8,6 ч) обладает изотоп  Общее количество астата во всей земной коре, согласно существующим оценкам, не превышает 30 г. Изотопы
Общее количество астата во всей земной коре, согласно существующим оценкам, не превышает 30 г. Изотопы  были получены при бомбардировке висмута
были получены при бомбардировке висмута  -частицами (см. разд. 1.3):
-частицами (см. разд. 1.3):

Предполагают, что астат, подобно иоду, способен накапливаться в щитовидной железе.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
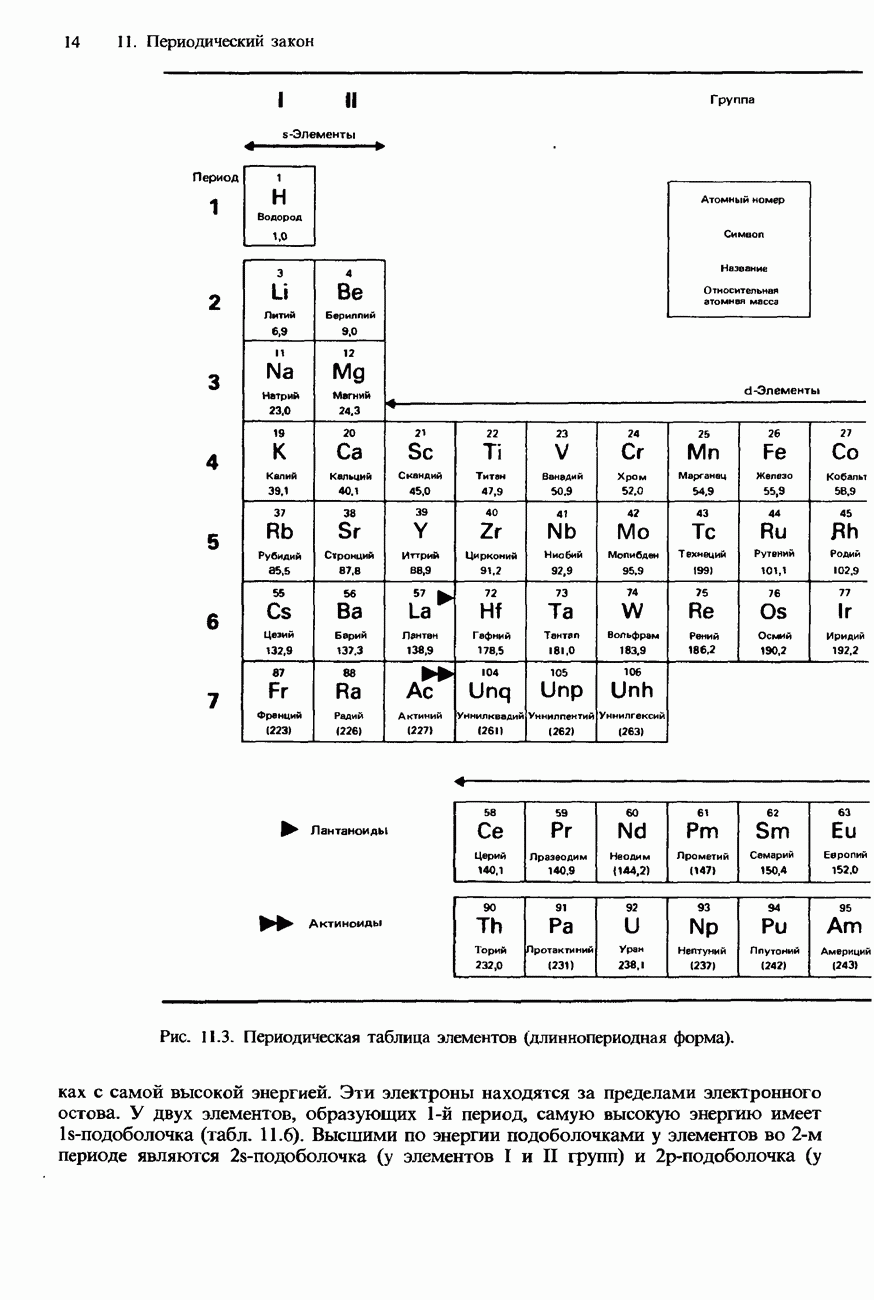
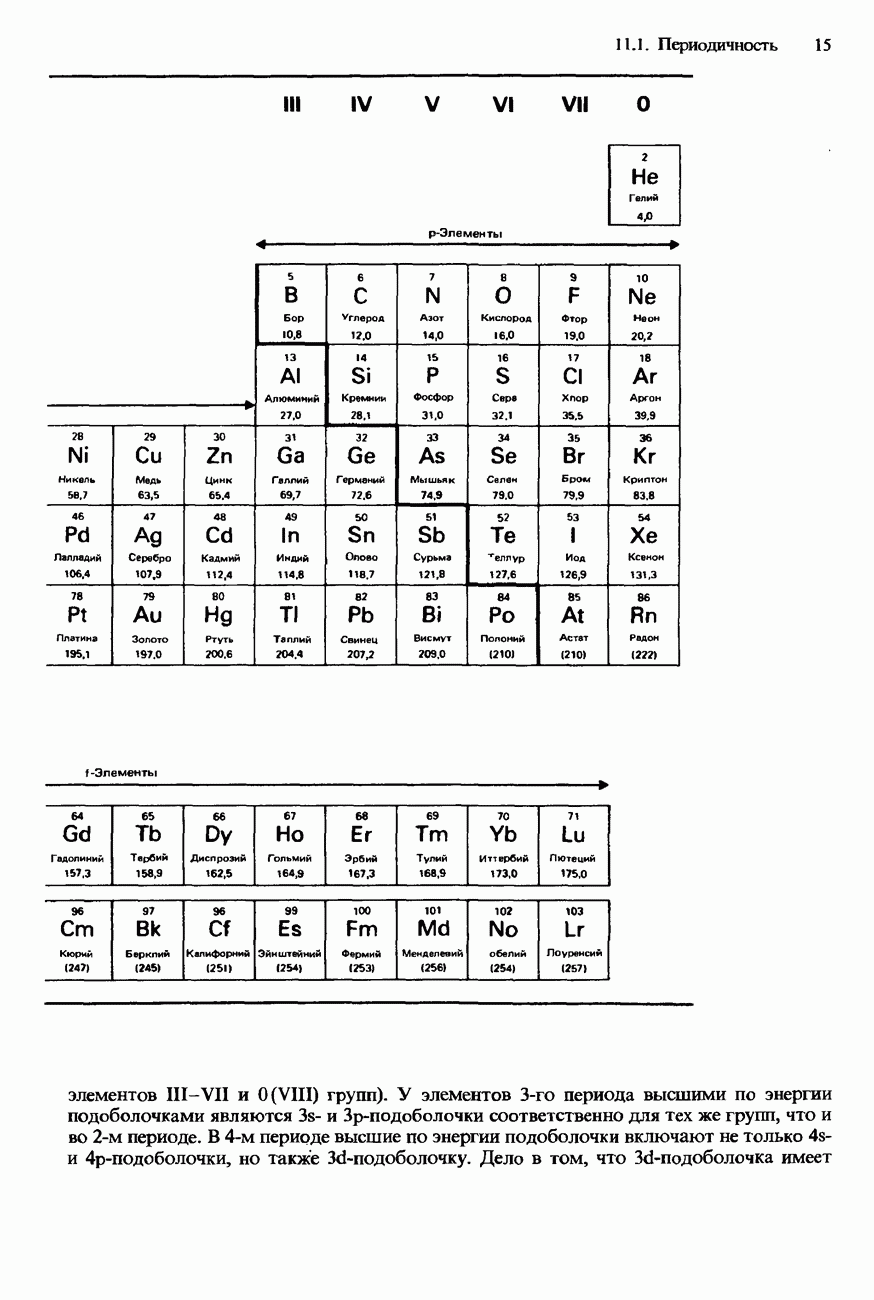
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
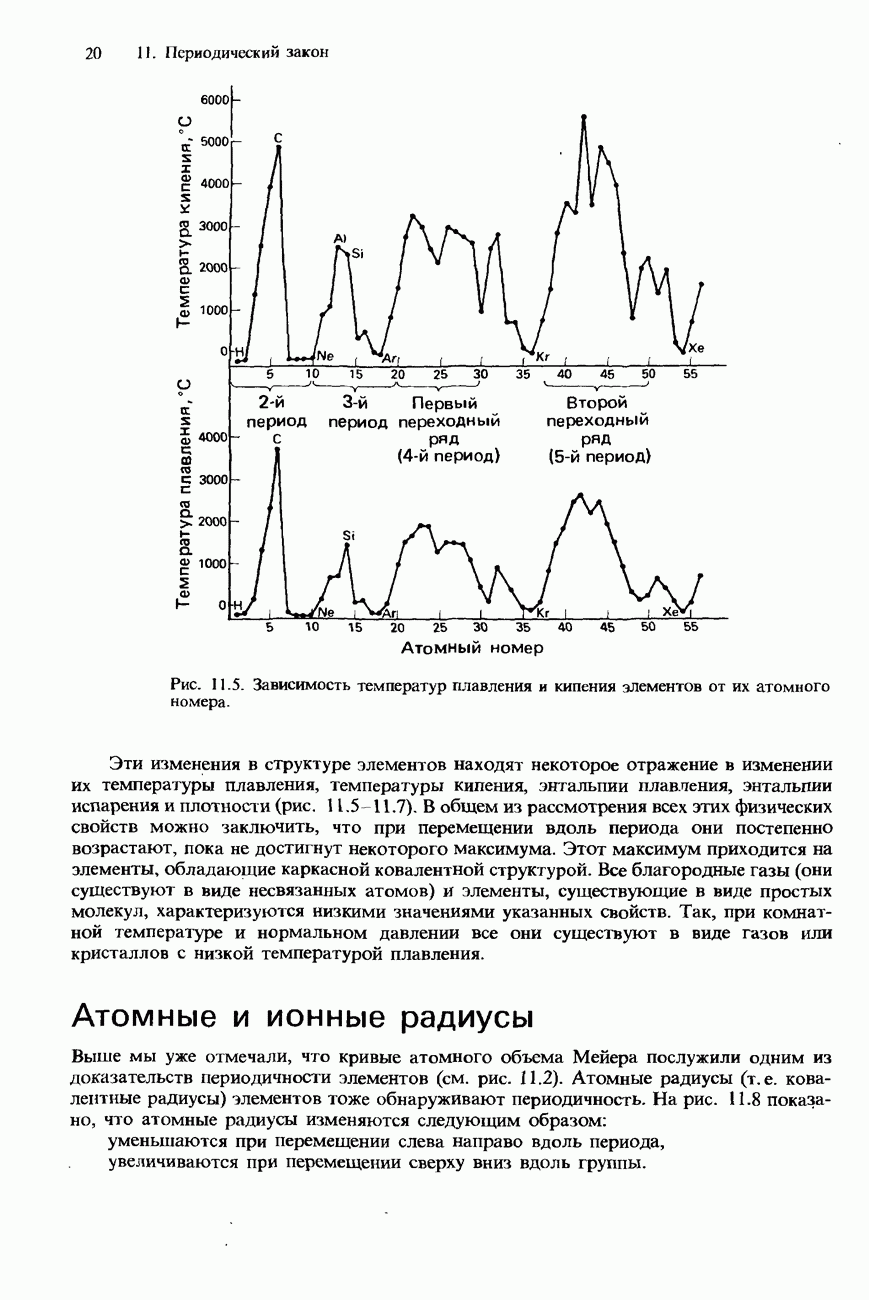
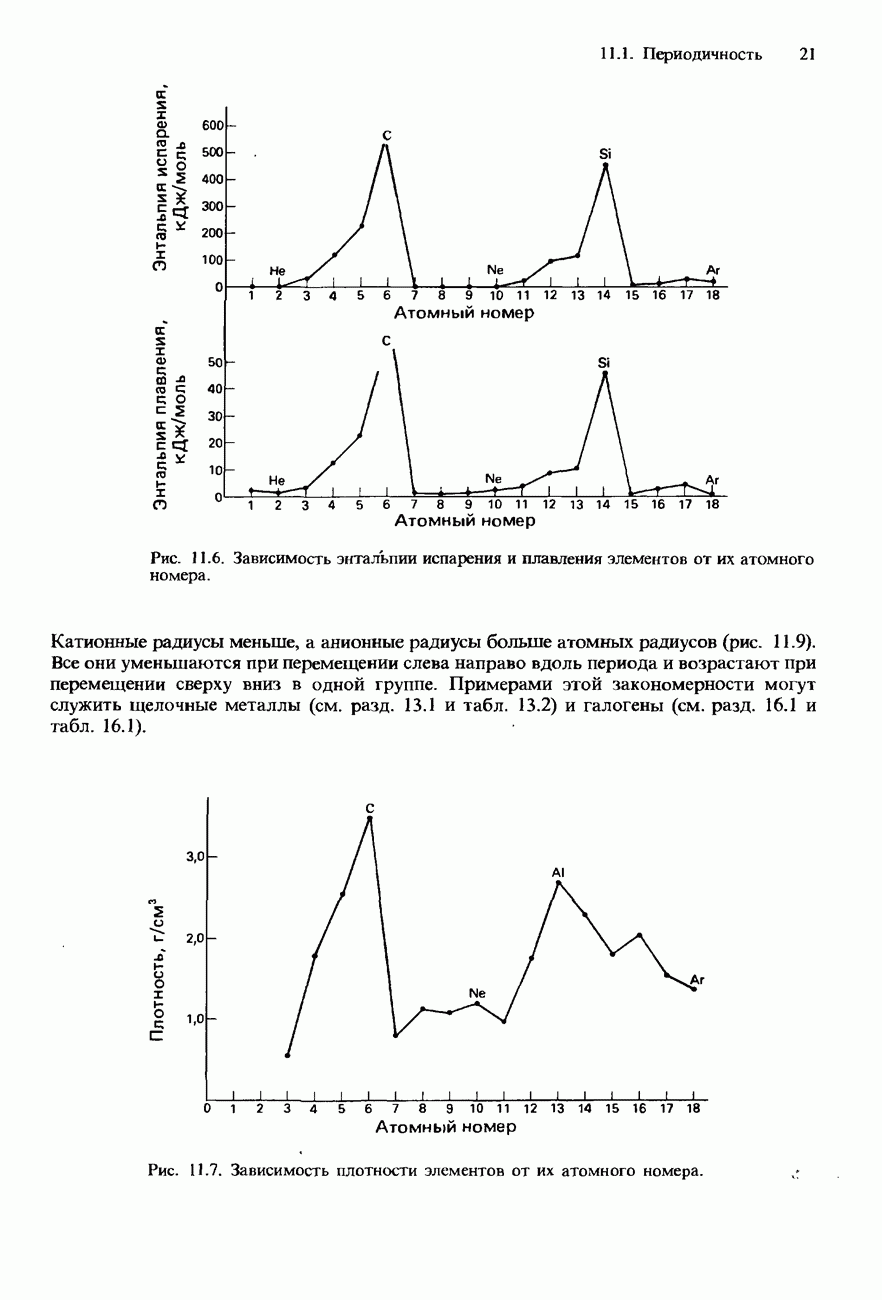
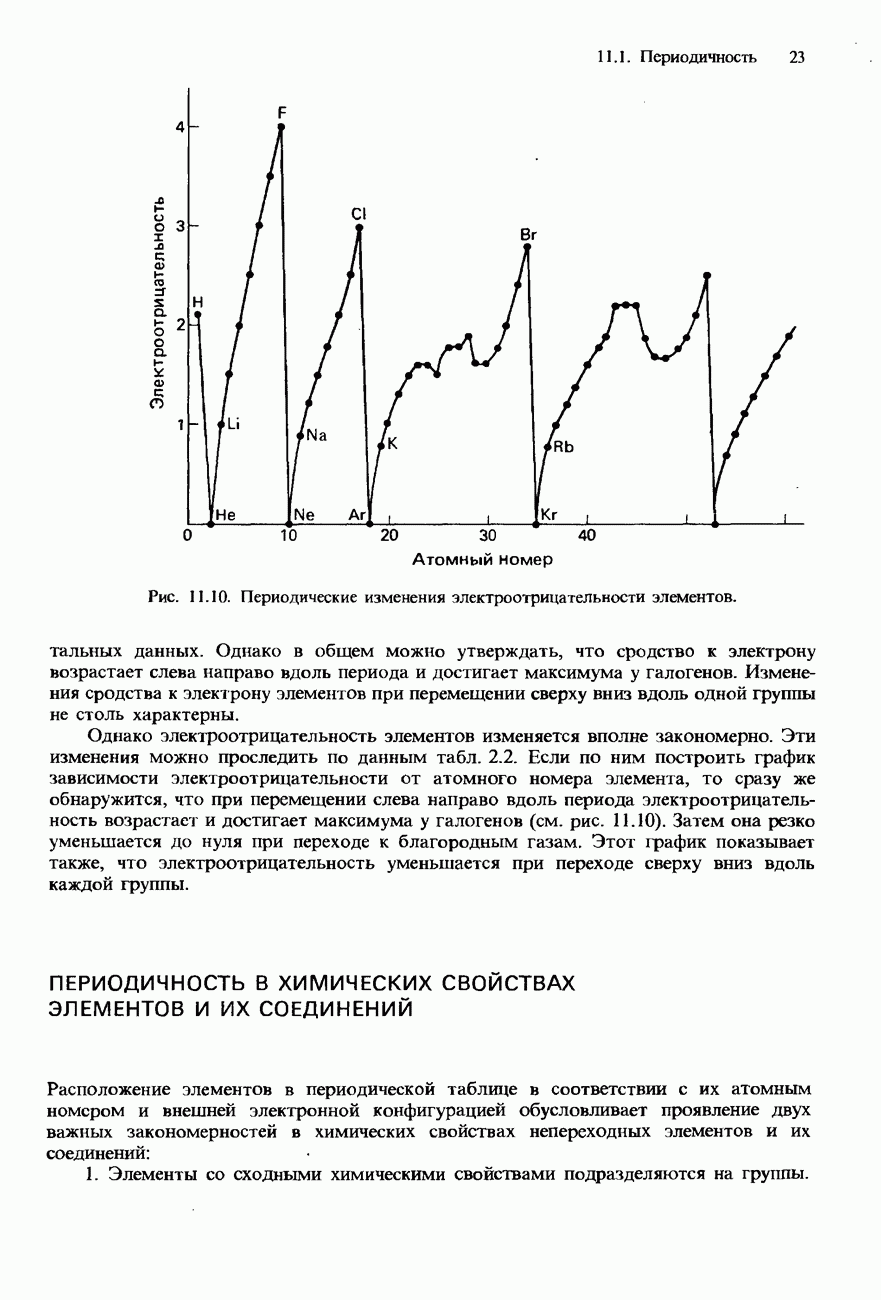
- ПЕРИОДИЧНОСТЬ
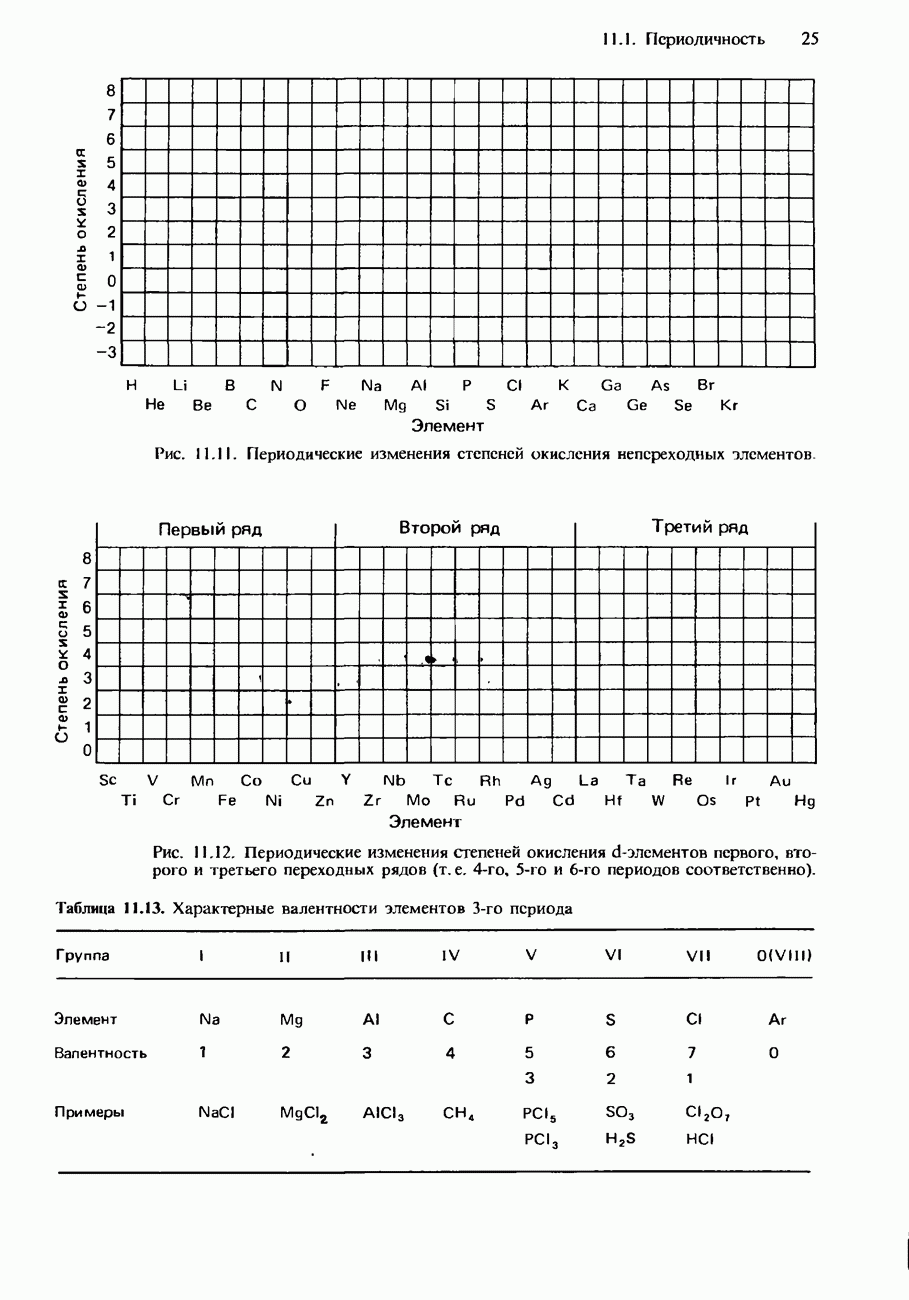
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
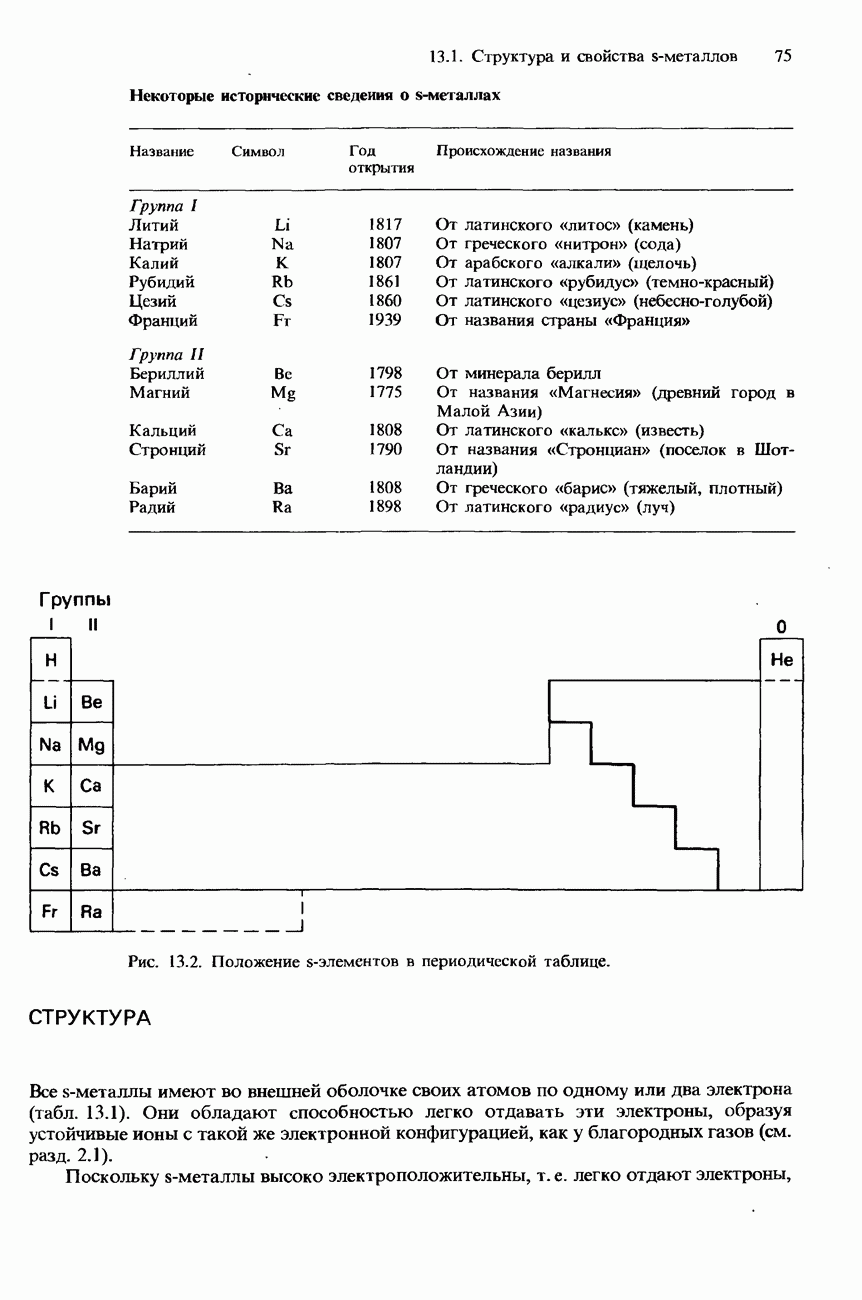
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
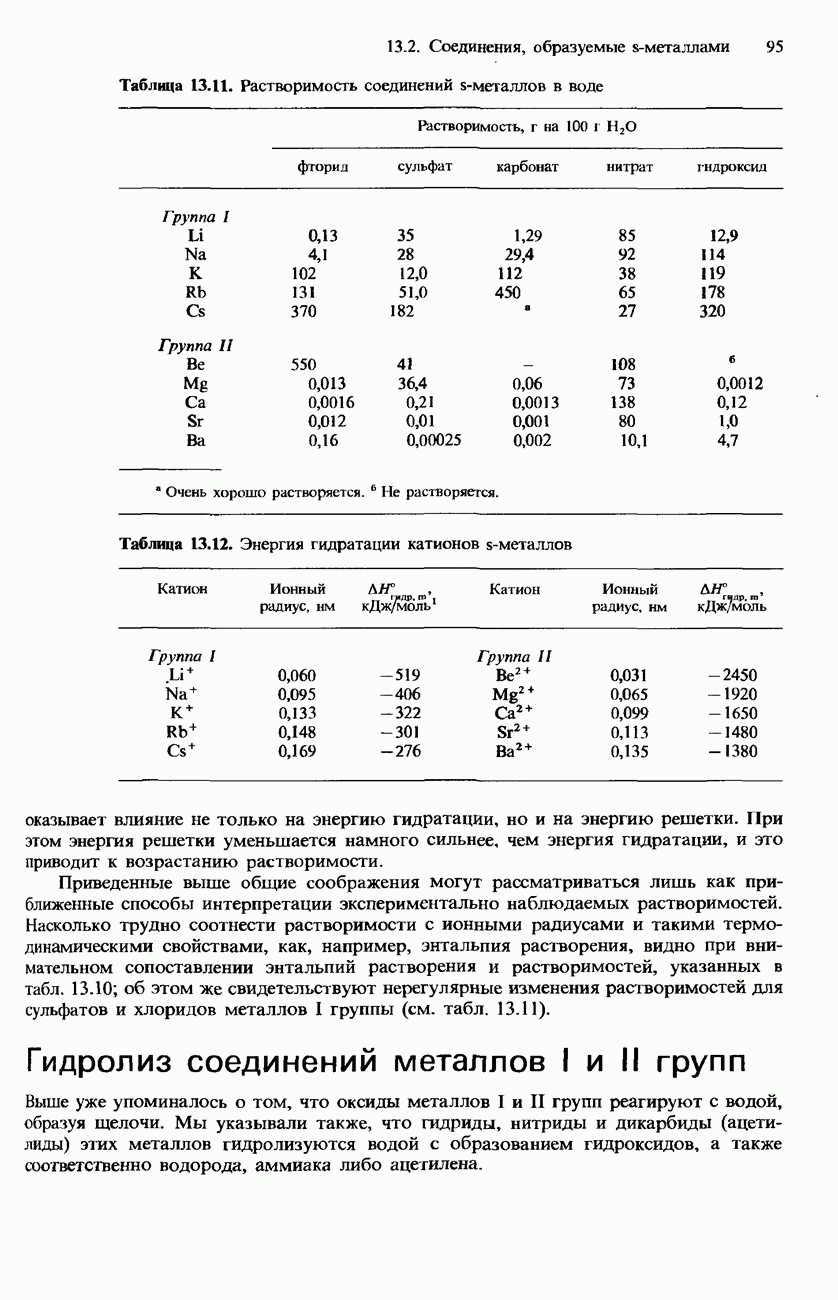
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
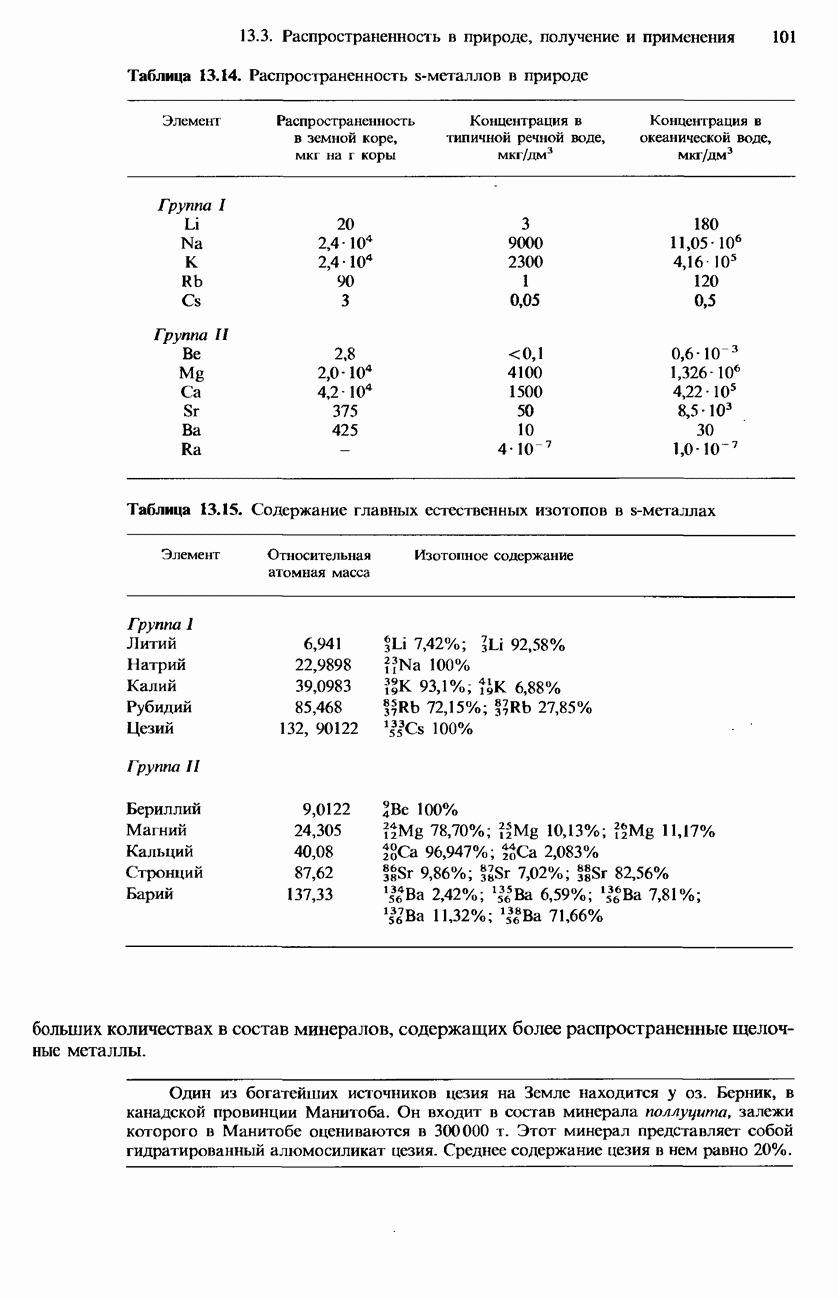
- 13.3. Распространенность в природе, получение и применение
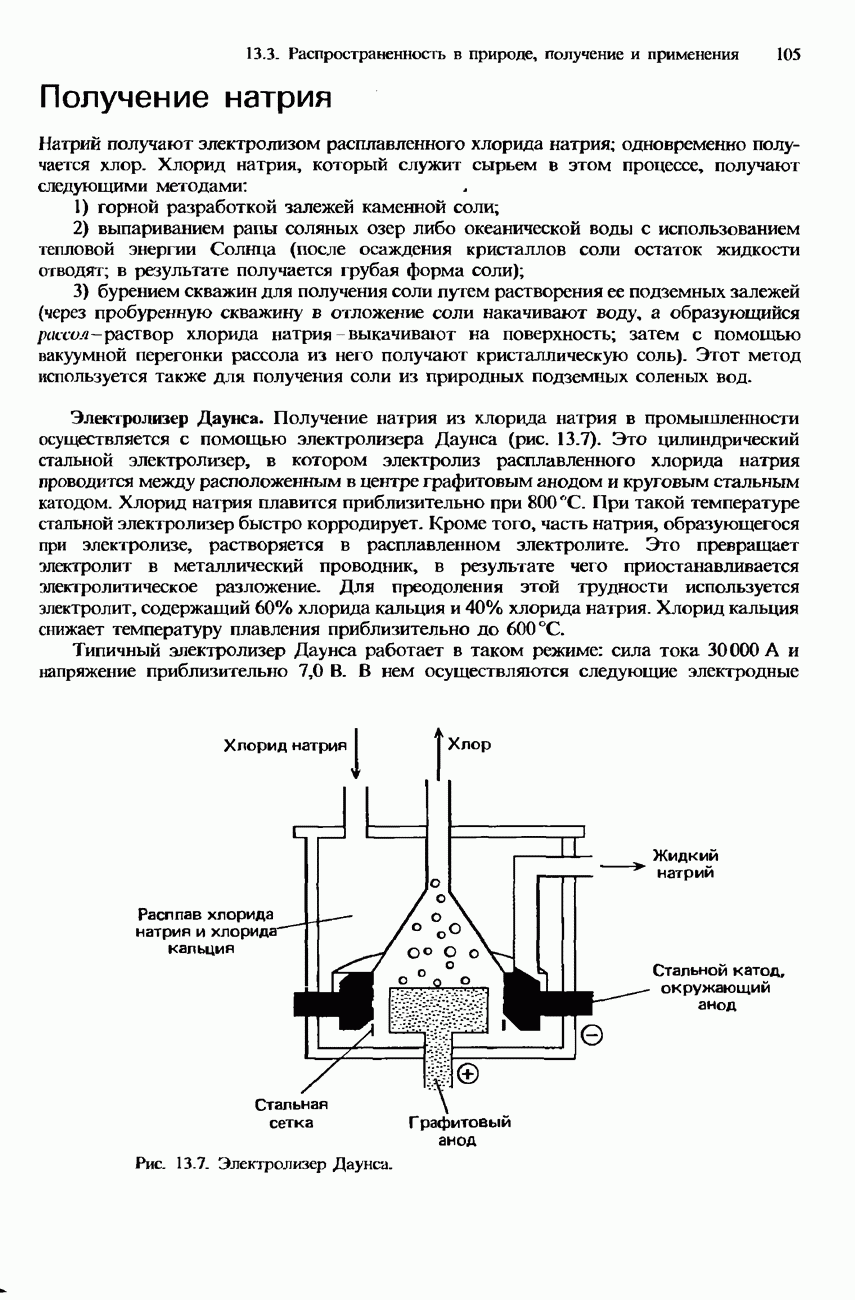
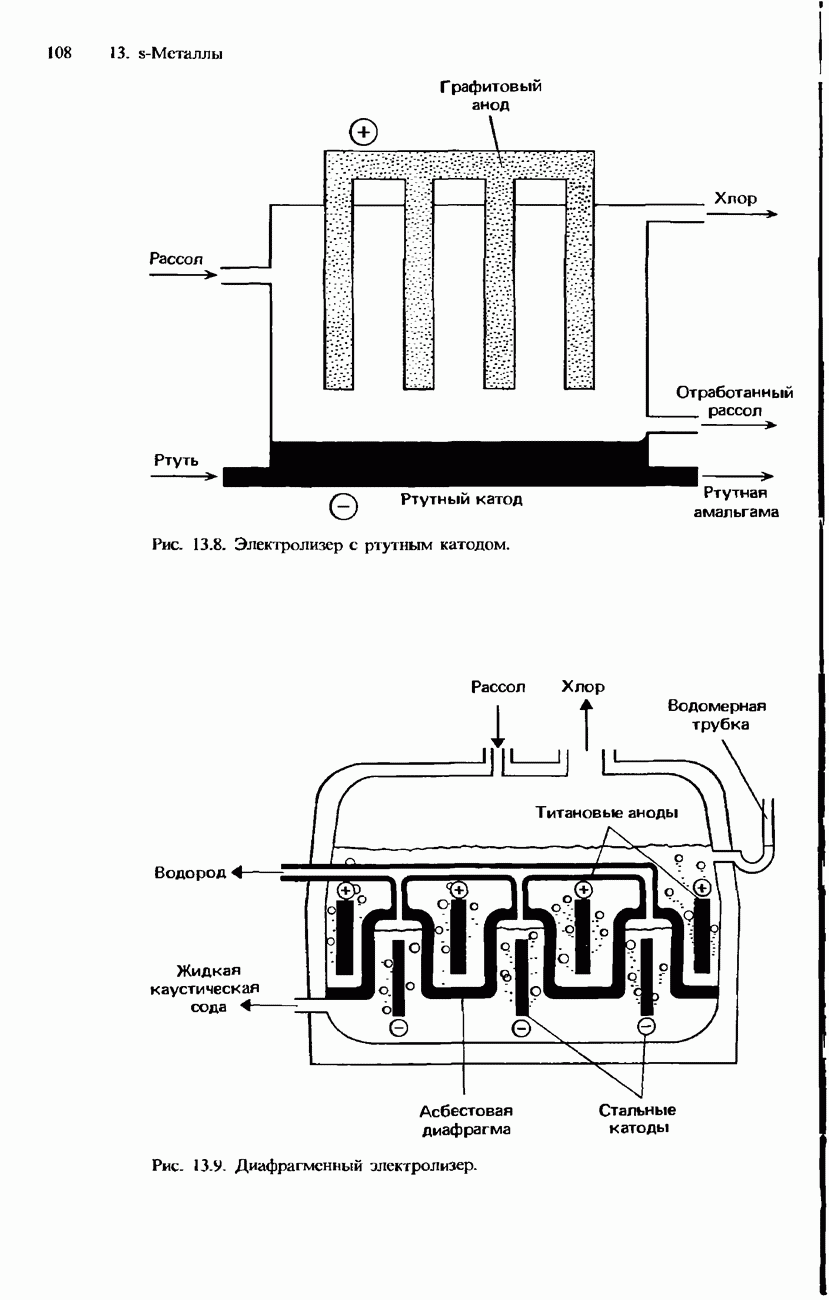
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
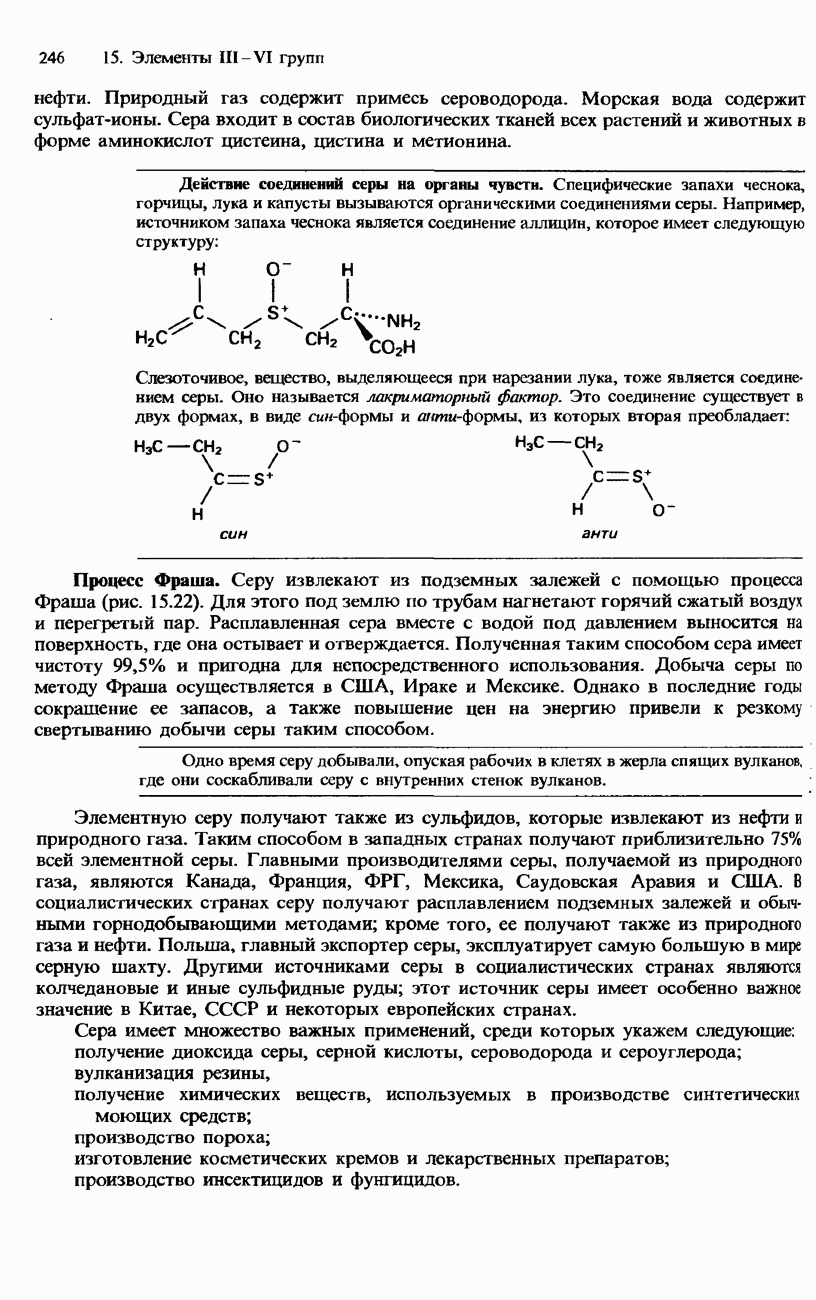
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
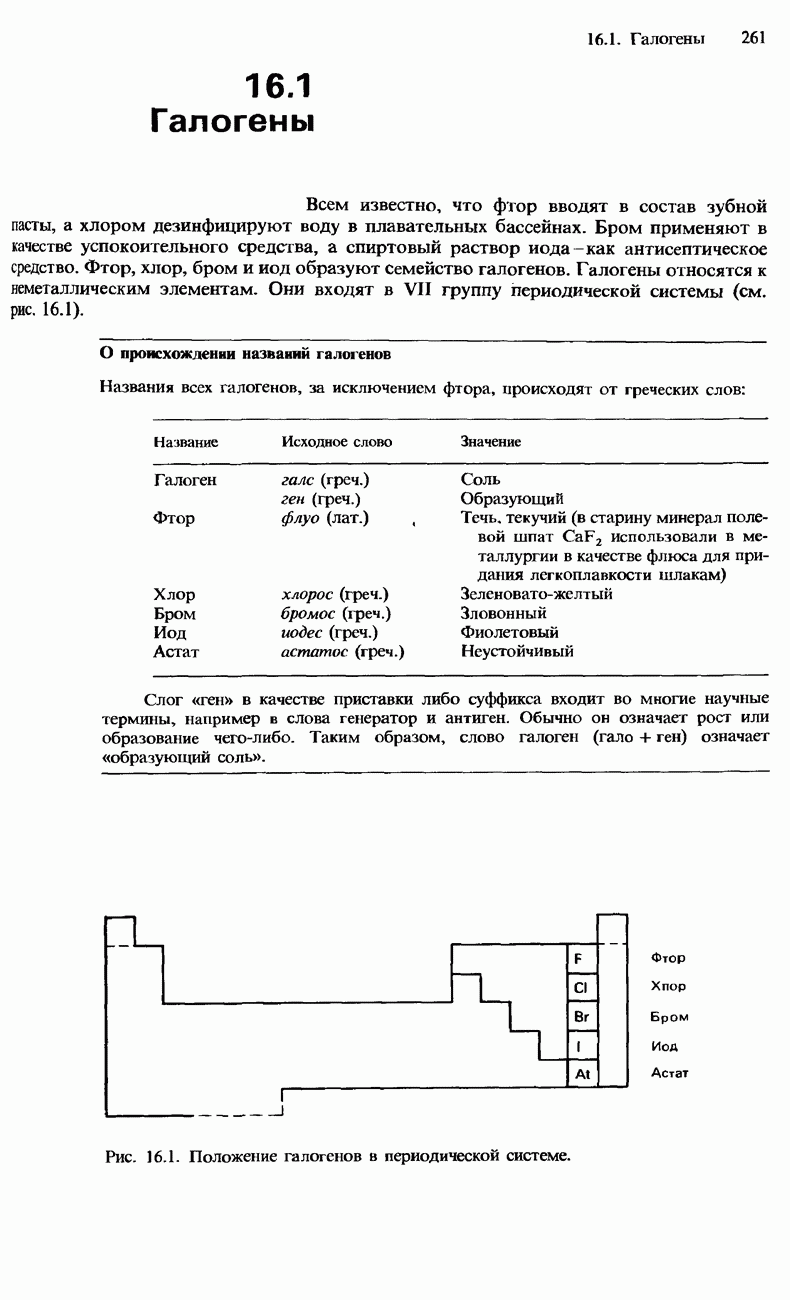
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
- 16.3. Распространенность, получение и применение галогенов и их соединений
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
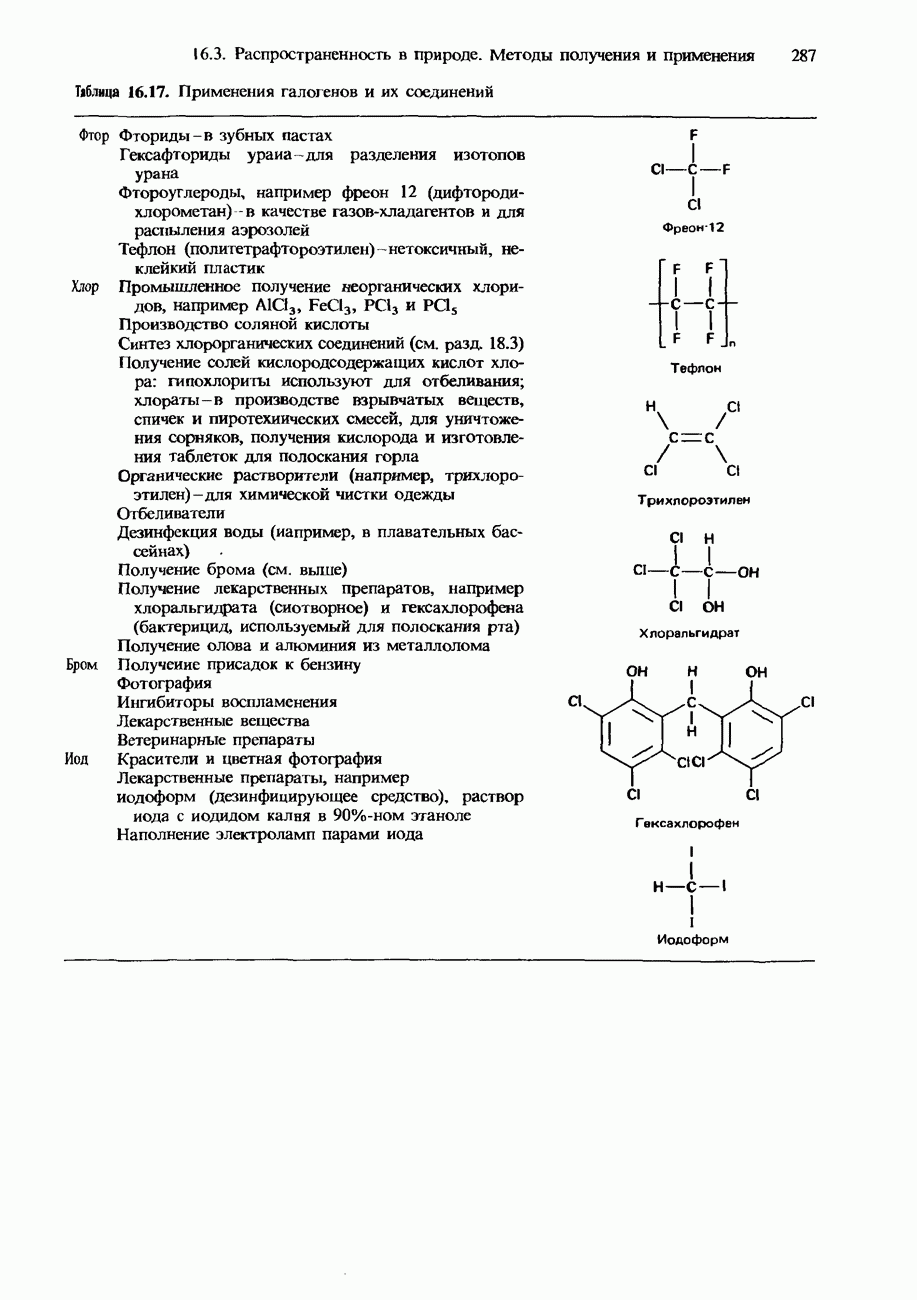
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
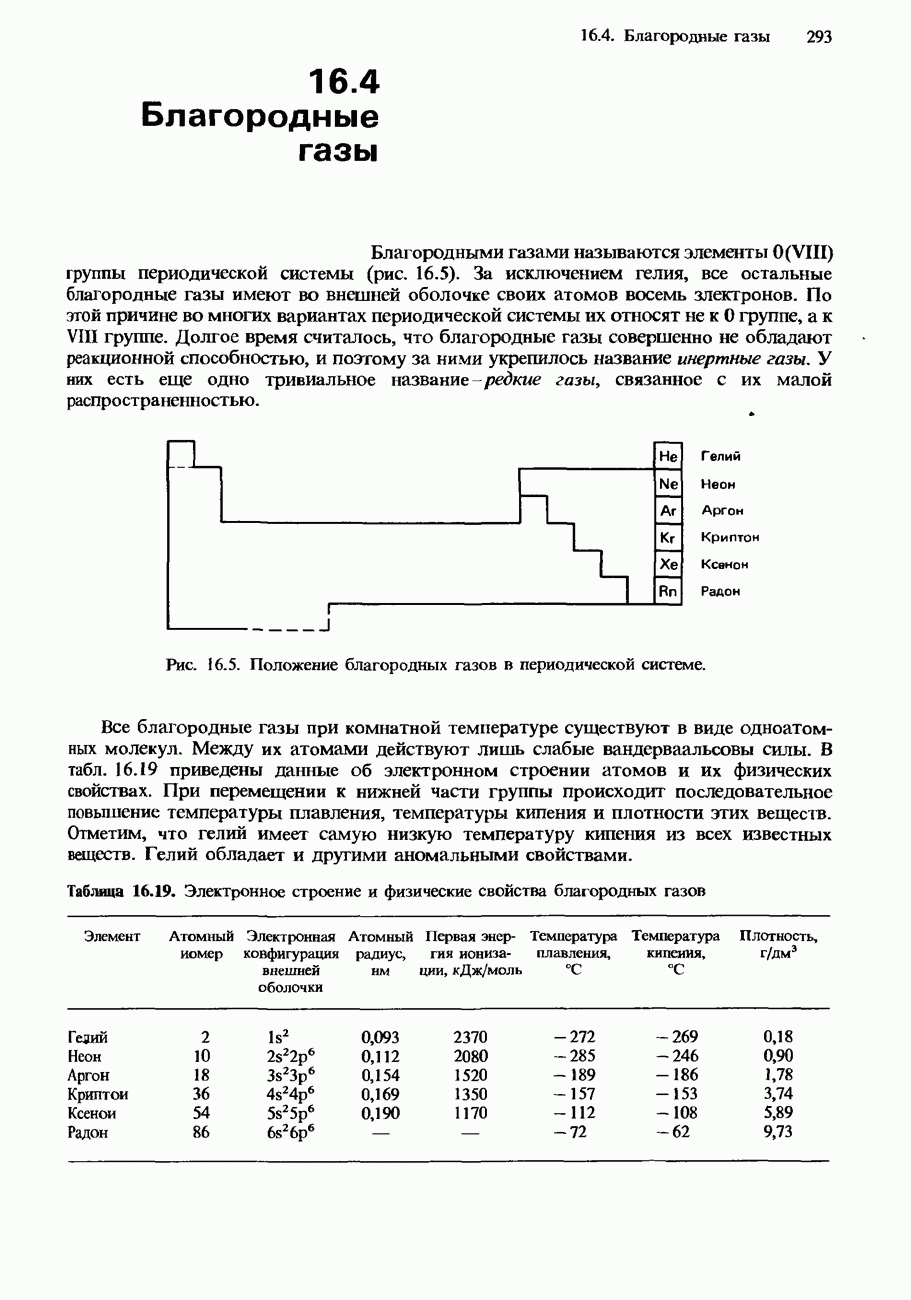
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
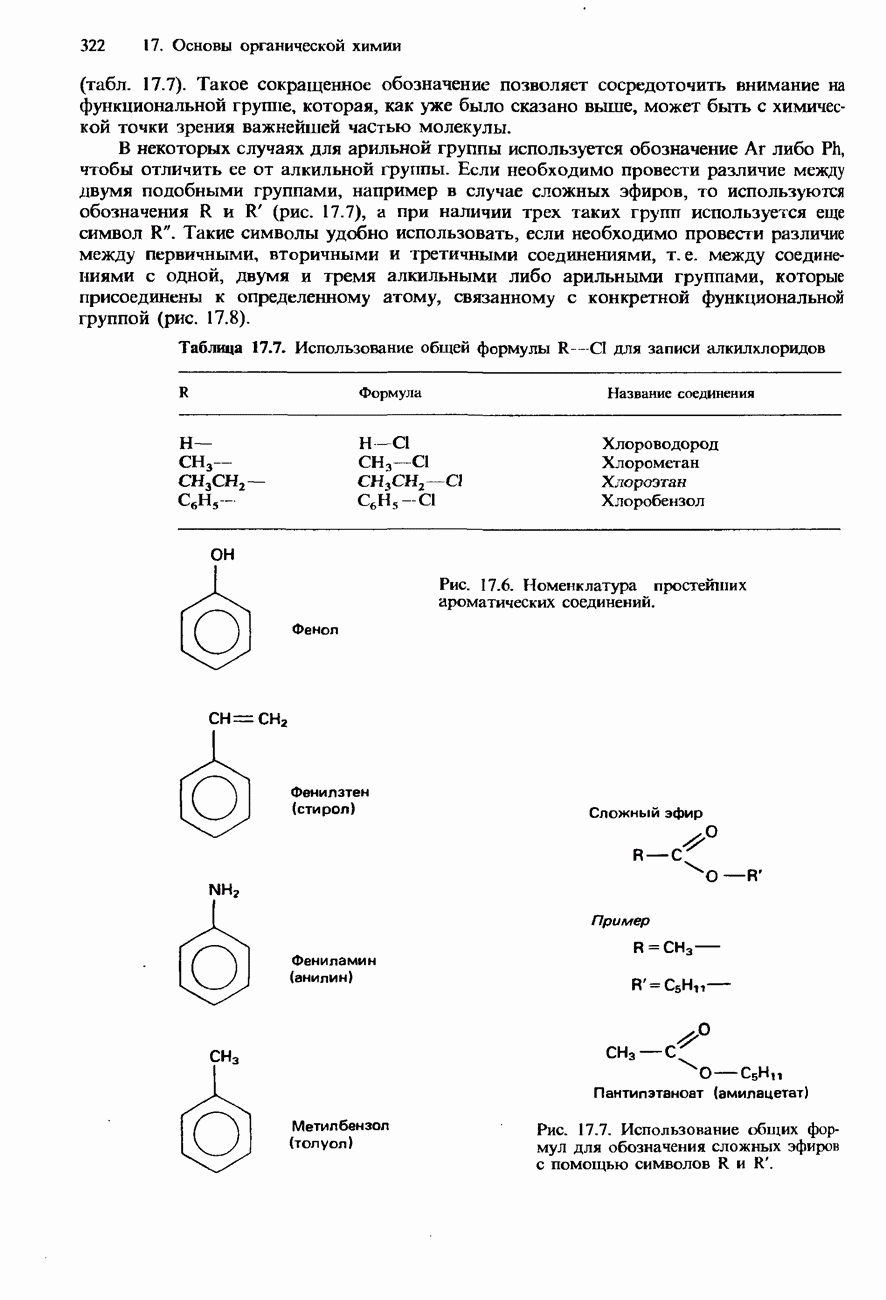
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
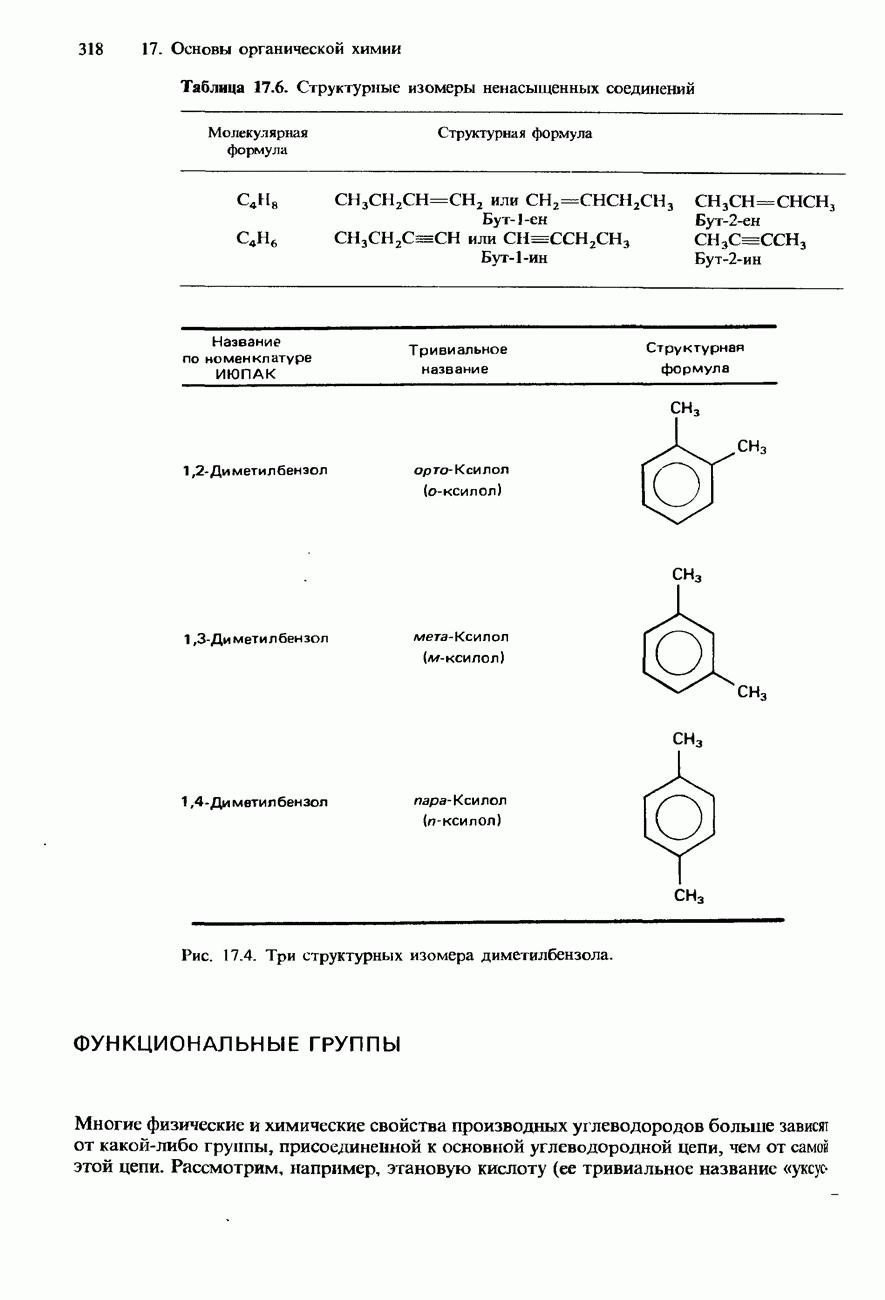
- УГЛЕВОДОРОДЫ
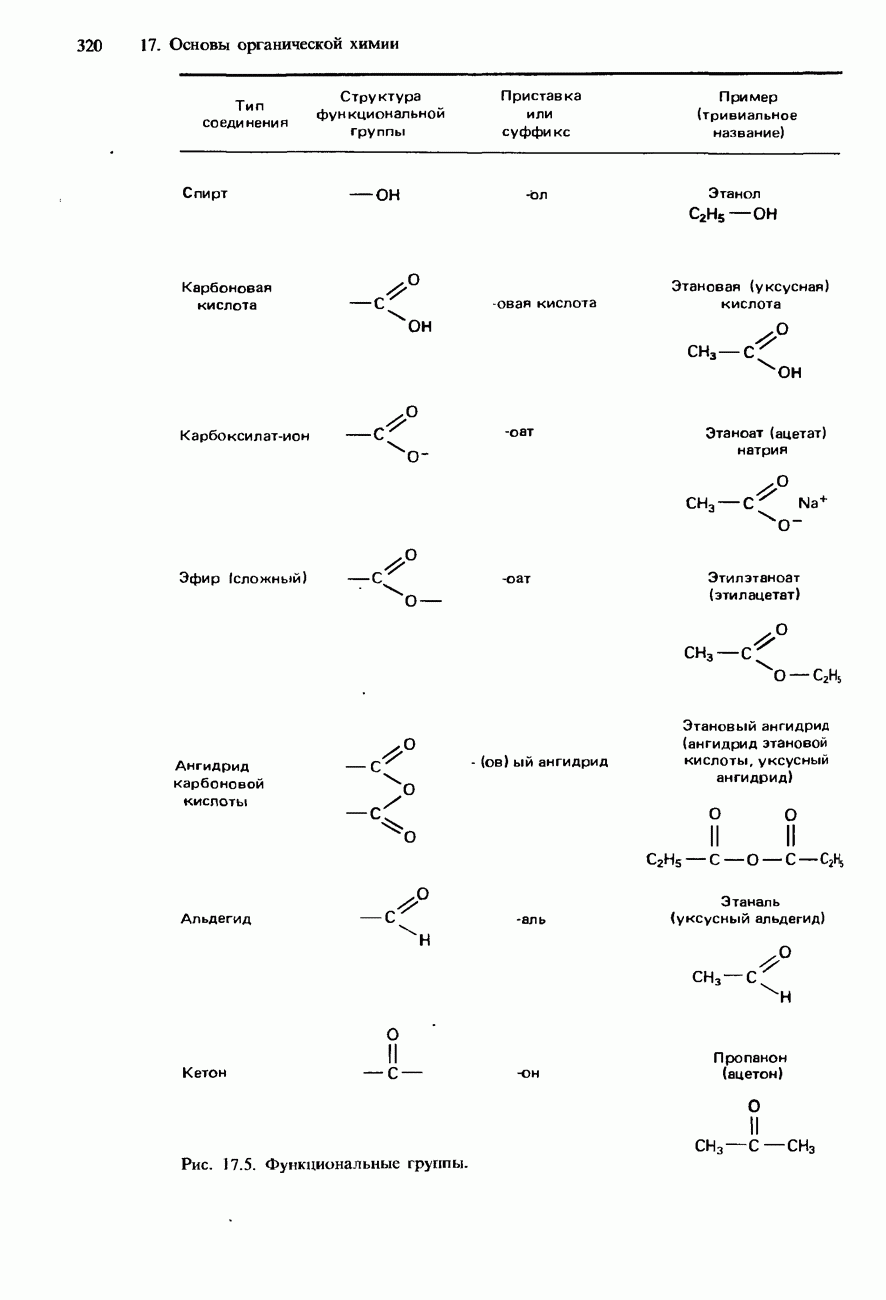
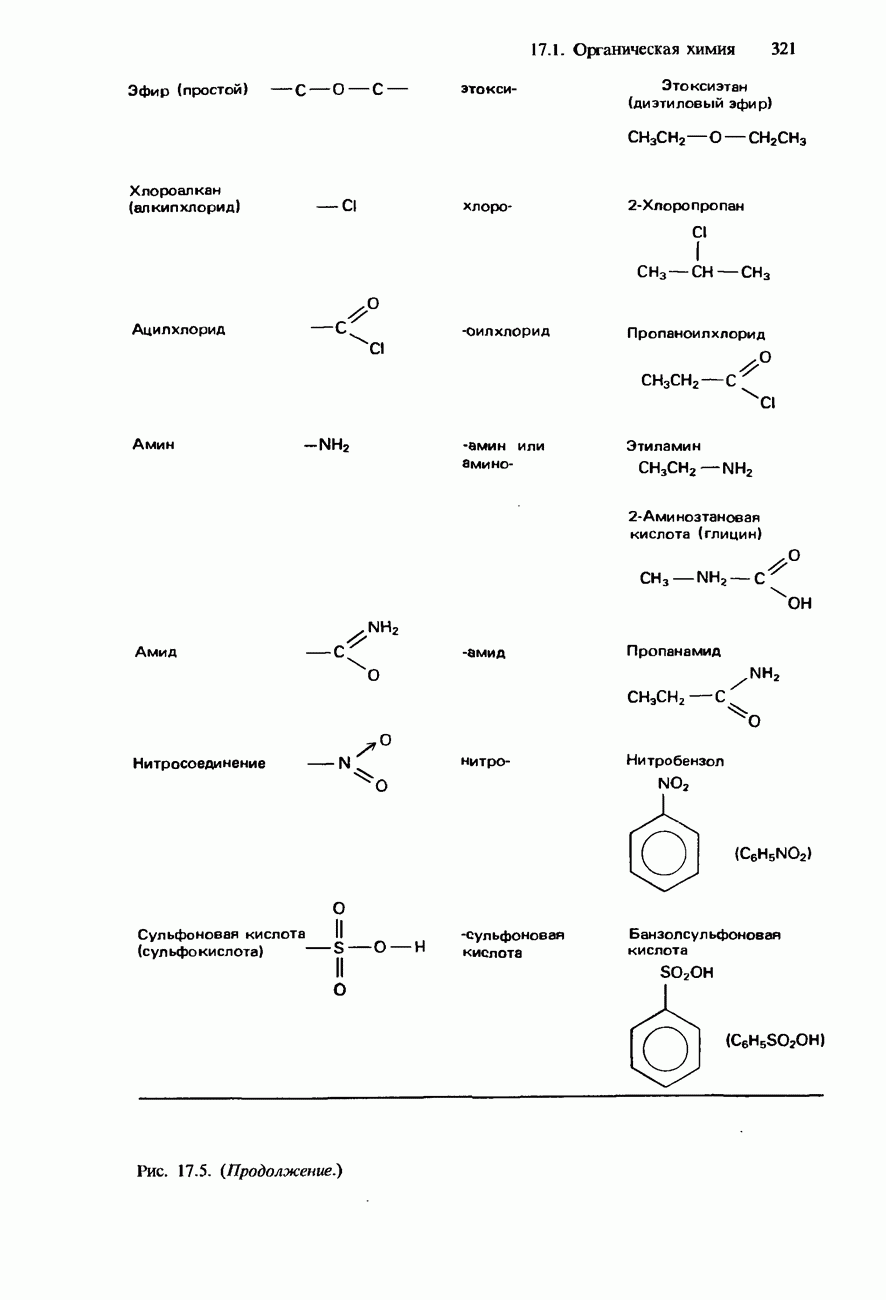
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
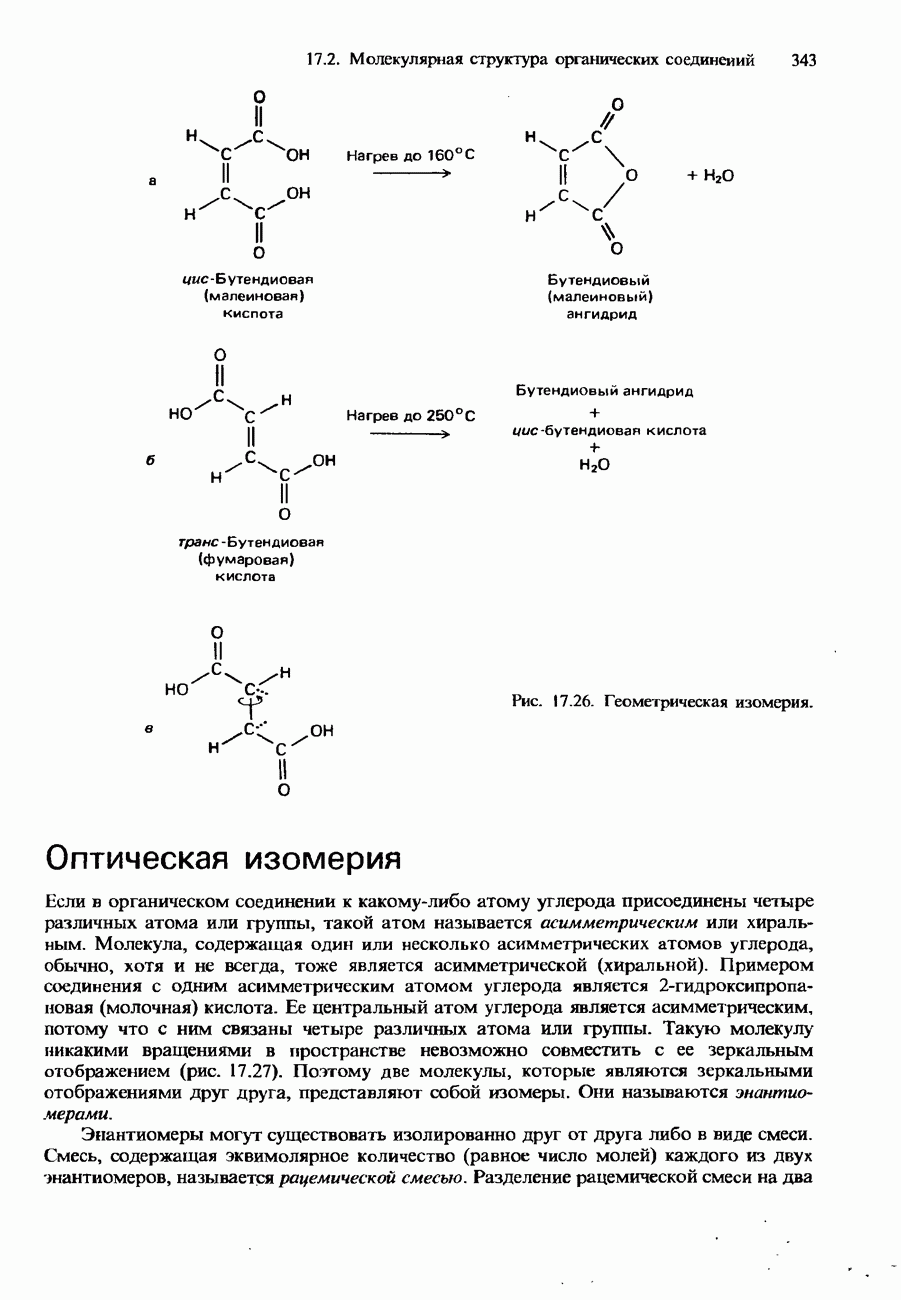
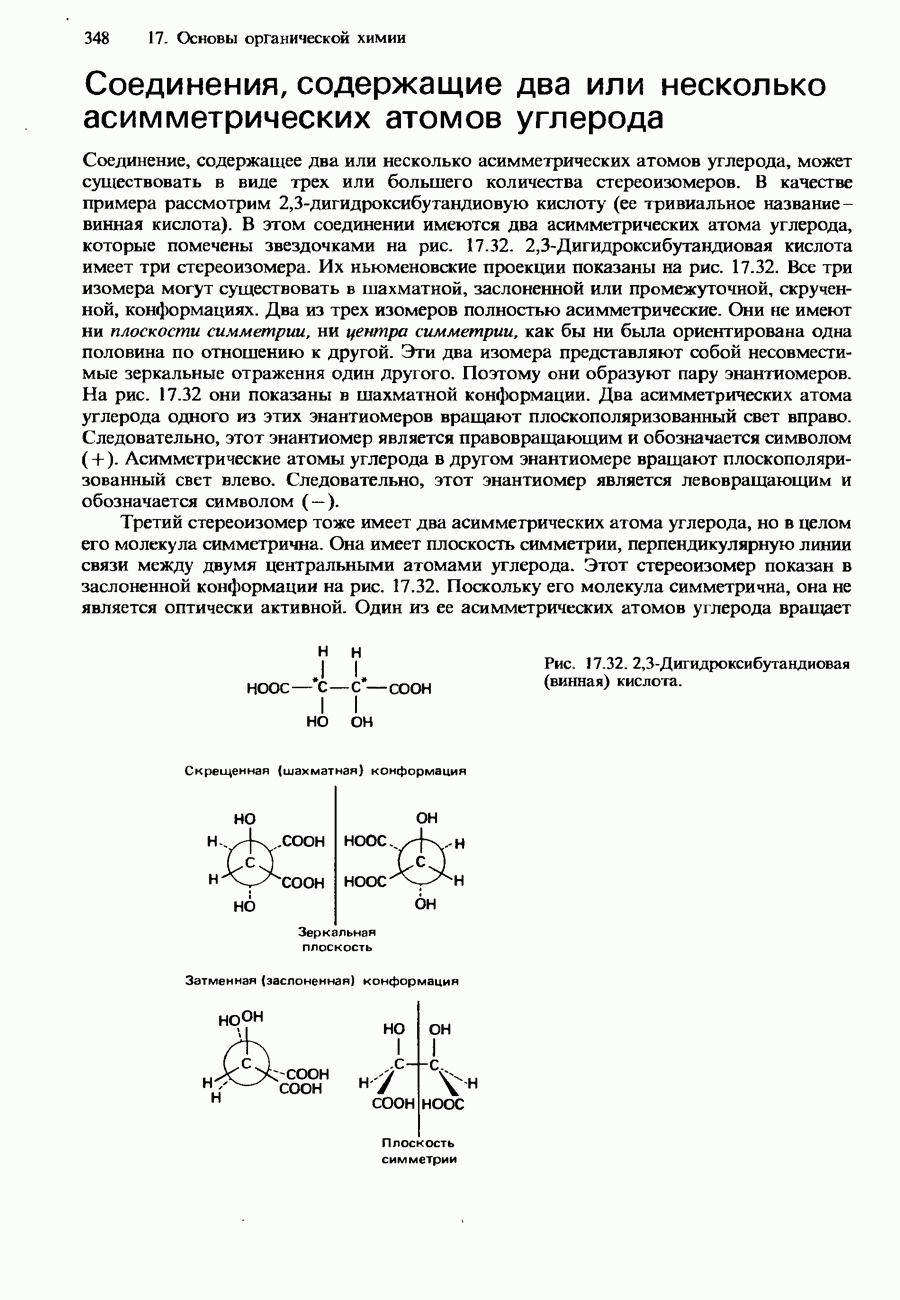
- СТЕРЕОИЗОМЕРИЯ
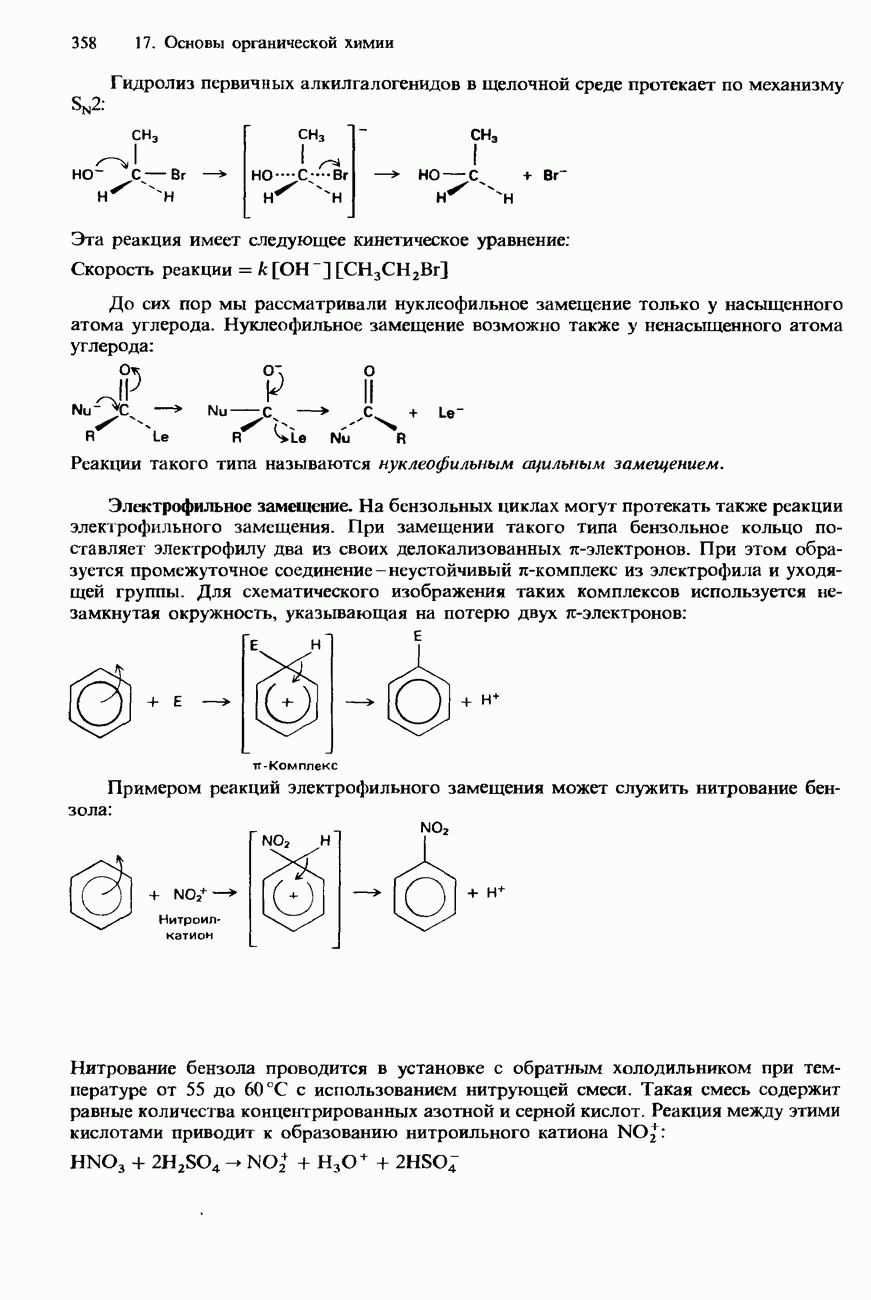
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
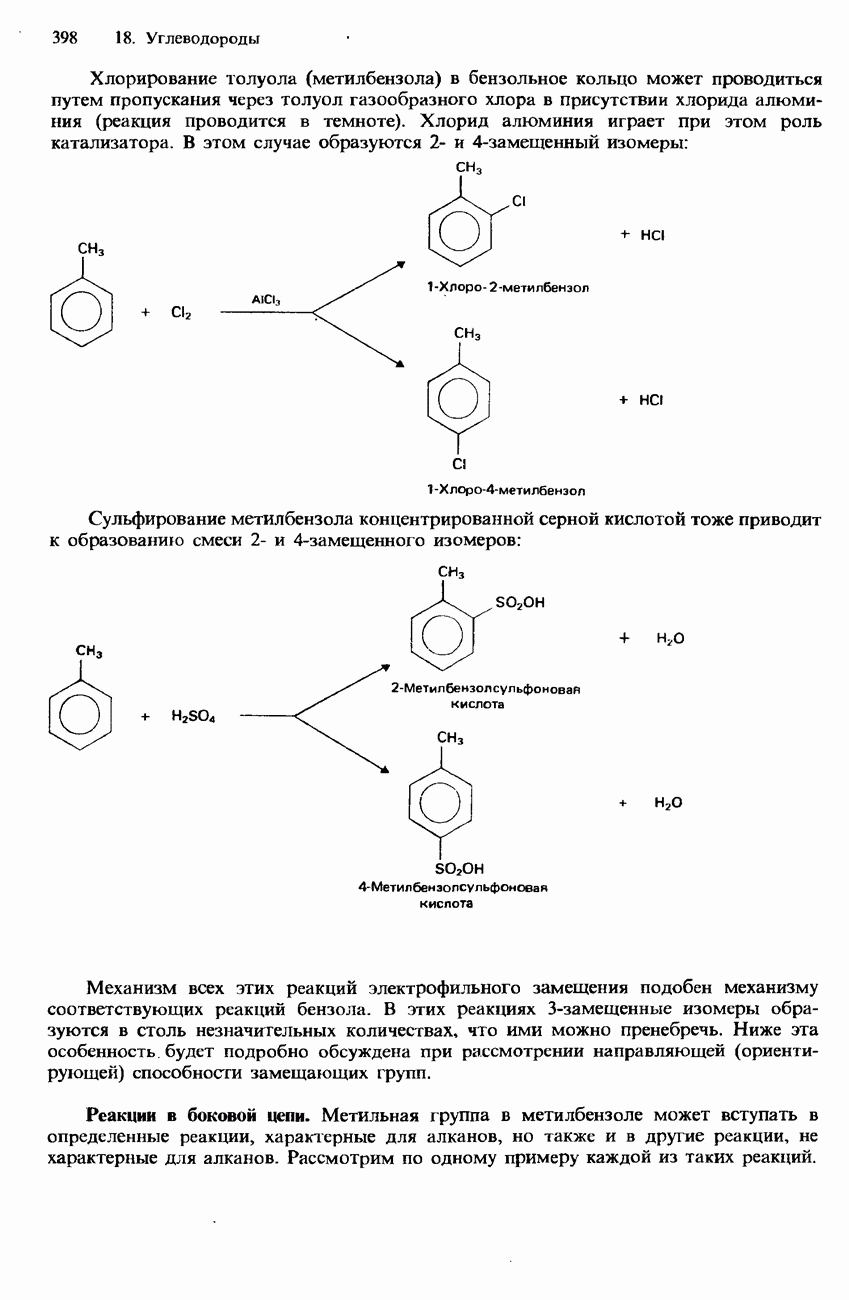
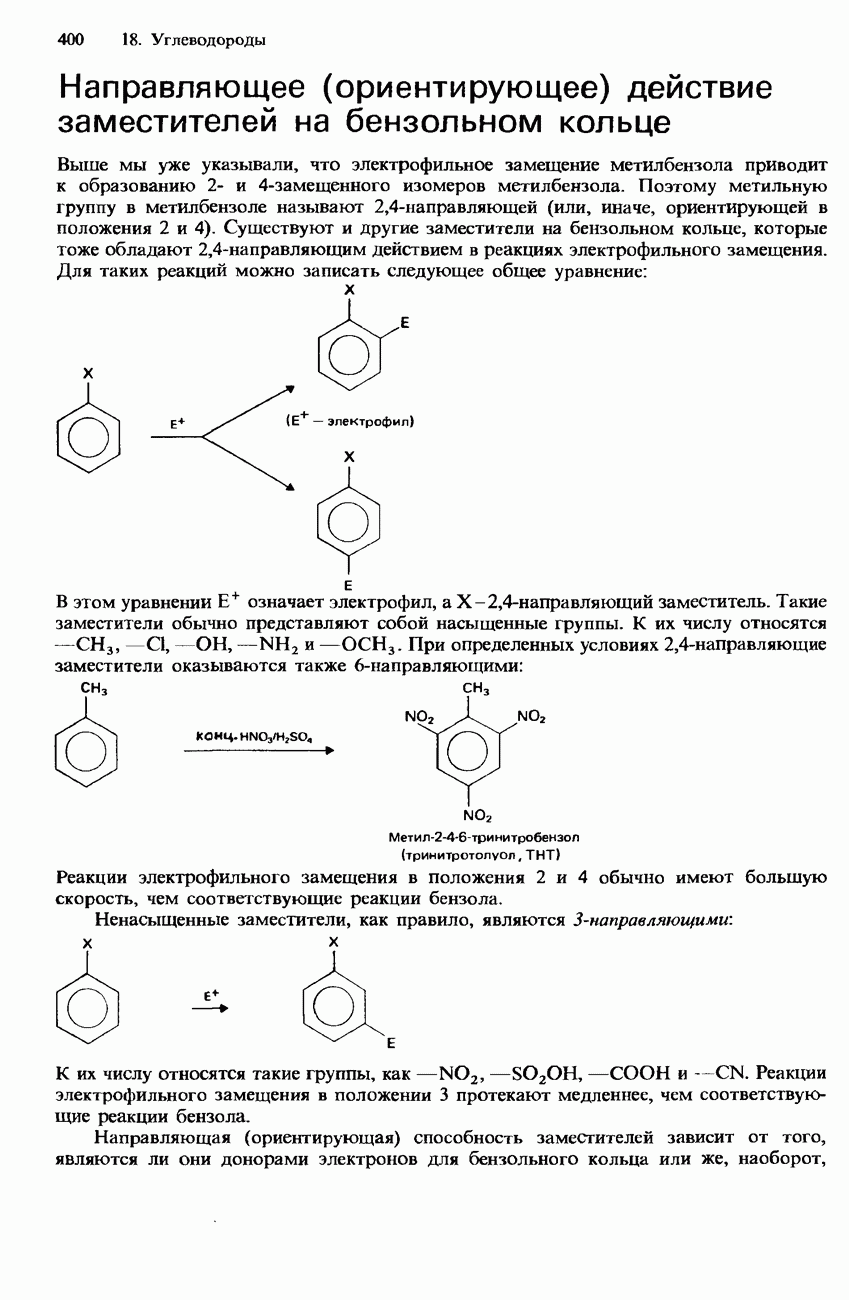
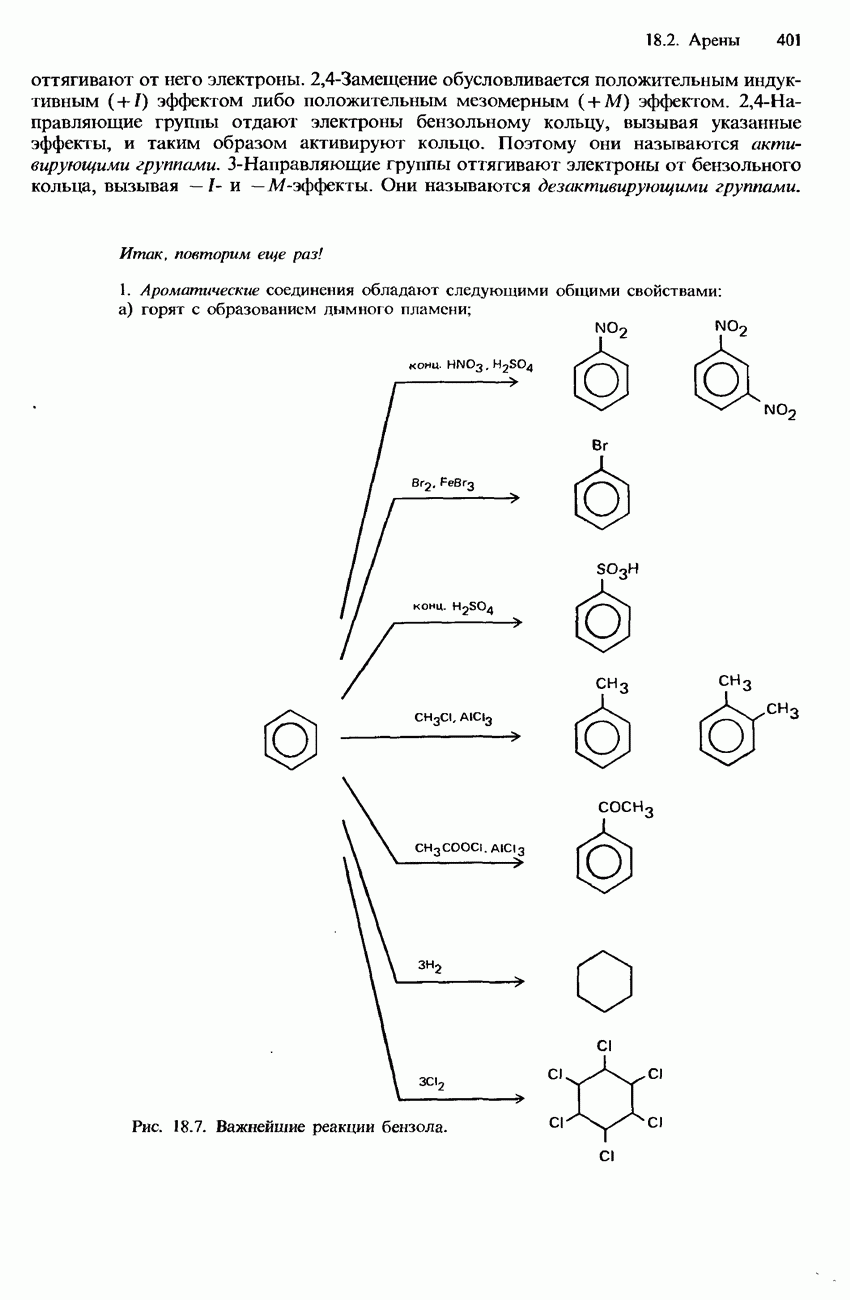
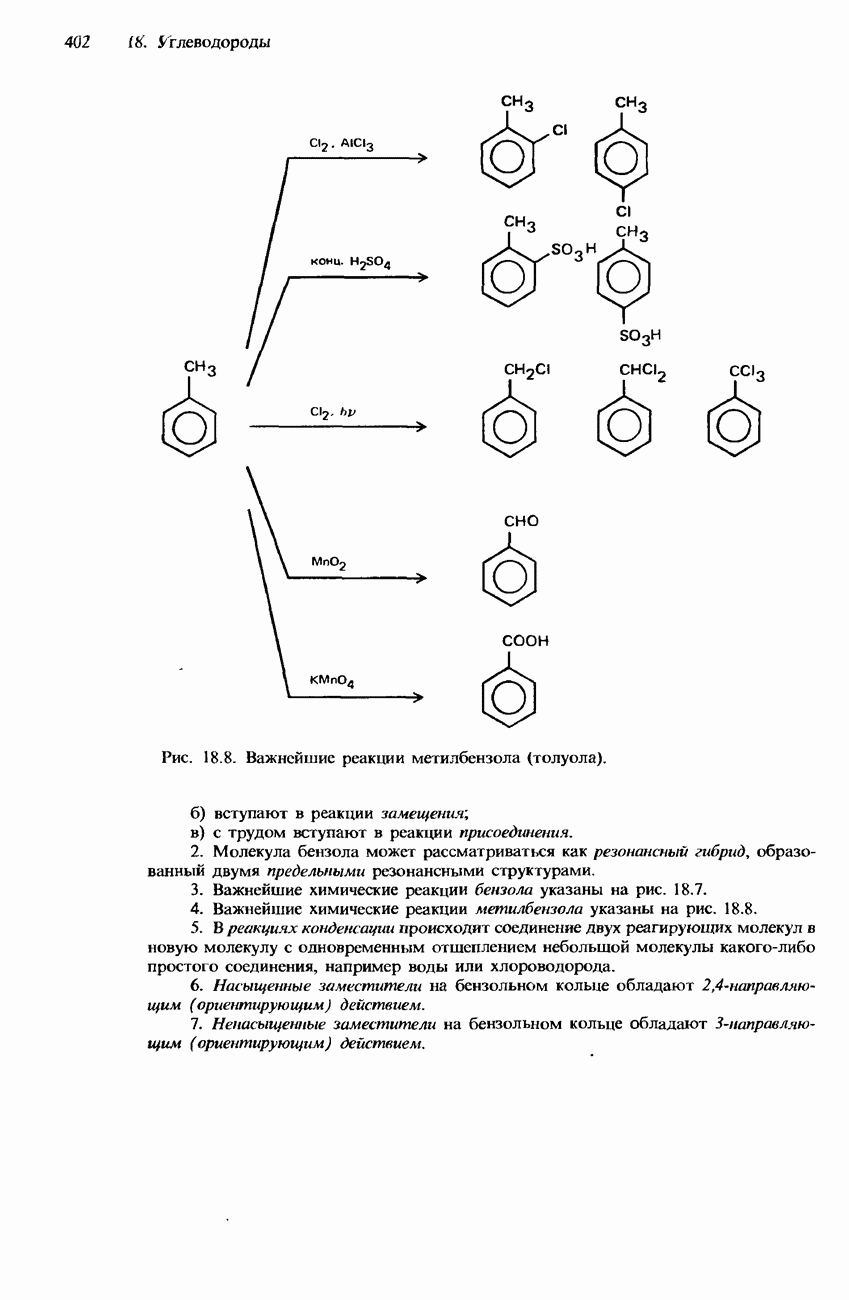
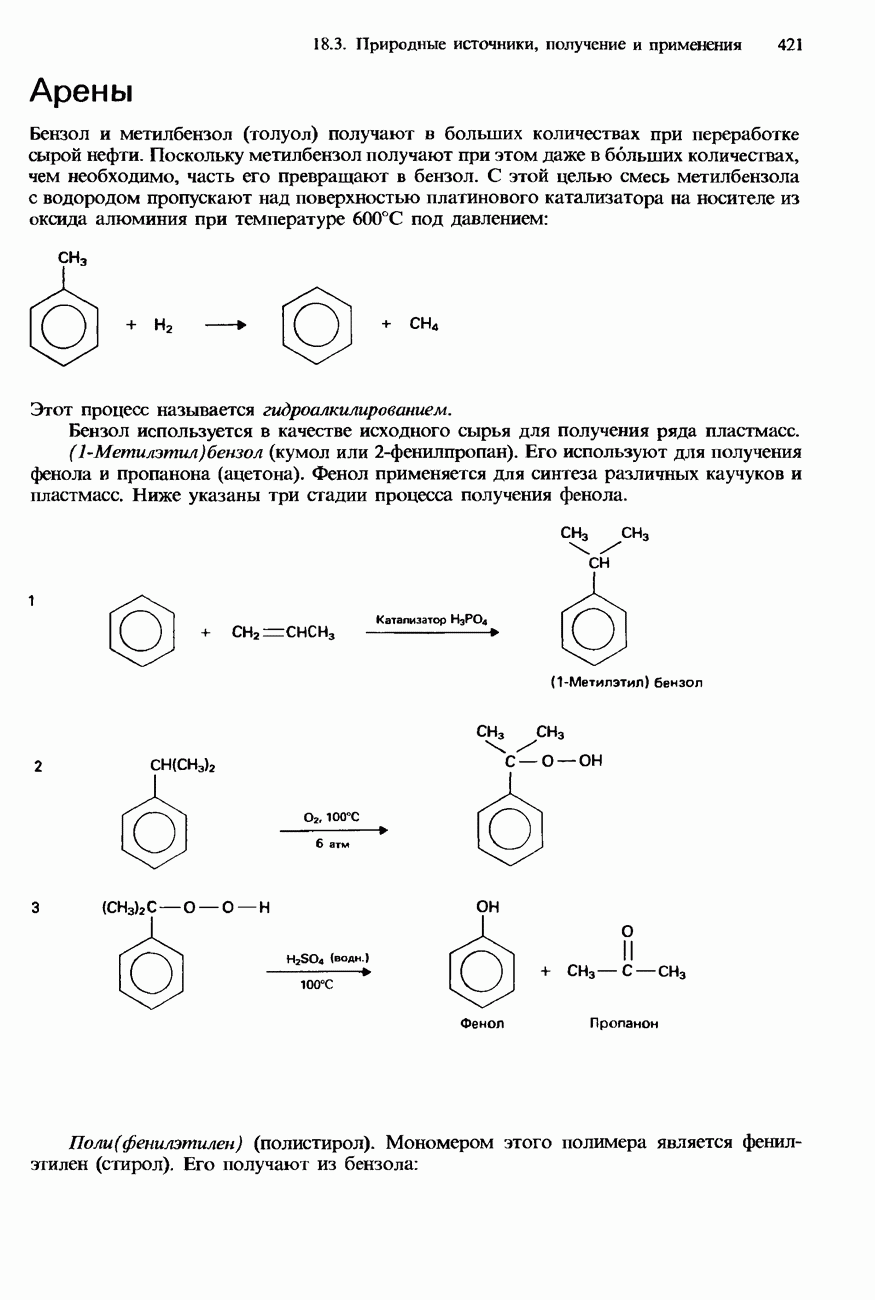
- 18.2. Арены
- БЕНЗОЛ
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
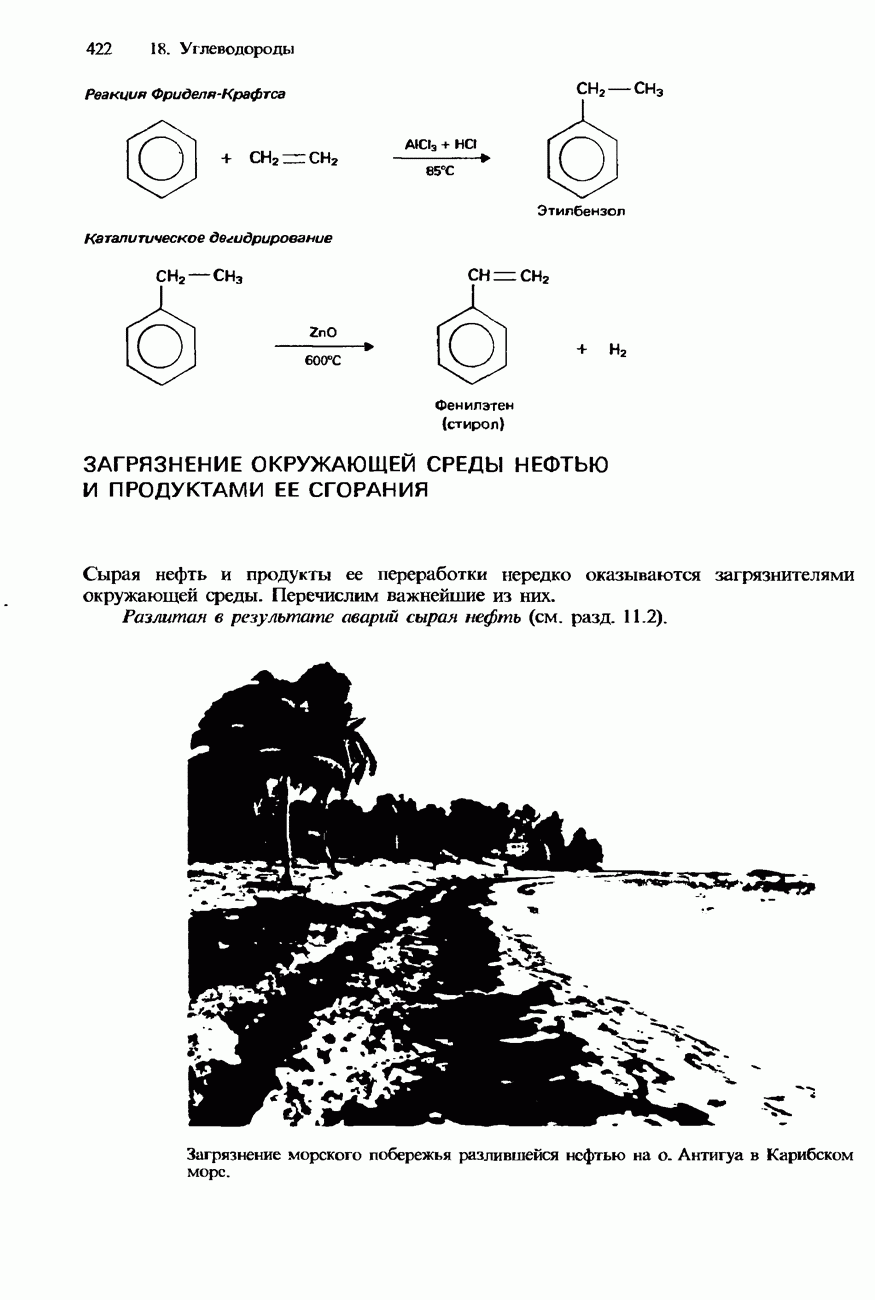
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
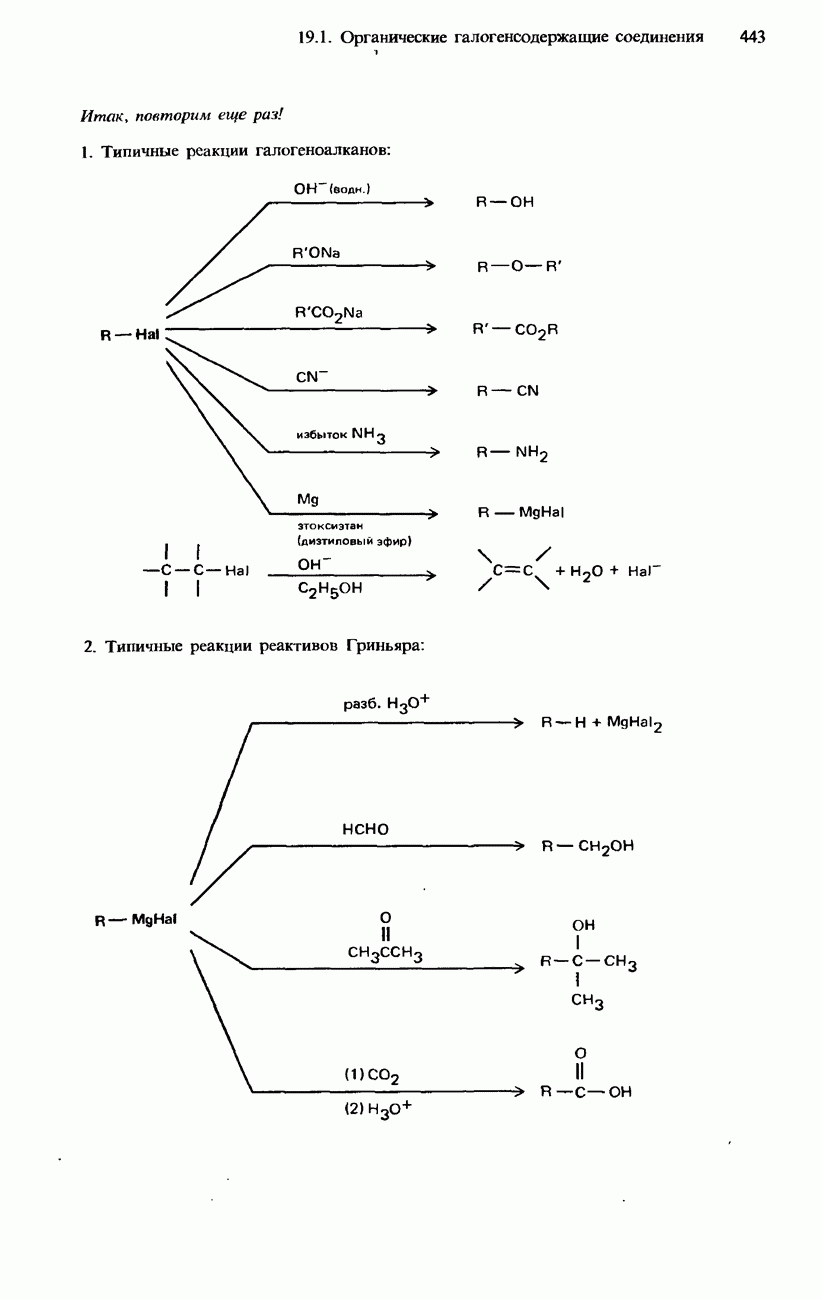
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
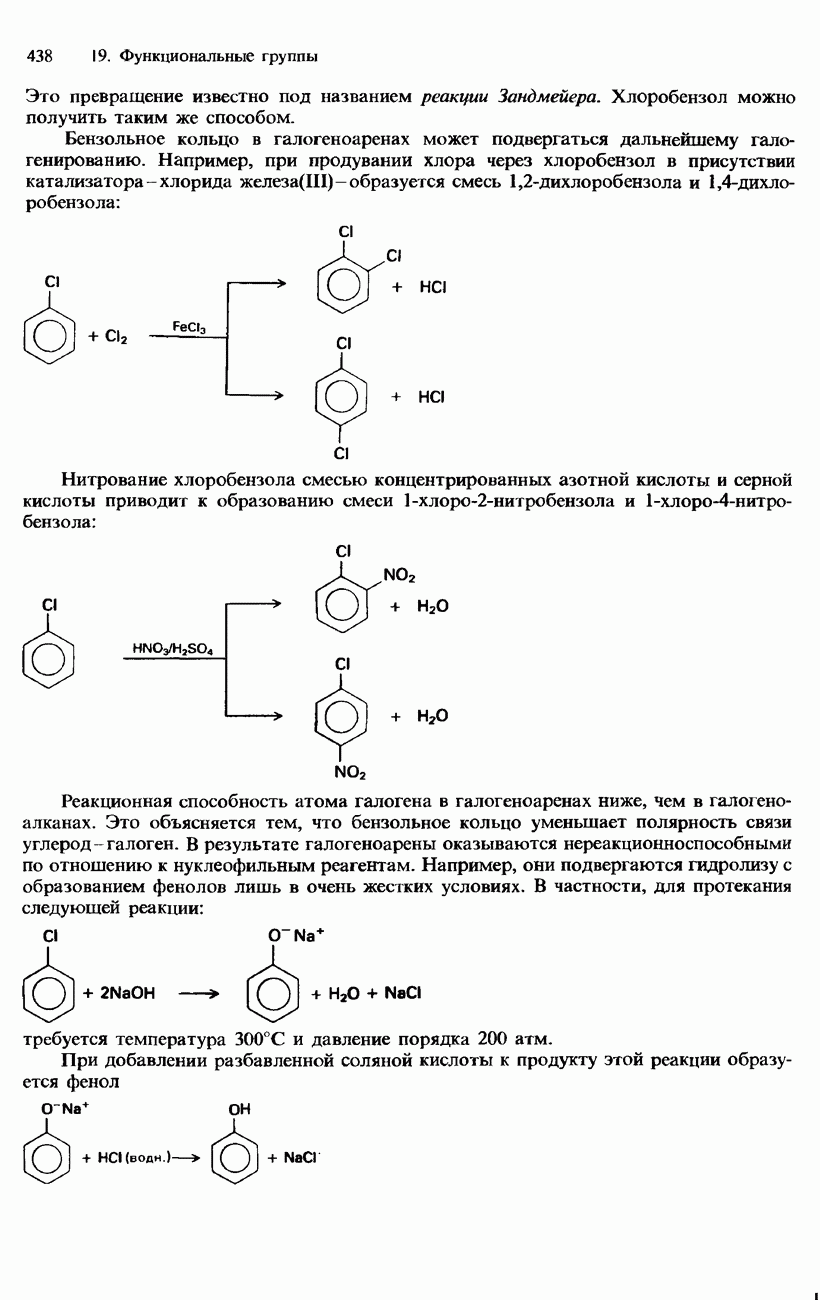
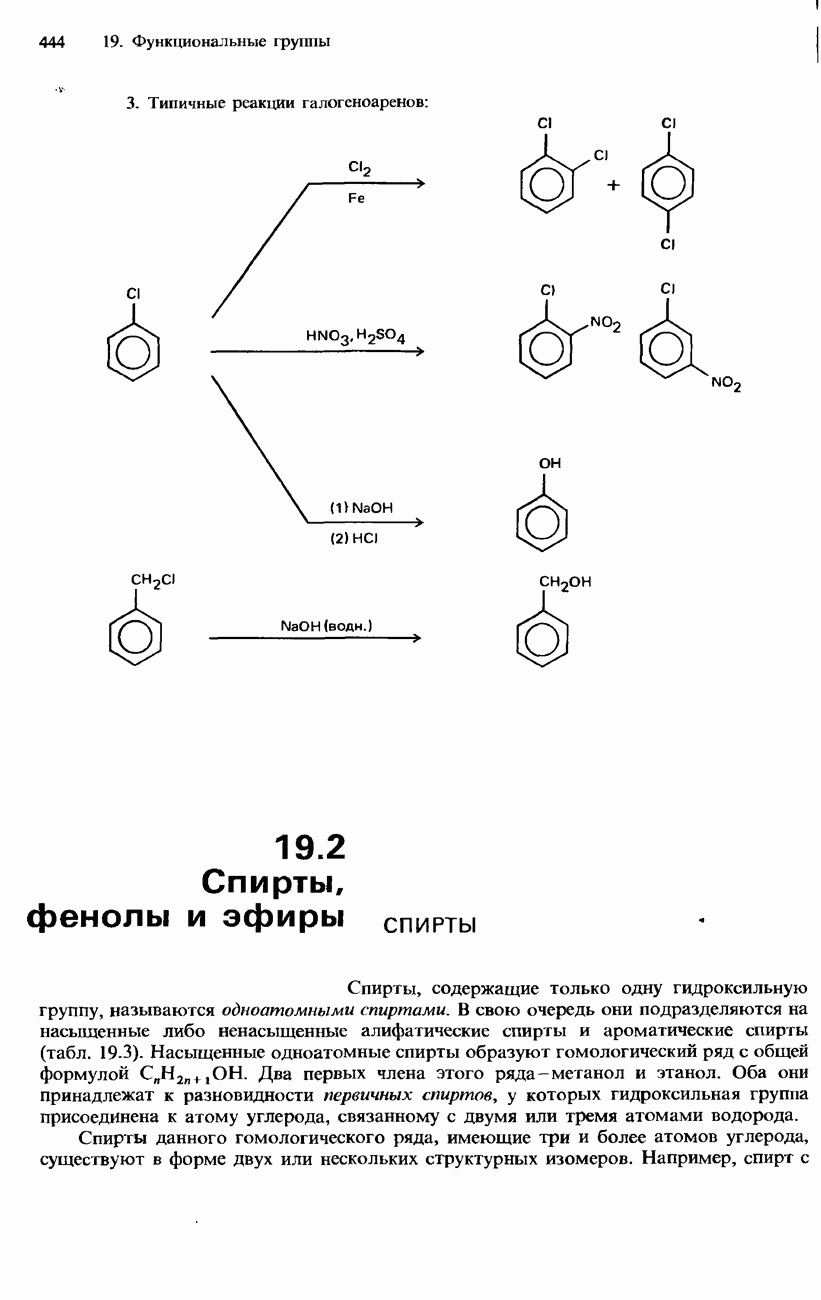
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
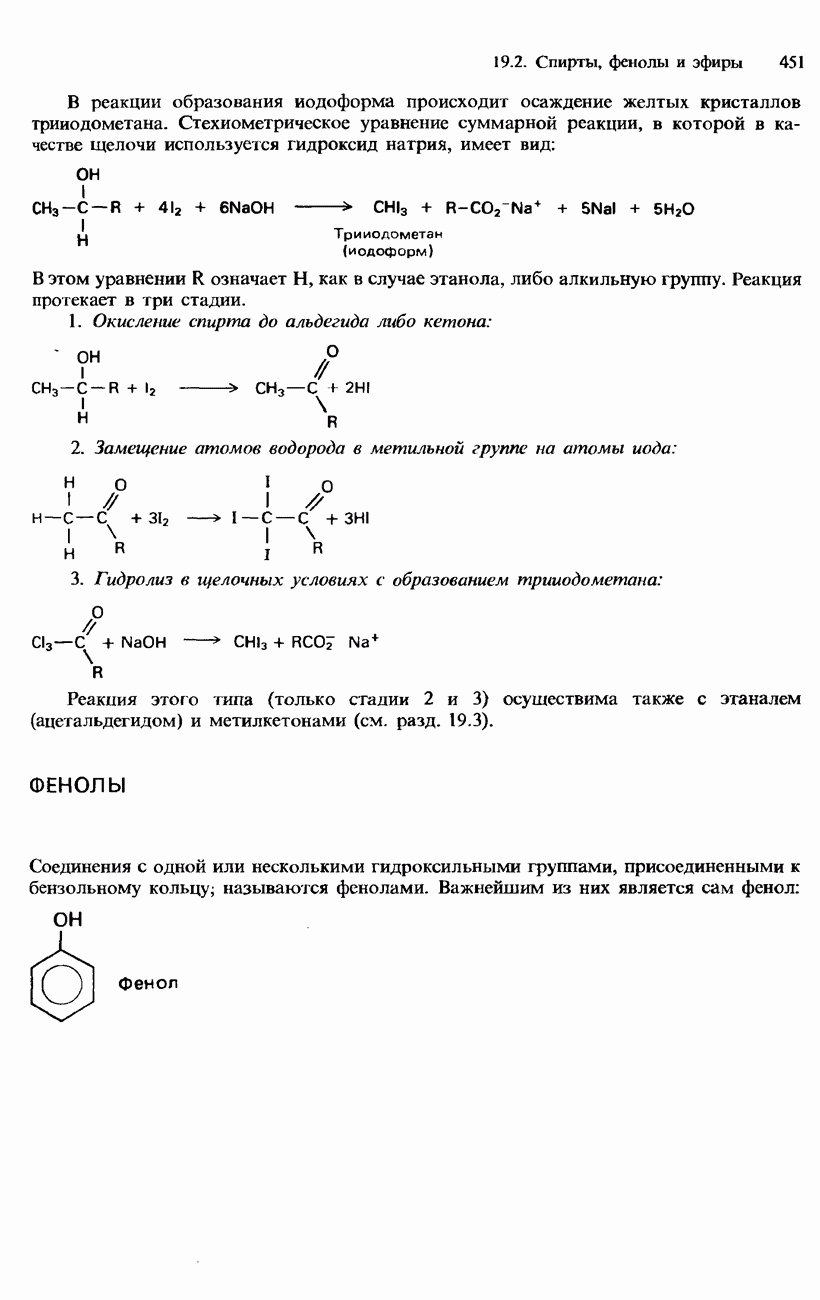
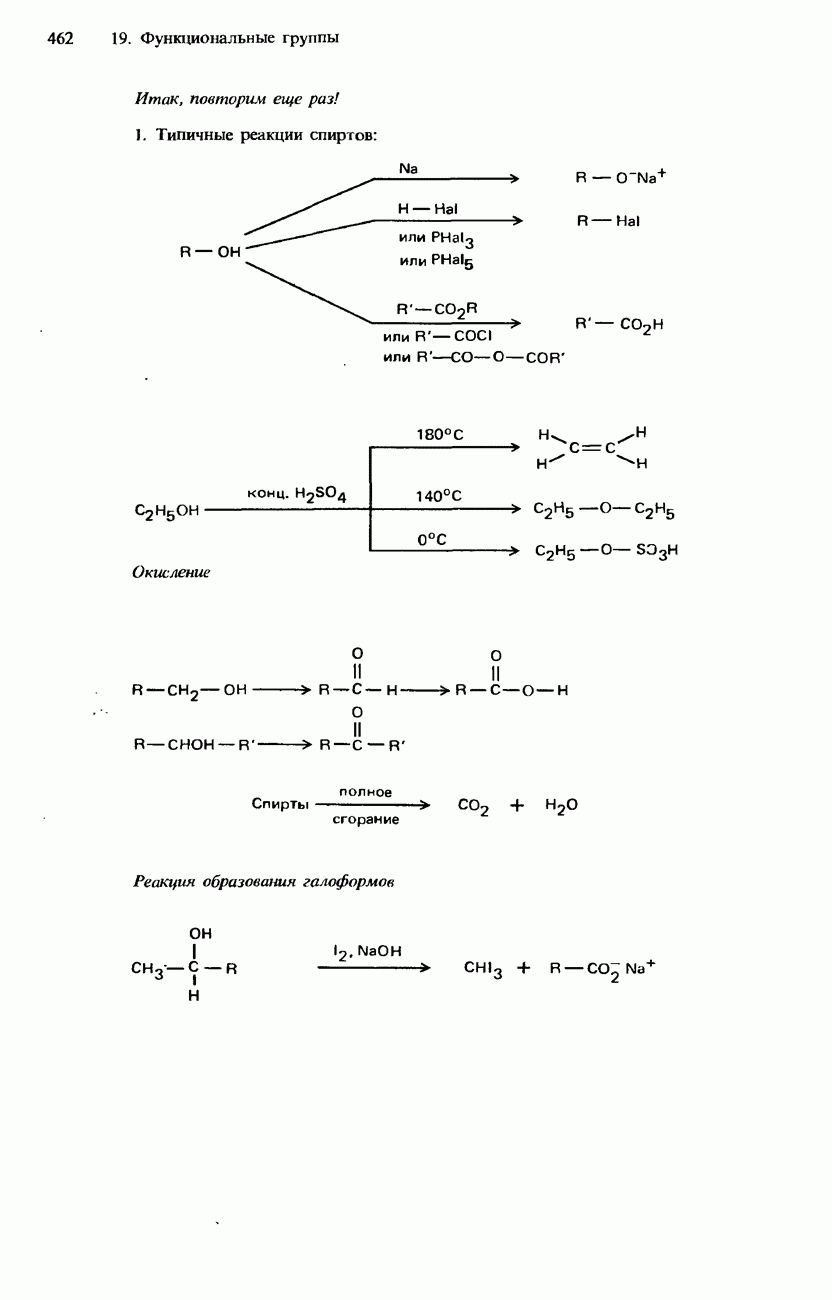
- 19.2. Спирты, фенолы и эфиры
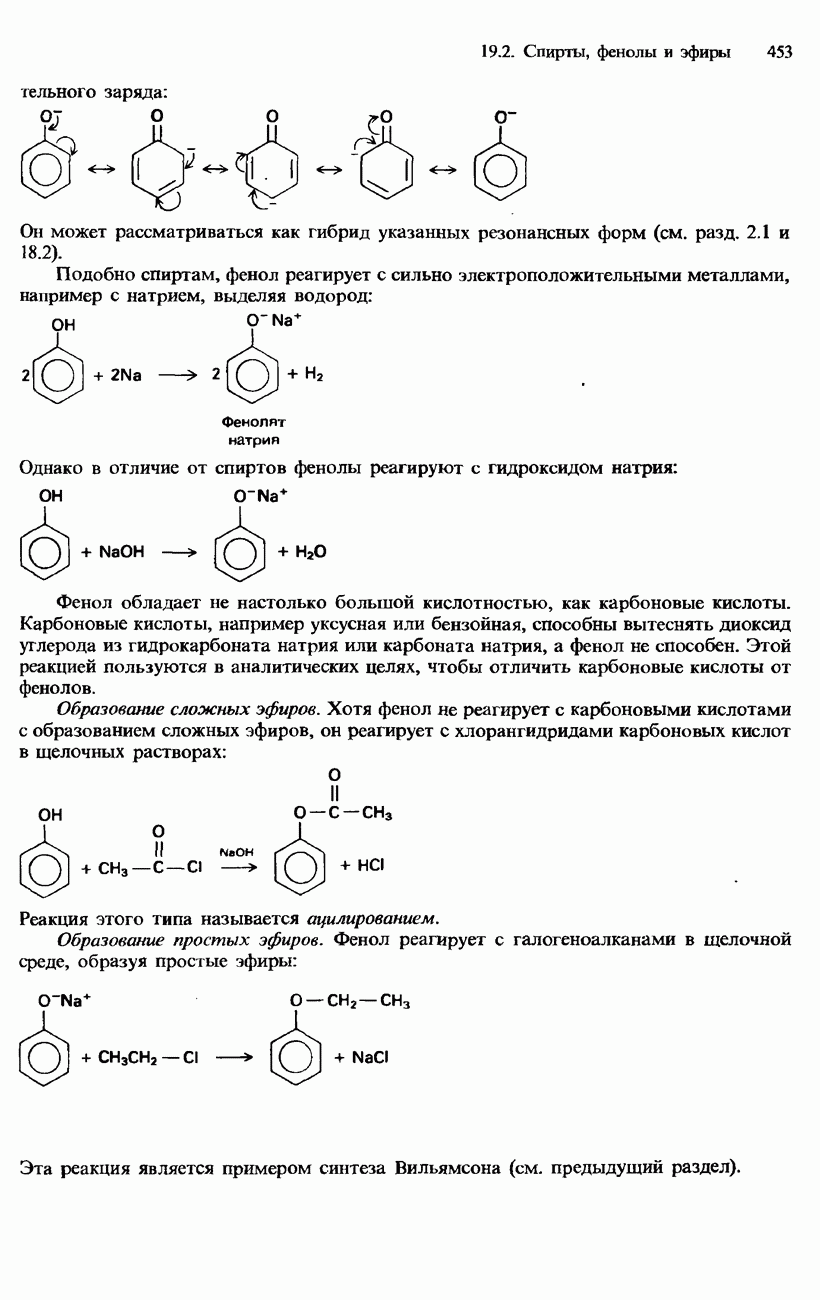
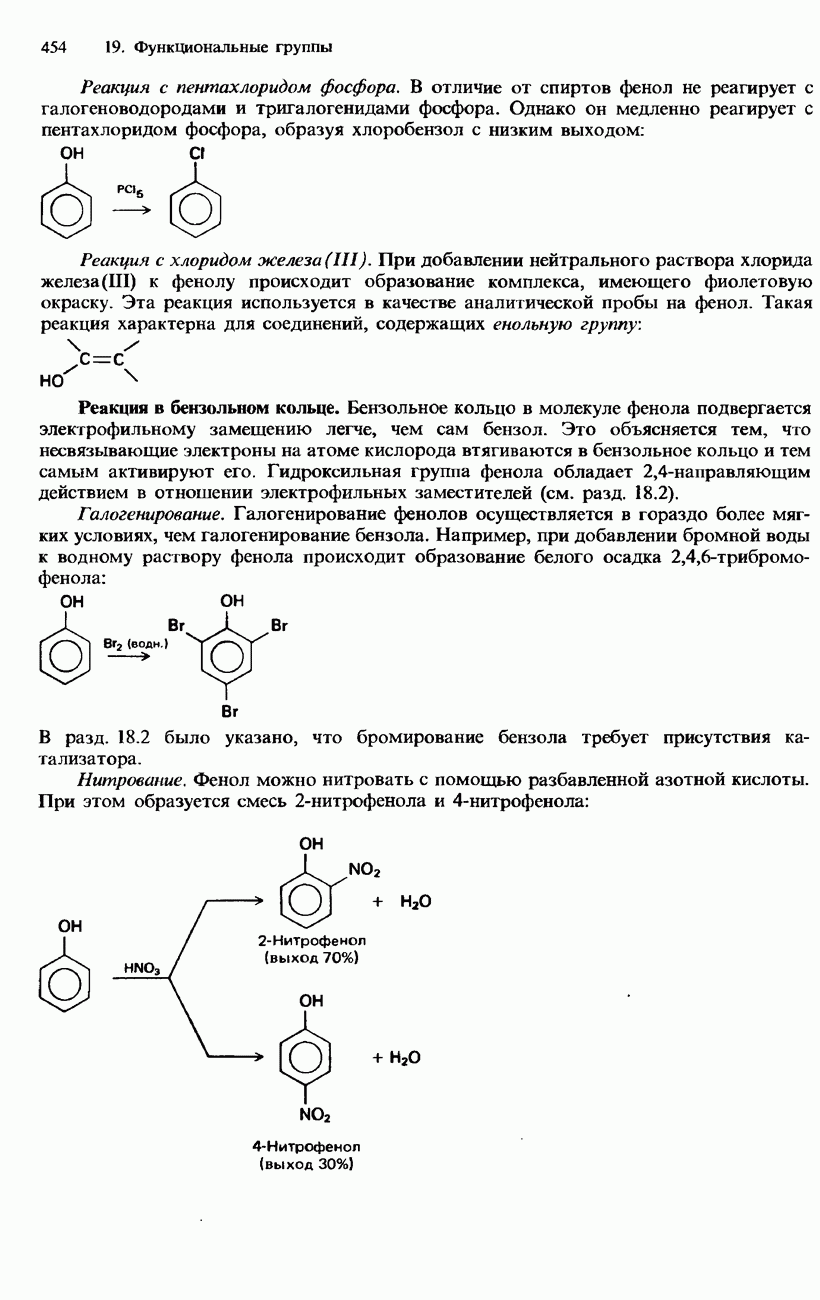
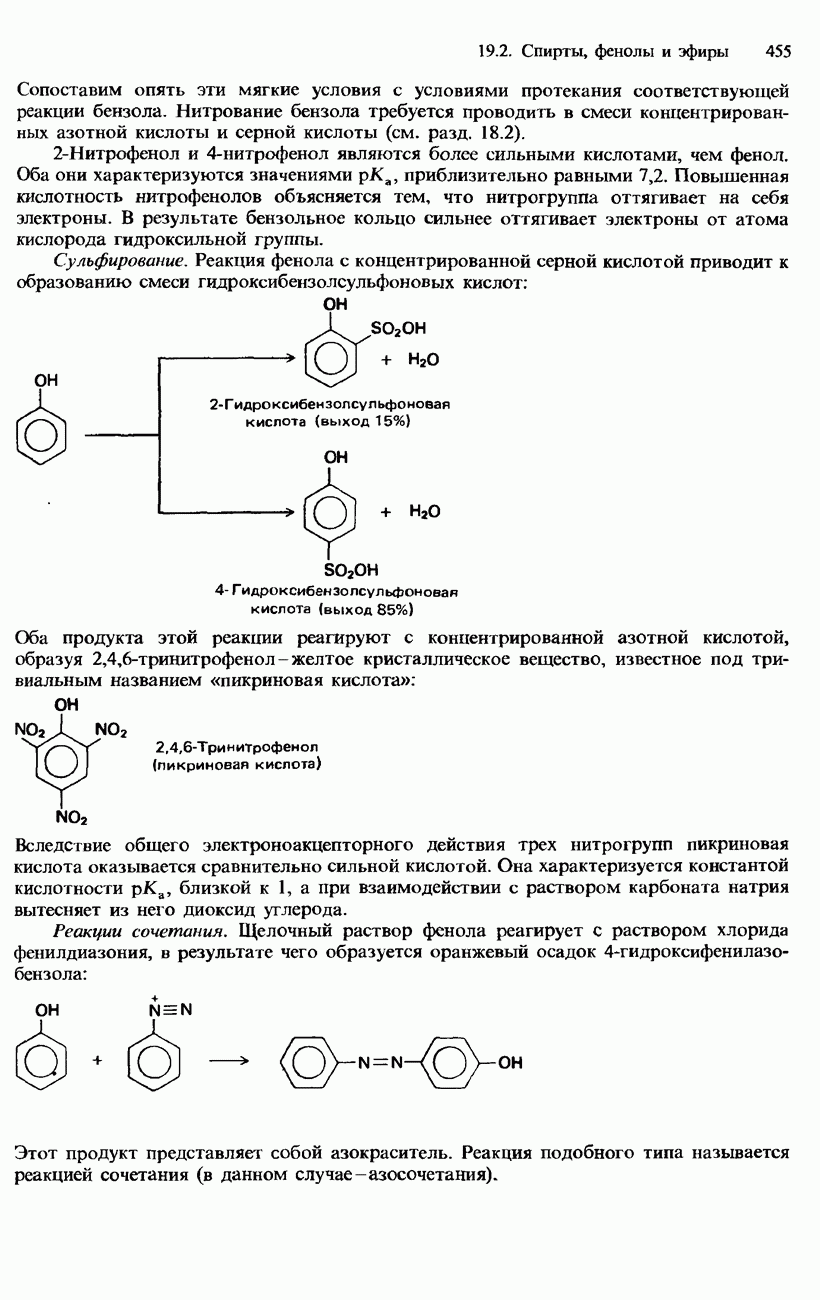
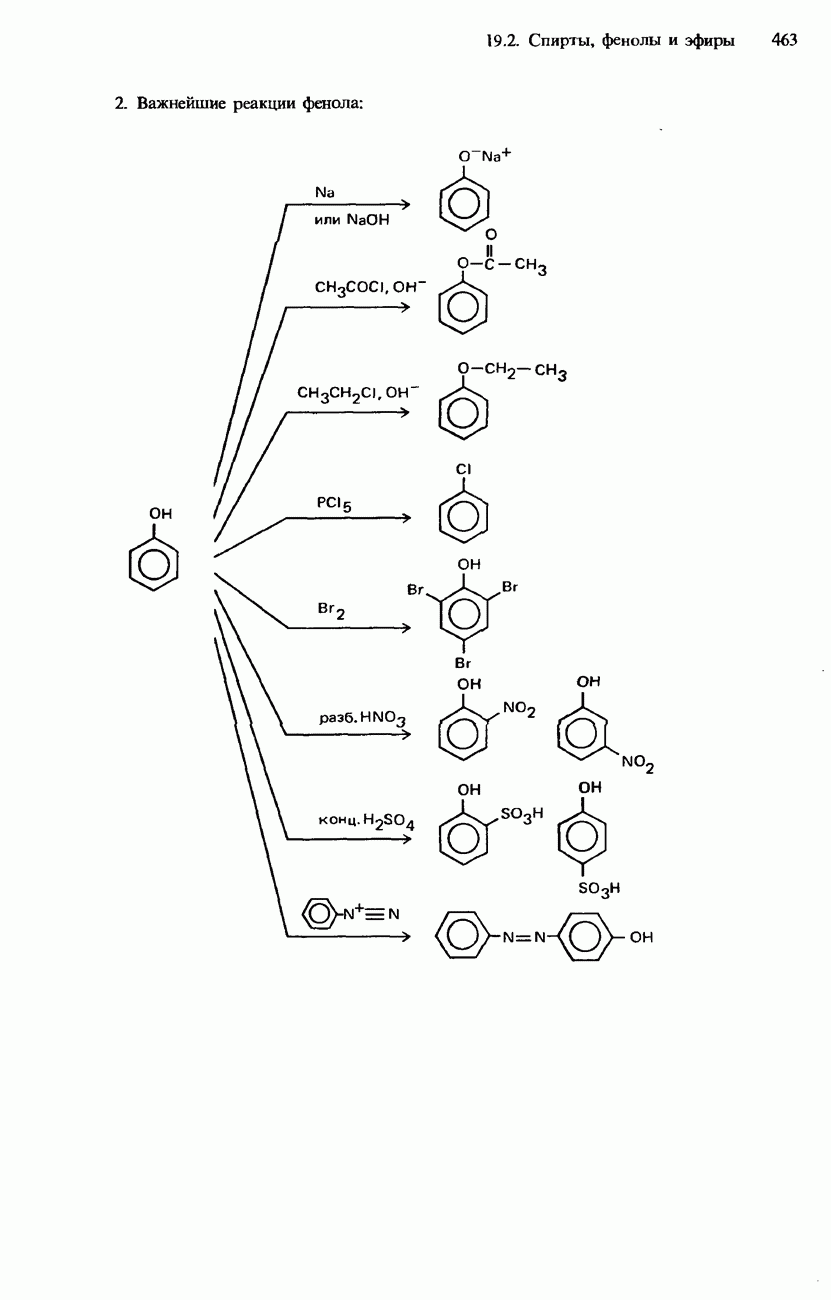
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
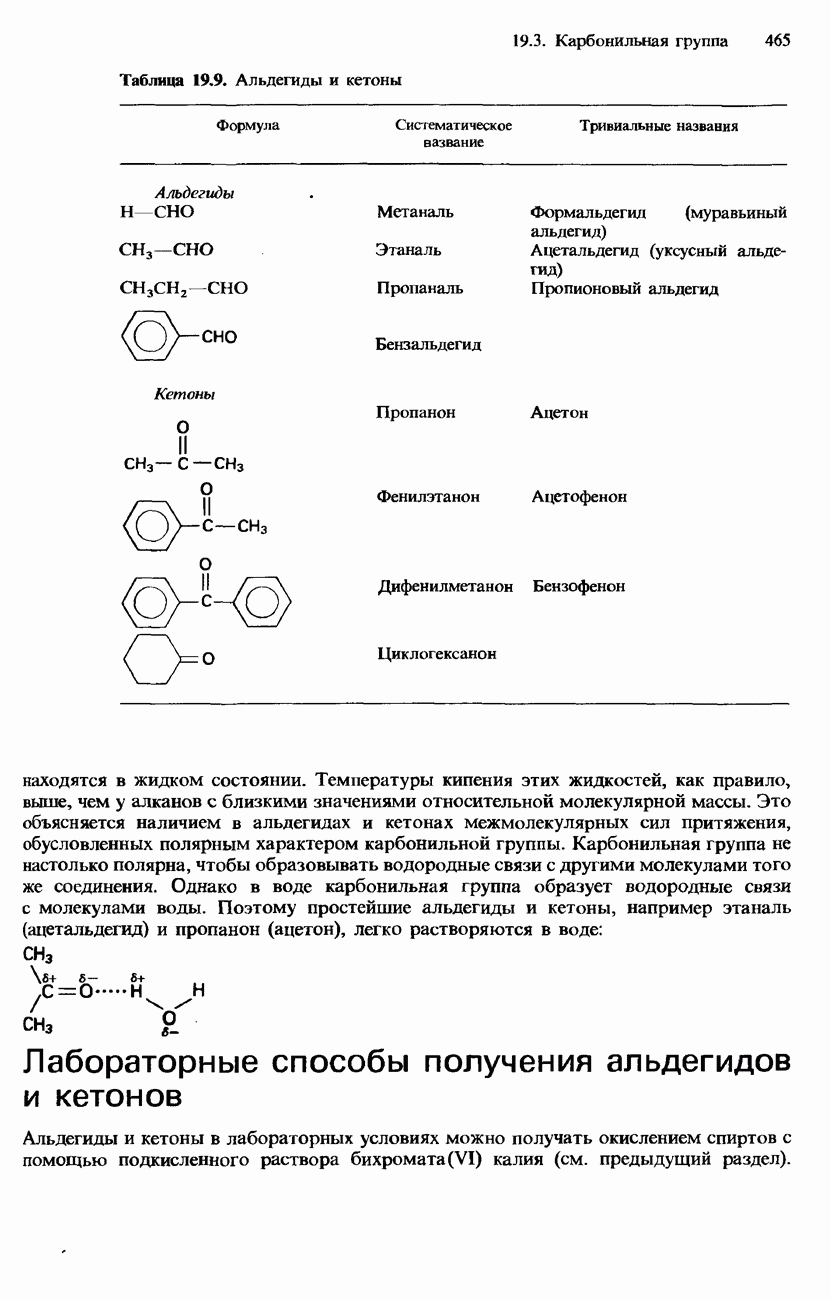
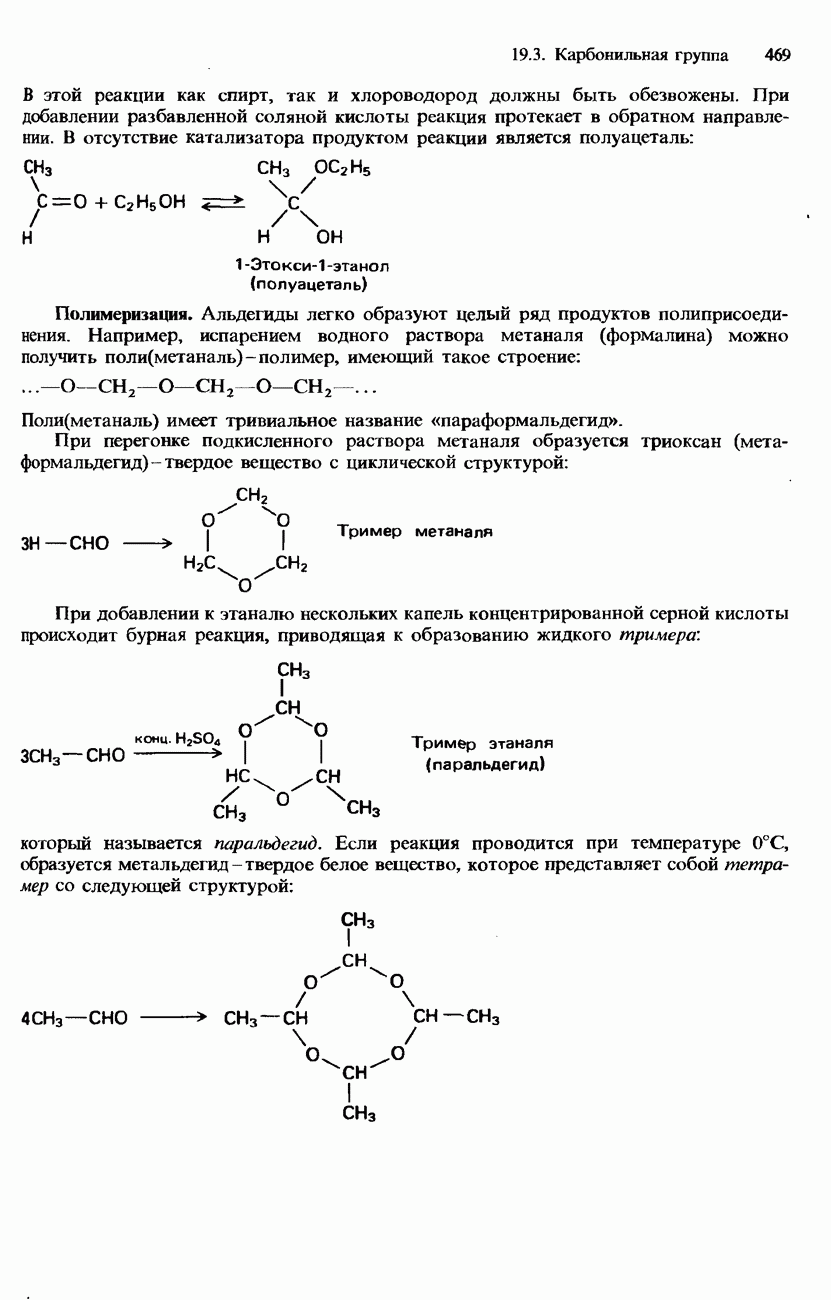
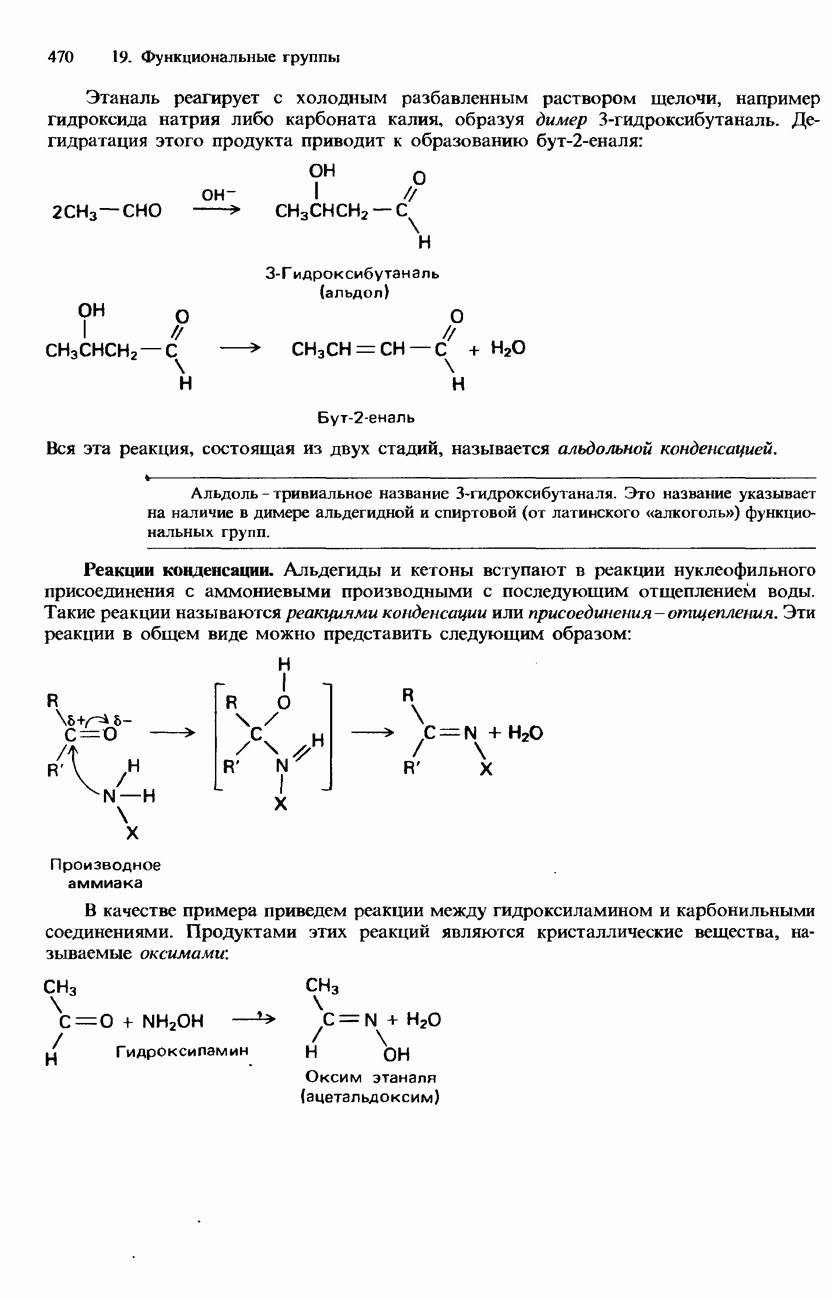
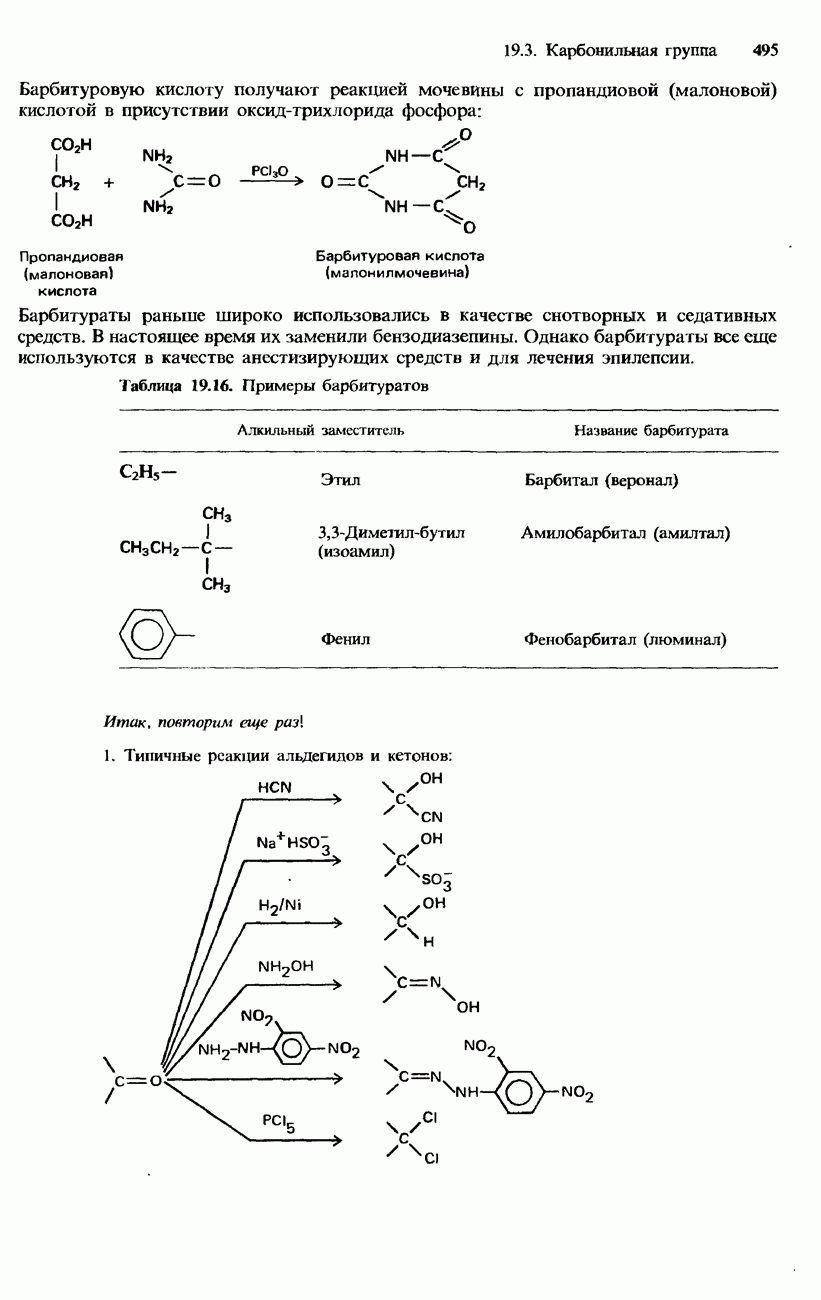
- 19.3. Карбонильная группа
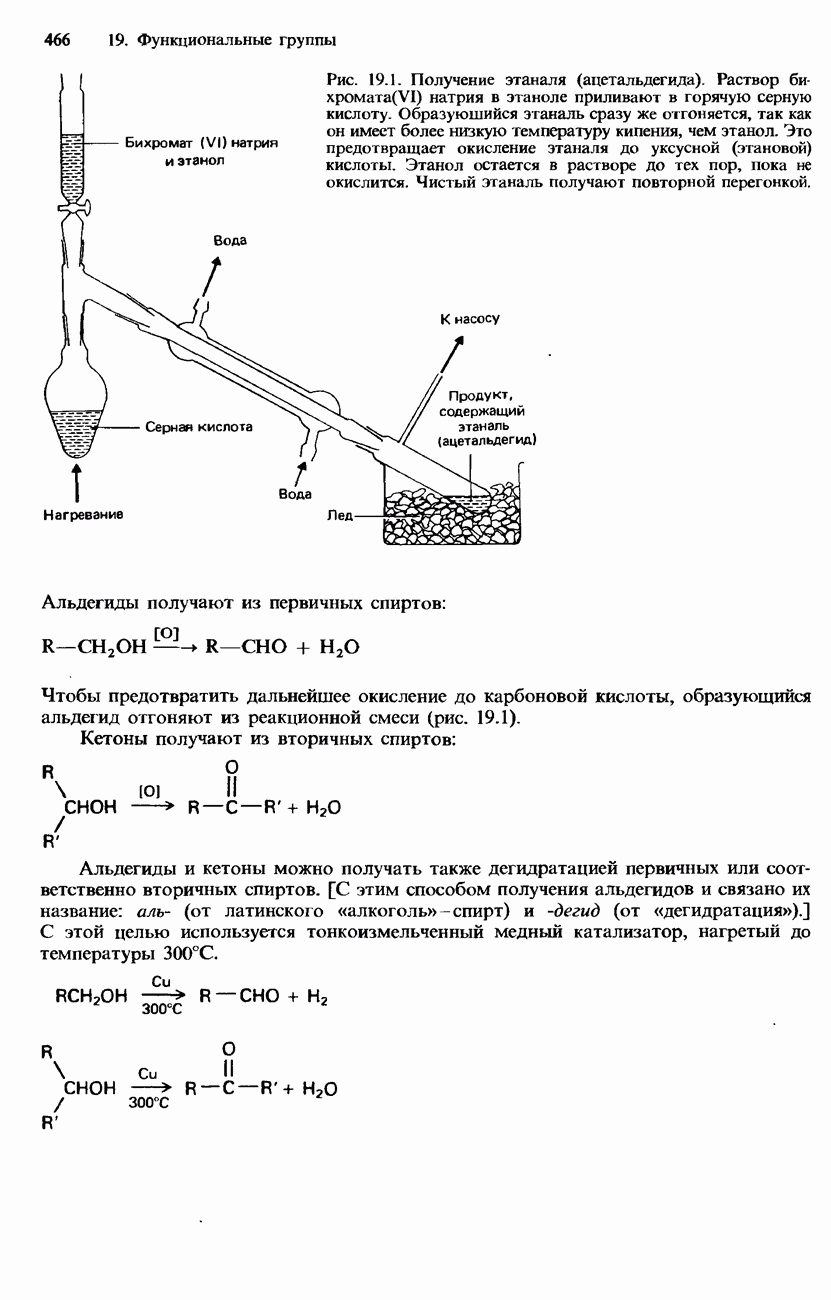
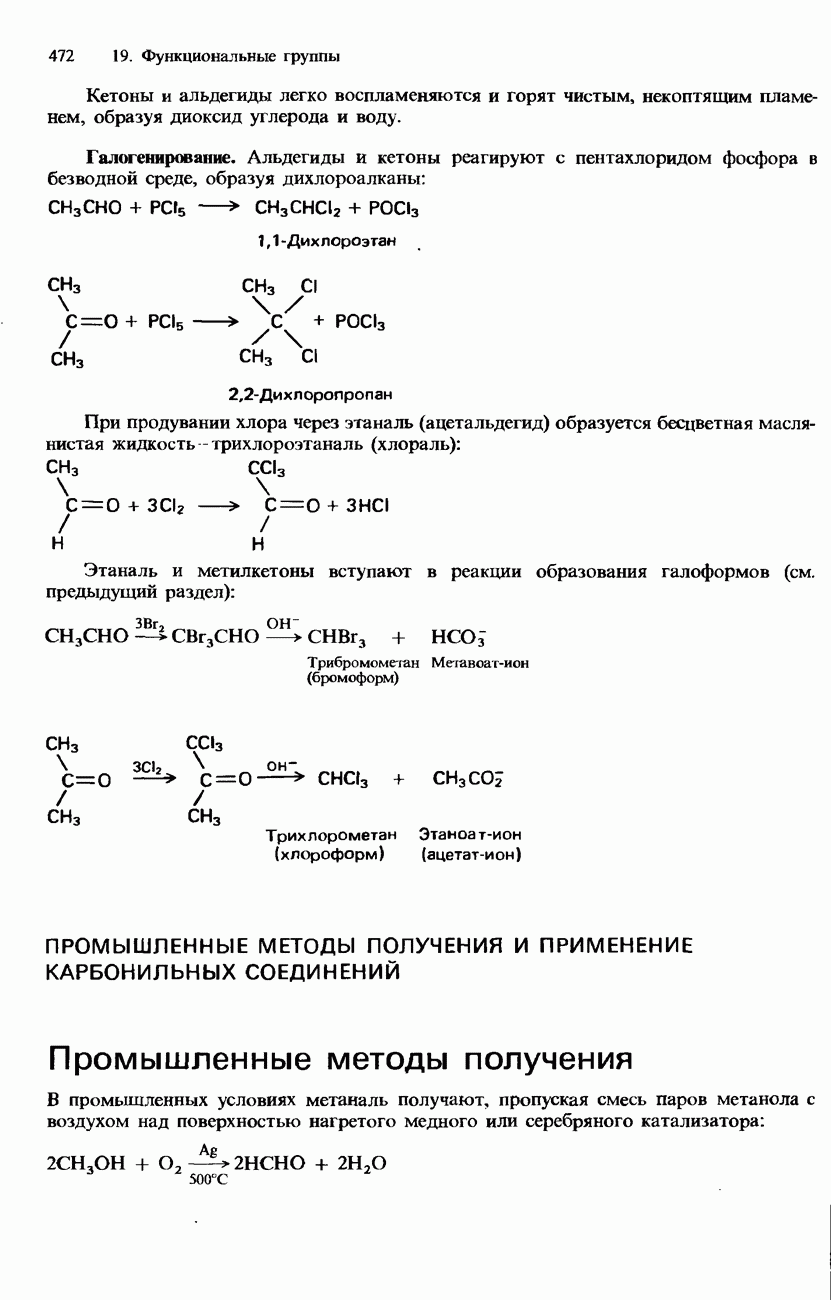
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
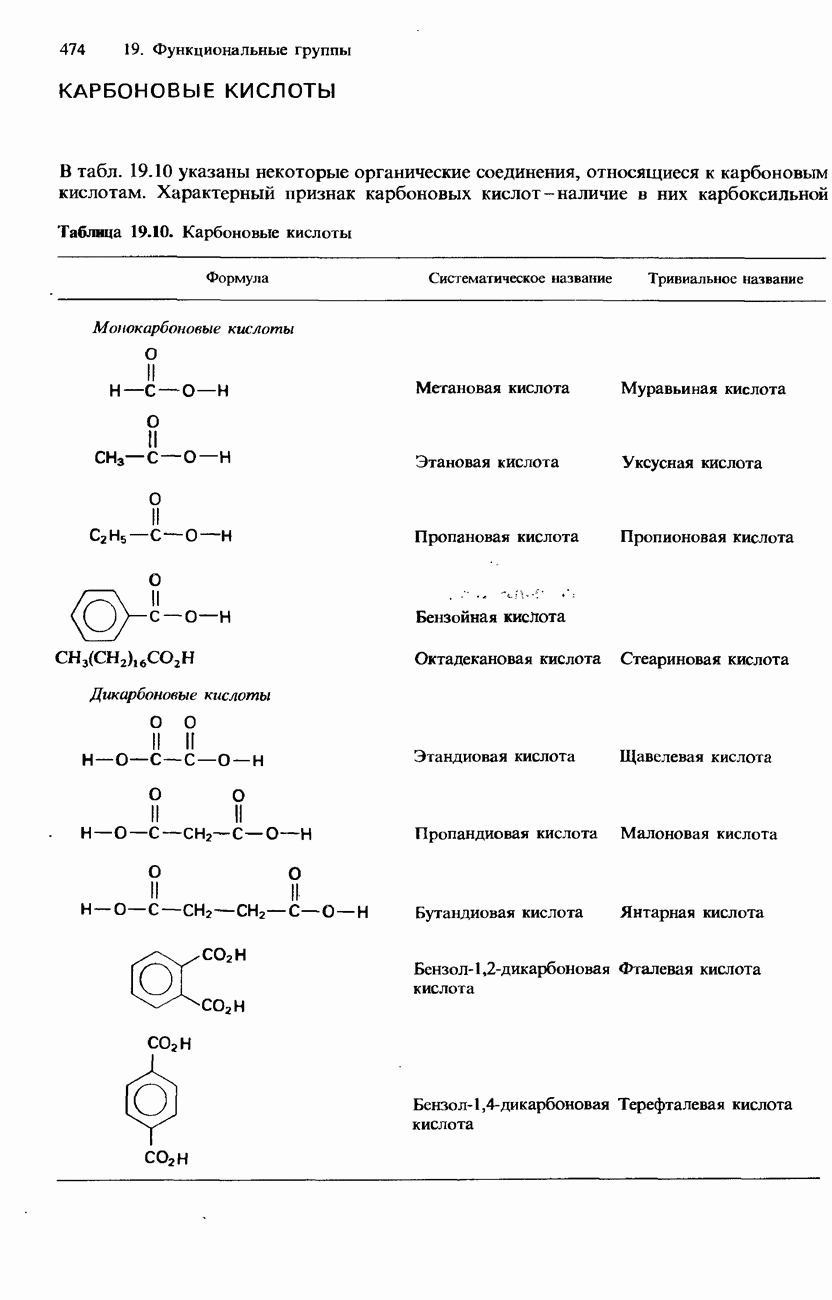
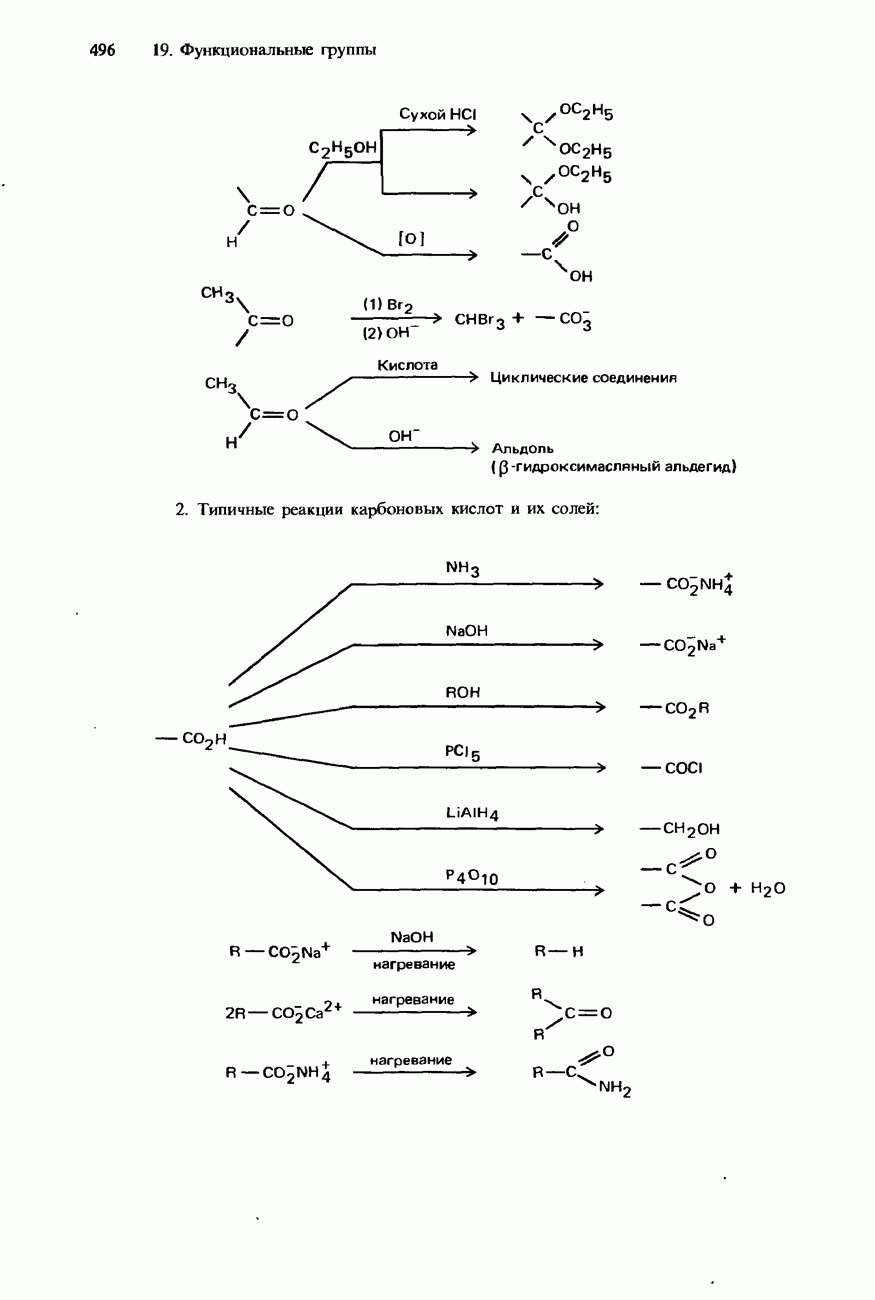
- КАРБОНОВЫЕ КИСЛОТЫ
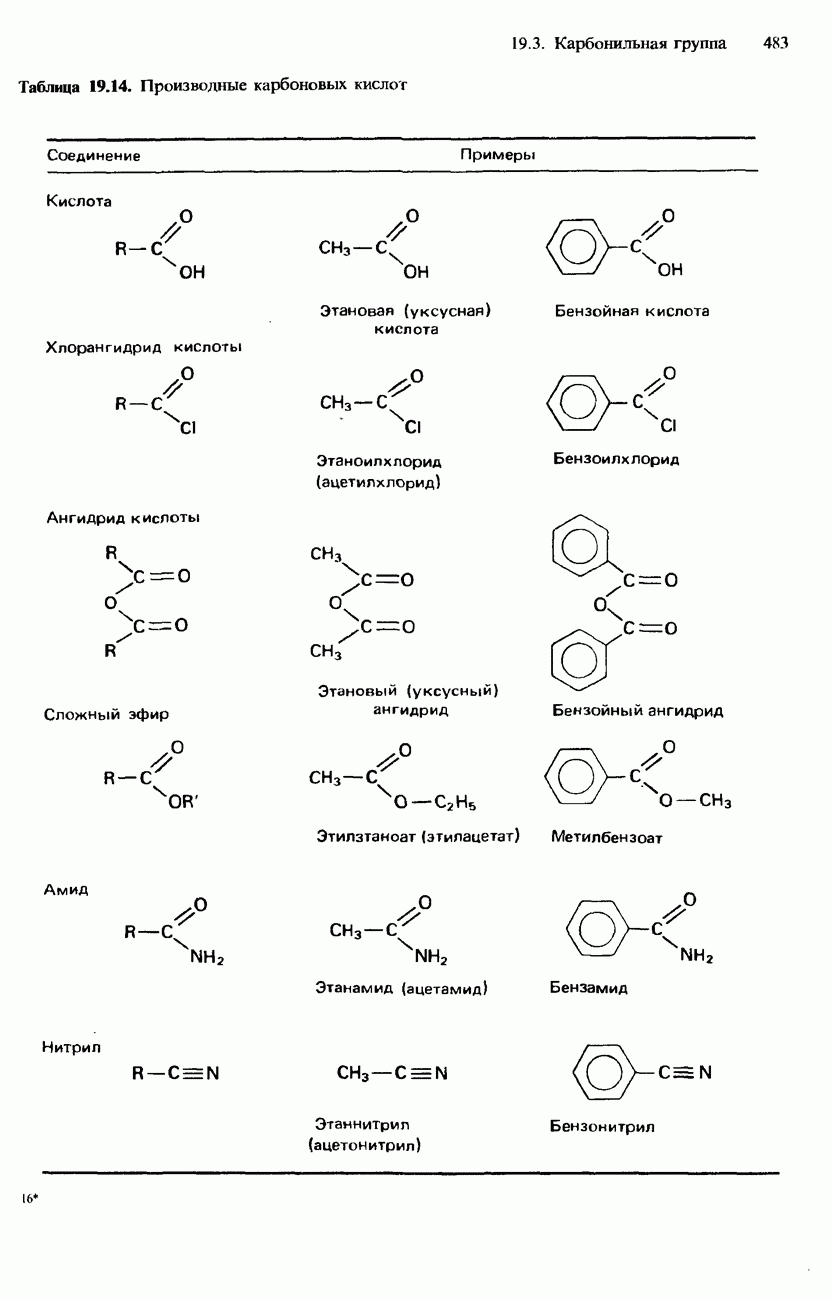
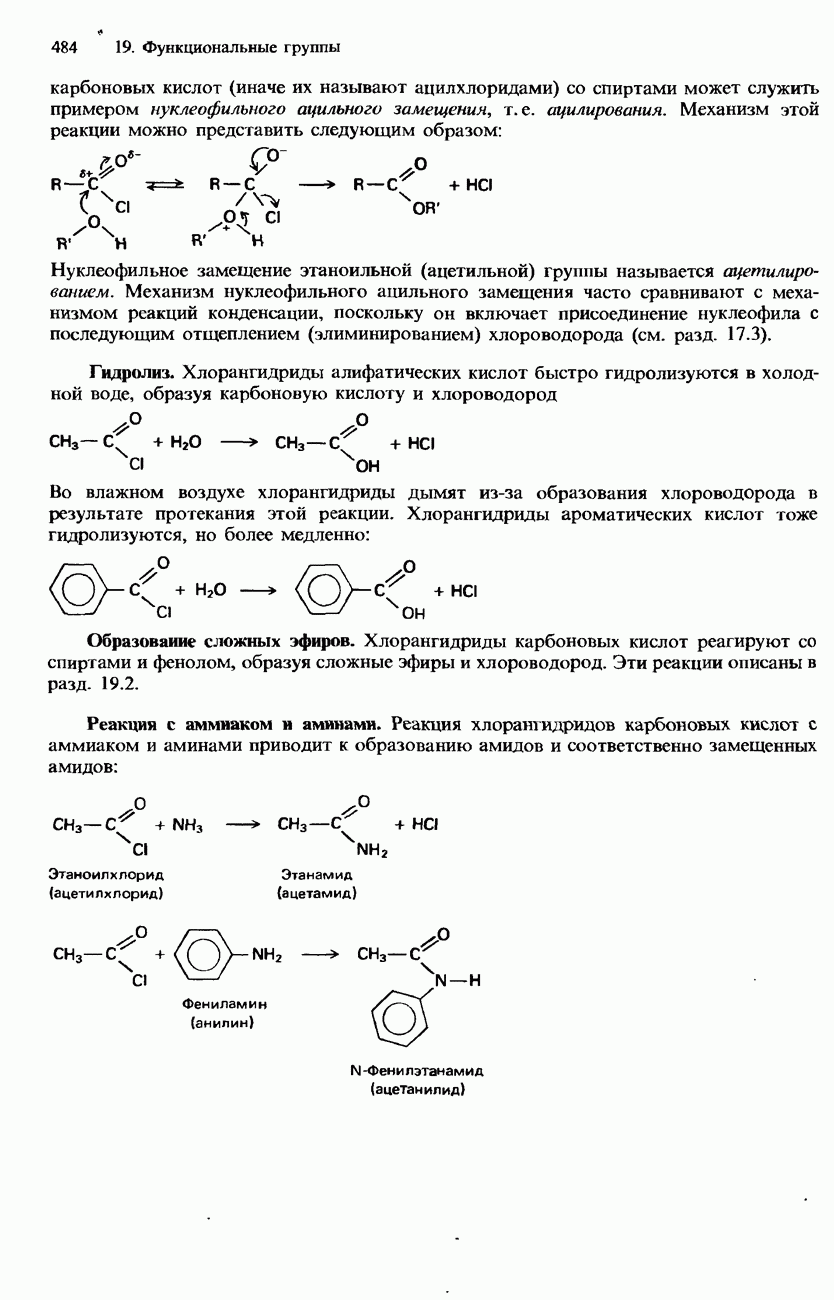
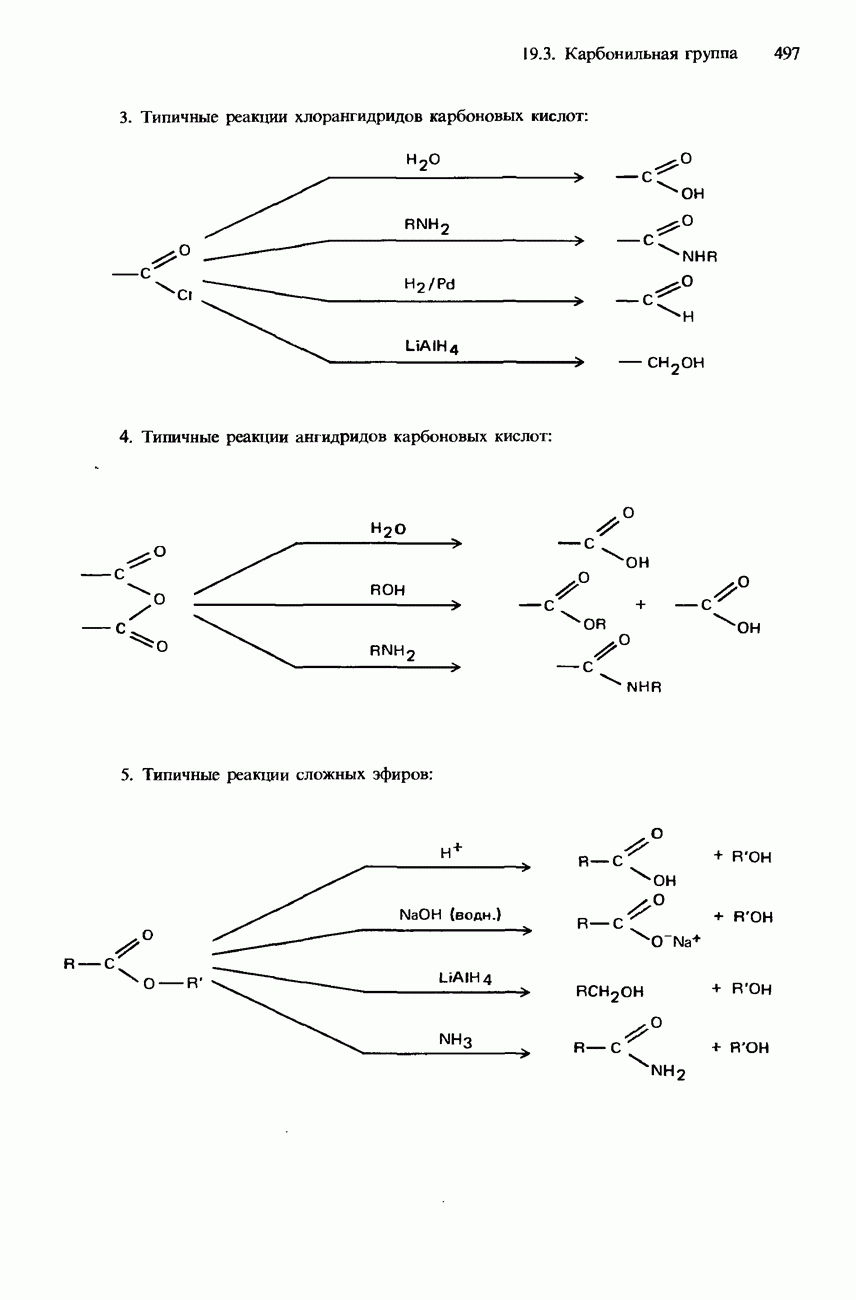
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
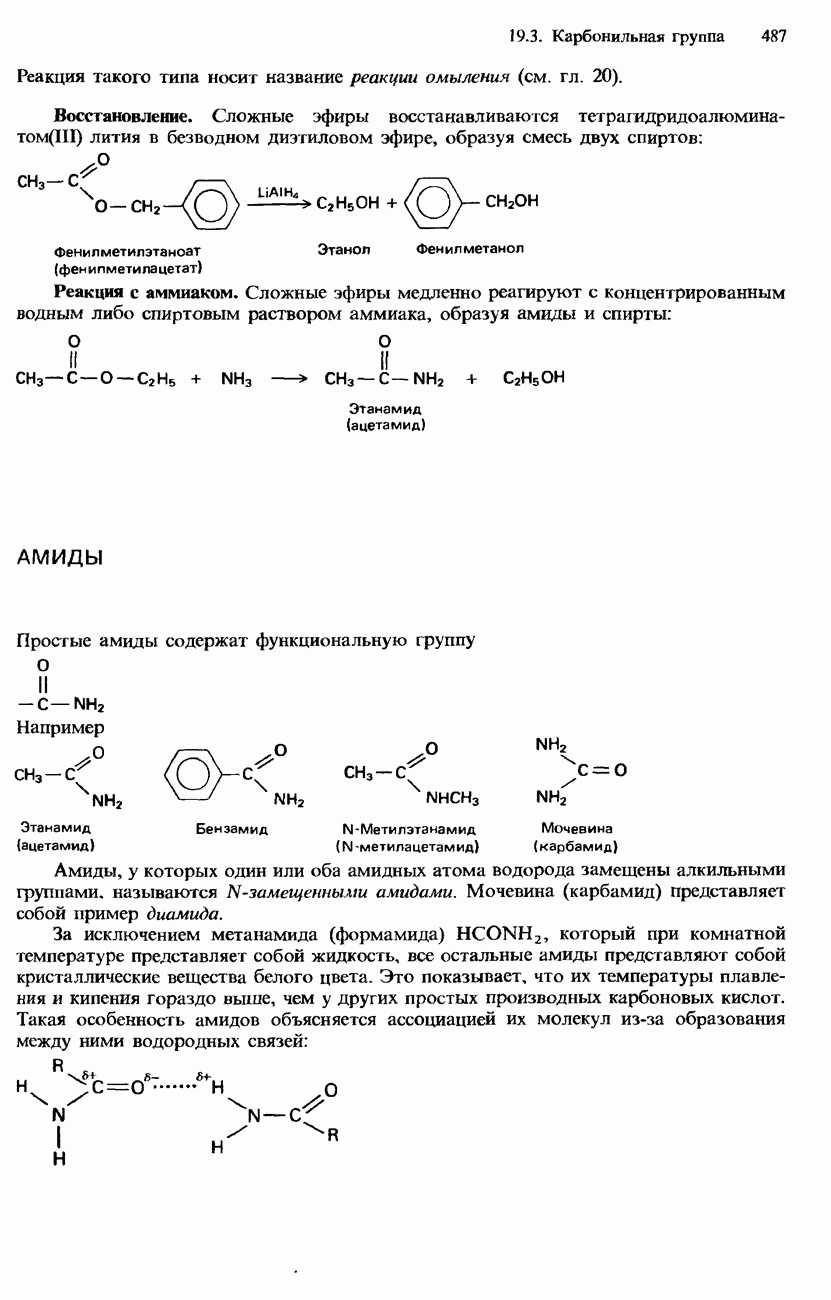
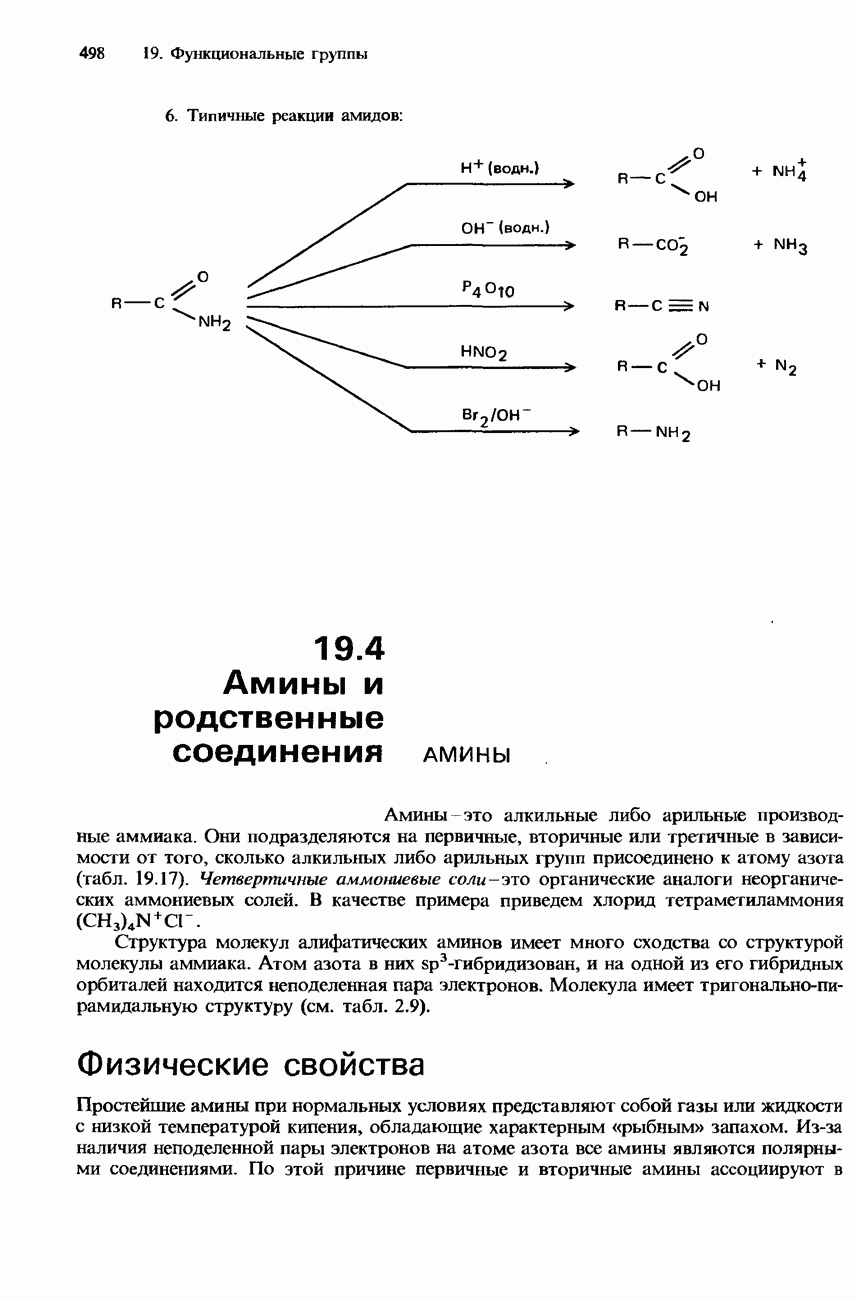
- АМИДЫ
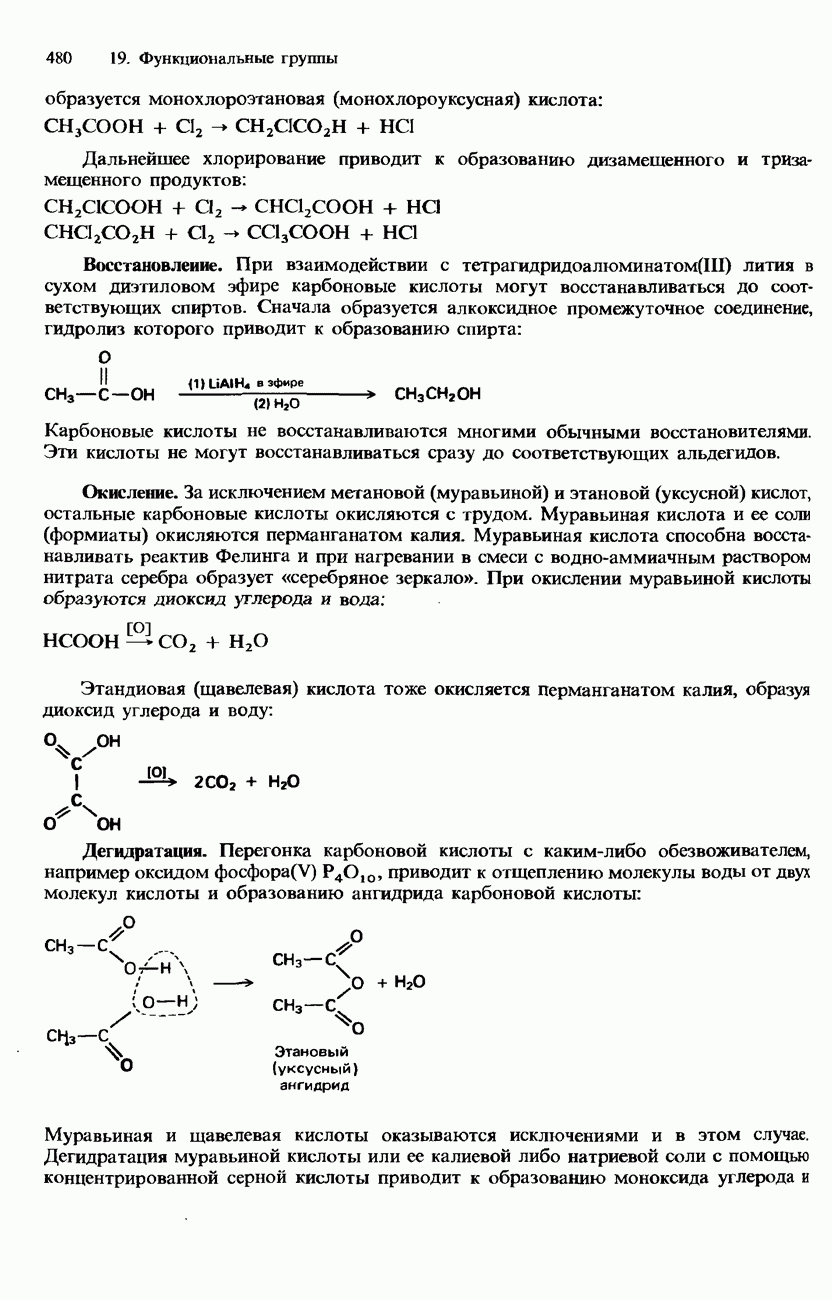
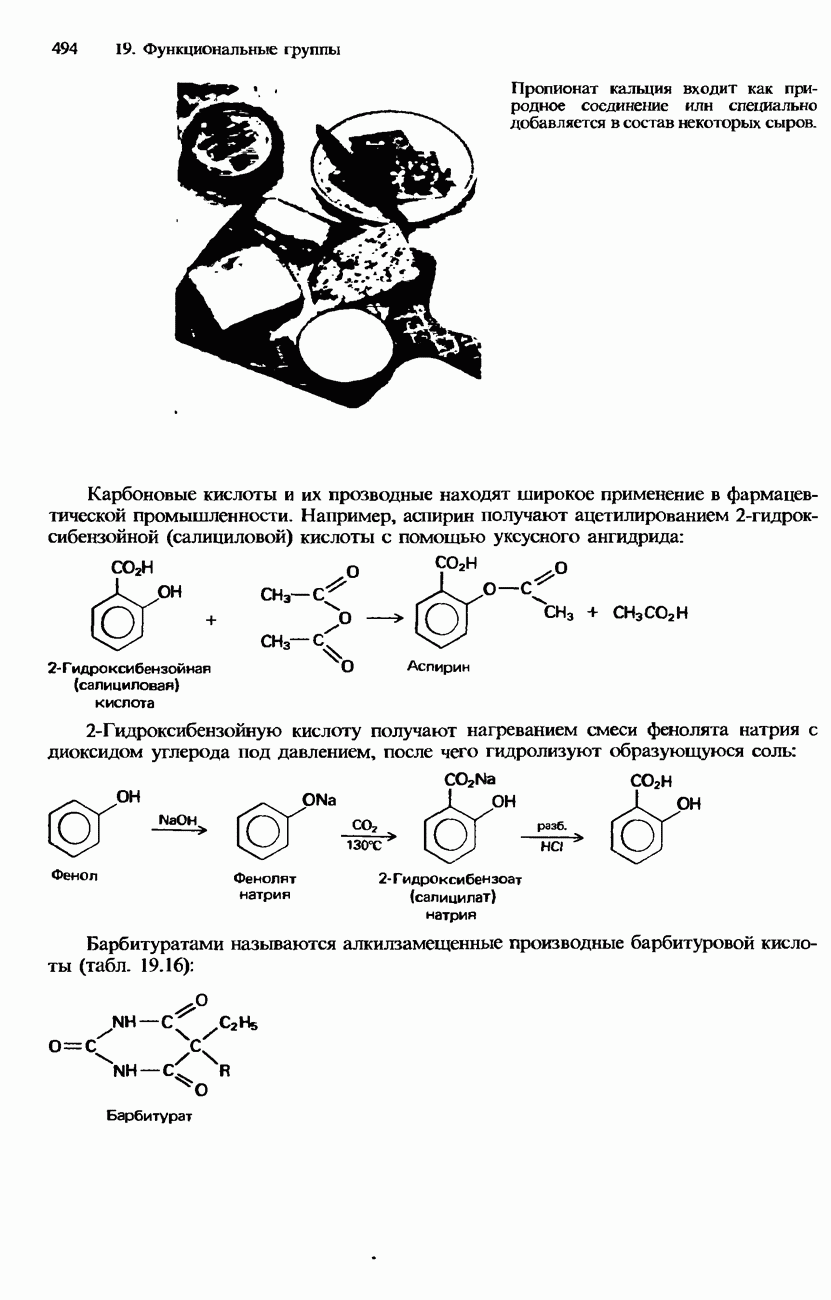
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
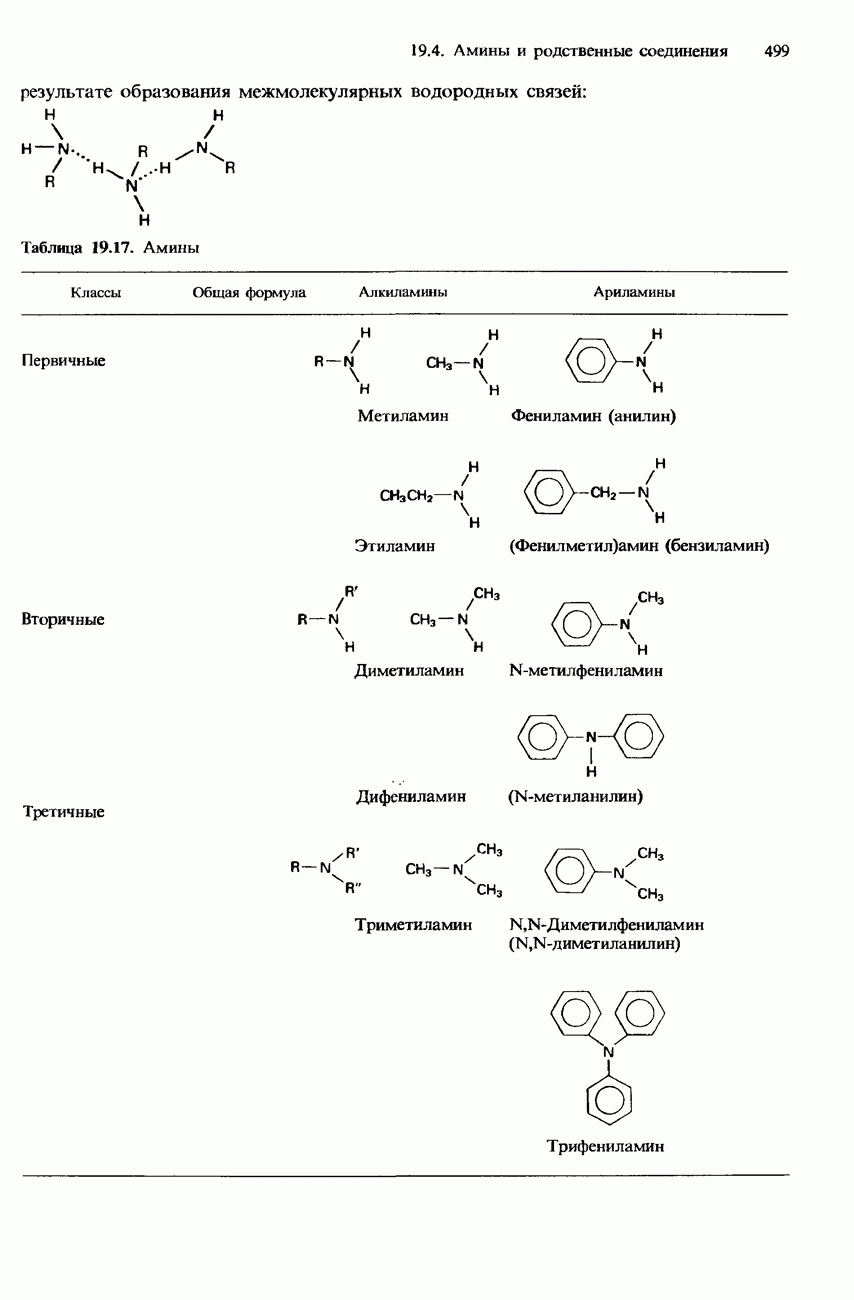
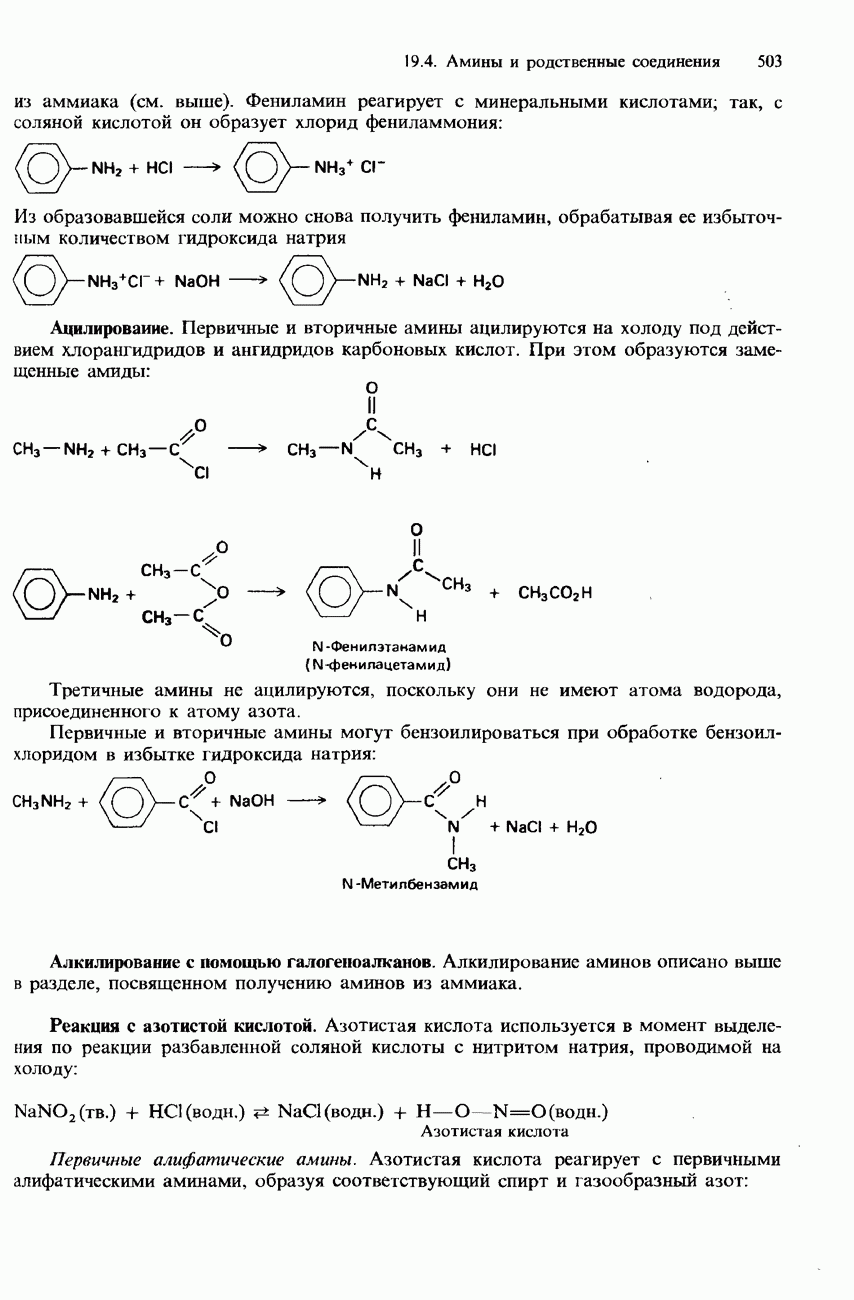
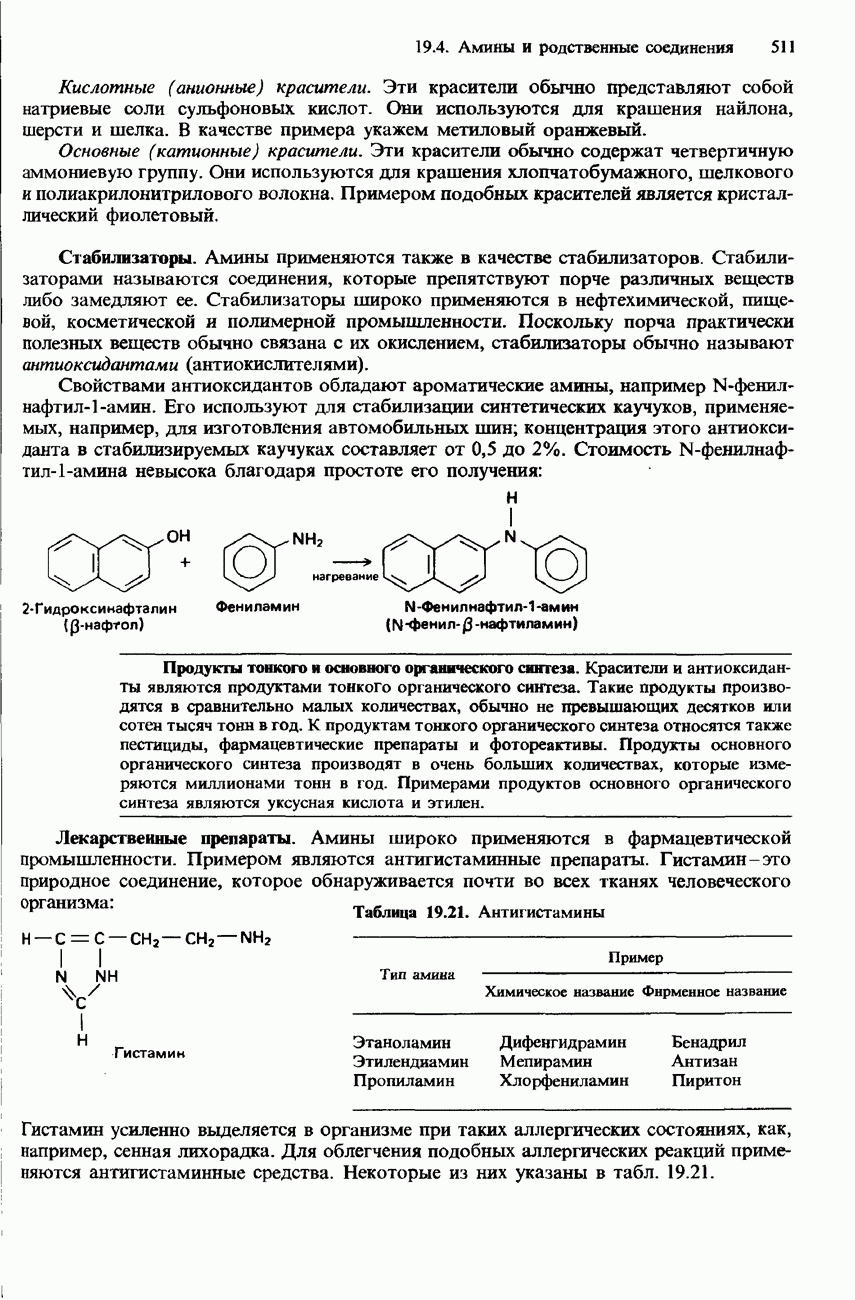
- 19.4 Амины и родственные соединения
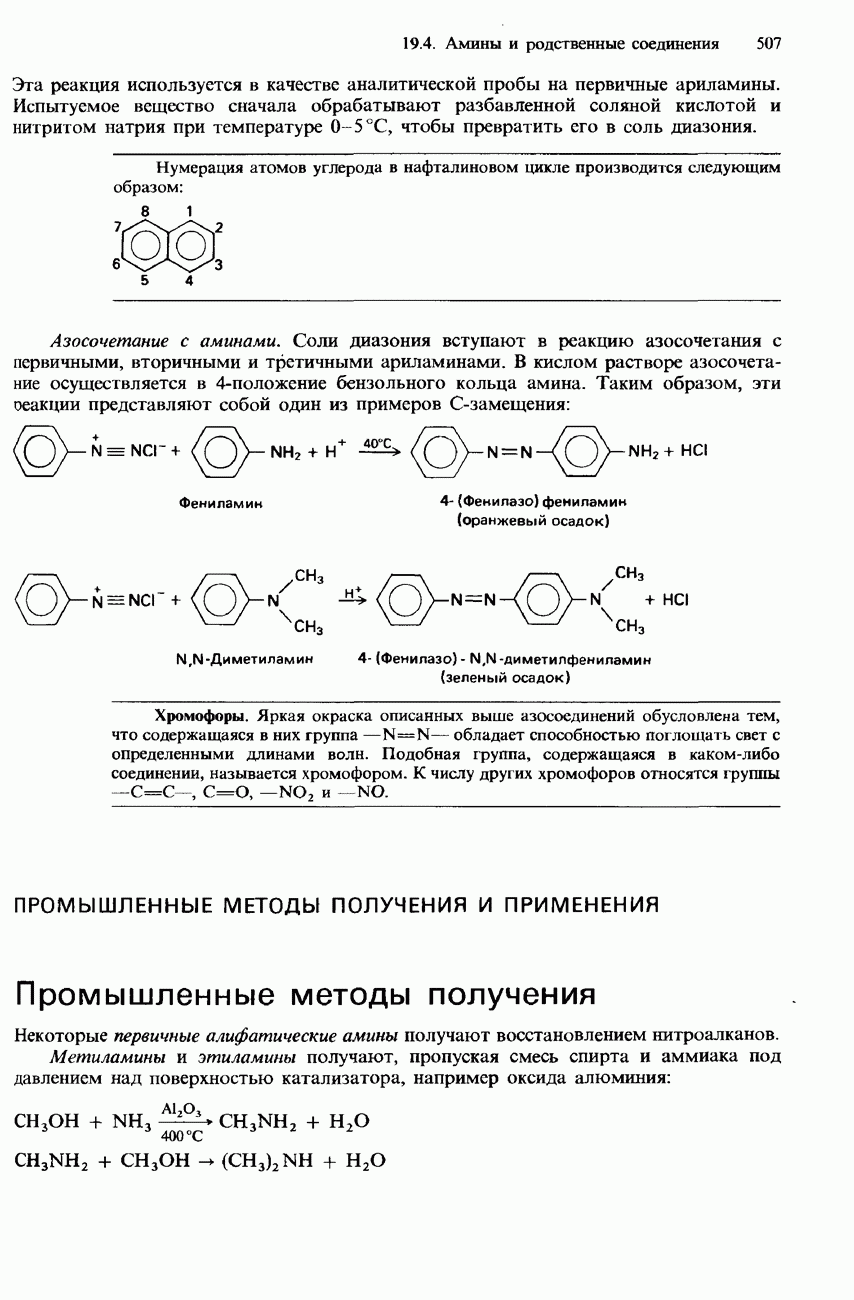
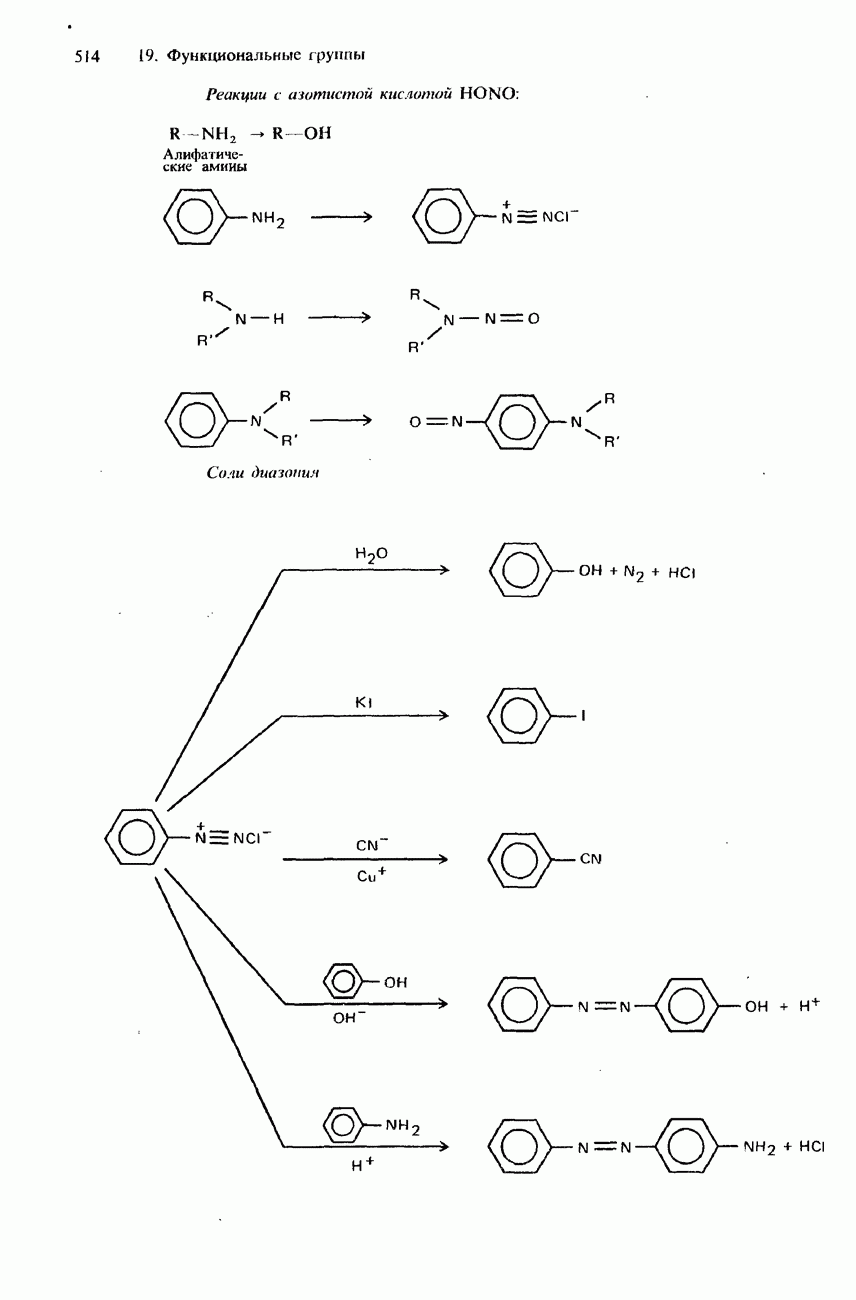
- СОЛИ ДИАЗОНИЯ
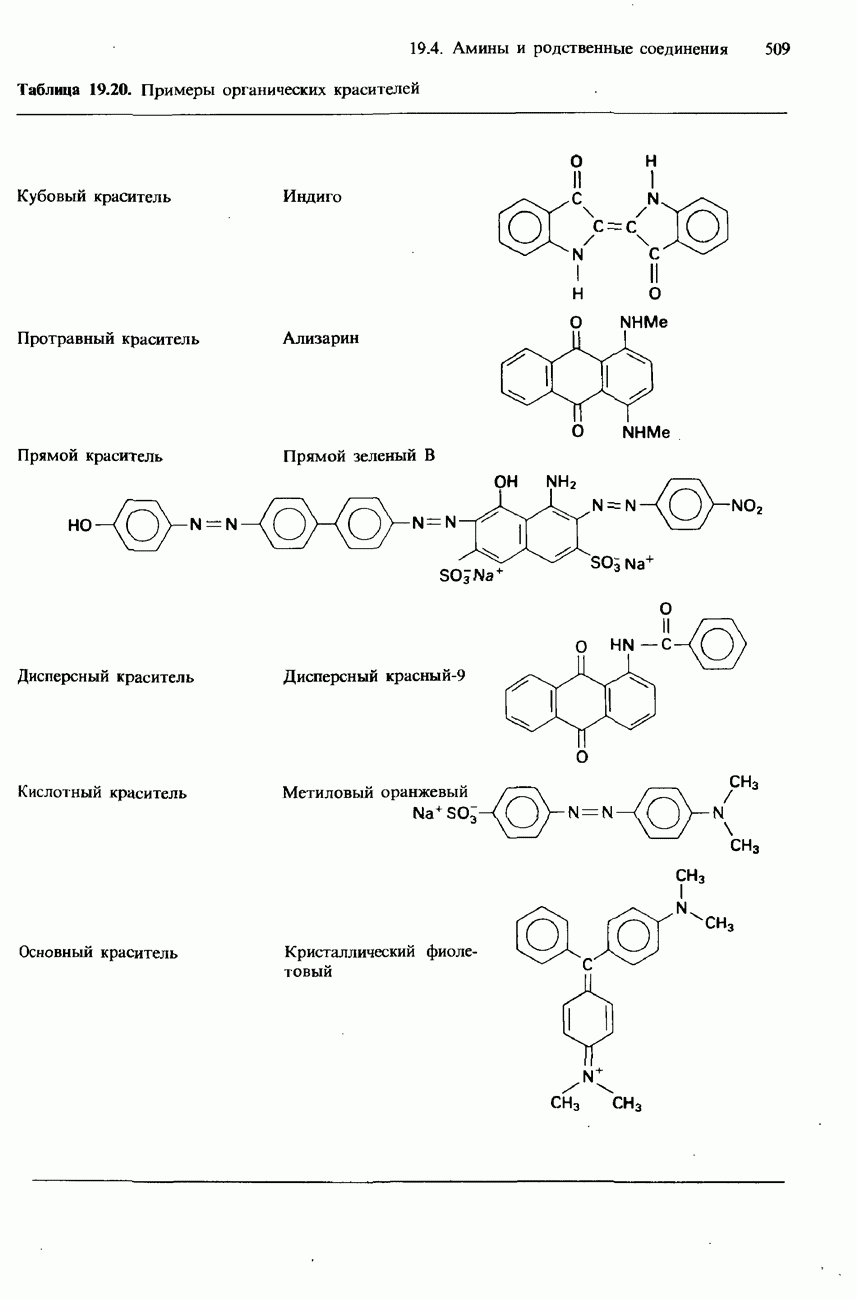
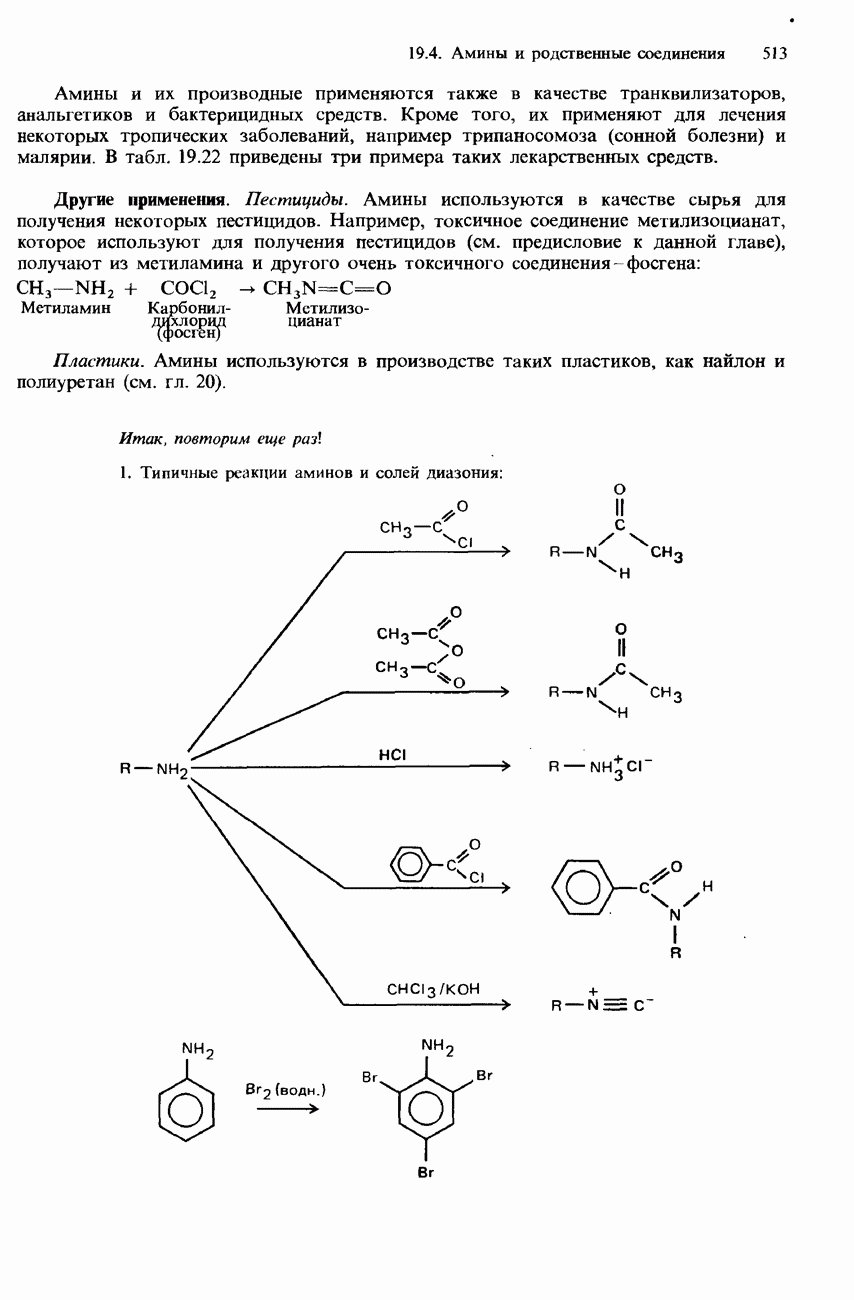
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
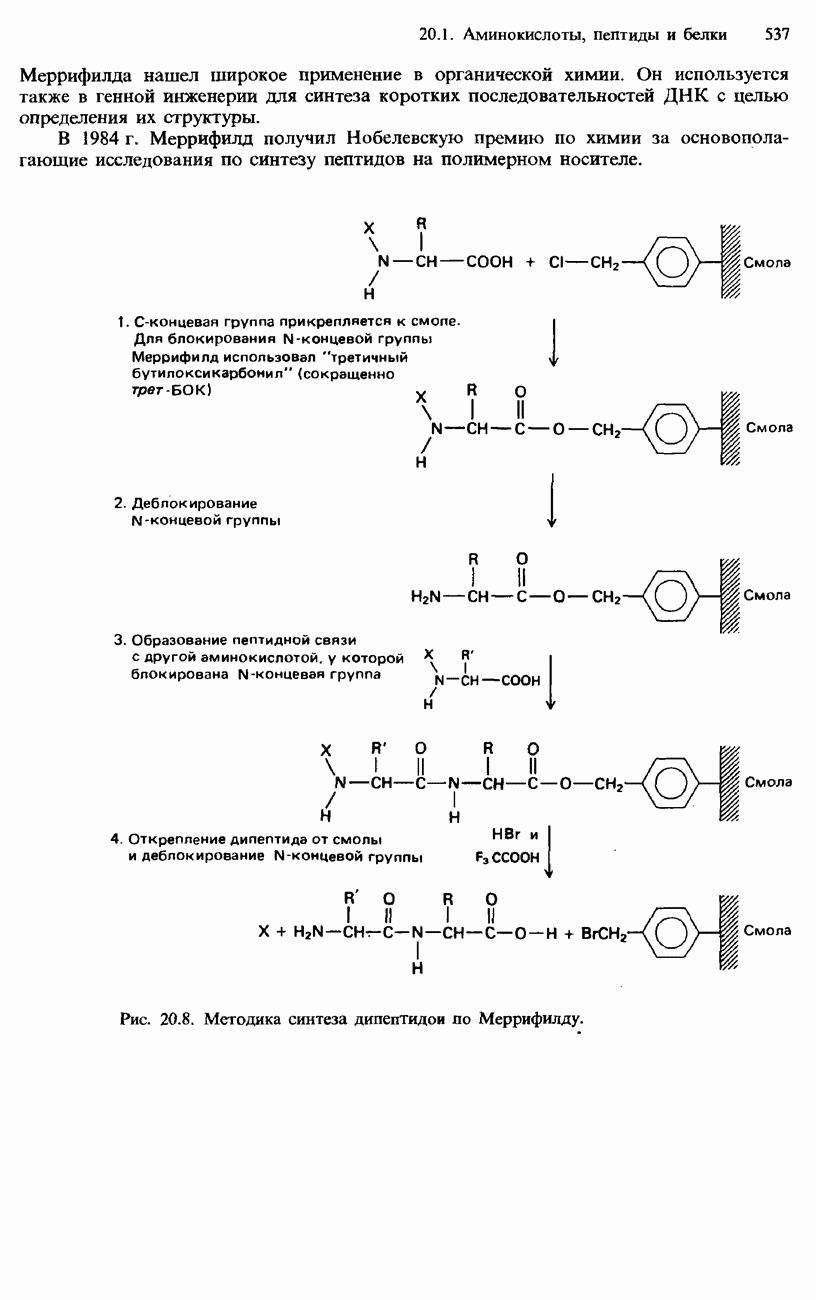
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
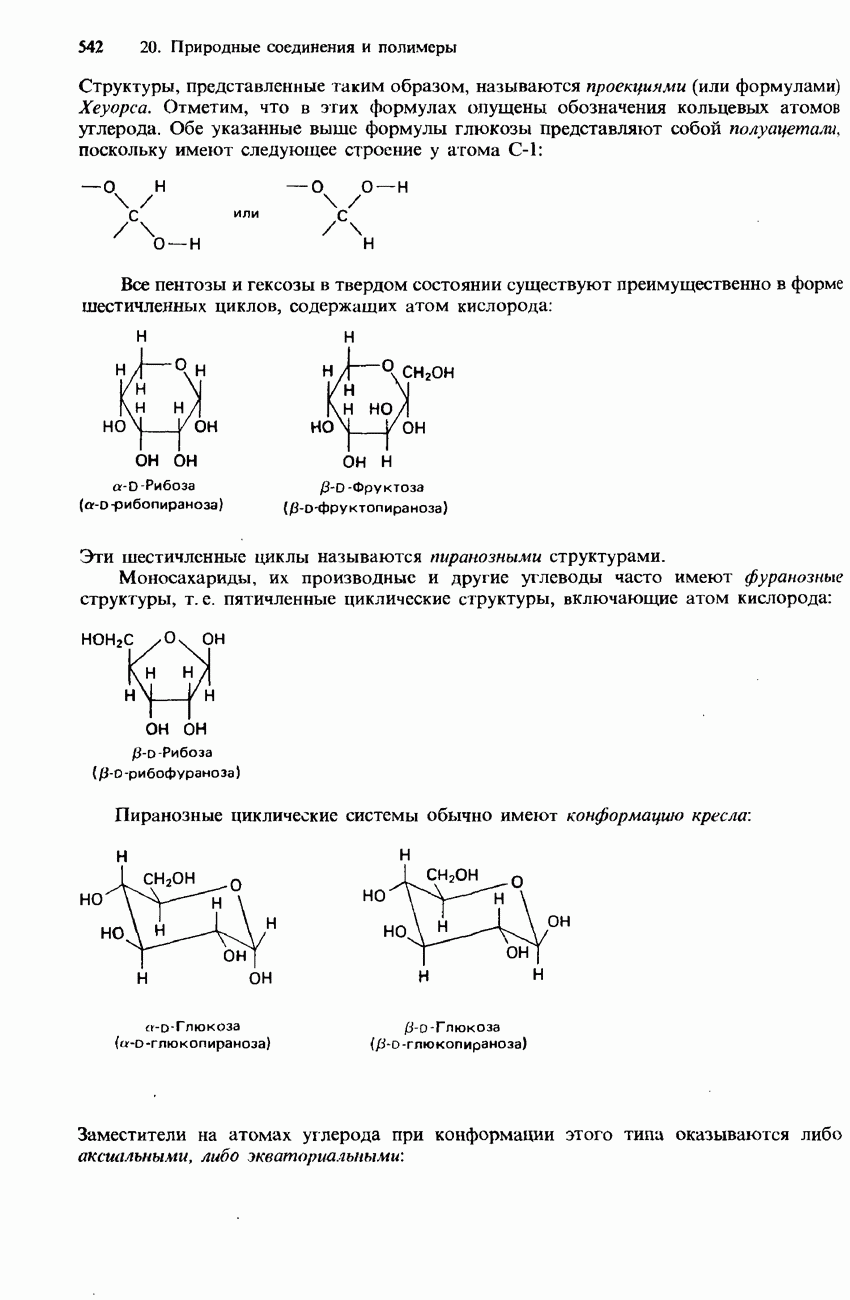
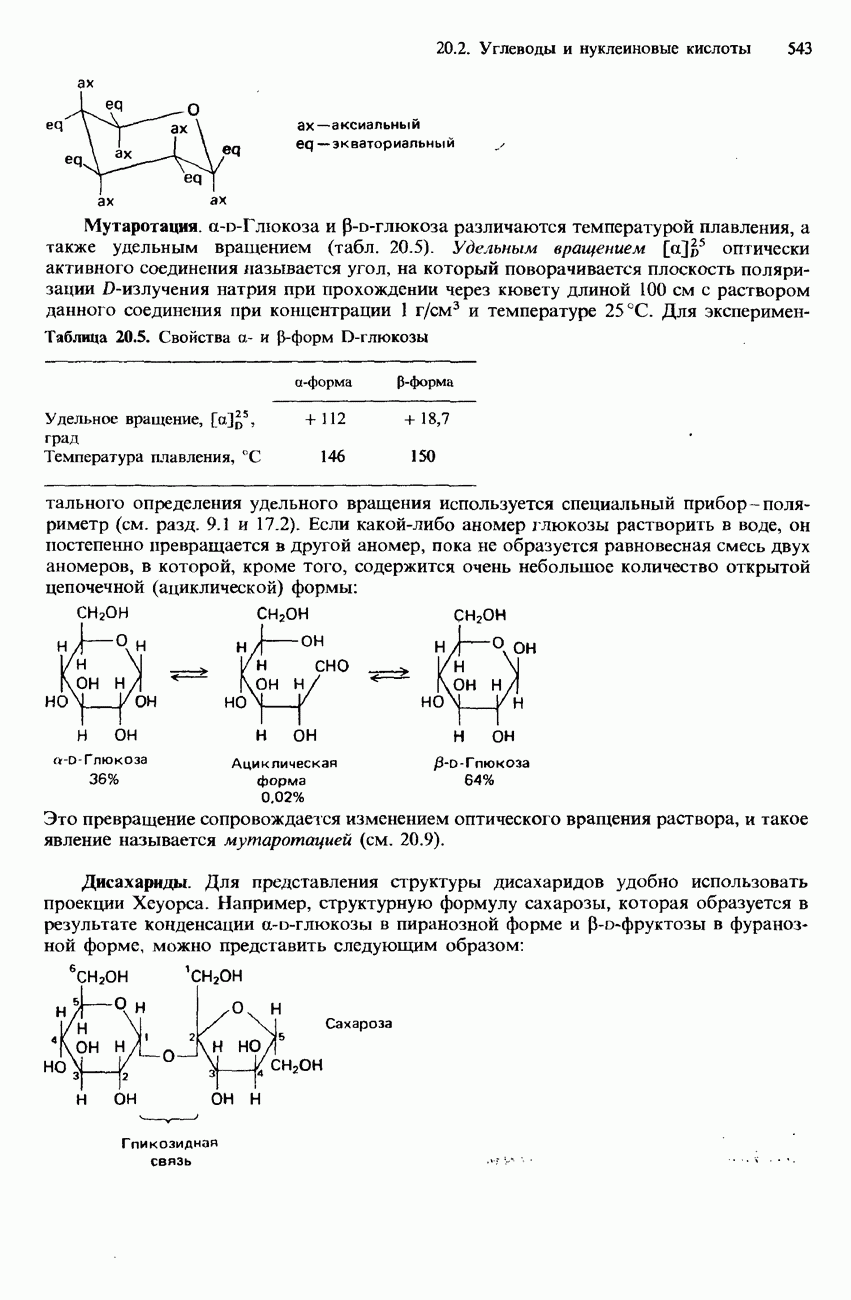
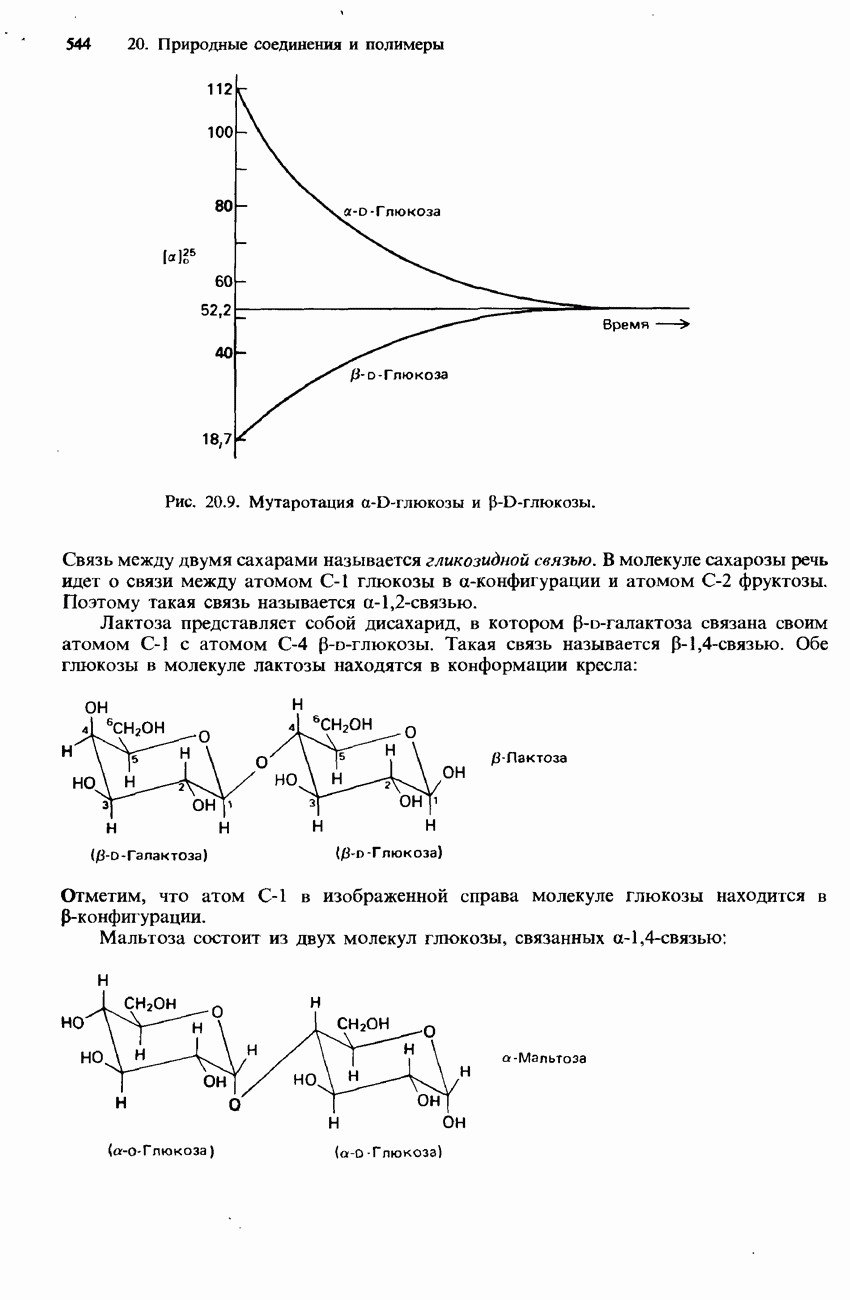
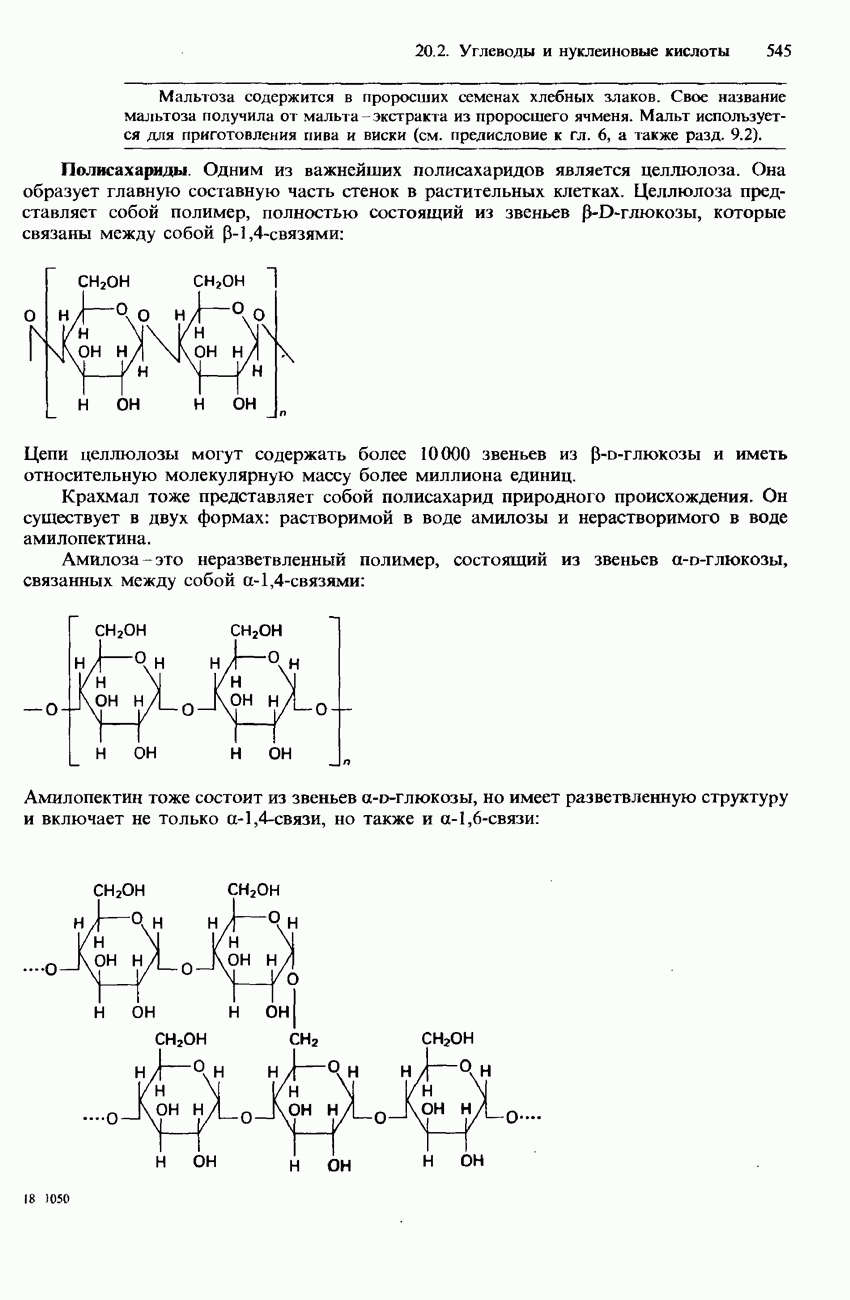
- 20.2. Углеводы и нуклеиновые кислоты
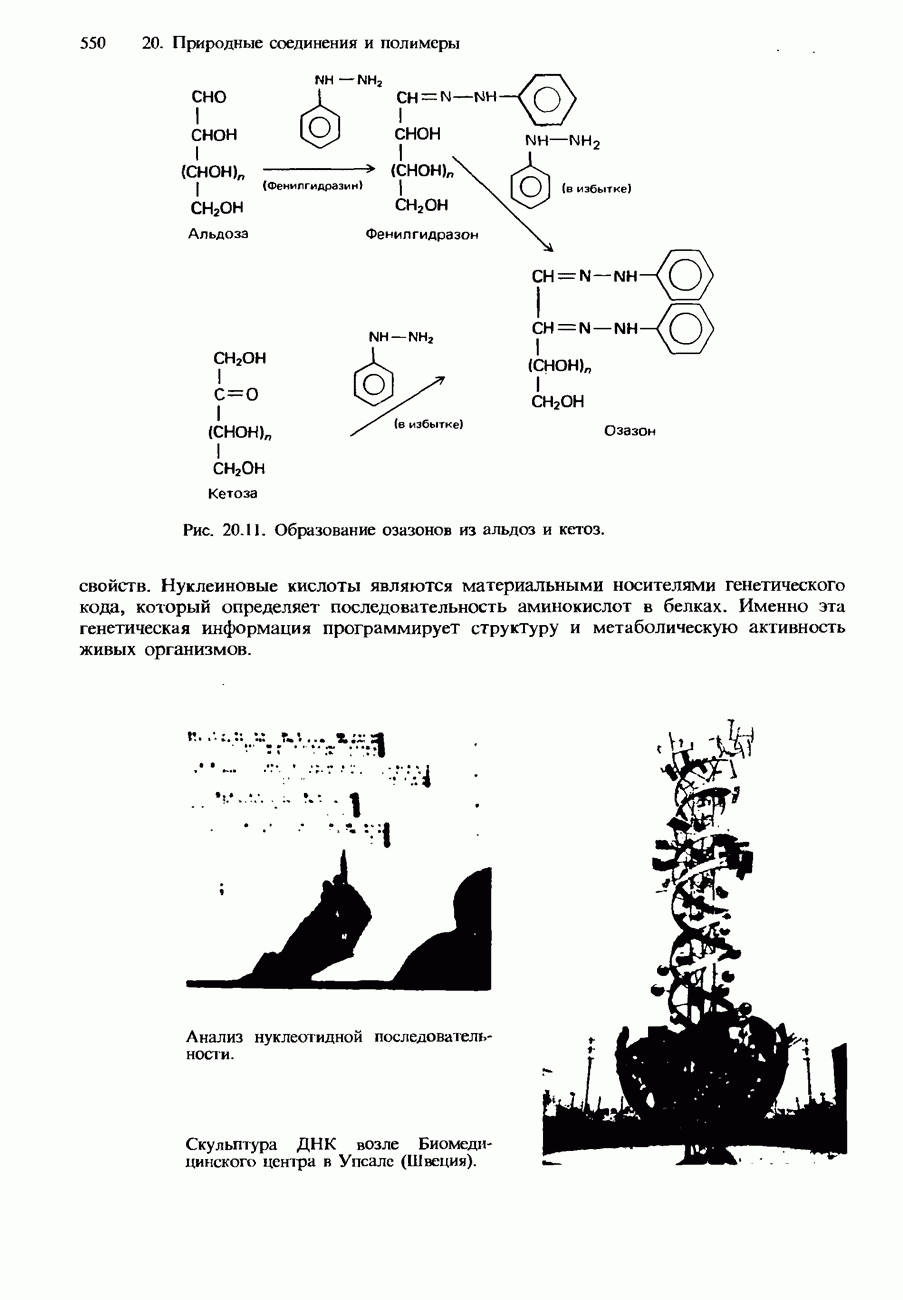
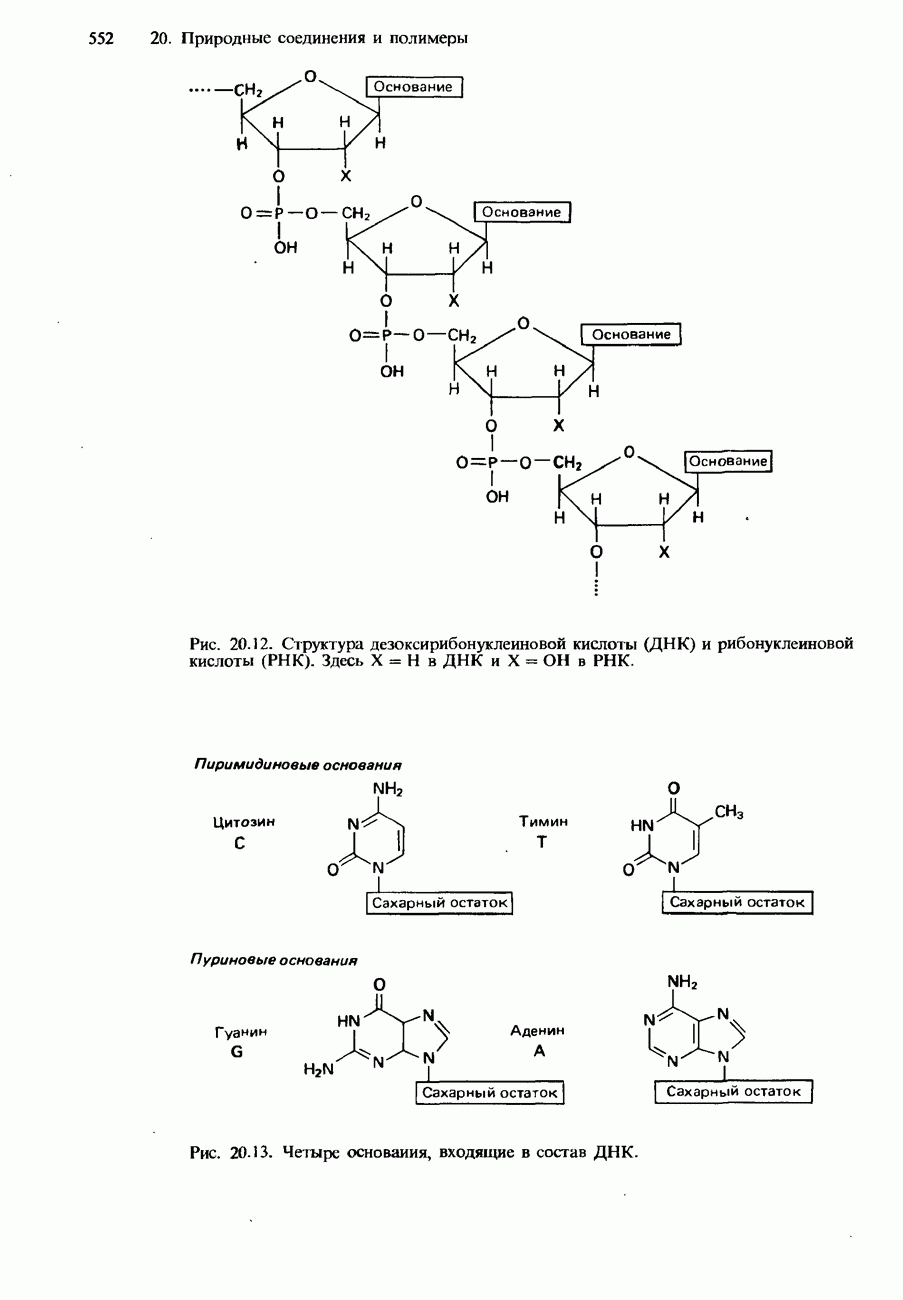
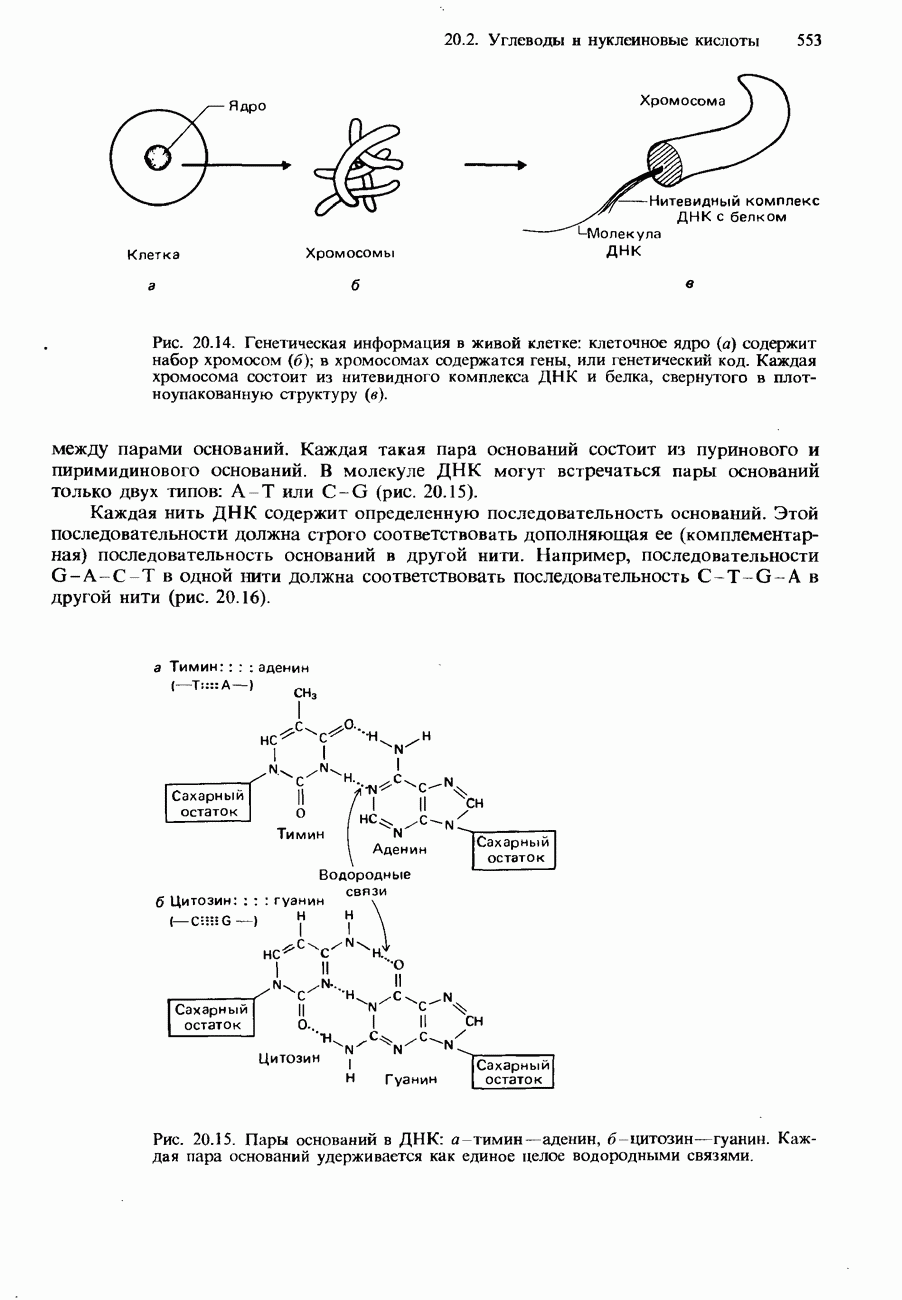
- НУКЛЕИНОВЫЕ КИСЛОТЫ
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
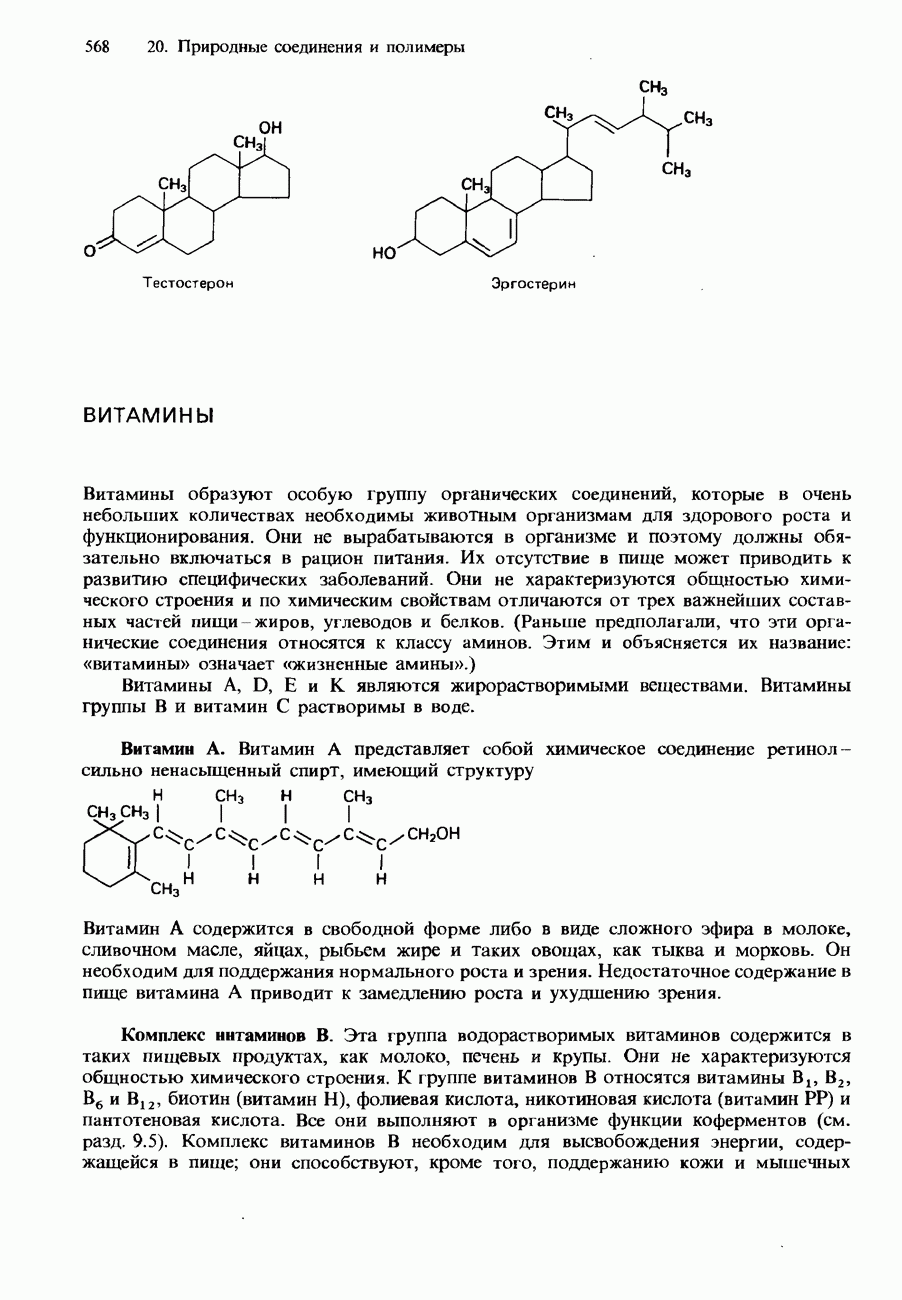
- ВИТАМИНЫ
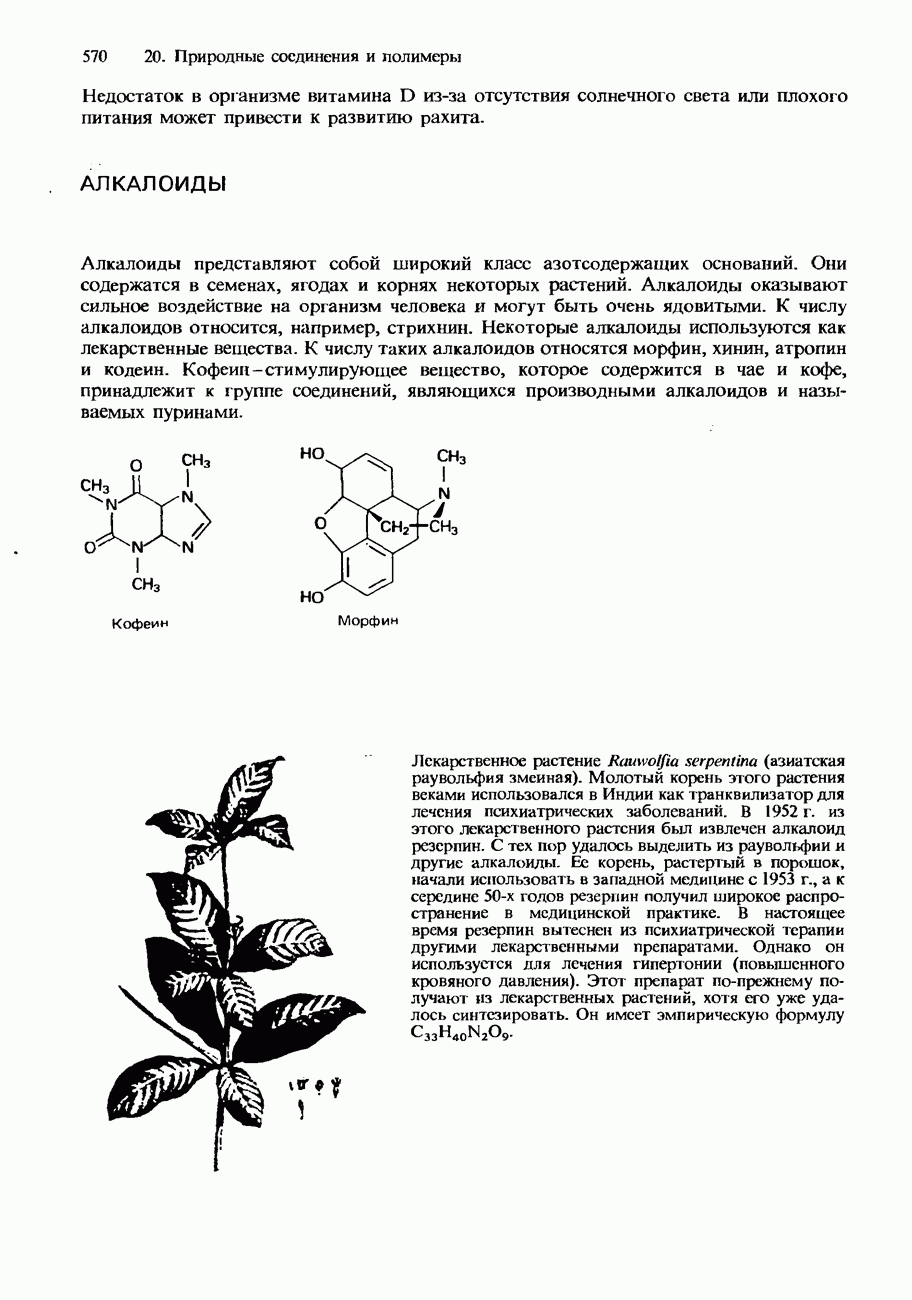
- АЛКАЛОИДЫ
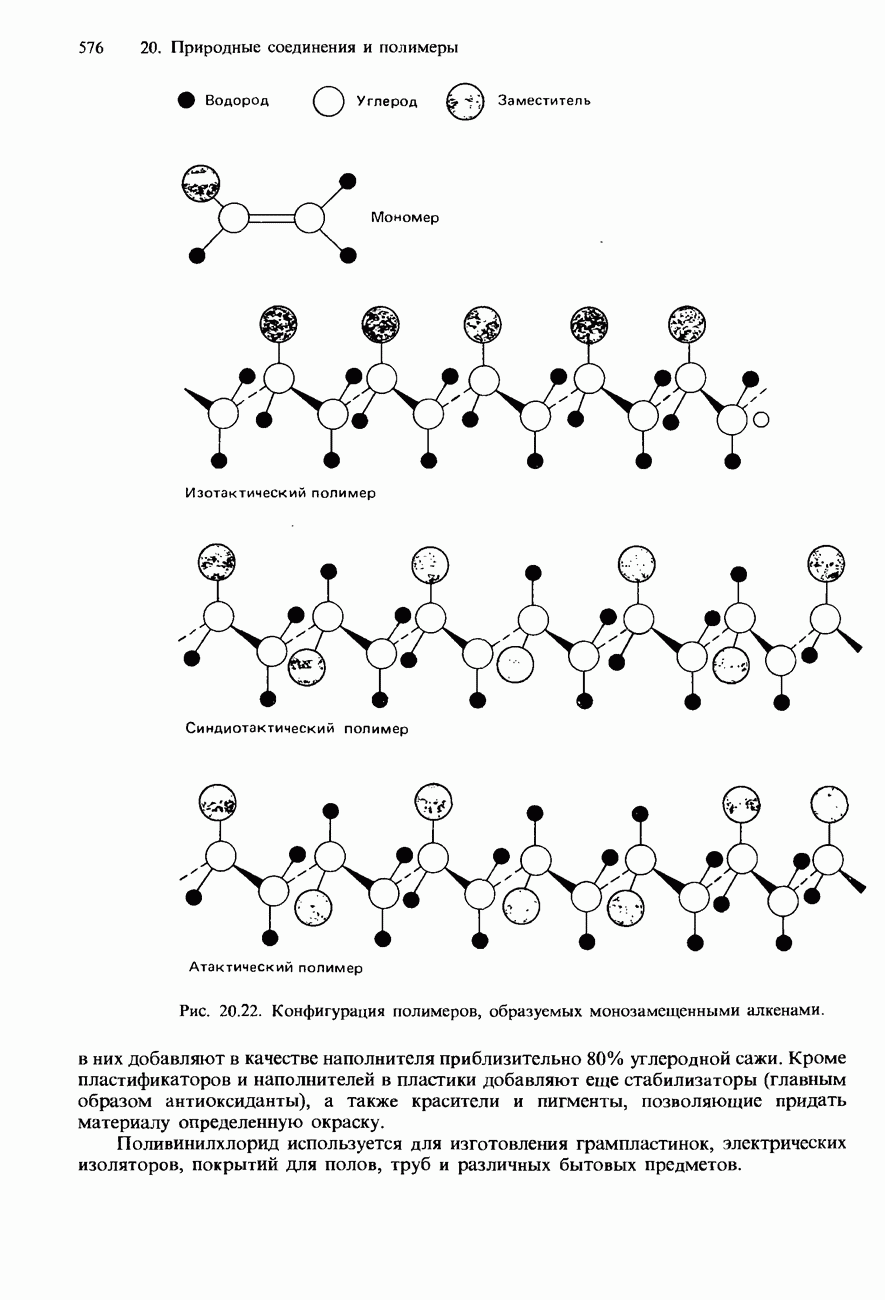
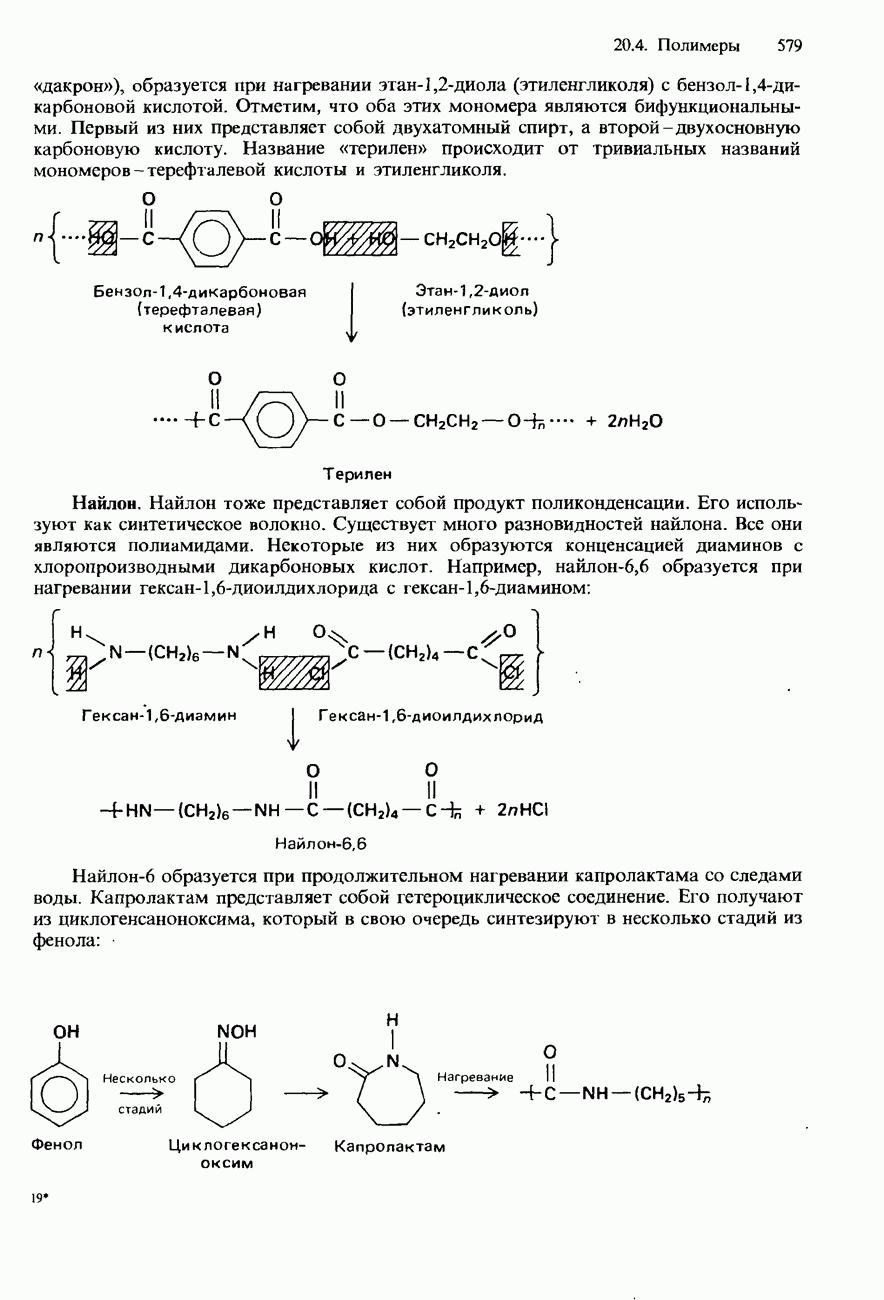
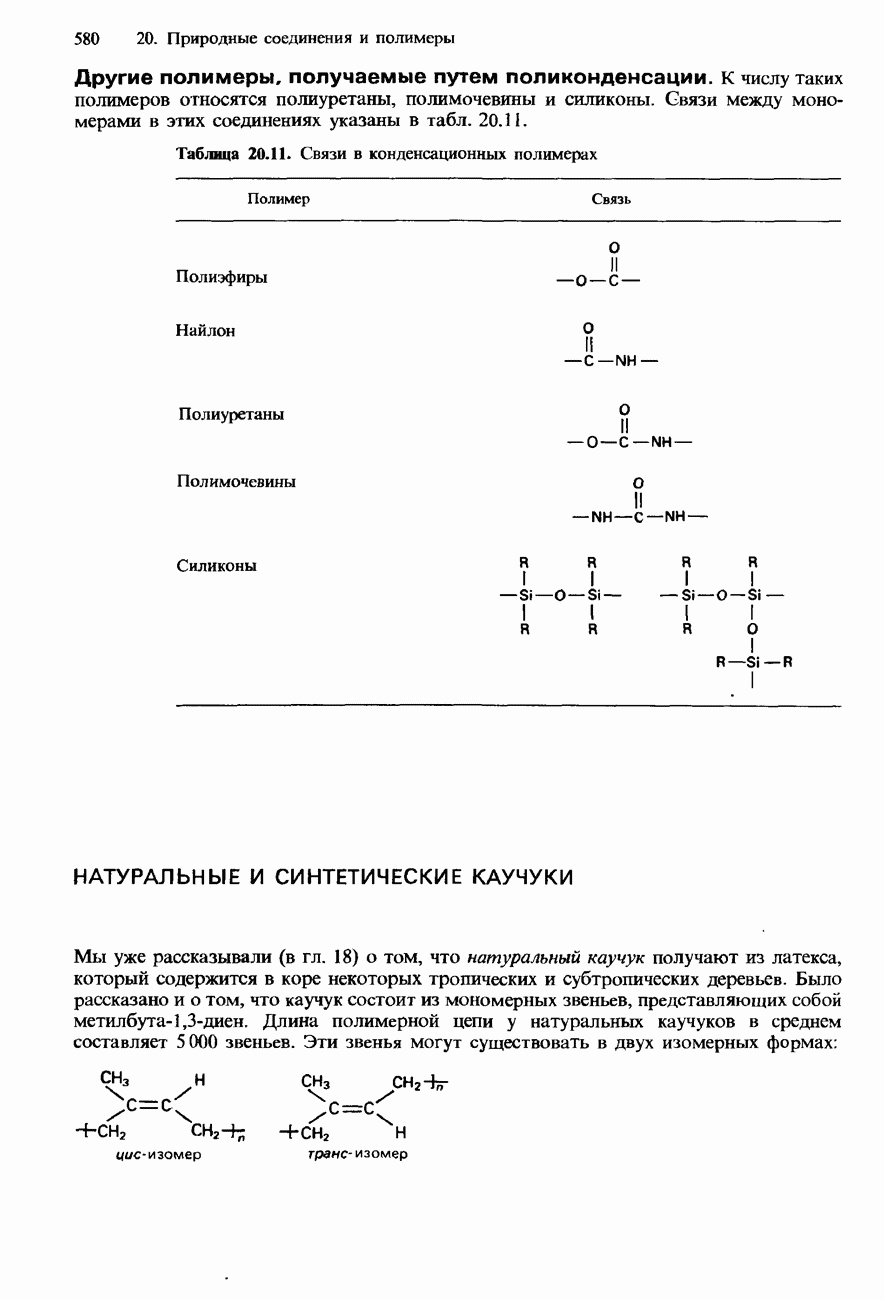
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ