| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
Расположение элементов в периодической таблице в соответствии с их атомным номером и внешней электронной конфигурацией обусловливает проявление двух важных закономерностей в химических свойствах непереходных элементов и их соединений:
1. Элементы со сходными химическими свойствами подразделяются на группы.
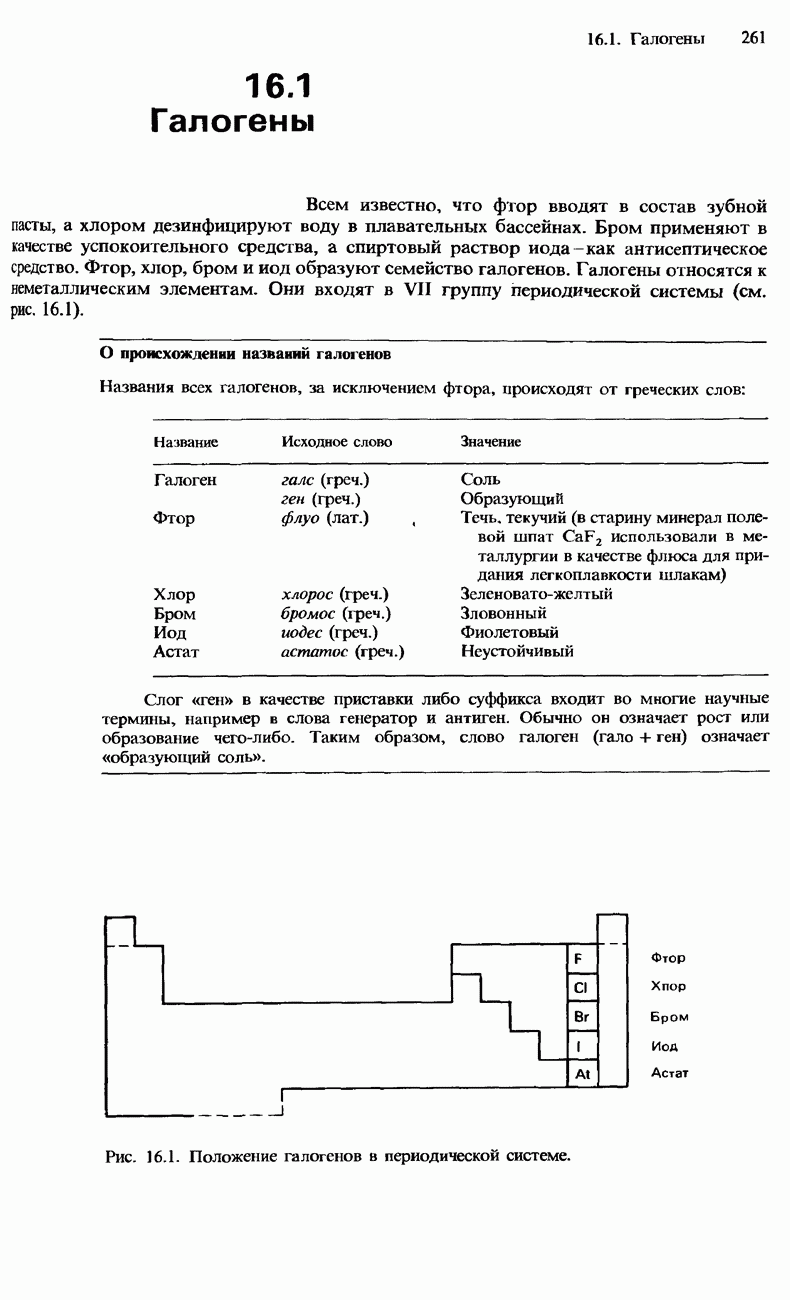
Например, все щелочные металлы находятся в группе I, а все галогены - в группе VII.
2. Наиболее электроположительные элементы, а следовательно наиболее реакционноспособные металлы, располагаются в нижнем левом углу периодической таблицы. Электроположительность элементов постепенно уменьшается при перемещении снизу вверх вдоль каждой группы и при перемещении слева направо вдоль каждого периода.
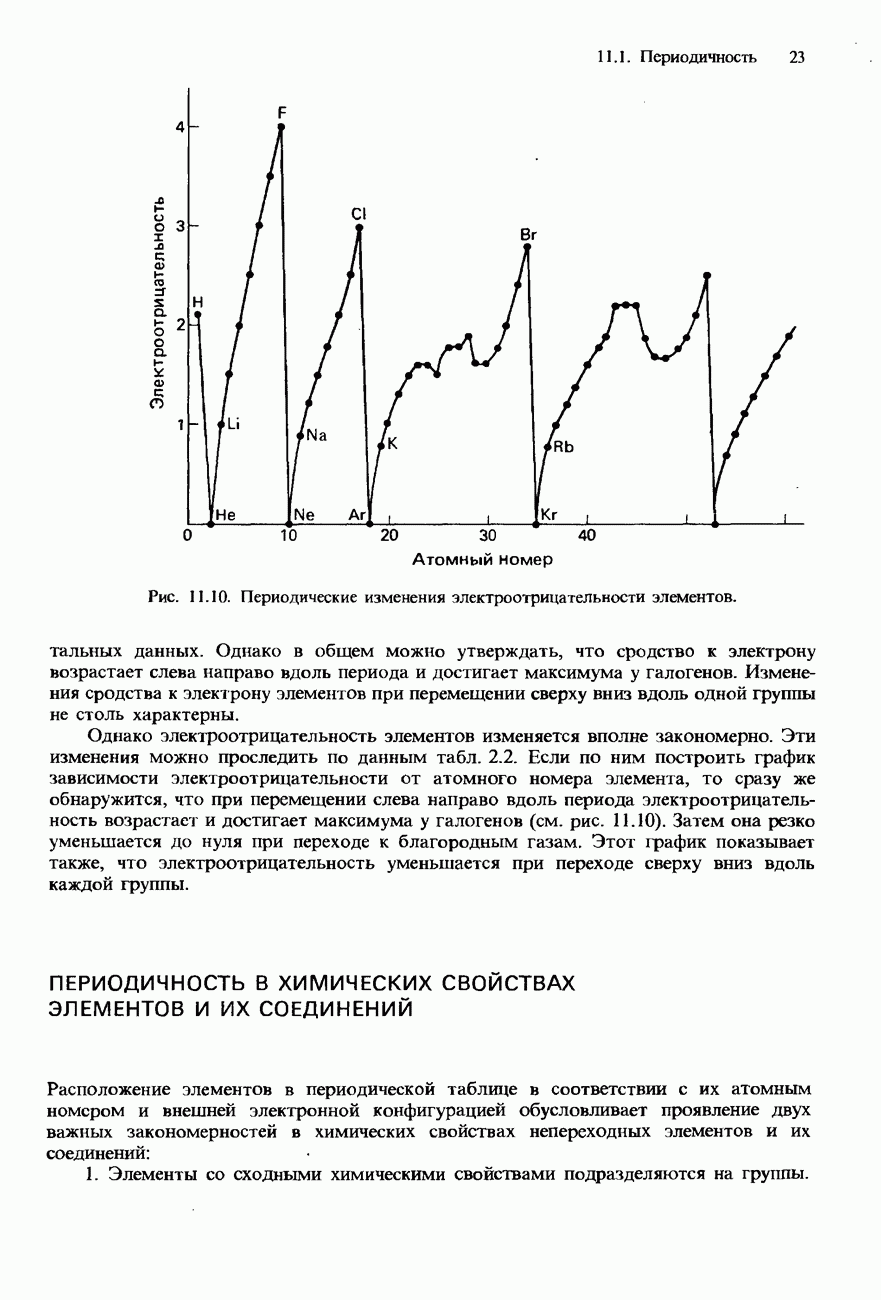
Наиболее электроотрицательные элементы, а следовательно, наиболее реакционноспособные неметаллы, располагаются в верхнем правом углу периодической таблицы. Электроотрицательность элементов возрастает при перемещении вдоль каждого периода в направлении от I группы к VII группе, но уменьшается при перемещении сверху вниз вдоль каждой группы.
Таблица 11.11. Закономерности в образовании соединений элементами 2-го и 3-го периодов

Таблица 11.12. Примеры лигандов, включающих p-элементы, в комплексных ионах d-элементов

Электроотрицательность или электроположительность элементов непосредственно связана с типами химических реакций, в которые способны вступать элементы, а значит, и с типами соединений, образуемых элементами. s-Металлы характеризуются способностью легко образовывать катионы и, таким образом, ионные соединения (см. табл. 11.11).  -Элементы, расположенные ближе к центру периодической таблицы, характеризуются способностью образовывать только ковалентные соединения. Более электроотрицательные p-элементы, расположенные ближе к правому краю периодической
-Элементы, расположенные ближе к центру периодической таблицы, характеризуются способностью образовывать только ковалентные соединения. Более электроотрицательные p-элементы, расположенные ближе к правому краю периодической

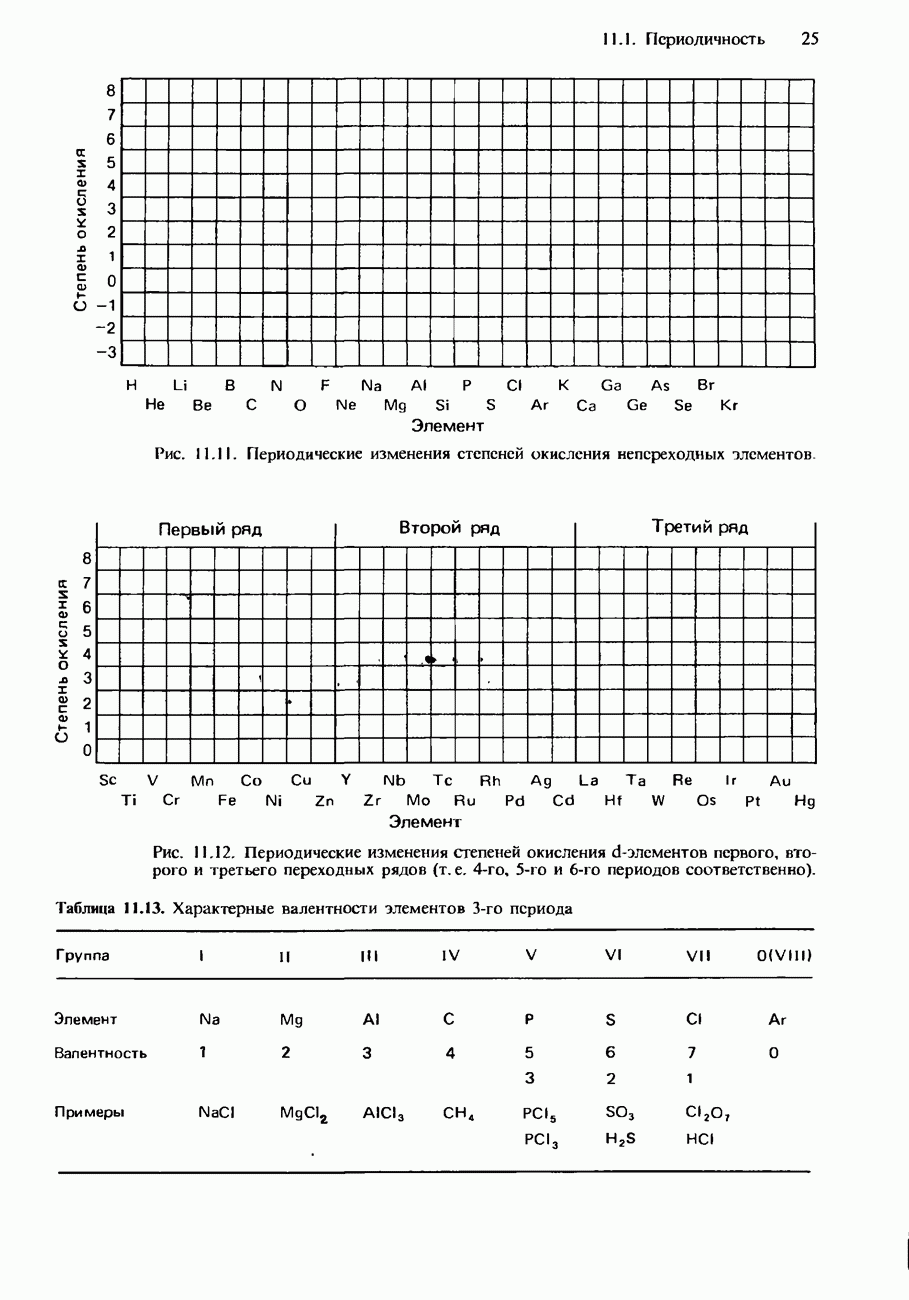
Рис. 11.11. Периодические изменения степеней окисления непереходных элементов

Рис. 11.12. Периодические изменения степеней окисления d-элементов первого, второго и третьего переходных рядов (т. е. 4-го, 5-го и 6-го периодов соответственно).
Таблица 11.13. Характерные валентности элементов 3-го периода

таблицы, способны образовывать как ковалентные, так и ионные соединения. Благородные газы, обладающие устойчивой электронной конфигурацией, образуют сравнительно мало соединений.
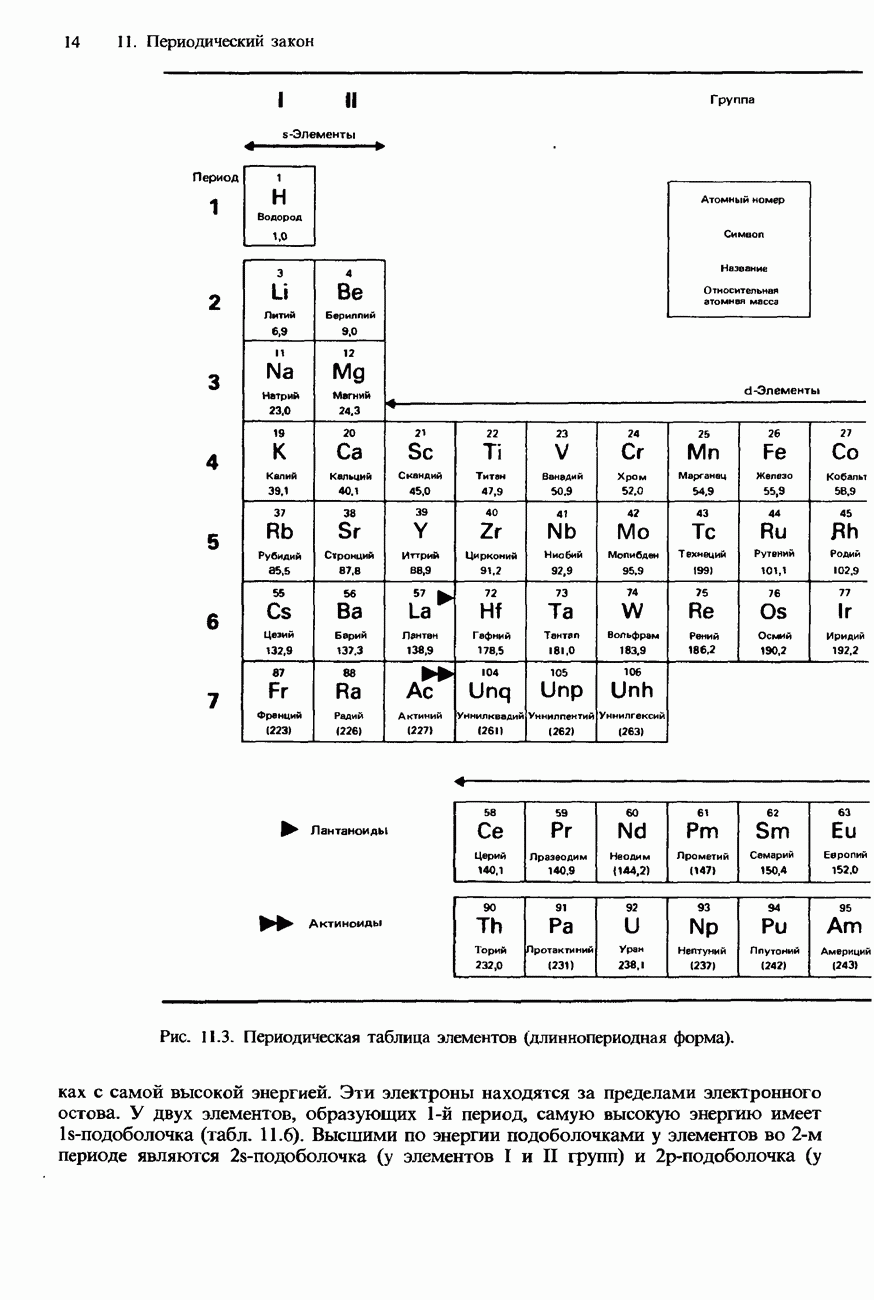
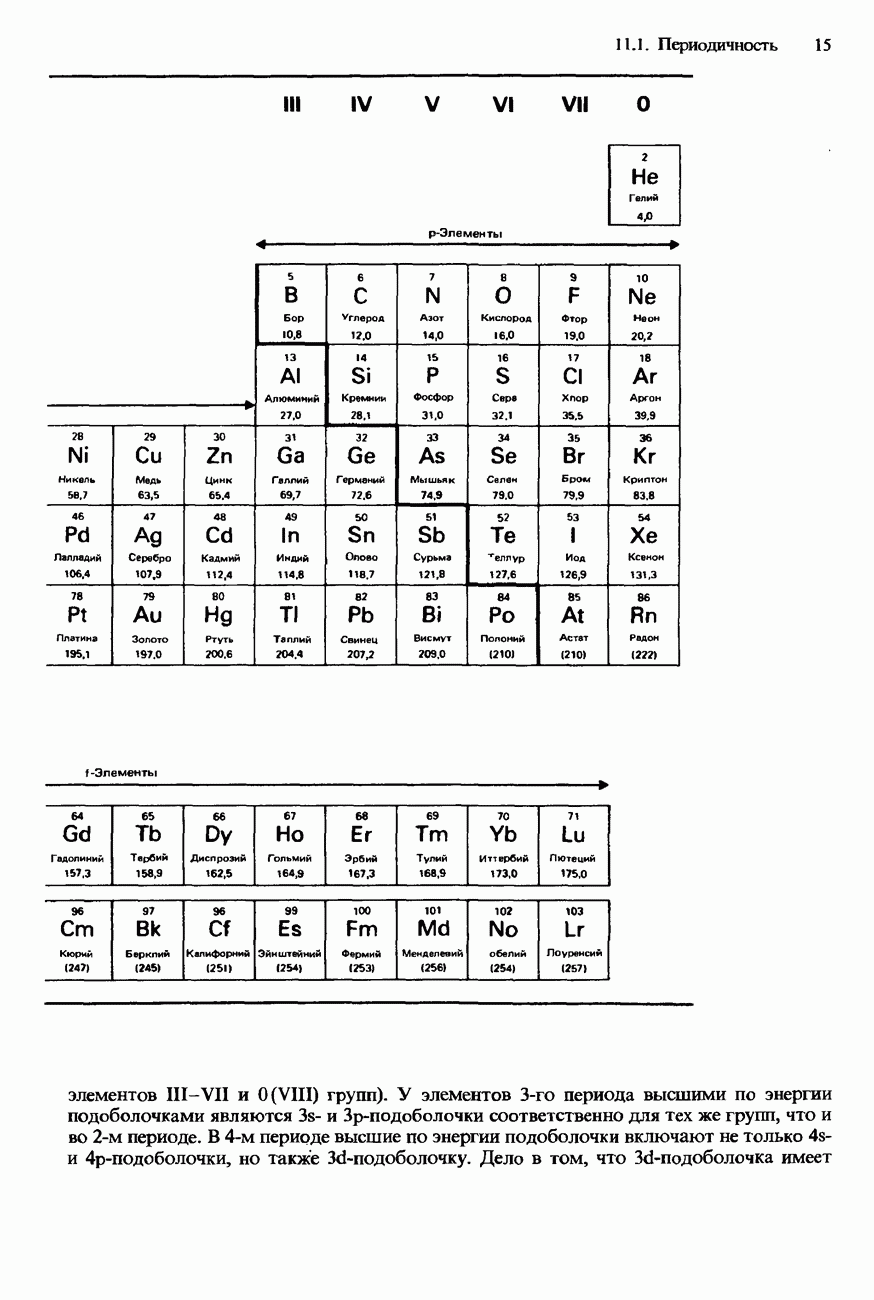
Как видно из рис. 11.3, d-элементы располагаются в периодической таблице между группами II и III. Все они - металлы, но менее электроположительные и, следовательно, более электроотрицательные, чем s-металлы (щелочные и щелочноземельные металлы). Вследствие этого их соединения, например оксиды и хлориды, как правило, являются либо ионными с высокой степенью ковалентного характера, либо ковалентными. Совместно с p-элементами, расположенными ближе к центральной части периодической таблицы, они нередко образуют соединения высокомолекулярного типа или соединения со слоистой либо цепочечной структурой.
d-Элементы обладают способностью образовывать как катионные, так и анионные комплексные ионы, что не характерно для s-металлов. р-Элементы часто входят в состав лигандов как в катионных, так и в анионных комплексах (табл. 11.12).
Валентности (см. гл. 4) непереходных элементов тоже обнаруживают периодические изменения. Из табл. 11.13 видно, что все элементы 3-го периода обнаруживают валентности, численно совпадающие с номером группы элемента. Кроме того, все элементы IV-VII групп обнаруживают валентности, равные разности между числом 8 и номером их группы.
Максимальные степени окисления элементов тоже обнаруживают периодические изменения (рис. 11.11 и 11.12). Как правило, они возрастают при перемещении слева направо вдоль периода и достигают максимальных значений в группах V-VII. Обращает на себя внимание и то обстоятельство, что элементы с высшими степенями окисления обнаруживают, кроме них, еще множество других степеней окисления. Например, хлор может существовать в состояниях со всеми степенями окисления от -1 до 
Во всех трех рядах переходных металлов ( -элементов) максимальная степень окисления достигается в средней части ряда (рис. 11.12).
-элементов) максимальная степень окисления достигается в средней части ряда (рис. 11.12).  -Элементы с высшими степенями окисления обнаруживают кроме них еще максимальное число других степеней окисления. Например, в первом ряду переходных металлов марганец обнаруживает пять положительных степеней окисления от
-Элементы с высшими степенями окисления обнаруживают кроме них еще максимальное число других степеней окисления. Например, в первом ряду переходных металлов марганец обнаруживает пять положительных степеней окисления от  до
до 
Периодичность окислительно-восстановительных свойств
Окислительно-восстановительные свойства элементов тоже обнаруживают периодические изменения. Закономерность этих изменений такова: элементы, занимающие левую часть периодической таблицы, т. е. щелочные и щелочноземельные металлы ( -металлы), являются сильными восстановителями. Затем, при перемещении вправо вдоль каждого периода элементы становятся все более слабыми восстановителями и все более сильными окислителями. Наконец, при переходе к VII группе элементы становятся сильными окислителями. Рассмотрим теперь эту закономерность несколько более подробно.
-металлы), являются сильными восстановителями. Затем, при перемещении вправо вдоль каждого периода элементы становятся все более слабыми восстановителями и все более сильными окислителями. Наконец, при переходе к VII группе элементы становятся сильными окислителями. Рассмотрим теперь эту закономерность несколько более подробно.
Восстановительные свойства  -металлов характеризуются:
-металлов характеризуются:
низкой энергией ионизации,
низким сродством к электрону,
низкой электроотрицательностью,
высокой «электроположительностью» (качественный термин - см. предыдущую сноску),
отрицательным стандартным окислительно-восстановительным потенциалом.
Примеры
1. Реакция с воздухом или кислородом

2. Реакция с хлором

Реакция с разбавленными кислотами

Все это примеры восстановительной способности s-металлов, так как в каждом случае металл легко отдает электроны:

Подробное обсуждение химии щелочных и щелочноземельных металлов проводится в гл. 13.
Окислительные свойства элементов VII группы характеризуются: высокой энергией ионизации, высоким сродством к электрону, высокой электроотрицательностью, низкой «электроположительностью»,
положительным стандартным окислительно-восстановительным потенциалом.
Пример
Хлор обладает свойствами сильного окислителя. Он бурно реагирует с водородом на солнечном свету, образуя хлороводород. В отличие от этого он не реагирует с другими окислителями, например с кислородом или разбавленными кислотами. Подробное обсуждение химии хлора и других галогенов проводится в гл. 16.
Свойства элементов из средней части периодов. Элементы группы VII относятся к p-элементам, которые расположены в правой части периодической таблицы. р-Элемен-ты, находящиеся ближе к средней части периодов, обнаруживают слабые восстановительные и (или) слабые окислительные свойства. Например, принадлежащий к группе IV кремний медленно реагирует с кислородом, образуя оксид 

Принадлежащий к группе V азот может выступать как в роли слабого восстановителя, так и в роли слабого окислителя. Например, он ведет себя как слабый восстановитель в реакции с кислородом:

В отличие от этого в реакции с водородом азот ведет себя как слабый окислитель:

Переходные  -элементы обладают свойствами слабых восстановителей. Например, раскаленное докрасна железо реагирует с водяным паром, образуя водород:
-элементы обладают свойствами слабых восстановителей. Например, раскаленное докрасна железо реагирует с водяным паром, образуя водород:

Периодичность свойств соединений
В образовании, структуре, а также физических и химических свойствах соединений тоже обнаруживаются периодические закономерности изменения. Эти закономерности мы проследим на примере оксидов, гидридов, гидроксидов и галогенидов.
Оксиды. Реакционная способность элементов во взаимодействии с кислородом, вообще говоря, уменьшается при перемещении вправо вдоль каждого периода. Например, в 3-м периоде два s-металла, натрий и магний, и два p-элемента, алюминий и фосфор, бурно реагируют с кислородом, образуя оксиды. В том же периоде элементы кремний и сера способны только медленно реагировать с кислородом. Хлор и аргон, расположенные в правом конце периода, вообще не реагируют с кислородом.
Электроположительные s-металлы образуют ионные оксиды, как, например, оксид натрия  и оксид магния
и оксид магния  Оксиды элементов, расположенных в средней и правой частях периода, являются преимущественно ковалентными соединениями, как, например, оксиды азота и серы.
Оксиды элементов, расположенных в средней и правой частях периода, являются преимущественно ковалентными соединениями, как, например, оксиды азота и серы.
Кислотно-основный характер оксидов тоже изменяется от основного у оксидов элементов левой части периода к амфотерному у оксидов элементов средней части периода и далее к кислотному у оксидов элементов правой части периода. Например, s-металлы обычно образуют оксиды, которые растворяются в воде с образованием щелочных растворов:

Молекулярные оксиды p-элементов, например диоксид углерода и триоксид серы, обычно обладают кислотными свойствами. Закономерное изменение основных свойств с переходом к кислотным свойствам наглядно проявляется у оксидов элементов 3-го периода.

Оксиды d-элементов обычно нерастворимы в воде и обладают основными свойствами, хотя один или два из них. например оксид цинка, обнаруживают амфотерные свойства (см. гл. 14).
Подробное рассмотрение химии оксидов проводится в разд. 15.4.
Гидриды. В образовании, структуре и свойствах гидридов прослеживаются закономерности, сходные с описанными выше для оксидов, хотя и не полностью одинаковые с ними.
s-Металлы, например натрий и магний, как правило, бурно реагируют в нагретом состоянии с сухим водородом, образуя ионные гидриды. Эти ионные гидриды обладают основными свойствами. Наиболее электроотрицательные  -элементы в правой части периодов, например сера и хлор, реагируют с водородом, образуя ковалентные гидриды, которые обладают кислотными свойствами. Исключениями являются метан
-элементы в правой части периодов, например сера и хлор, реагируют с водородом, образуя ковалентные гидриды, которые обладают кислотными свойствами. Исключениями являются метан  представляющий собой нейтральное соединение, а также аммиак
представляющий собой нейтральное соединение, а также аммиак  обладающий основными свойствами.
обладающий основными свойствами.
Более электроотрицательные  -элементы, например алюминий, кремний и фосфор, в нагретом состоянии не реагируют с водородом.
-элементы, например алюминий, кремний и фосфор, в нагретом состоянии не реагируют с водородом.
Переходные d-металлы в нагретом состоянии реагируют с водородом, образуя нестехиометрические гидриды.
Получение, структура и свойства гидридов подробно описаны в гл. 12.
Гидроксиды. Гидроксиды наиболее электроположительных элементов, например натрия и кальция, являются ионными соединениями с сильно основными свойствами. В отличие от этого сильно электроотрицательный элемент хлор образует кислотный гидроксид, хлорноватистую кислоту  . В этом соединении связь между атомами хлора и кислорода ковалентная. Гидроксиды некоторых менее электроотрицательных элементов обладают амфотерными свойствами. Нередко они неустойчивы и образуют оксиды.
. В этом соединении связь между атомами хлора и кислорода ковалентная. Гидроксиды некоторых менее электроотрицательных элементов обладают амфотерными свойствами. Нередко они неустойчивы и образуют оксиды.
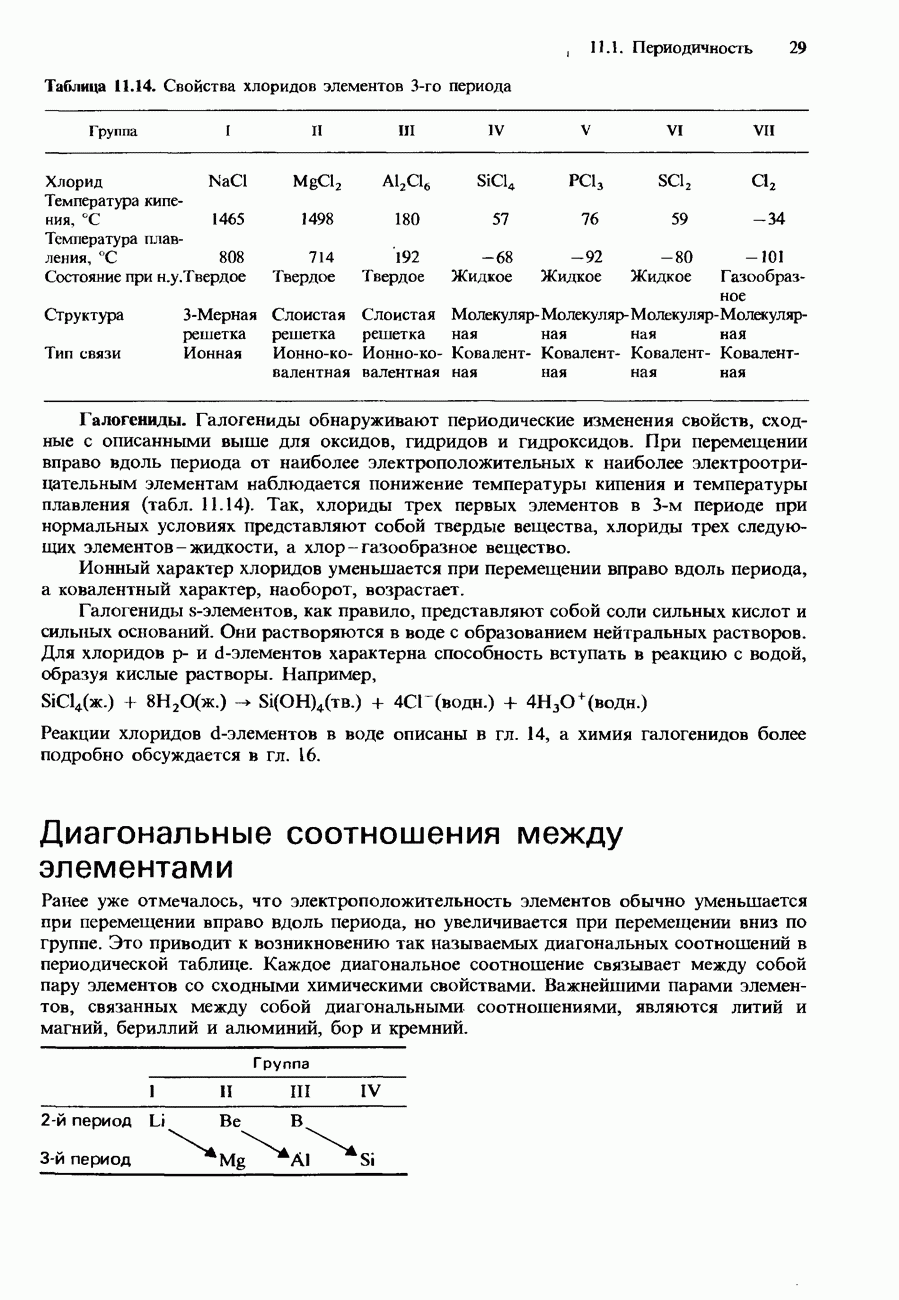
Таблица 11.14. Свойства хлоридов элементов 3-го периода

Галогениды. Галогениды обнаруживают периодические изменения свойств, сходные с описанными выше для оксидов, гидридов и гидроксидов. При перемещении вправо вдоль периода от наиболее электроположительных к наиболее электроотрицательным элементам наблюдается понижение температуры кипения и температуры плавления (табл. 11.14). Так, хлориды трех первых элементов в 3-м периоде при нормальных условиях представляют собой твердые вещества, хлориды трех следующих элементов - жидкости, а хлор - газообразное вещество.
Ионный характер хлоридов уменьшается при перемещении вправо вдоль периода, а ковалентный характер, наоборот, возрастает.
Галогениды s-элементов, как правило, представляют собой соли сильных кислот и сильных оснований. Они растворяются в воде с образованием нейтральных растворов. Для хлоридов p- и d-элементов характерна способность вступать в реакцию с водой, образуя кислые растворы. Например,

Реакции хлоридов d-элементов в воде описаны в гл. 14, а химия галогенидов более подробно обсуждается в гл. 16.
Диагональные соотношения между элементами
Ранее уже отмечалось, что электроположительность элементов обычно уменьшается при перемещении вправо вдоль периода, но увеличивается при перемещении вниз по группе. Это приводит к возникновению так называемых диагональных соотношений в периодической таблице. Каждое диагональное соотношение связывает между собой пару элементов со сходными химическими свойствами. Важнейшими парами элементов, связанных между собой диагональными соотношениями, являются литий и магний, бериллий и алюминий, бор и кремний.

Наличие диагональных соотношений объясняется тем, что уменьшение электроположительности при перемещении к каждому следующему элементу вправо вдоль периода компенсируется возрастанием электроположительности при перемещении к следующему элементу вниз по группе. Более подробное рассмотрение диагональных соотношений проводится в гл. 13.
Аномалии
Головные элементы в главных подгруппах. Элементы 2-го периода, «возглавляющие» группы I—VII (главные подгруппы в короткопериодной форме периодической таблицы. - Перев.), иногда называют головными элементами. Они представляют интерес в связи с тем, что некоторые свойства этих элементов и их соединений значительно отличаются от аналогичных свойств, характерных для других элементов соответствующих групп. Эти аномальные свойства могут быть приписаны меньшему размеру атомов головных элементов и их более высоким электроотрицательности и энергии ионизации. Например, галогениды лития и бериллия обнаруживают более ковалентный характер, чем галогениды других металлов из соответствующих групп. Литий, в отличие от остальных щелочных металлов, не образует твердого гидрокарбоната. В то время, как нитраты других щелочных металлов разлагаются при нагревании с образованием соответствующих нитритов и кислорода, нитрат лития разлагается с образованием оксида лития, кислорода и диоксида азота. Наконец, в отличие от гидроксидов других щелочных металлов гидроксид лития термически неустойчив. Аномальные свойства лития и других головных элементов подробно обсуждаются в гл. 13, 14 и 16.
Итак, повторим еще раз!
1. Элементы в современной периодической таблице располагаются в порядке возрастания их атомного номера.
2. Элементы одного периода имеют одинаковый электронный остов, с такой же конфигурацией, как у благородного газа, завершающего предыдущий период.
3. Элементы одной и той же группы имеют одинаковую внешнюю электронную конфигурацию.
4. Все  -элементы (за исключением водорода и гелия), а также d- и
-элементы (за исключением водорода и гелия), а также d- и  -элементы принадлежат к металлам.
-элементы принадлежат к металлам.
5. Водород и гелий относятся к неметаллам. Все остальные неметаллы принадлежат к р-элементам.
6. При перемещении слева направо вдоль периода металлические свойства элементов ослабевают, а при перемещении сверху вниз вдоль группы металлические свойства элементов усиливаются.
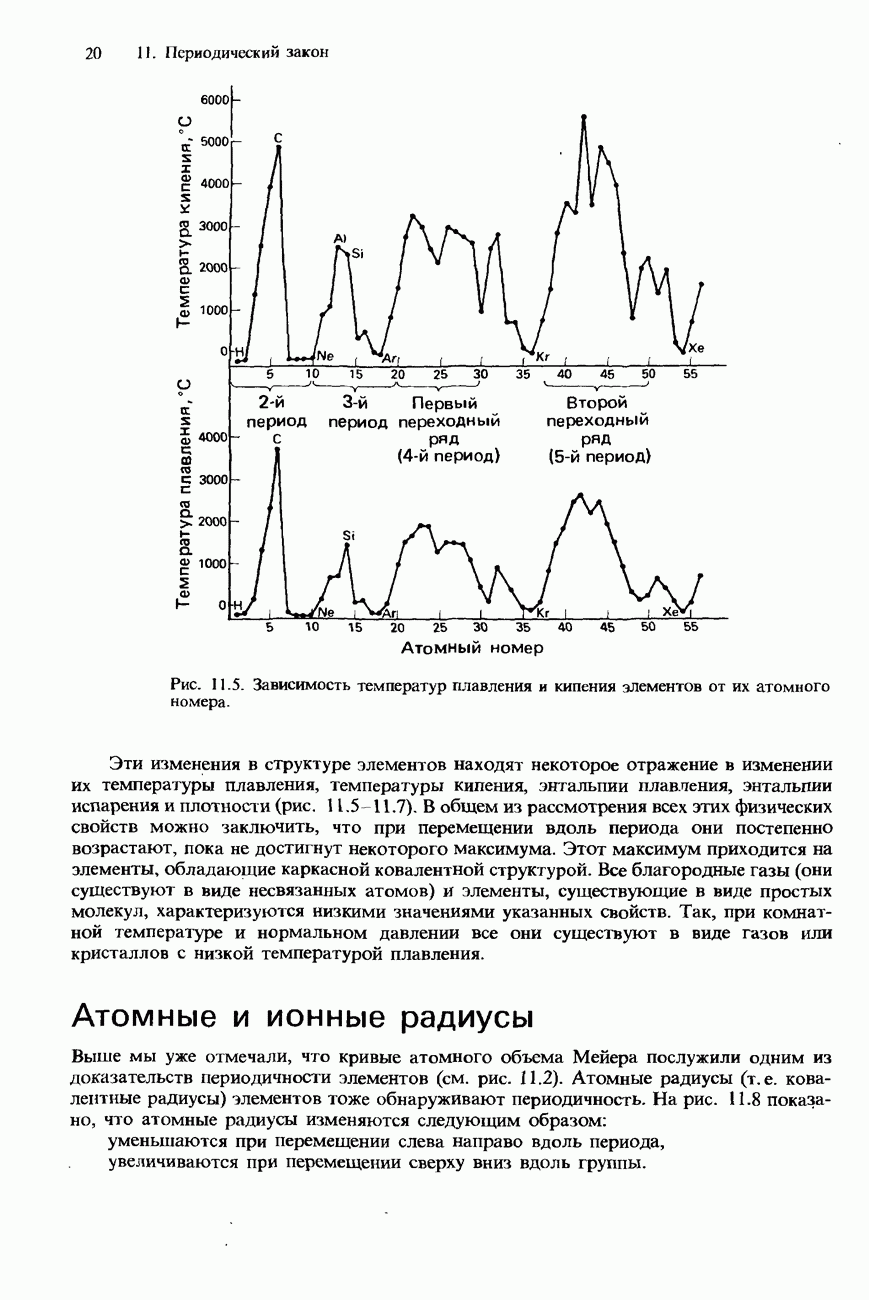
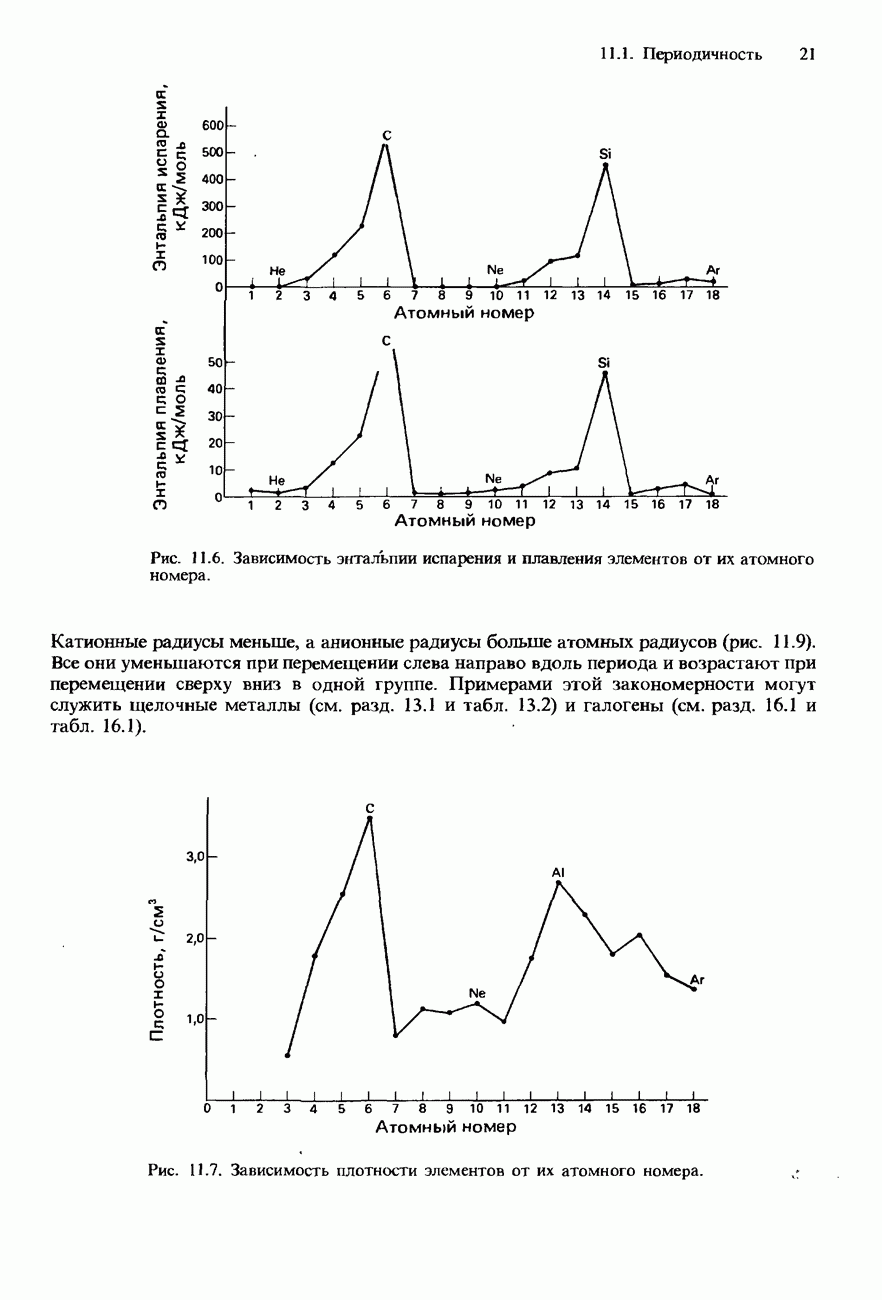
7. Физические свойства элементов (температуры плавления и кипения, энтальпии плавления и испарения, плотность) при перемещении слева направо вдоль периода сначала возрастают, а затем, после достижения максимума в средней части периода, уменьшаются.
8. Атомные и ионные радиусы элементов при перемещении слева направо вдоль периода уменьшаются, а при перемещении сверху вниз вдоль группы возрастают.
9. Первая энергия ионизации элементов при перемещении слева направо вдоль периода увеличивается, а при перемещении сверху вниз вдоль группы уменьшается.
10. Электроотрицательность элементов в пределах каждого периода возрастает, достигая максимума у галогенов, а при перемещении сверху вниз по группе уменьшается.
11. Наиболее электроположительные, а следовательно, наиболее реакционноспособные
способные (активные) металлы располагаются в левом нижнем углу периодической таблицы.
12. Наиболее электроотрицательные элементы располагаются в правом верхнем углу периодической таблицы.
13. s-Элементы, как правило, обнаруживают валентности, совпадающие с номером их группы.
14. р-Элементы имеют главные валентности, равные номеру их группы, а также равные разности между числом 8 и номером их группы.
15. d-Элементы обнаруживают много разных валентностей и степеней окисления.
16. Восстановительные свойства элементов при перемещении сверху вниз вдоль группы ослабевают.
17. Реакционная способность элементов по отношению к кислороду уменьшается при перемещении сверху вниз вдоль группы.
18. Ионный характер оксидов при перемещении слева направо вдоль периода уменьшается, а ковалентный характер увеличивается.
19. Оксиды, гидриды, гидроксиды и галогениды элементов обнаруживают одинаковую периодичность в изменении свойств.
20. Литий и магний обладают сходными химическими свойствами и тем самым демонстрируют наличие между ними диагонального соотношения.
21. Головные элементы, возглавляющие главные группы, обладают аномальными свойствами по отношению к остальным элементам своих групп.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
- ПЕРИОДИЧНОСТЬ
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
- 13.3. Распространенность в природе, получение и применение
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
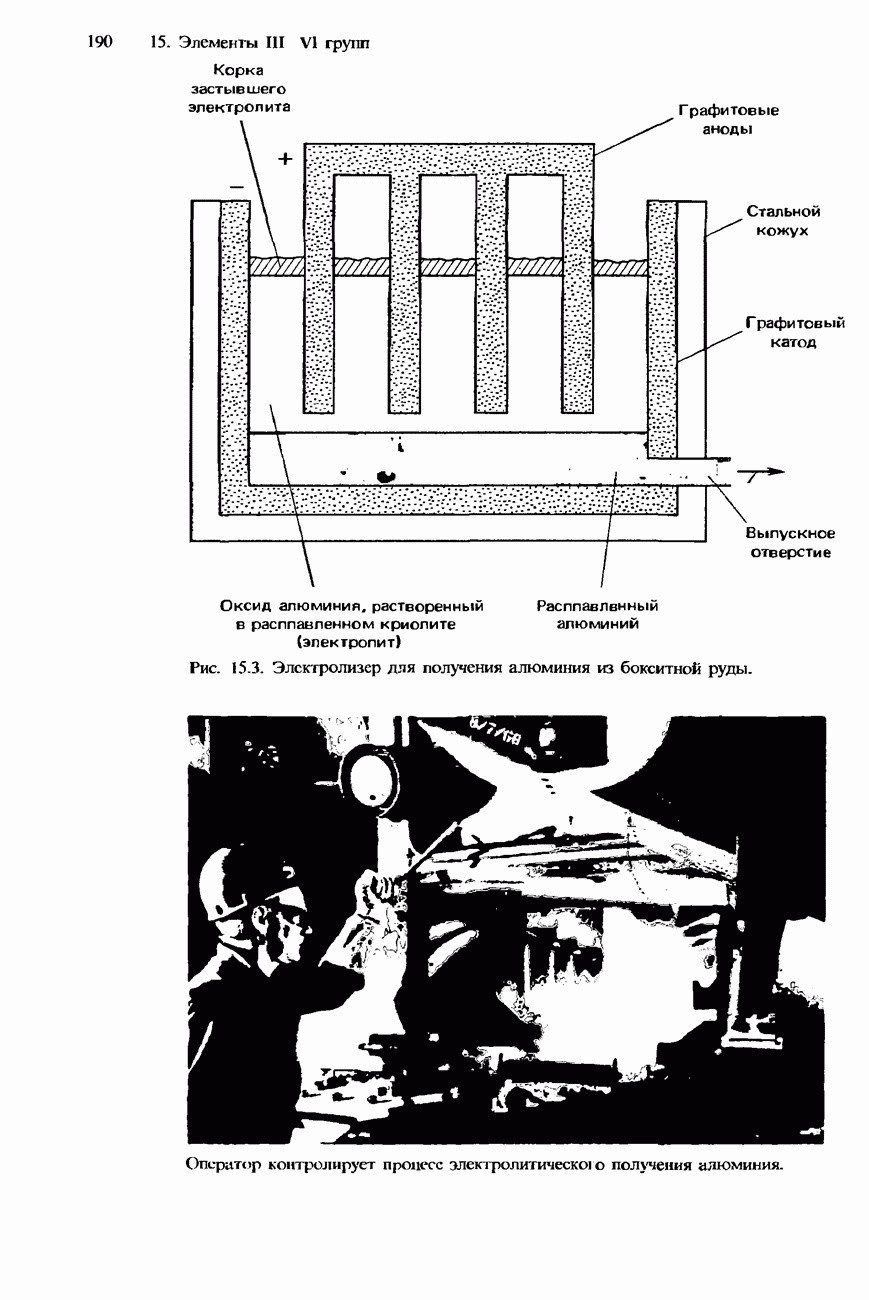
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
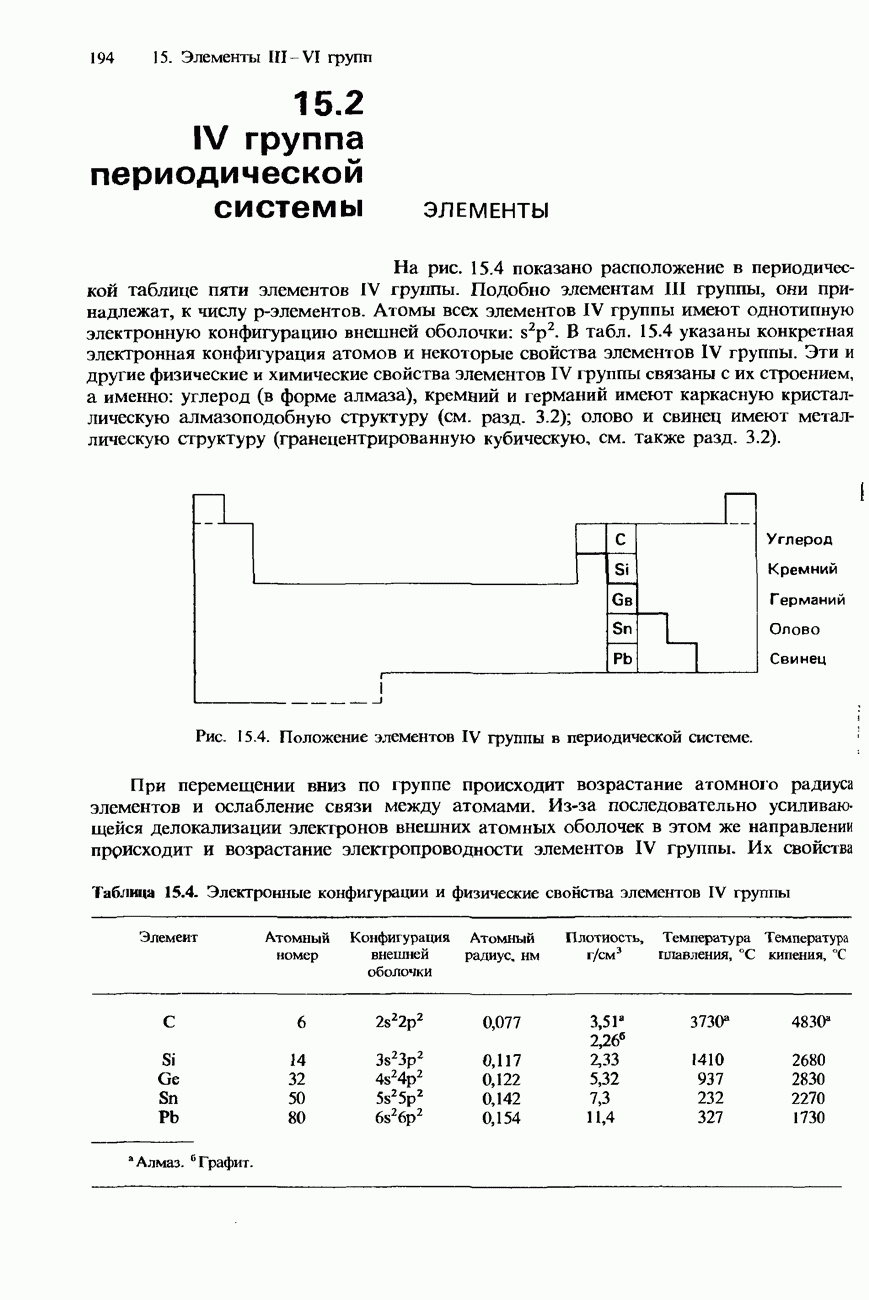
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
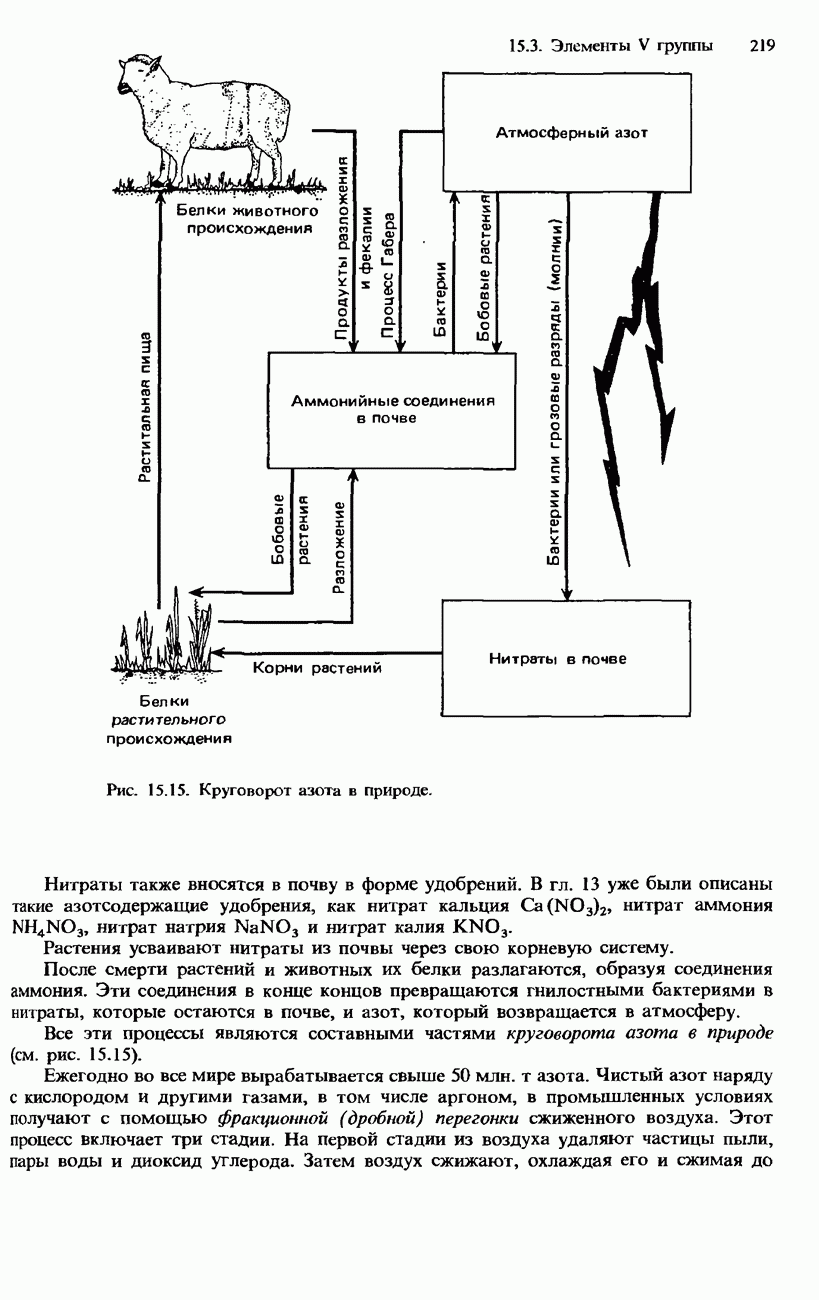
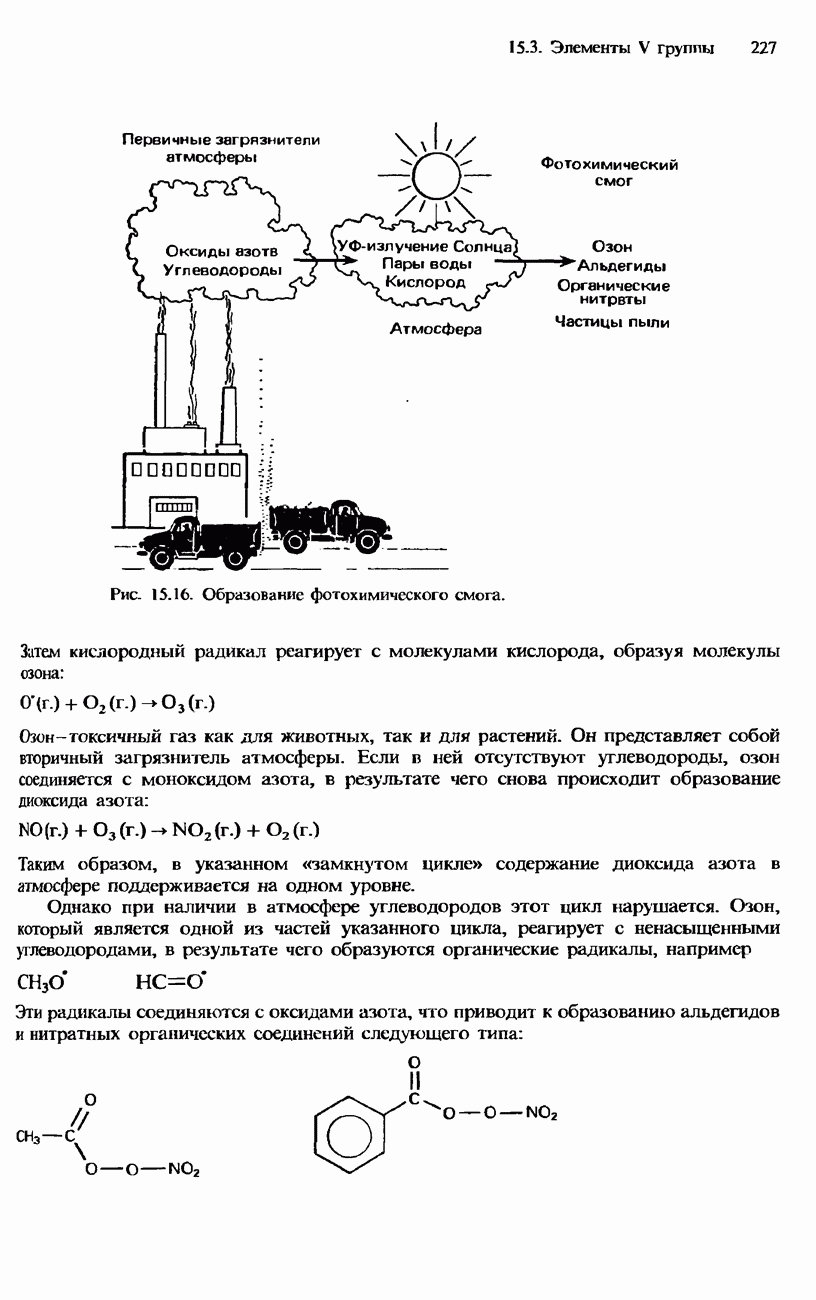
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
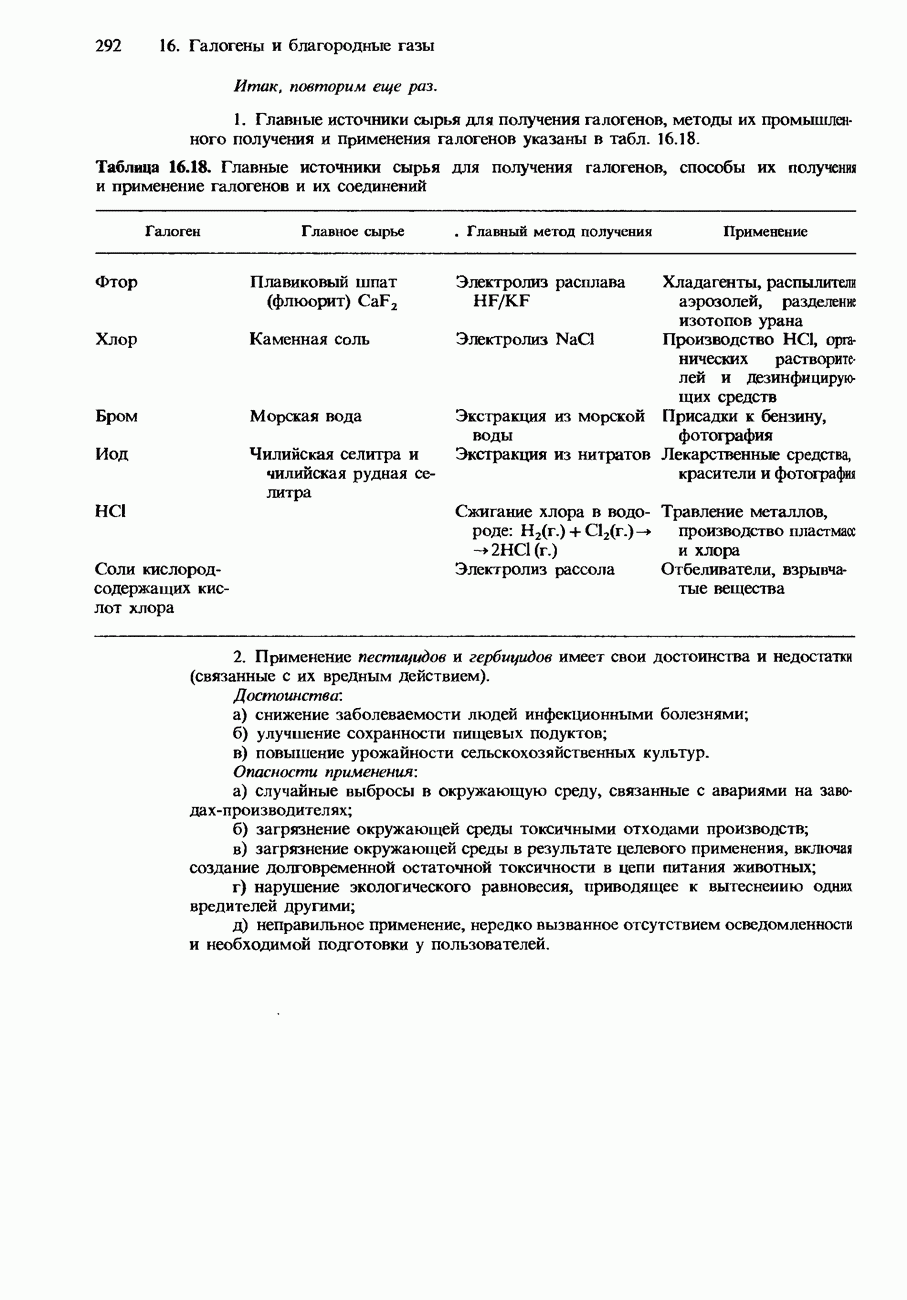
- 16.3. Распространенность, получение и применение галогенов и их соединений
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
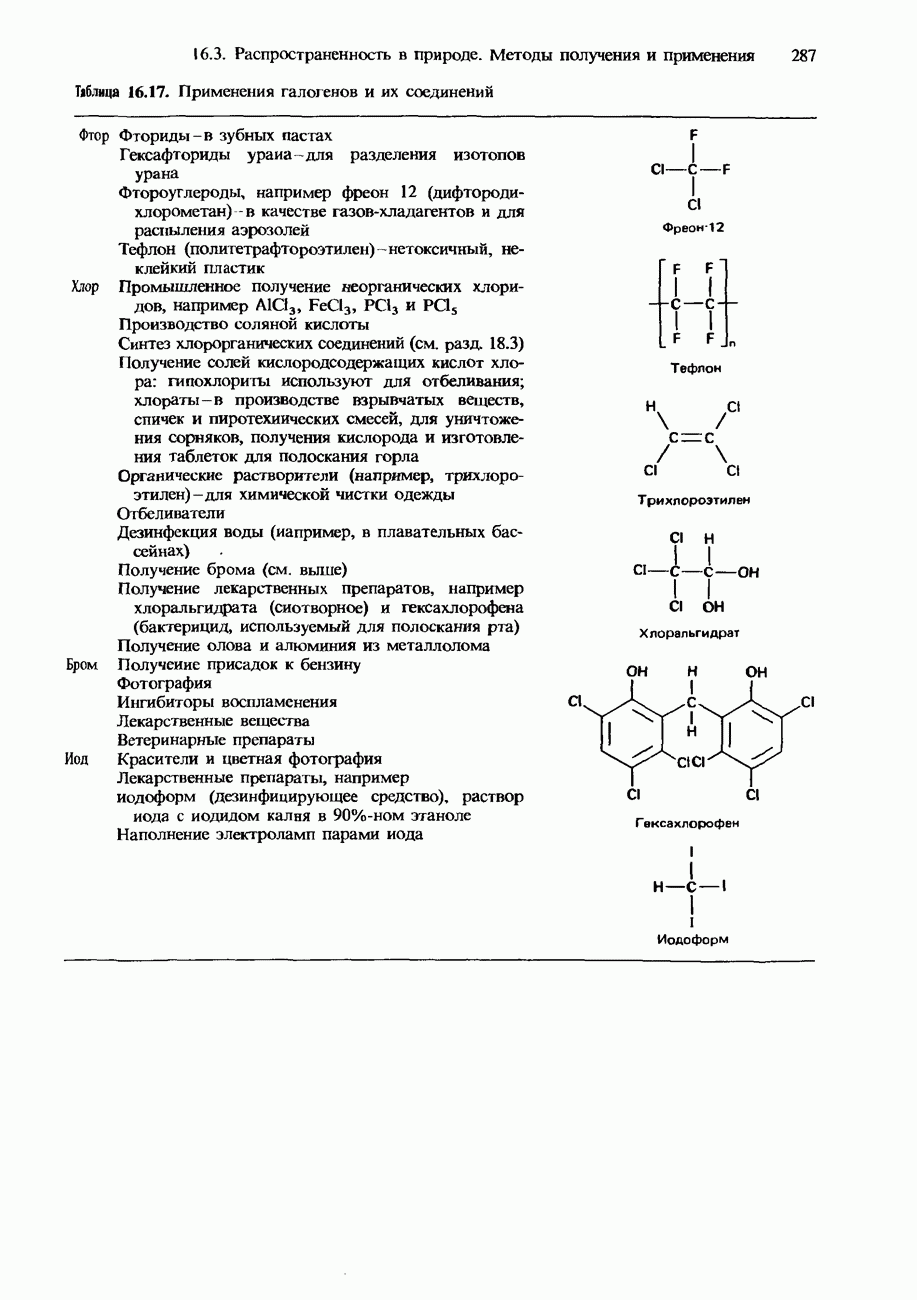
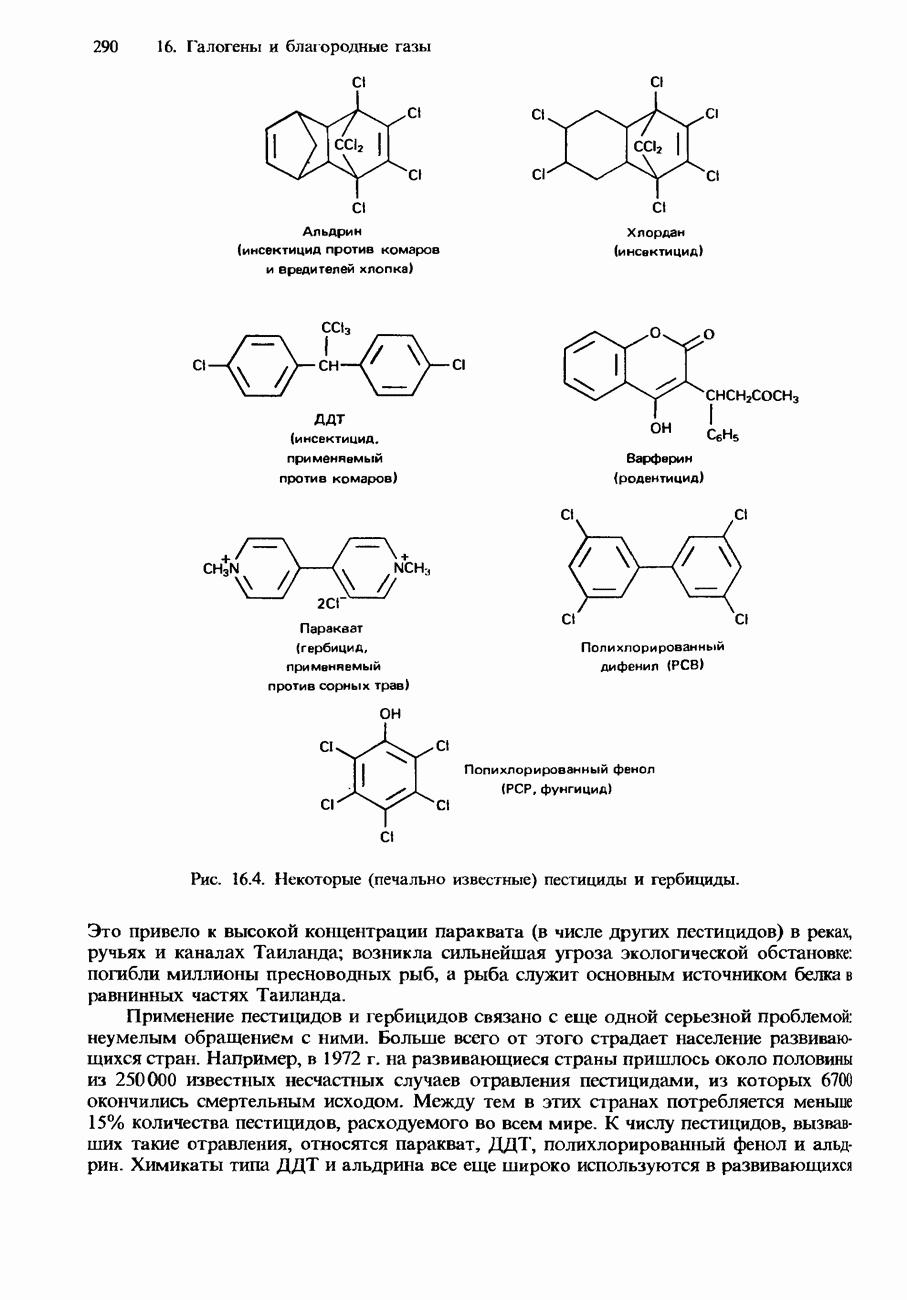
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
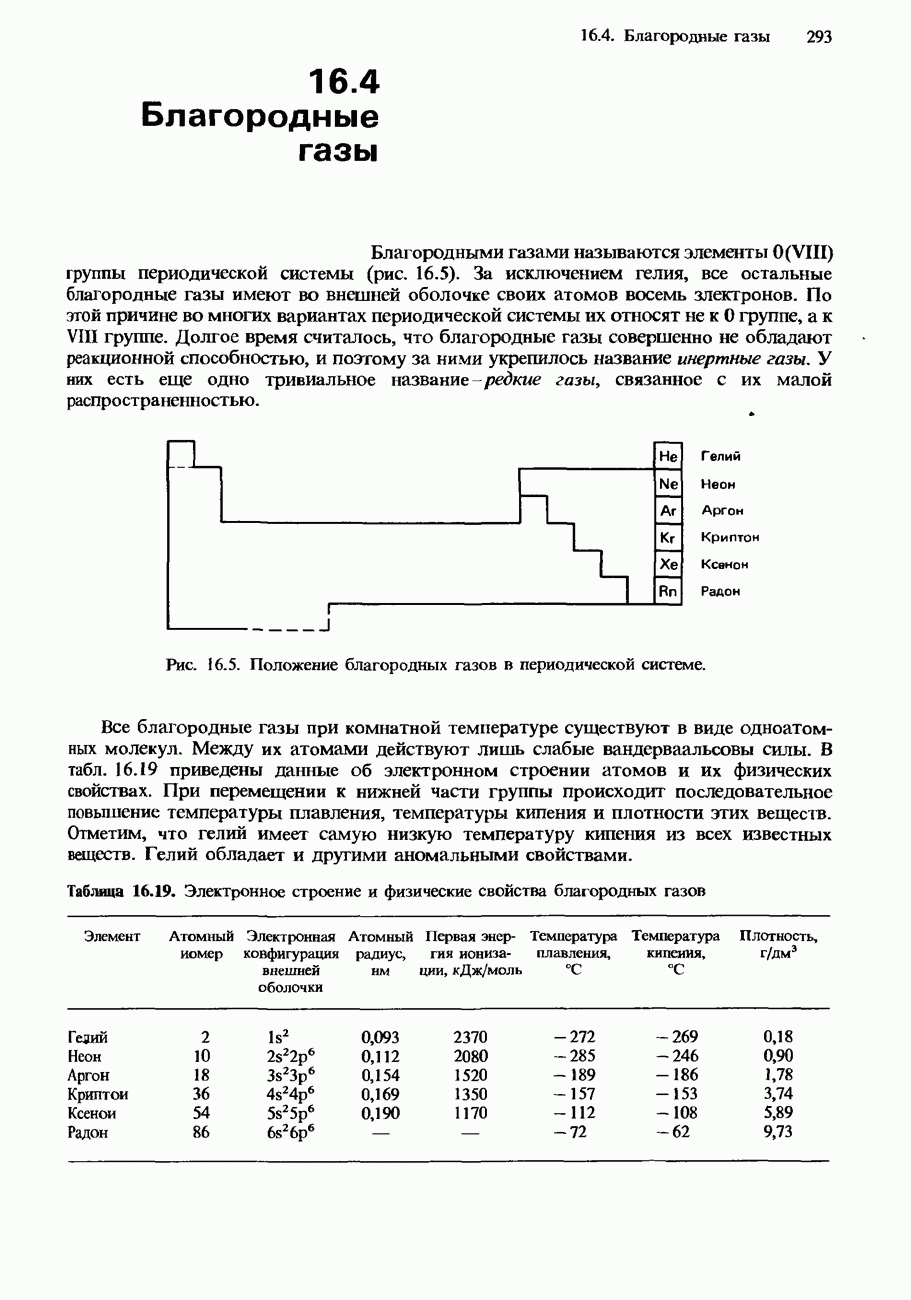
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- УГЛЕВОДОРОДЫ
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
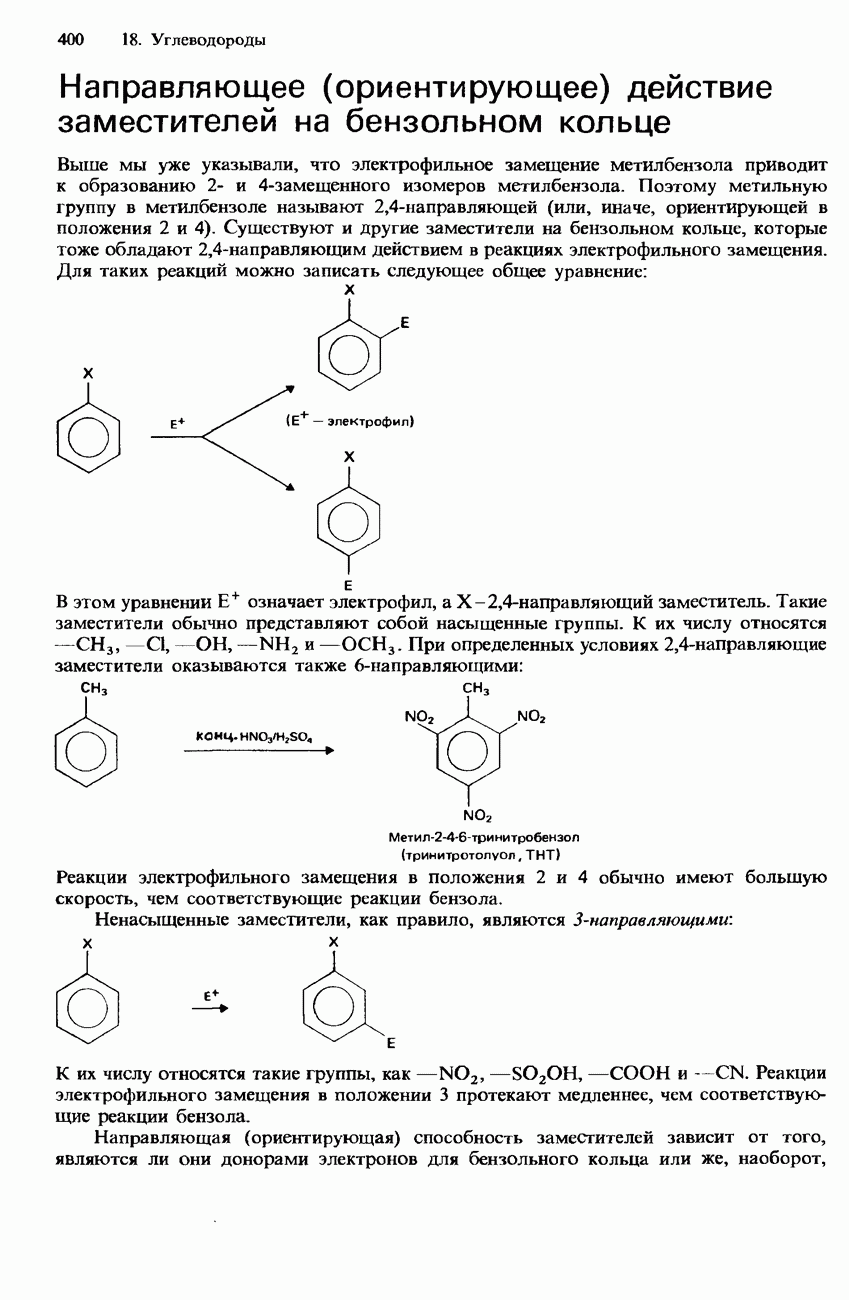
- 18.2. Арены
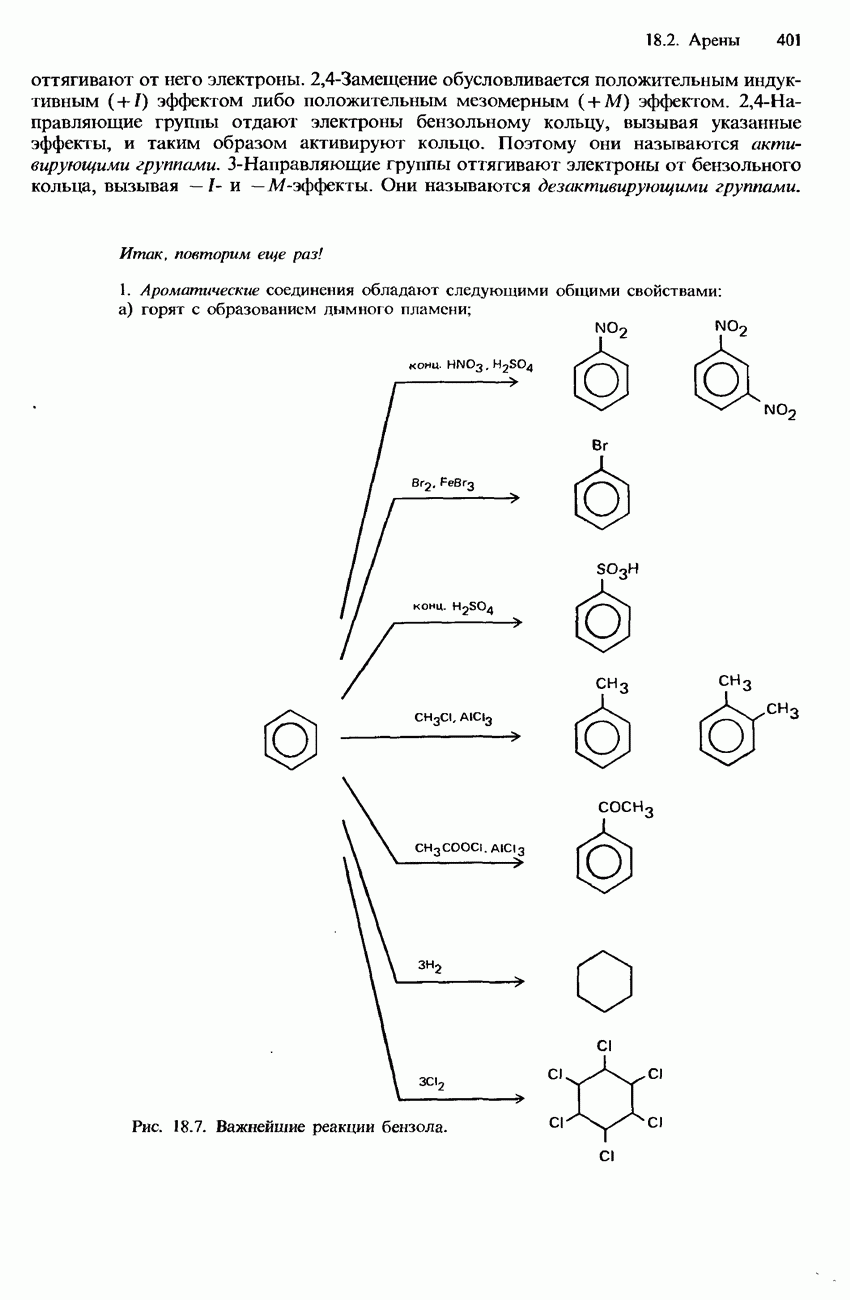
- БЕНЗОЛ
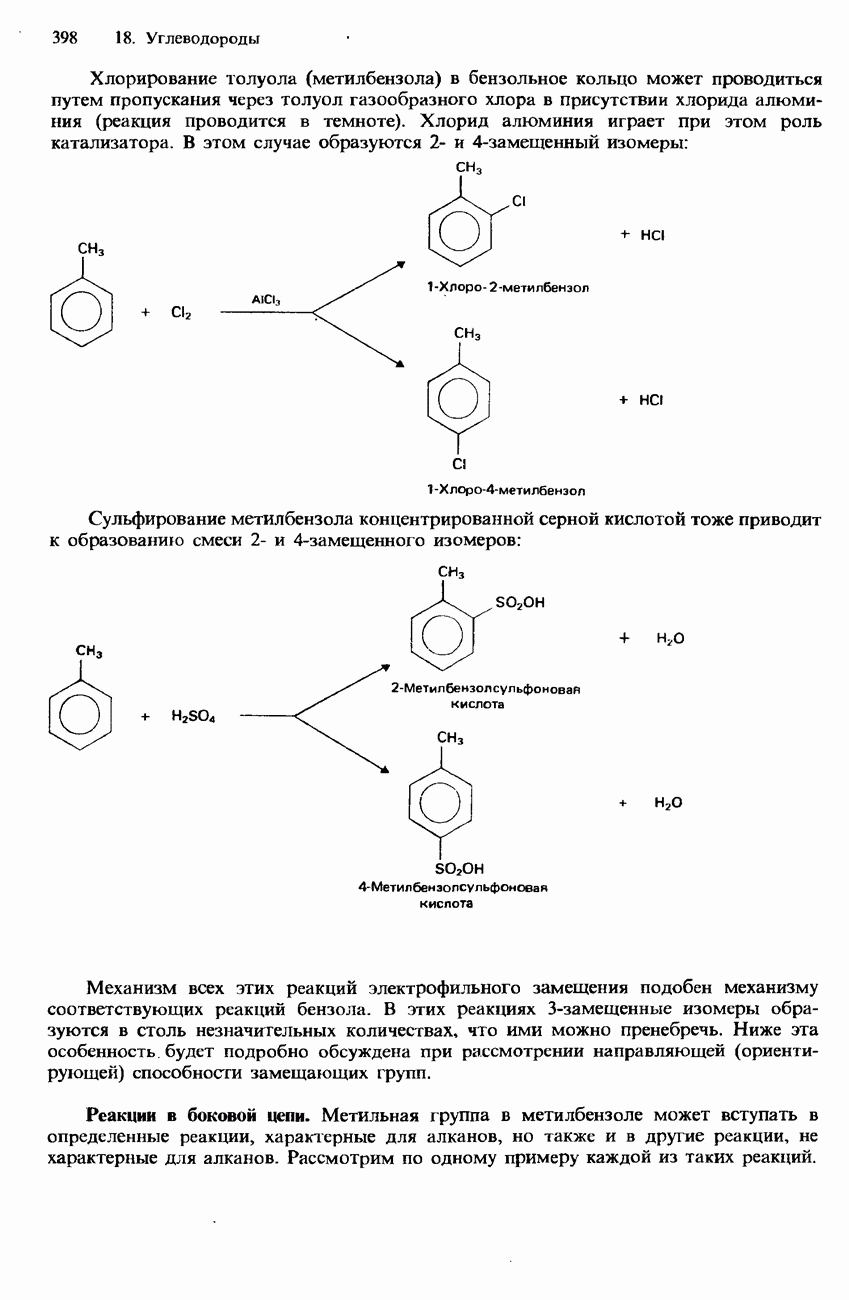
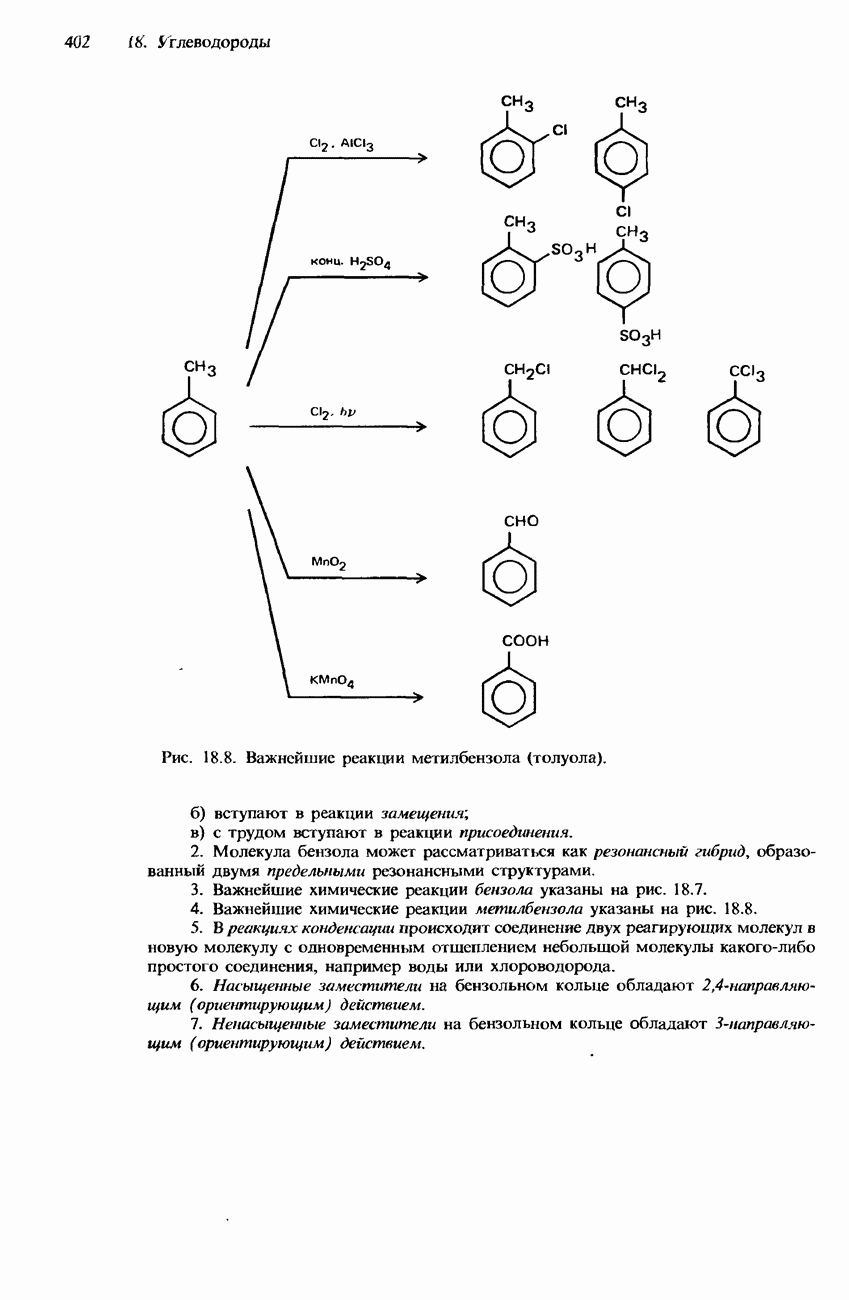
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
- 19.2. Спирты, фенолы и эфиры
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- КАРБОНОВЫЕ КИСЛОТЫ
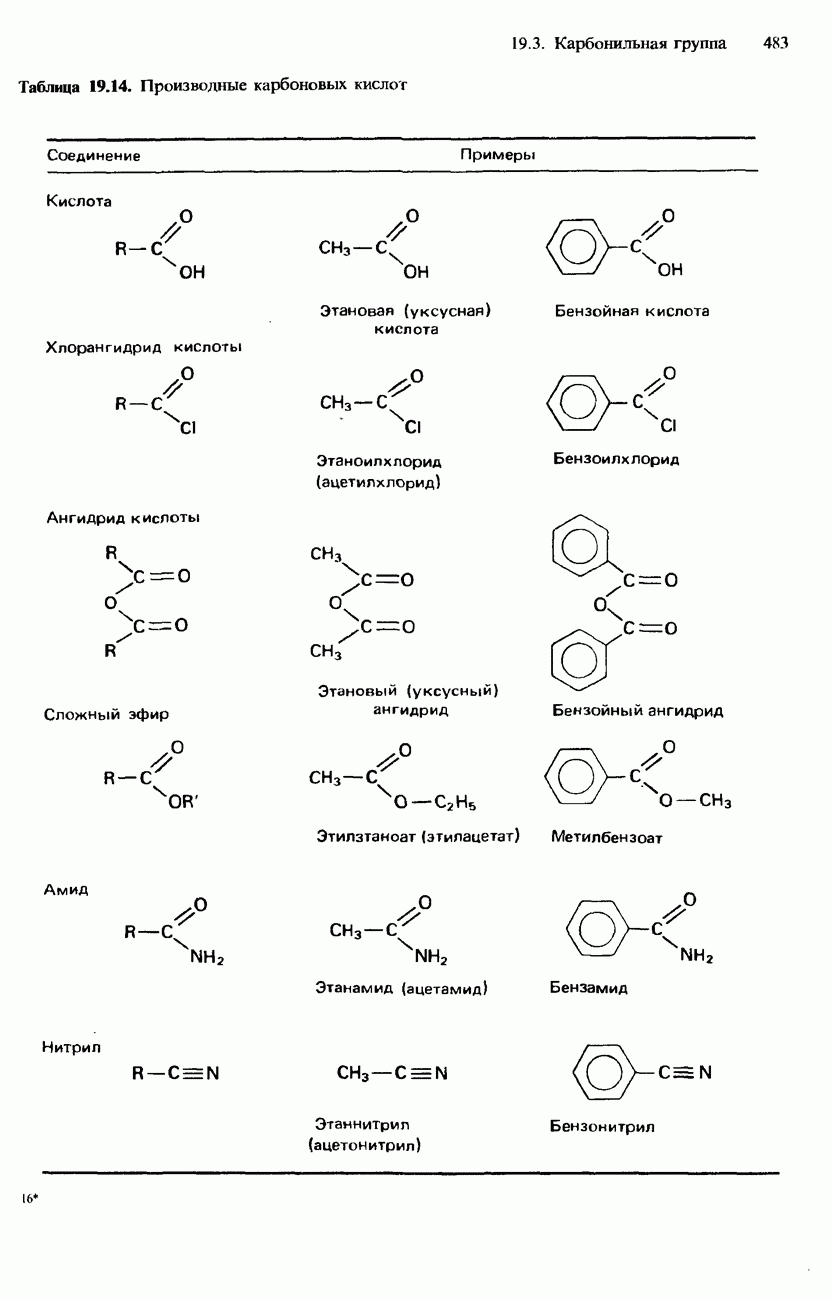
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
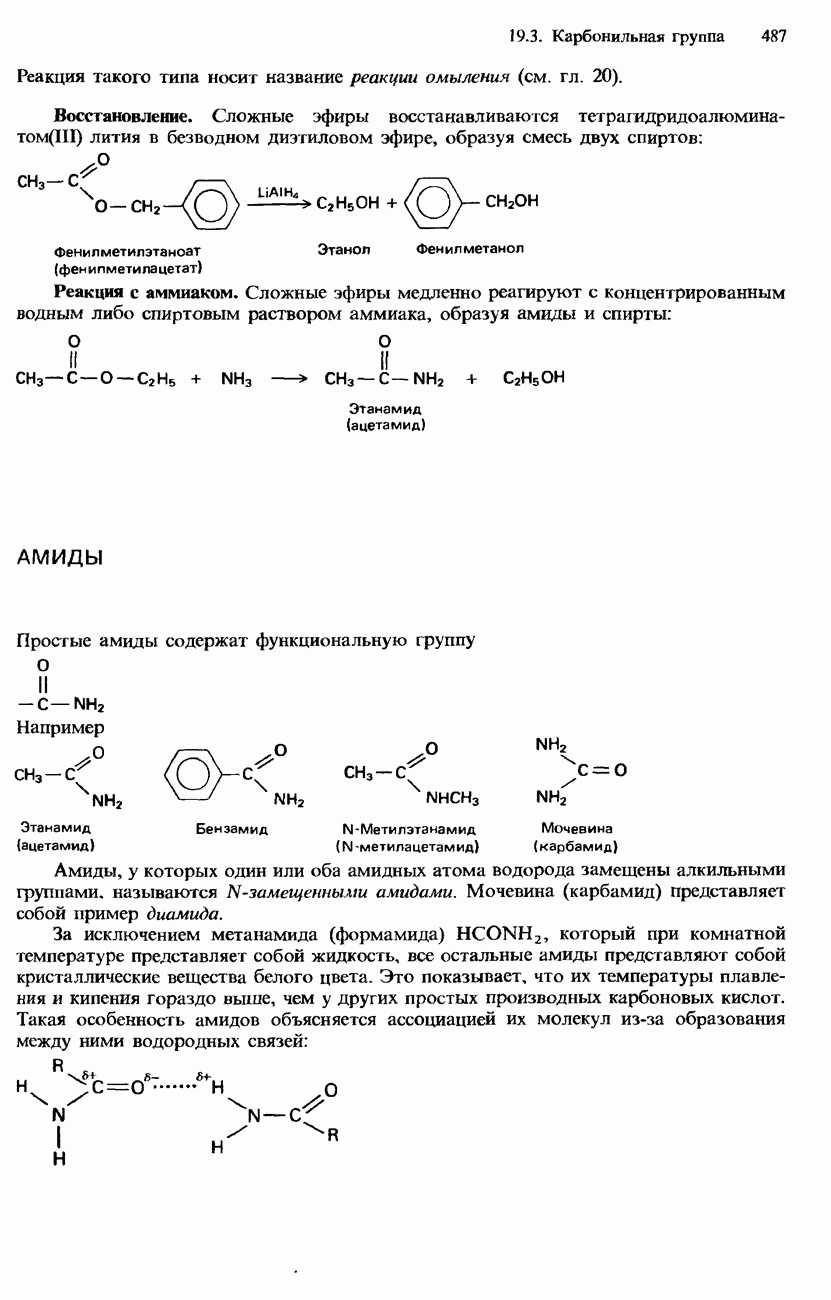
- АМИДЫ
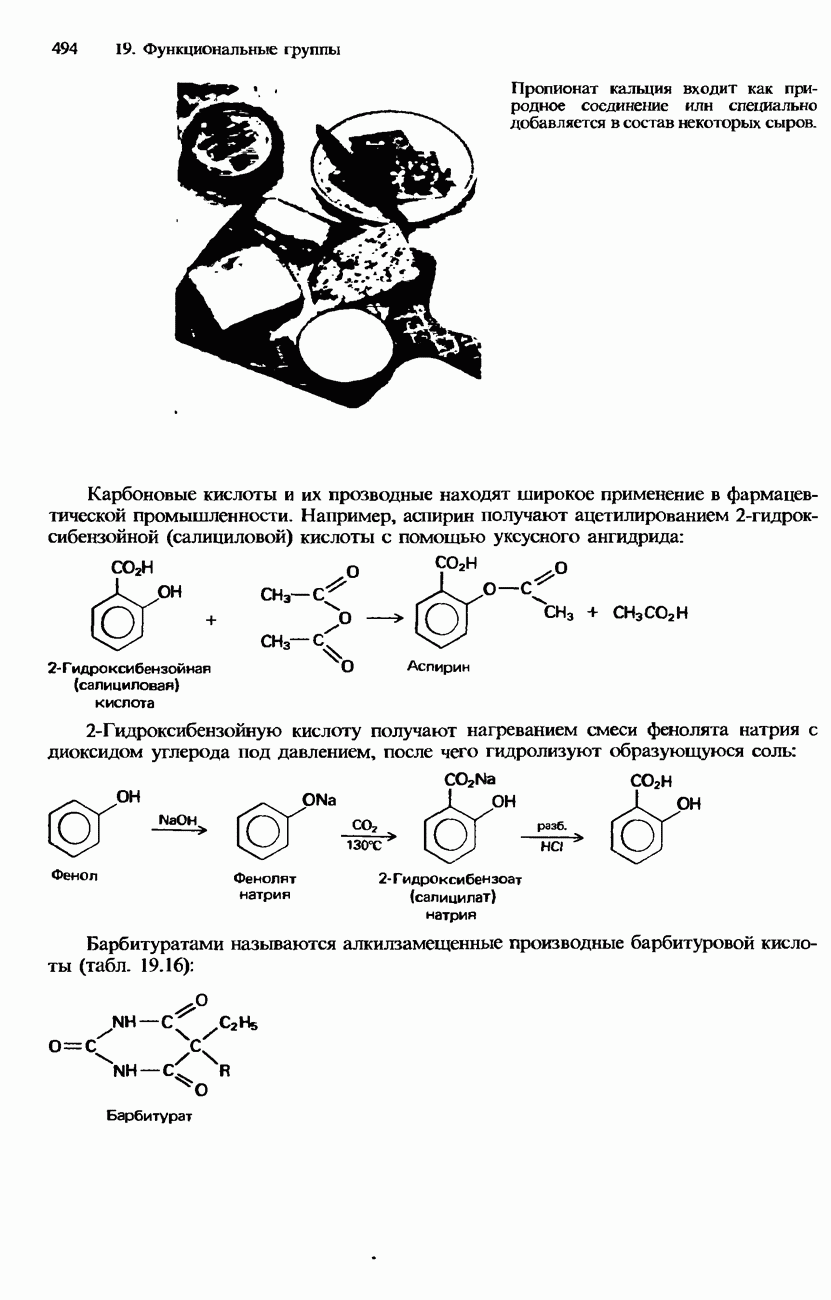
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
- 19.4 Амины и родственные соединения
- СОЛИ ДИАЗОНИЯ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
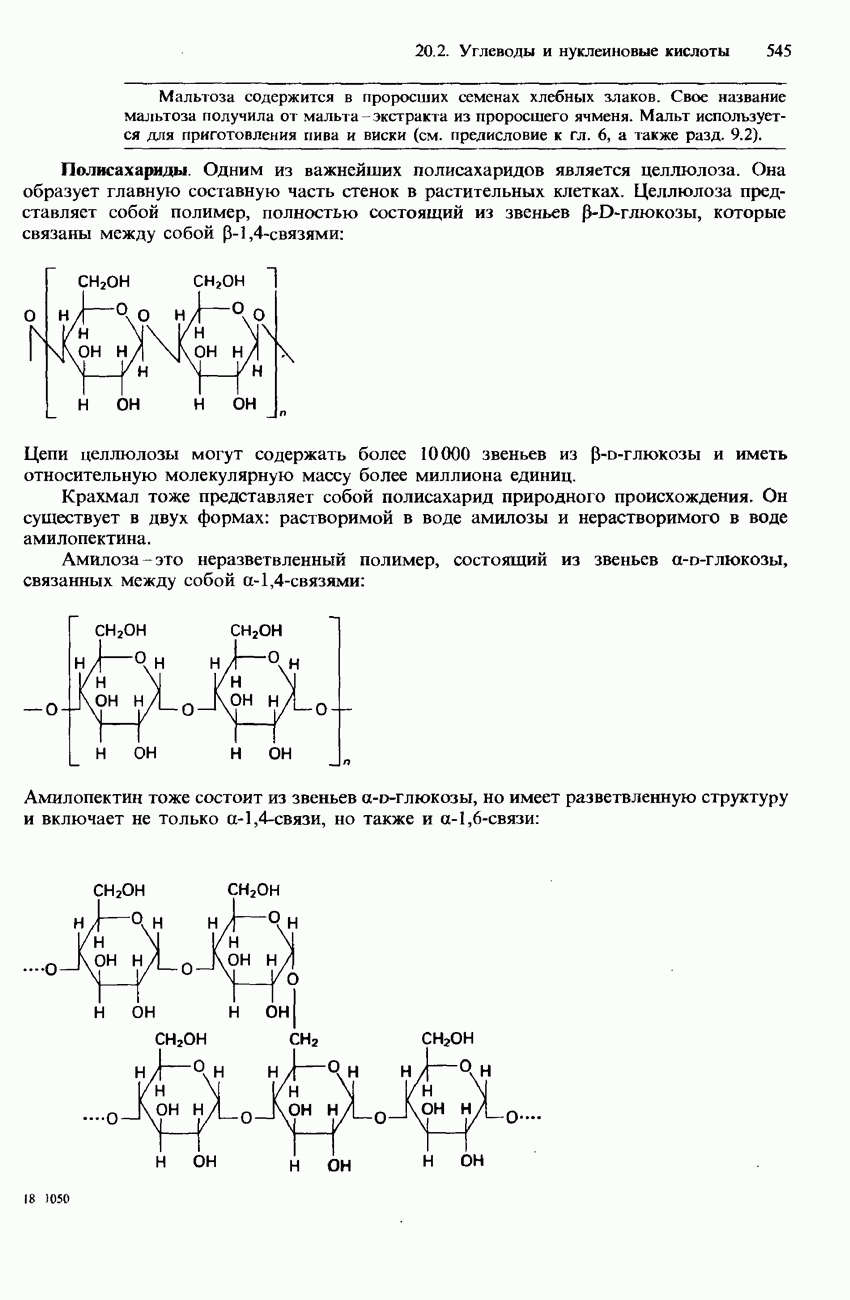
- 20.2. Углеводы и нуклеиновые кислоты
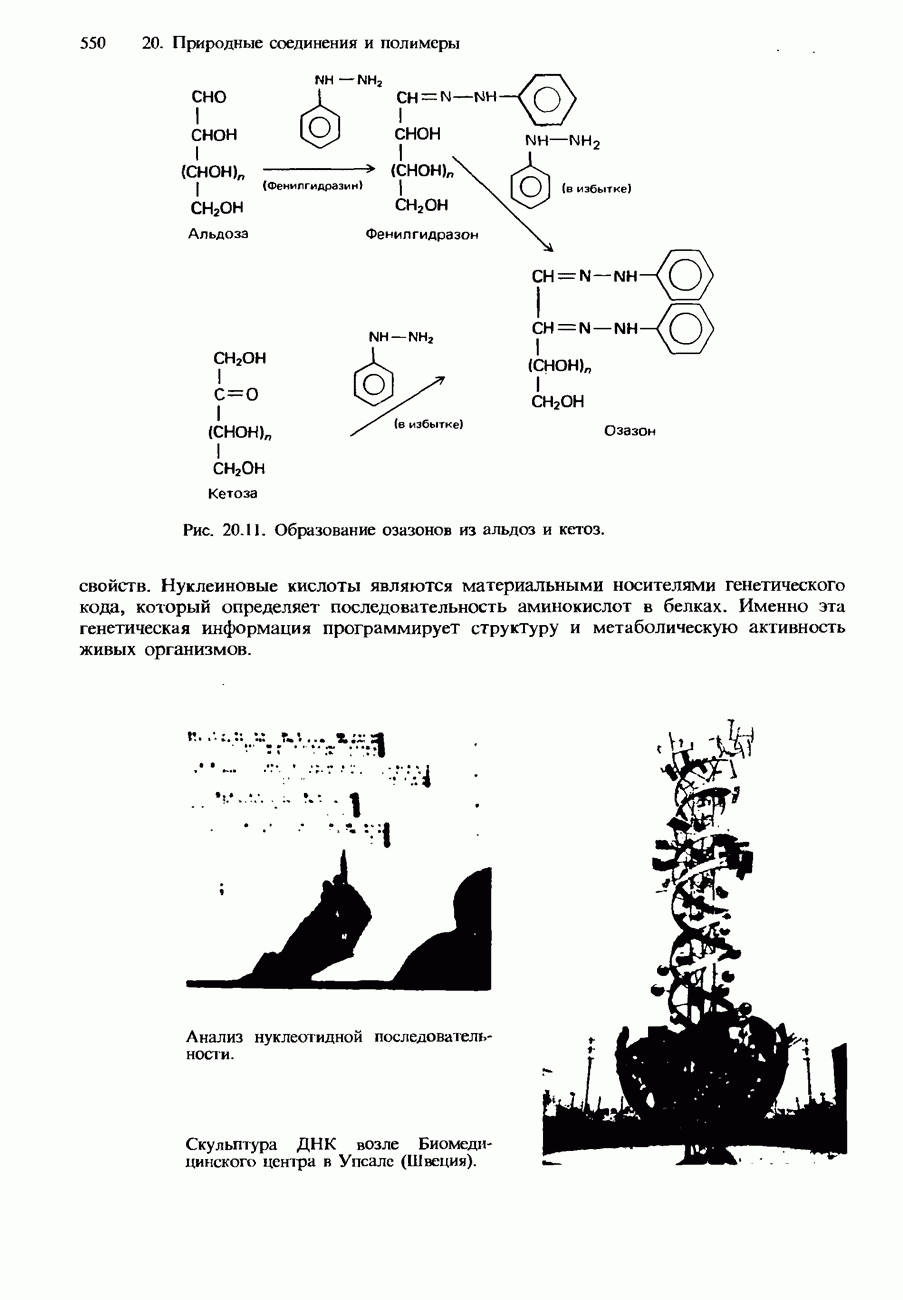
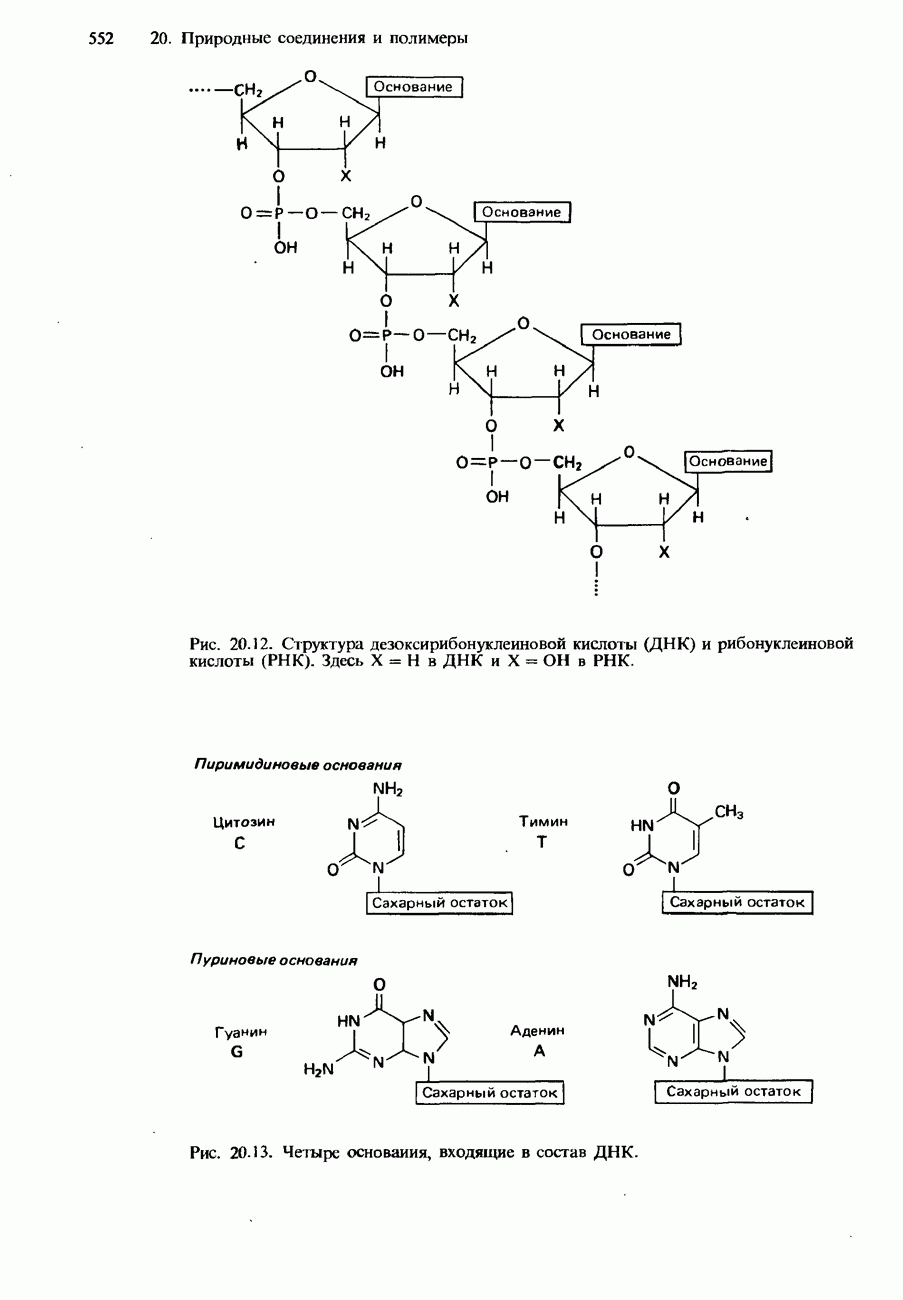
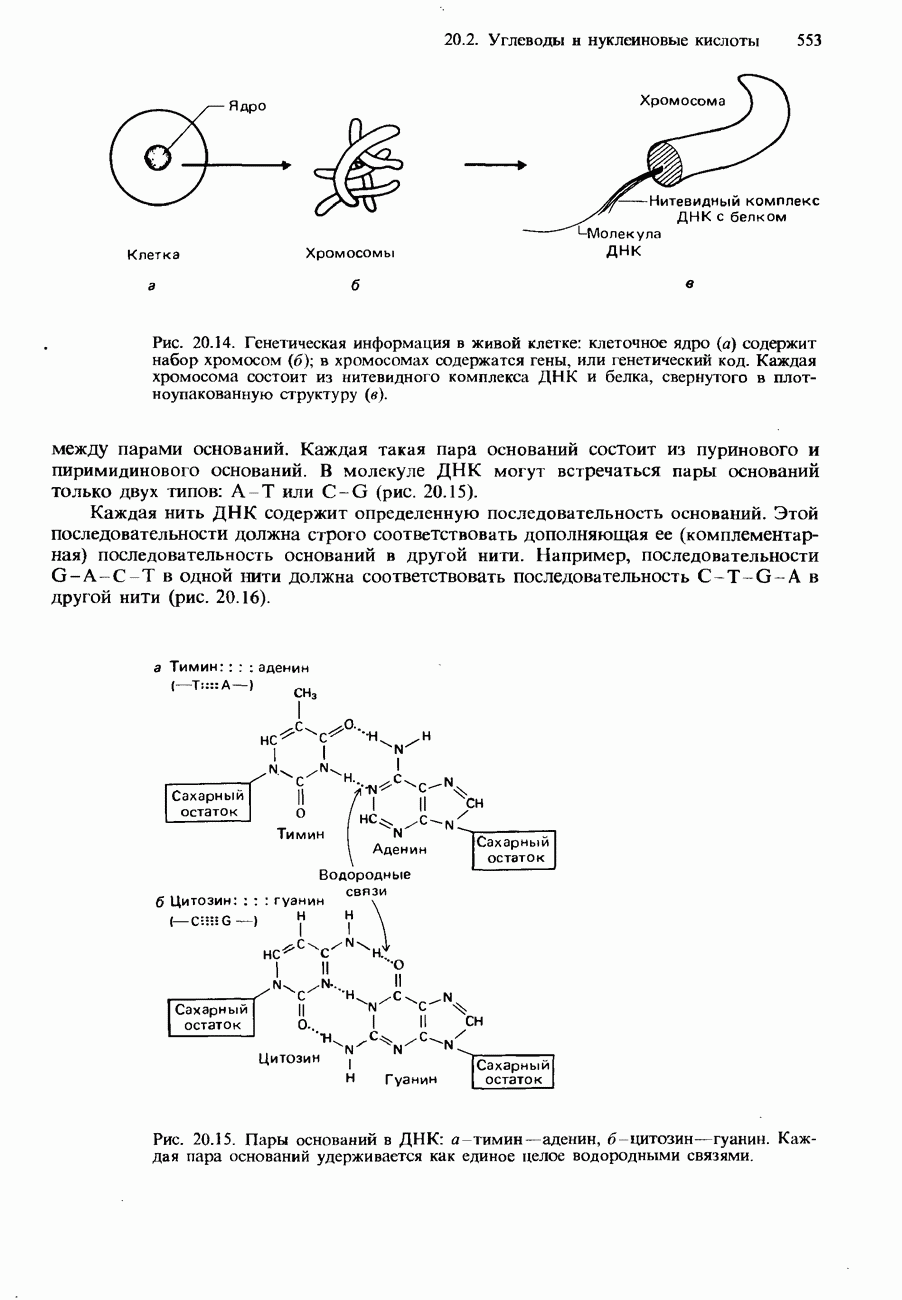
- НУКЛЕИНОВЫЕ КИСЛОТЫ
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
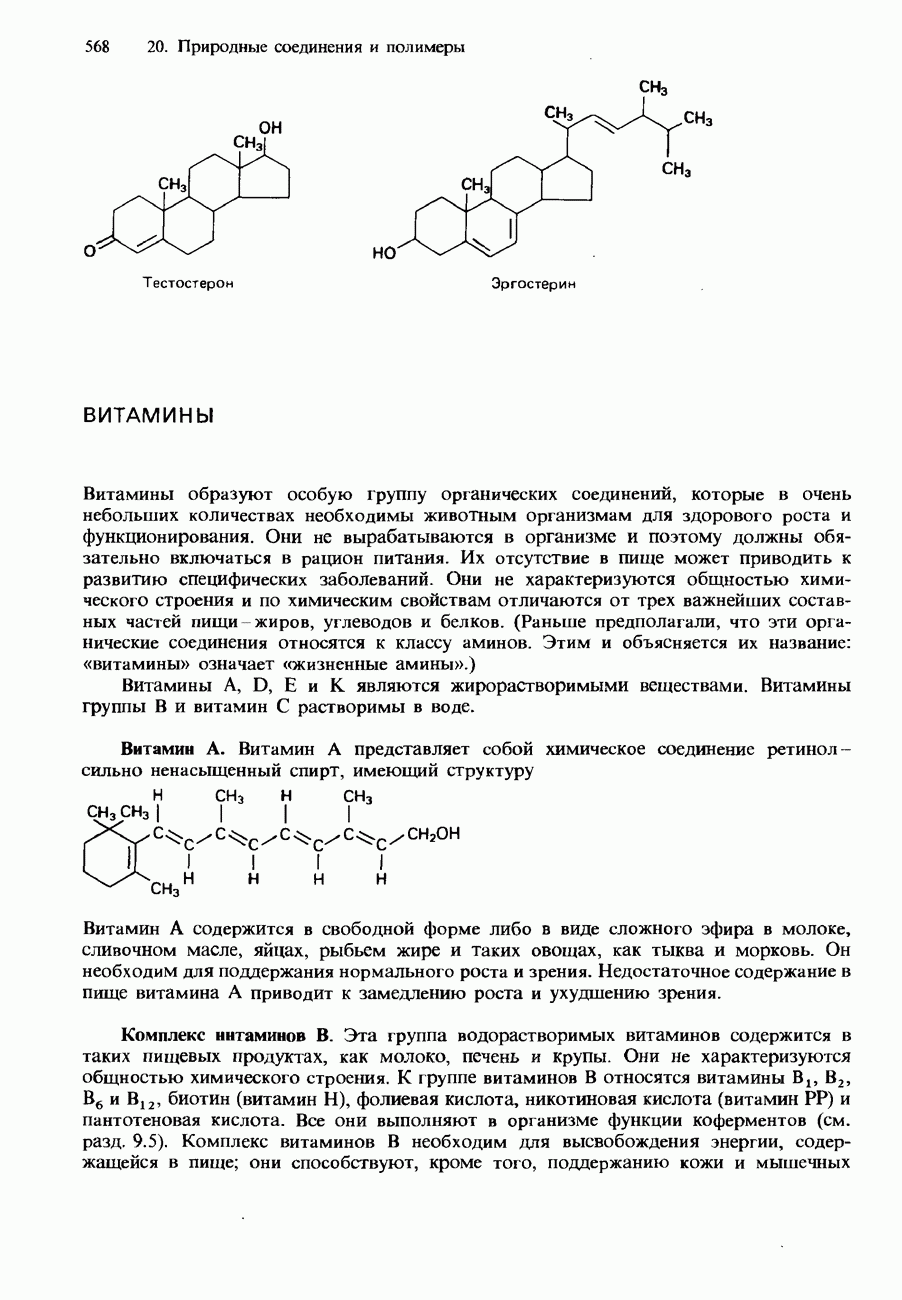
- ВИТАМИНЫ
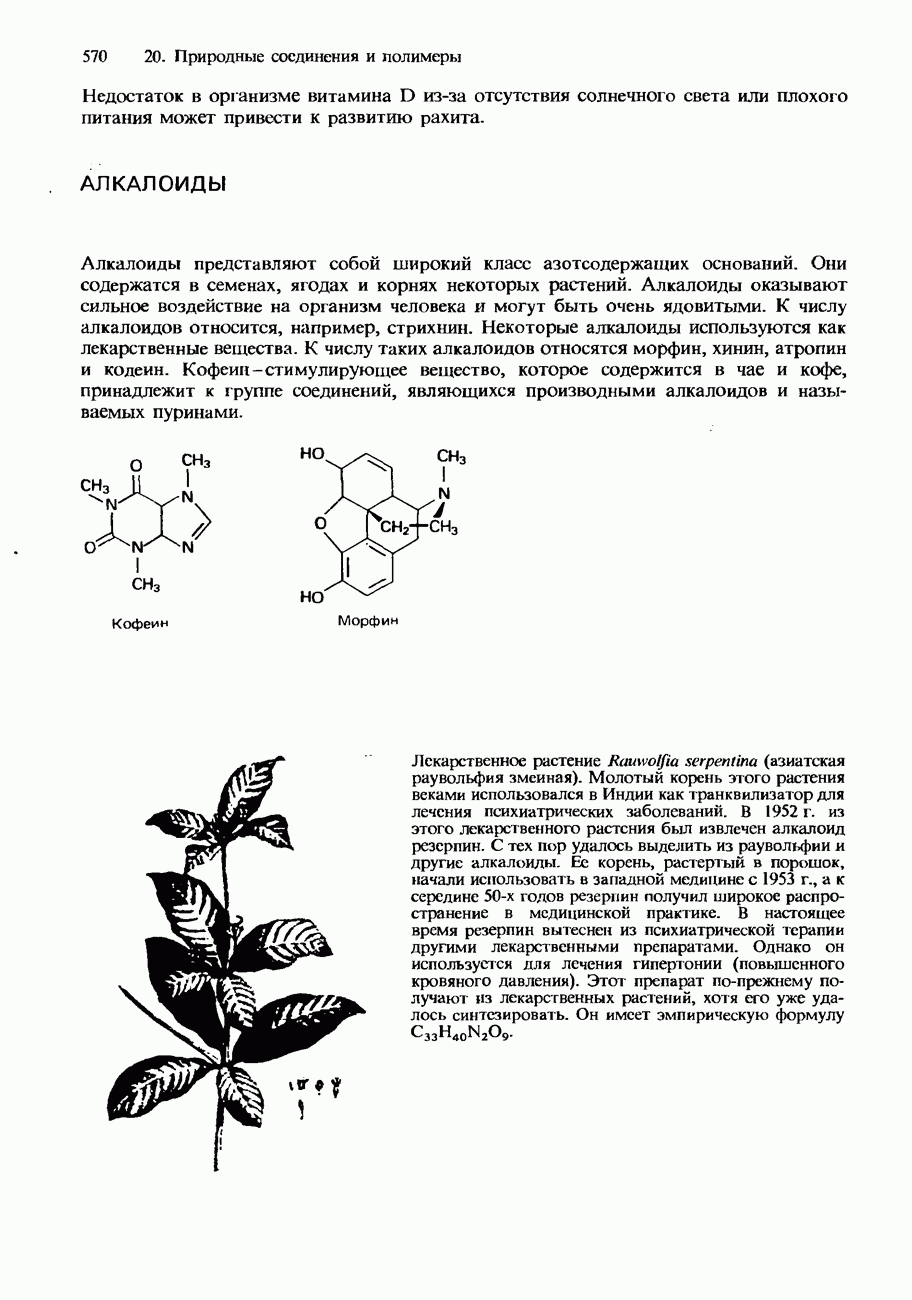
- АЛКАЛОИДЫ
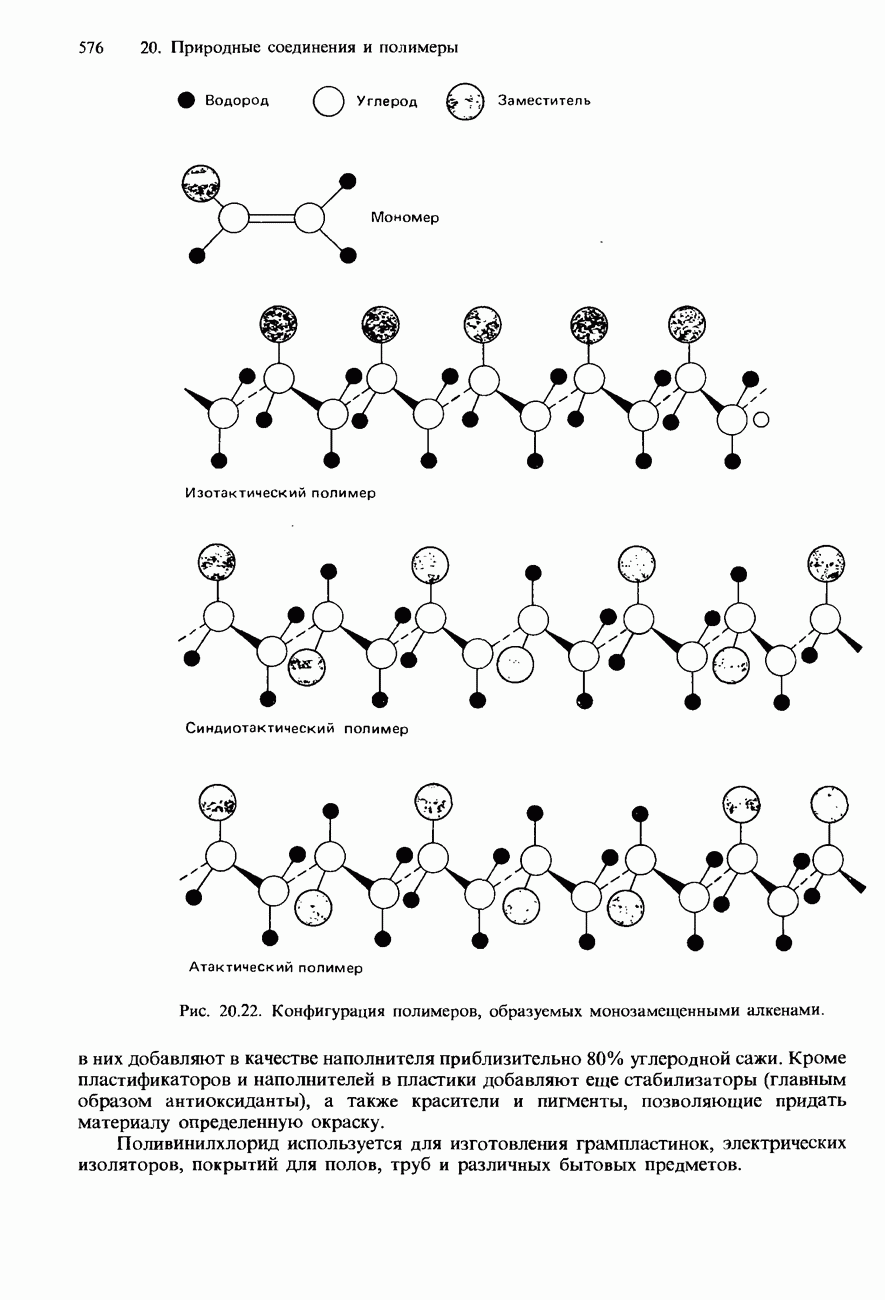
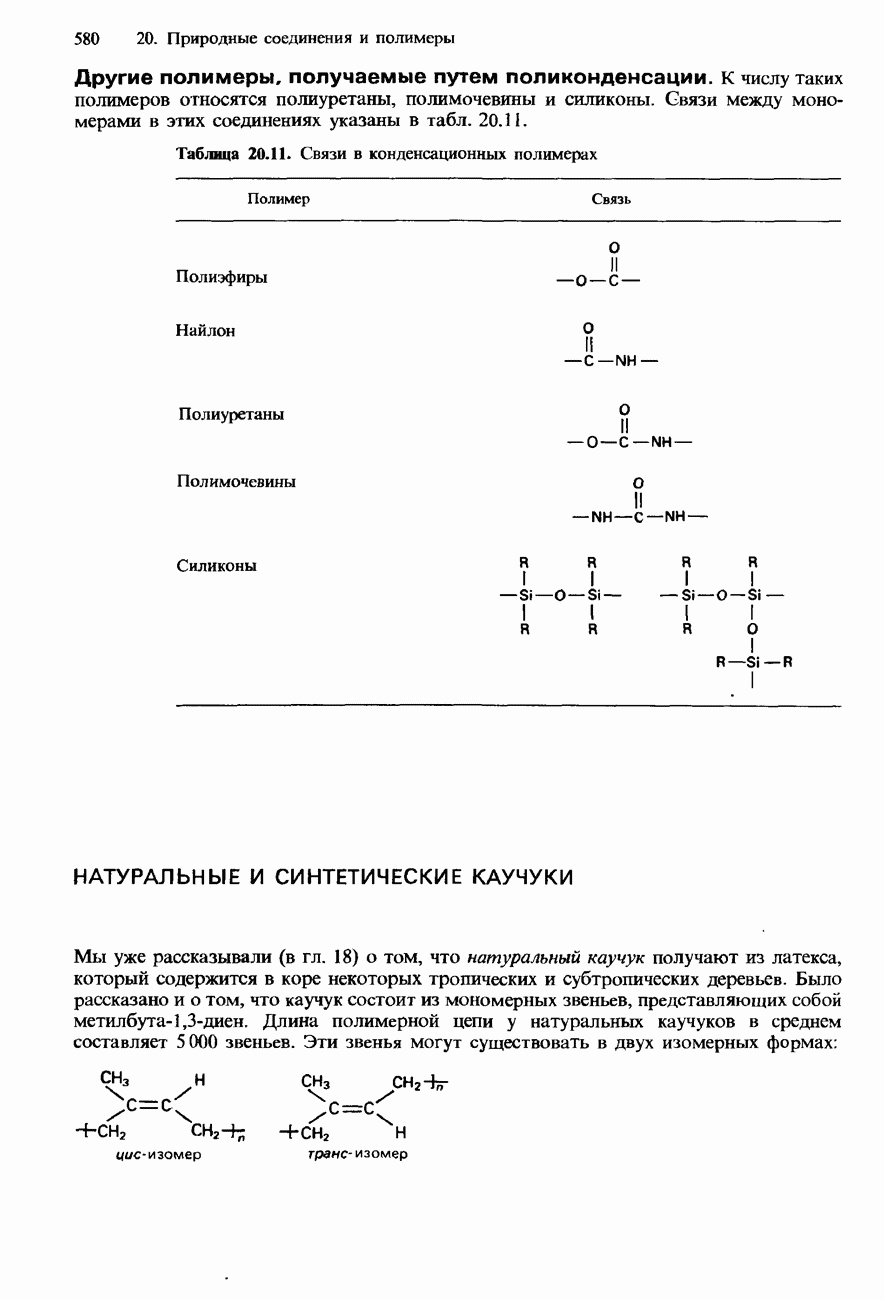
- 20.4. Полимеры
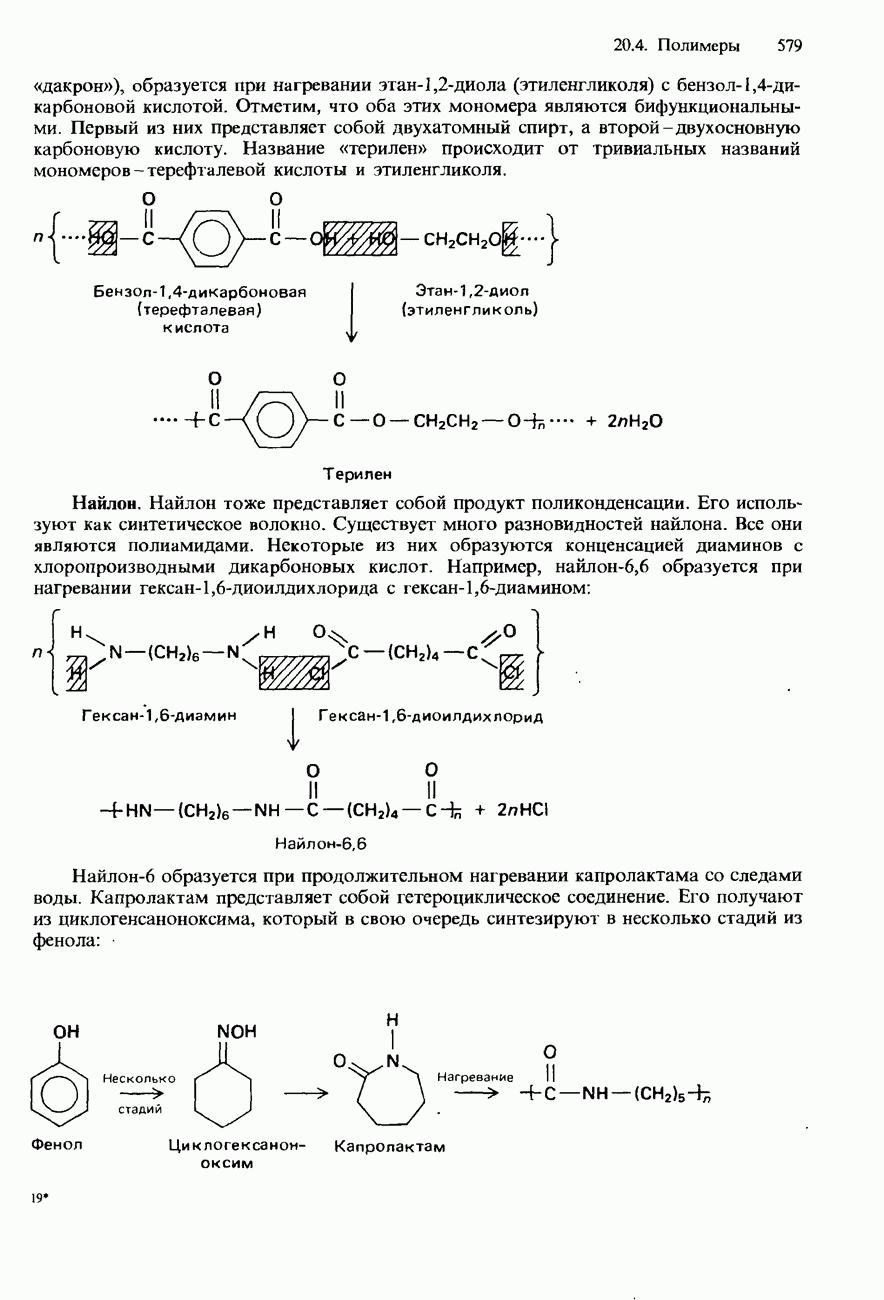
- ПОЛИМЕРИЗАЦИЯ
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ