| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
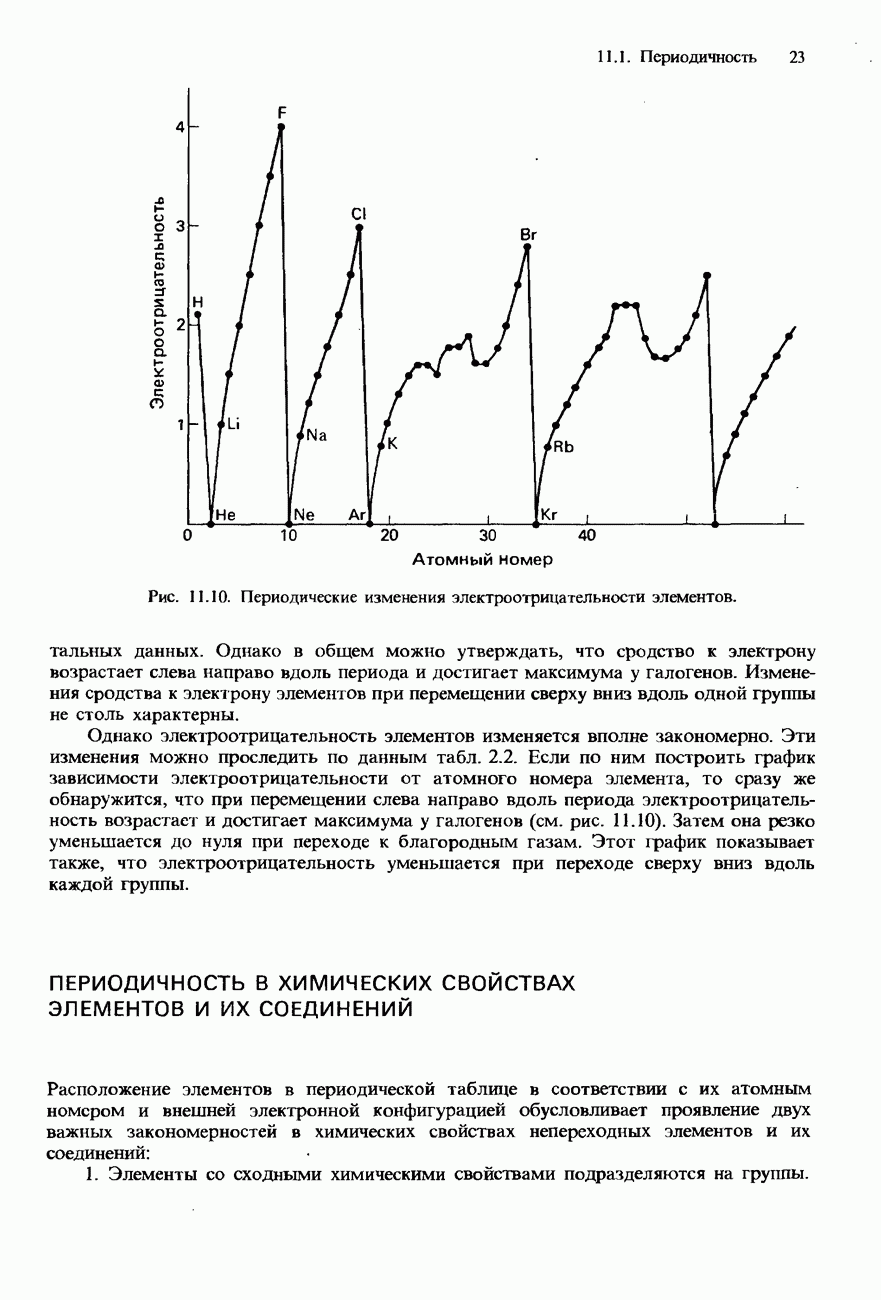
Современная периодическая таблица составлена с учетом работы Мозли, в которой были установлены атомные номера элементов. Согласно современной формулировке периодического закона, «свойства элемента периодически изменяются в соответствии с их атомным номером».
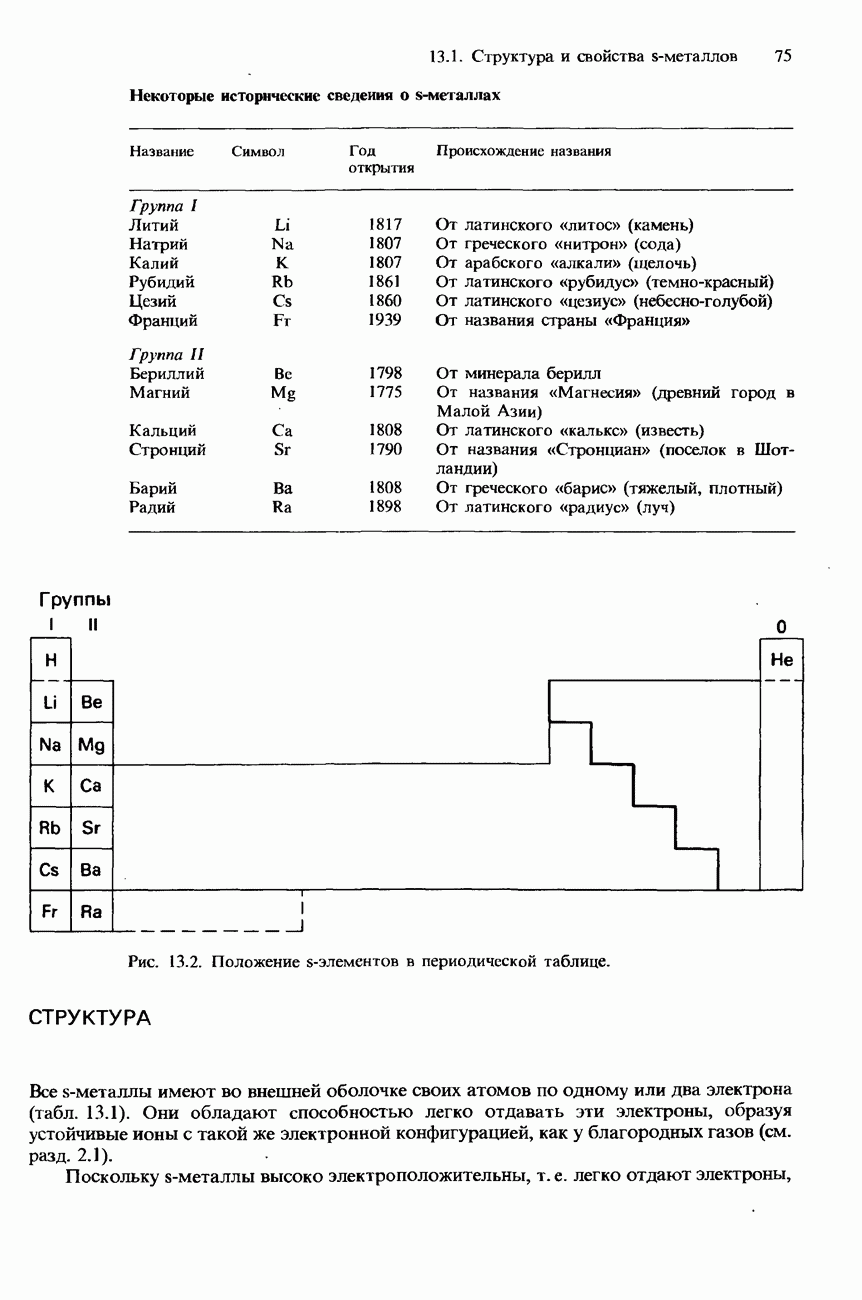
В любых современных вариантах периодической таблицы элементы располагаются в порядке возрастания их атомного номера. По мере возрастания атомного номера происходит постепенная «застройка» электронной структуры атомов элементов в соответствии с принципом заполнения (см. разд. 1.2). Таким образом, структура современной периодической таблицы связана с электронной структурой элементов. Она основана на электронной конфигурации электронов в самых внешних атомных оболочках и в подоболочках с самой высокой энергией. Дело в том, что только эти электроны определяют химические свойства элементов и их соединений.
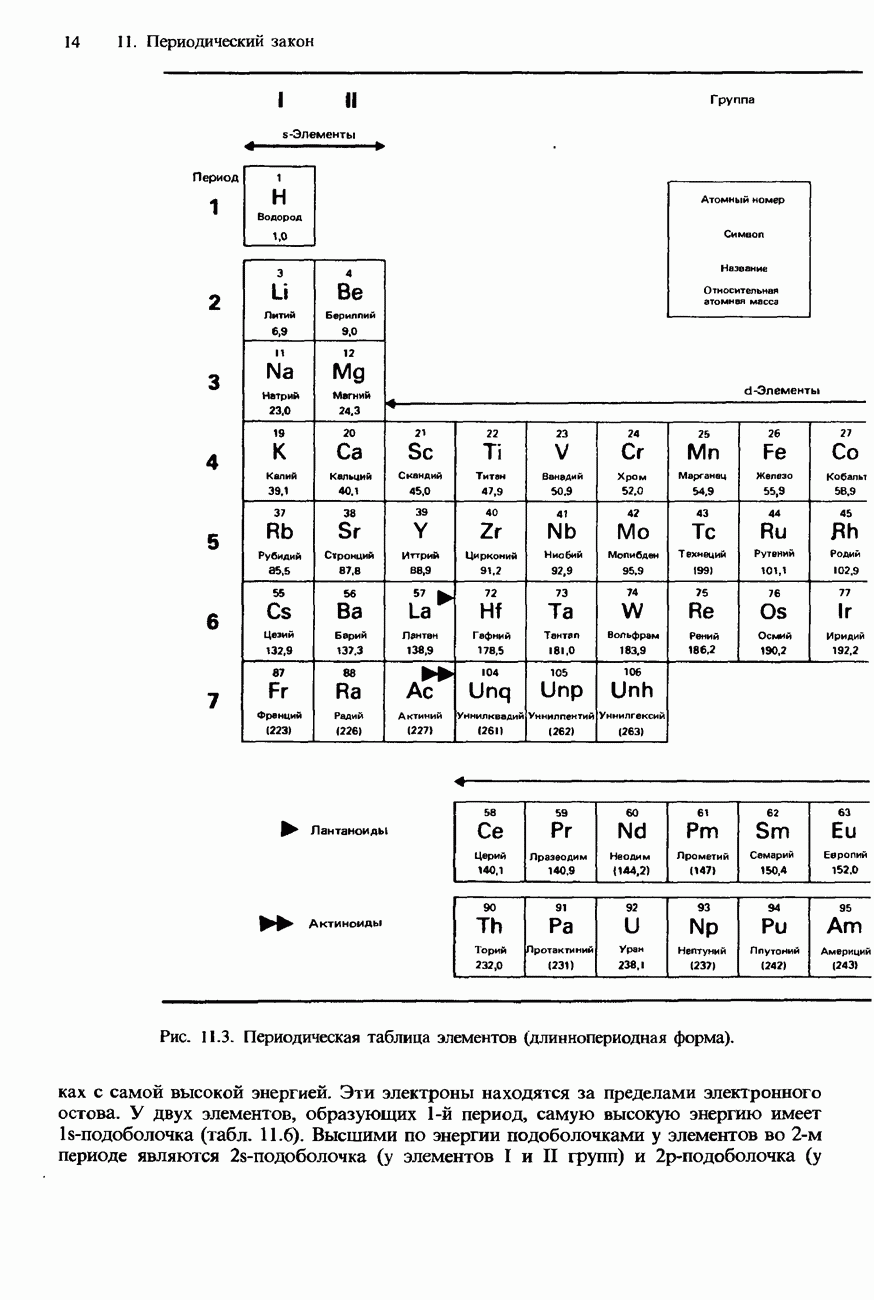
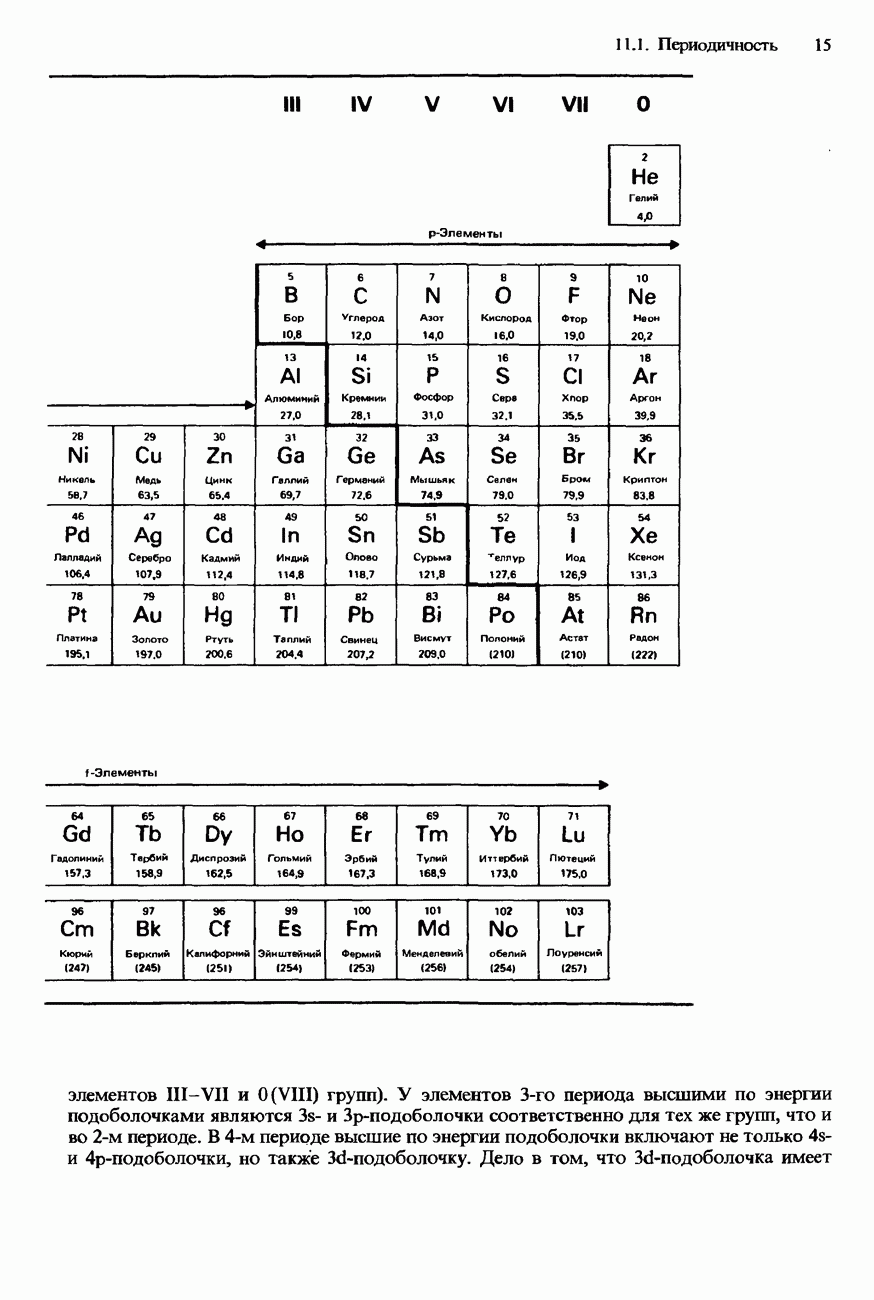
Существует много форм современной периодической таблицы. В 1984 г. Международный союз теоретической и прикладной химии (ИЮПАК) временно рекомендовал форму, показанную в табл. 11.4. Отметим, что в такой таблице водород находится в группе I, а галогены и благородные газы соответственно в группах 17 и 18. На рис. 11.3 показана форма периодической таблицы, рекомендованная в 1985 г. Ассоциацией научного образования (ASE). Именно эта форма будет использоваться в данной книге.
Что означает название «уннилкваднй». Так называется, согласно правилам ИЮПАК, элемент с атомным номером 104. Это название непосредственно связано с атомным номером элемента: «ун-» означает 1, «-нил-»-0 и «квад»-4. Элемент 104 был открыт в 1964 г. советскими физиками. Они назвали его «курчатовий» по имени известного русского физика-ядерщика И. В. Курчатова (1903-1960) и предложили для него символ  . В 1969 г. этот элемент был воспроизведен в США и получил название «резерфордий» (Rf) в честь Э. Резерфорда. Уннилквадий имеет символ Unq. Уннилквадий находится в 7-м периоде. Следующий элемент в этом периоде, имеющий атомный номер 105, называется уннилпентий (Unp), а элемент с атомным номером 106 называется уннилгексий (Unh).
. В 1969 г. этот элемент был воспроизведен в США и получил название «резерфордий» (Rf) в честь Э. Резерфорда. Уннилквадий имеет символ Unq. Уннилквадий находится в 7-м периоде. Следующий элемент в этом периоде, имеющий атомный номер 105, называется уннилпентий (Unp), а элемент с атомным номером 106 называется уннилгексий (Unh).
Периоды
Горизонтальные ряды элементов в периодической таблице называются периоды. Все элементы из одного периода имеют одинаковый электронный остов (внутренние электронные оболочки). Этот электронный остов имеет такую же структуру, как у благородного газа, которым завершается предыдущий период (табл. 11.5). Химические свойства всякого элемента зависят только от электронов, находящихся на подоболочках

Рис. 11.3. Периодическая таблица элементов (длиннопериодная форма).
с самой высокой энергией. Эти электроны находятся за пределами электронного остова. У двух элементов, образующих 1-й период, самую высокую энергию имеет  -подоболочка (табл. 11.6). Высшими по энергии подоболочками у элементов во 2-м периоде являются 2я-подоболочка (у элементов I и II групп) и 2я-подоболочка
-подоболочка (табл. 11.6). Высшими по энергии подоболочками у элементов во 2-м периоде являются 2я-подоболочка (у элементов I и II групп) и 2я-подоболочка

(у элементов III-VII и 0 (VIII) групп). У элементов 3-го периода высшими по энергии подоболочками являются 3s- и Зр-подоболочки соответственно для тех же групп, что и во 2-м периоде. В 4-м периоде высшие по энергии подоболочки включают не только  но также
но также  -подоболочку. Дело в том, что
-подоболочку. Дело в том, что  -подоболочка имеет
-подоболочка имеет
Таблица 11.4. Форма периодической таблицы элементов, рекомендованная ИЮПАК

Таблица 11.5. Электронная структура элементов в различных периодах

Таблица 11.6. Высшие по энергии подоболочки в атомах элементов различных периодов

более высокую энергию, чем  -подоболочка (см. рис. 1.21). Элементы этого периода, у которых высшие по энергии электроны располагаются в
-подоболочка (см. рис. 1.21). Элементы этого периода, у которых высшие по энергии электроны располагаются в  -подоболочке, называются
-подоболочке, называются  -элементами (см. гл. 14).
-элементами (см. гл. 14).
Группы
Вертикальные столбцы элементов в периодической таблице называются группами. Все элементы, принадлежащие какой-либо группе, имеют характерную для нее электронную конфигурацию высшей по энергии подоболочки (табл. 11.7). Например, для I группы характерна электронная конфигурация  для II группы - конфигурация
для II группы - конфигурация  для 111 группы - конфигурация
для 111 группы - конфигурация  и так далее до группы О (VIII), все элементы которой имеют конфигурацию
и так далее до группы О (VIII), все элементы которой имеют конфигурацию  . В табл. 11.8 указаны электронные конфигурации высших по энергии подоболочек и электронных остовов для пяти элементов из группы IV.
. В табл. 11.8 указаны электронные конфигурации высших по энергии подоболочек и электронных остовов для пяти элементов из группы IV.
Некоторые группы периодической таблицы имеют традиционные названия (табл. 11.9). Однако здесь следует остановиться на двух исключениях. Водород (внешняя электронная конфигурация  ) принадлежит к группе I, но не является щелочным металлом. Гелий, элемент группы О (VIII), относится к благородным газам, но в отличие от всех остальных элементов этой группы имеет внешнюю электронную конфигурацию
) принадлежит к группе I, но не является щелочным металлом. Гелий, элемент группы О (VIII), относится к благородным газам, но в отличие от всех остальных элементов этой группы имеет внешнюю электронную конфигурацию  . Элементы группы I (за исключением водорода) и группы II объединяют под названием s-металлы. Элементы групп III-VII и группы О (VIII) (за
. Элементы группы I (за исключением водорода) и группы II объединяют под названием s-металлы. Элементы групп III-VII и группы О (VIII) (за
Таблица 11.7. Электронная конфигурация высшей по энергии подоболочки у элементов различных групп

Таблица 11.8. Электронные конфигурации элементов IV группы

Таблица 11.9. Групповые названия и внешние электронные конфигурации элементов главных подгрупп

исключением гелия) называют p-элементами: s- и p-элементы принято называть непереходными, или элементами главных групп.
На рис. 11.3 указано расположение в периодической таблице d-элементов, иначе называемых переходными элементами (металлами). Они образуют три ряда: первый в 4-м периоде, второй в 5-м периоде и третий в 6-м периоде (см. также гл. 14). f-Элементы, называемые также внутренними переходными элементами (металлами), образуют в периодической таблице два ряда. Первый ряд - лантаноиды, или редкоземельные элементы (металлы), находятся в 6-м периоде, а второй ряд - актиноиды - в 7-м периоде. Отметим, что в варианте периодической таблицы, показанном на рис. 11.3, вертикальные столбцы, содержащие d- и f-элементы, не имеют номеров групп.
Металлы, неметаллы и металлоиды
Все элементы периодической системы можно подразделить, с учетом различий в их электропроводности, на металлы, неметаллы и металлоиды (полуметаллы).
Металлы хорошо проводят электрический ток. Их проводимость медленно уменьшается по мере повышения температуры. Все s-, d- и f-элементы, за исключением водорода и гелия, являются металлами. s-Металлы наиболее реакционноспособны из всех металлов, в связи с чем их иногда называют активными металлами. Элементы, расположенные в левой нижней части p-блока периодической таблицы, тоже представляют собой металлы (рис. 11.4). Они обладают невысокой реакционной способностью и обнаруживают некоторые свойства неметаллов.
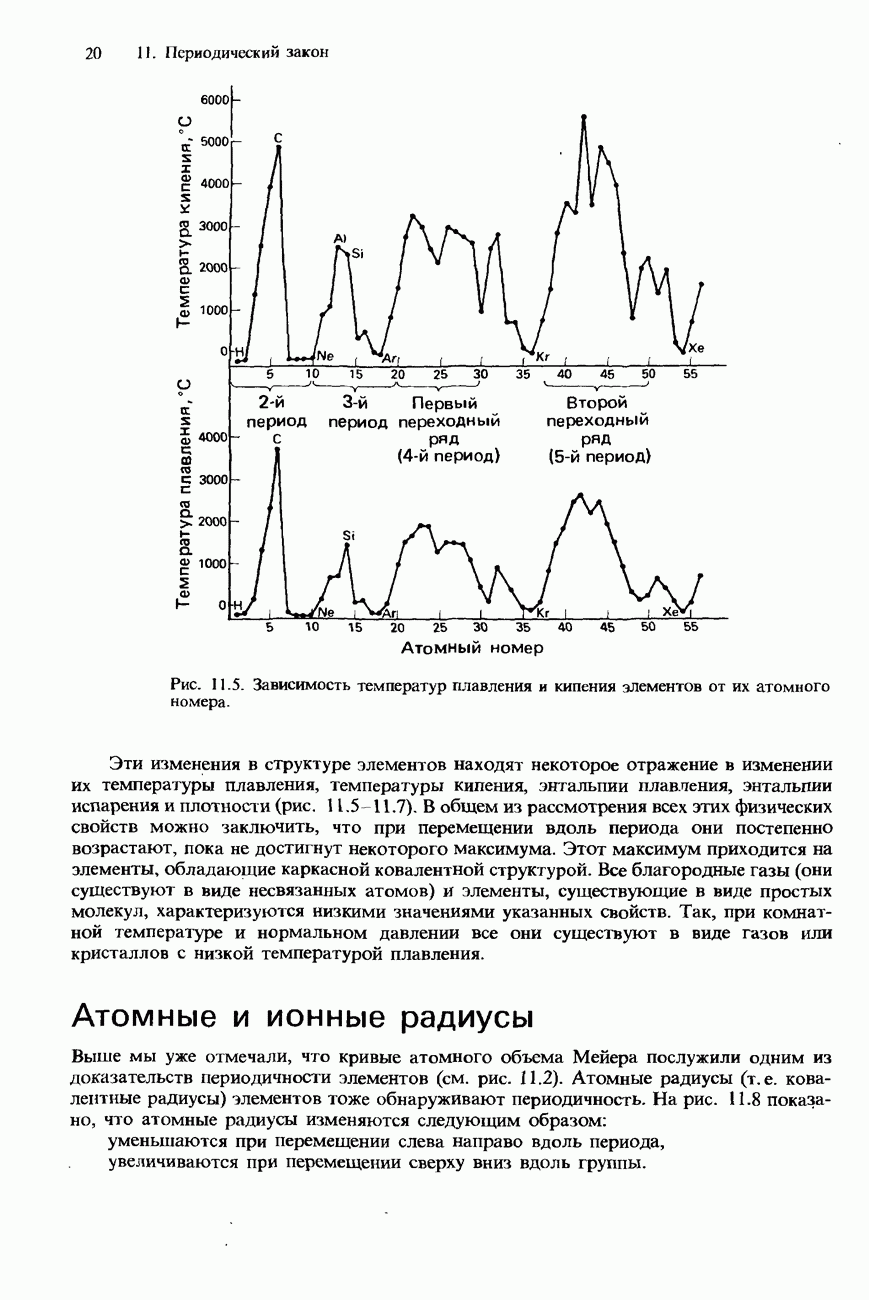
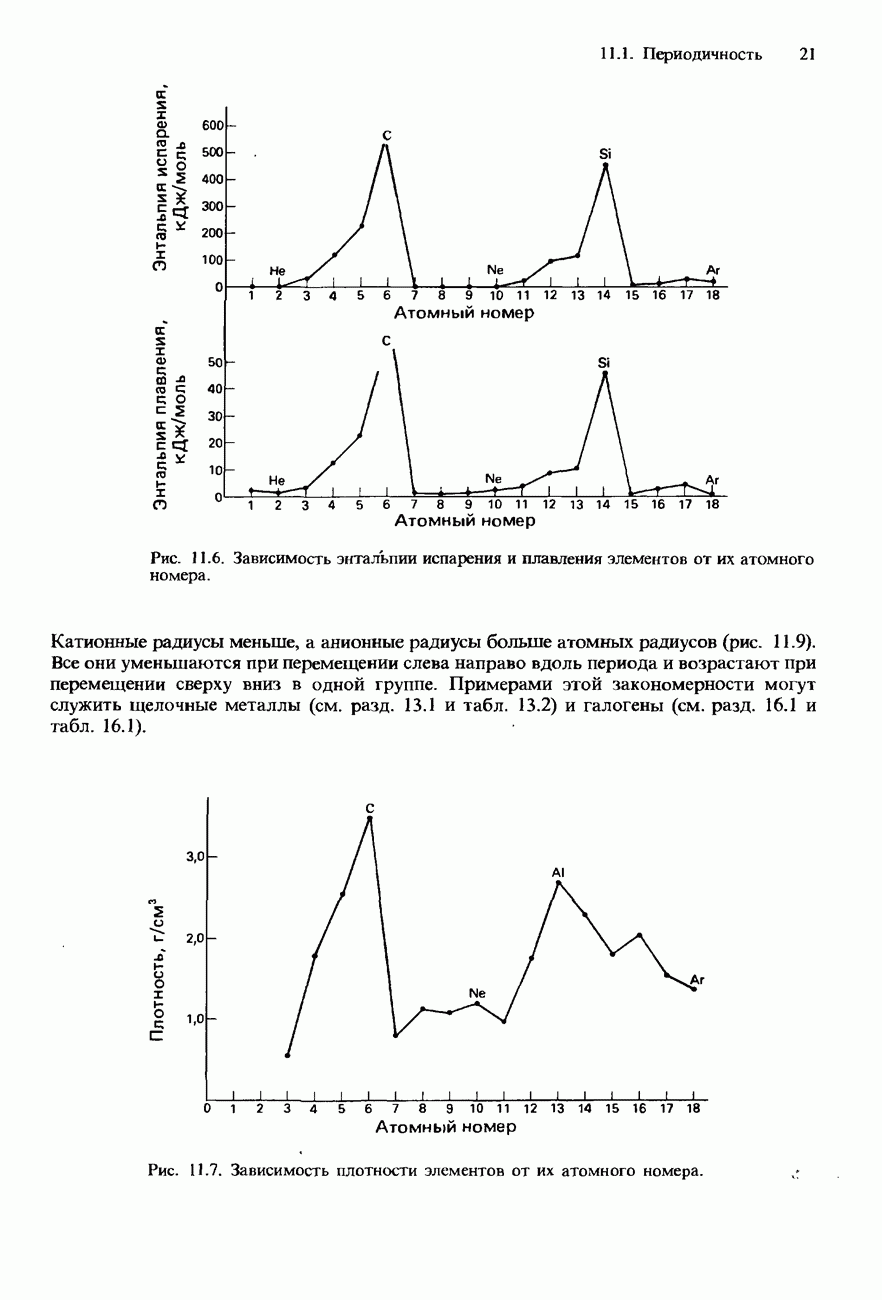
Все неметаллы являются диэлектриками (изоляторами); исключение составляет лишь углерод в форме графита. Они располагаются в верхней правой части периодической таблицы.
Металлоиды характеризуются низкой электропроводностью, которая возрастает при повышении температуры. Металлоиды называют также полуметаллами или полупроводниками. Они расположены вдоль диагональной полосы, идущей от верхнего левого угла p-блока периодической таблицы к его нижнему правому углу (рис. 11.4).

Рис. 11.4. р-Элементы.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
- ПЕРИОДИЧНОСТЬ
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
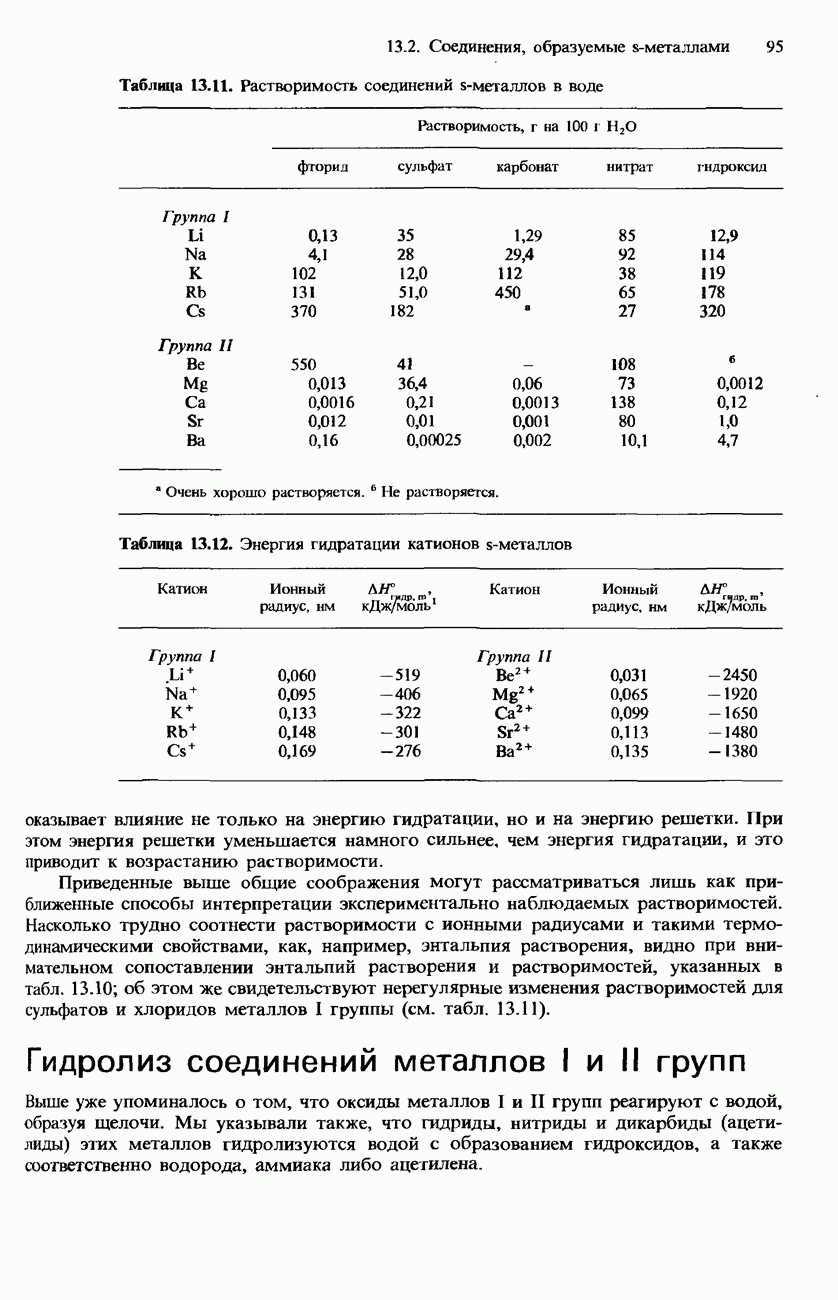
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
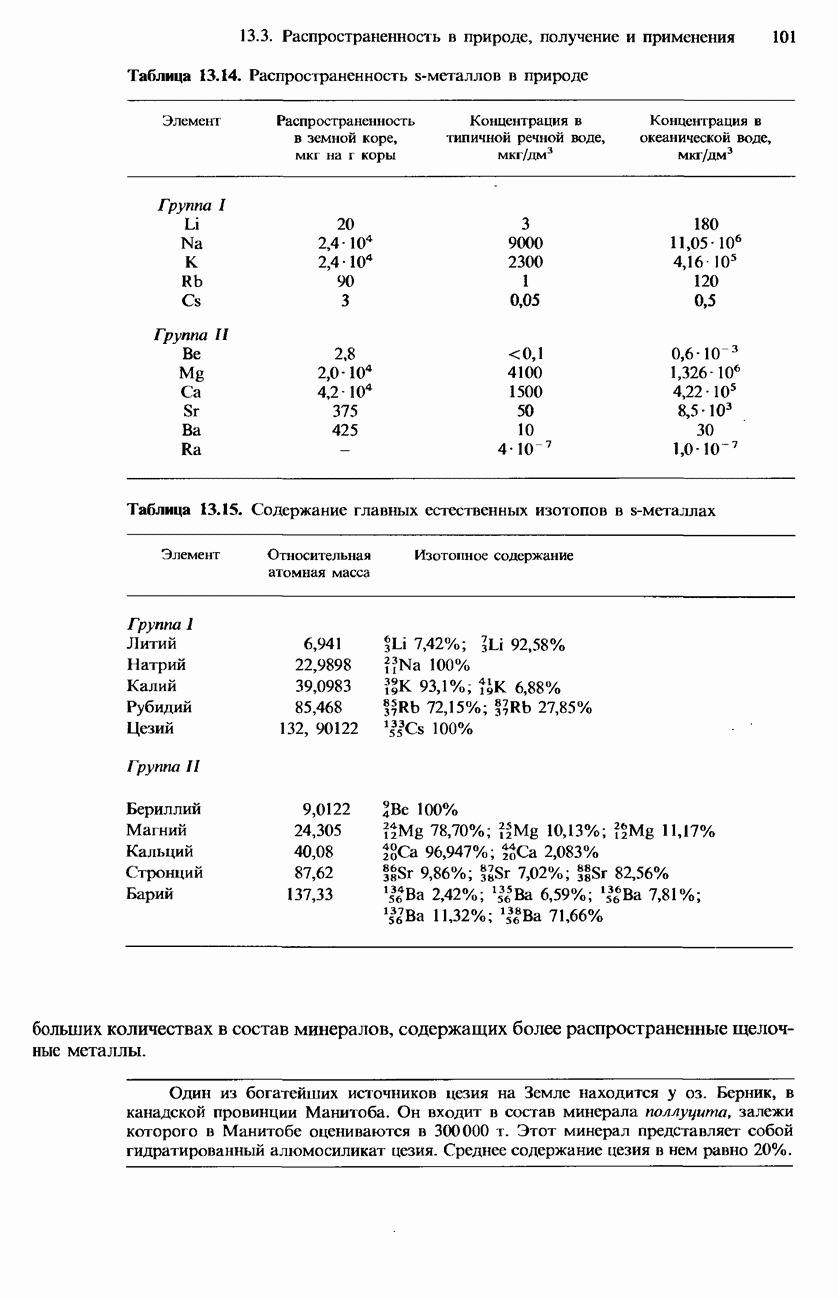
- 13.3. Распространенность в природе, получение и применение
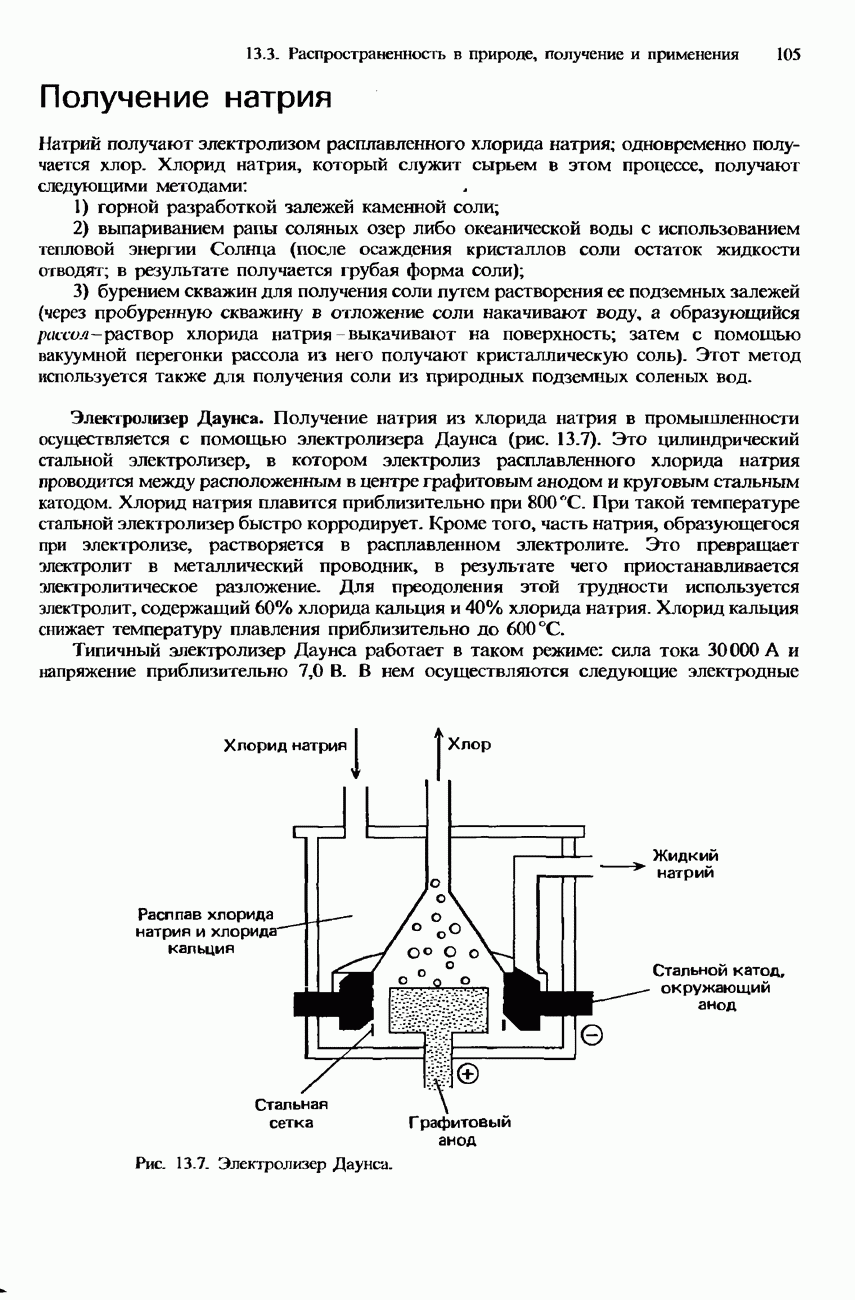
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
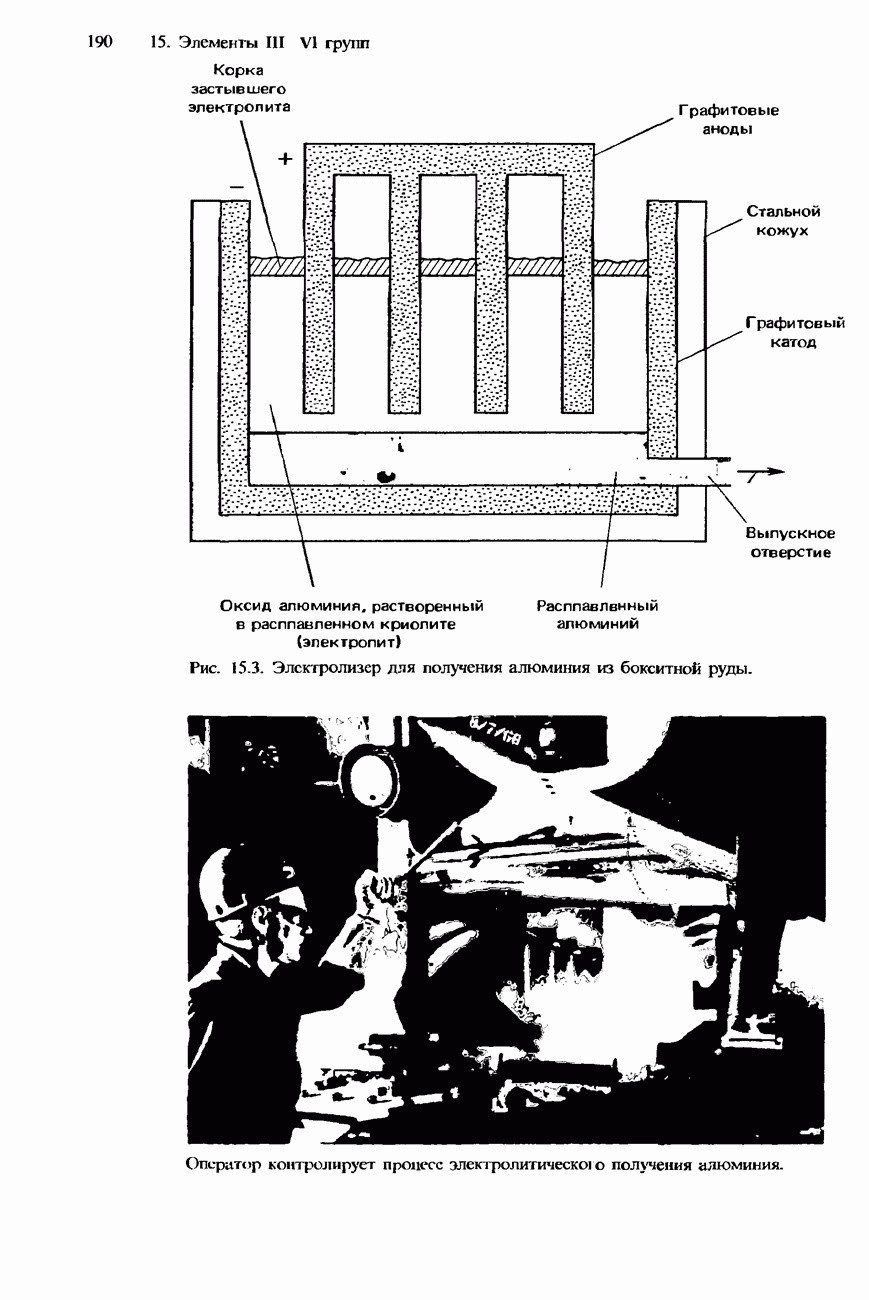
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
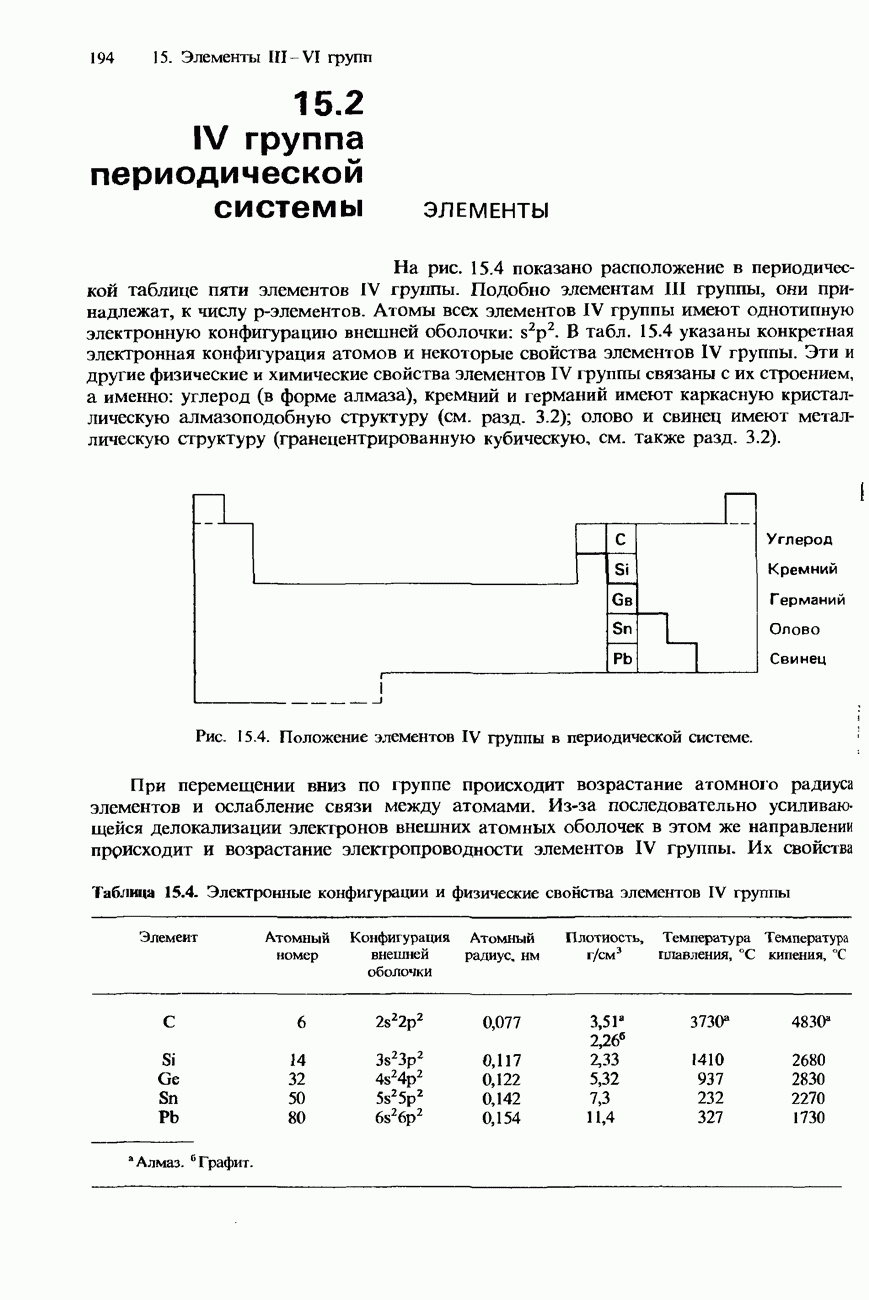
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
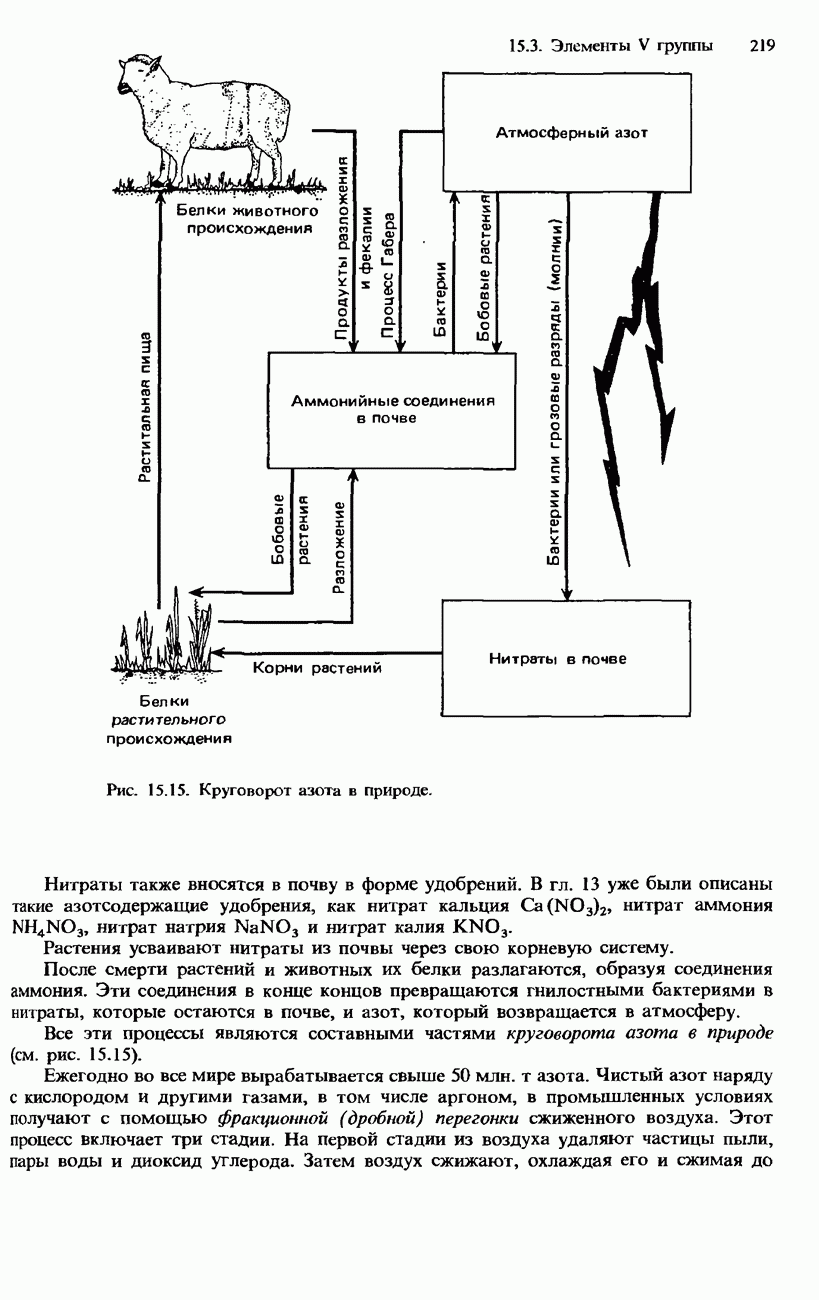
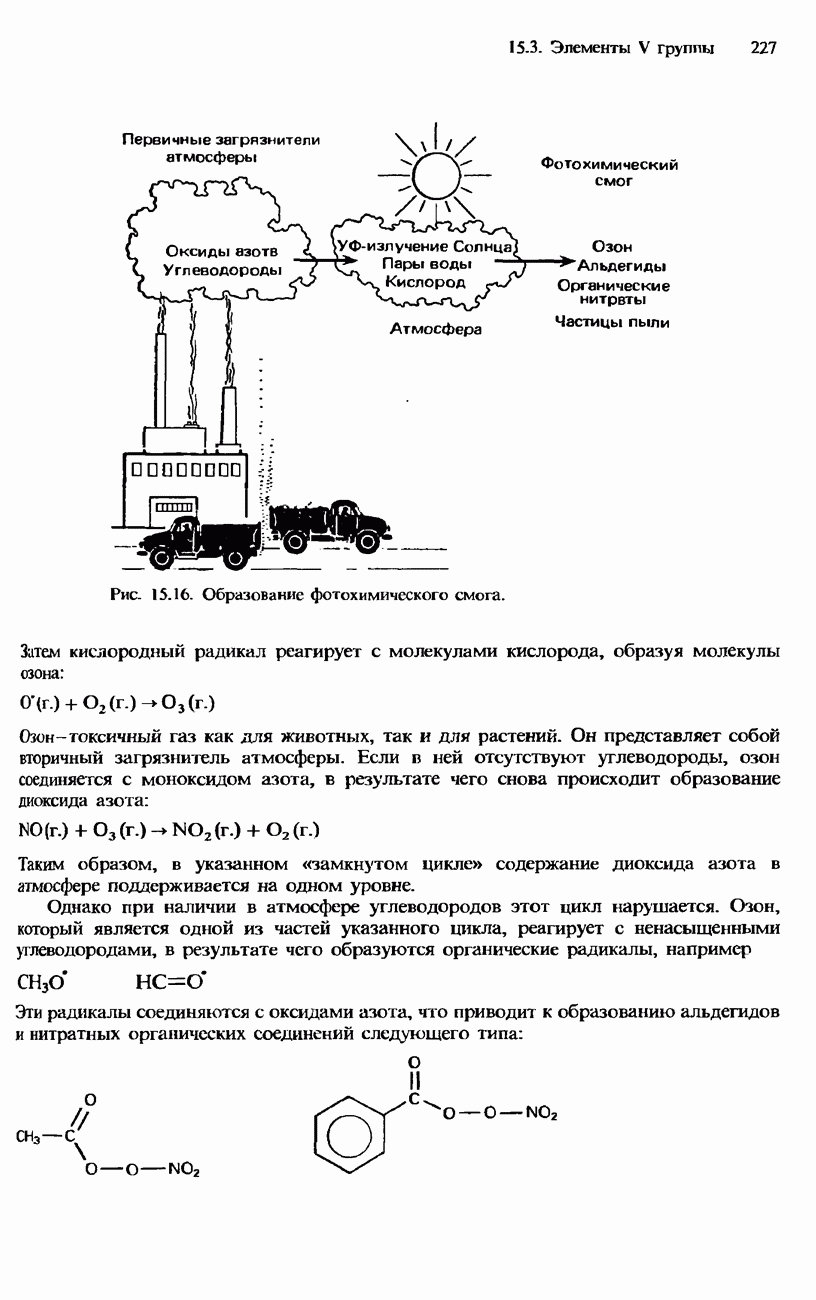
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
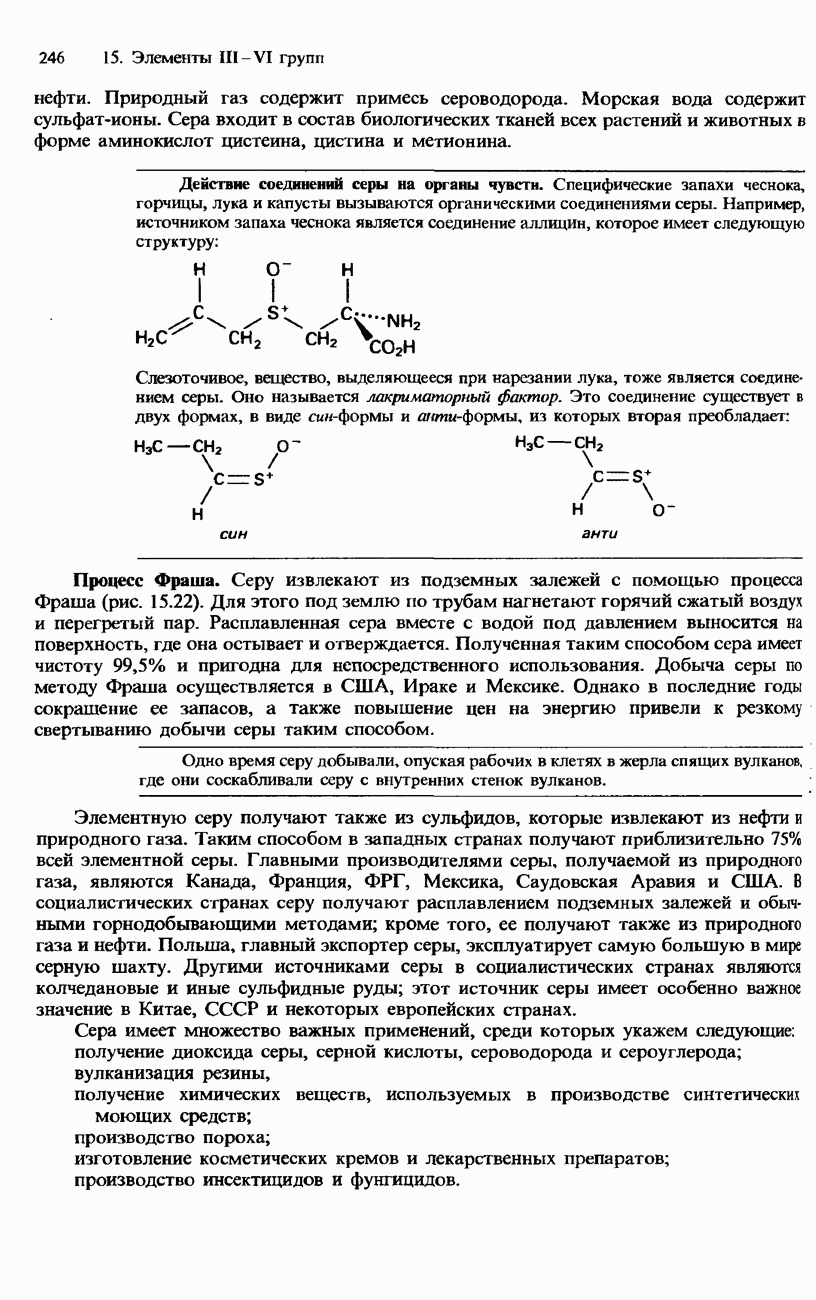
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
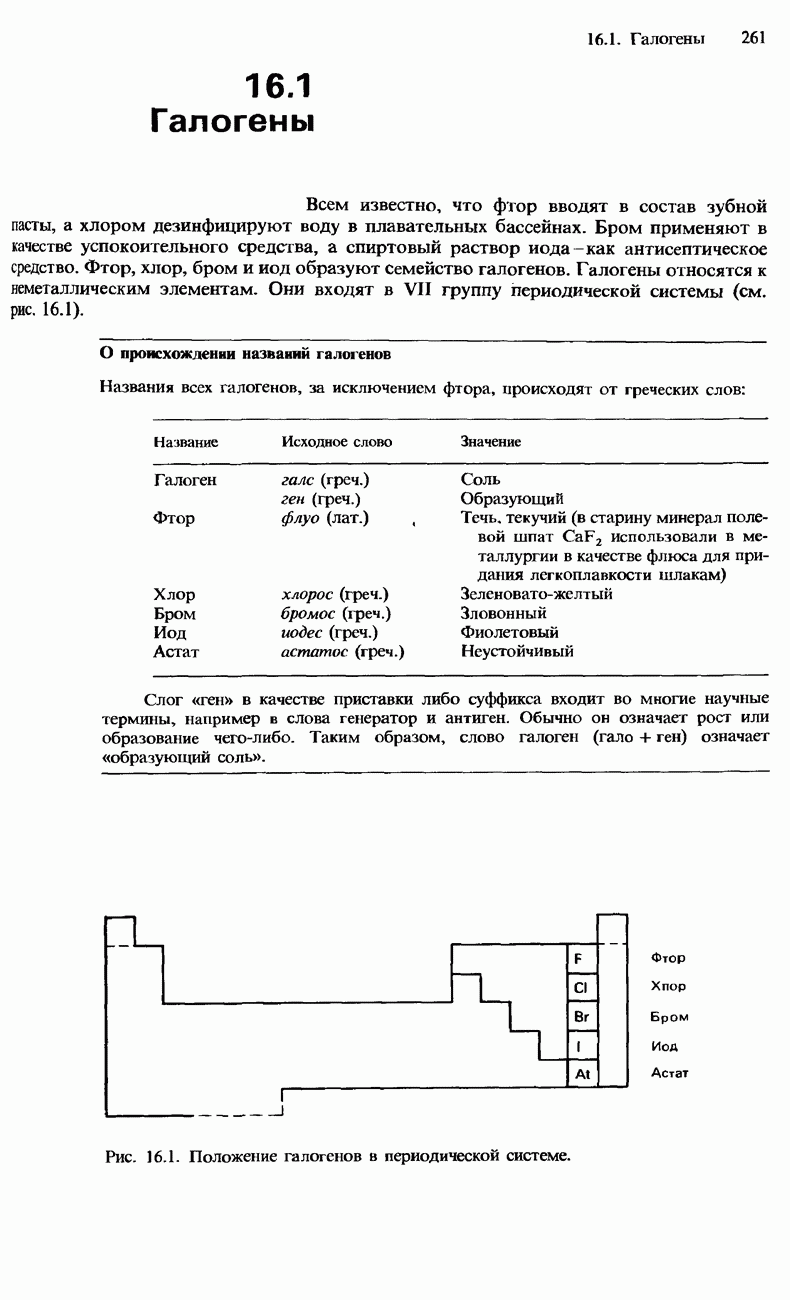
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
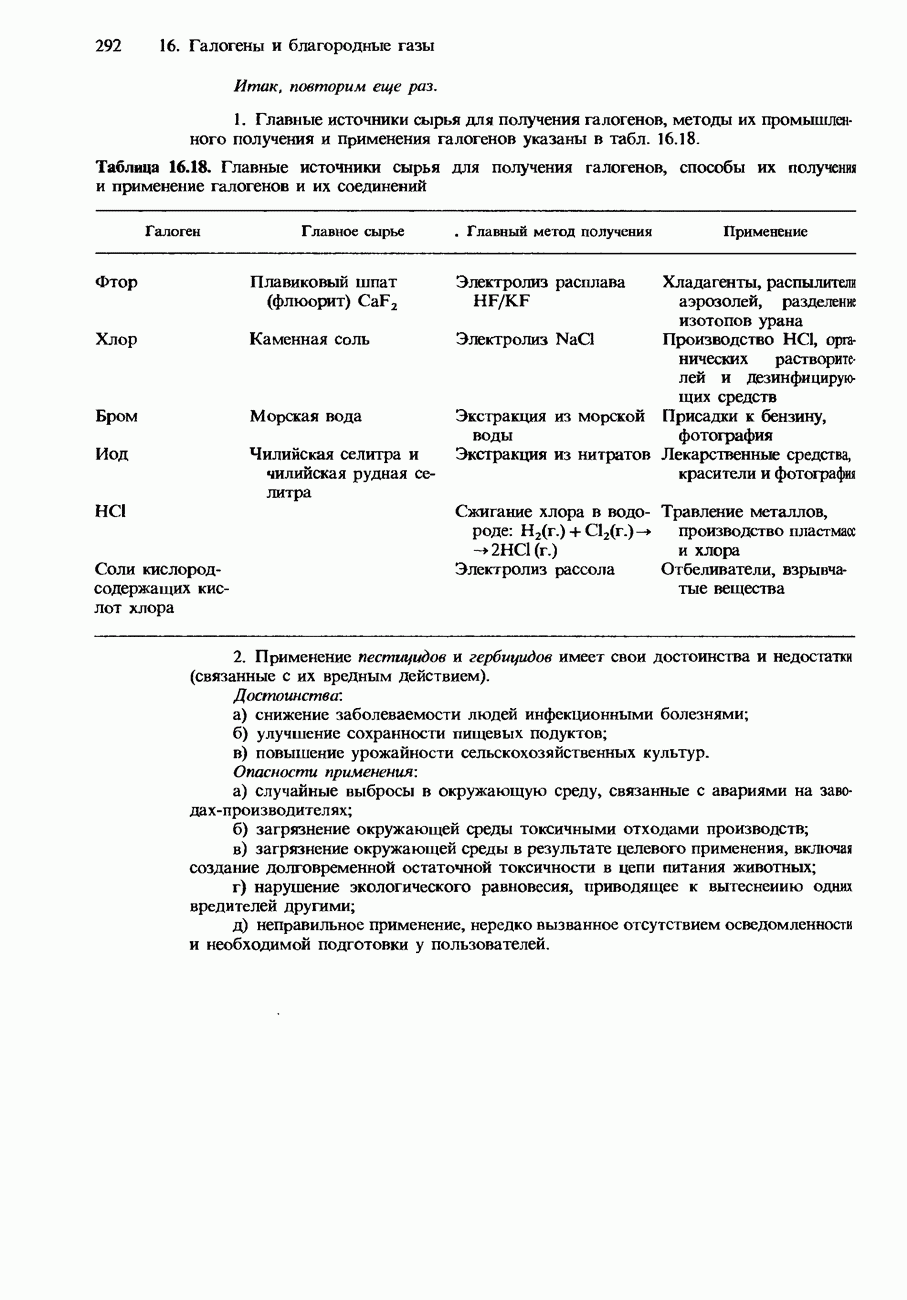
- 16.3. Распространенность, получение и применение галогенов и их соединений
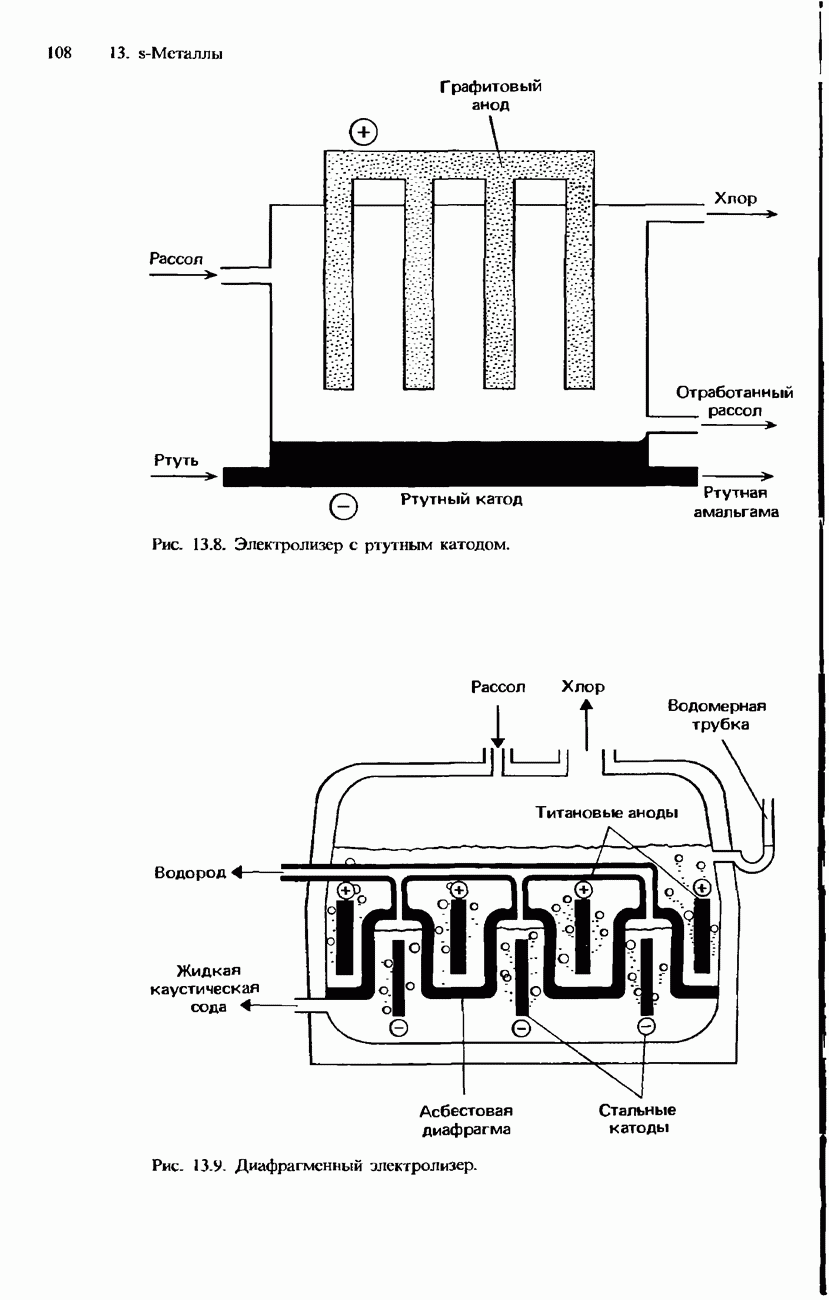
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
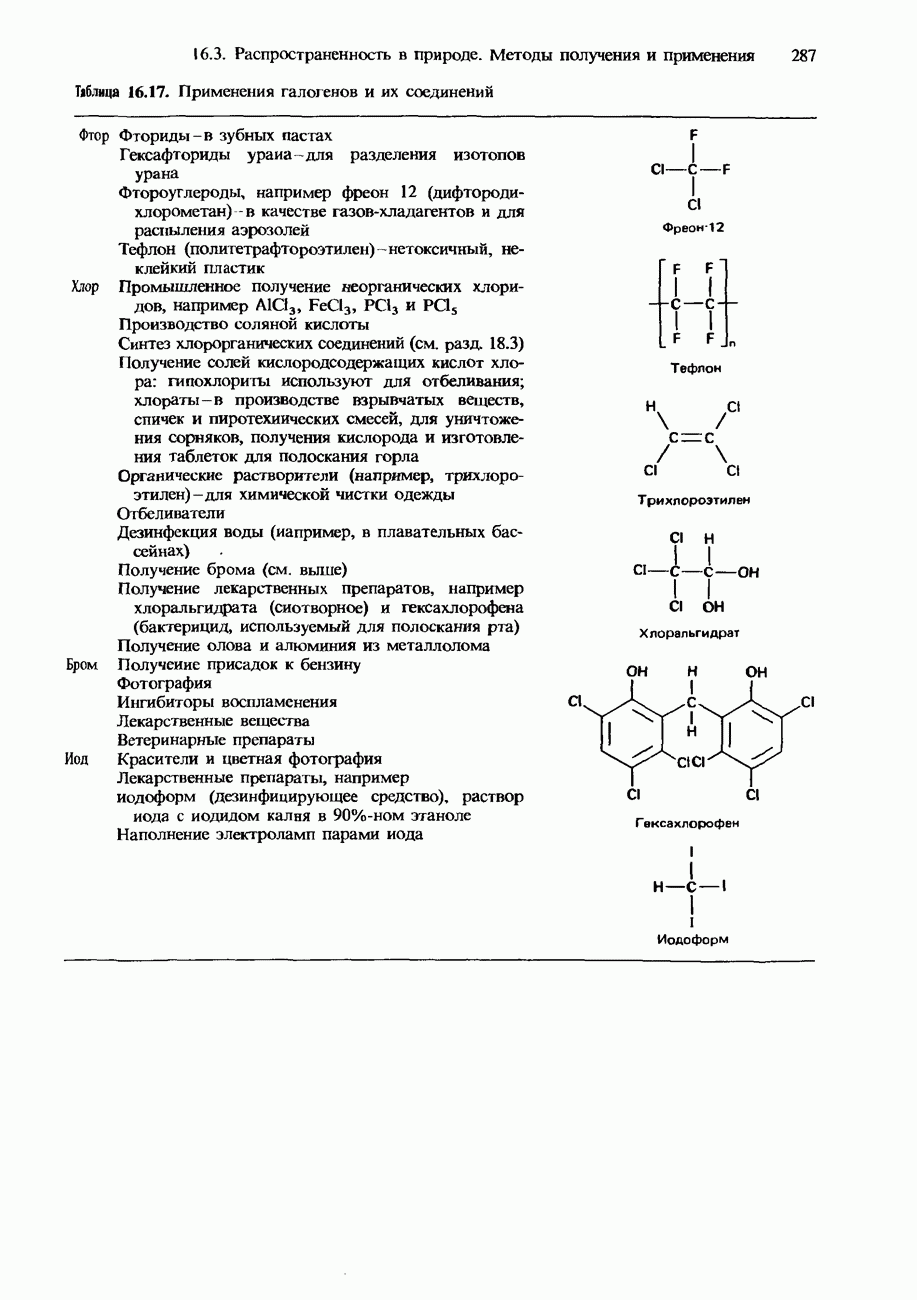
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
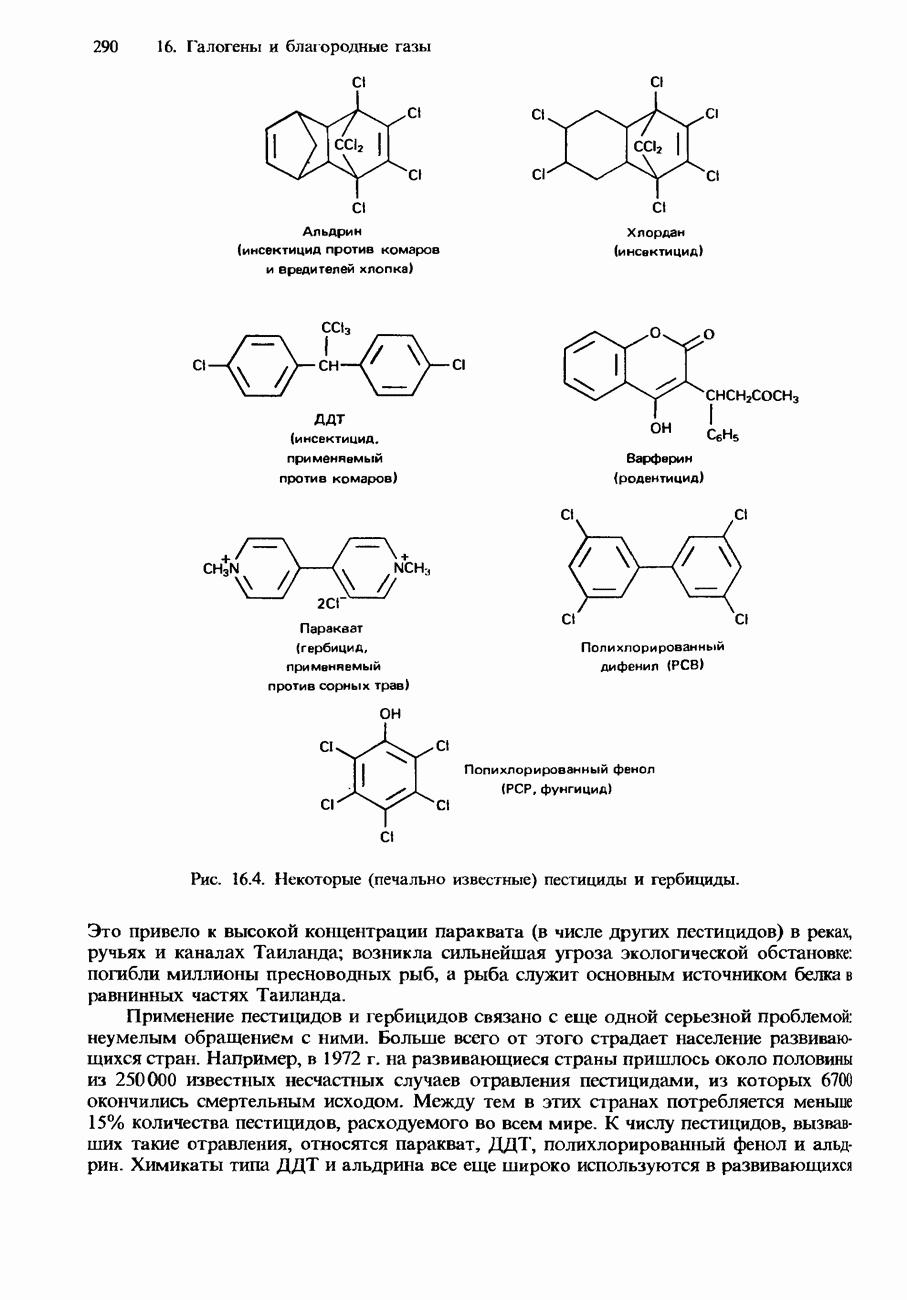
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
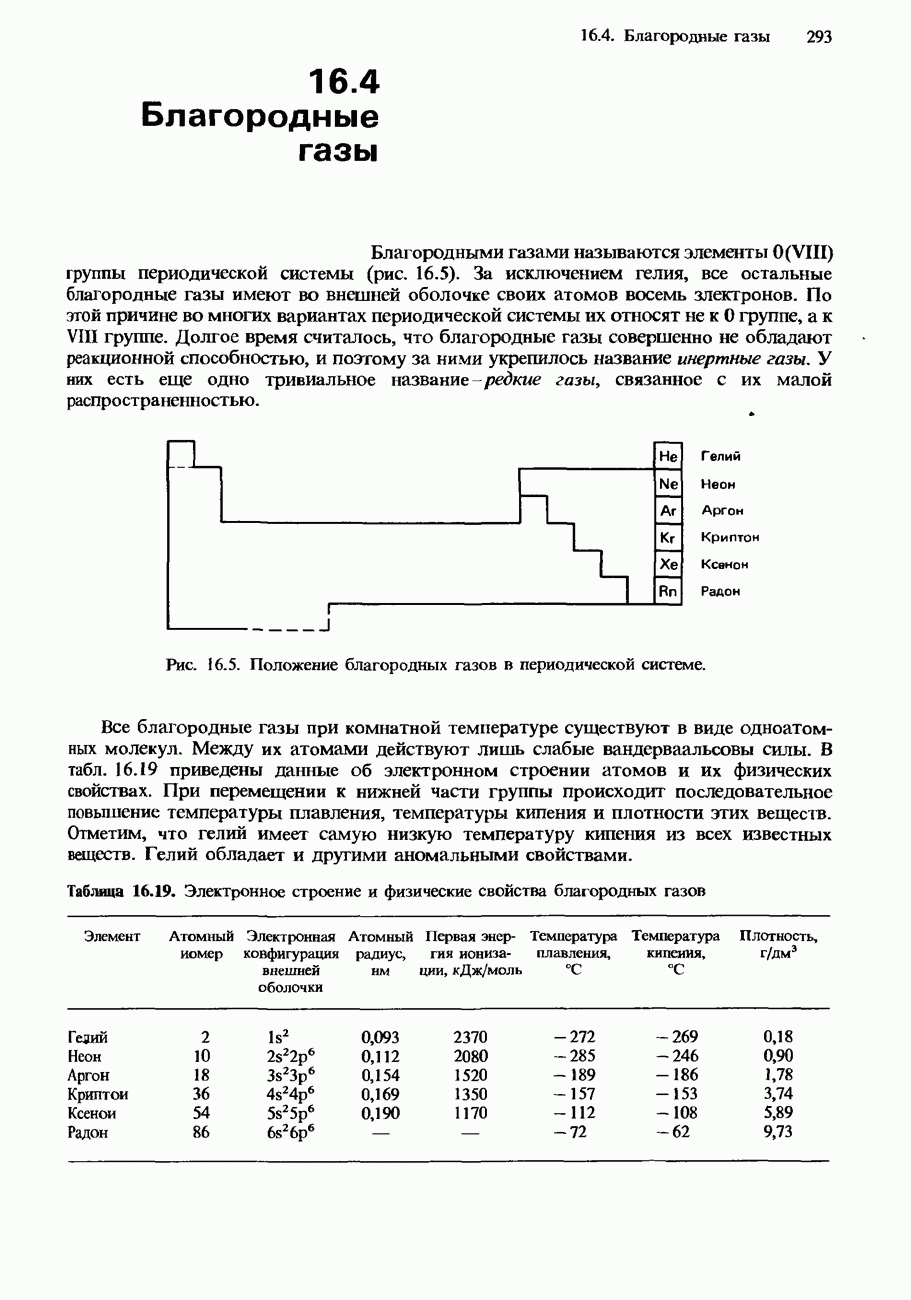
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- УГЛЕВОДОРОДЫ
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
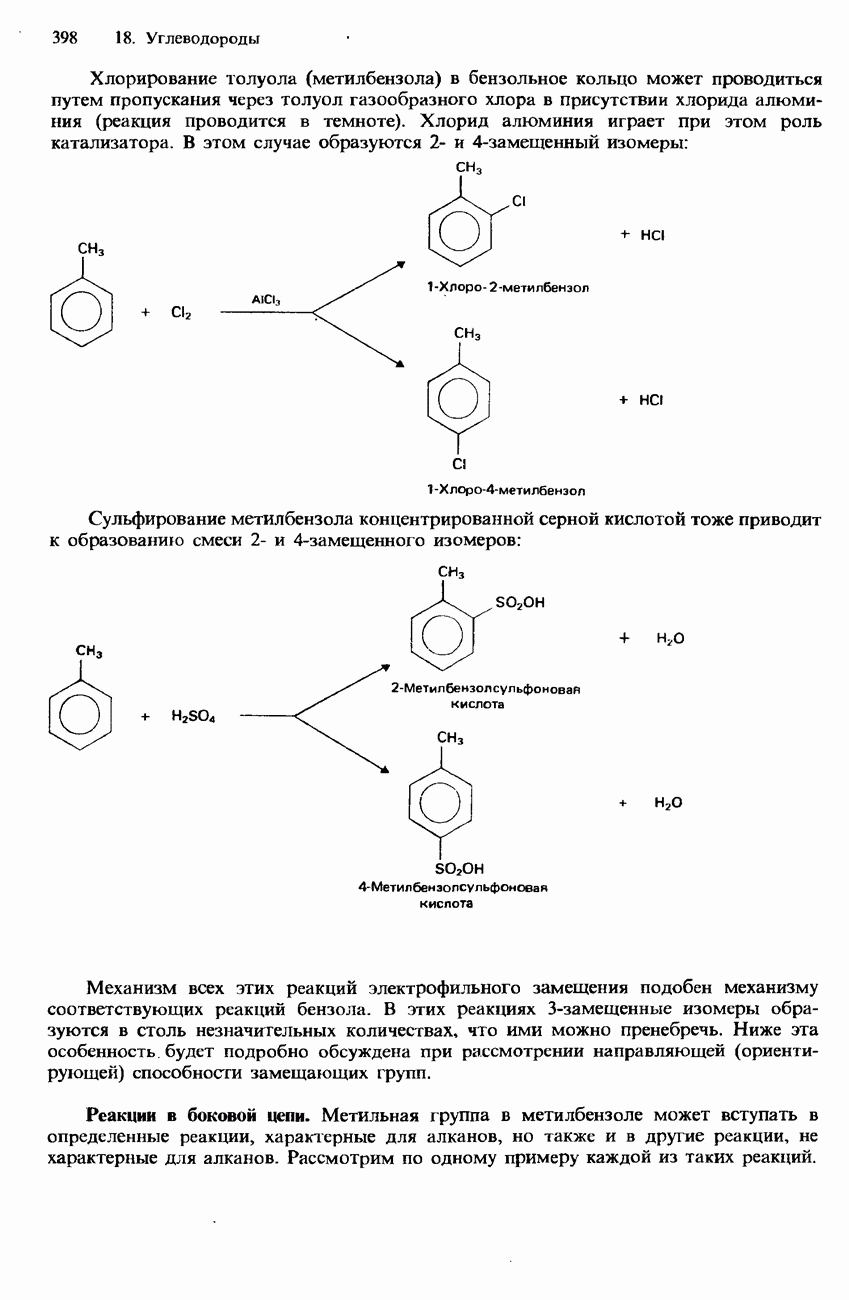
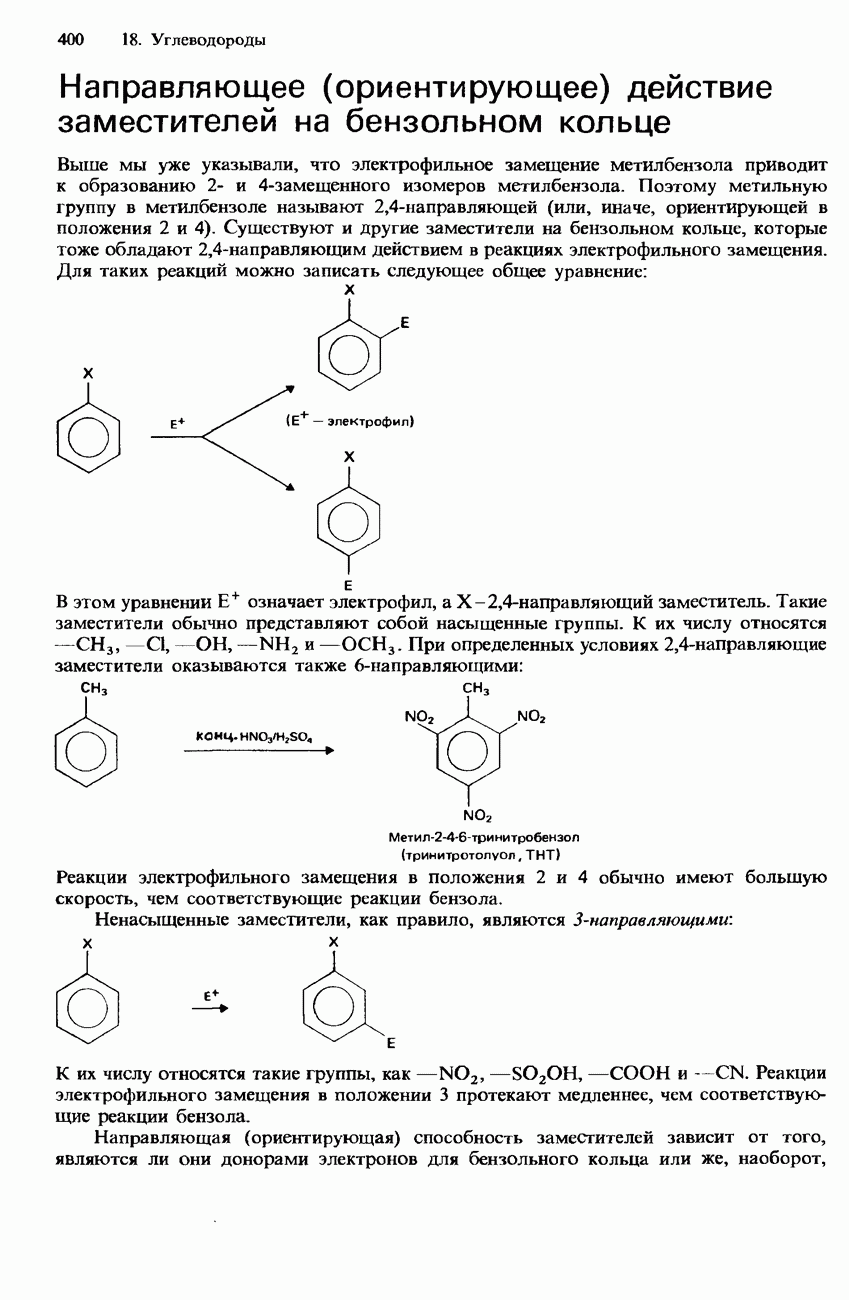
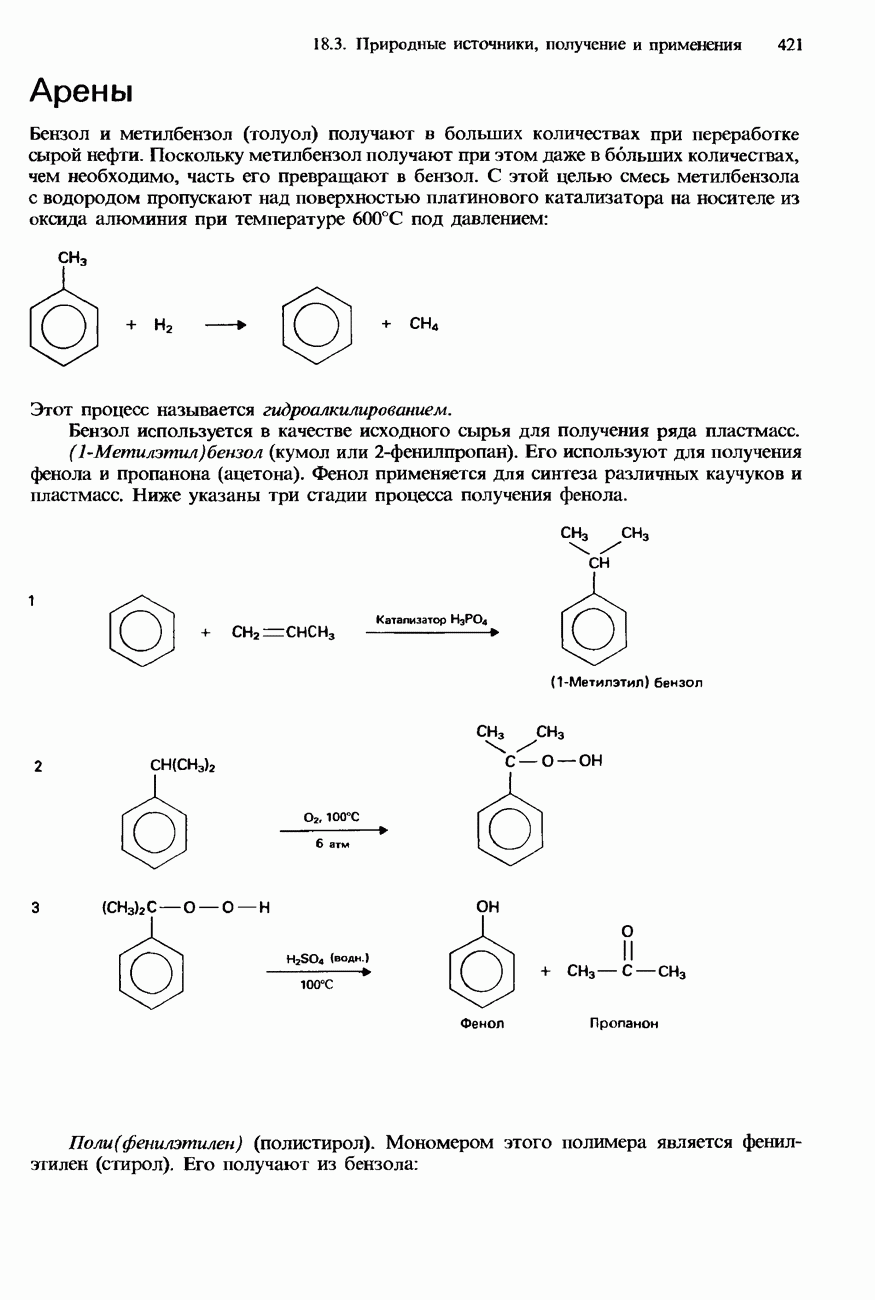
- 18.2. Арены
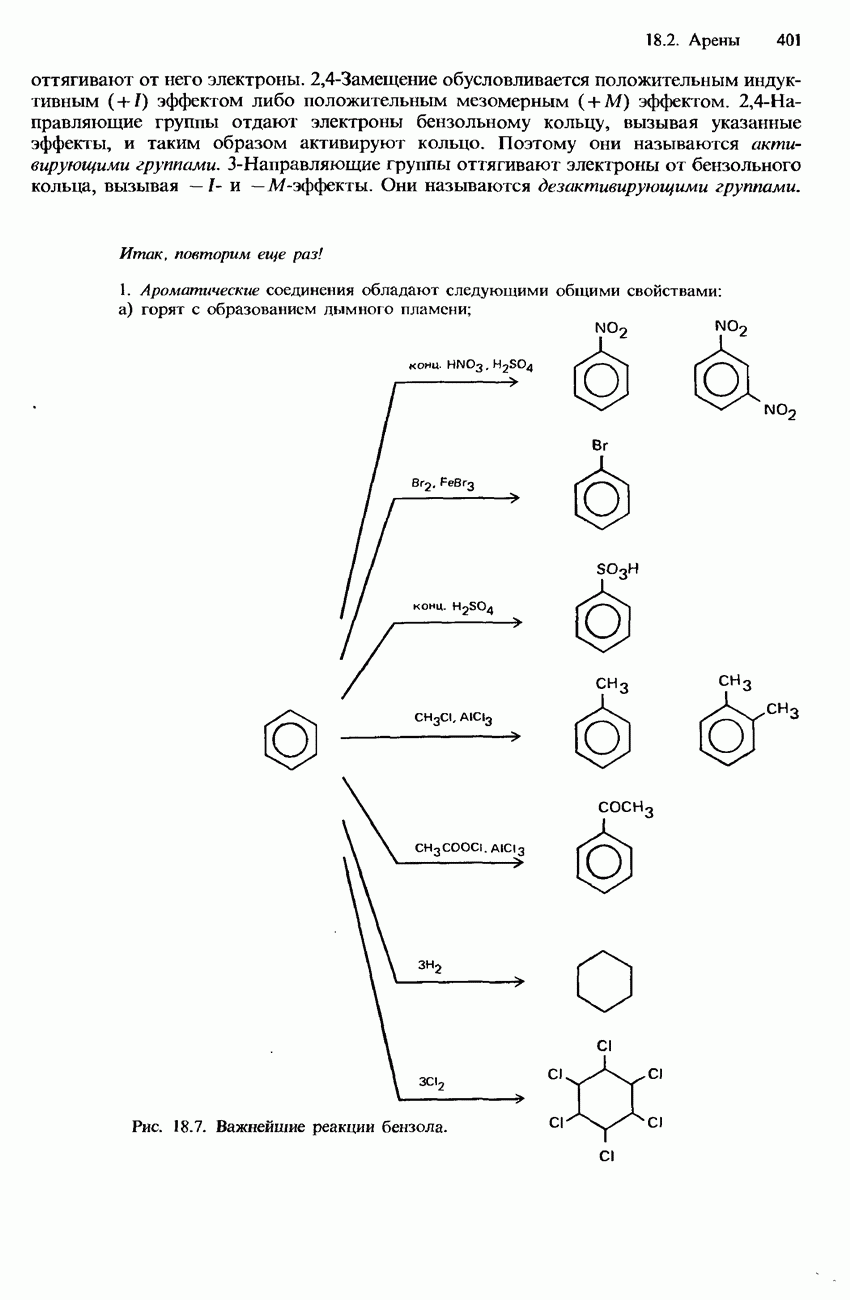
- БЕНЗОЛ
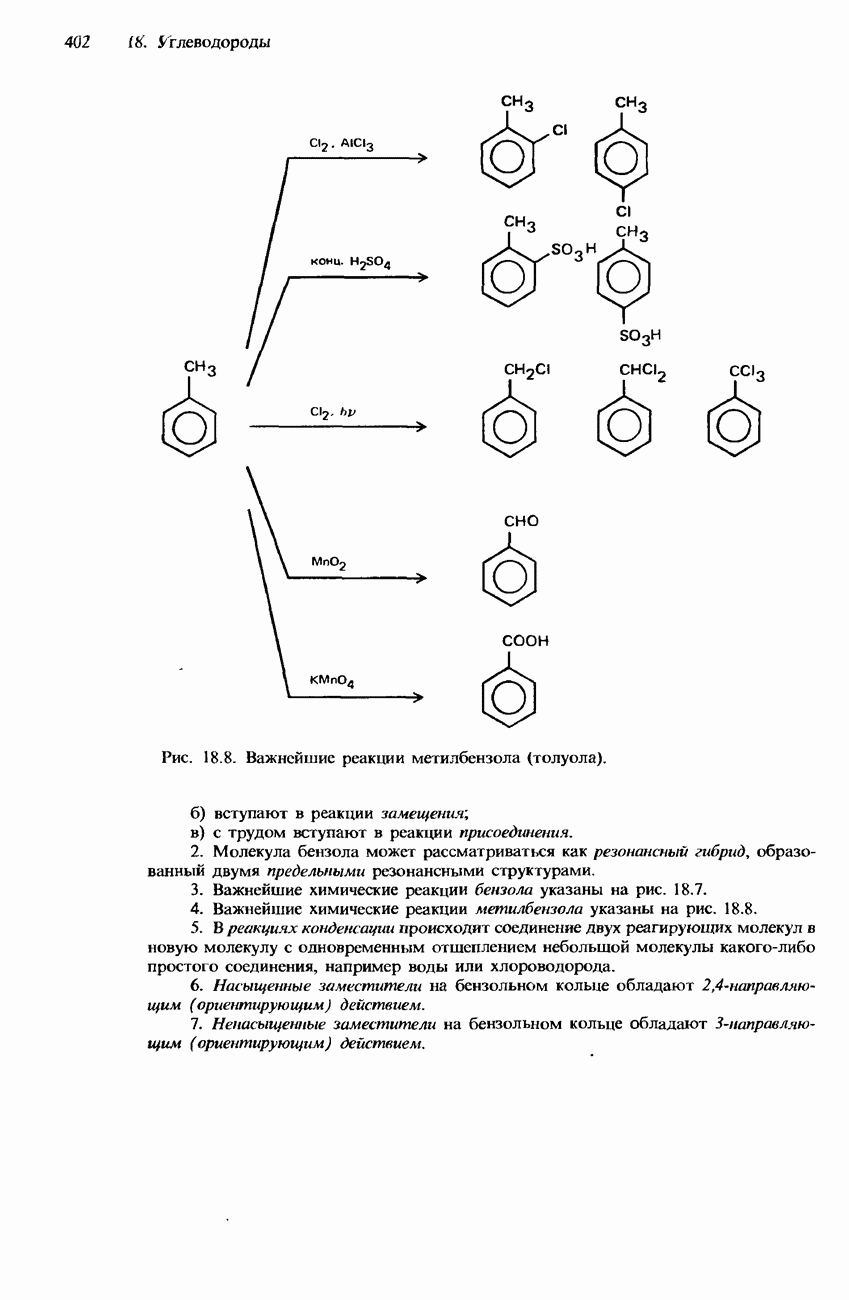
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
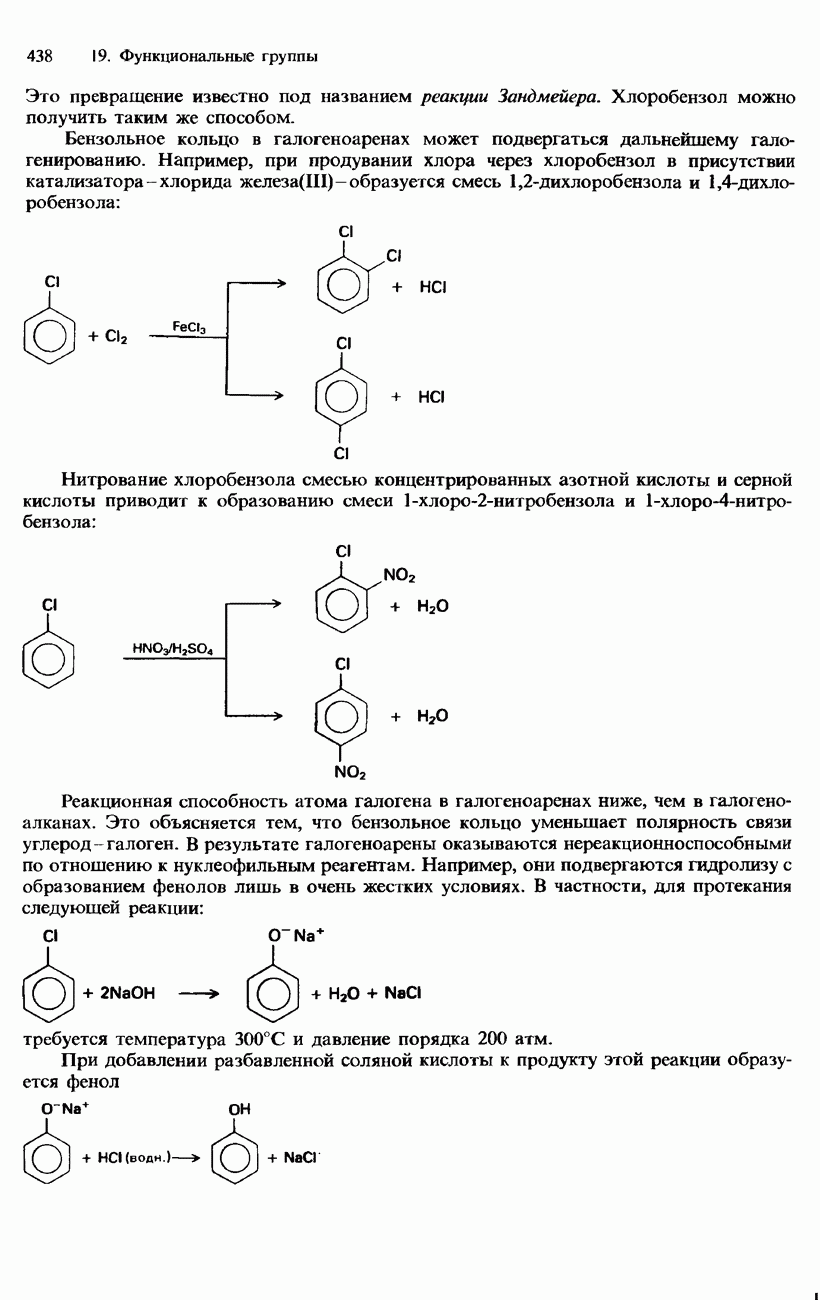
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
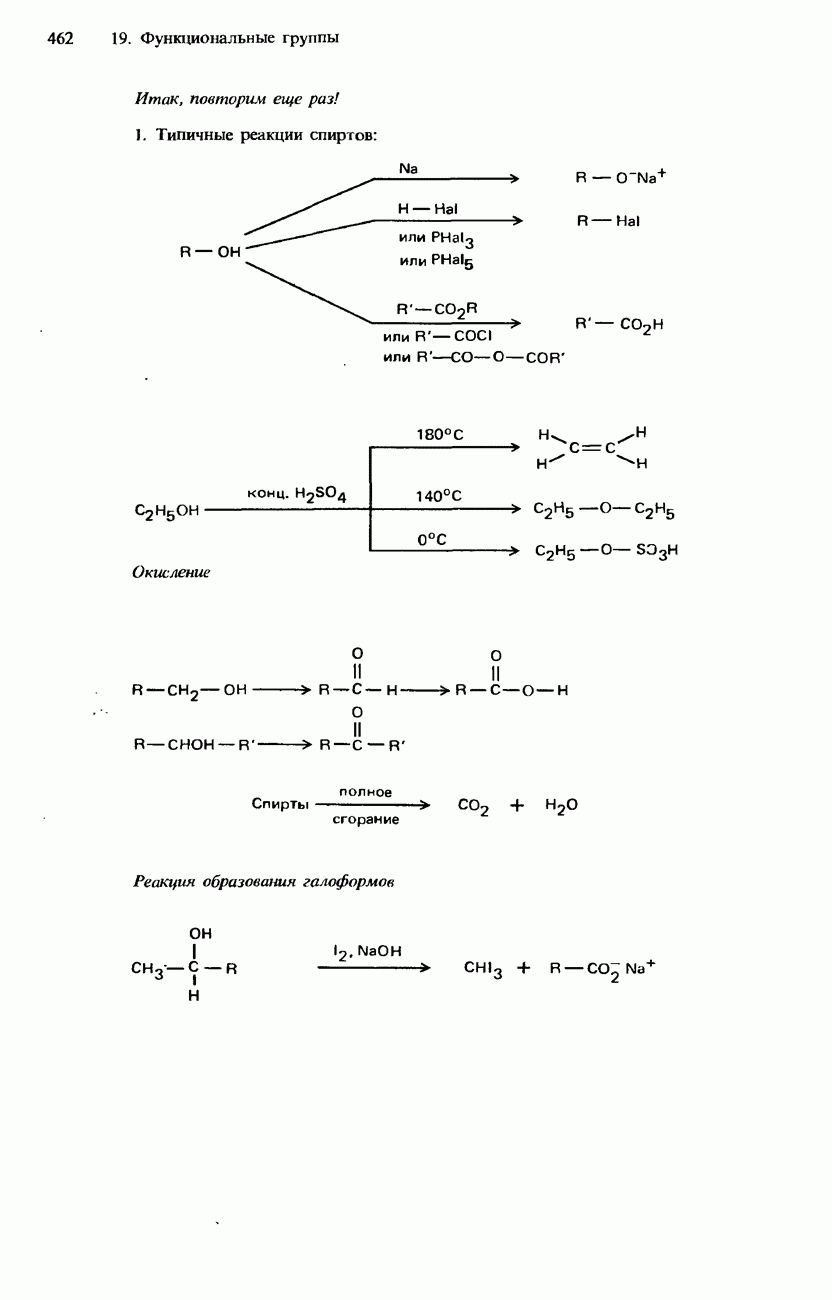
- 19.2. Спирты, фенолы и эфиры
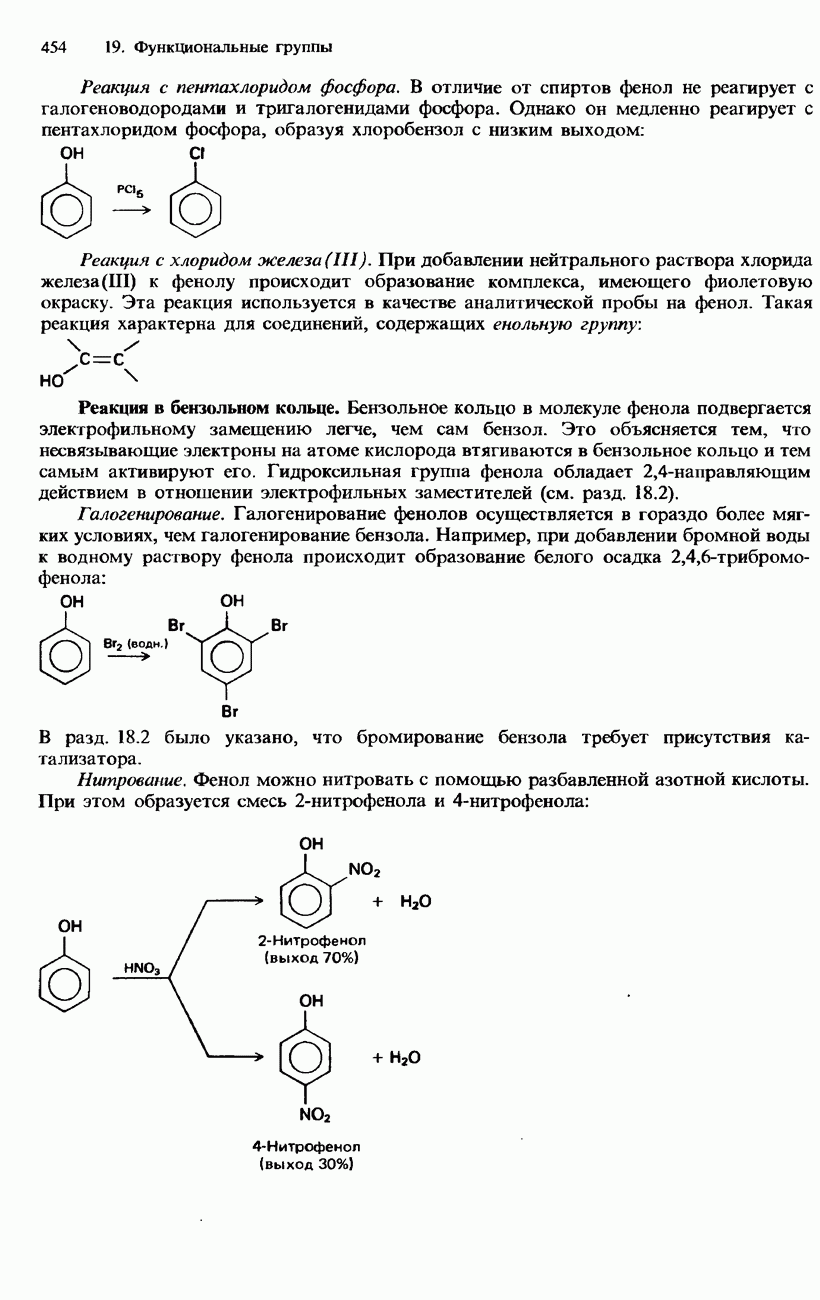
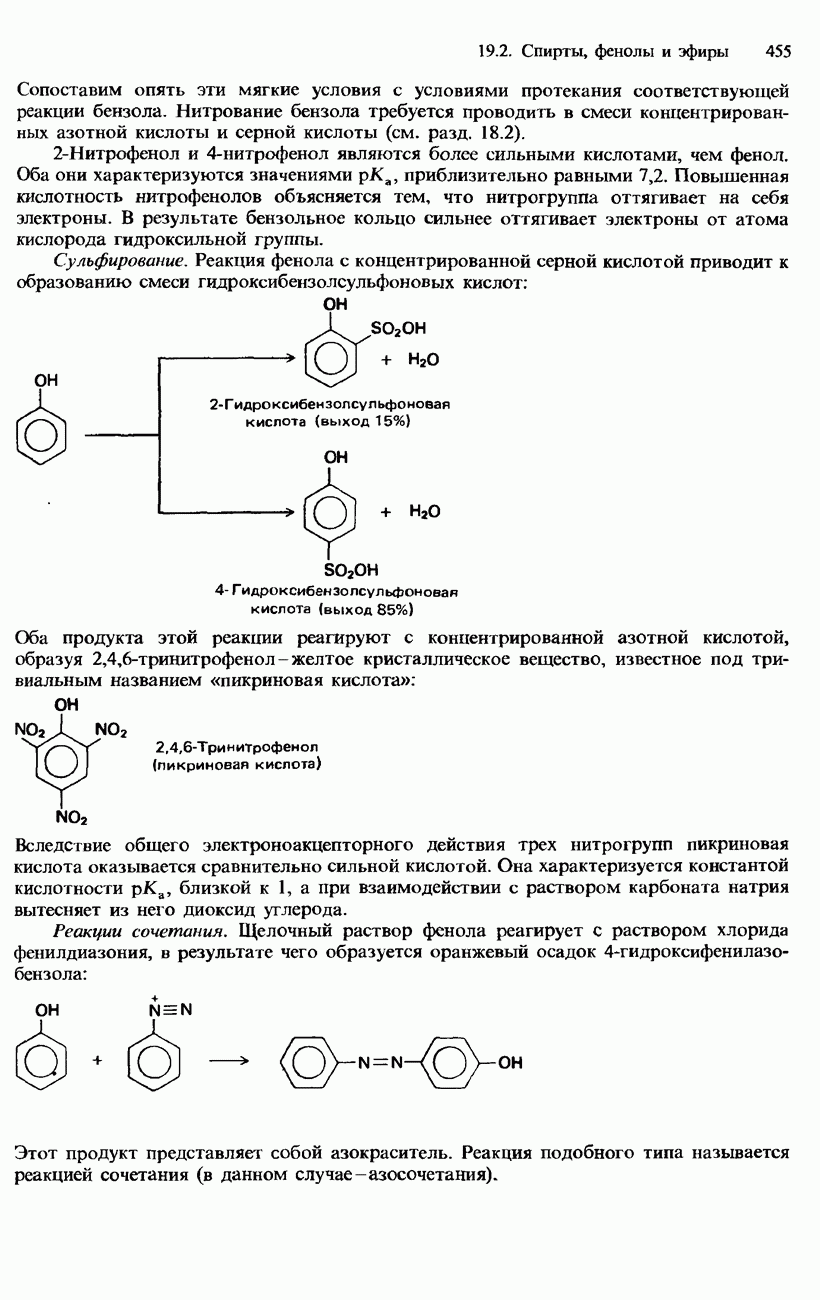
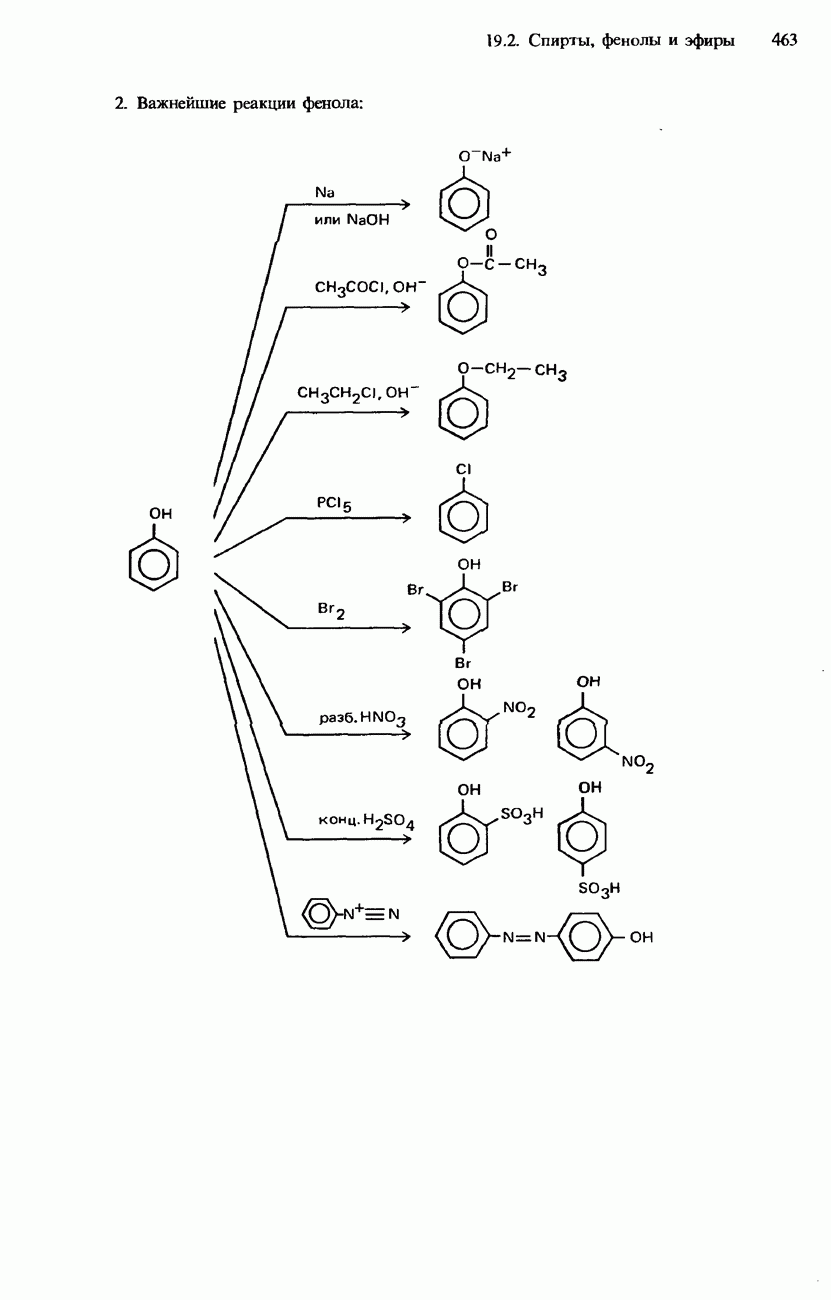
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
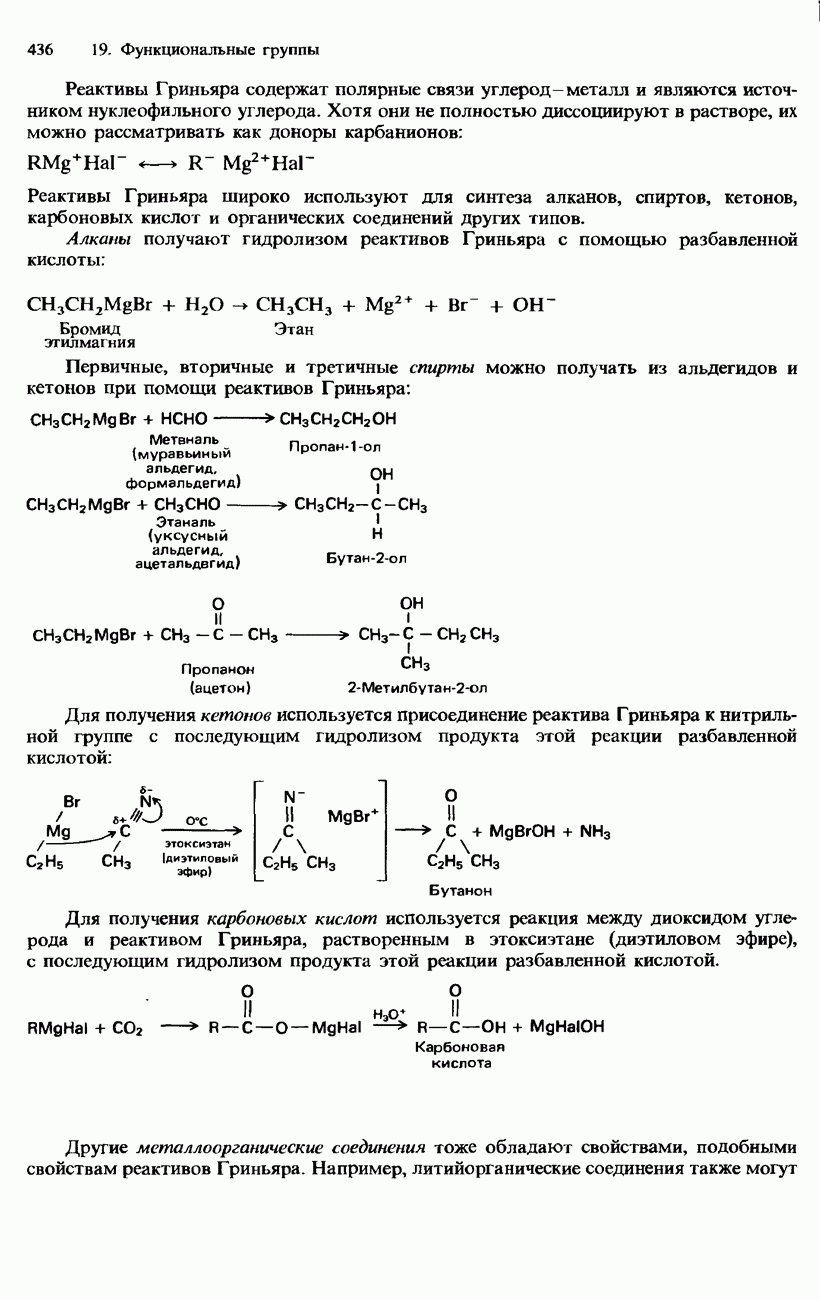
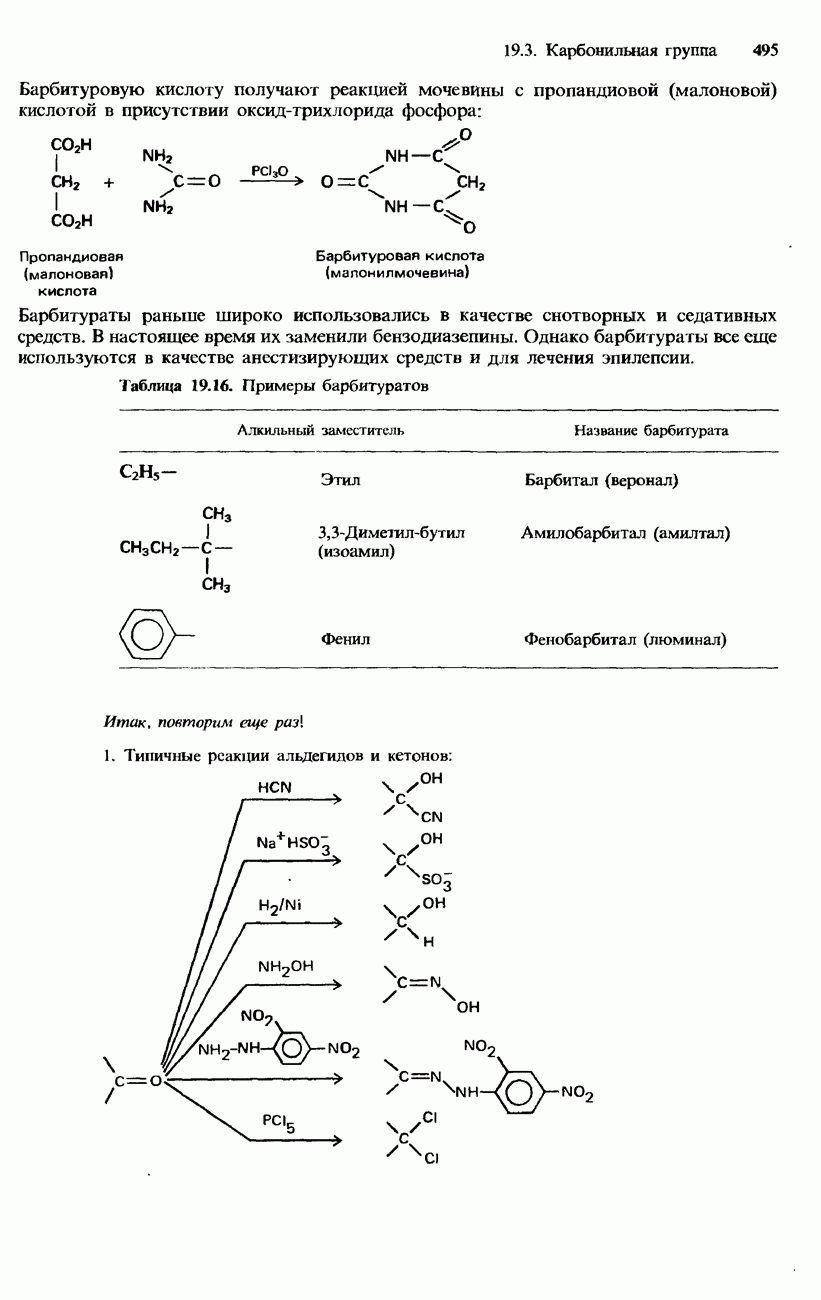
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
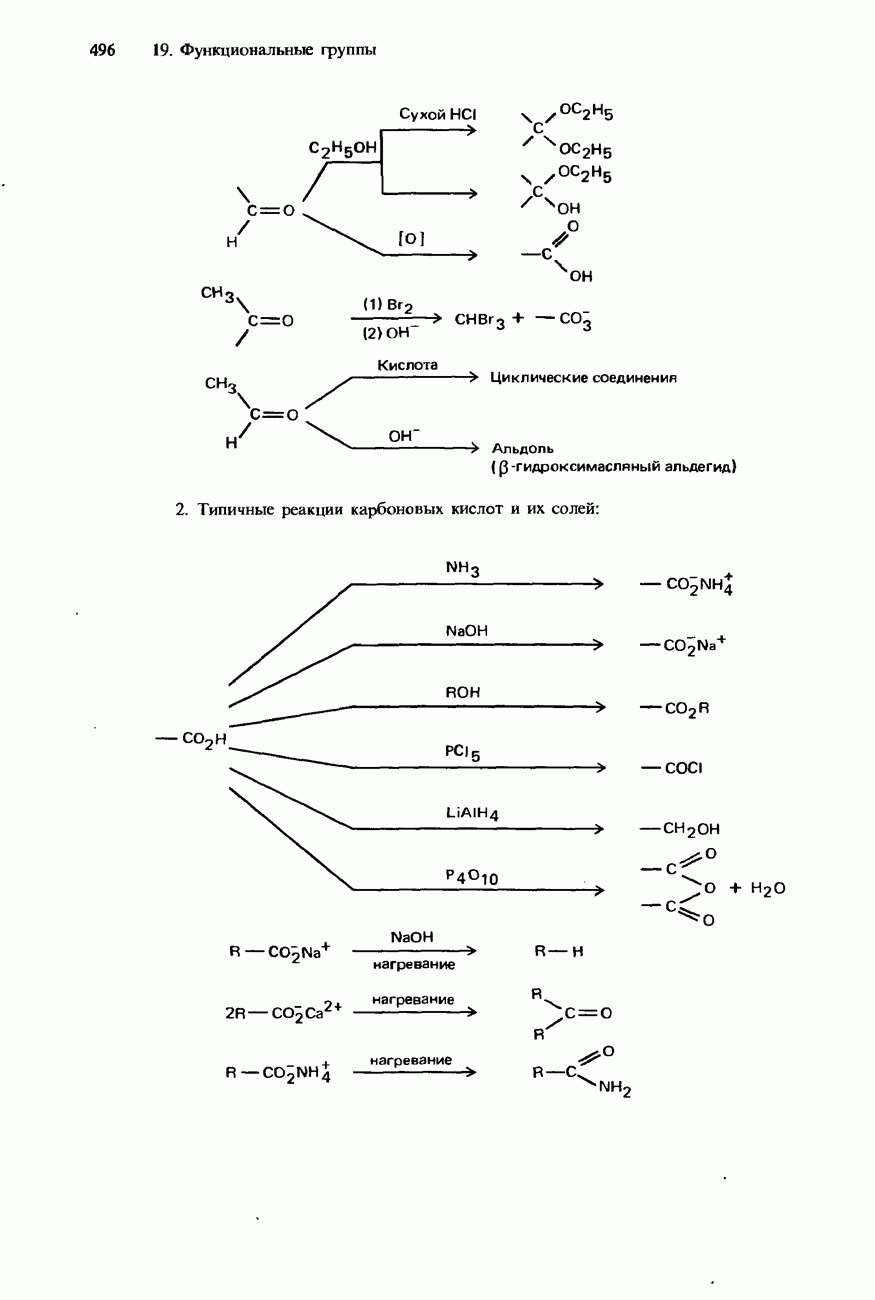
- КАРБОНОВЫЕ КИСЛОТЫ
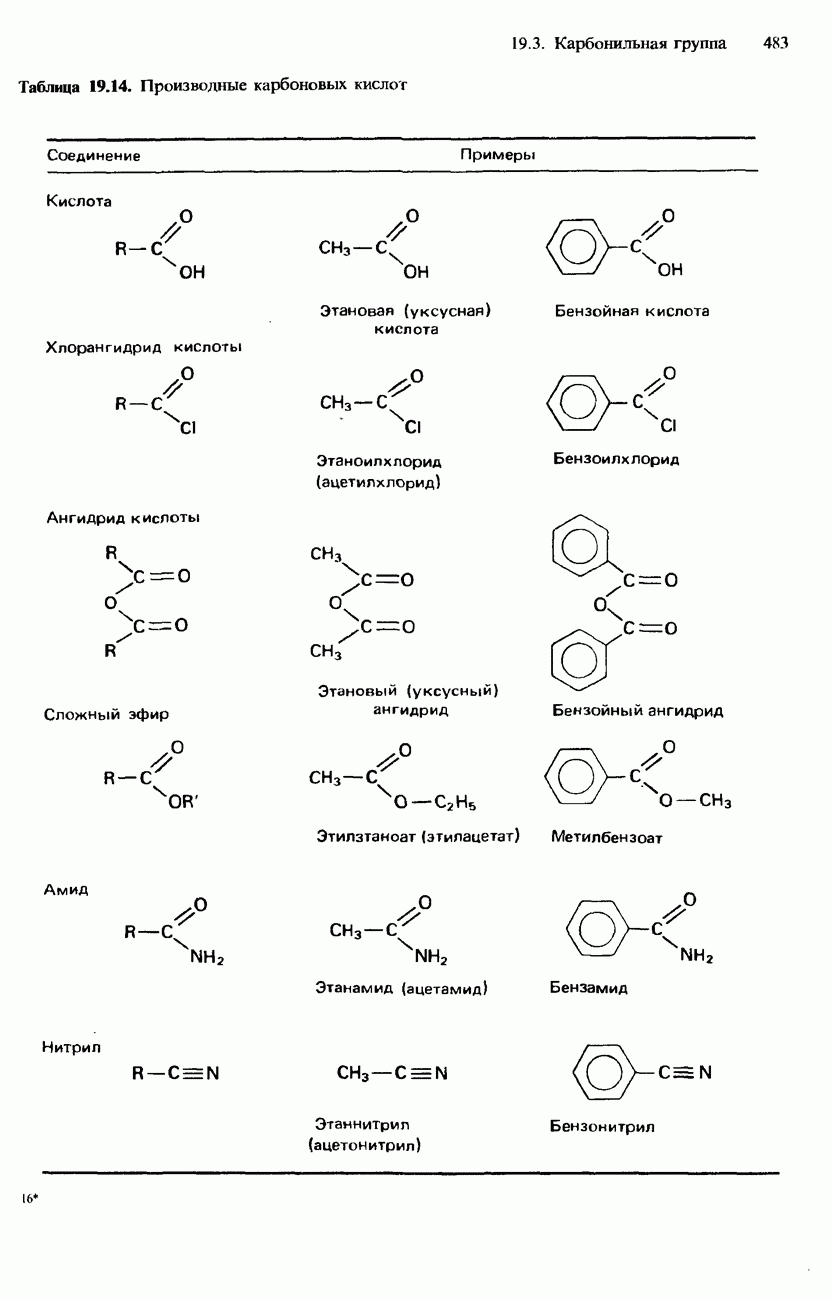
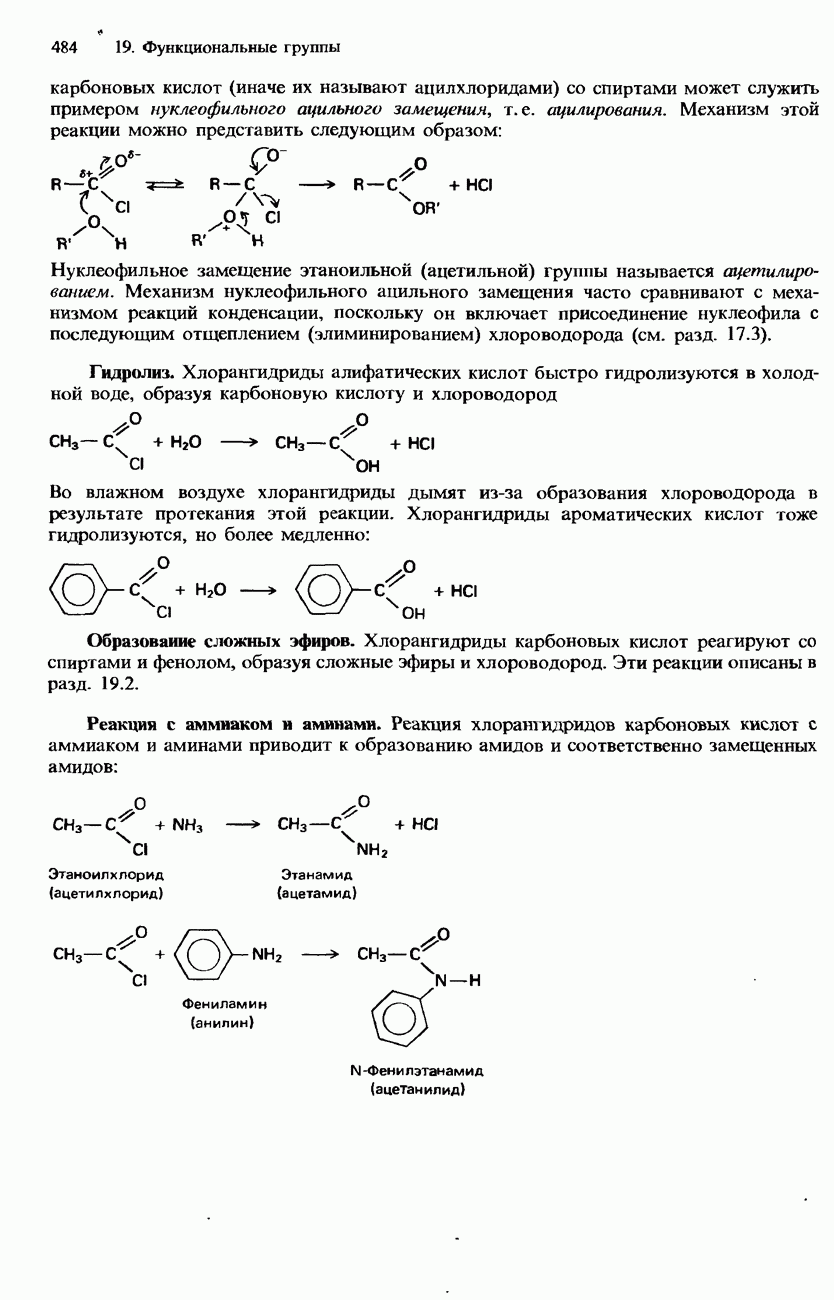
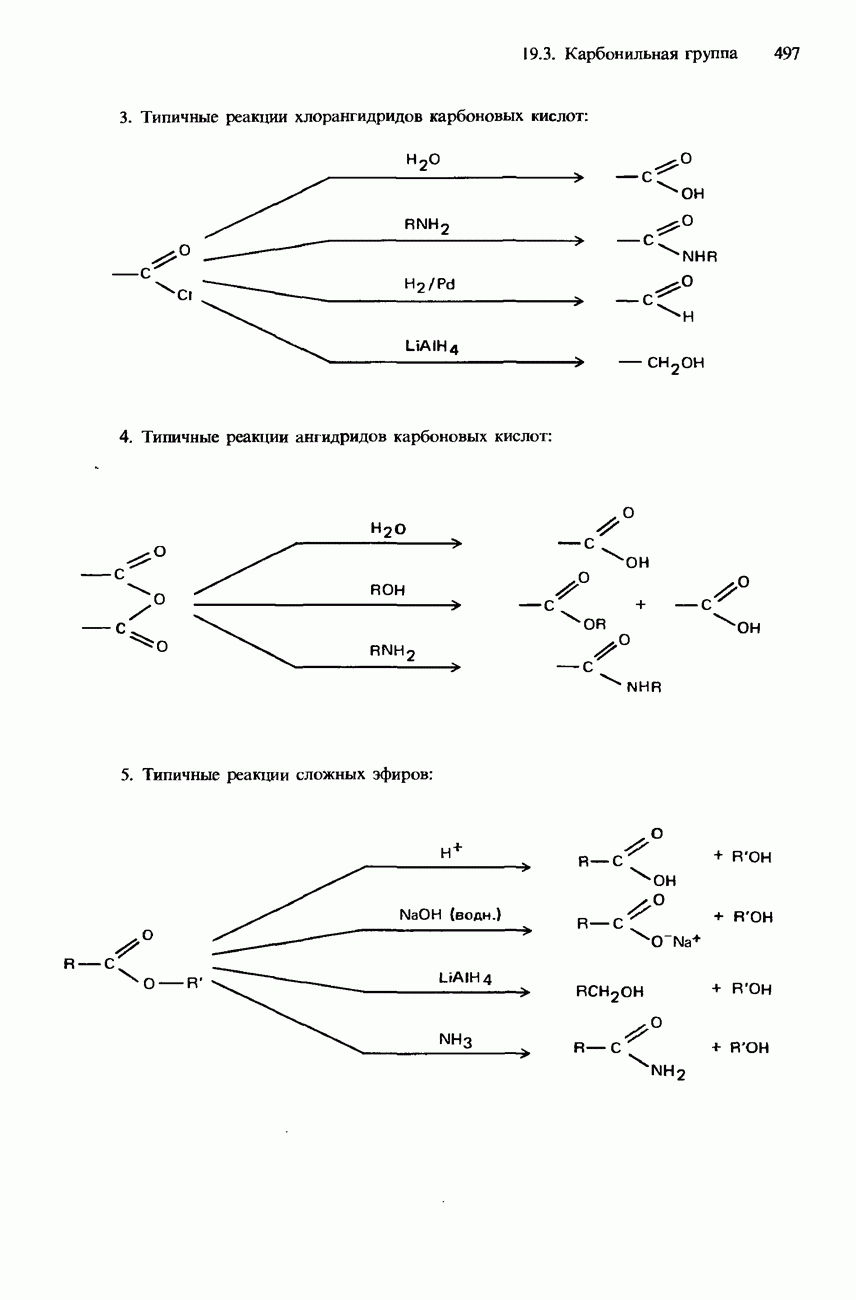
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
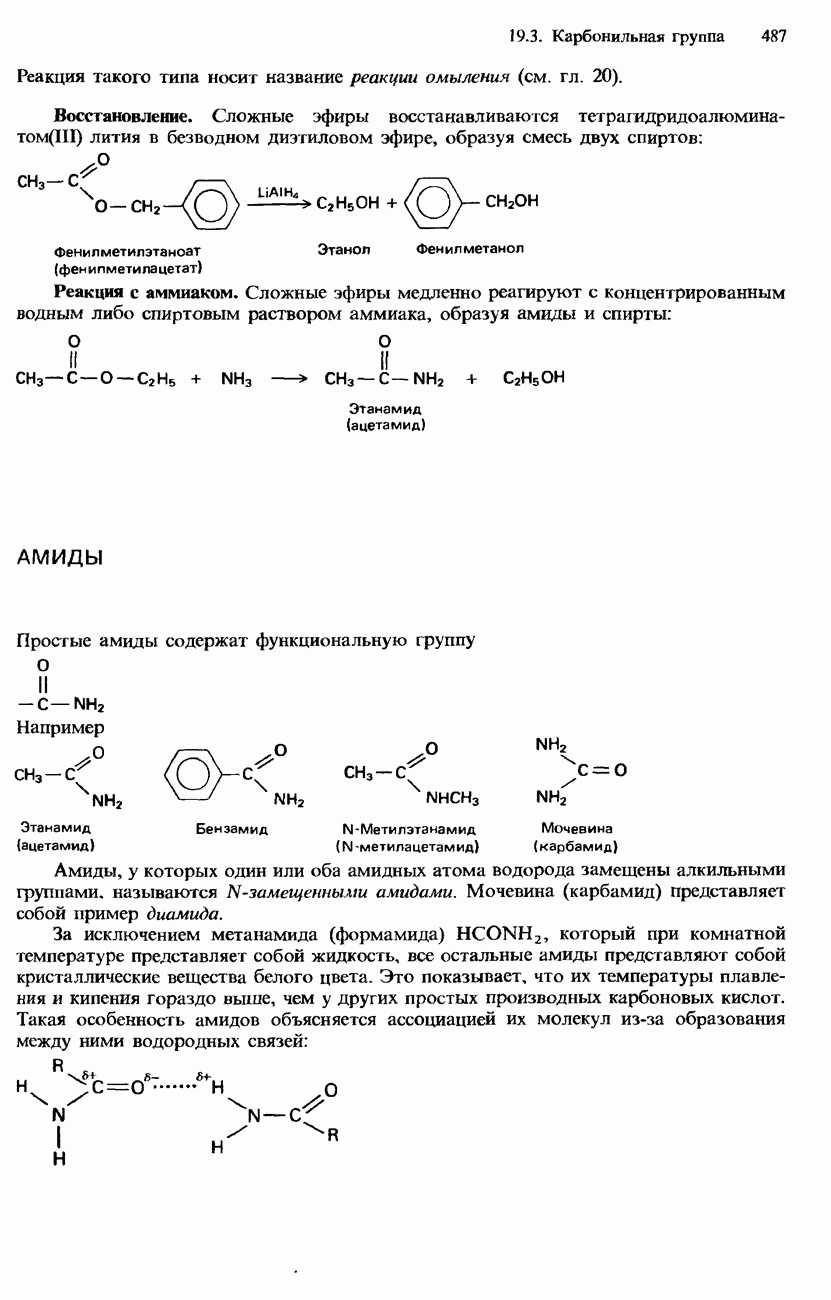
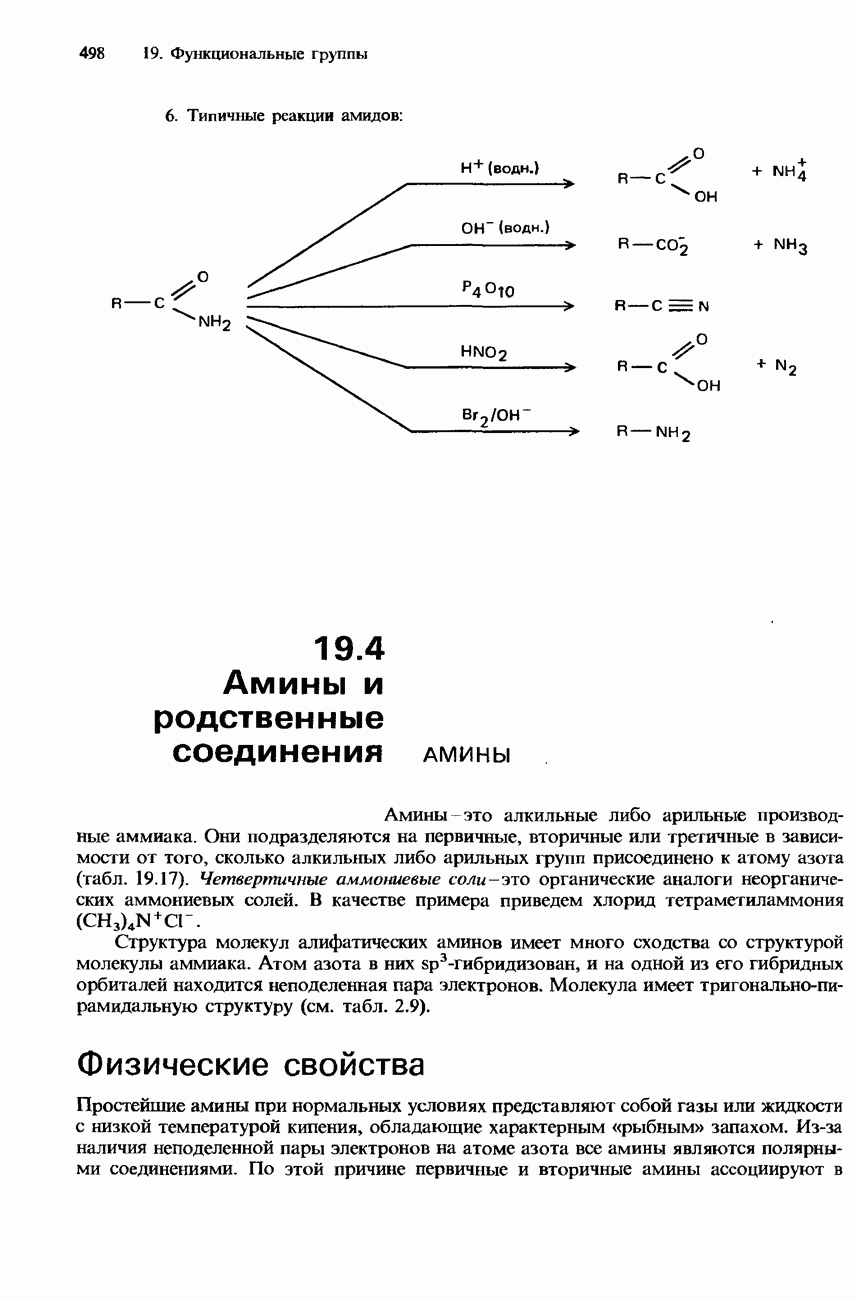
- АМИДЫ
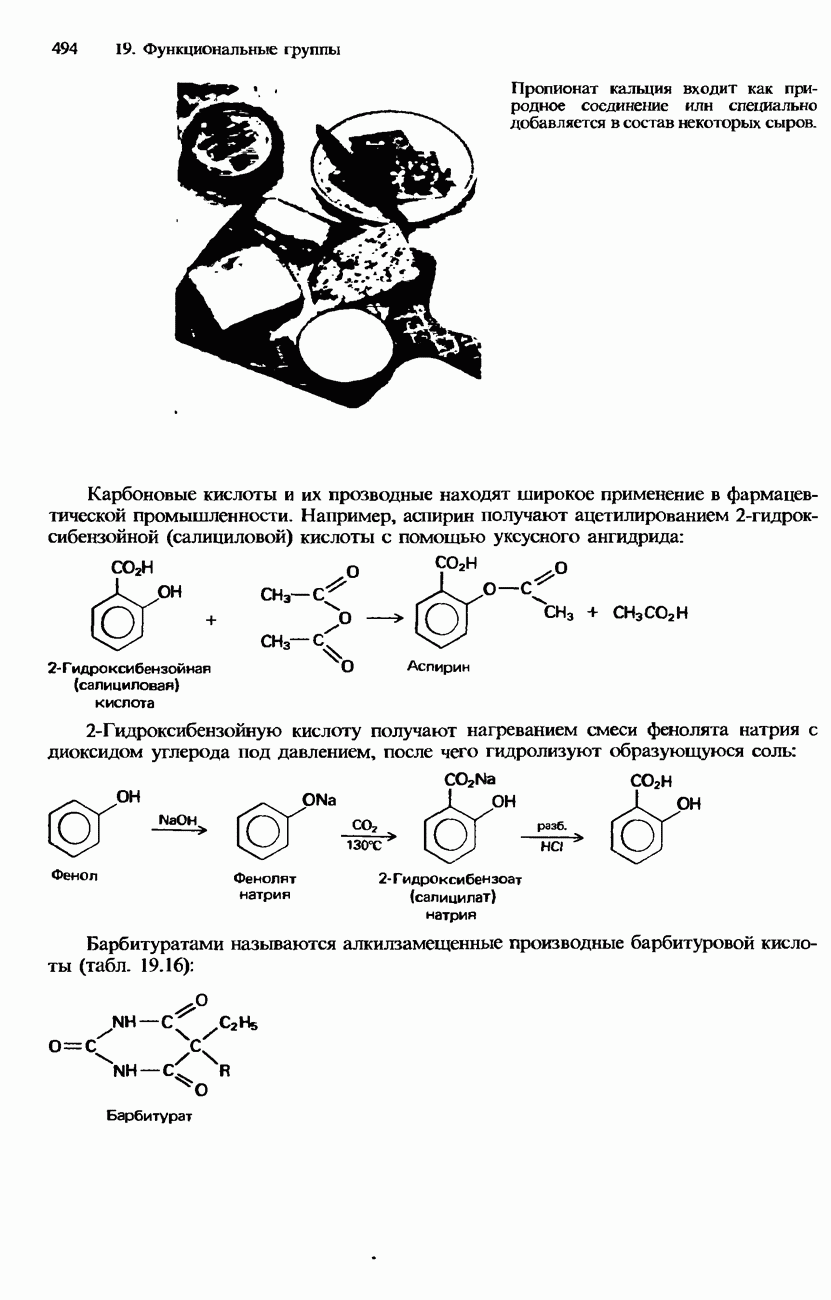
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
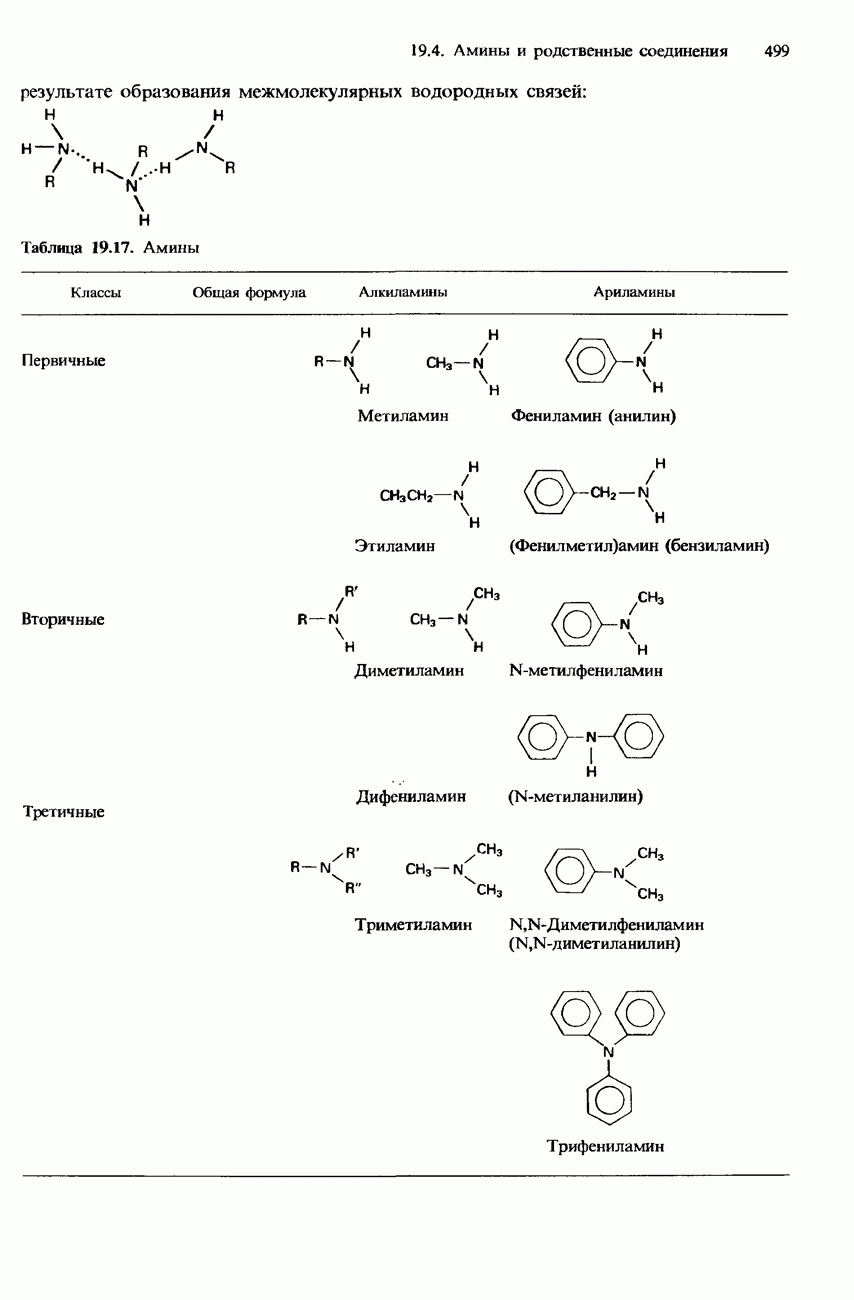
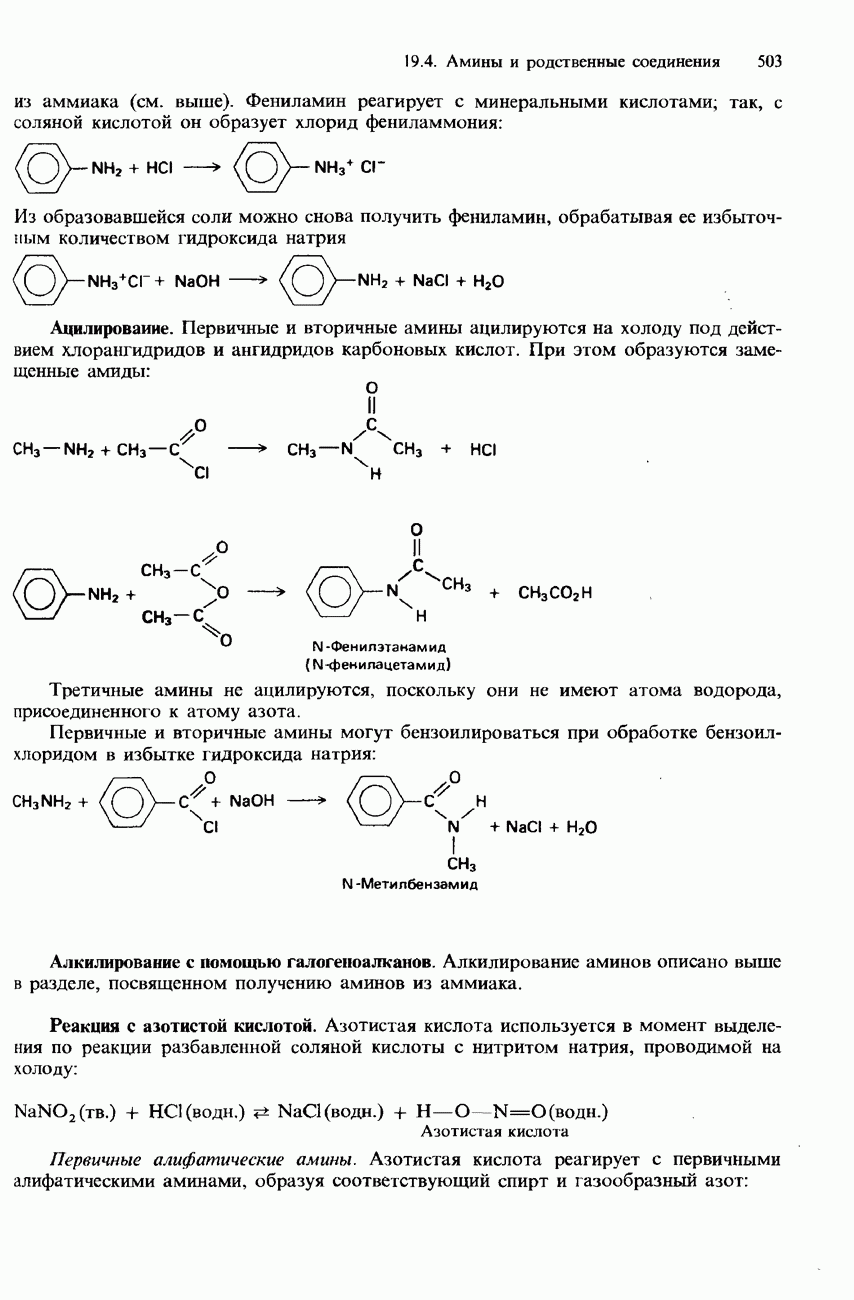
- 19.4 Амины и родственные соединения
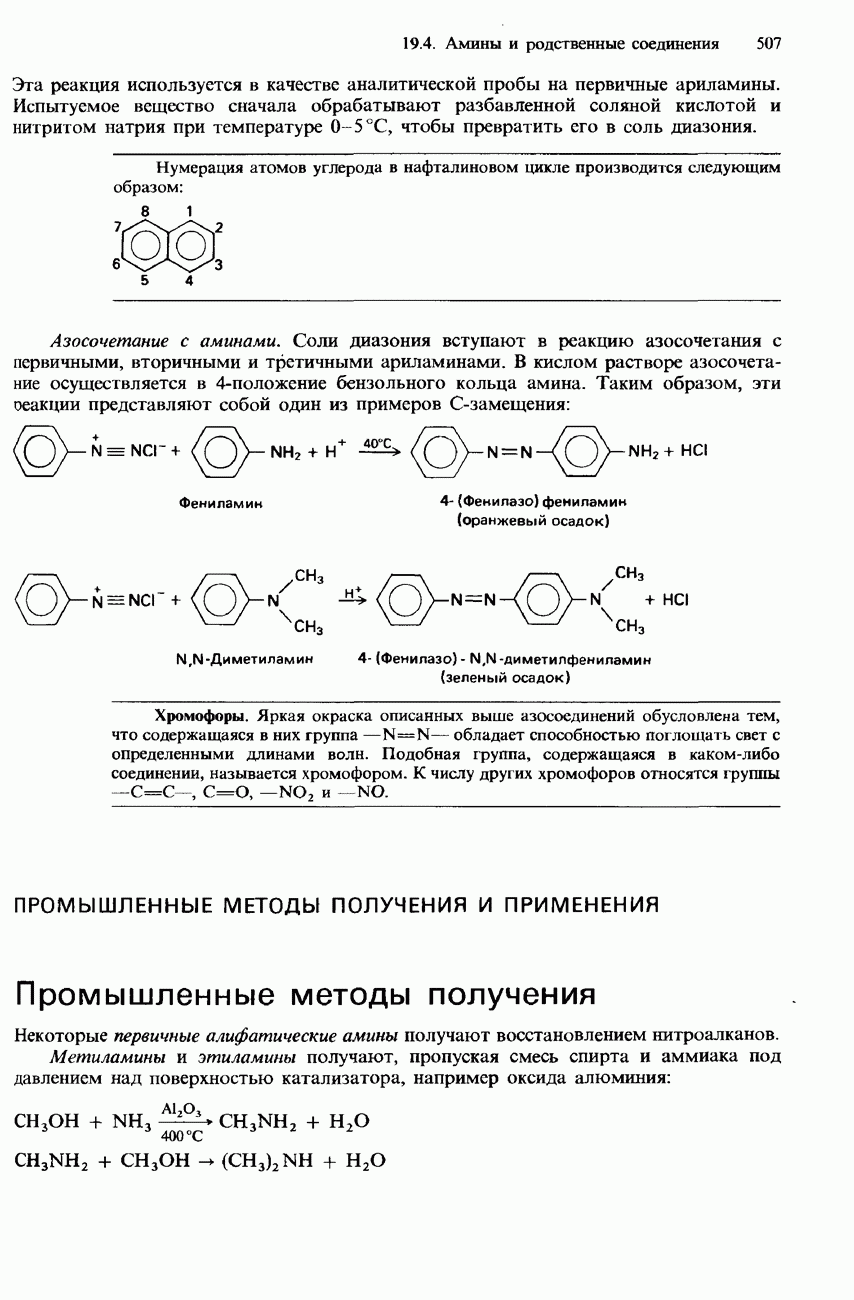
- СОЛИ ДИАЗОНИЯ
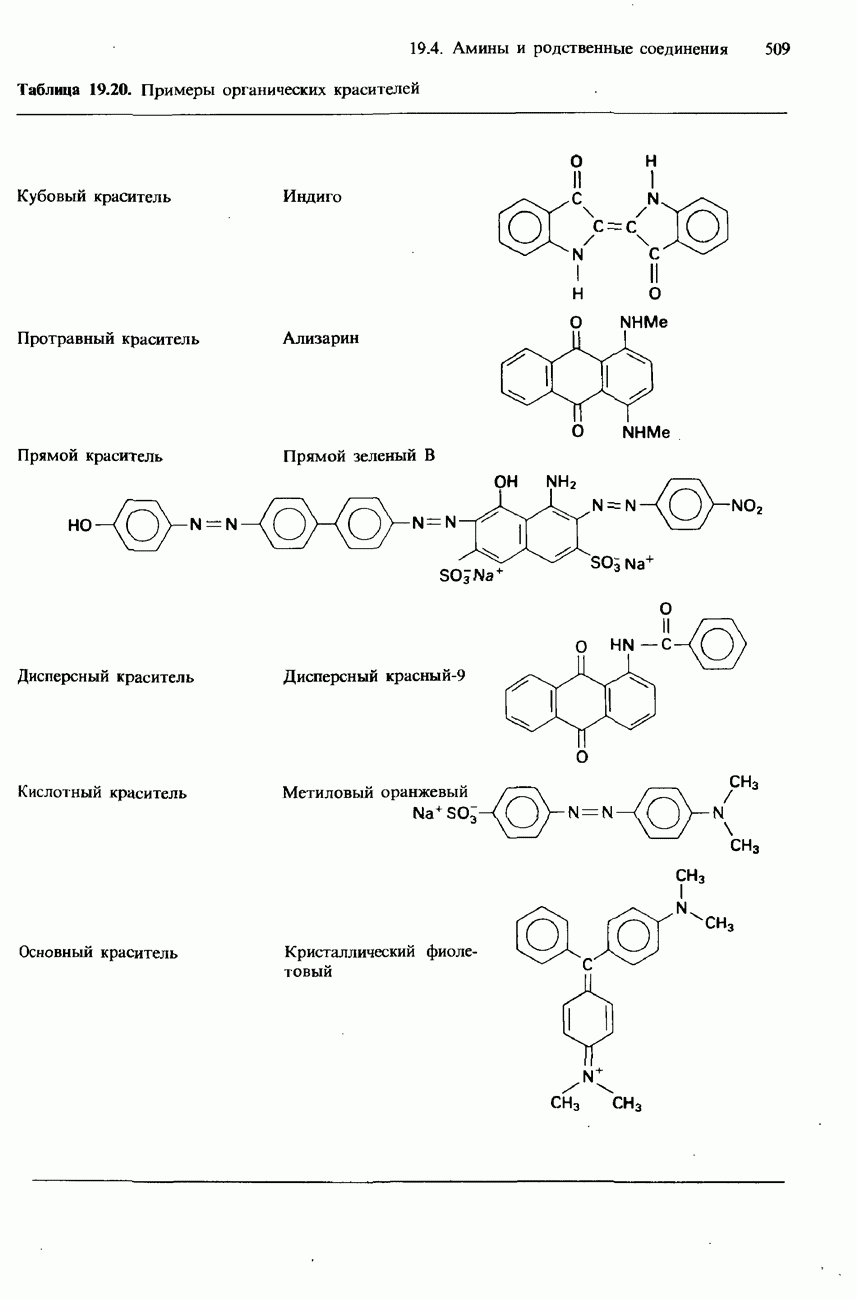
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
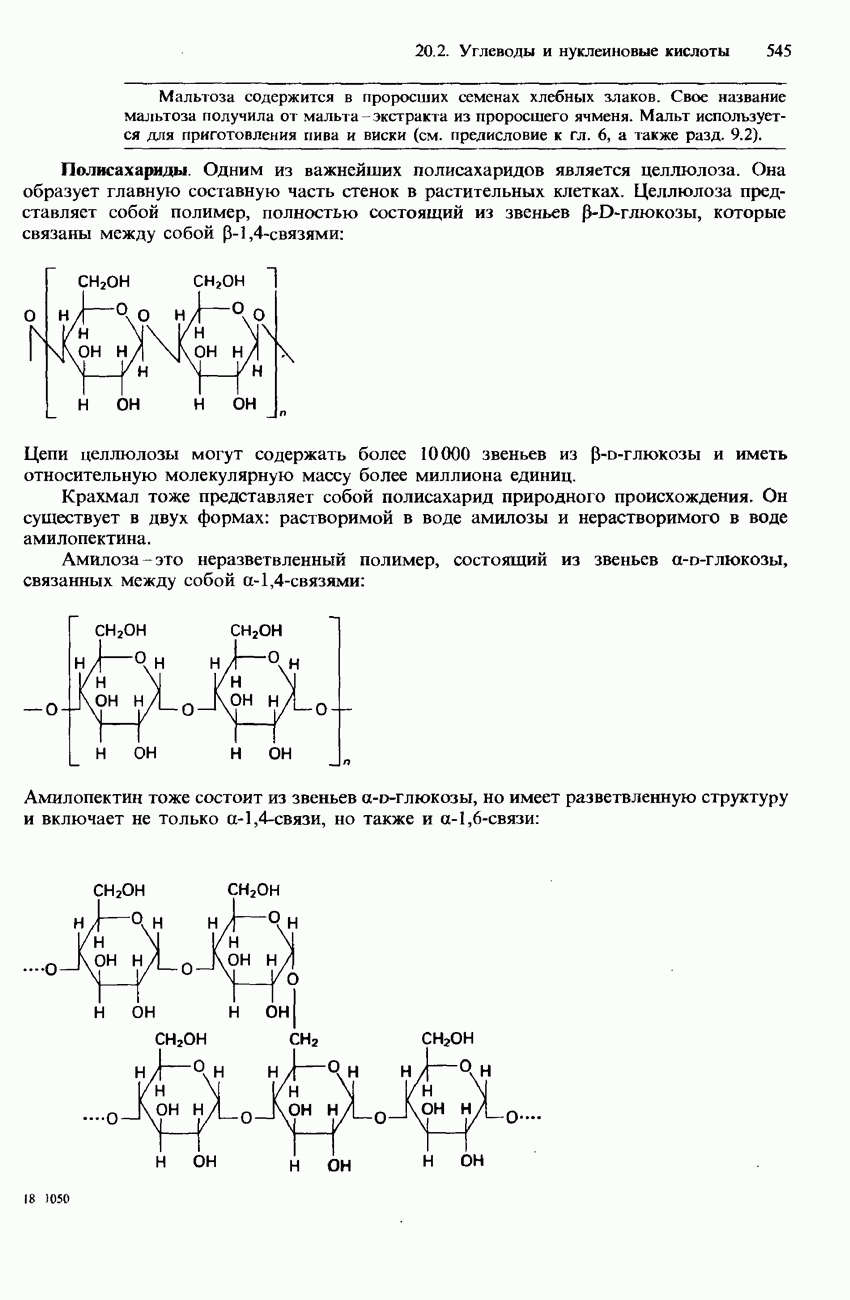
- 20.2. Углеводы и нуклеиновые кислоты
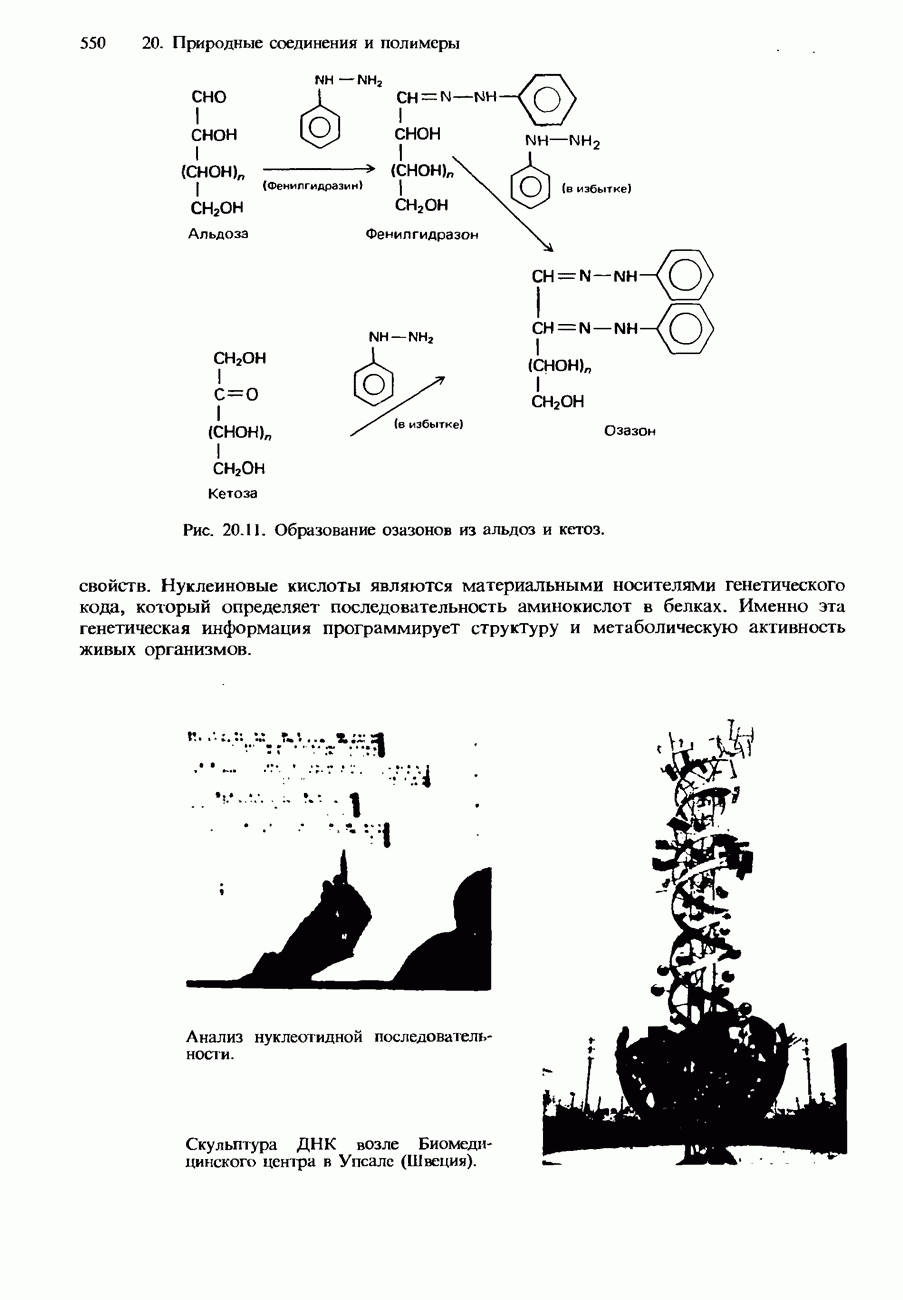
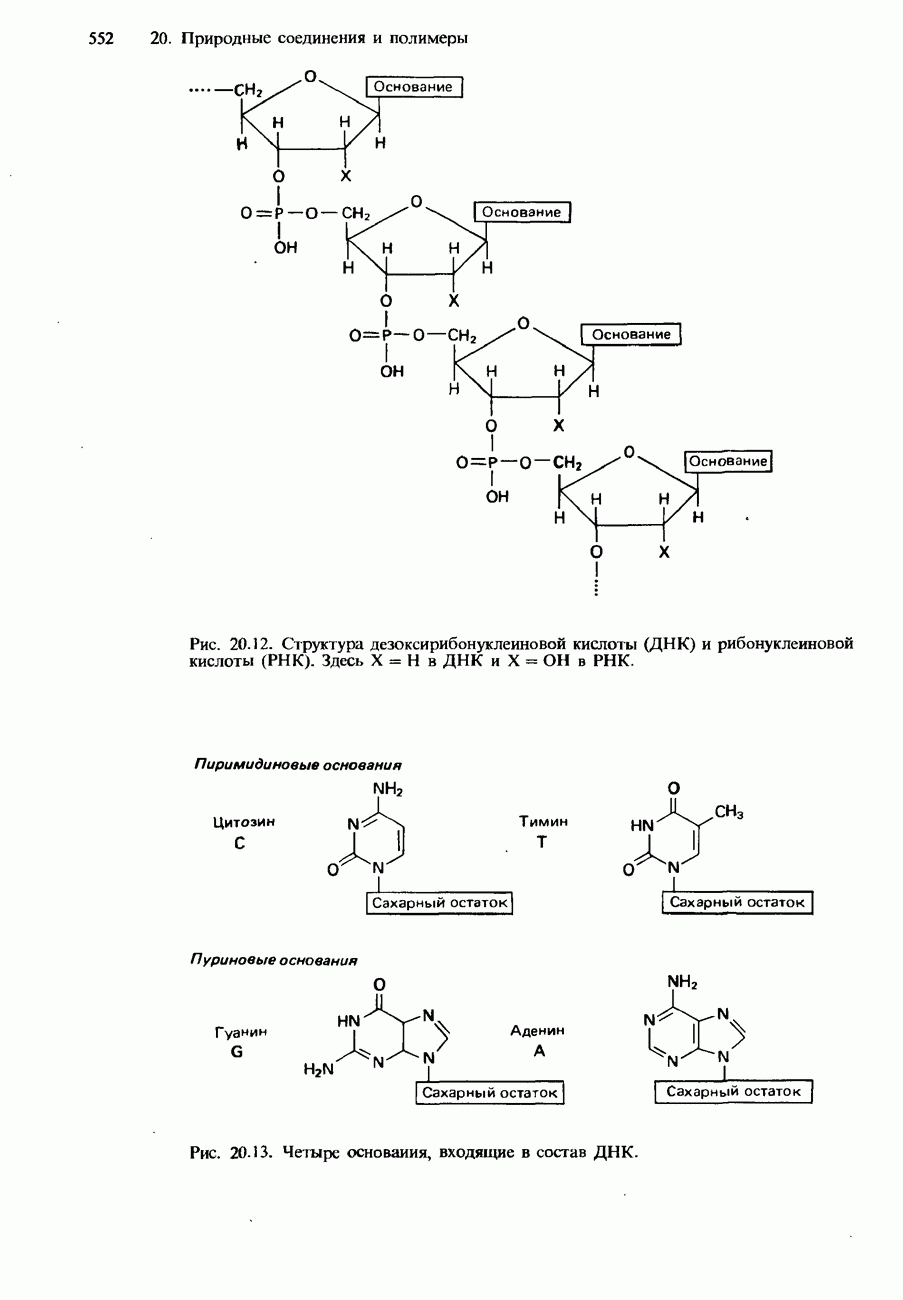
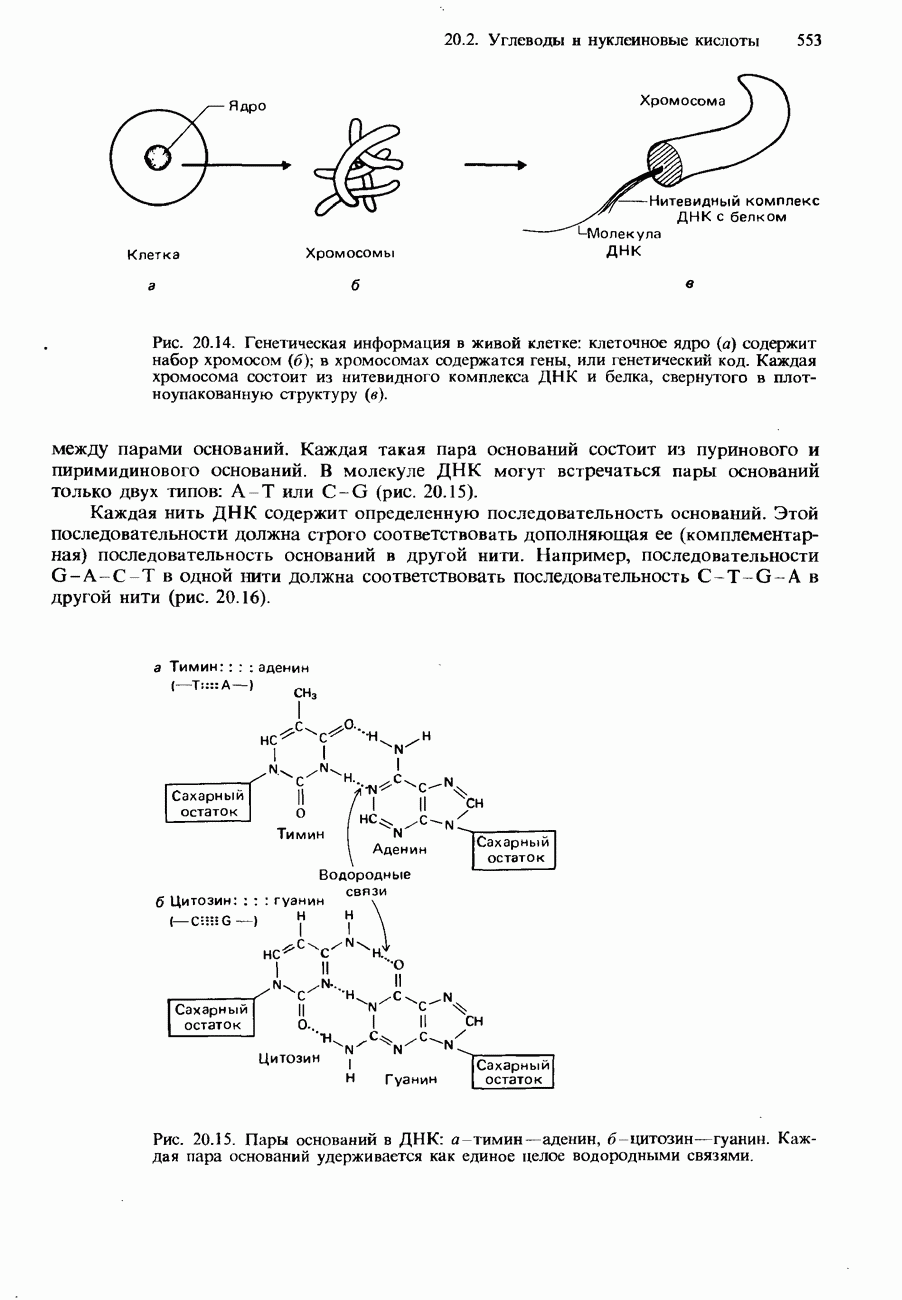
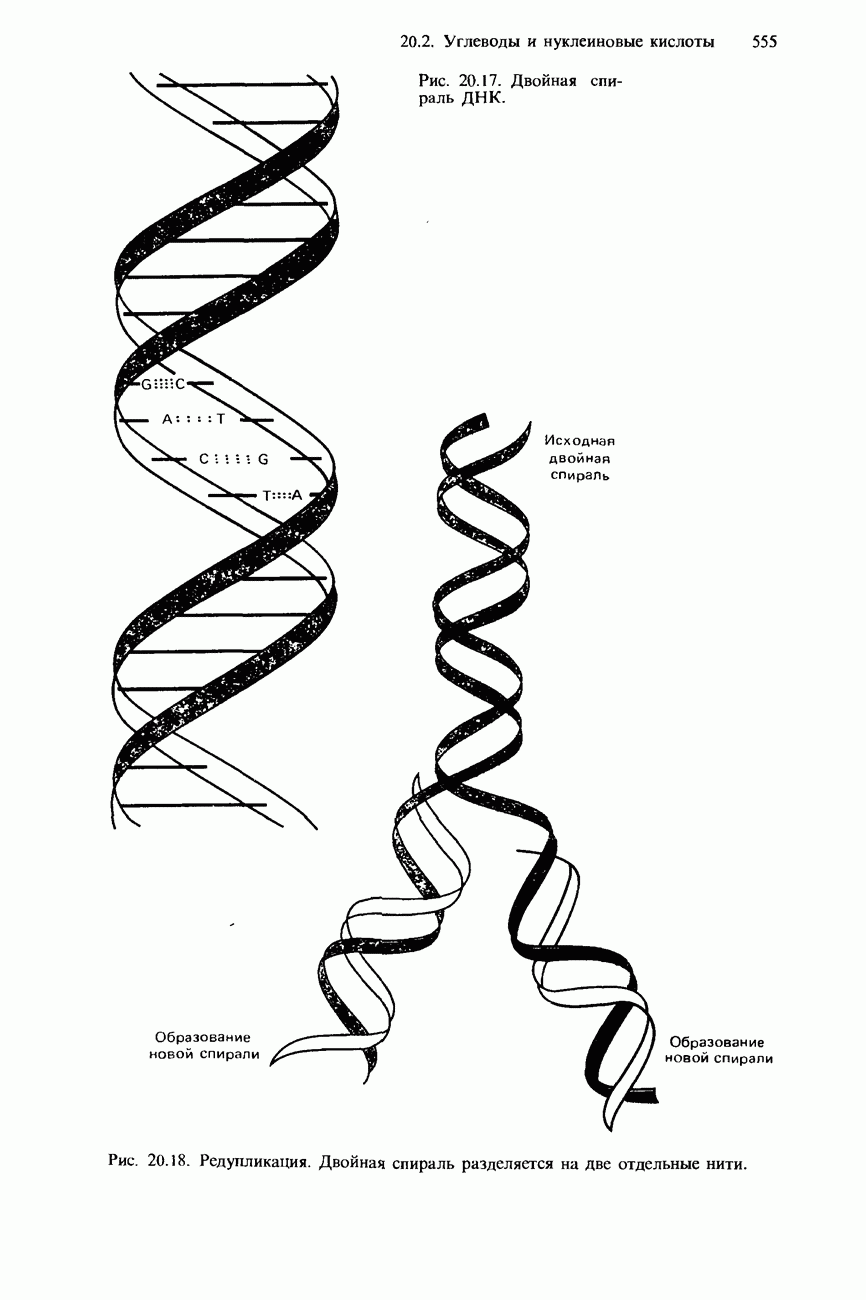
- НУКЛЕИНОВЫЕ КИСЛОТЫ
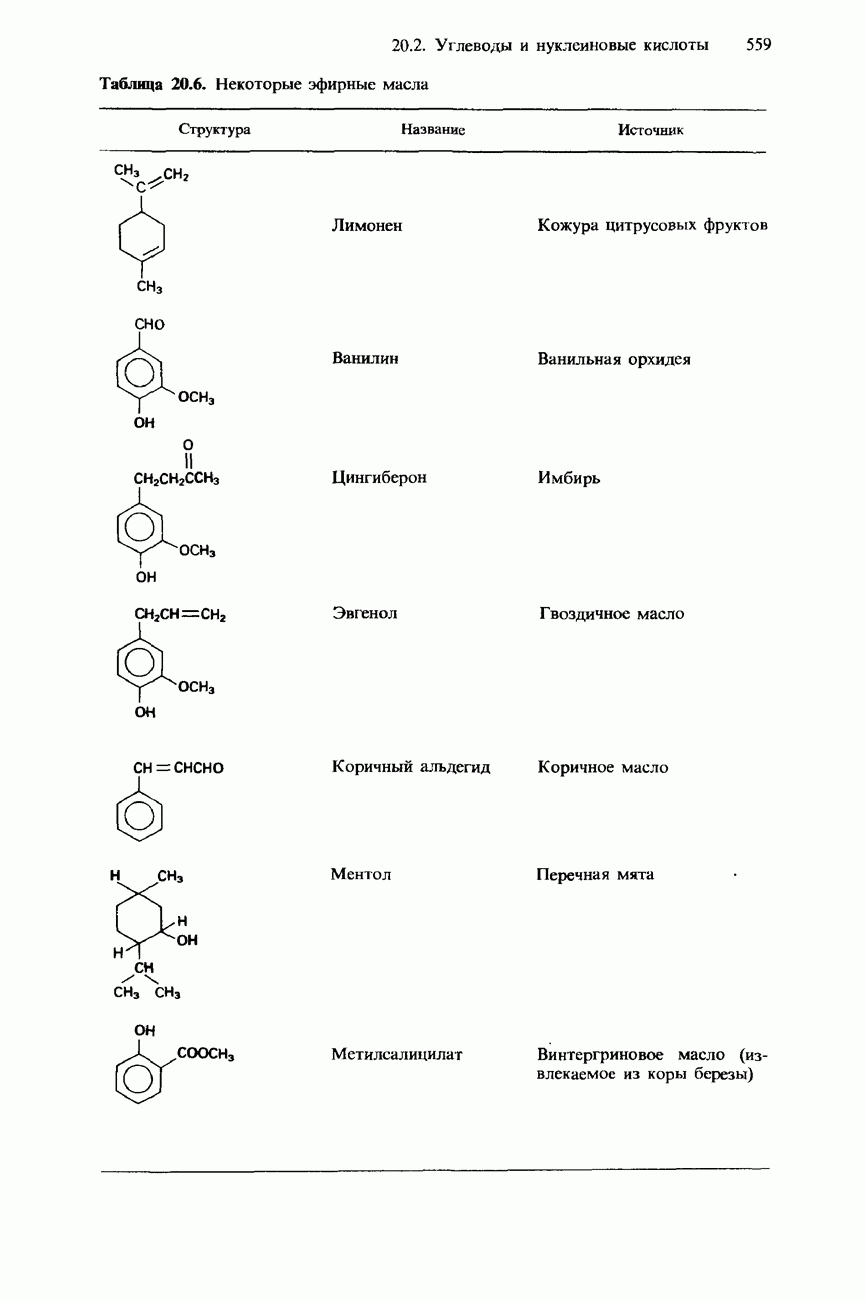
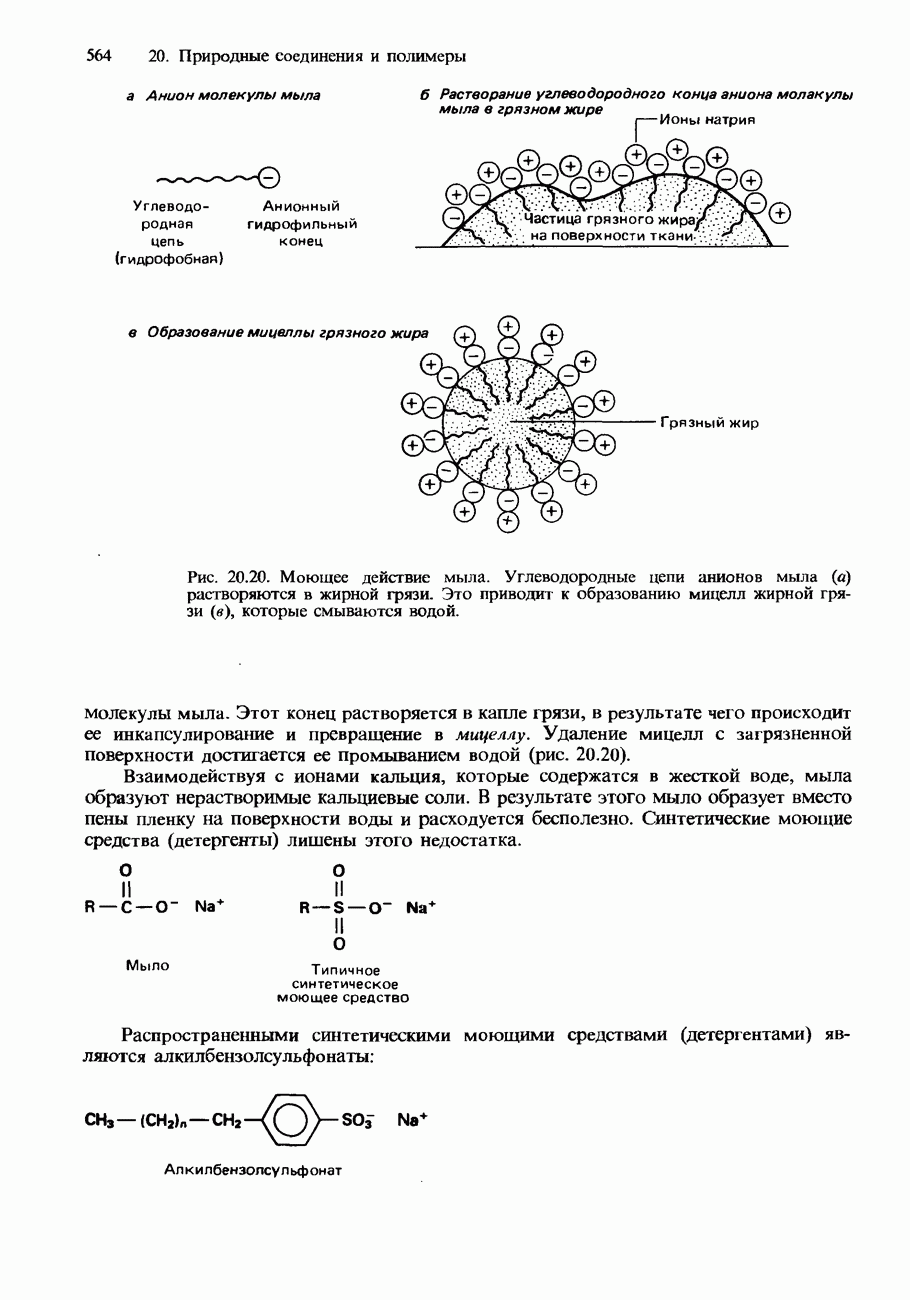
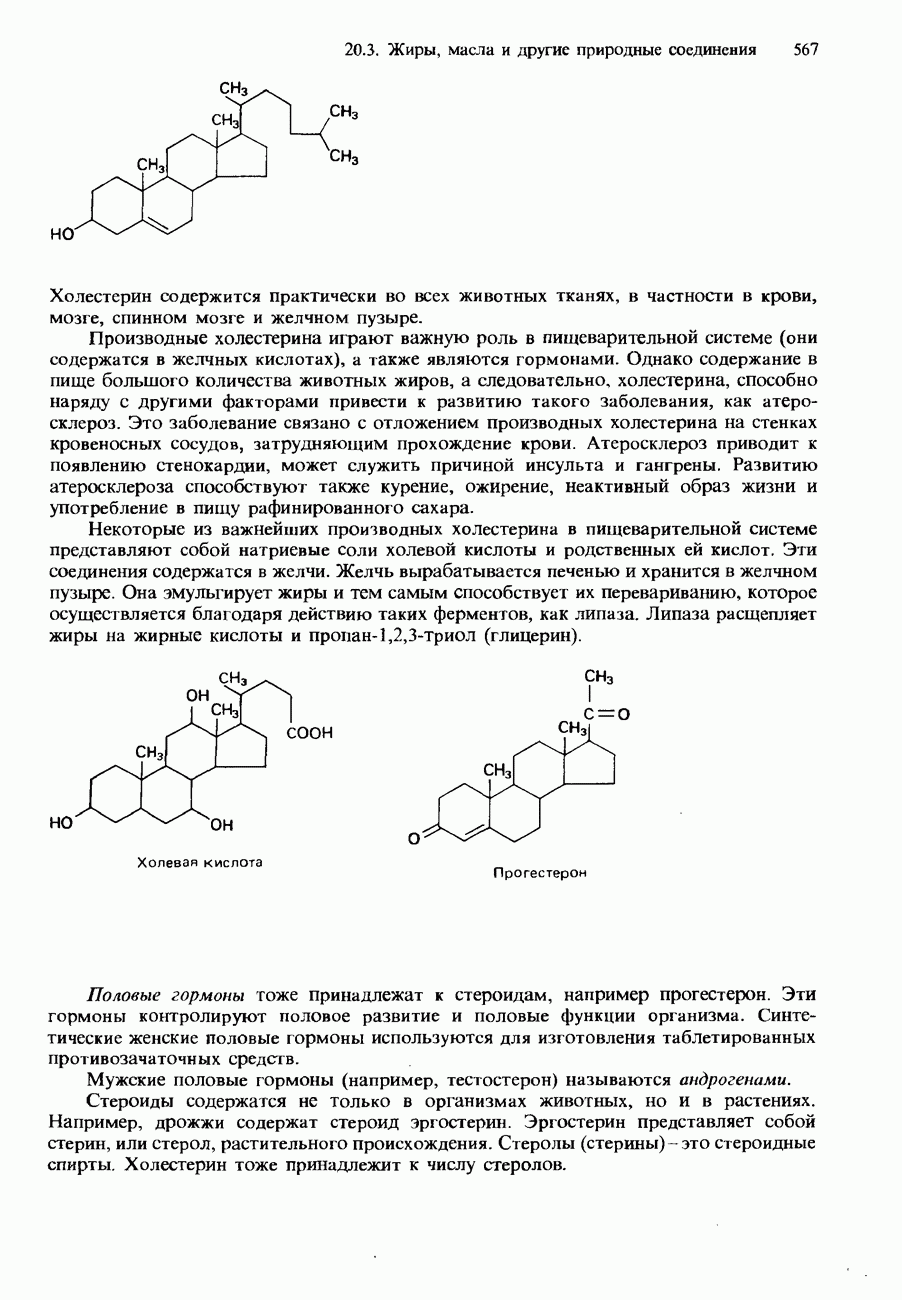
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
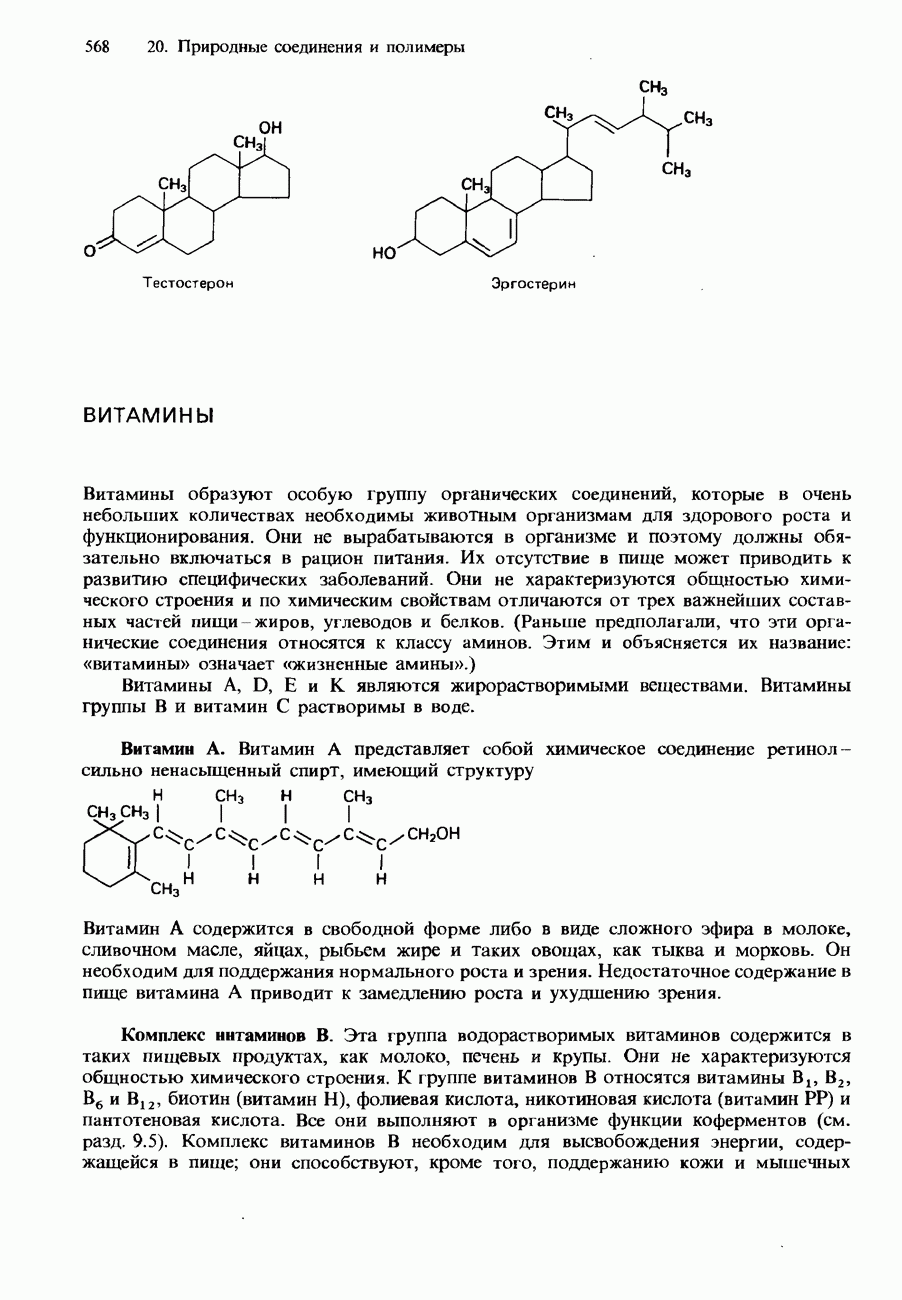
- ВИТАМИНЫ
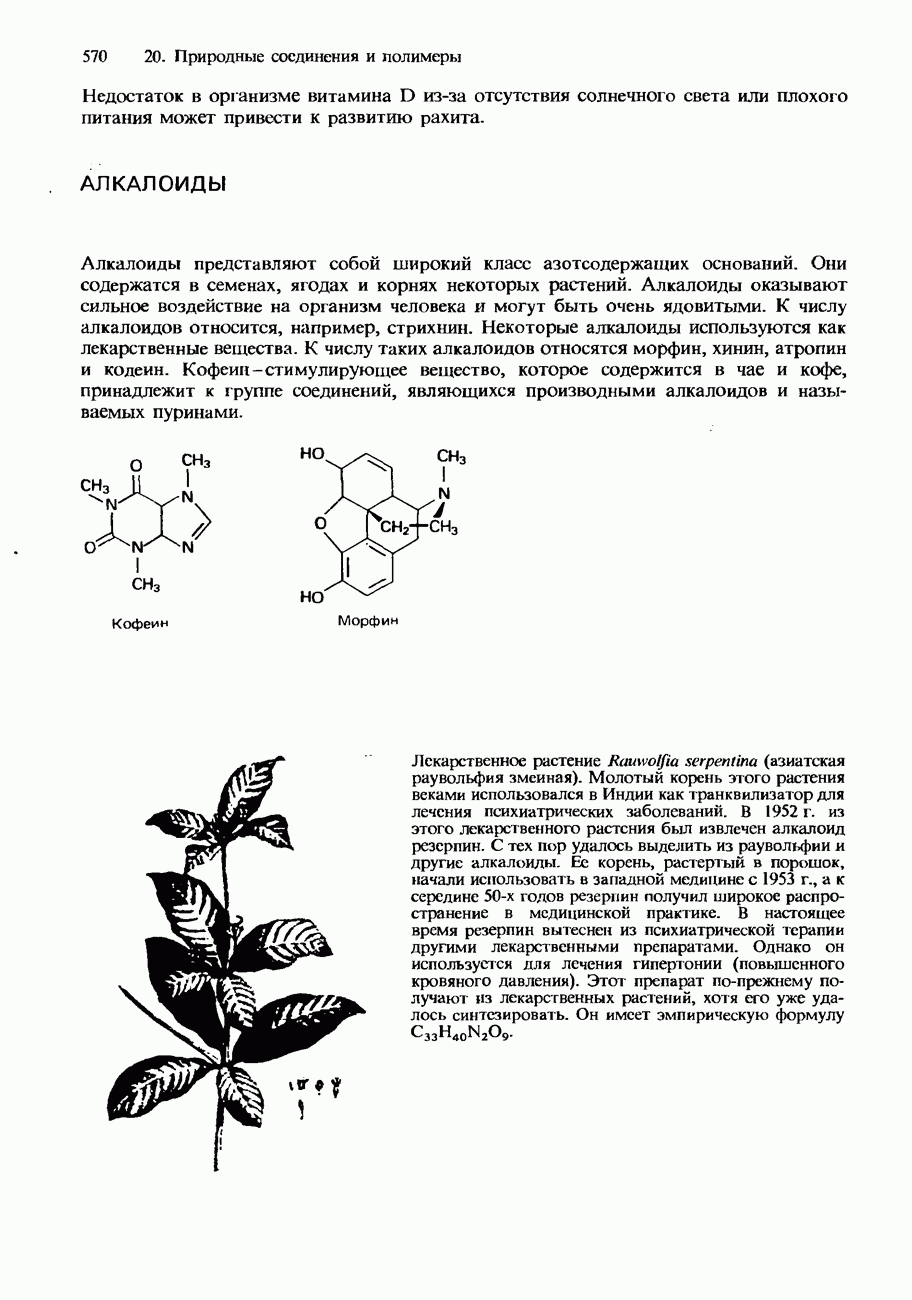
- АЛКАЛОИДЫ
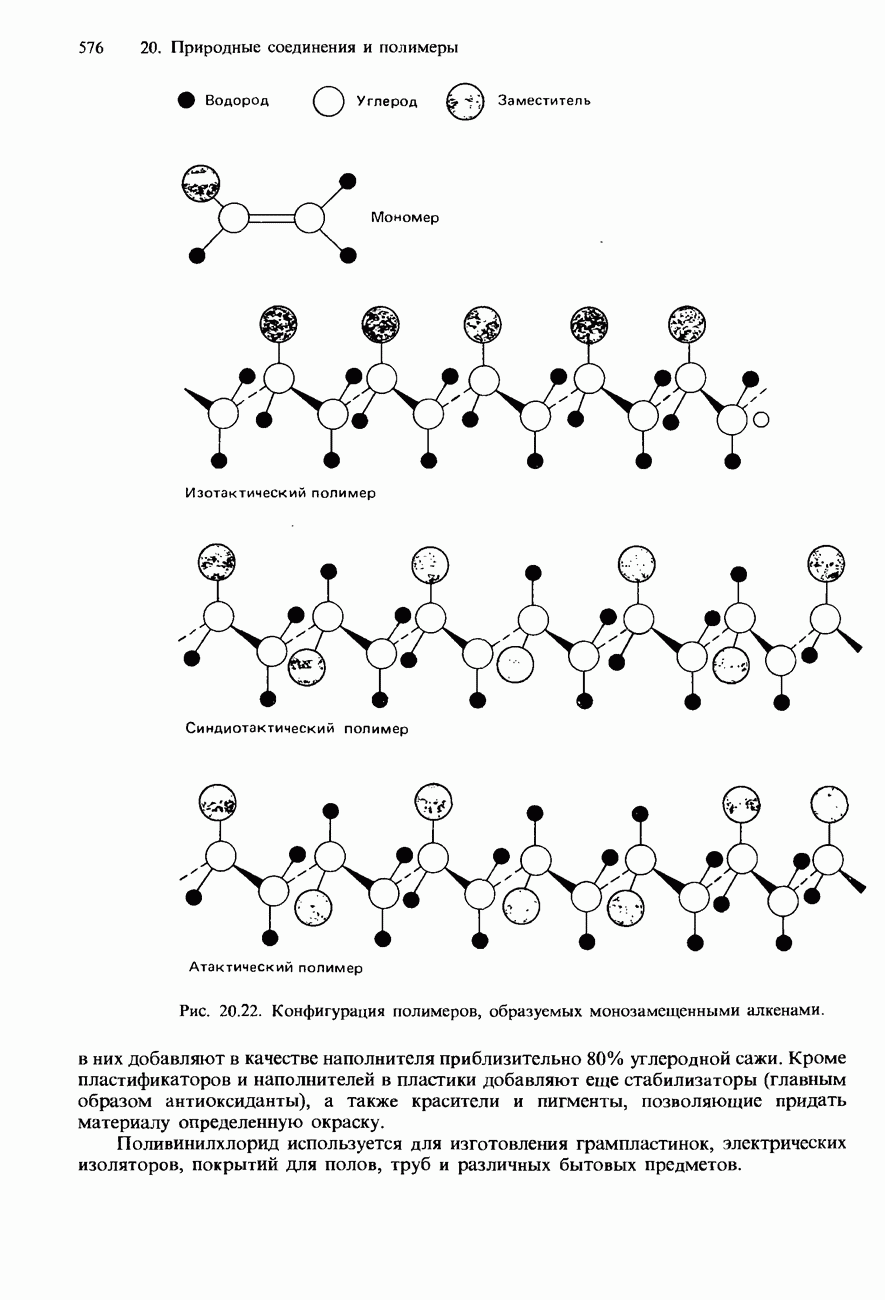
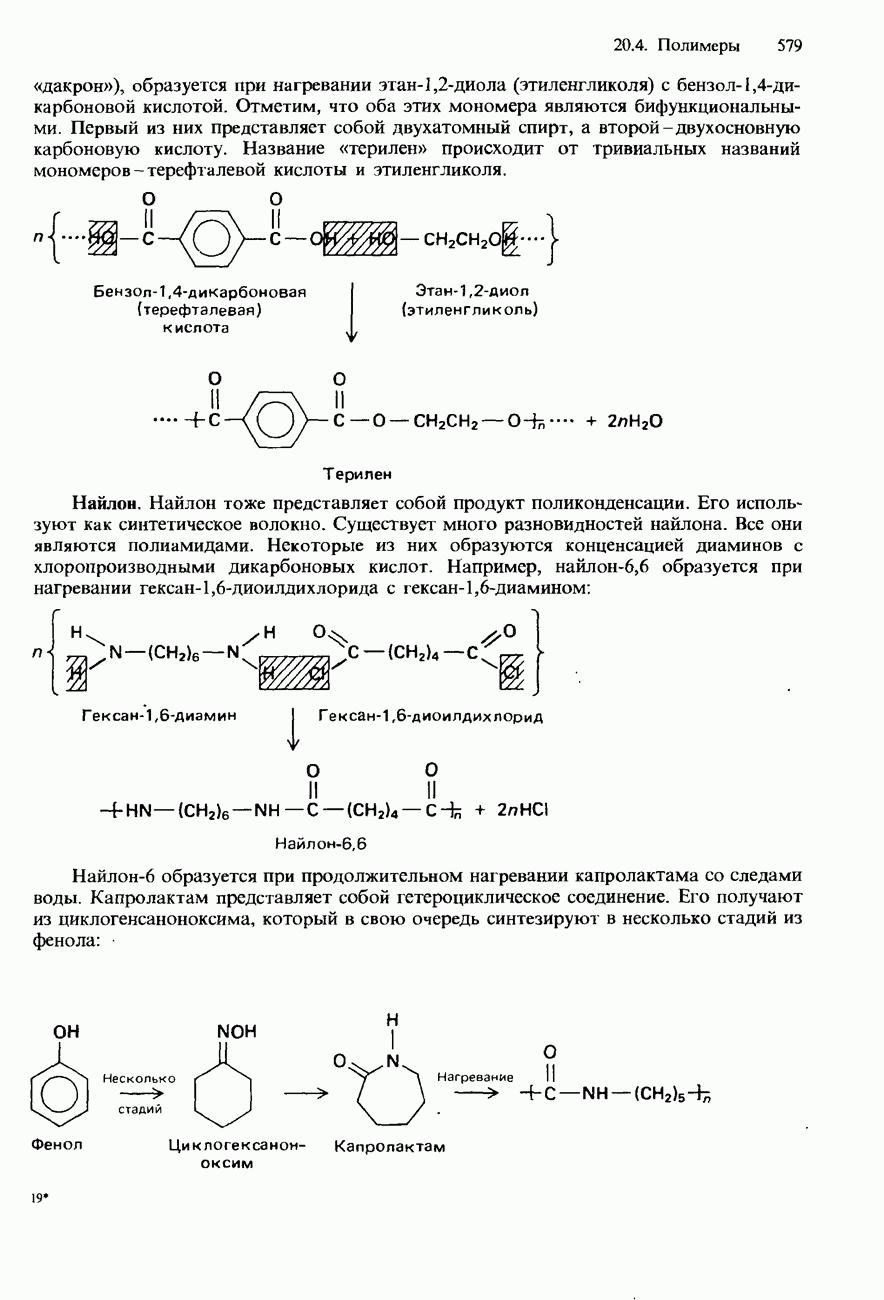
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
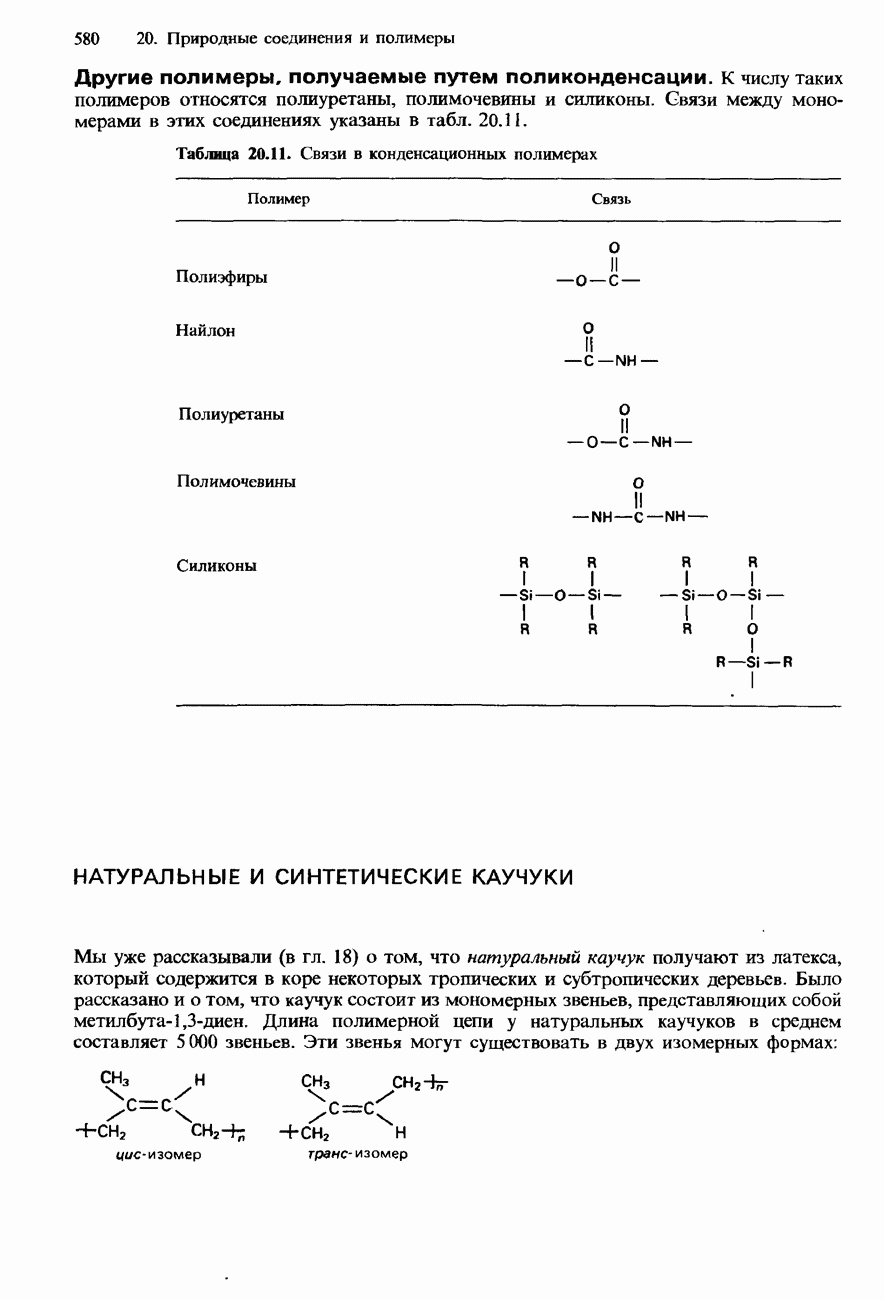
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ