| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
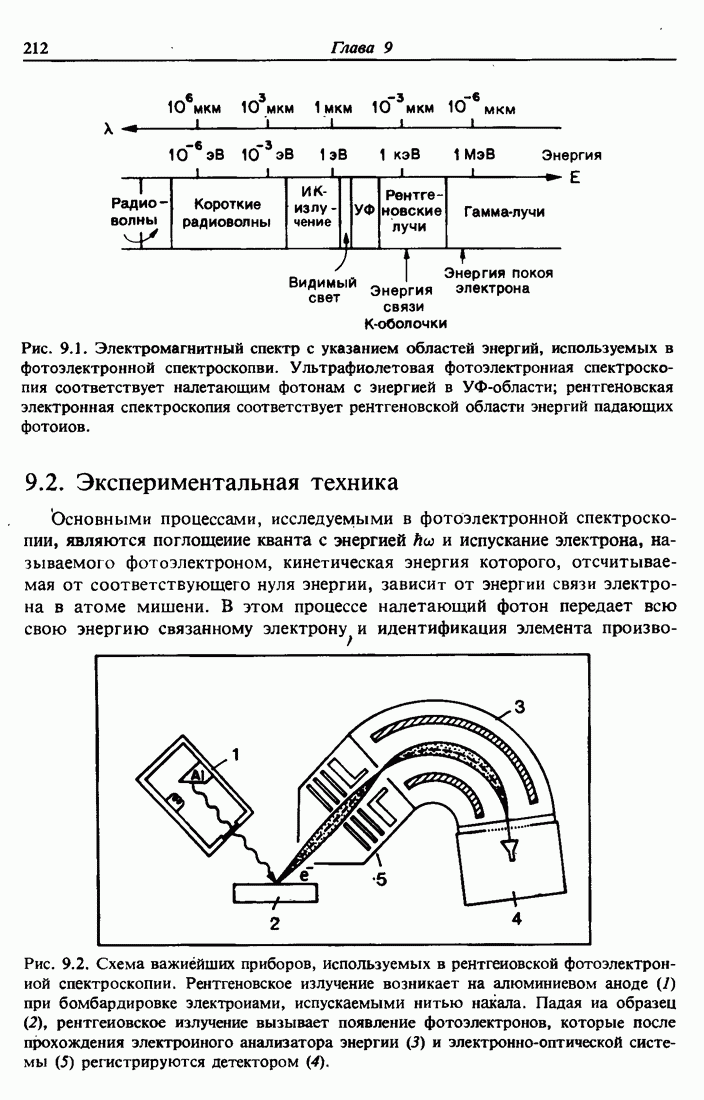
9.6. Сдвиги энергии связи; химические сдвиги
Точное значение энергии связи электрона в атоме зависит от его химического окружения. Рассмотрим энергетический уровень внутреннего электрона. Энергия электрона во внутренней оболочке определяется кулоновским взаимодействием с другими электронами и притягивающим потенциалом ядра. Любое изменение в химическом окружении элемента будет влиять на пространственное перераспределение заряда валентных электронов данного атома и вызывать изменение потенциала, заметное для внутреннего

Рис. 9.11. Химический сдвиг энергии связи линии  в кремнии и
в кремнии и  . Спектры получены с помощью излучения
. Спектры получены с помощью излучения  [17].
[17].
электрона. Перераспределение заряда влияет на потенциал внутренних электронов и приводит к изменению их энергии связи.
Сдвиг энергий связи внутренних электронов в зависимости от химического окружения продемонстрирован на рис. 9.11 для линии  . Измеренная энергия связи
. Измеренная энергия связи  сдвигается более чем на 4 эВ при переходе от кремниевой матрицы к
сдвигается более чем на 4 эВ при переходе от кремниевой матрицы к  . Существование химических сдвигов в XPS прямо привело к применению его в анализе вешеств. В ранней работе группы исследователей из Уппсалы [16] показано, что в энергиях связи внутренних электронов в молекулярных системах проявляются химические сдвиги, прямо связанные с ковалентностью.
. Существование химических сдвигов в XPS прямо привело к применению его в анализе вешеств. В ранней работе группы исследователей из Уппсалы [16] показано, что в энергиях связи внутренних электронов в молекулярных системах проявляются химические сдвиги, прямо связанные с ковалентностью.
Концепция химических сдвигов основана на идее, что внутренние электроны «чувствуют» изменение энергии вследствие изменения вклада валентной оболочки в потенциал за счет химических связей внешних электронов.

Рис. 9.12. Химический сдвиг в атоме углерода, входящем в состав трифторацетата. Четыре углеродные линии соответствуют четырем атомам углерода в молекуле [13].
В простейшем описании явления валентные электроны смешаются к ядру или от него в зависимости от типа связи. Чем больше электроотрицательность окружающих атомов, тем больше смещение электронного заряда от центра атома и тем выше наблюдаемые энергии связи внутренних электронов. Сдвиги энергии связи в атомах углерода в этилтрифторацетате  приведены в качестве примера на рис. 9.12. Каждый углеродный атом находится в различном химическом окружении и дает несколько отличающуюся линию XPS. Сдвиги энергии связи находятся в пределах 8 эВ.
приведены в качестве примера на рис. 9.12. Каждый углеродный атом находится в различном химическом окружении и дает несколько отличающуюся линию XPS. Сдвиги энергии связи находятся в пределах 8 эВ.
Пример сдвига в спектре XPS для  в результате образования
в результате образования  показан на рис. 9.13. Сдвиг линии поглощения никеля при переходе от
показан на рис. 9.13. Сдвиг линии поглощения никеля при переходе от  здесь равен 1,1 эВ. Уменьшение интенсивности пика вызвано уменьшением количества атомов никеля, содержащегося в
здесь равен 1,1 эВ. Уменьшение интенсивности пика вызвано уменьшением количества атомов никеля, содержащегося в  на глубине выхода электронов
на глубине выхода электронов  так как соединение обогащается кремнием. Это как раз пгример того, как информация об изменении стехиометрии получается непосредственно из вариаций интенсивности, сопровождающихся лишь малыми изменениями химического сдвига.
так как соединение обогащается кремнием. Это как раз пгример того, как информация об изменении стехиометрии получается непосредственно из вариаций интенсивности, сопровождающихся лишь малыми изменениями химического сдвига.
Энергия связи  эВ
эВ

Рис. 9.13. Трехмерное изображение спектров рентгеновского фотопоглощения для линии  где время нагрева образца отложено по оси Z. Спектры иллюстрируют рост плоского слоя силицидов различного состава, показанный на врезке вверху. Химические сдвиги здесь довольно малы, но на изменение состава указывает изменение интенсивности [18].
где время нагрева образца отложено по оси Z. Спектры иллюстрируют рост плоского слоя силицидов различного состава, показанный на врезке вверху. Химические сдвиги здесь довольно малы, но на изменение состава указывает изменение интенсивности [18].
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редактора перевода
- Предисловие
- Глава 1. ОСНОВНЫЕ ПОНЯТИЯ, ЕДИНИЦЫ ИЗМЕРЕНИЯ, АТОМ БОРА
- 1.2. Единицы измерения физических величин
- 1.3. Корпускулярно-волновой дуализм и кристаллическая структура
- 1.4. Модель Бора
- Задачи
- Глава 2. АТОМНЫЕ СТОЛКНОВЕНИЯ И СПЕКТРОМЕТРИЯ ОБРАТНОГО РАССЕЯНИЯ
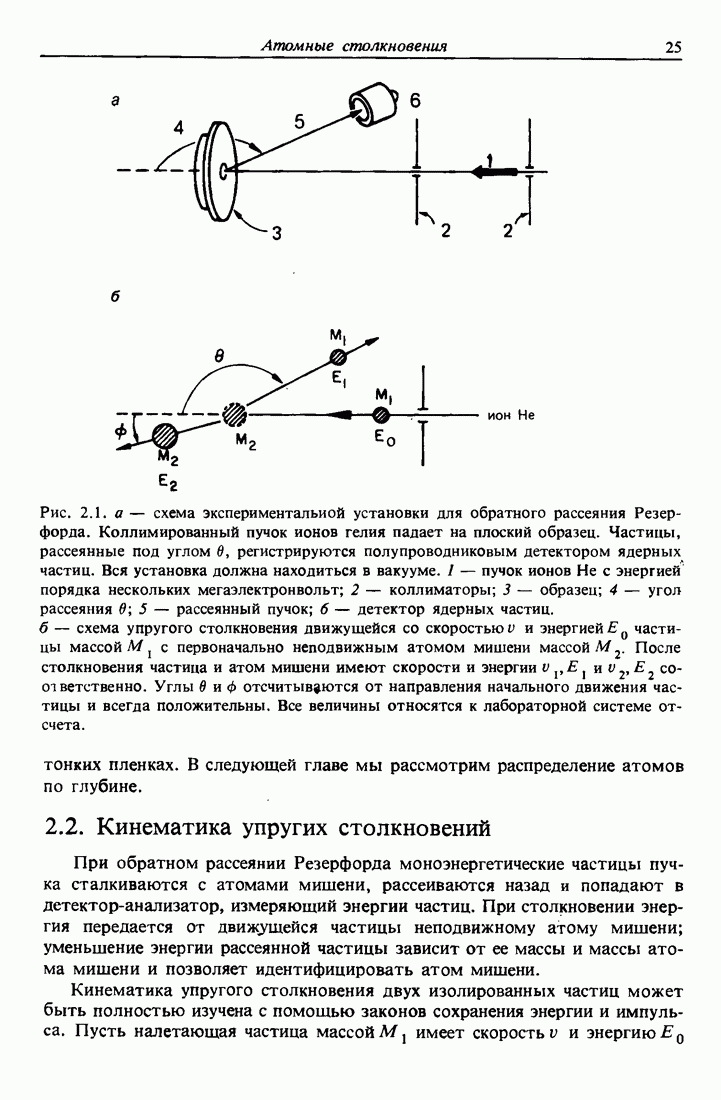
- 2.2. Кинематика упругих столкновений
- 2.3. Пример спектрометрии обратного рассеяния Резерфорда
- 2.4. Сечение рассеяния и прицельный параметр
- 2.5. Рассеяние в центральном поле
- 2.6. Сечение рассеяния в задаче двух тел
- 2.7. Отклонения от формулы Резерфорда при низких и высоких энергиях
- 2.8. Рассеяние ионов низких энергий (LEIS)
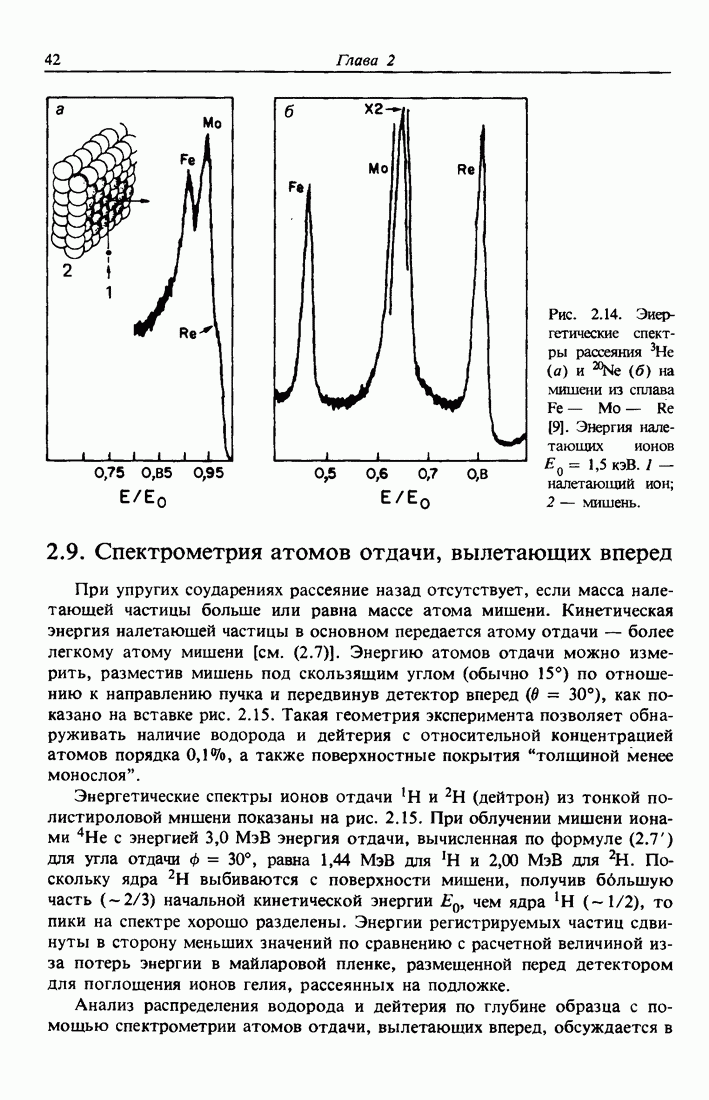
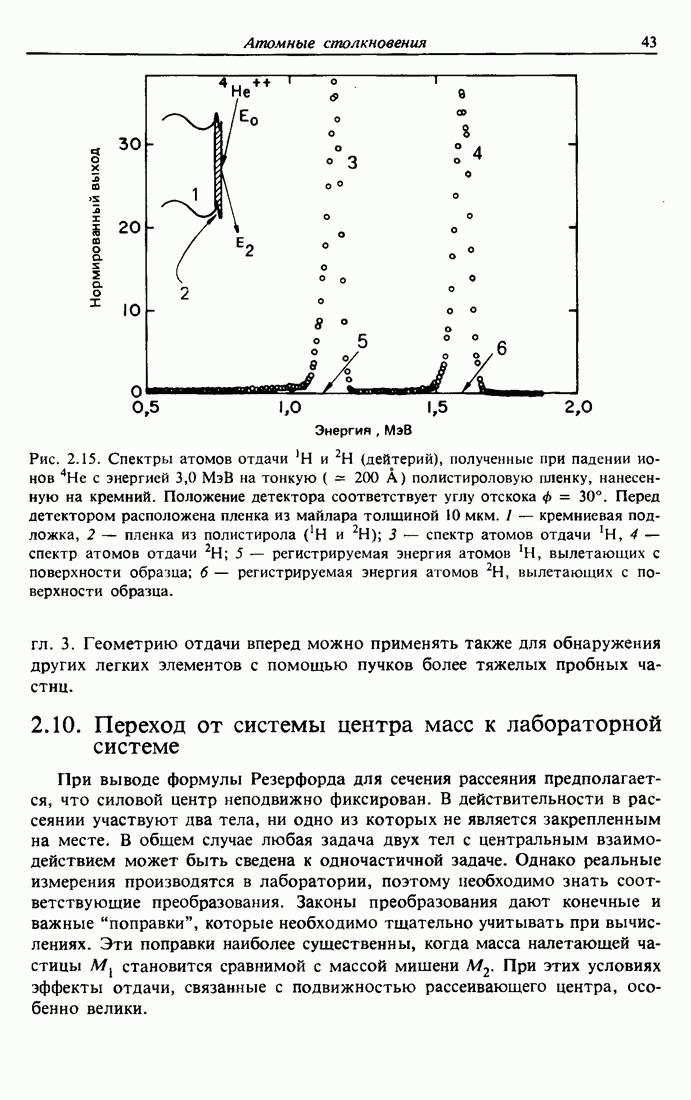
- 2.9. Спектрометрия атомов отдачи, вылетающих вперед
- 2.10. Переход от системы центра масс к лабораторной системе
- Задачи
- Глава 3. ПОТЕРИ ЭНЕРГИИ ЛЕГКИХ ИОНОВ И ПОЛУЧЕНИЕ РАСПРЕДЕЛЕНИЙ ПО ГЛУБИНЕ С ПОМОЩЬЮ ОБРАТНОГО РАССЕЯНИЯ
- 3.2. Общая картина потерь энергии и единицы их измерения
- 3.3. Потери энергии легких ионов высоких энергий в твердых телах
- 3.4. Потери энергии в химических соединениях и правило Брэгга
- 3.5. Ширина спектра энергии в обратном рассеянии
- 3.6. Форма спектра обратного рассеяния
- 3.7. Получение распределений по глубине с помощью рассеяния Резерфорда
- 3.8. Разрешение по глубине и флуктуации потерь энергии
- 3.9. Анализ распределения водорода и дейтерия по глубине
- 3.10. Пробеги ионов Н и Не
- 3.11. Распыление и пределы чувствительности
- 3.12. Сводка соотношений рассеяния
- Задачи
- Глава 4. ПРОФИЛИ РАСПЫЛЕНИЯ И МАСС-СПЕКТРОМЕТРИЯ ВТОРИЧНЫХ ИОНОВ
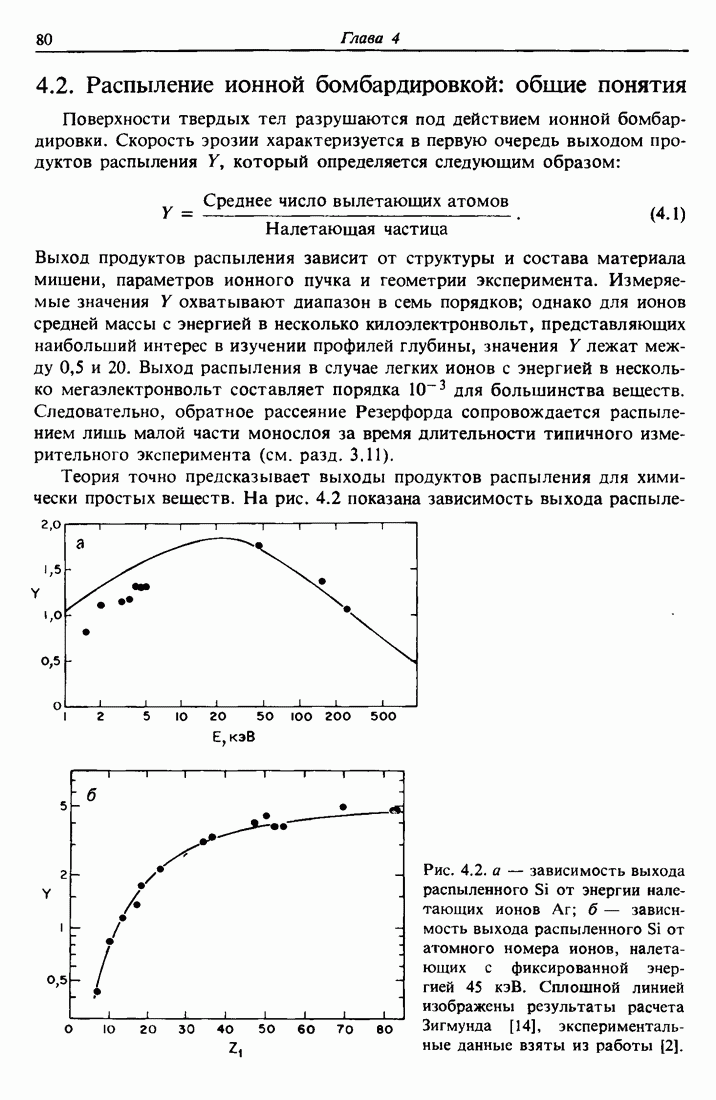
- 4.2. Распыление ионной бомбардировкой: общие понятия
- 4.3. Ядерные потери энергии
- 4.4. Выход продуктов распыления
- 4.5. Масс-спектрометрия вторичных ионов (SIMS)
- 4.6. Масс-спектрометрия вторичных нейтральных частиц (SNMS)
- 4.7. Избирательное распыление элементов и анализ их распределения по глубине
- 4.8. Уширение внутренней границы раздела и ионное перемешивание
- 4.9. Статистическая модель атома Томаса — Ферми
- Задачи
- Глава 5. КАНАЛИРОВАНИЕ
- 5.2. Каналирование в монокристаллах
- 5.3. Определение месторасположения примесей в кристаллах
- 5.4. Распределение потока каналированных частиц
- 5.5. Поверхностное взаимодействие в двухатомной модели
- 5.6. Поверхностный пик
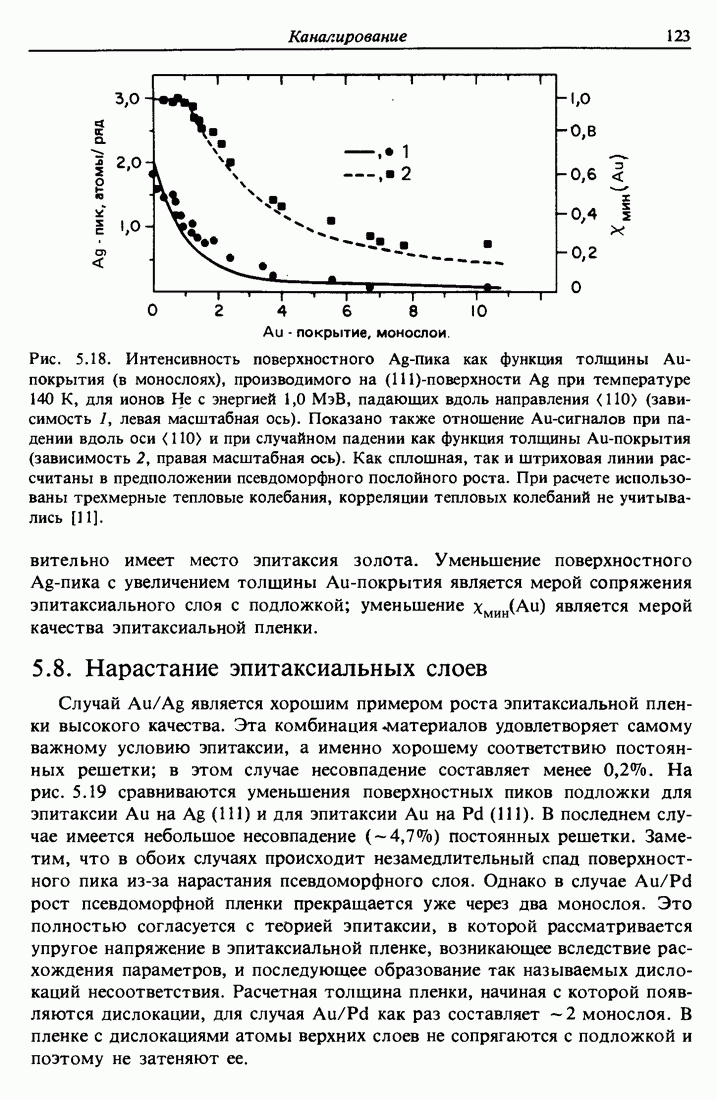
- 5.7. Затенение подложки Ag (111) эпитаксиальным Au
- 5.8. Нарастание эпитаксиальных слоев
- 5.9. Анализ тонких пленок
- Задачи
- Глава 6. ЭЛЕКТРОН-ЭЛЕКТРОННЫЕ ВЗАИМОДЕЙСТВИЯ И ЧУВСТВИТЕЛЬНОСТЬ К ГЛУБИНЕ В ЭЛЕКТРОННОЙ СПЕКТРОСКОПИИ
- 6.2. Анализ энергии в электронной спектроскопии
- 6.3. Глубина выхода электронов и исследуемый объем вещества
- 6.4. Неупругие электрон-электронные столкновения
- 6.5. Сечение ударной электронной ионизации
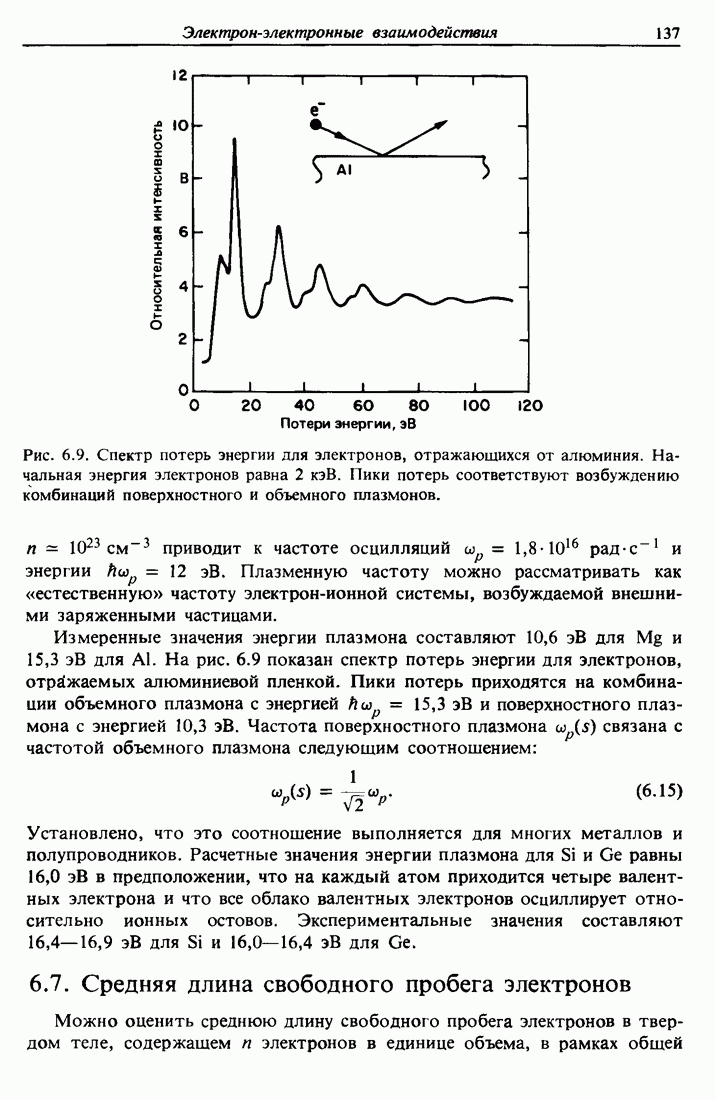
- 6.6. Плазмоны
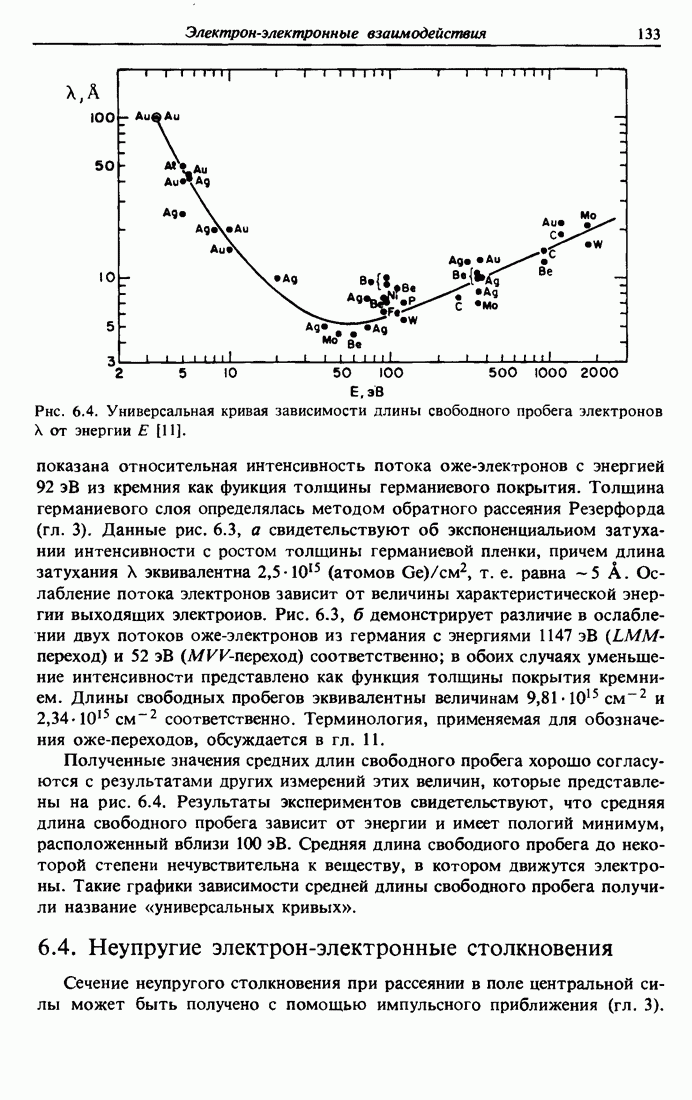
- 6.7. Средняя длина свободного пробега электронов
- 6.8. Влияние морфологии тонких пленок на уменьшение выхода электронов
- 6.9. Пробеги электронов в твердых телах
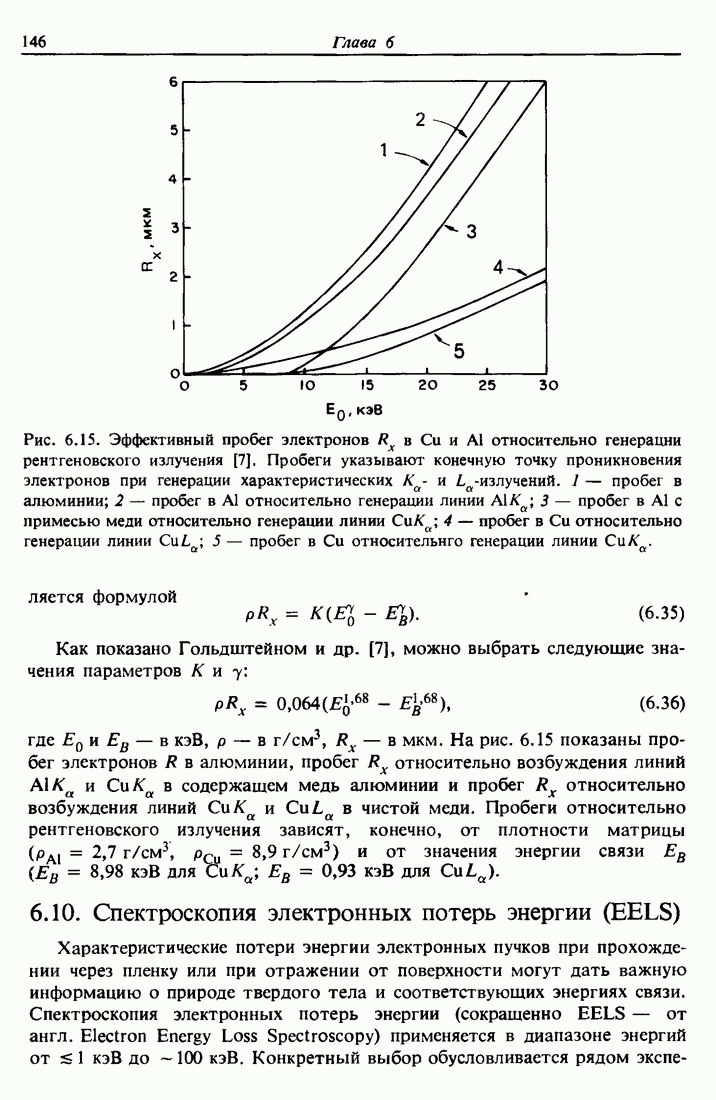
- 6.10. Спектроскопия электронных потерь энергии (EELS)
- 6.11. Тормозное излучение
- Задачи
- Глава 7. СТРУКТУРА ПОВЕРХНОСТИ
- 7.2. Параметры дифракции
- 7.3. Тепловые колебания и фактор Дебая — Валлера
- 7.4. Дифракция электронов низких энергий (LEED)
- 7.5. Дифракция рентгеновских лучей при скользящем падении
- 7.6. Просвечивающая электронная микроскопия
- Задачи
- Глава 8. ПОГЛОЩЕНИЕ ФОТОНОВ В ТВЕРДЫХ ТЕЛАХ И EXAFS
- 8.2. Уравнение Шредингера
- 8.3. Волновые функции
- 8.4. Квантовые числа, электронные конфигурации и обозначения
- 8.5. Вероятность переходов
- 8.6. Фотоэлектрический эффект в приближении прямоугольной ямы
- 8.7. Вероятность фотоэлектронных переходов для водородоподобного атома
- 8.8. Поглощение рентгеновского излучения
- 8.9. Растянутая тонкая структура рентгеновского поглощения (EXAFS)
- 8.10. Нестационарная теория возмущений
- Задачи
- Глава 9. РЕНТГЕНОВСКАЯ ФОТОЭЛЕКТРОННАЯ СПЕКТРОСКОПИЯ (XPS)
- 9.2. Экспериментальная техника
- 9.3. Кинетическая энергия фотоэлектронов
- 9.4. Энергетический спектр фотоэлектронов
- 9.5. Энергия связи и влияние конечных состояний
- 9.6. Сдвиги энергии связи; химические сдвиги
- 9.7. Количественный анализ
- Задачи
- Глава 10. ИЗЛУЧАТЕЛЬНЫЕ ПЕРЕХОДЫ И ЭЛЕКТРОННЫЙ МИКРОАНАЛИЗ
- 10.2. Обозначения в рентгеновской спектроскопии
- 10.3. Дипольные правила отбора
- 10.4. Электронный микроанализ
- 10.5. Скорости переходов при спонтанном излучении
- 10.6. Скорость перехода для излучения Ка в никеле
- 10.7. Электронный микроанализ: количественные результаты
- 10.8. Испускание рентгеновского излучения, возбуждаемого протонами и ионами гелия (PIXE)
- 10.9. Расчет вероятности излучательных переходов
- 10.10. Расчет отношения интенсивностей линий
- Задачи
- Глава 11. НЕИЗЛУЧАТЕЛЬНЫЕ ПЕРЕХОДЫ И ОЖЕ-ЭЛЕКТРОННАЯ СПЕКТРОСКОПИЯ
- 11.2. Оже-переходы
- 11.3. Выход оже-электронов и флюоресценция
- 11.4. Ширина атомных уровней и времена жизни
- 11.5. Оже-электронная спектроскопия
- 11.6. Количественный анализ
- 11.7. Получение профилей концентрации с помощью оже-спектроскопии
- Задачи
- Глава 12. АКТИВАЦИОННЫЙ И МГНОВЕННОРАДИАЦИОННЫЙ ЯДЕРНЫЕ МЕТОДЫ АНАЛИЗА
- 12.2. Значения Q и кинетические энергии
- 12.3. Радиоактивный распад
- 12.4. Закон радиоактивного распада
- 12.5. Получение радионуклидов
- 12.6. Активационный анализ
- 12.7. Мгновеннорадиационный анализ
- Задачи
- ПРИЛОЖЕНИЕ 1.
- ПРИЛОЖЕНИЕ 2.
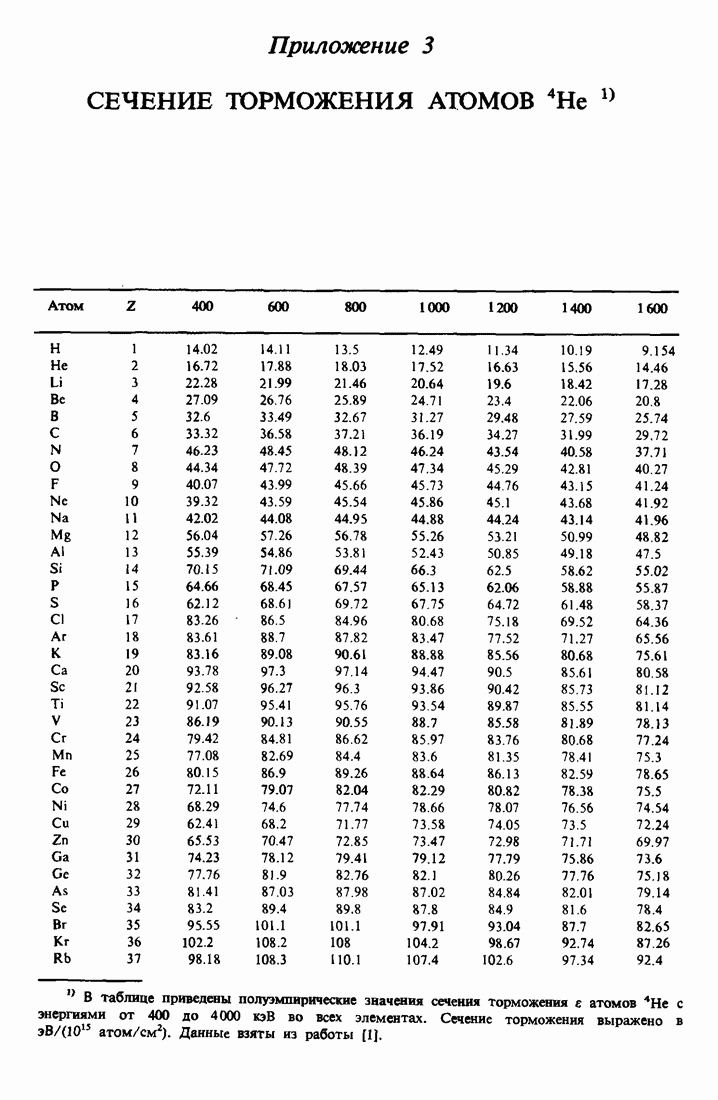
- ПРИЛОЖЕНИЕ 3.
- ПРИЛОЖЕНИЕ 4.
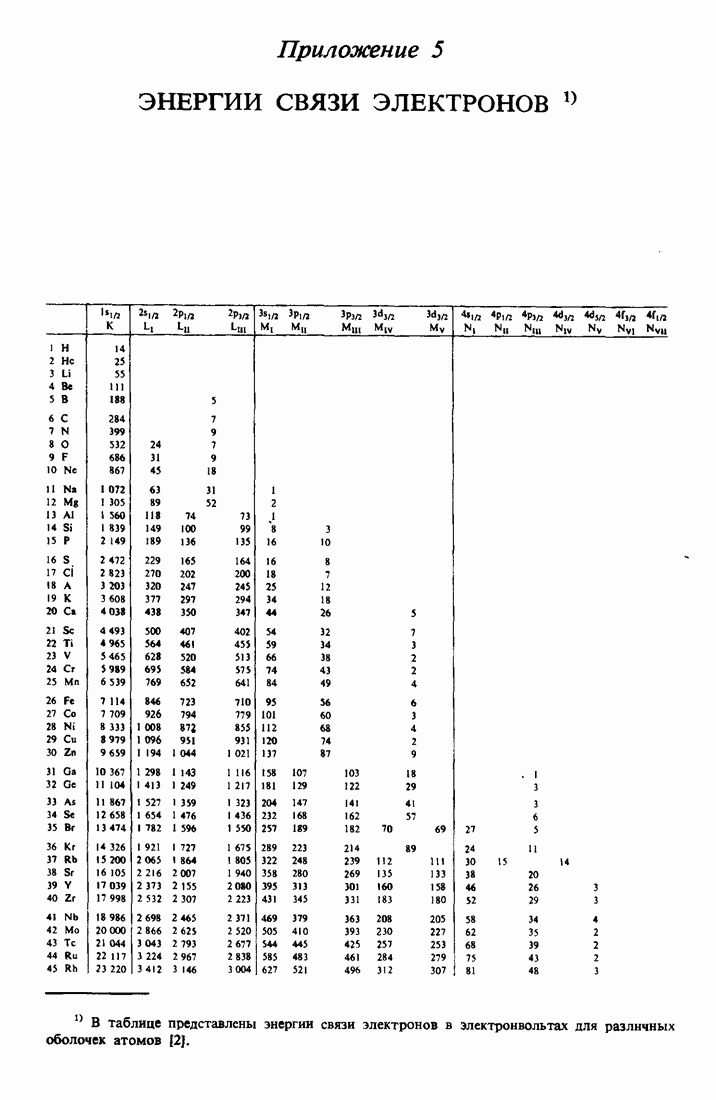
- ПРИЛОЖЕНИЕ 5. ЭНЕРГИИ СВЯЗИ ЭЛЕКТРОНОВ
- ПРИЛОЖЕНИЕ 6А. ВОЛН РЕНТГЕНОВСКОГО ИЗЛУЧЕНИЯ [3,4]
- ПРИЛОЖЕНИЕ 6б. МАССОВЫЕ КОЭФФИЦИЕНТЫ ПОГЛОЩЕНИЯ И ПЛОТНОСТЬ [4—6]
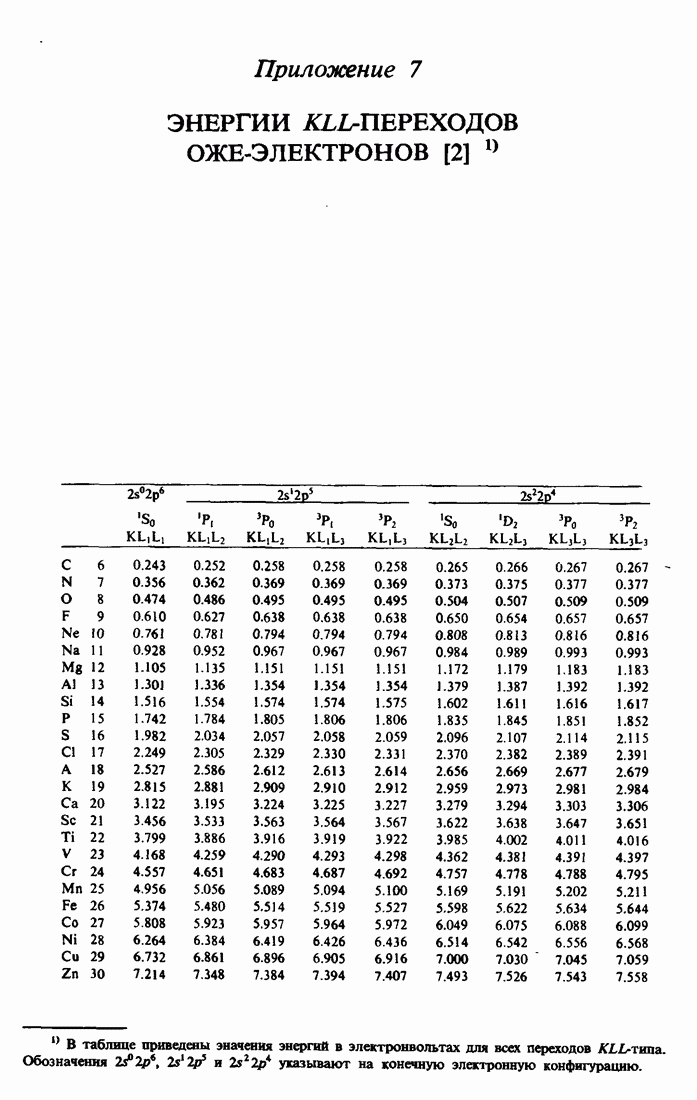
- ПРИЛОЖЕНИЕ 7. ЭНЕРГИИ KLL-ПЕРЕХОДОВ ОЖЕ-ЭЛЕКТРОНОВ [2]
- ПРИЛОЖЕНИЕ 8. ТАБЛИЦА ЭЛЕМЕНТОВ [7]
- ПРИЛОЖЕНИЕ 9.
- ПРИЛОЖЕНИЕ 10. ФИЗИЧЕСКИЕ ПОСТОЯННЫЕ, ПОЛЕЗНЫЕ КОМБИНАЦИИ И СООТНОШЕНИЯ ЕДИНИЦ