| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
Общие сведения. В биологическом материале свободные пуриновые и пиримидиновые основания встречаются в небольших количествах. Они, как известно, являются компонентами дезоксирибонуклеиновых и нуклеиновых кислот и освобождаются при их гидролитическом расщеплении. Подвергая гидролизу ДНК действием концентрированных растворов минеральных кислот (например, 6 н соляной кислоты или 12 н хлорной) при 100° С, можно добиться почти количественного освобождения пуриновых
и пиримидиновых оснований. Для высвобождения нуклеозидов и нуклеотидов следует применять более мягкий метод — энзиматический.
Значительно легче гидролизуются рибонуклеиновые кислоты. Уже  раствор серной или соляной кислот расщепляют РНК до пуриновых оснований и пиримидиновых нуклеотидов. Этот способ гидролиза позволяет установить неодинаковую прочность гликозидных связей в пуриновых и пиримидиновых нуклеотидах, так как последние в описанных условиях почти не подвергаются дальнейшему расщеплению. Пиримидиновые основания освобождаются лишь при гидролизе РНК 12 н раствором хлорной кислоты (1ч при 100°С).
раствор серной или соляной кислот расщепляют РНК до пуриновых оснований и пиримидиновых нуклеотидов. Этот способ гидролиза позволяет установить неодинаковую прочность гликозидных связей в пуриновых и пиримидиновых нуклеотидах, так как последние в описанных условиях почти не подвергаются дальнейшему расщеплению. Пиримидиновые основания освобождаются лишь при гидролизе РНК 12 н раствором хлорной кислоты (1ч при 100°С).
Для того чтобы выделить свободные мононуклеотиды, проводят гидролитическое расщепление РНК 0,3 н раствором едкого натра в течение 18 ч при температуре 37° С.
Стандартные растворы. Готовят раствор свободных пуриновых и пиримидиновых оснований  ) в 10%-ном растворе изопропанола, к которому добавляют 10% уксусной кислоты.
) в 10%-ном растворе изопропанола, к которому добавляют 10% уксусной кислоты.
Гуанин растворяют (в количестве 1 мг/мл) в 0,1 н растворе соляной кислоты.
Нуклеозиды и нуклеотиды (в концентрации 4 мг/мл) растворяют в  -ном растворе изопропанола. Их стандартные растворы сохраняют в морозильной камере холодильника при температуре
-ном растворе изопропанола. Их стандартные растворы сохраняют в морозильной камере холодильника при температуре  .
.
На хроматограммы наносят по  растворов.
растворов.
Системы растворителей.
Употребляют следующие системы растворителей.
I. Смесь бутанола, уксусной кислоты и воды 
5). Применяют для разделения смеси оснований, а также пуриновых и пиримидиновых нуклеозидов и нуклеотидов.
II. Смесь изопропанола, концентрированной соляной кислоты и воды  Используют для разделения свободных пуриновых и пиримидиновых оснований. В этой смеси разделение происходит медленно. Хроматограммы высушивают на воздухе при комнатной температуре. Для того чтобы удалить следы соляной кислоты, высушенную хроматограмму выдерживают несколько минут над кипящей водяной баней, а затем снова сушат на воздухе.
Используют для разделения свободных пуриновых и пиримидиновых оснований. В этой смеси разделение происходит медленно. Хроматограммы высушивают на воздухе при комнатной температуре. Для того чтобы удалить следы соляной кислоты, высушенную хроматограмму выдерживают несколько минут над кипящей водяной баней, а затем снова сушат на воздухе.
В табл. 3 представлены данные, характеризующие
Табл. 3. Значение  пуриновых и пиримидиновых оснований, нуклеозидов и нуклеотидов (бумага ватман № 1)
пуриновых и пиримидиновых оснований, нуклеозидов и нуклеотидов (бумага ватман № 1)

значения  пуриновых и пиримидиновых оснований, а также нуклеозидов и нуклеотидов в описанных системах растворителей.
пуриновых и пиримидиновых оснований, а также нуклеозидов и нуклеотидов в описанных системах растворителей.
Проявители. Проявители реагируют с пуриновыми и пиримидиновыми основаниями, пентозами и остатками фосфорной кислоты.
Ультрафиолетовые лучи. Пуриновые и пиримидиновые основания, а также нуклеозиды и нуклеотиды, в состав которых они входят, поглощают ультрафиолетовые лучи в границах 250—280 нм. При просмотре хроматограмм в ультрафиолетовых лучах они становятся заметными в виде темных пятен на светло-голубом флуоресцирующем фоне бумаги. Границы пятен очерчивают графитовым карандашом.
Азотнокислое серебро — двухромовокислый натрий. Является реактивом на пуриновые основания. В состав проявителя входят: а) азотнокислое серебро, 2%-ный раствор; б) двухромовокислый натрий (бихромат натрия), 0,5%;-ный раствор; в) азотная кислота, 0,5 н раствор.
Хроматограмму опрыскивают раствором азотнокислого серебра, после чего погружают в раствор бихромата натрия. Выпадает красный осадок хромата серебра. Затем хроматограмму переносят в раствор азотной кислоты, в котором происходит медленное растворение осадка. Красная окраска остается лишь в местах комплекса хромата серебра с аденином и гуанином. Если при этом фон хроматограммы сохраняет еще розовую окраску, бумагу следует перенести в сосуд с водой и несколько раз прополоскать.
Ртутный проявитель. С его помощью можно открыть пиримидиновые основания — урацил, цитозин, тимин.
Хроматограмму погружают на 30 секунд в раствор, состоящий из 1 части 0,1 М раствора уксуснокислой ртути, 3 частей 1 М раствора уксуснокислого натрия и 6 частей воды. Затем хроматограмму перекладывают на 20 секунд в кювету с проточной водой, после чего сразу же погружают в  -ный раствор сернокислого аммония до появления черных пятен.
-ный раствор сернокислого аммония до появления черных пятен.
Проявитель на фосфорную кислоту. Состоит из четырех компонентов: а) раствор молибденовокислого аммония (1 г соли в 8 мл воды); б) соляная кислота, концентрированная; в) хлорная кислота,  раствор; г) ацетон. Перечисленные компоненты смешивают в отношении
раствор; г) ацетон. Перечисленные компоненты смешивают в отношении  (перед употреблением). Указанной смесью опрыскивают хроматограмму, которую затем высушивают при комнатной температуре и освещают ультрафиолетовыми лучами (кварцевой лампой) в течение 30 мин. Соединения, в состав которых входят фосфатные группы, дают голубые пятна. Голубой оттенок фона можно снять парами аммиака.
(перед употреблением). Указанной смесью опрыскивают хроматограмму, которую затем высушивают при комнатной температуре и освещают ультрафиолетовыми лучами (кварцевой лампой) в течение 30 мин. Соединения, в состав которых входят фосфатные группы, дают голубые пятна. Голубой оттенок фона можно снять парами аммиака.
Хроматографическая идентификация продуктов гидролиза ДНК.
Реактивы и материалы: а) препарат  соляная кислота, 6 н раствор, в) соляная кислота, 0,1 н раствор, г) хроматографическая бумага ватман № 1 или
соляная кислота, 6 н раствор, в) соляная кислота, 0,1 н раствор, г) хроматографическая бумага ватман № 1 или  стандартные растворы пуриновых и пиримидиновых оснований (см. с. 62); е) системы растворителей I и II (см. с. 62); ж) проявитель азотнокислое серебро — двухромовокислый натрий; з) ртутный проявитель.
стандартные растворы пуриновых и пиримидиновых оснований (см. с. 62); е) системы растворителей I и II (см. с. 62); ж) проявитель азотнокислое серебро — двухромовокислый натрий; з) ртутный проявитель.
Г идролиз. 5—20 мг препарата ДНК вносят в пробирку, туда же прибавляют  н раствора соляной
н раствора соляной
кислоты. Пробирку запаивают и помещают в сушильный шкаф при 100° С на 3 ч. Полученный гидролизат досуха испаряют в вакуумном эксикаторе (над твердым КОН). Остаток растворяют в таком количестве 0,1 н раствора соляной кислоты, чтобы получить  раствор (учитывая количество ДНК, взятой для гидролиза).
раствор (учитывая количество ДНК, взятой для гидролиза).
Хроматография. Берут четыре листа хроматографической бумаги размерами 12X40 см. На середину линии старта наносят по 5 мкл исследуемого гидролизата, а по сторонам — стандартные растворы пуриновых и пиримидиновых оснований. Раствор гуанина наносят только на лист № 4.
Хроматограммы № 1 и 2 ставят в сосуды с системой растворителей I, а № 3 и 4 — в сосуды с системой II. Хроматографию продолжают до тех пор, пока фронт растворителя не поднимется хотя бы на 20 см (в системе I это продолжается около 3 ч, в системе II — 22-24 ч).
Хроматограммы высушивают (см. выше) и просматривают в ультрафиолетовых лучах. Пятна азотистых оснований очерчивают графитовым карандашом, после чего хроматограммы № 1 и 2 обрабатывают ртутным проявителем, а листы № 3 и 4 — проявителем азотнокислое серебро —двухромовокислый натрий. Определяют  соединений и с помощью табл. 3 производят их идентификацию.
соединений и с помощью табл. 3 производят их идентификацию.
Хроматографическая идентификация продуктов гидролиза РНК.
Реактивы и материалы: а) препарат РНК; б) соляная кислота, 1 н раствор; в)хроматографическая бумага ватман № 1 или  стандартные растворы пуриновых и пиримидиновых оснований; д) система растворителей II (см. с. 62); е) проявитель азотнокислое серебро — двухромовокислый натрий;
стандартные растворы пуриновых и пиримидиновых оснований; д) система растворителей II (см. с. 62); е) проявитель азотнокислое серебро — двухромовокислый натрий;
ж) проявитель на фосфорную кислоту (см. с. 64);
з) проявитель на а-диоловую группу: 1) иоднокислый калий (перйодат калия,  ), насыщенный раствор (около
), насыщенный раствор (около  бензидин, 0,1 М раствор в 50%-ном метаноле. Раствор бензидина смешивают с ацетоном и 0,2 н раствором соляной кислоты в отношении
бензидин, 0,1 М раствор в 50%-ном метаноле. Раствор бензидина смешивают с ацетоном и 0,2 н раствором соляной кислоты в отношении  3) бензидин, 0,1 М раствор в 50%,-ном метаноле, смешанный с 0,8 н раствором соляной кислоты в отношении 1: 1.
3) бензидин, 0,1 М раствор в 50%,-ном метаноле, смешанный с 0,8 н раствором соляной кислоты в отношении 1: 1.
Хроматограмму опрыскивают раствором 1, а через  раствором 2. Соединения, имеющие а-диоловую группу, дают белые пятна на голубом фоне.
раствором 2. Соединения, имеющие а-диоловую группу, дают белые пятна на голубом фоне.
С помощью этого же проявителя можно отличить кетозы и аминосахара от других соединений с а-диоловой группой. Для этого проявленную хроматограмму дополнительно опрыскивают раствором 3 и прогревают 1 мин. при 110°. Пятна кетоз и аминосахаров остаются белыми, тогда как остальных соединений принимают голубое окрашивание.
Гидролиз. 10 мг исследуемого препарата РНК вносят в пробирку с 1 мл 1 н раствора соляной кислоты. Пробирку запаивают и выдерживают 1 ч в сушильном шкафу при 100° С. Гидролизат охлаждают.
Хроматография. На листе хроматографической бумаги линию старта делят на три отрезка по 8 см. В каждом из них отмечают три точки. Отрезок А предназначен для идентификации пуриновых оснований гидролизата, В и С — для пиримидиновых оснований.
В среднюю точку каждого отрезка наносят по 5 мкл гидролизата, а в крайние — соответствующие стандартные растворы. Хроматографию проводят в системе II в течение 22-24 ч. За это время растворитель должен подняться по бумаге не менее чем на 20 см.
Хроматограмму высушивают на воздухе, просматривают в ультрафиолетовых лучах, пятна очерчивают графитовым карандашом, после чего бумагу разрезают на полоски, соответствующие отрезкам А, В и С. Отрезок А проявляют проявителем азотнокислое серебро — двухромовокислый натрий, В — проявителем на фосфорную кислоту, а отрезок С — проявителем на а-диолы.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
- ВИТАМИН В: (ТИАМИН)
- ВИТАМИН В2 (РИБОФЛАВИН)
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
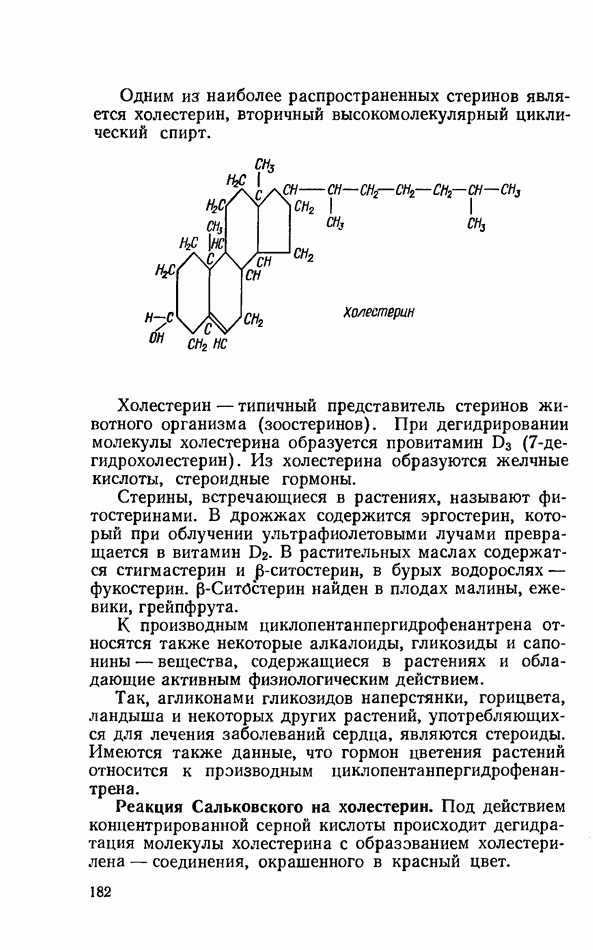
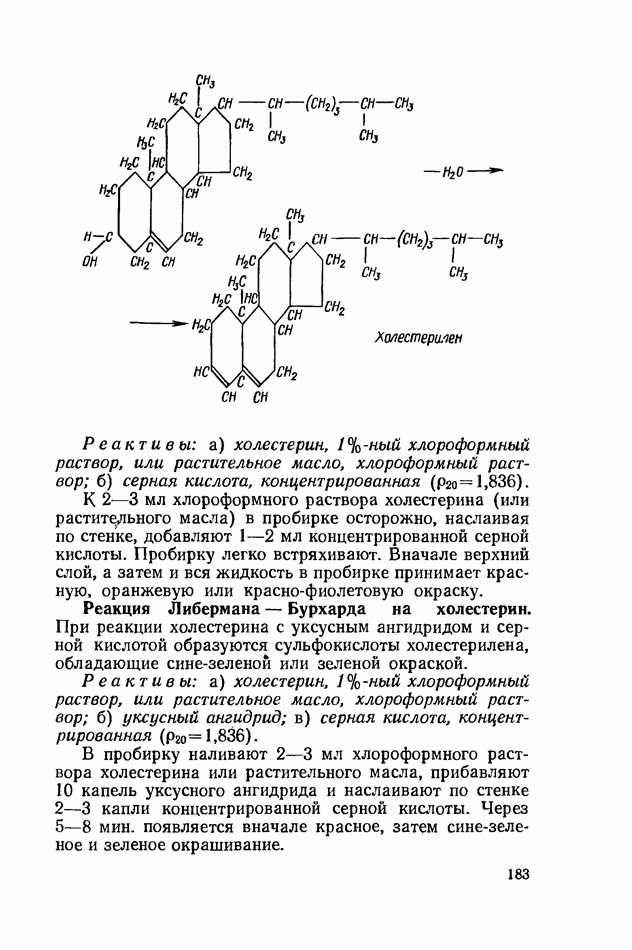
- СТЕРИНЫ
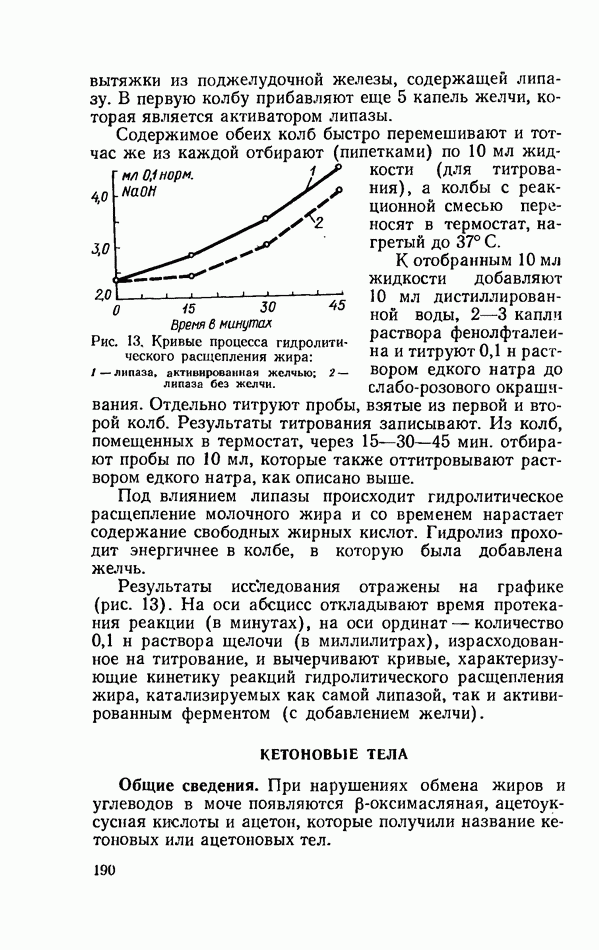
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
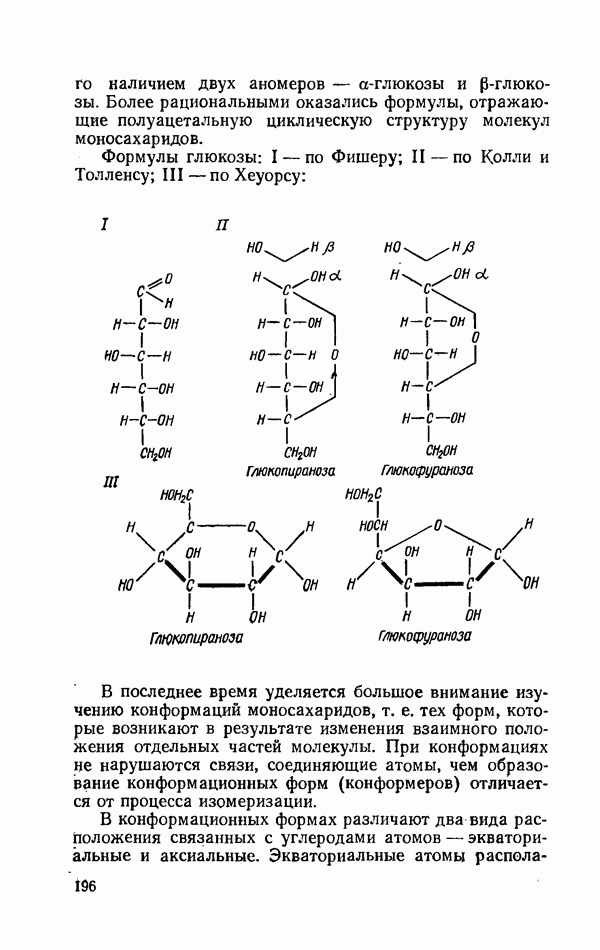
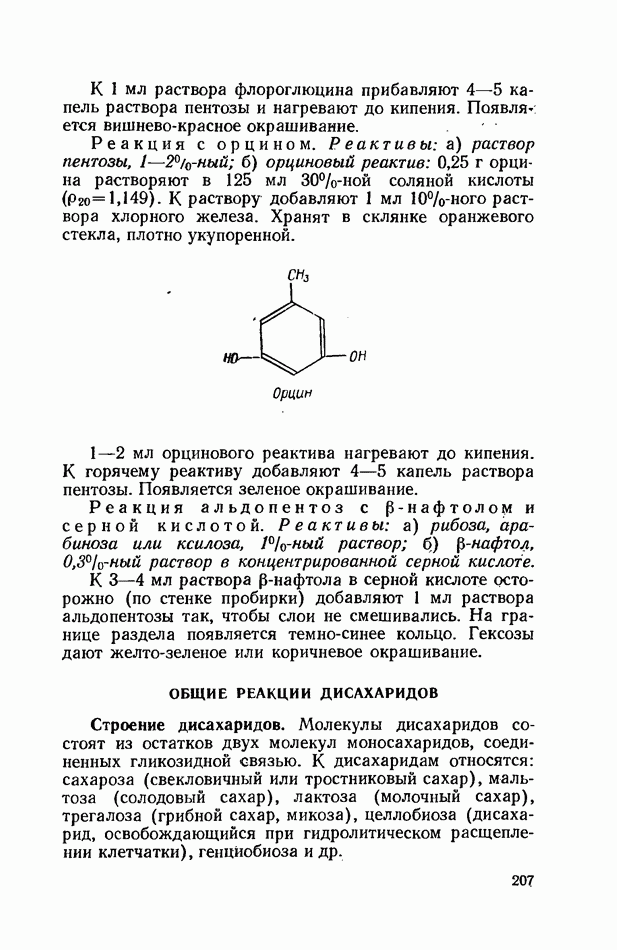
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
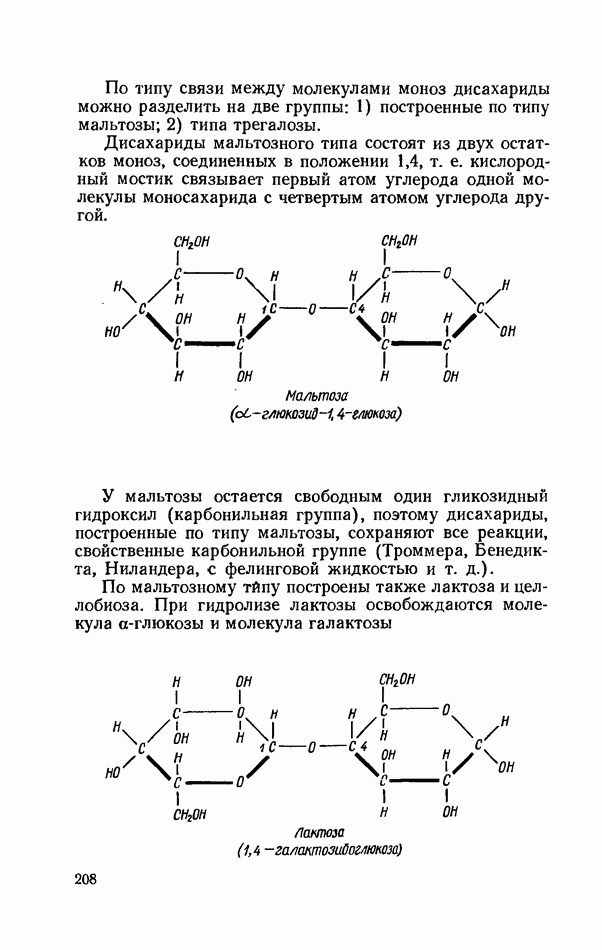
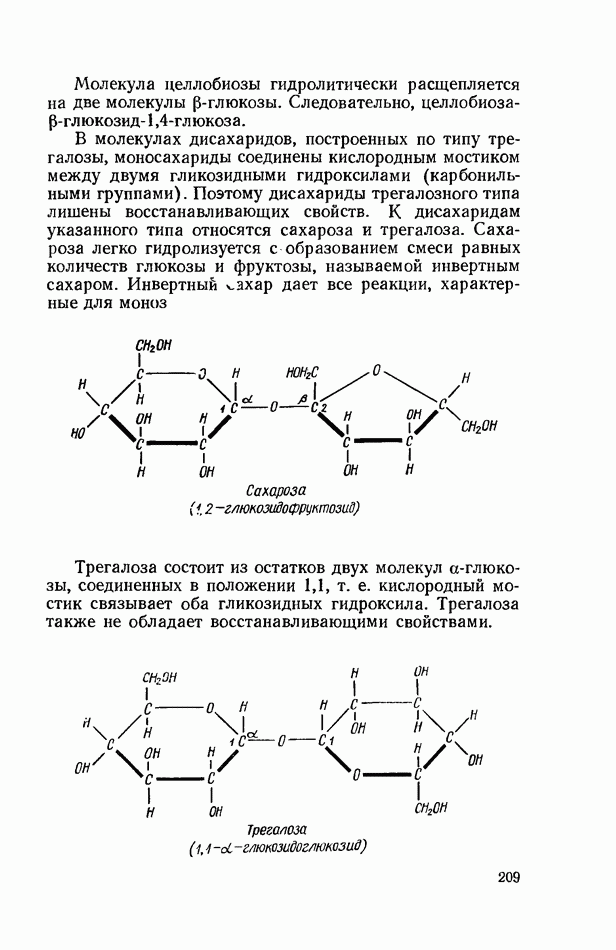
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
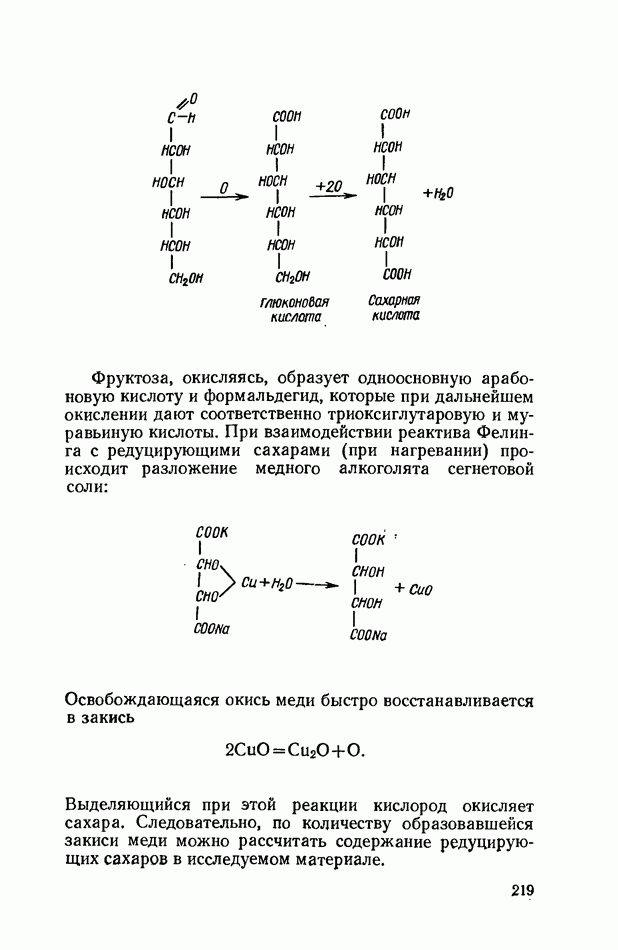
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
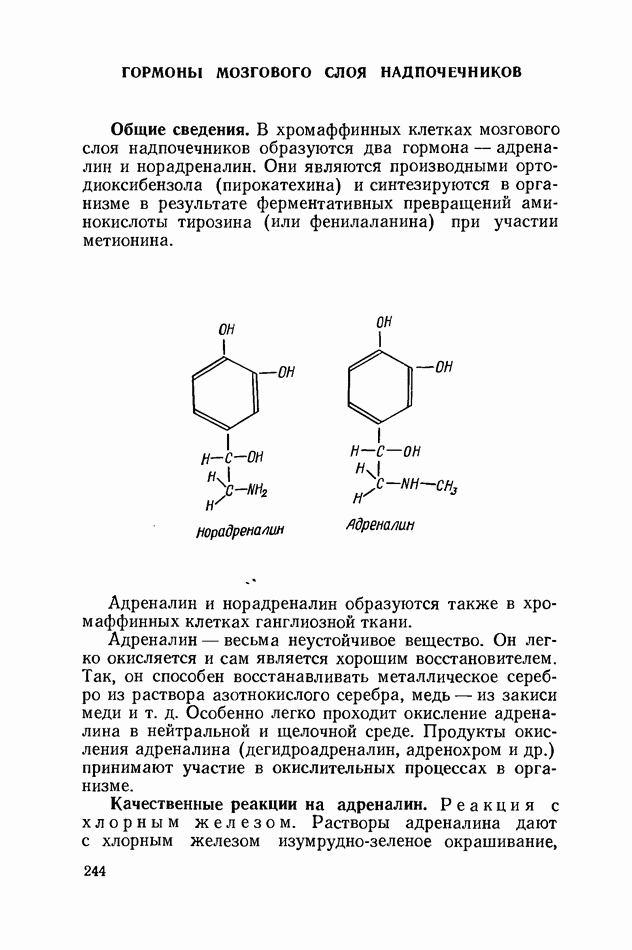
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
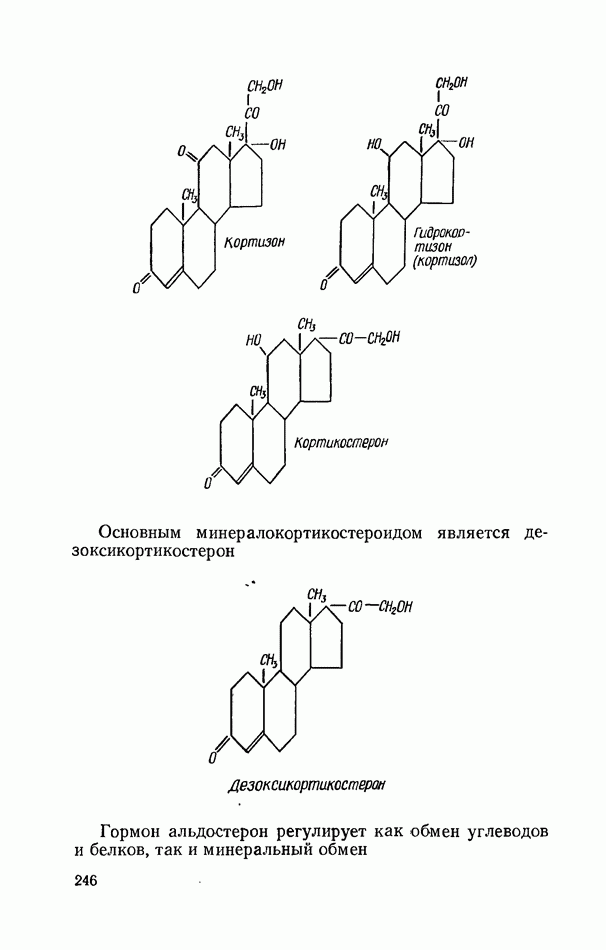
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
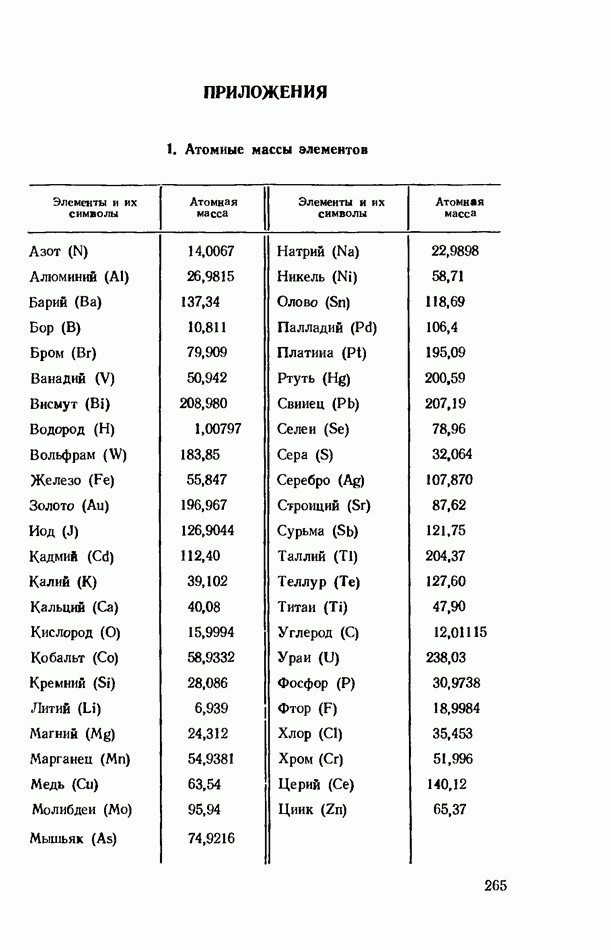
- ПРИЛОЖЕНИЯ