| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
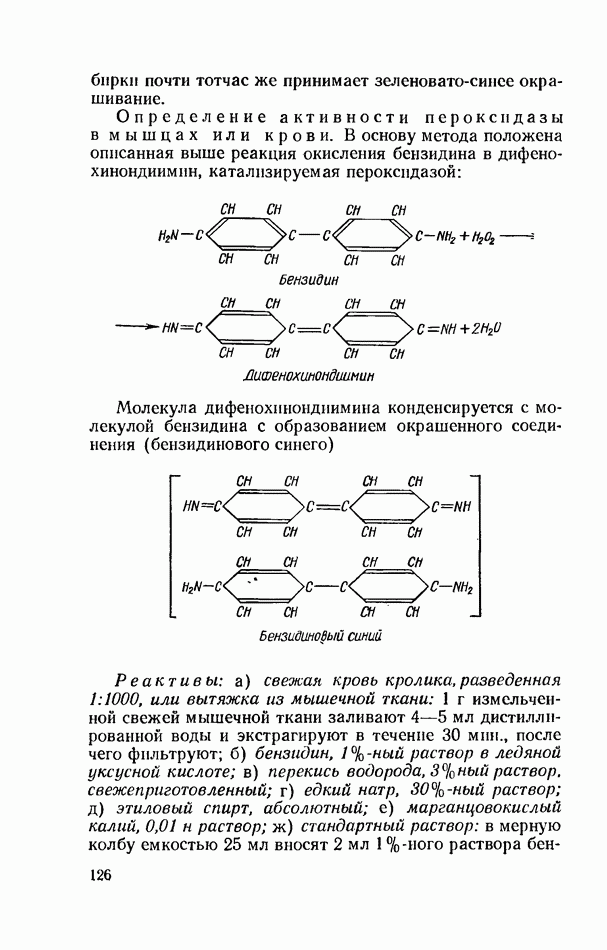
Распределительная хроматография аминокислот на бумаге
Общие сведения. Хроматографический метод анализа открыт русским ученым М. С. Цветом в 1903 г. В настоящее время многочисленные виды хроматографического анализа широко используются в различных областях химии и биологии.
В зависимости от физико-химических факторов, определяющих основной механизм процесса, методы хроматографического анализа делят на четыре основных вида: адсорбционные, распределительные, ионообменные и осадочные.
Для разделения смеси аминокислот чаще всего применяют метод распределительной хроматографии на бумаге. Он основан на различной степени распределения компонентов смеси между двумя несмешивающимися жидкими фазами (неподвижной водной фазой и подвижной фазой органического растворителя).
Органический растворитель (например, фенол, насыщенный водой, или смесь н-бутилового спирта, ледяной уксусной кислоты и воды), проходя через полоску фильтровальной бумаги, увлекает за собой аминокислоты, раствор которых был нанесен на бумагу. Различные аминокислоты передвигаются по бумаге с неодинаковой скоростью. Скорость перемещения аминокислот зависит от многих факторов: строения молекулы аминокислот, их способности легче растворяться в органическом растворителе или воде, избирательной адсорбции на бумаге, типа бумаги, условий проведения анализа и т. д. Чем лучше растворяется аминокислота в органическом растворителе, тем больший путь она пройдет с ним по бумаге.
Приняты два способа хроматографического разделения аминокислот на бумаге — восходящий и нисходящий. При восходящем способе растворитель поднимается по бумаге снизу вверх, при нисходящем — сверху вниз. Положение отдельных аминокислот обнаруживают путем проявления — обработки высушенной бумаги раствором нингидрина и последующего нагревания ее при 100° С. На полоске бумаги (хроматограмме) отчетливо видны пятна фиолетового, синего, голубого, желтого, оранжевого, коричневого цвета.
Положение аминокислот на бумаге можно установить и без проявления, рассматривая хроматограмму в ультрафиолетовых лучах. Пятна отчетливо флуоресцируют в ультрафиолете.
Для каждой аминокислоты характерна скорость перемещения, которую выражают с помощью коэффициента  Коэффициентом
Коэффициентом  называют отношение пути, пройденного аминокислотой (от места ее нанесения на бумагу до середины пятна на хроматограмме), к расстоянию от места нанесения смеси аминокислот до фронта растворителя:
называют отношение пути, пройденного аминокислотой (от места ее нанесения на бумагу до середины пятна на хроматограмме), к расстоянию от места нанесения смеси аминокислот до фронта растворителя:

где а — расстояние от места нанесения раствора смеси аминокислот до середины пятна данной аминокислоты, мм; b — путь, пройденный растворителем, мм.
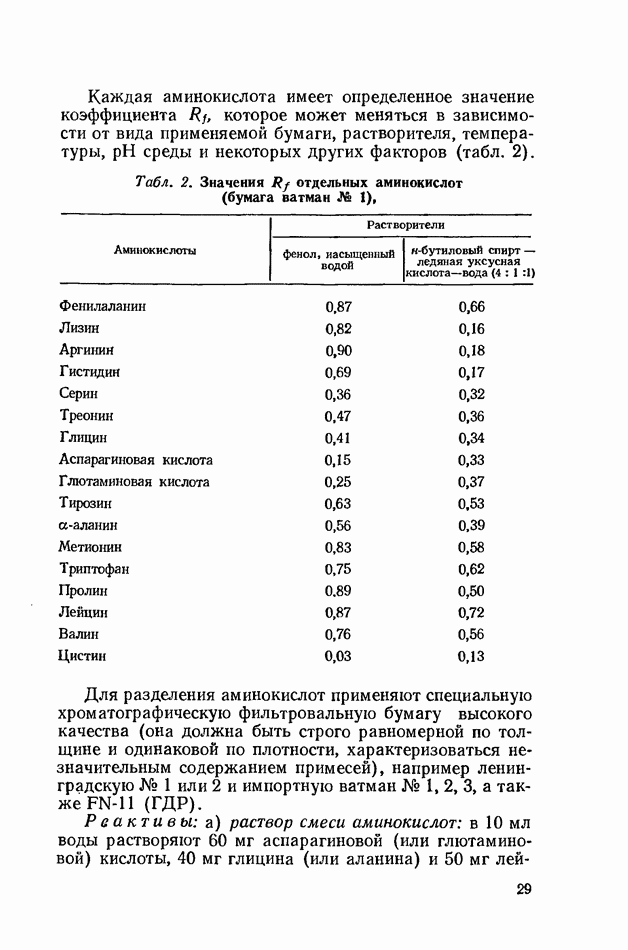
Каждая аминокислота имеет определенное значение коэффициента  которое может меняться в зависимости от вида применяемой бумаги, растворителя, температуры, pH среды и некоторых других факторов (табл. 2).
которое может меняться в зависимости от вида применяемой бумаги, растворителя, температуры, pH среды и некоторых других факторов (табл. 2).
Табл. 2. Значения  отдельных аминокислот (бумага ватман № 1),
отдельных аминокислот (бумага ватман № 1),

Для разделения аминокислот применяют специальную хроматографическую фильтровальную бумагу высокого качества (она должна быть строго равномерной по толщине и одинаковой по плотности, характеризоваться незначительным содержанием примесей), например ленинградскую № 1 или 2 и импортную ватман № 1, 2, 3, а также  (ГДР).
(ГДР).
Реактивы: а) раствор смеси аминокислот: в 10 мл воды растворяют 60 мг аспарагиновой (или глютаминовой) кислоты, 40 мг глицина (или аланина) и 50 мг лейцина;
б) фенол, насыщенный водой: к 100 г перегнанного фенола добавляют 35 мл воды и перемешивают, для ускорения растворения фенола смесь можно слегка подогреть; в) смесь н-бутанола, ледяной уксусной кислоты и воды (4:1:1 по объему): реактивы смешивают в указанном соотношении. Для того чтобы смесь не расслаивалась, рекомендуется дополнительно прибавить несколько капель уксусной кислоты; г) нингидрин, 0,2%-ный раствор в этиловом или бутиловом спирте.
Оборудование: а) термостат, отрегулированный на температуру 37—38° С; б) сушильный шкаф, отрегулированный на 100—105° С; в) пробирки стеклянные большого размера (длина 18—20 см, диаметр  см) с подобранными пробками; г) линейка с делениями на миллиметры; д) микропипетки; е) пульверизатор; ж) ножницы; з) игла с ниткой; и) штатив для пробирок.
см) с подобранными пробками; г) линейка с делениями на миллиметры; д) микропипетки; е) пульверизатор; ж) ножницы; з) игла с ниткой; и) штатив для пробирок.

Рис. 2. Упрощенный при бор для распределительной хроматографии аминокислот.
Материалы: Бумага фильтровальная хорошего качества (лучше пользоваться специальной хроматографической бумагой).
Вырезают полоску фильтровальной бумаги шириной 1,2 см, длиной 12—15 см (рис. 2). Один из концов полоски прокалывают иглой, протягивая нитку, которую завязывают петлей. На противоположном конце полоски, отступив на 1-1,5 см от ее края, графитовым карандашом очерчивают небольшой кружок (диаметром 3—5 мм), в который с помощью микропипетки вносят каплю раствора смеси аминокислот. Место нанесения раствора подсушивают на воздухе.
В сухую пробирку наливают около 1 мл насыщенного водой фенола или смеси  -бутанола, уксусной кислоты и воды, следя, чтобы при этом не смочить стенки. В пробирку осторожно (за нитку) опускают полоску бумаги, погружая ее нижний конец в растворитель на 2—3 мм (не более!), и закрепляют в висячем положении с помощью
-бутанола, уксусной кислоты и воды, следя, чтобы при этом не смочить стенки. В пробирку осторожно (за нитку) опускают полоску бумаги, погружая ее нижний конец в растворитель на 2—3 мм (не более!), и закрепляют в висячем положении с помощью
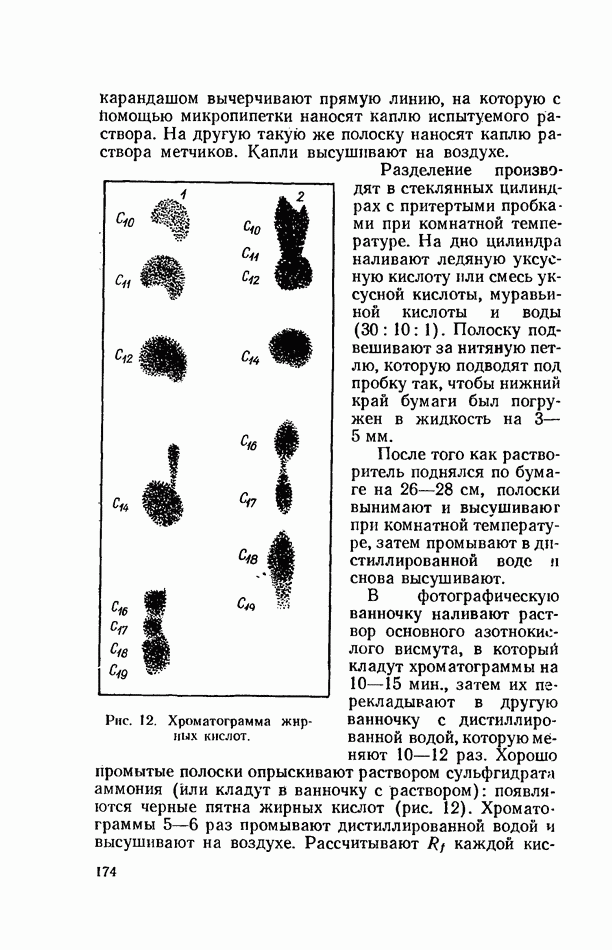
нитки и пробки. Полоска не должна касаться стенок пробирки. Пробирку ставят в термостат (при температуре 37—38°) на 1,5 ч, затем вынимают полоску и переносят ее на 10—12 мин. в сушильный шкаф, нагретый до 100—105°. В сушильном шкафу полоску подвешивают за нитяную петлю на стеклянную палочку. После испарения растворителя полоску вынимают из шкафа, опрыскивают раствором нингидрина (с помощью пульверизатора) и снова вносят в тот же сушильный шкаф на несколько минут. На хроматограмме появляются окрашенные пятна аминокислот (рис. 3). Линейкой измеряют расстояния:
а) от места нанесения капли раствора смеси аминокислот до середины данной кислоты;
б) от места нанесения капли раствора аминокислот до фронта растворителя. Рассчитывают  каждой аминокислоты.
каждой аминокислоты.

Рис. 3. Хроматограмма аминокислот.
Распределительная круговая хроматография аминокислот.
При круговой хроматографии вместо пятен аминокислот на бумаге получают концентрически расположенные кольца. В принципе метод остается таким же, как и в предыдущей работе. Хроматографирование проводят в эксикаторах небольшого размера.
Реактивы: см. «Распределительная хроматография аминокислот на бумаге».
Оборудование: а) эксикатор малого размера с хорошо притертой крышкой; б) термостат (37—38° С);
в) сушильный шкаф (100—105° С).
Из хорошей фильтровальной бумаги (лучше — специальной хроматографической) вырезают круг соответствующего диаметра (на 2—3 см больше диаметра узкой части эксикатора). Для того чтобы поступал растворитель, из круга вырезают «фитиль» — полоску, шириной 2— 3 мм (рис. 4).
На расстоянии 0,5-0,6 см от центра круга наносят каплю раствора смеси аминокислот и высушивают на воздухе.
Растворитель наливают в стеклянный стаканчик или фарфоровую чашечку или же прямо на дно эксикатора.
Бумажный круг кладут на выступ над узкой частью эксикатора. «Фитиль» отгибают и опускают в растворитель.

Рис. 4. Распределительная круговая хроматограмма аминокислот: 1 — бумажный фильтр; 2 — фитиль; 3 — растворитель.
Эксикатор плотно закрывают и ставят в термостат (37—38° С) на 1,5-2 ч, после чего с хроматограммой проделывают все те же операции, что и при хроматографировании на полосках бумаги.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
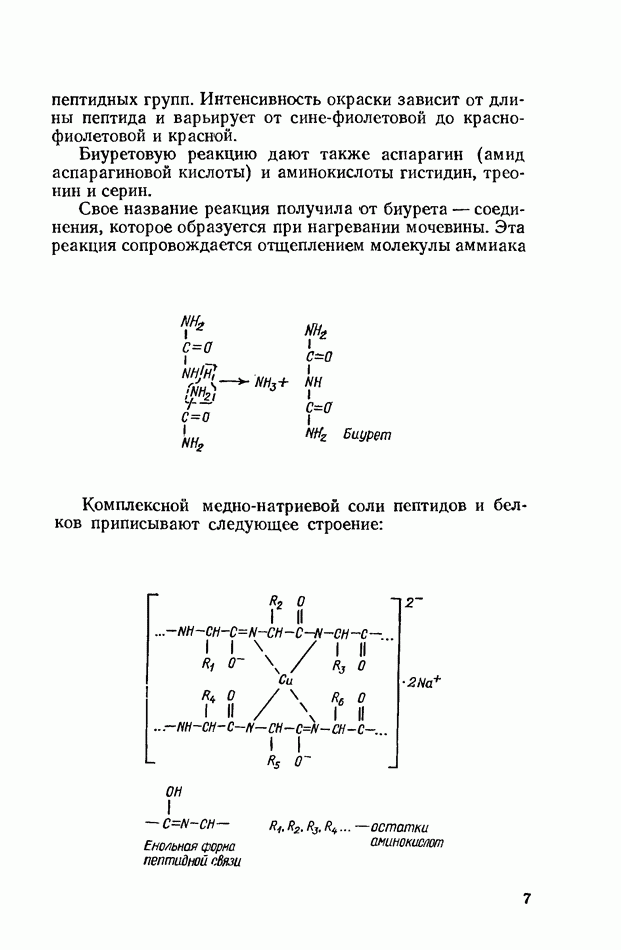
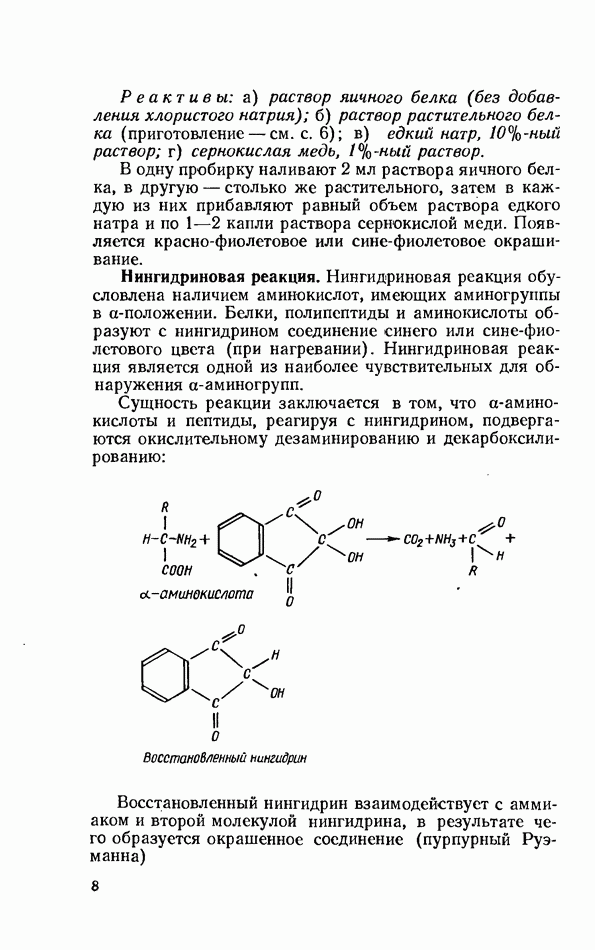
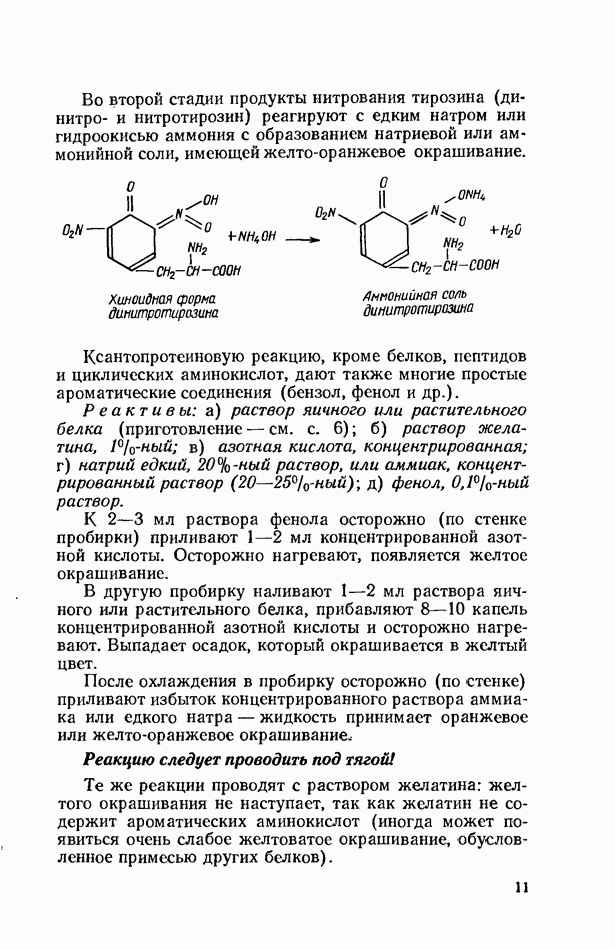
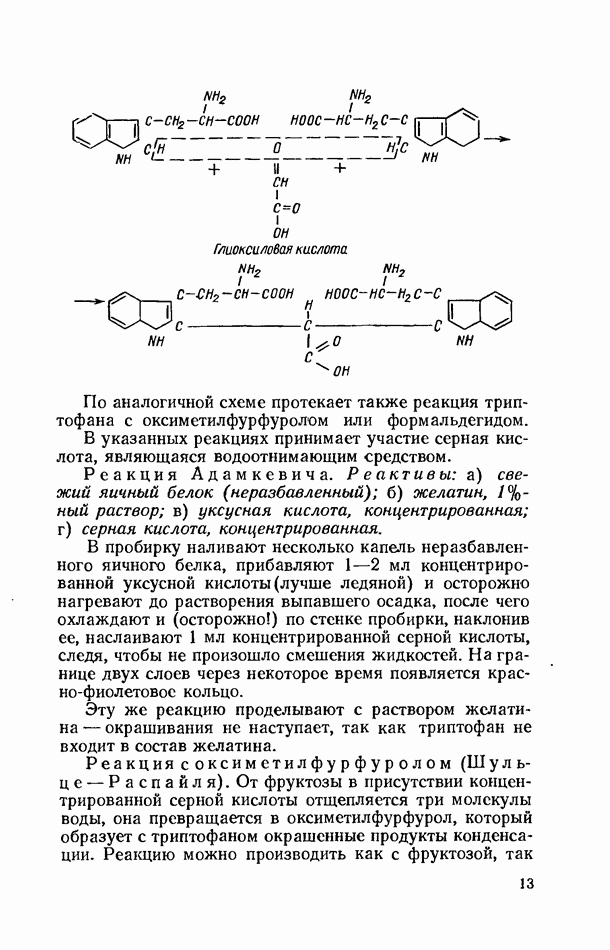
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
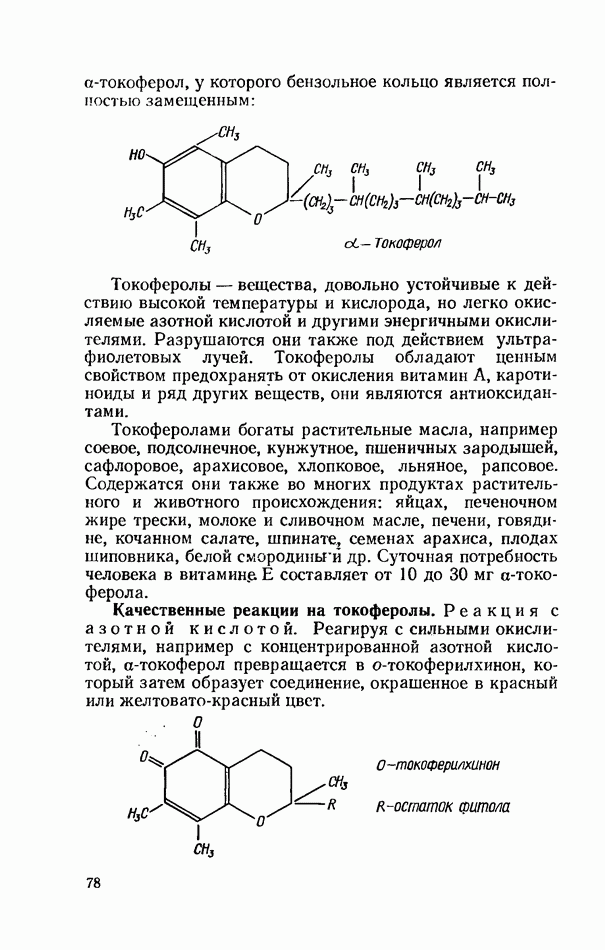
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
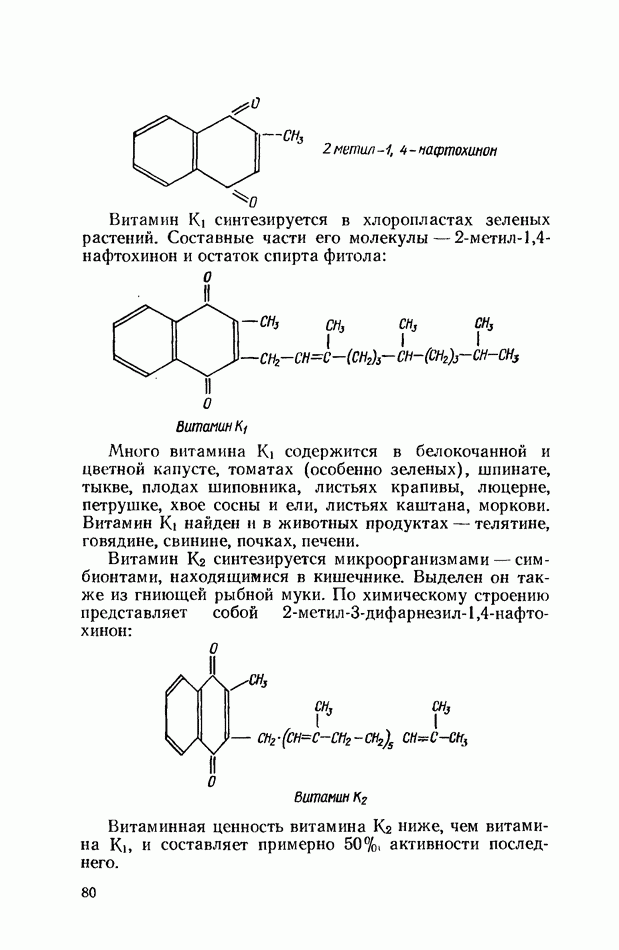
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
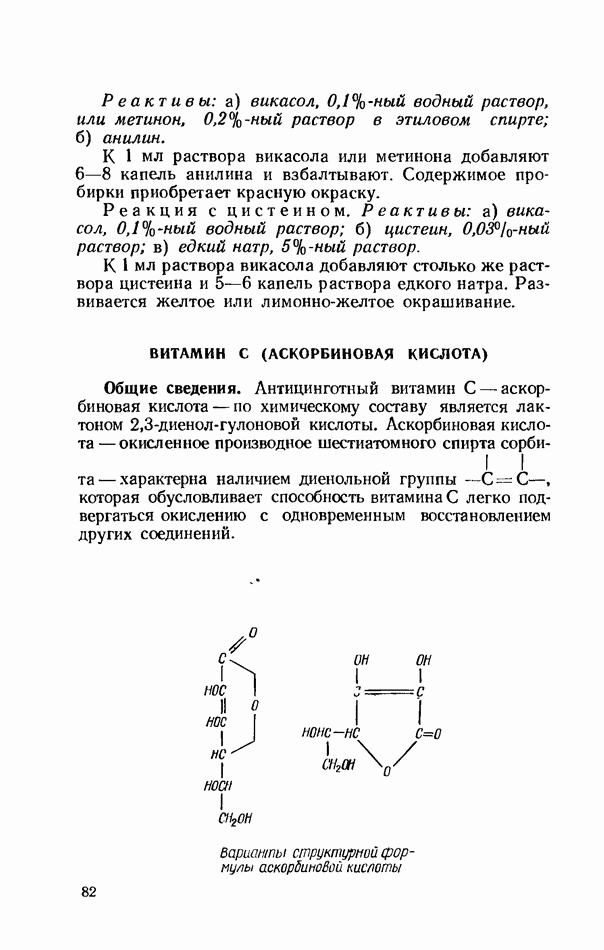
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
- ВИТАМИН В: (ТИАМИН)
- ВИТАМИН В2 (РИБОФЛАВИН)
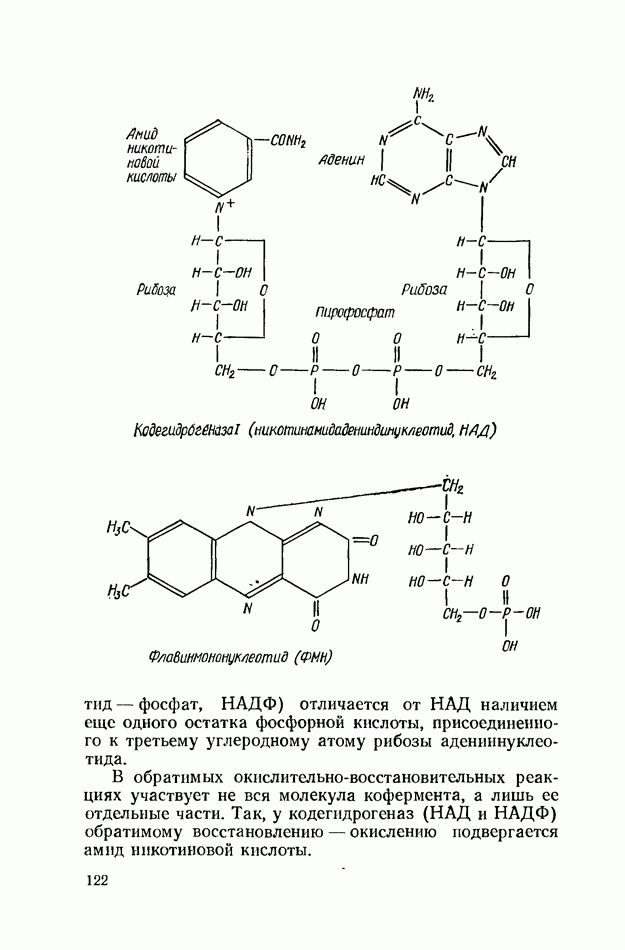
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
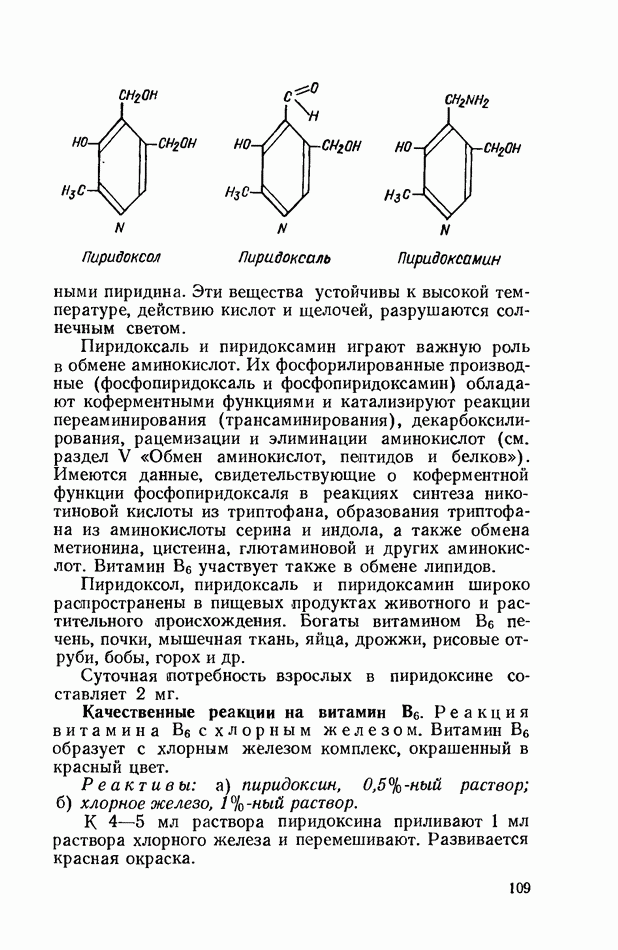
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
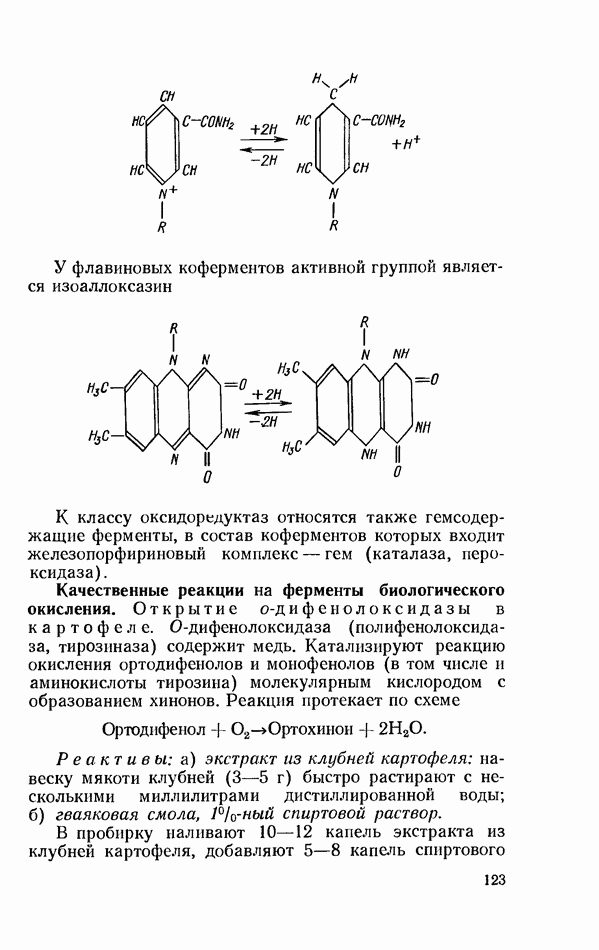
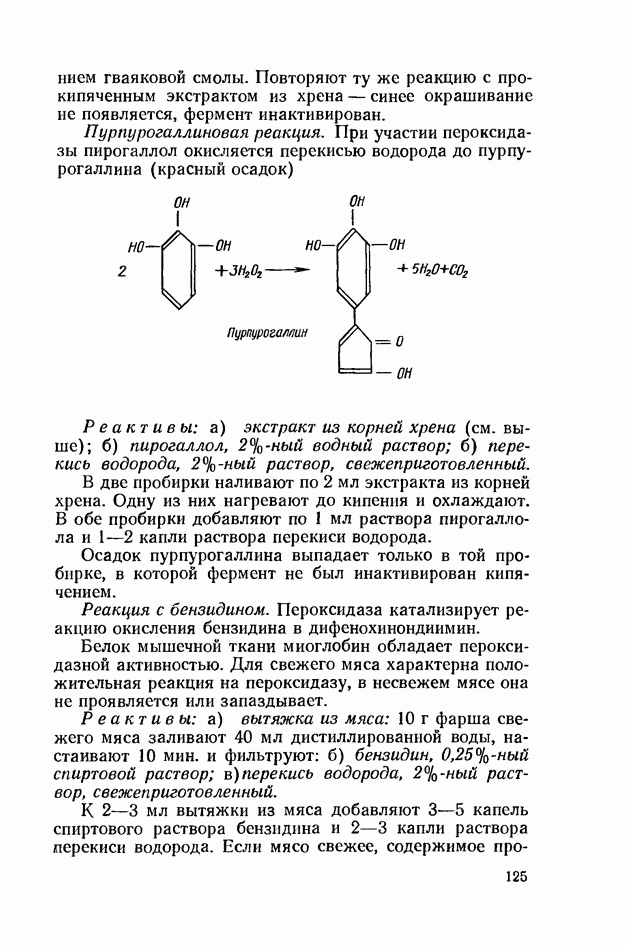
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
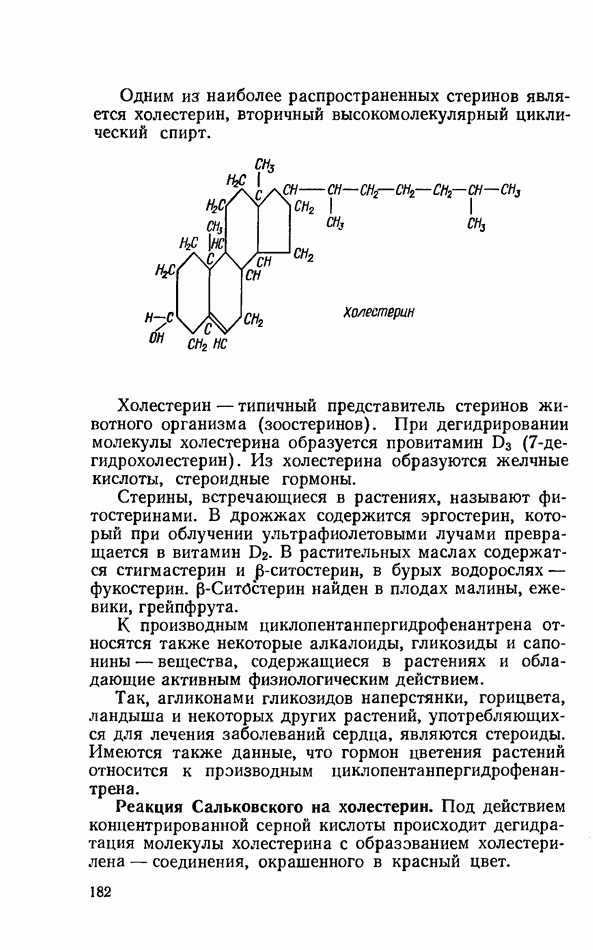
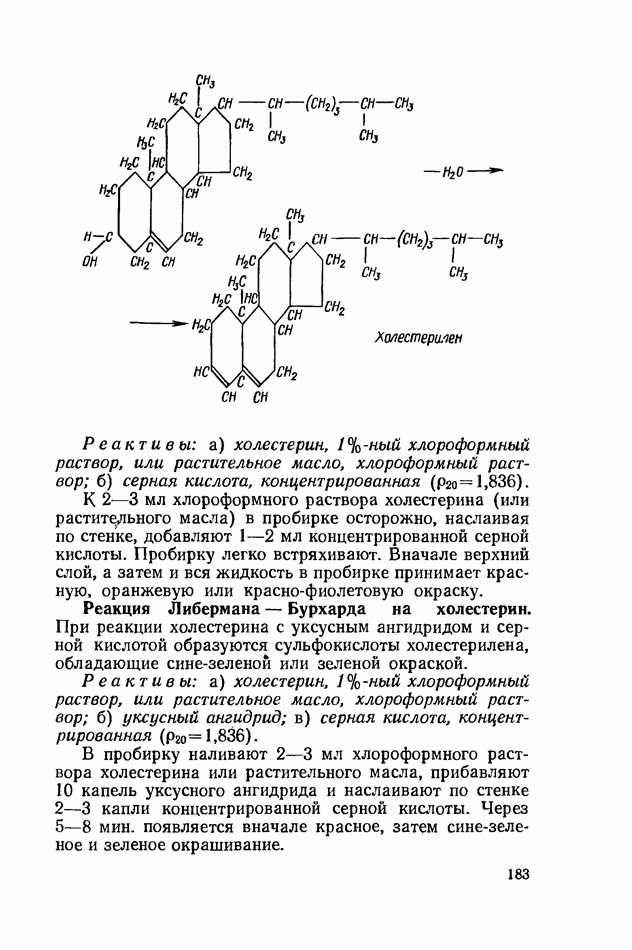
- СТЕРИНЫ
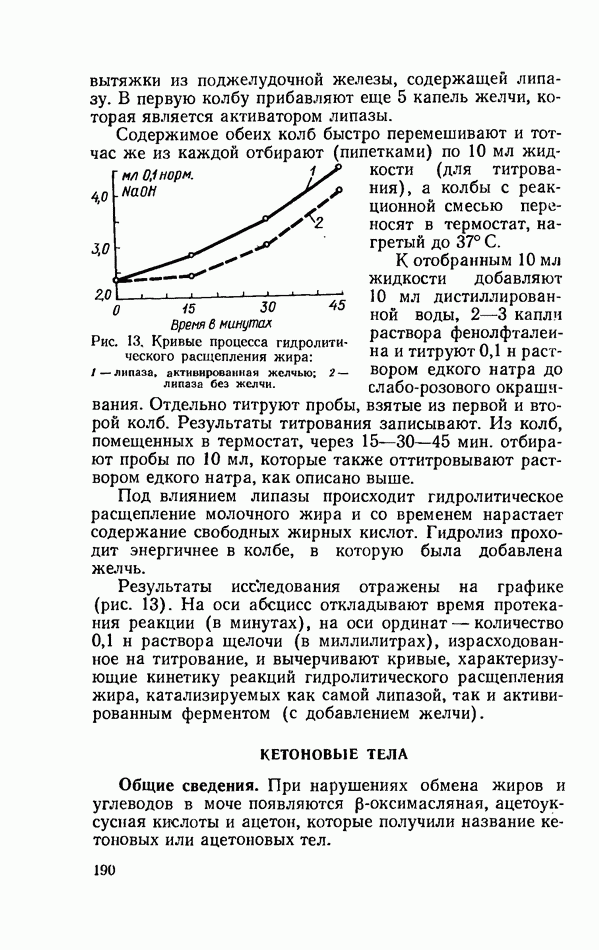
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
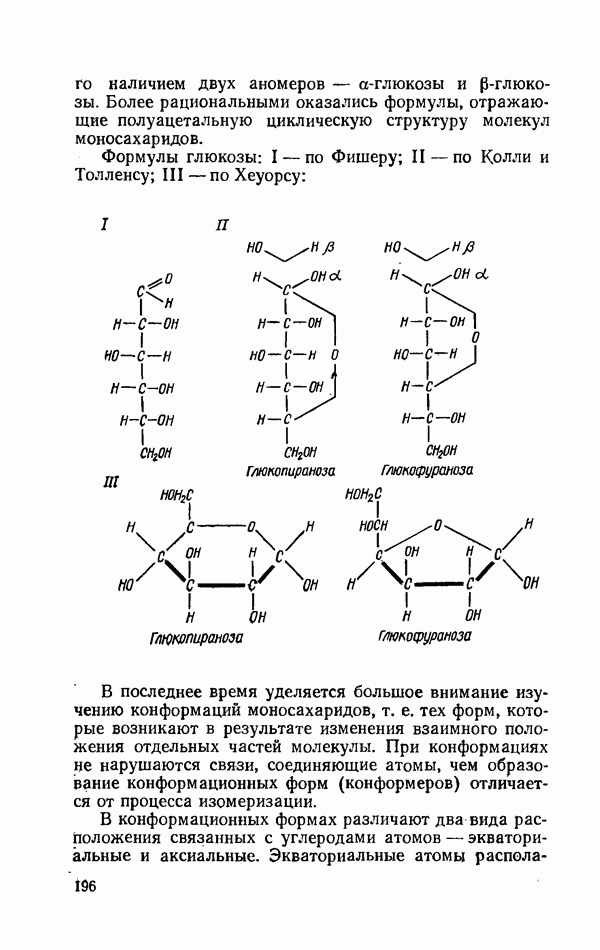
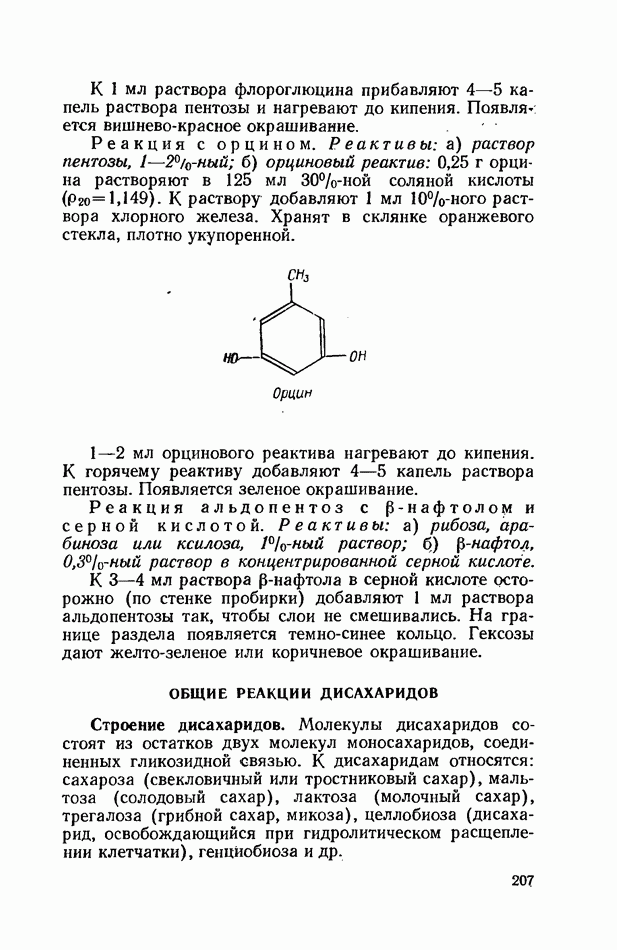
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
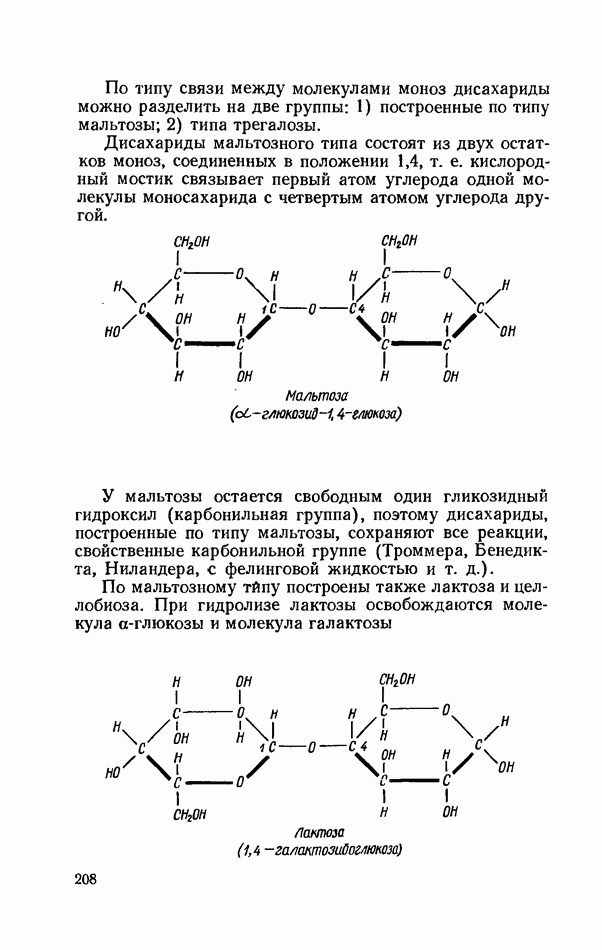
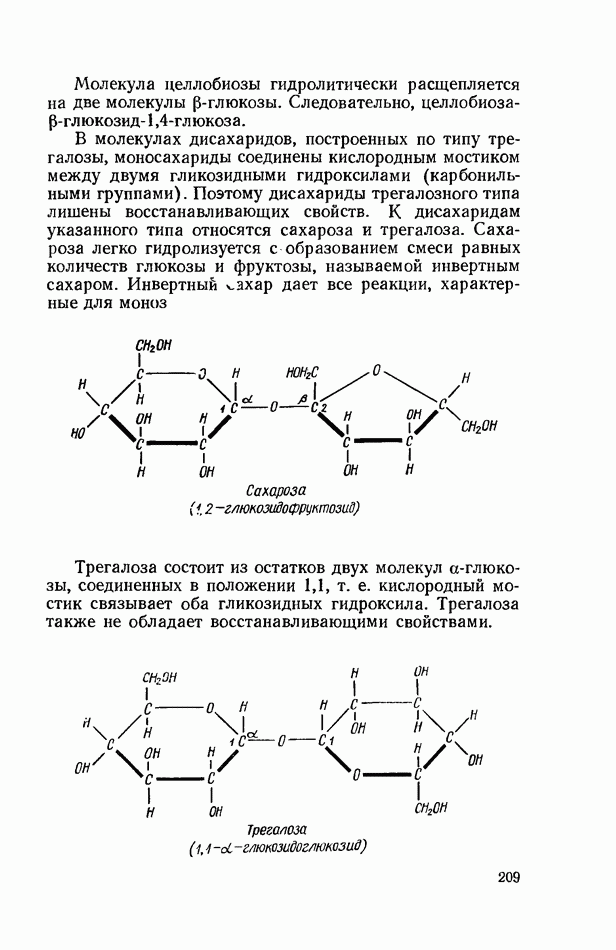
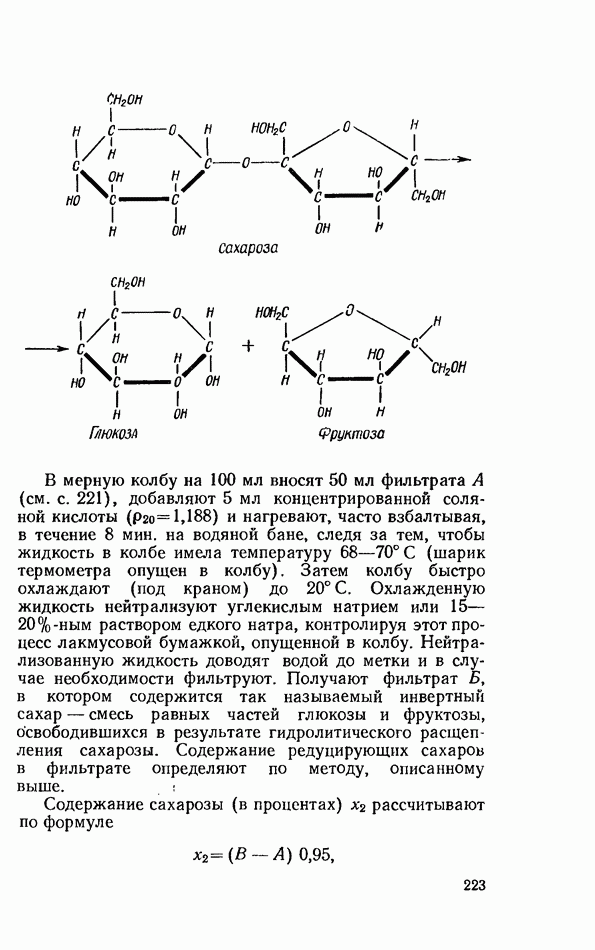
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
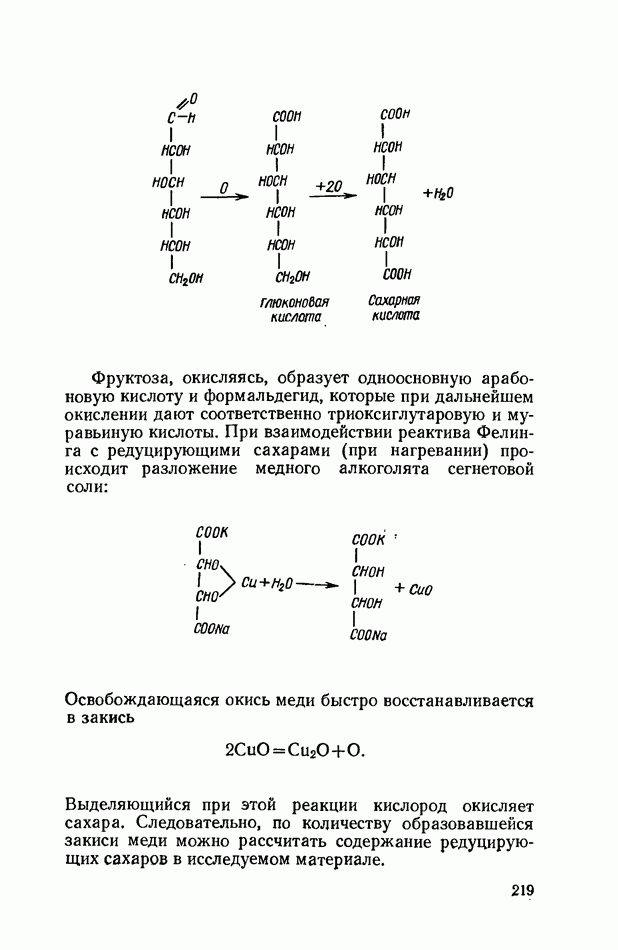
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
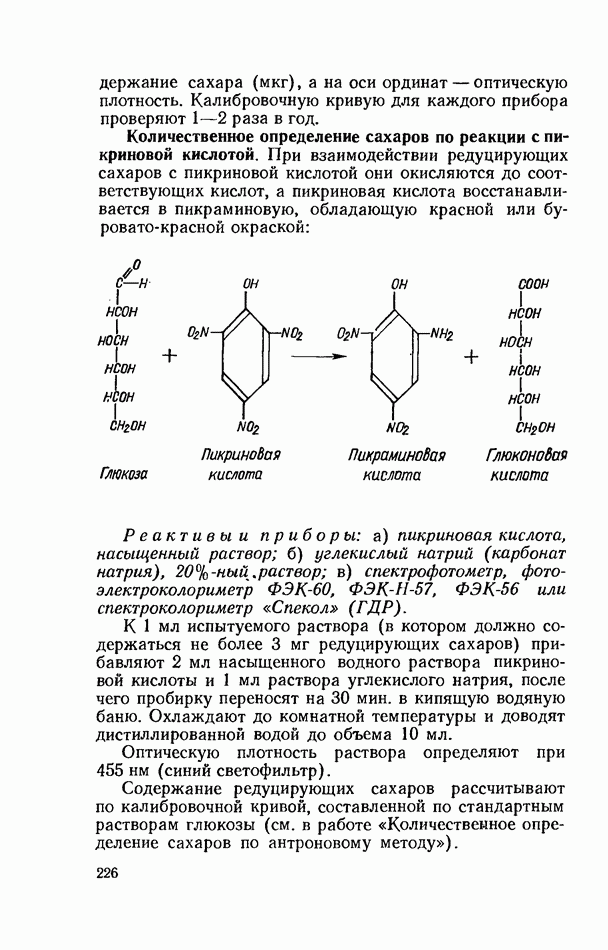
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
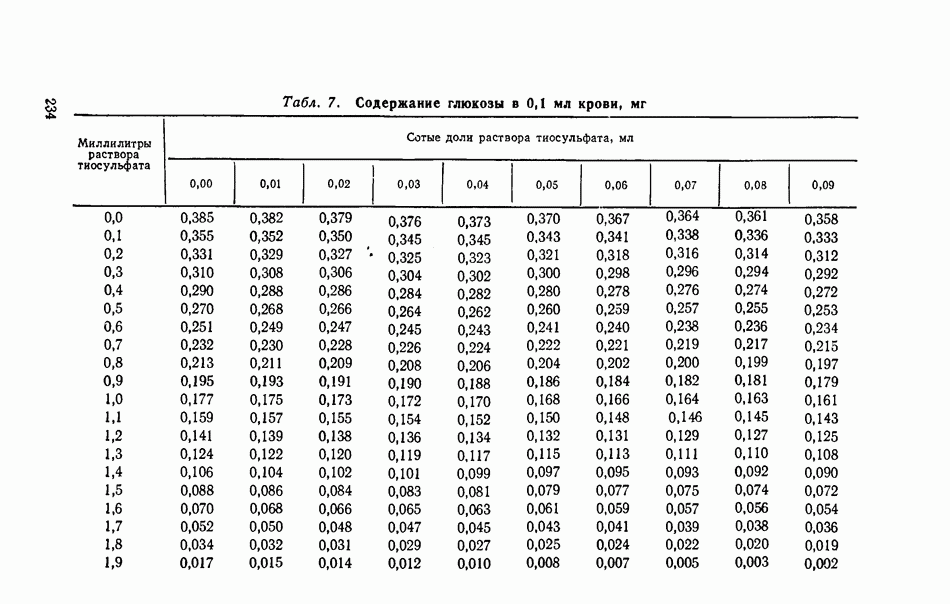
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
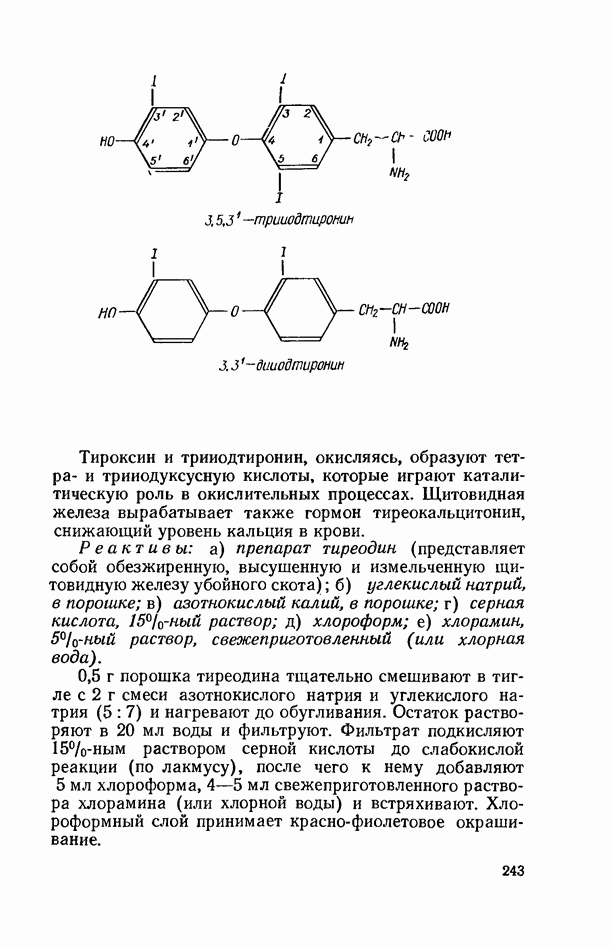
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
- ПРИЛОЖЕНИЯ