| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Электрофорез белков и аминокислот на бумаге
Общие сведения. Электрофорезом называют движение заряженных коллоидных частиц в постоянном электрическом поле к противоположно заряженному электроду.
Явление электрофореза было открыто профессором Московского университета Ф. Ф. Рейссом в 1807 г.
В молекулах белковых веществ возникновение электрических зарядов зависит от группировок, обладающих кислотными и основными свойствами. Кислотные свойства обусловлены карбоксильными и сульфгидрильными группами, а также фенольными гидроксилами. Основные свойства характерны для амино-, имино- и гуанидиновых групп.
Как известно, белки и аминокислоты являются биполярными ионами.

Процесс диссоциации белков во многом зависит от их изоэлектрической точки. Чем дальше будет отстоять значение pH среды от изоэлектрической точки, тем макромолекулы белка будут обладать большим зарядом и с большей скоростью передвигаться к положительному или отрицательному полюсу. Если в растворе находятся несколько белков, которые различаются своими изоэлектрическими точками, то скорость их перемещения в электрическом поле будет неодинаковой. Это явление положено в основу метода электрофоретического исследования биологических жидкостей, который находит широкое применение при анализе свойств белков и аминокислот, а также для диагностических целей.
Для практических работ используют различные варианты метода электрофореза на бумаге.
Аппарат для электрофореза на бумаге.
Основу аппарата составляет ванна из толстого стекла, в которую помещены две кюветы (анодная и катодная) с электродами, приспособления для размещения и закрепления полосок хроматографической бумаги (рамка, лабиринт, пружины) и некоторые вспомогательные части (рис. 5). Применяются платиновые или угольные электроды. Кюветы разделяются перегородками на два отделения — наружное и внутреннее, чтобы предотвратить попадание продуктов электролиза (что связано с изменением pH) на полоски бумаги. В наружных отделениях кювет располагаются электроды, во внутренние погружаются концы полосок бумаги, на которые наносится исследуемая
жидкость. Внутреннее и наружное отделения каждой кюветы соединяются посредством кусочков фильтровальной бумаги, которые кладутся на перегородки. Кюветы заполняются буферным раствором (боратным, фосфатным, вероналовым) с определенным значением pH и ионной силы. Одинаковый уровень жидкости в кюветах поддерживают с помощью сифона.

Рис. 5. Камера аппарата для электрофореза на бумаге (по В. И. Добрыниной и Е. Я. Свешниковой): 1 — ванна из толстого стекла; 2 — стеклянная крышка, пришлифованная к ванне; 3 — электродные кюветы (свободно вынимаются); 4 — продольная перегородка, разделяющая кювету пополам;  угольные электроды;
угольные электроды;  — бумажные полосы, концы их опускаются во внутреннее отделение кюветы; 7 — съемные пластинки, на которых укрепляются электроды (присоединяются К вание при помощи двух пружинок); 8 — рамка, на которой укрепляются и натягиваются бумажные полосы; Р—лабиринт для укрепления бумажных полос; 10 — пружины для натягивания бумажных полос; 11 — подставка для ванны;
— бумажные полосы, концы их опускаются во внутреннее отделение кюветы; 7 — съемные пластинки, на которых укрепляются электроды (присоединяются К вание при помощи двух пружинок); 8 — рамка, на которой укрепляются и натягиваются бумажные полосы; Р—лабиринт для укрепления бумажных полос; 10 — пружины для натягивания бумажных полос; 11 — подставка для ванны;  на подставке; 13 — установочные винты.
на подставке; 13 — установочные винты.
Для предотвращения испарения жидкости камеру (ванну) закрывают пришлифованной стеклянной крышкой.
В комплект аппарата входит также стабилизатор и выпрямитель.
В Советском Союзе аппараты для электрофореза на бумаге выпускает фрунзенский завод «Физприбор».
Разделение глютамина и глютаминовой кислоты с помощью электрофореза на бумаге (по прописи В. И. Добрыниной и Е. Я. Свешниковой).
Если на полоску фильтровальной бумаги нанести раствор смеси глютамина и глютаминовой кислоты, то после электрофореза при pH 8,0 в течение 1,5-2 ч и последующей окраски электрофореграммы можно наблюдать, что глютамин остается на месте нанесения капли раствора, а глютаминовая кислота передвигаетя к аноду на 3—4 см. Это обусловлено
тем, что молекулы глютамина при pH 8,0 электронейтральны и не передвигаются в электрическом поле, а молекулы глютаминовой кислоты при указанном pH имеют преобладающую диссоциацию карбоксильных групп, несут отрицательные заряды и поэтому передвигаются к аноду.
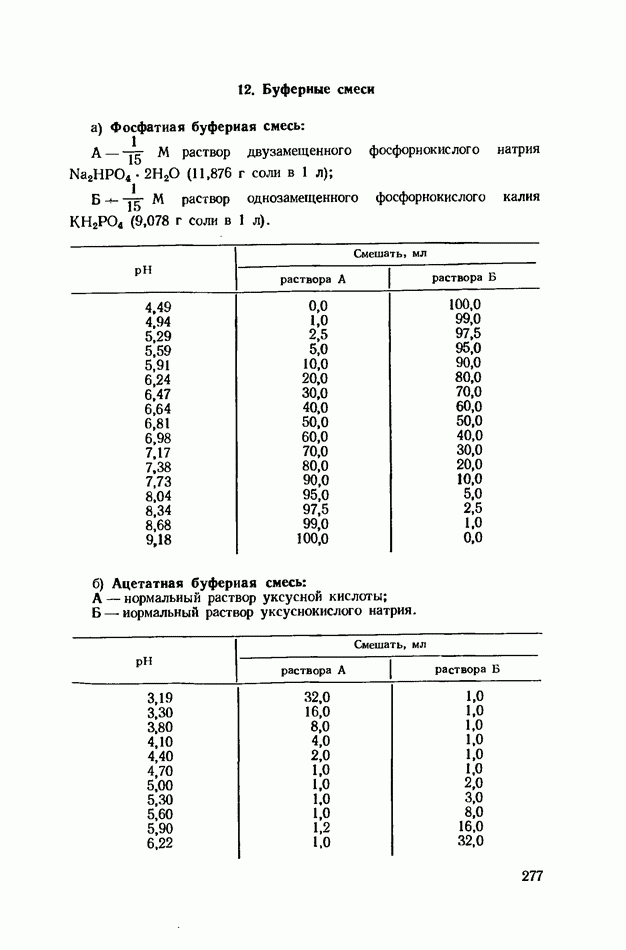
Реактивы: а) раствор глютаминовой кислоты: в 10 мл воды растворяют 50 мг глютаминовой кислоты; б) раствор глютамина: в 10 мл воды растворяют 50 мг глютамина; в) фосфатная буферная система. Готовят два раствора:  Для получения фосфатного буфера pH 8,0 смешивают 945 мл I раствора с 55 мл II раствора; г) нингидрин, 0,2%-ный раствор в этиловом или бутиловом спирте.
Для получения фосфатного буфера pH 8,0 смешивают 945 мл I раствора с 55 мл II раствора; г) нингидрин, 0,2%-ный раствор в этиловом или бутиловом спирте.
В обе кюветы аппарата наливают фосфатный буфер (pH 8,0, ионная сила 0,05). На перегородки между наружным и внутренним отделениями кюветы кладут по кусочку фильтровальной бумаги для установления электрической связи. Одинаковый уровень жидкости в обеих кюветах устанавливают при помощи резинового или стеклянного сифона, наполненного тем же буферным раствором. Полоску фильтровальной бумаги (лучше брать ватман № 2 или хроматографическую ленинградскую) размером  см берут двумя пинцетами (во избежание загрязнения), помещают на лист бумаги и в центре проводят карандашом поперечную линию, вдоль которой штриховыми движениями наносят из микропипетки 0,02 мл смеси растворов глютамина и глютаминовой кислоты. Каждую новую порцию наносят после того, как подсохнет предыдущая. На другую полоску наносят 0,02 мл раствора глютаминовой кислоты, на третью — столько же раствора глютамина. Полоски поочередно смачивают буферным раствором (в чашечке). Избыток влаги удаляют, раскладывая полоски на листе фильтровальной бумаги. Полоски переносят в прибор и концы их погружают в кюветы. В камеру можно уложить 6 полосок. Они должны лежать горизонтально и не провисать.
см берут двумя пинцетами (во избежание загрязнения), помещают на лист бумаги и в центре проводят карандашом поперечную линию, вдоль которой штриховыми движениями наносят из микропипетки 0,02 мл смеси растворов глютамина и глютаминовой кислоты. Каждую новую порцию наносят после того, как подсохнет предыдущая. На другую полоску наносят 0,02 мл раствора глютаминовой кислоты, на третью — столько же раствора глютамина. Полоски поочередно смачивают буферным раствором (в чашечке). Избыток влаги удаляют, раскладывая полоски на листе фильтровальной бумаги. Полоски переносят в прибор и концы их погружают в кюветы. В камеру можно уложить 6 полосок. Они должны лежать горизонтально и не провисать.
Камеру для электрофореза закрывают крышкой, и зажимы электродов фиксируют на выпрямителе — стабилизаторе тока. Выпрямитель подключают к электросети и постепенно увеличивают напряжение. Электрофорез проводят при напряжении 200—300 В и силе тока 1,5-2 мА
в течение 1,5-2 ч, после чего снижают напряжение до нуля и выключают прибор.
Полоски электрофореграмм вынимают чистыми пинцетами и с концов, погруженных в буферный раствор, удаляют избыток влаги фильтровальной бумагой. Полоски накалывают в горизонтальном положении на гвоздики рамы и помещают для фиксации в сушильный шкаф при температуре 100—105° С в течение 10—15 мин. Сухие полоски вынимают из шкафа и опрыскивают раствором нингидрина, после чего для проявления пятен снова помещают в тот же сушильный шкаф на 3—5 мин.
Кроме электрофореза на бумаге, в последнее время широкое распространение получили методы электрофоретического разделения веществ на полиакриламидном, агаровом, геле, крахмале и т. д.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
- ВИТАМИН В: (ТИАМИН)
- ВИТАМИН В2 (РИБОФЛАВИН)
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
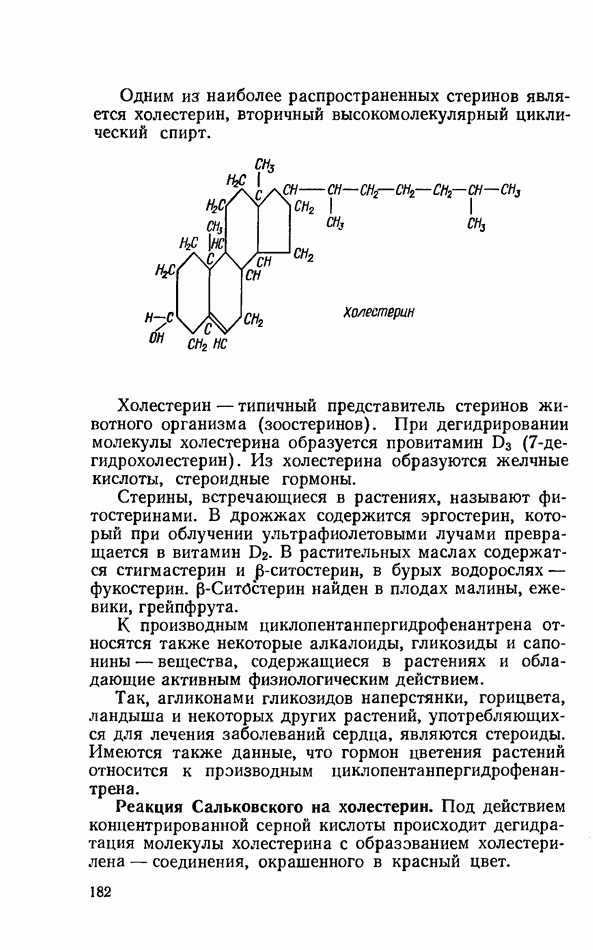
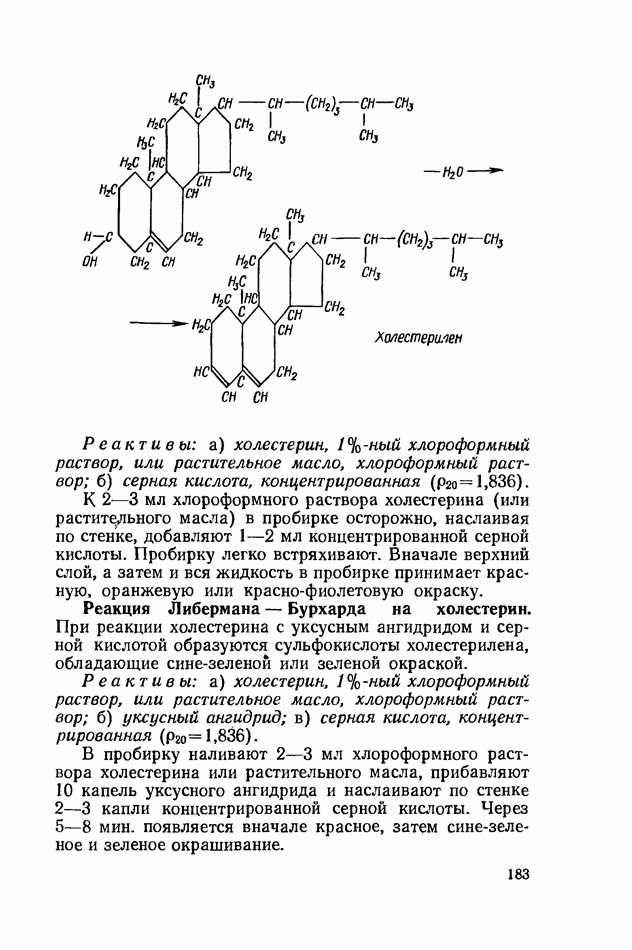
- СТЕРИНЫ
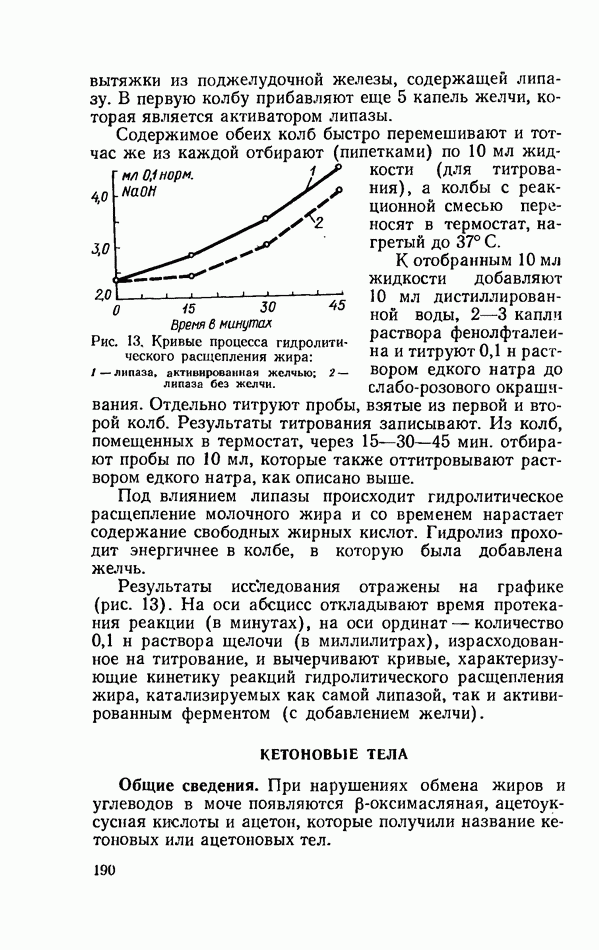
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
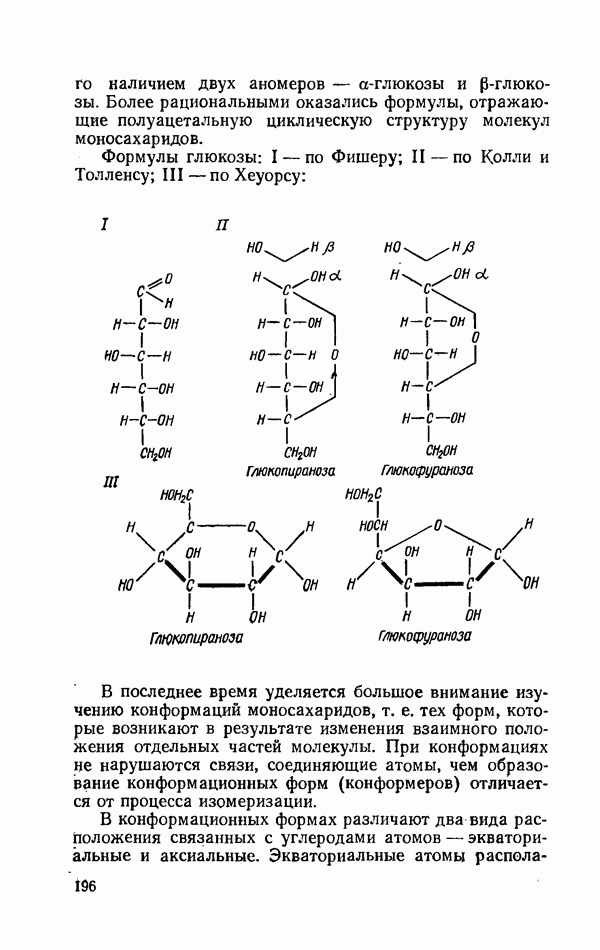
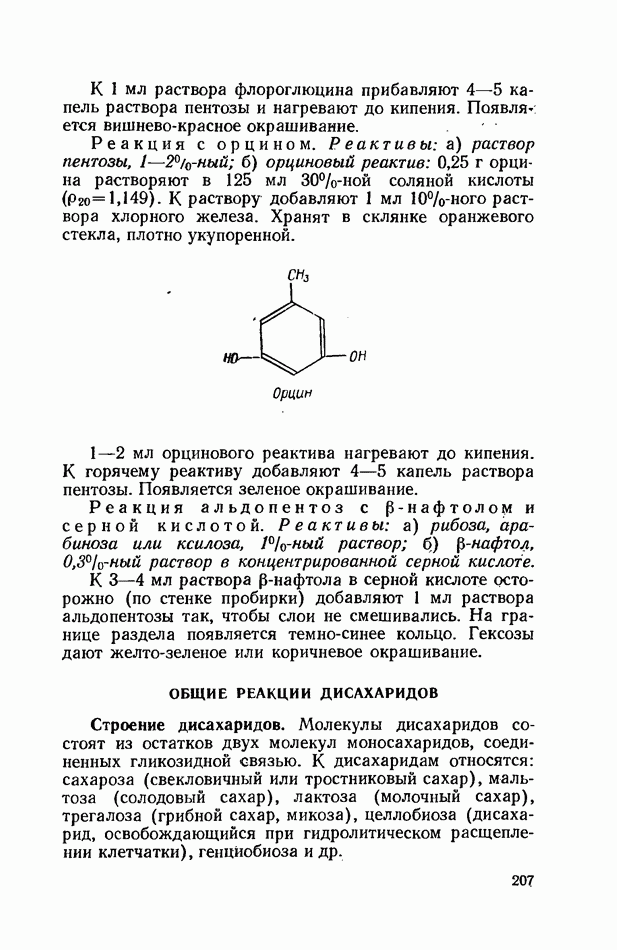
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
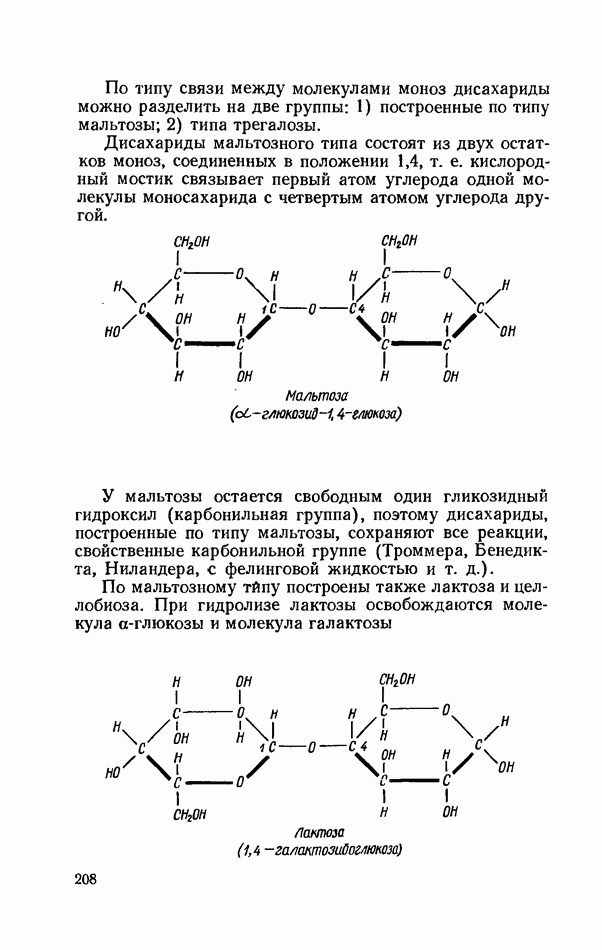
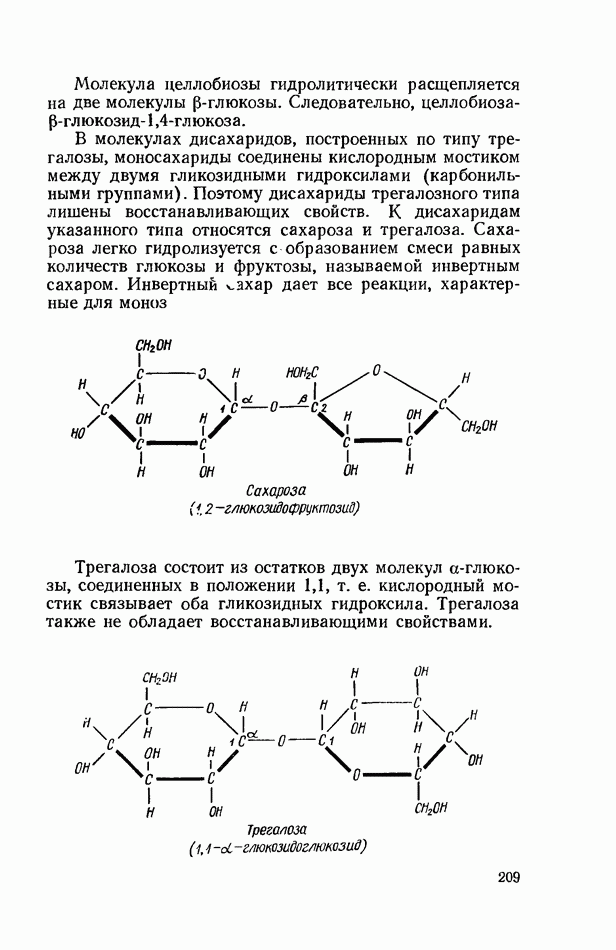
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
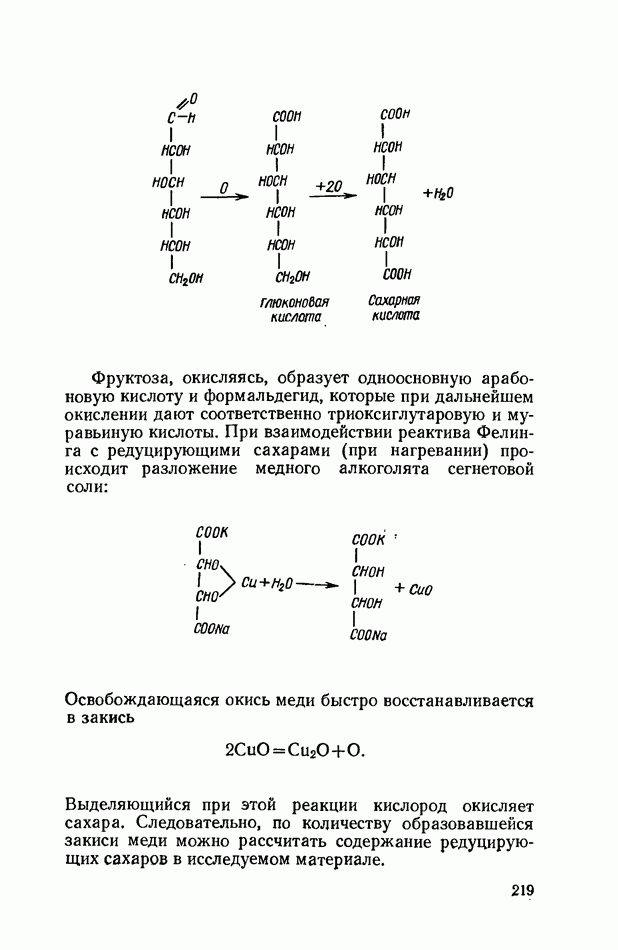
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
- ПРИЛОЖЕНИЯ