| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
Строение дисахаридов.
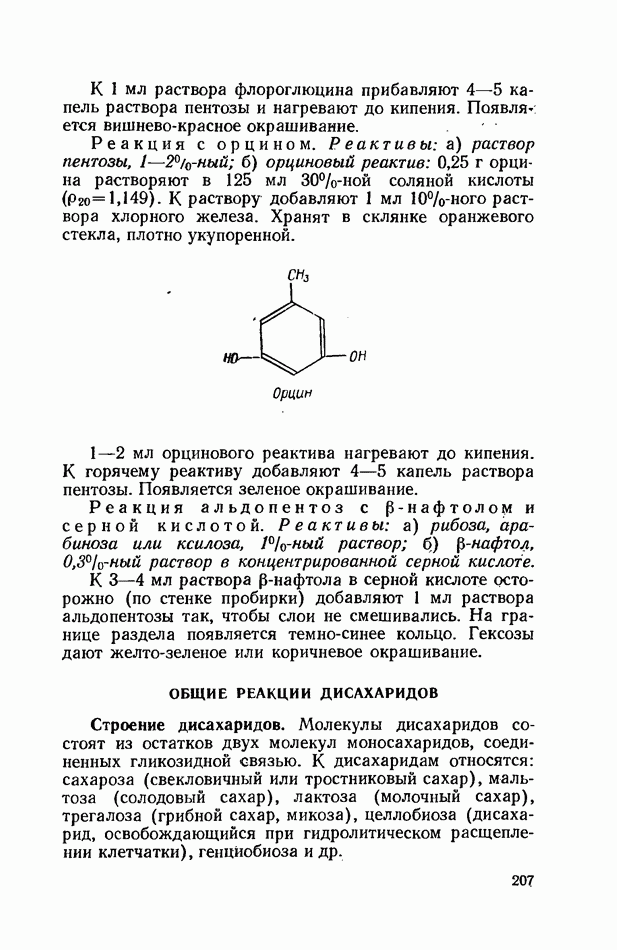
Молекулы дисахаридов состоят из остатков двух молекул моносахаридов, соединенных гликозидной связью. К дисахаридам относятся: сахароза (свекловичный или тростниковый сахар), мальтоза (солодовый сахар), лактоза (молочный сахар), трегалоза (грибной сахар, микоза), целлобиоза (дисахарид, освобождающийся при гидролитическом расщеплении клетчатки), генцйобиоза и др.
По типу связи между молекулами моноз дисахариды можно разделить на две группы: 1) построенные по типу мальтозы; 2) типа трегалозы.
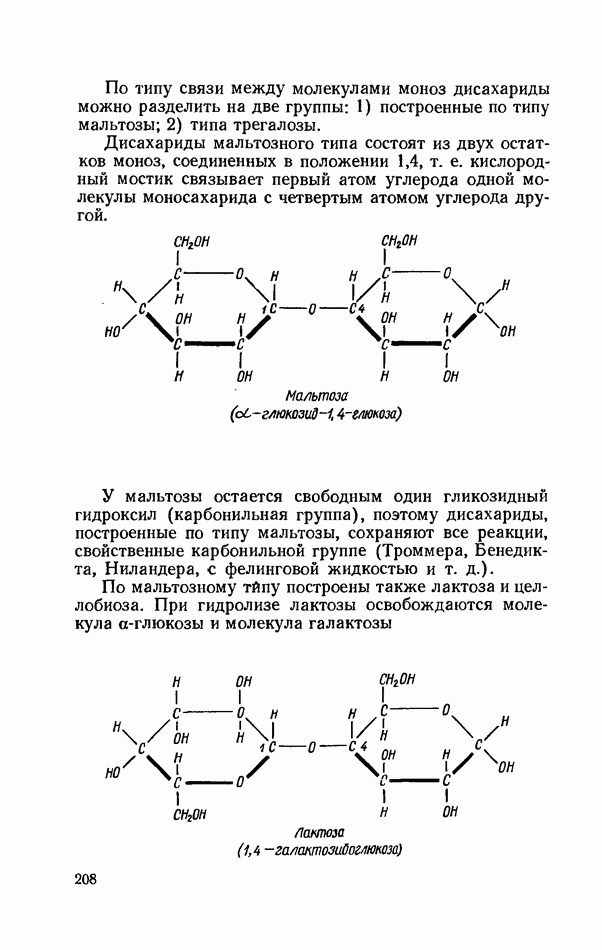
Дисахариды мальтозного типа состоят из двух остатков моноз, соединенных в положении 1,4, т. е. кислородный мостик связывает первый атом углерода одной молекулы моносахарида с четвертым атомом углерода другой.

У мальтозы остается свободным один гликозидный гидроксил (карбонильная группа), поэтому дисахариды, построенные по типу мальтозы, сохраняют все реакции, свойственные карбонильной группе (Троммера, Бенедикта, Ниландера, с фелинговой жидкостью и т. д.).
По мальтозному тйпу построены также лактоза и целлобиоза. При гидролизе лактозы освобождаются молекула а-глюкозы и молекула галактозы

Молекула целлобиозы гидролитически расщепляется на две молекулы  -глюкозы. Следовательно, целлобиоза-р-глюкозид-1,4-глюкоза.
-глюкозы. Следовательно, целлобиоза-р-глюкозид-1,4-глюкоза.
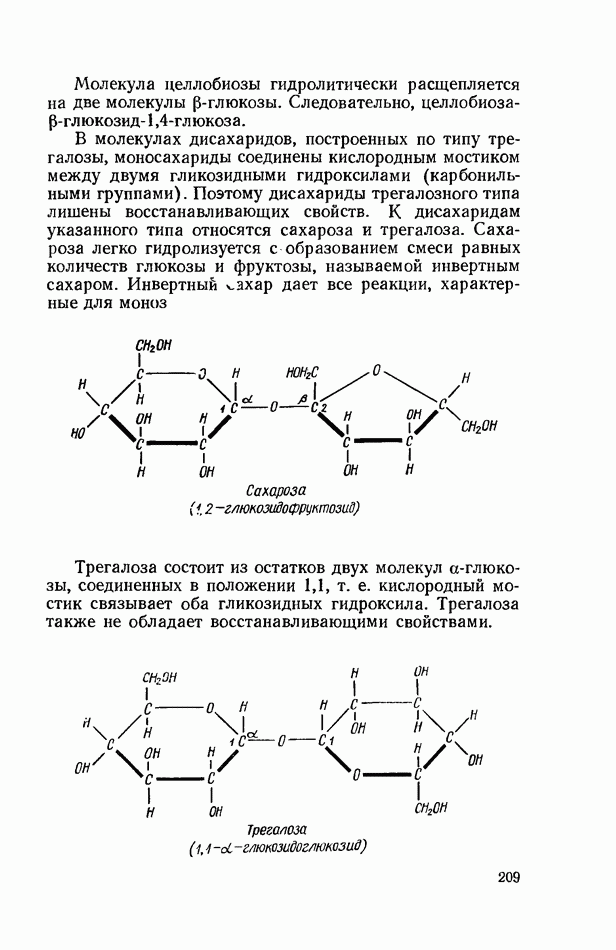
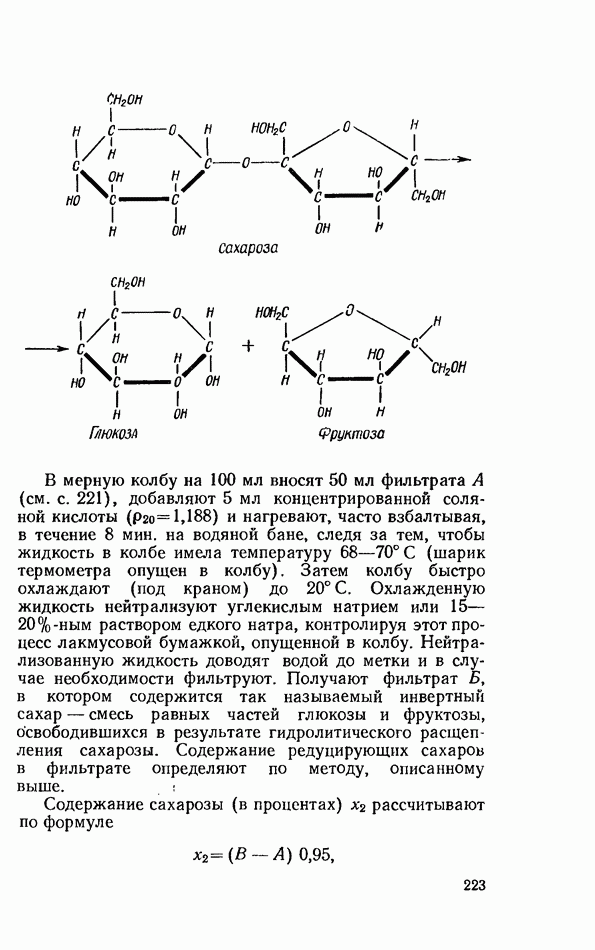
В молекулах дисахаридов, построенных по типу трегалозы, моносахариды соединены кислородным мостиком между двумя гликозидными гидроксилами (карбонильными группами). Поэтому дисахариды трегалозного типа лишены восстанавливающих свойств. К дисахаридам указанного типа относятся сахароза и трегалоза. Сахароза легко гидролизуется с образованием смеси равных количеств глюкозы и фруктозы, называемой инвертным сахаром. Инвертный сахар дает все реакции, характерные для моноз

Трегалоза состоит из остатков двух молекул а-глюкозы, соединенных в положении 1,1, т. е. кислородный мостик связывает оба гликозидных гидроксила. Трегалоза также не обладает восстанавливающими свойствами.

Исследование восстанавливающих свойств дисахаридов.
Реактивы: а) мальтоза,  раствор: б) лактоза,
раствор: б) лактоза,  -ный раствор; в) сахароза,
-ный раствор; в) сахароза,  -ный раствор; г) реактивы Бенедикта, Ниландера, фелингова жидкость; реактивы для реакции Троммера.
-ный раствор; г) реактивы Бенедикта, Ниландера, фелингова жидкость; реактивы для реакции Троммера.
В пробирки вносят по 3-4 мл растворов мальтозы, лактозы, сахарозы и производят с ними реакции Бенедикта, Ниландера, Троммера, с фелинговой жидкостью. Мальтоза и лактоза обладают восстанавливающими свойствами, сахароза, как уже было указано, лишена этой способности.
Инверсия сахарозы. Реактивы: а) сахароза,  -ный раствор; б) соляная кислота, концентрированная; в) едкий натр,
-ный раствор; б) соляная кислота, концентрированная; в) едкий натр,  -ный раствор; г) реактивы для реакций Троммера, Бенедикта, Ниландера, Селиванова.
-ный раствор; г) реактивы для реакций Троммера, Бенедикта, Ниландера, Селиванова.
В пробирку наливают 3-4 мл раствора сахарозы, добавляют 2—3 капли соляной кислоты и нагревают в кипящей водяной бане в течение 10—15 мин., после чего содержимое пробирки охлаждают и нейтрализуют раствором едкого натра (под контролем лакмусовой бумажки). С нейтрализованной пробой (инвертом) производят реакции Троммера, Ниландера или Бенедикта. Продукты инверсии сахарозы — глюкоза и фруктоза — обладают восстанавливающими свойствами. С частью инверта проделывают реакцию Селиванова на фруктозу.
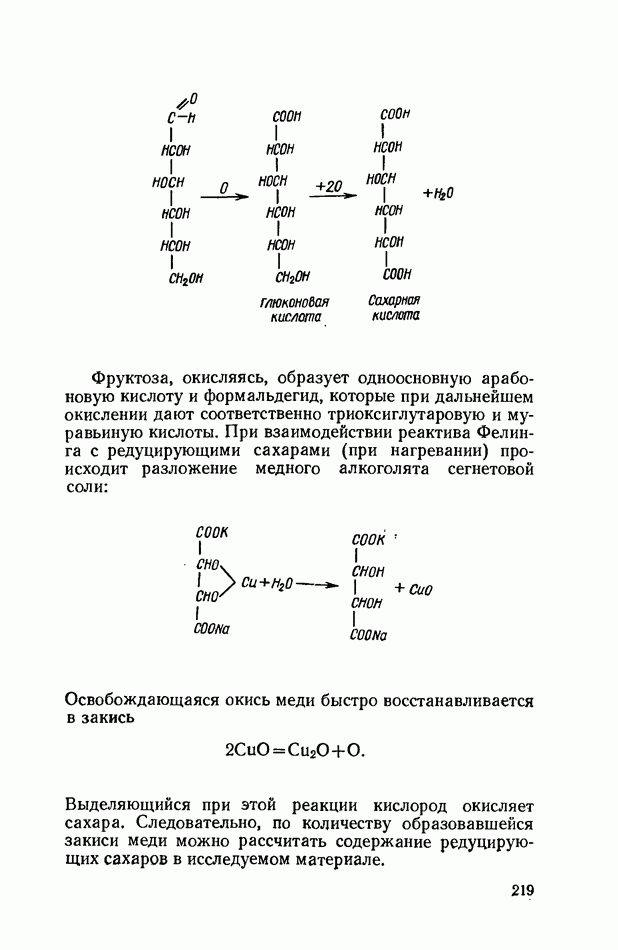
Реакция сахарозы с солями кобальта.
Сахароза в щелочной среде дает фиолетовое окрашивание с ионом 
Реактивы: а) сахароза,  -ный раствор; б) азотнокислый или сернокислый кобальт,
-ный раствор; б) азотнокислый или сернокислый кобальт,  -ный раствор; в) едкий натр или едкое кали,
-ный раствор; в) едкий натр или едкое кали,  -ный раствор.
-ный раствор.
К 2 мл раствора сахарозы добавляют 1 мл раствора щелочи и несколько капель раствора соли кобальта. Появляется фиолетовое окрашивание.
Реакция Барфеда (в модификации Таубера — Клейнера).
Реакция Барфеда позволяет быстро отличить моносахариды от дисахаридов мальтозного типа, обладающих, как известно, восстанавливающими свойствами (лактозы, мальтозы, целлобиозы). Она основана на том, что восстанавливающие свойства моносахаридов сохраняются также в кислой среде, тогда как дисахариды восстанавливают металлы только при щелочной реакции. При взаимодействии дисахаридов с реактивом Барфеда
красный осадок закиси меди появляется не сразу, а лишь спустя некоторое время (15—20 мин.), когда произойдет их гидролитический распад, который катализируется кислотами.
Реактивы: а) глюкоза,  -ный раствор; б) лактоза или мальтоза,
-ный раствор; б) лактоза или мальтоза,  -ный раствор; в) реактив Барфеда (в модификации Таубера и Клейнера): в 450 мл горячей воды растворяют 24 г уксуснокислой меди, прибавляют
-ный раствор; в) реактив Барфеда (в модификации Таубера и Клейнера): в 450 мл горячей воды растворяют 24 г уксуснокислой меди, прибавляют  -ной молочной кислоты и перемешивают до растворения осадка. После охлаждения доливают водой до 500 мл и фильтруют. Реактив Барфеда можно готовить и по следующей прописи: в 200 мл горячей воды растворяют 13,3 г уксуснокислой меди. Помешивают до растворения соли, фильтруют. К фильтрату прибавляют
-ной молочной кислоты и перемешивают до растворения осадка. После охлаждения доливают водой до 500 мл и фильтруют. Реактив Барфеда можно готовить и по следующей прописи: в 200 мл горячей воды растворяют 13,3 г уксуснокислой меди. Помешивают до растворения соли, фильтруют. К фильтрату прибавляют  ледяной уксусной кислоты.
ледяной уксусной кислоты.
В две пробирки наливают по 1 мл реактива Барфеда. В первую пробирку добавляют 1 мл раствора глюкозы, во вторую — столько же раствора лактозы или мальтозы. Пробирки встряхивают и ставят в кипящую водяную баню. В пробирке с глюкозой через 2—3 мин. появляется красный осадок закиси меди, тогда как в пробирке с дисахаридом реакция восстановления наблюдается лишь после 15-20-мииутной выдержки в водяной бане.
Ферментативный гидролиз сахарозы.
Фермент  -фруктофуранозидаза (инвертаза, сахараза) катализирует процесс расщепления сахарозы до глюкозы и фруктозы. Он содержится в пекарских дрожжах.
-фруктофуранозидаза (инвертаза, сахараза) катализирует процесс расщепления сахарозы до глюкозы и фруктозы. Он содержится в пекарских дрожжах.
Реактивы: а) пекарские дрожжи (прессованные); б) сахароза,  -ный раствор; в) реактив Бенедикта или реактивы для реакции Троммера (см. выше).
-ный раствор; в) реактив Бенедикта или реактивы для реакции Троммера (см. выше).
1-1,5 г пекарских дрожжей растирают в ступке с 10-12 мл воды до получения однородной взвеси. К 2 мл взвеси прибавляют 2 мл воды и производят реакцию Троммера или Бенедикта (проверка восстанавливающей способности дрожжей).
В две пробирки наливают по 3 мл взвеси дрожжей; одну из них ставят на 10 мин. в кипящую водяную баню (для тепловой инактивации фермента) и потом охлаждают под краном, вторую не нагревают. В обе пробирки добавляют по 3 мл раствора сахарозы и оставляют на 5—8 мин., после чего фильтруют. С фильтратами проделывают реакцию Троммера или Бенедикта. Записывают результаты опыта.
Распределительная хроматография сахаров на бумаге.
Теоретические основы метода и общие положения методики были описаны на с. 27.
Для хроматографического разделения сахаров употребляют бумагу № 1 и 2 Ленинградской фабрики им. Володарского, фабрики «Маяк революции» (I сорт), а также ватман № 1 и 2.
Восходящую хроматографию проводят в цилиндрах с притертыми пробками или больших пробирках (25X  ) с подобранными резиновыми пробками. Для круговой хроматографии используют эксикаторы небольшого размера или чашки Петри.
) с подобранными резиновыми пробками. Для круговой хроматографии используют эксикаторы небольшого размера или чашки Петри.
Реактивы: а) стандартные растворы сахаров (глюкозы, мальтозы, фруктозы, лактозы, сахарозы, пентоз): готовят из расчета 10 мг углевода в 1 мл раствора; б) смесь н-бутилового спирта, пиридина и воды в соотношении 6:4:1 (по объему); в) бензидин: 0,5 г препарата растворяют в 20 мл ледяной уксусной кислоты и 80 мл абсолютного этилового спирта; г) флороглюцин: 0,2 г препарата растворяют в 80 мл 90%-ного этилового спирта, доводят до объема  -ным раствором трихлоруксусной кислоты; д) динитросалициловая кислота,
-ным раствором трихлоруксусной кислоты; д) динитросалициловая кислота,  -ный раствор в
-ный раствор в  -ном растворе едкого натра; е) анилинфталат: 1,66 г фталевой кислоты и 0,93 г перегнанного анилина растворяют в 100 мл этилового спирта, насыщенного водой; ж) резорцин,
-ном растворе едкого натра; е) анилинфталат: 1,66 г фталевой кислоты и 0,93 г перегнанного анилина растворяют в 100 мл этилового спирта, насыщенного водой; ж) резорцин,  -ный раствор в этиловом спирте. К 10 мл раствора резорцина добавляют 90 мл 2 н соляной кислоты.
-ный раствор в этиловом спирте. К 10 мл раствора резорцина добавляют 90 мл 2 н соляной кислоты.
Хроматографическую бумагу нарезают на полоски длиной 17 см, шириной с одного конца 1,8 см, а с другого — 1,3 см. На расстоянии 1,5-2 см от узкого конца полоски графитовым карандашом очерчивают круг диаметром 0,5 см. Широкий конец полоски прокалывают иглой, протягивают нитку, которую завязывают петлей. Смешивают по 1 мл стандартных растворов сахаров. Одновременно ставят 7—8 хроматограмм (каждую в отдельной пробирке или цилиндре): на две полоски с помощью микропипеток наносят по капле смеси растворов сахаров, на другие — по капле стандартного раствора одного из сахаров. Объем капли —  Капли высушивают на воздухе.
Капли высушивают на воздухе.
В пробирки (или цилиндры) наливают растворитель (н-бутиловый спирт — пиридин — вода) в таком объеме,
чтобы толщина его слоя на дне сосуда составляла около 1,5-1,6 см. Наливая растворитель, надо следить за тем, чтобы не смочить им стенки пробирки. Полоски бумаги осторожно опускают в пробирки и погружают в жидкость на 2—3 мм, затем с помощью нитки и пробки закрепляют их в вертикальном положении (они не должны прикасаться к стенкам пробирки).
Хроматограммы выдерживают в сосудах 2-3 ч. Их вынимают, когда фронт растворителя приблизится к верхнему краю бумаги на 5—6 мм. Карандашом очерчивают уровень фронта растворителя и высушивают бумагу в течение 10 мин. при 100—105° С, после чего хроматограммы опрыскивают проявителями: одну из полосок, на которую была нанесена смесь сахаров, обрабатывают раствором бензидина или динитросалициловой кислоты, другую — раствором флороглюцина. Контрольные полоски, на которые был нанесен раствор только одного сахара, опрыскивают одним из проявителей, зная, что бензидин и динитросалициловая кислота реагируют только с восстанавливающими сахарами, а флороглюцин — с сахарозой и фруктозой. Полоски, обработанные проявителями, переносят в сушильный шкаф и прогревают 10 мин. при 100—105° С. Пятна пентоз окрашиваются в буровато-шоколадный цвет (окраска возникает быстро, ее можно заметить уже после 5-минутного нагрева), бурые пятна остальных восстанавливающих сахаров появляются через 8—10 мин. Пятна фруктозы и сахарозы окрашиваются флороглюцином в желто-оранжевый цвет.
Рассчитывают  сахаров на опытных и контрольных хроматограммах.
сахаров на опытных и контрольных хроматограммах.
Примечание. Вместо указанных проявителей можно пользоваться растворами анилинфталата и резорцина. Анилинфталат более чувствителен к альдозам, чем к кетозам, которые проявляются раствором резорцина. На хроматограммах, обработанных анилин-фталатом, желто-коричневые цвета глюкозы и галактозы проявляются при 100—105° С через 5 мин., пентозы окрашиваются в вишневый цвет. Мальтоза и лактоза проявляются после  -минугного нагревания при 100—105° С. Полоски, увлажненные раствором резорцина, сушат 10 мин. при 85—90° С. Фруктоза дает пятна красного цвета, ксилоза и арабиноза — синего.
-минугного нагревания при 100—105° С. Полоски, увлажненные раствором резорцина, сушат 10 мин. при 85—90° С. Фруктоза дает пятна красного цвета, ксилоза и арабиноза — синего.
Если разделяют сахара на круговой хроматограмме, то смесь углеводов наносят на два сектора круга, а стандартные растворы — на остальные секторы.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
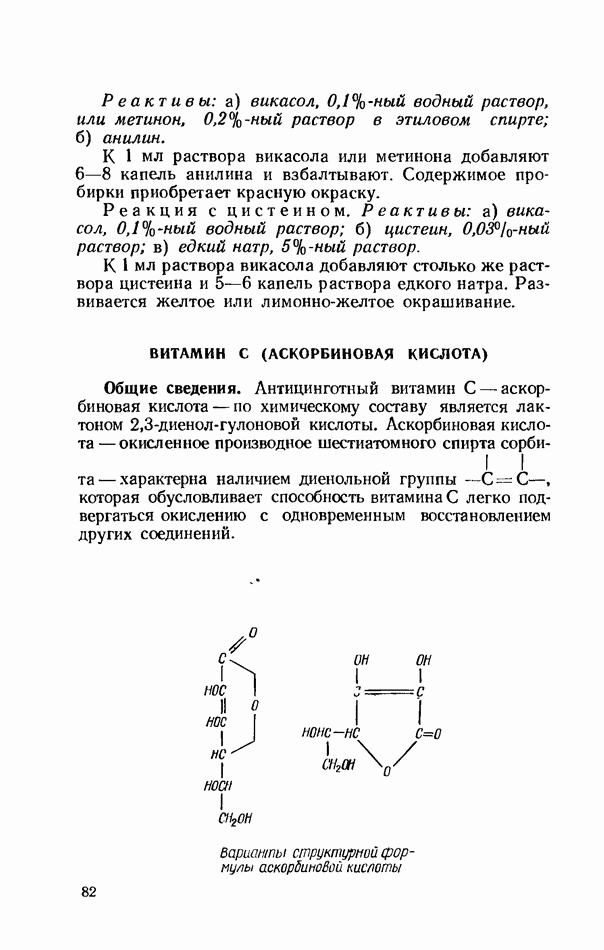
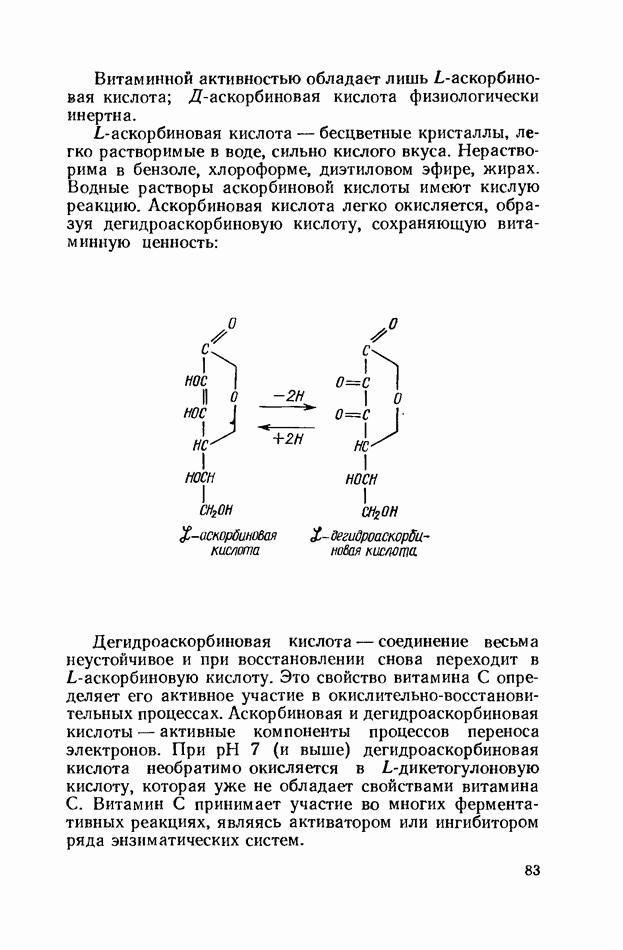
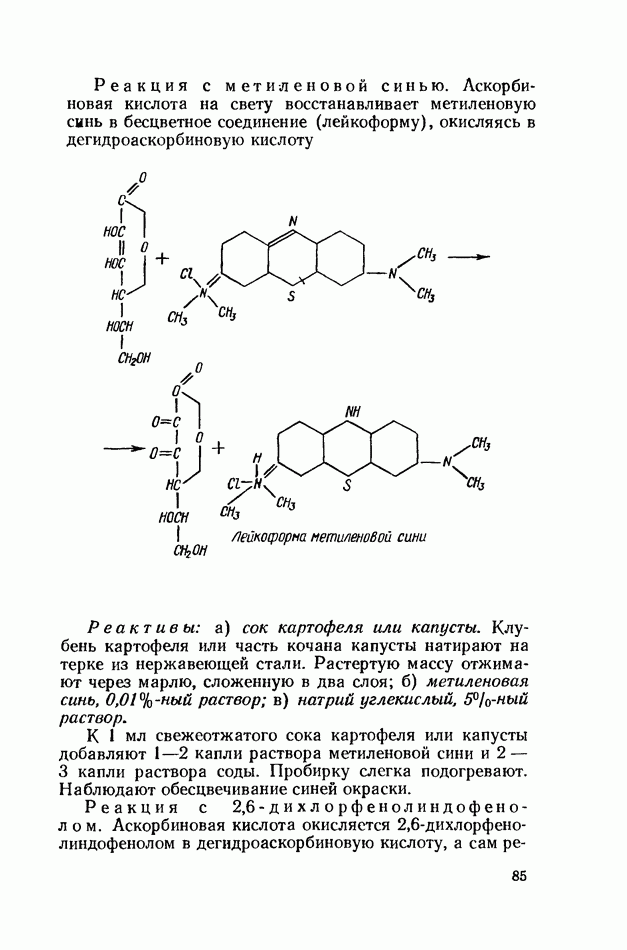
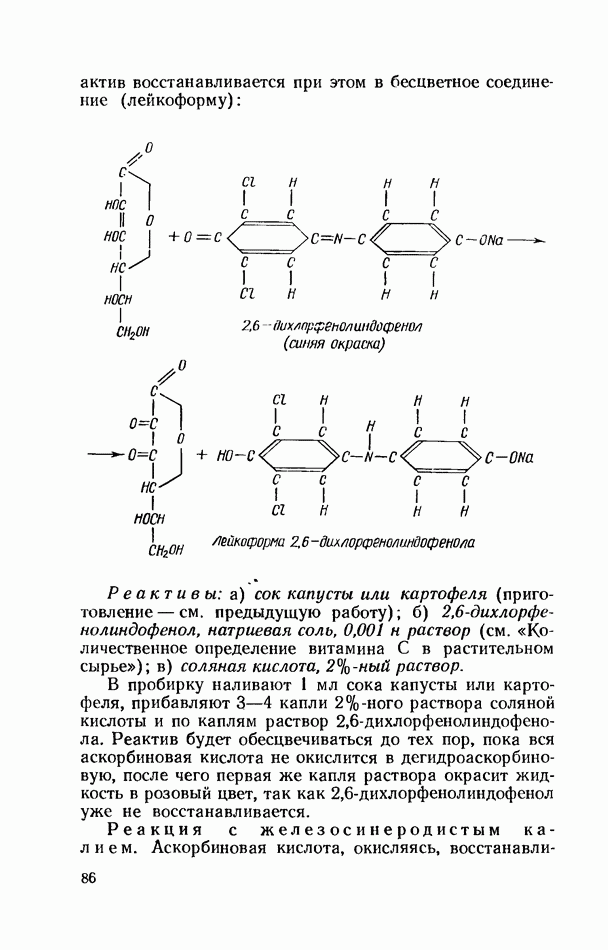
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
- ВИТАМИН В: (ТИАМИН)
- ВИТАМИН В2 (РИБОФЛАВИН)
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
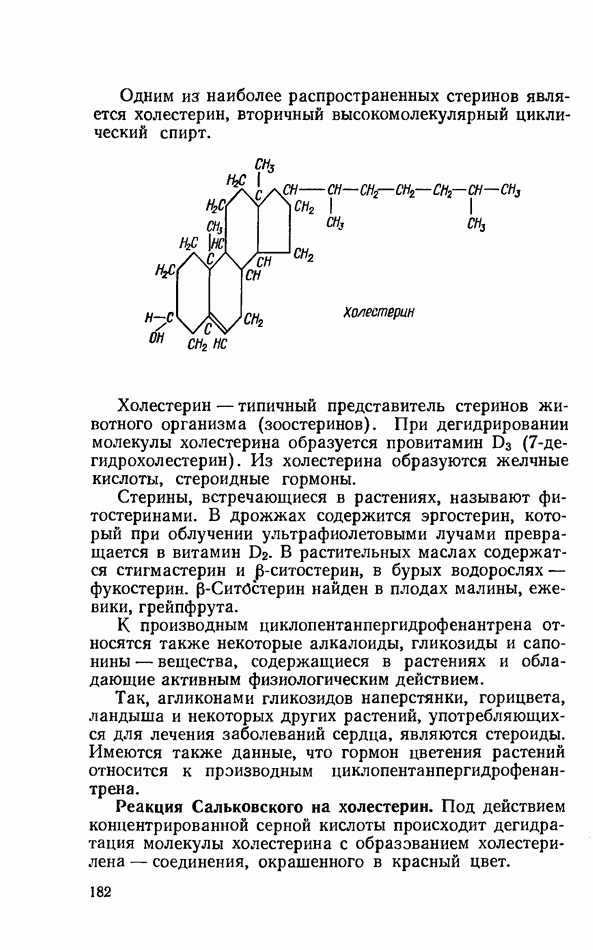
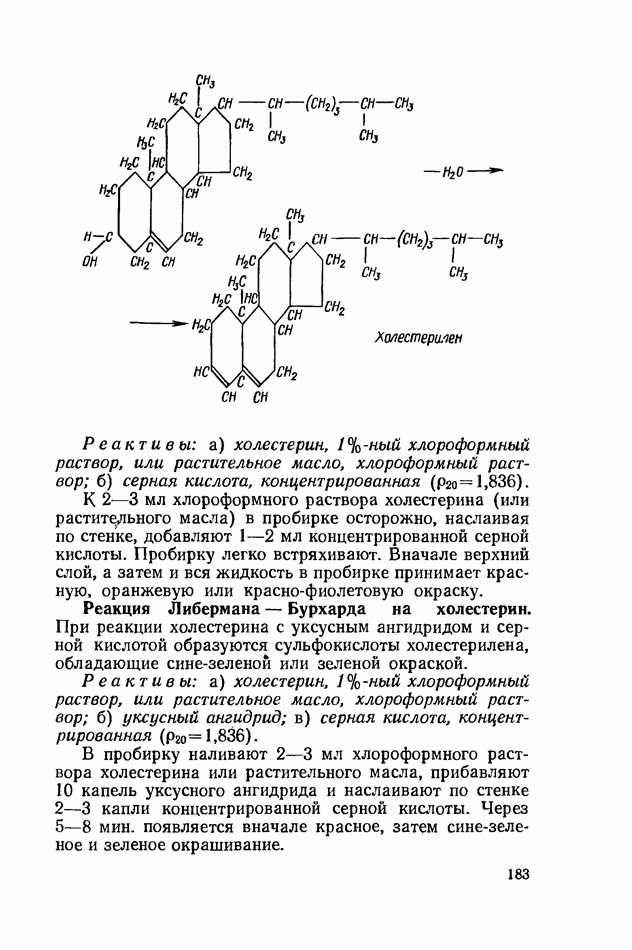
- СТЕРИНЫ
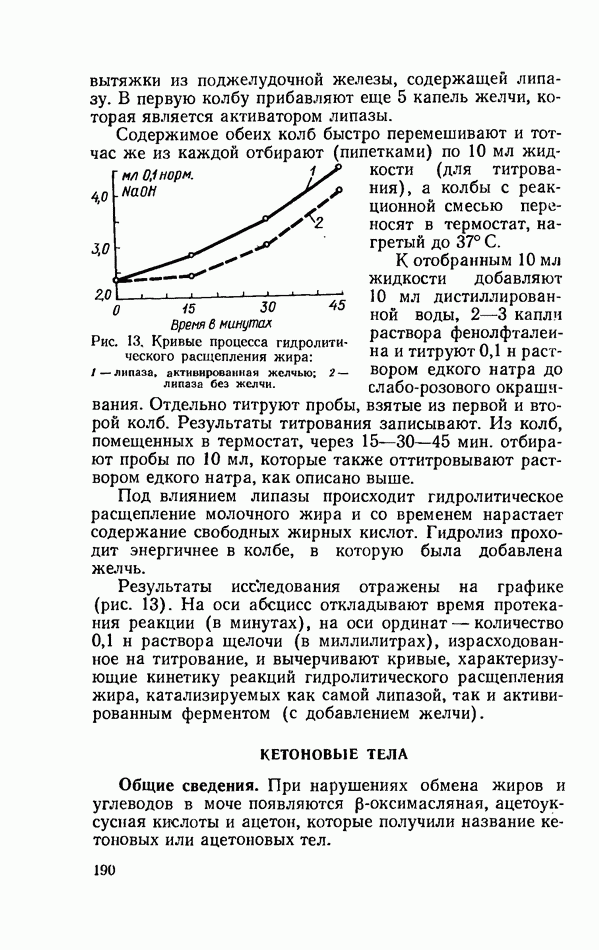
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
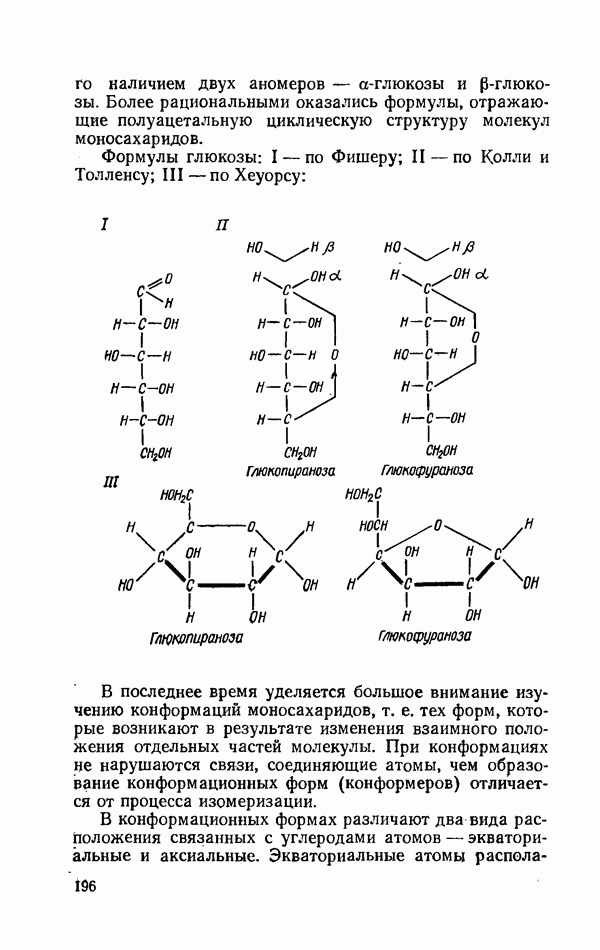
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
- ПРИЛОЖЕНИЯ