| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
Общие сведения.
Дезаминирование — один из путей дальнейшего превращения аминокислот в организме. В результате этого процесса аминокислоты отщепляют аммиак и превращаются в безазотистые соединения. Возможны несколько типов дезаминирования:
а) окислительное

б) восстановительное

в) гидролитическое

Окислительное дезаминирование превалирует у животных, растений и многих видов микроорганизмов, другие типы дезаминирования встречаются главным образом у некоторых анаэробных микробов. Окислительное дезаминирование протекает в два этапа.
Первый этап

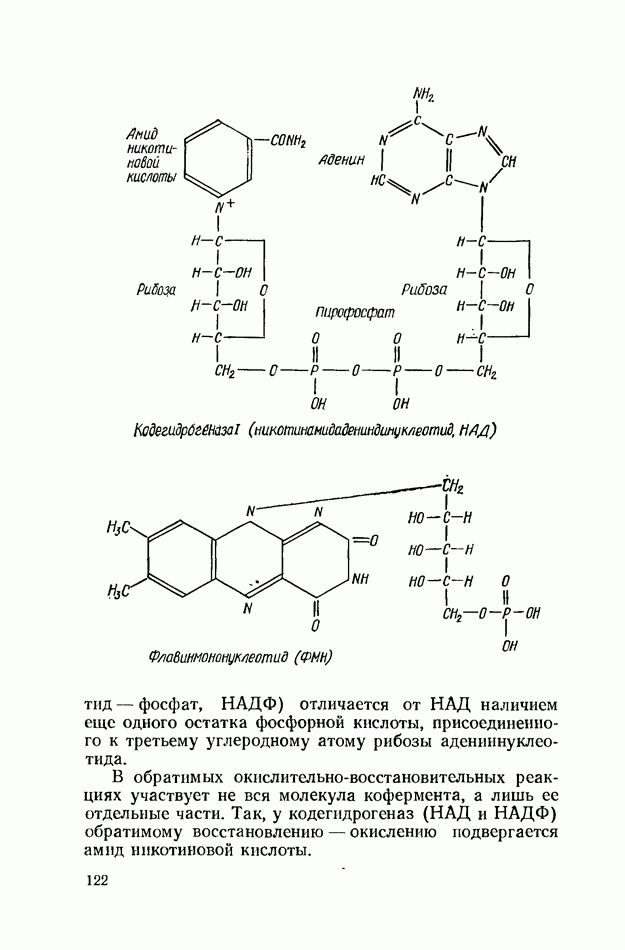
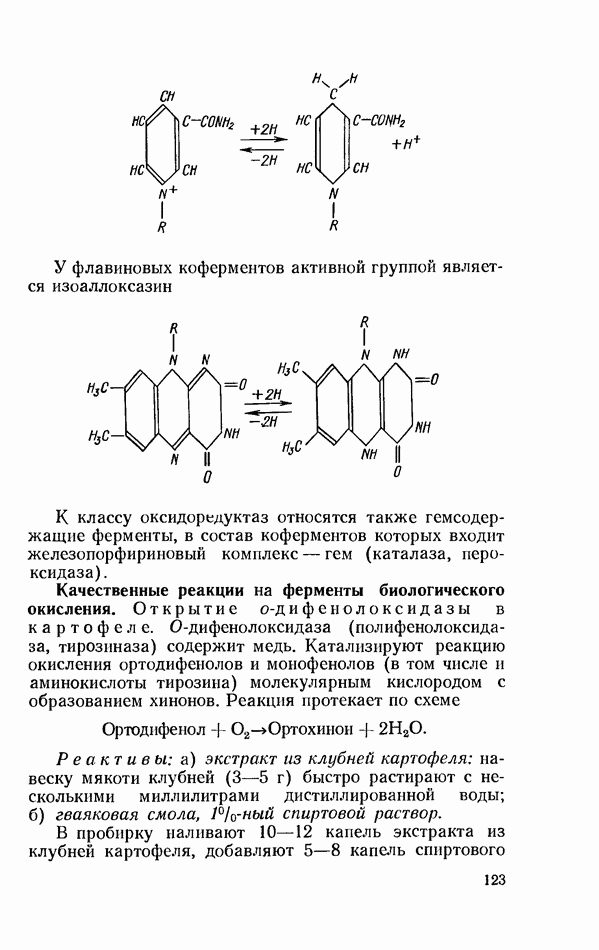
Промежуточными акцепторами водорода являются НАД или ФМН, которые восстанавливаются до НАД  или ФМН
или ФМН  . В дальнейшем водород восстановленных форм коферментов переносится на кислород с образованием воды.
. В дальнейшем водород восстановленных форм коферментов переносится на кислород с образованием воды.
Второй этап. Иминокислота присоединяет воду и распадается на кетокислоту и аммиак:

Второй этап проходит спонтанно, без участия ферментов.
Окислительное дезаминирование D-, L-аланина.
D-, L-аланин под действием фермента оксидазы-Д-аминокислот окисляется в пировиноградную кислоту. При этом отщепляется аммиак, который можно определить с помощью реактива Несслера.

Реактивы: а) ферментный препарат оксидазы-Д-аминокислот. Освобожденные от капсулы почки крысы на холоду тщательно разрезают ножницами на мелкие кусочки, которые затем растирают в ступке в кашицу. Кашицу дважды экстрагируют 10-кратным объемом охлажденного ацетона. Ацетон отсасывают на воронке Бюхнера, а осадок два раза промывают диэтиловым эфиром.
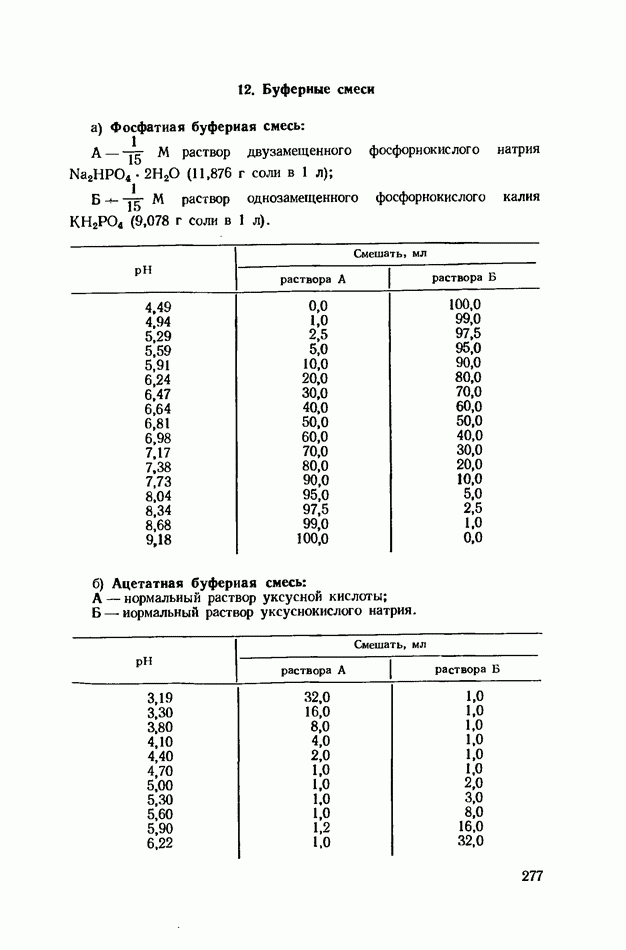
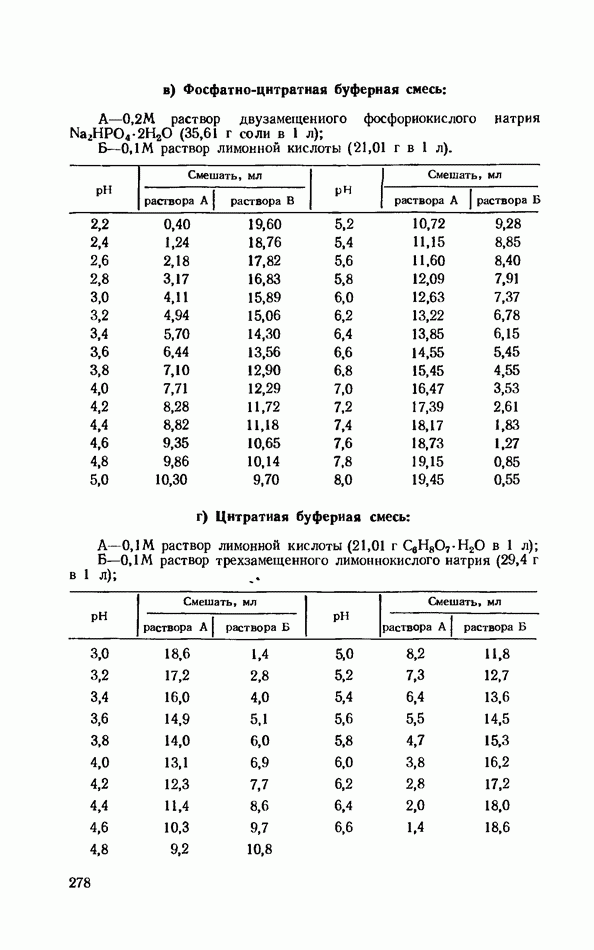
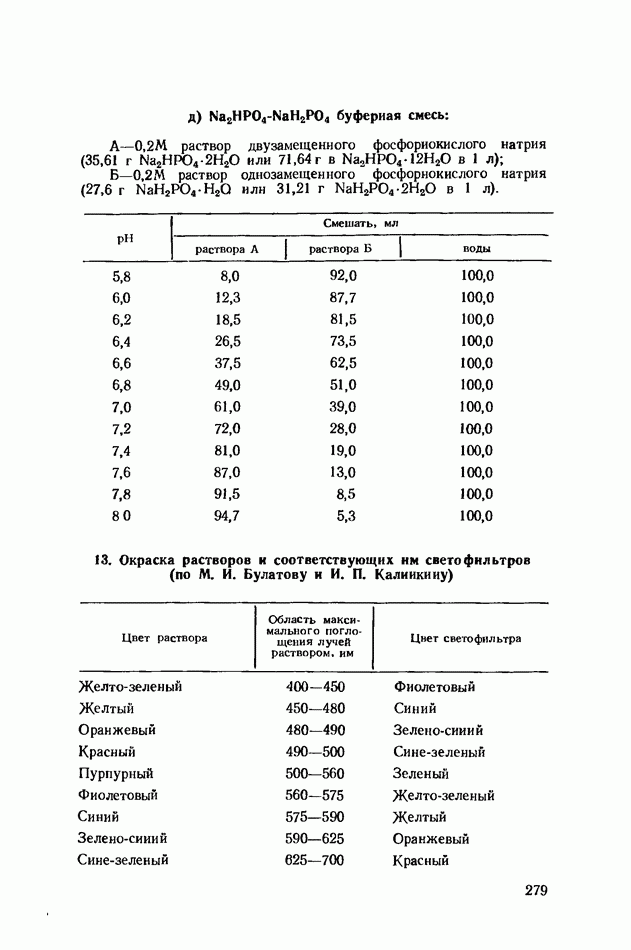
Эфир испаряют на воздухе (в вытяжном шкафу), выключив в лаборатории нагревательные приборы. Порошок ферментного препарата хранят в холодильнике. Он сохраняет свою активность в течение 5—7 дней. Перед употреблением порошок экстрагируют 20 мин. фосфатной буферной смесью (pH 7,6) в отношении 1 : 20, после чего центрифугируют 10 мин. при 3000 об/мин.; б) D-, L-аланин, 2,5%-ный раствор на фосфатной буферной смеси (pH 7,6); в) фосфатная буферная смесь pH 7,6 (приготовление см. прил. 12); г) серная кислота, 10%-ный раствор; д) реактив Несслера (см. работу «Колориметрическое определение общего количества азота»).
Опыт проводят в трех пробирках. В первую вносят 1 мл ферментного препарата (центрифугата) и 1 мл фосфатного буфера, во вторую — 1 мл раствора аланина и 1 мл буферной смеси, в третью — 1 мл ферментного препарата и 1 мл раствора аланина. Все пробы тщательно перемешивают, плотно закрывают заранее подобранными пробками и помещают в водяную баню 37—38° С на 1 ч (лучше пользоваться ультратермостатом). Во время инкубации тщательно следят за температурой воды в бане, не допуская ее повышения. По истечении указанного срока во все пробирки приливают по 1 мл 10%-ного раствора серной кислоты и 3-4 мл реактива Несслера и наблюдают за окраской жидкости. В опытной пробе (третья пробирка) появляется интенсивное желто-оранжевое окрашивание (до желто-бурого), вызванное продуктом взаимодействия аммиака с реактивом Несслера (иодидом меркураммония). Жидкость в первой и второй пробирках, которые служили контролем, примет бледно-желтую окраску.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
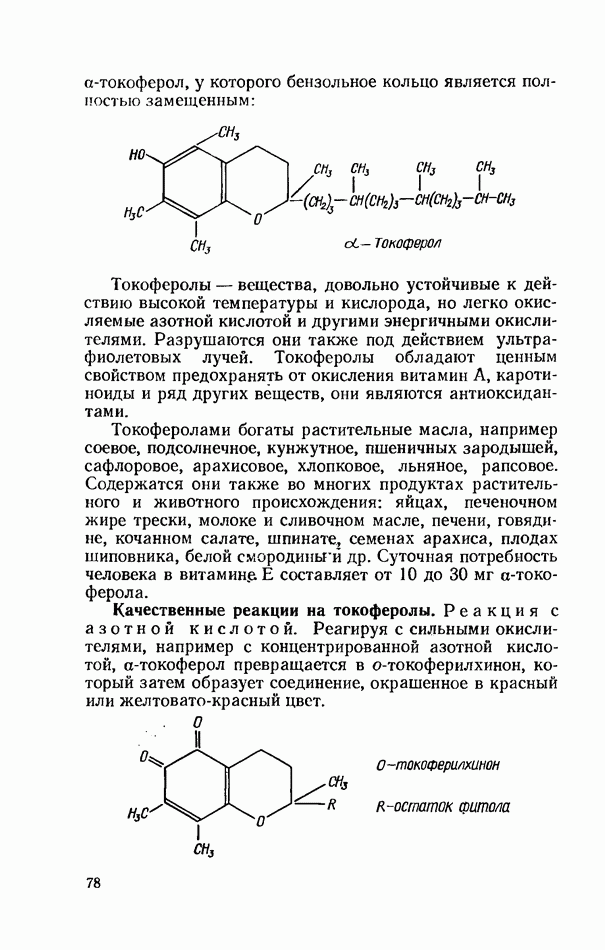
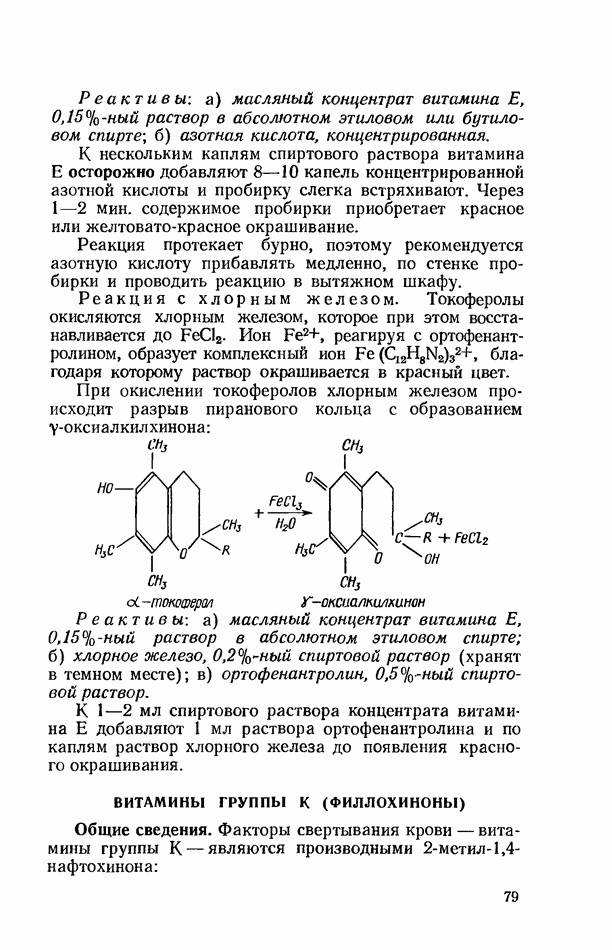
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
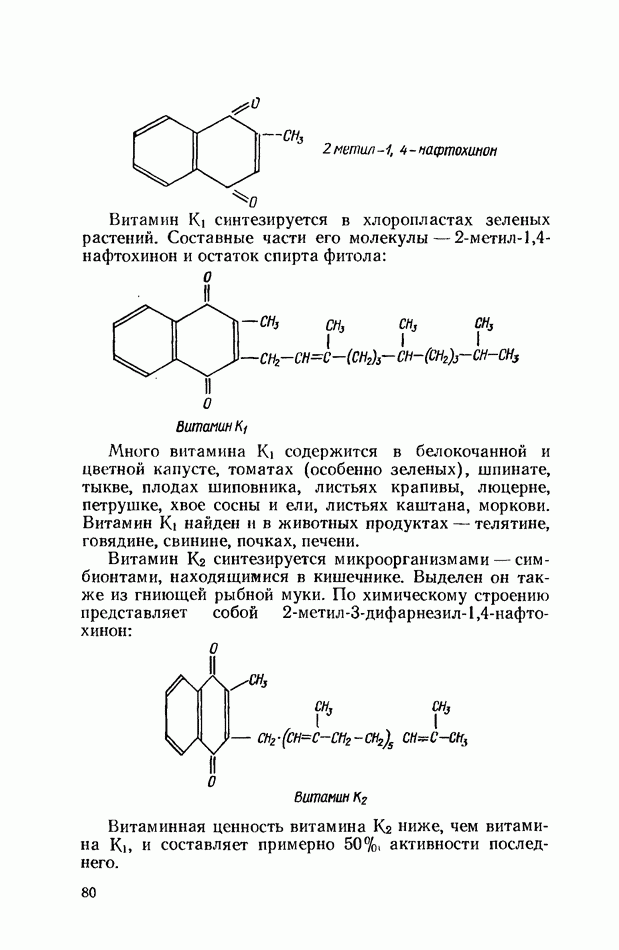
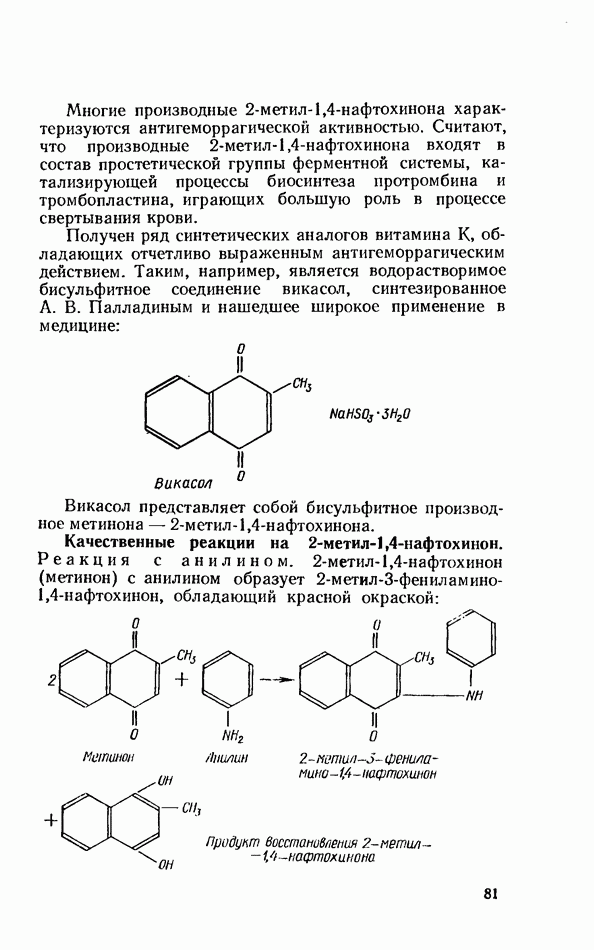
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
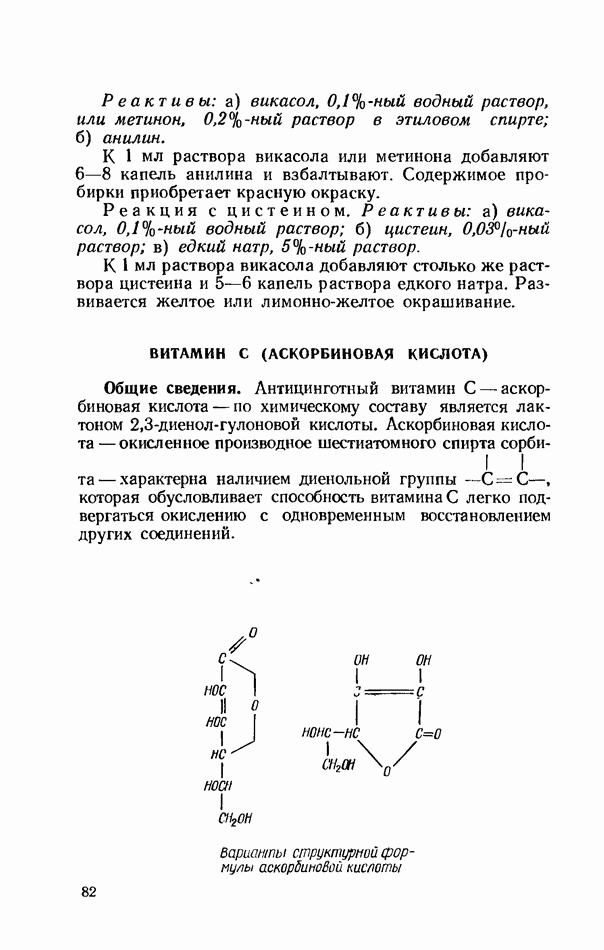
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
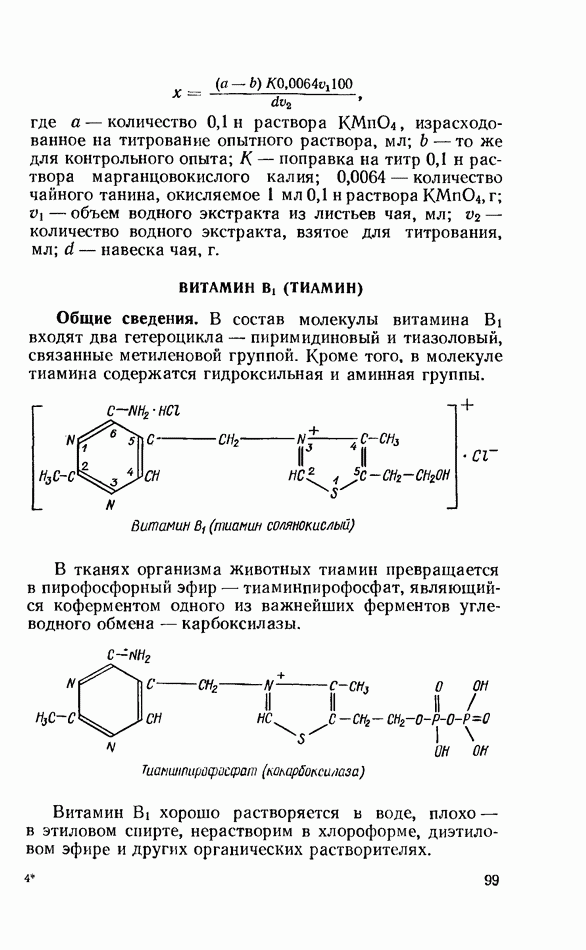
- ВИТАМИН В: (ТИАМИН)
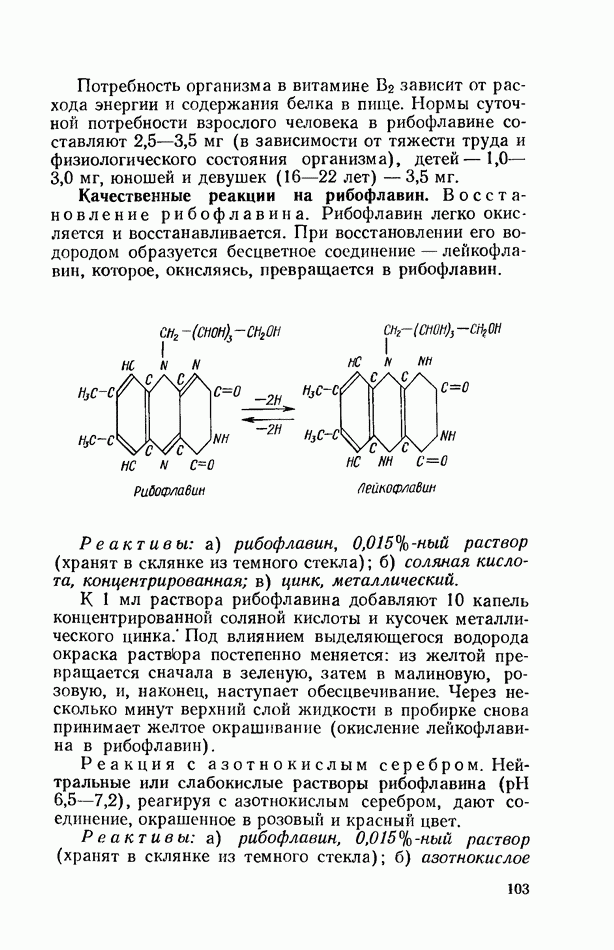
- ВИТАМИН В2 (РИБОФЛАВИН)
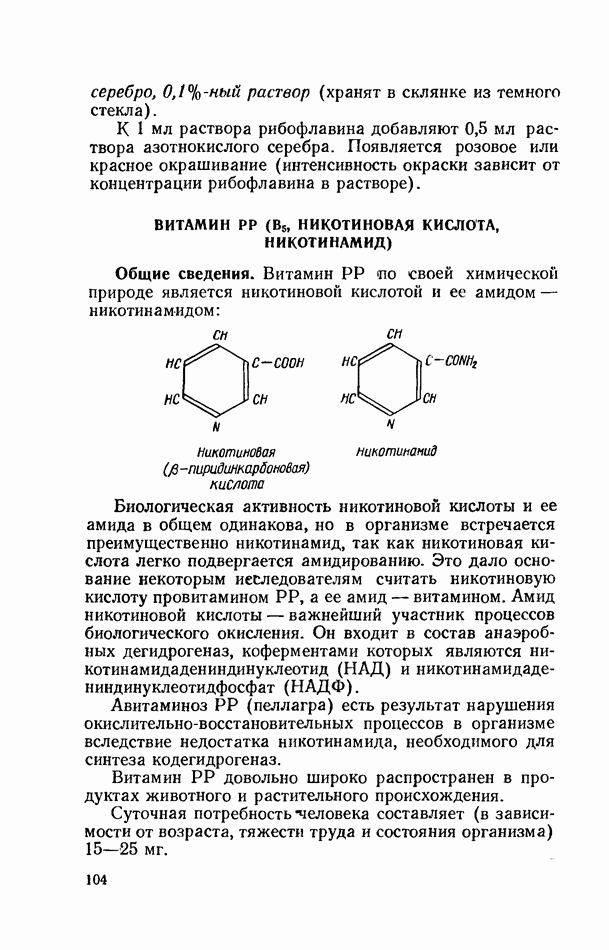
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
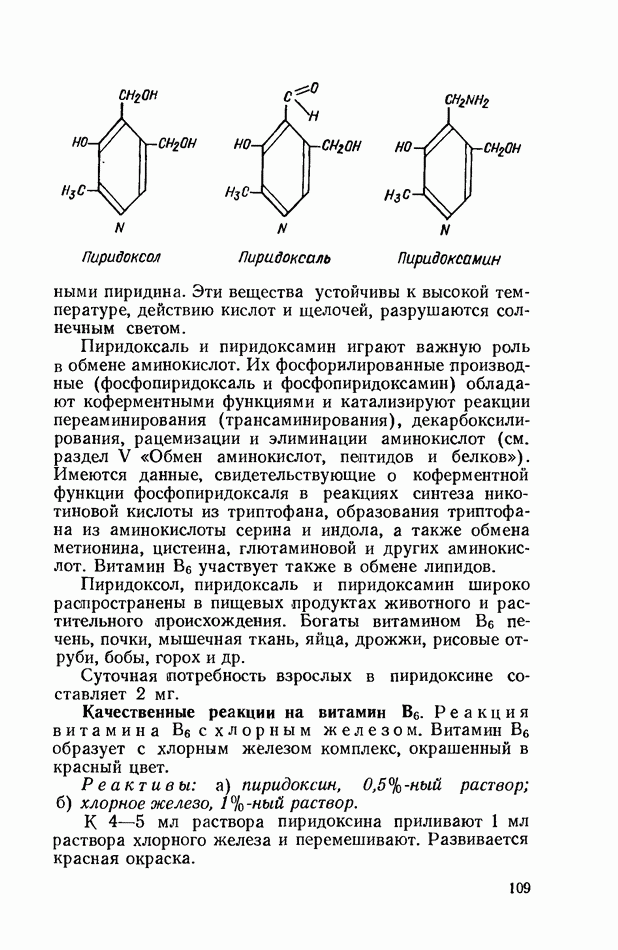
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
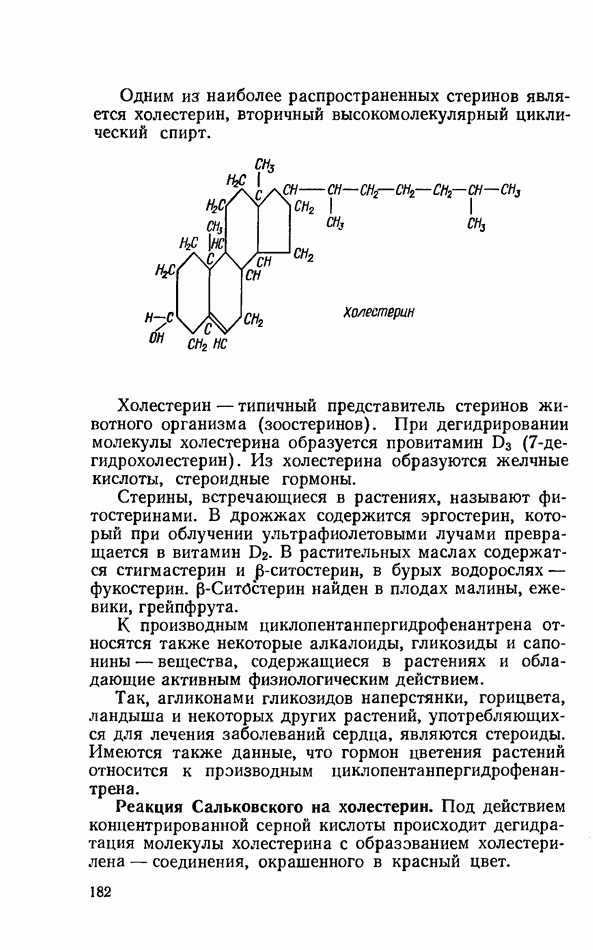
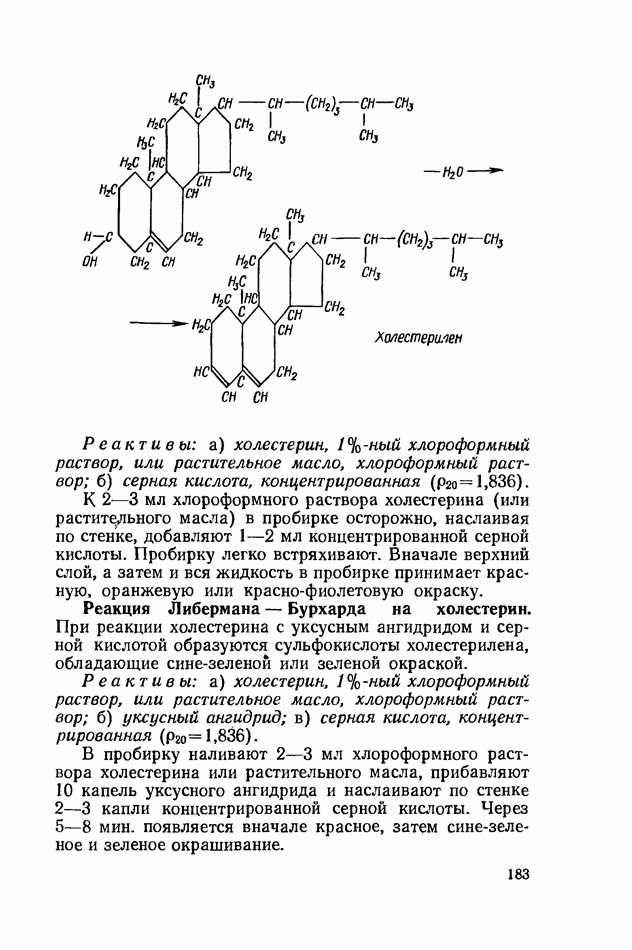
- СТЕРИНЫ
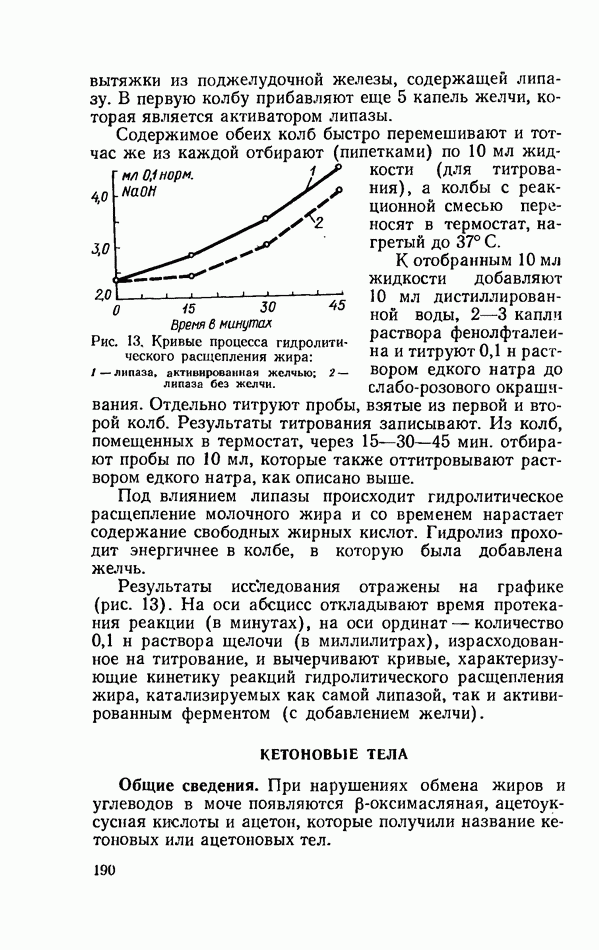
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
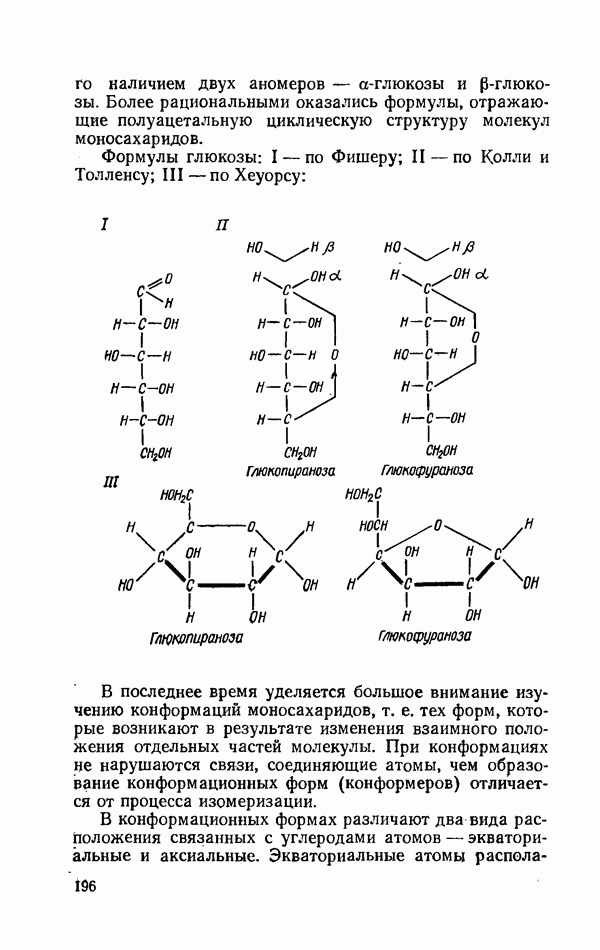
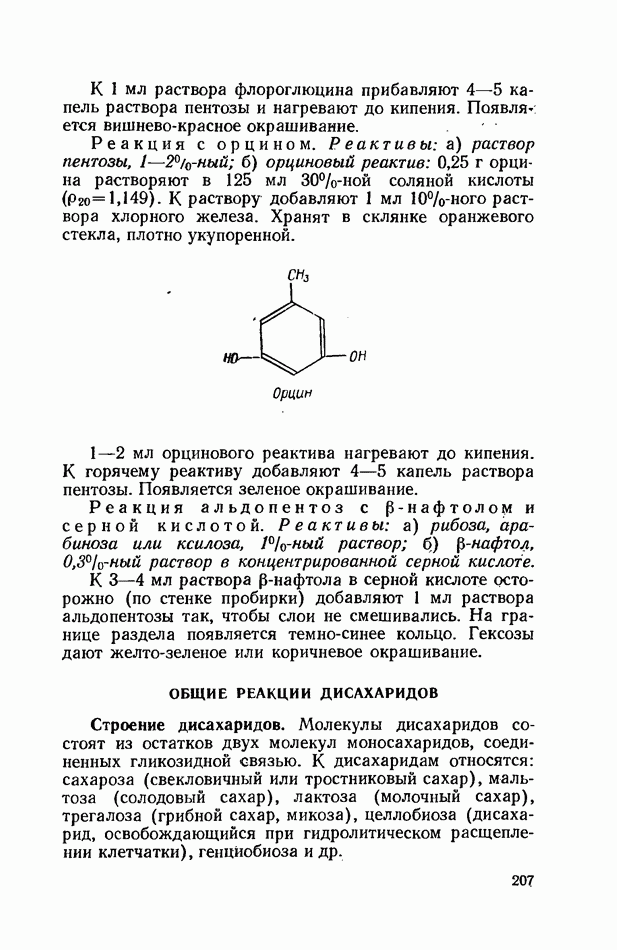
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
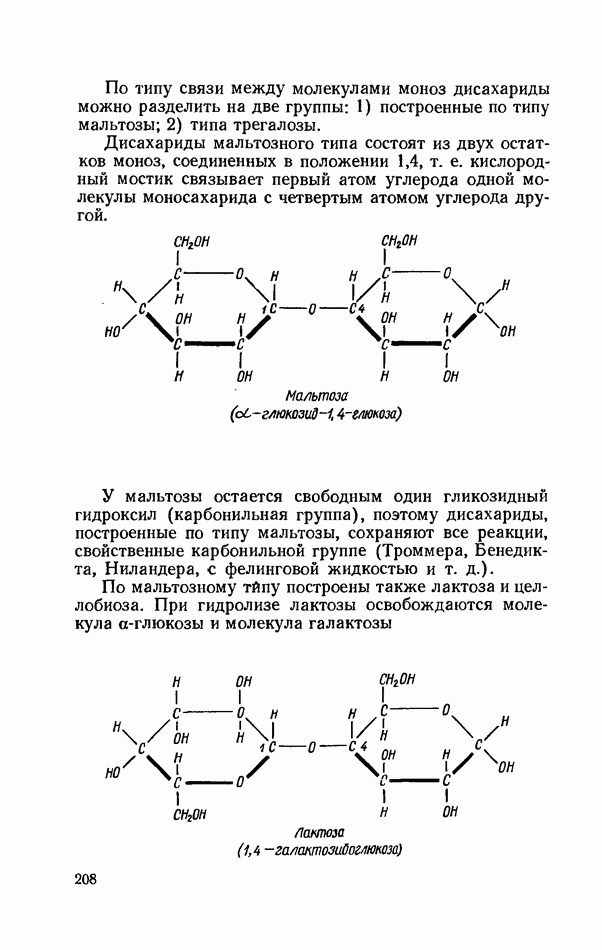
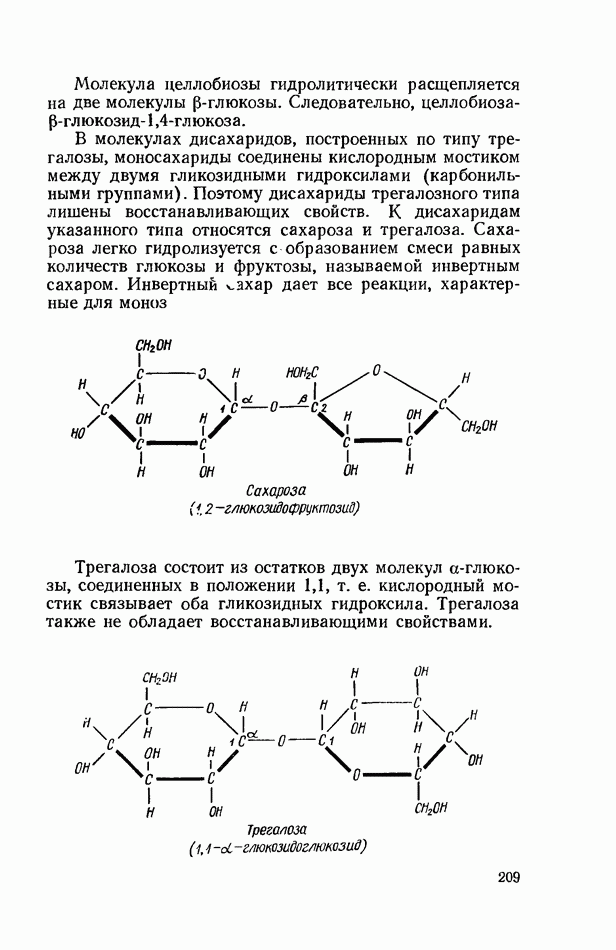
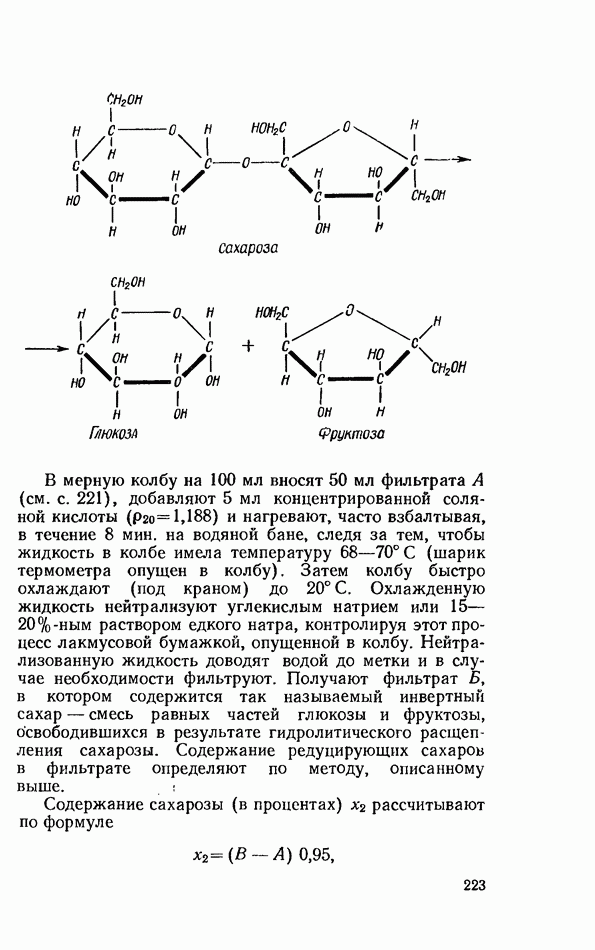
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
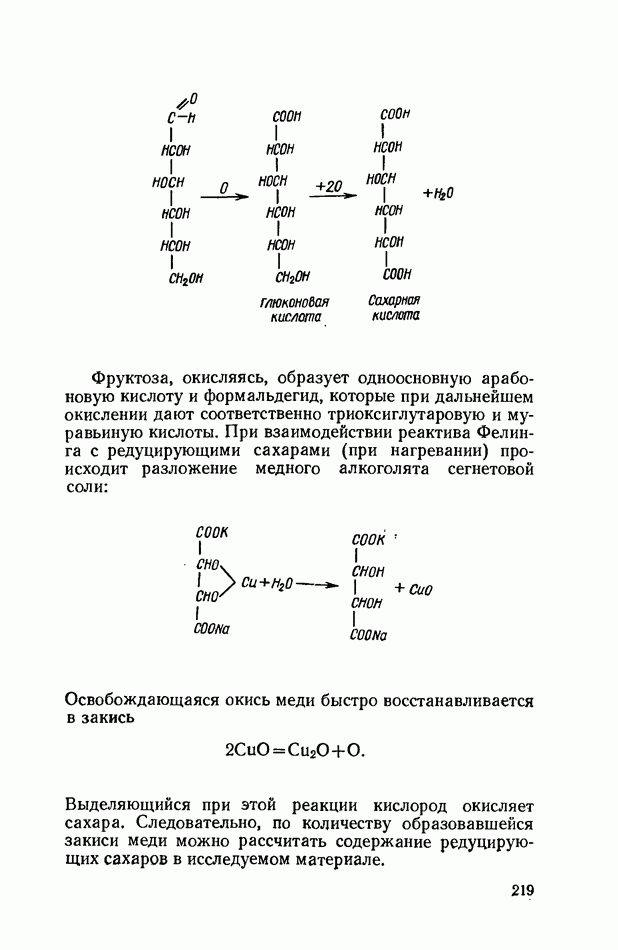
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
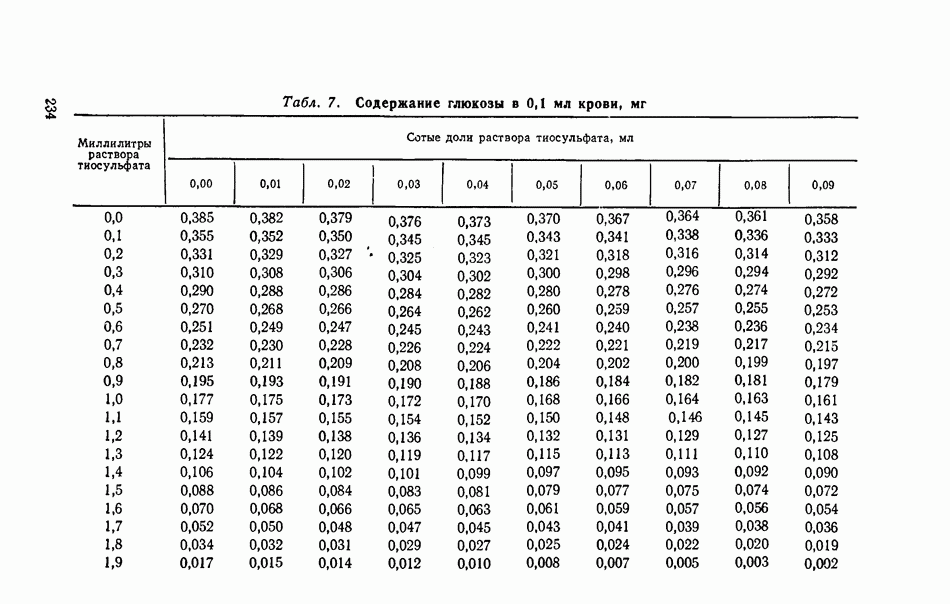
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
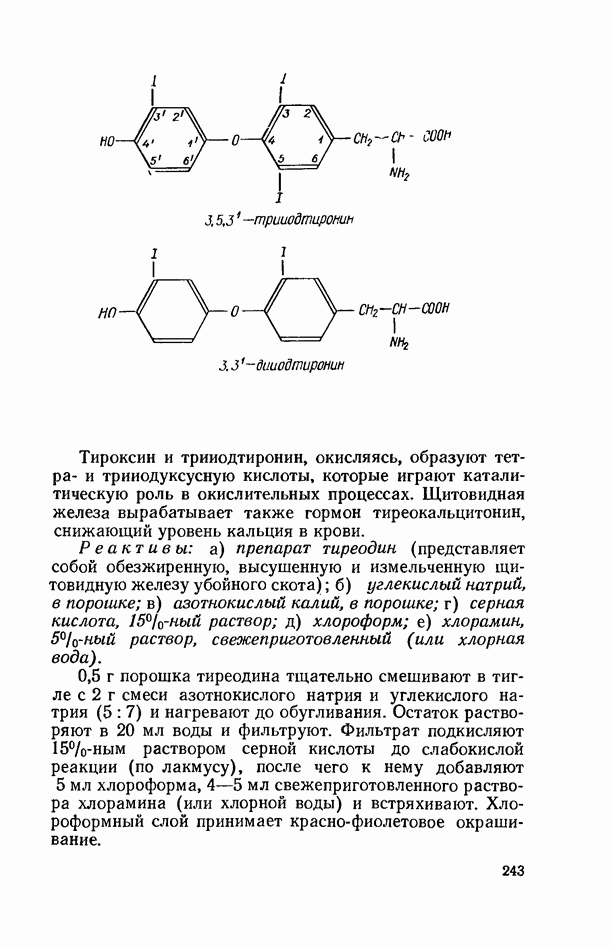
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
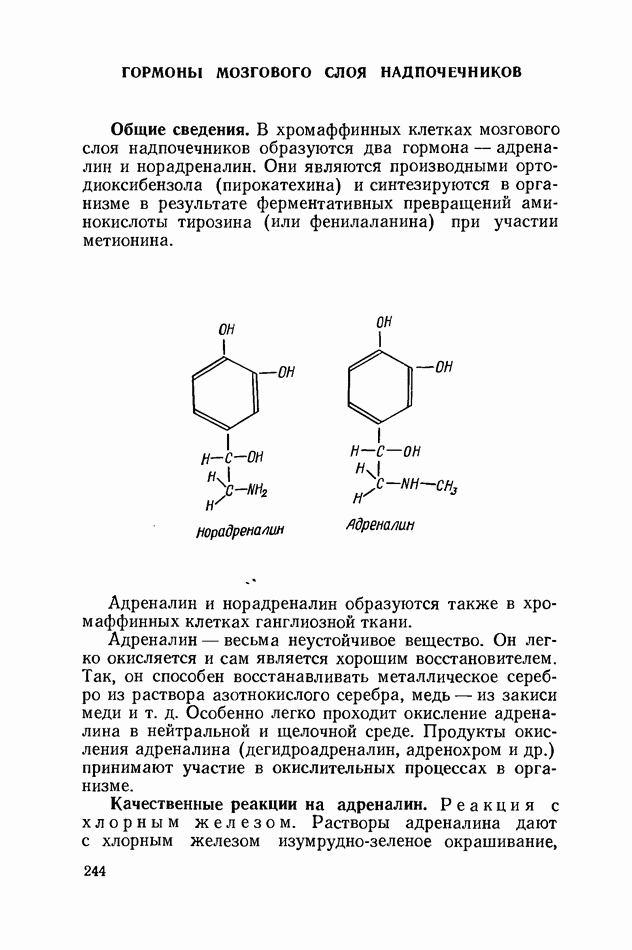
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
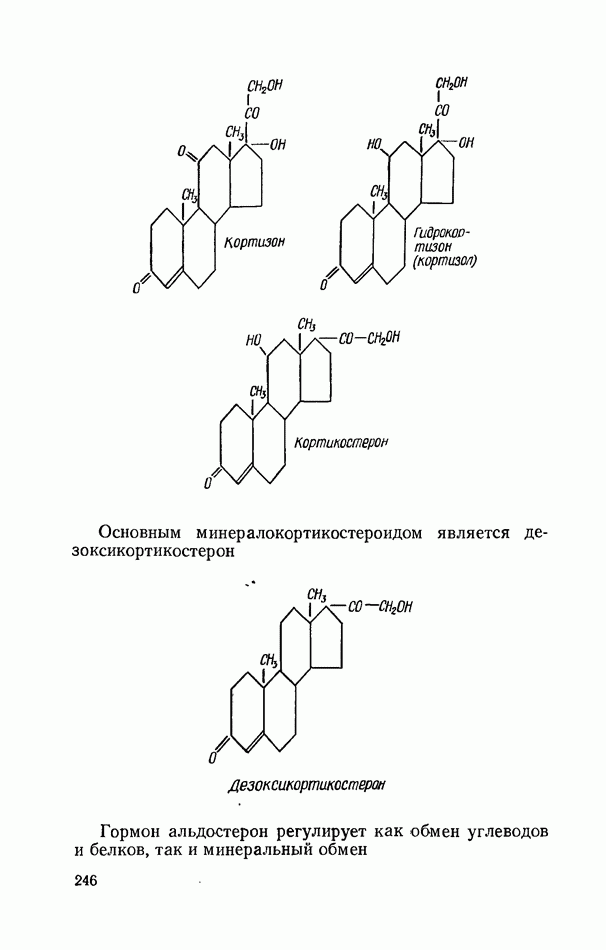
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
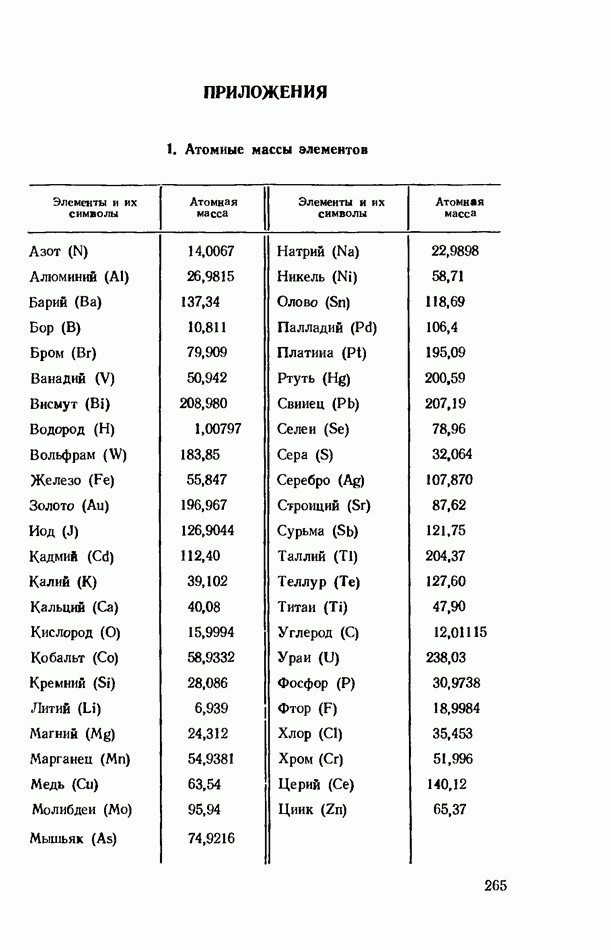
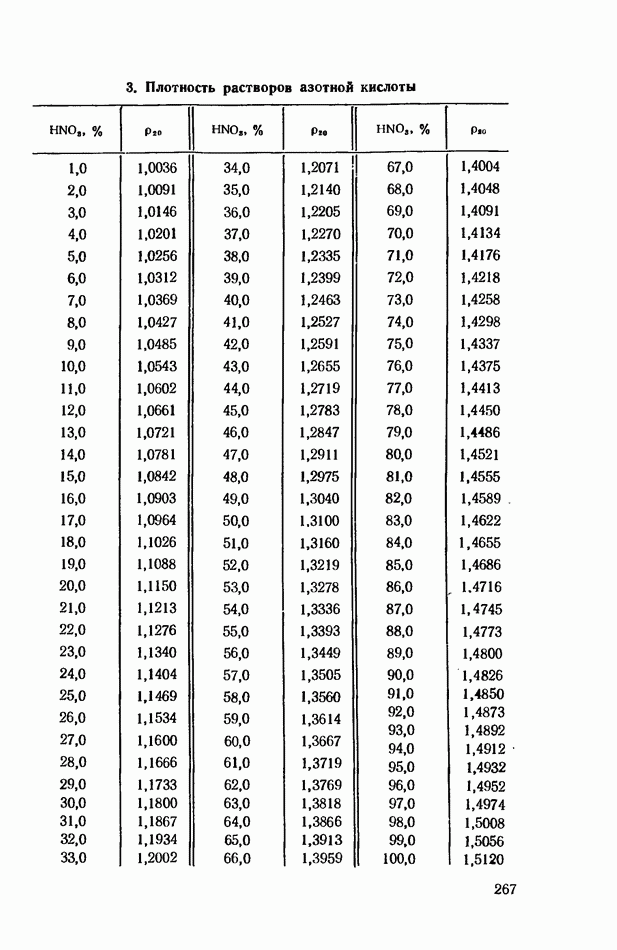
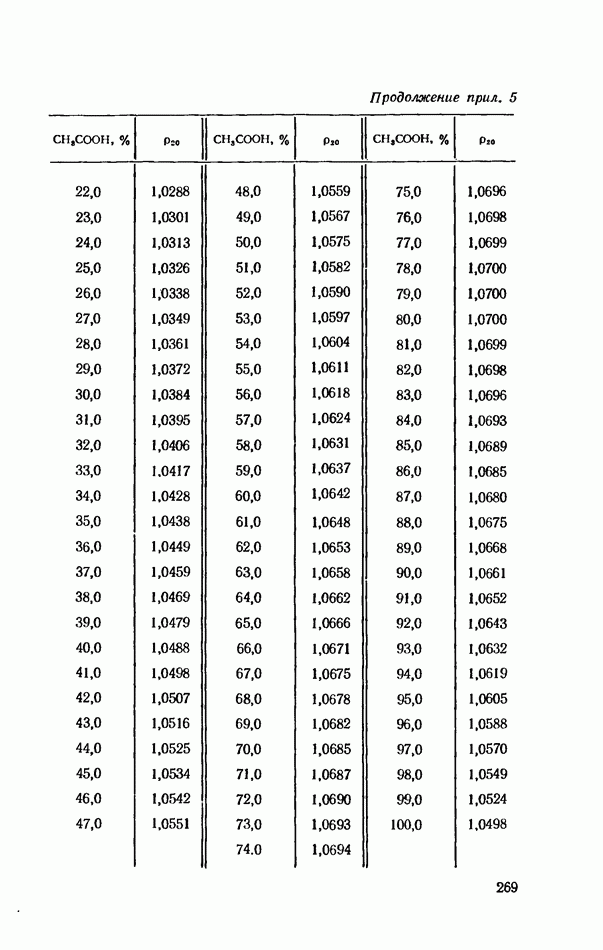
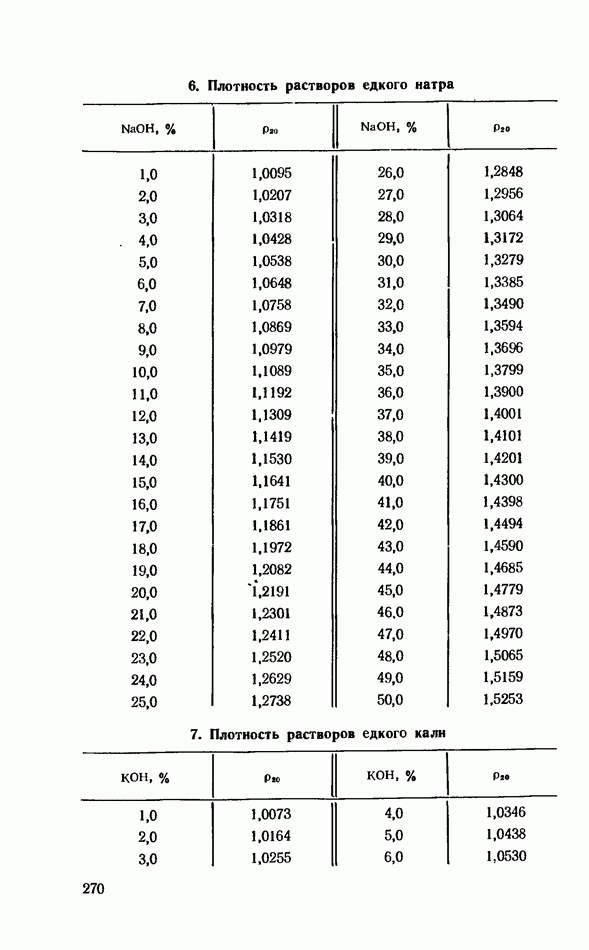
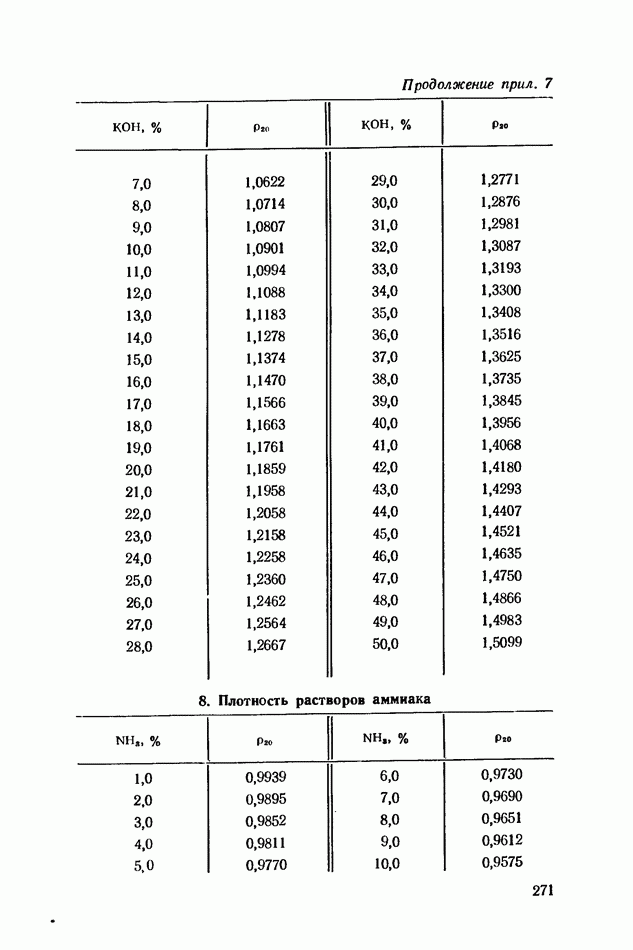
- ПРИЛОЖЕНИЯ